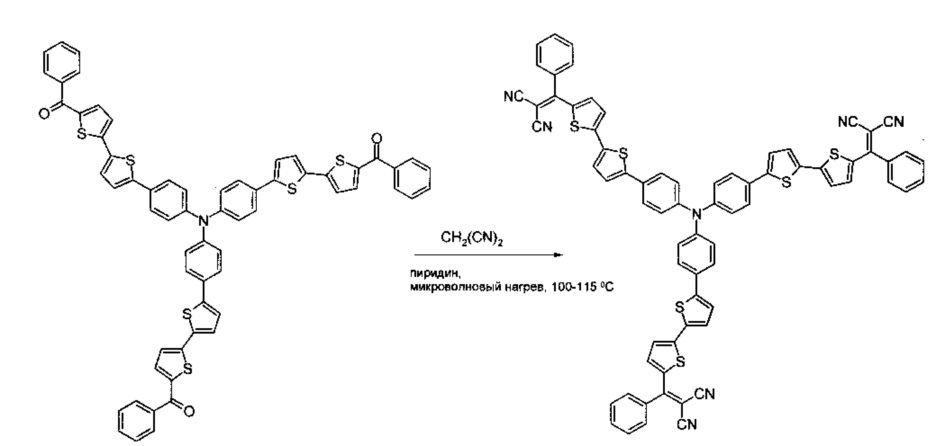
RU2667362C2 - Донорно-акцепторные олигомеры с фенилдициановинильными заместителями на основе трифениламина и способ их получения - Google Patents
Донорно-акцепторные олигомеры с фенилдициановинильными заместителями на основе трифениламина и способ их получения Download PDFInfo
- Publication number
- RU2667362C2 RU2667362C2 RU2015133973A RU2015133973A RU2667362C2 RU 2667362 C2 RU2667362 C2 RU 2667362C2 RU 2015133973 A RU2015133973 A RU 2015133973A RU 2015133973 A RU2015133973 A RU 2015133973A RU 2667362 C2 RU2667362 C2 RU 2667362C2
- Authority
- RU
- Russia
- Prior art keywords
- donor
- acceptor oligomers
- acceptor
- malononitrile
- ketone
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 12
- -1 phenyl dicyanovinyl substituents Chemical group 0.000 title description 15
- ODHXBMXNKOYIBV-UHFFFAOYSA-N triphenylamine Chemical compound C1=CC=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-N 0.000 title description 5
- 150000001875 compounds Chemical class 0.000 claims abstract description 26
- 150000002576 ketones Chemical class 0.000 claims abstract description 21
- CUONGYYJJVDODC-UHFFFAOYSA-N malononitrile Chemical compound N#CCC#N CUONGYYJJVDODC-UHFFFAOYSA-N 0.000 claims abstract description 15
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 claims description 23
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 claims description 20
- 239000002904 solvent Substances 0.000 claims description 13
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 claims description 12
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 claims description 10
- 238000006482 condensation reaction Methods 0.000 claims description 10
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 claims description 10
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 claims description 8
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 claims description 8
- 238000010521 absorption reaction Methods 0.000 claims description 7
- 239000000203 mixture Substances 0.000 claims description 7
- 239000003054 catalyst Substances 0.000 claims description 6
- 238000010438 heat treatment Methods 0.000 claims description 5
- 238000000862 absorption spectrum Methods 0.000 claims description 4
- 230000005855 radiation Effects 0.000 claims description 4
- 239000010409 thin film Substances 0.000 claims description 4
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 claims description 3
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 3
- 239000003960 organic solvent Substances 0.000 abstract description 8
- 125000000217 alkyl group Chemical group 0.000 abstract description 6
- 239000000126 substance Substances 0.000 abstract description 6
- 238000006000 Knoevenagel condensation reaction Methods 0.000 abstract description 2
- 230000000694 effects Effects 0.000 abstract description 2
- 238000006243 chemical reaction Methods 0.000 description 19
- 239000000047 product Substances 0.000 description 14
- 230000015572 biosynthetic process Effects 0.000 description 10
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 9
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 9
- 239000011541 reaction mixture Substances 0.000 description 9
- 238000003786 synthesis reaction Methods 0.000 description 9
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 9
- 238000002360 preparation method Methods 0.000 description 8
- 239000000243 solution Substances 0.000 description 7
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 6
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- 239000012634 fragment Substances 0.000 description 6
- 239000000843 powder Substances 0.000 description 5
- 238000000746 purification Methods 0.000 description 5
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 4
- 238000009833 condensation Methods 0.000 description 4
- 230000005494 condensation Effects 0.000 description 4
- 239000012153 distilled water Substances 0.000 description 4
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Divinylene sulfide Natural products C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 3
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 150000001299 aldehydes Chemical class 0.000 description 3
- 239000012298 atmosphere Substances 0.000 description 3
- 239000003480 eluent Substances 0.000 description 3
- 239000010410 layer Substances 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 238000001906 matrix-assisted laser desorption--ionisation mass spectrometry Methods 0.000 description 3
- 239000012044 organic layer Substances 0.000 description 3
- LEVJVKGPFAQPOI-UHFFFAOYSA-N phenylmethanone Chemical compound O=[C]C1=CC=CC=C1 LEVJVKGPFAQPOI-UHFFFAOYSA-N 0.000 description 3
- 239000002243 precursor Substances 0.000 description 3
- 229910052938 sodium sulfate Inorganic materials 0.000 description 3
- 235000011152 sodium sulphate Nutrition 0.000 description 3
- 125000001424 substituent group Chemical group 0.000 description 3
- 238000002411 thermogravimetry Methods 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- PASDCCFISLVPSO-UHFFFAOYSA-N benzoyl chloride Chemical compound ClC(=O)C1=CC=CC=C1 PASDCCFISLVPSO-UHFFFAOYSA-N 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 229940126214 compound 3 Drugs 0.000 description 2
- 238000004821 distillation Methods 0.000 description 2
- 238000005227 gel permeation chromatography Methods 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- SLCVBVWXLSEKPL-UHFFFAOYSA-N neopentyl glycol Chemical compound OCC(C)(C)CO SLCVBVWXLSEKPL-UHFFFAOYSA-N 0.000 description 2
- 150000002894 organic compounds Chemical class 0.000 description 2
- 239000012074 organic phase Substances 0.000 description 2
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 2
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 2
- 238000001953 recrystallisation Methods 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 2
- 229930192474 thiophene Natural products 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- 238000001429 visible spectrum Methods 0.000 description 2
- OHZAHWOAMVVGEL-UHFFFAOYSA-N 2,2'-bithiophene Chemical compound C1=CSC(C=2SC=CC=2)=C1 OHZAHWOAMVVGEL-UHFFFAOYSA-N 0.000 description 1
- 229910018072 Al 2 O 3 Inorganic materials 0.000 description 1
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical class C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- CIUQDSCDWFSTQR-UHFFFAOYSA-N [C]1=CC=CC=C1 Chemical compound [C]1=CC=CC=C1 CIUQDSCDWFSTQR-UHFFFAOYSA-N 0.000 description 1
- 239000011358 absorbing material Substances 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000012300 argon atmosphere Substances 0.000 description 1
- 150000001491 aromatic compounds Chemical class 0.000 description 1
- 125000000732 arylene group Chemical group 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 238000001460 carbon-13 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 238000011097 chromatography purification Methods 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 229940125782 compound 2 Drugs 0.000 description 1
- 239000007859 condensation product Substances 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 239000012043 crude product Substances 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 239000010408 film Substances 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 230000031700 light absorption Effects 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 229910000000 metal hydroxide Inorganic materials 0.000 description 1
- 150000004692 metal hydroxides Chemical class 0.000 description 1
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 230000005693 optoelectronics Effects 0.000 description 1
- 150000004045 organic chlorine compounds Chemical class 0.000 description 1
- 239000011368 organic material Substances 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 238000013021 overheating Methods 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 238000000039 preparative column chromatography Methods 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 239000012429 reaction media Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 238000001226 reprecipitation Methods 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical compound [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 238000001757 thermogravimetry curve Methods 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- 125000006617 triphenylamine group Chemical group 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/02—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings
- C07D333/04—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings not substituted on the ring sulphur atom
- C07D333/06—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings not substituted on the ring sulphur atom with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to the ring carbon atoms
- C07D333/08—Hydrogen atoms or radicals containing only hydrogen and carbon atoms
- C07D333/10—Thiophene
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K9/00—Tenebrescent materials, i.e. materials for which the range of wavelengths for energy absorption is changed as a result of excitation by some form of energy
- C09K9/02—Organic tenebrescent materials
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Photovoltaic Devices (AREA)
- Catalysts (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
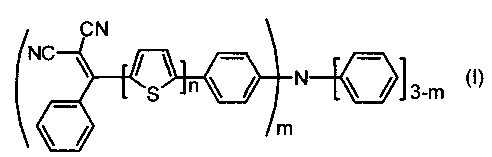
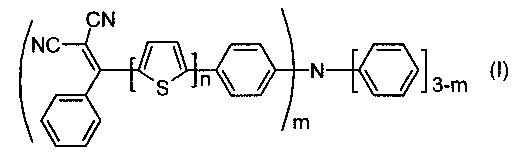
Изобретение относится к новым донорно-акцепторным олигомерам общей формулы (I)
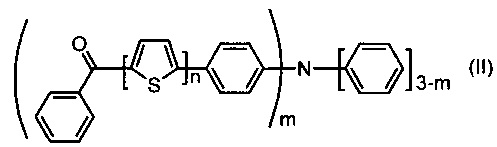
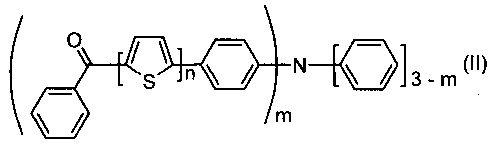
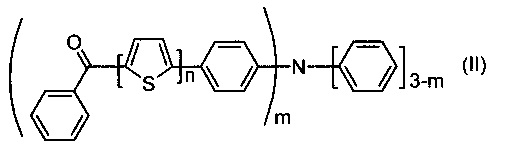
где n означает целое число от 1 до 5; m означает целое число от 1 до 3, а также способу их получения, который заключается в том, что осуществляют реакцию конденсации Кневенагеля между малононитрилом и кетоном, выбранным из ряда соединений общей формулы (II)
где n, m имеют вышеуказанные значения, новые соединения отличаются отсутствием алкильных групп, растворимостью в органических растворителях, высокой термической стабильностью и эффективным поглощением света в области от 400 до 800 нм. 2 н. и 8 з.п. ф-лы, 6 ил., 1 табл., 2 пр.
Description
Изобретение относится к области химической технологии органических соединений и может найти промышленное применение при получении новых функциональных органических материалов, обладающих эффективным поглощением в видимой части спектра, например, светопоглощающих материалов, новых органических красителей, фотоактивных материалов и т.д. Более конкретно, изобретение относится к донорно-акцепторным олигомерам с фенилдициановинильными заместителями на основе трифениламина и способу их получения.
К донорно-акцепторным олигомерам в рамках данного изобретения относятся такие органические соединения, которые, имеют, один электронодонорный трифениламиновый фрагмент, связанный через π-сопряженный тиофеновый спейсер (π-спейсер) с одним, двумя или тремя электроноакцепторным фенилдициановинильным фрагментами.
Известны разнообразные донорно-акцепторные олигомеры на основе трифениламина, содержащие самые различные по природе электроноакцепторные заместители и π-сопряженные ариленовые или гетероариленовые спейсеры (Высокомол. Соедин. Сер. С, 2014, т.56, №. 1, с. 111-143).
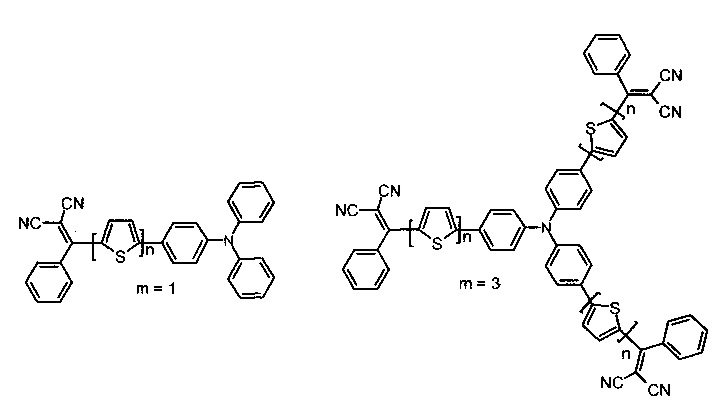
Наиболее близким по строению к заявляемым донорно-акцепторным олигомерам, можно отнести схожие соединения, имеющие также трифениламин в качестве электронодонорного фрагмента, тиофен или его производные в качестве π-спейсера, но дициановинильные (J. Am.Chem. Soc, 2006, 128, 3459-3466; Chem. Commun. 48, 8907 (2012), (Solar Energy Materials & Solar Cells 2013, 115, 52) или алкилдициановинильные (Патент 2012, WO 2012/100908 A1; Adv. Energy Mater. 2014, 4, 201301234) заместители в качестве электроноакцепторного фрагмента (см. Фиг. 1).
Как правило, синтез таких соединений основан на проведении конденсации Кневенагеля между малононитрилом и полученным заранее прекурсором, альдегидом в случае дициановинильных групп (J. Am.Chem. Soc, 2006, 128, 3459-3466), или кетоном, в случае алкилдициановинильных групп (Org. Electron., 2013, 14, 219-229; Adv. Energy Mater. 2014, 4, 201301234):
Однако подобные донорно-акцепторные олигомеры с фенилдициановинильными группами, а также метод их получения не описаны.
Несмотря на то, что вышеприведенные примеры донорно-акцепторных олигомеров с дициановинильными и алкилдициановинильными заместителями демонстрируют эффективное поглощение в длинноволновой области видимого спектра и в ряде работ были использованы в качестве компонента фотоактивного слоя органических солнечных батарей, они не лишены ряда недостатков, обусловленных особенностями их химического строения. Например, в дициановинильных группах присутствует реакционно-способный (активный) протон, т.к. для их синтеза используется альдегидный прекурсор. Наличие такого активного протона, может снижать долговременную стабильность донорно-акцепторных соединений при их использовании в оптоэлектронных устройствах, где они подвержены длительным фото-, электро- и термическим воздействиям. Например, недавно в работе (Faraday Discussions 2014,174, 313-339) было продемонстрированно, что звездообразные олигомеры на основе трифениламина обладают необратимым электрохимическим восстановлением. Также в этой и других работах было показано, что наличие алкильной группы вместо атома водорода, способно повышать электрохимическую стабильность таких донорно-акцепторных соединений. Однако, при проведении термогравиметрического анализа было найдено, что алкильные группы начинают первыми разлагаться при термическом воздействии как на воздухе, так и в инертной среде, что ведет к последующему разрушению алкилдициановинильной группы (Faraday Discussions 2014,174, 313-339, J. Mater. Chem. A, 2014, 2, 16135).
В данной заявке предлагается использовать новые донорно-акцепторные олигомеры, имеющие фенильный радикал при дициановинильной группе вместо атома водорода или алкильной группы. Благодаря тому, что подобные соединения не имеют никаких алкильных групп и активных групп вообще, они обладают повышенной термической стабильностью по сравнению с известными аналогами (см. Фиг. 2). Для реализации этой идеи при проведении конденсации Кневенагеля с малононитрилом используются кетоновые прекурсоры с концевыми фенильными группами.
Таким образом, задачей заявляемого изобретения, является получение нового технического результата, заключающегося в синтезе новых донорно-акцепторных олигомеров обладающих повышенной термо- и термоокислительной стабильностью, которые могут найти применение в различных устройствах органической электроники и фотоники. Например, в качестве фотоактивных, светопоглощающих или светопреобразующих материалов в органических и гибридных солнечных батареях, фотодетекторах и др. В качестве таких свойств в рамках данного изобретения выступают эффективное поглощение света в широком спектральном диапазоне, растворимость в органических растворителях и повышенная термическая стабильность как в инертной атмосфере, так и на воздухе.
Кроме того, задачей данного изобретения является разработка нового способа получения заявленных донорно-акцепторных олигомеров, позволяющего синтезировать продукты заданного строения высокой чистоты, и пригодного к применению в промышленных условиях.
Задача решается тем, что получены донорно-акцепторные олигомеры общей формулы (I)
где n означает целое число от 1 до 5;
m означает целое число от 1 до 3;
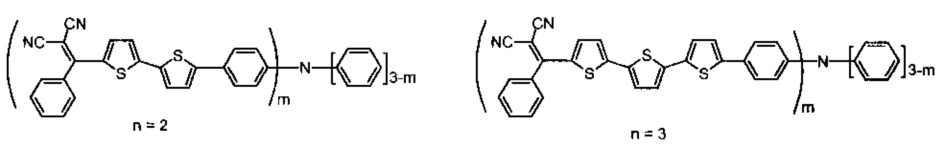
Преимущественные значения n от 2 до 3. В случае, когда донорно-акцепторные олигомеры имеют значение n равным 2 или 3, то их общая формула может быть представлена следующим образом:
Преимущественные значением m является 1 или 3. В случае, когда донорно-акцепторные олигомеры имеют значение m равным 1 или 3, их общая формула может быть представлена следующим образом:
Представленные значения n, m являются частными случаями и не исчерпывают все возможные значения и все возможные сочетания значений n, m между собой.
Донорно-акцепторные олигомеры отличаются тем, что они характеризуются термической стабильностью не ниже 400°С. В рамках данного изобретения термическая стабильность определяется как температура потери 5% массы при нагревании вещества в инертной атмосфере. Данная температура для различных частных случаев составляет не менее 400°С, предпочтительно не менее 425°С. Такая высокая стабильность, обусловлена тем, что в химической структуре таких соединений отсутствуют термически нестабильные фрагменты. Данные термогравиметрического анализа (ТГА), иллюстрирующие высокую термическую стабильность заявленных донорно-акцепторных олигомеров, в том числе и в сравнение с аналогом, имеющим алкилдициановинильные фрагменты, приведены на Фиг. 2, а также в Таблице 1.
Отличительной особенностью заявленных донорно-акцепторных олигомеров является то, что спектры поглощения их тонких пленок толщиной 50-300 нм имеют край поглощения не менее 600 нм. Данная особенность обусловлена тем, что донорно-акцепторные олигомеры содержат фрагменты, обладающие эффективным поглощением в диапазоне от 400 до 800 нм. В рамках данного изобретения способность к поглощению света в этом диапазоне определяется тем, что спектры поглощения их тонких пленок толщиной 50-300 нм имеют край поглощения не менее 600 нм. Данные, иллюстрирующие способность заявленных донорно-акцепторных олигомеров в пленках поглощать свет с краем поглощения не менее 600 нм приведены на Фиг. 3, а также в Таблице 1.
Отличительной особенностью заявленных донорно-акцепторных олигомеров является то, что они характеризуются растворимостью не менее 3 мг/мл в о-дихлорбензоле, при комнатной температуре. Растворимость является важным параметром для возможности использования донорно-акцепторных олигомеров в различных устройствах органической электроники. Поскольку в этом случае фотоактивный слой из этих соединений может быть получен из раствора, а не дорогостоящим вакуумным напылением. Предпочтительной растворимостью считается растворимость порядка 10 мг/мл о-дихлорбензоле. Заявленные донорно-акцепторные олигомеры могут быть растворимы и в других органических растворителях, например, в тетрагидрофуране, хлороформе, хлорбензоле, о-дихлорбензоле и т.д., а также в различных вариациях смесей этих растворителей. Данные, иллюстрирующие способность заявленных донорно-акцепторных олигомеров растворяться в о-дихлорбензоле приведены в Таблице 1.
Приведенные данные являются только демонстрационными примерами, и ни в коей мере не ограничивают характеристик, заявленных донорно-акцепторных олигомеров.
Задача решается также тем, что разработан способ получения донорно-акцепторных олигомеров, заключающийся в том, что осуществляют реакцию конденсации Кневенагеля между кетоном, выбранным из ряда соединений общей формулы (II), и малононитрилом,
где n, m имеют вышеуказанные значения.
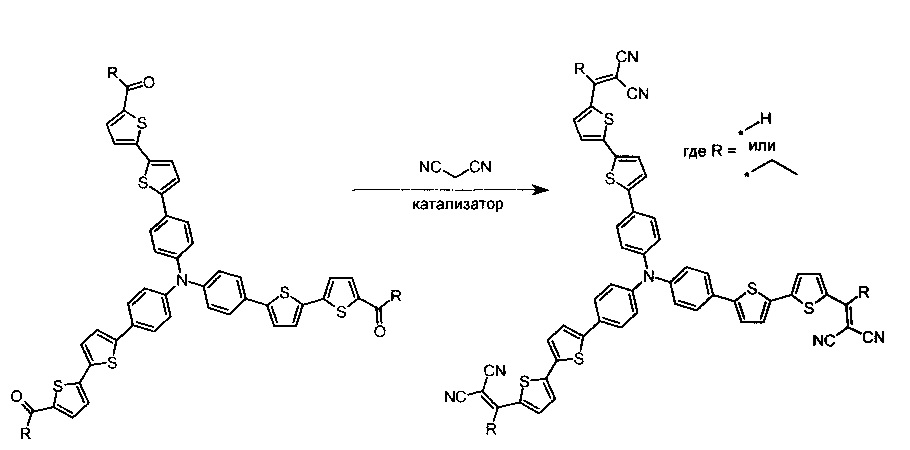
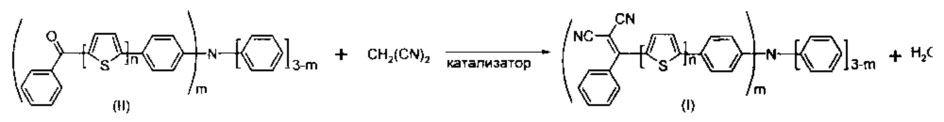
К реакции конденсации Кневенагеля относят конденсацию альдегидов или кетонов с соединениями, содержащими активную метиленовую группу, с образованием производных этилена (J. March, Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, McGraw-Hill, New York, NY: 1968, pp. 693, 697-698). В контексте данного изобретения реакция конденсации Кневенагеля между кетоном, выбранным из ряда соединений общей формулы (II), и малононитрилом приводит к замещению карбонильных групп в кетоне на дициановинильные с образованием донорно-акцепторного олигомера общей формулы (I). Общую схему реакции можно представить следующим образом:
В частности, реакцию конденсации Кневенагеля между кетоном и малононитрилом проводят в среде пиридина или его смеси с, по крайней мере, одним растворителем, выбранным из ряда толуол, тетрагидрофуран, хлороформ, дихлорэтан, хлорбензол, или смеси одного или нескольких из них, при этом пиридин является и катализатором. Наиболее предпочтительным является проведение реакции в каталитической среде пиридина без дополнительных органических растворителей. В этом случае, пиридин выполняет функцию как растворителя, так и катализатора. Необходимым условием проведения конденсации Кневенагеля является присутствие катализатора в реакционной среде. В качестве катализатора, могут быть использованы различные основания, например, органические (триэтиламин, пиридин, пиперидин, этилат натрия и др). или неорганические (ацетат аммония, гидроксиды металлов, например, NaOH, КОН, КОН, оксиды, Al2O3 и др., соли.), основания, а также их смеси с кислотами Льюиса (АlСl3, ТiСl4). Предпочтительным основанием является пиридин.
В частности, реакцию конденсации Кневенагеля между малононитрилом и кетоном проводят при температуре от +20 до +150°С, предпочтительно при температуре от +80 до +115°С. Проведение конденсации Кневенагеля при повышенных температурах способствует увеличению скорости реакции и повышению выхода целевого продукта.
В частности, реакцию конденсации Кневенагеля между малононитрилом и кетоном проводят при нагревании микроволновым излучением. Нагревание реакционной смеси можно проводить как традиционным способом, так и с использованием микроволнового излучения. Предпочтительно нагревание реакции за счет микроволнового излучения, поскольку в этом случае нагревание происходит более равномерно, без перегрева реакционной массы, что ведет к уменьшению побочных продуктов и снижению времени реакции.
Приведенные данные являются только демонстрационными примерами, и ни в коей мере не ограничивают характеристик заявленных донорно-акцепторных олигомеров.
После окончания реакции продукт конденсации выделяют по известным методикам. Например, добавляют воду и органический растворитель. Органическую фазу отделяют, промывают водой до нейтральной реакции и высушивают, после чего растворитель упаривают. В качестве органического растворителя может быть использован любой не смешивающийся или ограниченно смешивающийся с водой растворитель, например, выбранный из ряда эфиров: диэтиловый эфир, метилтретбутиловый эфир, или выбранный из ряда ароматических соединений: бензол, толуол, ксилол, или выбранный из ряда хлорорганических соединений: дихлорметан, хлороформ, четыреххлористый углерод, хлорбензол. Также для выделения могут использоваться смеси органических растворителей. Выделение продукта можно производить и без применения органических растворителей, например, отгонкой растворителей из реакционной смеси, или любым другим известным методом. Предпочтительным является выделение продукта отгонкой растворителя.
Очистку сырого продукта проводят любым известным методом, например, препаративной колоночной хроматографией в адсорбционном или эксклюзионом режиме, перекристаллизацией, дробным осаждением, дробным растворением или их любой комбинацией.
Чистоту и строение синтезированных соединений подтверждают совокупностью данных физико-химического анализа, хорошо известных специалистам, таких как хроматографические, спектроскопические, масс-спектроскопические. Наиболее предпочтительным подтверждением чистоты и структуры донорно-акцепторных олигомеров являются ЯМР-спектры на ядрах 1H и кривые, полученные методом гельпроникающей хроматографии (см. Фиг. 4-6).
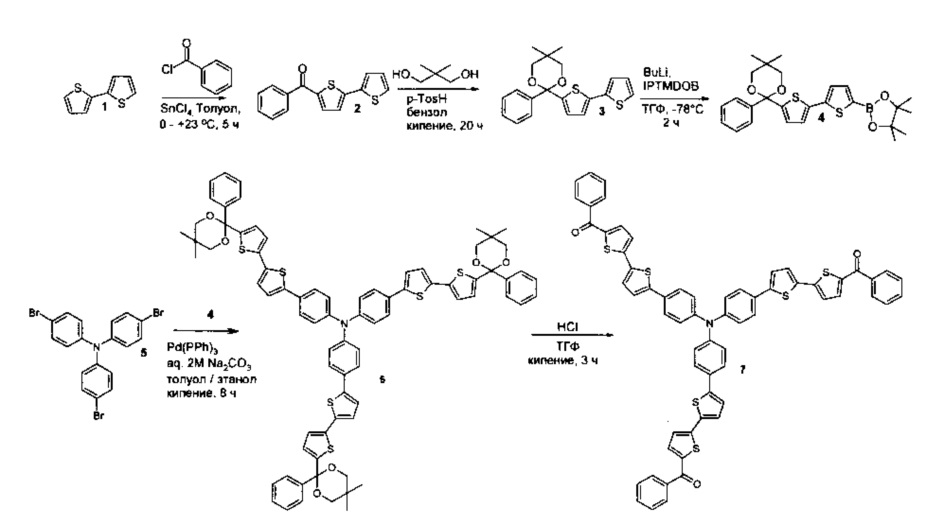
Исходные кетоны, выбранные из ряда соединений общей формулы (II), для синтеза донорно-акцепторных олигомеров получают в несколько стадий, используя для этого реакции органического и металлорганического синтеза в различной последовательности. Конкретный пример получения исходного кетона общей формулы (II), где n равно 2, m равно 3 проиллюстрирован ниже (см. Пример 1).
На Фиг. 1 в качестве иллюстрации представлены структурные формулы соединений наиболее близких по строению к заявляемым донорно-акцепторным олигомерам, но имеющие дициановинильные или алкилдициановинильные группы в качестве электроноакцепторных фрагментов.
На Фиг. 2 в качестве иллюстрации представлены ТГА кривые в азоте донорно-акцепторных олигомеров по примерам 2, 4, 4, 8, а также полного аналога олигомера по Примеру 2, но с алкильными (гексильными) заместителями (N(Ph-2T-DCN-Hex)3, Adv. Energy Mater. 2014, 4, 201301234).
На Фиг. 3 в качестве иллюстрации представлены спектры поглощения тонких пленок донорно-акцепторных олигомеров по Примерам 2, 4, 5, 8.
На Фиг. 4 представлен 1H ЯМР спектр соединения по Примеру 2.
На Фиг. 5 представлен 13С ЯМР спектр соединения по Примеру 2.
На Фиг. 6 представлены ГПХ кривая соединения, полученного по Примеру 2.
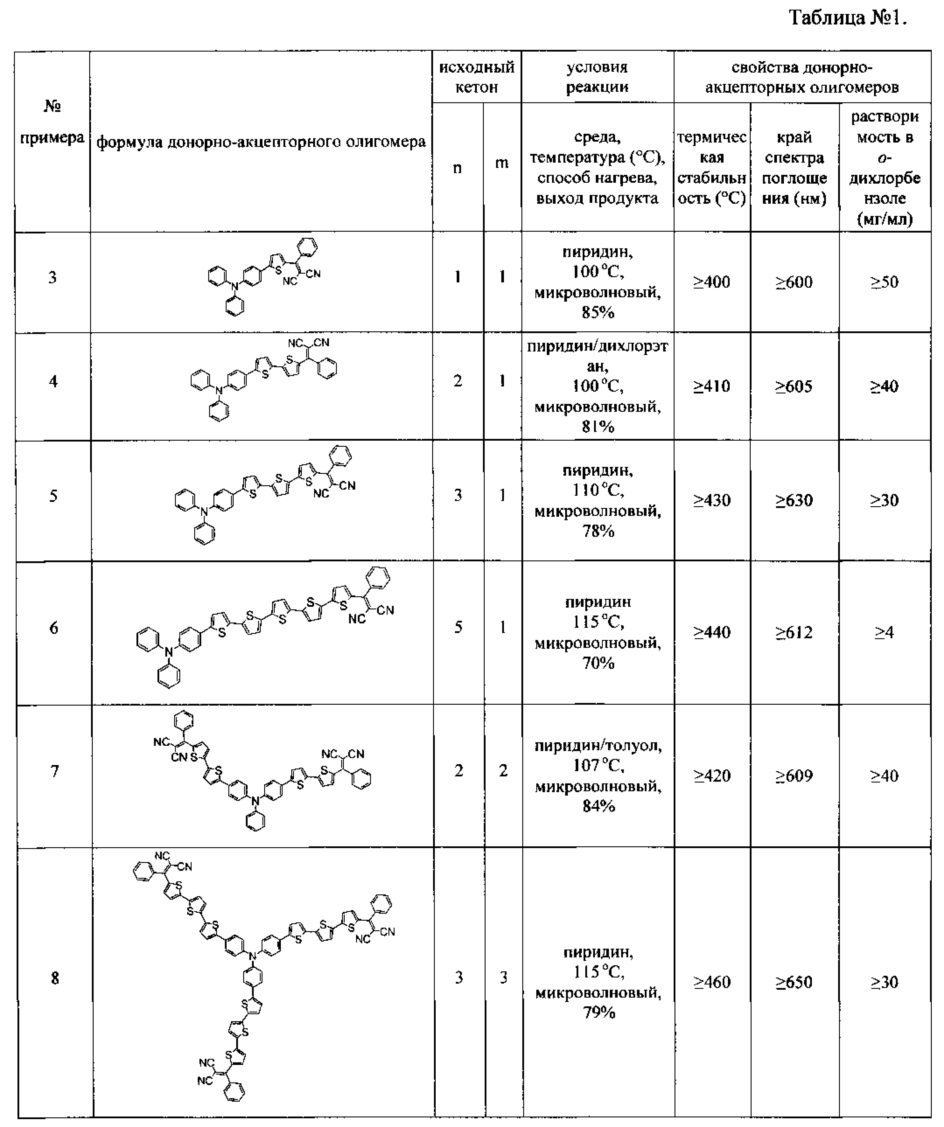
Изобретение может быть проиллюстрировано нижеприведенными примерами синтеза донорно-акцепторных олигомеров (см. Пример 2 и Таблицу 1 с Примерами 3-8). При этом использовали коммерчески доступные реагенты и растворители без дополнительной очистки: 1.6 M и 2.5 M растворы н-бутиллития (BuLi) в гексане, тетракис(трифенилфосфин) палладий (0) (Pd(PPh3)4), п-толуолсульфоновая кислота, (p-TosH), малононитрил, бензоилхлорид, 2,2-диметил-1,3-пропандиол, 2,2'-битиофен, и др. Дополнительные реагенты и вещества были получены, используя описанные в литературе методики. Все реакции, если не оговорено особо, проводили в атмосфере аргона.
Получение кетонов общей формулы (II) для синтеза донорно-акцепторных олигомеров.
Пример 1. Синтез кетона (7) общей формулы (II), где n равно 2, m равно 3, был осуществлен постадийно согласно приведенной ниже схеме:
Получение соединения 2. 2,2'-битиен-5-ил(фенил)метанон (2) был получен следующим образом: SnCl4 (15,15 г, 58,2 ммоль) был прикапан к смеси 2,2'-битиофена (9 г, 51,1 ммоль) и бензоил хлорида (7,61 г, 54,1 ммоль) в толуоле (80 мл) при 0°С. Реакционную смесь перемешивали в течение 2 часов при температуре 0-5°С. После завершения реакции в реакционную колбу был добавлен лед. Затем реакционную смесь вылили в 200 мл дистиллированной воды и экстрагировали дихлорэтаном. Органическую фазу отмывали дистиллированной водой и сушили над безводным Na2SO4. Растворитель был отогнан в вакууме и чистый продукт (12,73 г, 87%) был получен перекристаллизацией из гексана. Тпл: 75-76°С. 1Н ЯМР (250 МГц, DMSO-D6, δ, м.д.): 7,07 (т, 1Н, J=3,96 Гц), 7,19 (д, 1H, J1=3,90 Гц), 7,35 (т, 2Н, J=4,89 Гц), 7,45-7,63 (перекрывающиеся сигналы, 4Н), 7,84 (д, 2Н, J=7,33 Гц). 13С ЯМР (75 МГц, DMSO-D6): δ [м.д.] 124,93, 126,51, 127,91, 128,56, 128,60, 128,71, 132,34, 135,11, 136,62, 137,12, 140,56, 145,18, 186,67. Рассчитано (%) для C15H10OS2: С, 66,64; Н, 3,73; S, 23,72. Найдено: С,66,41; Н, 3,79; S, 23,63. MALDI-MS: найдено m/z 270,43; рассчитано для [М]+ 270,37.
Получение соединения 3. 2-(2,2'-битиен-5-ил)-5,5-диметил-2-фенил-1,3-диоксан (3) был получен следующим образом: 2,2'-битиен-5-ил(фенил)метанон (2) (8,0 г, 29,6 ммоль) растворили в сухом бензоле (160 мл). После добавили 2,2-диметил-1,3-пропандиол (18,49 г, 177.5 ммоль) и p-TosH (0.394 г, 2,1 ммоль). Реакцию перемешивали с насадкой Дина-Старка при кипячении 10 часов, после чего реакцию охладили и добавили 10 мл триэтиламина. Реакционную смесь вылили в 200 мл дистиллированной воды и трижды экстрагировали бензолом. Органический слой объединили и посушили над сульфатом натрия, а растворитель отогнали при пониженном давлении. Чистый продукт (9,23 г, 87%) был получен очисткой колоночной хроматографией на силикагеле (элюент, гексан). Белый порошок, Тпл: 57-58°С. 1H ЯМР (250 МГц, DMSO-D6, δ, м.д.): 0,83 (с, 3Н), 1.02 (с, 3Н), 3,49 (д, 2Н, J=11 Гц), 3,63 (д, 2Н, J = 11 Гц), 6,67 (д, 1Н, J=3.7 Гц), 7,01-7,11 (перекрывающиеся сигналы, 2Н), 7,25 (дд, 1H, J1=J2=1 Гц), 7,31-7,55 (перекрывающиеся сигналы, 6Н). 13С ЯМР (125 МГц, DMSO-D6): δ [м.д.] 21,77, 22,11, 29,57, 71,59, 98,75, 123,25, 124,12, 125,60, 126,21, 126,65, 128,28, 128,32, 128,53, 136,19, 136,84, 140,31, 145,70. Рассчитано (%) для C20H20O2S2: С, 67,38; Н, 5,65; S, 17,99. Найдено: С, 67,25; Н, 5,59; S, 17,89. MALDI MS: найдено m/z 356,42; рассчитано для [М]+ 356,51.
Получение соединения 4. 5,5-диметил-2-фенил-2-[5'-(4,4,5,5-тетраметил-1,3,2-диоксоборолан-2-ил)-2,2'-битиен-5-ил]-1,3-диоксан (4) был получен следующим образом: 1.6 M раствор бутиллития (13,7 мл, 22 ммоль) был прикапан к раствору соединения 3 (7,8 г, 22 ммоль) в 203 мл сухого ТГФ при -78°С. После чего реакцию перемешивали при -78°С в течение часа и добавили изопропокси-4,4,5,5-тетраметил-1,3,2-диоксоборолан (4,07 г, 22 ммоль) одной порцией. Реакцию перемешивали в течение часа при -78°С и после подняли температуру до комнатной. После завершения реакции реакционную смесь вылили в 200 мл дистиллированной воды, содержащей 22 мл 1 M НСl и трижды экстрагировали диэтиловым эфиром. Органический слой посушили над сульфатом натрия, а растворитель отогнали в вакууме. Продукт 10,43 г (99%) был использован в следующей стадии синтеза без дополнительной очистки. Серый порошок, Тпл: 71-72°С. 1H ЯМР (250 МГц, DMSO-D6, δ, м.д.): 0,82 (с, 3Н), 1,02 (с, 3Н), 1,27 (с, 12Н), 3,49 (д, 2Н, J=11 Гц), 3,63 (д, 2Н, J=11 Гц), 6,71 (д, 1Н, J=3.7 Гц), 7,16 (д, 1Н, J=3,7 Гц), 7,27-7,53 (перекрывающиеся сигналы, 7Н). 13С ЯМР (125 МГц, DMSO-D6): δ [м.д.] 21,75, 22,07, 24,51, 25,10, 29,56, 66,99, 71,58, 84,10, 98,72, 124,41, 125,40, 126,19, 126,76, 128,30, 128,54, 136,25, 138,39, 140,20, 143,09, 146,81. Расчитано (%) для C26H31BO4S2: С, 64,73; Н, 6,48; S, 13,29. Found: С, 64,69; Н, 6,39; S, 13,18. MALDI-MS: найдено m/z 482,36; рассчитано для [М]+ 482,47.
Получение соединения 6. Трис{4-[5'-(5,5-диметил-2-фенил-1,3-диоксан-2-ил)-2,2'-битиен-5-ил]фенил}амин (6) был получен следующим образом. В инертной атмосфере к Рd(РРh3)4 (173 мг, 0,14 ммоль) были добавлены дегазированные растворы соединения 4 (2.88 г, 6 ммоль) и 5 (0,8 g, 2 ммоль) в смеси толуол/этанол (50/5 мл), а также водный раствор 2М Nа2СО3 (9 мл). Реакционную смесь перемешивали при кипении в течение 8 часов, после чего ее охладили до комнатной температуры и вылили в делительную воронку, содержащую 75 мл дистилированной волы и 100 мл толуола. Водный слой трижды экстрагировали толуолом, и объединенный органический слой посушили над сульфатом натрия, а растворитель отогнали в вакууме. Чистый продукт был получен хроматографически очисткой на колонке с силикагелем (элюент - толуол). Выход продукта 6 (1,74 г) составил 80%. Темно-желтый порошок, Тпл: 115-116°С. 1H ЯМР (250 МГц, CDCl3): δ [м.д.] 0.88 (с, 9Н), 1,16 (с, 9Н), 3,59 (д, 6Н, J=11 Гц), 3,69 (д, 6Н, J=11 Гц), 6,64 (д, 3Н, J=3,7 Гц), 6,93-6.97 (уширенный сигнал, 3Н), 7,07-7,13 (перекрывающиеся пики, 12Н), 7,32-7,49 (перекрывающиеся пики, 15Н), 7,57 (д, 6Н). 13С ЯМР (125 МГц, DMSO-D6): δ [м.д.] 22,21, 22,67, 30,03, 72,43, 99,55, 122,73, 123,06, 124,37, 124,60. Рассчитано (%) for C78H69NO6S6: С, 71,58; Η, 5,31; S, 14,70; Ν, 1,07. Найдено: С, 71,50; Η, 5,27; S, 14,65; Ν, 1,04. MALDI-MS: найдено m/z 1308,73; рассчитано для [М]+ 1308,81.
Получение соединения 7. [нитрилотрис(4,1-фенилен-2,2'-битиен-5',5-диил)трис(фенилметанон) (7) был получен следующим образом: 2,4 мл 1М НСl добавили к раствору соединения 6 (1,5 g, 1 ммоль) в ТГФ (30 мл) и перемешивали реакцию при кипении в течение 3 часов. После чего реакционную смесь охладили, профильтровали. Продукт полученный на фильтре обильно промыли водой. После чего, растворили в ТГФ (50 мл), добавили к раствору 2 мл 1М НСl и перемешивали реакцию при кипении в течение 1,5 часов. Реакционную смесь охладили, профильтровали, полученный на фильтре продукт промыли водой и посушили в вакууме. Выход продукта 7 (1,15 г) составил 95%. Красный порошок, Тпл: 202-203°С. 1Н ЯМР (250 МГц, CDCl3): δ [м.д.] 7,04-7,38 (перекрывающиеся сигналы, 15Н), 7,42-7,68 (перекрывающиеся сигналы, 18Н), 7,84 (д, 6Н, J=7,32 Гц). Рассчитано (%) для C63H39N7O3S6: С, 72,04; Н, 3,74; N, 1,33; S, 18,32. Найдено: С, 72,09; Н, 3,78; N, 1,34; S, 18,29. MALDI MS: найдено m/z 1050,58; рассчитано для [М]+ 1050,40.
Получение донорно-акцепторных олигомеров.
Пример 2. Общая методика способа получения донорно-акцепторных олигомеров общей формулы (I) реакцией конденсации Кневенагеля между малононитрилом и кетоном, выбранным из ряда соединений общей формулы (II), приведена ниже на примере полученного выше кетона (соединение 7, пример 1), где n равно 2, m равно 3:
Кетон из примера 1 (0,65 g, 0.6 ммоль), малононитрил (0,2 g, 3,1 ммоль) и пиридин помещаются в реакционный сосуд и перемешиваются в атмосфере азота в течение 25 часов при 100-115°С, используя контролируемый микроволновый нагрев. После окончания реакции пиридин отгоняют при пониженном давлении. Продукт очищают методом колоночной хроматографии на силикагеле (элюент дихлорметан), с последующим очисткой методом переосаждения. Выход продукта (0,55 г) составил 75%. Черный порошок, Тпл: 247°С. 1Н ЯМР (250 МГц, CDCl3): δ [м.д.] 7,15 (д, 6Н, J=8,7 Гц), 7,23 (д, 3Н, J=4,0 Гц), 7,26 (д, 6Н, J=3,8 Гц), 7,33 (д, 3Н, J=4,0 Гц), 7,44-7,66 (перекрывающиеся сигналы, 24Н). 13С ЯМР (125 МГц, CDCl3): δ [м.д.] 114,12, 114,78, 123,87, 124,52, 126,86, 127,85, 128,40, 128,79, 129,30, 131,56, 133,74, 135,88, 136,12, 138,51, 146,44, 146,82, 148,65, 163,73. Рассчитано (%) для C72H39N7S6: С, 72,40; Н, 3,29; N, 8,21; S, 16,11. Найдено: С, 72,33; Н, 3,25; N, 8,14; S, 16,09. MALDI MS: найдено m/z 1194,54; рассчитано для [М]+ 1194,21.
Другие примеры (Примеры 3-8) донорно-акцепторных олигомеров общей формулы (I), полученных аналогичным способом, представлены в Таблице 1.
Claims (15)
1. Донорно-акцепторные олигомеры общей формулы (I)
где n означает целое число от 1 до 5;
m означает целое число от 1 до 3;
2. Донорно-акцепторные олигомеры по п. 1, отличающиеся тем, что n имеет значения от 2 до 3.
3. Донорно-акцепторные олигомеры по п. 1, отличающиеся тем, что m имеет значения 1 или 3.
4. Донорно-акцепторные олигомеры по п. 1, отличающиеся тем, что они характеризуются термической стабильностью не ниже 400°С.
5. Донорно-акцепторные олигомеры по п. 1, отличающиеся тем, что спектры поглощения их тонких пленок толщиной 50-300 нм имеют край поглощения не менее 600 нм.
6. Донорно-акцепторные олигомеры по п. 1, отличающиеся тем, что характеризуются растворимостью не менее 3 мг/мл в о-дихлорбензоле при комнатной температуре.
7. Способ получения донорно-акцепторных олигомеров по пп. 1-6, заключающийся в том, что осуществляют реакцию конденсации Кневенагеля между кетоном, выбранным из ряда соединений общей формулы (II) и малононитрилом
где n, m имеют вышеуказанные значения.
8. Способ по п. 7, отличающийся тем, что реакцию конденсации Кневенагеля между кетоном и малононитрилом проводят в среде пиридина или его смеси с по крайней мере одним растворителем, выбранным из ряда толуол, тетрагидрофуран, хлороформ, дихлорэтан, хлорбензол, при этом пиридин является одновременно и катализатором.
9. Способ по п. 7, отличающийся тем, что реакцию конденсации Кневенагеля между кетоном и малононитрилом проводят при температуре от +20 до +150°С, предпочтительно при температуре от +80 до +115°С.
10. Способ по п. 7, отличающийся тем, что реакцию конденсации Кневенагеля между малононитрилом и кетоном проводят при нагревании микроволновым излучением.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2015133973A RU2667362C2 (ru) | 2015-08-13 | 2015-08-13 | Донорно-акцепторные олигомеры с фенилдициановинильными заместителями на основе трифениламина и способ их получения |
| PCT/RU2016/000442 WO2017026917A1 (ru) | 2015-08-13 | 2016-07-15 | Донорно-акцепторные олигомеры с фенилдициановинильными заместителями на основе трифениламина и способ их получения |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2015133973A RU2667362C2 (ru) | 2015-08-13 | 2015-08-13 | Донорно-акцепторные олигомеры с фенилдициановинильными заместителями на основе трифениламина и способ их получения |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| RU2015133973A RU2015133973A (ru) | 2017-02-16 |
| RU2015133973A3 RU2015133973A3 (ru) | 2018-07-10 |
| RU2667362C2 true RU2667362C2 (ru) | 2018-09-19 |
Family
ID=57983918
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2015133973A RU2667362C2 (ru) | 2015-08-13 | 2015-08-13 | Донорно-акцепторные олигомеры с фенилдициановинильными заместителями на основе трифениламина и способ их получения |
Country Status (2)
| Country | Link |
|---|---|
| RU (1) | RU2667362C2 (ru) |
| WO (1) | WO2017026917A1 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2788650C2 (ru) * | 2020-10-19 | 2023-01-24 | Юрий Николаевич Лупоносов | Несимметричные люминесцентные донорно-акцепторные молекулы на основе трифениламин-тиофенового блока с различными электроноакцепторными группами и способ их получения |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012100908A1 (en) * | 2011-01-25 | 2012-08-02 | Heraeus Precious Metals Gmbh & Co. Kg | Star-shaped compounds for organic solar cells |
-
2015
- 2015-08-13 RU RU2015133973A patent/RU2667362C2/ru active
-
2016
- 2016-07-15 WO PCT/RU2016/000442 patent/WO2017026917A1/ru not_active Ceased
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012100908A1 (en) * | 2011-01-25 | 2012-08-02 | Heraeus Precious Metals Gmbh & Co. Kg | Star-shaped compounds for organic solar cells |
Non-Patent Citations (4)
| Title |
|---|
| JIN-LIANG WANG ET AL.: "Solution-Processed Bulk-Heterojunction Photovoltaic Cells Based on Dendritic and Star-Shaped D-[pi]-A Organic Dyes", CHEMISTRY - AN ASIAN JOURNAL, 2010, pages 1455-1465, no.5, DOI: 10.1002/asia.200900686. * |
| LELIEGE ANTOINE et al. Structural modulation of internal change transfer in smoll molecular donors for organic solar cellc. Chem.Commun., 2012, 48., pp.8907-8909, DOI:10.1039/C2C33921H. p.2. * |
| LELIEGE ANTOINE et al. Structural modulation of internal change transfer in smoll molecular donors for organic solar cellc. Chem.Commun., 2012, 48., pp.8907-8909, DOI:10.1039/C2C33921H. p.2. JIN-LIANG WANG ET AL.: "Solution-Processed Bulk-Heterojunction Photovoltaic Cells Based on Dendritic and Star-Shaped D-[pi]-A Organic Dyes", CHEMISTRY - AN ASIAN JOURNAL, 2010, pages 1455-1465, no.5, DOI: 10.1002/asia.200900686. * |
| ROQUET SOPHIE et al. "Triphenylamine-Thienylenevinylene Hybrid Systems with Internal Charge ransfer as Donor Materials for Heterojunction Solar Cells", J. AM. CHEM. SOC., 2006, VOL. 128, NO. 10, pp.3459-3466, DOI: 10.1021/JA058178E. * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2788650C2 (ru) * | 2020-10-19 | 2023-01-24 | Юрий Николаевич Лупоносов | Несимметричные люминесцентные донорно-акцепторные молекулы на основе трифениламин-тиофенового блока с различными электроноакцепторными группами и способ их получения |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2017026917A1 (ru) | 2017-02-16 |
| WO2017026917A8 (ru) | 2017-03-30 |
| RU2015133973A (ru) | 2017-02-16 |
| RU2015133973A3 (ru) | 2018-07-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5940548B2 (ja) | 新規なスピロビフルオレン化合物 | |
| RU2624820C2 (ru) | Донорно-акцепторные сопряженные молекулы и способ их получения | |
| US11685730B2 (en) | Cyclic compound formed by Friedel-Crafts reaction at positions 1 and 3 of carbazole and preparation method thereof | |
| TW201420581A (zh) | 芳香族化合物之製造方法 | |
| CN104530105A (zh) | 一种苯并噻二唑或苯并二噻吩桥联的双氟化硼络合二吡咯甲川衍生物有机染料及其制备方法 | |
| Jana et al. | Pyridine-cored V-shaped π-conjugated oligomers: synthesis and optical properties | |
| KR101851880B1 (ko) | 신규한 분지형 올리고아릴실란 및 이의 제조방법 | |
| Zong et al. | 3, 4-Alkylenedioxy ring formation via double Mitsunobu reactions: an efficient route for the synthesis of 3, 4-ethylenedioxythiophene (EDOT) and 3, 4-propylenedioxythiophene (ProDOT) derivatives as monomers for electron-rich conducting polymers | |
| CN112250686A (zh) | 一类口字型格空穴传输材料及其制备方法与应用 | |
| JP5147103B2 (ja) | ベンゾメタロールの合成方法および新規ジイン化合物 | |
| RU2667362C2 (ru) | Донорно-акцепторные олигомеры с фенилдициановинильными заместителями на основе трифениламина и способ их получения | |
| CN114249758A (zh) | 一种基于五元芳杂环并bodipy的二聚体及其制备方法 | |
| CN111423450B (zh) | 化合物、显示面板以及显示装置 | |
| CN105968130B (zh) | 一种中位含咔唑及桥联基团的双中心氟化硼络合二吡咯甲川衍生物及其制备方法 | |
| JP6698300B2 (ja) | ポリマー及びそれを用いた有機薄膜太陽電池 | |
| RU2694209C2 (ru) | Донорно-акцепторные олигомеры на основе трифениламина с п-фторфенилдициановинильными электроноакцепторными заместителями и способ их получения | |
| KR101424978B1 (ko) | 길만시약 화합물을 이용한 헤테로 융합고리 화합물의 신규한 제조방법 | |
| RU2788650C2 (ru) | Несимметричные люминесцентные донорно-акцепторные молекулы на основе трифениламин-тиофенового блока с различными электроноакцепторными группами и способ их получения | |
| JP2012236777A (ja) | インドロカルバゾール含有イミド化合物及び合成中間体、これらの製造方法、有機半導体組成物、ならびに有機太陽電池素子 | |
| JP5207516B2 (ja) | 2,3−ジシアノナフタレン誘導体の製造方法 | |
| KR101000784B1 (ko) | 덴드론구조가 치환된 폴리아센계 유기 화합물 및 이를이용한 유기박막트랜지스터 | |
| Yu et al. | Synthesis and through-space charge transfer of dioctyloxy diperfluorohexyl substituted [2.2] paracyclophane-1, 9-diene | |
| JP5408821B2 (ja) | ナフタロシアニン化合物及びその製造方法 | |
| JP7828052B2 (ja) | 5員環の縮合した縮合多環化合物の製造方法、インダセン誘導体、並びにp-フェニレンビニレン誘導体及びその製造方法 | |
| Crisp et al. | Preparation of Orthogonal π-Conjugated Aryl Alkynes and Cyclophanes |