RU2540481C2 - Офтальмологический раствор для защиты внутренних структур глазного яблока от уф-а лучей или для лечения кератоконуса методом трансэпителиального кросс-линкинга - Google Patents
Офтальмологический раствор для защиты внутренних структур глазного яблока от уф-а лучей или для лечения кератоконуса методом трансэпителиального кросс-линкинга Download PDFInfo
- Publication number
- RU2540481C2 RU2540481C2 RU2012106178/15A RU2012106178A RU2540481C2 RU 2540481 C2 RU2540481 C2 RU 2540481C2 RU 2012106178/15 A RU2012106178/15 A RU 2012106178/15A RU 2012106178 A RU2012106178 A RU 2012106178A RU 2540481 C2 RU2540481 C2 RU 2540481C2
- Authority
- RU
- Russia
- Prior art keywords
- riboflavin
- concentration
- cornea
- solution
- corneal
- Prior art date
Links
- 238000004132 cross linking Methods 0.000 title claims abstract description 50
- 201000002287 Keratoconus Diseases 0.000 title claims abstract description 28
- 239000002997 ophthalmic solution Substances 0.000 title claims abstract description 22
- 229940054534 ophthalmic solution Drugs 0.000 title claims abstract description 16
- 210000005252 bulbus oculi Anatomy 0.000 title claims abstract description 10
- AUNGANRZJHBGPY-SCRDCRAPSA-N Riboflavin Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-SCRDCRAPSA-N 0.000 claims abstract description 123
- AUNGANRZJHBGPY-UHFFFAOYSA-N D-Lyxoflavin Natural products OCC(O)C(O)C(O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-UHFFFAOYSA-N 0.000 claims abstract description 61
- 239000002151 riboflavin Substances 0.000 claims abstract description 61
- 229960002477 riboflavin Drugs 0.000 claims abstract description 61
- 235000019192 riboflavin Nutrition 0.000 claims abstract description 61
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 claims abstract description 31
- 229930003427 Vitamin E Natural products 0.000 claims abstract description 16
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 claims abstract description 16
- 239000011709 vitamin E Substances 0.000 claims abstract description 16
- 235000019165 vitamin E Nutrition 0.000 claims abstract description 16
- 229940046009 vitamin E Drugs 0.000 claims abstract description 16
- 239000000243 solution Substances 0.000 claims description 66
- 229920002307 Dextran Polymers 0.000 claims description 42
- 210000003560 epithelium corneal Anatomy 0.000 claims description 37
- 238000011282 treatment Methods 0.000 claims description 31
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 claims description 28
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 claims description 24
- 239000004471 Glycine Substances 0.000 claims description 15
- ACTIUHUUMQJHFO-UPTCCGCDSA-N coenzyme Q10 Chemical compound COC1=C(OC)C(=O)C(C\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CCC=C(C)C)=C(C)C1=O ACTIUHUUMQJHFO-UPTCCGCDSA-N 0.000 claims description 14
- 229960005337 lysine hydrochloride Drugs 0.000 claims description 14
- 229960002429 proline Drugs 0.000 claims description 14
- 229930064664 L-arginine Natural products 0.000 claims description 13
- 235000014852 L-arginine Nutrition 0.000 claims description 13
- 235000019454 L-leucine Nutrition 0.000 claims description 13
- 239000004395 L-leucine Substances 0.000 claims description 13
- 229930182821 L-proline Natural products 0.000 claims description 13
- 229960003136 leucine Drugs 0.000 claims description 13
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 claims description 12
- BVHLGVCQOALMSV-JEDNCBNOSA-N L-lysine hydrochloride Chemical compound Cl.NCCCC[C@H](N)C(O)=O BVHLGVCQOALMSV-JEDNCBNOSA-N 0.000 claims description 12
- ODKSFYDXXFIFQN-BYPYZUCNSA-N L-arginine Chemical compound OC(=O)[C@@H](N)CCCN=C(N)N ODKSFYDXXFIFQN-BYPYZUCNSA-N 0.000 claims description 11
- 235000017471 coenzyme Q10 Nutrition 0.000 claims description 11
- 150000001875 compounds Chemical class 0.000 claims description 10
- 230000035699 permeability Effects 0.000 claims description 9
- 239000003623 enhancer Substances 0.000 claims description 6
- 229960002449 glycine Drugs 0.000 claims description 6
- AOBORMOPSGHCAX-UHFFFAOYSA-N Tocophersolan Chemical compound OCCOC(=O)CCC(=O)OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C AOBORMOPSGHCAX-UHFFFAOYSA-N 0.000 claims description 5
- 239000003889 eye drop Substances 0.000 claims description 5
- 229940012356 eye drops Drugs 0.000 claims description 5
- 229940113116 polyethylene glycol 1000 Drugs 0.000 claims description 5
- 238000002360 preparation method Methods 0.000 claims description 5
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 claims description 5
- 230000001225 therapeutic effect Effects 0.000 claims description 5
- 229940100655 ophthalmic gel Drugs 0.000 claims 1
- 239000000126 substance Substances 0.000 abstract description 35
- 230000000694 effects Effects 0.000 abstract description 10
- 239000003814 drug Substances 0.000 abstract 1
- 210000004087 cornea Anatomy 0.000 description 82
- 239000000203 mixture Substances 0.000 description 56
- 238000012360 testing method Methods 0.000 description 42
- 238000000034 method Methods 0.000 description 20
- 239000012086 standard solution Substances 0.000 description 19
- 210000000981 epithelium Anatomy 0.000 description 16
- 230000035515 penetration Effects 0.000 description 16
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 15
- 210000000110 microvilli Anatomy 0.000 description 15
- MWUXSHHQAYIFBG-UHFFFAOYSA-N Nitric oxide Chemical compound O=[N] MWUXSHHQAYIFBG-UHFFFAOYSA-N 0.000 description 14
- 229960000686 benzalkonium chloride Drugs 0.000 description 13
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 13
- 230000005855 radiation Effects 0.000 description 12
- 239000010410 layer Substances 0.000 description 10
- 239000012085 test solution Substances 0.000 description 10
- 235000020776 essential amino acid Nutrition 0.000 description 9
- 239000003797 essential amino acid Substances 0.000 description 9
- 230000002262 irrigation Effects 0.000 description 9
- 238000003973 irrigation Methods 0.000 description 9
- 210000001519 tissue Anatomy 0.000 description 9
- 210000005081 epithelial layer Anatomy 0.000 description 8
- 210000001508 eye Anatomy 0.000 description 8
- 102000008186 Collagen Human genes 0.000 description 7
- 108010035532 Collagen Proteins 0.000 description 7
- 229920002385 Sodium hyaluronate Polymers 0.000 description 7
- 229920001436 collagen Polymers 0.000 description 7
- 229940010747 sodium hyaluronate Drugs 0.000 description 7
- YWIVKILSMZOHHF-QJZPQSOGSA-N sodium;(2s,3s,4s,5r,6r)-6-[(2s,3r,4r,5s,6r)-3-acetamido-2-[(2s,3s,4r,5r,6r)-6-[(2r,3r,4r,5s,6r)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2- Chemical compound [Na+].CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 YWIVKILSMZOHHF-QJZPQSOGSA-N 0.000 description 7
- 229920001285 xanthan gum Polymers 0.000 description 7
- 229940082509 xanthan gum Drugs 0.000 description 7
- 235000010493 xanthan gum Nutrition 0.000 description 7
- 239000000230 xanthan gum Substances 0.000 description 7
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 6
- 229960004747 ubidecarenone Drugs 0.000 description 6
- 230000000007 visual effect Effects 0.000 description 6
- 229940024606 amino acid Drugs 0.000 description 5
- 235000001014 amino acid Nutrition 0.000 description 5
- 150000001413 amino acids Chemical class 0.000 description 5
- 239000000969 carrier Substances 0.000 description 5
- 210000003683 corneal stroma Anatomy 0.000 description 5
- 238000002474 experimental method Methods 0.000 description 5
- 210000002919 epithelial cell Anatomy 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- 239000000546 pharmaceutical excipient Substances 0.000 description 4
- 229920006395 saturated elastomer Polymers 0.000 description 4
- 238000001228 spectrum Methods 0.000 description 4
- 239000002344 surface layer Substances 0.000 description 4
- 238000002054 transplantation Methods 0.000 description 4
- 102000001776 Matrix metalloproteinase-9 Human genes 0.000 description 3
- 108010015302 Matrix metalloproteinase-9 Proteins 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 208000021921 corneal disease Diseases 0.000 description 3
- 201000004573 corneal ectasia Diseases 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- CGIGDMFJXJATDK-UHFFFAOYSA-N indomethacin Chemical compound CC1=C(CC(O)=O)C2=CC(OC)=CC=C2N1C(=O)C1=CC=C(Cl)C=C1 CGIGDMFJXJATDK-UHFFFAOYSA-N 0.000 description 3
- -1 pyridin-2-ylcarbamoyl Chemical group 0.000 description 3
- 208000024891 symptom Diseases 0.000 description 3
- 230000002195 synergetic effect Effects 0.000 description 3
- AZQWKYJCGOJGHM-UHFFFAOYSA-N 1,4-benzoquinone Chemical compound O=C1C=CC(=O)C=C1 AZQWKYJCGOJGHM-UHFFFAOYSA-N 0.000 description 2
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 2
- XREILSQAXUAAHP-NXGXIAAHSA-N CC(C)=CCC/C(/C)=C/CC/C(/C)=C/CC(C(C(OC)=C1OC)=O)=C(C)C1=O Chemical compound CC(C)=CCC/C(/C)=C/CC/C(/C)=C/CC(C(C(OC)=C1OC)=O)=C(C)C1=O XREILSQAXUAAHP-NXGXIAAHSA-N 0.000 description 2
- 101000990902 Homo sapiens Matrix metalloproteinase-9 Proteins 0.000 description 2
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 description 2
- 102100030412 Matrix metalloproteinase-9 Human genes 0.000 description 2
- SBDNJUWAMKYJOX-UHFFFAOYSA-N Meclofenamic Acid Chemical compound CC1=CC=C(Cl)C(NC=2C(=CC=CC=2)C(O)=O)=C1Cl SBDNJUWAMKYJOX-UHFFFAOYSA-N 0.000 description 2
- ZRVUJXDFFKFLMG-UHFFFAOYSA-N Meloxicam Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=NC=C(C)S1 ZRVUJXDFFKFLMG-UHFFFAOYSA-N 0.000 description 2
- JZFPYUNJRRFVQU-UHFFFAOYSA-N Niflumic acid Chemical compound OC(=O)C1=CC=CN=C1NC1=CC=CC(C(F)(F)F)=C1 JZFPYUNJRRFVQU-UHFFFAOYSA-N 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000003855 balanced salt solution Substances 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 210000004045 bowman membrane Anatomy 0.000 description 2
- PUXBGTOOZJQSKH-UHFFFAOYSA-N carprofen Chemical compound C1=C(Cl)C=C2C3=CC=C(C(C(O)=O)C)C=C3NC2=C1 PUXBGTOOZJQSKH-UHFFFAOYSA-N 0.000 description 2
- RZEKVGVHFLEQIL-UHFFFAOYSA-N celecoxib Chemical compound C1=CC(C)=CC=C1C1=CC(C(F)(F)F)=NN1C1=CC=C(S(N)(=O)=O)C=C1 RZEKVGVHFLEQIL-UHFFFAOYSA-N 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- 210000003855 cell nucleus Anatomy 0.000 description 2
- GPUVGQIASQNZET-CCEZHUSRSA-N cinnoxicam Chemical compound C=1C=CC=CC=1/C=C/C(=O)OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=CC=CC=N1 GPUVGQIASQNZET-CCEZHUSRSA-N 0.000 description 2
- 230000001086 cytosolic effect Effects 0.000 description 2
- DCOPUUMXTXDBNB-UHFFFAOYSA-N diclofenac Chemical compound OC(=O)CC1=CC=CC=C1NC1=C(Cl)C=CC=C1Cl DCOPUUMXTXDBNB-UHFFFAOYSA-N 0.000 description 2
- HUPFGZXOMWLGNK-UHFFFAOYSA-N diflunisal Chemical compound C1=C(O)C(C(=O)O)=CC(C=2C(=CC(F)=CC=2)F)=C1 HUPFGZXOMWLGNK-UHFFFAOYSA-N 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000006196 drop Substances 0.000 description 2
- MNJVRJDLRVPLFE-UHFFFAOYSA-N etoricoxib Chemical compound C1=NC(C)=CC=C1C1=NC=C(Cl)C=C1C1=CC=C(S(C)(=O)=O)C=C1 MNJVRJDLRVPLFE-UHFFFAOYSA-N 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- LPEPZBJOKDYZAD-UHFFFAOYSA-N flufenamic acid Chemical compound OC(=O)C1=CC=CC=C1NC1=CC=CC(C(F)(F)F)=C1 LPEPZBJOKDYZAD-UHFFFAOYSA-N 0.000 description 2
- SYTBZMRGLBWNTM-UHFFFAOYSA-N flurbiprofen Chemical compound FC1=CC(C(C(O)=O)C)=CC=C1C1=CC=CC=C1 SYTBZMRGLBWNTM-UHFFFAOYSA-N 0.000 description 2
- 230000004907 flux Effects 0.000 description 2
- TZBJGXHYKVUXJN-UHFFFAOYSA-N genistein Natural products C1=CC(O)=CC=C1C1=COC2=CC(O)=CC(O)=C2C1=O TZBJGXHYKVUXJN-UHFFFAOYSA-N 0.000 description 2
- CYWFCPPBTWOZSF-UHFFFAOYSA-N ibufenac Chemical compound CC(C)CC1=CC=C(CC(O)=O)C=C1 CYWFCPPBTWOZSF-UHFFFAOYSA-N 0.000 description 2
- 229950009183 ibufenac Drugs 0.000 description 2
- 238000005470 impregnation Methods 0.000 description 2
- 230000007794 irritation Effects 0.000 description 2
- KHPKQFYUPIUARC-UHFFFAOYSA-N lumiracoxib Chemical compound OC(=O)CC1=CC(C)=CC=C1NC1=C(F)C=CC=C1Cl KHPKQFYUPIUARC-UHFFFAOYSA-N 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- HYYBABOKPJLUIN-UHFFFAOYSA-N mefenamic acid Chemical compound CC1=CC=CC(NC=2C(=CC=CC=2)C(O)=O)=C1C HYYBABOKPJLUIN-UHFFFAOYSA-N 0.000 description 2
- 238000001000 micrograph Methods 0.000 description 2
- CMWTZPSULFXXJA-VIFPVBQESA-N naproxen Chemical compound C1=C([C@H](C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-VIFPVBQESA-N 0.000 description 2
- HYWYRSMBCFDLJT-UHFFFAOYSA-N nimesulide Chemical compound CS(=O)(=O)NC1=CC=C([N+]([O-])=O)C=C1OC1=CC=CC=C1 HYWYRSMBCFDLJT-UHFFFAOYSA-N 0.000 description 2
- 239000000041 non-steroidal anti-inflammatory agent Substances 0.000 description 2
- 210000004940 nucleus Anatomy 0.000 description 2
- OFPXSFXSNFPTHF-UHFFFAOYSA-N oxaprozin Chemical compound O1C(CCC(=O)O)=NC(C=2C=CC=CC=2)=C1C1=CC=CC=C1 OFPXSFXSNFPTHF-UHFFFAOYSA-N 0.000 description 2
- TZRHLKRLEZJVIJ-UHFFFAOYSA-N parecoxib Chemical compound C1=CC(S(=O)(=O)NC(=O)CC)=CC=C1C1=C(C)ON=C1C1=CC=CC=C1 TZRHLKRLEZJVIJ-UHFFFAOYSA-N 0.000 description 2
- 230000007170 pathology Effects 0.000 description 2
- 239000002504 physiological saline solution Substances 0.000 description 2
- 230000002980 postoperative effect Effects 0.000 description 2
- 230000008439 repair process Effects 0.000 description 2
- RZJQGNCSTQAWON-UHFFFAOYSA-N rofecoxib Chemical compound C1=CC(S(=O)(=O)C)=CC=C1C1=C(C=2C=CC=CC=2)C(=O)OC1 RZJQGNCSTQAWON-UHFFFAOYSA-N 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- 238000005728 strengthening Methods 0.000 description 2
- YEZNLOUZAIOMLT-UHFFFAOYSA-N tolfenamic acid Chemical compound CC1=C(Cl)C=CC=C1NC1=CC=CC=C1C(O)=O YEZNLOUZAIOMLT-UHFFFAOYSA-N 0.000 description 2
- 230000000699 topical effect Effects 0.000 description 2
- LNPDTQAFDNKSHK-UHFFFAOYSA-N valdecoxib Chemical compound CC=1ON=C(C=2C=CC=CC=2)C=1C1=CC=C(S(N)(=O)=O)C=C1 LNPDTQAFDNKSHK-UHFFFAOYSA-N 0.000 description 2
- QZHGGBLUDJDFMD-UHFFFAOYSA-N 1,1-dioxo-2-(1,3-thiazol-2-yl)-1lambda6,2-benzothiazine-3-carboxamide Chemical compound S1C(=NC=C1)N1S(C2=C(C=C1C(=O)N)C=CC=C2)(=O)=O QZHGGBLUDJDFMD-UHFFFAOYSA-N 0.000 description 1
- KJMTZGRKMVZVAH-UHFFFAOYSA-N 1,1-dioxothiazin-4-one Chemical compound O=C1C=CS(=O)(=O)N=C1 KJMTZGRKMVZVAH-UHFFFAOYSA-N 0.000 description 1
- MFSJSVNVUDQHLV-UHFFFAOYSA-N 2-(3-benzoylphenyl)propanoic acid Chemical compound OC(=O)C(C)C1=CC=CC(C(=O)C=2C=CC=CC=2)=C1.OC(=O)C(C)C1=CC=CC(C(=O)C=2C=CC=CC=2)=C1 MFSJSVNVUDQHLV-UHFFFAOYSA-N 0.000 description 1
- MLKXDPUZXIRXEP-LQVWSKNFSA-N 2-[(3z)-6-fluoro-2-methyl-3-[[4-[(r)-methylsulfinyl]phenyl]methylidene]inden-1-yl]acetic acid Chemical compound CC1=C(CC(O)=O)C2=CC(F)=CC=C2\C1=C/C1=CC=C([S@@](C)=O)C=C1 MLKXDPUZXIRXEP-LQVWSKNFSA-N 0.000 description 1
- 125000005273 2-acetoxybenzoic acid group Chemical group 0.000 description 1
- SYCHUQUJURZQMO-UHFFFAOYSA-N 4-hydroxy-2-methyl-1,1-dioxo-n-(1,3-thiazol-2-yl)-1$l^{6},2-benzothiazine-3-carboxamide Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=NC=CS1 SYCHUQUJURZQMO-UHFFFAOYSA-N 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 208000002177 Cataract Diseases 0.000 description 1
- ACTIUHUUMQJHFO-UHFFFAOYSA-N Coenzym Q10 Natural products COC1=C(OC)C(=O)C(CC=C(C)CCC=C(C)CCC=C(C)CCC=C(C)CCC=C(C)CCC=C(C)CCC=C(C)CCC=C(C)CCC=C(C)CCC=C(C)C)=C(C)C1=O ACTIUHUUMQJHFO-UHFFFAOYSA-N 0.000 description 1
- 206010061788 Corneal infection Diseases 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 108010001103 Glutathione oxidase Proteins 0.000 description 1
- 229920002306 Glycocalyx Polymers 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- 241000446313 Lamella Species 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- CMWTZPSULFXXJA-UHFFFAOYSA-N Naproxen Natural products C1=C(C(C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-UHFFFAOYSA-N 0.000 description 1
- LDJVNWFKNMYYNT-FYWRMAATSA-N O=C1C2=CC=CC=C2S(=O)(=O)N(C)\C1=C(\O)NC1=CC=CC=N1 Chemical compound O=C1C2=CC=CC=C2S(=O)(=O)N(C)\C1=C(\O)NC1=CC=CC=N1 LDJVNWFKNMYYNT-FYWRMAATSA-N 0.000 description 1
- 206010067268 Post procedural infection Diseases 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- 208000003251 Pruritus Diseases 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 125000000738 acetamido group Chemical group [H]C([H])([H])C(=O)N([H])[*] 0.000 description 1
- 229960001138 acetylsalicylic acid Drugs 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 229940035676 analgesics Drugs 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 235000009697 arginine Nutrition 0.000 description 1
- 229960004277 benorilate Drugs 0.000 description 1
- FEJKLNWAOXSSNR-UHFFFAOYSA-N benorilate Chemical compound C1=CC(NC(=O)C)=CC=C1OC(=O)C1=CC=CC=C1OC(C)=O FEJKLNWAOXSSNR-UHFFFAOYSA-N 0.000 description 1
- 229960003184 carprofen Drugs 0.000 description 1
- 229960000590 celecoxib Drugs 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 229950001983 cinnoxicam Drugs 0.000 description 1
- 229940110767 coenzyme Q10 Drugs 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 230000002380 cytological effect Effects 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 229960001259 diclofenac Drugs 0.000 description 1
- 229960000616 diflunisal Drugs 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 229940120889 dipyrone Drugs 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 229960001850 droxicam Drugs 0.000 description 1
- OEHFRZLKGRKFAS-UHFFFAOYSA-N droxicam Chemical compound C12=CC=CC=C2S(=O)(=O)N(C)C(C2=O)=C1OC(=O)N2C1=CC=CC=N1 OEHFRZLKGRKFAS-UHFFFAOYSA-N 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- 229960005293 etodolac Drugs 0.000 description 1
- XFBVBWWRPKNWHW-UHFFFAOYSA-N etodolac Chemical compound C1COC(CC)(CC(O)=O)C2=N[C]3C(CC)=CC=CC3=C21 XFBVBWWRPKNWHW-UHFFFAOYSA-N 0.000 description 1
- 229960004945 etoricoxib Drugs 0.000 description 1
- RDJGLLICXDHJDY-UHFFFAOYSA-N fenoprofen Chemical compound OC(=O)C(C)C1=CC=CC(OC=2C=CC=CC=2)=C1 RDJGLLICXDHJDY-UHFFFAOYSA-N 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 229960004369 flufenamic acid Drugs 0.000 description 1
- 229960002390 flurbiprofen Drugs 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 235000006539 genistein Nutrition 0.000 description 1
- 229940045109 genistein Drugs 0.000 description 1
- ZCOLJUOHXJRHDI-CMWLGVBASA-N genistein 7-O-beta-D-glucoside Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=C2C(=O)C(C=3C=CC(O)=CC=3)=COC2=C1 ZCOLJUOHXJRHDI-CMWLGVBASA-N 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 210000004517 glycocalyx Anatomy 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 229960001680 ibuprofen Drugs 0.000 description 1
- 125000000593 indol-1-yl group Chemical group [H]C1=C([H])C([H])=C2N([*])C([H])=C([H])C2=C1[H] 0.000 description 1
- 229960000905 indomethacin Drugs 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 230000007803 itching Effects 0.000 description 1
- OZWKMVRBQXNZKK-UHFFFAOYSA-N ketorolac Chemical compound OC(=O)C1CCN2C1=CC=C2C(=O)C1=CC=CC=C1 OZWKMVRBQXNZKK-UHFFFAOYSA-N 0.000 description 1
- 229960004752 ketorolac Drugs 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- OXROWJKCGCOJDO-JLHYYAGUSA-N lornoxicam Chemical compound O=C1C=2SC(Cl)=CC=2S(=O)(=O)N(C)\C1=C(\O)NC1=CC=CC=N1 OXROWJKCGCOJDO-JLHYYAGUSA-N 0.000 description 1
- WLHQHAUOOXYABV-UHFFFAOYSA-N lornoxicam Chemical compound OC=1C=2SC(Cl)=CC=2S(=O)(=O)N(C)C=1C(=O)NC1=CC=CC=N1 WLHQHAUOOXYABV-UHFFFAOYSA-N 0.000 description 1
- 229960002202 lornoxicam Drugs 0.000 description 1
- 229960000994 lumiracoxib Drugs 0.000 description 1
- 229960003646 lysine Drugs 0.000 description 1
- 208000002780 macular degeneration Diseases 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 229960003803 meclofenamic acid Drugs 0.000 description 1
- 229960003464 mefenamic acid Drugs 0.000 description 1
- 229960001929 meloxicam Drugs 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- LVWZTYCIRDMTEY-UHFFFAOYSA-N metamizole Chemical compound O=C1C(N(CS(O)(=O)=O)C)=C(C)N(C)N1C1=CC=CC=C1 LVWZTYCIRDMTEY-UHFFFAOYSA-N 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- 230000000877 morphologic effect Effects 0.000 description 1
- 229960002009 naproxen Drugs 0.000 description 1
- 229960000916 niflumic acid Drugs 0.000 description 1
- 229960000965 nimesulide Drugs 0.000 description 1
- 238000000399 optical microscopy Methods 0.000 description 1
- 229960004662 parecoxib Drugs 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 239000003961 penetration enhancing agent Substances 0.000 description 1
- 150000002978 peroxides Chemical class 0.000 description 1
- 239000003075 phytoestrogen Substances 0.000 description 1
- 229960002702 piroxicam Drugs 0.000 description 1
- QYSPLQLAKJAUJT-UHFFFAOYSA-N piroxicam Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=CC=CC=N1 QYSPLQLAKJAUJT-UHFFFAOYSA-N 0.000 description 1
- 229960001369 piroxicam cinnamate Drugs 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 229960000371 rofecoxib Drugs 0.000 description 1
- 238000007665 sagging Methods 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 230000035807 sensation Effects 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 229950005175 sudoxicam Drugs 0.000 description 1
- MLKXDPUZXIRXEP-MFOYZWKCSA-N sulindac Chemical compound CC1=C(CC(O)=O)C2=CC(F)=CC=C2\C1=C/C1=CC=C(S(C)=O)C=C1 MLKXDPUZXIRXEP-MFOYZWKCSA-N 0.000 description 1
- 229960000894 sulindac Drugs 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000011477 surgical intervention Methods 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 229960002871 tenoxicam Drugs 0.000 description 1
- LZNWYQJJBLGYLT-UHFFFAOYSA-N tenoxicam Chemical compound OC=1C=2SC=CC=2S(=O)(=O)N(C)C=1C(=O)NC1=CC=CC=N1 LZNWYQJJBLGYLT-UHFFFAOYSA-N 0.000 description 1
- 150000003505 terpenes Chemical class 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 229960002905 tolfenamic acid Drugs 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-N trans-cinnamic acid Chemical compound OC(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-N 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 229960002004 valdecoxib Drugs 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 230000003313 weakening effect Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/20—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids
- A61K31/203—Retinoic acids ; Salts thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4415—Pyridoxine, i.e. Vitamin B6
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
- A61K31/51—Thiamines, e.g. vitamin B1
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
- A61K31/525—Isoalloxazines, e.g. riboflavins, vitamin B2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
Abstract
Изобретение относится к фармацевтической промышленности и представляет собой офтальмологический раствор, содержащий рибофлавин и витамин Е, для защиты внутренних структур глазного яблока от УФ-А-лучей или для лечения кератоконуса методом трансэпителиального кросс-линкинга. Изобретение обеспечивает расширение арсенала средств для защиты внутренних структур глазного яблока от УФ-А-лучей или для лечения кератоконуса методом трансэпителиального кросс-линкинга. 3 н. и 6 з.п. ф-лы, 10 ил.
Description
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение, в целом, относится к композициям для лечения и методам лечения кератоконуса и, более конкретно, к новому офтальмологическому раствору, применимому для защиты внутренних структур глазного яблока от УФ-А-лучей или при лечении с помощью роговичного кросс-линкинга.
УРОВЕНЬ ТЕХНИКИ
В книге [18] приводится обзор, описывающий проблемы и методы введения и усвоения офтальмологических растворов.
Роговичный (коллагеновый) кросс-линкинг (С3) с использованием рибофлавина (витамина В2), кратко называемый рибофлавин - С3, представляет собой инновационный метод лечения пациентов с кератоконусом и эктазией роговицы и заключается во введении рибофлавина и облучении ультрафиолетовым светом (УФ-А) для укрепления ткани роговицы [1], [2].
Лечение методом кросс-линкинга является относительно простым: рибофлавин по капле вливают в глаз (орошают глаз) и роговицу облучают соответствующей дозой УФ-А в течение пяти минут; процедуру затем повторяют шесть раз подряд, чтобы общее время УФ-А-облучения составляло 30 минут.
Наиболее важным клиническим показателем, который следует принимать во внимание при установлении пригодности для кросс-линкинга, является толщина роговицы, которая не должна быть менее 400 микрон.
Целью этого консервативного лечения кератоконуса является отсрочить или, как следует надеяться, исключить необходимость в пересадке (трансплантации) роговицы и повысить зрительную работоспособность пациентов, повышая качество их жизни [6], [7].
Метод кросс-линкинга применялся для лечения кератоконуса, патологии, характеризующейся прогрессирующим истончением роговицы по причине аномальной дряблости паренхимы роговицы вследствие пониженного сцепления коллагеновых волокон, из которых она состоит. При использовании УФ-А-излучения и рибофлавина между прилегающими молекулами коллагена роговицы образуются новые связи и обработанная роговица становится толще и крепче [3]. Роговица содержит несколько слоев коллагеновых нитей по толщине паренхимы; поперечные связи, так называемые "сшивки", которые связывают между собой различные слои коллагена, являются определяющими для жесткости роговицы. Целью кросс-линкинга роговичной ткани является повышение степени ее жесткости за счет образования большего числа этих поперечных связей.
Местное (топическое) применение (нанесение) рибофлавина на деэпителизированную роговицу с проницаемостью около 200 мкм и УФ-А-облучение молекул рибофлавина определяет нарушение химического равновесия молекул рибофлавина с последующим образованием свободных радикалов. Молекулы рибофлавина становятся неустойчивыми и стабилизируются путем связывания двух коллагеновых фибрилл. Между коллагеновыми фибриллами образуется ряд биохимических "мостиков" (т.е. сшивок), что приводит к общему укреплению роговичной ткани [3].
Фактически, лечение проводят после удаления наружного слоя роговицы (т.е. эпителия роговицы, роговичного эпителия). Этот способ осуществления кросс-линкинга (С3-R) кератоконуса и эктазии роговицы предполагает предварительное удаление роговичного эпителия с целью содействовать проникновению 0.1% стандартного раствора рибофлавин-декстрана (например, раствора, выпускаемого фирмой SOOFT ITALIA S.r.l. под торговой маркой RICROLIN™) в расположенную под ним строму, и стандарты этого лечения нормализуют к этим условиям. Согласно мнению сторонников этого метода, удаление эпителиального слоя необходимо для обеспечения (гарантии) наилучшей адсорбции раствора рибофлавина внутрь роговичной стромы и тем самым максимальной эффективности лечения.
К сожалению, удаление роговичного эпителия может вызвать зуд и жжение в глазах на следующий день после лечения и в последующие дни и временную нечеткость изображения; эти симптомы общеизвестны и сохраняются до восстановления роговичного эпителия и обычно лечатся в дни после C3-R [4-7] глазными каплями, содержащими нестероидные противовоспалительные препараты (НСПВС, NSAID), глазными каплями на основе заменителей натуральных слез и анальгетиков и применением терапевтических контактных линз.
Некоторые авторы доказывают, что можно осуществлять лечение C3-R по стандартной методике без удаления роговичного эпителия и что такое лечение будет эффективным и безопасным, как показывают полученные клинические результаты. Согласно этому методу лечение следует проводить без предварительного удаления роговичного эпителия (деэпителизации). Целью является избежать свойственных первому методу болезненных ощущений у пациентов, вызванных удалением эпителия, провести лечение в амбулаторных условиях и, в особенности, избежать риска послеоперационных инфекций, характерных для лечения, которое предполагает удаление эпителия с последующим обнажением нижних слоев роговицы. Сторонники такого способа осуществления лечения предлагают вводить рибофлавин в глаз (орошать глаз) в течение более продолжительного времени для обеспечения лучшей адсорбции рибофлавина в строму перед УФ-А-облучением [8].
Относительно того, удалять или нет эпителий при лечении кератоконуса и эктазии роговицы методом кросс-линкинга, в литературе имеются противоположные мнения.
С3-R лечение изучали и осуществляли после удаления роговичного эпителия с целью способствовать проникновению рибофлавина в строму роговицы. По имеющимся у авторов сведениям в литературе нет никакой информации об исследованиях по определению, проникает ли рибофлавин и в какой степени проникает в строму роговицы [9] при удалении или без удаления роговичного эпителия.
Осуществление кросс-линкинга без предварительной деэпителизации критикуется многими авторами, которые утверждают, что при таком способе рибофлавин не проходит через эпителий и что пока не показано, эффективно ли проникает или не проникает, а если проникает, то насколько, стандартный 0.1% раствор рибофлавин- декстрана в строму роговицы без удаления эпителия, и так же ли эффективно УФ-А облучение при трансэпителиальном способе, как и после удаления роговичного эпителия.
После попыток найти эффективные вещества для лечения кератоконуса методом кросс-линкинга без удаления роговичного эпителия Dr. Sporl предложил [17] использовать бензалкония хлорид для повышения проницаемости эпителия, а Dr. Pinelli предложил использовать смеси поверхностно-активных веществ с рибофлавином.
В итальянской патентной заявке No. MI2007A002162 [16] раскрывается новый раствор для лечения кератоконуса методом трансэпительного кросс-линкинга, содержащий рибофлавин и бензалкония хлорид.
Эксперименты, проведенные заявителями на роговице человека, результаты которых показаны ниже в данном описании, приводят к заключению, что второй метод, осуществляемый с применением стандартного раствора или композиции, предложенной Dr. Pinelli [16], не позволяет преодолеть трудности, вызванные удалением роговичного эпителия, так как он может разрушаться, при этом повышается риск инфицирования и изменения механизмов восстановления (репарации), которому подвергаются раскрытые (экспонированные) нижние слои.
Для осуществления кросс-линкинга роговицы было бы желательно иметь композицию, содержащую рибофлавин, которая могла бы проникать через роговичный эпителий за относительно короткое время и которая не поражала бы роговичный эпителий, что позволило бы избежать послеоперационных симптомов.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Заявители провели тщательное исследование с целью определить, насколько рибофлавин проникает самостоятельно или в смеси с другими продуктами ("энхансерами проницаемости") через роговицу человека с предварительным удалением или без предварительного удаления роговичного эпителия, а также эффективность и безопасность последующего лечения с применением УФ-А-облучения.
Было идентифицировано несколько подходящих веществ, выбранных из группы, состоящей из незаменимых и условно незаменимых (таких как аргинин, цистеин, глицин, глутамин, гистидин, пролин, серии и тирозин) аминокислот, кофермента Q, витамина E, L-пролина, глицина, лизина гидрохлорида, L-лейцина, L-аргинина и соединений, предназначенных для стимуляции продуцирования металлопротеиназы ММР9, более подробно рассмотренных ниже в данном описании, которые можно эффективно применять в качестве носителей ("энхансеров проницаемости") в офтальмологических растворах, пригодных для введения рибофлавина, в частности, со стандартным раствором рибофлавин-декстрана, через эпителий роговицы. Полученные таким образом офтальмологические растворы, которые могут продаваться в виде глазных капель, или в виде геля, или в виде водных растворов или эмульсий, или наносится на терапевтические контактные линзы, можно применять для лечения кератоконуса методом трансэпителиального кросс-линкинга, тем самым сохраняя роговичный эпителий.
Офтальмологические растворы могут в конечном счете содержать эксципиенты, например, такие как уксусная кислота, или вышеуказанные вещества перед смешением с рибофлавином можно обрабатывать уксусной кислотой или другим эксципиентом.
Помимо этого, данное изобретение предлагает применение по меньшей мере одного вещества, выбранного из группы, состоящей из незаменимых и условно незаменимых аминокислот, кофермента Q, витамина Е, L-пролина, глицина, лизина гидрохлорида, L-лейцина, L-аргинина и соединений, предназначенных для стимуляции продуцирования металлопротеиназы ММР9, более подробно рассмотренных ниже в данном описании, для приготовления офтальмологического раствора, содержащего рибофлавин, предназначенного для защиты внутренних структур глазного яблока от УФ-А-излучения или для лечения кератоконуса методом трансэпителиального кросс-линкинга и с применением соответствующего офтальмологического раствора, содержащего рибофлавин, в качестве носителя ("энхансера проницаемости") в композиции, пригодной для введения рибофлавина через роговичный эпителий.
Далее настоящее изобретение предлагает способ приготовления офтальмологического раствора, заключающийся в добавлении к раствору рибофлавина по меньшей мере одного из идентифицированных выше носителей.
Каждое из предлагаемых в качестве носителя веществ можно добавлять самостоятельно или в комбинации с другими предлагаемыми носителями к раствору, содержащему рибофлавин, в концентрациях, выбранных в интервалах концентраций, указанных в нижеприведенном описании типичных вариантов изобретения.
Объем изобретения определяется в прилагаемой Формуле изобретения.
КРАТКОЕ ОПИСАНИЕ ФИГУР
На Фиг.1 представлена визуальная, флуорометрическая, колориметрическая оценочная шкала, принятая для оценки прохождения 0.1% раствора рибофлавина через роговицу после нанесения трансэпителиальным способом.
На Фиг.2а представлено флуороскопическое изображение среза роговицы, на которую трансэпителиальным способом наносят четвертую тестируемую (тест-) композицию (орошают ею), через 15 минут.
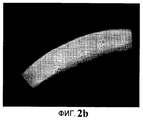
На Фиг.2b представлено флуороскопическое изображение среза роговицы, на которую трансэпителиальным способом наносят четвертую тестируемую (тест-) композицию, через 30 минут.
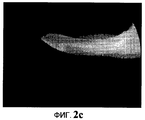
На Фиг.2c представлено флуороскопическое изображение среза роговицы, пролеченной методом трансэпителиального кросс-линкинга с применением четвертого нового раствора, на котором после обработки можно обнаружить интенсивную флуоресценцию вследствие прохождения четвертой композиции и релевантную жесткость ткани.
На Фиг.3а показана степень искривления роговицы, пролеченной трансэпителиальным кросс-линкингом с применением стандартного раствора.
На Фиг.3b показана степень искривления роговицы, пролеченной трансэпителиальным кросс-линкингом с применением четвертого нового тест-раствора.
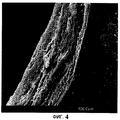
На Фиг.4 представлено изображение, сделанное с помощью сканирующего микроскопа, на котором видны ламеллы в срезе роговицы, пораженной кератоконусом.
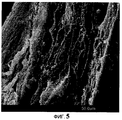
На Фиг.5 представлено сделанное с помощью сканирующего микроскопа увеличенное изображение роговицы на Фиг.4.
На Фиг.6 представлено изображение, сделанное с помощью сканирующего микроскопа, на котором видны ламеллы в срезе роговицы, пораженной кератоконусом, после трансэпителиального кросс-линкинга, проведенного с применением четвертой новой тестируемой композиции.
На Фиг.7 представлено изображение, сделанное с помощью сканирующего микроскопа, на котором показана морфология микроворсинок и поверхностных слоев эпителия в здоровой (нормальной) роговице.
На Фиг.8 представлено изображение, сделанное с помощью сканирующего микроскопа, на котором показана роговица, пролеченная стандартной дозой УФ-А-облучения после трансэпителиального нанесения стандартного 0.1% раствора рибофлавин-декстрана.
На Фиг.9 представлено изображение, сделанное с помощью сканирующего микроскопа, на котором показана роговица, пролеченная стандартной дозой УФ-А-облучения после трансэпителиального нанесения четвертой новой тестируемой композиции.
На Фиг.10 представлено изображение, сделанное с помощью сканирующего микроскопа, на котором показана роговица, пролеченная стандартной дозой УФ-А-облучения после трансэпителиального нанесения физиологического раствора.
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Все испытания проводят на человеческой роговице доноров, полученной из Azienda Ospedaliera Napoli 1 - Banca Occhi ("Eye Bank") - Regione Campania - Ospedale dei Pellegrini, после согласия, как предусмотрено протоколом эксплантации и в соответствии с разрешением Комиссии по этике - No. 0009304/2009 - Решение No.1269.
Наблюдают проникновение (пенетрацию) испытуемых композиций через целую человеческую роговицу, т.е. без предварительного удаления эпителия, причем роговица имеет толщину между 500 и 600 микрон, композиции представляют собой стандартный раствор рибофлавин-декстрана, композицию, приготовленную из рибофлавина-декстрана плюс бензалкония хлорид, предлагаемую в [16] и [17], и новые тестируемые (тест-) композиции, полученные смешением рибофлавина по меньшей мере с одним веществом, выбранным из группы, включающей витамин E, кофермент Q, L-пролин, глицин, лизина гидрохлорид, L-лейцин, в определенных концентрациях.
Концентрации веществ, используемые для создания (осуществления) новых тестируемых композиций, составляют следующие интервалы:
витамин Е: интервал концентраций составляет от 0.0001 мг % мл до 2000 мг % мл. Согласно более предпочтительному варианту изобретения интервалы концентраций составляют от 0.01 мг % до 1500 мг % мл. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют от 10 мг % мл до 1000 мг % мл. Согласно еще более предпочтительному варианту изобретения концентрация равна, примерно, 500 мг % мл;
витамин Q: интервал концентраций составляет от 0.0001 мг % мл до 2000 мг % мл. Согласно более предпочтительному варианту изобретения интервалы концентраций составляют от 0.01 мг % до 1500 мг % мл. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют от 1 мг % мл до 1000 мг % мл. Согласно еще более предпочтительному варианту изобретения концентрация равна, примерно, 100 мг % мл;
L-пролин: интервал концентраций составляет от 0.0001 мг % мл до 2000 мг % мл. Согласно более предпочтительному варианту изобретения интервалы концентраций составляют от 0.001 мг % до 100 мг % мл. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют от 0.005 мг % мл до 10 мг % мл. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют от 0.01 мг % мл до 1 мг % мл. Согласно еще более предпочтительному варианту изобретения концентрация равна, примерно, 0.1 мг % мл;
глицин: интервал концентраций составляет от 0.0001 мг % мл до 2000 мг % мл. Согласно более предпочтительному варианту изобретения интервалы концентраций составляют от 0.001 мг % до 100 мг % мл. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют от 0.005 мг % мл до 10 мг % мл. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют от 0.01 мг % мл до 1 мг % мл. Согласно еще более предпочтительному варианту изобретения концентрация равна, примерно, 0.1 мг % мл;
лизина гидрохлорид: интервал концентраций составляет от 0.0001 мг % мл до 2000 мг % мл. Согласно более предпочтительному варианту изобретения интервалы концентраций составляют от 0.001 мг % до 100 мг % мл. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют от 0.005 мг % мл до 10 мг % мл. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют от 0.01 мг % мл до 1 мг % мл. Согласно еще более предпочтительному варианту изобретения концентрация равна, примерно, 0.05 мг % мл;
L-лейцин: интервал концентраций составляет от 0.0001 мг % мл до 2000 мг % мл. Согласно более предпочтительному варианту изобретения интервалы концентраций составляют от 0.001 мг % до 100 мг % мл. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют от 0.005 мг % мл до 10 мг % мл. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют от 0.01 мг % мл до 1 мг % мл. Согласно еще более предпочтительному варианту изобретения концентрация равна, примерно, 0.08 мг % мл.
Новые растворы, применимые для лечения кератоконуса методом трансэпителиального кросс-линкинга или для защиты глазного яблока от УФ-А-излучения, получают смешением одного или нескольких вышеописанных веществ в указанных интервалах концентраций, с раствором, содержащим рибофлавин, например с раствором рибофлавин-декстрана в концентрации, выбранной из интервала концентраций от 0.0001% до 0.5%. Согласно более предпочтительному варианту изобретения интервалы концентраций раствора рибофлавин-декстрана составляют от 0.001% до 0.4%. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют от 0.005% до 0.3%. Согласно еще более предпочтительному варианту изобретения интервалы концентраций составляют, примерно, от 0.01% до 0.2%. Согласно еще более предпочтительному варианту изобретения концентрация равна, примерно, 0.1%.
Результаты испытаний показывают, что каждое из веществ идентифицированной группы применимо для содействия проникновению (пенетрации) рибофлавина и, в частности стандартного раствора рибофлавин-декстрана, через эпителий роговицы и для защиты роговицы от УФ-А-излучения.
Роговицу, применяемую (принимаемую во внимание) в испытании, отбракованную в банке роговицы из-за непригодности для трансплантации, хранят в соответствующих растворах, а перед испытаниями ее снова проверяют методом оптической микроскопии и путем изучения эндотелиальных клеток.
Используют только роговицу с высокой прозрачностью, толщиной в интервале от 500 до 600 микрон, с хорошей эндотелиальной мозаикой, в соответствии с тем, что предлагается в [10-15].
Роговицу располагают таким образом, чтобы накрыть цилиндрическую камеру, содержащую 0.4 мл заданного (предварительно определенного) раствора гиалуроната натрия плюс ксантановая камедь. На поверхность роговицы накладывают водозащитное герметизирующее металлическое кольцо того же диаметра, что и цилиндрический бокс. Затем на поверхность роговицы наносят испытуемые композиции, содержащие флуоресцентное вещество (рибофлавин). Измеряя флуоресценцию раствора внутри бокса в различные моменты, можно определить, какой объем новых растворов проникает в роговицу и какое время затрачивается на это.
Эффективность указанных веществ в качестве носителей в композициях для трансэпителиального введения рибофлавина и композиций, полученных смешением рибофлавина по меньшей мере с одним из указанных веществ, описывают на нижеприведенных примерах испытаний, только для иллюстрации, а не с целью ограничения.
Для краткости описываются только результаты испытаний, полученные при обработке роговицы следующими композициями:
1) стандартным 0.1% раствором рибофлавин-декстрана;
2) стандартным 0.1% раствором рибофлавин-декстрана+0.01% бензалкония хлорида в соответствии с [16];
3) первой новой тестируемой композицией, содержащей 0.1% рибофлавин-декстран+витамин E TPGS (D-альфа токоферил полиэтиленгликоль 1000 сукцинат) в концентрации 500 мг % мл;
4) второй новой тестируемой композицией, содержащей 0.1% рибофлавин-декстран+витамин Q 100 мг % мл;
5) третьей новой тестируемой композицией, содержащей 0.1% рибофлавин декстран+L-пролин 0.1 мг %+глицин 0.1 мг %, лизина гидрохлорид 0.05 мг %+L-лейцин 0.08 мг %;
6) четвертой новой тестируемой композицией, содержащей 0.1% рибофлавин-декстран+витамин Е (D-альфа токоферил полиэтиленгликоль 1000 сукцинат) 500 мг % мл+витамин Q 100 мг % мл+L-пролин 0.1 мг %+глицин 0.1 мг %+лизина гидрохлорид 0.05 мг %+L- лейцин 0.08 мг %.
Каждую из шести указанных композиций наносят на поверхность роговицы, выбранной и размещенной, как описано выше, и через 15 минут и через 30 минут оценивают пропитывание стромы роговицы вместе с присутствием флуоресцентного вещества в растворе гиалуроната натрия+ксантановая камедь 0.4 мл, помещенном внутрь контейнера под обрабатываемой роговицей.
Определение проникновения рибофлавина в строму роговицы проводят, делая срезы стромы с последующей оценкой под флуоресцентным микроскопом.
Присутствие рибофлавина в растворе гиалуроната натрия+ксантановая камедь 0.4 мл, которое демонстрирует проникновение через роговицу, оценивают как качественно, используя визуальную и флуоресцентную шкалу, как показано на Фиг.1, так и количественно по колориметрической шкале. Две цифры около каждого образца цвета обозначают соответственно число частей стандартного раствора рибофлавина, которое дает показанный цвет, и число частей раствора ксантановой камеди и гиалуроната натрия. Стандартную шкалу определяют, готовя разведения раствора рибофлавин- декстран 0.1% с ксантановой камедью+гиалуронатом натрия в следующих пропорциях (единицы/мл): 50/0, 40/10, 30/20, 20/30, 10/40, 0/50. Готовят визуальную шкалу и флуориметрическую шкалу, соответствующие определенным значениям в единицах/мл, и каждое разведение оценивают в баллах от 10 до 0. На колориметрической шкале предполагается минимальное процентное содержание желтого, равное 20% в отсутствие рибофлавина, оно соответствует колориметрическому спектру вещества, выбранного в качестве разбавителя.
Оценку по визуальной шкале проводят в условиях стандартного освещения путем непосредственного сравнения экспериментальных образцов со стандартным образцом и методом цифровой фотографии. Флуориметрическую оценку проводят с помощью флуоресцентного сканирующего микроскопа, снабженного цифровой фотокамерой, в темной комнате. Относительную оценку по визуальной и колориметрической шкале проводит третий исследователь на основании средних значений, полученных двумя методами.
Колориметрическую оценку осуществляют, помещая материал, имеющийся в конце эксперимента, внутрь цилиндрической камеры (и, следовательно, под роговицу) в прозрачную тару, и с помощью компьютерного анализа, сканируя при высоком разрешении предварительно определенные (готовые) растворы и оценивая процентное содержание желтого цвета с применением программы Photoshop™ 7.0 и монохромного фильтра. Таким способом можно сравнивать детектируемое процентное содержание желтого цвета в экспериментальных образцах с точно определенными концентрациями, выражаемыми в ед./мл, стандартного 0.1% раствора рибофлавина, как показано на Фиг.1.
На Фиг.2а представлено флуороскопическое изображение среза роговицы, обработанной методом трансэпителиального кросс-линкинга, после нанесения четвертого нового раствора (орошения четвертым новым раствором) в течение 15 минут. На Фиг.2b представлено флуороскопическое изображение среза роговицы, обработанной методом трансэпителиального кросс-линкинга, после нанесения четвертого нового раствора (орошения четвертым новым раствором) в течение 30 минут. На Фиг.2с представлено флуороскопическое изображение среза роговицы, обработанной методом трансэпителиального кросс-линкинга четвертым новым раствором. На этой последней фигуре можно заметить, что рибофлавин проник по всей роговице и что после кросс-линкинга ткань стала более жесткой.
Проведенные испытания показывают, что:
а) после 15 минут трансэпителиального нанесения (орошения) стандартного 0.1% раствора рибофлавин-декстрана строма роговицы частично пропитана, а флуоресцентный раствор не обнаруживается в веществе внутри контейнера, причем колориметрический спектр налагается на спектр (совместим со спектром) раствора гиалуронат натрия+ксантановая камедь 0.4 мл (оценка 0, как на Фиг.1 и процентное содержание желтого цвета на выше 20%);
б) после 30 минут трансэпителиального нанесения (орошения) стандартного 0.1% раствора рибофлавин-декстрана строма роговицы, по- видимому, полностью пропитана флуоресцентным раствором; можно оценить флуоресценцию в растворе гиалуронат натрия+ксантановая камедь 0.4 мл в контейнере 2- 3 баллами (Фиг.1), а процентное содержание желтого цвета, определенное вышеуказанным компьютерным методом, находится в диапазоне 75%- 80%;
в) после 15 минут трансэпителиального нанесения (орошения) первого нового тест-раствора (испытуемого, тестируемого раствора) 0.1% рибофлавин-декстран+витамин E TPGS (D-альфа-токоферил полиэтиленгликоль 1000 сукцинат) в концентрации 500 мг % мл, роговица полностью пропитана и внутри контейнера имеется флуоресцентный раствор (оценка 2-3 на Фиг.1, процентное содержание желтого цвета составляет 72-76%);
г) после 30 минут трансэпителиального нанесения (орошения) первого нового тест-раствора все слои роговицы полностью пропитаны, а внутри контейнера наблюдается высокая концентрация рибофлавина, что демонстрирует хорошую проницаемость ткани роговицы для самого продукта при контакте с поверхностью (оценка 3- 4 на Фиг.1, процентное содержание желтого цвета составляет 79- 84%);
д) композиция, предложенная в [16], и новые тест-растворы второй и третий, содержащие, соответственно: бензалкония хлорид 0.01%; витамин Q 100 мг % мл; L-пролин 0.1 мг %, глицин 0.1 мг %, лизина гидрохлорид 0.05 мг % и L-лейцин 0.08 мг %, демонстрируют, в тех же самых условиях, лучшее проникновение (пенетрацию) рибофлавина как в количественном отношении, так и с точки зрения скорости проникновения, чем один стандартный раствор (рибофлавин- декстран 0.1%) (оценка 3-4 на Фиг.1 через 15 минут и оценка 4-6 через 30 минут, с процентным содержанием желтого цвета 70-79% через 15 минут и 78-86% через 30 минут);
е) четвертая новая тестируемая композиция дает результаты, даже превосходящие результаты всех других тестируемых композиций. Различные концентрации окрашивающего вещества, обнаруживаемые с помощью флуоресценции и компьютерным анализом флуоресцентного вещества внутри контейнера после 15 минут и после 30 минут нанесения (орошения) продукта на поверхность эпителия, являются исключительно высокими (оценка 5- 6 на Фиг.1 через 15 минут, процентное содержание желтого цвета составляет 88- 91%; оценка 6-7 через 30 минут, содержание желтого цвета выше 90%»); более высокая концентрация флуоресцентного вещества в растворе, находящемся под роговицей, после трансэпителиального применения (орошения) четвертого нового тестируемого раствора (тест-раствора) становится, в частности, очевидной через 15 минут, в особенности по сравнению с результатами, полученными при применении стандартного раствора, который даже не обнаруживается в растворе внутри контейнера через то же самое время. Это можно объяснить, если предположить, что энхансеры проницаемости, при совместном применении (при смешении), проявляют синергический эффект, способствуя прохождению рибофлавина через роговичный эпителий.
Проиллюстрированные результаты показывают, что по меньшей мере следующие вещества:
- витамин E
где R1 обозначает CH3 или Н; R2 обозначает CH3 или Н; R3 обозначает CH3; можно привести, только в качестве примера витамин Е TPGS (D- альфа-токоферил полиэтиленгликоль 1000 сукцинат);
- кофермент Q
в окисленной форме,
в форме полухинона,
в восстановленной форме,
независимо от числа изопреноидных звеньев кофермента Q; только в качестве примера можно привести кофермент Q10;
- L- пролин
- глицин
- лизин
или лизина гидрохлорид;
- L-лейцин
самостоятельно или в их комбинации друг с другом, в конечном счете в комбинации с эксципиентами, такими как уксусная кислота, и в концентрации, выбранной в указанных выше интервалах, способствуют проникновению (пенетрации) рибофлавина через эпителий роговицы за более короткие временные интервалы, нежели временные интервалы, требующиеся для стандартного раствора рибофлавин-декстрана, и в количествах, достаточных для последующего кросс-линкинга.
Комбинация всех указанных соединений с рибофлавином проявляет неожиданный синергический эффект, давая лучшие результаты с точки зрения концентрации продукта, который проходит через ткани роговицы, и с точки зрения скорости, с которой он проникает через эти ткани.
Заявители проверяют in vitro эффективность трансэпителиального кросс-линкинга на человеческой роговице, нанося четвертую новую тестируемую композицию на человеческую роговицу и облучая УФ-А-лучами при потоке мощности 3 мВт/см в соответствии со стандартным протоколом. Роговицу для испытания готовят как в предыдущем эксперименте, фиксируя ее на соответствующей опоре и нанося (орошение) стандартный 0.1% раствор рибофлавин-декстрана и четвертую новую тестируемую композицию на поверхность эпителия (т.е. трансэпителиально) соответствующей роговицы в течение тридцати минут. Затем проводят стандартное УФ-А-облучение в течение тридцати минут, облучение проводят ступенчато (постадийно), по 5 минут стадия, с предшествующим повторным нанесением каждого раствора на поверхность роговицы. В конце эксперимента степень жесткости роговицы оценивают следующим образом: каждую роговицу поддерживают за концевой участок длиной 2 мм пинцетом для роговицы, находящимся в горизонтальном положении, и измеряют угол, образованный противоположным концом роговицы относительно горизонтали.
На Фиг.3а показана роговица после трансэпителиального кросс-линкинга, проводимого с применением стандартного 0.1% раствора рибофлавин-декстрана, которая изгибается вниз, примерно, на 40°, а на Фиг.3b показана другая роговица после кросс-линкинга, проводимого с применением четвертой новой тестируемой композиции и без предварительного удаления эпителия роговицы. При сравнении двух фигур становится очевидным, что трансэпителиальный кросс-линкинг с применением четвертой новой тестируемой композиции укрепляет роговицу, которая изгибается книзу только на 25°, что и требовалось.
Для дополнительного подтверждения эффективности трансэпителиального кросс-линкинга с применением четвертой новой тестируемой композиции этот метод лечения осуществляют in vitro на концевых участках человеческой роговицы от больных с кератоконусом, которые подверглись перфоративной кератопластике; в этих случаях вместо уничтожения роговицы, эксплантированной у пациента, ее использовали в лаборатории, обратив внимание на то, что в этом случае избегают диатермии в ходе операции, так что сохраняются поверхности слоев роговицы (трансплантация полной толщины). Лимбы (края) роговиц фиксируют на подходящей опоре. Стандартный 0.1% раствор рибофлавин-декстрана наносят на первую роговицу, а четвертый новый тестируемый раствор наносят на вторую роговицу, орошая поверхность роговиц растворами в течение тридцати минут без удаления эпителия. Затем осуществляют стандартное 340 нм УФ-А-облучение только роговицы, обработанной четвертым тестируемым раствором с потоком мощности 3 мВт/см в течение тридцати минут, разделенные на стадии по 5 минут каждая с предшествующим повторным нанесением композиции на поверхность роговицы. Другой концевой участок кератоконуса, фиксированный на подходящей подложке, обрабатывают только нанесением на роговицу стандартного раствора 0.1% рибофлавин- декстрана без последующего УФ-А-облучения. По окончании эксперимента проводят изучение паренхимы роговицы под сканирующим электронным микроскопом.
На Фиг.4 показано изображение ламелл среза роговицы пациента с непролеченным (необработанным) кератоконусом под сканирующим микроскопом. На Фиг.5 дано увеличенное изображение фрагмента Фиг.4. Эти две фигуры показывают ослабление ламелл на концевом участке роговицы, на которую наносят стандартный 0.1% раствор рибофлавин-декстрана, без УФ-А-облучения.
На Фиг.6 дано изображение под сканирующим микроскопом, на котором видно, как выглядят ламеллы среза роговицы, пораженной кератоконусом, после трансэпителиального кросс-линкинга с применением нового четвертого тестируемого раствора. Концевой участок кератоконуса (конической роговицы), пролеченного четвертым новым раствором, применяемым трансэпителиально, и УФ-А-облучением согласно стандартному протоколу, в течение тридцати минут, демонстрирует очень плотно (густо) распределенные и компактные ламеллы роговицы, которые показывают, что образовались новые биохимические поперечные связи.
Хорошие результаты получены также с новыми тестируемыми композициями первой, второй и третьей. Полученные результаты с применением новых тест-композиций также опровергают возражения некоторых авторов, заявляющих о гипотетическом ослаблении эффекта кросс-линкинга при осуществлении его трансэпителиальным методом, так как эпителий задерживает УФ-А-лучи. Предположение о снижении эффективности трансэпителиального кросс-линкинга неверно, как доказывают гистологические образцы, полученные в случае, когда к рибофлавину в качестве носителя (энхансера проницаемости) добавляют по меньшей мере одно из предлагаемых в данном описании веществ и облучение проводят в соответствии со стандартным протоколом.
Помимо этого, с помощью сканирующего электронного микроскопа (7500х) проводят сравнительное исследование действия трансэпителиального кросс-линкинга на морфологическую целостность или отсутствие целостности эпителиальных слоев роговицы и микроворсинок на поверхности эпителиальных клеток. Это исследование осуществляют с целью оценки переносимости трансэпителиального кросс-линкинга с применением четвертой новой тестируемой композиции на эпителии роговицы по сравнению со стандартным 0.1% раствором рибофлавин-декстрана и со смесью стандартная композиция+бензалкония хлорид 0.01%, предлагаемой в [16].
Этот тест проводят потому, что эпителиальные клетки представляют собой первые органические структуры, облучаемые потоком УФ-А, и могут поражаться вследствие поглощения этих лучей. По-видимому, ни в одной из имеющихся публикаций не рассматривается этот аспект, и в литературе отсутствуют соответствующие данные.
Показатели, рассматриваемые как наиболее надежные для оценки жизнеспособности эпителиальных клеток, получают в ходе цитологического исследования "впечатления", "оттиска" и, в частности, исследования под электронным микроскопом микроворсинок клеток поверхностного слоя эпителия роговицы. Наличие внешних изгибов мембраны (микроворсинок) цельных поверхностных клеточных элементов, содержащих в высокой концентрации муцины и достаточно гликокаликса, способствует оптимальному связыванию свободного муцина, из которого состоит глубокий слой предроговичной слезной пленки. Напротив, обусловленная болезнью (патологическая) утрата микроворсинок определяет трудность адгезии слоя слезной пленки к поверхности глаза и явления раздражения эпителия, вызванные дисфункцией самой предроговичной слезной пленки и, как следствие, воспаление.
Морфологию микроворсинок изучают под сканирующим электронным микроскопом после трансэпителиальной обработки in vitro УФ-А-лучами в соответствии со стандартными дозами. Человеческую роговицу толщиной от 500 до 600 микрон инкубируют в течение тридцати минут со сбалансированном солевым раствором, со стандартным 0.1% раствором рибофлавин-декстрана, со стандартным раствором+бензалкония хлорид 0.01% и с четвертой новой тестируемой композицией соответственно.
Предварительно изучают морфологию микроворсинок и поверхностного слоя эпителия роговицы, не подвергавшегося какой-либо обработке, с целью продемонстрировать, как должны выглядеть эпителиальные клетки и их микроворсинки, не подвергавшиеся никакой фотохимической обработке.
На Фиг.7 дано изображение под сканирующим микроскопом, которое показывает морфологию микроворсинок и поверхностного слоя эпителия в нормальной (здоровой) роговице, а на Фиг.8 представлено сделанное сканирующим микроскопом изображение роговицы (образцов роговицы), подвергшейся УФ-А-облучению после нанесения стандартного 0.1% раствора рибофлавин-декстрана в соответствии со стандартным протоколом. При сравнении с Фиг.7 видно, что все эпителиальные слои утрачены и мембрана Боумена обнажена.
Аналогичная ситуация наблюдается в тех образцах роговицы, которые обработаны композицией, содержащей стандартный раствор+бензалкония хлорид 0.01%, предложенной в [16].
На Фиг.9 представлено сделанное с помощью электронного микроскопа изображение роговицы, получавшей УФ-облучение в стандартной дозе после обработки четвертой новой тестируемой композицией. При сравнении с Фиг.7 и 8 можно заметить сохранение эпителиальных слоев, клеточных ядер и щелевидных соединений. Помимо этого, наблюдается значительное уменьшение плотности микроворсинок, хотя оставшиеся микроворсинки являются морфологически целыми, а глубже расположенная цитоплазматическая клеточная мембрана не подвергается опасности. Аналогичные результаты получают с первой, второй и третьей новыми тестируемыми композициями.
На Фиг.10 показано полученное с помощью сканирующего микроскопа изображение роговицы, облученной УФ-А в стандартной дозе, с применением, для сравнения, только физиологического раствора. Эпителиальные слои нарушены, многие клетки утратили ядра, и почти все щелевидные соединения и микроворсинки утрачены.
Полученные результаты можно кратко сформулировать следующим образом:
1) образцы роговицы, подвергшиеся УФ-А-облучению с предварительной инкубацией со стандартным 0.1% раствором рибофлавин-декстрана или с композицией, содержащей стандартный раствор+бензалкония хлорид 0.01% согласно стандартному протоколу, претерпевают тотальную утрату всех эпителиальных слоев и в результате боуменова мембрана становится обнаженной (Фиг.8). Фактически при использовании только стандартного раствора, к которому в конечном счете добавляют бензалкония хлорид, эпителий разрушается под действием УФ-А-излучения. Это заставляет думать, что кросс-линкинг, проводимый без удаления эпителия и с применением либо стандартного раствора, либо композиции рибофлавин-декстран+бензалкония хлорид, не позволит пациентам после лечения избежать симптомов раздражения, вызываемых хирургическим удалением эпителия;
2) образцы роговицы, получавшие стандартную дозу УФ-А-облучения после инкубации с композициями, содержащими рибофлавин-декстран и по меньшей мере носитель, выбранный из указанных выше носителей, и, в особенности, с четвертой новой тестируемой композицией, сохраняют свои эпителиальные слои, клеточные ядра и щелевидные соединения. Наблюдается заметное уменьшение плотности микроворсинок, хотя оставшиеся микроворсинки являются морфологически целыми. Глубже расположенная цитоплазматическая клеточная мембрана роговицы является целой;
3) в образцах роговицы, получавших стандартную дозу УФ-А-облучения после инкубации со сбалансированным солевым раствором (BSS), наблюдается разрушение эпителиальных слоев, утрата многочисленных клеток, эндоплазматических ядер и почти всех щелевидных соединений и микроворсинок.
С помощью сканирующего микроскопа получено также множество изображений образцов роговицы, обработанных новыми первой, второй и третьей композициями, но в данном описании они не приводятся, потому что они выглядят практически идентично изображениям роговицы, обработанной с помощью четвертой новой тестируемой композиции.
Эти результаты заставляют сделать вывод, что по меньшей мере витамин E, витамин Q или кофермент Q, тестированные аминокислоты, такие как L-пролин, глицин, лизина гидрохлорид и L-лейцин, помогают защитить эпителий роговицы и содействовать проникновению рибофлавина через эпителий роговицы. Из новых растворов, предлагаемых в данной заявке, четвертая композиция проявляет наилучшие показатели как с точки зрения времени проникновения, так и с точки зрения сохранения эпителия роговицы.
Пока не совсем ясно, почему предлагаемые вещества способствуют достижению таких замечательных результатов и почему вещества, используемые в четвертой тестируемой композиции, проявляют синергический эффект. Не ограничивая изобретение какой-либо теорией, заявители предполагают, что менее заметные поражения эпителия роговицы, которые обнаруживаются поле обработки четвертой новой тестируемой композицией, могут быть вызваны циторепаративным действием витамина E, например витамина Е-TPGS, и/или присутствием в растворе по меньшей мере одной незаменимой или частично незаменимой аминокислоты. Возможно, витамин E действует на глутатион оксидазу и на пероксиддисмутазу, которые являются ферментами, участвующими в репарации эпителия, или незаменимые или условно незаменимые аминокислоты оказывают циторепаративное действие и, вероятно, также будут способствовать эффекту кросс-линкинга. Кроме того, более полная пропитка ткани четвертым новым раствором определяет, вероятно, не только усиление эффекта кросс-линкинга, но также лучшее сохранение слоев эпителия роговицы при опасном воздействии УФ-А-лучей.
С помощью новых растворов рибофлавин-декстрана и по меньшей мере одного носителя (энхансера проницаемости), выбранного среди веществ, предложенных в данном описании, можно проводить кросс-линкинг, например, для лечения кератоконуса, без предварительного удаления эпителия роговицы. То, что эпителий роговицы не удаляется, позволяет избежать:
1) недомоганий, вызванных облучением, которые обычно возникают в первые дни после кросс-линкинга в соответствии со стандартным протоколом;
2) необходимости применения терапевтических контактных линз после лечения и, прежде всего,
3) риска послеоперационных инфекций роговицы вследствие удаления эпителия роговицы.
Помимо этого, отказ от хирургического вмешательства позволяет проводить лечение амбулаторно, отпадает необходимость в операционной и в операционном микроскопе.
Новые растворы можно также вводить в виде глазных капель или геля или наносить на терапевтические контактные линзы перед воздействием солнечных лучей, в особенности летом, чтобы повысить эффект естественного кросс-линкинга вследствие облучения рибофлавина солнечными лучами.
Далее, новые растворы могли бы защитить внутренние структуры глазного яблока от УФ-А-лучей и поэтому их можно применять, например, для защиты от дегенерации желтого пятна и/или предупреждения катаракты у людей с повышенным риском ее образования вследствие того, что они по много часов находятся на солнце.
Бензалкония хлорид в концентрации от 0.0001%-0.02%, предпочтительно, в концентрации, примерно, 0.01%, можно добавлять только лишь для того, чтобы как можно дольше сохранить новые растворы не в однодозовых контейнерах. Если новые растворы будут производиться и продаваться в однодозовых контейнерах для одноразового использования, добавление бензалкония хлорида не является обязательным. Помимо этого, в композиции можно добавлять консерванты, антимикробные агенты, противогрибковые агенты, эксципиенты (например, уксусную кислоту) и, в общем, любое вещество, применяемое в офтальмологии для приготовления устойчивых и стерильных офтальмологических растворов и/или для лучшего их усвоения.
Как указывается выше, заявители полагают, что хорошие характеристики композиции, полученные при добавлении к рибофлавину по меньшей мере одного вещества, выбранного из витамина Q, L-пролина, глицина, лизина гидрохлорида, L-лейцина, частично обусловлены тем фактом, что последние вещества являются незаменимыми или условно незаменимыми аминокислотами, которые проявляют циторепаративную функцию, повышая уровни металлопротеиназы ММР9. Это позволяет сделать вывод, что можно получить результаты, аналогичные результатам, полученным при использовании новых тестируемых композиций, первой, второй, третьей и четвертой, путем добавления к раствору рибофлавина, например к стандартному раствору рибофлавин-декстрана, по меньшей мере одного вещества, применяемого для увеличения металлопротеиназы ММР9, предположительно, в концентрации от 0.00001% до 0.5%.
Среди этих веществ, применяемых для увеличения (повышения уровня) металлопротеиназы ММР9, заслуживают упоминания генистеин(5,7-дигидрокси-3-(4-гидроксифенил)хромен-4-он), фитоэстрогены, цитокины и так называемые нестероидные противовоспалительные средства (препараты) (НСПВС, NSAID). Среди НСПВС, применяемых для приготовления офтальмологического раствора рибофлавина, заслуживают упоминания: ацетилсалициловая кислота(2-ацетоксибензойная) кислота, флуфенамовая кислота(2-{[3-(трифторметил)фенил]амино}бензойная кислота), меклофенамовая кислота (2-[(2,6-дихлор-3-метилфенил)амино]бензойная кислота), мефенамовая кислота(2-(2,3-диметилфенил)аминобензойная кислота), нифлумовая кислота(2-{[3-(трифторметил)фенил]амино}никотиновая кислота), толфенамовая кислота(2-[(3-хлор-2-метилфенил)амино]бензойная кислота), бенорилат(4-(ацетиламино)фенил 2-(ацетилокси)бензоат), карпрофен((RS)-2-(6-хлор-9H- карбазол-2-ил)пропановая кислота), целекоксиб(4-[5-(4-метилфенил)-3-(трифторметил)пиразол-1-ил]бензолсульфонамид), цинноксикам(пироксикам циннамат или [9-метил-10,10-диоксо-8-(пиридин-2-илкарбамоил)-10$1^{6}-тиа-9-азабицикло[4.4.0]дека-1, 3, 5, 7-тетраен-7-ил](Е)-3-фенилпроп-2-еноат), дифлунизал(2',4'-дифтор-4-гидроксибифенил-3-карбоновая кислота), диклофенак(2-[2-[(2,6-дихлорфенил)амино]фенил]уксусная кислота), дроксикам(2H,5H- 1,3-оксазино(5,6-с)(1,2)бензотиазин-2,4(3H)-дион, 5-метил-3-(2- пиридинил)-, 6,6-диоксид), этодолак((RS)-2-(1,8-диэтил-4,9-дигидро-3H-пирано[3,4-b]индол-1-ил)уксусная кислота), эторикоксиб(5-хлор-6'-метил-3-[4-(метилсульфонил)фенил]-2,3'-бипиридин), фенопрофен(2-(3-феноксифенил)пропановая кислота), флурбипрофен ((RS)-2-(2-фторбифенил-4-ил)пропановая кислота), ибуфенак (4-изобутилфенилуксусная кислота), ибупрофен((RS)-2-(4-(2- метилпропил)фенил) пропановая кислота), индометацин(2-{1-[(4-хлорфенил) карбонил]-5-метокси-2-метил-1H-индол-3-ил}уксусная кислота), кетопрофен((RS)-2-(3-бензоилфенил)пропановая кислота), кеторолак ((±)-5-бензоил-2,3-дигидро- 1
-пирролизин-1-карбоновая кислота, 2-амино-2-(гидроксиметил)-1,3-пропандиол), лорноксикам((3E)-6-хлор-3-[гидрокси(пиридин-2-иламино)метилен]-2-метил-2,3-дигидро-4H-тиено[2,3-е][1,2]тиазин-4-он 1,1-диоксид), лумиракоксиб ({2-[(2-хлор-6-фторфенил)амино]-5-метилфенил}уксусная кислота), мелоксикам (4-гидрокси-2-метил-N-(5-метил-2-тиазолил)-2Н-1,2-бензотиазин-3-карбоксамид-1,1-диоксид), метамизол (натрия [(2,3-дигидро-1,5-диметил-3-оксо-2-фенил-1H-пиразол-4-ил) метиламино] метансульфонат), напроксен ((+)-(S)-2-(6-метоксинафталин-2-ил)пропановая кислота), нимесулид(N-(4-нитро-2-феноксифенил)метансульфонамид), оксапрозин(3-(4,5-дифенил-1,3-оксазол-2-ил)пропановая кислота), парекоксиб(N-{[4-(5-метил-3-фенилизоксазол-4-ил)фенил]сульфонил}пропанамид), пироксикам((8E)-8-[гидрокси-(пиридин-2-иламино)метилиден]-9-метил-10,10-диоксо-10λ6-тиа-9-азабицикло[4.4.0]дека-1,3,5-триен-7-он), рофекоксиб(4-(4- метилсульфонилфенил)-3-фенил-5Н-фуран-2-он), сулиндак({(1Z)-5-фтор-2-метил-1-[4-(метилсульфинил)бензилиден]-1Н-инден-3-ил}уксусная кислота), судоксикам(4-гидрокси-2-метил-N(2)-тиазолил-2Н-1,2-бензотиазин-3-карбоксамид 1,1-диоксид), теноксикам((3E)-3-[гидрокси(пиридин-2-иламино)метилен]-2-метил-2,3-дигидро-4Н-тиено[2,3-е][1,2]тиазин-4-он 1,1-диоксид), вальдекоксиб(4-(5-метил-3-фенилизоксазол-4-ил) бензолсульфонамид).
Помимо этого, заявитель считает возможным получить результаты, аналогичные результатам, полученным с первой, второй, третьей и четвертой новой тестируемой композицией, прибавляя к раствору рибофлавина, например к раствору рибофлавин-декстрана, по меньшей мере одну незаменимую или условно незаменимую аминокислоту.
Среди потенциально применимых веществ наиболее обещающим кажется L-аргинин. Его можно смешивать с раствором рибофлавина, например со стандартным раствором рибофлавин-декстрана, с последующим добавлением одного или более вышеуказанных веществ для получения новых растворов. Хотя проверены еще не все эти вещества, заявителям кажется логичным предположить, что все незаменимые или условно незаменимые аминокислоты можно эффективно использовать для содействия проникновению (пенетрации) рибофлавина через эпителий роговицы, тем самым защищая роговицу от УФ-А-облучения и от солнечных лучей, поглощаемых рибофлавином. В частности, кажется резонным рассматривать L-аргинин как подходящий носитель, подобно предлагаемым выше веществам, так как логично предположить, что L-аргинин, аминокислотный предшественник оксида азота, может доставлять оксид азота (NO) на периферию. Применению оксида азота (NO) для лечения пациентов с кератоконусом с помощью топического нанесения на эпителий роговицы вещества, в котором NO растворяется, мешает плохая растворимость NO.
Именно экспериментально было проверено, насколько L-аргинин и другие незаменимые аминокислоты защищают микроворсинки эпителия от УФ-А-облучения при кросс-линкинге. Так как оказалось, что другие незаменимые или условно незаменимые аминокислоты, и в частности L-аргинин, применимы для приготовления офтальмологических растворов, которые способствуют осуществлению трансэпителиального кросс-линкинга, в то же время сохраняя эпителий роговицы, то заявители считают логичным, что их следует добавлять к раствору рибофлавина, например стандартному раствору рибофлавин-декстрана, в примерной концентрации от 0.00001% до 0.5%.
Согласно более предпочтительному варианту изобретения концентрация L-аргинина или другой незаменимой или условно незаменимой аминокислоты составляет от 0.001% до 0.4%. Согласно еще более предпочтительному варианту изобретения интервал концентраций составляет от 0.005% до 0.3%. Согласно еще более предпочтительному варианту изобретения интервал концентраций составляет от 0.01% до 0.2%. Согласно еще более предпочтительному варианту изобретения концентрация L-аргинина или другой незаменимой или условно незаменимой аминокислоты составляет около 0.1%.
В качестве варианта можно добавлять L-аргинин и/или любую другую незаменимую или условно незаменимую аминокислоту в любой из предлагаемых новых растворов.
Дозировка новых офтальмологических растворов зависит от выявленной патологии и от ее тяжести. Полагают, что доза может находиться в диапазоне от одной капли в глаз в день до, максимально, одной капли в час.
Заявляемая Формула изобретения является составной частью данного описания. Полное раскрытие приоритетных итальянских патентных заявок VA2009A000052 и VA2010A000044 на имя тех же самых заявителей вводится в данное описание в качестве ссылки.
ССЫЛКИ
1. Seiler Т., Spoerl Е., Huhle М., Kamouna A. Conservative therapy of keratoconus by enhancement of collagen cross-links. Invest Ophthalmol. Vis. Sci. 1996; 37: S1017.
2. Seiler Т., Quurke AW. Iatrogenic keratectasia after LASIK in a case of forme fruste keratoconus. J Cat Refract Surg. 1998; 24: 1007-1009.
3. Spoerl E., Huhle M., Seiler T. "Induction of cross-links in corneal tissue", Exp Eye Res. 1998; 66: 97-103.
4. Mazzotta C, Traversi C, Baiocchi S., Sergio P., Caporossi Т., Caporossi A. "Conservative treatment of keratoconus by riboflavin-uva-induced cross-linking of corneal collagen: qualitative investigation" Eur J Ophthalmol. 2006; 16: 530-5.
5. Caporossi A., Baiocchi S., Mazzotta C, Traversi C, Caporossi T. "Parasurgical therapy for keratoconus by riboflavin-ultraviolet type A rays induced cross-linking of corneal collagen: preliminary refractive results in an Italian study" J Cataract Refract Surg. 2006;32: 837 - 45.
6. Spoerl E., Seiler T. "Techniques for stiffening the cornea" J Refract Surg. 1999; 15: 711-713.
7. Hagele G., Boxer Wachler BS. "Corneal Collagen Crosslinking with Riboflavin (C3-R) for corneal stabilization" Presented at the International Congress of Corneal Cross Linking (CCL). December 9- 10,2005. Zurich, Switzerland.
8. Pinelli, R. "C3-Riboflavin for the treatment of keratoconus" J Cataract & Refractive Surgery Today Europe. 2006; 1: 49-50.
9. Pinelli R. "Eyeword", 2007; 5: 34-40.
10. Linda J. Muller, Elisabeth Pels, Gijs F. J. M. Vrensen: "The specific architecture of the anterior stroma accounts for maintenance of corneal curvature". Br J Ophthalmol 2001; 85:437- 443 (April).
11. Маy T. Tranl, Robert N. Lausch 2 and John E. Oakes: "Substance P Differentially Stimulates IL-8 Synthesis in Human Corneal Epithelial Cells" Investigative Ophthalmology and Visual Science. 2000; 41: 3871- 3877.
12. L.J. Muller, L. Pels and GF. Vrensen: "Novel aspects of the ultrastructural organization of human corneal keratocytes" Investigative Ophthalmology & Visual Science, Vol 36, 2557-2567.
13. G. Perrella, P. Brusini, R. Spelat, P. Hossain, A. Hopkinson, H. S. Dua: "Expression of haematopoietic stem cell markers, CD133 and CD34 on human corneal keratocytes" British Journal of Ophthalmology 2007; 91: 94- 99.
14. Tadashi Senoo, and Nancy C. Joyce: "Cell Cycle Kinetics in Corneal Endothelium from Old and Young Donors" Investigative Ophthalmology and Visual Science. 2000; 41: 660-667.
15. L.J. Mtiller, L. Pels and GF. Vrensen: "Ultrastructural organization of human corneal nerves" Investigative Ophthalmology & Visual Science, Vol 37,476- 488.
16. Italian patent application No. MI2007A002162, 14 Nov. 2007, R. Pinelli, "Collirio per il trattamento del cheratocono con tecnica cross- linking trans- epiteliale".
17. R. Pinelli, A. J. Kannellopoulos, B. S. B. Wachler, E. Spoerl, A. Ertan, S. L. Trokel, "C3- Riboflavin treatments: Where did we come from? Where are we now?", Cataract & Refractive Surgery Today Europe, Summer 2007.
18. Ashim K. Mitra, "Ophthalmic Drug Delivery Systems", Second Edition: Revised And Expanded, Marcell Dekker Inc., NY, 2003.
Claims (9)
1. Офтальмологический раствор, содержащий рибофлавин и витамин E, для защиты внутренних структур глазного яблока от УФ-А-лучей или для лечения кератоконуса методом трансэпителиального кросс-линкинга.
2. Офтальмологический раствор по п. 1, который содержит рибофлавин, витамин E и дополнительно по меньшей мере одно соединение, выбранное из группы, состоящей из кофермента Q, L-пролина, глицина, лизина гидрохлорида, L-лейцина и L-аргинина.
3. Офтальмологический раствор по п. 1, который содержит раствор рибофлавина в концентрации, выбранной из интервала концентраций от 0.0001% до 0.5%, причем рибофлавин обеспечивают в форме раствора рибофлавина-декстрана, дополнительно содержащего декстран в концентрации 20% масс., и витамин E в концентрации, выбранной из интервала концентраций от 0.0001 мг % до 2000 мг %.
4. Офтальмологический раствор по п. 3, который дополнительно содержит по меньшей мере одно из нижеприведенных соединений:
- кофермент Q в концентрации, выбранной из интервала концентраций от 0.0001 мг % до 2000 мг %;
- L-пролин в концентрации, выбранной из интервала концентраций от 0.0001 мг % до 2000 мг %;
- глицин в концентрации, выбранной из интервала концентраций от 0.0001 мг % до 2000 мг %;
- лизина гидрохлорид в концентрации, выбранной из интервала концентраций от 0.0001 мг % до 2000 мг %;
- L-лейцин в концентрации, выбранной из интервала концентраций от 0.0001 мг % до 2000 мг %;
- L-аргинин в концентрации, выбранной из интервала концентраций от 0.00001% до 0.5%.
- кофермент Q в концентрации, выбранной из интервала концентраций от 0.0001 мг % до 2000 мг %;
- L-пролин в концентрации, выбранной из интервала концентраций от 0.0001 мг % до 2000 мг %;
- глицин в концентрации, выбранной из интервала концентраций от 0.0001 мг % до 2000 мг %;
- лизина гидрохлорид в концентрации, выбранной из интервала концентраций от 0.0001 мг % до 2000 мг %;
- L-лейцин в концентрации, выбранной из интервала концентраций от 0.0001 мг % до 2000 мг %;
- L-аргинин в концентрации, выбранной из интервала концентраций от 0.00001% до 0.5%.
5. Офтальмологический раствор по п. 3, который содержит раствор рибофлавина-декстрана в концентрации около 0.1%, витамин E в концентрации около 500 мг %; и по меньшей мере одно из нижеприведенных соединений:
- кофермент Q в концентрации около 100 мг %;
- L-пролин в концентрации около 0.1 мг %;
- глицин в концентрации около 0.1 мг %;
- лизина гидрохлорид в концентрации около 0.05 мг %;
- L-лейцин в концентрации около 0.08 мг %;
- L-аргинин в концентрации около 0.1%.
- кофермент Q в концентрации около 100 мг %;
- L-пролин в концентрации около 0.1 мг %;
- глицин в концентрации около 0.1 мг %;
- лизина гидрохлорид в концентрации около 0.05 мг %;
- L-лейцин в концентрации около 0.08 мг %;
- L-аргинин в концентрации около 0.1%.
6. Офтальмологический раствор по п. 3, который содержит раствор рибофлавин-декстрана 0.1%, витамин E TPGS (D-альфа-токоферил полиэтиленгликоль 1000 сукцинат) 500 мг %, кофермент Q 100 мг %, L-пролин 0.1 мг %, глицин 0.1 мг %, лизина гидрохлорид 0.05 мг % и L-лейцин 0.08 мг %.
7. Офтальмологический раствор по любому из пп. 1-6, который приготовлен в форме глазных капель или офтальмологического геля или в форме, пригодной для нанесения на терапевтические контактные линзы.
8. Применение рибофлавина для приготовления офтальмологического раствора, содержащего витамин E, для защиты внутренних структур глазного яблока от УФ-А-лучей или для лечения кератоконуса методом трансэпителиального кросс-линкинга.
9. Энхансер проницаемости через эпителий роговицы офтальмологического раствора, содержащего рибофлавин, для защиты внутренних структур глазного яблока от УФ-А-лучей или для лечения кератоконуса методом трансэпителиального кросс-линкинга, состоящий из витамина E.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ITVA2009A000052 | 2009-07-27 | ||
| IT000052A ITVA20090052A1 (it) | 2009-07-27 | 2009-07-27 | Composizione per il trattamento del cheratocono con tecnica di cross-linking trans-epiteliale o per proteggere strutture interne del globo oculare da raggi uv-a |
| ITVA2010A000044 | 2010-05-20 | ||
| IT000044A ITVA20100044A1 (it) | 2010-05-20 | 2010-05-20 | Soluzione oftalmica per proteggere strutture interne del globo oculare da raggi uv-a o per il trattamento del cheratocono con tecnica di cross-linking trans-epiteliale |
| PCT/EP2010/060752 WO2011012557A1 (en) | 2009-07-27 | 2010-07-23 | Ophthalmic solution for protecting internal structures of the eyeball against uv-a rays or for the treatment of keratoconus with a trans-epithelial cross-linking technique |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2012106178A RU2012106178A (ru) | 2013-09-10 |
| RU2540481C2 true RU2540481C2 (ru) | 2015-02-10 |
Family
ID=42575807
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2012106178/15A RU2540481C2 (ru) | 2009-07-27 | 2010-07-23 | Офтальмологический раствор для защиты внутренних структур глазного яблока от уф-а лучей или для лечения кератоконуса методом трансэпителиального кросс-линкинга |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US9192594B2 (ru) |
| EP (1) | EP2459186B1 (ru) |
| JP (1) | JP2013500302A (ru) |
| KR (1) | KR20120038520A (ru) |
| CN (1) | CN102470120A (ru) |
| AU (1) | AU2010277668A1 (ru) |
| BR (1) | BR112012001998B8 (ru) |
| CA (1) | CA2805511C (ru) |
| ES (1) | ES2441227T3 (ru) |
| PT (1) | PT2459186E (ru) |
| RU (1) | RU2540481C2 (ru) |
| WO (1) | WO2011012557A1 (ru) |
| ZA (1) | ZA201201122B (ru) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9622911B2 (en) | 2010-09-30 | 2017-04-18 | Cxl Ophthalmics, Llc | Ophthalmic treatment device, system, and method of use |
| US9023092B2 (en) | 2011-08-23 | 2015-05-05 | Anthony Natale | Endoscopes enhanced with pathogenic treatment |
| WO2013028833A1 (en) | 2011-08-23 | 2013-02-28 | Anthony Natale | Systems and methods for treating pathogenic infection |
| CN102429767B (zh) * | 2011-08-25 | 2016-03-09 | 广东福地新视野光电技术有限公司 | 激光角膜热成形术系统 |
| ITMI20120355A1 (it) * | 2012-03-07 | 2013-09-08 | Ciro Caruso | Sostanza colorante per uso diagnostico oftalmologico |
| WO2013148896A1 (en) | 2012-03-29 | 2013-10-03 | Cxl Ophthalmics, Llc | Ocular treatment solutions, delivery devices and delivery augmentation methods |
| US9555111B2 (en) | 2012-03-29 | 2017-01-31 | Cxl Ophthalmics, Llc | Ocular cross-linking system and method for sealing corneal wounds |
| EP2830637A4 (en) | 2012-03-29 | 2016-03-16 | Cxl Ophthalmics Llc | COMPOSITIONS AND METHODS FOR TREATING OR PREVENTING DISEASES RELATED TO OXIDATIVE STRESS |
| ITRM20130248A1 (it) * | 2013-04-24 | 2014-10-25 | Medivis S R L | Formulazioni di riboflavina per il cross-linking transepiteliale. |
| RU2683651C2 (ru) * | 2013-06-18 | 2019-04-01 | Иван Дмитриевич Захаров | Лекарственное средство для лечения кератоконуса и других дегенеративных заболеваний роговицы и фармацевтические препараты на его основе |
| US9931199B2 (en) * | 2014-05-05 | 2018-04-03 | Roberto Gustavo ALBERTAZZI | Methods and apparatus for treating keratoconus |
| RU2556791C1 (ru) * | 2014-06-09 | 2015-07-20 | федеральное государственное бюджетное учреждение "Межотраслевой научно-технический комплекс "Микрохирургия глаза" имени академика С.Н. Федорова" Министерства здравоохранения Российской Федерации | Способ лечения кератоконуса |
| EP3324973B1 (en) * | 2015-07-21 | 2020-06-03 | Avedro, Inc. | Treament of an eye with a photosensitizer |
| US20180236077A1 (en) * | 2017-02-21 | 2018-08-23 | Avedro, Inc. | Formulations for eye treatments |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001037851A2 (en) * | 1999-11-25 | 2001-05-31 | Simonelli, Giuseppe | Use of ubiquinone q10 for the local treatment and prevention of post-surgical ophthalmologic pathologies |
| RU2201213C1 (ru) * | 2001-07-04 | 2003-03-27 | Общество с ограниченной ответственностью "Научно-экспериментальное производство Микрохирургия глаза" | Глазные капли "карнозин" |
| WO2009001396A1 (en) * | 2007-06-26 | 2008-12-31 | Sooft Italia Spa | Disposable sterile ocular solution for corneal cross- linking of cheratocone, and process for production thereof |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1106669A (zh) | 1994-10-10 | 1995-08-16 | 华中理工大学 | 一种防治白内障的滴眼液 |
| US5780446A (en) * | 1996-07-09 | 1998-07-14 | Baylor College Of Medicine | Formulations of vesicant drugs and methods of use thereof |
| ITMI981586A1 (it) * | 1998-07-10 | 2000-01-10 | Giorgio Panin | Vitamina e e suoi esteri per l'uso nel trattamento topico di patologie delle mucose |
| US6291519B1 (en) * | 1998-10-14 | 2001-09-18 | Novartis Ag | Method of preventing damage to eye tissue |
| US6441050B1 (en) | 2000-08-29 | 2002-08-27 | Raj K. Chopra | Palatable oral coenzyme Q liquid |
| JP5147156B2 (ja) * | 2003-08-08 | 2013-02-20 | ロート製薬株式会社 | 角膜障害抑制剤 |
| GB0404693D0 (en) * | 2004-03-02 | 2004-04-07 | Univ London | Pharmaceutical preparations for the treatment of ocular surface and other disorders |
| JP4604515B2 (ja) * | 2004-03-05 | 2011-01-05 | 大正製薬株式会社 | 眼科用剤 |
| ITMI20052036A1 (it) * | 2005-10-26 | 2007-04-27 | Professional Dietetics Srl | Composizioni farmaceutiche oftalmiche a base di amminoacidi e sodio ialuronato |
-
2010
- 2010-07-23 US US13/387,668 patent/US9192594B2/en active Active
- 2010-07-23 JP JP2012522123A patent/JP2013500302A/ja active Pending
- 2010-07-23 BR BR112012001998A patent/BR112012001998B8/pt active IP Right Grant
- 2010-07-23 EP EP10737873.9A patent/EP2459186B1/en active Active
- 2010-07-23 WO PCT/EP2010/060752 patent/WO2011012557A1/en active Application Filing
- 2010-07-23 KR KR1020127004681A patent/KR20120038520A/ko not_active Application Discontinuation
- 2010-07-23 CN CN2010800328001A patent/CN102470120A/zh active Pending
- 2010-07-23 PT PT107378739T patent/PT2459186E/pt unknown
- 2010-07-23 ES ES10737873.9T patent/ES2441227T3/es active Active
- 2010-07-23 AU AU2010277668A patent/AU2010277668A1/en not_active Abandoned
- 2010-07-23 CA CA2805511A patent/CA2805511C/en active Active
- 2010-07-23 RU RU2012106178/15A patent/RU2540481C2/ru active
-
2012
- 2012-02-15 ZA ZA2012/01122A patent/ZA201201122B/en unknown
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001037851A2 (en) * | 1999-11-25 | 2001-05-31 | Simonelli, Giuseppe | Use of ubiquinone q10 for the local treatment and prevention of post-surgical ophthalmologic pathologies |
| RU2201213C1 (ru) * | 2001-07-04 | 2003-03-27 | Общество с ограниченной ответственностью "Научно-экспериментальное производство Микрохирургия глаза" | Глазные капли "карнозин" |
| WO2009001396A1 (en) * | 2007-06-26 | 2008-12-31 | Sooft Italia Spa | Disposable sterile ocular solution for corneal cross- linking of cheratocone, and process for production thereof |
Non-Patent Citations (1)
| Title |
|---|
| KYMIONIS GD et al. "Customized pachymetric guided epithelial debridement for corneal collagen cross linking". BMC Ophtalmol. 2009 Aug 28; 9:10. * |
Also Published As
| Publication number | Publication date |
|---|---|
| US20120121567A1 (en) | 2012-05-17 |
| EP2459186A1 (en) | 2012-06-06 |
| CA2805511A1 (en) | 2011-02-03 |
| JP2013500302A (ja) | 2013-01-07 |
| AU2010277668A1 (en) | 2012-03-01 |
| CN102470120A (zh) | 2012-05-23 |
| ES2441227T3 (es) | 2014-02-03 |
| BR112012001998A2 (pt) | 2017-01-31 |
| CA2805511C (en) | 2017-04-11 |
| BR112012001998B8 (pt) | 2021-05-25 |
| BR112012001998B1 (pt) | 2020-12-01 |
| US9192594B2 (en) | 2015-11-24 |
| ZA201201122B (en) | 2013-05-29 |
| AU2010277668A8 (en) | 2012-04-19 |
| KR20120038520A (ko) | 2012-04-23 |
| PT2459186E (pt) | 2013-12-24 |
| EP2459186B1 (en) | 2013-10-09 |
| RU2012106178A (ru) | 2013-09-10 |
| WO2011012557A1 (en) | 2011-02-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2540481C2 (ru) | Офтальмологический раствор для защиты внутренних структур глазного яблока от уф-а лучей или для лечения кератоконуса методом трансэпителиального кросс-линкинга | |
| Ross et al. | Topical sustained drug delivery to the retina with a drug-eluting contact lens | |
| Cheng et al. | Ocular disease therapeutics: design and delivery of drugs for diseases of the eye | |
| Abdelkader et al. | Age-related cataract and drug therapy: opportunities and challenges for topical antioxidant delivery to the lens | |
| JP2019081798A (ja) | 安定で保存剤非含有の散瞳および抗炎症注射用液剤 | |
| KR20110046567A (ko) | 가능하게 리보플라빈과 관련된 인핸서의 사용, 및 원추각막 또는 다른 각막 확장 질병의 치료에서의 각막 가교를 위한 상응하는 안과용 조성물 | |
| KR20090082392A (ko) | 신체 조직의 물리적 및/또는 화학적 성질에 영향을 주는 광화학적 요법 | |
| ES2728071T3 (es) | Composiciones oftalmológicas y su uso | |
| CN1882339A (zh) | 黄斑变性和其他眼科疾病的缓解 | |
| US20170143653A1 (en) | Use of sulindac for protecting retinal pigment epithelial cells against oxidative stress | |
| KR102578102B1 (ko) | 엔도텔린 수용체 길항제의 국소 안용 제형 | |
| EP2521550A1 (en) | Treatment method | |
| Lian et al. | SIRT1 Inhibits High Glucose–Induced TXNIP/NLRP3 Inflammasome Activation and Cataract Formation | |
| Yu et al. | Safety of femtosecond laser‐assisted cataract surgery: assessment of aqueous humour and lens capsule | |
| EP4262809A1 (en) | Mydriatic compositions and methods for fabricating thereof | |
| US10792260B2 (en) | Retinopathy treatment | |
| ITVA20100044A1 (it) | Soluzione oftalmica per proteggere strutture interne del globo oculare da raggi uv-a o per il trattamento del cheratocono con tecnica di cross-linking trans-epiteliale | |
| Huynh | Factors governing photodynamic cross-linking of ocular coat | |
| US20220211654A1 (en) | Materials and methods for treating age-related macular degeneration | |
| WO2016179351A1 (en) | Treatment of levodopa-induced dyskinesias | |
| Arana et al. | The new preservative-free ophthalmic formulation of bilastine 0.6% preserves the ocular surface epithelial integrity in a comparative in vitro study | |
| Hafezi | Cross-linking of corneal collagen with UVA and riboflavin for the treatment of corneal disease | |
| BR102017026328A2 (pt) | Método de reticulação do colágeno corneano com genipina para aplicação no tratamento de ceratocone | |
| Hsu | The Ocular and Systemic Adverse Effects of Topical 0.1% Diclofenac in Healthy Cats | |
| ITVA20090052A1 (it) | Composizione per il trattamento del cheratocono con tecnica di cross-linking trans-epiteliale o per proteggere strutture interne del globo oculare da raggi uv-a |