RU2290454C2 - Способ изготовления газодиффузионных электродов - Google Patents
Способ изготовления газодиффузионных электродов Download PDFInfo
- Publication number
- RU2290454C2 RU2290454C2 RU2004101764/15A RU2004101764A RU2290454C2 RU 2290454 C2 RU2290454 C2 RU 2290454C2 RU 2004101764/15 A RU2004101764/15 A RU 2004101764/15A RU 2004101764 A RU2004101764 A RU 2004101764A RU 2290454 C2 RU2290454 C2 RU 2290454C2
- Authority
- RU
- Russia
- Prior art keywords
- catalyst
- silver
- porous
- rollers
- electrode
- Prior art date
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/88—Processes of manufacture
- H01M4/8878—Treatment steps after deposition of the catalytic active composition or after shaping of the electrode being free-standing body
- H01M4/8896—Pressing, rolling, calendering
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/88—Processes of manufacture
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/8605—Porous electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/8647—Inert electrodes with catalytic activity, e.g. for fuel cells consisting of more than one material, e.g. consisting of composites
- H01M4/8652—Inert electrodes with catalytic activity, e.g. for fuel cells consisting of more than one material, e.g. consisting of composites as mixture
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/88—Processes of manufacture
- H01M4/8878—Treatment steps after deposition of the catalytic active composition or after shaping of the electrode being free-standing body
- H01M4/8882—Heat treatment, e.g. drying, baking
- H01M4/8885—Sintering or firing
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/90—Selection of catalytic material
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/8647—Inert electrodes with catalytic activity, e.g. for fuel cells consisting of more than one material, e.g. consisting of composites
- H01M4/8657—Inert electrodes with catalytic activity, e.g. for fuel cells consisting of more than one material, e.g. consisting of composites layered
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/08—Fuel cells with aqueous electrolytes
- H01M8/083—Alkaline fuel cells
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/50—Fuel cells
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P70/00—Climate change mitigation technologies in the production process for final industrial or consumer products
- Y02P70/50—Manufacturing or production processes characterised by the final manufactured product
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Composite Materials (AREA)
- Physics & Mathematics (AREA)
- Thermal Sciences (AREA)
- Materials Engineering (AREA)
- Electrodes For Compound Or Non-Metal Manufacture (AREA)
- Inert Electrodes (AREA)
- Catalysts (AREA)
- Electrolytic Production Of Non-Metals, Compounds, Apparatuses Therefor (AREA)
Abstract
Изобретение относится к способу изготовления пористого газодиффузионного электрода. Пористую систему серебряного катализатора заполняют смачивающей жидкостью, твердое вещество с размером зерна больше размера зерна серебряного катализатора смешивают с ним в однородную массу, эту устойчивую при сжатии массу формуют в каландре в однородную катализаторную ленту, на втором этапе каландрирования в катализаторную ленту закатывают электропроводящий разрядный материал. Технический эффект - получение газодиффузионного электрода с крупными порами, обеспечивающими быстрый перенос газа, и мелкими порами в катализаторе, обеспечивающими его однородное использование. 5 з.п. ф-лы, 6 ил.
Description
Настоящее изобретение относится к способу изготовления пористых газодиффузионных электродов приведенного в п.1 формулы типа. Такой газодиффузионный электрод может быть основан, например, на каталитически активном серебре или серебряных сплавах для использования в электрохимических ячейках, в частности при электролизе растворов хлоридов щелочных металлов, или в щелочных топливных элементах.
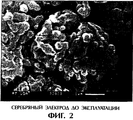
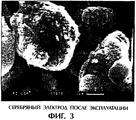
В электрохимических ячейках осуществляют восстановление кислорода на платине, серебре или углероде. Платина применима как в кислотной, так и в щелочной среде, а серебро и углерод, напротив, являются коррозионностойкими только в щелочных электролитах. Однако в случае серебряного катализатора даже в щелочных средах происходит быстрая дезактивация, объясняемая перегруппировкой оксидной поверхности серебра («Тексас Инструменте», US 3505120). Многократно предпринимались попытки уменьшить коррозионное воздействие на серебро посредством подходящих легирующих компонентов. При этом известны как сплавы с более благородными металлами, платиной, палладием, золотом и ртутью (DE 2021009), так и с неблагородными металлами, такими как никель (DE 1546728), медь и другие. Предпринимались также попытки достичь стабилизации серебра как за счет облагораживания, так и за счет анодной коррозионной защиты (локальный элемент). При коррозии сначала образуется серебрянооксидная поверхность. Поскольку оксид серебра относительно хорошо растворим в щелочах, может происходить, тем самым, перегруппировка кристалла серебра. На фиг.2 и 3 изображены сделанные растровым электронным микроскопом снимки серебряных электродов до и после эксплуатации. Очень хорошо видно уменьшение внутренней пористой структуры. Каталитическая активность падает.
Помимо стабилизации способ изготовления активного серебряного катализатора должен обеспечить также, чтобы активная поверхность серебра была достаточно большой, т.е. чтобы размер зерна серебра был как можно меньше. Так, например, из US 3668101 известно, что очень активные серебряные катализаторы получаются при диаметре частиц размером 5-10 мкм.
Кроме того, известны способы, в которых делается попытка получения мельчайших частиц устойчивых серебряных сплавов. Достаточно мелкие частицы серебра получают осаждением. Для того чтобы получить мельчайшие частицы серебра, важную роль, помимо контроля значения рН, температуры и перенасыщения, играют так называемые зародыши кристаллизации. Известен способ (ЕР 0115845), при котором смесь нитрата серебра и нитрата ртути осаждают на ПТФЭ-подложке за счет добавки едкого калия. Этим получают серебряную амальгаму с минимальным диаметром частиц.
Для изготовления из этих катализаторов так называемых газодиффузионных электродов, используемых в топливных элементах или при электролизе хлоридов, порошки должны быть переработаны в однородный поверхностный электрод. Этот электрод должен быть электропроводящим и обеспечивать как проникновение электролита, так и газа. Следовательно, одни участки электрода должны иметь возможность смачивания, а другие участки, напротив, должны быть защищены от смачивания. Одно решение этой проблемы основано на бипористой структуре. Электролит может сначала без труда проникать как в мелкие, так и в крупные поры. За счет избыточного давления газа или силы тяжести электролит снова удаляется из крупных пор. Такие бипористые структуры работают удовлетворительно только тогда, когда имеется разность давлений в газовом и электролитном пространствах. Могут ли возникнуть такие разности давлений, если анод и катод отделены друг от друга мембраной, это еще вопрос. Таким образом, эти электроды не могут быть использованы в хлорном электролизе или в топливных элементах с щелочными мембранами.
Поэтому были предприняты попытки создания бипористой структуры посредством свойств материалов. Это означает, что требуются гидрофильные и гидрофобные материалы. Подходящими гидрофобными материалами являются некоторые термопласты, например политетрафторэтилен. Названные катализаторы, а также серебро являются гидрофильными. Если смешать серебро и политетрафторэтилен и сформовать из них плоский электрод, то он будет иметь разные участки с гидрофильными и гидрофобными свойствами. В большинстве случаев интегрируют дополнительный металлический разрядник с тем, чтобы достичь лучших электрических свойств.
Известны некоторые способы изготовления так называемого газодиффузионного электрода из смесей политетрафторэтилена и катализатора. Так, например, в ЕР 0115845 предложено суспендировать материалы таким образом, что получают пасту, которую можно отливать в форму, прессовать и сушить. Недостатком таких «пастированных» электродов является неравномерное распределение материала - легко могут возникнуть дырки, через которые тогда может проникать газ или электролит. Во избежание этого электроды изготавливают толщиной по меньшей мере 0,8 мм. Из-за этого в электроде присутствуют очень большие количества серебра (примерно 2 кг/м2), так что ценовое преимущество серебра снова теряется, поскольку известны коммерческие кислородные электроды с содержанием платины/углерода 4-40 г/м2.
Известны два способа, при которых из таких гидрофильных/гидрофобных материалов прокатывают тонкий однородный газодиффузионный электрод. Способом, описанным в ЕР 0144002, US 4696872, в специальном смесителе частицы катализатора и политетрафторэтилена смешивают между собой так, что на катализаторе осаждается мелкоячеистая гидрофобная сетка. В порошковом вальце свободно засыпанную массу раскатывают в пленку толщиной около 0,2 мм. Этот способ зарекомендовал себя для смесей из политетрафторэтилена и углерода или политетрафторэтилена и никеля Ренея. Можно также раскатывать в пористую пленку серебряный сплав Ренея с 80% алюминия. Такой многовалковый каландр изображен на фиг.1. При необходимом усилии прижима 0,01-0,6 т/см2 в таких порошковых вальцах политетрафторэтилен и серебро спрессовывают в компактную, газо- и электролитнепроницаемую пленку. Вольт-амперная характеристика такого электрода изображена на фиг.5.
Для того чтобы можно было тем не менее изготовить серебряные электроды, сначала смесь оксида серебра и политетрафторэтилена обрабатывают в порошковом вальце, а затем подвергают электрохимическому восстановлению (DE 3710168). Оксид серебра достаточно стоек, чтобы противостоять усилию прижима вальцов. Кроме того, объем при переходе от оксида серебра к серебру уменьшается, в результате чего в газодиффузионном электроде образуются дополнительные поры. Посредством изменения параметров при восстановлении можно довольно оптимально установить размер зерна частиц. Недостаток этого способа в том, что до сих пор неизвестно, как можно электрохимически восстановить серебряные сплавы с каталитическими свойствами. Таким образом, также невозможно изготовлять посредством электрохимического восстановления стабильные в течение длительного времени серебряные электроды.
Задача настоящего изобретения состоит в том, чтобы создать способ изготовления газодиффузионного электрода, посредством которого можно было бы не только избежать недостатков уровня техники, но и достичь, в частности, воспроизводимых результатов у продукта способа.
Способом описанного выше рода эта задача решается согласно изобретению за счет того, что
- пористую систему серебряного катализатора заполняют смачивающей жидкостью;
- твердое вещество с размером зерна больше размера зерна серебряного катализатора смешивают с серебряным катализатором в однородную массу;
- эту устойчивую при сжатии массу формуют в каландре в однородную катализаторную ленту;
- на втором этапе каландрирования в катализаторную ленту закатывают электропроводящий разрядный материал.
В качестве смачивающей жидкости используют изопропанол в количестве 5%, а в качестве твердого вещества - карбонат или гидрокарбонат аммония в количестве 30% и оба этих наполнителя вытесняют после изготовления электрода на этапе отжига преимущественно при 110°С.
Альтернативно в качестве смачивающей жидкости применяют поверхностно-активное вещество, преимущественно тритон Х 100, в количестве 5%, которое проникает в пористую систему катализатора, а также снижает поверхностное трение, так что серебряный катализатор может выскользнуть из зоны уплотнения, а применяемый в качестве твердого вещества карбонат аммония и подложка из политетрафторэтилена воспринимают давление вальцов.
На первом этапе каландрирования изготавливают однородную катализаторную ленту толщиной 0,2-0,5 мм.
При этом при изготовлении однородной катализаторной ленты устанавливают между вальцами зазор 350 мкм и подачу вальцов - примерно на 2 м/мин.
Предпочтительно в качестве электропроводящего разрядного материала использовать ткань из посеребренной никелевой проволоки с толщиной нитей 0,15 мм и размером ячеек 0,45 мм с серебряным покрытием толщиной около 10 мкм.
Особенность способа согласно изобретению состоит в том, что внутреннюю пористую систему вязких материалов заполняют жидкостью. Поскольку эту жидкость нельзя уплотнить и она за счет капиллярных сил прочно связана в пористой системе, при имеющемся давлении максимум 600 кг/см2 жидкость нельзя удалить из микропор. Дополнительная добавка небольшого количества углеродного порошка или летучего карбоната аммония может воспринять механическое давление порошковых вальцов. За счет этих крупнозернистых добавок с диаметром зерна обычно 10-100 мкм пористая система с большим диаметром пор защищена от уплотнения. Посредством последующего этапа отжига можно вытеснить из электрода как жидкость, так и твердое вещество - карбонат аммония. Таким образом, в газодиффузионном электроде могут быть получены крупные поры, обеспечивающие быстрый перенос газа, и мелкие поры в катализаторе, обеспечивающие однородное использование катализатора.
Одно предпочтительное осуществление способа изложено ниже. Сначала серебро или серебряный сплав получают посредством процесса осаждения. При этом предпочтительно осуществлять осаждение на подложке из политетрафторэтилена. Наилучшие результаты достигаются со смесью из 15% политетрафторэтилена и 85% серебра. За счет добавки формальдегида при осаждении гидроксид серебра сразу же превращается в щелочном окружении в кристалл серебра. Осажденную массу промывают и сушат. Последующий отжиг при 200°С улучшает электрический контакт между частицами серебра и вытесняет остатки жидкости.
К этому порошку добавляют 5-40%, преимущественно, однако, 8% жидкости, которая может проникать в пористую систему политетрафторэтилена и серебра. Из-за гидрофобного характера политетрафторэтилена для этой цели подходят только изопропанол, этанол и метанол. Если порошок смочен и заполнен такими растворителями, то за этим может следовать обмен жидкостей. Если, например, пропитанный изопропанолом порошок поместить в водяную ванну или глицерин, то жидкости обменяются за счет диффузии в течение часов. Таким образом, в пористую систему политетрафторэтилена попадает жидкость, обычно отталкиваемая политетрафторэтиленом. Этот увлажненный, таким образом, материал ведет себя внешне, как порошок, поскольку жидкость находится только во внутренней пористой системе.
Другим типом смачивающих средств являются так называемые поверхностно-активные вещества. Они проникают в пористую систему, однако покрывают также поверхность катализатора и снижают, таким образом, шероховатость его поверхности. Эта меньшая шероховатость поверхности приводит в процессе прокатки к тому, что серебряный катализатор может выскользнуть из зоны уплотнения, тогда как другие компоненты порошка, которые не были обработаны, остаются в зоне уплотнения и образуют электродную композицию, в которую закатан серебряный катализатор (фиг.4). В качестве такого порошка напрашивается карбонат аммония или активированный уголь, который смешивают с серебряным катализатором в мельнице, описанной в ЕР 0144002, в однородную массу. Затем свободно засыпанную массу раскатывают посредством порошкового вальца в пленку толщиной около 0,2 мм.
Во второй вальцовой паре можно закатать металлический опорный каркас в виде тканых сеток или тянутых металлов и тем самым повысить механическую стойкость и электропроводность. По окончании этого процесса газодиффузионный электрод сушат. После этого электрод имеет серебряное покрытие 0,2-1,5 кг/м2. Обычно желательна масса 0,5 кг/м2. Таким образом, экономится до 75% требовавшегося до сих пор серебра. Несмотря на уменьшенную массу серебра, благодаря таким электродам достигаются вольт-амперные характеристики, показанные на фиг.6.
Этот способ можно, само собой разумеется, и с другими способами комбинировать. Так, при осаждении можно отказаться от загрязняющего окружающую среду формальдегида и осуществить восстановление газодиффузионного электрода электрохимическим путем. Можно получать также сплавы путем совместного осаждения серебра и ртути, титана, никеля, меди, кобальта или висмута.
Специально для хлорного электролиза на готовом газодиффузионном электроде могут быть предприняты изменения, обеспечивающие лучшее удаление возникающего едкого натра. Для этого можно было, например, посоветовать закатывание грубой отводящей системы. Это возможно, если на готовый электрод напрессовать сетку, а затем снова снять ее. Негативный отпечаток сетки образует каналы, по которым электролит позднее может стекать параллельно поверхности электрода.
Другие признаки, подробности и преимущества изобретения приведены на последующих чертежах, изображающих
- фиг.1: функциональную схему установки согласно изобретению;
- фиг.2: сделанный микроскопом снимок серебряного электрода до эксплуатации;
- фиг.3: то же после эксплуатации;
- фиг.4: заделанная в серебряный катализатор подложка из политетрафторэтилена;
- фиг.5: диаграмму ток/напряжение хлорного электролиза;
- фиг.6: ту же кривую, согласно изобретению.
Claims (6)
1. Способ изготовления пористого газодиффузионного электрода из серебряного катализатора на подложке из политетрафторэтилена, отличающийся тем, что пористую систему серебряного катализатора заполняют смачивающей жидкостью, твердое вещество с размером зерна больше размера зерна серебряного катализатора смешивают с серебряным катализатором в однородную массу, эту устойчивую при сжатии массу формуют в каландре в однородную катализаторную ленту, на втором этапе каландрирования в катализаторную ленту закатывают электропроводящий разрядный материал.
2. Способ по п.1, отличающийся тем, что в качестве смачивающей жидкости используют изопропанол в количестве 5%, а в качестве твердого вещества - карбонат или гидрокарбонат аммония в количестве 30% и оба этих наполнителя вытесняют после изготовления электрода на этапе отжига преимущественно при 110°С.
3. Способ по п.1, отличающийся тем, что в качестве смачивающей жидкости применяют поверхностно-активное вещество, преимущественно тритон Х 100, в количестве 5%, которое проникает в пористую систему катализатора, а также снижает поверхностное трение так, что серебряный катализатор может выскользнуть из зоны уплотнения, а применяемый в качестве твердого вещества карбонат аммония и подложка из политетрафторэтилена воспринимают давление вальцов.
4. Способ по п.1, отличающийся тем, что на первом этапе каландрирования изготавливают однородную катализаторную ленту толщиной 0,2-0,5 мм.
5. Способ по одному из предыдущих пунктов, отличающийся тем, что при изготовлении однородной катализаторной ленты устанавливают между вальцами зазор 350 мкм и подачу вальцов - примерно на 2 м/мин.
6. Способ по одному из предыдущих пунктов, отличающийся тем, что в качестве электропроводящего разрядного материала используют ткань из посеребренной никелевой проволоки с толщиной нитей 0,15 мм и размером ячеек 0,45 мм с серебряным покрытием толщиной около 10 мкм.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10130441.2 | 2001-06-23 | ||
| DE10130441A DE10130441B4 (de) | 2001-06-23 | 2001-06-23 | Verfahren zum Herstellen von Gasdiffusionselektroden |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2004101764A RU2004101764A (ru) | 2005-06-10 |
| RU2290454C2 true RU2290454C2 (ru) | 2006-12-27 |
Family
ID=7689282
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2004101764/15A RU2290454C2 (ru) | 2001-06-23 | 2002-06-18 | Способ изготовления газодиффузионных электродов |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US7226885B2 (ru) |
| EP (1) | EP1402587B1 (ru) |
| JP (1) | JP2004533544A (ru) |
| KR (1) | KR100855922B1 (ru) |
| CN (1) | CN1272865C (ru) |
| AT (1) | ATE279023T1 (ru) |
| AU (1) | AU2002325243A1 (ru) |
| BR (1) | BR0210536B1 (ru) |
| CA (1) | CA2451610C (ru) |
| DE (2) | DE10130441B4 (ru) |
| HK (1) | HK1065647A1 (ru) |
| RU (1) | RU2290454C2 (ru) |
| WO (1) | WO2003004726A2 (ru) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10130441B4 (de) * | 2001-06-23 | 2005-01-05 | Uhde Gmbh | Verfahren zum Herstellen von Gasdiffusionselektroden |
| TW558833B (en) * | 2002-09-09 | 2003-10-21 | Ind Tech Res Inst | Gas diffusion electrode and the method for making the same |
| DE102004034885A1 (de) * | 2004-07-19 | 2006-02-16 | Uhde Gmbh | Silber-Gasdiffusionselektrode für den Einsatz in CO2-haltiger Luft |
| KR100682862B1 (ko) * | 2005-01-11 | 2007-02-15 | 삼성에스디아이 주식회사 | 전기 화학 전지용 전극, 그 제조 방법 및 이를 채용한전기 화학 전지 |
| DE102005023615A1 (de) | 2005-05-21 | 2006-11-23 | Bayer Materialscience Ag | Verfahren zur Herstellung von Gasdiffusionselektroden |
| ITMI20060726A1 (it) * | 2006-04-12 | 2007-10-13 | De Nora Elettrodi S P A | Elettrodo a diffusione gassosa per celle a percolazione di elettrolita |
| CN101191237B (zh) * | 2006-11-29 | 2010-04-14 | 中国石油天然气集团公司 | 一种制氢储氢一体化电极制备方法 |
| KR101160853B1 (ko) | 2009-12-18 | 2012-07-02 | 주식회사 미트 | 면상발열체 시트 제조장치 및 그의 제조방법 |
| CN101774666B (zh) * | 2010-01-29 | 2011-12-21 | 北京化工大学 | 一种2-乙基蒽醌改性气体扩散电极及其制备方法 |
| DE102010030203A1 (de) | 2010-06-17 | 2011-12-22 | Bayer Materialscience Ag | Gasdiffusionselektrode und Verfahren zu ihrer Herstellung |
| DE102010039846A1 (de) | 2010-08-26 | 2012-03-01 | Bayer Materialscience Aktiengesellschaft | Sauerstoffverzehrelektrode und Verfahren zu ihrer Herstellung |
| DE102011008163A1 (de) | 2011-01-10 | 2012-07-12 | Bayer Material Science Ag | Beschichtung für metallische Zellelement-Werkstoffe einer Elektrolysezelle |
| DE102011005454A1 (de) | 2011-03-11 | 2012-09-13 | Bayer Materialscience Aktiengesellschaft | Verfahren zur Herstellung von Sauerstoffverzehrelektroden |
| EP2573213B1 (de) * | 2011-09-23 | 2017-10-25 | Covestro Deutschland AG | Sauerstoffverzehrelektrode und verfahren zu ihrer herstellung |
| CN102517602B (zh) * | 2011-12-29 | 2014-10-29 | 北京化工大学 | 一种气体扩散电极的明胶造孔方法 |
| DK2907184T3 (en) | 2012-10-09 | 2018-08-06 | Oxynergy Ltd | ELECTRICAL DEVICE AND METHOD OF PREPARING IT |
| DE102015215309A1 (de) * | 2015-08-11 | 2017-02-16 | Siemens Aktiengesellschaft | Präparationstechnik von kohlenwasserstoffselektiven Gasdiffusionselektroden basierend auf Cu-haltigen-Katalysatoren |
| DE102017209960A1 (de) | 2017-06-13 | 2018-12-13 | Robert Bosch Gmbh | Verfahren zum Herstellen einer Elektrode, insbesondere für eine Batterie |
| DE102018211189A1 (de) * | 2018-07-06 | 2020-01-09 | Robert Bosch Gmbh | Verfahren und Vorrichtung zur Herstellung eines Elektrodenmaterialbandes |
| DE102019203373A1 (de) | 2019-03-13 | 2020-09-17 | Robert Bosch Gmbh | Gasdiffusionslage für eine Brennstoffzelle und Brennstoffzelle |
| DE102022004678A1 (de) | 2022-12-13 | 2024-06-13 | Covestro Deutschland Ag | Verfahren zur Elektrolyse von Kohlendioxid mit Vorreduktion einer Silberoxid-enthaltenden Gasdiffusionselektrode |
Family Cites Families (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1546728C3 (de) | 1965-09-18 | 1975-07-17 | Varta Batterie Ag, 3000 Hannover | Verfahren zur Herstellung eines silberhaltigen pulverförmiger! Katalysators für Sauerstoffelektroden |
| US3502509A (en) * | 1966-05-23 | 1970-03-24 | Allis Chalmers Mfg Co | Silver catalyzed fuel cell electrode |
| US3505129A (en) | 1967-01-16 | 1970-04-07 | Hooker Chemical Corp | Chemical coating process for metal |
| US3668101A (en) * | 1968-07-22 | 1972-06-06 | Nat Res Dev | Membrane electrodes and cells |
| US3553032A (en) * | 1969-01-21 | 1971-01-05 | Sony Corp | Method of making a fuel cell electrode by thermal decomposition of silver carbonate |
| FR2049151A7 (en) | 1969-06-04 | 1971-03-26 | United Aircraft Corp | Silver mercury catalyst for fuel cell cath- - ode |
| US3930094A (en) * | 1972-08-31 | 1975-12-30 | Westinghouse Electric Corp | Hydrophobic mats for gas diffusion electrodes |
| JPS5738185A (en) * | 1980-08-20 | 1982-03-02 | Matsushita Electric Ind Co Ltd | Ink jet recording paper |
| JPS6044786B2 (ja) * | 1980-10-30 | 1985-10-05 | 日本電池株式会社 | ガス拡散電極 |
| US4370284A (en) * | 1980-10-31 | 1983-01-25 | Diamond Shamrock Corporation | Non-bleeding electrode |
| US4518705A (en) * | 1980-10-31 | 1985-05-21 | Eltech Systems Corporation | Three layer laminate |
| US4357262A (en) * | 1980-10-31 | 1982-11-02 | Diamond Shamrock Corporation | Electrode layer treating process |
| US4500647A (en) * | 1980-10-31 | 1985-02-19 | Diamond Shamrock Chemicals Company | Three layer laminated matrix electrode |
| DE3303779A1 (de) | 1983-02-04 | 1984-08-16 | Hoechst Ag, 6230 Frankfurt | Verfahren zur herstellung eines katalytisch wirksamen elektrodenmaterials fuer sauerstoffverzehr-elektroden |
| DE3331699C2 (de) * | 1983-09-02 | 1985-10-31 | Accumulatorenwerke Hoppecke Carl Zoellner & Sohn GmbH & Co KG, 5790 Brilon | Sauerstoffelektrode für alkalische galvanische Elemente und Verfahren ihrer Herstellung |
| DE3342969A1 (de) | 1983-11-28 | 1985-06-05 | Varta Batterie Ag, 3000 Hannover | Poroese gaselektrode |
| US4585711A (en) * | 1983-12-15 | 1986-04-29 | Communications Satellite Corporation | Hydrogen electrode for a fuel cell |
| DE3437472A1 (de) * | 1984-10-12 | 1986-04-24 | Varta Batterie Ag, 3000 Hannover | Verfahren zur herstellung von gasdiffusionselektroden-koerpern |
| US4568442A (en) * | 1985-02-01 | 1986-02-04 | The Dow Chemical Company | Gas diffusion composite electrode having polymeric binder coated carbon layer |
| NL8502435A (nl) | 1985-09-05 | 1987-04-01 | Electrochem Energieconversie | Werkwijze voor het vervaardigen van een katalytische laag voor een brandstofcelelectrode en een dergelijke katalytische laag. |
| EP0241432B1 (en) * | 1986-03-07 | 1993-08-11 | Tanaka Kikinzoku Kogyo K.K. | Gas permeable electrode |
| JPH0719608B2 (ja) * | 1986-06-05 | 1995-03-06 | 電気化学工業株式会社 | ガス拡散電極用材料の製造方法 |
| DE3710168A1 (de) | 1987-03-27 | 1988-10-13 | Varta Batterie | Verfahren zur herstellung einer kunststoffgebundenen gasdiffusionselektrode mit metallischen elektrokatalysatoren |
| JPH03112056A (ja) * | 1989-09-27 | 1991-05-13 | Toshiba Corp | 電池用ガス拡散電極 |
| JPH04118859A (ja) * | 1990-09-10 | 1992-04-20 | Fuji Electric Co Ltd | リン酸型燃料電池の製造方法 |
| CA2077474A1 (en) * | 1992-02-21 | 1993-08-22 | Carl W. Townsend | Dual porosity gas evolving electrode |
| JPH07176310A (ja) * | 1993-12-20 | 1995-07-14 | Sanyo Electric Co Ltd | 電極及びその電極とイオン交換膜との接合体 |
| JP3481010B2 (ja) * | 1995-05-30 | 2003-12-22 | ジャパンゴアテックス株式会社 | 高分子固体電解質膜/電極一体成形体及びその製法 |
| DE19611510A1 (de) * | 1996-03-23 | 1997-09-25 | Degussa | Gasdiffusionselektrode für Membranbrennstoffzellen und Verfahren zu ihrer Herstellung |
| JPH10208757A (ja) * | 1997-01-20 | 1998-08-07 | Fuji Electric Co Ltd | 燃料電池発電装置 |
| JPH1140168A (ja) * | 1997-07-15 | 1999-02-12 | Jatco Corp | ガス拡散電極及び該ガス拡散電極を用いた燃料電池 |
| JP2909539B1 (ja) * | 1998-05-29 | 1999-06-23 | 長一 古屋 | ガス拡散電極 |
| DE10130441B4 (de) * | 2001-06-23 | 2005-01-05 | Uhde Gmbh | Verfahren zum Herstellen von Gasdiffusionselektroden |
-
2001
- 2001-06-23 DE DE10130441A patent/DE10130441B4/de not_active Expired - Fee Related
-
2002
- 2002-06-18 US US10/481,775 patent/US7226885B2/en not_active Expired - Lifetime
- 2002-06-18 BR BRPI0210536-5A patent/BR0210536B1/pt not_active IP Right Cessation
- 2002-06-18 RU RU2004101764/15A patent/RU2290454C2/ru not_active IP Right Cessation
- 2002-06-18 KR KR1020037015632A patent/KR100855922B1/ko not_active IP Right Cessation
- 2002-06-18 AT AT02758237T patent/ATE279023T1/de not_active IP Right Cessation
- 2002-06-18 CA CA2451610A patent/CA2451610C/en not_active Expired - Fee Related
- 2002-06-18 DE DE50201245T patent/DE50201245D1/de not_active Expired - Lifetime
- 2002-06-18 AU AU2002325243A patent/AU2002325243A1/en not_active Abandoned
- 2002-06-18 WO PCT/EP2002/006706 patent/WO2003004726A2/de active IP Right Grant
- 2002-06-18 CN CNB028123433A patent/CN1272865C/zh not_active Expired - Fee Related
- 2002-06-18 EP EP02758237A patent/EP1402587B1/de not_active Expired - Lifetime
- 2002-06-18 JP JP2003510479A patent/JP2004533544A/ja active Pending
-
2004
- 2004-09-30 HK HK04107508A patent/HK1065647A1/xx not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| US7226885B2 (en) | 2007-06-05 |
| HK1065647A1 (en) | 2005-02-25 |
| BR0210536B1 (pt) | 2012-01-24 |
| KR100855922B1 (ko) | 2008-09-02 |
| DE50201245D1 (de) | 2004-11-11 |
| BR0210536A (pt) | 2004-06-22 |
| WO2003004726A3 (de) | 2003-10-02 |
| AU2002325243A1 (en) | 2003-01-21 |
| JP2004533544A (ja) | 2004-11-04 |
| WO2003004726A2 (de) | 2003-01-16 |
| DE10130441A1 (de) | 2003-03-27 |
| CA2451610A1 (en) | 2003-01-16 |
| DE10130441B4 (de) | 2005-01-05 |
| RU2004101764A (ru) | 2005-06-10 |
| US20040152588A1 (en) | 2004-08-05 |
| CA2451610C (en) | 2010-11-09 |
| EP1402587A2 (de) | 2004-03-31 |
| CN1272865C (zh) | 2006-08-30 |
| EP1402587B1 (de) | 2004-10-06 |
| KR20040020910A (ko) | 2004-03-09 |
| CN1526179A (zh) | 2004-09-01 |
| ATE279023T1 (de) | 2004-10-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2290454C2 (ru) | Способ изготовления газодиффузионных электродов | |
| Wang et al. | High catalytic activity of ultrafine nanoporous palladium for electro-oxidation of methanol, ethanol, and formic acid | |
| Umeda et al. | Porous-microelectrode study on Pt/C catalysts for methanol electrooxidation | |
| JP6646704B2 (ja) | 改良されたガス拡散電極およびその製造方法 | |
| JP6125144B2 (ja) | ガス拡散電極およびその製造方法 | |
| Kostowskyj et al. | Silver nanowire catalysts for alkaline fuel cells | |
| Bidault et al. | A novel cathode for alkaline fuel cells based on a porous silver membrane | |
| JP4498738B2 (ja) | ガス拡散電極の製造方法 | |
| Liu et al. | Microstructure, electrocatalytic and sensing properties of nanoporous Pt46Ni54 alloy nanowires fabricated by mild dealloying | |
| KR101726575B1 (ko) | 극소량의 백금이 도포된 니켈 전극촉매, 이의 제조방법 및 이를 이용한 음이온 교환막 물 전기분해 장치 | |
| KR101584725B1 (ko) | 니켈이 전기 도금된 친수성을 가지는 다공성 탄소 재료를 이용한 알칼리 음이온 교환막 물 전기 분해 장치 및 그 제조 방법 | |
| EP2273590A1 (en) | Fuel cell | |
| CA2372601A1 (en) | Hybrid membrane electrode assemblies | |
| Bidault et al. | Cathode development for alkaline fuel cells based on a porous silver membrane | |
| US20080292944A1 (en) | Silver Gas Diffusion Electrode for Use in Air Containing Co2, and Method for the Production Thereof | |
| JPS59219861A (ja) | 多孔性電極 | |
| JP5932791B2 (ja) | 酸素消費電極およびその製造方法 | |
| US3668014A (en) | Electrode and method of producing same | |
| GB2169001A (en) | Gas depolarized cathode | |
| Yi et al. | Novel nanoporous binary Ag-Ni electrocatalysts for hydrazine oxidation | |
| US9118082B2 (en) | Oxygen-consuming electrode and process for the production thereof | |
| TW202022165A (zh) | 膜電極組與電解產氫的方法 | |
| El-Nagar et al. | ELECTROCATALYTIC ACTIVITY OF NOVEL BINARY MODIFIED PLTANIUM SURFACES WITH COBALT AND NICKEL OXIDES NANOSTRUCTUREs TOWARD FORMIC ACID OXIDATION |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20200619 |