RU2207845C2 - Твердая лекарственная форма пролонгированного действия для парентерального введения и способ ее получения - Google Patents
Твердая лекарственная форма пролонгированного действия для парентерального введения и способ ее получения Download PDFInfo
- Publication number
- RU2207845C2 RU2207845C2 RU99113827/14A RU99113827A RU2207845C2 RU 2207845 C2 RU2207845 C2 RU 2207845C2 RU 99113827/14 A RU99113827/14 A RU 99113827/14A RU 99113827 A RU99113827 A RU 99113827A RU 2207845 C2 RU2207845 C2 RU 2207845C2
- Authority
- RU
- Russia
- Prior art keywords
- dosage form
- active principle
- form according
- solid
- mucous membrane
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M37/00—Other apparatus for introducing media into the body; Percutany, i.e. introducing medicines into the body by diffusion through the skin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0024—Solid, semi-solid or solidifying implants, which are implanted or injected in body tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61D—VETERINARY INSTRUMENTS, IMPLEMENTS, TOOLS, OR METHODS
- A61D7/00—Devices or methods for introducing solid, liquid, or gaseous remedies or other materials into or onto the bodies of animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M37/00—Other apparatus for introducing media into the body; Percutany, i.e. introducing medicines into the body by diffusion through the skin
- A61M37/0069—Devices for implanting pellets, e.g. markers or solid medicaments
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Dermatology (AREA)
- Biomedical Technology (AREA)
- Heart & Thoracic Surgery (AREA)
- Chemical & Material Sciences (AREA)
- Hematology (AREA)
- Anesthesiology (AREA)
- Medicinal Chemistry (AREA)
- Medical Informatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Rheumatology (AREA)
- Epidemiology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pain & Pain Management (AREA)
- Neurosurgery (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Media Introduction/Drainage Providing Device (AREA)
- Surgical Instruments (AREA)
- Endoscopes (AREA)
- Infusion, Injection, And Reservoir Apparatuses (AREA)
Abstract
Изобретение относится к химико-фармацевтической промышленности и касается твердой лекарственной формы прологированного действия и способа получения. Изобретение заключается в том, что твердый препарат отсроченного действия для парентерального введения включает в себя гомогенную смесь активного начала в недисперсном состоянии и биосовместимого биоразрушаемого эксципиента. Предложен также способ получения лекарственной формы пролонгированного действия. Изобретение обеспечивает улучшение локальной эффективности местного лечения, позволяет уменьшить дозы и побочные эффекты. 4 с. и 66 з.п. ф-лы, 39 ил.
Description
Предметом настоящего изобретения является терапевтический способ целевого лечения нежидкими галеновыми препаратами, а также получение и устройство для осуществления данного способа.
В практике известны преимущества применения лечения или местного введения медикамента, при котором активное начало (АН) преимущественно направляется в зону действия. С другой стороны, доказано, что оральное или парентеральное введение медикамента и его системная диффузия в некоторых случаях могут не давать удовлетворительных результатов. Кроме того, даже в случаях применения общего или системного лечения, в частности в случаях применения препаратов пролонгированного действия, предпочтительно вводить препарат в соответствующую область.
Кроме улучшения локальной эффективности местное лечение по сравнению с общим лечением позволяет прежде всего уменьшить дозы и побочные эффекты, в частности, связанные с АН в областях организма, где его присутствие не приносит никакой пользы или наносит вред.
Местное введение медикамента позволяет, следовательно, улучшить терапевтический показатель препарата при возможном уменьшении его общей токсичности и опасности системных эффектов.
Лекарственные формы для местного применения, такие как накожные, глазные, полостно-носовые, легочные, а также желудочные или ректальные, стали первыми непарентеральными формами для местного введения. В тех случаях, когда область введения препарата труднодоступна или требует инвазивных форм и когда лечение необходимо повторить или, более того, проводить постоянно, даже если преимущество местного лечения очевидно, на практике его применение наталкивается на сложность и даже на неудобство многократного терапевтического вмешательства.
С другой стороны, хорошо известны преимущества применения препаратов пролонгированного или отсроченного действия, позволяющего за один прием ввести больному необходимое ему лекарство на несколько дней, несколько недель или несколько месяцев.
Такая форма отсроченного действия способствует растяжимости процесса, так как строгое соблюдение курса лечения при этом зависит не от больного, не от медицинского персонала, а от способа приготовления. Такой пролонгированный эффект повышает комфорт для пациента, который больше не связан процедурами и получает таким образом регулярную постоянную дозу, не зависящую от приемов лекарств.
Развитие лекарственных форм отсроченного действия привело специалистов к необходимости изучения их местного применения, в частности, в вышеупомянутом случае, когда место введения труднодоступно. Форма отсроченного действия позволяет избегать многократного повторения введения лекарства или, что еще важнее, хирургического вмешательства. При этом можно вести поиск достижения повышенной локальной концентрации медикамента в течение длительного периода без применения значительных системных доз, а следовательно, с меньшими побочными эффектами. Такое решение особенно полезно применительно к быстро расщепляемым препаратам или имеющим короткий период полувыведения, когда они вводятся системным путем.
Таким образом, может быть предусмотрен курс локального целевого лечения пролонгированного действия такого, как внутрисуставные или околосуставные инъекции кортикостероидов отсроченного действия. Раковые заболевания и, в частности, твердые опухоли в первую очередь могут лечиться с применением локальных форм, позволяющих уменьшить общие инъекционные дозы цитотоксичного или противоопухолевого соединения и одновременно увеличить концентрацию в опухолевой зоне, являющейся объектом лечения. Это дает возможность избежать тяжелых побочных эффектов при таком типе лечения.
"Matrix Pharmaceutical" предлагает препарат отсроченного действия на основе коллагена, которой может вводиться внутрь опухоли путем инъекции (IntraDose CDDP-Cisplatin). Такой препарат вводится в раковые зоны или в места кожных поражений при помощи шприца на 3 куб. см и, в случае необходимости, иглы для биопсии для менее доступных зон. При объеме вязкой жидкости до 2 мл он, следовательно, ограничен возможностью применения только в относительно доступных (периферических) зонах и при послеоперационном лечении.
Можно также назвать патент MITSUI (FR 2497661; JP 562737), в котором описана полилактид-полигликолидная форма (PLGA) в виде палочки или иглы для локального применения, дающая возможность прямой имплантации в зону или орган внутри организма, например в опухолевую зону до или после экзереза.
В случае формы Gliadel (Guilford) описывается препарат на основе полиангидрида в виде облатки, содержащий кармустин, который может, например, вводиться во время хирургической операции на опухоли мозга (глиобластомы).
В современной медицинской технологии такое целевое лечение внутри организма пока еще часто связано со сложными хирургическими вмешательствами. Оно использует пролонгированное действие препарата, но его сложно осуществлять повторно.
Практикуют также операции, связанные с химиоэмболизацией, заключающиеся в инъецировании внутрь сосудов суспензий (микросфер), гелей или клеев вместе с растворителем, которые способны закупорить питающий сосудистый путь и высвободить АН на уровне опухоли. Закупорка достигается за счет отложений после удаления инъекционного носителя. При таком методе для введения жидкости в сосуд используют катетеры для чрескожной транслуминальной ангиопластики.
Местное применение форм отсроченного действия также предусмотрено для некоторых полостей тела и более доступных областей организма.
Система ®Ocusent (Alza) представляет собой овальный и гибкий глазной инсертат, образующий резервуарное устройство отсроченного действия, включающее в себя мембрану из этилен-винилацетатного сополимера, и который может содержать, например, пилокарпин.
Указанное устройство помещается в свод конъюнктивы и высвобождает препарат по нулевому профилю. Форма отсроченного действия позволяет значительно уменьшить дозу, необходимую для достижения такого же эффекта на внутриглазное давление. Терапевтическая эффективность пилокарпина при лечении глаукомы при этом повышается в 8-10 раз по сравнению с местными каплями благодаря применению формы отсроченного действия.
В американском патенте 3545439, приведенном в качестве ссылки, описана интравагинальная форма отсроченного действия, представляющая собой кольцо, изготовленное из силиконового эластомера, которая высвобождает медикамент в течение нескольких недель.
В данном случае местное введение препарата отсроченного действия на слизистую оболочку влагалища также позволяет, благодаря своему АН, обеспечить общий эффект (контрацепцию).
Медицинское устройство, описанное "Bukh Meditee" (международная патентная заявка РСТ WО 89/03232, приведенная в качестве ссылки), позволяет вводить в полость тела матриксную форму отсроченного действия, изготовленную на основе вещества, почти не пропускающего воду и содержащего АН.
Форма отсроченного действия в сочетании с устройством обеспечивает таким образом локальное поступление АН в течение всего времени, на которое установлено указанное устройство. Такое устройство может представлять собой, например, катетер для уретры, вводимый в мочевой пузырь и соединенный с антибиотической формой отсроченного действия, предупреждающей инфекцию мочевыводящих путей.
Для жидких форм большого объема возможно применение некоторых существующих способов местной инъекции. На основе интрауретральных способов, С.R. BARD, например, разработал форму (Transuretral delivery Kit), являющуюся шприцом с раствором коллагена в глутаралдегиде, который может легко инъецироваться в объемах от 2,5 до 7,5 мл, образующих имплантаты без активного начала в рамках пластики против недержания мочи.
Развитие световолоконных систем позволило изготовить катетеры, высвобождающие АН из своего конца прямо в точке назначения. В отличие от просто открытого катетера, применяемого для высвобождения жидкости, местное введение может быть достигнуто при помощи катетера с двойным баллончиком или пористого катетера с множеством отверстий. Такое решение местного применения вместе с тем ограничено временем внедрения катетера. Давление, необходимое для проникновения жидкости через стенку, также создает проблему переносимости.
Для жидких форм эффективная локальная инъекция в стенку может быть осуществлена при помощи инъекционной системы, соединенной с баллончиком (Interventional Technologies), или катетера со сужающейся иглой (Bavarian Medical Technologies). Вместе с тем срок применения медикамента не может быть длительным при таких жидких формах немедленного действия.
Часть устройства может оставаться в локальной области и, следовательно, может быть объединена с формой отсроченного действия. Это происходит при применении шунтов, используемых, например, в ангиопластике для предупреждения рестеноза, которые могут быть покрыты слоем, содержащим активное начало, иногда с эффектом отсроченного действия. В данном случае возникают две проблемы: первая заключается в достижении адекватности используемого медикамента специфичному способу "покрытия" ("coating"). Вторая проблема заключается в ограниченности общей дозы пространством и поверхностью, предоставляемыми шунтом.
При применении гепарина, например, в некоторых разработках упоминается значение местного лечения для предупреждения системных побочных эффектов. В соответствии с данными исследованиями гепарин подавляет пролиферацию гладких мышечных клеток после эндотелиального поражения. Его системное применение в виде подкожной формы или локальной формы отсроченного действия, вводимой в непосредственной близости от сосуда, всегда приводит к снижению неоинтимальной пролиферации, но при этом локальная форма является единственной, которая не влечет за собой системных нарушений свертываемости крови.
Можно также привести пример осмотических насосов, применяемых для облегчения местного введения лекарств пролонгированного действия, при этом основным недостатком является необходимость их хирургической имплантации. По этой причине в настоящее время они больше не применяются на людях.
Все эти примеры свидетельствуют о пользе и преимуществах местного лечения, особенного если оно может быть пролонгированным.
Вместе с тем, все эти технические решения имеют некоторые недостатки, среди которых самыми значительными являются отсутствие поливалентности каждого данного решения, необходимость сочетания со специфичным устройством, которое остается полностью или частично внедренным на все время введения медикамента, и, наконец, ограниченность инъецируемого объема, а следовательно, дозы АН.
Каждое из данных решений позволяет проводить лечение только одного или нескольких частных случаев в точно определенной области организма.
Векторизация при помощи местного введения иногда называется первым поколением по отношению к препаратам профилактического действия "prodrugs" и векторам (липосомы...), называемым вторым поколением, или по отношению к системам макромолекулярной диагностики или активации "специфической области", называемым третьим поколением. Однако такие решения еще больше, чем современные методы локального введения, являются весьма специфичными, применяемыми не во всех случаях и иногда не отличающимися точностью.
Задачей настоящего изобретения является разработка способа устранения существующих основных недостатков местного введения или векторизации путем внедрения эндоскопических методов гибкой (фиброскопия) или жесткой (эндоскопия) хирургии и операционной радиологии (активные или неактивные катетеры).
Преимуществом недисперсионных твердых или полутвердых препаратов является то, что они занимают минимальный объем при сохранении количества АН, соответствующего лечебной дозе. Таким образом, твердые и полутвердые формы отсроченного действия позволяют обеспечить несколько дней лечения при объеме в несколько микролитров.
Местное введение лекарственного препарата позволяет значительно сократить общую терапевтическую дозу при сохранении необходимого эффекта.
Сочетание твердой или полутвердой формы отсроченного действия с местным введением позволяет осуществлять микродозировку, адаптированную для локального введения через достаточно большие интервалы времени.
Современное развитие телевизионных, оптических и микромеханических технологий в применении к медицине в области разработки внутрисосудистого или полостного инструментария и хирургии с минимальным вмешательством привело к созданию все более тонких и точных инструментов, позволяющих осуществлять местное глубокое хирургическое вмешательство в организм с минимальными хирургическими травмами и, как следствие, увеличить число доступных для такого вмешательства зон.
Настоящее изобретение предлагает, таким образом, способ, устройство и препарат, соответствующие прогрессу и миниатюризации фармацевтических и медицинских технологий.
Являющийся предметом настоящего изобретения способ имплантации или внедрения активного начала, содержащегося в твердом или полутвердом препарате, в определенную область организма заключается в том, что получают твердый или полутвердый препарат, вводят его в устройство, которое может приводиться в действие дистанционно, доставить данное устройство в указанное место внедрения, поместив его внутри классических хирургических инструментов и внедрить или имплантировать указанный препарат путем приведения в действие указанного устройства.
В соответствии с другими признаками изобретения:
- указанное место внедрения не доступно для шприца или классического подкожного троакара;
- указанный твердый или полутвердый препарат после введения его в устройство приобретает тонкую и удлиненную форму;
- указанное устройство является тонким и удлиненным для того, чтобы оно могло легко перемещаться в классических хирургических инструментах;
- указанный твердый или полутвердый препарат является препаратом отсроченного действия;
- указанная тонкая и удлиненная форма отличается минимальным отношением длины к диаметру, равным 10;
- указанное устройство является емкостью для указанного препарата, адаптированного для принятия указанной формы;
- указанная форма и указанное устройство являются цилиндрическими;
- указанная имплантация осуществляется в ткань, в слизистую оболочку или внутреннюю стенку организма через полость;
- указанная имплантация осуществляется в ткань, в слизистую оболочку или внутреннюю стенку организма через сосуд, артериальный или венозный;
- указанная имплантация осуществляется в ткань, опухоль или патогенную зону хирургическим путем;
- указанное внедрение осуществляется в полость тела или в орган внутриполостным путем;
- указанное внедрение осуществляется в полость тела или в орган или в ткань инвазивным или хирургическим путем;
- указанное активное начало является противовоспалительным агентом;
- указанное активное начало является пептидом или аналогом пептида;
- указанное активное начало является противораковым средством;
- указанное активное начало является смесью двух или нескольких активных начал.
- указанное место внедрения не доступно для шприца или классического подкожного троакара;
- указанный твердый или полутвердый препарат после введения его в устройство приобретает тонкую и удлиненную форму;
- указанное устройство является тонким и удлиненным для того, чтобы оно могло легко перемещаться в классических хирургических инструментах;
- указанный твердый или полутвердый препарат является препаратом отсроченного действия;
- указанная тонкая и удлиненная форма отличается минимальным отношением длины к диаметру, равным 10;
- указанное устройство является емкостью для указанного препарата, адаптированного для принятия указанной формы;
- указанная форма и указанное устройство являются цилиндрическими;
- указанная имплантация осуществляется в ткань, в слизистую оболочку или внутреннюю стенку организма через полость;
- указанная имплантация осуществляется в ткань, в слизистую оболочку или внутреннюю стенку организма через сосуд, артериальный или венозный;
- указанная имплантация осуществляется в ткань, опухоль или патогенную зону хирургическим путем;
- указанное внедрение осуществляется в полость тела или в орган внутриполостным путем;
- указанное внедрение осуществляется в полость тела или в орган или в ткань инвазивным или хирургическим путем;
- указанное активное начало является противовоспалительным агентом;
- указанное активное начало является пептидом или аналогом пептида;
- указанное активное начало является противораковым средством;
- указанное активное начало является смесью двух или нескольких активных начал.
Предметом настоящего изобретения также является:
- метод терапевтического лечения, при котором активное начало, содержащееся в твердом или полутвердом препарате, внедряется в полость тела таким образом, чтобы указанное активное начало высвобождалось в жидкость на поверхности указанной полости и могло действовать локально в направлении дренажных зон указанных жидкостей;
- метод терапевтического лечения, при котором активное начало, содержащееся в твердом или полутвердом препарате, имплантируется в слизистую оболочку или в секреторную внутреннюю ткань организма таким образом, чтобы указанное активное начало высвобождалось и выделялось вместе с естественными жидкостями и могло действовать локально или в направлении дренажных зон;
- метод терапевтического лечения, при котором указанное активное начало имеет местное и/или системное действие, начиная с области, в которую помещен имплантат;
- метод терапевтического лечения оториноларингологических патологий, при котором активное начало в твердом или полутвердом препарате вводят в лицевую полость или в покрывающую ее слизистую оболочку;
- метод терапевтического лечения, при котором указанное активное начало является кортикоидом;
- метод терапевтического лечения заболеваний сосудов, вен или артерий, при котором активное начало, содержащееся в твердом и полутвердом препарате, вводится в стенку сосуда или вокруг нее путем интралуминальной инъекции.
- метод терапевтического лечения, при котором активное начало, содержащееся в твердом или полутвердом препарате, внедряется в полость тела таким образом, чтобы указанное активное начало высвобождалось в жидкость на поверхности указанной полости и могло действовать локально в направлении дренажных зон указанных жидкостей;
- метод терапевтического лечения, при котором активное начало, содержащееся в твердом или полутвердом препарате, имплантируется в слизистую оболочку или в секреторную внутреннюю ткань организма таким образом, чтобы указанное активное начало высвобождалось и выделялось вместе с естественными жидкостями и могло действовать локально или в направлении дренажных зон;
- метод терапевтического лечения, при котором указанное активное начало имеет местное и/или системное действие, начиная с области, в которую помещен имплантат;
- метод терапевтического лечения оториноларингологических патологий, при котором активное начало в твердом или полутвердом препарате вводят в лицевую полость или в покрывающую ее слизистую оболочку;
- метод терапевтического лечения, при котором указанное активное начало является кортикоидом;
- метод терапевтического лечения заболеваний сосудов, вен или артерий, при котором активное начало, содержащееся в твердом и полутвердом препарате, вводится в стенку сосуда или вокруг нее путем интралуминальной инъекции.
Фармацевтические и медицинские аспекты изобретения тесно переплетаются при разработке тонкой и миниатюрной системы, которая может легко помещаться и активироваться во всех областях организма при помощи катетеров для транслуминальной чрескожной ангиопластики, эндоскопов или любого другого инвазивного инструмента, достаточно тонкого и длинного для того, чтобы достичь области внедрения. Форма (тонкая и длинная) препарата в устройстве для введения облегчает его локальное введение. Данный признак системы в его фармацевтическом и медицинском аспекте обеспечит ее общее применение.
Если под внедрением понимается форма, откладываемая на поверхность, а под имплантацией - инъекция в ткань, то средство целевого, а также пролонгированного лечения внедряется внутрь естественной полости организма, если она может играть роль естественного резервуара, то есть если форма введения медикамента позволяет ему оставаться в этой полости по меньшей мере в течение срока его высвобождения. Такая форма может быть либо удлиненной, разработанной для облегчения ее введения вместе с устройством, либо изменяющейся после ее введения.
Следовательно, форма устройства и препарата не обязательно должна быть априори адаптирована к зоне внедрения, как Ocusert, вагинальное кольцо или шунты. Однако форма препарата может изменяться после введения для того, чтобы легче удерживаться в месте введения. После введения препарат не связан полностью или даже частично с устройством введения, а остается самостоятельно в месте введения.
Если в силу каких-либо потребностей специфичного терапевтического характера и на какой-либо срок внедрение в естественную полость организма нежелательно, лекарство местного и даже пролонгированного действия может также быть имплантировано в точно заданную ткань организма, чтобы позволить его введение на весь период высвобождения.
Указанная имплантация может быть осуществлена при помощи устройства, соединенного с классическими инструментами, чрескожным, сосудистым или полостным путем в слизистую оболочку или стенку организма, или хирургическим путем в заданную ткань.
Внедрение формы отсроченного действия обеспечит местное, поверхностное или внешнее лечение, а также заданность лечения для глубинного действия, даже для системного действия, например с введением в слизистую оболочку.
Точно так же имплантация формы отсроченного действия позволит осуществлять общее лечение, а также местное заданное лечение путем локальной гиперконцентрации или путем выделения.
Таким образом, в зависимости от терапевтического применения и области, внедрение так же, как и имплантация, может решать задачи системного назначения, местного внутреннего назначения или наконец внешнего заданного назначения.
Твердые или полутвердые препараты немедленного или отсроченного действия, применяемые в способе в соответствии с настоящим изобретением, могут быть любыми твердыми или полутвердыми препаратами при условии их изготовления или упаковки в форме и объеме, совместимыми со способом и устройством для введения.
Таким образом, твердые и полутвердые препараты могут преимущественно быть препаратами, изготавливаемыми на основе биодеградирующих эксципиентов таких, например, как неорганические соли (кальция, магния, висмута, цинка); липиды; углеводы (полисахариды, сахароза, глюкоза, агароза, декстрин, циклодекстрин и их смеси); протеины (желатин, модифицированный коллаген, альбумин, казеин, производные и смеси); натуральные или синтетические полимеры (полиизобутириловая кислота, полимолочная кислота, полигликолевая кислота, полилактид-полигликолидный сополимер (PLGA), полиэфир, поликапролактон, полиэтиленгликоль, полипропиленгликоль, ®Pluronics, полиангидриды и их смеси).
Твердые или полутвердые препараты могут быть изготовлены без эксципиента или структурироваться с небольшим количеством инъецируемого эксципиента типа маннита, гиалуроновои кислоты, производных целлюлозы и т.д.
Полутвердые препараты могут быть изготовлены путем смешения АН с или без эксципиента с водой, с органическим растворителем, с маслом или с любой другой пригодной для инъецирования жидкостью, способствующей образованию полутвердой формы.
Твердые или полутвердые препараты могут быть препаратами немедленного или отсроченного действия.
Твердые препараты немедленного действия могут быть изготовлены в соответствии с патентом SCRAS (Delivery of Solid Drug Compositions WО 96/07397). Полутвердые и твердые препараты отсроченного действия могут быть изготовлены в соответствии с формулой и способом, описанными в патенте SCRAS (Sustained Release of Peptides from Solid and Semisolid pharmaceutical compositions WО 96/07398), приведенном в качестве ссылки.
В преимущественном варианте твердые или полутвердые препараты должны изготавливаться в соответствии со способами, обеспечивающими большую концентрацию активного начала, превышающую 20% и даже 40%, а в предпочтительном варианте превышающую 50% и доходящую до 100% АН.
Перед введением твердые недисперсные препараты в соответствии с настоящим изобретением должны иметь тонкую и удлиненную форму; стержень, имплантат, лопаточка, палочка или игла, для их помещения в устройство для имплантации, которое в свою очередь в случае необходимости и в зависимости от глубины введения в тело может помещаться внутри эндоскопа или катетера. Дисперсные твердые препараты (порошки, шарики) должны располагаться в устройстве в продольном направлении.
В связи с этим твердые препараты, помещаемые в устройство, должны иметь максимальный диаметр 3 мм, а предпочтительно меньше 2,5 мм и даже меньше 2 мм, а в наиболее предпочтительном варианте меньше 1 мм. В зависимости от общей дозы и особенно для форм немедленного действия или для форм короткого срока действия или малой дозы (менее 0,1 мг в день) диаметр твердых форм должен быть еще меньше - до 0,1 мм.
В некоторых случаях минимальный диаметр имеет техническое преимущество для облегчения глубокой локальной имплантации, однако в случае применения катетеров и эндоскопов более значительный диаметр уже не будет иметь такого же недостатка (в частности, по отношению к комфорту больного), как при поверхностных инъекциях типа троакара (Zoladex, зарегистрированный товарный знак фирмы "Zeneca") или минитроакара (автоинъектор, ретроинъектор: Needle-less Parenteral Intrudction Device WО 96/08289, приводится в качестве ссылки), потому что применение медицинских устройств требует, кроме всего прочего, местной или общей анестезии, либо потому что глубинная зона имплантации менее чувствительна, чем кожа.
Твердые формы могут иметь длину в несколько сантиметров, в основном менее 3 см, а предпочтительно менее 2 см, и быть адаптированными для зоны введения.
Твердые формы предпочтительно должны иметь цилиндрическую форму; их получают с использованием технологии экструзии.
Полутвердые формы в соответствии с настоящим изобретением должны иметь достаточно высокую степень вязкости, чтобы обладать высокой концентрацией АН (предпочтительно выше 20%), и оставаться однородными, позволяя при этом осуществлять глубокие инъекции через иглу устройства в соответствии с настоящим изобретением.
Полутвердые формы могут представлять собой гели, масла, пасты или любые другие полутвердые дисперсии АН в жидком носителе.
Полутвердые формы должны иметь небольшой общий объем, в основном менее 300 мкл, а предпочтительнее менее 100 мкл и даже менее 50 мкл.
В способе и устройствах в соответствии с настоящим изобретением в предпочтительном варианте должны применяться инъецируемые эксципиенты - биодеградирующие, или естественным образом выводящиеся из организма, или растворяющиеся во внутренних жидкостях организма.
Вместе с тем, в способе могут применяться устройства или препараты, изготовленные на основе небиодеградирующих биосовместимых биоматериалов, если место введения и инструменты введения позволяют легко выводить указанное устройство или указанную форму после завершения ее действия, то есть применяться скорее для инсертатов, чем для имплантатов. Устройство или препарат должны иметь тонкую и удлиненную форму, как и другие твердые формы, адаптированные к глубокому местному введению. Примерами могут служить силиконовые имплантаты "Norplant", системы-резервуары "РНЕМА" фирмы "Hydromed", а также осмотические насосы "Duros'" фирмы "Alza".
Устройства в соответствии с настоящим изобретением соответствуют твердым или полутвердым формам, соединяемым с устройство для глубокого локального внедрения или имплантации.
Устройство в соответствии с настоящим изобретением для имплантации или внедрения активного начала, содержащегося в твердом или полутвердом препарате, в заданную область организма отличается тем, что оно включает в себя одну часть, вводимую внутрь тела пациента вместе со средствами упаковки этой твердой или полутвердой формы, средствами доставки до места введения, средствами инъекции или внедрения в указанное место введения и средствами возврата после инъекции или внедрения, и одну часть, остающуюся снаружи вместе со средствами активации функций устройства.
В соответствии с другими признаками:
- средства упаковки твердых или полутвердых форм являются также средствами доставки и инъекции;
- указанное устройство включает в себя поршень внутри направляющей трубки, могущий приводиться в действие внутри троакара или катетера;
- средством упаковки, доставки и инъекции является игла;
- после приведения в действие указанная игла может быть ориентирована по отношению к устройству за счет преформования или предварительного эластичного напряжения или механическими средствами;
- внешние средства активации устройства позволяют последовательно осуществить инъекцию иглы, поступательное движение поршня до фацетки иглы для выталкивания твердой или полутвердой формы, возврат иглы по поршню, комбинированный возврат иглы и поршня;
- последовательные действия устройства при помощи внешних средств управляются на расстоянии и в определенном порядке при помощи двух съемных упоров, первый из которых расположен на толкателе, установленном коаксиально поршню, а второй является трубчатой деталью, помещенной между направляющей трубкой и толкателем.
- средства упаковки твердых или полутвердых форм являются также средствами доставки и инъекции;
- указанное устройство включает в себя поршень внутри направляющей трубки, могущий приводиться в действие внутри троакара или катетера;
- средством упаковки, доставки и инъекции является игла;
- после приведения в действие указанная игла может быть ориентирована по отношению к устройству за счет преформования или предварительного эластичного напряжения или механическими средствами;
- внешние средства активации устройства позволяют последовательно осуществить инъекцию иглы, поступательное движение поршня до фацетки иглы для выталкивания твердой или полутвердой формы, возврат иглы по поршню, комбинированный возврат иглы и поршня;
- последовательные действия устройства при помощи внешних средств управляются на расстоянии и в определенном порядке при помощи двух съемных упоров, первый из которых расположен на толкателе, установленном коаксиально поршню, а второй является трубчатой деталью, помещенной между направляющей трубкой и толкателем.
Устройства могут применяться напрямую или в сочетании с медицинскими инструментами местной терапии (эндоскопами, фиброскопами, трубками, катетерами, гвоздями, аэраторами, канюлями, перфораторами, троакарами...).
Устройства вводятся до места, и с их помощью осуществляют внедрение или имплантацию полутвердых или твердых форм. После этого они сразу же извлекаются.
Так же, как и лекарственные формы, применяемые в соответствии с настоящим изобретением устройства для осуществления способа введения твердых или полутвердых препаратов являются поливалентными и имеют небольшой объем, а также соответствующую тонкую и удлиненную форму.
Поэтому устройства должны иметь максимальный диаметр 3 мм, а в предпочтительном варианте диаметр менее 2,5 мм и даже менее 2 мм. В зависимости от лекарственной формы диаметр устройства может быть еще меньше - до 0,3 мм.
В фиброскопе или эндоскопе, например 4-канальном (видеоканал, канал введения и извлечения жидкости, инструментальный канал и оптическое световолокно), устройство внедрения или имплантации может, как и классический инструмент (типа щипцов для биопсии), занимать инструментальный канал, что высвобождает канал введения жидкости и даже позволяет его убрать. В этом случае устройства могут иметь диаметр менее 2 мм, например 1,7 мм, как некоторые инструменты.
В катетере устройство для внедрения или имплантации может, как устройство для внедрения шунтов, занимать канал и быть активировано снаружи после его доставки на место. В этом случае устройство может иметь диаметр менее 2,5 мм, например 2 мм, как некоторые шунты.
В троакаре устройство внедрения или имплантации может, как устройство перфорирования, занимать полость троакара. Устройство может иметь диаметр менее 3 мм, например 2,5 мм, как некоторые перфораторы.
Другие признаки и преимущества изобретения очевидны из нижеследующего описания, приведенного со ссылками на чертежи приложения, которые иллюстрируют различные способы осуществления в качестве примеров, не ограничивая ими возможности изобретения.
Фиг. 1 - основной вид в продольном разрезе первого варианта устройства для введения твердых препаратов в соответствии с настоящим изобретением в случае введения препарата внутрь естественной полости организма, используемой как резервуар для препарата.
На фиг.2, 3 и 4 показана последовательность работы устройства, изображенного на фиг.1, при местном введении в организм твердого препарата.
Фиг. 5 - изображение наполовину внешнее, наполовину в продольном разрезе второго варианта устройства введения препаратов в соответствии с настоящим изобретением, показанного частично введенным в организм пациента и готовым к введению твердого препарата.
Фиг.6 - изображение в поперечном разрезе по линии 6-6 фиг. 5.
Фиг.7 - изображение, аналогичное фиг. 5, показывающее устройство при выталкивании твердой формы из направляющей трубки устройства, в положении готовности к ее введению в организм пациента.
Фиг.8 - изображение в поперечном разрезе по линии 8-8 фиг. 7.
Фиг. 9 - изображение, аналогичное фиг.5 и 7, устройства после частичного извлечения иглы, при этом твердая форма остается в организме.
Фиг.10 - изображение, аналогичное фиг.9, показывающее иглу и находящийся внутри нее поршень после их полного возврата в устройство.
Фиг. 11-16 - изображения, подобные соответственно фиг.5-10, на которых показано применение устройства для введения полутвердой формы.
Фиг. 17, 18 и 19 - изображение высвобождения in vitro инсертатов дексаметазона при концентрации соответственно 10, 15 и 20%.
Фиг. 20, 21 и 22 - изображение результатов фармакокинетических исследований на крысе инсертатов дексаметазона соответственно с концентрацией 10, 15 и 20% при подкожной (А) и внутрибрюшной (В) инъекции.
Фиг. 23 и 24 - изображение результатов фармакокинетических исследований твердой формы 12,8 мг ланреотидацетата соответственно на собаке при внутримышечной инъекции и на добровольном здоровом пациенте при подкожной (А) и внутримышечной (В) инъекции.
Фиг.25 - изображение фармакокинетического исследования на здоровом добровольном пациенте полутвердой формы 40 мг ланреотида при внутримышечной инъекции.
Фиг.26 - изображение профиля высвобождения in vitro матриксного препарата ацетата трипторелина/PLGA (75:25) при 20% активного начала.
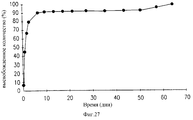
Фиг.27 - изображение профиля высвобождения in vitro препарата в соответствии с настоящим изобретением ацетата трипторелина/PLGA (75:25) при 52% активного начала.
Фиг. 28 - изображение профиля высвобождения in vitro препарата памоата трипторелина (активное начало) и PLGA (50:50) при 40% активного начала.
Фиг. 29 - изображение профиля высвобождения in vitro препарата памоата трипторелина (активное начало) и PLGA (50:50) при 52% активного начала.
Фиг. 30 - фотоизображение препарата ацетата трипторелина и PLGA (75:25) при 20% активного начала, помещенного в физиологическую среду (in vitro) после одного часа, 1 дня, 2 дней, 3 дней, 7 дней и 10 дней.
Фиг. 31 - фотоизображение препарата ацетата трипторелина и PLGA (75:25) при 52% активного начала, помещенного в физиологическую среду (in vitro) после одного часа, 1 дня, 2 дней, 3 дней, 7 дней и 10 дней.
Фиг. 32 - изображение профиля высвобождения in vitro трех форм в соответствии с настоящим изобретением при 52%, 70% и 80% активного начала (ацетат трипторелина) для дозы 9 мг.
Фиг. 33 - изображение профиля высвобождения in vitro двух форм в соответствии с настоящим изобретением при 52% активного начала (ацетат трипторелина) для доз 9 мг и 6 мг.
Фиг.34 - изображение изменения по времени уровня активного начала, остающегося в имплантатах, инъецированных крысе, для препаратов при 52%, 70% и 80% активного начала (ацетат трипторелина).
Фиг. 35 - изображение изменения по времени абсолютного остаточного количества активного начала, остающегося в имплантатах, инъецированных крысе, для препаратов при 52%, 70% и 80% активного начала (ацетат трипторелина).
Фиг. 36 - изображение кинетики у собаки в плазматических концентрациях для препарата ацетата трипторелина/PLGA (75:25) при 20% активного начала и при дозе 3 мг с отслеживанием фармацевтического эффекта по уровню тестостерона.
Фиг. 37 - изображение кинетики у собаки в плазматических концентрациях для препарата ацетата трипторелина/PLGA (75:25) при 52% активного начала и при дозе 6 мг с отслеживанием фармацевтического эффекта по уровню тестерона.
Фиг. 38 - изображение профиля высвобождения in vivo у собаки препарата ацетата трипторелина/PLGA (75:25) при 70% активного начала для дозы 9 мг (А) с отслеживанием фармацевтического эффекта по уровню тестостерона (В).
Фиг. 39 - изображение профиля высвобождения in vivo у собаки препарата ацетата трипторелина/PLGA при 52% активного начала для дозы 6 мг и при 70% активного начала для дозы 9 мг.
Устройство введения твердой формы 1, показанное на фиг.1, включает в себя направляющую трубку 2 с поршнем 3, способным вытолкнуть из направляющей трубки 2 находящуюся в ней твердую форму 1. Трубка 2 и поршень 3 имеют на своих противоположных концах соответствующие фланцы 4, 5 для ручного манипулирования.
На фиг.2 показан возможный пример инвазивной системы внедрения в организм пациента для приведения в действие устройства для введения твердой формы 1, показанной на фиг.1. В примере на фиг.2 инвазивная система представляет собой троакар 6 с мандреном-перфоратором 7, если для проникновения в естественную полость организма, используемую в качестве резервуара для твердого препарата 1, необходима перфорация внутренних тканей. На фиг.2 инвазивная система изображена частично введенной внутрь организма своей частью, находящейся справа от плоскости L в то время, как ее расположенная слева часть остается снаружи.
Если для проникновения в естественную полость организма не требуется перфорации внутренних тканей, то инвазивная система может представлять собой эндоскоп, фиброскоп или катетер (не показаны). Применяемую инвазивную систему вводят в полость тела (лицевая пазуха, пищевод, трахея, сосуд...) при помощи мандрена-перфоратора 7 в случае системы, показанной на фиг.2. Затем мандрен 7 извлекают из троакара 6 (или эндоскопа, катетера...) и внутрь троакара 6 (фиг. 3) помещают устройство для введения, показанное на фиг.1, до момента, когда фланец 4 трубки 2 упрется в кольцевой изогнутый конец 8 троакара 6.
После этого достаточно нажать на поршень 3, чтобы вытолкнуть твердую форму 1 из трубки 2, так как ее продвижение не встречает никакого сопротивления со стороны ткани (фиг.4).
Во втором варианте устройства для введения твердой формы 9, показанного на фиг. 5-10, указанное устройство предусмотрено для его введения внутрь ткани, стенки или слизистой оболочки из внутренней инвазивной системы, уже находящейся в полости, как показано на чертежах, а также из инвазивной системы, введенной во внутреннюю ткань.
Инвазивная система включает в себя трубчатую деталь 50, частично введенную в ткань через ее поверхность Р', и направляющую трубку 11, которая может быть фиброскопом или эндоскопом, в который может быть установлен катетер 12. Последний служит направляющей устройства для введения, состоящего из иглы 13 и поршня 14 для выталкивания твердой формы 9 в ткань 17.
Устройство включает в себя два съемных упора (10, 15), первый из которых является втулкой в толкателе 20, расположенном коаксиально поршню 14, при этом указанный упор 10 и толкатель усечены по длине (фиг. 8), а второй - трубчатой деталью 15, тоже усеченной (фиг.6) и помещенной между катетером 12 и толкателем 20.
Инъекция устройства для введения 13, 14, 9 может осуществляться путем перемещения направляющей трубки назад, однако в предпочтительном варианте она производится, как показано на фиг.7-10, следующим образом: вытягивают упор 15; при помощи толкателя 20 с упором 10 перемещают иглу 13 (фиг.7). В случае необходимости, как показано на фиг.7, в частности, при введении в сосуд, игла 13 может иметь на конце изогнутую форму 13а, получаемую путем освобождения иглы 13 от предварительно заданного эластичного напряжения в направляющей трубке. После освобождения от эластичного напряжения изогнутый конец 13а облегчает введение твердой формы 9 под углом в стенку или слизистую оболочку 17. Угол между иглой и направляющей трубкой может быть получен и регулироваться любым другим механизмом, обычно применяемым в таких устройствах.
После введения твердой формы 9 и изогнутого конца 13а из толкателя 20 удаляют упор 10 и вытаскивают иглу 13 при помощи выступов 16, не перемещая при этом поршень 14, чтобы отложить твердую форму 9 в ткань 17 (фиг.9). Как только фацетка 13b иглы 13 достигнет конца поршня 14, последний вытягивается вместе с иглой 13, оставляя твердую форму 9 на месте, при этом данная операция осуществляется при помощи перемещения назад толкателя 20 и выступов 16 (фиг.10).
Устройство, показанное на фиг.5-10, может также использоваться для введения полутвердой формы.
Устройство для введения, показанное на фиг.11-16, похоже на то, что показано на фиг.5-10, и отличается от него только тем, что поршень 14 действует на нетвердую форму 18, по принципу микрошприца, вплоть до конца инъектора.
В данном случае инвазивная система 9, 11, 12 тоже может вводиться во внутреннюю ткань 17.
Способ введения в данном случае заключается в введении, путем выталкивания из направляющей трубки 9, 11, 12, устройства для введения, состоящего из иглы 13, поршня 14 и полутвердой формы 18. Игла 13 может быть изогнутой, как в варианте осуществления, показанном на фиг.5-10. Поршень 14 перемещается в игле 13 для выталкивания полутвердой формы 18 (фиг.14) так же, как и в предыдущем варианте осуществления.
Поршень 14 и иглу 13 вытаскивают вместе через направляющую трубку 11, 12 при помощи выступов 16 и толкателя 20 (фиг.15 и 16), при этом оставленная в ткани 17 полутвердая форма 18 может принимать сферическую или эллипсоидную форму.
Схематические изображения, показанные на фиг. 1-16, позволят проиллюстрировать способы введения при нижеописанных различных специфических видах лечения. Указанные различные специфические виды лечения с использованием способа местного введения твердого или полутвердого препарата в соответствии с настоящим изобретением требуют соответствующего способа применения и в силу этого предполагают новые терапевтические решения, являющиеся составной частью настоящего изобретения. Различные приведенные примеры иллюстрируют сферу возможного применения настоящего изобретения, но не являются при этом исчерпывающим списком вариантов применения способа и, следовательно, не носят ограничительного характера.
В числе возможных видов лечения в рамках способа по настоящему изобретению можно указать такие виды лечебного воздействия, как анестезическое, обезболивающее, противовоспалительное, канцерологическое, кардиологическое, эндокринологическое, ревматологическое и т.д., а также и связанные с ними виды лечения. Среди эндоскопических или радиологических технологий, позволяющих применять указанный способ местного лечения, можно назвать урологию, гинекологию, артроскопию, оториноларингологию, бронхоскопию, гастрологию, хирургию с минимальным вмешательством, а также вазокардиологию.
Такие способы являются новыми, так как они используют галеновый твердый или полутвердый препарат отсроченного или немедленного действия малого объема (микролитры). Указанный препарат отличается от существующих для местного лечения, которые используются в специфических твердых формах, или жидких формах, или суспензиях большого объема.
В соответствии с данным способом и при применении нежидких препаратов препарат по своему составу и форме не разрабатывается для конкретной векторизации. Наоборот, препарат разрабатывается для инструмента или устройства, адаптированного для местного внутреннего введения и позволяющего управлять на расстоянии местной инъекцией или внедрением лекарства.
В указанной галеновой форме и с применением указанных инструментов способ позволяет использовать классические АН, в частности, такие, которые уже доказали свою применимость при местном введении, или такие, локальная применимость которых вытекает из образа действия АН, даже если оно пока не используется в данной форме, в частности, потому что такое применение не могло быть легко осуществимо без внедрения настоящего изобретения. Приведенные ниже примеры иллюстрируют возможности указанного способа.
Способ, формы и устройства позволяют производить внутриполостное и внутритканевое введение. Какой бы ни была
полость или ткань, преимуществом изобретения является то, что препарат может вводиться в зону без повреждения или с минимальным повреждением ткани.
полость или ткань, преимуществом изобретения является то, что препарат может вводиться в зону без повреждения или с минимальным повреждением ткани.
Указанные естественные полости могут использоваться в качестве резервуаров для терапевтического средства, в частности, когда их анатомическое строение позволяет "заключать" в себя препарат. Способ позволяет, например, производить введение в естественные полости или ткани лица. С использованием некоторых АН благодаря указанному способу достигается целый ряд ранее обозначенных целей (повышение локальной эффективности, сокращение дозы, увеличение времени действия, уменьшение болезненных ощущений и частоты процедур, сокращение побочных эффектов).
Внутрисинусные или околосинусные инсертаты или имплантаты доставляют АН в слизь благодаря движению ресничек слизистой оболочки или обеспечивают системную местную диффузию контактным путем. Можно также рассматривать возможность общего действия путем прогрессивной диффузии в направлении пищеварительного тракта для медикаментов, требующих ежедневного приема в небольших дозах.
Кортикоиды местного действия являются хорошим примером медикаментозного средства местного действия, хотя имеют недостатки при общем действии. Тем не менее лечение с применением существующих местных форм (капли, спреи...) наталкивается на сложности анатомического характера, затрудняющие достижение конкретно необходимой зоны, например среднего прохода, одноклеточный желобок). Кроме того, при данных существующих видах лечения необходимость постоянного присутствия АН в области действия требует частого повторения процедуры.
Указанный терапевтический способ в соответствии с настоящим изобретением позволяет достичь данной ключевой области с риносинусной патологией. Наряду с гайморовыми пазухами, при необходимости, можно проводить местное лечение решетчатых ячеек, клиновидных и лобных пазух, барабанную полость. Имплантированная или внедренная твердая или полутвердая форма отсроченного действия будет находиться в контакте с данной слизистой оболочкой, которая выделяет и покрывается слизью, перетекающей от желоба в носовые полости, вытекающей в заднюю носовую полость и вступающей в контакт с выступом в евстахиевой трубе и с самой евстахиевой трубой.
Способ позволяет, например, увеличивать и поддерживать концентрацию медикаментозного средства в одноклеточном желобке, являющемся центром патологии, в частности, воспалительных процессов. Если нежидкая форма отсроченного действия вводится внутрь синуса, то следует применять устройство, показанное на фиг.1, которое может быть введено при помощи классических дренажных инструментов, применяемых в оториноларингологии (ЛОР; троакары, трубки). Возможно также вводить препарат в слизистую оболочку носовой полости, в носовые раковины и в выступ евстахиевой трубы при помощи устройств, показанных на фиг.5-16. В зависимости от зоны введения и лекарственной формы действие будет преимущественно внешним, внутритканевым или системным.
В отоларингологии таким образом при помощи кортикостероидной терапии можно лечить, например, полипоз носовых пазух, аллергические и неаллергические риниты, некоторые отиты или неинфекционные синуситы и т.д. Кроме противовоспалительного лечения можно практиковать антибиотическое, антиаллергическое, иммуностимулирующее и другие виды лечения. Виды лечения можно также комбинировать. Указанные виды лечения основаны на местном действии.
Можно, например, изготавливать стержни матриксного дексаметазон-фосфата с уровнем 15% в PLGA в соответствии со следующими стадиями: взвешивание исходного сырья, смешивание двух порошков, экструзия, дозирование, кондиционирование и стерилизация. Полученный имплантат может иметь средний диаметр 2,4 мм при длине 12,5 мм. Он может вводиться в гайморовы пазухи при помощи устройства, показанного на фиг.1. Он может также быть имплантирован в слизистую оболочку носовой раковины при помощи устройства, показанного на фиг. 5-10.
Указанный твердый препарат является препаратом отсроченного действия на 1 месяц, содержащим 7,5 мг дексаметазона и высвобождающим в среднем 0,5 мг в день при наличии имплантата в каждом синусе. Для длительного лечения можно предусмотреть внутрипазушное применение полимерной формы (PLGA 75-25) со сроком действия в три месяца и даже резервуарную форму (типа Hydromed) со сроком действия в один год.
Указанные средства отсроченного действия могут помочь при амбулаторном лечении пациентам, страдающим, например, хронической закупоркой носа. Медицинское вмешательство для внутрипазушного введения будет таким же, как и обычные приемы, используемые в оториноларингологии и практикуемые в кабинете врача: пункция при помощи троакара с анестезией или без нее. При этом возможна подготовка пути, если без нее нельзя обойтись (меатотомия, гвозди, дренаж и т.д.).
Глубокая локализованная инъекция в носовую раковину или в слизистые оболочки носовых полостей может быть также упрощена благодаря применению устройства в сочетании с обычными инструментами эндоскопического исследования или независимо от них. Введение в носовые полости имеет небольшую глубину. В зависимости от полостей тела или места эндоскопической хирургии расстояние между внешней областью и внутренней областью введения может быть еще меньше или намного больше.
В ревматологии уже применяются кортикоиды отсроченного действия. В соответствии с указанным способом можно, например, осуществлять местное внутрисуставное или околосуставное введение формы отсроченного действия малого объема (кортикоиды, противовоспалительные средства) в место воспаления (неинфекционные тендинит, бурсит, артрит; артроз и т.д.). В соответствии со способом можно также осуществлять лечение глазных заболеваний путем введения-инъекции в слизистую оболочку под веко. Благодаря малому объему твердых или полутвердых форм такое введение не будет дискомфортным, а инъекция будет способствовать одновременно эффекту отсроченного действия и локальному поддержанию терапевтического действия лучше, чем введение в свод конъюнктивы, который подвергается интенсивному дренажу. Такой подход является особенно предпочтительным при длительном лечении, например, глаукомы при помощи пилокарпина.
В данном случае инъекция является практически поверхностной и не требует других инструментов, кроме устройства для введения полутвердых или твердых препаратов в микрообъеме.
Благодаря способу в соответствии с настоящим изобретением можно также лечить некоторые поверхностные опухоли или кожные заболевания путем местного внутрикожного или подкожного введения.
Например, дермопептин (BIM 23014C) может применяться как полутвердая форма отсроченного действия в 20%-ном водном растворе и в объеме 20 микролитров, что дает общую дозу в 4 мг соматулина. Препарат может инъецироваться на уровне келоидов или меланом, создавая таким образом повышенную и пролонгированную локальную концентрацию от зоны диффузионного градиента до места инъекции.
В случае некоторых твердых опухолей лечение может сочетаться с введением цитотоксического вещества (Type 5FU или цисплатин), диффузия которого будет регулироваться той же местной формой и локальная концентрация которого будет таким образом очень высокой при очень низкой общей дозе.
Те же препараты могут также использоваться при гораздо более глубоком применении, и в этом случае их используют совместно с инструментами типа активного катетера SMA (Shape memory Alloy) или фиброскопа и с такими методами, как операционная радиология или эндоскопическая или робототехническая хирургия.
Например, благодаря доступу в черепную коробку можно произвести внутримозговую имплантацию формы отсроченного действия BIM23014 С плюс цитотоксическое средство.
Твердые или полутвердые формы в соответствии с настоящим изобретением имеют преимущество по отношению к местному лечению по типу Gliadel, так как они могут применяться без трепанации как на поверхностном уровне, так и в глубоких отделах благодаря стереотаксической, эндоскопической и робототехнической хирургии.
Например, твердые опухоли, для лечения которых применяют колагеновые формы Matrix, можно также лечить указанными микродозами. Какой бы ни была твердая или полутвердая форма, преимущество объема позволяет векторизацию во все зоны и предупреждает риск распространения, которое может произойти при инъекции жидкого объема в несколько миллилитров.
При помощи все той же твердой или полутвердой формы, локализуемой на большей глубине в организме, после транслуминальной чрескожной ангиопластики можно лечить рестеноз путем местного внутрисосудистого введения. По сравнению с местным лечением при помощи шунта лечение согласно способу по изобретению имеет преимущество в том, что оно не наталкивается на нехватку пространства сосуда и поверхности устройства, и в том, что препарат не входит в прямой контакт с пораженной стенкой сосуда, обеспечивая при этом высокую локальную концентрацию во всех слоях сосуда и вокруг него, а также, в случае необходимости, системный эффект.
Можно, например, в соответствии со схемой, представленной на фиг.5-16, инъецировать ангиопептин самостоятельно или в сочетании с гепарином. Конечно, можно инъецировать любое другое АН, по отдельности или в комбинации, способное предупредить опасность рестеноза и способствовать лучшему результату.
В отношении указанной околососудистой терапии можно также упомянуть возможное использование полутвердых форм для внутрисосудистого введения с той же целью, что и химиоэмболизация при помощи суспензии, клея или геля. В данном случае преимущество состоит в применении формы отсроченного действия, объем которой (следовательно, и область введения) устанавливается заранее, что позволяет лучше локализовать закупорку в сосуде.
Способ и устройства в соответствии с настоящим изобретением в сочетании с фиброскопом или любым другим средством прямой или непрямой передачи изображения позволяют введение в стенки организма.
Например, когда осуществляется вмешательство на уровне мочевого пузыря через уретру, можно предусмотреть имплантацию лекарственного средства (профилактического препарата, антибиотика...) в толщу уретры.
Можно проникнуть в трахею и бронхи (шунты). Следовательно, в соответствии со способом по изобретению можно предусмотреть лечение легких либо путем введения твердой или полутвердой формы в легкое, либо путем имплантации в слизистую оболочку бронхов или трахеи в зависимости от местной переносимости при внутрилегочном введении, при этом твердая форма может быть дисперсной (порошок или сферы).
Например, для замены превентивного лечения путем ингаляции глюкокортикостероидов при легкой или умеренной астме ранней диагностики в легкое через бронхи или в перекрывающую их стенку, или в стенки трахеи можно вводить форму отсроченного действия с ежедневной дозой 0,4 мг будезонида, которая будет секретироваться в поток, если форма имплантирована, и которая будет доставляться при помощи влаги вглубь легочных альвеол. При указанном превентивном лечении малыми дозами без побочного эффекта больше не возникает проблем строгого наблюдения, в частности, при лечении детей. Такая форма может иметь срок действия от 1 до 3 месяцев и при необходимости даже больше. Для лечения пищеварительного тракта также имеются устройства для местного введения лекарственных средств в соответствии с настоящим изобретением.
В пищеводе и в желудке лечение варикозного расширения вен может быть предусмотрено при помощи местной формы, инъецируемой в стенку. Точно так же опухоли на этом уровне, носящие индивидуальный характер и поддающиеся лечению в настоящее время, например, с помощью PDT (фотохимиотерапия), после инъекции фоточувствительного вещества требуют освещения путем контролируемого введения светового диффузора на локальном уровне. Поэтому возможно также непосредственно инъецировать противораковые средства на этом уровне в твердой или полутвердой форме при помощи устройства по изобретению. В данном случае можно еще больше локализовать область лечения и избежать ненужных повреждений периферических тканей.
Способ местного введения твердых или полутвердых форм требует пролонгированного присутствия АН в месте введения. В случае необходимости можно добавлять к препарату средства, способствующие улучшению переносимости в месте введения. Например, можно добавлять слабую концентрацию дексаметазона, индометацина, гепарина и любого другого АН, способствующего устранению нежелательного местного эффекта.
Слизистые оболочки или стенки лучше поддаются проникновению, чем кожа, и существуют системы пластырей или биоадгезивов, накладываемых на слизистые (в частности, рта или носа), обеспечивающие системное проникновение АН. Недостатком иногда является недостаточная стойкость формы при контакте со слизистой оболочкой. Пролонгированный характер введения в соответствии со способом по изобретению на локальном уровне слизистых оболочек или внутренних стенок может поэтому иметь преимущество при разработке локальной формы системного действия. В зависимости от вида местного лечения к препарату можно добавлять небольшое количество любого эксципиента, способного выполнять роль вектора для внутритканевого проникновения с адаптацией к АН (органические растворители, поверхностно-активные вещества и т.д.). Таким образом, местная глубокая форма в преимущественном варианте может быть местом системной диффузии по отношению к слизистой оболочке рта или носа, например, на которую не возможно топическое нанесение пролонгированного действия.
Способ в соответствии с настоящим изобретением найдет также применение во время хирургических вмешательств с минимальной эндоскопической инвазивностью (лапароскопия, артроскопия и т.д.). Применяемые АН (местные анестетики, антикоагулянты. . . ) могут вводиться в виде твердой или полутвердой формы; здесь также проявляется преимущество микрообъема в соответствии с ограниченным пространством вмешательства и возможности введения инструментальным путем проникновения.
Само собой разумеется, что благодаря способу можно имплантировать любую другую твердую или полутвердую форму отсроченного действия, в частности, имплантаты PLGA. Их можно применять вместе с другими пептидами, рекомбинатными протеинами (интерферон), поликлональными или моноклональными антителами, олигонуклеотидами или антисмысловыми полинуклеотидами и т.д.
Твердые препараты или имплантаты, которые могут применяться для местного введения активного начала, как было описано выше, подходят также благодаря их длинной и тонкой форме и малому диаметру для других классических типов введения, например, для системного лечения путем кожной или внутримышечной инъекции.
Совершенно неожиданным образом было также обнаружено, что указанные твердые формы или имплантаты, в частности, вместе с эксципиентом PLGA с большой концентрацией активного начала, как описано выше, растворимым или нерастворимым, в частности, препараты, имеющие концентрацию между 40 и 100% и преимущественно выше 50% позволяют обеспечить in vivo чрезвычайно продолжительные сроки высвобождения - от одного до трех месяцев и больше, и очень равномерные, даже постоянные уровни высвобождения, при этом они выполнены в удлиненной и тонкой форме, с диаметром или поперечным габаритом меньше или равным 3 мм, например 2,5 или 2 мм, даже 1 мм и меньше, обладая при этом быстрой растворимостью in vitro, независимо от того, применяются ли они для местного действия или нет.
В классическом применении такие уровни активного начала предусматривались для препаратов мгновенного или быстрого высвобождения.
Изобретатели также обнаружили, что для некоторых форм при однородном распределении эксципиента, в частности PLGA, было возможным получить препарат отсроченного действия нематриксным способом, в котором эксципиент играл другую роль; это привело к получению более совершенных препаратов с другими характеристиками, что совершенно очевидно отличает их от существующих матриксных форм.
Указанные нематриксные формы могут быть квалифицированы как матриксные формы активного начала, в котором диспергируется эксципиент.
Применяемые в настоящее время и использующие PLGA матриксные формы могут быть либо дисперсными формами (микрочастицы), либо недисперсными формами (имплантаты).
Среди уже разработанных препаратов отсроченного действия в основном различают формы, называемые резервуарными, и матриксные формы.
В "резервуарных" формах используются диффузионные барьеры или мембраны между указанным активным началом и средой, которая должна служить регулятором высвобождения указанного активного начала. Медикамент может находиться внутри резервуара в виде твердой, полутвердой или жидкой формы. Он может быть в растворе или диспергированным в эксципиенте. Благодаря своей пористости мембрана обеспечивает регулируемый выход активного начала наружу. Среди "резервуарных" систем для растворимых активных начал можно назвать гидрофильные сетчатые мембраны из полиметакрилата гидроксиэтила (pHEMA, Hydro Med Services). "Резервуарные" формы позволяют получать относительно постоянный уровень высвобождения порядка 0. Основным недостатком указанных резервуарных технологий является необходимость изъятия биосовместимого имплантата, который не является биоразрушаемым после высвобождения активного начала.
В матриксных формах используется матрикс или полимерная основа, в которой содержится активное начало, высвобождаемое при диффузии, эрозии или при комбинации этих двух явлений.
Матриксные небиоразрушаемые формы, например имплантаты из гидрофобного полимера типа силикона PDMS (Norplant, прогестативные гормоны), действуют только посредством диффузии. Такой вид действия может повлечь за собой снижающееся высвобождение порядка 1, когда расстояние диффузии увеличивается. Недостатком здесь также является необходимость извлечения силиконового имплантата после высвобождения активного начала.
Биоразрушаемые матриксные формы не имеют такого недостатка, так как полимерный матрикс уничтожается организмом. Кроме того, такое уничтожение или разрушение может участвовать в регулировании высвобождения активного начала для достижения постоянного высвобождения.
В наиболее распространенных в настоящее время биоразрушаемых матриксных формах применяются полимеры молочной кислоты или гликолевой кислоты, сополимеры молочной кислоты и гликолевой кислоты (PLGA) или их смеси.
Так, в европейском патенте 52510, приведенном в качестве ссылки, описан препарат PLGA с инкапсулированным LHRH или его аналогом, который может быть дисперсной формой из микрокапсул, изготовленных при помощи коацервации, и особенностью которого является распределение активного начала в центре микрокапсулы с периферическим слоем PLGA.
Из европейского патента 58481, приведенного в качестве ссылки, известны препараты из пептидов и PLGA, дисперсные или недисперсные, такие как имплантаты, в которых активное начало однородно распределено до самой поверхности и в которых используется специфичный PLGA с возможностью взаимного перекрывания двух фаз высвобождения (диффузия и деградация) без перерыва в высвобождении активного начала.
Многие другие документы относятся к использованию PLGA в препаратах отсроченного действия для пептидов, а также для протеинов и генов. В патенте WO 96/40072, приведенном в качестве ссылки, описан препарат гормона человеческого роста, стабильность которого обеспечивается в матриксе и в органических растворителях, применяемых для микроинкапсулирования, а высвобождение которого обеспечивается матриксом PLGA. Процесс регулирования основан на разрушении полимера и следующим за ним открытием пор в структуре.
Все осуществленные на сегодняшний день разработки сходятся в том, что способ регулирования отсроченного действия с PLGA может повлечь за собой до трех фаз высвобождения. Начальная фаза, высвобождающая активное начало путем диффузии, латентная фаза, при которой не происходит никакого высвобождения, и фаза высвобождения связанных форм, коррелированная с потерей массы полимера.
Во всех препаратах, в которых используется PLGA, регулирование отсроченного действия достигается путем смешивания PLGA и активного начала таким образом, чтобы полимерный матрикс играл роль барьера для высвобождения активного начала, и даже участвовал в физико-химическом взаимодействии между активным началом и полимерным матриксом.
Во всех случаях такой способ высвобождения требует диспергирования активного начала в полимерном биоразрушаемом матриксе таким образом, чтобы изолировать зоны загрузки активным началом от внешней среды и удержать их внутри матрикса до момента, когда биоразрушение последнего высвободит активное начало, которое может после этого диффузировать наружу.
Такой тип матриксной формы отсроченного действия можно легко отличить, добавив в нее воду, которая гидратирует дисперсные зоны активного начала и приведет к разбуханию препарата под действием осмотических сил, так как активное начало не может высвободиться из матриксной структуры.
Указанные фазы в большей или меньшей степени смешиваются в зависимости от препаратов PLGA, при этом разрушение полимера приводит, например, к увеличению размеров полостей, через которые может диффузировать активное начало.
Кроме PLGA и вышеупомянутых полимолочных кислот, существует довольно мало инъецируемых эксципиентов для форм отсроченного действия. Тем не менее можно назвать некоторые полимеры, гели и жиры. Полиангидриды, например, являются полимерами, процесс поверхностной эрозии которых дает профиль высвобождения, отличающийся от профиля, получаемого с PLGA и более зависящий от формы введения, чем PLGA, который подвергается глобальному разрушению.
В некоторых препаратах отсроченного действия применяют коллаген или желатин для достижения высвобождения, растянутого во времени. В других препаратах применяют гели или гидрогели. Например, в Matrix Pharmaceutical® применяют вязкий инъецируемый гель (AccuSite®, Itradose®).
Указанные препараты, состоящие из матрикса, в меньшей степени изолирующего активное начало от среды или уничтожаемого быстрее, в основном имеют слабое процентное содержание активного начала.
Указанные препараты, состоящие из матрикса, в меньшей степени изолирующего активное начало от среды или уничтожаемого быстрее, в основном имеют слабое процентное содержание активного начала.
Также применяются другие инъецируемые эксципиенты, такие как маннит, полиэтиленгликоли, гиалуроновая кислота, чаще в качестве добавок для коррекции профиля отсроченного действия.
Кроме матриксных или резервуарных технологий в настоящее время существует мало других решений, позволяющих достичь достаточно долгого, равномерного и точного высвобождения.
Тем не менее можно упомянуть случай применения имплантатов, полностью или частично покрытых оболочкой ("coating"), играющей роль барьера при диффузии активного начала.
В дисперсных или недисперсных матриксных препаратах некоторое количество активного начала не попадает внутрь полимерного матрикса, а оказывается на поверхности препарата.
В дисперсных матриксных формах при заданном количестве активного начала поверхностное активное начало представляет собой относительно большое количество по отношению к общему количеству активного начала по причине большой площади поверхности по отношению к общему объему.
Для увеличения наполнения или "core-loading" (C.L.) активным началом приходится поэтому инъецировать большой объем полимерного матрикса для данного объема активного начала.
Этот недостаток еще больше проявляется в недисперсных формах или имплантатах, так как их объем при большом количестве наполнителя требует применения троакара для инъекции препарата.
Само собой разумеется, что было проведено немало работ для создания препаратов с повышенным C.L., но на опыте убедились в существовании феномена, известного под названием перколяции, который заключается в быстром высвобождении почти всего количества активного начала из-за того, что зоны загрузки находятся в соприкосновении друг с другом, и при этом полимер (PLGA) не обеспечивает функции матрикса.
В визуальном плане данный феномен заключается в том, что после гидратации препарата активное начало высвобождается за очень короткий промежуток времени без разбухания препарата, при этом активное начало выводится из препарата циркулирующей в полимерном матриксе водой.
В матриксных формах отсроченного действия тип PLGA и его физико-химические параметры четко очерчены и определяют рамки осуществимости. Непосредственное влияние PLGA на высвобождение АН благодаря его роли матриксного барьера, его роль в отношениях (гидрофобных, гидрофильных и т.д.) с активным началом и значение его разрушения делают обязательным условие точного выбора PLGA.
Указанная связь между PLGA и высвобождением АН ясно проявляется, например, в продолжительности действия матриксного препарата.
В таком препарате продолжительность высвобождения напрямую зависит от времени разрушения PLGA (вторая фаза или второй скачок). Поэтому выбор PLGA осуществляется в зависимости от искомой продолжительности. Например, PLGA 50:50 со сроком деполимеризации один месяц должны применяться для приготовления препарата со сроком пролонгированного действия один месяц, тогда как для приготовления препарата с 3-месячным сроком потребует использования PLGA с более поздним гидролизом, например PLGA 75:25.
В препаратах по настоящему изобретению эксципиент, в частности PLGA, не влияет на высвобождение, поэтому становится возможным, например, добиться высвобождения сроком на три месяца с применением PLGA 50:50, который полностью выводится из организма за 60 дней, или получить формы со сроком один месяц с применением PLGA 75: 25, гидролиз которого еще не начнется, в то время как активное начало уже высвободится. Это стало возможным благодаря тому, что весовое содержание PLGA всегда ниже, чем активного начала; что означает, что роль матрикса выполняет уже не PLGA, а активное начало, которое и будет подвергаться внешнему воздействию, в частности воздействию воды. Таким образом, именно активное начало будет определять продолжительность действия, в частности, своим общим количеством.
В этой связи предметом настоящего изобретения являются также указанные препараты системного назначения или для местного лечения с классической или уменьшенной (для местного действия) дозировкой.
В более конкретном плане предметом настоящего изобретения является препарат отсроченного действия для парентерального введения, включающий в себя гомогенную смесь из активного начала в недисперсном состоянии, образующего непрерывную фазу и по меньшей мере одна часть которого находится в непосредственном контакте с поверхностью обмена между препаратом и внешней биологической средой, и из биосовместимого биоразрушаемого эксципиента, при этом в препарате количество активного начала составляет по меньшей мере 50% по отношению к общему весу препарата, препарат имеет профиль высвобождения АН, независимый от состава эксципиента, от молекулярной массы эксципиента или от весового соотношения "активное начало/эксципиент", он (профиль высвобождения) зависит исключительно от общего количества активного начала в препарате.
В отличие от известных матриксных форм, позволяющих "загрузку активного начала" в пределах, превышающих 30% активного начала, чтобы избежать феномена перколяции, препараты в соответствии с настоящим изобретением содержат более 50% активного начала, что позволяет уменьшить объем вводимого средства в 3-10 раз по отношению к объему матриксных форм.
Поэтому для твердой формы препараты в соответствии с настоящим изобретением содержат предпочтительно, как до, так и после введения, по меньшей мере 50%, в предпочтительном варианте по меньшей мере 51%, в еще более предпочтительном варианте по меньшей мере 60% и в еще более предпочтительном варианте по меньшей мере 70% и до 99,999% активного начала по отношению к общему весу препарата, при этом эксципиент составляет менее 50%, предпочтительно менее 49%, еще более предпочтительно менее 30% по отношению к общему весу препарата.
В качестве эксципиентов применяются традиционные вещества, используемые в твердых формах замедленного высвобождения, в частности биоразрушаемые полимеры.
В качестве примера можно назвать полимеры полимолочной или полигликолевой кислоты, или сополимеры полимолочной и полигликолевой кислот, или смеси указанных полимеров и/или сополимеров.
Выбор биосовместимого биоразрушаемого полимера для формирования эксципиента не играет роли, так как он не влияет на степень диффузии активного начала в полимере.
Можно, например, использовать в качестве эксципиента для препаратов по изобретению инъецируемое жировое вещество, такое как полимеризованная или насыщенная жирная кислота типа ®Compiritol, или такие эксципиенты, как поливинилпирролидон (ПВП) или полиэтиленгликоль (ПЭГ).
Вязкость полимеров может быть очень разнообразной. Было показано, что полимеры с низкой вязкостью могут подходить для так называемого монофазного вида высвобождения активного начала. В вышеупомянутых европейских патентах 58481 и 52510, а также в европейских патентах 21234 и 26599, приведенных в качестве ссылки, делается акцент на полимеры низкой вязкости. Такие полимеры могут применяться и в настоящем изобретении (например, вязкость ниже 0,5 дл/г в хлороформе). Заявитель уже показал в своей ранее поданной заявке FR 9704837 и в нижеприведенных примерах, что неожиданным образом полимеры высокой вязкости, в частности выше 0,5, даже 0,6 и до 1,2 дл/г, могут подходить и им отдается предпочтение для получения монофазного высвобождения.
Можно применять DL-PLGA или L-PLGA, предпочтительнее DL-PLGA, полученный из 70-80% DL-лактида и 20-30% гликолида. PLGA синтезированный из 75% DL-лактида при 25% гликолида подходит особенно хорошо, но могут также применяться и другие сополимеры, включая PLGA 50-50. Можно также использовать D или DL-лактидные полимеры.
PLGA могут быть гидрофильными или гидрофобными. Препараты в соответствии с настоящим изобретением можно получать с гидрофильными полимерами.
Однако в качестве биосовместимого биоразрушаемого полимера предпочитают использовать PLGA, в частности гидрофильный PLGA, имеющий в предпочтительном варианте вязкость в хлороформе выше 0,6 дл/г при 3 г/100 мл.
Продолжительность действия препарата отсроченного действия определяется исключительно общим количеством содержащегося в нем активного начала.
Под активным началом в недисперсном состоянии понимается, что различные частицы активного начала, присутствующие в препарате, в большинстве своем находятся в физическом контакте друг с другом вплоть до поверхности препарата.
Поэтому понятно, что под непрерывной фазой понимают такое распределение, при котором все или большинство внутренних частей активного начала отделяются от поверхности только самим активным началом или смесью активного начала и вещества, не препятствующего диффузии или растворению активного начала.
В предпочтительном варианте смесь, образованная активным началом и эксципиентом, должна быть гомогенной по всему своему объему.
Препараты отсроченного действия в соответствии с настоящим изобретением отличаются друг от друга продолжительностью высвобождения in vitro и in vivo.
Так, препараты в соответствии с настоящим изобретением, помещенные в водную физиологическую среду, высвобождают активное начало в течение периода менее 7 дней, тогда как продолжительность действия in vivo значительно превышает указанный срок, в предпочтительном варианте она составляет по меньшей мере один месяц, а в более предпочтительном варианте - по меньшей мере три месяца.
Матриксные препараты, содержащие такое же количество активного начала, наоборот, высвобождали это АН in vitro дольше при том же количественном порядке, чем in vivo.
Удивительно то, что, несмотря на ограниченную продолжительность высвобождения in vitro, препараты по изобретению позволяют достичь гораздо большей продолжительности высвобождения in vivo безотносительно к продолжительности преципитации in vitro.
Кроме того, профиль высвобождения in vivo значительно отличается от профиля двухфазных матриксных форм и будет псевдопорядка 0, что соответствует постоянной диффузии активного начала в течение времени.
Указанный профиль высвобождения является еще одним преимуществом, так как он обеспечивает постоянный уровень высвобождения активного начала в организме.
Препараты в соответствии с настоящим изобретением инъецируются непосредственно в твердой форме без присутствия какого-либо жидкого эксципиента; высокая доля активного вещества является в этой связи определяющим преимуществом, позволяя значительно сократить объем препарата.
Так, по сравнению с матриксной формой 20% активного начала новые препараты по изобретению, например при 70% активного начала, позволяют сократить объем в 3,5 раза или увеличить дозу в 3,5 раза при идентичном объеме.
Это значит, что там, где для активного начала недисперсной матриксной формы требовался троакар для инъекции имплантата диаметром больше 1,8 мм, теперь достаточно стандартной иглы для внутримышечного введения, чтобы ввести микроимплантат препарата по изобретению, имеющий диаметр меньше 1 мм.
Кроме того, характер высвобождения препарата по изобретению без абсорбции жидкости и начального разбухания матрикса имеет преимущество стабильности активного начала, которое сохраняется в контролируемой среде. В этой связи формы отсроченного действия по изобретению являются особенно преимущественными для нестойких активных начал, таких как рекомбинантные протеины.
Поскольку, учитывая природу биосовместимого биоразрушаемого полимера, образующего эксципиент, ограничений для активного начала нет, то возможно вносить в препараты в соответствии с настоящим изобретением активные начала с высокой молекулярной массой, которые не могли диффузировать в матриксных формах при существующем уровне техники, в частности синтетические или натуральные макромолекулы, в частности протеины или их аналоги.
Таким образом, настоящее изобретение позволяет высвобождение в течение длительного периода нестойких молекул, в частности пептидов и протеинов или их аналогов.
Среди активных веществ, которые могут использоваться для целей настоящего изобретения, можно назвать протеины, пептиды, выбранные, например, из группы, состоящей из ацетата, трипторелина, ацетата ланреотида, соединения с активностью LH-RH, такого как трипторелин, госерелин, лейпрорелин, бусерелин или их соли, антагонист LH-RH, антагонист GPIIb/IIIa, соединение с активностью, сходной с антагонистом GPIIb/IIIa, эритропоэтин (ЕРО) или один из его аналогов, различные интерфероны α, интерферон β или γ, соматостатин, производное соматостатина, описанное в европейском патенте 215171, приведенном в качестве ссылки, аналог соматостатина, описанный в американском патенте 5552520 (указанный патент содержит список других патентов, описывающих аналоги сомастотатина и включенных в настоящую заявку в качестве ссылки), инсулин, гормон роста, фактор, освобождающий гормон роста (GRF), эпидермальный фактор роста (EGF), меланоцитостимулирующий гормон (MSH), гормон, освобождающий тиреотропин (TRH), гормон, стимулирующий щитовидную железу (TSH), лютеинизирующий гормон (LH), фолликулостимулирующий гормон (FSH), паратиреоидный гормон (РТН) или одно из его производных, хлороводородное соединение лизоцима, N-концевой фрагмент пептида (положение 1->34) человеческого гормона РТН, вазопрессин или одно из его производных, окситоцин, кальцитонин, производное кальцитонина, обладающее сходной акивностью, глюкагон, гастрин, секретин, панкреозимин, холецистокинин, ангиотенсин, лактоген плаценты человека, человеческий хорионический гонадотропин (HCG), энкефалин, колониестимулирующий фактор (CSF), производное энкефалина, эндорфин, киоторфин, интерлейкины, например интерлейкин 2, туфтсин, тимопоэтин, тимостимулин, гуморальный тимусный фактор (THF), сывороточный тимусный фактор (FTS), производное сывороточного тимусного фактора (FTS), тимозин, тимусный фактор X, фактор некроза опухоли, мотилин, бомбезин или одно из его производных, описанных в американском патенте 5552520 (в этом патенте содержится список других патентов, описывающих производные бомбезина и включенных в настоящую заявку в качестве ссылки), пролактин, нейротенсин, динорфин, церулеин, вещество Р, урокиназа, аспарагиназа, брадикинин, калликреин, фактор роста нервов, фактор свертывания крови, полимиксин В, колистин, грамицин, бацитрацин, пептид, стимулирующий белковый синтез, антагонист эндотелина или одна из его солей или производных, вазоактивный кишечный полипептид (VIP), адренокортикотропный гормон (АСТН), фактор роста, полученный из тромбоцитов (PDGF), морфогенетический костный протеин (BMP) и желудочный полипептид-ингибитор (GIF). Специалисты могут использовать в случае надобности любое другое водорастворимое вещество или одну из его солей или предшественников.
Преимущественно следует использовать водорастворимое вещество, полученное путем солеобразования в виде катиона, например, с помощью уксусной кислоты. Вместе с тем можно использовать нерастворимую соль, например памоат.
Под пептидом и/или протеином понимается как сам пептид и/или протеин, так и фрагменты указанных фармакологически активных пептидов или протеинов.
Активным водорастворимым веществом, применяемым для приготовления препаратов или имплантатов в соответствии с настоящим изобретением, может быть ацетат трипторелина, ацетат ланреотида, госелерин, лейпрорелин, бусерелин или их соли.
Преимущество указанных препаратов состоит также в том, что они могут вводиться благодаря вышеописанному устройству для способа по изобретению.
Способы получения препаратов в соответствии с настоящим изобретением основываются на технологиях смешивания, сжатия, экструзии в расплавленном состоянии и формования, обычно применяемых в области изготовления галеновых форм отсроченного действия.
Предметом настоящего изобретения является также способ получения препарата отсроченного действия в соответствии с настоящим изобретением, включающего в себя следующие стадии:
- приготовление гомогенной смеси активного начала и эксципиента с содержанием активного начала не менее 50%;
- сжатие указанной смеси; и
- экструзия указанной сжатой смеси в расплавленном состоянии.
- приготовление гомогенной смеси активного начала и эксципиента с содержанием активного начала не менее 50%;
- сжатие указанной смеси; и
- экструзия указанной сжатой смеси в расплавленном состоянии.
Альтернативный способ, применяющийся в основном для матриксных и нематриксных композиций независимо от содержания активного начала и эксципиента, в частности PLGA, предназначенных для местного и неместного применения и не требующих ни растворителя, ни нагревания смеси, включает в себя следующие стадии:
- получение гомогенной смеси активного начала и эксципиента;
- сжатие гомогенной смеси, предпочтительно при усилии, превышающем 1000 кг;
- раздробление полученных компактов; и
- изготовление формы, соответствующей виду введения.
- получение гомогенной смеси активного начала и эксципиента;
- сжатие гомогенной смеси, предпочтительно при усилии, превышающем 1000 кг;
- раздробление полученных компактов; и
- изготовление формы, соответствующей виду введения.
В соответствии с первым способом осуществляют, например, следующие операции.
Берут навеску активного начала (АН) и PLGA в требуемых весовых пропорциях (например, 70% АН и 30% PLGA).
Производят смешивание для получения гомогенной смеси, например, при помощи смесителя ®Turbulat. Затем смесь загружают в прессовую форму.
Производят уплотнение, фактически соответствующее "мягкому" прессованию, позволяющему получать прессованные формы, например, диаметром в 13 мм и толщиной в 5 мм. Указанная операция осуществляется преимущественно при помощи коленчато-рычажного пресса.
Производят измельчение прессованных форм, которое может осуществляться, например, путем грохочения, при помощи шаровой криомельницы или ножевой мельницы.
Данная операция должна способствовать улучшению потока порошковой смеси во время экструзии, что необходимо особенно в ситуации, когда расплавленная часть составляет меньше 50% от общего количества.
Производят экструзию смеси через фильеру с диаметром, равным диаметру требуемых микроимплантатов. После проверки диаметра при помощи лазерных лучей (Кеуепсе) на протяжном ленточном приборе получают экструдированное вещество.
В предпочтительном варианте калибровка микроимплантатов осуществляется при помощи экструзионной насадки, а не протяжного прибора.
Экструдированное вещество разрезают по длине на необходимые отрезки в зависимости от аналитического контроля для получения микроимплантатов, которые потом будут заряжаться в инъекторы перед гамма-излучением (25 кГр).
По второму способу осуществляют, например, следующие операции.
После получения смеси АН и PLGA производят не простое уплотнение, а прессование под высоким давлением смеси из тех же компонентов (эксципиент и активное начало).
Такое гиперсжатие может быть достигнуто при приложении усилия минимум в одну тонну.
Результатом такого гиперсжатия, производимого на достаточно большом диаметре, например 13 мм или выше, является преобразование данного термопластичного (способного плавиться при температуре) эксципиента в структуру, сходную со структурой, получаемой при горячей обработке, то есть прозрачной и стекловидной, весьма отличной от предыдущей структуры, получаемой после простого уплотнения.
Указанная операция проводится при температуре окружающей среды, в холоде и даже ниже 0oС. Во время указанного гиперсжатия при низкой температуре достигается переход к пластическому состоянию эксципиента внутри смеси.
Полученные гиперпресованные формы затем измельчают, как в предыдущем способе, и уплотняют до формы микрокомпактов, подобных вышеописанным микроимплантатам.
Такая технология, специально приспособленная для получения форм PLGA отсроченного действия, позволяет без температуры, растворителя и специальных производственных носителей получать галеновые формы, способные сохранять целостность активного начала, в частности, нестойких молекул, например, таких как рекомбинантные протеины.
Указанный способ интересен также для изготовления матриксных форм (содержащих не более 50% активного начала), дисперсных или недисперсных. Для матриксных форм сжатие PLGA позволяет получить матриксную структуру, эквивалентную получаемой при расплавлении эксципиента.
Гиперпресованные формы после измельчения могут
непосредственно применяться в форме дисперсии микрочастиц.
непосредственно применяться в форме дисперсии микрочастиц.
Дисперсная форма может инъецироваться непосредственно после зарядки в иглу вышеописанного устройства либо инъецироваться в виде суспензии в жидкой среде (например, в случае микросфер).
Одним из возможных аспектов для твердой формы является удлиненный цилиндр.
Препарат, описанный выше, может преимущественно иметь формы и размеры, определенные выше, соответствующие описанному устройству для местного введения.
В предпочтительном варианте препарат имеет форму цилиндра диметром меньше 3 мм, предпочтительно меньше 1 мм и длиной меньше 50 мм, предпочтительно меньше 30 мм, при этом общий объем должен быть меньше 55 мм3, предпочтительно меньше 20 мм3.
Предметом настоящего изобретения является также метод терапевтического лечения, включающий в себя инъекцию пациенту, нуждающемуся в лечении, которое требует высвобождения активного начала в течение длительного периода времени, препарата по изобретению.
Препарат может быть инъецирован преимущественно подкожным или внутримышечным путем.
Это может быть осуществлено при помощи любого соответствующего средства, в частности стандартной инъекционной иглы диаметром меньше 1 мм.
Предметом настоящего изобретения является также применение вышеописанного твердого препарата для достижения отсроченного эффекта.
Нижеследующие примеры иллюстрируют изобретение.
ПРИМЕР 1.
Внутрипазушный инсертат фосфата дексаметазона, форма PLGA.
Изготовление инсертатов дексаметазона фосфата осуществляют в соответствии со следующими фазами.
Навеска сырья, смешивание, первая экструзия, измельчание и грохочение, дозирование и упаковка, все под ламинарными потоками класса А в белом зале класса D, и наконец стерилизация.
Для одной партии можно, например, взвесить 38,25 г сополимера лактида-когликолида PLGA (50: 50) и добавить 6,75 г дексаметазона-21-двунатриевого фосфата, измельченных до размера менее 100 микрометров.
Порошок смешивают в смесителе с трехмерным движением и при первой экструзии контролируют качество смеси (% АН).
После экструзии смесь вновь измельчают и экструдируют в виде прутков диаметром 2-2,5 мм, при этом проверяют ее однородность (% АН, содержание АН/длина). Затем рассчитывают вес инсертата, необходимый для получения дозы, эквивалентной 7,5 мг дексаметазона фосфата. Цилиндры разрезают по длине на отрезки, соответствующие необходимому весу, и упаковывают их в индивидуальном порядке в контейнерные устройства под воздействием гамма-излучения (25 кГр).
Устройство может непосредственно применяться внутри троакара диаметром 3 мм и длиной 10 см, как показано на фиг.5-10.
Перед тем, как провести исследование эффективности указанных инсертатов на гайморовой пазухе, например, при хронической закупорке носа, проверяют высвобождение АН in vitro и in vivo на объекте, дающем возможность сделать прогноз по продолжительности действия инсертата.
In vitro, высвобождение наблюдают, измеряя количество АН в HPLC в изотонической среде, в которую помещают инсертат. На фиг. 17, 18 и 19 показаны значения высвобождения in vitro для трех различных концентраций АН, соответственно 10, 15 и 20%.
Исследования in vivo проводят на модели крысы. Инсертат вводят либо подкожным, либо внутрибрюшным путем и высвобождение в течение одного месяца оценивают приблизительно путем определения количества АН, остающегося в инсертате после забоя животных и взятия проб через определенные промежутки времени.
На фиг. 20, 21 и 22 показаны результаты этого контроля in-vivo для трех концентраций при подкожном введении (А) и внутрибрюшном введении (В).
ПРИМЕР 2.
Транслуминальный имплантат ацетата ланреотида, твердая форма.
Изготовлены имплантаты или цилиндры диаметром 0,75 мм и длиной 30 мм. Они содержат 12,80 мг ланреотида (BIM2301-4С) в составе 90% ацетата ланреотида и 10% маннита.
Для партии из 200 единиц или 4,5 г твердого препарата (ацетат ланреотида-маннит) получение состоит из следующих стадий: взятие навесок, связывание, разрежение, гидратация, смешивание, экструзия, сушка, расфасовка и облучение.
Навеска соответствует объему раствора вода-маннит, с одной стороны, в одном шприце и порошку ацетата соматулина в другом шприце.
Связывание заключается в соединении двух шприцев через посредство шарового трехканального клапана.
Вакуум создается внутри порошка АН.
Гидратацию проводят за счет контакта порошка в вакууме с раствором маннита. Смесь получается при помощи поступательно-возвратного движения приведенных в действие поршней двух шприцев. После проверки HPLC на гомогенность производится экструзия прутка через фильеру, настроенную на нужный диаметр. Экструзия также осуществляется путем приведения в действия поршня шприца при помощи двигателя.
Сушку производят до или после нарезки цилиндров. Она заключается в выпаривании воды из пастообразной смеси для получения сухого цилиндра.
Расфасовка состоит в помещении цилиндра внутри инъекционной иглы в устройство диаметром 1 мм, показанное на фиг.5.
Стерилизационное облучение после упаковки устройства осуществляют при 25 кГр.
Указанное устройство может быть инъецировано на местном уровне для введения цилиндра ланреотида до или после ангиопластики, как шунт, через канал катетера.
Местное отсроченное действие этого препарата было предварительно проверено путем внутримышечного (вмв) введения на собаке и путем внутримышечного и подкожного (пкв) введения на человеке.
На фиг.23 показан результат фармакокинетического исследования на собаке твердой формы 12,8 мг ланреотида при внутримышечном введении.
На фиг. 24 показан результат кинетического исследования на добровольном здоровом пациенте при подкожном (А) и внутримышечном введении (В).
Полученные результаты позволяют рассчитывать на отсроченное действие на местном уровне при ангиопластике с высокой местной концентрацией на указанный период.
ПРИМЕР 3.
Полутвердая форма ацетата ланреотида.
Ацетат ланреотида образует вместе с водой пасту или инъецируемую полутвердую форму отсроченного действия.
Эффект отсроченного действия достигается отложением непосредственно из активного начала. Данный эффект зависит от процентного содержания. Продолжительность действия в данном случае прямо пропорционально эрозии или уничтожению указанного полутвердого отложения. Поэтому в соединении может участвовать любое другое активное начало, местный эффект которого в сочетании с ланреотидом будет представлять интерес. Продолжительность действия активного начала или активных начал оценивают единственно на основе фармакокинетики ланреотида.
Изготовление полутвердой формы похоже на способ, описанный в примере 2, но без маннита. Экструзия, сушка и расфасовка заменены распределением. Например, для 200 единиц готовят 40 г ацетата ланреотида в случае формы месячного действия с 35% ацетата ланреотида, 65% воды и для вводимых доз 40 мг АН.
Стадиями получения являются взятие навесок, связывание, разрежение, гидратация, смешивание, распределение и облучение.
Распределение состоит в объемном заполнении инъектора (фиг.11-16), например, при помощи роторного поршня из шприца-смесители. Указанный полутвердый препарат прошел клиническое испытание путем внутримышечного введения (фиг.25) добровольному здоровому пациенту.
Таким образом можно получить форму с продолжительностью местного действия в один месяц. Концентрация и количество пасты будут определять продолжительность и интенсивность локальной диффузии.
ПРИМЕР 4.
Сравнение матриксной формы с 20% активного начала с нематриксной формой с 52%.
Легкорастворимую соль ацетата трипторелина (AT) смешивают с PLGA (75:25) с молекулярной массой более 100000 и с вязкостью 1 дл/г в хлороформе, которая только через месяц подвергается гидролизу с потерей массы, влияющему на высвобождение из матрикса.
Таким образом изготавливают смеси с 20% (до перколяции) и с 52% по весу активного начала в PLGA. Смеси экструдируют таким образом, чтобы получить имплантаты, которые проверяют на высвобождение in vitro при 37oС в 10 мл физиологической сыворотки и без взбалтывания.
Имплантаты с 20% активного начала высвобождают только 4% общей дозы за два дня и только 6,7% за 36 дней до того, как произойдет потеря массы полимера, которая влечет за собой высвобождение активного начала между 36-м и 60-м днями (фиг.26). Имплантаты с 52% активного начала высвобождают 66% общей дозы за два дня и более 90% за одну неделю (фиг.27).
ПРИМЕР 5.
Сравнение матриксной и нематриксной форм с нерастворимой солью трипторелина (памоат трипторелина).
Готовят два препарата памоата трипторелина и PLGA (50:50), первый с 40% и второй с 52% активного начала.
Сравнивают на модели in vitro высвобождение этих двух препаратов (низкая растворимость активных начал требует объема суспензирования в 100 мл).
Несмотря на нерастворимость активного начала, отмечают высвобождение по матриксному типу с 40% (фиг.28). При 52% (фиг.29) высвобождение уже в значительной степени независима от матрикса.
Следовательно, действие in vitro активного начала по отношению к PLGA в матриксной и нематриксной форме не зависит от растворимости его соли.
ПРИМЕР 6.
Макроскопическое различие в принципе действия между матриксной и нематриксной формами.
Матриксный препарат, описанный в примере 4, PLGA 75:25 - ацетат трипторелина (80%-20%) - в недисперсной форме после пребывания в течение десяти дней в физиологической среде in vitro содержит практически все свое активное начало; он имеет вид светопроницаемого вещества с увеличением диаметра и уменьшением длины по отношению к времени 0 (фиг.30), что указывает на деформацию матрикса PLGA.
Нематриксный препарат PLGA 75:25 - ацетат трипторелина (48%-52%) - в тех же условиях после десяти дней практически полностью освобождается от активного начала. При этом он не претерпел изменений ни по диаметру, ни по длине (фиг.31).
Таким образом, активное начало высвободилось из нематриксной структуры PLGA. В данном случае активное начало не подвергается никакому физико-химическому деформационному воздействию вместе с полимером. PLGA остается неизменным в течение высвобождения активного начала.
ПРИМЕР 7.
Сравнение между нематриксной формой (52% ацетата трипторелина) и нематриксными формами (70% и 80% ацетата трипторелина).
На такой же модули in vitro, как и в примере 4, произвели сравнение трех нематриксных форм одинаковой дозы в 9 мг. Результаты высвобождения АН за один день (фиг.32) показывают сходство в действии этих трех препаратов. Следовательно, значение высвобождения, достигнутого in vitro, не имеет прямо пропорциональной зависимости от C.L. Это показывает роль активного начала и его общего количества в действии нематриксных форм.
ПРИМЕР 8.
Сравнение высвобождения in vitro нематриксных форм с 52% АН для доз в 6 мг и 9 мг.
Два препарата, в которых используется тот же PLGA 75:25 с молекулярной массой больше 100000, изготовлены с C.L. 52% ацетата трипторелина (AT). Контроль за этими двумя препаратами проводился in vitro, первый препарат с дозой в 9 мг (52% AT в 9 мг), а второй - дозой в 6 мг (52% AT в 6 мг). Результаты (фиг.33) показывают различие в кинетике высвобождения, связанное с различием в дозе активного начала.
ПРИМЕР 9.
Сравнение матриксных форм с 52%, 70% и 80% активного начала (ацетат трипторелина) при испытании in vivo на крысе.
Две партии имплантатов с 52% активного начала, одна партия с 70% активного начала и одна партия с 80% активного начала, были инъецированы подкожным путем четырем группам из 12 крыс каждая: по четыре крысы из каждой группы были умерщвлены на 1-й день, на 4-й день и на 19-й день. Имплантаты были извлечены и отдозированы по HPLC для определения остаточного количества активного начала.
На фиг.34 показаны результаты, отражающие остаточный уровень имплантатов в процентном выражении в промежутке с 0 по 19-й день.
Отмечается очевидная параллельность в уменьшении данного процентного содержания между формами 52%, 70% и 80%.
На фиг. 35 показано изменение остаточного количества чистого активного начала в мг. Отмечается, что в отличие от результатов in vitro после 19 дней в среднем активное начало остается в количестве, которое является значительным и эквивалентным в имплантатах 52% и в имплантатах 70% и 80%.
У живых крыс перед умерщвлением были взяты пробы плазмы, и указанный результат был подтвержден путем анализа RIA.
ПРИМЕР 10.
Результаты фармакокинетического исследования матриксного препарата (20% активного начала) и нематриксного препарата (52% активного начала) на собаке.
Препараты 20% ацетата трипторелина и 52% были инъецированы внутримышечным путем в два приема шести собакам в общих дозах соответственно 3 и 6 мг чистого трипторелина и при помощи анализа RIA плазматических проб отслеживали кинетику и динамическую эффективность активного начала в сравнении с уровнями тестостерона (фиг.36 и 37).
Результаты показывают активность высвобождения в течение трех месяцев в обоих случаях.
Кинетика формы 20% имеет классический профиль (с пиком и повторным скачком). Кинетика формы 52% несравнима с классическими формами PLGA, но имеет профиль псевдопорядка 0 без пиков и повторных скачков.
ПРИМЕР 11.
Результаты фармакокинетического исследования нематриксной формы с 70% активного начала на собаке.
Препарат с тем же PLGA и тем же активным началом, что и препарат с 52% активного начала (пример 10), был изготовлен с 70% и 30% PLGA.
Указанный препарат был инъецирован внутримышечным путем собаке общей дозой 9 мг чистого трипторелина. При помощи анализа RIA плазматических проб была отслежена кинетика (фиг.38А), а также динамическая эффективность активного начала с уровнями тестостерона (фиг.38В).
Результаты показывают активность высвобождения в течение по меньшей мере трех месяцев, как и для формы 52% активного начала, с единственным отличием, заключающимся в более высоком уровне высвобождения при изменении общей дозы.
Изменение загрузки между 52% и 70% не влияет ни на продолжительность, ни на профиль, и уровень высвобождения зависит от общей введенной дозы (фиг. 39).
Claims (70)
1. Твердая лекарственная форма пролонгированного действия, содержащая по меньшей мере одно активное начало и биоразрушаемый эксципиент, отличающаяся тем, что эксципиентом является полилактид-гликолидный сополимер (PLGA), и тем, что концентрация активного начала составляет по меньшей мере 40%.
2. Лекарственная форма пролонгированного действия по п.1, отличающаяся тем, что концентрация активного начала составляет по меньшей мере 50%.
3. Лекарственная форма пролонгированного действия по одному из пп.1 и 2, отличающаяся тем, что она имеет тонкую и удлиненную форму с диаметром, не превышающим 3 мм.
4. Лекарственная форма пролонгированного действия по п.3, отличающаяся тем, что ее диаметр не превышает 2 мм.
5. Лекарственная форма пролонгированного действия по п.3, отличающаяся тем, что ее диаметр составляет порядка 0,1 мм.
6. Лекарственная форма пролонгированного действия по одному из пп.1-5, отличающаяся тем, что минимальное соотношение длина/диаметр равно 10.
7. Лекарственная форма пролонгированного действия по одному из пп.1-6, отличающаяся тем, что она содержит активное начало пептидного или белкового происхождения.
8. Лекарственная форма по одному из пп.1-7, отличающаяся тем, что она содержит низкую дозу активного начала по сравнению с обычной дозой рассматриваемого активного начала для лечения системным путем.
9. Лекарственная форма по одному из пп.1-8, являющаяся твердой, которая может быть деформирована предварительным напряжением в доводочном устройстве удлиненной формы и восстанавливать первоначальную форму in situ.
10. Лекарственная форма по одному из пп.1-9, отличающаяся тем, что она выполнена таким образом, чтобы высвобождение активного начала происходило в анатомической полости, в которую указанная лекарственная форма вводится.
11. Лекарственная форма по п.10, отличающаяся тем, что она имеет заранее рассчитанную форму, адаптированную к анатомической полости организма таким образом, чтобы предотвратить ее смещение или уничтожение.
12. Лекарственная форма по п.11, отличающаяся тем, что она подвергается предварительному напряжению в указанных доводочных средствах и восстанавливает свою непрямолинейную форму после введения в заданную область.
13. Лекарственная форма по п.11, отличающаяся тем, что ее длина и диаметр рассчитаны таким образом, чтобы предупредить ее уничтожение или смещение.
14. Лекарственная форма по одному из пп.1-13, отличающаяся тем, что указанная лекарственная форма и содержащееся в ней активное начало выполнены таким образом, чтобы активное начало высвобождалось в секрет слизистой оболочки.
15. Лекарственная форма по одному из пп.10-14, отличающаяся тем, что указанная полость или слизистая оболочка являются полостью или слизистой оболочкой лицевой области или области ЛОР.
16. Лекарственная форма по п.14, отличающаяся тем, что указанная слизистая оболочка является трахеопульмональной слизистой оболочкой.
17. Лекарственная форма по п.14, отличающаяся тем, что указанная слизистая оболочка является слизистой оболочкой рта и пищевода.
18. Лекарственная форма по одному из пп.14-17, отличающаяся тем, что она выполнена таким образом, чтобы быть помещенной на поверхность указанной слизистой оболочки для того, чтобы активное начало распространялось со слизью.
19. Лекарственная форма по одному из пп.14-17, отличающаяся тем, что она выполнена таким образом, чтобы быть помещенной внутри слизистой оболочки.
20. Лекарственная форма по п.19, отличающаяся тем, что указанная лекарственная форма и содержащееся в ней активное начало предназначены для введения в субпальпербральную слизистую оболочку.
21. Лекарственная форма по одному из пп.10-20, отличающаяся тем, что она включает в себя кортикоид для лечения, в полости, стенке полости или слизистой оболочке, полипоза пазух носа, аллергических и неаллергических ринитов, неинфекционных отитов или синуситов путем введения в гайморову пазуху, клиновидную пазуху и лобную пазуху, в слизистую оболочку носа, решетчатые ячейки или барабанную полость.
22. Лекарственная форма по одному из пп.1-9, отличающаяся тем, что указанная лекарственная форма и содержащееся в ней активное начало предназначены для введения в/или вокруг стенки сосуда путем интра- или транслуминально.
23. Лекарственная форма по п.22, применяемая, в частности, после транслуминальной чрескожной ангиопластики, содержащая активное начало для профилактики или лечения рестеноза.
24. Лекарственная форма по п.23, содержащая только ангиопептин или ангиопептин в сочетании с другим активным началом, в частности, с гепарином.
25. Лекарственная форма по одному из пп.1-9, отличающаяся тем, что указанная лекарственная форма и содержащееся в ней активное начало предназначены для введения под опухолевую ткань для противоопухолевого действия.
26. Лекарственная форма по п. 25, в которой активное начало содержит фоточувствительное вещество.
27. Лекарственная форма по одному из пп.1-9, отличающаяся тем, что указанная лекарственная форма и содержащееся в ней активное начало выполнены для внутри- или околосуставного введения.
28. Лекарственная форма по одному из пп.1-27, отличающаяся тем, что она содержит противовоспалительное активное начало.
29. Лекарственная форма по одному из пп.1-28, отличающаяся тем, что она содержит активное начало пептидного или белкового происхождения.
30. Твердая лекарственная форма пролонгированного действия для парентерального введения, содержащая гомогенную смесь активного начала в недисперсном состоянии, образующую непрерывную фазу, по меньшей мере одна часть которой находится в непосредственном контакте с обменной поверхностью препарата и внешней биологической среды, и биосовместимого биоразрушаемого эксципиента, в котором количество активного начала составляет по меньшей мере 50% по отношению к общему весу препарата и имеет профиль высвобождения, не зависящий от состава эксципиента, от молекулярной массы эксципиента и от весового соотношения "активное начало/эксципиент", при этом профиль высвобождения в основном зависит исключительно от общего количества активного начала, присутствующего в препарате.
31. Лекарственная форма пролонгированного действия по п.30, отличающаяся тем, что биосовместимым биоразрушаемым эксципентом является полимер или сополимер молочной и/или гликолевой кислот или смесь полимеров и/или сополимера молочной и/или гликолевой кислот.
32. Лекарственная форма пролонгированного действия по п.31, отличающаяся тем, что указанный биосовместимый биоразрушаемый полимер является сополимером молочной кислоты и гликолевой кислоты (PLGA).
33. Лекарственная форма пролонгированного действия по пп.30-32, отличающаяся тем, что указанный биосовместимый биоразрушаемый полимер является сополимером молочной и гликолевой кислот и обладает вязкостью в хлороформе при 1 г на 100 мл, превышающей 0,6 дл/г.
34. Лекарственная форма пролонгированного действия по п.32 или 33, отличающаяся тем, что сополимер молочной кислоты и гликолевой кислоты является гидрофильным.
35. Лекарственная форма пролонгированного действия по одному из пп.30-33, отличающаяся тем, что при введении in vitro в жидкую физиологическую среду она высвобождает почти все активное начало менее чем за одну неделю.
36. Лекарственная форма пролонгированного действия по одному из пп.30-35, отличающаяся тем, что она содержит полностью гомогенную смесь активного начала и эксципиента.
37. Лекарственная форма пролонгированного действия по одному из пп.30-36, отличающаяся тем, что высвобождение активного начала происходит в одну единственную фазу - фазу диффузии.
38. Лекарственная форма пролонгированного действия по одному из пп.30-37, отличающаяся тем, что содержание активного начала составляет по меньшей мере 51%, предпочтительно по меньшей мере 60%, еще более предпочтительно по меньшей мере 70% и до 99,999% по отношению к общему весу препарата, а эксципиент составляет менее 50%, предпочтительно менее 40% и еще более предпочтительно менее 30% по отношению к общему весу препарата.
39. Лекарственная форма пролонгированного действия по одному из пп.30-38, отличающаяся тем, что активное начало является пептидом, аналогом пептида или протеином, в частности, LHRH, или аналогом LHRH, в частности, трипторелином.
40. Лекарственная форма пролонгированного действия по одному из пп.30-39, отличающаяся тем, что она имеет цилиндрическую форму и диаметр меньше или равный 3 мм, предпочтительно меньше 1 мм.
41. Лекарственная форма пролонгированного действия по одному из пп.30-40 для введения подкожным путем.
42. Лекарственная форма пролонгированного действия по одному из пп.30-41, отличающаяся тем, что она выполнена в виде имплантата.
43. Лекарственная форма пролонгированного действия по одному из пп.30-42, отличающаяся тем, что ее применяют для получения медикамента, предназначенного для парентерального введения в сухом виде.
44. Лекарственная форма по одному из пп.30-42, отличающаяся тем, что она содержит низкую дозу активного начала по сравнению с обычной дозой рассматриваемого активного начала для лечения системным путем.
45. Лекарственная форма по одному из пп.30-42, отличающаяся тем, что она имеет тонкую и удлиненную форму, в частности, цилиндрическую.
46. Лекарственная форма по п.45, отличающаяся тем, что она имеет диаметр от 0,1 до 2-3 мм.
47. Лекарственная форма по одному из пп.45 и 46, отличающаяся тем, что ее форма имеет минимальное соотношение длина/диаметр 10.
48. Лекарственная форма по одному из пп.30-47, являющаяся твердой, которая может быть деформирована предварительным напряжением в доводочном устройстве удлиненной формы и восстанавливать первоначальную форму in situ.
49. Лекарственная форма по одному из пп.30-48, отличающаяся тем, что она выполнена таким образом, чтобы высвобождение активного начала происходило в анатомической полости, в которую указанная лекарственная форма вводится.
50. Лекарственная форма по п.49, отличающаяся тем, что она имеет заранее рассчитанную форму, адаптированную к анатомической полости организма таким образом, чтобы предотвратить ее смещение или уничтожение.
51. Лекарственная форма по п.50, отличающаяся тем, что она подвергается предварительному напряжению в указанных доводочных средствах и восстанавливает свою непрямолинейную форму после введения в заданную область.
52. Лекарственная форма по п.50, отличающаяся тем, что ее длина и диаметр рассчитаны таким образом, чтобы предупредить ее уничтожение или смещение.
53. Лекарственная форма по одному из пп.30-52, отличающаяся тем, что указанная лекарственная форма и содержащееся в ней активное начало выполнены таким образом, чтобы активное начало высвобождалось в секрет слизистой оболочки.
54. Лекарственная форма по одному из пп.49-53, отличающаяся тем, что указанная полость или слизистая оболочка являются полостью или слизистой оболочкой лицевой области или области ЛОР.
55. Лекарственная форма по п.53, отличающаяся тем, что указанная слизистая оболочка является трахеопульмональной слизистой оболочкой.
56. Лекарственная форма по п.53, отличающаяся тем, что указанная слизистая оболочка является слизистой оболочкой рта и пищевода.
57. Лекарственная форма по одному из пп.53-56, отличающаяся тем, что она выполнена таким образом, чтобы быть помещенной на поверхность указанной слизистой оболочки для того, чтобы активное начало распространялось со слизью.
58. Лекарственная форма по одному из пп.53-56, отличающаяся тем, что она выполнена таким образом, чтобы быть помещенной внутри слизистой оболочки.
59. Лекарственная форма по п.58, отличающаяся тем, что указанная лекарственная форма и содержащееся в ней активное начало предназначены для введения в субпальпебральную слизистую оболочку.
60. Лекарственная форма по одному из пп.49-59, отличающаяся тем, что она включает в себя кортикоид для лечения, в полости, стенке полости или слизистой оболочке, полипоза пазух носа, аллергических и неаллергических ринитов, неинфекционных отитов или синуситов путем введения в гайморову пазуху, клиновидную пазуху или лобную пазуху, в слизистую оболочку носа, решетчатые ячейки или барабанную полость.
61. Лекарственная форма по одному из пп.30-48, отличающаяся тем, что указанная лекарственная форма и содержащееся в ней активное начало предназначены для введения вокруг стенки сосуда путем интра- или транслуминального введения.
62. Лекарственная форма по п. 61, применяемая, в частности, после транслуминальной чрескожной ангиопластики, содержащая активное начало для профилактики или лечения рестеноза.
63. Лекарственная форма по п.62, содержащая только ангиопептин или ангиопептин в сочетании с другим активным началом, в частности, с гепарином.
64. Лекарственная форма по одному из пп.30-48, отличающаяся тем, что указанная лекарственная форма и содержащееся в ней активное начало предназначены для введения в/под опухолевую ткань для противоопухолевого действия.
65. Лекарственная форма по п. 64, в которой активное начало содержит фоточувствительное вещество.
66. Лекарственная форма по одному из пп.30-48, отличающаяся тем, что указанная лекарственная форма и содержащееся в ней активное начало выполнены для внутри- или околосуставного введения.
67. Лекарственная форма по одному из пп.30-66, отличающаяся тем, что она содержит противовоспалительное активное начало.
68. Лекарственная форма по одному из пп.30-67, отличающаяся тем, что она содержит активное начало пептидного или белкового происхождения.
69. Способ получения лекарственной формы пролонгированного действия по одному из пп.30-42, включающий в себя следующие стадии: приготовление гомогенной смеси активного начала и эксципиента с минимальным содержанием активного начала 50%, уплотнение указанной смеси, и экструзия указанной смеси в расплавленном состоянии.
70. Способ получения лекарственной формы пролонгированного действия по одному из пп.1-7 и 30-42, включающий в себя следующие стадии: приготовление гомогенной смеси активного начала и эксципиента с минимальным содержанием активного начала 50% сжатие гомогенной смеси при высоком давлении, раздробление полученных прессованных форм и придание формы для последующего введения.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR9614755A FR2756493B1 (fr) | 1996-12-02 | 1996-12-02 | Dispositif d'administration locale de formulations solides ou semi-solides |
| FR9614755 | 1996-12-02 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU99113827A RU99113827A (ru) | 2001-04-20 |
| RU2207845C2 true RU2207845C2 (ru) | 2003-07-10 |
Family
ID=9498235
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU99113827/14A RU2207845C2 (ru) | 1996-12-02 | 1997-12-02 | Твердая лекарственная форма пролонгированного действия для парентерального введения и способ ее получения |
Country Status (21)
| Country | Link |
|---|---|
| EP (2) | EP0952867B1 (ru) |
| JP (2) | JP2001506144A (ru) |
| KR (1) | KR100483447B1 (ru) |
| CN (2) | CN1210080C (ru) |
| AT (1) | ATE370764T1 (ru) |
| AU (1) | AU742061B2 (ru) |
| BR (1) | BR9713675A (ru) |
| CA (1) | CA2273017C (ru) |
| CZ (1) | CZ301103B6 (ru) |
| DE (1) | DE69738048T2 (ru) |
| DK (1) | DK0952867T3 (ru) |
| ES (1) | ES2290971T3 (ru) |
| FR (1) | FR2756493B1 (ru) |
| HU (1) | HU228236B1 (ru) |
| IL (1) | IL130211A (ru) |
| NO (1) | NO332358B1 (ru) |
| NZ (1) | NZ336074A (ru) |
| PL (1) | PL194894B1 (ru) |
| PT (1) | PT952867E (ru) |
| RU (1) | RU2207845C2 (ru) |
| WO (1) | WO1998024504A2 (ru) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8354095B2 (en) | 2004-12-10 | 2013-01-15 | Hallux, Inc. | Compositions and methods for treating conditions of the nail unit |
| US8591870B2 (en) | 2004-12-10 | 2013-11-26 | Hallux, Inc. | Compositions and methods for treating conditions of the nail unit |
| US8721622B2 (en) | 2004-05-05 | 2014-05-13 | Q-Med Ab | Use of a viscoelastic composition for treating increased intraocular pressure |
| US9375558B2 (en) | 2013-03-14 | 2016-06-28 | Hallux, Inc. | Method of treating infections, diseases or disorders of nail unit |
| RU2702740C2 (ru) * | 2015-06-10 | 2019-10-10 | Эвоник Рём ГмбХ | Способ получения порошка, содержащего белок, представляющий собой фактор свертывания крови человека, и полимер на основе молочной кислоты |
Families Citing this family (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2779340B1 (fr) | 1998-06-04 | 2000-12-29 | Delab | Dispositif intraluminal implantable |
| DE19961197B4 (de) * | 1999-12-18 | 2007-02-08 | Gaplast Gmbh | Implantatspritze |
| US6428559B1 (en) * | 2001-04-03 | 2002-08-06 | Cordis Corporation | Removable, variable-diameter vascular filter system |
| US7083607B2 (en) * | 2001-07-12 | 2006-08-01 | Bavarian Nordic A/S | Injection device and method for injecting capsules |
| GB0122113D0 (en) * | 2001-09-11 | 2001-10-31 | Astrazeneca Ab | Composition |
| NZ542459A (en) * | 2003-03-14 | 2008-12-24 | Debio Rech Pharma Sa | Subcutaneous delivery system, process for the preparation of the same and use of the same for the treatment of cholinergic deficient disorders |
| US7544192B2 (en) | 2003-03-14 | 2009-06-09 | Sinexus, Inc. | Sinus delivery of sustained release therapeutics |
| FR2865938B1 (fr) * | 2004-02-05 | 2006-06-02 | Sod Conseils Rech Applic | Formulation retard solide comprenant de l'acetate de triptoreline |
| AU2004100402B4 (en) * | 2004-05-28 | 2005-04-07 | Stephen Paul Holdings Pty Ltd | Integrated water supply system for multi-floor buildings |
| US7442187B2 (en) * | 2005-01-27 | 2008-10-28 | Boston Scientific Scimed, Inc. | Multiple needle injection catheter |
| CA2603081C (en) | 2005-04-04 | 2013-09-03 | Sinexus, Inc. | Device and methods for treating paranasal sinus conditions |
| US20070173706A1 (en) * | 2005-11-11 | 2007-07-26 | Isense Corporation | Method and apparatus for insertion of a sensor |
| US7887521B2 (en) | 2006-05-17 | 2011-02-15 | Alcon Research, Ltd. | Ophthalmic injection system |
| US7811252B2 (en) | 2006-05-17 | 2010-10-12 | Alcon Research, Ltd. | Dosage control device |
| US7815603B2 (en) | 2006-05-17 | 2010-10-19 | Alcon Research, Ltd. | Ophthalmic injection method |
| US8535707B2 (en) | 2006-07-10 | 2013-09-17 | Intersect Ent, Inc. | Devices and methods for delivering active agents to the osteomeatal complex |
| US20080281292A1 (en) | 2006-10-16 | 2008-11-13 | Hickingbotham Dyson W | Retractable Injection Port |
| US9022970B2 (en) | 2006-10-16 | 2015-05-05 | Alcon Research, Ltd. | Ophthalmic injection device including dosage control device |
| SE0701811L (sv) | 2007-08-02 | 2008-08-26 | Novoaim Ab | Kirurgiskt kit för fettransplantation |
| DK2200684T3 (en) | 2007-08-17 | 2016-12-12 | Medtronic Minimed Inc | Injection device for making an injection in a pre-determined depth in the skin |
| DK2231065T3 (da) | 2007-12-18 | 2021-02-01 | Intersect Ent Inc | Selvekspanderende anordninger |
| CA2732355A1 (en) | 2008-08-01 | 2010-02-04 | Intersect Ent, Inc. | Methods and devices for crimping self-expanding devices |
| WO2010107507A1 (en) * | 2009-03-20 | 2010-09-23 | Incube Labs, Llc | Solid drug delivery apparatus, formulations and methods of use |
| US20100239632A1 (en) * | 2009-03-23 | 2010-09-23 | Warsaw Orthopedic, Inc. | Drug depots for treatment of pain and inflammation in sinus and nasal cavities or cardiac tissue |
| WO2010123563A2 (en) * | 2009-04-23 | 2010-10-28 | Sustained Nano Systems Llc | Controlled release dispensing device |
| US8372036B2 (en) | 2009-05-06 | 2013-02-12 | Alcon Research, Ltd. | Multi-layer heat assembly for a drug delivery device |
| EP3103502A1 (en) | 2009-05-15 | 2016-12-14 | Intersect ENT, Inc. | Expandable devices and methods therefor |
| US20110092918A1 (en) * | 2009-10-19 | 2011-04-21 | Ferrosan A/S | Malleable tip for applying an agent to a target site |
| US8177747B2 (en) | 2009-12-22 | 2012-05-15 | Alcon Research, Ltd. | Method and apparatus for drug delivery |
| CN101884570A (zh) * | 2010-08-04 | 2010-11-17 | 苏州欧莱美生物工程科技有限公司 | 一种针头刺入引导装置 |
| JP5696279B2 (ja) * | 2010-12-01 | 2015-04-08 | 学校法人自治医科大学 | 長期徐放型薬剤硬膜外腔留置システム |
| DE102011116973A1 (de) | 2011-10-26 | 2013-05-02 | Amw Gmbh | Implanter |
| JP2013172803A (ja) * | 2012-02-24 | 2013-09-05 | Masanori Saeki | 製剤注入具 |
| EP3636227B1 (en) | 2013-03-14 | 2024-08-28 | Intersect ENT, Inc. | Systems and devices for treating a sinus condition |
| ITMI20131992A1 (it) | 2013-11-28 | 2015-05-29 | Valerio Cigaina | Assieme comprendente un dispositivo per elettroneuromodulazione totalmente impiantabile ed uno strumento di impiantazione di detto dispositivo |
| US10596330B2 (en) * | 2015-08-26 | 2020-03-24 | Medtronic Xomed, Inc. | Resorbable, drug-eluting submucosal turbinate implant device and method |
| JP7493796B2 (ja) | 2017-07-11 | 2024-06-03 | サステインドナノシステムズエルエルシー | 超圧縮医薬製剤 |
| AU2018300071B2 (en) | 2017-07-11 | 2024-09-19 | Sustained Nano Systems Llc | Radiation sterilization of hypercompressed polymer dosage forms |
| DE102017007893A1 (de) * | 2017-08-19 | 2019-02-21 | Gaplast Gmbh | Implantatspritze |
| CN108187216B (zh) * | 2017-12-29 | 2021-03-16 | 耿海涛 | 一种肿瘤部位给药装置 |
| IL276048B1 (en) | 2018-02-09 | 2024-07-01 | Icon Bioscience Inc | Systems, kits and methods for loading and transferring a small amount of dose from a syringe |
| WO2020021878A1 (ja) * | 2018-07-26 | 2020-01-30 | 株式会社カネカ | 生体内留置物およびその留置システム |
| EP3833631A4 (en) * | 2018-08-10 | 2022-04-20 | Azura Ophthalmics Ltd | DISPENSER FOR ACCURATE EXTRACTION OF A SEMI-SOLID PRODUCT |
| US11464914B2 (en) | 2019-10-21 | 2022-10-11 | Ripple Therapeutics Corporation | Intravitreal injector |
| JP2023510499A (ja) | 2020-01-10 | 2023-03-14 | アズーラ オフサルミックス エルティーディー. | 組成物および過敏症のための指示 |
| CN112156170B (zh) * | 2020-11-03 | 2022-10-21 | 北京康欣东弘医药科技有限公司 | 可供皮下注射的曲普瑞林缓释微球及其制备方法和用途 |
| AU2021396978A1 (en) | 2020-12-08 | 2023-02-23 | Ruminant Biotech Corp Limited | Improvements to devices and methods for delivery of substances to animals |
| CN112451850B (zh) * | 2020-12-11 | 2023-05-09 | 王姗姗 | 一种碘-125粒子用植入装置 |
| CN112472207B (zh) * | 2020-12-14 | 2021-11-05 | 中南大学湘雅医院 | 一种神经外科用临床介入治疗装置 |
| CN112970670B (zh) * | 2021-02-06 | 2022-08-05 | 澎立生物医药技术(上海)股份有限公司 | 一种肠粘膜炎动物模型的构建方法 |
| JP7562090B1 (ja) | 2023-10-19 | 2024-10-07 | 国立大学法人高知大学 | マーカー、マーカー留置具及びマーカー検出装置 |
| CN117771475B (zh) * | 2024-02-27 | 2024-05-10 | 山东永聚医药科技股份有限公司 | 固体制剂用植入式预灌封注射器及其制备方法 |
| CN117942456B (zh) * | 2024-03-27 | 2024-07-12 | 山东永聚医药科技股份有限公司 | 缓释型非牛顿流体制剂用预灌封注射器及其制备工艺 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE522404C (de) * | 1929-01-09 | 1931-04-08 | Hans E Hellwig | Instrument zur Einfuehrung von Radiumnadeln |
| US3545439A (en) | 1968-01-04 | 1970-12-08 | Upjohn Co | Medicated devices and methods |
| GB2091554B (en) * | 1981-01-13 | 1984-09-12 | Mitsui Toatsu Chemicals | Rod like moulded drug |
| WO1984000304A1 (en) * | 1982-07-08 | 1984-02-02 | Mitchell Harman | Injectible sustained release dosage cylinders |
| CA1196864A (en) * | 1983-06-10 | 1985-11-19 | Mattheus F.A. Goosen | Controlled release of injectable and implantable insulin compositions |
| AU571922B2 (en) * | 1984-01-26 | 1988-04-28 | Schering Agrochemicals Limited | Veterinary implants comprising melatonin and derivatives thereof |
| US4758435A (en) * | 1986-08-11 | 1988-07-19 | American Cyanamid Company | Estradiol implant composition and method for preparation |
| US4863736A (en) * | 1987-03-16 | 1989-09-05 | Monsanto Company | Somatotropin prolonged release |
| DK530787D0 (da) | 1987-10-09 | 1987-10-09 | Bukh Meditec | Indretning til indfoering i en legemshulhed |
| US5088935A (en) | 1991-04-05 | 1992-02-18 | Penn Engineering & Manufacturing Corp. | Electrical connector panel |
| US5219358A (en) * | 1991-08-29 | 1993-06-15 | Ethicon, Inc. | Shape memory effect surgical needles |
| EP0596161B1 (en) * | 1992-11-06 | 1998-02-04 | Texas Instruments Incorporated | Apparatus for subcutaneous introduction of a needle |
| DK42093D0 (da) * | 1993-04-07 | 1993-04-07 | Bukh Meditec | Administrationsmetode |
| JP3495045B2 (ja) * | 1994-04-27 | 2004-02-09 | 大研医器株式会社 | 液体注入装置 |
| US5573542A (en) * | 1994-08-17 | 1996-11-12 | Tahoe Surgical Instruments-Puerto Rico | Endoscopic suture placement tool |
| US5582591A (en) | 1994-09-02 | 1996-12-10 | Delab | Delivery of solid drug compositions |
| US5542920A (en) * | 1994-09-12 | 1996-08-06 | Delab | Needle-less parenteral introduction device |
-
1996
- 1996-12-02 FR FR9614755A patent/FR2756493B1/fr not_active Expired - Fee Related
-
1997
- 1997-12-02 ES ES97948983T patent/ES2290971T3/es not_active Expired - Lifetime
- 1997-12-02 CN CNB971813035A patent/CN1210080C/zh not_active Expired - Fee Related
- 1997-12-02 HU HU9904601A patent/HU228236B1/hu not_active IP Right Cessation
- 1997-12-02 DE DE69738048T patent/DE69738048T2/de not_active Expired - Lifetime
- 1997-12-02 AT AT97948983T patent/ATE370764T1/de active
- 1997-12-02 NZ NZ336074A patent/NZ336074A/en not_active IP Right Cessation
- 1997-12-02 AU AU76232/98A patent/AU742061B2/en not_active Ceased
- 1997-12-02 CZ CZ0191999A patent/CZ301103B6/cs not_active IP Right Cessation
- 1997-12-02 DK DK97948983T patent/DK0952867T3/da active
- 1997-12-02 JP JP52527798A patent/JP2001506144A/ja active Pending
- 1997-12-02 PL PL360774A patent/PL194894B1/pl unknown
- 1997-12-02 KR KR10-1999-7004879A patent/KR100483447B1/ko not_active IP Right Cessation
- 1997-12-02 EP EP97948983A patent/EP0952867B1/fr not_active Expired - Lifetime
- 1997-12-02 RU RU99113827/14A patent/RU2207845C2/ru not_active IP Right Cessation
- 1997-12-02 PT PT97948983T patent/PT952867E/pt unknown
- 1997-12-02 CA CA002273017A patent/CA2273017C/fr not_active Expired - Fee Related
- 1997-12-02 IL IL130211A patent/IL130211A/en not_active IP Right Cessation
- 1997-12-02 CN CNA200510074284XA patent/CN1698580A/zh active Pending
- 1997-12-02 WO PCT/FR1997/002182 patent/WO1998024504A2/fr active IP Right Grant
- 1997-12-02 BR BR9713675-1A patent/BR9713675A/pt not_active IP Right Cessation
- 1997-12-02 EP EP01118964A patent/EP1159957A3/fr not_active Withdrawn
-
1999
- 1999-05-31 NO NO19992610A patent/NO332358B1/no not_active IP Right Cessation
-
2008
- 2008-10-15 JP JP2008266758A patent/JP5138537B2/ja not_active Expired - Fee Related
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8721622B2 (en) | 2004-05-05 | 2014-05-13 | Q-Med Ab | Use of a viscoelastic composition for treating increased intraocular pressure |
| US8354095B2 (en) | 2004-12-10 | 2013-01-15 | Hallux, Inc. | Compositions and methods for treating conditions of the nail unit |
| US8591870B2 (en) | 2004-12-10 | 2013-11-26 | Hallux, Inc. | Compositions and methods for treating conditions of the nail unit |
| US8747820B2 (en) | 2004-12-10 | 2014-06-10 | Hallux, Inc. | Methods for treating conditions of the nail unit |
| US9446009B2 (en) | 2004-12-10 | 2016-09-20 | Hallux, Inc. | Methods for treating conditions of the nail unit |
| US9375558B2 (en) | 2013-03-14 | 2016-06-28 | Hallux, Inc. | Method of treating infections, diseases or disorders of nail unit |
| US9498612B2 (en) | 2013-03-14 | 2016-11-22 | Hallux, Inc. | Method of treating infections, diseases or disorders of nail unit |
| US10456568B2 (en) | 2013-03-14 | 2019-10-29 | Hallux, Inc. | Method of treating infections, diseases or disorders of nail unit |
| RU2702740C2 (ru) * | 2015-06-10 | 2019-10-10 | Эвоник Рём ГмбХ | Способ получения порошка, содержащего белок, представляющий собой фактор свертывания крови человека, и полимер на основе молочной кислоты |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2207845C2 (ru) | Твердая лекарственная форма пролонгированного действия для парентерального введения и способ ее получения | |
| US7815928B2 (en) | Device for local administration of solid or semi-solid formulations and delayed-release formulations for proposal parenteral administration and preparation process | |
| US10814115B2 (en) | Microneedle devices and uses thereof | |
| US20090270308A1 (en) | Controlled release implantable dispensing device and method | |
| US9867910B2 (en) | Clonidine compounds in a biodegradable fiber | |
| Langer | Controlling the movement of molecules | |
| JP2011513337A (ja) | 椎間板ヘルニアを治療するための方法および組成物 | |
| CA2759807C (en) | Controlled release dispensing device | |
| AU2004240186B2 (en) | Device for local administration of solid or semi-solid formulations and delayed-release formulations for parenteral administration and preparation process | |
| AU779691B2 (en) | Device for local administration of solid and semisolid formulations, delayed-release formulations for parenteral administration and method of preparation | |
| US20100173000A1 (en) | Controlled release implantable dispensing device and method | |
| MXPA99005030A (en) | Device for local administration of solid and semisolid formulations, sustained-release formulations for parenteral administration and method of preparation | |
| US20200397873A1 (en) | Compositions, systems, and methods for scar tissue modification | |
| FR2770134A1 (fr) | Formulations solides ou semi-solides pour administration locale |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20131203 |