RU2158268C2 - Секомакролиды класса эритромицинов и способ их получения - Google Patents
Секомакролиды класса эритромицинов и способ их получения Download PDFInfo
- Publication number
- RU2158268C2 RU2158268C2 RU98104446/04A RU98104446A RU2158268C2 RU 2158268 C2 RU2158268 C2 RU 2158268C2 RU 98104446/04 A RU98104446/04 A RU 98104446/04A RU 98104446 A RU98104446 A RU 98104446A RU 2158268 C2 RU2158268 C2 RU 2158268C2
- Authority
- RU
- Russia
- Prior art keywords
- group
- hydrogen
- formula
- represent
- cladinosyl
- Prior art date
Links
- 0 CC(C)C(*)C(C)*(CNC(C)C(C(C)(C(C)*)O)O*)=O Chemical compound CC(C)C(*)C(C)*(CNC(C)C(C(C)(C(C)*)O)O*)=O 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H15/00—Compounds containing hydrocarbon or substituted hydrocarbon radicals directly attached to hetero atoms of saccharide radicals
- C07H15/02—Acyclic radicals, not substituted by cyclic structures
- C07H15/04—Acyclic radicals, not substituted by cyclic structures attached to an oxygen atom of the saccharide radical
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H15/00—Compounds containing hydrocarbon or substituted hydrocarbon radicals directly attached to hetero atoms of saccharide radicals
- C07H15/26—Acyclic or carbocyclic radicals, substituted by hetero rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Crystallography & Structural Chemistry (AREA)
- Saccharide Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
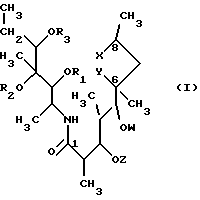
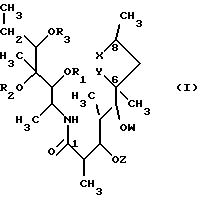
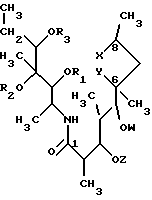
Описываются новые соединения - секомакролиды класса эритромицинов А общей формулы I, где значения R1, R2, R3, Z, W, Х, У указаны в п.1 формулы изобретения. Они являются потенциальными промежуточными соединениями для получения новых антибиотиков - макролидов. Описывается также способ их получения. 2 с. и 19 з.п. ф-лы.
Description
Область техники, к которой относится изобретение
A 61 K 31/70, C 07 H 17/08
Техническая проблема
Настоящее изобретение относится к новым соединениям класса хорошо известного антибиотика-макролида эритромицина A. В частности, настоящее изобретение относится к новым секомакролидам - потенциальным промежуточным соединениям для получения новых макролидов с антибактериальным действием, а также к способу их получения.
A 61 K 31/70, C 07 H 17/08
Техническая проблема
Настоящее изобретение относится к новым соединениям класса хорошо известного антибиотика-макролида эритромицина A. В частности, настоящее изобретение относится к новым секомакролидам - потенциальным промежуточным соединениям для получения новых макролидов с антибактериальным действием, а также к способу их получения.
Известный уровень техники
Эритромицин является антибиотиком-макролидом, чье строение характеризуется 14-членным лактоновым кольцом с кето-группой в C-9 положении и двумя сахарами - L-кладинозой и D-дезозамином, присоединенными посредством гликозидных связей в положениях C-3 и C-5 агликоновой группы молекулы (McGuire, Antibiot. Chemother. , 1952; 2:281). Свыше 40 лет он считался безопасным и эффективным противомикробным средством при лечении респираторных инфекций и инфекций половых органов, вызываемых грамположительными бактериями, некоторыми видами Legionella, Mycoplasma, Chlamidia и Helicobacter. Значительные изменения в биологической доступности после введения пероральных препаратов, желудочная непереносимость у многих пациентов и потеря активности в кислой среде из-за образования неактивного метаболита ангидроэритромицина являются основными недостатками при терапевтическом применении эритромицина A. Однако спироциклизация агликонового кольца успешно ингибируется путем химической трансформации C-9-кетона или гидроксильных групп в положении C-6 и/или C-12. Так например, оксимированием C-9-кетона эритромицина A гидрохлоридом гидроксиламина, перегруппировкой Бекмана полученного 9(E)-оксима и восстановлением полученного простого 6,9-иминоэфира (6,9-циклического иминоэфира 6-дезокси-9-дезоксо-9а-азагомоэритромицина) получен 9-дезоксо-9а-аза-9а-гомоэритромицин A - первый полусинтетический макролид с 15-членным азалактоновым кольцом (Kobrehel G. et al, патент США 4328334, 5/1982). В соответствии со способом Эшвайлера-Кларка, посредством восстановительного метилирования вновь введенной эндоциклической 9а-аминогруппы, синтезирован 9-дезоксо-9а-метил-9а-аза-9а-гомоэритромицин A (AZITHROMYCIN) прототип нового класса антибиотиков-азалидов (Kobrehel G. et al., патент Бельгии 892357, 7/1982). Кроме широкого противомикробного спектра действия, включающего также грамотрицательные бактерии, азитромицин характеризуется также длительным биологическим полупериодом существования, специфическим механизмом переноса к месту использования и коротким сроком лечения. Азитромицин легко проникает в фагоциты человека и накапливается в них, в результате чего улучшается активность в отношении внутриклеточных патогенных микроорганизмов классов Leqionella, Chlamidia и Helicobacter.
Эритромицин является антибиотиком-макролидом, чье строение характеризуется 14-членным лактоновым кольцом с кето-группой в C-9 положении и двумя сахарами - L-кладинозой и D-дезозамином, присоединенными посредством гликозидных связей в положениях C-3 и C-5 агликоновой группы молекулы (McGuire, Antibiot. Chemother. , 1952; 2:281). Свыше 40 лет он считался безопасным и эффективным противомикробным средством при лечении респираторных инфекций и инфекций половых органов, вызываемых грамположительными бактериями, некоторыми видами Legionella, Mycoplasma, Chlamidia и Helicobacter. Значительные изменения в биологической доступности после введения пероральных препаратов, желудочная непереносимость у многих пациентов и потеря активности в кислой среде из-за образования неактивного метаболита ангидроэритромицина являются основными недостатками при терапевтическом применении эритромицина A. Однако спироциклизация агликонового кольца успешно ингибируется путем химической трансформации C-9-кетона или гидроксильных групп в положении C-6 и/или C-12. Так например, оксимированием C-9-кетона эритромицина A гидрохлоридом гидроксиламина, перегруппировкой Бекмана полученного 9(E)-оксима и восстановлением полученного простого 6,9-иминоэфира (6,9-циклического иминоэфира 6-дезокси-9-дезоксо-9а-азагомоэритромицина) получен 9-дезоксо-9а-аза-9а-гомоэритромицин A - первый полусинтетический макролид с 15-членным азалактоновым кольцом (Kobrehel G. et al, патент США 4328334, 5/1982). В соответствии со способом Эшвайлера-Кларка, посредством восстановительного метилирования вновь введенной эндоциклической 9а-аминогруппы, синтезирован 9-дезоксо-9а-метил-9а-аза-9а-гомоэритромицин A (AZITHROMYCIN) прототип нового класса антибиотиков-азалидов (Kobrehel G. et al., патент Бельгии 892357, 7/1982). Кроме широкого противомикробного спектра действия, включающего также грамотрицательные бактерии, азитромицин характеризуется также длительным биологическим полупериодом существования, специфическим механизмом переноса к месту использования и коротким сроком лечения. Азитромицин легко проникает в фагоциты человека и накапливается в них, в результате чего улучшается активность в отношении внутриклеточных патогенных микроорганизмов классов Leqionella, Chlamidia и Helicobacter.
Недавно описан гидролиз и алкоголиз C-1-лактона эритромицина A и B, посредством чего образуются соответствующие линейные секокислоты и сложные эфиры (Martin S., J.Am.Chem. Soc., 1991; 113: 5478). Кроме того, описано также катализированное щелочью превращение эритромицина A, ведущее к раскрытию макроциклического кольца с образованием C-1-карбоксилата (Waddel S.T. and Blizzard T.A., PCT, WO 94/15617, 7/1994). Также описан способ получения новых макролидных и азолидных колец путем сочетания истерн ("восточных")-C-1/C-8-и C-1/C-9-групп молекул 9-дезоксо-8а-аза-8а-гомоэритромицина A и 9-дезоксо-9а-аза-9а-гомоэритромицина A, соответственно, с различными фрагментами, которые становятся вестерн ("западной")-группой молекулы. Подчеркнуто, что линейные фрагменты C-1/C-9, полученные таким образом, отличаются от соответствующего фрагмента азитромицина наличием дополнительной этильной группы у атома углерода C-9. В EP 0735041 Al (Lazarevski G. et al., 2/1996) описан синтез новых секоазалидов посредством воздействия гидрохлорида гидроксиламина на простой 6,9-циклический иминоэфир и последующего катализированного щелочью внутримолекулярного ацилирования вновь образованной C-10-аминогруппы и C-1-лактона. Строение полученных таким образом C-1-амидов характеризуется истерн-фрагментом C-1/C-9, который идентичен фрагменту в азатромицине и ветерн-фрагменту C-10/C-15 эритромицина A, обратимо связанному с атомом углерода C-1. Однако при действии кислот на 6,9-циклический иминоэфир при расщеплении двойной связи C-9/9-а-N образуется 6-дезокси-6,9-эпокси-8(R)-метил-10-амино-9,10-секоэритромицин A с концевой C-10-группой. Объектом настоящего изобретения является синтез новых секомакролидов - потенциальных промежуточных соединений в синтезе биологически активных химерных макролидов, исходя из 6-дезокси-6,9-эпокси-8(R)-метил-10-амино-9,10-секоэритромицина A.
Краткое изложение сущности изобретения
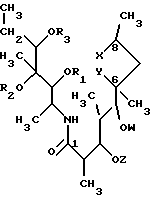
Согласно известному и установленному уровню техники до сих пор не описаны секомакролиды общей формулы (I)
где R1 представляет водород, (C1-C4)-алканоильную группу, арилкарбонильную группу или вместе с R2 и атомами углерода, с которыми они связаны, циклическую карбонильную или тиокарбонильную группу;
R2 представляет водород или вместе с R1 и атомами углерода, с которыми они связаны, циклическую карбонильную или тиокарбонильную группу;
R3 представляет водород, (C1-C4)-алканоильную или арилкарбонильную группу;
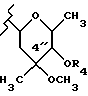
Z представляет водород или L-кладинозильную группу формулы (i).
Согласно известному и установленному уровню техники до сих пор не описаны секомакролиды общей формулы (I)
где R1 представляет водород, (C1-C4)-алканоильную группу, арилкарбонильную группу или вместе с R2 и атомами углерода, с которыми они связаны, циклическую карбонильную или тиокарбонильную группу;
R2 представляет водород или вместе с R1 и атомами углерода, с которыми они связаны, циклическую карбонильную или тиокарбонильную группу;
R3 представляет водород, (C1-C4)-алканоильную или арилкарбонильную группу;
Z представляет водород или L-кладинозильную группу формулы (i).
где R4 представляет водород или (C1-C4)-алканоильную группу;
W представляет водород или D-дезозаминильную группу формулы (ii)
где R5 представляет водород или (C1-C4)-алканоильную или арилкарбонильную группу;
X и Y вместе представляют лактон или X представляет группу CH2OR6, где R6 представляет водород или (C1-C4)-алканоильную группу, a Y представляет гидроксильную группу.
Настоящее изобретение также относится к их фармацевтически приемлемым солям присоединения неорганических или органических кислот.
Подробное описание изобретения
Новые секомакролиды общей формулы (I)
где X, Y, Z и W имеют установленные выше значения, и их фармацевтически приемлемые соли присоединения неорганических или органических кислот получают, подвергая 6-дезокси-6,9-эпокси-8(R)-метил-10-амино-9,10-секоэритромицин A (EP 0735041 A1, 2/1996) формулы (II)
взаимодействию с полярными растворителями в течение времени, необходимого для того, чтобы путем внутримолекулярного ацилирования первичной C-10-аминогруппы и C-1-лактона, образовалось соединение общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X и Y вместе представляют лактон [соединение (Ia)], которое далее подвергают
А) взаимодействию с кислотами в условиях гидролиза одного или обоих сахаров, получая соединение общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z является водородом, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X и Y вместе представляют лактон [соединение (Ib)], и соединение общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z и W являются одинаковыми и представляют водород, и X и Y вместе представляют лактон [соединение (Ic)], или
Б) О-ацилированию с ангидридами или хлорангидридами карбоновых кислот, получая
Б1) при О-ацилировании с ангидридами или хлорангидридами (C1-C4)-алкилкарбоновых кислот соединение общей формулы (I), где R1 и R3 являются одинаковыми и представляют (C1-C4)-алканоильные группы и R2 представляет водород, Z является L-кладинозильной группой формулы (i), где R4 представляет (C1-C4)-алканоильную группу, W является D-дезозаминильной группой формулы (ii), где R5 представляет (C1-C4)-алканоильную группу, и X и Y вместе представляют лактон, которое затем, если требуется, подвергают реакции сольволиза, получая соединение общей формулы (I), где R1 и R3 являются одинаковыми и представляют (C1-C4)-алканоильные группы и R2 представляет водород, Z является L-кладинозильной группой формулы (i), где R4 представляет (C1-C4)-алканоильную группу, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X и Y вместе представляют лактон, или получая
Б2) при О-ацилировании с хлорангидридами арилкарбоновых кислот, когда
Б2а) используют по меньшей мере 1,1 эквимолярный избыток хлорангидрида кислоты, соединение общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, W является D-дезозаминильной группой формулы (ii), где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, которое, если требуется, подвергают О-ацилированию в соответствии с Б1), получая соединение общей формулы (I), где R1 и R3 являются одинаковыми и представляют (C1-C4)-алканоильные группы и R2 представляет водород, Z является L-кладинозильной группой формулы (i), где R4 представляет (C1-C4)-алканоильную группу, W является D-дезозаминильной группой формулы (ii), где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, или
Б2б) используя по меньшей мере 5-эквимолярный избыток хлорангидрида кислоты, смесь соединений общей формулы (I), где R1 представляет арилкарбонильную группу, a R2 и R3 являются одинаковыми и представляют водород, или где R3 представляет арилкарбонильную группу, а R1 и R2 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, a W является D-дезозаминильной группой формулы (ii), где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, и эти соединения разделяют с помощью колоночной хроматографии на силикагеле, а затем, если требуется, подвергают реакции сольволиза, получая соединение общей формулы (I), где R1 представляет арилкарбонильную группу, a R2 и R3 являются одинаковыми и представляют водород, или где R3 представляет арилкарбонильную группу, а R1 и R2 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X и Y вместе представляют лактон,
или
B) реакции переэтерификации с производными карбоновых кислот, получая соединение общей формулы (I), где R1 и R2 вместе с атомами углерода, с которыми они связаны, представляют циклическую карбонильную или тиокарбонильную группу, а R3 представляет водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X и Y вместе представляют лактон,
или
Г) восстановлению, получая соединение общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X представляет группу CH2OR6, где R6 представляет водород, а Y представляет гидроксильную группу, которое, необязательно, подвергают О-ацилированию в соответствии с Б1), получая соединение общей формулы (I), где R1 и R3 являются одинаковыми и представляют (C1-C4)-алканоильные группы, R2 представляет водород, Z является L-кладинозильной группой формулы (i), где R4 представляет (C1-C4)-алканоильную группу, W является D-дезозаминильной группой формулы (ii), где R5 представляет (C1-C4)-алканоильную группу, X представляет группу CH2OR6, где R6 представляет водород, а Y представляет гидроксильную группу.
Новые секомакролиды общей формулы (I)
где X, Y, Z и W имеют установленные выше значения, и их фармацевтически приемлемые соли присоединения неорганических или органических кислот получают, подвергая 6-дезокси-6,9-эпокси-8(R)-метил-10-амино-9,10-секоэритромицин A (EP 0735041 A1, 2/1996) формулы (II)
взаимодействию с полярными растворителями в течение времени, необходимого для того, чтобы путем внутримолекулярного ацилирования первичной C-10-аминогруппы и C-1-лактона, образовалось соединение общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X и Y вместе представляют лактон [соединение (Ia)], которое далее подвергают
А) взаимодействию с кислотами в условиях гидролиза одного или обоих сахаров, получая соединение общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z является водородом, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X и Y вместе представляют лактон [соединение (Ib)], и соединение общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z и W являются одинаковыми и представляют водород, и X и Y вместе представляют лактон [соединение (Ic)], или
Б) О-ацилированию с ангидридами или хлорангидридами карбоновых кислот, получая
Б1) при О-ацилировании с ангидридами или хлорангидридами (C1-C4)-алкилкарбоновых кислот соединение общей формулы (I), где R1 и R3 являются одинаковыми и представляют (C1-C4)-алканоильные группы и R2 представляет водород, Z является L-кладинозильной группой формулы (i), где R4 представляет (C1-C4)-алканоильную группу, W является D-дезозаминильной группой формулы (ii), где R5 представляет (C1-C4)-алканоильную группу, и X и Y вместе представляют лактон, которое затем, если требуется, подвергают реакции сольволиза, получая соединение общей формулы (I), где R1 и R3 являются одинаковыми и представляют (C1-C4)-алканоильные группы и R2 представляет водород, Z является L-кладинозильной группой формулы (i), где R4 представляет (C1-C4)-алканоильную группу, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X и Y вместе представляют лактон, или получая
Б2) при О-ацилировании с хлорангидридами арилкарбоновых кислот, когда
Б2а) используют по меньшей мере 1,1 эквимолярный избыток хлорангидрида кислоты, соединение общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, W является D-дезозаминильной группой формулы (ii), где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, которое, если требуется, подвергают О-ацилированию в соответствии с Б1), получая соединение общей формулы (I), где R1 и R3 являются одинаковыми и представляют (C1-C4)-алканоильные группы и R2 представляет водород, Z является L-кладинозильной группой формулы (i), где R4 представляет (C1-C4)-алканоильную группу, W является D-дезозаминильной группой формулы (ii), где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, или
Б2б) используя по меньшей мере 5-эквимолярный избыток хлорангидрида кислоты, смесь соединений общей формулы (I), где R1 представляет арилкарбонильную группу, a R2 и R3 являются одинаковыми и представляют водород, или где R3 представляет арилкарбонильную группу, а R1 и R2 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, a W является D-дезозаминильной группой формулы (ii), где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, и эти соединения разделяют с помощью колоночной хроматографии на силикагеле, а затем, если требуется, подвергают реакции сольволиза, получая соединение общей формулы (I), где R1 представляет арилкарбонильную группу, a R2 и R3 являются одинаковыми и представляют водород, или где R3 представляет арилкарбонильную группу, а R1 и R2 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X и Y вместе представляют лактон,
или
B) реакции переэтерификации с производными карбоновых кислот, получая соединение общей формулы (I), где R1 и R2 вместе с атомами углерода, с которыми они связаны, представляют циклическую карбонильную или тиокарбонильную группу, а R3 представляет водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X и Y вместе представляют лактон,
или
Г) восстановлению, получая соединение общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы (i), где R4 представляет водород, W является D-дезозаминильной группой формулы (ii), где R5 представляет водород, и X представляет группу CH2OR6, где R6 представляет водород, а Y представляет гидроксильную группу, которое, необязательно, подвергают О-ацилированию в соответствии с Б1), получая соединение общей формулы (I), где R1 и R3 являются одинаковыми и представляют (C1-C4)-алканоильные группы, R2 представляет водород, Z является L-кладинозильной группой формулы (i), где R4 представляет (C1-C4)-алканоильную группу, W является D-дезозаминильной группой формулы (ii), где R5 представляет (C1-C4)-алканоильную группу, X представляет группу CH2OR6, где R6 представляет водород, а Y представляет гидроксильную группу.
Внутримолекулярное ацилирование C-10-аминогруппы с C-1-лактоном соединения (II) проводят в воде или в смеси воды и органического растворителя, предпочтительно низших спиртов или ацетона, при комнатной температуре или при повышенной температуре для ускорения переацилирования по известному способу (March J., Advanced Organic Chemistry: Reactions, Mechanisms and Structure; Third Ed., 1985, p. 375).
Гидролиз соединений (Ia) в соответствии с A) проводят хорошо известным способом в две стадии. На первой стадии взаимодействием с разбавленными неорганическими кислотами, предпочтительно с 0,25 N хлористоводородной кислотой при комнатной температуре проводят расщепление нейтрального сахара L-кладинозы, в результате чего образуется 5-O-дезозаминильное производное (Ib), которое затем, если требуется, подвергают действию более концентрированных кислот, предпочтительно 2-6 N хлористоводородной кислоты, в присутствии инертного органического растворителя, предпочтительно хлороформа, при повышенной температуре, предпочтительно при кипячении реакционной смеси с обратным холодильником, посредством чего, после отщепления второго сахара D-дезозамина, получают соединение (Ic).
Реакцию О-ацилирования соединения (Ia) в соответствии с Б1) проводят с ангидридами или хлорангидридами (C1-C4)-карбоновых кислот хорошо известным способом в инертном для реакции растворителе при температуре от 0 до 30oC в присутствии подходящих оснований (Jones et al., J.Med.Chem., 1971, 15, 631, и Banaszek et ai., Rocy.Chem., 1969, 43, 763). В качестве инертного растворителя можно использовать метиленхлорид, дихлорэтан, ацетон, пиридин, этилацетат, тетрагидрофуран и другие подобные растворители. В качестве подходящих оснований используют гидрокарбонат натрия, карбонат натрия, карбонат калия, триэтиламин, пиридин, трибутиламин и некоторые другие неогранические и органические основания. Так например, ацилированием (Ia) с ангидридом уксусной кислоты в пиридине при комнатной температуре в течение 3 суток получают тетраацетат (Id) (R1 = R3 = R4 = R5 = ацетил, R2 является водородом, X и Y вместе представляют лактон). Сольволиз полученных тетраацильных производных проводят в низших спиртах при комнатной температуре или при повышенной температуре для ускорения реакции, в результате чего проходит деацилирование в положение 2'. В этом случае в качестве низшего спирта можно использовать метанол, этанол, пропанол или бутанол. Например, когда тетраацетат (Id) оставляют стоять в метаноле при комнатной температуре в течение 3 суток, образуется триацетат (Ie) (R1 = R3 = R4 = ацетил, R2 = R5 = водород, X и Y вместе представляют лактон). О-Ацилирование соединения (Ia) с хлорангидридами арилкарбоновых кислот в соответствии с Б2), где термин "арил" означает незамещенную или замещенную фенильную группу, предпочтительно - (C1-C4)-алкилфенильную или галоидфенильную группу, проводят, предпочтительно, в инертных растворителях, предпочтительно - в ацетоне, в присутствии неорганических или органических оснований, предпочтительно гидрокарбоната натрия, в результате чего, в зависимости от эквимолярного соотношения реагентов, температуры реакции и времени ацилирования, образуются соответствующие моно- или диарилкарбонильные производные. Так например, ацилированием (Ia), по меньшей мере, с 1,1 эквимолярным избытком 4-бромбензоилхлорида в сухом ацетоне при 0-5oC получают 2'-моно-бромбензоат (If) (R1 = R2 = R3 = R4 = H, R5 = 4-бромбензоил и X и Y вместе представляют лактон). Полученные 2'-моноарилкарбонильные производные, если требуется, О-ацилируют по способу Б1). Так например, при взаимодействии с ангидридом уксусной кислоты по описанному выше способу получают триацетат (Ig) (R1 = R3 = R4 = ацетил, R2 = R5 = 4-бромбензоил и X и Y вместе представляют лактон). В случае дизамещенных производных одновременно с ацилированием 2'- гидроксильной группы происходит ацилирование гидроксильных групп в положении 1-N-[2- или 1N-[4-соединения (Ia). Посредством О-ацилирования, по меньшей мере, с 5 эквивалентами хлорангидрида арилкарбоновых кислот, предпочтительно с 4-бромбензиолхлоридом, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, образуется смесь дибромбензоата (lh) (R1 = R5 = 4-бромбензоил, R2 = R3 = R4 = H, X и Y вместе представляют лактон) и (Ii) (R3 = R5 = 4-бромбензоил, R1 = R2 = R4 = H, X и Y вместе представляют лактон), которую разделяют с помощью хроматографии на колонке с силикагелем, используя, предпочтительно, систему растворителей CH2Cl2/CH3OH, 95:5, и затем, если требуется, подвергают сольволизу по описанному выше способу, в результате чего, при деацилировании сложных 2'-эфиров, предпочтительно 2'-O-(4-бромбензоата), образуются монобромбензоат (Ik) (R1 = 4-бромбензоил, R2 = R3 = R4 = R5 = H, X и Y вместе представляют лактон) и (Ij) (R3 = 4-бромбензоил, R1 = R2 = R4 = R5 = H, X и Y вместе представляют лактон).
Переэтерификацию соединения (Ia) по B) проводят с производными карбоновых кислот, предпочтительно с 3-5 эквимолярным избытком этиленкарбоната или 1,1-тиокарбонилдиимидазола по отношению к исходному соединению (Ia), в подходящем растворителе, предпочтительно в ароматических растворителях, например в бензоле, хлорсодержащих углеводородах или низших алкилалканоатах, например в этилацетате, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, в течение 3-9 часов, получая циклический карбонат или тиокарбонат (R1 и R2 вместе представляют группы C = O или C = S, R3 = R4 = R5 = H, X и Y вместе представляют лактон).
Восстановление соединения (Ia) по Г) проводят с металлогидридными комплексами, предпочтительно с борогидридом натрия, в присутствии третичных спиртов, предпочтительно трет-бутанола, в инертном растворителе, предпочтительно в низших спиртах, предпочтительно в метаноле, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, получая смесь изомерных 9-гидрокси-8(R)- (Im) и 9-гидрокси-8(S)-производного (In) (R1 = R2 = R3 = R4 = R5 = H, X представляет группу CH2OR6, где R6 является водородом, и Y представляет гидроксильную группу), которые, если требуется, разделяют посредством колоночной хроматографии на силикагеле и затем, если требуется, подвергают O-ацилированию в соответствии с Б1).
Фармацевтически приемлемые соли присоединения, которые также являются объектом настоящего изобретения, получают взаимодействием секопроизводных общей формулы (I), по меньшей мере, с эквимолярным количеством подходящей неорганической или органической кислоты, такой как хлористоводородная, иодистоводородная, серная, фосфорная, уксусная, пропионовая, трифторуксусная, малеиновая, лимонная, стеариновая, янтарная, этилянтарная, метансульфоновая, бензолсульфоновая, п-толуолсульфоновая, лаурилсульфоновая кислота и подобные кислоты, в инертном для реакции растворителе. Соли присоединения кислот выделяют фильтрованием, если они нерастворимы в инертном для реакции растворителе, осаждением с помощью растворителя, в котором соли нерастворимы, или выпариванием растворителя, наиболее часто лиофилизацией.
С помощью приведенной серии реакций 6-дезокси-6,9-эпокси-8(R)-метил-10-амино-9,10-секоэритромицина A формулы (II) получают ряд новых, до настоящего времени не описанных, линейных производных с весьма реакционноспособными концевыми функциональными группами, что открывает возможность получения целого ряда новых макролидов с модифицированным макроциклическим агликоном. Для простоты, нумерация атомов водорода и углерода в данных спектрометрии новых секомакролидов в экспериментальной части данной заявки на патент является такой же, как для атомов до инверсии фрагмента C-10/C-15.
Настоящее изобретение иллюстрируется приведенными далее примерами, которые никоим образом не ограничивают его объем.
ПРИМEP 1. 1-N-(2,3,4-тригидрокси-1,3-димегилгексил)-амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпокси-9,10-секоэритромицина A (Iа)
Способ 1
6-Дезокси-6,9-эпокси-8(R)-метил-10-амино-9,10-секоэритромицин A (EP 0735041 A1, 02.10.1996) (15 г, 0,02 моль) растворяют в 540 мл смеси ацетона с водой (1:5) и нагревают при перемешивании в течение 2 часов при температуре 55-60oC. Реакционную смесь упаривают при пониженном давлении, добавляют к водному остатку CHCl3 (100 мл) (pH 7,45) и затем, после подщелачивания до pH 9,0 (10% NaOH), слои разделяют и водный слой экстрагируют два раза CHCl3 (100 мл). Объединенные органические экстракты сушат над K2CO3 и упаривают и получают твердый остаток (12,9 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CHCl3/CH3OH/конц.NH4OH, 6: 1: 0,1 из сырого продукта (2,5 г) получают хроматографически однородное вещество (Ia) (1,48 г) с приведенными ниже физико-химическими константами.
Способ 1
6-Дезокси-6,9-эпокси-8(R)-метил-10-амино-9,10-секоэритромицин A (EP 0735041 A1, 02.10.1996) (15 г, 0,02 моль) растворяют в 540 мл смеси ацетона с водой (1:5) и нагревают при перемешивании в течение 2 часов при температуре 55-60oC. Реакционную смесь упаривают при пониженном давлении, добавляют к водному остатку CHCl3 (100 мл) (pH 7,45) и затем, после подщелачивания до pH 9,0 (10% NaOH), слои разделяют и водный слой экстрагируют два раза CHCl3 (100 мл). Объединенные органические экстракты сушат над K2CO3 и упаривают и получают твердый остаток (12,9 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CHCl3/CH3OH/конц.NH4OH, 6: 1: 0,1 из сырого продукта (2,5 г) получают хроматографически однородное вещество (Ia) (1,48 г) с приведенными ниже физико-химическими константами.
Rf 0,337, EtAc/(н-C6H6)/NHEt2, 100:100:20.
Rf 0,621, CH2Cl2/CH3OH/NH4OH, 90:9:1,5.
ИК (CHCl3) см-1 3400, 2980, 2950, 1770, 1660, 1540, 1460, 1390, 1270, 1110, 1050, 1005.
1H ЯМР (300 МГц, CDCl3) δ: 7.45 (CONH), 4.93 (H-1''), 4.37 (H-1'), 4.19 (H-3), 4.11 (H-10), 3.80 (H-11), 3.65 (H-5), 3.28 (3''-OCH3), 3.20 (H-13), 2.79 (H-8), 2.46 (H-2), 2.27 /3'-N(CH3)2/, 2.20 (H-7a), 2.00 (H-4), 1.98 (H-7b), 1.59 (H-14a), 1.55 (6-CH3), 1.35 (H-14b), 1.28 (8-CH3), 1.26 (10-CH3), 1.14 (12-CH3), 1.11 (2-CH3), 1.09 (4-CH3), 1.05 (15-CH3).
13C ЯМР (75 МГц, CDCl3) δ: 179.4 (C-9), 174.5 (C-1), 105.6 (C-1'), 96.3 (C-1''), 86.4 (C-6), 86.2 (C-5), 83.3 (C-13), 79.5(C-3), 75.2 (C-11), 74.9 (C-12). 49.3 (3''-OCH3), 48.8 (C-10), 42.6 (C-2), 40.0 /3'-N(CH3)2/, 39.1 (C-7), 38.5 (C-4), 34.2 (C-8), 25.0 (C-14), 23.8 (6-CH3), 21.3 (12-CH3), 15.7 (10-CH3), 14.9 (8-CH3), 11.6 (15-CH3), 11.0 (4-CH3), 9.9 (2-CH3).
МC, ЭУ (EI, электронный удар), m/z 748.
Способ 2
6-Дезокси-6,9-эпокси-8(R)-метил-10-амино-9,10-секоэритромицин A (EP 0735041 A1, 02.10.1996) (1 г, 0,00134 моль) суспендируют в 100 мл воды и оставляют стоять в течение 3 часов при комнатной температуре. К реакционной смеси добавляют CHCl3 (30 мл) и доводят pH 9,0, добавляя 10% NaOH, слои разделяют и водный слой экстрагируют еще два раза CHCl3 (60 мл). Объединенные органические экстракты сушат над K2CO3, упаривают на роторном испарителе и затем очищают колоночной хроматографией на силикагеле с использованием системы растворителей CHCl3/CH3OH/конц.NH4OH, 6:1:0,1, как описано в способе A.
6-Дезокси-6,9-эпокси-8(R)-метил-10-амино-9,10-секоэритромицин A (EP 0735041 A1, 02.10.1996) (1 г, 0,00134 моль) суспендируют в 100 мл воды и оставляют стоять в течение 3 часов при комнатной температуре. К реакционной смеси добавляют CHCl3 (30 мл) и доводят pH 9,0, добавляя 10% NaOH, слои разделяют и водный слой экстрагируют еще два раза CHCl3 (60 мл). Объединенные органические экстракты сушат над K2CO3, упаривают на роторном испарителе и затем очищают колоночной хроматографией на силикагеле с использованием системы растворителей CHCl3/CH3OH/конц.NH4OH, 6:1:0,1, как описано в способе A.
ПРИМЕР 2. 5-O-Дезозаминил-1-N-(2,3,4-тригидрокси-1,3- диметилгексил)амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9 - эпокси-9,10-секоэритромицин A (Ib)
1-N-(2,3,4-Тригидрокси-1,3-диметилгексил)амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпокси-8(R)-метил-9,10-секоэритромицин A (Ia) из примера 1 (6 г, 0,008 моль) растворяют в 300 мл 0,25 N HCl и затем перемешивают в течение 2 часов при комнатной температуре. К реакционной смеси добавляют CHCl3 (40 мл) (pH 2,0), слои разделяют и водный слой снова дважды экстрагируют CHCl3. После подщелачивания до pH 10,0 (20% NaOH) водный слой снова экстрагируют CHCl3. Объединенные органические экстракты сушат при pH 10 над K2CO3, фильтруют и упаривают и получают сырой продукт (1,3 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH/конц. NH4OH, 90:9:1, получают хроматографически однородный продукт (Ib) (0,85 г) с приведенными ниже физико-химическими константами.
1-N-(2,3,4-Тригидрокси-1,3-диметилгексил)амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпокси-8(R)-метил-9,10-секоэритромицин A (Ia) из примера 1 (6 г, 0,008 моль) растворяют в 300 мл 0,25 N HCl и затем перемешивают в течение 2 часов при комнатной температуре. К реакционной смеси добавляют CHCl3 (40 мл) (pH 2,0), слои разделяют и водный слой снова дважды экстрагируют CHCl3. После подщелачивания до pH 10,0 (20% NaOH) водный слой снова экстрагируют CHCl3. Объединенные органические экстракты сушат при pH 10 над K2CO3, фильтруют и упаривают и получают сырой продукт (1,3 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH/конц. NH4OH, 90:9:1, получают хроматографически однородный продукт (Ib) (0,85 г) с приведенными ниже физико-химическими константами.
Т.пл. 87-89oC.
Rf 0,324, CH2Cl2/CH3OH/NH4OH, 90:9:1,5.
Rf 0,222, CHCl3CH3OH, 7:3.
ИК (CHCl3) см-1, 3420, 2980, 2940, 2870, 1740, 1640, 1500, 1480, 1380, 1295, 1230, 1170, 1140, 1120, 980.
ПРИМЕР 3. 1-N-(2,3,4-Тригидрокси-1,3-диметилгексил)амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпокси-8(R)-метил-9,10- секоэритронолид A (Ic)
5-О-Дезозаминил-1-N-(2,3,4-тригидрокси-1,3-диметилгексил)амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпокси-9,10-секоэритромицин A (Ib) из примера 2 (4 г, 0,0068 моль) растворяют в 20 мл CHCl3, добавляют 2 N HCl (40 мл) и затем реакционную смесь перемешивают при кипячении с обратным холодильником в течение 2 часов. После охлаждения до комнатной температуры отделяют CHCl3-слой и водный слой снова дважды экстрагируют CHCl3 (25 мл). Водный раствор упаривают при пониженном давлении, к твердому остатку добавляют CH3OH (40 мл) и реакционную суспензию перемешивают в течение 1 часа при комнатной температуре, фильтруют и прозрачный фильтрат упаривают на роторном испарителе и получают твердый остаток (3 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CHCl3/CH3OH, 7:3, из сырого продукта (0,6 г) получают хроматографически однородное вещество (Ic) (0,28 г) с приведенными ниже физико-химическими константами.
5-О-Дезозаминил-1-N-(2,3,4-тригидрокси-1,3-диметилгексил)амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпокси-9,10-секоэритромицин A (Ib) из примера 2 (4 г, 0,0068 моль) растворяют в 20 мл CHCl3, добавляют 2 N HCl (40 мл) и затем реакционную смесь перемешивают при кипячении с обратным холодильником в течение 2 часов. После охлаждения до комнатной температуры отделяют CHCl3-слой и водный слой снова дважды экстрагируют CHCl3 (25 мл). Водный раствор упаривают при пониженном давлении, к твердому остатку добавляют CH3OH (40 мл) и реакционную суспензию перемешивают в течение 1 часа при комнатной температуре, фильтруют и прозрачный фильтрат упаривают на роторном испарителе и получают твердый остаток (3 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CHCl3/CH3OH, 7:3, из сырого продукта (0,6 г) получают хроматографически однородное вещество (Ic) (0,28 г) с приведенными ниже физико-химическими константами.
Rf 0,793, CHCl3/CH3OH, 7:3.
ИК (CHCl3) см-1, 3420, 2980, 2940, 2890, 1760, 1615, 1550, 1460, 1390, 1300, 1240, 1160, 1100, 970.
1H ЯМР (300 МГц, Py-d5) δ: 8.84 (CONH), 4.85 (H-10), 4.44 (H-3), 4.41 (H-11), 4.01 (H-5), 4.00 (H-13), 3.06 (H-2), 2.81 (H-8), 2.41 (H-4), 2.30 (H-7a), 2.10 (H-7b), 2.03 (H-14a), 1.72 (H-14b), 1.60 (2-CH3), 1.59 (10-CH3), 1.55 (12-CH3), 1.46 (4-CH3), 1.44 (6-CH3), 1.21 (8-CH3), 1.17 (15-CH3).
13C ЯМР (75 МГц, Py-d5) δ: 179.4 (C-9), 174.4 (C-1), 86.5 (C-6), 79.2 (C-5), 79.2 (C-13), 77.8 (C-3), 77.1 (C-11), 75.6 (C-12), 47.0 (C-10), 44.9 (C-2), 39.3 (C-7), 36.6 (C-4), 34.5 (C-8), 24.9 (C-14), 22.0 (6-CH3), 20.0 (12-CH3), 15.3 (10-CH3), 15.5 (8-CH3), 12.1 (15-CH3), 8.2 (4-CH3), 16.3 (2-CH3).
МC, ЭУ, m/z 432.
ПРИМЕР 4. 2',4'-O-Диацетил-1-N-(2,4-O-диацетил-3-гидрокси-1,3-диметилгексил)амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпокси-9,10-секоэритромицин A (Id)
К раствору вещества (Ia) (3,38 г, 0,0045 моль) из примера 1 в пиридине (40 мл) добавляют ангидрид уксусной кислоты (12 мл) и затем реакционную смесь оставляют стоять в течение 3 суток при комнатной температуре. Раствор выливают в смесь воды со льдом (pH 4,8), доводят pH смеси до 9,0, добавляя 10% NaOH и полученный продукт экстрагируют CHCl3. Объединенные органические слои сушат над K2CO3, фильтруют и упаривают и получают сырой продукт (4,15 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH/конц. NH4OH, 90:9:1,5 из продукта (1,2 г) получают хроматографически однородный тетраацетат (Id) (0,65 г) с приведенными ниже физико-химическими константами.
К раствору вещества (Ia) (3,38 г, 0,0045 моль) из примера 1 в пиридине (40 мл) добавляют ангидрид уксусной кислоты (12 мл) и затем реакционную смесь оставляют стоять в течение 3 суток при комнатной температуре. Раствор выливают в смесь воды со льдом (pH 4,8), доводят pH смеси до 9,0, добавляя 10% NaOH и полученный продукт экстрагируют CHCl3. Объединенные органические слои сушат над K2CO3, фильтруют и упаривают и получают сырой продукт (4,15 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH/конц. NH4OH, 90:9:1,5 из продукта (1,2 г) получают хроматографически однородный тетраацетат (Id) (0,65 г) с приведенными ниже физико-химическими константами.
Rf 0,622, EtAc/(н-C6H6)/NHEt2, 100:100:20.
ИК (CHCl3) см-1, 1745, 1720, 1650, 1515, 1450, 1370, 1240, 1165, 1110, 1060.
1H ЯМР (300 МГц, CDCl3) δ: 6.87 (CONH), 4.86 (H-11), 4.86 (H-1''), 4.51 (H-2'). 4.81 (H-13), 4.66 (H-4''), 4.51 (H-1'), 4.43 (H-10), 3.95 (H-3), 3.75 (H-5), 3.37 (3''-ОCH3), 2.75 (H-8), 2.23 (H-2), 2.29 /3'-N(CH3)2/, 2.16 (H-7a), 2.15, 2.07, 2.05 and 2.03 (COCH3), 1.90 (H-7b), 1.84 (H-14a), 1.66 (H-4), 1.58 (6-CH3), 1.56 (H-14b). 1.29 (12-CH3), 1.25 (8-CH3), 1.23 (5'-CH3), 1.21 (10-CH3), 1.12 (2-CH3), 1.11 (3''-CH3), 1.11 (5''-CH3), 106 (4-CH3), 0.90 (15-CH3).
13C ЯМР (75 МГц, CDCl3) δ: 179.8 (C-9), 173.7 (C-1), 170.3, 170.3, 170.1 and 169.6 (CОCH3), 101.0 (C-1'), 96.2 (C-1''), 85.5 (C- 6), 81.5 (C-5), 78.6 (C-4''), 78.1 (C-3), 76.8 (C-13), 76.0 (C-11), 74.9 (C-12). 62.7 (C-3'), 62.3 (C-5''), 49.4 (3''-ОCH3), 45.1 (C-10), 44.7 (C-2), 40.3 /3'-N(CH3)2/, 39.8 (C-7), 39.8 (C-4), 33.3 (C-8), 30.6 (C-4'), 24.7 (6-CH3), 21.9 (C-14), 21.0, 20.7, 20.6, 20.5 (COCH3), 20.9 (3''-CH3), 20.7 (5'-CH3), 18.4 (12-CH3), 17.2 (5''-CH3), 16.0 (10-CH3), 14.5 (8-CH3), 11.3 (4-CH3), 10.7 (15-CH3), 10.5 (2-CH3).
МC, ЭУ, m/z 916.
ПРИМЕР 5. 4''-O-Ацетил-1-N-(2,4,-O-диацетил-3-гидрокси-1,3-диметилгексил)амидо-10,11,12,13,14,15-гексанор-6-деазокси-6,9-эпокси-9,10-секоэритромицин A (Ie)
Раствор вещества (Id) (2 г, 0,00218 моль) из примера 4 в CH3OH (50 мл) оставляют стоять в течение 3 суток при комнатной температуре. Посредством выпаривания при пониженном давлении реакционную смесь концентрируют примерно до 1/4 объема, добавляют воду (100 мл) (pH 6,9) и затем полученный продукт выделяют экстракцией CH2Cl2 при pH 9,0 (10% NaOH). Объединенные органические экстракты сушат над K2CO3, фильтруют и упаривают и получают сырой продукт (1,72 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH, 85:15, получают хроматографически однородный триацетат (Ie) (0,85 г) с приведенными ниже физико-химическими константами.
Раствор вещества (Id) (2 г, 0,00218 моль) из примера 4 в CH3OH (50 мл) оставляют стоять в течение 3 суток при комнатной температуре. Посредством выпаривания при пониженном давлении реакционную смесь концентрируют примерно до 1/4 объема, добавляют воду (100 мл) (pH 6,9) и затем полученный продукт выделяют экстракцией CH2Cl2 при pH 9,0 (10% NaOH). Объединенные органические экстракты сушат над K2CO3, фильтруют и упаривают и получают сырой продукт (1,72 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH, 85:15, получают хроматографически однородный триацетат (Ie) (0,85 г) с приведенными ниже физико-химическими константами.
Rf 0,582, EtAc/(н-C6H6)/NHEt2, 100:100:20.
ИК (CHCl3), см-1: 1740, 1710, 1665, 1515, 1460, 1380, 1240, 1170, 1130, 1060.
1H ЯМР (300 МГц, CDCl3) δ: 7.14 (CONH), 4.87 (H-13), 4.85 (H-1''), 4.77 (H-11), 4.65 (H-4''), 4.47 (H-10), 4.41 (H-1'), 4.37 (C-5''), 4.07 (H-3), 3.75 (H-5), 3.33 (3''- ОCH3), 3.26 (H-2'), 2.75 (H-8), 2.50 (H-2), 2.32 /3'-N(CH3)2/, 2.13, 2.06, and 2.03. (COCH3), 2.09 (H-7a), 1.91 (H-4), 1.83 (H-14a), 1.58 (6-CH3), 1.54 (H-14b), 1.29 (12-CH3), 1.26 (8-CH3), 1.23 (5'-CH3, 1.18 (10-CH3), 1.15 (4-CH3), 1.12 (2-CH3), 1.10 (3''-CH3), 1.08 (5''-CH3), 0.90 (H-15).
13C ЯМР (75 МГц, CDCl3) δ: 179.1 (C-9), 173.8 (C-1), 170.4, 170.1 and 170.1 (CОCH3), 103.4 (C-1'), 96.0 (C-1''), 85.6 (C-6), 79.4 (C-3). 82.8 (C-5), 78.2 (C-11), 75.5 (C-13), 74.5 (C-12), 69.9 (C-2'), 65.0 (C-3'), 62.1 (C-5''), 49.1 (3''-OCH3), 44.5 (C-10), 42.6 (C-2), 39.7 /3'-N(CH3)2/, 38.1 (C-7), 38.5 (C-4), 33.4 (C-8), 23.7 (6-CH3), 21.5 (C-14), 20.5, 20.3 and 20.2 (COCH3), 20.6 (3''-CH3 and 5'-CH3), 18.1 (12-CH3), 16.7 (5''-CH3), 16.2 (4-CH3), 14.3 (8-CH3), 11.2 (10-CH3), 10.9 (2-CH3), 10.4 (C-15).
МC, ЭУ, m/z 874.
ПРИМЕР 6. 2-O-(4-Бромбензоил-1-N-(2,3,4-тригидрокси-1,3-диметилгексил)-амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-этокси-9,10-секоэритромицин A (If)
Вещество (Ia) (2,0 г, 0,0027 моль) из примера 1 растворяют в сухом ацетоне (10 мл), добавляют NaHCO3 (0,4 г, 0,00476 моль) и затем, после перемешивания в течение 1 часа при 0-5oC, добавляют по каплям раствор 4-бромбензоилхлорида (0,83 г, 0,0038 моль) в ацетоне (10 мл). Реакционную смесь перемешивают затем 3 часа при этой температуре, фильтруют, ацетон удаляют перегонкой при пониженном давлении и к полученному остатку добавляют воду (30 мл), после чего экстракцией CHCl3 при pH 8,5 выделяют продукт. После сушки над K2CO3 и упаривания объединенных органических экстрактов выделяют сырой продукт (2,3 г). Посредством колоночной хроматографии на силикагеле с использованем системы растворителей CHCl3/CH3OH/конц. NH4OH, 90:9:1,5, получают хроматографически однородное 2'-(п-бромбензоильное) производное (If) (1,23 г) с приведенными ниже физико-химическими константами.
Вещество (Ia) (2,0 г, 0,0027 моль) из примера 1 растворяют в сухом ацетоне (10 мл), добавляют NaHCO3 (0,4 г, 0,00476 моль) и затем, после перемешивания в течение 1 часа при 0-5oC, добавляют по каплям раствор 4-бромбензоилхлорида (0,83 г, 0,0038 моль) в ацетоне (10 мл). Реакционную смесь перемешивают затем 3 часа при этой температуре, фильтруют, ацетон удаляют перегонкой при пониженном давлении и к полученному остатку добавляют воду (30 мл), после чего экстракцией CHCl3 при pH 8,5 выделяют продукт. После сушки над K2CO3 и упаривания объединенных органических экстрактов выделяют сырой продукт (2,3 г). Посредством колоночной хроматографии на силикагеле с использованем системы растворителей CHCl3/CH3OH/конц. NH4OH, 90:9:1,5, получают хроматографически однородное 2'-(п-бромбензоильное) производное (If) (1,23 г) с приведенными ниже физико-химическими константами.
Rf 0,390, EtAc/(н-C6H6)/NHEt2, 100:100:20.
Rf 0,814, CH2Cl2/CH3OH/NH4OH, 90:9:1,5.
ИК (CHCl3), см-1: 1740, 1710, 1650, 1580, 1500, 1450, 1390, 1370, 1340, 1265, 1165, 1160, 1120, 1100, 1055, 1010.
1H ЯМР (300 МГц, CDCl3) δ: 7.73 (Ph), 6.61 (CONH), 5.04 (H-2'), 4.86 (H-1''), 4.61 (H-1'), 4.02 (H-10), 3.98 (H-5''), 3.92 (H-3), 3.82 (H-11), 3.73 (H-5), 3.59 (H-5'), 3.36 (3''-ОCH3), 3.26 (H-3'), 3.25 (H-13), 3.03 (H-4''), 2.87 (H-3'), 2.77 (H-8), 2.37 (H-2''), 2.30 /3'-N(CH3)2/, 2.20 (H-7a), 2.16 (H-2), 1.84 (H-4'a), 1.78 (H-7b), 1.56 (H-14a), 1.59 (6-CH3), 1.56 (H-4), 1.41 (H-14b), 1.27 (10-CH3), 1.57 (6-CH3), 1.23 (8-CH3), 1.13 (12-CH3), 0.83 (4-CH3), 1.05 (2-CH3), 1.04 (C-15).
13C ЯМР (75 МГц, CDCl3) δ: 180.6 (C-9), 175.6 (C-1), 164.7 (COBr), 131.7, 131.3, 129.2 and 128.1 (aryl), 101.1 (C.1'), 94.8 (C-1''), 86.1 (C-6), 79.9 (C-3), 82.2 (C-5), 81.2 (C-13), 78.0 (C-3), 75.9 (C-11), 74.3 (C-12), 73.0 (C-3''), 72.2 (C-2'), 65.4 (C-5''), 63.5 (C-3'), 49.6 (3''-ОCH3), 48.1 (C-10), 45.3 (C-2), 41.7 (C-4), 40.2 /3'-N(CH3)2/, 37.0 (C-7), 34.8 (C-2''), 33.8 (C-8), 31.1 (C-4'), 25.3 (6-CH3), 24.9 (C-14), 21.7 (12-CH3), 18.1 (5''-CH3), 13.8 (10-CH3), 14.7 (8-CH3), 11.8 (4-CH3), 11.1 (C-15), 10.0 (2-CH3).
МC, ЭУ, m/z 931.
ПРИМЕР 7. 2'-O(4-Бромбензоил)-4''-О-ацетил-1-N-(2,4-O-диацетил-3-гидрокси-1,3-диметилгексил)-амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпокси-9,10-секоэритромицина A (Ig)
К раствору вещества (If) (0,50 г, 0,00054 моль) из примера 6 в пиридине (10 мл) добавляют ангидрид уксусной кислоты (2,5 мл) и затем реакционную смесь оставляют стоять в течение 3 суток при комнатной температуре. Раствор выливают в смесь воды со льдом, доводят pH смеси до 9,0, добавляя 10% NaOH и полученный продукт выделяют экстракцией CHCl3. Объединенные органические экстракты сушат над K2CO3, фильтруют, упаривают при пониженном давлении и получают сырой продукт (0,57 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH/конц. NH4OH, 90: 9: 1,5, из полученного осадка (1,2 г) получают хроматографически однородное вещество (Ig) (0,18 г) с приведенными ниже физико-химическими константами.
К раствору вещества (If) (0,50 г, 0,00054 моль) из примера 6 в пиридине (10 мл) добавляют ангидрид уксусной кислоты (2,5 мл) и затем реакционную смесь оставляют стоять в течение 3 суток при комнатной температуре. Раствор выливают в смесь воды со льдом, доводят pH смеси до 9,0, добавляя 10% NaOH и полученный продукт выделяют экстракцией CHCl3. Объединенные органические экстракты сушат над K2CO3, фильтруют, упаривают при пониженном давлении и получают сырой продукт (0,57 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH/конц. NH4OH, 90: 9: 1,5, из полученного осадка (1,2 г) получают хроматографически однородное вещество (Ig) (0,18 г) с приведенными ниже физико-химическими константами.
Rf 0,773, EtAc/(н-C6H6)/NHEt2, 100:100:20.
Rf 0,938, CH2CI2/CH3OH/NH4OH, 90:9:1,5.
ИК (CHCl3), см-1: 3340, 2970, 1740, 1710, 1650, 1580, 1515, 1450, 1370, 1240, 1160, 1130, 1100, 1040, 1010.
1H ЯМР (300 МГц, CDCl3) δ: 7.73 (Ph), 6.83 (CONH), 3.38 (3''-ОCH3), 2.28 /3'-N(CH3)2/, 2.17, 2.03 and 2.02 (COCH3).
ПРИМЕР 8. 2'-O-(4-Бромбензоил)-1-N-[2-(4-бромбензоил)-3,4-дигидpoкси-1,3-диметилгексил] aмидo-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпoкcи-9,10-cекoэритромицина A (Ih) и
2'-О-(4-бромбензоил)-1-N-[4-(4-бромбензоил)-2,3-дигидрокси-1,3-диметилгексил] амидо-10,11,12,13,14,15-гекcанop-6-дезокси-6,9-эпокси-9,10-секоэритромицин A (Ii)
Вещество (Ia) (7,8 г, 0,0104 моль) из примера 1 растворяют в сухом ацетоне (200 мл) и добавляют NaHCO3 (23,55 г, 0,280 моль) и затем реакционную суспензию при перемешивании нагревают до температуры кипения. После перемешивания в течение 30 минут добавляют по каплям раствор 4-бромбензоилхлорида (11,45 г, 0,052 моль) в ацетоне (80 мл), реакционную суспензию перемешивают еще в течение 30 часов при кипячении с обратным холодильником, охлаждают до комнатной температуры, фильтруют и упаривают при пониженном давлении. Полученный осадок растворяют в CH2Cl2 (100 мл), добавляют воду (60 мл), после чего экстракцией CHCl3 при pH 9,0 выделяют продукт. Объединенные органические экстракты промывают насыщенным раствором NaHCO3 (80 мл) и водой (40 мл) и сушат над K2CO3. После удаления растворителя получают смесь (12,0 г) дибромбензоатов (Ih) и (Ii), которую разделяют колоночной хроматографией на силикагеле с использованием системы растворителей CH2Cl2/CH3OH, 95:5 и получают хроматографически однородные, названные в заголовке продукты (Ih) и (Ii) с физико-химическими константами, приведенными ниже.
2'-О-(4-бромбензоил)-1-N-[4-(4-бромбензоил)-2,3-дигидрокси-1,3-диметилгексил] амидо-10,11,12,13,14,15-гекcанop-6-дезокси-6,9-эпокси-9,10-секоэритромицин A (Ii)
Вещество (Ia) (7,8 г, 0,0104 моль) из примера 1 растворяют в сухом ацетоне (200 мл) и добавляют NaHCO3 (23,55 г, 0,280 моль) и затем реакционную суспензию при перемешивании нагревают до температуры кипения. После перемешивания в течение 30 минут добавляют по каплям раствор 4-бромбензоилхлорида (11,45 г, 0,052 моль) в ацетоне (80 мл), реакционную суспензию перемешивают еще в течение 30 часов при кипячении с обратным холодильником, охлаждают до комнатной температуры, фильтруют и упаривают при пониженном давлении. Полученный осадок растворяют в CH2Cl2 (100 мл), добавляют воду (60 мл), после чего экстракцией CHCl3 при pH 9,0 выделяют продукт. Объединенные органические экстракты промывают насыщенным раствором NaHCO3 (80 мл) и водой (40 мл) и сушат над K2CO3. После удаления растворителя получают смесь (12,0 г) дибромбензоатов (Ih) и (Ii), которую разделяют колоночной хроматографией на силикагеле с использованием системы растворителей CH2Cl2/CH3OH, 95:5 и получают хроматографически однородные, названные в заголовке продукты (Ih) и (Ii) с физико-химическими константами, приведенными ниже.
Вещество (Ih)
Rf 0,539, CH2Cl2/CH3OH/NH4OH, 90:9:0,5.
Rf 0,539, CH2Cl2/CH3OH/NH4OH, 90:9:0,5.
ИК (CHCl3), см-1: 1755, 1720, 1660, 1590, 1520, 1490, 1450, 1390, 1370, 1340, 1270, 1165, 1160, 1120, 1100, 1060, 1015, 850.
1H ЯМР (300 МГц, CDCl3) δ: 7.72 (Ph), 7.00 (CONH), 5.27 (H-11), 4.96 (H-2'), 4.72 (H-1''), 4.56 (H-1'), 4.53 (H-10), 3.93 (H-5''), 3.77 (H-3), 3.65 (H-5), 3.13 (H-13), 3.57 (H-5'), 3.25 (3''-ОCH3), 3.05 (H-4''), 2.82 (H-3'), 2.42 (H-2''), 2.34 (H-8), 2.24 /3'N(CH3)2/, 2.02 (H-7a), 2.05 (H-2), 2.04 (H-2''a), 1.81 (H-4'a), 1.77 (H-7b), 1.71 (H-14a), 1.51 (H-2''b), 1.41 (H-14b), 1.50 (H-4), 1.41 (H-4'b), 1.36 (10-CH3), 1.27 (12-CH3), 1.30 (5''-CH3), 1.28 (5'-CH3), 1.24 (6-CH3), 1.23 (3''-CH3), 1.14 (8- CH3), 1.01 (2-CH3), 0.98 (H-15), 0.83 (4-CH3), 0.80 (H-2''b).
13C ЯМР (75 МГц, CDCl3) δ: 180.3 (C-9), 174.6 (C-1), 166.4 and 164.5 (COBr), 131.6, 131.5, 129.1, 128.5, 128.2, 127.8 (Ph), 101.1 (C-1'), 96.3 (C-1''), 85.5 (C-6), 81.5 (C-5), 79.3 (C-11), 78.1 (C-3), 77.8 (C-4''), 77.0 (C-13), 75.7 (C-12), 72.6 (C-3''), 72.0 (C-2'), 68.9 (C-5'), 64.9 (C-5''), 63.0 (C-3'), 49.2 (3''-ОCH3), 45.3 (C-10), 45.3 (C-2), 40.6 (C-4), 40.6 /3'N(CH3)2/, 36.9 (C-7), 33.1 (C-8), 34.5 (C-2''), 30.7 (C-4'), 24.3 (6-CH3), 22.6 (C-14), 21.3 (3''-CH3), 20.6 (5'-CH3), 17.8 (5''-CH3), 17.7 (12-CH3), 15.3 (10-CH3), 14.2 (8-CH3), 11.5 (4-CH3), 11.3 (C-15), 10.0 (2-CH3).
Вещество (Ii)
Rf 0,744, CH2Cl2/CH3OH/NH4OH, 90:9:0,5.
Rf 0,744, CH2Cl2/CH3OH/NH4OH, 90:9:0,5.
ИК (CHCl3), см-1: 3450, 2980, 2940, 1770, 1730, 1650, 1600, 1540, 1495, 1460, 1405, 1390, 1350, 1280, 1170, 1110, 1070, 1015, 850.
1H ЯМР (300 МГц, CDCl3) δ: 7.72 (Ph), 6.51 (CONH), 5.13 (H-13), 5.00 (H-2'), 4.55 (H-1'), 4.52 (H-1''), 4.09 (H-10), 3.92 (H-3), 3.85 (H-5''), 3.68 (H-5), 3.65 (H-11), 3.54 (H-5'), 3.28 (3''-ОCH3), 3.00 (H-4''), 2.79 (H-3'), 2.69 (H-8), 2.25 /3'N(CH3)2/, 2.16 (H-7a), 2.10 (H-2), 2.04 (H-2''a), 2.00 (H-14a), 1.80 (H-4'a), 1.76 (H-7b), 1.62 (H-14b), 1.53 (H-4), 1.44 (H-4'b), 1.27 (5'-CH3), 1.27 (5'-CH3), 1.14 (3''-CH3), 1.04 (H-15), 0.80 (H-2''b).
13C ЯМР (75 МГц, CDCl3) δ: 180.1 (C-9), 174.9 (C-1). 165.8 and 164.7 (COBr), 131.8, 131.6, 131.5, 131.2, 131.0, 129.3, 129.1, 127.9 (Ph). 101.2 (C-1'), 94.1 (C-1''), 85.5 (C-6), 81.4 (C-5), 76.9 (C-3), 77.2 (C-4''), 78.3 (C-13), 74.6 (C-12), 72.6 (C-3''), 71.9 (C-2'), 70.2 (C-11), 69.0 (C-5'), 65.2 (C-5''), 63.3 (C-3'), 49.2 (3''-OCH3), 46.7 (C-10), 44.8 (C-2), 41.5 (C-4), 40.5 /3'N(CH3)2/, 36.9 (C-7), 33.3 (C-8), 33.2 (C-2''), 30.8 (C-4'), 25.0 (6-CH3), 21.7 (C-14), 21.3 (3''-CH3), 20.8 (5'-CH3), 17.5 (5''-CH3), 16.3 (12-CH3), 14.4 (8-CH3), 13.5 (10-CH3), 11.1 (C-15), 10.7 (4-CH3), 9.8 (2-CH3).
ПРИМЕР 9. 1-N-[2,3-Дигидрокси-4-(4-бромбензоил)-1,3-ди-метилгексил] амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпокси-9,10-секоэритромицин A (Ij)
Продукт (Ii) (4,6 г) примера 8 растворяют в метаноле (50 мл), добавляют воду (10 мл) и затем реакционный раствор оставляют стоять в течение 24 часов при комнатной температуре. Выпариванием при пониженном давлении удаляют метанол, к маслянистому остатку добавляют воду (20 мл) и экстракцией CHCl3 при pH 9,0 выделяют продукт. После сушки над K2CO3 и упаривания объединенных органических экстрактов получают сырой продукт (4,1 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH/конц. NH4OH, 90:9:0,5, из сырого продукта (1,90, г) выделяют хроматографически (ТСХ) (0,72 г) однородный монобромбензоат (Ij) с физико-химическими константами, приведенными ниже.
Продукт (Ii) (4,6 г) примера 8 растворяют в метаноле (50 мл), добавляют воду (10 мл) и затем реакционный раствор оставляют стоять в течение 24 часов при комнатной температуре. Выпариванием при пониженном давлении удаляют метанол, к маслянистому остатку добавляют воду (20 мл) и экстракцией CHCl3 при pH 9,0 выделяют продукт. После сушки над K2CO3 и упаривания объединенных органических экстрактов получают сырой продукт (4,1 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH/конц. NH4OH, 90:9:0,5, из сырого продукта (1,90, г) выделяют хроматографически (ТСХ) (0,72 г) однородный монобромбензоат (Ij) с физико-химическими константами, приведенными ниже.
Rf 0,391, CH2Cl2/CH3OH/NH4OH, 90:9:0,5.
ИК (CHCl3), см-1: 3400, 2980, 2950, 1770, 1660, 1540, 1460, 1390, 1270, 1110, 1050, 1005.
1H ЯМР (300 МГц, CDCl3) δ: 7.72 (aryl), 7.26 (CONH), 5.13 (H-13), 4.54 (H-1''), 4.36 (H-1'), 4.20 (H-10), 4.14 (H-3), 3.87 (H-5''), 3.70 (H-5), 3.57 (H-5'), 3.54 (H-11), 3.29 (H-2'), 3.19 (3''-ОCH3), 2.94 (H-4''), 2.53 (H-8), 2.53 (H-2), 2.45 (H-3'), 2.30 /3'N(CH3)2/, 2.15 (H-7a), 2.02 (H-14a), 2.00 (H-7b), 1.98 (H-2''a), 1.86 (H-4), 1.69 (H-4'a), 1.61 (H-14b), 1.50 (6-CH3), 1.33 (H-4'b), 1.29 (12-CH3), 1.26 (5'-CH3), 1.27 (3''-CH3), 1.26 (8-CH3), 1.25 (5''-CH3), 1.20 (10-CH3), 1.10 (3''-CH3), 1.02 (2-CH3), 0.99 (4-CH3), 0.92 (H-15), 0.88 (H-2''b).
13C ЯМР (75 МГц, CDCl3) δ: 179.3 (C-9), 174.4 (C-1), 165.9 (COBr), 131.8, 131.1, 129.0 and 128.1 (aryl), 104.9 (C-1'), 94.6 (C-1''), 86.1 (C-6), 84.5 (C-5), 76.9 (C-3), 78.1 (C-13), 74.6 (C-12), 70.5 (C-11), 70.2 (C-2'), 65.3 (C-5''), 65.8 (C-3'), 49.0 (3''- ОCH3), 46.1 (C-10), 41.6 (C-2), 41.0 /3'N(CH3)2/, 39.1 (C-4), 38.7 (C-7), 33.9 (C-2''), 33.8 (C-8), 27.8 (C-4'), 21.6 (C-14), 23.6 (6-CH3), 20.9 (5'-CH3), 21.2 (3''-CH3), 17.2 (5''-CH3), 16.2 (12-CH3), 14.5 (8-CH3), 13.6 (10-CH3), 9.9 (2-CH3), 10.6 (4-CH3), 10.9 (C-15).
ПРИМЕР 10. 1-N-[2-(4-бромбензоил)-3,4-дигидpoкcи-1,3-диметилгексил] амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпокси-9,10-секоэритромицин A (Ik)
Из продукта (Ih) (2,20 г) примера 8 по способу, описанному в примере 9, после очистки сырого продукта колоночной хроматографией на силикагеле и упаривания фракций с Rf 0,283 получают хроматографически однородный, названный в заголовке продукт (Ik) (0,95 г).
Из продукта (Ih) (2,20 г) примера 8 по способу, описанному в примере 9, после очистки сырого продукта колоночной хроматографией на силикагеле и упаривания фракций с Rf 0,283 получают хроматографически однородный, названный в заголовке продукт (Ik) (0,95 г).
Rf 0,283, CH2Cl2/CH3OH/NH4OH, 90:9:0,5.
1H ЯМР (300 МГц, CDCl3) δ: 7.72 (Ph), 7.00 (CONH), 5.20 (H-11), 4.72 (H-1''), 4.36 (H-1'), 4.53 (H-10), 3.93 (H-5''), 3.77 (H-3), 3.65 (H-5), 3.23 (H-13), 3.59 (H-5'), 3.36 (H-2'), 3.25 (3''-ОCH3), 3.05 (H-4''), 2.72 (H-3'), 2.42 (H-2''), 2.34 (H-8), 2.28 /3'N(CH3)2/, 2.02 (H-7a), 2.05 (H-2), 2.04 (H-2''a), 1.71 (H-4'a), 1.77 (H-7b), 1.71 (H-14a), 1.51 (H-2''b), 1.41 (H-14b), 1.50 (H-4), 1.26 (H-4'b), 1.36 (10-CH3), 1.27 (12-CH3), 1.26 (5''-CH3), 1.26 (5'-CH3), 1.64 (6-CH3), 1.20 (3''-CH3), 1.14 (8-CH3), 1.01(2-CH3), 0.98 (H-15), 0.83 (4-CH3), 0.80 (H-2''b).
ПРИМЕР 11. 2,3-Циклический карбонат 1-N-[4-гидрокси-1,3-диметилгексил] амидо-10,11,12,13,14,15-гексанор-6-дезокси-6,9-эпокси-9,10-секоэритромицина A (Il)
Вещество (Ia) из примера 1 (10,0 г, 0,0134 моль) растворяют в сухом бензоле (100 мл) и добавляют этиленкарбонат (5,0 г, 0,057 моль) и затем, после растворения реагента, добавляют K2CO3 (2,0 г, 0,0145 моль). Реакционную суспензию при перемешивании кипятят с обратным холодильником в течение 9 часов, оставляют стоять в течение ночи, упаривают при пониженном давлении и получают сырой продукт (Il) (11,0 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH/конц. NH4OH, 90: 9: -1,5, из сырого продукта (3,0 г) получают хроматографически однородное вещество (Il) (1,25 г) с физико-химическими константами, приведенными ниже.
Вещество (Ia) из примера 1 (10,0 г, 0,0134 моль) растворяют в сухом бензоле (100 мл) и добавляют этиленкарбонат (5,0 г, 0,057 моль) и затем, после растворения реагента, добавляют K2CO3 (2,0 г, 0,0145 моль). Реакционную суспензию при перемешивании кипятят с обратным холодильником в течение 9 часов, оставляют стоять в течение ночи, упаривают при пониженном давлении и получают сырой продукт (Il) (11,0 г). Посредством колоночной хроматографии на силикагеле с использованием системы растворителей CH2Cl2/CH3OH/конц. NH4OH, 90: 9: -1,5, из сырого продукта (3,0 г) получают хроматографически однородное вещество (Il) (1,25 г) с физико-химическими константами, приведенными ниже.
ИК (CHCl3), см-1: 3540, 3300, 1790, 1760, 1660, 1530, 1450, 1380, 1300, 1280, 1230, 1165, 1000.
1H ЯМР (300 МГц, Py) δ: 8.46 (CONH), 5.26 (H-11), 5.18 (H-1''), 4.81 (H-1'), 4.61 (H-10), 4.54 (H-3), 4.52 (H-5''), 4.19 (H-5), 3.79 (H-13), 3.76 (H-5'), 3.60 (H-2'), 3.41 (3''-ОCH3), 3.29 (H-4''), 3.07 (H-2), 2.88 (H-8), 2.61 (H-3'), 255 (H-7а), 2.50 (H-2''а), 2.50 (H-4), 2.24 /3'N(CH3)2/, 2.20 (H-7b), 2.24 (H-4'a), 1.75 (6-CH3), 1.73 (H-14а), 1.65 (3''-CH3), 1.65 (3''-CH3), 1.58 (H-2''b), 1.55 (4-CH3), 1.55 (5''-CH3), 1.41 (10-CH3), 1.43 (2-CH3), 1.33 (12-CH3), 1.30 (8-CH3), 1.28 (5'-CH3), 1.16 (H-4'b), 1.16 (H-15).
13C ЯМР (75 МГц, Py) δ: 180.1 (C-9), 175.9 (C-1), 155.0 (CO carbonate), 105.2 (C-1'), 97.7 (C-1''), 88.9 (C-12), 87.1 (C-6), 83.0 (C-5), 82.2 (C-13), 80.8 (C-11), 79.1 (C-3), 70.2 (C-2'), 66.5 (C-5''), 66.2 (C-3'), 50.0 (3''-ОCH3), 46.1 (C-10), 44.8 (C-2), 41.0 /3'N(CH3)2/, 40.5 (C-4), 39.3 (C-7), 36.4 (C-2''), 34.9 (C-8). 30.9 (C-4'), 25.2 (6- CH3), 24.6 (C-14), 22.1 (5'-CH3), 21.9 (3''-CH3), 19.3 (5''-CH3), 17.2 (12-CH3), 16.8 (2-CH3), 15.7 (10-CH3), 13.9 (8-CH3), 11.3 (4-CH3), 11.6 (C-15).
МC, ЭУ, m/z 774.
ПРИМЕР 12. 1-N-Тригидрокси-1,3-диметилгексил]амидо-10,11,12,13,14,15-гексанор-9-дезоксо-9-гидрокси-8(R)-метил-9,10-секоэритромицин A (Im) и
1-N-[2,3,4-Тригидрокси-1,3-диметилгексил] амидо-10,11,12,13,14,15-гексанор-9-дезоксо-9-гидрокси-8(S)-метил-9,10-секоэритромицин A (In)
При кипячении с обратным холодильником раствора вещества (Ia) из примера 1 (3,0 г, 0,004 моль) и NaBH4 (2,4 г, 0,063 моль) в трет-бутаноле (32 моль), после перемешивания в течение 5 часов, добавляют к нему по каплям метанол (32 мл) и раствор кипятят с обратным холодильником еще в течение 2 часов. К охлажденной смеси добавляют воду (15 мл) и затем экстрагируют CH2Cl2 при pH 2,5. Объединенные органические экстракты сушат над K2CO3, фильтруют и упаривают при пониженном давлении. Сырой продукт (2,4 г) очищают колоночной хроматографией на силикагеле с использованием системы растворителей CHCl3/CH3OH/конц. NH4OH, 6:1:0,1. Объединяя и упаривая фракции с более высоким Rf (0,600), чем у исходного 6,9-лактона (Ia)
(Rf 0,553), получают смесь (0,45 г) изомеров (Im) и (In). Изомеры разделяют повторной колоночной хроматографией на силикагеле с использованием системы EtAc/н-C6H6)/Et2NH, 100:100:20. Выпаривая объединенные фракции с Rf 0,158, получают изомер (Im) (0,2 г), а выпаривая фракции с Rf 0,197 получают изомер (In) (0,05 г).
1-N-[2,3,4-Тригидрокси-1,3-диметилгексил] амидо-10,11,12,13,14,15-гексанор-9-дезоксо-9-гидрокси-8(S)-метил-9,10-секоэритромицин A (In)
При кипячении с обратным холодильником раствора вещества (Ia) из примера 1 (3,0 г, 0,004 моль) и NaBH4 (2,4 г, 0,063 моль) в трет-бутаноле (32 моль), после перемешивания в течение 5 часов, добавляют к нему по каплям метанол (32 мл) и раствор кипятят с обратным холодильником еще в течение 2 часов. К охлажденной смеси добавляют воду (15 мл) и затем экстрагируют CH2Cl2 при pH 2,5. Объединенные органические экстракты сушат над K2CO3, фильтруют и упаривают при пониженном давлении. Сырой продукт (2,4 г) очищают колоночной хроматографией на силикагеле с использованием системы растворителей CHCl3/CH3OH/конц. NH4OH, 6:1:0,1. Объединяя и упаривая фракции с более высоким Rf (0,600), чем у исходного 6,9-лактона (Ia)
(Rf 0,553), получают смесь (0,45 г) изомеров (Im) и (In). Изомеры разделяют повторной колоночной хроматографией на силикагеле с использованием системы EtAc/н-C6H6)/Et2NH, 100:100:20. Выпаривая объединенные фракции с Rf 0,158, получают изомер (Im) (0,2 г), а выпаривая фракции с Rf 0,197 получают изомер (In) (0,05 г).
Вещество (Im)
ИК (CHCl3), см-1: 3660, 3600, 3350, 2980, 2930, 1755, 1655, 1515, 1450, 1380, 1150, 1110.
ИК (CHCl3), см-1: 3660, 3600, 3350, 2980, 2930, 1755, 1655, 1515, 1450, 1380, 1150, 1110.
1H ЯМР (300 МГц, CDCl3) δ: 7.57 (CONH), 4.97 (H-1''), 4.36 (H-1'), 4.17 (H-10), 4.23 (H-3), 4.04 (H-5''), 3.76 (H-11), 3.70 (H-5'), 3.60 (H-9a), 3.46 (H-2'), 3.41 (H-5), 3.28 (3''-ОCH3), 3.27 (H-9b), 3.19 (H-13), 2.93 (H-4''), 2.77 (H-3'), 2.50 (H-2), 2.38 (H-2''a), 2.30 /3'N(CH3)2/, 2.09 (H-8), 1.95 (H-4), 1.78 (H-4'a), 1.57 (H-14a), 1.40 (H-7b), 1.40 (H-2''b), 1.36 (H-4'b), 1.36 (H-14b), 1.33 (6-CH3), 1.28 (5'-CH3), 1.25 (10-CH3), 1.23 (5''-CH3), 1.18 (3''-CH3), 1.14 (12-CH3), 1.09 (2-CH3), 1.06 (4-CH3), 1.05 (H-15), 0.95 (8-CH3).
13C ЯМР (75 МГц, CDCl3) δ: 173.4 (C-1), 106.7 (C-1'), 96.4 (C-1''), 92.5 (C-5), 83.7 (C-13), 80.1 (C-3), 75.0 (C-6), 74.7 (C-11), 74.6 (C-12), 70.2 (C-2'), 69.0 (C-9), 65.4 (C-5''), 64.1 (C-3'), 50.0 (3''-ОCH3), 49.0 (C-10), 44.1 (C-7), 41.3 (C-2), 39.5 /3'N(CH3)2/, 37.4 (C-4), 34.8 (C-2''), 31.0 (C-8), 27.8 (C-4'), 24.7 (C-14), 22.1 (6-CH3), 21.4 (12-CH3), 20.7 (5'-CH3), 21.1 (3''- CH3), 20.0 (8-CH3), 17.3 (5''-CH3), 16.0 (10-CH3), 10.1 (4-CH3), 11.3 (C-15), 8.4 (2-CH3).
Вещество (In)
1H ЯМР (300 МГц, CDCl3) δ: 7.63 (CONH), 5.05 (H-1''), 4.34 (H-1'), 4.22 (H-10), 4.25 (H-3), 4.06 (H-5''), 3.74 (H-11), 3.71 (H-5'), 3.48 (H-9a), 3.34 (H-2'), 3.70 (H-5), 3.28 (3''-ОCH3), 3.29 (H-9b), 3.14 (H-13), 2.93 (H-4''), 2.84 (H-3'), 2.50 (H-2), 2.32 (H-2''a), 2.28 /3'N(CH3)2/, 1.74 (H-8), 1.93 (H-4), 1.76 (H-4'a), 1.56 (H-14a), 1.74 (H-7a), 1.64 (H-7b), 1.41 (H-2''b), 1.32 (H-4'b), 1.36 (H-14b), 1.34 (6-CH3), 1.27 (5'-CH3), 1.25 (10-CH3), 1.23 (5''-CH3), 1.17 (3''-CH3), 1.15 (12-CH3), 1.11 (2-CH3), 1.07 (4-CH3), 1.46 (H-15), 0.89 (8-CH3).
1H ЯМР (300 МГц, CDCl3) δ: 7.63 (CONH), 5.05 (H-1''), 4.34 (H-1'), 4.22 (H-10), 4.25 (H-3), 4.06 (H-5''), 3.74 (H-11), 3.71 (H-5'), 3.48 (H-9a), 3.34 (H-2'), 3.70 (H-5), 3.28 (3''-ОCH3), 3.29 (H-9b), 3.14 (H-13), 2.93 (H-4''), 2.84 (H-3'), 2.50 (H-2), 2.32 (H-2''a), 2.28 /3'N(CH3)2/, 1.74 (H-8), 1.93 (H-4), 1.76 (H-4'a), 1.56 (H-14a), 1.74 (H-7a), 1.64 (H-7b), 1.41 (H-2''b), 1.32 (H-4'b), 1.36 (H-14b), 1.34 (6-CH3), 1.27 (5'-CH3), 1.25 (10-CH3), 1.23 (5''-CH3), 1.17 (3''-CH3), 1.15 (12-CH3), 1.11 (2-CH3), 1.07 (4-CH3), 1.46 (H-15), 0.89 (8-CH3).
13C ЯМР (75 МГц, CDCl3) δ: 173.6 (C-1), 107.3 (C-1'), 96.3 (C-1''), 91.2 (C-5), 84.5 (C-13), 78.9 (C-3), 75.5 (C-6), 75.1 (C-11), 74.8 (C-12), 70.5 (C-2'), 69.4 (C-9), 65.7 (C-5''), 63.4 (C-3'), 49.3 (3''-ОCH3), 49.7 (C-10), 46.7 (C-7), 41.9 (C-2), 39.3 /3'N(CH3)2/, 37.4 (C-4), 34.7 (C-2''), 32.0 (C-8), 27.8 (C-4'), 26.2 (6-CH3), 24.9 (C-14), 21.9 (12-CH3), 21.1 (3''-CH3), 20.7 (5'-CH3), 19.6 (8-CH3), 17.4 (5''-CH3), 16.7 (10-CH3), 11.4 (C-15), 10.1 (4-CH3), 8.1 (2-CH3).
ПРИМЕР 13. 2', 4''-O-Диацетил-1N-[2,4-O-диацетил-3-гидрокси-1,3-диметилгексил] амидо-10,11,12,13,14,15-гексанор-9-дезоксо-9-O-ацетил-8(R)-метил-9,10-секоэритромицин A (Io)
Вещество (Im) (0,70 г) из примера 12 растворяют в пиридине (10 мл), добавляют ангидрид уксусной кислоты (5 мл) и оставляют стоять в течение 2 суток при комнатной температуре. Реакционную смесь выливают на лед (50 мл) и экстрагируют с CHCl3 при pH 5 и pH 9. Сушка над K2CO3 и упаривание объединенных органических экстрактов при pH 9 дает сырой продукт (0,87 г), который суспендируют в петролейном эфире, перемешивают в течение 30 минут при 0-5oC, фильтруют и сушат в вакуумном сушильном шкафу при 50oC и получают хроматографически однородный, названный в заголовке продукт (Iо) (0,61 г).
Вещество (Im) (0,70 г) из примера 12 растворяют в пиридине (10 мл), добавляют ангидрид уксусной кислоты (5 мл) и оставляют стоять в течение 2 суток при комнатной температуре. Реакционную смесь выливают на лед (50 мл) и экстрагируют с CHCl3 при pH 5 и pH 9. Сушка над K2CO3 и упаривание объединенных органических экстрактов при pH 9 дает сырой продукт (0,87 г), который суспендируют в петролейном эфире, перемешивают в течение 30 минут при 0-5oC, фильтруют и сушат в вакуумном сушильном шкафу при 50oC и получают хроматографически однородный, названный в заголовке продукт (Iо) (0,61 г).
Rf 0,473, EtAc/(н-C6H6)/Et2NH, 100:100:20.
ИК (CHCl3), см-1: 3510, 3395, 2980, 2950, 1740, 1660, 1535, 1460, 1370, 1240, 1170, 1045.
1H ЯМР (300 МГц, CDCl3) δ: 6.53 (CONH), 4.94 (H-13), 4.84 (H-1''), 4.83 (H-2'), 4.66 (H-4''). 4.65 (H-1'), 4.57 (H-10), 4.36 (H-5''), 4.02 (H-3), 3.73 (H-5'), 3.47 (H-5), 3.33 (3''-ОCH3), 2.78 (H-3'), 2.53 (H-2), 2.40 (H-2''а), 2.27 /3'-N(CH3)/2, 2.14 (H-8), 2.13, 2.12, 2.07, 2.05 and 2.02 (CОCH3), 1.92 (H-4), 1.83 (H-14a), 1.73 (H-4'a), 1.56 (H-2''b), 1.50 (H-7a), 1.44 (H-14b), 1.36 (H-4'b), 1.28 (6-CH3), 1.26 (H-7b), 1.22 (5'-CH3), 1.20 (12-CH3), 1.15 (2-CH3), 1.13 (10-CH3), 1.11 (3''-CH3), 1.11 (5''-CH3), 1.02 (8-CH3), 0.98 (4-CH3), 0.89 (15-CH3).
Примечания: В приведенных выше спектрах ЯМР указанные ниже слова обозначают следующее:
and - и,
aryl - арил,
carbonate - карбонат.
and - и,
aryl - арил,
carbonate - карбонат.
Claims (21)
1. Секомакролиды класса эритромицинов общей формулы I
R1 - водород, (C1 - C4)алканоильная группа;
R2 - водород или R1 и R2 вместе с атомами углерода, с которыми они связаны, образуют циклическую карбонильную группу;
R3 - (C1 - C4)алканоильная группа или арилкарбонильная группа;
Z - водород или L-кладинозильная группа формулы i
где R4 - водород или (C1 - C4)алканоильная группа;
W - D-дезозаминильная группа формулы ii
где R5 - водород, (C1 - C4)алканоильная или арилкарбонильная группа;
X и Y вместе представляют лактон или X представляет CH2OR6 группу, где R6 представляет (C1 - C4)алканоил, а Y представляет гидроксил,
или их фармацевтически приемлемые соли присоединения неорганических или органических кислот.
R1 - водород, (C1 - C4)алканоильная группа;
R2 - водород или R1 и R2 вместе с атомами углерода, с которыми они связаны, образуют циклическую карбонильную группу;
R3 - (C1 - C4)алканоильная группа или арилкарбонильная группа;
Z - водород или L-кладинозильная группа формулы i
где R4 - водород или (C1 - C4)алканоильная группа;
W - D-дезозаминильная группа формулы ii
где R5 - водород, (C1 - C4)алканоильная или арилкарбонильная группа;
X и Y вместе представляют лактон или X представляет CH2OR6 группу, где R6 представляет (C1 - C4)алканоил, а Y представляет гидроксил,
или их фармацевтически приемлемые соли присоединения неорганических или органических кислот.
2. Соединение по п. 1, в котором R1, R2 и R3 являются одинаковыми и представляют водород, Z представляет водород или L-кладинозильную группу формулы (i), где R4 представляет водород, W представляет D-дезозаминильную группу формулы (ii), где R5 представляет водород и X и Y вместе представляют лактон.
3. Соединение по п.2, в котором Z представляет L-кладинозильную группу формулы i, где R4 представляет водород, а W представляет D-дезозаминильную группу формулы ii, где R5 представляет водород.
4. Соединение по п.2, в котором Z представляет водород, а W представляет D-дезозаминильную группу формулы ii, где R5 представляет водород.
5. Соединение по п.2, в котором Z представляет водород.
6. Соединение по п.1, в котором R1 и R3 являются одинаковыми и представляют (C1 - C4)алканоильную группу, R2 является водородом, Z представляет L-кладинозильную группу формулы i, где R4 представляет (C1 - C4)алканоильную группу, W представляет D-дезозаминильную группу формулы ii, где R5 представляет водород или (C1 - C4)алканоильную группу и X и Y вместе представляют лактон.
7. Соединение по п.6, в котором R1 и R3 являются одинаковыми и представляют ацетильную группу, R2 является водородом, Z представляет L-кладинозильную группу формулы i, где R4 представляет ацетильную группу, W представляет D-дезозаминильную группу формулы ii, где R5 представляет водород.
8. Соединение по п.6, в котором R1 и R3 являются одинаковыми и представляют ацетильную группу, R2 является водородом, Z представляет L-кладинозильную группу формулы i, где R4 представляет ацетильную группу, W представляет D-дезозаминильную группу формулы ii, где R5 представляет ацетильную группу.
9. Соединение по п.1, в котором R1 и R3 являются одинаковыми или различными и представляют водород, (C1 - C4)алканоильную группу, R2 является водородом, Z представляет L-кладинозильную группу формулы i, где R4 представляет водород или (C1 - C4)алканоильную группу, W представляет D-дезозаминильную группу формулы ii, где R5 представляет водород или арилокарбонильную группу и X и Y вместе представляют лактон.
10. Соединение по п. 9, в котором R1, R2 и R3 являются одинаковыми и представляют водород, Z представляет L-кладинозильную группу формулы i, где R4 представляет водород, W представляет D-дезозаминильную группу формулы ii, где R5 представляет 4-бромбензоильную группу.
11. Соединение по п.9, в котором R1 и R3 являются одинаковыми и представляют ацетильную группу, R2 представляет водород, Z представляет L-кладинозильную группу формулы i, где R4 представляет ацетильную группу, W представляет D-дезозаминильную группу формулы ii, где R5 представляет 4-бромбензоильную группу.
12. Соединение по п.9, в котором R2 и R3 являются одинаковыми и представляют водород, Z представляет L-кладинозильную группу формулы i, где R4 представляет водород, W представляет D-дезозаминильную группу формулы ii, где R5 представляет 4-бромбензоильную группу.
13. Соединение по п.9, в котором R2 и R3 являются одинаковыми и представляют водород, Z представляет L-кладинозильную группу формулы i, где R4 представляет водород, W представляет D-дезозаминильную группу формулы ii, где R5 представляет водород.
14. Соединение по п. 9, в котором R3 представляет 4-бромбензоильную группу, R1 и R2 являются одинаковыми и представляют водород, Z представляет L-кладинозильную группу формулы i, где R4 представляет водород, W представляет D-дезозаминильную группу формулы ii, где R5 представляет 4-бромбензоильную группу.
15. Соединение по п.9, в котором R3 представляет 4-бромбензоильную группу, R1 и R2 являются одинаковыми и представляют водород, Z представляет L-кладинозильную группу формулы i, где R4 представляет водород, W представляет D-дезозаминильную группу формулы ii, где R5 представляет водород.
16. Соединение по п.1, в котором R1 и R2 вместе с атомами углерода, с которыми они связаны, представляют циклическую карбонильную группу, R3 представляет водород, Z представляет L-кладинозильную группу формулы i, где R4 представляет водород, W представляет D-дезозаминильную группу формулы ii, где R5 представляет водород и X и Y вместе представляют лактон.
17. Соединение по п.16, в котором R1 и R2 вместе с атомами углерода, с которыми они связаны, представляют циклическую карбонильную группу и R3 представляет водород.
18. Соединение по п.1, в котором R1 и R3 являются одинаковыми и представляют водород, R2 представляет водород, Z представляет L-кладинозильную группу формулы i, где R4 представляет водород или (C1 - C4)алканоильную группу, W представляет D-дезозаминильную группу формулы ii, где R5 представляет водород или (C1 - C4)алканоильную группу, X представляет группу CH2OR6, где R6 представляет (C1 - C4)алканоильную группу и Y представляет гидроксильную группу.
19. Соединение по п. 18, в котором R1, R2 и R3 являются одинаковыми и представляют водород, Z представляет L-кладинозильную группу формулы i, где R4 представляет водород, W представляет D-дезозаминильную группу формулы ii, где R5 представляет водород, X представляет группу CH2OR6 и Y представляет гидроксильную группу.
20. Соединение по п.18, в котором R3 представляет ацетильную группу, R2 представляет водород, Z представляет L-кладинозильную группу формулы i, где R4 представляет ацетильную группу, W представляет D-дезозаминильную группу формулы ii, где R5 представляет ацетильную группу, X представляет группу CH2OR6, где R6 представляет ацетильную группу и Y представляет гидроксильную группу.
21. Способ получения соединения общей формулы I
где R1, R2, R3, R4, R5, X, Y, Z и W определены в п.1,
или его фармацевтически приемлемых солей присоединения неорганических или органических кислот, отличающийся тем, что 6-дезокси-6,9-эпокси-8(R)-метил-10-амино-9,10-секоэритромицин А общей формулы II
подвергают воздействию полярных растворителей, предпочтительно воды или смеси воды и ацетона, в течение времени, необходимого для того, чтобы посредством внутримолекулярного переацилирования образовалось соединение общей формулы I, где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, W является D-дезозаминильной группой формулы ii, где R5 представляет водород и X и Y вместе представляют лактоновую группу, которое далее, если требуется, подвергают
А) взаимодействию с разбавленными неорганическими кислотами, предпочтительно с 0,25N хлористоводородной кислотой, при комнатной температуре, с образованием соединения общей формулы I, где R1, R2 и R3 являются одинаковыми и представляют водород, Z является водородом, W является D-дезозаминильной группой формулы ii, где R5 представляет водород, X и Y вместе представляют лактон, или взаимодействию с более концентрированными кислотами, предпочтительно с 2N хлористоводородной кислотой, в присутствии инертного растворителя, предпочтительно хлороформа, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, с образованием соединения общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z представляет водород, и X и Y вместе представляют лактон, или
Б) О-ацилированию ангидридами или хлорангидридами карбоновых кислот с образованием Б1) при О-ацилировании ангидридами или хлорангидридами (C1 - C4)алкилкарбоновых кислот, предпочтительно ангидридом уксусной кислоты, в инертном для реакции растворителе, предпочтительно пиридине, при температуре 0 - 30oС, предпочтительно при комнатной температуре, соединения общей формулы I, где R1 и R3 являются одинаковыми и представляют (C1 - C4)алканоильные группы, и R2 представляет водород, Z является L-кладинозильной группой формулы i, где R4 представляет (C1 - C4)алканоильную группу, W является D-дезозаминильной группой формулы ii, где R5 представляет (C1 - C4)алканоильную группу, и X и Y вместе представляют лактон, которое затем, если требуется, подвергают реакции сольволиза в низших спиртах, предпочтительно в метаноле, при комнатной температуре в течение 3 дней, с образованием соединения общей формулы I, где R1 и R3 являются одинаковыми и представляют (C1 - C4)алканоильные группы, и R2 представляет водород, Z является L-кладинозильной группой формулы i, где R4 представляет (C1 - C4)алканоильную группу, W является D-дезозаминильной группой формулы ii, где R5 представляет водород, и X и Y вместе представляют лактон, или с образованием
Б2) при О-ацилировании хлорангидридами арилкарбоновых кислот, когда
Б2а) используют, по меньшей мере, 1,1 - эквимолярный избыток хлорангидрида кислоты, предпочтительно 4-бромбензоилхлорида, в сухом ацетоне при температуре 0 - 5oС соединения общей формулы I, где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, W является D-дезозаминильной группой формулы ii, где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, которое далее, если требуется, подвергают О-ацилированию в соответствии с Б1), с образованием соединения общей формулы I, где R1 и R3 являются одинаковыми и представляют (C1 - C4)алканоильные группы, и R2 представляет водород, Z является L-кладинозильной группой формулы i, где R4 представляет (C1 - C4)алканоильную группу, W является D-дезозаминильной группой формулы ii, где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, или
Б2б) используют, по меньшей мере, 5-эквимолярный избыток хлорангидрида кислоты, предпочтительно 4-бромбензоилхлорида, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, смеси соединений общей формулы I, где R1 представляет арилкарбонильную группу, а R2 и R3 являются одинаковыми и представляют водород, или где R3 представляет арилкарбонильную группу, а R1 и R2 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, а W является D-дезозаминильной группой формулы ii, где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, и эти соединения разделяют с помощью колоночной хроматографии на силикагеле, а затем, если требуется, подвергают реакции сольволиза, с образованием соединения общей формулы I, где R1, R2 и R3 являются одинаковыми и представляют водород, или где R3 представляет арилкарбонильную группу, а R1 и R2 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, а W является D-дезозаминильной группой формулы ii, где R5 представляет водород, и X и Y вместе представляют лактон, или
В) реакции переэтерификации с производными карбоновых кислот, предпочтительно с 3-5-эквимолярным избытком этиленкарбоната, в инертном растворителе, предпочтительно в бензоле, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, в течение 3 - 9 ч, с образованием соединения общей формулы I, где R1 и R2 вместе с атомами углерода, с которыми они связаны, представляют циклическую карбонильную группу, а R3 представляет водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, W является D-дезозаминильной группой формулы ii, где R5 представляет водород, и X и Y вместе представляют лактон, или
Г) восстановлению с металлогидридными комплексами, предпочтительно с борогидридом натрия, в присутствии третичных спиртов, предпочтительно трет-бутанола, в инертном растворителе, предпочтительно в метаноле, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, с образованием соединения общей формулы I, где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, W является D-дезозаминильной группой формулы ii, где R5 представляет водород, и X представляет группу CH2OR6, а Y представляет гидроксильную группу, которое далее, если требуется, подвергают О-ацилированию в соответствии с Б1), предпочтительно с ангидридом уксусной кислоты, с образованием соединения общей формулы I, где R1 и R3 являются одинаковыми и представляют (C1 - C4)алканоильные группы, R2 представляет водород, Z является L-кладинозильной группой формулы i, где R4 представляет (C1 - C4)алканоильную группу, W является D-дезозаминильной группой формулы ii, где R5 представляет (C1 - C4)алканоильную группу, X представляет группу CH2OR6, где R6 представляет (C1 - C4)алканоильную группу, и Y представляет гидроксильную группу,
и затем, если требуется, полученные секомакролиды подвергают взаимодействию с, по крайней мере, эквимолярным количеством соответствующей неорганической или органической кислоты в растворителе, инертном для реакции, с образованием соответствующих солей присоединения кислоты.
где R1, R2, R3, R4, R5, X, Y, Z и W определены в п.1,
или его фармацевтически приемлемых солей присоединения неорганических или органических кислот, отличающийся тем, что 6-дезокси-6,9-эпокси-8(R)-метил-10-амино-9,10-секоэритромицин А общей формулы II
подвергают воздействию полярных растворителей, предпочтительно воды или смеси воды и ацетона, в течение времени, необходимого для того, чтобы посредством внутримолекулярного переацилирования образовалось соединение общей формулы I, где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, W является D-дезозаминильной группой формулы ii, где R5 представляет водород и X и Y вместе представляют лактоновую группу, которое далее, если требуется, подвергают
А) взаимодействию с разбавленными неорганическими кислотами, предпочтительно с 0,25N хлористоводородной кислотой, при комнатной температуре, с образованием соединения общей формулы I, где R1, R2 и R3 являются одинаковыми и представляют водород, Z является водородом, W является D-дезозаминильной группой формулы ii, где R5 представляет водород, X и Y вместе представляют лактон, или взаимодействию с более концентрированными кислотами, предпочтительно с 2N хлористоводородной кислотой, в присутствии инертного растворителя, предпочтительно хлороформа, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, с образованием соединения общей формулы (I), где R1, R2 и R3 являются одинаковыми и представляют водород, Z представляет водород, и X и Y вместе представляют лактон, или
Б) О-ацилированию ангидридами или хлорангидридами карбоновых кислот с образованием Б1) при О-ацилировании ангидридами или хлорангидридами (C1 - C4)алкилкарбоновых кислот, предпочтительно ангидридом уксусной кислоты, в инертном для реакции растворителе, предпочтительно пиридине, при температуре 0 - 30oС, предпочтительно при комнатной температуре, соединения общей формулы I, где R1 и R3 являются одинаковыми и представляют (C1 - C4)алканоильные группы, и R2 представляет водород, Z является L-кладинозильной группой формулы i, где R4 представляет (C1 - C4)алканоильную группу, W является D-дезозаминильной группой формулы ii, где R5 представляет (C1 - C4)алканоильную группу, и X и Y вместе представляют лактон, которое затем, если требуется, подвергают реакции сольволиза в низших спиртах, предпочтительно в метаноле, при комнатной температуре в течение 3 дней, с образованием соединения общей формулы I, где R1 и R3 являются одинаковыми и представляют (C1 - C4)алканоильные группы, и R2 представляет водород, Z является L-кладинозильной группой формулы i, где R4 представляет (C1 - C4)алканоильную группу, W является D-дезозаминильной группой формулы ii, где R5 представляет водород, и X и Y вместе представляют лактон, или с образованием
Б2) при О-ацилировании хлорангидридами арилкарбоновых кислот, когда
Б2а) используют, по меньшей мере, 1,1 - эквимолярный избыток хлорангидрида кислоты, предпочтительно 4-бромбензоилхлорида, в сухом ацетоне при температуре 0 - 5oС соединения общей формулы I, где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, W является D-дезозаминильной группой формулы ii, где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, которое далее, если требуется, подвергают О-ацилированию в соответствии с Б1), с образованием соединения общей формулы I, где R1 и R3 являются одинаковыми и представляют (C1 - C4)алканоильные группы, и R2 представляет водород, Z является L-кладинозильной группой формулы i, где R4 представляет (C1 - C4)алканоильную группу, W является D-дезозаминильной группой формулы ii, где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, или
Б2б) используют, по меньшей мере, 5-эквимолярный избыток хлорангидрида кислоты, предпочтительно 4-бромбензоилхлорида, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, смеси соединений общей формулы I, где R1 представляет арилкарбонильную группу, а R2 и R3 являются одинаковыми и представляют водород, или где R3 представляет арилкарбонильную группу, а R1 и R2 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, а W является D-дезозаминильной группой формулы ii, где R5 представляет арилкарбонильную группу, и X и Y вместе представляют лактон, и эти соединения разделяют с помощью колоночной хроматографии на силикагеле, а затем, если требуется, подвергают реакции сольволиза, с образованием соединения общей формулы I, где R1, R2 и R3 являются одинаковыми и представляют водород, или где R3 представляет арилкарбонильную группу, а R1 и R2 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, а W является D-дезозаминильной группой формулы ii, где R5 представляет водород, и X и Y вместе представляют лактон, или
В) реакции переэтерификации с производными карбоновых кислот, предпочтительно с 3-5-эквимолярным избытком этиленкарбоната, в инертном растворителе, предпочтительно в бензоле, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, в течение 3 - 9 ч, с образованием соединения общей формулы I, где R1 и R2 вместе с атомами углерода, с которыми они связаны, представляют циклическую карбонильную группу, а R3 представляет водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, W является D-дезозаминильной группой формулы ii, где R5 представляет водород, и X и Y вместе представляют лактон, или
Г) восстановлению с металлогидридными комплексами, предпочтительно с борогидридом натрия, в присутствии третичных спиртов, предпочтительно трет-бутанола, в инертном растворителе, предпочтительно в метаноле, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, с образованием соединения общей формулы I, где R1, R2 и R3 являются одинаковыми и представляют водород, Z является L-кладинозильной группой формулы i, где R4 представляет водород, W является D-дезозаминильной группой формулы ii, где R5 представляет водород, и X представляет группу CH2OR6, а Y представляет гидроксильную группу, которое далее, если требуется, подвергают О-ацилированию в соответствии с Б1), предпочтительно с ангидридом уксусной кислоты, с образованием соединения общей формулы I, где R1 и R3 являются одинаковыми и представляют (C1 - C4)алканоильные группы, R2 представляет водород, Z является L-кладинозильной группой формулы i, где R4 представляет (C1 - C4)алканоильную группу, W является D-дезозаминильной группой формулы ii, где R5 представляет (C1 - C4)алканоильную группу, X представляет группу CH2OR6, где R6 представляет (C1 - C4)алканоильную группу, и Y представляет гидроксильную группу,
и затем, если требуется, полученные секомакролиды подвергают взаимодействию с, по крайней мере, эквимолярным количеством соответствующей неорганической или органической кислоты в растворителе, инертном для реакции, с образованием соответствующих солей присоединения кислоты.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CRP970141A | 1997-03-12 | ||
| HR970141A HRP970141A2 (en) | 1997-03-12 | 1997-03-12 | New secomacrolydes of erythromicin a, and a process for the preparation thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU98104446A RU98104446A (ru) | 2000-01-10 |
| RU2158268C2 true RU2158268C2 (ru) | 2000-10-27 |
Family
ID=10946552
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU98104446/04A RU2158268C2 (ru) | 1997-03-12 | 1998-03-11 | Секомакролиды класса эритромицинов и способ их получения |
Country Status (15)
| Country | Link |
|---|---|
| US (1) | US6077944A (ru) |
| EP (1) | EP0864581A1 (ru) |
| JP (1) | JPH10330393A (ru) |
| KR (1) | KR19980080182A (ru) |
| CN (1) | CN1066455C (ru) |
| AR (1) | AR015573A1 (ru) |
| BG (1) | BG62935B1 (ru) |
| CA (1) | CA2229111A1 (ru) |
| CZ (1) | CZ72098A3 (ru) |
| HR (1) | HRP970141A2 (ru) |
| HU (1) | HUP9800536A3 (ru) |
| NO (1) | NO981063L (ru) |
| PL (1) | PL325307A1 (ru) |
| RU (1) | RU2158268C2 (ru) |
| SK (1) | SK30398A3 (ru) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CZ211798A3 (cs) * | 1997-07-16 | 1999-02-17 | Pliva, Farmaceutska, Kemijska, Prehrambena I Kozmetička Industrije, Dioničko Društvo | Lineární 8a-sekoazalidy a způsob jejich výroby |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5210235A (en) * | 1992-08-26 | 1993-05-11 | Merck & Co., Inc. | Methods of elaborating erythromycin fragments into amine-containing fragments of azalide antibiotics |
| HRP950145A2 (en) * | 1995-03-27 | 1997-08-31 | Sour Pliva | New compounds of the secomacrolide and secoazalide class and a process for the preparation thereof |
-
1997
- 1997-03-12 HR HR970141A patent/HRP970141A2/hr not_active Application Discontinuation
-
1998
- 1998-03-06 EP EP98104062A patent/EP0864581A1/en not_active Withdrawn
- 1998-03-06 SK SK303-98A patent/SK30398A3/sk unknown
- 1998-03-10 CZ CZ98720A patent/CZ72098A3/cs unknown
- 1998-03-11 BG BG102315A patent/BG62935B1/bg unknown
- 1998-03-11 CA CA002229111A patent/CA2229111A1/en not_active Abandoned
- 1998-03-11 CN CN98108073A patent/CN1066455C/zh not_active Expired - Fee Related
- 1998-03-11 JP JP10059826A patent/JPH10330393A/ja active Pending
- 1998-03-11 AR ARP980101076A patent/AR015573A1/es not_active Application Discontinuation
- 1998-03-11 NO NO981063A patent/NO981063L/no not_active Application Discontinuation
- 1998-03-11 HU HU9800536A patent/HUP9800536A3/hu unknown
- 1998-03-11 RU RU98104446/04A patent/RU2158268C2/ru active
- 1998-03-12 KR KR1019980008293A patent/KR19980080182A/ko not_active Application Discontinuation
- 1998-03-12 PL PL98325307A patent/PL325307A1/xx unknown
- 1998-03-12 US US09/038,901 patent/US6077944A/en not_active Expired - Fee Related
Non-Patent Citations (1)
| Title |
|---|
| Ф.П.Тринус Фармако-терапевтический справочник. - Киев, "Здоровья", 1989, с.406. J.Amer. Chem. Soc. 1991, 113, 5478. March J. Advonced organic Chemistry, Reactions, Mechanisms and Structure. Third Ed., 1985, p.375. * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN1066455C (zh) | 2001-05-30 |
| KR19980080182A (ko) | 1998-11-25 |
| HUP9800536A3 (en) | 1999-01-28 |
| HUP9800536A2 (hu) | 1998-10-28 |
| JPH10330393A (ja) | 1998-12-15 |
| CN1197075A (zh) | 1998-10-28 |
| AR015573A1 (es) | 2001-05-16 |
| NO981063L (no) | 1998-09-14 |
| PL325307A1 (en) | 1998-09-14 |
| BG102315A (en) | 1999-08-31 |
| SK30398A3 (en) | 1998-11-04 |
| NO981063D0 (no) | 1998-03-11 |
| US6077944A (en) | 2000-06-20 |
| BG62935B1 (bg) | 2000-11-30 |
| CZ72098A3 (cs) | 1998-09-16 |
| CA2229111A1 (en) | 1998-09-12 |
| HRP970141A2 (en) | 1999-02-28 |
| HU9800536D0 (en) | 1998-04-28 |
| EP0864581A1 (en) | 1998-09-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BG64600B1 (bg) | Кетолиди от класа на 15-членни лактами с антибактериална активност | |
| DE69400817T2 (de) | 9a-N-(N'-Carbamoyl)-und 9a-N-(N'Thiocarbamoyl)-Derivate von 9-Deoxo-9a-aza-9a-homoerythromycin A | |
| HU193157B (en) | Process for preparing 4"-epi-erythromycin a and derivatives thereof | |
| US5434140A (en) | 9-deoxo-9a-aza-11-deoxy-9a-homoerythromycin a 9a,11-cyclic carbamates | |
| US4351937A (en) | N-Glycosyl derivatives of anthracycline antibiotics and the method of their preparation | |
| KR920000646B1 (ko) | 플루오로-치환 에피포도필로톡신 배당체 | |
| EP1181298B1 (en) | Novel 8a- and 9a-15-membered lactams | |
| RU2130936C1 (ru) | 9а-азалидные фрагменты макролидных антибиотиков класса азалидов, способ их получения и промежуточные соединения для их получения | |
| RU2158268C2 (ru) | Секомакролиды класса эритромицинов и способ их получения | |
| RU2234510C2 (ru) | Производные класса олеандомицина и способ их получения | |
| JP3063943B2 (ja) | 血漿中において抗菌活性の持続する新規16員環マクロリド誘導体及びその合成中間体とそれらの製造法 | |
| EA001733B1 (ru) | Производные эритромицина, способ их получения и применение | |
| HU180298B (en) | Process for preparing new glycoside compunds | |
| CZ20014362A3 (cs) | 4´-Demykarosyl-8a-aza-8a-homotylosiny a způsob jejich výroby | |
| Lazarevski et al. | Acid catalyzed ring opening reactions of 6-deoxy-9-deoxo-9a-aza-9a-homoerythromycin A 6, 9-cyclic imino ether | |
| Roy et al. | Synthesis of (R)-4, 6-O-pyruvated trisaccharide related to the repeating unit of the antigen from Shigella dysenteriae type 9 in the form of its 2-(trimethylsilyl) ethyl glycoside | |
| HUT74073A (en) | New compounds of the secomacrolide and secoazalide class and a process for the preparation thereof |