RU2015137C1 - Способ получения 3-нитросалицилового альдегида - Google Patents
Способ получения 3-нитросалицилового альдегида Download PDFInfo
- Publication number
- RU2015137C1 RU2015137C1 SU4836049A RU2015137C1 RU 2015137 C1 RU2015137 C1 RU 2015137C1 SU 4836049 A SU4836049 A SU 4836049A RU 2015137 C1 RU2015137 C1 RU 2015137C1
- Authority
- RU
- Russia
- Prior art keywords
- aldehyde
- nitrosalicylic
- target product
- mol
- pri
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 11
- 230000015572 biosynthetic process Effects 0.000 title abstract description 4
- 238000003786 synthesis reaction Methods 0.000 title abstract 2
- 125000002485 formyl group Chemical class [H]C(*)=O 0.000 title 1
- LPXPTNMVRIOKMN-UHFFFAOYSA-M sodium nitrite Chemical compound [Na+].[O-]N=O LPXPTNMVRIOKMN-UHFFFAOYSA-M 0.000 claims abstract description 18
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 claims abstract description 15
- 150000001299 aldehydes Chemical class 0.000 claims abstract description 13
- SMQUZDBALVYZAC-UHFFFAOYSA-N salicylaldehyde Chemical compound OC1=CC=CC=C1C=O SMQUZDBALVYZAC-UHFFFAOYSA-N 0.000 claims abstract description 8
- 230000003647 oxidation Effects 0.000 claims abstract description 3
- 238000007254 oxidation reaction Methods 0.000 claims abstract description 3
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 claims description 12
- 235000010288 sodium nitrite Nutrition 0.000 claims description 7
- 229960000583 acetic acid Drugs 0.000 claims description 4
- 150000004699 copper complex Chemical class 0.000 claims description 4
- 238000006396 nitration reaction Methods 0.000 claims description 4
- OPQARKPSCNTWTJ-UHFFFAOYSA-L copper(ii) acetate Chemical compound [Cu+2].CC([O-])=O.CC([O-])=O OPQARKPSCNTWTJ-UHFFFAOYSA-L 0.000 claims description 3
- NWFNSTOSIVLCJA-UHFFFAOYSA-L copper;diacetate;hydrate Chemical compound O.[Cu+2].CC([O-])=O.CC([O-])=O NWFNSTOSIVLCJA-UHFFFAOYSA-L 0.000 claims description 3
- 239000012362 glacial acetic acid Substances 0.000 claims description 3
- 230000002378 acidificating effect Effects 0.000 claims 1
- 238000006243 chemical reaction Methods 0.000 abstract description 3
- 239000003153 chemical reaction reagent Substances 0.000 abstract 2
- 239000000126 substance Substances 0.000 abstract 1
- 239000000047 product Substances 0.000 description 14
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 238000003756 stirring Methods 0.000 description 5
- 239000010949 copper Substances 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 229910017604 nitric acid Inorganic materials 0.000 description 2
- ZYECOAILUNWEAL-NUDFZHEQSA-N (4z)-4-[[2-methoxy-5-(phenylcarbamoyl)phenyl]hydrazinylidene]-n-(3-nitrophenyl)-3-oxonaphthalene-2-carboxamide Chemical compound COC1=CC=C(C(=O)NC=2C=CC=CC=2)C=C1N\N=C(C1=CC=CC=C1C=1)/C(=O)C=1C(=O)NC1=CC=CC([N+]([O-])=O)=C1 ZYECOAILUNWEAL-NUDFZHEQSA-N 0.000 description 1
- IQUPABOKLQSFBK-UHFFFAOYSA-N 2-nitrophenol Chemical compound OC1=CC=CC=C1[N+]([O-])=O IQUPABOKLQSFBK-UHFFFAOYSA-N 0.000 description 1
- YTHJCZRFJGXPTL-UHFFFAOYSA-N 4-hydroxy-3-nitrobenzaldehyde Chemical compound OC1=CC=C(C=O)C=C1[N+]([O-])=O YTHJCZRFJGXPTL-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 1
- 125000003172 aldehyde group Chemical group 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- -1 aromatic nitro compounds Chemical class 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 238000001256 steam distillation Methods 0.000 description 1
- 238000002211 ultraviolet spectrum Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Landscapes
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Использование: в качестве полупродукта для получения регенерируемых кислородоносителей, используемых в аэрокосмических объектах. Сущность изобретения: продукт - 3-нитросалициловый альдегид, т.пл. 109°С, выход 75%. Реагент 1: салициловый альдегид. Реагент 2: NaNO2 . Условия реакции: в среде CH3COOH и ледяной CH3COOH в присутствии Cu(OCOCH3)2·H2O при молярном соотношении салициловый альдегид: Cu(OCOCH3)2·H2O:NaNO2:CH3COOH , равном 1 : (0,5 - 0,6) : (2 - 2,5) : (4 - 5), при 10 - 15°С с последующим окислением промежуточного медного комплекса 3-нитрозосалицилового альдегида.
Description
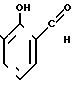
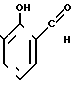
Изобретение относится к области химии ароматических нитросоединений, а именно к усовершенствованному способу получения 3-нитросалицилового альдегида формулы
который используется в качестве полупродукта для получения регенерируемых кислородоносителей, используемых в аэрокосмических объектах.
который используется в качестве полупродукта для получения регенерируемых кислородоносителей, используемых в аэрокосмических объектах.
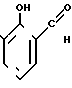
Известен метод прямого введения альдегидной группы в молекулу о-нитрофенола путем формирования исходной молекулы хлороформом в водной натриевой щелочи по схеме [1]:
+ CHCl3 +
Недостатком этого метода является низкий выход целевого продукта (11%) и образование второго изомера 3-нитро-4-оксибензальдегида. Другой известный способ заключается в прямом нитровании салицилового альдегида азотной кислотой, однако наряду с 5-нитросалициловым альдегидом образуется и 3-нитросалициловый альдегид [2].
+ CHCl3 +
Недостатком этого метода является низкий выход целевого продукта (11%) и образование второго изомера 3-нитро-4-оксибензальдегида. Другой известный способ заключается в прямом нитровании салицилового альдегида азотной кислотой, однако наряду с 5-нитросалициловым альдегидом образуется и 3-нитросалициловый альдегид [2].
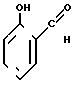
Наиболее близким к предлагаемому является способ прямого нитрования салицилового альдегида азотной кислотой (d = 1,5) [3].
+ HNO3 +
При этом получается 27,7% 5-нитросалицилового альдегида и 14,6 - 16,8% целевого 3-нитросалицилового альдегида. Основными недостатками данного метода являются селективность процесса, приводящая к образованию двух изомеров с низким содержанием целевого продукта, длительное (24 дня) и трудоемкое разделение и очистка образующихся изомеров через их натриевые соли.
При этом получается 27,7% 5-нитросалицилового альдегида и 14,6 - 16,8% целевого 3-нитросалицилового альдегида. Основными недостатками данного метода являются селективность процесса, приводящая к образованию двух изомеров с низким содержанием целевого продукта, длительное (24 дня) и трудоемкое разделение и очистка образующихся изомеров через их натриевые соли.
Целью изобретения является повышение выхода целевого продукта.
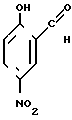
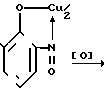
Поставленная цель достигается тем, что салициловый альдегид обрабатывают нитритом натрия в среде трифторуксусной и ледяной уксусной кислот в присутствии моногидрата ацетата меди при молярном соотношении салициловый альдегид - моногидрат ацетата меди - нитрит натрия - трифторуксусная кислота, равном 1:(0,5-0,6):(2-2,5):(4-5), при 10-15оС с последующим окислением промежуточного медного комплекса 3-нитрозосалицилового альдегида по схеме:
+ NaNO2
П р и м е р 1. При комнатной температуре и перемешивании готовят раствор 10 г (0,05 моль) моногидрата ацетата меди в 30 мл (0,4 моль) трифторуксусной кислоты. Полученный раствор разбавляют 50 мл ледяной уксусной кислоты и в полученной смеси растворяют при перемешивании 12,2 г (0,1 моль) салицилового альдегида. В полученный раствор при 10-15оС и перемешивании 13,8 г (0,2 моль) нитрита натрия в течение 3 ч. После выдержки в течение 8 ч реакционную массу выливают в 0,5 л воды, содержащей 3 г мочевины, отделяют конечный продукт фильтрованием и промывают 0,2 л воды. Полученные желтые кристаллы подвергают очистке перегонкой с водяным паром. Получено 12,7 г (75%) 3-нитросалицилового альдегида с температурой плавления 109оС.
+ NaNO2
П р и м е р 1. При комнатной температуре и перемешивании готовят раствор 10 г (0,05 моль) моногидрата ацетата меди в 30 мл (0,4 моль) трифторуксусной кислоты. Полученный раствор разбавляют 50 мл ледяной уксусной кислоты и в полученной смеси растворяют при перемешивании 12,2 г (0,1 моль) салицилового альдегида. В полученный раствор при 10-15оС и перемешивании 13,8 г (0,2 моль) нитрита натрия в течение 3 ч. После выдержки в течение 8 ч реакционную массу выливают в 0,5 л воды, содержащей 3 г мочевины, отделяют конечный продукт фильтрованием и промывают 0,2 л воды. Полученные желтые кристаллы подвергают очистке перегонкой с водяным паром. Получено 12,7 г (75%) 3-нитросалицилового альдегида с температурой плавления 109оС.
П р и м е р 2. Аналогично примеру 1, при растворении 8 г (0,04 моль) ацетата меди получают 7,8 г (47%) целевого продукта.
П р и м е р 3. Аналогично примеру 1, при растворении 12 г (0,06 моль) ацетата меди получают 12,7 (75%) целевого продукта.
П р и м е р 4. Аналогично примеру 1, при использовании 22,3 мл (0,3 моль) трифторуксусной кислоты получают 9 г (54%) целевого продукта.
П р и м е р 5. Аналогично примеру 1, при использовании 37,1 мл (0,5 моль) трифторуксусной кислоты получают 12,7 г (75%) целевого продукта.
П р и м е р 6. Аналогично примеру 1, при добавлении 10,35 г (0,15 моль) нитрита натрия получают 7 г (42%) целевого продукта.
П р и м е р 7. Аналогично примеру 1, при добавлении 17,25 г (0,25 моль) нитрита натрия получают 12,7 г (75%) целевого продукта.
П р и м е р 8. Аналогично примеру 1, при 20оС получают 10,8 г (65%) целевого продукта.
П р и м е р 9. Аналогично примеру 1, при 5оС получают 12,5 г (74%) целевого продукта.
П р и м е р 10. Аналогично примеру 1, после добавления 6,9 г (0,1 моль) нитрита натрия в течение 1,5 ч при перемешивании и выдержке в течение 1 ч при комнатной температуре реакционную массу выливают в 0,5 л воды. Выпавшие кристаллы красно-фиолетового цвета отделяют фильтрованием и промывают 0,5 л холодной воды. После высушивания на воздухе и промывки 0,15 л этанола получают 13,1 г (72%) медного комплекса 3-нитрозосалицилового альдегида с т.пл. 246оС с разложением.
Найдено,%: С 46,02; 45,91; Н 2,38; 2,24; N 7,44; 7,53; Cu 17,26; 17,34.
С14Н8N2O6Cu.
Вычислено,% C 46,15; Н 2,20; N 7,69; Cu 17,58.
УФ-спектры в воде λ1 = 338 нм lg ε1 = =3,53; λ2= 422 нм lgε2 = 3,09 λ3= 529 нм lg ε3= 317.
П р и м е р 11. Готовят раствор 18,2 г (0,05 моль) медного комплекса 3-нитрозосалицилового альдегида в смеси 100 мл уксусной кислоты и 20 мл концентрированной соляной кислоты. В полученный раствор вносят при 40-45оС и перемешивании 50 мл (0,5 моль) 34% перекиси водорода в течение 1,5 ч. После нагревания при 70-75оС в течение 2 ч реакционную массу разбавляют 150 мл воды и перегоняют с паром. Получают 11 г (90%) 3-нитросалицилового альдегида с т.пл. 109оС
П р и м е р 12. Аналогично примеру 11 без добавления перекиси водорода при выдержке реакционной массы в течение 8 ч. при 70-75оС получают 11 г (90%) целевого продукта.
П р и м е р 12. Аналогично примеру 11 без добавления перекиси водорода при выдержке реакционной массы в течение 8 ч. при 70-75оС получают 11 г (90%) целевого продукта.
П р им е р 13. Аналогично примеру 11 без добавления перекиси водорода при выдержке реакционной массы в течение 8 ч при комнатной температуре получают 11 г (90%) целевого продукта.
Таким образом, используя предложенный метод удается значительно повысить выход целевого продукта по сравнению с прототипом.
Claims (1)
- СПОСОБ ПОЛУЧЕНИЯ 3-НИТРОСАЛИЦИЛОВОГО АЛЬДЕГИДА путем нитрования салицилового альдегида в кислой среде, отличающийся тем, что, с целью повышения выхода целевого продукта, процесс нитрования проводят обработкой нитритом натрия в среде трифторуксусной и ледяной уксусной кислот в присутствии моногидрата ацетата меди при молярном соотношении салициловый альдегид: моногидрат ацетата меди : нитрит натрия : трифторуксусная кислота, равном 1 : (0,5 - 0,6) : (2 - 2,5) : (4 - 5) при 10 - 15oС с последующим окислением промежуточного медного комплекса 3-нитрозосалицилового альдегида.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| SU4836049 RU2015137C1 (ru) | 1990-06-07 | 1990-06-07 | Способ получения 3-нитросалицилового альдегида |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| SU4836049 RU2015137C1 (ru) | 1990-06-07 | 1990-06-07 | Способ получения 3-нитросалицилового альдегида |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2015137C1 true RU2015137C1 (ru) | 1994-06-30 |
Family
ID=21519179
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| SU4836049 RU2015137C1 (ru) | 1990-06-07 | 1990-06-07 | Способ получения 3-нитросалицилового альдегида |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2015137C1 (ru) |
-
1990
- 1990-06-07 RU SU4836049 patent/RU2015137C1/ru active
Non-Patent Citations (3)
| Title |
|---|
| 1. J. Indian. chem. Soc., 9, 173(1932). * |
| 2. Chem. Ber., 20, 1927,(1887). * |
| 3. Методы получения химических реактивов и препаратов. М.: Химия, 1966, вып.15, с.111. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR0123935B1 (ko) | 에리트로마이신 a옥심 또는 그의 염의 제조방법 | |
| RU2036918C1 (ru) | Способ получения чистых изофлановых производных | |
| US4579683A (en) | 5-Cyano-10-isonitroso-10,11-dihydro-5H-dibenz[b,f]azepine | |
| KR101342086B1 (ko) | 엘-바이옵테린의 제조방법 | |
| CS257292B2 (en) | Production method of amikacine | |
| RU2015137C1 (ru) | Способ получения 3-нитросалицилового альдегида | |
| US4743704A (en) | Esters of salsalate with guaiacol, for treating phlogistic bronchopneumopathies | |
| JP2021195344A (ja) | 5−ブロモ−2−ハロゲン化安息香酸の製造方法 | |
| US3953512A (en) | Process for manufacturing 2-aminobutanol | |
| RU2009121C1 (ru) | Способ получения 2-метил-6-нитрофенола | |
| WO2003104194A1 (fr) | Procede de preparation de 1,3,5-triaminobenzene et son hydrolyse en phloroglucinol de haute purete | |
| CN110407846B (zh) | 一种5-单硝酸异山梨酯的制备方法 | |
| RU2181719C2 (ru) | N-нитрооксазолидины-1,3 и способ их получения | |
| US7476760B2 (en) | Purification and production methods of 1-aminocyclopropanecarboxylic acid | |
| SU1731770A1 (ru) | Способ получени 3,3,5,5-тетраметилбензидина | |
| RU2069656C1 (ru) | Способ получения 4-нитро-1,3-диаминобензола | |
| RU2817042C1 (ru) | Способ синтеза промежуточного соединения для получения ингибитора натрий-зависимого котранспортера глюкозы (sglt) | |
| RU2024482C1 (ru) | Способ получения 3-бром-4-гидроксибензальдегида | |
| SU915423A1 (ru) | Способ получения 1-аминотетразола1 | |
| SU1456404A1 (ru) | Способ получени 2-нитрозо-1-нафтола | |
| KR101170192B1 (ko) | 1,2-벤즈이속사졸-3-메탄술폰아미드의 원-포트 제조방법 | |
| KR100228919B1 (ko) | 벤조페논유도체의 제조방법 | |
| SU1504235A1 (ru) | Способ получени 5-фенилэтинилфурфурола | |
| US1280119A (en) | Arsenical compound. | |
| CN117658866A (zh) | 一种叠氮氨基酸衍生物的合成方法 |