KR20220004703A - Cd8 조작된 t 세포 요법을 사용한 암의 치료를 위한 조성물 및 방법 - Google Patents
Cd8 조작된 t 세포 요법을 사용한 암의 치료를 위한 조성물 및 방법 Download PDFInfo
- Publication number
- KR20220004703A KR20220004703A KR1020217038746A KR20217038746A KR20220004703A KR 20220004703 A KR20220004703 A KR 20220004703A KR 1020217038746 A KR1020217038746 A KR 1020217038746A KR 20217038746 A KR20217038746 A KR 20217038746A KR 20220004703 A KR20220004703 A KR 20220004703A
- Authority
- KR
- South Korea
- Prior art keywords
- cd8α
- cell
- seq
- domain
- cd8β
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/7051—T-cell receptor (TcR)-CD3 complex
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/17—Lymphocytes; B-cells; T-cells; Natural killer cells; Interferon-activated or cytokine-activated lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/10—Cellular immunotherapy characterised by the cell type used
- A61K40/11—T-cells, e.g. tumour infiltrating lymphocytes [TIL] or regulatory T [Treg] cells; Lymphokine-activated killer [LAK] cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/30—Cellular immunotherapy characterised by the recombinant expression of specific molecules in the cells of the immune system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/30—Cellular immunotherapy characterised by the recombinant expression of specific molecules in the cells of the immune system
- A61K40/32—T-cell receptors [TCR]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/40—Cellular immunotherapy characterised by antigens that are targeted or presented by cells of the immune system
- A61K40/41—Vertebrate antigens
- A61K40/42—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/40—Cellular immunotherapy characterised by antigens that are targeted or presented by cells of the immune system
- A61K40/41—Vertebrate antigens
- A61K40/42—Cancer antigens
- A61K40/4201—Neoantigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
- C07K14/61—Growth hormone [GH], i.e. somatotropin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/70514—CD4
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/70517—CD8
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1137—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/87—Introduction of foreign genetic material using processes not otherwise provided for, e.g. co-transformation
- C12N15/90—Stable introduction of foreign DNA into chromosome
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/87—Introduction of foreign genetic material using processes not otherwise provided for, e.g. co-transformation
- C12N15/90—Stable introduction of foreign DNA into chromosome
- C12N15/902—Stable introduction of foreign DNA into chromosome using homologous recombination
- C12N15/907—Stable introduction of foreign DNA into chromosome using homologous recombination in mammalian cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/0004—Oxidoreductases (1.)
- C12N9/0071—Oxidoreductases (1.) acting on paired donors with incorporation of molecular oxygen (1.14)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/16—Hydrolases (3) acting on ester bonds (3.1)
- C12N9/22—Ribonucleases [RNase]; Deoxyribonucleases [DNase]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/02—Fusion polypeptide containing a localisation/targetting motif containing a signal sequence
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/50—Fusion polypeptide containing protease site
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/20—Type of nucleic acid involving clustered regularly interspaced short palindromic repeats [CRISPR]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2302—Interleukin-2 (IL-2)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2307—Interleukin-7 (IL-7)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2315—Interleukin-15 (IL-15)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Genetics & Genomics (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Biomedical Technology (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- General Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Cell Biology (AREA)
- Microbiology (AREA)
- Epidemiology (AREA)
- Medicinal Chemistry (AREA)
- Biophysics (AREA)
- Plant Pathology (AREA)
- Physics & Mathematics (AREA)
- Hematology (AREA)
- Virology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Toxicology (AREA)
- Pharmacology & Pharmacy (AREA)
- Mycology (AREA)
- Developmental Biology & Embryology (AREA)
- Endocrinology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Peptides Or Proteins (AREA)
Abstract
본 발명은 CD8 발현 구축물로의 네오TCR 기반 세포 요법을 포함하는 조성물 및 이를 사용한 암의 치료 방법에 관한 것이다. 특정 실시양태에서, 본 개시된 대상은 외인성 T 세포 수용체 (TCR), 및 외인성 CD8을 포함하는 세포를 제공한다. 특정 실시양태에서, 외인성 CD8은 적어도 1종의 단량체를 포함한다. 특정 실시양태에서, 외인성 CD8의 적어도 1종의 단량체는 세포외 도메인, 막횡단 도메인, 세포내 도메인, 그의 단편, 또는 이들의 조합을 포함한다.
Description
관련 출원에 대한 상호 참조
본 출원은 2019년 5월 1일에 출원된 미국 가출원 번호 62/841,748, 및 2019년 5월 1일에 출원된 미국 가출원 번호 62/841,753에 대해 우선권을 주장하며, 이들의 내용은 그 전문이 포함되고, 그에 대한 우선권이 주장된다.
서열 목록
본 출원은 ASCII 형식으로 전자적으로 제출되었고, 그 전문이 본원에 참조로 포함되는 서열 목록을 함유한다. 2020년 4월 30일에 생성된 상기 ASCII 사본은 087520_0145_SL.txt로 명명되고, 120,294 바이트의 크기이다.
T 세포의 활성화는 T 세포 수용체 (TCR) 및 그의 공수용체 분자를 통한 신호전달을 요구한다. CD4 및 CD8은 펩티드-주요 조직적합성 (pMHC) 리간드 및 TCR 사이의 상호작용을 안정화시킴으로써 TCR 신호전달을 증진시키는 공수용체로서 역할을 하는 T 헬퍼 세포 및 세포독성 T 림프구 상에 발현되는 막 단백질이다 (Li QJ, et al. (2004) CD4 enhances T cell sensitivity to antigen by coordinating Lck accumulation at the immunological synapse. Nat Immunol 5:791-799; Holler PD, Kranz DM (2003) Quantitative analysis of the contribution of TCR/pepMHC affinity and CD8 to T cell activation. Immunity 18:255-264). 구체적으로, CD4 및 CD8 공수용체는 신호전달의 개시에 필수적인데, 이는 이들이 TCR-pMHC 복합체에 대한 키나제의 동원을 용이하게 하기 때문이다. 더욱이, 연구는 CD4 및 CD8 공수용체가 둘 다 그의 리간드에 대한 T 세포 민감도를 증강시키지만, 단지 CD8만이 TCR-pMHC 상호작용의 안정화에 있어서 역할을 함을 보였다.
더욱이, 천연 발생 MHC-I TCR은 공동 CD8 공-수용체가 펩티드-MHC 결합을 안정화시키는 것을 도울 것이 요구되는 것으로 추정되지만, 보다 높은 친화도 TCR은 CD8-비의존성 표적 결합 및 T 세포 활성화를 유도한다. 따라서, CD4 T 세포는, 고 친화도 네오TCR(NeoTCR)로 조작되는 경우, 펩티드-MHC-I 표적을 인식하고 이펙터 T 세포 기능을 촉발시킬 수 있다. 그러나, 보다 낮은 친화도 TCR은 T 세포 활성화를 촉발시키기 위해 CD8 공-수용체에 의존한다.
따라서, CD8 공-수용체 발현을 갖도록 조작된 네오TCR 세포 요법은 TCR-pMHC 상호작용을 안정화시키고, 이러한 CD8 공-수용체에 의존하는 저 친화도 TCR을 포함하는 네오TCR 세포 요법의 효능을 증가시킬 수 있다.
특정 실시양태에서, 본 개시된 대상은 외인성 T 세포 수용체 (TCR), 및 외인성 CD8을 포함하는 세포를 제공한다. 특정 실시양태에서, 외인성 CD8은 적어도 1종의 단량체를 포함한다. 특정 실시양태에서, 외인성 CD8의 적어도 1종의 단량체는 세포외 도메인, 막횡단 도메인, 세포내 도메인, 그의 단편, 또는 이들의 조합을 포함한다. 특정 실시양태에서, 세포외 도메인은 CD8α 세포외 도메인 또는 CD8β 세포외 도메인을 포함한다. 특정 실시양태에서, 막횡단 도메인은 CD8α 막횡단 도메인 또는 CD8β 막횡단 도메인을 포함한다. 특정 실시양태에서, 세포내 도메인은 CD8α 세포내 도메인 또는 CD8β 세포내 도메인을 포함한다. 특정 실시양태에서, 세포내 도메인은 CD4 세포내 도메인을 포함한다.
특정 실시양태에서, 적어도 1종의 단량체는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인을 포함한다. 특정 실시양태에서, 적어도 1종의 단량체는 CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인을 포함한다. 특정 실시양태에서, 적어도 1종의 단량체는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인을 포함한다. 특정 실시양태에서, 적어도 1종의 단량체는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함한다. 특정 실시양태에서, 적어도 1종의 단량체는 신호 펩티드를 포함한다. 특정 실시양태에서, 신호 펩티드는 CD8 신호 펩티드이다.
특정 실시양태에서, 세포외 도메인은 서열식별번호(SEQ ID NO): 140, 또는 서열식별번호: 145에 제시된 아미노산 서열을 포함한다. 특정 실시양태에서, 막횡단 도메인은 서열식별번호: 141, 또는 서열식별번호: 146에 제시된 아미노산 서열을 포함한다. 특정 실시양태에서, 세포내 도메인은 서열식별번호: 142, 서열식별번호: 147, 또는 서열식별번호: 148에 제시된 아미노산 서열을 포함한다. 특정 실시양태에서, 신호 펩티드는 서열식별번호: 139, 또는 서열식별번호: 144에 제시된 아미노산 서열을 포함한다.
특정 실시양태에서, 외인성 CD8은 2A 서열을 포함한다. 특정 실시양태에서, 외인성 CD8은 링커를 포함한다. 특정 실시양태에서, 링커는 서열식별번호: 137에 제시된 아미노산 서열을 포함한다. 특정 실시양태에서, 외인성 CD8은 프로테아제 절단 부위를 포함한다. 특정 실시양태에서, 프로테아제 절단 부위는 푸린 절단 부위이다.
특정 실시양태에서, 외인성 TCR은 환자 유래 TCR이다. 특정 실시양태에서, 외인성 TCR은 신호 서열, 제1 및 제2 2A 서열, 및 TCR 폴리펩티드 서열을 포함한다. 특정 실시양태에서, 외인성 TCR은 암 항원을 인식한다. 특정 실시양태에서, 암 항원은 신생항원이다. 특정 실시양태에서, 암 항원은 환자 특이적 항원이다.
특정 실시양태에서, 세포는 1차 세포이다. 특정 실시양태에서, 세포는 환자-유래 세포이다. 특정 실시양태에서, 세포는 림프구이다. 특정 실시양태에서, 세포는 T 세포이다. 특정 실시양태에서, 세포는 어린 T 세포이다. 특정 실시양태에서, 세포는 CD45RA+, CD62L+, CD28+, CD95-, CCR7+, 및 CD27+이다. 특정 실시양태에서, 세포는 CD45RA+, CD62L+, CD28+, CD95+, CD27+, CCR7+이다. 특정 실시양태에서, 세포는 CD45RO+, CD62L+, CD28+, CD95+, CCR7+, CD27+, CD127+이다.
특정 실시양태에서, 세포는 세포 존속을 증진시키고/거나 기억 세포 분화를 증진시키는 유전자 변형을 추가로 포함한다. 특정 실시양태에서, 세포의 살해 활성은 외인성 CD8을 갖지 않는 세포의 살해 활성과 비교하여 약 10% 내지 약 500% 증가된다. 특정 실시양태에서, 항원에의 TCR의 결합 시 세포의 증식은 외인성 CD8을 갖지 않는 세포의 증식과 비교하여 약 10% 내지 약 500% 증가된다. 특정 실시양태에서, 세포에 의한 항원에의 TCR의 결합 시 전염증성 시토카인의 분비는 외인성 CD8을 갖지 않는 세포에 의한 분비와 비교하여 약 10% 내지 약 500% 증가된다. 특정 실시양태에서, 세포의 LCK 친화도는 외인성 CD8을 갖지 않는 세포의 LCK 친화도와 비교하여 약 10% 내지 약 500% 증가된다. 특정 실시양태에서, 세포의 존속은 외인성 CD8을 갖지 않는 세포의 존속과 비교하여 약 10% 내지 약 500% 증가된다. 특정 실시양태에서, 세포의 종양 침윤 능력은 외인성 CD8을 갖지 않는 세포의 종양 침윤 능력과 비교하여 약 10% 내지 약 500% 증가된다.
특정 실시양태에서, 외인성 TCR은 CD8-의존성 TCR이다. 특정 실시양태에서, 외인성 TCR은 CD8-비의존성 TCR이다. 특정 실시양태에서, 외인성 CD8은 CD8 구축물 1, CD8 구축물 2, CD8 구축물 3, 또는 CD8 구축물 4에 의해 코딩된다. 특정 실시양태에서, 외인성 CD8은 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함한다. 특정 실시양태에서, 외인성 CD8은 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함한다.
특정 실시양태에서, 본 개시된 대상은 세포 내로 상동성 재조합 (HR) 주형 핵산 서열을 도입하며, 여기서 HR 주형은 제1 및 제2 표적 핵산 서열에 대해 상동성인 제1 및 제2 상동성 아암, 제1 및 제2 상동성 아암 사이에 위치한 TCR 유전자 서열, 제1 및 제2 상동성 아암 사이에 위치한 CD8 유전자 서열을 포함하는 것인 단계, 및 HR 주형 핵산을 세포의 내인성 로커스 내로 재조합하는 단계를 포함하는, 세포를 변형시키는 방법을 제공한다. 특정 실시양태에서, HR 주형은 CD8 유전자 서열의 상류에 위치한 제1 2A-코딩 서열, CD8 유전자 서열의 하류 및 TCR 유전자 서열의 상류에 위치한 제2 2A-코딩 서열, 및 TCR 유전자 서열의 하류에 위치한 제3 2A-코딩 서열을 포함하며; 여기서 제1, 제2, 및 제3 2A-코딩 서열은 동일한 아미노산 서열을 코딩하고, 서로에 대해 코돈-분기된다. 특정 실시양태에서, HR 주형은 제1, 제2, 및/또는 제3 2A-코딩 서열의 바로 상류에 위치한 아미노산 서열 Gly Ser Gly를 코딩하는 서열을 포함한다. 특정 실시양태에서, HR 주형은 제1, 제2, 및/또는 제3 2A-코딩 서열의 상류에 위치한 푸린 절단 부위를 코딩하는 서열을 추가로 포함한다. 특정 실시양태에서, HR 주형은 TCR 유전자 서열 및/또는 CD8 유전자 서열의 바로 상류에 위치한 신호 서열을 코딩하는 서열을 추가로 포함한다.
특정 실시양태에서, HR 주형은 제3 2A-코딩 서열 및 제2 상동성 아암 사이에 위치한 제2 TCR 서열을 포함한다. 특정 실시양태에서, HR 주형은 제1 TCR 유전자 서열의 바로 상류에 위치한 제1 신호 서열을 코딩하는 서열, 및 제2 TCR 유전자 서열의 바로 상류에 위치한 제2 신호 서열을 코딩하는 서열을 포함한다. 특정 실시양태에서, HR 주형은 제1 CD8 유전자 서열 및 제2 2A-코딩 서열 사이에 위치한 제2 CD8 유전자 서열을 포함한다. 특정 실시양태에서, 2A 코딩 서열은 제1 및 제2 CD8 유전자 서열 사이에 위치한다. 특정 실시양태에서, 아미노산 서열 Gly Ser Gly를 코딩하는 서열은 제1 및 제2 CD8 유전자 서열 사이에 위치한다. 특정 실시양태에서, 푸린 절단 부위를 코딩하는 서열은 제1 및 제2 CD8 유전자 서열 사이에 위치한다.
특정 실시양태에서, CD8 유전자 서열은 세포외 도메인을 코딩하는 서열, 세포내 도메인을 코딩하는 서열, 세포내 도메인을 코딩하는 서열, 그의 단편, 또는 이들의 조합을 포함한다. 특정 실시양태에서, 세포외 도메인을 코딩하는 서열은 CD8α 세포외 도메인 또는 CD8β 세포외 도메인을 코딩하는 서열을 포함한다. 특정 실시양태에서, 막횡단 도메인을 코딩하는 서열은 CD8α 막횡단 도메인 또는 CD8β 막횡단 도메인을 코딩하는 서열을 포함한다. 특정 실시양태에서, 세포내 도메인을 코딩하는 서열은 CD8α 세포내 도메인 또는 CD8β 세포내 도메인을 코딩하는 서열을 포함한다. 특정 실시양태에서, 세포내 도메인을 코딩하는 서열은 CD4 세포내 도메인을 코딩하는 서열을 포함한다.
특정 실시양태에서, CD8 유전자 서열은 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인을 코딩하는 서열을 포함한다. 특정 실시양태에서, CD8 유전자 서열은 CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인을 코딩하는 서열을 포함한다. 특정 실시양태에서, CD8 유전자 서열은 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인을 코딩하는 서열을 포함한다. 특정 실시양태에서, CD8 유전자 서열은 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 코딩하는 서열을 포함한다.
특정 실시양태에서, HR 주형은 제1 CD8 유전자 서열의 바로 상류에 위치한 제1 신호 서열을 코딩하는 서열, 및 제2 CD8 유전자 서열의 바로 상류에 위치한 제2 신호 서열을 코딩하는 서열을 포함한다. 특정 실시양태에서, 신호 서열은 CD8 신호 서열, 인간 성장 호르몬 신호 서열, 그의 단편, 또는 이들의 조합이다. 특정 실시양태에서, HR 주형의 제1 및 제2 상동성 아암은 각각 약 300개 염기 내지 약 2,000개 염기의 길이이다. 특정 실시양태에서, HR 주형의 제1 및 제2 상동성 아암은 각각 약 600개 염기 내지 약 2,000개 염기의 길이이다.
특정 실시양태에서, 외인성 TCR은 환자 유래 TCR이다. 특정 실시양태에서, 외인성 TCR은 신호 서열, 제1 및 제2 2A 서열, 및 TCR 폴리펩티드 서열을 포함한다. 특정 실시양태에서, 외인성 TCR은 암 항원을 인식한다. 특정 실시양태에서, 암 항원은 신생항원이다. 특정 실시양태에서, 암 항원은 환자 특이적 항원이다. 특정 실시양태에서, HR 주형은 비-바이러스성이다. 특정 실시양태에서, HR 주형은 원형 DNA이다. 특정 실시양태에서, HR 주형은 선형 DNA이다. 특정 실시양태에서, 도입은 전기천공을 통해 일어난다.
특정 실시양태에서, 재조합은 뉴클레아제에 의한 내인성 로커스의 절단, 및 상동성 지정 복구에 의한 내인성 로커스 내로의 HR 주형 핵산 서열의 재조합을 포함한다. 특정 실시양태에서, 뉴클레아제는 클러스터링된 규칙적 간격의 짧은 회문구조 반복부 (CRISPR) 패밀리 뉴클레아제, 또는 그의 유도체이다. 특정 실시양태에서, 뉴클레아제는 gRNA를 추가로 포함한다.
특정 실시양태에서, 방법은 세포를 배양하는 것을 추가로 포함한다. 특정 실시양태에서, 배양은 적어도 1종의 시토카인의 존재 하에서 수행된다. 특정 실시양태에서, 배양은 IL2, IL7, IL15, 또는 이들의 임의의 조합의 존재 하에서 수행된다. 특정 실시양태에서, 배양은 IL7 및 IL15의 존재 하에서 수행된다. 특정 실시양태에서, 방법은 세포 존속을 증진시키고/거나 기억 세포 분화를 증진시키는 유전자 변형을 포함한다.
특정 실시양태에서, 세포는 1차 세포이다. 특정 실시양태에서, 세포는 환자-유래 세포이다. 특정 실시양태에서, 세포는 림프구이다. 특정 실시양태에서, 세포는 T 세포이다. 특정 실시양태에서, 세포는 어린 T 세포이다. 특정 실시양태에서, 세포는 CD45RA+, CD62L+, CD28+, CD95-, CCR7+, 및 CD27+이다. 특정 실시양태에서, 세포는 CD45RA+, CD62L+, CD28+, CD95+, CD27+, CCR7+이다. 특정 실시양태에서, 세포는 CD45RO+, CD62L+, CD28+, CD95+, CCR7+, CD27+, CD127+이다.
특정 실시양태에서, 세포의 살해 활성은 CD8 유전자 서열을 갖지 않는 세포의 살해 활성과 비교하여 약 10% 내지 약 500% 증가된다. 특정 실시양태에서, 항원에의 TCR의 결합 시 세포의 증식은 CD8 유전자 서열을 갖지 않는 세포의 증식과 비교하여 약 10% 내지 약 500% 증가된다. 특정 실시양태에서, 세포에 의한 항원에의 TCR의 결합 시 전염증성 시토카인의 분비는 CD8 유전자 서열을 갖지 않는 세포에 의한 분비와 비교하여 약 10% 내지 약 500% 증가된다. 특정 실시양태에서, 세포의 LCK 친화도는 CD8 유전자 서열을 갖지 않는 세포의 LCK 친화도와 비교하여 약 10% 내지 약 500% 증가된다. 세포의 존속이 CD8 유전자 서열을 갖지 않는 세포의 존속과 비교하여 약 10% 내지 약 500% 증가되는 것인 제43항 내지 제95항 중 어느 한 항의 방법. 특정 실시양태에서, 세포의 종양 침윤 능력은 CD8 유전자 서열을 갖지 않는 세포의 종양 침윤 능력과 비교하여 약 10% 내지 약 500% 증가된다.
특정 실시양태에서, TCR 유전자는 CD8-의존성 TCR을 코딩한다. 특정 실시양태에서, TCR 유전자는 CD8-비의존성 TCR을 코딩한다. 특정 실시양태에서, CD8 유전자 서열은 CD8 구축물 1, CD8 구축물 2, CD8 구축물 3, 또는 CD8 구축물 4에 의해 코딩된다. 특정 실시양태에서, CD8 유전자 서열은 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, CD4 세포내 도메인을 포함한다. 특정 실시양태에서, CD8 유전자 서열은 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함한다.
특정 실시양태에서, 본 개시된 대상은 본원에 개시된 임의의 방법에 의해 변형된 세포를 제공한다.
특정 실시양태에서, 본 개시된 대상은 본원에 개시된 세포의 유효량을 포함하는 조성물을 제공한다. 특정 실시양태에서, 조성물은 제약상 허용되는 부형제를 추가로 포함하는 제약 조성물이다. 특정 실시양태에서, 조성물은 암의 치료를 위해 이를 필요로 하는 환자에게 투여된다. 특정 실시양태에서, 조성물은 동결보존제를 포함한다. 특정 실시양태에서, 조성물은 혈청 알부민을 포함한다. 특정 실시양태에서, 조성물은 플라스마-라이트(Plasma-Lyte) A, HSA, 및 크리오스토르(CryoStor) CS10을 포함한다.
특정 실시양태에서, 본 개시된 대상은 본원에 개시된 세포 또는 조성물의 치료 유효량을 투여하는 것을 포함하는, 암의 치료를 필요로 하는 대상체에서 암을 치료하는 방법을 제공한다.
특정 실시양태에서, 본원에 개시된 세포의 치료 유효량을 투여하기 전에, 비-골수소멸성 림프구고갈 레지멘이 대상체에게 투여된다. 특정 실시양태에서, 암은 고형 종양이다. 특정 실시양태에서, 암은 액상 종양이다. 특정 실시양태에서, 고형 종양은 흑색종, 흉부암, 폐암, 난소암, 유방암, 췌장암, 두경부암, 전립선암, 부인과암, 중추 신경계암, 피부암, HPV+ 암, 식도암, 갑상선암, 위암, 간세포암, 담관암종, 신세포암, 고환암, 육종, 및 결장직장암으로 이루어진 군으로부터 선택된다. 특정 실시양태에서, 액상 종양은 소포성 림프종, 백혈병, 및 다발성 골수종으로 이루어진 군으로부터 선택된다.
특정 실시양태에서, 본 개시된 대상은 본원에 개시된 세포, 본원에 개시된 방법을 수행하기 위한 시약, 또는 본원에 개시된 조성물을 포함하는 키트를 제공한다. 특정 실시양태에서, 키트는 암을 치료하는 것에 대한 서면 지시서를 추가로 포함한다.
특정 실시양태에서, 본 개시된 대상은 외인성 T 세포 수용체 (TCR); 및 CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 외인성 CD8을 포함하는 세포를 제공한다.
특정 실시양태에서, 본 개시된 대상은 외인성 T 세포 수용체 (TCR); 및 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함하는 외인성 CD8을 포함하는 세포를 제공한다.
특정 실시양태에서, 본 개시된 대상은 세포 내로 상동성 재조합 (HR) 주형 핵산 서열을 도입하며, 여기서 HR 주형은 제1 및 제2 표적 핵산 서열에 대해 상동성인 제1 및 제2 상동성 아암; 제1 및 제2 상동성 아암 사이에 위치한 TCR 유전자 서열; 제1 및 제2 상동성 아암 사이에 위치한 CD8 유전자 서열을 포함하는 것인 단계; 및 HR 주형 핵산을 세포의 내인성 로커스 내로 재조합하는 단계를 포함하는, 세포를 변형시키는 방법으로서, 여기서 CD8 유전자 서열은 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 것인 방법을 제공한다.
특정 실시양태에서, 본 개시된 대상은 세포 내로 상동성 재조합 (HR) 주형 핵산 서열을 도입하며, 여기서 HR 주형은 제1 및 제2 표적 핵산 서열에 대해 상동성인 제1 및 제2 상동성 아암; 제1 및 제2 상동성 아암 사이에 위치한 TCR 유전자 서열; 제1 및 제2 상동성 아암 사이에 위치한 CD8 유전자 서열을 포함하는 것인 단계; 및 HR 주형 핵산을 세포의 내인성 로커스 내로 재조합하는 단계를 포함하는, 세포를 변형시키는 방법으로서, 여기서 CD8 유전자 서열은 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함하는 것인 방법을 제공한다.
특정 실시양태에서, 본 개시된 대상은 세포를 포함하는 조성물로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 것인 조성물을 제공한다.
특정 실시양태에서, 본 개시된 대상은 세포를 포함하는 조성물로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함하는 것인 조성물을 제공한다.
특정 실시양태에서, 본 개시된 대상은 치료 유효량의 세포를 투여하는 것을 포함하는, 암의 치료를 필요로 하는 대상체에서 암을 치료하는 방법으로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 것인 방법을 제공한다.
특정 실시양태에서, 본 개시된 대상은 치료 유효량의 세포를 투여하는 것을 포함하는 암의 치료를 필요로 하는 대상체에서 암을 치료하는 방법으로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함하는 것인 방법을 제공한다.
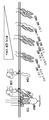
도 1a-1c. 도 1a-1c는 네오TCR 산물을 제조하는데 사용될 수 있는 네오E(NeoE) TCR 카세트 및 유전자 편집 방법의 예를 나타낸다. 도 1a는 신생항원-특이적 TCR 구축물 (네오TCR)을 TCRα 로커스 내로 통합하는데 사용된 일반적인 표적화 전략을 나타내는 개략도를 나타낸다. 도 1b 및 1c는 네오TCR을 TCRα 로커스 내로 통합하는데 사용된 신생항원-특이적 TCR 구축물 디자인을 나타내며, 여기서 카세트는 신호 서열 ("SS"), 프로테아제 절단 부위 ("P"), 및 2A 펩티드 ("2A")를 갖는 것으로 나타내어진다. 도 1b는 표적 TCRα 로커스 (내인성 TRAC, 상부 패널) 및 그의 CRISPR Cas9 표적 부위 (수평 줄무늬, 절단 부위는 화살표에 의해 표시됨), 및 통합 전에 좌측 및 우측 상동성 아암 (각각 "LHA" 및 "RHA") 사이에 위치한 네오TCR을 코딩하는 폴리뉴클레오티드를 갖는 원형 플라스미드 HR 주형 (하부 패널)을 나타낸다. 도 1c는 TCRα 로커스에서의 통합된 네오TCR (상부 패널), 전사되고 스플라이싱된 네오TCR mRNA (중간 패널), 및 발현된 네오TCR의 번역 및 프로세싱 (하부 패널)을 나타낸다.
도 2a-2d. 도 2a-2d는 CD8 구축물 1, 2, 3, 및 4를 코딩하는데 사용된 원형 플라스미드를 나타낸다. 도 2a는 CD8 산물 1을 제조하는데 사용된 CD8 구축물 1을 나타낸다. 도 2b는 CD8 산물 2를 제조하는데 사용된 CD8 구축물 2를 나타낸다. 도 2c는 CD8 산물 3을 제조하는데 사용된 CD8 구축물 3을 나타낸다. 도 2d는 CD8 산물 4를 제조하는데 사용된 CD8 구축물 4를 나타낸다. 도 2a-2d에 나타내어진 바와 같이, SS는 신호 서열을 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, SS는 HGH일 수 있지만; 적절한 트래피킹을 위해 필요에 따라 다른 신호 서열이 사용될 수 있다. 도 2a-2d에 나타내어진 바와 같이, P는 프로테아제 절단 부위를 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, P는 푸린일 수 있지만; 본원에 기재된 절단 작용을 제공하기 위해 적절한 경우 다른 프로테아제 절단 부위가 사용될 수 있다. 도 2a-2d에 나타내어진 바와 같으, 2A는 2A 펩티드를 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, 2A는 P2A 펩티드일 수 있지만; 다른 2A 펩티드가 사용될 수 있다.
도 3. 도 3a-3d는 CD8 산물 1, 2, 3, 및 4를 생성하는 CD8 구축물 1, 2, 3, 및 4 각각의 전사/스플라이싱 및 번역 프로세싱을 나타낸다. 도 3a-3d에 나타내어진 바와 같이, SS는 신호 서열을 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, SS는 HGH일 수 있지만; 적절한 트래피킹을 위해 필요에 따라 다른 신호 서열이 사용될 수 있다. 도 3a-3d에 나타내어진 바와 같이, P는 프로테아제 절단 부위를 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, P는 푸린일 수 있지만; 본원에 기재된 절단 작용을 제공하기 위해 적절한 경우 다른 프로테아제 절단 부위가 사용될 수 있다. 도 3a-3d에 나타내어진 바와 같이, 2A는 2A 펩티드를 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, 2A는 P2A 펩티드일 수 있지만; 다른 2A 펩티드가 사용될 수 있다.
도 4a 및 4b. 도 4a는 CD8 산물 1 및 CD8 산물 2의 번역된 산물을 나타낸다. 도 4b는 CD8 산물 3 및 CD8 산물 4의 번역된 산물을 나타낸다.
도 5. 도 5는 도 1a-1c에 기재된 네오TCR 구축물의 예시적인 DNA 서열을 제공한다. 핵산의 보존적 치환은 동일한 번역된 산물을 생성하기 위해 전반에 걸쳐 사용될 수 있다. 더욱이, 아미노산이 기능의 변화 없이 치환될 수 있는 경우, 도 5에 제공된 핵산의 치환은 또한 번역된 단백질의 실질적으로 유사하거나 동일한 기능을 부여하는 치환된 아미노산을 달성하는데 사용될 수 있다.
도 6. 도 6은 도 2a, 3a, 및 4a에 기재된 CD8 구축물 1 (및 번역된 CD8 산물 1)의 예시적인 DNA 서열을 제공한다. 핵산의 보존적 치환은 동일한 번역된 산물을 생성하기 위해 전반에 걸쳐 사용될 수 있다. 더욱이, 아미노산이 기능의 변화 없이 치환될 수 있는 경우, 도 6에 제공된 핵산의 치환은 또한 번역된 단백질의 실질적으로 유사하거나 동일한 기능을 부여하는 치환된 아미노산을 달성하는데 사용될 수 있다.
도 7. 도 7은 도 2b, 3b, 및 4a에 기재된 CD8 구축물 2 (및 번역된 CD8 산물 2)의 예시적인 DNA 서열을 제공한다. 핵산의 보존적 치환은 동일한 번역된 산물을 생성하기 위해 전반에 걸쳐 사용될 수 있다. 더욱이, 아미노산이 기능의 변화 없이 치환될 수 있는 경우, 도 7에 제공된 핵산의 치환은 또한 번역된 단백질의 실질적으로 유사하거나 동일한 기능을 부여하는 치환된 아미노산을 달성하는데 사용될 수 있다.
도 8. 도 8은 도 2c, 3c, 및 4b에 기재된 CD8 구축물 3 (및 번역된 CD8 산물 3)의 예시적인 DNA 서열을 제공한다. 핵산의 보존적 치환은 동일한 번역된 산물을 생성하기 위해 전반에 걸쳐 사용될 수 있다. 더욱이, 아미노산이 기능의 변화 없이 치환될 수 있는 경우, 도 8에 제공된 핵산의 치환은 또한 번역된 단백질의 실질적으로 유사하거나 동일한 기능을 부여하는 치환된 아미노산을 달성하는데 사용될 수 있다.
도 9. 도 9는 도 2d, 3d, 및 4b에 기재된 CD8 구축물 4 (및 번역된 CD8 산물 4)의 예시적인 DNA 서열을 제공한다. 핵산의 보존적 치환은 동일한 번역된 산물을 생성하기 위해 전반에 걸쳐 사용될 수 있다. 더욱이, 아미노산이 기능의 변화 없이 치환될 수 있는 경우, 도 9에 제공된 핵산의 치환은 또한 번역된 단백질의 실질적으로 유사하거나 동일한 기능을 부여하는 치환된 아미노산을 달성하는데 사용될 수 있다.
도 10. 도 10은 CD8 산물 1, 2, 3, 및 4 각각의 예측된 LCK 활성과 함께 CD8 산물 1, 2, 3, 및 4의 시각적 묘사를 제시한다.
도 11a-11d. 도 11a는 CD8 산물 1의 예시적인 발현 구축물을 제공한다. 도 11b는 CD8 산물 2의 예시적인 발현 구축물을 제공한다. 도 11c는 CD8 산물 3의 예시적인 발현 구축물을 제공한다. 도 11d는 CD8 산물 4의 예시적인 발현 구축물을 제공한다.
도 12. 도 12는 CD8 산물의 살해 능력을 나타내는 인큐사이트(Incucyte) 실험의 디자인을 도해한다.
도 13a 및 13b. 도 13a 및 13b는 CD4 T 세포의 집단에서 CD8 산물 4와 동일한 네오TCR을 갖는 네오TCR 산물에 비해 CD8 산물 4의 증가된 종양 살해 능력을 나타낸다. 구체적으로, CD8 산물 4 및 네오TCR 산물 둘 다는 TCR097을 발현한다. 그러나, CD8 산물 4는 또한 CD8α의 세포외 도메인 및 CD4의 세포내 도메인을 포함하는 CD8 구축물 4를 발현한다. 이펙터:표적 세포 비 (E:T 비)는 1:1 (도 13a) 또는 2:1 (도 13b)이었고, 각각은 세포주 당 유전자 편집에 대해 정규화되었다. 이 실험에 사용된 SW620 COX6C R20Q 이형접합성 종양 세포는 TCR097에 대한 동족 항원을 발현하는 세포주였다 (CD8 의존성 TCR). 이는 TCR097의 저 친화도 결합이 CD8α의 세포외 도메인 및 CD4의 세포내 도메인을 공동-발현시킴으로써 세이브될 수 있음을 나타낸다.
도 14. 도 14는 CD4 T 세포의 집단에서 CD8 산물 4와 동일한 네오TCR을 갖는 네오TCR 산물에 비해 CD8 산물 4의 증가된 종양 살해 능력을 나타낸다. 구체적으로, CD8 산물 4 및 네오TCR 산물 둘 다는 TCR097을 발현한다. 그러나, CD8 산물 4는 또한 CD8a의 세포외 도메인 및 CD4의 세포내 도메인을 포함하는 CD8 구축물 4를 발현한다. 이펙터:표적 세포 비 (E:T 비)는 1:1, 1:2, 또는 1:4이었고, 각각은 세포주 당 유전자 편집에 대해 정규화되었다. 이 실험에 사용된 SW620 COX6C R20Q 동형접합성 종양 세포는 TCR097에 대한 동족 항원을 발현하는 세포주였다. 도 13a 및 13b에 나타내어진 것에 비해 이 실험에서 증가된 살해를 볼 수 있는데, 이는 세포주가 동족 항원 발현에 대해 동형접합성이기 때문이며; 따라서, 비록 TCR97이 저 친화도 TCR이라 하더라도, 동족 항원의 증가된 양은 저 친화도 한계를 극복하였다.
도 15a 및 15b. 도 15a 및 15b는 CD4 T 세포 (도 15a 및 15b에서 상부 그래프) 또는 CD8 T 세포 (도 15a 및 15b에서 하부 그래프)의 집단에서 CD8 산물 4와 동일한 네오TCR을 갖는 네오TCR 산물에 비해 CD8 산물 4의 증가된 종양 살해 능력이 있음 및 CD8 산물 4가 CD8 T 세포에서 네오TCR 구축물 및 CD8 산물 4를 단순히 발현시키는 것보다 종양 살해에 있어서 더 효과적임을 나타내는 예시적인 대조군 실험을 제공한다. 도 15a는 2:1의 E:T 비를 나타내고, 도 15b는 1:1의 E:T 비를 나타낸다.
도 16. 도 16은 CD8 구축물 4의 표면 발현을 나타낸다. 피크 #1은 CD4+/CD8- T 세포 (TCR089를 발현함)에서의 네오TCR 산물이다. 피크 #2는 CD8+/CD4+ T 세포에서의 CD8 산물 4이다. 피크 #3은 CD8+/CD4- T 세포에서의 네오TCR 산물이다. 나타내어진 바와 같이, CD8 구축물 4는 네오TCR 산물처럼 적절하고 필적하는 표면 발현을 나타내었다. 다른 CD8 구축물로 유사한 결과가 달성되었다 (데이터는 나타내지 않음).
도 17a 및 17b. 도 17a 및 17b는 CD8α 발현이 특이성을 유지하면서 CD4 T 세포 민감도를 신장시킴을 나타낸다. 도 17a는 CD8 구축물 1-4의 발현이 T 세포의 민감도를 증가시키고, 네오TCR에 대한 CD8 산물의 특이성을 변화시키지 않음을 나타낸다. 나타내어진 바와 같이, CD8 구축물의 공동-발현은 EC50을 감소시키며, 이는 네오TCR에 대한 증가된 민감도를 나타낸다. 도 17b는 CD8 산물 1-4가 네오TCR 097에 대한 동족 항원에 대해 특이적임을 나타내는데, 이는 단지 동족 항원의 존재 하에서 CD8 산물 1-4의 CD8 세포에 의한 INFγ 생산이 있기 때문이다 (즉, 미스매칭된 항원의 존재 하에서 CD8 산물 1-4의 CD8 세포에 의한 INFγ 생산 없음). 도 17a 및 17b에 나타내어진 것과 동일한 실험을 INFγ 대신 CD107a로 수행하였으며, INFγ로의 결과를 확인하는 네오TCR에 대한 유지된 특이성과 함께 동일한 증가된 민감도가 보여졌다 (데이터는 나타내지 않음).
도 18. 도 18은 CD8α 발현이 CD8-비의존성 네오TCR 중에서 CD4 T 세포 민감도를 신장시킴을 나타낸다. 도면은 CD8-비의존성 네오TCR089로부터의 데이터를 나타낸다. 이는 네오TCR이 CD8-비의존성인 경우에도, CD8 산물 4의 민감도의 증가가 있음을 나타낸다. 이는 민감도가 심지어 CD8-비의존성 TCR에 대해서도 증가될 수 있음을 발견하는 놀라운 결과였다. CD8 산물 1-3으로 유사한 결과가 달성되었다 (데이터는 나타내지 않음). 따라서, CD8-의존성 (예를 들어, 네오TCR097) 및 CD8-비의존성 (예를 들어, 네오TCR089)은 동일한 네오TCR을 발현하는 네오TCR 산물에 비해 증가된 민감도를 나타낸다.
도 2a-2d. 도 2a-2d는 CD8 구축물 1, 2, 3, 및 4를 코딩하는데 사용된 원형 플라스미드를 나타낸다. 도 2a는 CD8 산물 1을 제조하는데 사용된 CD8 구축물 1을 나타낸다. 도 2b는 CD8 산물 2를 제조하는데 사용된 CD8 구축물 2를 나타낸다. 도 2c는 CD8 산물 3을 제조하는데 사용된 CD8 구축물 3을 나타낸다. 도 2d는 CD8 산물 4를 제조하는데 사용된 CD8 구축물 4를 나타낸다. 도 2a-2d에 나타내어진 바와 같이, SS는 신호 서열을 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, SS는 HGH일 수 있지만; 적절한 트래피킹을 위해 필요에 따라 다른 신호 서열이 사용될 수 있다. 도 2a-2d에 나타내어진 바와 같이, P는 프로테아제 절단 부위를 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, P는 푸린일 수 있지만; 본원에 기재된 절단 작용을 제공하기 위해 적절한 경우 다른 프로테아제 절단 부위가 사용될 수 있다. 도 2a-2d에 나타내어진 바와 같으, 2A는 2A 펩티드를 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, 2A는 P2A 펩티드일 수 있지만; 다른 2A 펩티드가 사용될 수 있다.
도 3. 도 3a-3d는 CD8 산물 1, 2, 3, 및 4를 생성하는 CD8 구축물 1, 2, 3, 및 4 각각의 전사/스플라이싱 및 번역 프로세싱을 나타낸다. 도 3a-3d에 나타내어진 바와 같이, SS는 신호 서열을 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, SS는 HGH일 수 있지만; 적절한 트래피킹을 위해 필요에 따라 다른 신호 서열이 사용될 수 있다. 도 3a-3d에 나타내어진 바와 같이, P는 프로테아제 절단 부위를 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, P는 푸린일 수 있지만; 본원에 기재된 절단 작용을 제공하기 위해 적절한 경우 다른 프로테아제 절단 부위가 사용될 수 있다. 도 3a-3d에 나타내어진 바와 같이, 2A는 2A 펩티드를 나타낸다. 도 6, 7, 8, 및 9에 기재된 바와 같이, 2A는 P2A 펩티드일 수 있지만; 다른 2A 펩티드가 사용될 수 있다.
도 4a 및 4b. 도 4a는 CD8 산물 1 및 CD8 산물 2의 번역된 산물을 나타낸다. 도 4b는 CD8 산물 3 및 CD8 산물 4의 번역된 산물을 나타낸다.
도 5. 도 5는 도 1a-1c에 기재된 네오TCR 구축물의 예시적인 DNA 서열을 제공한다. 핵산의 보존적 치환은 동일한 번역된 산물을 생성하기 위해 전반에 걸쳐 사용될 수 있다. 더욱이, 아미노산이 기능의 변화 없이 치환될 수 있는 경우, 도 5에 제공된 핵산의 치환은 또한 번역된 단백질의 실질적으로 유사하거나 동일한 기능을 부여하는 치환된 아미노산을 달성하는데 사용될 수 있다.
도 6. 도 6은 도 2a, 3a, 및 4a에 기재된 CD8 구축물 1 (및 번역된 CD8 산물 1)의 예시적인 DNA 서열을 제공한다. 핵산의 보존적 치환은 동일한 번역된 산물을 생성하기 위해 전반에 걸쳐 사용될 수 있다. 더욱이, 아미노산이 기능의 변화 없이 치환될 수 있는 경우, 도 6에 제공된 핵산의 치환은 또한 번역된 단백질의 실질적으로 유사하거나 동일한 기능을 부여하는 치환된 아미노산을 달성하는데 사용될 수 있다.
도 7. 도 7은 도 2b, 3b, 및 4a에 기재된 CD8 구축물 2 (및 번역된 CD8 산물 2)의 예시적인 DNA 서열을 제공한다. 핵산의 보존적 치환은 동일한 번역된 산물을 생성하기 위해 전반에 걸쳐 사용될 수 있다. 더욱이, 아미노산이 기능의 변화 없이 치환될 수 있는 경우, 도 7에 제공된 핵산의 치환은 또한 번역된 단백질의 실질적으로 유사하거나 동일한 기능을 부여하는 치환된 아미노산을 달성하는데 사용될 수 있다.
도 8. 도 8은 도 2c, 3c, 및 4b에 기재된 CD8 구축물 3 (및 번역된 CD8 산물 3)의 예시적인 DNA 서열을 제공한다. 핵산의 보존적 치환은 동일한 번역된 산물을 생성하기 위해 전반에 걸쳐 사용될 수 있다. 더욱이, 아미노산이 기능의 변화 없이 치환될 수 있는 경우, 도 8에 제공된 핵산의 치환은 또한 번역된 단백질의 실질적으로 유사하거나 동일한 기능을 부여하는 치환된 아미노산을 달성하는데 사용될 수 있다.
도 9. 도 9는 도 2d, 3d, 및 4b에 기재된 CD8 구축물 4 (및 번역된 CD8 산물 4)의 예시적인 DNA 서열을 제공한다. 핵산의 보존적 치환은 동일한 번역된 산물을 생성하기 위해 전반에 걸쳐 사용될 수 있다. 더욱이, 아미노산이 기능의 변화 없이 치환될 수 있는 경우, 도 9에 제공된 핵산의 치환은 또한 번역된 단백질의 실질적으로 유사하거나 동일한 기능을 부여하는 치환된 아미노산을 달성하는데 사용될 수 있다.
도 10. 도 10은 CD8 산물 1, 2, 3, 및 4 각각의 예측된 LCK 활성과 함께 CD8 산물 1, 2, 3, 및 4의 시각적 묘사를 제시한다.
도 11a-11d. 도 11a는 CD8 산물 1의 예시적인 발현 구축물을 제공한다. 도 11b는 CD8 산물 2의 예시적인 발현 구축물을 제공한다. 도 11c는 CD8 산물 3의 예시적인 발현 구축물을 제공한다. 도 11d는 CD8 산물 4의 예시적인 발현 구축물을 제공한다.
도 12. 도 12는 CD8 산물의 살해 능력을 나타내는 인큐사이트(Incucyte) 실험의 디자인을 도해한다.
도 13a 및 13b. 도 13a 및 13b는 CD4 T 세포의 집단에서 CD8 산물 4와 동일한 네오TCR을 갖는 네오TCR 산물에 비해 CD8 산물 4의 증가된 종양 살해 능력을 나타낸다. 구체적으로, CD8 산물 4 및 네오TCR 산물 둘 다는 TCR097을 발현한다. 그러나, CD8 산물 4는 또한 CD8α의 세포외 도메인 및 CD4의 세포내 도메인을 포함하는 CD8 구축물 4를 발현한다. 이펙터:표적 세포 비 (E:T 비)는 1:1 (도 13a) 또는 2:1 (도 13b)이었고, 각각은 세포주 당 유전자 편집에 대해 정규화되었다. 이 실험에 사용된 SW620 COX6C R20Q 이형접합성 종양 세포는 TCR097에 대한 동족 항원을 발현하는 세포주였다 (CD8 의존성 TCR). 이는 TCR097의 저 친화도 결합이 CD8α의 세포외 도메인 및 CD4의 세포내 도메인을 공동-발현시킴으로써 세이브될 수 있음을 나타낸다.
도 14. 도 14는 CD4 T 세포의 집단에서 CD8 산물 4와 동일한 네오TCR을 갖는 네오TCR 산물에 비해 CD8 산물 4의 증가된 종양 살해 능력을 나타낸다. 구체적으로, CD8 산물 4 및 네오TCR 산물 둘 다는 TCR097을 발현한다. 그러나, CD8 산물 4는 또한 CD8a의 세포외 도메인 및 CD4의 세포내 도메인을 포함하는 CD8 구축물 4를 발현한다. 이펙터:표적 세포 비 (E:T 비)는 1:1, 1:2, 또는 1:4이었고, 각각은 세포주 당 유전자 편집에 대해 정규화되었다. 이 실험에 사용된 SW620 COX6C R20Q 동형접합성 종양 세포는 TCR097에 대한 동족 항원을 발현하는 세포주였다. 도 13a 및 13b에 나타내어진 것에 비해 이 실험에서 증가된 살해를 볼 수 있는데, 이는 세포주가 동족 항원 발현에 대해 동형접합성이기 때문이며; 따라서, 비록 TCR97이 저 친화도 TCR이라 하더라도, 동족 항원의 증가된 양은 저 친화도 한계를 극복하였다.
도 15a 및 15b. 도 15a 및 15b는 CD4 T 세포 (도 15a 및 15b에서 상부 그래프) 또는 CD8 T 세포 (도 15a 및 15b에서 하부 그래프)의 집단에서 CD8 산물 4와 동일한 네오TCR을 갖는 네오TCR 산물에 비해 CD8 산물 4의 증가된 종양 살해 능력이 있음 및 CD8 산물 4가 CD8 T 세포에서 네오TCR 구축물 및 CD8 산물 4를 단순히 발현시키는 것보다 종양 살해에 있어서 더 효과적임을 나타내는 예시적인 대조군 실험을 제공한다. 도 15a는 2:1의 E:T 비를 나타내고, 도 15b는 1:1의 E:T 비를 나타낸다.
도 16. 도 16은 CD8 구축물 4의 표면 발현을 나타낸다. 피크 #1은 CD4+/CD8- T 세포 (TCR089를 발현함)에서의 네오TCR 산물이다. 피크 #2는 CD8+/CD4+ T 세포에서의 CD8 산물 4이다. 피크 #3은 CD8+/CD4- T 세포에서의 네오TCR 산물이다. 나타내어진 바와 같이, CD8 구축물 4는 네오TCR 산물처럼 적절하고 필적하는 표면 발현을 나타내었다. 다른 CD8 구축물로 유사한 결과가 달성되었다 (데이터는 나타내지 않음).
도 17a 및 17b. 도 17a 및 17b는 CD8α 발현이 특이성을 유지하면서 CD4 T 세포 민감도를 신장시킴을 나타낸다. 도 17a는 CD8 구축물 1-4의 발현이 T 세포의 민감도를 증가시키고, 네오TCR에 대한 CD8 산물의 특이성을 변화시키지 않음을 나타낸다. 나타내어진 바와 같이, CD8 구축물의 공동-발현은 EC50을 감소시키며, 이는 네오TCR에 대한 증가된 민감도를 나타낸다. 도 17b는 CD8 산물 1-4가 네오TCR 097에 대한 동족 항원에 대해 특이적임을 나타내는데, 이는 단지 동족 항원의 존재 하에서 CD8 산물 1-4의 CD8 세포에 의한 INFγ 생산이 있기 때문이다 (즉, 미스매칭된 항원의 존재 하에서 CD8 산물 1-4의 CD8 세포에 의한 INFγ 생산 없음). 도 17a 및 17b에 나타내어진 것과 동일한 실험을 INFγ 대신 CD107a로 수행하였으며, INFγ로의 결과를 확인하는 네오TCR에 대한 유지된 특이성과 함께 동일한 증가된 민감도가 보여졌다 (데이터는 나타내지 않음).
도 18. 도 18은 CD8α 발현이 CD8-비의존성 네오TCR 중에서 CD4 T 세포 민감도를 신장시킴을 나타낸다. 도면은 CD8-비의존성 네오TCR089로부터의 데이터를 나타낸다. 이는 네오TCR이 CD8-비의존성인 경우에도, CD8 산물 4의 민감도의 증가가 있음을 나타낸다. 이는 민감도가 심지어 CD8-비의존성 TCR에 대해서도 증가될 수 있음을 발견하는 놀라운 결과였다. CD8 산물 1-3으로 유사한 결과가 달성되었다 (데이터는 나타내지 않음). 따라서, CD8-의존성 (예를 들어, 네오TCR097) 및 CD8-비의존성 (예를 들어, 네오TCR089)은 동일한 네오TCR을 발현하는 네오TCR 산물에 비해 증가된 민감도를 나타낸다.
정의
달리 정의되지 않는 한, 본원에 사용된 모든 기술 및 과학 용어는 관련 기술분야의 통상의 기술자에 의해 통상적으로 이해되는 의미를 갖는다. 하기 참고문헌은 통상의 기술자에게 본 개시된 대상에 사용된 많은 용어의 일반적 정의를 제공한다: 문헌 [Singleton et al., Dictionary of Microbiology and Molecular Biology (2nd ed. 1994)]; [The Cambridge Dictionary of Science and Technology (Walker ed., 1988)]; [The Glossary of Genetics, 5th Ed., R. Rieger et al. (eds.), Springer Verlag (1991)]; 및 [Hale & Marham, The Harper Collins Dictionary of Biology (1991)]. 본원에 사용된 하기 용어는 달리 특정되지 않는 한, 하기 그들에 주어진 의미를 갖는다.
본원에 기재된 본 발명의 측면 및 실시양태는 "포함하는", "이루어진", 및 "본질적으로 이루어진" 측면 및 실시양태를 포함함이 이해된다. 용어 "포함한다" 및 "포함하는"은 미국 특허법에서 그들에 주어진 넓은 의미를 갖는 것으로 의도되며, "포괄한다", "포괄하는" 등을 의미할 수 있다.
본원에 사용된 용어 "약" 또는 "대략"은 값이 측정되거나 결정되는 방법, 즉, 측정 시스템의 한계에 부분적으로 의존할 관련 기술분야의 통상의 기술자에 의해 결정된 바와 같은 특정 값에 대한 허용되는 오차 범위 내를 의미한다. 예를 들어, "약"은 관련 기술분야의 관행에 따라, 3 또는 3 초과의 표준 편차 내를 의미할 수 있다. 대안적으로, "약"은 주어진 값의 최대 20%, 예를 들어, 최대 10%, 최대 5%, 또는 최대 1%의 범위를 의미할 수 있다. 대안적으로, 특히 생물학적 시스템 또는 프로세스에 관하여, 상기 용어는 값의 한 자릿수 내, 예를 들어, 5배 내 또는 2배 내를 의미할 수 있다.
본원에 사용된 용어 "항체"는 가장 넓은 의미로 사용되며, 이들이 목적하는 항원-결합 활성을 나타내는 한, 모노클로날 항체, 폴리클로날 항체, 다중특이적 항체 (예를 들어, 이중특이적 및 삼중-특이적 항체), 및 항체 단편 (예를 들어, 비스-Fab)을 포함하나 이에 제한되지는 않는 다양한 항체 구조를 포괄한다. 본원에 사용된 "항체 단편"은 무손상 항체가 결합하는 항원에 결합하는 무손상 항체의 부분을 포함하는 무손상 항체 이외의 분자를 지칭한다. 항체 단편의 예는 비스-Fab; Fv; Fab; Fab, Fab'-SH; F(ab')2; 디아바디; 선형 항체; 단일-쇄 항체 분자 (예를 들어, scFv); 및 항체 단편으로부터 형성된 다중특이적 항체를 포함하나 이에 제한되지는 않는다.
용어 "암" 및 "종양"은 본원에서 상호교환가능하게 사용된다. 본원에 사용된 용어 "암" 또는 "종양"은 악성이든 양성이든 모든 신생물성 세포 성장 및 증식, 및 모든 전암성 및 암성 세포 및 조직을 지칭한다. 상기 용어는 또한 전형적으로 비조절된 세포 성장/증식을 특징으로 하는 포유동물에서의 생리학적 상태를 지칭하거나 기재하기 위해 사용된다. 암은 방광, 뼈, 뇌, 유방, 연골, 신경아교, 식도, 나팔관, 담낭, 심장, 장, 신장, 간, 폐, 림프절, 신경 조직, 난소, 췌장, 전립선, 골격근, 피부, 척수, 비장, 위, 고환, 흉선, 갑상선, 기관, 비뇨생식관, 요관, 요도, 자궁, 및 질로 이루어진 군으로부터 선택되는 기관, 또는 그의 조직 또는 세포 유형을 포함하나 이에 제한되지는 않는 다양한 세포 유형, 조직, 또는 기관에 영향을 미칠 수 있다. 암은 육종, 암종, 또는 형질세포종 (형질 세포의 악성 종양)과 같은 암을 포함한다. 암의 예는 본원에 기재된 것들을 포함하나 이에 제한되지는 않는다. 용어 "암" 또는 "종양" 및 "증식성 장애"는 본원에 사용된 바와 같이 상호 배타적이지 않다.
"CD8"은 면역계 내의 효율적인 세포-세포 상호작용을 매개하는 대부분의 세포독성 T 림프구 상에서 발견되는 세포 표면 당단백질이다. CD8 항원은 부류 I MHC 분자의 맥락에서 항원 제시 세포에 의해 제시되는 항원을 인식하는 T 림프구 상의 T-세포 수용체와의 공수용체로서 작용한다.
본원에 사용된 "CD8 세포"는 1종 이상의 네오TCR 및 CD8 구축물을 발현하도록 정확성 조작된 1종 이상의 세포를 의미한다.
본원에 사용된 "CD8 구축물"은 CD8 구축물 1, CD8 구축물 2, CD8 구축물 3, 또는 CD8 구축물 4 중 어느 하나를 의미한다.
본원에 사용된 "CD8 산물"은 CD8 세포를 포함하는 산물을 의미한다.
"CD8 구축물 1" 및 "CD8 산물 1"은 네오TCR 및 CD8α (CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인)를 포함하는 구축물 및 발현된 네오TCR 및 CD8α를 포함하는 생성된 산물을 지칭한다. CD8 산물 1의 비-제한적 예는 도 2a, 3a, 및 6에 제공된다. CD8 산물 1의 비-제한적 예는 도 4a에 제공된다.
"CD8 구축물 2" 및 "CD8 산물 2"는 네오TCR, CD8α (CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인), 및 CD8β (CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인)를 포함하는 구축물 및 발현된 네오TCR, CD8α, 및 CD8β를 포함하는 생성된 산물을 지칭한다. CD8 산물 2의 비-제한적 예는 도 2b, 3b, 및 7에 제공된다. CD8 산물 1의 비-제한적 예는 도 4a에 제공된다.
"CD8 구축물 3" 및 "CD8 산물 3"은 네오TCR, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인을 포함하는 구축물 및 발현된 네오TCR, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인을 포함하는 생성된 산물을 지칭한다. CD8 산물 3의 비-제한적 예는 도 2c, 3c, 및 8에 제공된다. CD8 산물 1의 비-제한적 예는 도 4b에 제공된다.
"CD8 구축물 4" 및 "CD8 산물 4"는 네오TCR, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 구축물 및 발현된 네오TCR, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 생성된 산물을 지칭한다. CD8 산물 4의 비-제한적 예는 도 2d, 3d, 및 9에 제공된다. CD8 산물 1의 비-제한적 예는 도 4b에 제공된다.
"보존적 치환" 또는 "보존적 아미노산"은 화학적으로 또는 기능적으로 유사한 아미노산으로의 아미노산의 치환을 지칭한다. 유사한 아미노산을 제공하는 보존적 치환 표는 관련 기술분야에 널리 공지되어 있다.
특정 실시양태에서, 산성 아미노산 D 및 E는 서로에 대해 보존적 치환이고; 염기성 아미노산 K, R, 및 H는 서로에 대해 보존적 치환이고; 친수성 비하전된 아미노산 S, T, N, 및 Q는 서로에 대해 보존적 치환이고; 지방족 비하전된 아미노산 G, A, V, L, 및 I는 서로에 대해 보존적 치환이고; 비-극성 비하전된 아미노산 C, M, 및 P는 서로에 대해 보존적 치환이고; 방향족 아미노산 F, Y, 및 W는 서로에 대해 보존적 치환이고; A, S, 및 T는 서로에 대해 보존적 치환이고; D 및 E는 서로에 대해 보존적 치환이고; N 및 Q는 서로에 대해 보존적 치환이고; R 및 K는 서로에 대해 보존적 치환이고; I, L, 및 M은 서로에 대해 보존적 치환이고; F, Y, 및 W는 서로에 대해 보존적 치환이고; A 및 G는 서로에 대해 보존적 치환이고; D 및 E는 서로에 대해 보존적 치환이고; N 및 Q는 서로에 대해 보존적 치환이고; R, K 및 H는 서로에 대해 보존적 치환이고; I, L, M, 및 V는 서로에 대해 보존적 치환이고; F, Y 및 W는 서로에 대해 보존적 치환이고; S 및 T는 서로에 대해 보존적 치환이고; C 및 M은 서로에 대해 보존적 치환이다.
추가의 보존적 치환은 예를 들어, 문헌 [Creighton, Proteins: Structures and Molecular Properties 2nd ed. (1993) W. H. Freeman & Co., New York, NY]에서 발견될 수 있다.
"치료하다", "치료", 및 "치료하는"은 상호교환가능하게 사용되며, 본원에 사용된 바와 같이 임상적 결과를 포함한 유익하거나 목적하는 결과를 얻는 것을 의미한다. 치료의 목적하는 효과는 질환의 발생 또는 재발을 방지하는 것, 증상의 경감, 질환의 임의의 직접적 또는 간접적 병리학적 결과의 감소, 전이를 방지하는 것, 질환 진행의 속도를 감소시키는 것, 질환 상태의 개선 또는 경감, 및 완화 또는 개선된 예후를 포함하나 이에 제한되지는 않는다. 일부 실시양태에서, 본 발명의 네오TCR 산물은 증식성 장애 (예를 들어, 암)의 발달을 지연시키거나 이러한 질환의 진행을 감속시키는데 사용된다.
본원에 사용된 "덱스트라머"는 그의 동족 네오TCR에 특이적으로 결합하는 다량체화된 네오에피토프-HLA 복합체를 의미한다.
본원에 사용된 용어 "신생항원", "네오에피토프" 또는 "네오E"는 예를 들어, 체세포 돌연변이(들)로부터 발생하고, "비-자기"로서 인식되는 새롭게 형성된 항원 결정자를 지칭한다. "신생항원", "네오에피토프" 또는 "네오E"를 발생시키는 돌연변이는 프레임시프트 또는 비-프레임시프트 indel, 미스센스 또는 넌센스 치환, 스플라이스 부위 변경 (예를 들어, 대체 스플라이싱된 전사체), 게놈 재배열 또는 유전자 융합, 임의의 게놈 또는 발현 변경, 또는 임의의 번역후 변형을 포함할 수 있다.
본원에 사용된 "네오TCR", "네오E TCR" 및 "외인성 TCR"은 예를 들어, 유전자 편집 방법에 의해 T 세포 내로 도입된 네오에피토프-특이적 T 세포 수용체를 의미한다. 본원에 사용된 용어 "TCR 유전자 서열"은 네오TCR 유전자 서열을 지칭한다.
본원에 사용된 "네오TCR 세포"는 1종 이상의 네오TCR을 발현하도록 정확성 조작된 1종 이상의 세포를 의미한다. 특정 실시양태에서, 세포는 T 세포이다. 특정 실시양태에서, T 세포는 CD8+ 및/또는 CD4+ T 세포이다. 특정 실시양태에서, CD8+ 및/또는 CD4+ T 세포는 네오TCR 산물이 투여될 환자로부터의 자가 세포이다. 용어 "네오TCR 세포" 및 "네오TCR-P1 T 세포" 및 "네오TCR-P1 세포"는 본원에서 상호교환가능하게 사용된다.
본원에 사용된 "네오TCR 산물"은 1종 이상의 네오TCR 세포를 포함하는 제약 제제를 의미한다. 네오TCR 산물은 자가 정확성 게놈-조작된 CD8+ 및 CD4+ T 세포로 이루어진다. 표적화된 DNA-매개 비-바이러스 정확성 게놈 조작 접근법을 사용하여, 내인성 TCR의 발현은 제거되고, 종양-배타적 네오에피토프를 표적화하는 말초 CD8+ T 세포로부터 단리된 환자-특이적 네오TCR에 의해 대체된다. 특정 실시양태에서, 생성된 조작된 CD8+ 또는 CD4+ T 세포는 천연 서열, 천연 발현 수준, 및 천연 TCR 기능의 그들의 표면 상에 네오TCR을 발현한다. 네오TCR 외부 결합 도메인 및 세포질 신호전달 도메인의 서열은 천연 CD8+ T 세포로부터 단리된 TCR로부터 비변형된다. 네오TCR 유전자 발현의 조절은 네오TCR 유전자 카세트가 게놈 내로 통합된 상류에 위치한 천연 내인성 TCR 프로모터에 의해 유도된다. 이 접근법을 통해, 네오TCR 발현의 천연 수준은 비자극된 및 항원-활성화된 T 세포 상태에서 관찰된다.
각각의 환자에 대해 제조된 네오TCR 산물은 그 동일한 환자의 말초 혈액으로부터 개별적으로 단리된 네오E-특이적 CD8+ T 세포로부터 클로닝된 단일 네오E-특이적 TCR을 발현하도록 정확성 게놈 조작된 한정된 용량의 자가 CD8+ 및/또는 CD4+ T 세포를 나타낸다.
본원에 사용된 "네오TCR 바이러스 산물"은 게놈 조작이 바이러스 매개 방법을 사용하여 수행되는 것을 제외하고는 네오TCR 산물의 동일한 정의를 갖는다.
"제약 제제"는 그 안에 함유된 활성 성분의 생물학적 활성이 유효하게 되는 것을 허용하도록 하는 형태이고, 제제가 투여될 대상체에게 비허용가능하게 독성인 추가의 성분을 함유하지 않는 제제를 지칭한다. 명확성을 위해, 네오TCR 산물에 사용된 대량의 DMSO는 비허용가능하게 독성인 것으로 간주되지 않는다.
치료의 목적을 위한 "대상체", "환자", 또는 "개체"는 인간, 가축 및 농장 동물, 및 동물원, 경기, 또는 애완 동물, 예컨대 개, 말, 고양이, 소 등을 포함한 포유동물로서 분류되는 임의의 동물을 지칭한다. 바람직하게는, 포유동물은 인간이다.
본원에 사용된 "TCR"은 T 세포 수용체를 의미한다.
본원에 사용된 용어 "종양 항원"은 정상 또는 비-신생물성 세포에 비해 종양 세포 상에 고유하게 또는 차등적으로 발현된 항원 (예를 들어, 폴리펩티드)을 지칭한다. 특정 실시양태에서, 종양 항원은 항원-인식 수용체를 통해 면역 반응을 활성화시키거나 유도할 수 있는 또는 수용체-리간드 결합을 통해 면역 반응을 억제할 수 있는 종양에 의해 발현된 임의의 폴리펩티드를 포함한다.
"2A" 및 "2A 펩티드"는 본원에서 상호교환가능하게 사용되며, 진핵생물 세포에서 번역 동안 펩티드의 절단을 매개할 수 있는 18-22 아미노산 길이의 바이러스성 자기-절단 펩티드의 부류를 의미한다.
2A 펩티드 부류의 4가지 널리 공지된 구성원은 T2A, P2A, E2A, 및 F2A이다. T2A 펩티드는 토세아 아시그나(Thosea asigna) 바이러스 2A에서 최초로 확인되었다. P2A 펩티드는 돼지 테스코바이러스-1 2A에서 최초로 확인되었다. E2A 펩티드는 말 A형 비염 바이러스에서 최초로 확인되었다. F2A 펩티드는 구제역 바이러스에서 최초로 확인되었다.
2A 펩티드의 자기-절단 메커니즘은 2A의 C-말단에서 글리실-프롤릴 펩티드 결합의 형성을 스키핑하는 리보솜의 결과이다. 구체적으로, 2A 펩티드는 입체 장해 및 리보솜 스키핑의 생성에 필요한 C-말단 보존된 서열을 갖는다. 리보솜 스키핑은 3가지 옵션 중 하나를 발생시킬 수 있다: 1) 2개의 절단된 단백질을 발생시키는 번역의 성공적인 스키핑 및 재개 (C-말단 프롤린을 제외하고 완전한 2A 펩티드에 부착된 2A 단백질의 상류 및 N-말단에서 하나의 프롤린에 부착된 2A 단백질의 하류; 2) 중단된 번역 및 단지 2A의 상류의 단백질을 발생시키는 성공적인 스키핑, 그러나 리보솜 떨어짐; 또는 3) 비성공적인 스키핑 및 계속된 번역 (즉, 융합 단백질).
본원에 사용된 용어 "내인성"은 세포 또는 조직에서 정상적으로 발현되는 핵산 분자 또는 폴리펩티드를 지칭한다.
본원에 사용된 용어 "외인성"은 세포에 내인적으로 존재하지 않는 핵산 분자 또는 폴리펩티드를 지칭한다. 따라서, 용어 "외인성"은 세포에서 발현된 임의의 재조합 핵산 분자 또는 폴리펩티드, 예컨대 외래, 이종, 및 과-발현된 핵산 분자 및 폴리펩티드를 포괄한다. "외인성" 핵산이란 천연 야생형 세포에 존재하지 않는 핵산을 의미하며; 예를 들어, 외인성 핵산은 서열에 의해, 위치/장소에 의해, 또는 둘 다에 의해 내인성 대응물과는 다를 수 있다. 명확성을 위해, 외인성 핵산은 그의 천연 내인성 대응물에 비해 동일하거나 상이한 서열을 가질 수 있으며; 이는 세포 자체 또는 그의 전구체 내로의 유전자 조작에 의해 도입될 수 있고, 임의로 대안적 제어 서열, 예컨대 비-천연 프로모터 또는 분비 서열에 연결될 수 있다.
그것이 T 세포에 관한 것일 때 "어린" 또는 "보다 어린" 또는 "어린 T 세포"는 기억 줄기 세포 (TMSC) 및 중심 기억 세포 (TCM)를 의미한다. 이들 세포는 특이적 활성화 시 T 세포 증식을 가지며, 다중 세포 분열에 적격이다. 이들은 또한 재-주입 후 그라프팅되어, 그들의 동족 항원에의 노출 시 이펙터 T 세포로 급속하게 분화되고, 종양 세포를 표적화하고 살해할 뿐만 아니라, 진행중인 암 감시 및 제어를 위해 존속하는 능력을 갖는다.
네오TCR 산물
일부 실시양태에서, 그 전문이 본원에 포함되는 PCT/US2020/17887 및 PCT/US2019/025415에 기재된 유전자 편집 기술 및 네오TCR 단리 기술을 사용하여, 네오TCR은 네오TCR을 발현하도록 조작된 정확성 게놈에 의해 (도 1a-1c에 기재된 바와 같은 DNA-매개 (비-바이러스) 방법을 사용하여) 암을 갖는 동일한 환자로부터의 자가 CD8+ 및 CD4+ T 세포에서 클로닝된다. 다시 말해서, 종양 특이적인 네오TCR을 암 환자에서 확인하고, 이어서 이러한 네오TCR을 클로닝하고, 이어서 클로닝된 네오TCR을 암 환자의 T 세포 내로 삽입한다. 이어서 네오TCR 발현 T 세포를 "어린" T 세포 표현형을 보존하는 방식으로 확장시켜, T 세포의 대다수가 T 기억 줄기 세포 및 T 중심 기억 표현형을 나타내는 네오TCR-P1 산물 (즉, 네오TCR 산물)을 생성한다.
이들 '어린' 또는 '보다 어린' 또는 덜-분화된 T 세포 표현형은 개선된 그라프팅 잠재성 및 주입 후 연장된 존속을 부여하는 것으로 기재된다. 따라서, 유의하게 '어린' T 세포 표현형으로 이루어진 네오TCR 산물의 투여는 개선된 그라프팅 잠재성, 주입 후 연장된 존속, 및 신체 전반에 걸쳐 종양 세포를 근절시키는 이펙터 T 세포로의 급속한 분화를 통해, 암을 갖는 환자를 유익하게 할 잠재성을 갖는다.
생체외 작용 메커니즘 연구를 또한 암을 갖는 환자로부터의 T 세포로 제조된 네오TCR 산물로 수행하였다. T 세포 살해 활성, 증식, 및 시토카인 생산의 항원-특이성에 의해 측정된 바와 같은 필적하는 유전자 편집 효율 및 기능적 활성이 관찰되었으며, 이는 본원에 기재된 제조 프로세스가 출발 물질로서 암을 갖는 환자로부터의 T 세포를 갖는 산물을 생성하는데 있어서 성공적임을 입증한다.
특정 실시양태에서, 네오TCR 산물 제조 프로세스는 가이드 RNA 서열에 결합된 CRISPR-Cas9 뉴클레아제의 이중 리보핵단백질 종의 전기천공을 수반하며, 각각의 종은 게놈 TCRα 및 게놈 TCRβ 로커스를 표적화한다. Cas9 뉴클레아제를 각각의 게놈 로커스에 표적화하는 특이성은 고도로 특이적인 것으로 문헌에 이전에 기재되었다. 각각 COSMID 및 GUIDE-seq를 사용하여, 네오TCR 산물의 포괄적인 시험을 시험관내에서 및 인 실리코 분석에서 수행하여 가능한 오프-타겟 게놈 절단 부위를 조사하였다. 건강한 공여자로부터의 다중 네오TCR 산물 또는 필적하는 세포 산물을 딥 시퀀싱에 의해 후보 오프-타겟 부위의 절단에 대해 평가하였으며, 이는 선택된 뉴클레아제가 고도로 특이적이라는 공개된 증거를 뒷받침한다.
정확성 게놈 조작 프로세스의 추가의 측면은 안전성에 대해 평가되었다. 표적화된 로커스 증폭 (TLA) 또는 표준 FISH 세포유전학에 의해 다중 네오TCR 산물을 평가하는데 있어서 정확성 게놈 조작 후의 게놈 불안정성의 증거는 발견되지 않았다. 네오TCR 서열의 게놈 내로 어디에서도 오프-타겟 통합은 검출되지 않았다. 잔여 Cas9의 증거는 세포 산물에서 발견되지 않았다.
네오TCR 산물 및 정확성 게놈 조작 프로세스의 포괄적인 평가는 네오TCR 산물이 환자로의 재주입 후 잘 내성화될 것임을 지시한다.
본원에 기재된 게놈 조작 접근법은 고형 및 액상 종양을 갖는 환자에 대한 개인화된 입양 세포 요법을 위한 맞춤 네오TCR T 세포 (즉, 네오TCR 산물)의 고도로 효율적인 생성을 가능하게 한다. 더욱이, 조작 방법은 T 세포에서의 사용에 제한되지 않으며, 또한 자연 킬러 및 조혈 줄기 세포를 포함한 다른 1차 세포 유형에 성공적으로 적용되었다.
CD8 산물
정확성 게놈 조작된 CD4 T 세포에서의 MHC 부류 I-제한된 네오TCR 및 이소성 CD8 수용체의 공동발현은 항원-특이적 이펙터 기능을 유의하게 강화시킨다.
종양-배타적 돌연변이로부터의 네오에피토프는 고형 종양을 갖는 환자에 대한 개인화된 네오E-특이적 자가 TCR-T 세포 요법을 위한 강렬한 표적을 나타낸다. 그 전문이 참조로 포함되는 PCT/US2020/17887에 기재된 바와 같은 imPACT 단리 기술은 고형 암을 갖는 환자의 혈액으로부터 네오E-특이적 CD8 T 세포를 포획하기 위한 초-민감성 및 고-처리량 프로세스이다. 이 기술을 지렛대로 하여, 네오에피토프-특이적 MHC 부류 I-제한된 TCR ("MHC-I 네오TCR")을 개별적으로 포획된 CD8 T 세포로부터 클로닝하였다. 실시예 1에 기재된 바와 같은 DNA-매개 (비-바이러스) 유전자 편집을 사용하여, 암을 갖는 동일한 환자로부터의 신선한 CD8 및 CD4 T 세포를 MHC-I 네오TCR를 발현하도록 조작하였다 (내인성 TCR의 제거와 수반하여).
천연 발생 MHC-I TCR은 공동 CD8 공-수용체가 펩티드-MHC 결합을 안정화하는 것을 도울 것이 요구되는 것으로 추정되었지만, 보다 높은 친화도 TCR은 CD8-비의존성 표적 결합 및 T 세포 활성화를 유도할 수 있었다. 따라서, CD4 T 세포는, 고 친화도 네오TCR로 조작되는 경우, 펩티드-MHC-I 표적을 인식하고, 이펙터 T 세포 기능을 촉발시킬 수 있었다. 그러나, 보다 낮은 친화도 TCR은 T 세포 활성화를 촉발시키기 위해 CD8 공-수용체에 의존적이었다. 네오TCR과 함께 CD8 공-수용체 유전자를 CD4 T 세포 내로 정확성 게놈 조작함으로써, MHC-I 네오TCR은 항원-특이적 이펙터 T 세포 기능을 촉발시키는데 적격이도록 만들어졌다.
CD8은 TCR-pMHC 상호작용을 안정화시키고, 결합력을 위해 TCR과 상승작용한다. CD8은 또한 저 친화도 TCR로부터 결합력을 증진시키는 역할을 하는 반면, CD8α의 세포내 도메인은 증진된 T 세포 활성화를 위해 중요하다. CD8의 발현은 CD4 T 세포 반응을 증진시킬 수 있으며, 이는 pMHC의 생리학적 농도에 반응하지 않을 수 있다. MHC에의 CD8 결합의 파괴는 캐치-결합 TCR-pMHC를 슬립-결합으로 전환시킬 수 있으며, 이는 심지어 CD8에 비의존성인 pMHC에 결합하는 TCR에 대해서도 CD8-MHC 상호작용의 중요성을 강조한다.
CD8α는 CD8β보다 LCK에 대한 더 낮은 친화도를 가지며, 이는 CD8α 및 CD8β 둘다의 공동-발현 또는 세포외 CD8α 및 CD8β의 세포내 도메인을 함유하는 키메라 CD8α-CD8β 분자의 생성 중 어느 하나가 유효성을 개선시킬 수 있음을 시사한다. 본원에 기재된 CD8 구축물은 하기이다:
1. CD8α 동종이량체 (CD8 구축물 1)
2. CD8α-P2A-CD8β (CD8 구축물 2)
3. CD8β 세포내 도메인을 갖는 CD8α (CD8 구축물 3)
4. CD4 세포내 도메인을 갖는 CD8α 동종이량체 (CD8 구축물 4).
일부 실시양태에서, 상기 기재된 네오TCR 산물은 CD8 구축물 1, CD8 구축물 2, CD8 구축물 3, 또는 CD8 구축물 4 (각각의 CD8 산물)의 발현을 포함하는 추가의 변형을 포함한다. 구체적으로, 그 전문이 본원에 포함되는 PCT/US2020/17887 및 PCT/US2019/025415에 기재된 유전자 편집 기술 및 네오TCR 단리 기술을 사용하여, 네오TCR은 네오TCR을 발현하도록 조작된 정확성 게놈에 의해 (도 1a-1c에 기재된 바와 같은 DNA-매개 (비-바이러스) 방법을 사용하여) 암을 갖는 동일한 환자로부터의 자가 CD8+ 및 CD4+ T 세포에서 클로닝된다.
CD8 구축물 각각은, 발현되는 경우, CD8 산물을 생성한다. 표 1은 각각의 구축물 및 산물의 설명을 제공한다.
표 1. CD8 산물 및 CD8 구축물
특정 실시양태에서, CD8 산물 1은 네오TCR 및 CD8 동종이량체를 포함한다. 특정 실시양태에서, CD8 산물 1은 네오TCR, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인의 발현을 포함한다. 특정 실시양태에서, CD8 산물 1은 CD8α 신호 펩티드의 발현을 추가로 포함한다. 특정 실시양태에서, CD8 산물 1은 도 3a에 제시된 번역된 요소를 포함한다. 비-제한적인 예시적인 실시양태에서, CD8 산물 1은 네오TCR, CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142)을 포함한다. 특정 실시양태에서, 각각의 요소의 기능을 보존하거나 실질적으로 보존하는 CD8α 신호 펩티드, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인의 서열 변형은 이루어질 수 있다. 특정 실시양태에서, 이러한 서열 변형은 아미노산의 보존적 치환이다.
비-제한적 실시양태에서, CD8 산물 1은 도 6에 제공된 CD8 구축물 1로부터 제조된다. 특정 실시양태에서, 도 6에 제공된 CD8 구축물 1의 서열은 CD8α 신호 펩티드, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인의 번역이 보존된 기능을 갖는 각각의 요소를 남기는 한, 임의의 수의 방식으로 변형될 수 있다. 특정 실시양태에서, 도 6에서 CD8 구축물 1의 각각의 요소의 순서는 동일하게 남아 있지만, 각각의 개별적인 요소의 서열은 핵산이 코딩하는 아미노산이 동일하게 남아 있거나 단지 보존적 치환을 포함하는 한, 변화될 수 있다. 특정 실시양태에서, 도 6에서 CD8 구축물 1의 각각의 요소의 순서는 동일하게 남아 있지만, 각각의 개별적인 요소의 서열은 코딩된 단백질의 기능이 실질적으로 변화되지 않은 채 남아 있는 한, 변화될 수 있다.
특정 실시양태에서, CD8 산물 2는 네오TCR, CD8α, 및 CD8β를 포함한다. 특정 실시양태에서, CD8α 및 CD8β는 발현을 위한 CD8 산물 2 구축물에서의 프로테아제 절단 부위 및 2A 펩티드에 의해 분리된다. 특정 실시양태에서, CD8 산물 2는 네오TCR, CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인의 발현을 포함한다. 특정 실시양태에서, CD8 산물 2는 CD8α 신호 펩티드의 발현을 추가로 포함한다. 특정 실시양태에서, CD8 산물은 CD8β 신호 펩티드의 발현을 추가로 포함한다. 특정 실시양태에서, CD8 산물은 CD8α 신호 펩티드 및 CD8β 신호 펩티드의 발현을 추가로 포함한다. 특정 실시양태에서, CD8 산물 2는 도 3b에 제시된 번역된 요소를 포함한다. 비-제한적인 예시적인 실시양태에서, CD8 산물 2는 네오TCR, CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147)을 포함한다. 특정 실시양태에서, 각각의 요소의 기능을 보존하거나 실질적으로 보존하는 CD8α 신호 펩티드, CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인의 서열 변형이 이루어질 수 있다. 특정 실시양태에서, 이러한 서열 변형은 아미노산의 보존적 치환이다.
비-제한적 실시양태에서, CD8 산물 2는 도 7에 제공된 CD8 구축물 2로부터 제조된다. 특정 실시양태에서, 도 7에 제공된 CD8 구축물 2의 서열은 CD8α 신호 펩티드, CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인의 번역이 보존된 기능을 갖는 각각의 요소를 남기는 한, 임의의 수의 방식으로 변형될 수 있다. 특정 실시양태에서, 도 7에서 CD8 구축물 2의 각각의 요소의 순서는 동일하게 남아 있지만, 각각의 개별적인 요소의 서열은 핵산이 코딩하는 아미노산이 동일하게 남아 있거나 단지 보존적 치환을 포함하는 한, 변화될 수 있다. 특정 실시양태에서, 도 7에서 CD8 구축물 2의 각각의 요소의 순서는 동일하게 남아 있지만, 각각의 개별적인 요소의 서열은 코딩된 단백질의 기능이 실질적으로 변화되지 않은 채 남아 있는 한, 변화될 수 있다.
특정 실시양태에서, CD8 산물 3은 네오TCR 및 CD8β 세포내 도메인을 갖는 CD8α를 포함한다. 특정 실시양태에서, CD8 산물 3은 네오TCR, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인의 발현을 포함한다. 특정 실시양태에서, CD8 산물 3은 CD8α 신호 펩티드의 발현을 추가로 포함한다. 특정 실시양태에서, CD8 산물 3은 도 3c에 제시된 번역된 요소를 포함한다. 비-제한적인 예시적인 실시양태에서, CD8 산물 3은 네오TCR, CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147)을 포함한다. 특정 실시양태에서, 각각의 요소의 기능을 보존하거나 실질적으로 보존하는 CD8α 신호 펩티드, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인의 서열 변형이 이루어질 수 있다. 특정 실시양태에서, 이러한 서열 변형은 아미노산의 보존적 치환이다.
비-제한적 실시양태에서, CD8 산물 3은 도 8에 제공된 CD8 구축물 3으로부터 제조된다. 특정 실시양태에서, 도 8에 제공된 CD8 구축물 3의 서열은 CD8α 신호 펩티드, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인의 번역이 보존된 기능을 갖는 각각의 요소를 남기는 한, 임의의 수의 방식으로 변형될 수 있다. 특정 실시양태에서, 도 8에서 CD8 구축물 3의 각각의 요소의 순서는 동일하게 남아 있지만, 각각의 개별적인 요소의 서열은 핵산이 코딩하는 아미노산이 동일하게 남아 있거나 단지 보존적 치환을 포함하는 한, 변화될 수 있다. 특정 실시양태에서, 도 8에서 CD8 구축물 3의 각각의 요소의 순서는 동일하게 남아 있지만, 각각의 개별적인 요소의 서열은 코딩된 단백질의 기능이 실질적으로 변화되지 않은 채 남아 있는 한, 변화될 수 있다.
특정 실시양태에서, CD8 산물 4는 네오TCR 및 CD4 세포내 도메인을 갖는 CD8α 동종이량체를 포함한다. 특정 실시양태에서, CD8 산물 4는 네오TCR, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인의 발현을 포함한다. 특정 실시양태에서, CD8 산물 4는 CD8α 신호 펩티드의 발현을 추가로 포함한다. 특정 실시양태에서, CD8 산물 4는 도 3d에 제시된 번역된 요소를 포함한다. 비-제한적인 예시적인 실시양태에서, CD8 산물 4는 네오TCR, CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함한다. 특정 실시양태에서, 각각의 요소의 기능을 보존하거나 실질적으로 보존하는 CD8α 신호 펩티드, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인의 서열 변형이 이루어질 수 있다. 특정 실시양태에서, 이러한 서열 변형은 아미노산의 보존적 치환이다.
비-제한적 실시양태에서, CD8 산물 4는 도 9에 제공된 CD8 구축물 4로부터 제조된다. 특정 실시양태에서, 도 9에 제공된 CD8 구축물 4의 서열은 CD8α 신호 펩티드, CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인의 번역이 보존된 기능을 갖는 각각의 요소를 남기는 한, 임의의 수의 방식으로 변형될 수 있다. 특정 실시양태에서, 도 9에서 CD8 구축물 4의 각각의 요소의 순서는 동일하게 남아 있지만, 각각의 개별적인 요소의 서열은 핵산이 코딩하는 아미노산이 동일하게 남아 있거나 단지 보존적 치환을 포함하는 한, 변화될 수 있다. 특정 실시양태에서, 도 9에서 CD8 구축물 4의 각각의 요소의 순서는 동일하게 남아 있지만, 각각의 개별적인 요소의 서열은 코딩된 단백질의 기능이 실질적으로 변화되지 않은 채 남아 있는 한, 변화될 수 있다.
특정 실시양태에서, CD8 산물은 TET2 넉아웃 또는 TET2 넉다운을 포함한다. 특정 실시양태에서, CD8 산물의 세포는 비-바이러스 방법을 사용하여 TET2 유전자를 넉아웃시키도록 추가로 조작된다. 특정 실시양태에서, CD8 산물의 세포는 바이러스 방법을 사용하여 TET2 유전자를 넉아웃시키도록 추가로 조작된다. 특정 실시양태에서, CD8 산물의 세포는 비-바이러스 방법을 사용하여 T 세포 존속과 연관된 유전자의 기능을 넛아웃시키거나, 넉다운시키거나, 변형시킴으로써 T 세포 존속을 증가시키도록 추가로 조작된다. 특정 실시양태에서, CD8 산물의 세포는 바이러스 방법을 사용하여 T 세포 존속과 연관된 유전자의 기능을 넛아웃시키거나, 넉다운시키거나, 변형시킴으로써 T 세포 존속을 증가시키도록 추가로 조작된다.
일부 실시양태에서, CD8 산물은 바이러스 방법을 사용하여 네오TCR 및 CD8 구축물을 발현하도록 조작된 세포를 포함한다 (즉, CD8 바이러스 산물). 특정 실시양태에서, CD8 바이러스 산물의 세포는 비-바이러스 방법을 사용하여 TET2 유전자를 넉아웃시키도록 추가로 조작된다. 특정 실시양태에서, CD8 바이러스 산물의 세포는 바이러스 방법을 사용하여 TET2 유전자를 넉아웃시키도록 추가로 조작된다. 특정 실시양태에서, CD8 바이러스 산물의 세포는 비-바이러스 방법을 사용하여 T 세포 존속과 연관된 유전자의 기능을 넛아웃시키거나, 넉다운시키거나, 변형시킴으로써 T 세포 존속을 증가시키도록 추가로 조작된다. 특정 실시양태에서, CD8 바이러스 산물의 세포는 바이러스 방법을 사용하여 T 세포 존속과 연관된 유전자의 기능을 넛아웃시키거나, 넉다운시키거나, 변형시킴으로써 T 세포 존속을 증가시키도록 추가로 조작된다.
특정 실시양태에서, 넉아웃되거나, 넉다운되거나, 변형된 기능을 갖는 T 세포 존속 유전자는 T 세포 활성의 하향조절을 부여하는 유전자이다. 특정 실시양태에서, 넉아웃되거나, 넉다운되거나, 변형된 유전자는 T 세포 기억 기능을 하향조절하는 유전자이다. 특정 실시양태에서, 넉아웃되거나, 넉다운되거나, 변형된 유전자는 T-세포 기능, 증식, 및/또는 생존을 감소시키는 유전자이다.
특정 실시양태에서, CD8 산물 및 그의 CD8 세포에 대한 추가의 변형은 종양 미세환경 회복력을 증가시키고, T 세포 활성을 증가시키고, 종양 미세환경 귀소/체류를 증가시키고, T 세포 존속을 증가시키고, T 세포의 이소성 이펙터 기능을 증가시키는 변형을 포함한다. 특정 실시양태에서, 종양 미세환경 회복력은 음성 환경적 신호를 전환시키는/반대작용하는 것을 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, TCR-매개 신호 증진은 T 세포 활성을 증가시키는 것을 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, 종양 미세환경 귀소/체류는 종양 침윤을 증진시키는 것을 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, 기능적 T 세포 존속은 대사 및 전사 조절을 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, 이소성 이펙터 기능은 TCR-유도된 항체, 시토카인, 또는 펩티드 분비를 포함하나 이에 제한되지는 않는다.
특정 실시양태에서, 기능적 T 세포 존속은 본원에 기재된 바와 같은 유전자 조작에 의해, 변형된 T 세포 (본원에 기재된 바와 같은 적어도 네오TCR을 혼입하도록 변형됨)의 기능적 T 세포 존속을 개선시키는 제약 작용제의 공동-투여에 의해, 및 변형된 T 세포 (본원에 기재된 바와 같은 적어도 네오TCR을 혼입하도록 변형됨)의 제조 및 배양 조건에 의해 달성될 수 있다.
특정 실시양태에서, 이소성 이펙터 기능을 개선시키는데 사용되는 TCR-유도된 항체는 본원에 기재된 항체 또는 기능적 그의 단편 중 어느 하나이다. 특정 실시양태에서, 이소성 이펙터 기능을 개선시키는데 사용되는 TCR-유도된 시토카인은 천연 발생 시토카인, 변형된 시토카인, 시토카인의 융합 단백질, 또는 이들의 임의의 조합이다. 특정 실시양태에서, TCR-유도된 시토카인은 시토카인이 아니지만, 오히려 내인성 시토카인 생산을 유도하는 다른 보조-인자 또는 발현 요소이다.
특정 실시양태에서, CD8 산물 및 그의 CD8 세포에 대한 추가의 변형은 1종 이상의 추가의 유전자 및/또는 기능적 단백질을 넉인시키는 변형을 포함한다. 특정 실시양태에서, 넉인된 유전자 및/또는 기능적 단백질은 c-Myb, 우성 음성 FAS, FAS 말단절단물, FBXW7, CTP1A, OPA1, GLUT1, CA-STAT5A, 우성 음성 TGFβR, DNMT3a, 우성 음성 PD-1R, 우성 음성 PD-1 또는 PD-L1, 또는 PD-L2, 우성 음성 SHIP-1 단백질, 인테그린, 케모카인 수용체, 시토카인, 및 인터류킨을 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, 유전자의 우성 음성 형태는 유전자의 길항제인 항체 또는 그의 기능적 단편이다. 예를 들어, 우성 음성 PD-1은 항-PD-1 항체 또는 그의 기능적 단편일 수 있다. 특정 실시양태에서, 임의의 넉인 유전자 및/또는 기능적 단백질은 유전자 및/또는 단백질의 기능적 단편 (말단절단물을 포함하나 이에 제한되지는 않음)이다.
특정 실시양태에서, CD8 산물 및 그의 CD8 세포에 대한 추가의 변형은 1종 이상의 추가의 유전자 및/또는 기능적 단백질을 넉아웃 또는 넉다운시키는 변형을 포함한다. 특정 실시양태에서, 넉아웃되거나 넉다운된 유전자 및/또는 기능적 단백질은 TET2, IFNGR1, RICTOR, NR4A1, DNMT3A, SUV39H1, PPP2RD, 아데노신 2A 수용체, PP2A3, 및 PP2A4를 포함하나 이에 제한되지는 않는다.
특정 실시양태에서, 기능적 단백질의 발현을 위한 유전자를 넉인시키는 대신, 상이한 유전자는 그렇지 않다면 넉인될 유전자의 발현을 상향조절하는 본원에 기재된 유전자 조작을 통해 조정될 수 있다.
특정 실시양태에서, 유전자를 넉아웃시키거나 넉다운시키는 대신, 상이한 유전자는 그렇지 않다면 넉아웃될 유전자의 발현을 하향조절하는 본원에 기재된 유전자 조작을 통해 조정될 수 있다.
CD8 산물 제조 프로세스는 가이드 RNA 서열에 결합된 CRISPR-Cas9 뉴클레아제의 이중 리보핵단백질 종의 전기천공을 수반하며, 각각의 종은 게놈 TCRα 및 게놈 TCRβ 로커스를 표적화한다. Cas9 뉴클레아제를 각각의 게놈 로커스에 표적화하는 특이성은 고도로 특이적인 것으로 문헌에 이전에 기재되었다. 각각 COSMID 및 GUIDE-seq를 사용하여, CD8 산물의 포괄적인 시험을 시험관내에서 및 인 실리코 분석에서 수행하여 가능한 오프-타겟 게놈 절단 부위를 조사하였다. 건강한 공여자로부터의 다중 CD8 산물 또는 필적하는 세포 산물을 딥 시퀀싱에 의해 후보 오프-타겟 부위의 절단에 대해 평가하였으며, 이는 선택된 뉴클레아제가 고도로 특이적이라는 공개된 증거를 뒷받침한다.
특정 실시양태에서, 본원에 기재된 CD8 산물은 T 세포, NK 세포, NKT 세포, 대식세포, 조혈 줄기 세포 (HSC), HSC로부터 유래된 세포, 또는 수지상/항원-제시 세포일 수 있다.
특정 실시양태에서, CD8 세포는 "어린" T 세포 표현형을 보존하는 방식으로 확장되어, T 세포의 대다수가 T 기억 줄기 세포 및 T 중심 기억 표현형을 나타내는 CD8 산물을 생성한다.
이들 '어린' 또는 '보다 어린' 또는 덜-분화된 T 세포 표현형은 개선된 그라프팅 잠재성 및 주입 후 연장된 존속을 부여하는 것으로 기재된다. 따라서, 유의하게 '어린' T 세포 표현형으로 이루어진 CD8 산물의 투여는 개선된 그라프팅 잠재성, 주입 후 연장된 존속, 및 신체 전반에 걸쳐 종양 세포를 근절시키는 이펙터 T 세포로의 급속한 분화를 통해, 암을 갖는 환자를 유익하게 할 잠재성을 갖는다.
특정 실시양태에서, CD8 산물의 CD8 세포는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 우세하게 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 적어도 25%는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 적어도 30%는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 적어도 35%는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 적어도 40%는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 적어도 45%는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 적어도 50%는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 적어도 55%는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 적어도 60%는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 적어도 65%는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 적어도 70%는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 적어도 75%는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. 특정 실시양태에서, CD8 산물의 CD8 세포의 75% 초과는 기억 줄기 세포 (Tmsc) 및/또는 중심 기억 세포 (Tcm)를 포함한다. Tmsc는 CD45RA+CD62L+, CD28+CD95+, 및 CCR7+CD27+인 세포로서 특징규명된다. Tcm은 CD45RO+CD62L+, CD28+CD95+, 및 CCR7+CD27+CD127+인 세포로서 특징규명된다. Tmsc 및 Tcm 둘 다는 약한 이펙터 T 세포 기능, 왕성한 증식, 왕성한 그라프팅, 및 긴 텔로미어를 갖는 것으로서 특징규명된다.
특정 실시양태에서, 본원에 개시된 CD8 세포는 CD8 구축물을 갖지 않는 세포와 비교하여 약 10%, 약 20%, 약 30%, 약 40%, 약 50%, 약 60%, 약 70%, 약 80%, 약 100%, 약 150%, 약 200%, 약 250%, 약 300%, 약 350%, 약 400%, 약 450%, 또는 약 500%의 개선된 특성 (예를 들어, 살해 활성, 세포 증식, 시토카인의 분비, LCK 친화도, 존속, 종양 침윤 능력)을 나타낸다.
어린 표현형을 갖는 CD8 산물을 제조하는 방법
특정 실시양태에서, 본 개시내용은 부분적으로 조작된 "어린" T 세포의 제조에 관한 것이다. 특정 실시양태에서, 본 개시내용은 원래 대상체로부터 수득되거나 이러한 샘플로부터 단리된 항원-특이적 세포를 활성화시키고, 조작하고, 확장시키는 것을 포함하는, 생체외에서 항원-특이적 세포, 예를 들어, T 세포를 제조하는 방법을 포함한다.
특정 실시양태에서, 세포를 활성화시키는 방법은 TCR/CD3 복합체를 활성화시키는 단계를 포함한다. 예를 들어, 제한 없이, T 세포는 CD3 효능제, CD28 효능제, 또는 이들의 조합과 함께 인큐베이션되고/거나 배양될 수 있다.
특정 실시양태에서, 조작된 활성화된 항원-특이적 세포, 예를 들어, 조작된 활성화된 T 세포는 조작된 활성화된 항원-특이적 세포, 예를 들어, T 세포를 시토카인, 케모카인, 가용성 펩티드, 또는 이들의 조합과 함께 배양함으로써 확장될 수 있다. 특정 실시양태에서, 조작된 활성화된 항원-특이적 세포, 예를 들어, 조작된 활성화된 T 세포는 1종 이상의 시토카인과 함께 배양될 수 있다. 특정 실시양태에서, 시토카인은 IL2, IL7, IL15, 또는 이들의 조합일 수 있다. 예를 들어, 조작된 활성화된 항원-특이적 세포, 예를 들어, 조작된 활성화된 T 세포는 IL7 및 IL15와 함께 배양될 수 있다. 특정 실시양태에서, 조작된 활성화된 항원-특이적 세포, 예를 들어, 조작된 활성화된 T 세포 배양과 관련하여 사용된 시토카인은 약 1 pg/ml 내지 약 1 g/ml, 약 1 ng/ml 내지 약 1 g/ml, 약 1 μg/ml 내지 약 1 g/ml, 또는 약 1 mg/ml 내지 약 1g/ml, 및 그 사이에 있는 임의의 값의 농도로 존재할 수 있다.
제약 제제.
CD8 산물의 제약 제제는 세포의 '어린' 표현형을 동결보존된 상태로 보존할 수 있는 용액에서 CD8 세포를 배합함으로써 제조된다. 표 1은 한 이러한 제약 제제의 예를 제공한다. 대안적으로, CD8 산물의 제약 제제는 세포의 '어린' 표현형을 산물을 동결하거나 동결보존할 필요 없이 보존할 수 있는 용액에서 CD8 세포를 배합함으로써 제조될 수 있다 (즉, CD8 산물은 수용액에서 또는 비-동결된/동결보존된 세포 펠릿으로서 유지된다).
추가의 제약상 허용되는 담체, 완충제, 안정화제, 및/또는 보존제는 또한 동결보존 용액 또는 수성 저장 용액 (CD8 산물이 동결보존되지 않는 경우)에 첨가될 수 있다. 크리오스토르, 크리오스토르 CS5, 셀뱅커(CELLBANKER), 및 DMSO를 임의로 포함하는 주문제작 동결보존 배지를 포함하나 이에 제한되지는 않는 임의의 동결보존제 및/또는 배지는 CD8 산물을 동결보존하는데 사용될 수 있다.
유전자-편집 방법
특정 실시양태에서, 본 개시내용은 부분적으로 인간 세포, 예를 들어, 조작된 T 세포 또는 조작된 인간 줄기 세포를 조작하는 방법을 수반한다. 특정 실시양태에서, 본 개시내용은 부분적으로 인간 세포, 예를 들어, NK 세포, NKT 세포, 대식세포, 조혈 줄기 세포 (HSC), HSC로부터 유래된 세포, 또는 수지상/항원-제시 세포를 조작하는 방법을 수반한다. 특정 실시양태에서, 이러한 조작은 게놈 편집을 수반한다. 예를 들어 (그러나 제한은 아님), 이러한 게놈 편집은 1개 이상의 내인성 로커스, 예를 들어, TCR 알파 (TCRα) 로커스 및 TCR 베타 (TCRβ) 로커스를 표적화하는 뉴클레아제로 달성될 수 있다. 특정 실시양태에서, 뉴클레아제는 내인성 표적 서열에서 단일-가닥 DNA 닉 또는 이중-가닥 DNA 파단을 생성할 수 있다. 특정 실시양태에서, 뉴클레아제는 게놈의 코딩 또는 비-코딩 부분, 예를 들어, 엑손, 인트론을 표적화할 수 있다. 특정 실시양태에서, 본원에서 고려되는 뉴클레아제는 귀소 엔도뉴클레아제, 메가뉴클레아제, 메가TAL 뉴클레아제, 전사 활성화제-유사 이펙터 뉴클레아제 (TALEN), 아연-핑거 뉴클레아제 (ZFN), 및 클러스터링된 규칙적 간격의 짧은 회문구조 반복부 (CRISPR)/Cas 뉴클레아제를 포함한다. 특정 실시양태에서, 뉴클레아제는 자체가 예를 들어, 아미노산 치환 및/또는 결실의 도입을 통해, 커팅 활성의 효율을 증가시키도록 조작될 수 있다.
특정 실시양태에서, CRISPR/Cas 뉴클레아제 시스템은 인간 세포를 조작하는데 사용된다. 특정 실시양태에서, CRISPR/Cas 뉴클레아제 시스템은 Cas 뉴클레아제, 및 Cas 뉴클레아제를 내인성 표적 서열에 동원하는 1개 이상의 RNA, 예를 들어, 단일 가이드 RNA를 포함한다. 특정 실시양태에서, Cas 뉴클레아제 및 RNA는 세포에서 예를 들어 상이한 벡터 또는 조성물을 사용하여 별개로, 또는 예를 들어, 폴리시스트론성 구축물 또는 단일 단백질-RNA 복합체에서 함께 도입된다. 특정 실시양태에서, Cas 뉴클레아제는 Cas9 또는 Cas12a이다. 특정 실시양태에서, Cas9 폴리펩티드는 제한 없이, 스트렙토코쿠스 피오게네스(Streptococcus pyogenes) 또는 네이세리아 메넨기티디스(Neisseria menengitidis)를 포함하는 박테리아 종으로부터 수득된다. CRISPR/Cas 시스템의 추가의 예는 관련 기술분야에 공지되어 있다. 그것이 교시하는 전부에 대해 본원에 참조로 포함되는 문헌 [Adli, Mazhar. "The CRISPR tool kit for genome editing and beyond." Nature communications vol. 9,1 1911 (2018)]을 참조한다.
특정 실시양태에서, 게놈 편집은 면역학적 반응을 조절하는 1개 이상의 게놈 로커스에서 일어난다. 특정 실시양태에서, 로커스는 제한 없이, TCR 알파 (TCRα) 로커스, TCR 베타 (TCRβ) 로커스, TCR 감마 (TCRγ), 및 TCR 델타 (TCRδ)를 포함한다. 특정 실시양태에서, CD8 구축물을 삽입하기 위한 로커스는 게놈의 어디에나 있다. 특정 실시양태에서, CD8 구축물을 삽입하기 위한 로커스는 TRAC 로커스이다. 특정 실시양태에서, CD8 구축물을 삽입하기 위한 로커스는 2개의 TRBC 로커스 중 하나이다. 특정 실시양태에서, CD8 구축물을 삽입하기 위한 로커스는 TRAC 로커스 또는 TRAB 로커스 이외의 로커스이다. 특정 실시양태에서, CD8 구축물을 삽입하기 위한 로커스는 유전자 로커스 내로 삽입되며, 여기서 이러한 유전자는 넉아웃된다. 비-제한적 예로서, CD8 산물의 목적하는 표현형이 네오TCR의 발현, CD8 구축물의 발현, 및 TET2 유전자 또는 AAVS1 유전자의 넉아웃인 경우, CD8 구축물은 TET2 로커스 또는 AAVS1 로커스에서 삽입될 수 있다. 특정 실시양태에서, CD8 구축물의 삽입은 네오TCR 삽입과 나란하다. 특정 실시양태에서, CD8 구축물의 삽입은 네오TCR 삽입과는 별개의 로커스이다.
특정 실시양태에서, 게놈 편집은 비-바이러스 전달 시스템을 사용함으로써 수행된다. 예를 들어, 핵산 분자는 핵산을 리포펙션 (Feigner et al., Proc. Natl. Acad. Sci. U.S.A. 84:7413, 1987; Ono et al., Neuroscience Letters 17:259, 1990; Brigham et al., Am. J. Med. Sci. 298:278, 1989; Staubinger et al., Methods in Enzymology 101:512, 1983), 아시알로오로소뮤코이드-폴리리신 접합 (Wu et al., Journal of Biological Chemistry 263:14621, 1988; Wu et al., Journal of Biological Chemistry 264:16985, 1989)의 존재 하에서, 또는 외과적 조건 하에서의 미세-주사에 의해 (Wolff et al., Science 247:1465, 1990) 투여함으로써 세포 내로 도입될 수 있다. 유전자 전달을 위한 다른 비-바이러스 수단은 인산칼슘, DEAE 덱스트란, 전기천공, 및 원형질체 융합을 사용한 시험관내에서의 형질감염을 포함한다. 리포솜은 또한 세포 내로의 DNA의 전달을 위해 잠재적으로 유익할 수 있다. 대상체의 질환에 걸린 조직 내로의 정상 유전자의 이식은 또한 정상 핵산을 생체외에서 배양가능한 세포 유형 (예를 들어, 자가 또는 이종 1차 세포 또는 그의 자손) 내로 전달하고, 그 후 세포 (또는 그의 후손)를 표적화된 조직 내로 주사하거나, 전신적으로 주사함으로써 달성될 수 있다.
특정 실시양태에서, 게놈 편집은 바이러스 전달 시스템을 사용함으로써 수행된다. 특정 실시양태에서, 바이러스 방법은 표적화된 통합 (AAV를 포함하나 이에 제한되지는 않음) 및 무작위 통합 (렌티바이러스 접근법을 포함하나 이에 제한되지는 않음)을 포함한다. 특정 실시양태에서, 바이러스 전달은 뉴클레아제의 통합 없이 달성될 것이다. 이러한 실시양태에서, 바이러스 전달 시스템은 렌티플래쉬(Lentiflash) 또는 또 다른 유사한 전달 시스템일 수 있다.
상동성 재조합 주형
특정 실시양태에서, 본 개시내용은 상동성 재조합 (HR) 주형 핵산 서열을 세포의 내인성 로커스 내로 도입하고 재조합하는 것에 의한 세포의 게놈 편집을 제공한다. 특정 실시양태에서, HR 주형 핵산 서열은 선형이다. 특정 실시양태에서, HR 주형 핵산 서열은 원형이다. 특정 실시양태에서, 원형 HR 주형은 플라스미드, 미니서클, 또는 나노플라스미드일 수 있다. 특정 실시양태에서, HR 주형 핵산 서열은 제1 및 제2 상동성 아암을 포함한다. 특정 실시양태에서, 상동성 아암은 약 300개 염기 내지 약 2,000개 염기의 것일 수 있다. 예를 들어, 각각의 상동성 아암은 1,000개 염기일 수 있다. 특정 실시양태에서, 상동성 아암은 세포의 제1 및 제2 내인성 서열에 대해 상동성일 수 있다. 특정 실시양태에서, 내인성 로커스는 TCR 로커스이다. 예를 들어, 제1 및 제2 내인성 서열은 TCR 알파 로커스 또는 TCR 베타 로커스 내에 있다. 특정 실시양태에서, HR 주형은 TCR 유전자 서열을 포함한다. 비-제한적 실시양태에서, TCR 유전자 서열은 환자 특이적 TCR 유전자 서열이다. 비-제한적 실시양태에서, TCR 유전자 서열은 종양-특이적이다. 비-제한적 실시양태에서, TCR 유전자 서열은 그의 내용이 본원에 참조로 포함되는 PCT/US2020/017887에 기재된 방법을 사용하여 확인되고 수득될 수 있다. 특정 실시양태에서, HR 주형은 TCR 알파 유전자 서열 및 TCR 베타 유전자 서열을 포함한다.
특정 실시양태에서, HR 주형은 폴리시스트론성 폴리뉴클레오티드이다. 특정 실시양태에서, HR 주형은 유연성 폴리펩티드 서열 (예를 들어, Gly-Ser-Gly 서열)을 코딩하는 서열을 포함한다. 특정 실시양태에서, HR 주형은 내부 리보솜 진입 부위 (IRES)를 코딩하는 서열을 포함한다. 특정 실시양태에서, HR 주형은 2A 펩티드 (예를 들어, P2A, T2A, E2A, 및 F2A)를 포함한다. HR 주형 핵산 및 그의 세포를 변형시키는 방법에 대한 추가의 정보는 그의 내용이 본원에 참조로 포함되는 국제 특허 출원 번호 PCT/US2018/058230에서 발견될 수 있다.
치료 방법
본 개시된 대상은 면역 반응의 유도 및/또는 증가를 필요로 하는 대상체에서 면역 반응을 유도하고/거나 증가시키는 방법을 제공한다. CD8 산물은 대상체에서 암을 치료하고/거나 예방하는데 사용될 수 있다. CD8 산물은 암을 앓고 있는 대상체의 생존을 연장시키는데 사용될 수 있다. CD8 산물은 또한 대상체에서 암을 치료하고/거나 예방하는데 사용될 수 있다. CD8 산물은 또한 대상체에서 종양 부담을 감소시키는데 사용될 수 있다. 이러한 방법은 유효량으로 CD8 산물 또는 이를 포함하는 조성물 (예를 들어, 제약 조성물)을 투여하여, 기존의 상태의 경감 또는 재발의 방지인 목적하는 효과를 달성하는 것을 포함한다. 치료를 위해, 투여되는 양은 목적하는 효과를 생성하는데 있어서 유효한 양이다. 유효량은 하나 또는 일련의 투여로 제공될 수 있다. 유효량은 볼루스로 또는 연속적 관류에 의해 제공될 수 있다.
특정 실시양태에서, CD8 산물은 바이러스성 또는 박테리아성 질환을 치료하는데 사용될 수 있다. 특정 실시양태에서, CD8 산물은 자가면역 질환을 치료하는데 사용될 수 있다.
특정 실시양태에서, CD8 산물의 유효량은 IV 투여를 통해 전달된다. 특정 실시양태에서, CD8 산물은 단일 투여로 IV 투여를 통해 전달된다. 특정 실시양태에서, CD8 산물은 다중 투여로 IV 투여를 통해 전달된다. 특정 실시양태에서, CD8 산물은 2회 이상의 투여로 IV 투여를 통해 전달된다. 특정 실시양태에서, CD8 산물은 2회의 투여로 IV 투여를 통해 전달된다. 특정 실시양태에서, CD8 산물은 3회의 투여로 IV 투여를 통해 전달된다.
본 개시된 대상은 대상체에서 암을 치료하고/거나 예방하는 방법을 제공한다. 특정 실시양태에서, 방법은 유효량의 CD8 산물을 암을 갖는 대상체에게 투여하는 것을 포함한다.
암의 비-제한적 예는 혈액암 (예를 들어 백혈병, 림프종, 및 골수종), 난소암, 유방암, 방광암, 뇌암, 결장암, 장암, 간암, 폐암, 췌장암, 전립선암, 피부 암, 위암, 교모세포종, 인후암, 흑색종, 신경모세포종, 선암종, 신경아교종, 연조직 육종, 및 다양한 암종 (전립선 및 소세포 폐암을 포함함)을 포함한다. 적합한 암종은 성상세포종, 섬유육종, 점액육종, 지방육종, 희소돌기아교세포종, 뇌실막세포종, 수모세포종, 원시 신경 외배엽 종양 (PNET), 연골육종, 골원성 육종, 췌장 관 선암종, 소 및 대 세포 폐 선암종, 척삭종, 혈관육종, 내피육종, 편평 세포 암종, 기관지폐포암종, 상피 선암종, 및 그의 간 전이, 림프관육종, 림프관내피육종, 간암, 담관암종, 윤활막종, 중피종, 유잉 종양, 횡문근육종, 결장 암종, 기저 세포 암종, 한선 암종, 유두상 암종, 피지선 암종, 유두상 선암종, 낭선암종, 수질 암종, 기관지원성 암종, 신세포 암종, 담관 암종, 융모막암종, 고환종, 배아 암종, 윌름스 종양, 고환 종양, 수모세포종, 두개인두종, 뇌실막세포종, 송과체종, 혈관모세포종, 청신경 집종, 희소돌기아교세포종, 수막종, 신경모세포종, 망막모세포종, 백혈병, 다발성 골수종, 발덴스트롬 마크로글로불린혈증, 및 중쇄 질환, 유방 종양, 예컨대 도관 및 소엽 선암종, 자궁 경부의 편평 및 선암종, 자궁 및 난소 상피 암종, 전립선 선암종, 방광의 이행 편평 세포 암종, B 및 T 세포 림프종 (결절성 및 미만성) 형질세포종, 급성 및 만성 백혈병, 악성 흑색종, 연조직 육종 및 평활근육종을 포함하나 이에 제한되지는 않는 종양학의 분야에 공지된 임의의 것을 추가로 포함한다. 특정 실시양태에서, 신생물은 혈액암 (예를 들어 백혈병, 림프종, 및 골수종), 난소암, 전립선암, 유방암, 방광암, 뇌암, 결장암, 장암, 간암, 폐암, 췌장암, 전립선암, 피부암, 위암, 교모세포종, 및 인후암으로 이루어진 군으로부터 선택된다. 특정 실시양태에서, 본 개시된 어린 T 세포 및 이를 포함하는 조성물은 통상적인 치료 개입으로 처리할 수 없는 혈액암 (예를 들어, 백혈병, 림프종, 및 골수종) 또는 난소암을 치료하고/거나 예방하는데 사용될 수 있다.
특정 실시양태에서, 신생물은 고형 암 또는 고형 종양이다. 특정 실시양태에서, 고형 종양 또는 고형 암은 교모세포종, 전립선 선암종, 신장 유두상 세포 암종, 육종, 난소암, 췌장 선암종, 직장 선암종, 결장 선암종, 식도 암종, 자궁 체부 자궁내막모양 암종, 유방암, 피부 피부 흑색종, 폐 선암종, 위 선암종, 자궁경부 및 자궁경관내 암, 신장 투명 세포 암종, 고환 배 세포 종양, 및 공격성 B-세포 림프종으로 이루어진 군으로부터 선택된다.
대상체는 질환의 진행된 형태를 가질 수 있으며, 이 경우 치료 목적은 질환 진행의 완화 또는 반전, 및/또는 부작용의 개선을 포함할 수 있다. 대상체는 그들이 이미 치료된 상태의 병력을 가질 수 있으며, 이 경우 치료 목적은 전형적으로 재발의 위험을 감소시키거나 지연시키는 것을 포함할 것이다.
요법을 위한 적합한 인간 대상체는 전형적으로 임상적 기준에 의해 구별될 수 있는 2개의 치료 군을 포함한다. "진행된 질환" 또는 "높은 종양 부담"을 갖는 대상체는 임상적으로 측정가느안 종양을 갖는 것들이다. 임상적으로 측정가능한 종양은 종양 질량에 기반하여 검출될 수 있는 것이다 (예를 들어, 촉진, CAT 스캔, 초음파도, 유방촬영상 또는 X-선에 의해; 그들 자신 상의 양성 생화학적 또는 조직병리학적 마커는 이 집단을 확인하는데 불충분함). 제약 조성물은 그들의 상태를 경감시킬 목적으로 항-종양 반응을 유발하기 위해 이들 대상체에게 투여된다. 이상적으로, 종양 질량의 감소는 결과로서 일어나지만, 임의의 임상적 개선은 유익을 구성한다. 임상적 개선은 진행의 감소된 위험 또는 속도 또는 종양의 병리학적 결과의 감소를 포함한다.
제조품
CD8 산물은 제조품과 조합으로 사용될 수 있다. 이러한 제조품은 증식성 장애 (예를 들어, 암)의 예방 또는 치료에 유용할 수 있다. 제조품의 예는 용기 (예를 들어, 주입 백, 보틀, 저장 용기, 플라스크, 바이알, 시린지, 튜브, 및 IV 용액 백) 및 용기 상의 또는 그와 연관된 표지 또는 패키지 삽입물을 포함하나 이에 제한되지는 않는다. 용기는 CD8 산물 내의 CD8 세포의 저장 및 보존을 위해 허용되는 임의의 물질로 제조될 수 있다. 특정 실시양태에서, 용기는 피하 주사 바늘에 의해 천공가능한 스토퍼를 갖는 정맥내 용액 백 또는 바이알일 수 있다. 예를 들어, 용기는 크리오맥스(CryoMACS) 동결 백일 수 있다. 표지 또는 패키지 삽입물은 CD8 산물이 선택의 상태 및 기원의 환자를 치료하는데 사용됨을 지시한다. 환자는 CD8 산물의 용기 상에서 확인되는데, 이는 CD8 산물이 자가 세포로부터 제조되고, 환자-특이적 및 개별화된 치료로서 조작되기 때문이다.
제조품은 1) 그 안에 함유된 CD8 산물을 갖는 제1 용기를 포함할 수 있다.
제조품은 1) 그 안에 함유된 CD8 산물을 갖는 제1 용기; 및 2) 그 안에 함유된 제1 용기와 동일한 CD8 산물을 갖는 제2 용기를 포함할 수 있다. 임의로, 제1 및 제2 용기와 동일한 CD8 산물을 갖는 추가의 용기가 제조되고 만들어질 수 있다. 임의로, 상이한 세포독성제 또는 다르게는 치료제를 포함하는 조성물을 함유하는 추가의 용기는 또한 상기 기재된 용기와 조합될 수 있다.
제조품은 1) 그 안에 함유된 CD8 산물을 갖는 제1 용기; 및 2) 그 안에 함유된 조성물을 갖는 제2 용기를 포함할 수 있으며, 여기서 조성물은 추가의 세포독성제 또는 다르게는 치료제를 포함한다.
제조품은 1) 그 안에 함유된 2종의 CD8 산물을 갖는 제1 용기; 및 2) 그 안에 함유된 조성물을 갖는 제2 용기를 포함할 수 있으며, 여기서 조성물은 추가의 세포독성제 또는 다르게는 치료제를 포함한다.
제조품은 1) 그 안에 함유된 CD8 산물을 갖는 제1 용기; 2) 그 안에 함유된 제2 CD8 산물을 갖는 제2 용기; 및 3) 임의로 그 안에 함유된 조성물을 갖는 제3 용기를 포함할 수 있으며, 여기서 조성물은 추가의 세포독성제 또는 다르게는 치료제를 포함한다. 특정 실시양태에서, 제1 및 제2 CD8 산물은 상이한 CD8 산물이다. 특정 실시양태에서, 제1 및 제2 CD8 산물은 동일한 CD8 산물이다.
제조품 1) 그 안에 함유된 3종의 CD8 산물을 갖는 제1 용기; 및 2) 임의로 그 안에 함유된 조성물을 갖는 제2 용기를 포함할 수 있으며, 여기서 조성물은 추가의 세포독성제 또는 다르게는 치료제를 포함한다.
제조품은 1) 그 안에 함유된 CD8 산물을 갖는 제1 용기; 2) 그 안에 함유된 제2 CD8 산물을 갖는 제2 용기; 3) 그 안에 함유된 제3 CD8 산물을 갖는 제3 용기; 및 4) 임의로 그 안에 함유된 조성물을 갖는 제4 용기를 포함할 수 있으며, 여기서 조성물은 추가의 세포독성제 또는 다르게는 치료제를 포함한다. 특정 실시양태에서, 제1, 제2, 및 제3 CD8 산물은 상이한 CD8 산물이다. 특정 실시양태에서, 제1, 제2, 및 제3 CD8 산물은 동일한 CD8 산물이다. 특정 실시양태에서, 제1, 제2, 및 제3 CD8 산물 중 2개는 동일한 CD8 산물이다.
제조품은 1) 그 안에 함유된 4종의 CD8 산물을 갖는 제1 용기; 및 2) 임의로 그 안에 함유된 조성물을 갖는 제2 용기를 포함할 수 있으며, 여기서 조성물은 추가의 세포독성제 또는 다르게는 치료제를 포함한다.
제조품은 1) 그 안에 함유된 CD8 산물을 갖는 제1 용기; 2) 그 안에 함유된 제2 CD8 산물을 갖는 제2 용기; 3) 그 안에 함유된 제3 CD8 산물을 갖는 제3 용기; 4) 그 안에 함유된 제4 CD8 산물을 갖는 제4 용기; 및 5) 임의로 그 안에 함유된 조성물을 갖는 제5 용기를 포함할 수 있으며, 여기서 조성물은 추가의 세포독성제 또는 다르게는 치료제를 포함한다. 특정 실시양태에서, 제1, 제2, 제3, 및 제4 CD8 산물은 상이한 CD8 산물이다. 특정 실시양태에서, 제1, 제2, 제3, 및 제4 CD8 산물은 동일한 네오TCR 산물이다. 특정 실시양태에서, 제1, 제2, 제3, 및 제4 CD8 산물 중 2개는 동일한 네오TCR 산물이다. 특정 실시양태에서, 제1, 제2, 제3, 및 제4 CD8 산물 중 3개는 동일한 CD8 산물이다.
제조품은 1) 그 안에 함유된 5종 이상의 CD8 산물을 갖는 제1 용기; 및 2) 임의로 그 안에 함유된 조성물을 갖는 제2 용기를 포함할 수 있으며, 여기서 조성물은 추가의 세포독성제 또는 다르게는 치료제를 포함한다.
제조품은 1) 그 안에 함유된 CD8 산물을 갖는 제1 용기; 2) 그 안에 함유된 제2 CD8 산물을 갖는 제2 용기; 3) 그 안에 함유된 제3 CD8 산물을 갖는 제3 용기; 4) 그 안에 함유된 제4 CD8 산물을 갖는 제4 용기; 5) 그 안에 함유된 제5 CD8 산물을 갖는 제5 용기; 6) 임의로 그 안에 함유된 제6 이상의 CD8 산물을 갖는 제6 이상의 추가의 용기; 및 7) 임의로 그 안에 함유된 조성물을 갖는 추가의 용기를 포함할 수 있으며, 여기서 조성물은 추가의 세포독성제 또는 다르게는 치료제를 포함한다. 특정 실시양태에서, CD8 산물의 모든 용기는 상이한 CD8 산물이다. 특정 실시양태에서, CD8 산물의 모든 용기는 동일한 CD8 산물이다. 특정 실시양태에서, 환자의 종양 샘플(들)에서 검출가능한 CD8의 이용가능성, 환자에 대한 다중 CD8 산물을 가질 필요성 및/또는 목적, 및 1개 이상의 용기를 요구하거나 그로부터 이익을 얻을 수 있는 어느 하나의 CD8 산물의 이용가능성에 기반하여 5개 이상의 용기에 동일하거나 상이한 CD8 산물의 임의의 조합이 있을 수 있다.
제조품은 1) 그 안에 함유된 CD8 산물을 갖는 제1 용기; 2) 그 안에 함유된 제2 CD8 산물을 갖는 제2 용기; 및 3) 그 안에 함유된 제3 CD8 산물을 갖는 제3 용기를 포함할 수 있다.
제조품은 1) 그 안에 함유된 CD8 산물을 갖는 제1 용기; 2) 그 안에 함유된 제2 CD8 산물을 갖는 제2 용기; 3) 그 안에 함유된 제3 CD8 산물을 갖는 제3 용기; 및 4) 임의로 그 안에 함유된 제4 CD8 산물을 갖는 제4 용기를 포함할 수 있다.
제조품은 1) 그 안에 함유된 CD8 산물을 갖는 제1 용기; 2) 그 안에 함유된 제2 CD8 산물을 갖는 제2 용기; 3) 그 안에 함유된 제3 CD8 산물을 갖는 제3 용기; 4) 그 안에 함유된 제4 CD8 산물을 갖는 제4 용기; 및 5) 임의로 그 안에 함유된 제4 CD8 산물을 갖는 제5 용기를 포함할 수 있다.
제조품은 그 안에 함유된 1종의 CD8 산물을 갖는 용기를 포함할 수 있다. 제조품은 그 안에 함유된 2종의 CD8 산물을 갖는 용기를 포함할 수 있다. 제조품은 그 안에 함유된 3종의 CD8 산물을 갖는 용기를 포함할 수 있다. 제조품은 그 안에 함유된 4종의 CD8 산물을 갖는 용기를 포함할 수 있다. 제조품은 그 안에 함유된 5종의 CD8 산물을 갖는 용기를 포함할 수 있다.
제조품은 1) 그 안에 함유된 1종의 CD8 산물을 갖는 제1 용기, 및 2) 그 안에 함유된 2종의 CD8 산물을 갖는 제2 용기를 포함할 수 있다. 제조품은 1) 그 안에 함유된 2종의 CD8 산물을 갖는 제1 용기, 및 2) 그 안에 함유된 1종의 CD8 산물을 갖는 제2 용기를 포함할 수 있다. 상기 예에서, 1종 이상의 추가의 CD8 산물을 포함하는 제3 및/또는 제4 용기는 제조품에 포함될 수 있다. 추가적으로, 1종 이상의 추가의 CD8 산물을 포함하는 제5 용기는 제조품에 포함될 수 있다.
더욱이, 본원에 기재된 CD8 산물의 임의의 용기는 다중 시점의 투여를 위해 및/또는 환자에 대한 적절한 용량에 기반하여 2, 3, 또는 4개의 별개의 용기로 분할될 수 있다.
특정 실시양태에서, CD8 산물은 키트에 제공된다. 키트는 비-제한적 예로서, 패키지 삽입물(들), 표지, CD8 산물(들)을 사용하는 것에 대한 지시서, 시린지, 처리 지시서, 투여 지시서, 튜빙, 바늘, 및 임상의가 CD8 산물(들)을 적절하게 투여하기 위해 필요로 할 다른 것을 함유할 수 있다.
치료 조성물 및 제조 방법
본원에 기재된 바와 같이, CD8 산물의 우수 제조 관행 (GMP) 제조를 위한 플라스미드 DNA-매개 정확성 게놈 조작 프로세스가 개발되었다. 환자-특이적 네오TCR의 표적화된 통합은 CRISPR 엔도뉴클레아제 리보핵단백질 (RNP)을 플라스미드 DNA에 의해 코딩된 개인화된 네오TCR 유전자 카세트와 함께 전기천공함으로써 달성되었다. 네오TCR에 추가로, CD8 구축물은 그들을 네오TCR 벡터 내로 혼입하고, 이어서 상기 기재된 바와 같은 CRISPR 엔도뉴클레아제 리보핵단백질 (RNP)로 천기천공함으로써 삽입되었다.
CD8 산물은 임상적 제조 프로세스를 사용하여 약물 산물로 제제화될 수 있다. 이 프로세스 하에서, CD8 산물은 크리오맥스 동결 백에서 동결보존된다. 1개 이상의 백은 환자 필요에 따라 각각의 환자에 대한 부위에 선적될 수 있다. 산물은 그 환자의 종양 세포의 표면 상에 배타적으로 존재하는 내인성 HLA 수용체 중 하나에 복합체화된 네오에피토프를 표적화하는 1종 이상의 자가 네오TCR을 발현하도록 정확성 게놈 조작된 분리반출술-유래, 환자-자가, CD8 및 CD4 T 세포로 구성된다.
최종 산물은 5% 디메틸 술폭시드 (DMSO), 인간 혈청 알부민, 및 플라스마-라이트를 함유할 것이다. 최종 세포 산물은 표 2에 제공된 성분의 목록을 함유할 것이다.
표 2. CD8 산물의 조성
조성물 및 벡터
본 개시된 대상은 본원에 개시된 세포 (예를 들어, 면역반응성 세포)를 포함하는 조성물을 제공한다.
특정 실시양태에서, 본 개시된 대상은 본원에 개시된 네오TCR을 코딩하는 폴리뉴클레오티드를 포함하는 핵산 조성물을 제공한다. 특정 실시양태에서, 본원에 개시된 핵산 조성물은 본원에 개시된 CD8 구축물을 코딩하는 폴리뉴클레오티드를 포함한다. 또한, 이러한 핵산 조성물을 포함하는 세포가 제공된다.
특정 실시양태에서, 핵산 조성물은 본원에 개시된 네오TCR에 작동가능하게 연결된 프로모터를 추가로 포함한다. 특정 실시양태에서, 핵산 조성물은 본원에 개시된 CD8 구축물에 작동가능하게 연결된 프로모터를 추가로 포함한다.
특정 실시양태에서, 프로모터는 내인성 또는 외인성이다. 특정 실시양태에서, 외인성 프로모터는 신장 인자 (EF)-1 프로모터, CMV 프로모터, SV40 프로모터, PGK 프로모터, 긴 말단 반복부 (LTR) 프로모터 및 메탈로티오네인 프로모터로 이루어진 군으로부터 선택된다. 특정 실시양태에서, 프로모터는 유도성 프로모터이다. 특정 실시양태에서, 유도성 프로모터는 NFAT 전사 반응 요소 (TRE) 프로모터, CD69 프로모터, CD25 프로모터, IL-2 프로모터, IL-12 프로모터, p40 프로모터, 및 Bcl-xL 프로모터로 이루어진 군으로부터 선택된다.
조성물 및 핵산 조성물은 관련 기술분야에 공지된 또는 본원에 기재된 바와 같은 방법에 의해 대상체에게 투여되고/거나 세포 내로 전달될 수 있다. 세포 (예를 들어, T 세포)의 유전자 변형은 실질적으로 균질한 세포 조성물을 재조합 DNA 구축물로 형질도입함으로써 달성될 수 있다. 특정 실시양태에서, 레트로바이러스 벡터 (감마-레트로바이러스 벡터 또는 렌티바이러스 벡터 중 어느 하나)는 세포 내로의 DNA 구축물의 도입을 위해 사용된다. 비-바이러스 벡터는 또한 사용될 수 있다.
가능한 형질도입 방법은 또한 예를 들어, 문헌 [Bregni, et al. (1992) Blood 80:1418-1422]의 방법에 의한 생산자 세포와의 세포의 직접적 공동-배양, 또는 예를 들어, 문헌 [Xu, et al. (1994) Exp. Hemat. 22:223-230]; 및 [Hughes, et al. (1992) J. Clin. Invest. 89:1817]의 방법에 의해 적절한 성장 인자 및 다가양이온과 함께 또는 없이 바이러스 상청액 단독으로 또는 농축된 벡터 스톡과 함께 배양하는 것을 포함한다.
다른 형질도입 바이러스 벡터는 세포를 변형시키는데 사용될 수 있다. 특정 실시양태에서, 선택된 벡터는 높은 효율의 감염 및 안정한 통합 및 발현을 나타낸다 (예를 들어, 문헌 [Cayouette et al., Human Gene Therapy 8:423-430, 1997]; [Kido et al., Current Eye Research 15:833-844, 1996]; [Bloomer et al., Journal of Virology 71:6641-6649, 1997]; [Naldini et al., Science 272:263-267, 1996]; 및 [Miyoshi et al., Proc. Natl. Acad. Sci. U.S.A. 94:10319, 1997] 참조). 사용될 수 있는 다른 바이러스 벡터는 예를 들어, 아데노바이러스, 렌티바이러스, 및 아데노-연관 바이러스 벡터, 우두 바이러스, 소 유두종 바이러스, 또는 포진 바이러스, 예컨대 엡스타인-바르 바이러스를 포함한다 (또한, 예를 들어, 문헌 [Miller, Human Gene Therapy 15-14, 1990]; [Friedman, Science 244:1275-1281, 1989]; [Eglitis et al., BioTechniques 6:608-614, 1988]; [Tolstoshev et al., Current Opinion in Biotechnology 1:55-61, 1990]; [Sharp, The Lancet 337:1277-1278, 1991]; [Cornetta et al., Nucleic Acid Research and Molecular Biology 36:311-322, 1987]; [Anderson, Science 226:401-409, 1984]; [Moen, Blood Cells 17:407-416, 1991]; [Miller et al., Biotechnology 7:980-990, 1989]; [LeGal La Salle et al., Science 259:988-990, 1993]; 및 [Johnson, Chest 107:77S- 83S, 1995]의 벡터 참조). 레트로바이러스 벡터는 특히 잘 개발되어 있으며, 임상적 환경에서 사용되었다 (Rosenberg et al., N. Engl. J. Med 323:370, 1990; Anderson et al., 미국 특허 번호 5,399,346).
비-바이러스 접근법은 또한 세포의 유전자 변형에 사용될 수 있다. 예를 들어, 핵산 분자는 핵산을 리포펙션 (Feigner et al., Proc. Natl. Acad. Sci. U.S.A. 84:7413, 1987; Ono et al., Neuroscience Letters 17:259, 1990; Brigham et al., Am. J. Med. Sci. 298:278, 1989; Staubinger et al., Methods in Enzymology 101:512, 1983), 아시알로오로소뮤코이드-폴리리신 접합 (Wu et al., Journal of Biological Chemistry 263:14621, 1988; Wu et al., Journal of Biological Chemistry 264:16985, 1989)의 존재 하에서, 또는 외과적 조건 하에서의 미세-주사에 의해 (Wolff et al., Science 247:1465, 1990) 투여함으로써 세포 내로 도입될 수 있다. 유전자 전달을 위한 다른 비-바이러스 수단은 인산칼슘, DEAE 덱스트란, 전기천공, 및 원형질체 융합을 사용한 시험관내에서의 형질감염을 포함한다. 리포솜은 또한 세포 내로의 DNA의 전달을 위해 잠재적으로 유익할 수 있다. 대상체의 질환에 걸린 조직 내로의 정상 유전자의 이식은 또한 정상 핵산을 생체외에서 배양가능한 세포 유형 (예를 들어, 자가 또는 이종 1차 세포 또는 그의 자손) 내로 전달하고, 그 후 세포 (또는 그의 후손)를 표적화된 조직 내로 주사하거나, 전신적으로 주사함으로써 달성될 수 있다.
폴리뉴클레오티드 요법 방법은 임의의 적합한 프로모터 (예를 들어, 인간 시토메갈로바이러스 (CMV), 원숭이 바이러스 40 (SV40), 또는 메탈로티오네인 프로모터)로부터 지정되고, 임의의 적절한 포유동물 조절 요소 또는 인트론 (예를 들어 신장 인자 1a 인핸서/프로모터/인트론 구조)에 의해 조절될 수 있다. 예를 들어, 목적하는 경우, 특이적 세포 유형에서 유전자 발현을 우선적으로 지정하는 것으로 공지된 인핸서는 핵산의 발현을 지정하는데 사용될 수 있다. 사용되는 인핸서는 제한 없이, 조직- 또는 세포-특이적 인핸서로서 특징규명된 것들을 포함할 수 있다. 대안적으로, 게놈 클론이 치료 구축물로서 사용되는 경우, 조절은 동족 조절 서열에 의해, 또는 목적하는 경우, 상기 기재된 임의의 프로모터 또는 조절 요소를 포함한 이종 공급원으로부터 유래된 조절 서열에 의해 매개될 수 있다.
생성된 세포는 비변형된 세포에 대한 것들과 유사한 조건 하에서 성장될 수 있으며, 그에 의해 변형된 세포는 확장되고 다양한 목적을 위해 사용될 수 있다.
키트
본 개시된 대상은 면역 반응을 유도하고/거나 증진시키고/거나, 대상체에서 암 또는 병원체 감염을 치료하고/거나 예방하기 위한 키트를 제공한다. 특정 실시양태에서, 키트는 본 개시된 세포 또는 이를 포함하는 제약 조성물의 유효량을 포함한다. 특정 실시양태에서, 키트는 멸균 용기를 포함하며; 이러한 용기는 박스, 앰풀, 보틀, 바이알, 튜브, 백, 파우치, 블리스터-팩, 또는 관련 기술분야에 공지된 다른 적합한 용기 형태일 수 있다. 이러한 용기는 플라스틱, 융리, 적층 종이, 금속 호일, 또는 의약을 보유하는데 적합한 다른 물질로 제조될 수 있다. 특정 비-제한적 실시양태에서, 키트는 본 개시된 HR 주형을 코딩하는 단리된 핵산 분자를 포함한다.
목적하는 경우, 세포 및/또는 핵산 분자는 세포 또는 핵산 분자를 암 또는 병원체 또는 면역 장애를 갖거나 이를 발달시킬 위험이 있는 대상체에게 투여하는 것에 대한 지시서와 함께 제공된다. 지시서는 일반적으로 암 또는 병원체 감염의 치료 및/또는 예방을 위한 조성물의 사용에 관한 정보를 포함한다. 특정 실시양태에서, 지시서는 하기 중 적어도 하나를 포함한다: 치료제의 설명; 신생물, 병원체 감염, 또는 면역 장애 또는 그의 증상의 치료 또는 예방을 위한 투여 스케줄 및 투여; 예방책; 경고; 적응증; 금기증; 과다-투여량 정보; 유해 반응; 동물 약리학; 임상 연구; 및/또는 참고문헌. 지시서는 용기 상에 직접적으로 인쇄될 수 있거나 (존재하는 경우), 용기에 적용된 표지로서, 또는 별개의 쉬트, 팸플릿, 카드, 또는 용기에 또는 그와 함께 공급된 폴더로서일 수 있다. 생성된 세포는 비변형된 세포에 대한 것들과 유사한 조건 하에서 성장될 수 있으며, 그에 의해 변형된 세포는 확장되고 다양한 목적을 위해 사용될 수 있다.
예시적인 실시양태
A. 특정 비-제한적 실시양태에서, 본 개시된 대상은 외인성 T 세포 수용체 (TCR), 및 외인성 CD8을 포함하는 세포를 제공한다.
A1. 외인성 CD8이 적어도 1종의 단량체를 포함하는 것인 A의 상기 세포.
A2. 외인성 CD8의 적어도 1종의 단량체가 세포외 도메인, 막횡단 도메인, 세포내 도메인, 그의 단편, 또는 이들의 조합을 포함하는 것인 A1의 상기 세포.
A3. 세포외 도메인이 CD8α 세포외 도메인 또는 CD8β 세포외 도메인을 포함하는 것인 A2의 상기 세포.
A4. 막횡단 도메인이 CD8α 막횡단 도메인 또는 CD8β 막횡단 도메인을 포함하는 것인 A2 또는 A3의 상기 세포.
A5. 세포내 도메인이 CD8α 세포내 도메인 또는 CD8β 세포내 도메인을 포함하는 것인 A2-A4의 상기 세포.
A6. 세포내 도메인이 CD4 세포내 도메인을 포함하는 것인 A2-A4의 상기 세포.
A7. 적어도 1종의 단량체가 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인을 포함하는 것인 A1-A5의 상기 세포.
A8. 적어도 1종의 단량체가 CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인을 포함하는 것인 A1-A5의 상기 세포.
A9. 적어도 1종의 단량체가 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인을 포함하는 것인 A1-A5의 상기 세포.
A10. 적어도 1종의 단량체가 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 것인 A1-A6의 상기 세포.
A11. 적어도 1종의 단량체가 신호 펩티드를 포함하는 것인 A1-A10의 상기 세포.
A12. 신호 펩티드가 CD8 신호 펩티드인 A11의 상기 세포.
A13. 세포외 도메인이 서열식별번호: 140, 또는 서열식별번호: 145에 제시된 아미노산 서열을 포함하는 것인 A2-A12의 상기 세포.
A14. 막횡단 도메인이 서열식별번호: 141, 또는 서열식별번호: 146에 제시된 아미노산 서열을 포함하는 것인 A2-A13의 상기 세포.
A15. 세포내 도메인이 서열식별번호: 142, 서열식별번호: 147, 또는 서열식별번호: 148에 제시된 아미노산 서열을 포함하는 것인 A2-A14의 상기 세포.
A16. 신호 펩티드가 서열식별번호: 139, 또는 서열식별번호: 144에 제시된 아미노산 서열을 포함하는 것인 A11-A15의 상기 세포.
A17. 외인성 CD8이 2A 서열을 포함하는 것인 A-A16의 상기 세포.
A18. 외인성 CD8이 링커를 포함하는 것인 A-A17의 상기 세포.
A19. 링커가 서열식별번호: 137에 제시된 아미노산 서열을 포함하는 것인 A18의 상기 세포.
A20. 외인성 CD8이 프로테아제 절단 부위를 포함하는 것인 A-A19의 상기 세포.
A21. 프로테아제 절단 부위가 푸린 절단 부위인 A-A20의 상기 세포.
A22. 외인성 TCR이 환자 유래 TCR인 A-A21의 상기 세포.
A23. 외인성 TCR이 신호 서열, 제1 및 제2 2A 서열, 및 TCR 폴리펩티드 서열을 포함하는 것인 A-A22의 상기 세포.
A24. 외인성 TCR이 암 항원을 인식하는 것인 A-A23의 상기 세포.
A25. 암 항원이 신생항원인 A24의 상기 세포.
A26. 암 항원이 환자 특이적 항원인 A24의 상기 세포.
A27. 세포가 1차 세포인 A-A26의 상기 세포.
A28. 세포가 환자-유래 세포인 A-A26의 상기 세포.
A29. 세포가 림프구인 A-A26의 상기 세포.
A30. 세포가 T 세포인 A-A26의 상기 세포.
A31. 세포가 어린 T 세포인 A-A26의 상기 세포.
A32. 세포가 CD45RA+, CD62L+, CD28+, CD95-, CCR7+, 및 CD27+인 A31의 상기 세포.
A33. 세포가 CD45RA+, CD62L+, CD28+, CD95+, CD27+, CCR7+인 A31의 상기 세포.
A34. 세포가 CD45RO+, CD62L+, CD28+, CD95+, CCR7+, CD27+, CD127+인 A31의 상기 세포.
A35. 세포 존속을 증진시키고/거나 기억 세포 분화를 증진시키는 유전자 변형을 추가로 포함하는 A-A34의 상기 세포.
A36. 세포의 살해 활성이 외인성 CD8을 갖지 않는 세포의 살해 활성과 비교하여 약 10% 내지 약 500% 증가되는 것인 A-A35의 상기 세포.
A37. 항원에의 TCR의 결합 시 세포의 증식이 외인성 CD8을 갖지 않는 세포의 증식과 비교하여 약 10% 내지 약 500% 증가되는 것인 A-A36의 상기 세포.
A38. 세포에 의한 항원에의 TCR의 결합 시 전염증성 시토카인의 분비가 외인성 CD8을 갖지 않는 세포에 의한 분비와 비교하여 약 10% 내지 약 500% 증가되는 것인 A-A37의 상기 세포.
A39. 세포의 LCK 친화도가 외인성 CD8을 갖지 않는 세포의 LCK 친화도와 비교하여 약 10% 내지 약 500% 증가되는 것인 A-A38의 상기 세포.
A40. 세포의 존속이 외인성 CD8을 갖지 않는 세포의 존속과 비교하여 약 10% 내지 약 500% 증가되는 것인 A-A39의 상기 세포.
A41. 세포의 종양 침윤 능력이 외인성 CD8을 갖지 않는 세포의 종양 침윤 능력과 비교하여 약 10% 내지 약 500% 증가되는 것인 A-A40의 상기 세포.
A42. 외인성 TCR이 CD8-의존성 TCR인 A-A41의 상기 세포.
A43. 외인성 TCR이 CD8-비의존성 TCR인 A-A41의 상기 세포.
A44. 외인성 CD8이 CD8 구축물 1, CD8 구축물 2, CD8 구축물 3, 또는 CD8 구축물 4에 의해 코딩되는 것인 A-A43의 상기 세포.
A45. 외인성 CD8이 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 것인 A-A43의 상기 세포.
A46. 외인성 CD8이 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함하는 것인 A-A43의 상기 세포.
B. 특정 비-제한적 실시양태에서, 본 개시된 대상은 세포 내로 상동성 재조합 (HR) 주형 핵산 서열을 도입하며, 여기서 HR 주형은 제1 및 제2 표적 핵산 서열에 대해 상동성인 제1 및 제2 상동성 아암, 제1 및 제2 상동성 아암 사이에 위치한 TCR 유전자 서열, 및 제1 및 제2 상동성 아암 사이에 위치한 CD8 유전자 서열을 포함하는 것인 단계, 및 HR 주형 핵산을 세포의 내인성 로커스 내로 재조합하는 단계를 포함하는, 세포를 변형시키는 방법을 제공한다.
B1. HR 주형이 CD8 유전자 서열의 상류에 위치한 제1 2A-코딩 서열, CD8 유전자 서열의 하류 및 TCR 유전자 서열의 상류에 위치한 제2 2A-코딩 서열, 및 TCR 유전자 서열의 하류에 위치한 제3 2A-코딩 서열을 포함하며; 여기서 제1, 제2, 및 제3 2A-코딩 서열은 동일한 아미노산 서열을 코딩하고, 서로에 대해 코돈-분기된 것인 B의 상기 방법.
B2. HR 주형이 제1, 제2, 및/또는 제3 2A-코딩 서열의 바로 상류에 위치한 아미노산 서열 Gly Ser Gly를 코딩하는 서열을 포함하는 것인 B 또는 B1의 상기 방법.
B3. HR 주형이 제1, 제2, 및/또는 제3 2A-코딩 서열의 상류에 위치한 푸린 절단 부위를 코딩하는 서열을 추가로 포함하는 것인 B1 또는 B2의 상기 방법.
B4. HR 주형이 TCR 유전자 서열 및/또는 CD8 유전자 서열의 바로 상류에 위치한 신호 서열을 코딩하는 서열을 추가로 포함하는 것인 B-B3의 상기 방법.
B5. HR 주형이 제3 2A-코딩 서열 및 제2 상동성 아암 사이에 위치한 제2 TCR 서열을 포함하는 것인 B-B4의 상기 방법.
B6. HR 주형이 제1 TCR 유전자 서열의 바로 상류에 위치한 제1 신호 서열을 코딩하는 서열; 및 제2 TCR 유전자 서열의 바로 상류에 위치한 제2 신호 서열을 코딩하는 서열을 포함하는 것인 B5의 상기 방법.
B7. HR 주형이 제1 CD8 유전자 서열 및 제2 2A-코딩 서열 사이에 위치한 제2 CD8 유전자 서열을 포함하는 것인 B-B6의 상기 방법.
B8. 2A 코딩 서열이 제1 및 제2 CD8 유전자 서열 사이에 위치하는 것인 B7의 상기 방법.
B9. 아미노산 서열 Gly Ser Gly를 코딩하는 서열이 제1 및 제2 CD8 유전자 서열 사이에 위치하는 것인 B7 또는 B8의 상기 방법.
B10. 푸린 절단 부위를 코딩하는 서열이 제1 및 제2 CD8 유전자 서열 사이에 위치하는 것인 B7-B9의 상기 방법.
B11. CD8 유전자 서열이 세포외 도메인을 코딩하는 서열, 세포내 도메인을 코딩하는 서열, 세포내 도메인을 코딩하는 서열, 그의 단편, 또는 이들의 조합을 포함하는 것인 B-B10의 상기 방법.
B12. 세포외 도메인을 코딩하는 서열이 CD8α 세포외 도메인 또는 CD8β 세포외 도메인을 코딩하는 서열을 포함하는 것인 B11의 상기 방법.
B13. 막횡단 도메인을 코딩하는 서열이 CD8α 막횡단 도메인 또는 CD8β 막횡단 도메인을 코딩하는 서열을 포함하는 것인 B11 또는 B12의 상기 방법.
B14. 세포내 도메인을 코딩하는 서열이 CD8α 세포내 도메인 또는 CD8β 세포내 도메인을 코딩하는 서열을 포함하는 것인 B11-B13의 상기 방법.
B15. 세포내 도메인을 코딩하는 서열이 CD4 세포내 도메인을 코딩하는 서열을 포함하는 것인 B11-B14의 상기 방법.
B16. CD8 유전자 서열이 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인을 코딩하는 서열을 포함하는 것인 B11-B15의 상기 방법.
B17. CD8 유전자 서열이 CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인을 코딩하는 서열을 포함하는 것인 B11-B15의 상기 방법.
B18. CD8 유전자 서열이 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인을 코딩하는 서열을 포함하는 것인 B11-B15의 상기 방법.
B19. CD8 유전자 서열이 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 코딩하는 서열을 포함하는 것인 B11-B15의 상기 방법.
B20. HR 주형이 제1 CD8 유전자 서열의 바로 상류에 위치한 제1 신호 서열을 코딩하는 서열; 및 제2 CD8 유전자 서열의 바로 상류에 위치한 제2 신호 서열을 코딩하는 서열을 포함하는 것인 B7-B19의 상기 방법.
B21. 신호 서열이 CD8 신호 서열, 인간 성장 호르몬 신호 서열, 그의 단편, 또는 이들의 조합인 B4-B20의 상기 방법.
B22. HR 주형의 제1 및 제2 상동성 아암이 각각 약 300개 염기 내지 약 2,000개 염기의 길이인 B-B21의 상기 방법.
B23. HR 주형의 제1 및 제2 상동성 아암이 각각 약 600개 염기 내지 약 2,000개 염기의 길이인 B-B22의 상기 방법.
B24. 외인성 TCR이 환자 유래 TCR인 B-B23의 상기 방법.
B25. 외인성 TCR이 신호 서열, 제1 및 제2 2A 서열, 및 TCR 폴리펩티드 서열을 포함하는 것인 B-B24의 상기 방법.
B26. 외인성 TCR이 암 항원을 인식하는 것인 B-B25의 상기 방법.
B27. 암 항원이 신생항원인 B26의 상기 방법.
B28. 암 항원이 환자 특이적 항원인 B26의 상기 방법.
B29. HR 주형이 비-바이러스성인 B-B28의 상기 방법.
B30. HR 주형이 원형 DNA인 B-B29의 상기 방법.
B31. HR 주형이 선형 DNA인 B-B29의 상기 방법.
B32. 도입이 전기천공을 통해 일어나는 것인 B-B31의 상기 방법.
B33. 재조합이 뉴클레아제에 의한 내인성 로커스의 절단; 및 상동성 지정 복구에 의한 내인성 로커스 내로의 HR 주형 핵산 서열의 재조합을 포함하는 것인 B-B32의 상기 방법.
B34. 뉴클레아제가 클러스터링된 규칙적 간격의 짧은 회문구조 반복부 (CRISPR) 패밀리 뉴클레아제, 또는 그의 유도체인 B33의 상기 방법.
B35. gRNA를 추가로 포함하는 B34의 상기 방법.
B36. 프로세스가 세포를 배양하는 것을 추가로 포함하는 것인 B-B35의 상기 방법.
B37. 배양이 적어도 1종의 시토카인의 존재 하에서 수행되는 것인 B36의 상기 방법.
B38. 배양이 IL2, IL7, IL15, 또는 이들의 임의의 조합의 존재 하에서 수행되는 것인 B36 또는 B37의 상기 방법.
B39. 배양이 IL7 및 IL15의 존재 하에서 수행되는 것인 B36 또는 B37의 상기 방법.
B40. 세포 존속을 증진시키고/거나 기억 세포 분화를 증진시키는 유전자 변형을 추가로 포함하는 B-B39의 상기 방법.
B41. 세포가 1차 세포인 B-B40의 상기 방법.
B42. 세포가 환자-유래 세포인 B-B40의 상기 방법.
B43. 세포가 림프구인 B-B40의 상기 방법.
B44. 세포가 T 세포인 B-B40의 상기 방법.
B45. 세포가 어린 T 세포인 B-B40의 상기 방법.
B46. 세포가 CD45RA+, CD62L+, CD28+, CD95-, CCR7+, 및 CD27+인 B45의 상기 방법.
B47. 세포가 CD45RA+, CD62L+, CD28+, CD95+, CD27+, CCR7+인 B45의 상기 방법.
B48. 세포가 CD45RO+, CD62L+, CD28+, CD95+, CCR7+, CD27+, CD127+인 B45의 상기 방법.
B49. 세포의 살해 활성이 CD8 유전자 서열을 갖지 않는 세포의 살해 활성과 비교하여 약 10% 내지 약 500% 증가되는 것인 B-B48의 상기 방법.
B50. 항원에의 TCR의 결합 시 세포의 증식이 CD8 유전자 서열을 갖지 않는 세포의 증식과 비교하여 약 10% 내지 약 500% 증가되는 것인 B-B49의 상기 방법.
B51. 세포에 의한 항원에의 TCR의 결합 시 전염증성 시토카인의 분비가 CD8 유전자 서열을 갖지 않는 세포에 의한 분비와 비교하여 약 10% 내지 약 500% 증가되는 것인 B-B50의 상기 방법.
B52. 세포의 LCK 친화도가 CD8 유전자 서열을 갖지 않는 세포의 LCK 친화도와 비교하여 약 10% 내지 약 500% 증가되는 것인 B-B51의 상기 방법.
B53. 세포의 존속이 CD8 유전자 서열을 갖지 않는 세포의 존속과 비교하여 약 10% 내지 약 500% 증가되는 것인 B-B52의 상기 방법.
B54. 세포의 종양 침윤 능력이 CD8 유전자 서열을 갖지 않는 세포의 종양 침윤 능력과 비교하여 약 10% 내지 약 500% 증가되는 것인 B-B53의 상기 방법.
B55. TCR 유전자가 CD8-의존성 TCR을 코딩하는 것인 B-B54의 상기 방법.
B56. TCR 유전자가 CD8-비의존성 TCR을 코딩하는 것인 B-B54의 상기 방법.
B57. CD8 유전자 서열이 CD8 구축물 1, CD8 구축물 2, CD8 구축물 3, 또는 CD8 구축물 4에 의해 코딩되는 것인 B-B56의 상기 방법.
B58. CD8 유전자 서열이 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, CD4 세포내 도메인을 포함하는 것인 B-B56의 상기 방법.
B59. CD8 유전자 서열이 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함하는 것인 B-B56의 상기 방법.
C. 특정 비-제한적 실시양태에서, 본 개시된 대상은 B-B57의 방법에 의해 변형된 세포를 제공한다.
D. 특정 비-제한적 실시양태에서, 본 개시된 대상은 A-A46의 세포 또는 C의 세포의 유효량을 포함하는 조성물을 제공한다.
D1. 조성물이 제약상 허용되는 부형제를 추가로 포함하는 제약 조성물인 D의 상기 조성물.
D2. 조성물이 암의 치료를 위해 이를 필요로 하는 환자에게 투여되는 것인 D 또는 D1의 상기 조성물.
D3. 조성물이 동결보존제를 포함하는 것인 D-D2의 상기 조성물.
D4. 조성물이 혈청 알부민을 포함하는 것인 D-D3의 상기 조성물.
D5. 조성물이 플라스마-라이트 A, HSA, 및 크리오스토르 CS10을 포함하는 것인 D-D4의 상기 조성물.
E. 특정 비-제한적 실시양태에서, 본 개시된 대상은 A-A46의 세포, 제C항의 세포, 또는 D-D5의 조성물의 치료 유효량을 투여하는 것을 포함하는, 암의 치료를 필요로 하는 대상체에서 암을 치료하는 방법을 제공한다.
E1. 세포의 치료 유효량을 투여하기 전에, 비-골수소멸성 림프구고갈 레지멘이 대상체에게 투여되는 것인 E의 상기 방법.
E2. 암이 고형 종양인 E 또는 E1의 상기 방법.
E3. 암이 액상 종양인 E 또는 E1의 상기 방법.
E4. 고형 종양이 흑색종, 흉부암, 폐암, 난소암, 유방암, 췌장암, 두경부암, 전립선암, 부인과암, 중추 신경계암, 피부암, HPV+ 암, 식도암, 갑상선암, 위암, 간세포암, 담관암종, 신세포암, 고환암, 육종, 및 결장직장암으로 이루어진 군으로부터 선택되는 것인 E2의 상기 방법.
E5. 액상 종양이 소포성 림프종, 백혈병, 및 다발성 골수종으로 이루어진 군으로부터 선택되는 것인 E3의 상기 방법.
F. 특정 비-제한적 실시양태에서, 본 개시된 대상은 A-A46의 세포, B-B57의 방법을 수행하기 위한 시약, C의 세포, 또는 D-D5의 조성물을 포함하는 키트를 제공한다.
F1. 키트가 암을 치료하는 것에 대한 서면 지시서를 추가로 포함하는 것인 F의 상기 키트.
G. 특정 비-제한적 실시양태에서, 본 개시된 대상은 외인성 T 세포 수용체 (TCR); 및 CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 외인성 CD8을 포함하는 세포를 제공한다.
H. 특정 비-제한적 실시양태에서, 본 개시된 대상은 외인성 T 세포 수용체 (TCR); 및 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함하는 외인성 CD8을 포함하는 세포를 제공한다.
I. 특정 비-제한적 실시양태에서, 본 개시된 대상은 세포 내로 상동성 재조합 (HR) 주형 핵산 서열을 도입하며, 여기서 HR 주형은 제1 및 제2 표적 핵산 서열에 대해 상동성인 제1 및 제2 상동성 아암; 제1 및 제2 상동성 아암 사이에 위치한 TCR 유전자 서열; 제1 및 제2 상동성 아암 사이에 위치한 CD8 유전자 서열을 포함하는 것인 단계; 및 HR 주형 핵산을 세포의 내인성 로커스 내로 재조합하는 단계를 포함하는, 세포를 변형시키는 방법으로서, 여기서 CD8 유전자 서열은 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 것인 방법을 제공한다.
J. 특정 비-제한적 실시양태에서, 본 개시된 대상은 세포 내로 상동성 재조합 (HR) 주형 핵산 서열을 도입하며, 여기서 HR 주형은 제1 및 제2 표적 핵산 서열에 대해 상동성인 제1 및 제2 상동성 아암; 제1 및 제2 상동성 아암 사이에 위치한 TCR 유전자 서열; 제1 및 제2 상동성 아암 사이에 위치한 CD8 유전자 서열을 포함하는 것인 단계; 및 HR 주형 핵산을 세포의 내인성 로커스 내로 재조합하는 단계를 포함하는, 세포를 변형시키는 방법으로서, 여기서 CD8 유전자 서열은 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함하는 것인 방법을 제공한다.
K. 특정 비-제한적 실시양태에서, 본 개시된 대상은 세포를 포함하는 조성물로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 것인 조성물을 제공한다.
L. 특정 비-제한적 실시양태에서, 본 개시된 대상은 세포를 포함하는 조성물로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함하는 것인 조성물을 제공한다.
M. 특정 비-제한적 실시양태에서, 본 개시된 대상은 치료 유효량의 세포를 투여하는 것을 포함하는, 암의 치료를 필요로 하는 대상체에서 암을 치료하는 방법으로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인; CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 것인 방법을 제공한다.
N. 치료 유효량의 세포를 투여하는 것을 포함하는, 암의 치료를 필요로 하는 대상체에서 암을 치료하는 방법으로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147); CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는 CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148)을 포함하는 것인 방법.
실시예
하기는 본 발명의 방법 및 조성물의 실시예이다. 상기 제공된 일반적 설명을 고려하여, 다양한 다른 실시양태가 실시될 수 있음이 이해된다.
실시예 1. 네오TCR 산물의 생성
PCT/US2020/17887 (그 전문이 본원에 참조로 포함됨)에 기재된 imPACT 단리 기술에 의해 확인된 네오에피토프-특이적 TCR을 사용하여 상동성 재조합 (HR) DNA 주형을 생성하였다. 이들 HR 주형을 부위-특이적 뉴클레아제와 나란히 1차 인간 T 세포 내로 형질감염시켰다 (도 1a-1c 참조). 단일-단계 비-바이러스 정확성 게놈 조작은 내인성 프로모터에 의해 발현된 환자의 네오에피토프-특이적 TCR로의 내인성 TCR의 심리스 대체를 발생시켰다. 표면 상에 발현된 TCR은 서열에 있어서 전체적으로 천연이다.
네오TCR-T 세포 게놈 조작의 정확성을 오프-타겟 통합 핫 스팟 또는 전위에 대한 표적화된 로커스 증폭 (TLA)에 의해, 및 차세대 시퀀싱 기반 오프-타겟 절단 검정에 의해 평가하고, 비의도된 결과의 증거를 결여함을 발견하였다.
도 1a-1c에 나타내어진 바와 같이, 관심의 유전자를 함유하는 구축물을 내인성 로커스 내로 삽입하였다. 이는 좌측 및 우측 HR 아암에 의해 플랭킹된 관심의 유전자의 코딩 서열을 함유하는 상동성 복구 주형의 사용으로 달성되었다. HR 아암에 추가로, 관심의 유전자를 2A 펩티드, 관심의 상류 번역된 유전자로부터 2A 펩티드를 제거하는 2A 펩티드의 상류인 프로테아제 절단 부위, 및 신호 서열 사이에 끼워 넣었다 (도 1b). 게놈 내로 통합되면, 관심의 발현 유전자 카세트의 유전자를 단일 메신저 RNA로서 전사하였다. 메신저 RNA에서의 관심의 이 유전자의 번역 동안, 플랭킹 영역을 자기-절단 2A 펩티드에 의해 관심의 유전자로부터 풀고, 프로테아제 절단 부위를 관심의 번역된 유전자로부터 상류의 2A 펩티드의 제거를 위해 절단하였다 (도 1c). 2A 펩티드 및 프로테아제 절단 부위에 추가로, gly-ser-gly (GSG) 링커를 각각의 2A 펩티드 앞에 삽입하여 발현 카세트에서 다른 요소로부터 관심의 유전자의 분리를 추가로 증진시켰다.
P2A 펩티드는 그의 효율적인 절단 때문에 세포 산물에 대해 다른 2A 펩티드보다 우수한 것으로 결정되었다. 따라서, 두 (2)가지 P2A 펩티드 및 코돈 분기성을 사용하여, P2A 펩티드로부터 관심의 유전자의 어느 하나의 말단 상에 나머지 아미노산으로부터 임의의 외인성 에피토프를 도입하지 않고 관심의 유전자를 발현시켰다. 외인성 에피토프를 갖지 않는 (즉, 관심의 유전자의 어느 하나의 측 상에 플랭킹 P2A 펩티드 아미노산을 갖지 않는) 유전자 편집된 세포의 유익은 면역원성이 대폭 감소되고, 유전자 편집된 세포를 함유하는 세포 산물로 주입된 환자가 유전자 편집된 세포에 대한 면역 반응을 가질 가능성이 적다는 것이다.
PCT/US/2018/058230에 기재된 바와 같이, 네오TCR은 T 세포의 TCRα 로커스 내로 통합되었다. 구체적으로, 좌측 및 우측 HR 아암에 의해 플랭킹된 네오TCR 코딩 서열을 함유하는 상동성 복구 주형을 사용하였다. 또한, 내인성 TCRβ 로커스는 파괴되어 단지 네오TCR 구축물에 의해 코딩된 TCR 서열의 발현을 초래하였다. 일반적 전략을 원형 HR 주형을 사용하여 뿐만 아니라 선형 주형으로 적용하였다.
표적 TCRα 로커스 (Cα)는 플라스미드 HR 주형과 함께 나타내어지고, 생성된 편집된 서열 및 하류 mRNA/단백질 산물은 도 1b 및 1c에 나타내어진다. 표적 TCRα 로커스 (내인성 TRAC) 및 그의 CRISPR Cas9 표적 부위 (수평 줄무늬, 절단 부위는 화살표에 의해 표시됨)가 나타내어진다 (도 1a-1c). 네오TCR을 코딩하는 폴리뉴클레오티드를 갖는 원형 플라스미드 HR 주형은 좌측 및 우측 상동성 아암 (각각 "LHA" 및 "RHA") 사이에 위치한다. 코돈 최적화된 HR 주형에 의해 도입된 TRAC의 영역이 나타내어진다 (수직 줄무늬). TCRβ 불변 도메인은 TRBC2로부터 유래되었으며, 이는 TRBC1에 대해 기능적으로 등가인 것으로 지시된다. 네오TCR 카세트 중의 다른 요소는 2A = 2A 리보솜 스키핑 요소 (비-제한적 예로서, 카세트에 사용된 2A 펩티드는 번역된 산물에서 임의의 그러지 않다면 발생하는 비-내인성 에피토프를 제거하는 코돈 분기성과 조합으로 사용된 둘 다의 P2A 서열임); P = 상류 TCRβ 단백질로부터 2A 태그를 제거하는 2A의 상류의 프로테아제 절단 부위 (비-제한적 예로서, 프로테아제 절단 부위는 푸린 프로테아제 절단 부위일 수 있음); SS = 신호 서열 (비-제한된 예로서, 신호 서열은 인간 성장 호르몬 신호 서열일 수 있음)을 포함한다. 네오TCR 발현 유전자 카세트의 HR 주형은 TCRα 가이드 RNA를 갖는 CRISPR Cas9 뉴클레아제 RNP에 의해 표적화된 TCRα 게놈 로커스 내로의 삽입을 지정하는 2개의 플랭킹 상동성 아암을 포함한다. 이들 상동성 아암 (LHA 및 RHA)은 네오TCR 발현 유전자 카세트의 네오E-특이적 TCR 서열을 플랭킹한다. 이 실시예에 사용된 프로테아제 절단 부위는 푸린 프로테아제 절단 부위였지만, 관련 기술분야의 통상의 기술자에게 공지된 임의의 적절한 프로테아제 절단 부위가 사용될 수 있다. 유사하게, HGH는 이 실시예를 위해 선택된 신호 서열이었지만, 관련 기술분야의 통상의 기술자에게 공지된 임의의 신호 서열은 목적하는 트래피킹에 기반하여 선택되고 사용될 수 있다.
게놈 내로 통합되면 (도 1c), 네오TCR 발현 유전자 카세트는 그 개별적인 T 세포로부터의 내인성 TCRα 폴리펩티드의 부분을 여전히 포함하는 내인성 TCRα 프로모터로부터 단일 메신저 RNA로서 전사된다 (도 1c). 이 단일 네오TCR 메신저 RNA의 리보솜 폴리펩티드 번역 동안, 네오TCR 서열은 P2A 펩티드에서의 자기-절단에 의해 내인성, CRISPR-파괴된 TCRα 폴리펩티드로부터 풀린다 (도 1c). 코딩된 네오TCRα 및 네오TCRβ 폴리펩티드는 또한 네오TCR 발현 유전자 카세트에 포함된 내인성 세포성 인간 푸린 프로테아제 및 제2 자기-절단 P2A 서열 모티프에 의한 절단을 통해 서로로부터 풀린다 (도 1c). 네오TCRα 및 네오TCRβ 폴리펩티드는 T 세포 표면에 대한 네오TCR 단백질 복합체의 다량체 어셈블리 및 트래피킹을 위해 신호 리더 서열 (인간 성장 호르몬, HGH로부터 유래됨)에 의해 세포질 세망에 별개로 표적화된다. 푸린 프로테아제 절단 부위의 포함은 상류 TCRβ 쇄로부터 2A 서열의 제거를 용이하게 하여 TCRβ 기능의 잠재적 간섭을 감소시킨다. 각각의 2A 앞에 gly-ser-gly 링커의 포함 (나타내지 않음)은 3개의 폴리펩티드의 분리를 추가로 증진시킨다.
추가적으로, 3개의 반복된 단백질 서열은 HR 주형 내에서 코돈 분기되어 게놈 안정성을 촉진시킨다. TCR 유전자 카세트 내에서, 2개의 P2A는 서로에 대해 코돈 분기될 뿐만 아니라 2개의 HGH 신호 서열은 서로에 대해 코돈 분기되어 생체외 조작된 T 세포의 게놈 내의 도입된 네오TCR 카세트 서열의 안정성을 촉진시킨다. 유사하게, TRAC 엑손 1 (수직 줄무늬)의 재-도입된 5' 말단은 전체 카세트가 2개의 직접적 반복부의 개재 서열의 제거를 통해 시간 경과에 따라 소실될 가능성을 감소시킨다.
네오TCR 산물에 추가로, 이 방법은 임의의 CD8 산물에 사용될 수 있다.
인-아웃 PCR을 사용하여 네오E TCR 카세트의 정확한 표적 통합을 확인하였다. 아가로스 겔은 통합 카세트 및 부위에 특이적인 프라이머를 사용한 PCR의 결과가 단지 뉴클레아제 및 DNA 주형 둘 다로 처리된 세포 (KOKI 및 KOKIKO)에 대해서만 예상된 크기의 산물을 생성함을 나타내며, 이는 부위-특이적 및 정확한 통합을 입증한다.
더욱이, 표적화된 로커스 증폭 (TLA)을 사용하여 표적화된 통합의 특이성을 확인하였다. 가교, 라이게이션, 및 네오TCR 삽입물에 특이적인 프라이머의 사용을 사용하여 통합의 부위(들) 주위의 서열을 얻었다. 게놈에 대해 맵핑된 판독물은 10 kb 간격으로 비닝된다. 유의한 판독물 깊이를 단지 염색체 14 상의 의도된 부위 통합 부위 주위에서 얻었으며, 이는 공통 오프-타겟 삽입 부위의 증거가 없음을 나타낸다.
내인성 TCR에 대한 항체 염색 및 및 네오TCR에 대한 펩티드-HLA 염색은 조작이 네오TCR의 고 빈도 넉-인을 발생시킴을 밝혀내었으며, 일부 TCR- 세포 및 소수의 WT T 세포가 남는다. 넉-인은 외인성 프로모터의 부재 하에서 네오TCR 발현에 의해 입증된다. 조작을 유사한 결과를 갖는 동일한 네오TCR을 사용하여 다수회 수행하였다. 따라서, 조작된 T 세포에서 네오TCR의 효율적이고 일관된 발현 및 내인성 TCR의 넉아웃이 달성되었다.
실시예 2. CD8 산물 1의 생성
T 세포 단리 및 편집. CD4 및 CD8 T 세포를 밀테니(Miltenyi) 프로디지(Prodigy) 또는 밀테니 MACS 분리 칼럼을 제조업체의 지시서에 따라 사용하여 건강한 공여자 PBMC로부터 단리하였다. 양성-선택된 CD4 및 CD8 T 세포 (밀테니 항체 및 단리 칼럼을 사용하여)를 신선하게 사용하거나 1% 인간 혈청 알부민 (게미니(Gemini)), 49% 플라스마라이트 (백스터(Baxter)), 및 50% CS10 (시그마(Sigma))에서 동결보존하였다. 동결보존된 세포를 해동시키고, TexMACS (밀테니) + 10% 인간 AB 혈청 (밸리 바이오메디칼(Valley Biomedical))에서 세척하고, TexMACS + 3% 인간 AB 혈청 (배양 배지)에서 mL 당 2 x 106개 세포의 밀도로 시딩하였다. 해동 후 1일에, 또는 신선하게 사용되는 경우 즉시, 세포를 세척하고, 부피로 배양 배지 + 12.5 ng/mL IL7 + 12.5 ng/mL IL15 + 1:17.5 비의 트랜스ACT(TransACT) T 세포 활성화 시약 (모든 시약은 밀테니로부터)에서 mL 당 1.46 x 106개 세포의 밀도로 재-시딩하였다. 활성화 후 2일에, T 세포를 i) 네오TCR 산물의 생산을 위한 플라스미드 (예를 들어, 도 1b 참조) 또는 ii) CD8 구축물 1 (예를 들어, 네오TCR 베타 및 알파 서열의 상류의 P2A 부위에 의해 플랭킹된 CD8α의 코딩 서열 및 TCR 알파 및 베타 로커스를 표적화하는 gRNA-Cas9 RNP로 이루어짐; 예를 들어, 도 2a 참조)로 전기천공하였다. CD8 구축물 1의 예시적인 발현 구축물은 도 11a에 나타내어진다. T 세포를 100 μL 큐벳 중 론자(Lonza) X-유닛 및 프로그램 EO-115를 사용하여 전기천공하였다. T 세포를 12.5 ng/mL IL7 + 12.5 ng/mL IL15로 보충된 배양 배지에서 확장시킨다. 보충된 배지를 활성화 후 13일인 연구의 종료시까지 2-3일마다 교체하였다.
comPACT 및 comPACT-덱스트라머 제조. 신생항원-특이적 펩티드-HLA 복합체 폴리펩티드 (각각의 "comPACT")를 그 전문이 본원에 참조로 포함되는 PCT/US2019/025415에 기재된 바와 같은 방법에 따라 제조하였다. comPACT-덱스트라머 복합체를 네오TCR 발현 T 세포의 표지화를 위해 제조하였다. 비오티닐화 comPACT 단백질을 스트렙타비딘-접합된 형광단과 함께 실온 (RT)에서 10분 동안 인큐베이션하였다. 비오틴-40-덱스트란 (NANOCS)을 혼합물에 첨가하고 RT에서 추가의 10분 동안 인큐베이션하였다. comPACT-덱스트라머를 4℃에서 저장하였다.
네오TCR 편집된 T 세포에의 comPACT 결합의 확인. T 세포를 유동 세포계측법을 위해 염색하였다. 세포를 먼저 생존력 염료로 4℃에서 20분 동안 염색하고, 이어서 세척하고, comPACT-덱스트라머로 4℃에서 10분 동안 염색하였다. 표면 항체 (항-CD8α, 항-CD8β, 항-CD4)를 세포 및 comPACT-덱스트라머의 현탁액에 첨가하고, 세포를 4℃에서 추가의 20분 동안 인큐베이션하였다. 이어서 세포를 세척하고, 세포내 고정 완충제 (비디 바이오사이언시스(BD Biosciences))에서 고정시켰다. 모든 세포를 애튠(Attune) NxT 유동 세포계측기 (써모피셔 사이언티픽(ThermoFisher Scientific)) 상에서 획득하고, 데이터를 FCS 익스프레스(FCS Express) 또는 플로우조(FlowJo) 중 어느 하나로 분석하였다.
세포계측 비드 어레이 (CBA). 스트렙타비딘 코팅된 플레이트 (이글 바이오사이언시스(Eagle Biosciences))를 세척 완충제 (1% BSA 및 0.05% 트윈20으로 보충된 PBS)로 3회 세척하고, 이어서 100-0.01 ng/웰의 범위의 상이한 농도로 comPACT로 코팅하였다. comPACT를 갖지 않는 웰 및 미스매칭된 comPACT로 코팅된 웰을 대조군으로서 사용하였다. 플레이트를 실온에서 2시간 동안 인큐베이션하고, 세척 완충제로 3회 세척하고, 이어서 3% 인간 AB 혈청으로 보충된 TexMACS로 3회 세척하여 트윈20을 제거하였다. T 세포를 3% 인간 AB 혈청으로 보충된 TexMACS로 2회 세척하고, 3% 인간 AB 혈청으로 보충된 TexMACS 및 1X 페니실린-스트렙토마이신 용액에서 100만개 세포/mL로 재현탁시켰다. T 세포를 comPACT 코팅된 플레이트 상으로 100 μL/웰로 플레이팅하고, 37℃, 5% CO2에서 인큐베이션하였다. 24시간 후, 상청액을 수집하고, 시토카인 농도를 BD 세포계측 비드 어레이 (CBA) 인간 Th1/Th2 시토카인 키트 II (카탈로그 번호 551809)를 제조업체의 프로토콜에 따라 사용하여 분석하였다. 포획 비드를 배양 상청액과 혼합하고, 광으로부터 보호된 RT에서 3시간 동안 검출 시약과 함께 인큐베이션하고, 세척하고, 세척 완충제에 재현탁시켰다. 샘플을 애튠 NxT 유동 세포계측기 상에서 검정하고, 데이터를 플로우조로 분석하였다. EC50은 최대 반응의 50%를 유발하는 동족 comPACT의 농도를 나타내며, 다양한 comPACT 농도에 걸친 IFNγ 분비의 최소-제곱 적합을 이용하여 계산된다.
세포내 염색. T 세포를 지시된 날에 유동 세포계측법을 위해 염색하였다. T 세포를 먼저 생존력 염료로 4℃에서 20분 동안 염색하고, 이어서 세척하고, 표면 항체 (항-CD8α, 항-CD8β, 항-CD4)와 함께 4℃에서 추가의 20분 동안 인큐베이션하였다. 이어서 T 세포를 세척하고, 세포내 염색을 위해 투과화하였다. T 세포를 항-2A 펩티드로 또는 항-IFNγ, 항-TNF, 또는 항-IL2로 투과화 완충제에서 4℃에서 20분 동안 염색하였다. T 세포를 세포내 고정 완충제 (비디 바이오사이언시스)에서 고정시켰다. 샘플을 애튠 NxT 유동 세포계측기 (써모피셔 사이언티픽) 상에서 검정하고, FCS 익스프레스 또는 플로우조 중 어느 하나로 분석하였다.
T 세포 증식 검정. 편집된 CD4 및 CD8 T 세포를 e450 증식 염료 (이바이오사이언스(eBioscience))로 제조업체의 지시서에 따라 표지하였다. 표지된 세포를 상기 기재된 바와 같이 다양한 농도로 comPACT 코팅된 플레이트 상에서 자극시켰다. T 세포를 48-96시간에 걸쳐 수거하고, e450 염료의 희석에 의해 측정된 바와 같은 증식에 대해 분석하였다.
T 세포 살해 검정. HLA-매칭된 세포주를 동족 신생항원 펩티드 또는 미스매칭된 펩티드로 37℃, 5% CO2에서 1시간 동안 펄싱하였다. 세포를 배지로 3회 세척하여 임의의 비결합된 펩티드를 제거하고, 이어서 상기 기재된 e450 증식 염료로 표지된 편집된 CD4 및 CD8 T 세포와 공동-배양하였다. 공동-배양물을 37℃에서 48시간 동안 5% CO2와 함께 인큐베이션한 후, 수거하였다. 세포를 세척하고, 고정가능한 생존력 염료로 염색하여 살해 효율을 결정하였다. e450 증식 염료를 사용하여 편집된 T 세포를 표적 세포로부터 구별하였다.
CD8 산물 1의 생성 및 확인. 네오TCR 베타 및 알파 서열의 상류의 P2A 부위에 의해 플랭킹된 CD8α의 코딩 서열 (CDS)로 이루어진 발현 구축물을 합성한다. 간략하게, 인간 CD8α의 CDS를 제한 부위의 상류의 및 그로 플랭킹된 GSG-링커 및 P2A 부위로 합성한다. 관심의 네오TCR 발현 벡터 및 합성된 CD8α 구축물을 제한 효소와 함께 인큐베이션하고, 함께 라이게이션하여 최종 HDR 구축물을 생성하였다. CD8 구축물 1을 TCRα 및 β 로커스를 표적화하는 gRNA-Cas9 RNP와 함께 전기천공하였다. CD8 T 세포 (그러나 CD4 T 세포는 아님) 중에서 덱스트라머에 결합하는 것으로 공지된 모델 네오TCR (예를 들어 TCR097)을 사용하여 CD8α 트랜스진의 발현이 이들 TCR이 CD4 T 세포 중에서 덱스트라머에 결합하는 것을 가능하게 함을 입증하였다.
유전자 전달 및 CD4 T 세포의 표면 상의 CD8α의 발현의 효율을 시험하기 위해, 조작된 CD4 T 세포를 항-CD8α 항체로 염색하고, 트랜스진의 표면 발현을 상기 기재된 바와 같이 유동 세포계측법에 의해 확인한다. 단지 CD8 T 세포 중에서 덱스트라머에 결합하는 것으로 공지된 네오TCR (예를 들어, TCR 097)을 사용하여 CD8α 트랜스진의 발현이 이들 TCR이 CD4 T 세포 중에서 덱스트라머에 결합하는 것을 가능하게 함을 입증하였다. 도 13a, 13b, 14, 15a, 및 15b를 참조한다. 더욱이, 야생형 및 유전자 조작된 CD8α T 세포 상의 CD8α 발현을 평가하여 CD8α 트랜스진의 첨가가 CD8 T 세포 상의 CD8α의 표면 수준을 증가시켰는지 여부를 결정하였다. CD8α 트랜스진을 발현하도록 조작된 CD4 T 세포는 CD4 및 CD8α에 대해 이중-양성이었다.
CD8 T 세포를 또한 CD8α 트랜스진을 발현하도록 조작하고, 상기 기재된 바와 같이 특징규명하였다. 도 15a 및 15b. 상대 CD8α 유전자 발현을 또한 RT-qPCR을 통해 정량화하고, 대조군 비-조작된 CD8 T 세포와 비교하였다. CD8α 트랜스진을 발현하는 CD8 T 세포는 CD8α 발현의 내인성 수준보다 더 높았다.
동족 항원의 직면 시 T 세포 증식에 대한 CD8 발현의 효과. 편집된 T 세포를 상기 기재된 바와 같이 증식 염료로 염색하였다. 염색 후, T 세포를 다양한 농도의 동족 comPACT 단백질로 자극시켰다. 48-72시간 후, T 세포를 수거하고, 상기 기재된 바와 같이 항-CD4, 항-CD8, 및 항-2A 펩티드로 염색하였다. 편집된 T 세포를 2A 발현에 의해 확인하였다. CD4 및 CD8 T 세포의 증식을 증식성 염료의 희석을 정량화함으로써 결정하였다. CD8α 트랜스진을 결여한 네오TCR-발현 T 세포를 음성 대조군으로서 사용하였다. CD8α 트랜스진을 발현하는 네오TCR CD4 T 세포는 CD8α 발현을 결여한 CD4 T 세포보다 더 낮은 농도의 동족 comPACT에 반응하여 증식하였다.
동족 항원의 직면 시 시토카인 생산에 대한 CD8α 발현의 효과. 증식에 추가로, 세포내 시토카인 염색을 통한 이펙터 시토카인 생산을 측정하였다. 이 검정에서, 네오TCR 산물 및 CD8 산물 1을 브레펠딘 A의 존재 하에서 5시간 동안 다양한 농도의 동족 comPACT로 자극시켰다. 자극 후, T 세포를 항-CD4 및 항-CD8α로 염색하였다. 세포를 투과화하고, 항-P2A 펩티드, 항-IFNy, 항-TNF, 및 항-IL2로 염색하였다. CD8α 트랜스진을 발현하는 네오TCR CD4 T 세포는 CD8α 발현을 결여한 네오TCR CD4 T 세포보다 더 낮은 농도의 동족 comPACT에 반응하여 이펙터 시토카인을 생산하였다.
동족 항원의 직면 시 살해 활성에 대한 CD8α 발현의 효과. 이펙터 기능을 평가하기 위해, 편집된 CD4 및 CD8 T 세포를 상기 기재된 바와 같이 동족 펩티드로 펄싱된 HLA-매칭된 표적 세포와 함께 배양하였다. CD4 및 CD8 T 세포를 별개로 편집하여 표적 세포를 살해하는 CD8α를 발현하는 CD4 T 세포의 능력을 평가하였다. CD8α 트랜스진을 발현하는 네오TCR CD4 T 세포는 CD8α 발현을 결여한 네오TCR CD4 T 세포보다 더 큰 분율의 동족 펩티드를 제시하는 표적 세포를 살해하였다.
실시예 3. CD8 산물 2의 생성
CD8α를 발현하도록 조작된 CD4 T 세포는 CD8β 발현을 결여한다. 그러나, CD8β는 LCK에 대해 더 높은 친화도를 갖는다 (Irie et al., 1998, J. Immunol, 161(1), 183-191). 따라서, T 세포를 CD8α와 함께 CD8β를 공동-발현하도록 편집하였다 (즉, CD8 산물 2). 이전에 기재된 바와 같이 P2A 부위에 의해 플랭킹된 CD8β, P2A 부위에 의해 플랭킹된 CD8α, 이어서 TRB 및 TRA 대립유전자를 함유하는 추가의 구축물을 생성한다. CD8α 및 CD8β를 발현하는 CD4 및 CD8 T 세포를 상기 기재된 동일한 검정을 사용하여 평가한다. CD8α 및 CD8 β 서열을 갖는 예시적인 발현 구축물은 도 11b에 나타내어진다.
CD8β 발현을 또한 편집된 CD4 T 세포에서 평가하였다. CD8α 및 CD8β 트랜스진을 발현하는 네오TCR CD4 T 세포는 CD8α 트랜스진 단독을 발현하는 CD4 T 세포보다 더 낮은 농도의 동족 comPACT에 반응하여 증식하였다. CD8α 및 CD8β 트랜스진을 발현하는 네오TCR CD4 T 세포는 또한 CD8α 트랜스진 단독을 발현하는 네오TCR CD4 T 세포보다 더 낮은 농도의 동족 comPACT에 반응하여 이펙터 시토카인을 생산하였다. 그리고, CD8α 및 CD8β 트랜스진을 발현하는 네오TCR CD4 T 세포는 CD8α 트랜스진 단독을 발현하는 네오TCR CD4 T 세포보다 더 큰 분율의 동족 펩티드를 제시하는 표적 세포를 살해하였다.
실시예 4. 키메라 CD8α 및 CD8β 구축물 및 CD8 산물 3 및 4의 생성
T 세포의 효율적인 편집 및 네오TCR의 발현을 보장하기 위해, CD8β의 세포내 도메인에 연결된 CD8α의 세포외 및 막횡단 도메인에 대한 코딩 서열로 구성된 키메라 단백질을 생성하였다. CD8β 서열의 세포내 도메인에 연결된 CD8α의 세포외 및 막횡단 도메인을 갖는 예시적인 발현 구축물 (즉, CD8 산물 3)은 도 11c에 나타내어진다.
더욱이, CD4의 세포내 도메인은 CD8보다 훨씬 더 높은 LCK에 대한 친화도를 갖는다 (Irie et al., 1998). 따라서, CD4의 세포내 도메인에 연결된 CD8α의 세포외 및 막횡단 도메인에 대한 코딩 서열을 함유하는 제2 키메라 단백질을 생성하였다. CD4 서열의 세포내 도메인에 연결된 CD8α의 세포외 및 막횡단 도메인을 갖는 예시적인 발현 구축물 (즉, CD8 산물 4)은 도 11d에 나타내어진다.
CD8 산물 3 및 4를 발현하는 CD4 및 CD8 T 세포를 상기 기재된 동일한 검정을 사용하여 평가하였다.
CD8α-CD8β-ID 트랜스진을 발현하는 네오TCR CD4 T 세포는 CD8α 트랜스진 단독을 발현하는 CD4 T 세포보다 더 낮은 농도의 동족 comPACT에 반응하여 증식하였다. CD8α-CD8β-ID 트랜스진을 발현하는 네오TCR CD4 T 세포는 CD8α 트랜스진 단독을 발현하는 네오TCR CD4 T 세포보다 더 낮은 농도의 동족 comPACT에 반응하여 이펙터 시토카인을 생산하였다. CD8α-CD8β-ID 트랜스진을 발현하는 네오TCR CD4 T 세포는 CD8α-CD8β-ID 트랜스진을 발현하는 네오TCR CD4 T 세포보다 더 큰 분율의 동족 펩티드를 제시하는 표적 세포를 살해하였다.
CD8α-CD4-ID 트랜스진을 발현하는 네오TCR CD4 T 세포는 CD8α-CD8β-ID 트랜스진을 발현하는 네오TCR CD4 T 세포보다 더 낮은 농도의 동족 comPACT에 반응하여 증식하였다. CD8α-CD4 트랜스진을 발현하는 네오TCR CD4 T 세포는 CD8α-CD8β-ID 트랜스진을 발현하는 네오TCR CD4 T 세포보다 더 낮은 농도의 동족 comPACT에 반응하여 이펙터 시토카인을 생산하였다.
CD8α-CD4-ID 트랜스진을 발현하는 네오TCR CD4 T 세포는 CD8α-CD8β-ID 트랜스진을 발현하는 네오TCR CD4 T 세포보다 더 큰 분율의 동족 펩티드를 제시하는 표적 세포를 살해하였다. CD8α-CD4-ID 트랜스진을 발현하는 네오TCR CD8 T 세포 트랜스진을 결여한 네오TCR CD8 T 세포보다 더 낮은 농도의 동족 comPACT에 반응하여 증식하였다. CD8α-CD4 트랜스진을 발현하는 네오TCR CD8 T 세포는 트랜스진을 결여한 네오TCR CD8 T 세포보다 더 낮은 농도의 동족 comPACT에 반응하여 이펙터 시토카인을 생산하였다. CD8α-CD4-ID 트랜스진을 발현하는 네오TCR CD8 T 세포는 트랜스진을 결여한 네오TCR CD8 T 세포보다 더 큰 분율의 동족 펩티드를 제시하는 표적 세포를 살해하였다.
실시예 5. CD8 산물은 네오E-HLA 표적 인식에 대한 증가된 민감도를 가지며, 전염증성 및 세포독성 기능을 촉발시킨다
MHC-I 네오TCR을 결장직장암을 갖는 환자의 혈액으로부터 포획된 네오E-특이적 T 세포로부터 클로닝하였다. 건강한 공여자 CD8 및 CD4 T 세포를 클로닝된 MHC-I 네오TCR 단독을 발현하도록 또는 유전자-편집된 T 세포에서 이소성 CD8 공-수용체의 조작을 포함하도록 정확성 게놈 조작하였다. 유동 세포계측 분석을 사용하여 네오TCR 및 이소성 CD8 공-수용체 (즉, CD8 구축물 1-4의 CD8 및 CD4 성분)의 표면 발현을 각각 평가하였다. 보다 낮은 친화도, CD8-의존성 네오TCR에 대해 CD4 T 세포 중에서 네오TCR 결합의 구제를 관찰하였다. 중요하게는, 동족 항원으로의 자극에 반응하여, CD107a 및 세포내 IFNy 염색은 CD4 T 세포에 의한 MHC-I 네오TCR-유도된 이펙터 기능의 민감도의 10-100배 증가를 밝혀내었으며, 특이성에 대한 효과는 없었다. 기능성 또는 민감도의 변화는 추가의 CD8 공-수용체의 발현에 의해 CD8 T 세포 상에서 보이지 않았다.
이들 결과는 CD4 T 세포 내로의 CD8-의존성 MHC-I 네오TCR과 함께 CD8 공-수용체의 동시 정확성 게놈 조작 (즉, CD8 산물 1-4)이 네오E-HLA 표적 인식에 대한 그들의 민감도를 유의하게 증가시킬 뿐만 아니라, 항원-특이성을 손상시키지 않으면서 전염증성 및 세포독성 기능을 촉발시킴을 입증한다.
실시예 6. 다양한 LCK 친화도를 갖는 CD8 산물의 생성 및 디자인
본원에 기재된 바와 같이, 4가지 부류의 CD8 산물을 생성하였다:
1. CD8α 동종이량체 (CD8 구축물 1)
2. CD8α-P2A-CD8β (CD8 구축물 2)
3. CD8β 세포내 도메인을 갖는 CD8α (CD8 구축물 3)
4. CD4 세포내 도메인을 갖는 CD8α 동종이량체 (CD8 구축물 4)
도 10에 나타내어진 바와 같이, 이들 CD8 구축물 및 생성된 CD8 산물을 다양한 정도의 LCK 친화도를 허용하도록 디자인하였다. 예측된 바와 같이, CD8 산물 1은 가장 낮은 LCK 친화도를 갖는 것으로 나타났고, 이어서 CD8 산물 2, CD8 산물 3, 및 CD8 산물 4였다 (그 순서에서 CD8 산물 4는 가장 높은 LCK 친화도를 가짐).
CD8 산물 4의 높은 친화도에 기반하여, 이 산물을 네오TCR 산물에 비해 CD8 산물 1-4의 증가된 세포 살해 능력을 예시하는 세포 살해 검정에 사용하였다.
CD4+ T 세포를 도 2d 및 3d에 기재된 CD8 산물 4 (산물에서 네오TCR로서 TCR097을 가짐)를 발현하도록 본원에 기재된 바와 같이 조작하였다. SW620 세포주는 R20Q 돌연변이 (TCR097에 대한 동족 항원)를 이종으로 발현하도록 조작되었다. 네오TCR097을 발현하는 CD8 산물 4를 SW620 이종 세포와 조합하였다. 도 13a 및 13b에 나타내어진 바와 같이, CD8 산물 4는 TCR097을 또한 발현하는 네오TCR 산물보다 동족 항원 발현 SW620 세포의 실질적으로 더 양호한 살해를 제공하였다. 도 13a에 나타내어진 실험을 1:1의 E:T 비로 수행하였으며, 그래프에 나타내어진 바와 같이, TCR097을 발현하는 네오TCR 산물은 동족 항원 발현 SW620 세포의 살해에 있어서 임의의 효능을 나타내지 않았다. 도 13b에 나타내어진 실험을 2:1의 E:T 비로 수행하였으며, TCR097을 발현하는 네오TCR 산물은 동족 항원 발현 SW620 세포를 살해하는 일부 능력을 나타내었지만, TCR097을 발현하는 CD8 산물 4가 우수한 효능을 가졌음이 실험으로부터 명백하였다.
도 13a 및 13b에 제공된 데이터를 갖는 상기 실험에 사용된 동일한 조작된 CD4+ 세포를 또한 R20Q 돌연변이를 동형접합성으로 발현하도록 조작된 SW620 세포주에 대해 시험하였다. 이 실험에서, 동족 항원의 높은 발현은 저 친화도 네오TCR097에 대해 보상할 수 있었으며, TCR097을 발현하는 네오TCR 산물 및 TCR097을 발현하는 CD8 산물 4 둘 다는 SW620 세포를 살해하는데 있어서 효능을 나타내었다. 그러나, 동형접합성 SW620 세포에서 동족 항원의 높은 발현은 생리학적으로 관련되지 않으며, 이 실험은 그들을 CD4 세포내 도메인을 갖는 CD8α 동종이량체를 또한 포함하도록 추가로 조작함으로써 (즉, CD8 산물 4), 효과적으로 종양 세포와 결속하고 이를 살해할 수 없는 저 친화도 TCR을 갖는 네오TCR 산물을 구제하는 능력을 강조하는 역할을 한다.
CD8 산물의 효능의 최종 제어 및 입증으로서, CD8 T 세포를 또한 네오TCR097 및 CD4 세포내 도메인을 갖는 CD8α 동종이량체를 발현하도록 형질감염시켰다 (즉, CD4 T 세포 대신 CD8 T 세포를 사용한 CD8 산물 4). 도 15a 및 15b에서 상부 그래프에 나타내어진 바와 같이, CD8 산물 4는 산물이 CD4 T 세포로부터 제조된 경우 네오TCR 산물보다 SW620 세포의 실질적으로 더 양호한 살해를 제공하였다. 그러나, CD8 산물 4 및 네오TCR 산물이 CD8 T 세포로부터 제조된 경우 (도 15a 및 15b에서 하부 그래프), 네오TCR 산물의 능력은 CD8 T 세포에서의 내인성 CD8 발현 때문에 구제되었다. 그래프의 오버레이가 나타내어지지 않지만, 도 15a 및 15b에서 상부 그래프에 나타내어진 CD4 T 세포에서의 CD8 산물 4는 하부 2개의 그래프에서 CD8 T 세포에서의 CD8 산물 4보다 더 양호한 효능을 갖는 것으로 나타남은 또한 주목할 만하며; 이는 종양 사멸 및 치료를 필요로 하는 암을 갖는 환자의 유효 치료를 초래하는 종양 세포의 동족 항원과 결속하는 본원에 기재된 CD8 산물의 우수한 능력을 시사한다.
실시예 6. CD8 산물은 네오TCR 민감도를 유지하면서 증가된 CD4 T 세포 민감도를 갖는다
CD8 구축물이 적절하게 발현되었음을 확인하기 위해, CD8 산물 1, 2, 3, 및 4를 시험하여 CD8α의 표면 발현을 결정하였다. CD8 산물 1, 2, 3, 및 4 각각은 정상적인 CD8α 표면 발현을 나타내었음이 보여졌다. CD8 산물 4로부터의 대표적인 데이터는 도 16에 나타내어진다.
CD8 구축물이 어떻게 CD8 산물에서 발현된 네오TCR의 동족 항원에 대한 CD4 T 세포 민감도 및 특이성에 영향을 미치는지를 결정하는 것은 또한 중요하였다. 민감도 실험을 수행하였으며, CD8 산물 1-4는 증가된 CD4 T 세포 민감도를 나타내었음이 보여졌다 (도 17a). 특이성 실험을 또한 CD8 산물 1-4에 대해 수행하였다. CD8 산물 1, 2, 3, 및 4는 네오TCR097로 제조되었다. CD8 산물 1, 2, 3, 및 4 (네오TCR097을 발현함)를 시험하여 네오TCR097에 대한 동족 항원에 대한 이들 산물의 특이성을 평가하는 실험을 수행하였다. 도 17b에 나타내어진 바와 같이, CD8 산물 1, 2, 3, 및 4 (네오TCR097을 발현함)는 네오TCR097에 대한 동족 항원에 대해 특이적이었으며, 미스매칭된 항원에 노출된 경우 활성을 나타내지 않았다. 특이성을 T 세포 활성화의 증거인 INFγ 및 CD107 생산에 의해 결정하였다. 따라서, 본원에 기재된 CD8 산물은 동일한 네오TCR을 발현하는 네오TCR 산물에 비해 CD4 T 세포에 대한 증가된 민감도를 가지며, 발현된 네오TCR에 대한 동족 항원에 대한 그들의 특이성을 유지한다.
마지막으로, CD8 구축물이 CD8-의존성 및 CD8-비의존성 네오TCR에 대해 갖는 영향을 조사하기 위한 실험을 수행하였다. CD8-의존성 네오TCR은 CD8 세포가 CD8α를 발현하도록 조작될 것이기 때문에 동족 항원에 대해 증가된 민감도를 나타낼 것으로 및 CD8-비의존성 네오TCR은 네오TCR의 비의존성 성질 때문에 증가된 민감도를 나타내지 않을 것으로 예상되었다. 그러나, 네오TCR 산물 1, 2, 3, 및 4는 놀랍게도 CD8-의존성 (예를 들어, 네오TCR097) 및 CD8-비의존성 (예를 들어, 네오TCR089) 네오TCR의 민감도를 증가시킨 것으로 나타났다. 따라서, CD8 구축물 1, 2, 3, 및 4는 이들이 CD8-의존성 또는 CD8-비의존성인지 여부와 무관하게, 모든 네오TCR에 대해 동족 네오TCR 항원을 갖는 종양 세포의 네오TCR 결속 및 T 세포 살해를 개선시킬 수 있는 것으로 나타났다.
본 발명을 자세하게 및 일부는 특히 몇몇 기재된 실시양태에 관하여 기재하였지만, 이는 임의의 이러한 상세사항 또는 실시양태 또는 임의의 특정 실시양태에 제한되어야 하는 것으로 의도되지 않으며, 이는 첨부된 청구범위에 관하여, 종래 기술의 관점에서 이러한 청구범위의 가장 넓은 가능한 해석을 제공하도록, 및 따라서, 본 발명의 의도된 범위를 효과적으로 포괄하도록 해석되어야 한다.
본원에 언급된 모든 간행물, 특허 출원, 특허, 및 다른 참고문헌은 그 전문이 참조로 포함된다. 상충되는 경우, 정의를 포함한 본 명세서가 지배할 것이다. 또한, 섹션 표제, 물질, 방법, 및 실시예는 단지 예시적이며, 제한적인 것으로 의도되지 않는다.
SEQUENCE LISTING
<110> PACT PHARMA, INC.
<120> COMPOSITIONS AND METHODS FOR THE TREATMENT OF CANCER USING A CD8
ENGINEERED T CELL THERAPY
<130> 087520.0145
<140>
<141>
<150> 62/841,748
<151> 2019-05-01
<150> 62/841,753
<151> 2019-05-01
<160> 148
<170> PatentIn version 3.5
<210> 1
<211> 926
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Left Homology Arm_NeoTCR Product
<400> 1
acattaaaaa cacaaaatcc tacggaaata ctgaagaatg agtctcagca ctaaggaaaa 60
gcctccagca gctcctgctt tctgagggtg aaggatagac gctgtggctc tgcatgactc 120
actagcactc tatcacggcc atattctggc agggtcagtg gctccaacta acatttgttt 180
ggtactttac agtttattaa atagatgttt atatggagaa gctctcattt ctttctcaga 240
agagcctggc taggaaggtg gatgaggcac catattcatt ttgcaggtga aattcctgag 300
atgtaaggag ctgctgtgac ttgctcaagg ccttatatcg agtaaacggt agtgctgggg 360
cttagacgca ggtgttctga tttatagttc aaaacctcta tcaatgagag agcaatctcc 420
tggtaatgtg atagatttcc caacttaatg ccaacatacc ataaacctcc cattctgcta 480
atgcccagcc taagttgggg agaccactcc agattccaag atgtacagtt tgctttgctg 540
ggcctttttc ccatgcctgc ctttactctg ccagagttat attgctgggg ttttgaagaa 600
gatcctatta aataaaagaa taagcagtat tattaagtag ccctgcattt caggtttcct 660
tgagtggcag gccaggcctg gccgtgaacg ttcactgaaa tcatggcctc ttggccaaga 720
ttgatagctt gtgcctgtcc ctgagtccca gtccatcacg agcagctggt ttctaagatg 780
ctatttcccg tataaagcat gagaccgtga cttgccagcc ccacagagcc ccgcccttgt 840
ccatcactgg catctggact ccagcctggg ttggggcaaa gagggaaatg agatcatgtc 900
ctaaccctga tcctcttgtc ccacag 926
<210> 2
<211> 74
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRAC CDS I_NeoTCR Product
<400> 2
atatccagaa ccctgaccct gccgtgtacc agctgagaga ctctaaatcc agtgacaagt 60
ctgtctgcct attc 74
<210> 3
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_NeoTCR Product
<400> 3
gaattcggct ccgga 15
<210> 4
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A 1_NeoTCR Product
<400> 4
gccactaact tctccctgtt gaaacaggct ggcgatgttg aagaaaaccc cggtcct 57
<210> 5
<211> 78
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
HGH Signal Sequence and Furin sequence_NeoTCR Product
<400> 5
atggccaccg gctctagaac aagcctgctg ctcgcttttg gcctgctctg cctcccatgg 60
ctccaagaag gatctgct 78
<210> 6
<211> 345
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Exemplary TRB_VDJ (TCR097)_NeoTCR Product
<400> 6
aatgctggtg tcactcagac cccaaaattc cgcatcctga agataggaca gagcatgaca 60
ctgcagtgta cccaggatat gaaccataac tacatgtact ggtatcgaca agacccaggc 120
atggggctga agctgattta ttattcagtt ggtgctggta tcactgataa aggagaagtc 180
ccgaatggct acaacgtctc cagatcaacc acagaggatt tcccgctcag gctggagttg 240
gctgctccct cccagacatc tgtgtacttc tgtgccagct ccctacaggt tccctacaat 300
gagcagttct tcgggccagg gacacggctc accgtgctag aggac 345
<210> 7
<211> 534
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRBC Constant Region_NeoTCR Product
<400> 7
ctgaaaaacg tgttccctcc aaaagtggcc gtgttcgagc cttctgaggc cgagatcagc 60
cacacacaga aagccacact cgtgtgtctg gctaccggct tctaccccga tcacgtggaa 120
ctgtcttggt gggtcaacgg caaagaggtg cacagcggcg tcagcacaga tccccagcct 180
ctgaaagaac agcccgctct gaacgacagc cgctactgcc tgtctagcag actgagagtg 240
tccgccacct tctggcagaa ccccagaaac cacttcagat gccaggtcca gttctacggc 300
ctgagcgaga acgatgagtg gacccaggac agagccaagc ctgtgacaca gatcgtgtct 360
gccgaagcct ggggcagagc cgattgtggc tttaccagcg agtcatacca gcagggcgtg 420
ctgtctgcca ccatcctgta tgagatcctg ctcggcaagg ccacactgta cgctgtgctg 480
gtgtctgctc tggtgctgat ggctatggtc tcccgggagc gcatccccga ggcc 534
<210> 8
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Furin cleavage site_NeoTCR Product
<400> 8
cgggccaagc gg 12
<210> 9
<211> 9
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_NeoTCR Product
<400> 9
ggcagcggc 9
<210> 10
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_NeoTCR Product
<400> 10
gccaccaact tcagcctgct gaagcaggcc ggcgacgtgg aggagaaccc cggccct 57
<210> 11
<211> 78
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
HGH SS_NeoTCR Product
<400> 11
atggccacag gcagcagaac atctctgctg ctggccttcg gactgctgtg tctgccttgg 60
ctgcaagagg gttccgcc 78
<210> 12
<211> 337
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Exemplary TRA-VDJ (TCR097)_NeoTCR Product
<400> 12
gctcagacag tcactcagtc tcaaccagag atgtctgtgc aggaggcaga gaccgtgacc 60
ctgagctgca catatgacac cagtgagagt gattattatt tattctggta caagcagcct 120
cccagcaggc agatgattct cgttattcgc caagaagctt ataagcaaca gaatgcaaca 180
gagaatcgtt tctctgtgaa cttccagaaa gcagccaaat ccttcagtct caagatctca 240
gactcacagc tgggggatgc cgcgatgtat ttctgtgctt ttgggaactt caacaaattt 300
tactttggat ctgggaccaa actcaatgta aaaccaa 337
<210> 13
<211> 74
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TCR-alpha/constant_NeoTCR Product
<400> 13
atattcagaa ccccgatcct gctgtgtatc agctgcgcga cagcaagagc agcgacaaga 60
gcgtgtgttt gttc 74
<210> 14
<211> 200
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRAC CDS/Right HR arm_NeoTCR Product
<400> 14
accgattttg attctcaaac aaatgtgtca caaagtaagg attctgatgt gtatatcaca 60
gacaaaactg tgctagacat gaggtctatg gacttcaaga gcaacagtgc tgtggcctgg 120
agcaacaaat ctgactttgc atgtgcaaac gccttcaaca acagcattat tccagaagac 180
accttcttcc ccagcccagg 200
<210> 15
<211> 800
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Right HR arm_NeoTCR Product
<400> 15
taagggcagc tttggtgcct tcgcaggctg tttccttgct tcaggaatgg ccaggttctg 60
cccagagctc tggtcaatga tgtctaaaac tcctctgatt ggtggtctcg gccttatcca 120
ttgccaccaa aaccctcttt ttactaagaa acagtgagcc ttgttctggc agtccagaga 180
atgacacggg aaaaaagcag atgaagagaa ggtggcagga gagggcacgt ggcccagcct 240
cagtctctcc aactgagttc ctgcctgcct gcctttgctc agactgtttg ccccttactg 300
ctcttctagg cctcattcta agccccttct ccaagttgcc tctccttatt tctccctgtc 360
tgccaaaaaa tctttcccag ctcactaagt cagtctcacg cagtcactca ttaacccacc 420
aatcactgat tgtgccggca catgaatgca ccaggtgttg aagtggagga attaaaaagt 480
cagatgaggg gtgtgcccag aggaagcacc attctagttg ggggagccca tctgtcagct 540
gggaaaagtc caaataactt cagattggaa tgtgttttaa ctcagggttg agaaaacagc 600
taccttcagg acaaaagtca gggaagggct ctctgaagaa atgctacttg aagataccag 660
ccctaccaag ggcagggaga ggaccctata gaggcctggg acaggagctc aatgagaaag 720
gagaagagca gcaggcatga gttgaatgaa ggaggcaggg ccgggtcaca gggccttcta 780
ggccatgaga gggtagacag 800
<210> 16
<211> 6
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Artificial Sequence_NeoTCR Product
<400> 16
gctagc 6
<210> 17
<211> 620
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
pBR322_origin_NeoTCR Product
<400> 17
cgcgttgctg gcgtttttcc ataggctccg cccccctgac gagcatcaca aaaatcgacg 60
ctcaagtcag aggtggcgaa acccgacagg actataaaga taccaggcgt ttccccctgg 120
aagctccctc gtgcgctctc ctgttccgac cctgccgctt accggatacc tgtccgcctt 180
tctcccttcg ggaagcgtgg cgctttctca tagctcacgc tgtaggtatc tcagttcggt 240
gtaggtcgtt cgctccaagc tgggctgtgt gcacgaaccc cccgttcagc ccgaccgctg 300
cgccttatcc ggtaactatc gtcttgagtc caacccggta agacacgact tatcgccact 360
ggcagcagcc actggtaaca ggattagcag agcgaggtat gtaggcggtg ctacagagtt 420
cttgaagtgg tggcctaact acggctacac tagaagaaca gtatttggta tctgcgctct 480
gctgaagcca gttaccttcg gaaaaagagt tggtagctct tgatccggca aacaaaccac 540
cgctggtagc ggtggttttt ttgtttgcaa gcagcagatt acgcgcagaa aaaaaggatc 600
tcaagaagat cctttgatct 620
<210> 18
<211> 810
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Kanamycin resistance gene (KanR2) _NeoTCR Product
<400> 18
ttagaaaaac tcatcgagca tcaaatgaaa ctgcaattta ttcatatcag gattatcaat 60
accatatttt tgaaaaagcc gtttctgtaa tgaaggagaa aactcaccga ggcagttcca 120
taggatggca agatcctggt atcggtctgc gattccgact cgtccaacat caatacaacc 180
tattaatttc ccctcgtcaa aaataaggtt atcaagtgag aaatcaccat gagtgacgac 240
tgaatccggt gagaatggca aaagtttatg catttctttc cagacttgtt caacaggcca 300
gccattacgc tcgtcatcaa aatcactcgc atcaaccaaa ccgttattca ttcgtgattg 360
cgcctgagcc agacgaaata cgcgatcgct gttaaaagga caattacaaa caggaatcga 420
atgcaaccgg cgcaggaaca ctgccagcgc atcaacaata ttttcacctg aatcaggata 480
ttcttctaat acctggaatg ctgtttttcc ggggatcgca gtggtgagta accatgcatc 540
atcaggagta cggataaaat gcttgatggt cggaagaggc ataaattccg tcagccagtt 600
tagtctgacc atctcatctg taacatcatt ggcaacgcta cctttgccat gtttcagaaa 660
caactctggc gcatcgggct tcccatacaa gcgatagatt gtcgcacctg attgcccgac 720
attatcgcga gcccatttat acccatataa atcagcatcc atgttggaat ttaatcgcgg 780
cctcgacgtt tcccgttgaa tatggctcat 810
<210> 19
<211> 99
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Kanamycin promoter _NeoTCR Product
<400> 19
aacacccctt gtattactgt ttatgtaagc agacagtttt attgttcatg atgatatatt 60
tttatcttgt gcaatgtaac atcagagatt ttgagacac 99
<210> 20
<211> 5137
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Complete NeoTCR Product construct with TCR97 insertion_NeoTCR
Product
<400> 20
ggtaccacat taaaaacaca aaatcctacg gaaatactga agaatgagtc tcagcactaa 60
ggaaaagcct ccagcagctc ctgctttctg agggtgaagg atagacgctg tggctctgca 120
tgactcacta gcactctatc acggccatat tctggcaggg tcagtggctc caactaacat 180
ttgtttggta ctttacagtt tattaaatag atgtttatat ggagaagctc tcatttcttt 240
ctcagaagag cctggctagg aaggtggatg aggcaccata ttcattttgc aggtgaaatt 300
cctgagatgt aaggagctgc tgtgacttgc tcaaggcctt atatcgagta aacggtagtg 360
ctggggctta gacgcaggtg ttctgattta tagttcaaaa cctctatcaa tgagagagca 420
atctcctggt aatgtgatag atttcccaac ttaatgccaa cataccataa acctcccatt 480
ctgctaatgc ccagcctaag ttggggagac cactccagat tccaagatgt acagtttgct 540
ttgctgggcc tttttcccat gcctgccttt actctgccag agttatattg ctggggtttt 600
gaagaagatc ctattaaata aaagaataag cagtattatt aagtagccct gcatttcagg 660
tttccttgag tggcaggcca ggcctggccg tgaacgttca ctgaaatcat ggcctcttgg 720
ccaagattga tagcttgtgc ctgtccctga gtcccagtcc atcacgagca gctggtttct 780
aagatgctat ttcccgtata aagcatgaga ccgtgacttg ccagccccac agagccccgc 840
ccttgtccat cactggcatc tggactccag cctgggttgg ggcaaagagg gaaatgagat 900
catgtcctaa ccctgatcct cttgtcccac agatatccag aaccctgacc ctgccgtgta 960
ccagctgaga gactctaaat ccagtgacaa gtctgtctgc ctattcgaat tcggctccgg 1020
agccactaac ttctccctgt tgaaacaggc tggcgatgtt gaagaaaacc ccggtcctat 1080
ggccaccggc tctagaacaa gcctgctgct cgcttttggc ctgctctgcc tcccatggct 1140
ccaagaagga tctgctaatg ctggtgtcac tcagacccca aaattccgca tcctgaagat 1200
aggacagagc atgacactgc agtgtaccca ggatatgaac cataactaca tgtactggta 1260
tcgacaagac ccaggcatgg ggctgaagct gatttattat tcagttggtg ctggtatcac 1320
tgataaagga gaagtcccga atggctacaa cgtctccaga tcaaccacag aggatttccc 1380
gctcaggctg gagttggctg ctccctccca gacatctgtg tacttctgtg ccagctccct 1440
acaggttccc tacaatgagc agttcttcgg gccagggaca cggctcaccg tgctagagga 1500
cctgaaaaac gtgttccctc caaaagtggc cgtgttcgag ccttctgagg ccgagatcag 1560
ccacacacag aaagccacac tcgtgtgtct ggctaccggc ttctaccccg atcacgtgga 1620
actgtcttgg tgggtcaacg gcaaagaggt gcacagcggc gtcagcacag atccccagcc 1680
tctgaaagaa cagcccgctc tgaacgacag ccgctactgc ctgtctagca gactgagagt 1740
gtccgccacc ttctggcaga accccagaaa ccacttcaga tgccaggtcc agttctacgg 1800
cctgagcgag aacgatgagt ggacccagga cagagccaag cctgtgacac agatcgtgtc 1860
tgccgaagcc tggggcagag ccgattgtgg ctttaccagc gagtcatacc agcagggcgt 1920
gctgtctgcc accatcctgt atgagatcct gctcggcaag gccacactgt acgctgtgct 1980
ggtgtctgct ctggtgctga tggctatggt ctcccgggag cgcatccccg aggcccgggc 2040
caagcggggc agcggcgcca ccaacttcag cctgctgaag caggccggcg acgtggagga 2100
gaaccccggc cctatggcca caggcagcag aacatctctg ctgctggcct tcggactgct 2160
gtgtctgcct tggctgcaag agggttccgc cgctcagaca gtcactcagt ctcaaccaga 2220
gatgtctgtg caggaggcag agaccgtgac cctgagctgc acatatgaca ccagtgagag 2280
tgattattat ttattctggt acaagcagcc tcccagcagg cagatgattc tcgttattcg 2340
ccaagaagct tataagcaac agaatgcaac agagaatcgt ttctctgtga acttccagaa 2400
agcagccaaa tccttcagtc tcaagatctc agactcacag ctgggggatg ccgcgatgta 2460
tttctgtgct tttgggaact tcaacaaatt ttactttgga tctgggacca aactcaatgt 2520
aaaaccaaat attcagaacc ccgatcctgc tgtgtatcag ctgcgcgaca gcaagagcag 2580
cgacaagagc gtgtgtttgt tcaccgattt tgattctcaa acaaatgtgt cacaaagtaa 2640
ggattctgat gtgtatatca cagacaaaac tgtgctagac atgaggtcta tggacttcaa 2700
gagcaacagt gctgtggcct ggagcaacaa atctgacttt gcatgtgcaa acgccttcaa 2760
caacagcatt attccagaag acaccttctt ccccagccca ggtaagggca gctttggtgc 2820
cttcgcaggc tgtttccttg cttcaggaat ggccaggttc tgcccagagc tctggtcaat 2880
gatgtctaaa actcctctga ttggtggtct cggccttatc cattgccacc aaaaccctct 2940
ttttactaag aaacagtgag ccttgttctg gcagtccaga gaatgacacg ggaaaaaagc 3000
agatgaagag aaggtggcag gagagggcac gtggcccagc ctcagtctct ccaactgagt 3060
tcctgcctgc ctgcctttgc tcagactgtt tgccccttac tgctcttcta ggcctcattc 3120
taagcccctt ctccaagttg cctctcctta tttctccctg tctgccaaaa aatctttccc 3180
agctcactaa gtcagtctca cgcagtcact cattaaccca ccaatcactg attgtgccgg 3240
cacatgaatg caccaggtgt tgaagtggag gaattaaaaa gtcagatgag gggtgtgccc 3300
agaggaagca ccattctagt tgggggagcc catctgtcag ctgggaaaag tccaaataac 3360
ttcagattgg aatgtgtttt aactcagggt tgagaaaaca gctaccttca ggacaaaagt 3420
cagggaaggg ctctctgaag aaatgctact tgaagatacc agccctacca agggcaggga 3480
gaggacccta tagaggcctg ggacaggagc tcaatgagaa aggagaagag cagcaggcat 3540
gagttgaatg aaggaggcag ggccgggtca cagggccttc taggccatga gagggtagac 3600
aggctagccg cgttgctggc gtttttccat aggctccgcc cccctgacga gcatcacaaa 3660
aatcgacgct caagtcagag gtggcgaaac ccgacaggac tataaagata ccaggcgttt 3720
ccccctggaa gctccctcgt gcgctctcct gttccgaccc tgccgcttac cggatacctg 3780
tccgcctttc tcccttcggg aagcgtggcg ctttctcata gctcacgctg taggtatctc 3840
agttcggtgt aggtcgttcg ctccaagctg ggctgtgtgc acgaaccccc cgttcagccc 3900
gaccgctgcg ccttatccgg taactatcgt cttgagtcca acccggtaag acacgactta 3960
tcgccactgg cagcagccac tggtaacagg attagcagag cgaggtatgt aggcggtgct 4020
acagagttct tgaagtggtg gcctaactac ggctacacta gaagaacagt atttggtatc 4080
tgcgctctgc tgaagccagt taccttcgga aaaagagttg gtagctcttg atccggcaaa 4140
caaaccaccg ctggtagcgg tggttttttt gtttgcaagc agcagattac gcgcagaaaa 4200
aaaggatctc aagaagatcc tttgatcttt agaaaaactc atcgagcatc aaatgaaact 4260
gcaatttatt catatcagga ttatcaatac catatttttg aaaaagccgt ttctgtaatg 4320
aaggagaaaa ctcaccgagg cagttccata ggatggcaag atcctggtat cggtctgcga 4380
ttccgactcg tccaacatca atacaaccta ttaatttccc ctcgtcaaaa ataaggttat 4440
caagtgagaa atcaccatga gtgacgactg aatccggtga gaatggcaaa agtttatgca 4500
tttctttcca gacttgttca acaggccagc cattacgctc gtcatcaaaa tcactcgcat 4560
caaccaaacc gttattcatt cgtgattgcg cctgagccag acgaaatacg cgatcgctgt 4620
taaaaggaca attacaaaca ggaatcgaat gcaaccggcg caggaacact gccagcgcat 4680
caacaatatt ttcacctgaa tcaggatatt cttctaatac ctggaatgct gtttttccgg 4740
ggatcgcagt ggtgagtaac catgcatcat caggagtacg gataaaatgc ttgatggtcg 4800
gaagaggcat aaattccgtc agccagttta gtctgaccat ctcatctgta acatcattgg 4860
caacgctacc tttgccatgt ttcagaaaca actctggcgc atcgggcttc ccatacaagc 4920
gatagattgt cgcacctgat tgcccgacat tatcgcgagc ccatttatac ccatataaat 4980
cagcatccat gttggaattt aatcgcggcc tcgacgtttc ccgttgaata tggctcataa 5040
caccccttgt attactgttt atgtaagcag acagttttat tgttcatgat gatatatttt 5100
tatcttgtgc aatgtaacat cagagatttt gagacac 5137
<210> 21
<211> 5140
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Complete NeoTCR Product construct with TCR89 insertion_NeoTCR
Product
<400> 21
ggtaccacat taaaaacaca aaatcctacg gaaatactga agaatgagtc tcagcactaa 60
ggaaaagcct ccagcagctc ctgctttctg agggtgaagg atagacgctg tggctctgca 120
tgactcacta gcactctatc acggccatat tctggcaggg tcagtggctc caactaacat 180
ttgtttggta ctttacagtt tattaaatag atgtttatat ggagaagctc tcatttcttt 240
ctcagaagag cctggctagg aaggtggatg aggcaccata ttcattttgc aggtgaaatt 300
cctgagatgt aaggagctgc tgtgacttgc tcaaggcctt atatcgagta aacggtagtg 360
ctggggctta gacgcaggtg ttctgattta tagttcaaaa cctctatcaa tgagagagca 420
atctcctggt aatgtgatag atttcccaac ttaatgccaa cataccataa acctcccatt 480
ctgctaatgc ccagcctaag ttggggagac cactccagat tccaagatgt acagtttgct 540
ttgctgggcc tttttcccat gcctgccttt actctgccag agttatattg ctggggtttt 600
gaagaagatc ctattaaata aaagaataag cagtattatt aagtagccct gcatttcagg 660
tttccttgag tggcaggcca ggcctggccg tgaacgttca ctgaaatcat ggcctcttgg 720
ccaagattga tagcttgtgc ctgtccctga gtcccagtcc atcacgagca gctggtttct 780
aagatgctat ttcccgtata aagcatgaga ccgtgacttg ccagccccac agagccccgc 840
ccttgtccat cactggcatc tggactccag cctgggttgg ggcaaagagg gaaatgagat 900
catgtcctaa ccctgatcct cttgtcccac agatatccag aaccctgacc ctgccgtgta 960
ccagctgaga gactctaaat ccagtgacaa gtctgtctgc ctattcgaat tcggctccgg 1020
agccactaac ttctccctgt tgaaacaggc tggcgatgtt gaagaaaacc ccggtcctat 1080
ggccaccggc tctagaacaa gcctgctgct cgcttttggc ctgctctgcc tcccatggct 1140
ccaagaagga tctgctgatg ctggaatcac ccagagccca agatacaaga tcacagagac 1200
aggaaggcag gtgaccttga tgtgtcacca gacttggagc cacagctata tgttctggta 1260
tcgacaagac ctgggacatg ggctgaggct gatctattac tcagcagctg ctgatattac 1320
agataaagga gaagtctccg atggctatgt tgtctccaga tccaagacag agaatttccc 1380
cctcactctg gagtcagcta cccgctccca gacatctgtg tatttctgcg ccagcagtga 1440
ggacagttac gagcagtact tcgggccggg caccaggctc acggtcacag aggacctgaa 1500
aaacgtgttc cctccaaaag tggccgtgtt cgagccttct gaggccgaga tcagccacac 1560
acagaaagcc acactcgtgt gtctggctac cggcttctac cccgatcacg tggaactgtc 1620
ttggtgggtc aacggcaaag aggtgcacag cggcgtcagc acagatcccc agcctctgaa 1680
agaacagccc gctctgaacg acagccgcta ctgcctgtct agcagactga gagtgtccgc 1740
caccttctgg cagaacccca gaaaccactt cagatgccag gtccagttct acggcctgag 1800
cgagaacgat gagtggaccc aggacagagc caagcctgtg acacagatcg tgtctgccga 1860
agcctggggc agagccgatt gtggctttac cagcgagtca taccagcagg gcgtgctgtc 1920
tgccaccatc ctgtatgaga tcctgctcgg caaggccaca ctgtacgctg tgctggtgtc 1980
tgctctggtg ctgatggcta tggtctcccg ggagcgcatc cccgaggccc gggccaagcg 2040
gggcagcggc gccaccaact tcagcctgct gaagcaggcc ggcgacgtgg aggagaaccc 2100
cggccctatg gccacaggca gcagaacatc tctgctgctg gccttcggac tgctgtgtct 2160
gccttggctg caagagggtt ccgccgccca gtcagtgacc cagcctgaca tccacatcac 2220
tgtctctgaa ggagcctcac tggagttgag atgtaactat tcctatgggg caacacctta 2280
tctcttctgg tatgtccagt cccccggcca aggcctccag ctgctcctga agtacttttc 2340
aggagacact ctggttcaag gcattaaagg ctttgaggct gaatttaaga ggagtcaatc 2400
ttccttcaat ctgaggaaac cctctgtgca ttggagtgat gctgctgagt acttctgtgc 2460
tgtgggtgaa ttggacacag gctttcagaa acttgtattt ggaactggca cccgacttct 2520
ggtcagtcca aatattcaga accccgatcc tgctgtgtat cagctgcgcg acagcaagag 2580
cagcgacaag agcgtgtgtt tgttcaccga ttttgattct caaacaaatg tgtcacaaag 2640
taaggattct gatgtgtata tcacagacaa aactgtgcta gacatgaggt ctatggactt 2700
caagagcaac agtgctgtgg cctggagcaa caaatctgac tttgcatgtg caaacgcctt 2760
caacaacagc attattccag aagacacctt cttccccagc ccaggtaagg gcagctttgg 2820
tgccttcgca ggctgtttcc ttgcttcagg aatggccagg ttctgcccag agctctggtc 2880
aatgatgtct aaaactcctc tgattggtgg tctcggcctt atccattgcc accaaaaccc 2940
tctttttact aagaaacagt gagccttgtt ctggcagtcc agagaatgac acgggaaaaa 3000
agcagatgaa gagaaggtgg caggagaggg cacgtggccc agcctcagtc tctccaactg 3060
agttcctgcc tgcctgcctt tgctcagact gtttgcccct tactgctctt ctaggcctca 3120
ttctaagccc cttctccaag ttgcctctcc ttatttctcc ctgtctgcca aaaaatcttt 3180
cccagctcac taagtcagtc tcacgcagtc actcattaac ccaccaatca ctgattgtgc 3240
cggcacatga atgcaccagg tgttgaagtg gaggaattaa aaagtcagat gaggggtgtg 3300
cccagaggaa gcaccattct agttggggga gcccatctgt cagctgggaa aagtccaaat 3360
aacttcagat tggaatgtgt tttaactcag ggttgagaaa acagctacct tcaggacaaa 3420
agtcagggaa gggctctctg aagaaatgct acttgaagat accagcccta ccaagggcag 3480
ggagaggacc ctatagaggc ctgggacagg agctcaatga gaaaggagaa gagcagcagg 3540
catgagttga atgaaggagg cagggccggg tcacagggcc ttctaggcca tgagagggta 3600
gacaggctag ccgcgttgct ggcgtttttc cataggctcc gcccccctga cgagcatcac 3660
aaaaatcgac gctcaagtca gaggtggcga aacccgacag gactataaag ataccaggcg 3720
tttccccctg gaagctccct cgtgcgctct cctgttccga ccctgccgct taccggatac 3780
ctgtccgcct ttctcccttc gggaagcgtg gcgctttctc atagctcacg ctgtaggtat 3840
ctcagttcgg tgtaggtcgt tcgctccaag ctgggctgtg tgcacgaacc ccccgttcag 3900
cccgaccgct gcgccttatc cggtaactat cgtcttgagt ccaacccggt aagacacgac 3960
ttatcgccac tggcagcagc cactggtaac aggattagca gagcgaggta tgtaggcggt 4020
gctacagagt tcttgaagtg gtggcctaac tacggctaca ctagaagaac agtatttggt 4080
atctgcgctc tgctgaagcc agttaccttc ggaaaaagag ttggtagctc ttgatccggc 4140
aaacaaacca ccgctggtag cggtggtttt tttgtttgca agcagcagat tacgcgcaga 4200
aaaaaaggat ctcaagaaga tcctttgatc tttagaaaaa ctcatcgagc atcaaatgaa 4260
actgcaattt attcatatca ggattatcaa taccatattt ttgaaaaagc cgtttctgta 4320
atgaaggaga aaactcaccg aggcagttcc ataggatggc aagatcctgg tatcggtctg 4380
cgattccgac tcgtccaaca tcaatacaac ctattaattt cccctcgtca aaaataaggt 4440
tatcaagtga gaaatcacca tgagtgacga ctgaatccgg tgagaatggc aaaagtttat 4500
gcatttcttt ccagacttgt tcaacaggcc agccattacg ctcgtcatca aaatcactcg 4560
catcaaccaa accgttattc attcgtgatt gcgcctgagc cagacgaaat acgcgatcgc 4620
tgttaaaagg acaattacaa acaggaatcg aatgcaaccg gcgcaggaac actgccagcg 4680
catcaacaat attttcacct gaatcaggat attcttctaa tacctggaat gctgtttttc 4740
cggggatcgc agtggtgagt aaccatgcat catcaggagt acggataaaa tgcttgatgg 4800
tcggaagagg cataaattcc gtcagccagt ttagtctgac catctcatct gtaacatcat 4860
tggcaacgct acctttgcca tgtttcagaa acaactctgg cgcatcgggc ttcccataca 4920
agcgatagat tgtcgcacct gattgcccga cattatcgcg agcccattta tacccatata 4980
aatcagcatc catgttggaa tttaatcgcg gcctcgacgt ttcccgttga atatggctca 5040
taacacccct tgtattactg tttatgtaag cagacagttt tattgttcat gatgatatat 5100
ttttatcttg tgcaatgtaa catcagagat tttgagacac 5140
<210> 22
<211> 926
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Left HR arm_CD8 Product 1
<400> 22
acattaaaaa cacaaaatcc tacggaaata ctgaagaatg agtctcagca ctaaggaaaa 60
gcctccagca gctcctgctt tctgagggtg aaggatagac gctgtggctc tgcatgactc 120
actagcactc tatcacggcc atattctggc agggtcagtg gctccaacta acatttgttt 180
ggtactttac agtttattaa atagatgttt atatggagaa gctctcattt ctttctcaga 240
agagcctggc taggaaggtg gatgaggcac catattcatt ttgcaggtga aattcctgag 300
atgtaaggag ctgctgtgac ttgctcaagg ccttatatcg agtaaacggt agtgctgggg 360
cttagacgca ggtgttctga tttatagttc aaaacctcta tcaatgagag agcaatctcc 420
tggtaatgtg atagatttcc caacttaatg ccaacatacc ataaacctcc cattctgcta 480
atgcccagcc taagttgggg agaccactcc agattccaag atgtacagtt tgctttgctg 540
ggcctttttc ccatgcctgc ctttactctg ccagagttat attgctgggg ttttgaagaa 600
gatcctatta aataaaagaa taagcagtat tattaagtag ccctgcattt caggtttcct 660
tgagtggcag gccaggcctg gccgtgaacg ttcactgaaa tcatggcctc ttggccaaga 720
ttgatagctt gtgcctgtcc ctgagtccca gtccatcacg agcagctggt ttctaagatg 780
ctatttcccg tataaagcat gagaccgtga cttgccagcc ccacagagcc ccgcccttgt 840
ccatcactgg catctggact ccagcctggg ttggggcaaa gagggaaatg agatcatgtc 900
ctaaccctga tcctcttgtc ccacag 926
<210> 23
<211> 74
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRAC CDS_CD8 Product 1
<400> 23
atatccagaa ccctgaccct gccgtgtacc agctgagaga ctctaaatcc agtgacaagt 60
ctgtctgcct attc 74
<210> 24
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_CD8 Product 1
<400> 24
gaattcggct ccgga 15
<210> 25
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 1
<400> 25
gccactaact tcagcctgtt gaagcaggcc ggcgacgttg aggaaaaccc cggtcct 57
<210> 26
<211> 63
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A Signal peptide_CD8 Product 1
<400> 26
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg 60
ccg 63
<210> 27
<211> 483
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A Extracellular domain_CD8 Product 1
<400> 27
agccagttcc gggtgtcgcc gctggatcgg acctggaacc tgggcgagac agtggagctg 60
aagtgccagg tgctgctgtc caacccgacg tcgggctgct cgtggctctt ccagccgcgc 120
ggcgccgccg ccagtcccac cttcctccta tacctctccc aaaacaagcc caaggcggcc 180
gaggggctgg acacccagcg gttctcgggc aagaggttgg gggacacctt cgtcctcacc 240
ctgagcgact tccgccgaga gaacgagggc tactatttct gctcggccct gagcaactcc 300
atcatgtact tcagccactt cgtgccggtc ttcctgccag cgaagcccac cacgacgcca 360
gcgccgcgac caccaacacc ggcgcccacc atcgcgtcgc agcccctgtc cctgcgccca 420
gaggcgtgcc ggccagcggc ggggggcgca gtgcacacga gggggctgga cttcgcctgt 480
gat 483
<210> 28
<211> 63
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A transmembrane domain_CD8 Product 1
<400> 28
atctacatct gggcgccctt ggccgggact tgtggggtcc ttctcctgtc actggttatc 60
acc 63
<210> 29
<211> 96
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A Intracellular domain_CD8 Product 1
<400> 29
ctttactgca accacaggaa ccgaagacgt gtttgcaaat gtccccggcc tgtggtcaaa 60
tcgggagaca agcccagcct ttcggcgaga tacgtc 96
<210> 30
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Furin cleavage site_CD8 Product 1
<400> 30
agggctaaac gg 12
<210> 31
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_CD8 Product 1
<400> 31
gaattcggct ccgga 15
<210> 32
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 1
<400> 32
gccactaact tctccctgtt gaaacaggct ggcgatgttg aagaaaaccc cggtcct 57
<210> 33
<211> 78
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
HGH/SS/2_CD8 Product 1
<400> 33
atggccaccg gctctagaac aagcctgctg ctcgcttttg gcctgctctg cctcccatgg 60
ctccaagaag gatctgct 78
<210> 34
<211> 345
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Exemplary TRB_VDJ (TCR097) _CD8 Product 1
<400> 34
aatgctggtg tcactcagac cccaaaattc cgcatcctga agataggaca gagcatgaca 60
ctgcagtgta cccaggatat gaaccataac tacatgtact ggtatcgaca agacccaggc 120
atggggctga agctgattta ttattcagtt ggtgctggta tcactgataa aggagaagtc 180
ccgaatggct acaacgtctc cagatcaacc acagaggatt tcccgctcag gctggagttg 240
gctgctccct cccagacatc tgtgtacttc tgtgccagct ccctacaggt tccctacaat 300
gagcagttct tcgggccagg gacacggctc accgtgctag aggac 345
<210> 35
<211> 534
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TCR-beta/constant_CD8 Product 1
<400> 35
ctgaaaaacg tgttccctcc aaaagtggcc gtgttcgagc cttctgaggc cgagatcagc 60
cacacacaga aagccacact cgtgtgtctg gctaccggct tctaccccga tcacgtggaa 120
ctgtcttggt gggtcaacgg caaagaggtg cacagcggcg tcagcacaga tccccagcct 180
ctgaaagaac agcccgctct gaacgacagc cgctactgcc tgtctagcag actgagagtg 240
tccgccacct tctggcagaa ccccagaaac cacttcagat gccaggtcca gttctacggc 300
ctgagcgaga acgatgagtg gacccaggac agagccaagc ctgtgacaca gatcgtgtct 360
gccgaagcct ggggcagagc cgattgtggc tttaccagcg agtcatacca gcagggcgtg 420
ctgtctgcca ccatcctgta tgagatcctg ctcggcaagg ccacactgta cgctgtgctg 480
gtgtctgctc tggtgctgat ggctatggtc tcccgggagc gcatccccga ggcc 534
<210> 36
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Furin cleavage site_CD8 Product 1
<400> 36
cgggccaagc gg 12
<210> 37
<211> 9
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG linker_CD8 Product 1
<400> 37
ggcagcggc 9
<210> 38
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 1
<400> 38
gccaccaact tcagcctgct gaagcaggcc ggcgacgtgg aggagaaccc cggccct 57
<210> 39
<211> 78
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
HGH/SS_CD8 Product 1
<400> 39
atggccacag gcagcagaac atctctgctg ctggccttcg gactgctgtg tctgccttgg 60
ctgcaagagg gttccgcc 78
<210> 40
<211> 337
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Exemplary TRA-VDJ (TCR097) _CD8 Product 1
<400> 40
gctcagacag tcactcagtc tcaaccagag atgtctgtgc aggaggcaga gaccgtgacc 60
ctgagctgca catatgacac cagtgagagt gattattatt tattctggta caagcagcct 120
cccagcaggc agatgattct cgttattcgc caagaagctt ataagcaaca gaatgcaaca 180
gagaatcgtt tctctgtgaa cttccagaaa gcagccaaat ccttcagtct caagatctca 240
gactcacagc tgggggatgc cgcgatgtat ttctgtgctt ttgggaactt caacaaattt 300
tactttggat ctgggaccaa actcaatgta aaaccaa 337
<210> 41
<211> 74
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TCR-alpha/constant_CD8 Product 1
<400> 41
atattcagaa ccccgatcct gctgtgtatc agctgcgcga cagcaagagc agcgacaaga 60
gcgtgtgttt gttc 74
<210> 42
<211> 200
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRAC CDS/right HR arm_CD8 Product 1
<400> 42
accgattttg attctcaaac aaatgtgtca caaagtaagg attctgatgt gtatatcaca 60
gacaaaactg tgctagacat gaggtctatg gacttcaaga gcaacagtgc tgtggcctgg 120
agcaacaaat ctgactttgc atgtgcaaac gccttcaaca acagcattat tccagaagac 180
accttcttcc ccagcccagg 200
<210> 43
<211> 800
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Right HR arm_CD8 Product 1
<400> 43
taagggcagc tttggtgcct tcgcaggctg tttccttgct tcaggaatgg ccaggttctg 60
cccagagctc tggtcaatga tgtctaaaac tcctctgatt ggtggtctcg gccttatcca 120
ttgccaccaa aaccctcttt ttactaagaa acagtgagcc ttgttctggc agtccagaga 180
atgacacggg aaaaaagcag atgaagagaa ggtggcagga gagggcacgt ggcccagcct 240
cagtctctcc aactgagttc ctgcctgcct gcctttgctc agactgtttg ccccttactg 300
ctcttctagg cctcattcta agccccttct ccaagttgcc tctccttatt tctccctgtc 360
tgccaaaaaa tctttcccag ctcactaagt cagtctcacg cagtcactca ttaacccacc 420
aatcactgat tgtgccggca catgaatgca ccaggtgttg aagtggagga attaaaaagt 480
cagatgaggg gtgtgcccag aggaagcacc attctagttg ggggagccca tctgtcagct 540
gggaaaagtc caaataactt cagattggaa tgtgttttaa ctcagggttg agaaaacagc 600
taccttcagg acaaaagtca gggaagggct ctctgaagaa atgctacttg aagataccag 660
ccctaccaag ggcagggaga ggaccctata gaggcctggg acaggagctc aatgagaaag 720
gagaagagca gcaggcatga gttgaatgaa ggaggcaggg ccgggtcaca gggccttcta 780
ggccatgaga gggtagacag 800
<210> 44
<211> 6
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Artificial Sequence_CD8 Product 1
<400> 44
gctagc 6
<210> 45
<211> 620
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
pBR322_origin_CD8 Product 1
<400> 45
cgcgttgctg gcgtttttcc ataggctccg cccccctgac gagcatcaca aaaatcgacg 60
ctcaagtcag aggtggcgaa acccgacagg actataaaga taccaggcgt ttccccctgg 120
aagctccctc gtgcgctctc ctgttccgac cctgccgctt accggatacc tgtccgcctt 180
tctcccttcg ggaagcgtgg cgctttctca tagctcacgc tgtaggtatc tcagttcggt 240
gtaggtcgtt cgctccaagc tgggctgtgt gcacgaaccc cccgttcagc ccgaccgctg 300
cgccttatcc ggtaactatc gtcttgagtc caacccggta agacacgact tatcgccact 360
ggcagcagcc actggtaaca ggattagcag agcgaggtat gtaggcggtg ctacagagtt 420
cttgaagtgg tggcctaact acggctacac tagaagaaca gtatttggta tctgcgctct 480
gctgaagcca gttaccttcg gaaaaagagt tggtagctct tgatccggca aacaaaccac 540
cgctggtagc ggtggttttt ttgtttgcaa gcagcagatt acgcgcagaa aaaaaggatc 600
tcaagaagat cctttgatct 620
<210> 46
<211> 810
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Kanamycin resistance (KanR2) _CD8 Product 1
<400> 46
ttagaaaaac tcatcgagca tcaaatgaaa ctgcaattta ttcatatcag gattatcaat 60
accatatttt tgaaaaagcc gtttctgtaa tgaaggagaa aactcaccga ggcagttcca 120
taggatggca agatcctggt atcggtctgc gattccgact cgtccaacat caatacaacc 180
tattaatttc ccctcgtcaa aaataaggtt atcaagtgag aaatcaccat gagtgacgac 240
tgaatccggt gagaatggca aaagtttatg catttctttc cagacttgtt caacaggcca 300
gccattacgc tcgtcatcaa aatcactcgc atcaaccaaa ccgttattca ttcgtgattg 360
cgcctgagcc agacgaaata cgcgatcgct gttaaaagga caattacaaa caggaatcga 420
atgcaaccgg cgcaggaaca ctgccagcgc atcaacaata ttttcacctg aatcaggata 480
ttcttctaat acctggaatg ctgtttttcc ggggatcgca gtggtgagta accatgcatc 540
atcaggagta cggataaaat gcttgatggt cggaagaggc ataaattccg tcagccagtt 600
tagtctgacc atctcatctg taacatcatt ggcaacgcta cctttgccat gtttcagaaa 660
caactctggc gcatcgggct tcccatacaa gcgatagatt gtcgcacctg attgcccgac 720
attatcgcga gcccatttat acccatataa atcagcatcc atgttggaat ttaatcgcgg 780
cctcgacgtt tcccgttgaa tatggctcat 810
<210> 47
<211> 99
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Kanamycin promoter_CD8 Product 1
<400> 47
aacacccctt gtattactgt ttatgtaagc agacagtttt attgttcatg atgatatatt 60
tttatcttgt gcaatgtaac atcagagatt ttgagacac 99
<210> 48
<211> 5926
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Complete CD8 Product 1 construct with TCR97 insertion_CD8
Product 1
<400> 48
ggtaccacat taaaaacaca aaatcctacg gaaatactga agaatgagtc tcagcactaa 60
ggaaaagcct ccagcagctc ctgctttctg agggtgaagg atagacgctg tggctctgca 120
tgactcacta gcactctatc acggccatat tctggcaggg tcagtggctc caactaacat 180
ttgtttggta ctttacagtt tattaaatag atgtttatat ggagaagctc tcatttcttt 240
ctcagaagag cctggctagg aaggtggatg aggcaccata ttcattttgc aggtgaaatt 300
cctgagatgt aaggagctgc tgtgacttgc tcaaggcctt atatcgagta aacggtagtg 360
ctggggctta gacgcaggtg ttctgattta tagttcaaaa cctctatcaa tgagagagca 420
atctcctggt aatgtgatag atttcccaac ttaatgccaa cataccataa acctcccatt 480
ctgctaatgc ccagcctaag ttggggagac cactccagat tccaagatgt acagtttgct 540
ttgctgggcc tttttcccat gcctgccttt actctgccag agttatattg ctggggtttt 600
gaagaagatc ctattaaata aaagaataag cagtattatt aagtagccct gcatttcagg 660
tttccttgag tggcaggcca ggcctggccg tgaacgttca ctgaaatcat ggcctcttgg 720
ccaagattga tagcttgtgc ctgtccctga gtcccagtcc atcacgagca gctggtttct 780
aagatgctat ttcccgtata aagcatgaga ccgtgacttg ccagccccac agagccccgc 840
ccttgtccat cactggcatc tggactccag cctgggttgg ggcaaagagg gaaatgagat 900
catgtcctaa ccctgatcct cttgtcccac agatatccag aaccctgacc ctgccgtgta 960
ccagctgaga gactctaaat ccagtgacaa gtctgtctgc ctattcgaat tcggctccgg 1020
agccactaac ttcagcctgt tgaagcaggc cggcgacgtt gaggaaaacc ccggtcctat 1080
ggccttacca gtgaccgcct tgctcctgcc gctggccttg ctgctccacg ccgccaggcc 1140
gagccagttc cgggtgtcgc cgctggatcg gacctggaac ctgggcgaga cagtggagct 1200
gaagtgccag gtgctgctgt ccaacccgac gtcgggctgc tcgtggctct tccagccgcg 1260
cggcgccgcc gccagtccca ccttcctcct atacctctcc caaaacaagc ccaaggcggc 1320
cgaggggctg gacacccagc ggttctcggg caagaggttg ggggacacct tcgtcctcac 1380
cctgagcgac ttccgccgag agaacgaggg ctactatttc tgctcggccc tgagcaactc 1440
catcatgtac ttcagccact tcgtgccggt cttcctgcca gcgaagccca ccacgacgcc 1500
agcgccgcga ccaccaacac cggcgcccac catcgcgtcg cagcccctgt ccctgcgccc 1560
agaggcgtgc cggccagcgg cggggggcgc agtgcacacg agggggctgg acttcgcctg 1620
tgatatctac atctgggcgc ccttggccgg gacttgtggg gtccttctcc tgtcactggt 1680
tatcaccctt tactgcaacc acaggaaccg aagacgtgtt tgcaaatgtc cccggcctgt 1740
ggtcaaatcg ggagacaagc ccagcctttc ggcgagatac gtcagggcta aacgggaatt 1800
cggctccgga gccactaact tctccctgtt gaaacaggct ggcgatgttg aagaaaaccc 1860
cggtcctatg gccaccggct ctagaacaag cctgctgctc gcttttggcc tgctctgcct 1920
cccatggctc caagaaggat ctgctaatgc tggtgtcact cagaccccaa aattccgcat 1980
cctgaagata ggacagagca tgacactgca gtgtacccag gatatgaacc ataactacat 2040
gtactggtat cgacaagacc caggcatggg gctgaagctg atttattatt cagttggtgc 2100
tggtatcact gataaaggag aagtcccgaa tggctacaac gtctccagat caaccacaga 2160
ggatttcccg ctcaggctgg agttggctgc tccctcccag acatctgtgt acttctgtgc 2220
cagctcccta caggttccct acaatgagca gttcttcggg ccagggacac ggctcaccgt 2280
gctagaggac ctgaaaaacg tgttccctcc aaaagtggcc gtgttcgagc cttctgaggc 2340
cgagatcagc cacacacaga aagccacact cgtgtgtctg gctaccggct tctaccccga 2400
tcacgtggaa ctgtcttggt gggtcaacgg caaagaggtg cacagcggcg tcagcacaga 2460
tccccagcct ctgaaagaac agcccgctct gaacgacagc cgctactgcc tgtctagcag 2520
actgagagtg tccgccacct tctggcagaa ccccagaaac cacttcagat gccaggtcca 2580
gttctacggc ctgagcgaga acgatgagtg gacccaggac agagccaagc ctgtgacaca 2640
gatcgtgtct gccgaagcct ggggcagagc cgattgtggc tttaccagcg agtcatacca 2700
gcagggcgtg ctgtctgcca ccatcctgta tgagatcctg ctcggcaagg ccacactgta 2760
cgctgtgctg gtgtctgctc tggtgctgat ggctatggtc tcccgggagc gcatccccga 2820
ggcccgggcc aagcggggca gcggcgccac caacttcagc ctgctgaagc aggccggcga 2880
cgtggaggag aaccccggcc ctatggccac aggcagcaga acatctctgc tgctggcctt 2940
cggactgctg tgtctgcctt ggctgcaaga gggttccgcc gctcagacag tcactcagtc 3000
tcaaccagag atgtctgtgc aggaggcaga gaccgtgacc ctgagctgca catatgacac 3060
cagtgagagt gattattatt tattctggta caagcagcct cccagcaggc agatgattct 3120
cgttattcgc caagaagctt ataagcaaca gaatgcaaca gagaatcgtt tctctgtgaa 3180
cttccagaaa gcagccaaat ccttcagtct caagatctca gactcacagc tgggggatgc 3240
cgcgatgtat ttctgtgctt ttgggaactt caacaaattt tactttggat ctgggaccaa 3300
actcaatgta aaaccaaata ttcagaaccc cgatcctgct gtgtatcagc tgcgcgacag 3360
caagagcagc gacaagagcg tgtgtttgtt caccgatttt gattctcaaa caaatgtgtc 3420
acaaagtaag gattctgatg tgtatatcac agacaaaact gtgctagaca tgaggtctat 3480
ggacttcaag agcaacagtg ctgtggcctg gagcaacaaa tctgactttg catgtgcaaa 3540
cgccttcaac aacagcatta ttccagaaga caccttcttc cccagcccag gtaagggcag 3600
ctttggtgcc ttcgcaggct gtttccttgc ttcaggaatg gccaggttct gcccagagct 3660
ctggtcaatg atgtctaaaa ctcctctgat tggtggtctc ggccttatcc attgccacca 3720
aaaccctctt tttactaaga aacagtgagc cttgttctgg cagtccagag aatgacacgg 3780
gaaaaaagca gatgaagaga aggtggcagg agagggcacg tggcccagcc tcagtctctc 3840
caactgagtt cctgcctgcc tgcctttgct cagactgttt gccccttact gctcttctag 3900
gcctcattct aagccccttc tccaagttgc ctctccttat ttctccctgt ctgccaaaaa 3960
atctttccca gctcactaag tcagtctcac gcagtcactc attaacccac caatcactga 4020
ttgtgccggc acatgaatgc accaggtgtt gaagtggagg aattaaaaag tcagatgagg 4080
ggtgtgccca gaggaagcac cattctagtt gggggagccc atctgtcagc tgggaaaagt 4140
ccaaataact tcagattgga atgtgtttta actcagggtt gagaaaacag ctaccttcag 4200
gacaaaagtc agggaagggc tctctgaaga aatgctactt gaagatacca gccctaccaa 4260
gggcagggag aggaccctat agaggcctgg gacaggagct caatgagaaa ggagaagagc 4320
agcaggcatg agttgaatga aggaggcagg gccgggtcac agggccttct aggccatgag 4380
agggtagaca ggctagccgc gttgctggcg tttttccata ggctccgccc ccctgacgag 4440
catcacaaaa atcgacgctc aagtcagagg tggcgaaacc cgacaggact ataaagatac 4500
caggcgtttc cccctggaag ctccctcgtg cgctctcctg ttccgaccct gccgcttacc 4560
ggatacctgt ccgcctttct cccttcggga agcgtggcgc tttctcatag ctcacgctgt 4620
aggtatctca gttcggtgta ggtcgttcgc tccaagctgg gctgtgtgca cgaacccccc 4680
gttcagcccg accgctgcgc cttatccggt aactatcgtc ttgagtccaa cccggtaaga 4740
cacgacttat cgccactggc agcagccact ggtaacagga ttagcagagc gaggtatgta 4800
ggcggtgcta cagagttctt gaagtggtgg cctaactacg gctacactag aagaacagta 4860
tttggtatct gcgctctgct gaagccagtt accttcggaa aaagagttgg tagctcttga 4920
tccggcaaac aaaccaccgc tggtagcggt ggtttttttg tttgcaagca gcagattacg 4980
cgcagaaaaa aaggatctca agaagatcct ttgatcttta gaaaaactca tcgagcatca 5040
aatgaaactg caatttattc atatcaggat tatcaatacc atatttttga aaaagccgtt 5100
tctgtaatga aggagaaaac tcaccgaggc agttccatag gatggcaaga tcctggtatc 5160
ggtctgcgat tccgactcgt ccaacatcaa tacaacctat taatttcccc tcgtcaaaaa 5220
taaggttatc aagtgagaaa tcaccatgag tgacgactga atccggtgag aatggcaaaa 5280
gtttatgcat ttctttccag acttgttcaa caggccagcc attacgctcg tcatcaaaat 5340
cactcgcatc aaccaaaccg ttattcattc gtgattgcgc ctgagccaga cgaaatacgc 5400
gatcgctgtt aaaaggacaa ttacaaacag gaatcgaatg caaccggcgc aggaacactg 5460
ccagcgcatc aacaatattt tcacctgaat caggatattc ttctaatacc tggaatgctg 5520
tttttccggg gatcgcagtg gtgagtaacc atgcatcatc aggagtacgg ataaaatgct 5580
tgatggtcgg aagaggcata aattccgtca gccagtttag tctgaccatc tcatctgtaa 5640
catcattggc aacgctacct ttgccatgtt tcagaaacaa ctctggcgca tcgggcttcc 5700
catacaagcg atagattgtc gcacctgatt gcccgacatt atcgcgagcc catttatacc 5760
catataaatc agcatccatg ttggaattta atcgcggcct cgacgtttcc cgttgaatat 5820
ggctcataac accccttgta ttactgttta tgtaagcaga cagttttatt gttcatgatg 5880
atatattttt atcttgtgca atgtaacatc agagattttg agacac 5926
<210> 49
<211> 926
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Left HR Arm_CD8 Product 2
<400> 49
acattaaaaa cacaaaatcc tacggaaata ctgaagaatg agtctcagca ctaaggaaaa 60
gcctccagca gctcctgctt tctgagggtg aaggatagac gctgtggctc tgcatgactc 120
actagcactc tatcacggcc atattctggc agggtcagtg gctccaacta acatttgttt 180
ggtactttac agtttattaa atagatgttt atatggagaa gctctcattt ctttctcaga 240
agagcctggc taggaaggtg gatgaggcac catattcatt ttgcaggtga aattcctgag 300
atgtaaggag ctgctgtgac ttgctcaagg ccttatatcg agtaaacggt agtgctgggg 360
cttagacgca ggtgttctga tttatagttc aaaacctcta tcaatgagag agcaatctcc 420
tggtaatgtg atagatttcc caacttaatg ccaacatacc ataaacctcc cattctgcta 480
atgcccagcc taagttgggg agaccactcc agattccaag atgtacagtt tgctttgctg 540
ggcctttttc ccatgcctgc ctttactctg ccagagttat attgctgggg ttttgaagaa 600
gatcctatta aataaaagaa taagcagtat tattaagtag ccctgcattt caggtttcct 660
tgagtggcag gccaggcctg gccgtgaacg ttcactgaaa tcatggcctc ttggccaaga 720
ttgatagctt gtgcctgtcc ctgagtccca gtccatcacg agcagctggt ttctaagatg 780
ctatttcccg tataaagcat gagaccgtga cttgccagcc ccacagagcc ccgcccttgt 840
ccatcactgg catctggact ccagcctggg ttggggcaaa gagggaaatg agatcatgtc 900
ctaaccctga tcctcttgtc ccacag 926
<210> 50
<211> 74
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRAC CDS_CD8 Product 2
<400> 50
atatccagaa ccctgaccct gccgtgtacc agctgagaga ctctaaatcc agtgacaagt 60
ctgtctgcct attc 74
<210> 51
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_CD8 Product 2
<400> 51
gaattcggct ccgga 15
<210> 52
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 2
<400> 52
gccactaact tcagcctgtt gaagcaggcc ggcgacgttg aggaaaaccc cggtcct 57
<210> 53
<211> 63
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A Signal Peptide_CD8 Product 2
<400> 53
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg 60
ccg 63
<210> 54
<211> 483
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A Extracellular domain_CD8 Product 2
<400> 54
agccagttcc gggtgtcgcc gctggatcgg acctggaacc tgggcgagac agtggagctg 60
aagtgccagg tgctgctgtc caacccgacg tcgggctgct cgtggctctt ccagccgcgc 120
ggcgccgccg ccagtcccac cttcctccta tacctctccc aaaacaagcc caaggcggcc 180
gaggggctgg acacccagcg gttctcgggc aagaggttgg gggacacctt cgtcctcacc 240
ctgagcgact tccgccgaga gaacgagggc tactatttct gctcggccct gagcaactcc 300
atcatgtact tcagccactt cgtgccggtc ttcctgccag cgaagcccac cacgacgcca 360
gcgccgcgac caccaacacc ggcgcccacc atcgcgtcgc agcccctgtc cctgcgccca 420
gaggcgtgcc ggccagcggc ggggggcgca gtgcacacga gggggctgga cttcgcctgt 480
gat 483
<210> 55
<211> 63
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A Transmembrane domain_CD8 Product 2
<400> 55
atctacatct gggcgccctt ggccgggact tgtggggtcc ttctcctgtc actggttatc 60
acc 63
<210> 56
<211> 96
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A intracellular domain_CD8 Product 2
<400> 56
ctttactgca accacaggaa ccgaagacgt gtttgcaaat gtccccggcc tgtggtcaaa 60
tcgggagaca agcccagcct ttcggcgaga tacgtc 96
<210> 57
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Furin cleavage site_CD8 Product 2
<400> 57
agagcaaagc gg 12
<210> 58
<211> 9
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_CD8 Product 2
<400> 58
ggctccgga 9
<210> 59
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 2
<400> 59
gctaccaatt ttagcctcct gaagcaggct ggcgatgttg aggaaaaccc tggtccc 57
<210> 60
<211> 63
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8B Signal Peptide_CD8 Product 2
<400> 60
atgcggccgc ggctgtggct cctcttggcc gcgcagctga cagttctcca tggcaactca 60
gtc 63
<210> 61
<211> 447
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8B Extracellular domain_CD8 Product 2
<400> 61
ctccagcaga cccctgcata cataaaggtg caaaccaaca agatggtgat gctgtcctgc 60
gaggctaaaa tctccctcag taacatgcgc atctactggc tgagacagcg ccaggcaccg 120
agcagtgaca gtcaccacga gttcctggcc ctctgggatt ccgcaaaagg gactatccac 180
ggtgaagagg tggaacagga gaagatagct gtgtttcggg atgcaagccg gttcattctc 240
aatctcacaa gcgtgaagcc ggaagacagt ggcatctact tctgcatgat cgtcgggagc 300
cccgagctga ccttcgggaa gggaactcag ctgagtgtgg ttgatttcct tcccaccact 360
gcccagccca ccaagaagtc caccctcaag aagagagtgt gccggttacc caggccagag 420
acccagaagg gcccactttg tagcccc 447
<210> 62
<211> 63
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8B Transmembrane domain_CD8 Product 2
<400> 62
atcacccttg gcctgctggt ggctggcgtc ctggttctgc tggtttccct gggagtggcc 60
atc 63
<210> 63
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8B Intracellular domain_CD8 Product 2
<400> 63
cacctgtgct gccggcggag gagagcccgg cttcgtttca tgaaacaatt ttacaaa 57
<210> 64
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Furin cleavage site_CD8 Product 2
<400> 64
agggctaaac gg 12
<210> 65
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_CD8 Product 2
<400> 65
gaattcggct ccgga 15
<210> 66
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 2
<400> 66
gccactaact tctccctgtt gaaacaggct ggcgatgttg aagaaaaccc cggtcct 57
<210> 67
<211> 78
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
HGH/SS/2_CD8 Product 2
<400> 67
atggccaccg gctctagaac aagcctgctg ctcgcttttg gcctgctctg cctcccatgg 60
ctccaagaag gatctgct 78
<210> 68
<211> 345
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Exemplary TRB_VDJ (TCR097) _CD8 Product 2
<400> 68
aatgctggtg tcactcagac cccaaaattc cgcatcctga agataggaca gagcatgaca 60
ctgcagtgta cccaggatat gaaccataac tacatgtact ggtatcgaca agacccaggc 120
atggggctga agctgattta ttattcagtt ggtgctggta tcactgataa aggagaagtc 180
ccgaatggct acaacgtctc cagatcaacc acagaggatt tcccgctcag gctggagttg 240
gctgctccct cccagacatc tgtgtacttc tgtgccagct ccctacaggt tccctacaat 300
gagcagttct tcgggccagg gacacggctc accgtgctag aggac 345
<210> 69
<211> 534
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TCR-beta/constant_CD8 Product 2
<400> 69
ctgaaaaacg tgttccctcc aaaagtggcc gtgttcgagc cttctgaggc cgagatcagc 60
cacacacaga aagccacact cgtgtgtctg gctaccggct tctaccccga tcacgtggaa 120
ctgtcttggt gggtcaacgg caaagaggtg cacagcggcg tcagcacaga tccccagcct 180
ctgaaagaac agcccgctct gaacgacagc cgctactgcc tgtctagcag actgagagtg 240
tccgccacct tctggcagaa ccccagaaac cacttcagat gccaggtcca gttctacggc 300
ctgagcgaga acgatgagtg gacccaggac agagccaagc ctgtgacaca gatcgtgtct 360
gccgaagcct ggggcagagc cgattgtggc tttaccagcg agtcatacca gcagggcgtg 420
ctgtctgcca ccatcctgta tgagatcctg ctcggcaagg ccacactgta cgctgtgctg 480
gtgtctgctc tggtgctgat ggctatggtc tcccgggagc gcatccccga ggcc 534
<210> 70
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Furin cleavage site_CD8 Product 2
<400> 70
cgggccaagc gg 12
<210> 71
<211> 9
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG linker_CD8 Product 2
<400> 71
ggcagcggc 9
<210> 72
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 2
<400> 72
gccaccaact tcagcctgct gaagcaggcc ggcgacgtgg aggagaaccc cggccct 57
<210> 73
<211> 78
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
HGH/SS_CD8 Product 2
<400> 73
atggccacag gcagcagaac atctctgctg ctggccttcg gactgctgtg tctgccttgg 60
ctgcaagagg gttccgcc 78
<210> 74
<211> 337
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Exemplary TRA-VDJ (TCR097) _CD8 Product 2
<400> 74
gctcagacag tcactcagtc tcaaccagag atgtctgtgc aggaggcaga gaccgtgacc 60
ctgagctgca catatgacac cagtgagagt gattattatt tattctggta caagcagcct 120
cccagcaggc agatgattct cgttattcgc caagaagctt ataagcaaca gaatgcaaca 180
gagaatcgtt tctctgtgaa cttccagaaa gcagccaaat ccttcagtct caagatctca 240
gactcacagc tgggggatgc cgcgatgtat ttctgtgctt ttgggaactt caacaaattt 300
tactttggat ctgggaccaa actcaatgta aaaccaa 337
<210> 75
<211> 74
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TCR-alpha/constant_CD8 Product 2
<400> 75
atattcagaa ccccgatcct gctgtgtatc agctgcgcga cagcaagagc agcgacaaga 60
gcgtgtgttt gttc 74
<210> 76
<211> 200
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRAC CDS/right HR arm_CD8 Product 2
<400> 76
accgattttg attctcaaac aaatgtgtca caaagtaagg attctgatgt gtatatcaca 60
gacaaaactg tgctagacat gaggtctatg gacttcaaga gcaacagtgc tgtggcctgg 120
agcaacaaat ctgactttgc atgtgcaaac gccttcaaca acagcattat tccagaagac 180
accttcttcc ccagcccagg 200
<210> 77
<211> 800
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Right HR arm_CD8 Product 2
<400> 77
taagggcagc tttggtgcct tcgcaggctg tttccttgct tcaggaatgg ccaggttctg 60
cccagagctc tggtcaatga tgtctaaaac tcctctgatt ggtggtctcg gccttatcca 120
ttgccaccaa aaccctcttt ttactaagaa acagtgagcc ttgttctggc agtccagaga 180
atgacacggg aaaaaagcag atgaagagaa ggtggcagga gagggcacgt ggcccagcct 240
cagtctctcc aactgagttc ctgcctgcct gcctttgctc agactgtttg ccccttactg 300
ctcttctagg cctcattcta agccccttct ccaagttgcc tctccttatt tctccctgtc 360
tgccaaaaaa tctttcccag ctcactaagt cagtctcacg cagtcactca ttaacccacc 420
aatcactgat tgtgccggca catgaatgca ccaggtgttg aagtggagga attaaaaagt 480
cagatgaggg gtgtgcccag aggaagcacc attctagttg ggggagccca tctgtcagct 540
gggaaaagtc caaataactt cagattggaa tgtgttttaa ctcagggttg agaaaacagc 600
taccttcagg acaaaagtca gggaagggct ctctgaagaa atgctacttg aagataccag 660
ccctaccaag ggcagggaga ggaccctata gaggcctggg acaggagctc aatgagaaag 720
gagaagagca gcaggcatga gttgaatgaa ggaggcaggg ccgggtcaca gggccttcta 780
ggccatgaga gggtagacag 800
<210> 78
<211> 6
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Artificial Sequence_CD8 Product 2
<400> 78
gctagc 6
<210> 79
<211> 620
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
pBR322_origin_CD8 Product 2
<400> 79
cgcgttgctg gcgtttttcc ataggctccg cccccctgac gagcatcaca aaaatcgacg 60
ctcaagtcag aggtggcgaa acccgacagg actataaaga taccaggcgt ttccccctgg 120
aagctccctc gtgcgctctc ctgttccgac cctgccgctt accggatacc tgtccgcctt 180
tctcccttcg ggaagcgtgg cgctttctca tagctcacgc tgtaggtatc tcagttcggt 240
gtaggtcgtt cgctccaagc tgggctgtgt gcacgaaccc cccgttcagc ccgaccgctg 300
cgccttatcc ggtaactatc gtcttgagtc caacccggta agacacgact tatcgccact 360
ggcagcagcc actggtaaca ggattagcag agcgaggtat gtaggcggtg ctacagagtt 420
cttgaagtgg tggcctaact acggctacac tagaagaaca gtatttggta tctgcgctct 480
gctgaagcca gttaccttcg gaaaaagagt tggtagctct tgatccggca aacaaaccac 540
cgctggtagc ggtggttttt ttgtttgcaa gcagcagatt acgcgcagaa aaaaaggatc 600
tcaagaagat cctttgatct 620
<210> 80
<211> 810
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Kanamycin resistance (KanR2) _CD8 Product 2
<400> 80
ttagaaaaac tcatcgagca tcaaatgaaa ctgcaattta ttcatatcag gattatcaat 60
accatatttt tgaaaaagcc gtttctgtaa tgaaggagaa aactcaccga ggcagttcca 120
taggatggca agatcctggt atcggtctgc gattccgact cgtccaacat caatacaacc 180
tattaatttc ccctcgtcaa aaataaggtt atcaagtgag aaatcaccat gagtgacgac 240
tgaatccggt gagaatggca aaagtttatg catttctttc cagacttgtt caacaggcca 300
gccattacgc tcgtcatcaa aatcactcgc atcaaccaaa ccgttattca ttcgtgattg 360
cgcctgagcc agacgaaata cgcgatcgct gttaaaagga caattacaaa caggaatcga 420
atgcaaccgg cgcaggaaca ctgccagcgc atcaacaata ttttcacctg aatcaggata 480
ttcttctaat acctggaatg ctgtttttcc ggggatcgca gtggtgagta accatgcatc 540
atcaggagta cggataaaat gcttgatggt cggaagaggc ataaattccg tcagccagtt 600
tagtctgacc atctcatctg taacatcatt ggcaacgcta cctttgccat gtttcagaaa 660
caactctggc gcatcgggct tcccatacaa gcgatagatt gtcgcacctg attgcccgac 720
attatcgcga gcccatttat acccatataa atcagcatcc atgttggaat ttaatcgcgg 780
cctcgacgtt tcccgttgaa tatggctcat 810
<210> 81
<211> 99
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Kanamycin promoter_CD8 Product 2
<400> 81
aacacccctt gtattactgt ttatgtaagc agacagtttt attgttcatg atgatatatt 60
tttatcttgt gcaatgtaac atcagagatt ttgagacac 99
<210> 82
<211> 6634
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Complete CD8 Product 2 construct with TCR97 insertion_CD8
Product 2
<400> 82
ggtaccacat taaaaacaca aaatcctacg gaaatactga agaatgagtc tcagcactaa 60
ggaaaagcct ccagcagctc ctgctttctg agggtgaagg atagacgctg tggctctgca 120
tgactcacta gcactctatc acggccatat tctggcaggg tcagtggctc caactaacat 180
ttgtttggta ctttacagtt tattaaatag atgtttatat ggagaagctc tcatttcttt 240
ctcagaagag cctggctagg aaggtggatg aggcaccata ttcattttgc aggtgaaatt 300
cctgagatgt aaggagctgc tgtgacttgc tcaaggcctt atatcgagta aacggtagtg 360
ctggggctta gacgcaggtg ttctgattta tagttcaaaa cctctatcaa tgagagagca 420
atctcctggt aatgtgatag atttcccaac ttaatgccaa cataccataa acctcccatt 480
ctgctaatgc ccagcctaag ttggggagac cactccagat tccaagatgt acagtttgct 540
ttgctgggcc tttttcccat gcctgccttt actctgccag agttatattg ctggggtttt 600
gaagaagatc ctattaaata aaagaataag cagtattatt aagtagccct gcatttcagg 660
tttccttgag tggcaggcca ggcctggccg tgaacgttca ctgaaatcat ggcctcttgg 720
ccaagattga tagcttgtgc ctgtccctga gtcccagtcc atcacgagca gctggtttct 780
aagatgctat ttcccgtata aagcatgaga ccgtgacttg ccagccccac agagccccgc 840
ccttgtccat cactggcatc tggactccag cctgggttgg ggcaaagagg gaaatgagat 900
catgtcctaa ccctgatcct cttgtcccac agatatccag aaccctgacc ctgccgtgta 960
ccagctgaga gactctaaat ccagtgacaa gtctgtctgc ctattcgaat tcggctccgg 1020
agccactaac ttcagcctgt tgaagcaggc cggcgacgtt gaggaaaacc ccggtcctat 1080
ggccttacca gtgaccgcct tgctcctgcc gctggccttg ctgctccacg ccgccaggcc 1140
gagccagttc cgggtgtcgc cgctggatcg gacctggaac ctgggcgaga cagtggagct 1200
gaagtgccag gtgctgctgt ccaacccgac gtcgggctgc tcgtggctct tccagccgcg 1260
cggcgccgcc gccagtccca ccttcctcct atacctctcc caaaacaagc ccaaggcggc 1320
cgaggggctg gacacccagc ggttctcggg caagaggttg ggggacacct tcgtcctcac 1380
cctgagcgac ttccgccgag agaacgaggg ctactatttc tgctcggccc tgagcaactc 1440
catcatgtac ttcagccact tcgtgccggt cttcctgcca gcgaagccca ccacgacgcc 1500
agcgccgcga ccaccaacac cggcgcccac catcgcgtcg cagcccctgt ccctgcgccc 1560
agaggcgtgc cggccagcgg cggggggcgc agtgcacacg agggggctgg acttcgcctg 1620
tgatatctac atctgggcgc ccttggccgg gacttgtggg gtccttctcc tgtcactggt 1680
tatcaccctt tactgcaacc acaggaaccg aagacgtgtt tgcaaatgtc cccggcctgt 1740
ggtcaaatcg ggagacaagc ccagcctttc ggcgagatac gtcagagcaa agcggggctc 1800
cggagctacc aattttagcc tcctgaagca ggctggcgat gttgaggaaa accctggtcc 1860
catgcggccg cggctgtggc tcctcttggc cgcgcagctg acagttctcc atggcaactc 1920
agtcctccag cagacccctg catacataaa ggtgcaaacc aacaagatgg tgatgctgtc 1980
ctgcgaggct aaaatctccc tcagtaacat gcgcatctac tggctgagac agcgccaggc 2040
accgagcagt gacagtcacc acgagttcct ggccctctgg gattccgcaa aagggactat 2100
ccacggtgaa gaggtggaac aggagaagat agctgtgttt cgggatgcaa gccggttcat 2160
tctcaatctc acaagcgtga agccggaaga cagtggcatc tacttctgca tgatcgtcgg 2220
gagccccgag ctgaccttcg ggaagggaac tcagctgagt gtggttgatt tccttcccac 2280
cactgcccag cccaccaaga agtccaccct caagaagaga gtgtgccggt tacccaggcc 2340
agagacccag aagggcccac tttgtagccc catcaccctt ggcctgctgg tggctggcgt 2400
cctggttctg ctggtttccc tgggagtggc catccacctg tgctgccggc ggaggagagc 2460
ccggcttcgt ttcatgaaac aattttacaa aagggctaaa cgggaattcg gctccggagc 2520
cactaacttc tccctgttga aacaggctgg cgatgttgaa gaaaaccccg gtcctatggc 2580
caccggctct agaacaagcc tgctgctcgc ttttggcctg ctctgcctcc catggctcca 2640
agaaggatct gctaatgctg gtgtcactca gaccccaaaa ttccgcatcc tgaagatagg 2700
acagagcatg acactgcagt gtacccagga tatgaaccat aactacatgt actggtatcg 2760
acaagaccca ggcatggggc tgaagctgat ttattattca gttggtgctg gtatcactga 2820
taaaggagaa gtcccgaatg gctacaacgt ctccagatca accacagagg atttcccgct 2880
caggctggag ttggctgctc cctcccagac atctgtgtac ttctgtgcca gctccctaca 2940
ggttccctac aatgagcagt tcttcgggcc agggacacgg ctcaccgtgc tagaggacct 3000
gaaaaacgtg ttccctccaa aagtggccgt gttcgagcct tctgaggccg agatcagcca 3060
cacacagaaa gccacactcg tgtgtctggc taccggcttc taccccgatc acgtggaact 3120
gtcttggtgg gtcaacggca aagaggtgca cagcggcgtc agcacagatc cccagcctct 3180
gaaagaacag cccgctctga acgacagccg ctactgcctg tctagcagac tgagagtgtc 3240
cgccaccttc tggcagaacc ccagaaacca cttcagatgc caggtccagt tctacggcct 3300
gagcgagaac gatgagtgga cccaggacag agccaagcct gtgacacaga tcgtgtctgc 3360
cgaagcctgg ggcagagccg attgtggctt taccagcgag tcataccagc agggcgtgct 3420
gtctgccacc atcctgtatg agatcctgct cggcaaggcc acactgtacg ctgtgctggt 3480
gtctgctctg gtgctgatgg ctatggtctc ccgggagcgc atccccgagg cccgggccaa 3540
gcggggcagc ggcgccacca acttcagcct gctgaagcag gccggcgacg tggaggagaa 3600
ccccggccct atggccacag gcagcagaac atctctgctg ctggccttcg gactgctgtg 3660
tctgccttgg ctgcaagagg gttccgccgc tcagacagtc actcagtctc aaccagagat 3720
gtctgtgcag gaggcagaga ccgtgaccct gagctgcaca tatgacacca gtgagagtga 3780
ttattattta ttctggtaca agcagcctcc cagcaggcag atgattctcg ttattcgcca 3840
agaagcttat aagcaacaga atgcaacaga gaatcgtttc tctgtgaact tccagaaagc 3900
agccaaatcc ttcagtctca agatctcaga ctcacagctg ggggatgccg cgatgtattt 3960
ctgtgctttt gggaacttca acaaatttta ctttggatct gggaccaaac tcaatgtaaa 4020
accaaatatt cagaaccccg atcctgctgt gtatcagctg cgcgacagca agagcagcga 4080
caagagcgtg tgtttgttca ccgattttga ttctcaaaca aatgtgtcac aaagtaagga 4140
ttctgatgtg tatatcacag acaaaactgt gctagacatg aggtctatgg acttcaagag 4200
caacagtgct gtggcctgga gcaacaaatc tgactttgca tgtgcaaacg ccttcaacaa 4260
cagcattatt ccagaagaca ccttcttccc cagcccaggt aagggcagct ttggtgcctt 4320
cgcaggctgt ttccttgctt caggaatggc caggttctgc ccagagctct ggtcaatgat 4380
gtctaaaact cctctgattg gtggtctcgg ccttatccat tgccaccaaa accctctttt 4440
tactaagaaa cagtgagcct tgttctggca gtccagagaa tgacacggga aaaaagcaga 4500
tgaagagaag gtggcaggag agggcacgtg gcccagcctc agtctctcca actgagttcc 4560
tgcctgcctg cctttgctca gactgtttgc cccttactgc tcttctaggc ctcattctaa 4620
gccccttctc caagttgcct ctccttattt ctccctgtct gccaaaaaat ctttcccagc 4680
tcactaagtc agtctcacgc agtcactcat taacccacca atcactgatt gtgccggcac 4740
atgaatgcac caggtgttga agtggaggaa ttaaaaagtc agatgagggg tgtgcccaga 4800
ggaagcacca ttctagttgg gggagcccat ctgtcagctg ggaaaagtcc aaataacttc 4860
agattggaat gtgttttaac tcagggttga gaaaacagct accttcagga caaaagtcag 4920
ggaagggctc tctgaagaaa tgctacttga agataccagc cctaccaagg gcagggagag 4980
gaccctatag aggcctggga caggagctca atgagaaagg agaagagcag caggcatgag 5040
ttgaatgaag gaggcagggc cgggtcacag ggccttctag gccatgagag ggtagacagg 5100
ctagccgcgt tgctggcgtt tttccatagg ctccgccccc ctgacgagca tcacaaaaat 5160
cgacgctcaa gtcagaggtg gcgaaacccg acaggactat aaagatacca ggcgtttccc 5220
cctggaagct ccctcgtgcg ctctcctgtt ccgaccctgc cgcttaccgg atacctgtcc 5280
gcctttctcc cttcgggaag cgtggcgctt tctcatagct cacgctgtag gtatctcagt 5340
tcggtgtagg tcgttcgctc caagctgggc tgtgtgcacg aaccccccgt tcagcccgac 5400
cgctgcgcct tatccggtaa ctatcgtctt gagtccaacc cggtaagaca cgacttatcg 5460
ccactggcag cagccactgg taacaggatt agcagagcga ggtatgtagg cggtgctaca 5520
gagttcttga agtggtggcc taactacggc tacactagaa gaacagtatt tggtatctgc 5580
gctctgctga agccagttac cttcggaaaa agagttggta gctcttgatc cggcaaacaa 5640
accaccgctg gtagcggtgg tttttttgtt tgcaagcagc agattacgcg cagaaaaaaa 5700
ggatctcaag aagatccttt gatctttaga aaaactcatc gagcatcaaa tgaaactgca 5760
atttattcat atcaggatta tcaataccat atttttgaaa aagccgtttc tgtaatgaag 5820
gagaaaactc accgaggcag ttccatagga tggcaagatc ctggtatcgg tctgcgattc 5880
cgactcgtcc aacatcaata caacctatta atttcccctc gtcaaaaata aggttatcaa 5940
gtgagaaatc accatgagtg acgactgaat ccggtgagaa tggcaaaagt ttatgcattt 6000
ctttccagac ttgttcaaca ggccagccat tacgctcgtc atcaaaatca ctcgcatcaa 6060
ccaaaccgtt attcattcgt gattgcgcct gagccagacg aaatacgcga tcgctgttaa 6120
aaggacaatt acaaacagga atcgaatgca accggcgcag gaacactgcc agcgcatcaa 6180
caatattttc acctgaatca ggatattctt ctaatacctg gaatgctgtt tttccgggga 6240
tcgcagtggt gagtaaccat gcatcatcag gagtacggat aaaatgcttg atggtcggaa 6300
gaggcataaa ttccgtcagc cagtttagtc tgaccatctc atctgtaaca tcattggcaa 6360
cgctaccttt gccatgtttc agaaacaact ctggcgcatc gggcttccca tacaagcgat 6420
agattgtcgc acctgattgc ccgacattat cgcgagccca tttataccca tataaatcag 6480
catccatgtt ggaatttaat cgcggcctcg acgtttcccg ttgaatatgg ctcataacac 6540
cccttgtatt actgtttatg taagcagaca gttttattgt tcatgatgat atatttttat 6600
cttgtgcaat gtaacatcag agattttgag acac 6634
<210> 83
<211> 926
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Left HR Arm_CD8 Product 3
<400> 83
acattaaaaa cacaaaatcc tacggaaata ctgaagaatg agtctcagca ctaaggaaaa 60
gcctccagca gctcctgctt tctgagggtg aaggatagac gctgtggctc tgcatgactc 120
actagcactc tatcacggcc atattctggc agggtcagtg gctccaacta acatttgttt 180
ggtactttac agtttattaa atagatgttt atatggagaa gctctcattt ctttctcaga 240
agagcctggc taggaaggtg gatgaggcac catattcatt ttgcaggtga aattcctgag 300
atgtaaggag ctgctgtgac ttgctcaagg ccttatatcg agtaaacggt agtgctgggg 360
cttagacgca ggtgttctga tttatagttc aaaacctcta tcaatgagag agcaatctcc 420
tggtaatgtg atagatttcc caacttaatg ccaacatacc ataaacctcc cattctgcta 480
atgcccagcc taagttgggg agaccactcc agattccaag atgtacagtt tgctttgctg 540
ggcctttttc ccatgcctgc ctttactctg ccagagttat attgctgggg ttttgaagaa 600
gatcctatta aataaaagaa taagcagtat tattaagtag ccctgcattt caggtttcct 660
tgagtggcag gccaggcctg gccgtgaacg ttcactgaaa tcatggcctc ttggccaaga 720
ttgatagctt gtgcctgtcc ctgagtccca gtccatcacg agcagctggt ttctaagatg 780
ctatttcccg tataaagcat gagaccgtga cttgccagcc ccacagagcc ccgcccttgt 840
ccatcactgg catctggact ccagcctggg ttggggcaaa gagggaaatg agatcatgtc 900
ctaaccctga tcctcttgtc ccacag 926
<210> 84
<211> 74
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRAC (part of homology arm) _CD8 Product 3
<400> 84
atatccagaa ccctgaccct gccgtgtacc agctgagaga ctctaaatcc agtgacaagt 60
ctgtctgcct attc 74
<210> 85
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_CD8 Product 3
<400> 85
gaattcggct ccgga 15
<210> 86
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 3
<400> 86
gccactaact tcagcctgtt gaagcaggcc ggcgacgttg aggaaaaccc cggtcct 57
<210> 87
<211> 63
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A Signal Peptide_CD8 Product 3
<400> 87
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg 60
ccg 63
<210> 88
<211> 483
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A Extracellular domain_CD8 Product 3
<400> 88
agccagttcc gggtgtcgcc gctggatcgg acctggaacc tgggcgagac agtggagctg 60
aagtgccagg tgctgctgtc caacccgacg tcgggctgct cgtggctctt ccagccgcgc 120
ggcgccgccg ccagtcccac cttcctccta tacctctccc aaaacaagcc caaggcggcc 180
gaggggctgg acacccagcg gttctcgggc aagaggttgg gggacacctt cgtcctcacc 240
ctgagcgact tccgccgaga gaacgagggc tactatttct gctcggccct gagcaactcc 300
atcatgtact tcagccactt cgtgccggtc ttcctgccag cgaagcccac cacgacgcca 360
gcgccgcgac caccaacacc ggcgcccacc atcgcgtcgc agcccctgtc cctgcgccca 420
gaggcgtgcc ggccagcggc ggggggcgca gtgcacacga gggggctgga cttcgcctgt 480
gat 483
<210> 89
<211> 63
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A Transmembrane domain_CD8 Product 3
<400> 89
atctacatct gggcgccctt ggccgggact tgtggggtcc ttctcctgtc actggttatc 60
acc 63
<210> 90
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8B intracellular domain_CD8 Product 3
<400> 90
cacctgtgct gccggcggag gagagcccgg cttcgtttca tgaaacaatt ttacaaa 57
<210> 91
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Furin cleavage site_CD8 Product 3
<400> 91
agggctaaac gg 12
<210> 92
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_CD8 Product 3
<400> 92
gaattcggct ccgga 15
<210> 93
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 3
<400> 93
gccactaact tctccctgtt gaaacaggct ggcgatgttg aagaaaaccc cggtcct 57
<210> 94
<211> 78
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
HGH/SS/2_CD8 Product 3
<400> 94
atggccaccg gctctagaac aagcctgctg ctcgcttttg gcctgctctg cctcccatgg 60
ctccaagaag gatctgct 78
<210> 95
<211> 345
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRB_VDJ (TCR097)_CD8 Product 3
<400> 95
aatgctggtg tcactcagac cccaaaattc cgcatcctga agataggaca gagcatgaca 60
ctgcagtgta cccaggatat gaaccataac tacatgtact ggtatcgaca agacccaggc 120
atggggctga agctgattta ttattcagtt ggtgctggta tcactgataa aggagaagtc 180
ccgaatggct acaacgtctc cagatcaacc acagaggatt tcccgctcag gctggagttg 240
gctgctccct cccagacatc tgtgtacttc tgtgccagct ccctacaggt tccctacaat 300
gagcagttct tcgggccagg gacacggctc accgtgctag aggac 345
<210> 96
<211> 534
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TCR-beta/constant_CD8 Product 3
<400> 96
ctgaaaaacg tgttccctcc aaaagtggcc gtgttcgagc cttctgaggc cgagatcagc 60
cacacacaga aagccacact cgtgtgtctg gctaccggct tctaccccga tcacgtggaa 120
ctgtcttggt gggtcaacgg caaagaggtg cacagcggcg tcagcacaga tccccagcct 180
ctgaaagaac agcccgctct gaacgacagc cgctactgcc tgtctagcag actgagagtg 240
tccgccacct tctggcagaa ccccagaaac cacttcagat gccaggtcca gttctacggc 300
ctgagcgaga acgatgagtg gacccaggac agagccaagc ctgtgacaca gatcgtgtct 360
gccgaagcct ggggcagagc cgattgtggc tttaccagcg agtcatacca gcagggcgtg 420
ctgtctgcca ccatcctgta tgagatcctg ctcggcaagg ccacactgta cgctgtgctg 480
gtgtctgctc tggtgctgat ggctatggtc tcccgggagc gcatccccga ggcc 534
<210> 97
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Furin cleavage site_CD8 Product 3
<400> 97
cgggccaagc gg 12
<210> 98
<211> 9
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG linker_CD8 Product 3
<400> 98
ggcagcggc 9
<210> 99
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 3
<400> 99
gccaccaact tcagcctgct gaagcaggcc ggcgacgtgg aggagaaccc cggccct 57
<210> 100
<211> 78
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
HGH/SS_CD8 Product 3
<400> 100
atggccacag gcagcagaac atctctgctg ctggccttcg gactgctgtg tctgccttgg 60
ctgcaagagg gttccgcc 78
<210> 101
<211> 337
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Exemplary TRA-VDJ (TCR097) _CD8 Product 3
<400> 101
gctcagacag tcactcagtc tcaaccagag atgtctgtgc aggaggcaga gaccgtgacc 60
ctgagctgca catatgacac cagtgagagt gattattatt tattctggta caagcagcct 120
cccagcaggc agatgattct cgttattcgc caagaagctt ataagcaaca gaatgcaaca 180
gagaatcgtt tctctgtgaa cttccagaaa gcagccaaat ccttcagtct caagatctca 240
gactcacagc tgggggatgc cgcgatgtat ttctgtgctt ttgggaactt caacaaattt 300
tactttggat ctgggaccaa actcaatgta aaaccaa 337
<210> 102
<211> 74
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TCR-alpha/constant_CD8 Product 3
<400> 102
atattcagaa ccccgatcct gctgtgtatc agctgcgcga cagcaagagc agcgacaaga 60
gcgtgtgttt gttc 74
<210> 103
<211> 200
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRAC CDS/right HR arm_CD8 Product 3
<400> 103
accgattttg attctcaaac aaatgtgtca caaagtaagg attctgatgt gtatatcaca 60
gacaaaactg tgctagacat gaggtctatg gacttcaaga gcaacagtgc tgtggcctgg 120
agcaacaaat ctgactttgc atgtgcaaac gccttcaaca acagcattat tccagaagac 180
accttcttcc ccagcccagg 200
<210> 104
<211> 800
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Right HR arm_CD8 Product 3
<400> 104
taagggcagc tttggtgcct tcgcaggctg tttccttgct tcaggaatgg ccaggttctg 60
cccagagctc tggtcaatga tgtctaaaac tcctctgatt ggtggtctcg gccttatcca 120
ttgccaccaa aaccctcttt ttactaagaa acagtgagcc ttgttctggc agtccagaga 180
atgacacggg aaaaaagcag atgaagagaa ggtggcagga gagggcacgt ggcccagcct 240
cagtctctcc aactgagttc ctgcctgcct gcctttgctc agactgtttg ccccttactg 300
ctcttctagg cctcattcta agccccttct ccaagttgcc tctccttatt tctccctgtc 360
tgccaaaaaa tctttcccag ctcactaagt cagtctcacg cagtcactca ttaacccacc 420
aatcactgat tgtgccggca catgaatgca ccaggtgttg aagtggagga attaaaaagt 480
cagatgaggg gtgtgcccag aggaagcacc attctagttg ggggagccca tctgtcagct 540
gggaaaagtc caaataactt cagattggaa tgtgttttaa ctcagggttg agaaaacagc 600
taccttcagg acaaaagtca gggaagggct ctctgaagaa atgctacttg aagataccag 660
ccctaccaag ggcagggaga ggaccctata gaggcctggg acaggagctc aatgagaaag 720
gagaagagca gcaggcatga gttgaatgaa ggaggcaggg ccgggtcaca gggccttcta 780
ggccatgaga gggtagacag 800
<210> 105
<211> 6
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Artificial Sequence_CD8 Product 3
<400> 105
gctagc 6
<210> 106
<211> 620
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
pBR322_origin_CD8 Product 3
<400> 106
cgcgttgctg gcgtttttcc ataggctccg cccccctgac gagcatcaca aaaatcgacg 60
ctcaagtcag aggtggcgaa acccgacagg actataaaga taccaggcgt ttccccctgg 120
aagctccctc gtgcgctctc ctgttccgac cctgccgctt accggatacc tgtccgcctt 180
tctcccttcg ggaagcgtgg cgctttctca tagctcacgc tgtaggtatc tcagttcggt 240
gtaggtcgtt cgctccaagc tgggctgtgt gcacgaaccc cccgttcagc ccgaccgctg 300
cgccttatcc ggtaactatc gtcttgagtc caacccggta agacacgact tatcgccact 360
ggcagcagcc actggtaaca ggattagcag agcgaggtat gtaggcggtg ctacagagtt 420
cttgaagtgg tggcctaact acggctacac tagaagaaca gtatttggta tctgcgctct 480
gctgaagcca gttaccttcg gaaaaagagt tggtagctct tgatccggca aacaaaccac 540
cgctggtagc ggtggttttt ttgtttgcaa gcagcagatt acgcgcagaa aaaaaggatc 600
tcaagaagat cctttgatct 620
<210> 107
<211> 810
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Kanamycin resistance (KanR2) _CD8 Product 3
<400> 107
ttagaaaaac tcatcgagca tcaaatgaaa ctgcaattta ttcatatcag gattatcaat 60
accatatttt tgaaaaagcc gtttctgtaa tgaaggagaa aactcaccga ggcagttcca 120
taggatggca agatcctggt atcggtctgc gattccgact cgtccaacat caatacaacc 180
tattaatttc ccctcgtcaa aaataaggtt atcaagtgag aaatcaccat gagtgacgac 240
tgaatccggt gagaatggca aaagtttatg catttctttc cagacttgtt caacaggcca 300
gccattacgc tcgtcatcaa aatcactcgc atcaaccaaa ccgttattca ttcgtgattg 360
cgcctgagcc agacgaaata cgcgatcgct gttaaaagga caattacaaa caggaatcga 420
atgcaaccgg cgcaggaaca ctgccagcgc atcaacaata ttttcacctg aatcaggata 480
ttcttctaat acctggaatg ctgtttttcc ggggatcgca gtggtgagta accatgcatc 540
atcaggagta cggataaaat gcttgatggt cggaagaggc ataaattccg tcagccagtt 600
tagtctgacc atctcatctg taacatcatt ggcaacgcta cctttgccat gtttcagaaa 660
caactctggc gcatcgggct tcccatacaa gcgatagatt gtcgcacctg attgcccgac 720
attatcgcga gcccatttat acccatataa atcagcatcc atgttggaat ttaatcgcgg 780
cctcgacgtt tcccgttgaa tatggctcat 810
<210> 108
<211> 99
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Kanamycin promoter_CD8 Product 3
<400> 108
aacacccctt gtattactgt ttatgtaagc agacagtttt attgttcatg atgatatatt 60
tttatcttgt gcaatgtaac atcagagatt ttgagacac 99
<210> 109
<211> 5887
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Complete CD8 Product 3 construct with TCR97 insertion_CD8
Product 3
<400> 109
ggtaccacat taaaaacaca aaatcctacg gaaatactga agaatgagtc tcagcactaa 60
ggaaaagcct ccagcagctc ctgctttctg agggtgaagg atagacgctg tggctctgca 120
tgactcacta gcactctatc acggccatat tctggcaggg tcagtggctc caactaacat 180
ttgtttggta ctttacagtt tattaaatag atgtttatat ggagaagctc tcatttcttt 240
ctcagaagag cctggctagg aaggtggatg aggcaccata ttcattttgc aggtgaaatt 300
cctgagatgt aaggagctgc tgtgacttgc tcaaggcctt atatcgagta aacggtagtg 360
ctggggctta gacgcaggtg ttctgattta tagttcaaaa cctctatcaa tgagagagca 420
atctcctggt aatgtgatag atttcccaac ttaatgccaa cataccataa acctcccatt 480
ctgctaatgc ccagcctaag ttggggagac cactccagat tccaagatgt acagtttgct 540
ttgctgggcc tttttcccat gcctgccttt actctgccag agttatattg ctggggtttt 600
gaagaagatc ctattaaata aaagaataag cagtattatt aagtagccct gcatttcagg 660
tttccttgag tggcaggcca ggcctggccg tgaacgttca ctgaaatcat ggcctcttgg 720
ccaagattga tagcttgtgc ctgtccctga gtcccagtcc atcacgagca gctggtttct 780
aagatgctat ttcccgtata aagcatgaga ccgtgacttg ccagccccac agagccccgc 840
ccttgtccat cactggcatc tggactccag cctgggttgg ggcaaagagg gaaatgagat 900
catgtcctaa ccctgatcct cttgtcccac agatatccag aaccctgacc ctgccgtgta 960
ccagctgaga gactctaaat ccagtgacaa gtctgtctgc ctattcgaat tcggctccgg 1020
agccactaac ttcagcctgt tgaagcaggc cggcgacgtt gaggaaaacc ccggtcctat 1080
ggccttacca gtgaccgcct tgctcctgcc gctggccttg ctgctccacg ccgccaggcc 1140
gagccagttc cgggtgtcgc cgctggatcg gacctggaac ctgggcgaga cagtggagct 1200
gaagtgccag gtgctgctgt ccaacccgac gtcgggctgc tcgtggctct tccagccgcg 1260
cggcgccgcc gccagtccca ccttcctcct atacctctcc caaaacaagc ccaaggcggc 1320
cgaggggctg gacacccagc ggttctcggg caagaggttg ggggacacct tcgtcctcac 1380
cctgagcgac ttccgccgag agaacgaggg ctactatttc tgctcggccc tgagcaactc 1440
catcatgtac ttcagccact tcgtgccggt cttcctgcca gcgaagccca ccacgacgcc 1500
agcgccgcga ccaccaacac cggcgcccac catcgcgtcg cagcccctgt ccctgcgccc 1560
agaggcgtgc cggccagcgg cggggggcgc agtgcacacg agggggctgg acttcgcctg 1620
tgatatctac atctgggcgc ccttggccgg gacttgtggg gtccttctcc tgtcactggt 1680
tatcacccac ctgtgctgcc ggcggaggag agcccggctt cgtttcatga aacaatttta 1740
caaaagggct aaacgggaat tcggctccgg agccactaac ttctccctgt tgaaacaggc 1800
tggcgatgtt gaagaaaacc ccggtcctat ggccaccggc tctagaacaa gcctgctgct 1860
cgcttttggc ctgctctgcc tcccatggct ccaagaagga tctgctaatg ctggtgtcac 1920
tcagacccca aaattccgca tcctgaagat aggacagagc atgacactgc agtgtaccca 1980
ggatatgaac cataactaca tgtactggta tcgacaagac ccaggcatgg ggctgaagct 2040
gatttattat tcagttggtg ctggtatcac tgataaagga gaagtcccga atggctacaa 2100
cgtctccaga tcaaccacag aggatttccc gctcaggctg gagttggctg ctccctccca 2160
gacatctgtg tacttctgtg ccagctccct acaggttccc tacaatgagc agttcttcgg 2220
gccagggaca cggctcaccg tgctagagga cctgaaaaac gtgttccctc caaaagtggc 2280
cgtgttcgag ccttctgagg ccgagatcag ccacacacag aaagccacac tcgtgtgtct 2340
ggctaccggc ttctaccccg atcacgtgga actgtcttgg tgggtcaacg gcaaagaggt 2400
gcacagcggc gtcagcacag atccccagcc tctgaaagaa cagcccgctc tgaacgacag 2460
ccgctactgc ctgtctagca gactgagagt gtccgccacc ttctggcaga accccagaaa 2520
ccacttcaga tgccaggtcc agttctacgg cctgagcgag aacgatgagt ggacccagga 2580
cagagccaag cctgtgacac agatcgtgtc tgccgaagcc tggggcagag ccgattgtgg 2640
ctttaccagc gagtcatacc agcagggcgt gctgtctgcc accatcctgt atgagatcct 2700
gctcggcaag gccacactgt acgctgtgct ggtgtctgct ctggtgctga tggctatggt 2760
ctcccgggag cgcatccccg aggcccgggc caagcggggc agcggcgcca ccaacttcag 2820
cctgctgaag caggccggcg acgtggagga gaaccccggc cctatggcca caggcagcag 2880
aacatctctg ctgctggcct tcggactgct gtgtctgcct tggctgcaag agggttccgc 2940
cgctcagaca gtcactcagt ctcaaccaga gatgtctgtg caggaggcag agaccgtgac 3000
cctgagctgc acatatgaca ccagtgagag tgattattat ttattctggt acaagcagcc 3060
tcccagcagg cagatgattc tcgttattcg ccaagaagct tataagcaac agaatgcaac 3120
agagaatcgt ttctctgtga acttccagaa agcagccaaa tccttcagtc tcaagatctc 3180
agactcacag ctgggggatg ccgcgatgta tttctgtgct tttgggaact tcaacaaatt 3240
ttactttgga tctgggacca aactcaatgt aaaaccaaat attcagaacc ccgatcctgc 3300
tgtgtatcag ctgcgcgaca gcaagagcag cgacaagagc gtgtgtttgt tcaccgattt 3360
tgattctcaa acaaatgtgt cacaaagtaa ggattctgat gtgtatatca cagacaaaac 3420
tgtgctagac atgaggtcta tggacttcaa gagcaacagt gctgtggcct ggagcaacaa 3480
atctgacttt gcatgtgcaa acgccttcaa caacagcatt attccagaag acaccttctt 3540
ccccagccca ggtaagggca gctttggtgc cttcgcaggc tgtttccttg cttcaggaat 3600
ggccaggttc tgcccagagc tctggtcaat gatgtctaaa actcctctga ttggtggtct 3660
cggccttatc cattgccacc aaaaccctct ttttactaag aaacagtgag ccttgttctg 3720
gcagtccaga gaatgacacg ggaaaaaagc agatgaagag aaggtggcag gagagggcac 3780
gtggcccagc ctcagtctct ccaactgagt tcctgcctgc ctgcctttgc tcagactgtt 3840
tgccccttac tgctcttcta ggcctcattc taagcccctt ctccaagttg cctctcctta 3900
tttctccctg tctgccaaaa aatctttccc agctcactaa gtcagtctca cgcagtcact 3960
cattaaccca ccaatcactg attgtgccgg cacatgaatg caccaggtgt tgaagtggag 4020
gaattaaaaa gtcagatgag gggtgtgccc agaggaagca ccattctagt tgggggagcc 4080
catctgtcag ctgggaaaag tccaaataac ttcagattgg aatgtgtttt aactcagggt 4140
tgagaaaaca gctaccttca ggacaaaagt cagggaaggg ctctctgaag aaatgctact 4200
tgaagatacc agccctacca agggcaggga gaggacccta tagaggcctg ggacaggagc 4260
tcaatgagaa aggagaagag cagcaggcat gagttgaatg aaggaggcag ggccgggtca 4320
cagggccttc taggccatga gagggtagac aggctagccg cgttgctggc gtttttccat 4380
aggctccgcc cccctgacga gcatcacaaa aatcgacgct caagtcagag gtggcgaaac 4440
ccgacaggac tataaagata ccaggcgttt ccccctggaa gctccctcgt gcgctctcct 4500
gttccgaccc tgccgcttac cggatacctg tccgcctttc tcccttcggg aagcgtggcg 4560
ctttctcata gctcacgctg taggtatctc agttcggtgt aggtcgttcg ctccaagctg 4620
ggctgtgtgc acgaaccccc cgttcagccc gaccgctgcg ccttatccgg taactatcgt 4680
cttgagtcca acccggtaag acacgactta tcgccactgg cagcagccac tggtaacagg 4740
attagcagag cgaggtatgt aggcggtgct acagagttct tgaagtggtg gcctaactac 4800
ggctacacta gaagaacagt atttggtatc tgcgctctgc tgaagccagt taccttcgga 4860
aaaagagttg gtagctcttg atccggcaaa caaaccaccg ctggtagcgg tggttttttt 4920
gtttgcaagc agcagattac gcgcagaaaa aaaggatctc aagaagatcc tttgatcttt 4980
agaaaaactc atcgagcatc aaatgaaact gcaatttatt catatcagga ttatcaatac 5040
catatttttg aaaaagccgt ttctgtaatg aaggagaaaa ctcaccgagg cagttccata 5100
ggatggcaag atcctggtat cggtctgcga ttccgactcg tccaacatca atacaaccta 5160
ttaatttccc ctcgtcaaaa ataaggttat caagtgagaa atcaccatga gtgacgactg 5220
aatccggtga gaatggcaaa agtttatgca tttctttcca gacttgttca acaggccagc 5280
cattacgctc gtcatcaaaa tcactcgcat caaccaaacc gttattcatt cgtgattgcg 5340
cctgagccag acgaaatacg cgatcgctgt taaaaggaca attacaaaca ggaatcgaat 5400
gcaaccggcg caggaacact gccagcgcat caacaatatt ttcacctgaa tcaggatatt 5460
cttctaatac ctggaatgct gtttttccgg ggatcgcagt ggtgagtaac catgcatcat 5520
caggagtacg gataaaatgc ttgatggtcg gaagaggcat aaattccgtc agccagttta 5580
gtctgaccat ctcatctgta acatcattgg caacgctacc tttgccatgt ttcagaaaca 5640
actctggcgc atcgggcttc ccatacaagc gatagattgt cgcacctgat tgcccgacat 5700
tatcgcgagc ccatttatac ccatataaat cagcatccat gttggaattt aatcgcggcc 5760
tcgacgtttc ccgttgaata tggctcataa caccccttgt attactgttt atgtaagcag 5820
acagttttat tgttcatgat gatatatttt tatcttgtgc aatgtaacat cagagatttt 5880
gagacac 5887
<210> 110
<211> 926
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Left HR Arm_CD8 Product 4
<400> 110
acattaaaaa cacaaaatcc tacggaaata ctgaagaatg agtctcagca ctaaggaaaa 60
gcctccagca gctcctgctt tctgagggtg aaggatagac gctgtggctc tgcatgactc 120
actagcactc tatcacggcc atattctggc agggtcagtg gctccaacta acatttgttt 180
ggtactttac agtttattaa atagatgttt atatggagaa gctctcattt ctttctcaga 240
agagcctggc taggaaggtg gatgaggcac catattcatt ttgcaggtga aattcctgag 300
atgtaaggag ctgctgtgac ttgctcaagg ccttatatcg agtaaacggt agtgctgggg 360
cttagacgca ggtgttctga tttatagttc aaaacctcta tcaatgagag agcaatctcc 420
tggtaatgtg atagatttcc caacttaatg ccaacatacc ataaacctcc cattctgcta 480
atgcccagcc taagttgggg agaccactcc agattccaag atgtacagtt tgctttgctg 540
ggcctttttc ccatgcctgc ctttactctg ccagagttat attgctgggg ttttgaagaa 600
gatcctatta aataaaagaa taagcagtat tattaagtag ccctgcattt caggtttcct 660
tgagtggcag gccaggcctg gccgtgaacg ttcactgaaa tcatggcctc ttggccaaga 720
ttgatagctt gtgcctgtcc ctgagtccca gtccatcacg agcagctggt ttctaagatg 780
ctatttcccg tataaagcat gagaccgtga cttgccagcc ccacagagcc ccgcccttgt 840
ccatcactgg catctggact ccagcctggg ttggggcaaa gagggaaatg agatcatgtc 900
ctaaccctga tcctcttgtc ccacag 926
<210> 111
<211> 74
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRAC CDS_CD8 Product 4
<400> 111
atatccagaa ccctgaccct gccgtgtacc agctgagaga ctctaaatcc agtgacaagt 60
ctgtctgcct attc 74
<210> 112
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_CD8 Product 4
<400> 112
gaattcggct ccgga 15
<210> 113
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 4
<400> 113
gccactaact tcagcctgtt gaagcaggcc ggcgacgttg aggaaaaccc cggtcct 57
<210> 114
<211> 63
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A Signal peptide_CD8 Product 4
<400> 114
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg 60
ccg 63
<210> 115
<211> 483
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A Extracellular Domain_CD8 Product 4
<400> 115
agccagttcc gggtgtcgcc gctggatcgg acctggaacc tgggcgagac agtggagctg 60
aagtgccagg tgctgctgtc caacccgacg tcgggctgct cgtggctctt ccagccgcgc 120
ggcgccgccg ccagtcccac cttcctccta tacctctccc aaaacaagcc caaggcggcc 180
gaggggctgg acacccagcg gttctcgggc aagaggttgg gggacacctt cgtcctcacc 240
ctgagcgact tccgccgaga gaacgagggc tactatttct gctcggccct gagcaactcc 300
atcatgtact tcagccactt cgtgccggtc ttcctgccag cgaagcccac cacgacgcca 360
gcgccgcgac caccaacacc ggcgcccacc atcgcgtcgc agcccctgtc cctgcgccca 420
gaggcgtgcc ggccagcggc ggggggcgca gtgcacacga gggggctgga cttcgcctgt 480
gat 483
<210> 116
<211> 63
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8A transmembrane domain_CD8 Product 4
<400> 116
atctacatct gggcgccctt ggccgggact tgtggggtcc ttctcctgtc actggttatc 60
acc 63
<210> 117
<211> 120
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD4 intracellular domain_CD8 Product 4
<400> 117
tgtgtcaggt gccggcaccg aaggcgccaa gcagagcgga tgtctcagat caagagactc 60
ctcagtgaga agaagacctg ccagtgtcct caccggtttc agaagacatg tagccccatt 120
<210> 118
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Furin Cleavage site_CD8 Product 4
<400> 118
agggctaaac gg 12
<210> 119
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_CD8 Product 4
<400> 119
gaattcggct ccgga 15
<210> 120
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 4
<400> 120
gccactaact tctccctgtt gaaacaggct ggcgatgttg aagaaaaccc cggtcct 57
<210> 121
<211> 78
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
HGH/SS/2_CD8 Product 4
<400> 121
atggccaccg gctctagaac aagcctgctg ctcgcttttg gcctgctctg cctcccatgg 60
ctccaagaag gatctgct 78
<210> 122
<211> 345
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRB_VDJ (TCR097) _CD8 Product 4
<400> 122
aatgctggtg tcactcagac cccaaaattc cgcatcctga agataggaca gagcatgaca 60
ctgcagtgta cccaggatat gaaccataac tacatgtact ggtatcgaca agacccaggc 120
atggggctga agctgattta ttattcagtt ggtgctggta tcactgataa aggagaagtc 180
ccgaatggct acaacgtctc cagatcaacc acagaggatt tcccgctcag gctggagttg 240
gctgctccct cccagacatc tgtgtacttc tgtgccagct ccctacaggt tccctacaat 300
gagcagttct tcgggccagg gacacggctc accgtgctag aggac 345
<210> 123
<211> 534
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TCR-beta/constant_CD8 Product 4
<400> 123
ctgaaaaacg tgttccctcc aaaagtggcc gtgttcgagc cttctgaggc cgagatcagc 60
cacacacaga aagccacact cgtgtgtctg gctaccggct tctaccccga tcacgtggaa 120
ctgtcttggt gggtcaacgg caaagaggtg cacagcggcg tcagcacaga tccccagcct 180
ctgaaagaac agcccgctct gaacgacagc cgctactgcc tgtctagcag actgagagtg 240
tccgccacct tctggcagaa ccccagaaac cacttcagat gccaggtcca gttctacggc 300
ctgagcgaga acgatgagtg gacccaggac agagccaagc ctgtgacaca gatcgtgtct 360
gccgaagcct ggggcagagc cgattgtggc tttaccagcg agtcatacca gcagggcgtg 420
ctgtctgcca ccatcctgta tgagatcctg ctcggcaagg ccacactgta cgctgtgctg 480
gtgtctgctc tggtgctgat ggctatggtc tcccgggagc gcatccccga ggcc 534
<210> 124
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Furin cleavage site_CD8 Product 4
<400> 124
cgggccaagc gg 12
<210> 125
<211> 9
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG linker_CD8 Product 4
<400> 125
ggcagcggc 9
<210> 126
<211> 57
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Product 4
<400> 126
gccaccaact tcagcctgct gaagcaggcc ggcgacgtgg aggagaaccc cggccct 57
<210> 127
<211> 78
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
HGH/SS_CD8 Product 4
<400> 127
atggccacag gcagcagaac atctctgctg ctggccttcg gactgctgtg tctgccttgg 60
ctgcaagagg gttccgcc 78
<210> 128
<211> 337
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Exemplary TRA-VDJ (TCR097) _CD8 Product 4
<400> 128
gctcagacag tcactcagtc tcaaccagag atgtctgtgc aggaggcaga gaccgtgacc 60
ctgagctgca catatgacac cagtgagagt gattattatt tattctggta caagcagcct 120
cccagcaggc agatgattct cgttattcgc caagaagctt ataagcaaca gaatgcaaca 180
gagaatcgtt tctctgtgaa cttccagaaa gcagccaaat ccttcagtct caagatctca 240
gactcacagc tgggggatgc cgcgatgtat ttctgtgctt ttgggaactt caacaaattt 300
tactttggat ctgggaccaa actcaatgta aaaccaa 337
<210> 129
<211> 74
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TCR-alpha/constant_CD8 Product 4
<400> 129
atattcagaa ccccgatcct gctgtgtatc agctgcgcga cagcaagagc agcgacaaga 60
gcgtgtgttt gttc 74
<210> 130
<211> 200
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
TRAC CDS/right HR arm_CD8 Product 4
<400> 130
accgattttg attctcaaac aaatgtgtca caaagtaagg attctgatgt gtatatcaca 60
gacaaaactg tgctagacat gaggtctatg gacttcaaga gcaacagtgc tgtggcctgg 120
agcaacaaat ctgactttgc atgtgcaaac gccttcaaca acagcattat tccagaagac 180
accttcttcc ccagcccagg 200
<210> 131
<211> 800
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Right HR arm_CD8 Product 4
<400> 131
taagggcagc tttggtgcct tcgcaggctg tttccttgct tcaggaatgg ccaggttctg 60
cccagagctc tggtcaatga tgtctaaaac tcctctgatt ggtggtctcg gccttatcca 120
ttgccaccaa aaccctcttt ttactaagaa acagtgagcc ttgttctggc agtccagaga 180
atgacacggg aaaaaagcag atgaagagaa ggtggcagga gagggcacgt ggcccagcct 240
cagtctctcc aactgagttc ctgcctgcct gcctttgctc agactgtttg ccccttactg 300
ctcttctagg cctcattcta agccccttct ccaagttgcc tctccttatt tctccctgtc 360
tgccaaaaaa tctttcccag ctcactaagt cagtctcacg cagtcactca ttaacccacc 420
aatcactgat tgtgccggca catgaatgca ccaggtgttg aagtggagga attaaaaagt 480
cagatgaggg gtgtgcccag aggaagcacc attctagttg ggggagccca tctgtcagct 540
gggaaaagtc caaataactt cagattggaa tgtgttttaa ctcagggttg agaaaacagc 600
taccttcagg acaaaagtca gggaagggct ctctgaagaa atgctacttg aagataccag 660
ccctaccaag ggcagggaga ggaccctata gaggcctggg acaggagctc aatgagaaag 720
gagaagagca gcaggcatga gttgaatgaa ggaggcaggg ccgggtcaca gggccttcta 780
ggccatgaga gggtagacag 800
<210> 132
<211> 6
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Artificial Sequence_CD8 Product 4
<400> 132
gctagc 6
<210> 133
<211> 620
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
pBR322_origin_CD8 Product 4
<400> 133
cgcgttgctg gcgtttttcc ataggctccg cccccctgac gagcatcaca aaaatcgacg 60
ctcaagtcag aggtggcgaa acccgacagg actataaaga taccaggcgt ttccccctgg 120
aagctccctc gtgcgctctc ctgttccgac cctgccgctt accggatacc tgtccgcctt 180
tctcccttcg ggaagcgtgg cgctttctca tagctcacgc tgtaggtatc tcagttcggt 240
gtaggtcgtt cgctccaagc tgggctgtgt gcacgaaccc cccgttcagc ccgaccgctg 300
cgccttatcc ggtaactatc gtcttgagtc caacccggta agacacgact tatcgccact 360
ggcagcagcc actggtaaca ggattagcag agcgaggtat gtaggcggtg ctacagagtt 420
cttgaagtgg tggcctaact acggctacac tagaagaaca gtatttggta tctgcgctct 480
gctgaagcca gttaccttcg gaaaaagagt tggtagctct tgatccggca aacaaaccac 540
cgctggtagc ggtggttttt ttgtttgcaa gcagcagatt acgcgcagaa aaaaaggatc 600
tcaagaagat cctttgatct 620
<210> 134
<211> 810
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Kanamycin resistance (KanR2) _CD8 Product 4
<400> 134
ttagaaaaac tcatcgagca tcaaatgaaa ctgcaattta ttcatatcag gattatcaat 60
accatatttt tgaaaaagcc gtttctgtaa tgaaggagaa aactcaccga ggcagttcca 120
taggatggca agatcctggt atcggtctgc gattccgact cgtccaacat caatacaacc 180
tattaatttc ccctcgtcaa aaataaggtt atcaagtgag aaatcaccat gagtgacgac 240
tgaatccggt gagaatggca aaagtttatg catttctttc cagacttgtt caacaggcca 300
gccattacgc tcgtcatcaa aatcactcgc atcaaccaaa ccgttattca ttcgtgattg 360
cgcctgagcc agacgaaata cgcgatcgct gttaaaagga caattacaaa caggaatcga 420
atgcaaccgg cgcaggaaca ctgccagcgc atcaacaata ttttcacctg aatcaggata 480
ttcttctaat acctggaatg ctgtttttcc ggggatcgca gtggtgagta accatgcatc 540
atcaggagta cggataaaat gcttgatggt cggaagaggc ataaattccg tcagccagtt 600
tagtctgacc atctcatctg taacatcatt ggcaacgcta cctttgccat gtttcagaaa 660
caactctggc gcatcgggct tcccatacaa gcgatagatt gtcgcacctg attgcccgac 720
attatcgcga gcccatttat acccatataa atcagcatcc atgttggaat ttaatcgcgg 780
cctcgacgtt tcccgttgaa tatggctcat 810
<210> 135
<211> 99
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8 Product 4 Kanamycin promoter
<400> 135
aacacccctt gtattactgt ttatgtaagc agacagtttt attgttcatg atgatatatt 60
tttatcttgt gcaatgtaac atcagagatt ttgagacac 99
<210> 136
<211> 5950
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Complete CD8 Product 4 construct with TCR97 insertion_CD8
Product 4
<400> 136
ggtaccacat taaaaacaca aaatcctacg gaaatactga agaatgagtc tcagcactaa 60
ggaaaagcct ccagcagctc ctgctttctg agggtgaagg atagacgctg tggctctgca 120
tgactcacta gcactctatc acggccatat tctggcaggg tcagtggctc caactaacat 180
ttgtttggta ctttacagtt tattaaatag atgtttatat ggagaagctc tcatttcttt 240
ctcagaagag cctggctagg aaggtggatg aggcaccata ttcattttgc aggtgaaatt 300
cctgagatgt aaggagctgc tgtgacttgc tcaaggcctt atatcgagta aacggtagtg 360
ctggggctta gacgcaggtg ttctgattta tagttcaaaa cctctatcaa tgagagagca 420
atctcctggt aatgtgatag atttcccaac ttaatgccaa cataccataa acctcccatt 480
ctgctaatgc ccagcctaag ttggggagac cactccagat tccaagatgt acagtttgct 540
ttgctgggcc tttttcccat gcctgccttt actctgccag agttatattg ctggggtttt 600
gaagaagatc ctattaaata aaagaataag cagtattatt aagtagccct gcatttcagg 660
tttccttgag tggcaggcca ggcctggccg tgaacgttca ctgaaatcat ggcctcttgg 720
ccaagattga tagcttgtgc ctgtccctga gtcccagtcc atcacgagca gctggtttct 780
aagatgctat ttcccgtata aagcatgaga ccgtgacttg ccagccccac agagccccgc 840
ccttgtccat cactggcatc tggactccag cctgggttgg ggcaaagagg gaaatgagat 900
catgtcctaa ccctgatcct cttgtcccac agatatccag aaccctgacc ctgccgtgta 960
ccagctgaga gactctaaat ccagtgacaa gtctgtctgc ctattcgaat tcggctccgg 1020
agccactaac ttcagcctgt tgaagcaggc cggcgacgtt gaggaaaacc ccggtcctat 1080
ggccttacca gtgaccgcct tgctcctgcc gctggccttg ctgctccacg ccgccaggcc 1140
gagccagttc cgggtgtcgc cgctggatcg gacctggaac ctgggcgaga cagtggagct 1200
gaagtgccag gtgctgctgt ccaacccgac gtcgggctgc tcgtggctct tccagccgcg 1260
cggcgccgcc gccagtccca ccttcctcct atacctctcc caaaacaagc ccaaggcggc 1320
cgaggggctg gacacccagc ggttctcggg caagaggttg ggggacacct tcgtcctcac 1380
cctgagcgac ttccgccgag agaacgaggg ctactatttc tgctcggccc tgagcaactc 1440
catcatgtac ttcagccact tcgtgccggt cttcctgcca gcgaagccca ccacgacgcc 1500
agcgccgcga ccaccaacac cggcgcccac catcgcgtcg cagcccctgt ccctgcgccc 1560
agaggcgtgc cggccagcgg cggggggcgc agtgcacacg agggggctgg acttcgcctg 1620
tgatatctac atctgggcgc ccttggccgg gacttgtggg gtccttctcc tgtcactggt 1680
tatcacctgt gtcaggtgcc ggcaccgaag gcgccaagca gagcggatgt ctcagatcaa 1740
gagactcctc agtgagaaga agacctgcca gtgtcctcac cggtttcaga agacatgtag 1800
ccccattagg gctaaacggg aattcggctc cggagccact aacttctccc tgttgaaaca 1860
ggctggcgat gttgaagaaa accccggtcc tatggccacc ggctctagaa caagcctgct 1920
gctcgctttt ggcctgctct gcctcccatg gctccaagaa ggatctgcta atgctggtgt 1980
cactcagacc ccaaaattcc gcatcctgaa gataggacag agcatgacac tgcagtgtac 2040
ccaggatatg aaccataact acatgtactg gtatcgacaa gacccaggca tggggctgaa 2100
gctgatttat tattcagttg gtgctggtat cactgataaa ggagaagtcc cgaatggcta 2160
caacgtctcc agatcaacca cagaggattt cccgctcagg ctggagttgg ctgctccctc 2220
ccagacatct gtgtacttct gtgccagctc cctacaggtt ccctacaatg agcagttctt 2280
cgggccaggg acacggctca ccgtgctaga ggacctgaaa aacgtgttcc ctccaaaagt 2340
ggccgtgttc gagccttctg aggccgagat cagccacaca cagaaagcca cactcgtgtg 2400
tctggctacc ggcttctacc ccgatcacgt ggaactgtct tggtgggtca acggcaaaga 2460
ggtgcacagc ggcgtcagca cagatcccca gcctctgaaa gaacagcccg ctctgaacga 2520
cagccgctac tgcctgtcta gcagactgag agtgtccgcc accttctggc agaaccccag 2580
aaaccacttc agatgccagg tccagttcta cggcctgagc gagaacgatg agtggaccca 2640
ggacagagcc aagcctgtga cacagatcgt gtctgccgaa gcctggggca gagccgattg 2700
tggctttacc agcgagtcat accagcaggg cgtgctgtct gccaccatcc tgtatgagat 2760
cctgctcggc aaggccacac tgtacgctgt gctggtgtct gctctggtgc tgatggctat 2820
ggtctcccgg gagcgcatcc ccgaggcccg ggccaagcgg ggcagcggcg ccaccaactt 2880
cagcctgctg aagcaggccg gcgacgtgga ggagaacccc ggccctatgg ccacaggcag 2940
cagaacatct ctgctgctgg ccttcggact gctgtgtctg ccttggctgc aagagggttc 3000
cgccgctcag acagtcactc agtctcaacc agagatgtct gtgcaggagg cagagaccgt 3060
gaccctgagc tgcacatatg acaccagtga gagtgattat tatttattct ggtacaagca 3120
gcctcccagc aggcagatga ttctcgttat tcgccaagaa gcttataagc aacagaatgc 3180
aacagagaat cgtttctctg tgaacttcca gaaagcagcc aaatccttca gtctcaagat 3240
ctcagactca cagctggggg atgccgcgat gtatttctgt gcttttggga acttcaacaa 3300
attttacttt ggatctggga ccaaactcaa tgtaaaacca aatattcaga accccgatcc 3360
tgctgtgtat cagctgcgcg acagcaagag cagcgacaag agcgtgtgtt tgttcaccga 3420
ttttgattct caaacaaatg tgtcacaaag taaggattct gatgtgtata tcacagacaa 3480
aactgtgcta gacatgaggt ctatggactt caagagcaac agtgctgtgg cctggagcaa 3540
caaatctgac tttgcatgtg caaacgcctt caacaacagc attattccag aagacacctt 3600
cttccccagc ccaggtaagg gcagctttgg tgccttcgca ggctgtttcc ttgcttcagg 3660
aatggccagg ttctgcccag agctctggtc aatgatgtct aaaactcctc tgattggtgg 3720
tctcggcctt atccattgcc accaaaaccc tctttttact aagaaacagt gagccttgtt 3780
ctggcagtcc agagaatgac acgggaaaaa agcagatgaa gagaaggtgg caggagaggg 3840
cacgtggccc agcctcagtc tctccaactg agttcctgcc tgcctgcctt tgctcagact 3900
gtttgcccct tactgctctt ctaggcctca ttctaagccc cttctccaag ttgcctctcc 3960
ttatttctcc ctgtctgcca aaaaatcttt cccagctcac taagtcagtc tcacgcagtc 4020
actcattaac ccaccaatca ctgattgtgc cggcacatga atgcaccagg tgttgaagtg 4080
gaggaattaa aaagtcagat gaggggtgtg cccagaggaa gcaccattct agttggggga 4140
gcccatctgt cagctgggaa aagtccaaat aacttcagat tggaatgtgt tttaactcag 4200
ggttgagaaa acagctacct tcaggacaaa agtcagggaa gggctctctg aagaaatgct 4260
acttgaagat accagcccta ccaagggcag ggagaggacc ctatagaggc ctgggacagg 4320
agctcaatga gaaaggagaa gagcagcagg catgagttga atgaaggagg cagggccggg 4380
tcacagggcc ttctaggcca tgagagggta gacaggctag ccgcgttgct ggcgtttttc 4440
cataggctcc gcccccctga cgagcatcac aaaaatcgac gctcaagtca gaggtggcga 4500
aacccgacag gactataaag ataccaggcg tttccccctg gaagctccct cgtgcgctct 4560
cctgttccga ccctgccgct taccggatac ctgtccgcct ttctcccttc gggaagcgtg 4620
gcgctttctc atagctcacg ctgtaggtat ctcagttcgg tgtaggtcgt tcgctccaag 4680
ctgggctgtg tgcacgaacc ccccgttcag cccgaccgct gcgccttatc cggtaactat 4740
cgtcttgagt ccaacccggt aagacacgac ttatcgccac tggcagcagc cactggtaac 4800
aggattagca gagcgaggta tgtaggcggt gctacagagt tcttgaagtg gtggcctaac 4860
tacggctaca ctagaagaac agtatttggt atctgcgctc tgctgaagcc agttaccttc 4920
ggaaaaagag ttggtagctc ttgatccggc aaacaaacca ccgctggtag cggtggtttt 4980
tttgtttgca agcagcagat tacgcgcaga aaaaaaggat ctcaagaaga tcctttgatc 5040
tttagaaaaa ctcatcgagc atcaaatgaa actgcaattt attcatatca ggattatcaa 5100
taccatattt ttgaaaaagc cgtttctgta atgaaggaga aaactcaccg aggcagttcc 5160
ataggatggc aagatcctgg tatcggtctg cgattccgac tcgtccaaca tcaatacaac 5220
ctattaattt cccctcgtca aaaataaggt tatcaagtga gaaatcacca tgagtgacga 5280
ctgaatccgg tgagaatggc aaaagtttat gcatttcttt ccagacttgt tcaacaggcc 5340
agccattacg ctcgtcatca aaatcactcg catcaaccaa accgttattc attcgtgatt 5400
gcgcctgagc cagacgaaat acgcgatcgc tgttaaaagg acaattacaa acaggaatcg 5460
aatgcaaccg gcgcaggaac actgccagcg catcaacaat attttcacct gaatcaggat 5520
attcttctaa tacctggaat gctgtttttc cggggatcgc agtggtgagt aaccatgcat 5580
catcaggagt acggataaaa tgcttgatgg tcggaagagg cataaattcc gtcagccagt 5640
ttagtctgac catctcatct gtaacatcat tggcaacgct acctttgcca tgtttcagaa 5700
acaactctgg cgcatcgggc ttcccataca agcgatagat tgtcgcacct gattgcccga 5760
cattatcgcg agcccattta tacccatata aatcagcatc catgttggaa tttaatcgcg 5820
gcctcgacgt ttcccgttga atatggctca taacacccct tgtattactg tttatgtaag 5880
cagacagttt tattgttcat gatgatatat ttttatcttg tgcaatgtaa catcagagat 5940
tttgagacac 5950
<210> 137
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
GSG Linker_CD8 Products 1, 2, 3, 4
<400> 137
Gly Ser Gly
1
<210> 138
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
P2A_CD8 Products 1, 2, 3, 4
<400> 138
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
1 5 10 15
Pro Gly Pro
<210> 139
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8alpha Signal Peptide_CD8 Products 1, 2, 3, 4
<400> 139
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro
20
<210> 140
<211> 161
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8alpha Extracellular Domain_CD8 Products 1, 2, 3, 4
<400> 140
Ser Gln Phe Arg Val Ser Pro Leu Asp Arg Thr Trp Asn Leu Gly Glu
1 5 10 15
Thr Val Glu Leu Lys Cys Gln Val Leu Leu Ser Asn Pro Thr Ser Gly
20 25 30
Cys Ser Trp Leu Phe Gln Pro Arg Gly Ala Ala Ala Ser Pro Thr Phe
35 40 45
Leu Leu Tyr Leu Ser Gln Asn Lys Pro Lys Ala Ala Glu Gly Leu Asp
50 55 60
Thr Gln Arg Phe Ser Gly Lys Arg Leu Gly Asp Thr Phe Val Leu Thr
65 70 75 80
Leu Ser Asp Phe Arg Arg Glu Asn Glu Gly Tyr Tyr Phe Cys Ser Ala
85 90 95
Leu Ser Asn Ser Ile Met Tyr Phe Ser His Phe Val Pro Val Phe Leu
100 105 110
Pro Ala Lys Pro Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
115 120 125
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
130 135 140
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
145 150 155 160
Asp
<210> 141
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8alpha Transmembrane Domain_CD8 Products 1, 2, 3, 4
<400> 141
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
1 5 10 15
Ser Leu Val Ile Thr
20
<210> 142
<211> 32
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8alpha Intracellular Domain_CD8 Product 1 and 2
<400> 142
Leu Tyr Cys Asn His Arg Asn Arg Arg Arg Val Cys Lys Cys Pro Arg
1 5 10 15
Pro Val Val Lys Ser Gly Asp Lys Pro Ser Leu Ser Ala Arg Tyr Val
20 25 30
<210> 143
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
Furin Cleavage Site_CD8 Products 1, 2, 3, 4
<400> 143
Arg Ala Lys Arg
1
<210> 144
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8beta Signal Peptide _CD8 Product 2
<400> 144
Met Arg Pro Arg Leu Trp Leu Leu Leu Ala Ala Gln Leu Thr Val Leu
1 5 10 15
His Gly Asn Ser Val
20
<210> 145
<211> 149
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8beta Extracellular Domain _CD8 Product 2
<400> 145
Leu Gln Gln Thr Pro Ala Tyr Ile Lys Val Gln Thr Asn Lys Met Val
1 5 10 15
Met Leu Ser Cys Glu Ala Lys Ile Ser Leu Ser Asn Met Arg Ile Tyr
20 25 30
Trp Leu Arg Gln Arg Gln Ala Pro Ser Ser Asp Ser His His Glu Phe
35 40 45
Leu Ala Leu Trp Asp Ser Ala Lys Gly Thr Ile His Gly Glu Glu Val
50 55 60
Glu Gln Glu Lys Ile Ala Val Phe Arg Asp Ala Ser Arg Phe Ile Leu
65 70 75 80
Asn Leu Thr Ser Val Lys Pro Glu Asp Ser Gly Ile Tyr Phe Cys Met
85 90 95
Ile Val Gly Ser Pro Glu Leu Thr Phe Gly Lys Gly Thr Gln Leu Ser
100 105 110
Val Val Asp Phe Leu Pro Thr Thr Ala Gln Pro Thr Lys Lys Ser Thr
115 120 125
Leu Lys Lys Arg Val Cys Arg Leu Pro Arg Pro Glu Thr Gln Lys Gly
130 135 140
Pro Leu Cys Ser Pro
145
<210> 146
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8beta Transmembrane Domain_CD8 Product 2
<400> 146
Ile Thr Leu Gly Leu Leu Val Ala Gly Val Leu Val Leu Leu Val Ser
1 5 10 15
Leu Gly Val Ala Ile
20
<210> 147
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD8beta Intracellular Domain_CD8 Products 2 and 3
<400> 147
His Leu Cys Cys Arg Arg Arg Arg Ala Arg Leu Arg Phe Met Lys Gln
1 5 10 15
Phe Tyr Lys
<210> 148
<211> 40
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
CD4 Intracellular Domain_CD8 Product 4
<400> 148
Cys Val Arg Cys Arg His Arg Arg Arg Gln Ala Glu Arg Met Ser Gln
1 5 10 15
Ile Lys Arg Leu Leu Ser Glu Lys Lys Thr Cys Gln Cys Pro His Arg
20 25 30
Phe Gln Lys Thr Cys Ser Pro Ile
35 40
Claims (130)
- 하기를 포함하는 세포:
a. 외인성 T 세포 수용체 (TCR); 및
b. 외인성 CD8. - 제1항에 있어서, 외인성 CD8이 적어도 1종의 단량체를 포함하는 것인 세포.
- 제2항에 있어서, 외인성 CD8의 적어도 1종의 단량체가 세포외 도메인, 막횡단 도메인, 세포내 도메인, 그의 단편, 또는 이들의 조합을 포함하는 것인 세포.
- 제3항에 있어서, 세포외 도메인이 CD8α 세포외 도메인 또는 CD8β 세포외 도메인을 포함하는 것인 세포.
- 제3항 또는 제4항에 있어서, 막횡단 도메인이 CD8α 막횡단 도메인 또는 CD8β 막횡단 도메인을 포함하는 것인 세포.
- 제3항 내지 제5항 중 어느 한 항에 있어서, 세포내 도메인이 CD8α 세포내 도메인 또는 CD8β 세포내 도메인을 포함하는 것인 세포.
- 제3항 내지 제5항 중 어느 한 항에 있어서, 세포내 도메인이 CD4 세포내 도메인을 포함하는 것인 세포.
- 제2항 내지 제6항 중 어느 한 항에 있어서, 적어도 1종의 단량체가 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인을 포함하는 것인 세포.
- 제2항 내지 제6항 중 어느 한 항에 있어서, 적어도 1종의 단량체가 CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인을 포함하는 것인 세포.
- 제2항 내지 제6항 중 어느 한 항에 있어서, 적어도 1종의 단량체가 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인을 포함하는 것인 세포.
- 제2항 내지 제7항 중 어느 한 항에 있어서, 적어도 1종의 단량체가 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 포함하는 것인 세포.
- 제2항 내지 제11항 중 어느 한 항에 있어서, 적어도 1종의 단량체가 신호 펩티드를 포함하는 것인 세포.
- 제12항에 있어서, 신호 펩티드가 CD8 신호 펩티드인 세포.
- 제3항 내지 제13항 중 어느 한 항에 있어서, 세포외 도메인이 서열식별번호: 140, 또는 서열식별번호: 145에 제시된 아미노산 서열을 포함하는 것인 세포.
- 제3항 내지 제14항 중 어느 한 항에 있어서, 막횡단 도메인이 서열식별번호: 141, 또는 서열식별번호: 146에 제시된 아미노산 서열을 포함하는 것인 세포.
- 제3항 내지 제15항 중 어느 한 항에 있어서, 세포내 도메인이 서열식별번호: 142, 서열식별번호: 147, 또는 서열식별번호: 148에 제시된 아미노산 서열을 포함하는 것인 세포.
- 제12항 내지 제16항 중 어느 한 항에 있어서, 신호 펩티드가 서열식별번호: 139, 또는 서열식별번호: 144에 제시된 아미노산 서열을 포함하는 것인 세포.
- 제1항 내지 제17항 중 어느 한 항에 있어서, 외인성 CD8이 2A 서열을 포함하는 것인 세포.
- 제1항 내지 제18항 중 어느 한 항에 있어서, 외인성 CD8이 링커를 포함하는 것인 세포.
- 제19항에 있어서, 링커가 서열식별번호: 137에 제시된 아미노산 서열을 포함하는 것인 세포.
- 제1항 내지 제20항 중 어느 한 항에 있어서, 외인성 CD8이 프로테아제 절단 부위를 포함하는 것인 세포.
- 제21항에 있어서, 프로테아제 절단 부위가 푸린 절단 부위인 세포.
- 제1항 내지 제22항 중 어느 한 항에 있어서, 외인성 TCR이 환자 유래 TCR인 세포.
- 제1항 내지 제23항 중 어느 한 항에 있어서, 외인성 TCR이 신호 서열, 제1 및 제2 2A 서열, 및 TCR 폴리펩티드 서열을 포함하는 것인 세포.
- 제1항 내지 제24항 중 어느 한 항에 있어서, 외인성 TCR이 암 항원을 인식하는 것인 세포.
- 제25항에 있어서, 암 항원이 신생항원인 세포.
- 제25항에 있어서, 암 항원이 환자 특이적 항원인 세포.
- 제1항 내지 제27항 중 어느 한 항에 있어서, 세포가 1차 세포인 세포.
- 제1항 내지 제27항 중 어느 한 항에 있어서, 세포가 환자-유래 세포인 세포.
- 제1항 내지 제27항 중 어느 한 항에 있어서, 세포가 림프구인 세포.
- 제1항 내지 제27항 중 어느 한 항에 있어서, 세포가 T 세포인 세포.
- 제1항 내지 제27항 중 어느 한 항에 있어서, 세포가 어린 T 세포인 세포.
- 제32항에 있어서, 세포가 CD45RA+, CD62L+, CD28+, CD95-, CCR7+, 및 CD27+인 세포.
- 제32항에 있어서, 세포가 CD45RA+, CD62L+, CD28+, CD95+, CD27+, CCR7+인 세포.
- 제32항에 있어서, 세포가 CD45RO+, CD62L+, CD28+, CD95+, CCR7+, CD27+, CD127+인 세포.
- 제1항 내지 제35항 중 어느 한 항에 있어서, 세포 존속을 증진시키고/거나 기억 세포 분화를 증진시키는 유전자 변형을 추가로 포함하는 세포.
- 제1항 내지 제36항 중 어느 한 항에 있어서, 세포의 살해 활성이 외인성 CD8을 갖지 않는 세포의 살해 활성과 비교하여 약 10% 내지 약 500% 증가되는 것인 세포.
- 제1항 내지 제37항 중 어느 한 항에 있어서, 항원에의 TCR의 결합 시 세포의 증식이 외인성 CD8을 갖지 않는 세포의 증식과 비교하여 약 10% 내지 약 500% 증가되는 것인 세포.
- 제1항 내지 제38항 중 어느 한 항에 있어서, 세포에 의한 항원에의 TCR의 결합 시 전염증성 시토카인의 분비가 외인성 CD8을 갖지 않는 세포에 의한 분비와 비교하여 약 10% 내지 약 500% 증가되는 것인 세포.
- 제1항 내지 제39항 중 어느 한 항에 있어서, 세포의 LCK 친화도가 외인성 CD8을 갖지 않는 세포의 LCK 친화도와 비교하여 약 10% 내지 약 500% 증가되는 것인 세포.
- 제1항 내지 제40항 중 어느 한 항에 있어서, 세포의 존속이 외인성 CD8을 갖지 않는 세포의 존속과 비교하여 약 10% 내지 약 500% 증가되는 것인 세포.
- 제1항 내지 제41항 중 어느 한 항에 있어서, 세포의 종양 침윤 능력이 외인성 CD8을 갖지 않는 세포의 종양 침윤 능력과 비교하여 약 10% 내지 약 500% 증가되는 것인 세포.
- 제1항 내지 제42항 중 어느 한 항에 있어서, 외인성 TCR이 CD8-의존성 TCR인 세포.
- 제1항 내지 제42항 중 어느 한 항에 있어서, 외인성 TCR이 CD8-비의존성 TCR인 세포.
- 제1항 내지 제44항 중 어느 한 항에 있어서, 외인성 CD8이 CD8 구축물 1, CD8 구축물 2, CD8 구축물 3, 또는 CD8 구축물 4에 의해 코딩되는 것인 세포.
- 제1항 내지 제44항 중 어느 한 항에 있어서, 외인성 CD8이 하기를 포함하는 것인 세포:
a. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인;
b. CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인;
c. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는
d. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인. - 제1항 내지 제44항 중 어느 한 항에 있어서, 외인성 CD8이 하기를 포함하는 것인 세포:
a. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142);
b. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147);
c. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는
d. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148). - 하기 단계를 포함하는, 세포를 변형시키는 방법:
a. 세포 내로 상동성 재조합 (HR) 주형 핵산 서열을 도입하며, 여기서 HR 주형은 하기를 포함하는 것인 단계:
i. 제1 및 제2 표적 핵산 서열에 대해 상동성인 제1 및 제2 상동성 아암;
ii. 제1 및 제2 상동성 아암 사이에 위치한 TCR 유전자 서열;
iii. 제1 및 제2 상동성 아암 사이에 위치한 CD8 유전자 서열; 및
b. HR 주형 핵산을 세포의 내인성 로커스 내로 재조합하는 단계. - 제48항에 있어서, HR 주형이 CD8 유전자 서열의 상류에 위치한 제1 2A-코딩 서열, CD8 유전자 서열의 하류 및 TCR 유전자 서열의 상류에 위치한 제2 2A-코딩 서열, 및 TCR 유전자 서열의 하류에 위치한 제3 2A-코딩 서열을 포함하며; 여기서 제1, 제2, 및 제3 2A-코딩 서열이 동일한 아미노산 서열을 코딩하고, 서로에 대해 코돈-분기된 것인 방법.
- 제48항 또는 제49항에 있어서, HR 주형이 제1, 제2, 및/또는 제3 2A-코딩 서열의 바로 상류에 위치한 아미노산 서열 Gly Ser Gly를 코딩하는 서열을 포함하는 것인 방법.
- 제49항 또는 제50항에 있어서, HR 주형이 제1, 제2, 및/또는 제3 2A-코딩 서열의 상류에 위치한 푸린 절단 부위를 코딩하는 서열을 추가로 포함하는 것인 방법.
- 제48항 내지 제51항 중 어느 한 항에 있어서, HR 주형이 TCR 유전자 서열 및/또는 CD8 유전자 서열의 바로 상류에 위치한 신호 서열을 코딩하는 서열을 추가로 포함하는 것인 방법.
- 제48항 내지 제52항 중 어느 한 항에 있어서, HR 주형이 제3 2A-코딩 서열 및 제2 상동성 아암 사이에 위치한 제2 TCR 서열을 포함하는 것인 방법.
- 제53항에 있어서, HR 주형이 하기를 포함하는 것인 방법:
a. 제1 TCR 유전자 서열의 바로 상류에 위치한 제1 신호 서열을 코딩하는 서열; 및
b. 제2 TCR 유전자 서열의 바로 상류에 위치한 제2 신호 서열을 코딩하는 서열. - 제48항 내지 제54항 중 어느 한 항에 있어서, HR 주형이 제1 CD8 유전자 서열 및 제2 2A-코딩 서열 사이에 위치한 제2 CD8 유전자 서열을 포함하는 것인 방법.
- 제55항에 있어서, 2A 코딩 서열이 제1 및 제2 CD8 유전자 서열 사이에 위치하는 것인 방법.
- 제55항 또는 제56항에 있어서, 아미노산 서열 Gly Ser Gly를 코딩하는 서열이 제1 및 제2 CD8 유전자 서열 사이에 위치하는 것인 방법.
- 제55항 내지 제57항 중 어느 한 항에 있어서, 푸린 절단 부위를 코딩하는 서열이 제1 및 제2 CD8 유전자 서열 사이에 위치하는 것인 방법.
- 제48항 내지 제58항 중 어느 한 항에 있어서, CD8 유전자 서열이 세포외 도메인을 코딩하는 서열, 세포내 도메인을 코딩하는 서열, 세포내 도메인을 코딩하는 서열, 그의 단편, 또는 이들의 조합을 포함하는 것인 방법.
- 제59항에 있어서, 세포외 도메인을 코딩하는 서열이 CD8α 세포외 도메인 또는 CD8β 세포외 도메인을 코딩하는 서열을 포함하는 것인 방법.
- 제59항 또는 제60항에 있어서, 막횡단 도메인을 코딩하는 서열이 CD8α 막횡단 도메인 또는 CD8β 막횡단 도메인을 코딩하는 서열을 포함하는 것인 방법.
- 제59항 내지 제61항 중 어느 한 항에 있어서, 세포내 도메인을 코딩하는 서열이 CD8α 세포내 도메인 또는 CD8β 세포내 도메인을 코딩하는 서열을 포함하는 것인 방법.
- 제59항 내지 제61항 중 어느 한 항에 있어서, 세포내 도메인을 코딩하는 서열이 CD4 세포내 도메인을 코딩하는 서열을 포함하는 것인 방법.
- 제59항 내지 제62항 중 어느 한 항에 있어서, CD8 유전자 서열이 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인을 코딩하는 서열을 포함하는 것인 방법.
- 제59항 내지 제62항 중 어느 한 항에 있어서, CD8 유전자 서열이 CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인을 코딩하는 서열을 포함하는 것인 방법.
- 제59항 내지 제62항 중 어느 한 항에 있어서, CD8 유전자 서열이 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인을 코딩하는 서열을 포함하는 것인 방법.
- 제59항 내지 제63항 중 어느 한 항에 있어서, CD8 유전자 서열이 CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인을 코딩하는 서열을 포함하는 것인 방법.
- 제55항 내지 제67항 중 어느 한 항에 있어서, HR 주형이 하기를 포함하는 것인 방법:
a. 제1 CD8 유전자 서열의 바로 상류에 위치한 제1 신호 서열을 코딩하는 서열; 및
b. 제2 CD8 유전자 서열의 바로 상류에 위치한 제2 신호 서열을 코딩하는 서열. - 제52항 내지 제68항 중 어느 한 항에 있어서, 신호 서열이 CD8 신호 서열, 인간 성장 호르몬 신호 서열, 그의 단편, 또는 이들의 조합인 방법.
- 제48항 내지 제69항 중 어느 한 항에 있어서, HR 주형의 제1 및 제2 상동성 아암이 각각 약 300개 염기 내지 약 2,000개 염기의 길이인 방법.
- 제48항 내지 제70항 중 어느 한 항에 있어서, HR 주형의 제1 및 제2 상동성 아암이 각각 약 600개 염기 내지 약 2,000개 염기의 길이인 방법.
- 제48항 내지 제71항 중 어느 한 항에 있어서, 외인성 TCR이 환자 유래 TCR인 방법.
- 제48항 내지 제72항 중 어느 한 항에 있어서, 외인성 TCR이 신호 서열, 제1 및 제2 2A 서열, 및 TCR 폴리펩티드 서열을 포함하는 것인 방법.
- 제48항 내지 제73항 중 어느 한 항에 있어서, 외인성 TCR이 암 항원을 인식하는 것인 방법.
- 제74항에 있어서, 암 항원이 신생항원인 방법.
- 제74항에 있어서, 암 항원이 환자 특이적 항원인 방법.
- 제48항 내지 제76항 중 어느 한 항에 있어서, HR 주형이 비-바이러스성인 방법.
- 제48항 내지 제77항 중 어느 한 항에 있어서, HR 주형이 원형 DNA인 방법.
- 제48항 내지 제77항 중 어느 한 항에 있어서, HR 주형이 선형 DNA인 방법.
- 제48항 내지 제79항 중 어느 한 항에 있어서, 도입이 전기천공을 통해 일어나는 것인 방법.
- 제48항 내지 제80항 중 어느 한 항에 있어서, 재조합이 하기를 포함하는 것인 방법:
a. 뉴클레아제에 의한 내인성 로커스의 절단; 및
b. 상동성 지정 복구에 의한 내인성 로커스 내로의 HR 주형 핵산 서열의 재조합. - 제81항에 있어서, 뉴클레아제가 클러스터링된 규칙적 간격의 짧은 회문구조 반복부 (CRISPR) 패밀리 뉴클레아제, 또는 그의 유도체인 방법.
- 제82항에 있어서, gRNA를 추가로 포함하는 방법.
- 제48항 내지 제83항 중 어느 한 항에 있어서, 프로세스가 세포를 배양하는 것을 추가로 포함하는 것인 방법.
- 제84항에 있어서, 배양이 적어도 1종의 시토카인의 존재 하에서 수행되는 것인 방법.
- 제84항 또는 제85항에 있어서, 배양이 IL2, IL7, IL15, 또는 이들의 임의의 조합의 존재 하에서 수행되는 것인 방법.
- 제84항 또는 제85항에 있어서, 배양이 IL7 및 IL15의 존재 하에서 수행되는 것인 방법.
- 제48항 내지 제87항 중 어느 한 항에 있어서, 세포 존속을 증진시키고/거나 기억 세포 분화를 증진시키는 유전자 변형을 추가로 포함하는 방법.
- 제48항 내지 제88항 중 어느 한 항에 있어서, 세포가 1차 세포인 방법.
- 제48항 내지 제88항 중 어느 한 항에 있어서, 세포가 환자-유래 세포인 방법.
- 제48항 내지 제88항 중 어느 한 항에 있어서, 세포가 림프구인 방법.
- 제48항 내지 제88항 중 어느 한 항에 있어서, 세포가 T 세포인 방법.
- 제48항 내지 제88항 중 어느 한 항에 있어서, 세포가 어린 T 세포인 방법.
- 제93항에 있어서, 세포가 CD45RA+, CD62L+, CD28+, CD95-, CCR7+, 및 CD27+인 방법.
- 제93항에 있어서, 세포가 CD45RA+, CD62L+, CD28+, CD95+, CD27+, CCR7+인 방법.
- 제93항에 있어서, 세포가 CD45RO+, CD62L+, CD28+, CD95+, CCR7+, CD27+, CD127+인 방법.
- 제48항 내지 제96항 중 어느 한 항에 있어서, 세포의 살해 활성이 CD8 유전자 서열을 갖지 않는 세포의 살해 활성과 비교하여 약 10% 내지 약 500% 증가되는 것인 방법.
- 제48항 내지 제97항 중 어느 한 항에 있어서, 항원에의 TCR의 결합 시 세포의 증식이 CD8 유전자 서열을 갖지 않는 세포의 증식과 비교하여 약 10% 내지 약 500% 증가되는 것인 방법.
- 제48항 내지 제98항 중 어느 한 항에 있어서, 세포에 의한 항원에의 TCR의 결합 시 전염증성 시토카인의 분비가 CD8 유전자 서열을 갖지 않는 세포에 의한 분비와 비교하여 약 10% 내지 약 500% 증가되는 것인 방법.
- 제48항 내지 제99항 중 어느 한 항에 있어서, 세포의 LCK 친화도가 CD8 유전자 서열을 갖지 않는 세포의 LCK 친화도와 비교하여 약 10% 내지 약 500% 증가되는 것인 방법.
- 제48항 내지 제100항 중 어느 한 항에 있어서, 세포의 존속이 CD8 유전자 서열을 갖지 않는 세포의 존속과 비교하여 약 10% 내지 약 500% 증가되는 것인 방법.
- 제48항 내지 제101항 중 어느 한 항에 있어서, 세포의 종양 침윤 능력이 CD8 유전자 서열을 갖지 않는 세포의 종양 침윤 능력과 비교하여 약 10% 내지 약 500% 증가되는 것인 방법.
- 제48항 내지 제102항 중 어느 한 항에 있어서, TCR 유전자가 CD8-의존성 TCR을 코딩하는 것인 방법.
- 제48항 내지 제102항 중 어느 한 항에 있어서, TCR 유전자가 CD8-비의존성 TCR을 코딩하는 것인 방법.
- 제48항 내지 제104항 중 어느 한 항에 있어서, CD8 유전자 서열이 CD8 구축물 1, CD8 구축물 2, CD8 구축물 3, 또는 CD8 구축물 4에 의해 코딩되는 것인 방법.
- 제48항 내지 제104항 중 어느 한 항에 있어서, CD8 유전자 서열이 하기를 포함하는 것인 방법:
a. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인;
b. CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인;
c. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는
d. CD8α 세포외 도메인, CD8α 막횡단 도메인, CD4 세포내 도메인. - 제48항 내지 제104항 중 어느 한 항에 있어서, CD8 유전자 서열이 하기를 포함하는 것인 방법:
a. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142);
b. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147);
c. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는
d. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148). - 제48항 내지 제107항 중 어느 한 항의 방법에 의해 변형된 세포.
- 제1항 내지 제47항 중 어느 한 항의 세포 또는 제108항의 세포의 유효량을 포함하는 조성물.
- 제109항에 있어서, 조성물이 제약상 허용되는 부형제를 추가로 포함하는 제약 조성물인 조성물.
- 제109항 또는 제110항에 있어서, 조성물이 암의 치료를 위해 이를 필요로 하는 환자에게 투여되는 것인 조성물.
- 제109항 내지 제111항 중 어느 한 항에 있어서, 조성물이 동결보존제를 포함하는 것인 조성물.
- 제109항 내지 제112항 중 어느 한 항에 있어서, 조성물이 혈청 알부민을 포함하는 것인 조성물.
- 제109항 내지 제113항 중 어느 한 항에 있어서, 조성물이 플라스마-라이트(Plasma-Lyte) A, HSA, 및 크리오스토르(CryoStor) CS10을 포함하는 것인 조성물.
- 제1항 내지 제47항 중 어느 한 항의 세포, 제108항의 세포, 또는 제109항 내지 제114항 중 어느 한 항의 조성물의 치료 유효량을 투여하는 것을 포함하는, 암의 치료를 필요로 하는 대상체에서 암을 치료하는 방법.
- 제115항에 있어서, 세포의 치료 유효량을 투여하기 전에, 비-골수소멸성 림프구고갈 레지멘이 대상체에게 투여되는 것인 방법.
- 제115항 또는 제116항에 있어서, 암이 고형 종양인 방법.
- 제115항 또는 제116항에 있어서, 암이 액상 종양인 방법.
- 제117항에 있어서, 고형 종양이 흑색종, 흉부암, 폐암, 난소암, 유방암, 췌장암, 두경부암, 전립선암, 부인과암, 중추 신경계암, 피부암, HPV+ 암, 식도암, 갑상선암, 위암, 간세포암, 담관암종, 신세포암, 고환암, 육종, 및 결장직장암으로 이루어진 군으로부터 선택되는 것인 방법.
- 제118항에 있어서, 액상 종양이 소포성 림프종, 백혈병, 및 다발성 골수종으로 이루어진 군으로부터 선택되는 것인 방법.
- 제1항 내지 제47항 중 어느 한 항의 세포, 제48항 내지 제107항 중 어느 한 항의 방법을 수행하기 위한 시약, 제108항의 세포, 또는 제109항 내지 제114항 중 어느 한 항의 조성물을 포함하는 키트.
- 제121항에 있어서, 키트가 암을 치료하는 것에 대한 서면 지시서를 추가로 포함하는 것인 키트.
- 하기를 포함하는 세포:
a. 외인성 T 세포 수용체 (TCR); 및
b. 하기를 포함하는 외인성 CD8:
i. CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인;
ii. CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인;
iii. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는
iv. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인. - 하기를 포함하는 세포:
a. 외인성 T 세포 수용체 (TCR); 및
b. 하기를 포함하는 외인성 CD8:
i. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142);
ii. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147);
iii. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는
iv. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148). - 하기 단계를 포함하는, 세포를 변형시키는 방법으로서:
a. 세포 내로 상동성 재조합 (HR) 주형 핵산 서열을 도입하며, 여기서 HR 주형은 하기를 포함하는 것인 단계:
i. 제1 및 제2 표적 핵산 서열에 대해 상동성인 제1 및 제2 상동성 아암;
ii. 제1 및 제2 상동성 아암 사이에 위치한 TCR 유전자 서열;
iii. 제1 및 제2 상동성 아암 사이에 위치한 CD8 유전자 서열; 및
b. HR 주형 핵산을 세포의 내인성 로커스 내로 재조합하는 단계,
여기서 CD8 유전자 서열은 하기를 포함하는 것인 방법:
i. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인;
ii. CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인;
iii. CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8β 세포내 도메인; 또는
iv. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인. - 하기 단계를 포함하는, 세포를 변형시키는 방법으로서:
a. 세포 내로 상동성 재조합 (HR) 주형 핵산 서열을 도입하며, 여기서 HR 주형은 하기를 포함하는 것인 단계:
i. 제1 및 제2 표적 핵산 서열에 대해 상동성인 제1 및 제2 상동성 아암;
ii. 제1 및 제2 상동성 아암 사이에 위치한 TCR 유전자 서열;
iii. 제1 및 제2 상동성 아암 사이에 위치한 CD8 유전자 서열; 및
b. HR 주형 핵산을 세포의 내인성 로커스 내로 재조합하는 단계,
여기서 CD8 유전자 서열은 하기를 포함하는 것인 방법:
i. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142);
ii. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147);
iii. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는
iv. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148). - 세포를 포함하는 조성물로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 하기를 포함하는 것인 조성물:
a. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인;
b. CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인,
c. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는
d. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인. - 세포를 포함하는 조성물로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 하기를 포함하는 것인 조성물:
a. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142);
b. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147);
c. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는
d. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148). - 치료 유효량의 세포를 투여하는 것을 포함하는, 암의 치료를 필요로 하는 대상체에서 암을 치료하는 방법으로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 하기를 포함하는 것인 방법:
a. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8α 세포내 도메인;
b. CD8α 세포외 도메인, CD8α 막횡단 도메인, CD8α 세포내 도메인, CD8β 세포외 도메인, CD8β 막횡단 도메인, 및 CD8β 세포내 도메인,
c. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD8β 세포내 도메인; 또는
d. CD8α 세포외 도메인, CD8α 막횡단 도메인, 및 CD4 세포내 도메인. - 치료 유효량의 세포를 투여하는 것을 포함하는 암의 치료를 필요로 하는 대상체에서 암을 치료하는 방법으로서, 여기서 세포는 외인성 T 세포 수용체 (TCR) 및 외인성 CD8을 포함하며, 여기서 외인성 CD8은 하기를 포함하는 것인 방법:
a. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8α 세포내 도메인 (서열식별번호: 142);
b. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), CD8α 세포내 도메인 (서열식별번호: 142), CD8β 신호 펩티드 (서열식별번호: 144), CD8β 세포외 도메인 (서열식별번호: 145), CD8β 막횡단 도메인 (서열식별번호: 146), 및 CD8β 세포내 도메인 (서열식별번호: 147);
c. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD8β 세포내 도메인 (서열식별번호: 147); 또는
d. CD8α 신호 펩티드 (서열식별번호: 139), CD8α 세포외 도메인 (서열식별번호: 140), CD8α 막횡단 도메인 (서열식별번호: 141), 및 CD4 세포내 도메인 (서열식별번호: 148).
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962841753P | 2019-05-01 | 2019-05-01 | |
| US201962841748P | 2019-05-01 | 2019-05-01 | |
| US62/841,753 | 2019-05-01 | ||
| US62/841,748 | 2019-05-01 | ||
| PCT/US2020/030818 WO2020223537A1 (en) | 2019-05-01 | 2020-04-30 | Compositions and methods for the treatment of cancer using a cdb engineered t cell therapy |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220004703A true KR20220004703A (ko) | 2022-01-11 |
Family
ID=73029470
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020217038746A Pending KR20220004703A (ko) | 2019-05-01 | 2020-04-30 | Cd8 조작된 t 세포 요법을 사용한 암의 치료를 위한 조성물 및 방법 |
| KR1020217038747A Pending KR20220005050A (ko) | 2019-05-01 | 2020-04-30 | Tet2 조작된 t 세포 요법을 사용한 암의 치료를 위한 조성물 및 방법 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020217038747A Pending KR20220005050A (ko) | 2019-05-01 | 2020-04-30 | Tet2 조작된 t 세포 요법을 사용한 암의 치료를 위한 조성물 및 방법 |
Country Status (11)
| Country | Link |
|---|---|
| US (3) | US20210085720A1 (ko) |
| EP (2) | EP3962938A4 (ko) |
| JP (2) | JP2022531231A (ko) |
| KR (2) | KR20220004703A (ko) |
| CN (1) | CN113748127B (ko) |
| AU (2) | AU2020266579A1 (ko) |
| CA (2) | CA3136740A1 (ko) |
| IL (2) | IL287639A (ko) |
| MX (2) | MX2021013225A (ko) |
| SG (2) | SG11202111532SA (ko) |
| WO (3) | WO2020223537A1 (ko) |
Families Citing this family (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3856769A4 (en) * | 2018-09-28 | 2022-08-17 | Memorial Sloan Kettering Cancer Center | Immunoresponsive cells expressing dominant negative fas and uses thereof |
| CN114729325A (zh) * | 2019-09-06 | 2022-07-08 | 克里斯珀医疗股份公司 | 在培养物中具有改善的持久性的基因工程化t细胞 |
| IL297539A (en) * | 2020-04-24 | 2022-12-01 | Pact Pharma Inc | Methods for determining the efficiency of gene editing in cells |
| WO2022109277A1 (en) * | 2020-11-20 | 2022-05-27 | Pact Pharma, Inc. | COMPOSITIONS AND METHODS FOR THE TREATMENT OF CANCER USING A TGFβRII ENGINEERED T CELL THERAPY |
| CA3201767A1 (en) * | 2020-12-14 | 2022-06-23 | Thomas M. Schmitt | Compositions and methods for cellular immunotherapy |
| WO2022140361A1 (en) * | 2020-12-22 | 2022-06-30 | Ludwig Institute For Cancer Research Ltd | Genetically engineered lymphocytes for adoptive cell therapy |
| WO2022177970A1 (en) * | 2021-02-18 | 2022-08-25 | University Of Florida Research Foundation, Incorporated | Enhancing metabolic fitness of t cells to treat cancer |
| AU2022226655A1 (en) | 2021-02-25 | 2023-07-27 | Lyell Immunopharma, Inc. | Codon-optimized nucleotide sequences encoding an ap-1 transcription factor |
| KR20230148837A (ko) | 2021-02-25 | 2023-10-25 | 라이엘 이뮤노파마, 인크. | Ror1 표적화 키메라 항원 수용체 |
| JP2024523014A (ja) * | 2021-06-11 | 2024-06-25 | パクト ファーマ インコーポレイテッド | 細胞製剤を査定する方法 |
| AU2022379192A1 (en) | 2021-10-28 | 2024-05-02 | Lyell Immunopharma, Inc. | Methods for culturing cells expressing c-jun |
| JP2024540099A (ja) | 2021-10-28 | 2024-10-31 | ライエル・イミュノファーマ・インコーポレイテッド | Ror1結合タンパク質を発現する細胞を培養する方法 |
| CN114373511B (zh) * | 2022-03-15 | 2022-08-30 | 南方医科大学南方医院 | 基于5hmC分子标志物检测的肠癌模型及肠癌模型构建方法 |
| WO2023212507A1 (en) * | 2022-04-26 | 2023-11-02 | Fred Hutchinson Cancer Center | Compositions and methods for cellular immunotherapy |
| EP4561602A1 (en) | 2022-07-28 | 2025-06-04 | Stemcell Technologies Canada Inc. | Polynucleotides encoding linked antigens and uses thereof |
| KR20250073155A (ko) * | 2022-09-19 | 2025-05-27 | 에멘도바이오 인코포레이티드 | Faslg의 이중 대립유전자 녹아웃 |
| KR20250072710A (ko) * | 2022-09-19 | 2025-05-26 | 에멘도바이오 인코포레이티드 | Tet2의 이중 대립유전자 녹아웃 |
| CN120202302A (zh) * | 2022-09-19 | 2025-06-24 | 埃门多生物公司 | Ctla4双等位基因敲除 |
| WO2024064958A1 (en) | 2022-09-23 | 2024-03-28 | Lyell Immunopharma, Inc. | Methods for culturing nr4a-deficient cells |
| WO2024064952A1 (en) | 2022-09-23 | 2024-03-28 | Lyell Immunopharma, Inc. | Methods for culturing nr4a-deficient cells overexpressing c-jun |
| WO2024077174A1 (en) | 2022-10-05 | 2024-04-11 | Lyell Immunopharma, Inc. | Methods for culturing nr4a-deficient cells |
| CN116179495B (zh) * | 2022-11-28 | 2025-06-06 | 上海恩凯细胞技术有限公司 | 转基因免疫细胞及其应用 |
| WO2025010272A1 (en) | 2023-07-03 | 2025-01-09 | Neoimmunetech, Inc. | Heterodimeric fc molecules and uses thereof |
| WO2025027088A1 (en) * | 2023-07-31 | 2025-02-06 | T-Knife Gmbh | An enhanced chimeric human cd8 co-receptor, a nucleic acid encoding the enhanced chimeric human cd8 co-receptor, corresponding vectors, isolated t-cells transduced with the nucleic acid or corresponding vectors and kits for preparing them, as well as corresponding pharmaceutical compositions and methods for treating a patient having a disease |
| WO2025045752A1 (en) * | 2023-08-25 | 2025-03-06 | T-Knife Gmbh | Chimeric human cd 95 switch receptor, t-cell expressing said receptor together with an engineered t-cell receptor, respective vectors, kits, pharmaceutical compositions and methods for treating a patient having a disease |
Family Cites Families (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5399346A (en) | 1989-06-14 | 1995-03-21 | The United States Of America As Represented By The Department Of Health And Human Services | Gene therapy |
| US20020127594A1 (en) * | 2000-06-22 | 2002-09-12 | Gearing David P. | Don-1 gene and polypeptides and uses therefor |
| US6355412B1 (en) * | 1999-07-09 | 2002-03-12 | The European Molecular Biology Laboratory | Methods and compositions for directed cloning and subcloning using homologous recombination |
| US7485291B2 (en) * | 2003-06-03 | 2009-02-03 | Cell Genesys, Inc. | Compositions and methods for generating multiple polypeptides from a single vector using a virus derived peptide cleavage site, and uses thereof |
| US8119772B2 (en) * | 2006-09-29 | 2012-02-21 | California Institute Of Technology | MART-1 T cell receptors |
| WO2013033626A2 (en) * | 2011-08-31 | 2013-03-07 | Trustees Of Dartmouth College | Nkp30 receptor targeted therapeutics |
| US10316289B2 (en) * | 2012-09-06 | 2019-06-11 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Methods of producing T memory stem cell populations |
| HUE051523T2 (hu) * | 2013-11-21 | 2021-03-01 | Ucl Business Ltd | Sejt |
| JP6898244B2 (ja) * | 2014-11-06 | 2021-07-07 | ユニバーシティー オブ メリーランド,ボルティモア | CD8αおよびT細胞受容体の変異体ならびに免疫細胞の応答の調節においてそれらを使用する方法 |
| KR102699643B1 (ko) * | 2015-04-06 | 2024-08-28 | 리제너론 파아마슈티컬스, 인크. | 비인간 동물에서의 인간화 t 세포 매개 면역반응 |
| MA44907A (fr) * | 2015-09-11 | 2018-07-18 | Agenus Inc | Cellules hôtes génétiquement modifiées et leurs procédés d'utilisation |
| BR112018005295A2 (pt) * | 2015-09-17 | 2018-12-11 | Novartis Ag | terapias com célula t car com eficácia aumentada |
| SG11201805157TA (en) * | 2015-12-18 | 2018-07-30 | Sangamo Therapeutics Inc | Targeted disruption of the mhc cell receptor |
| EP3440101B1 (en) * | 2016-04-04 | 2021-10-06 | Indi Molecular, Inc. | Cd8-specific capture agents, compositions, and methods of using and making |
| JP6866475B2 (ja) * | 2016-09-23 | 2021-04-28 | フレッド ハッチンソン キャンサー リサーチ センター | マイナー組織適合性(h)抗原ha−1に特異的なtcr及びその使用 |
| EP3545001A4 (en) * | 2016-11-22 | 2020-10-21 | Alloplex Biotherapeutics | ALLOGENIC TUMOR CELL VACCINE |
| JP7037577B2 (ja) * | 2017-03-15 | 2022-03-16 | フレッド ハッチンソン キャンサー リサーチ センター | 高親和性mage-a1特異的tcr及びその使用 |
| JP2020513828A (ja) | 2017-03-22 | 2020-05-21 | ノバルティス アーゲー | 増強された有効性を有するバイオマーカー及びcar t細胞療法 |
| US11851659B2 (en) * | 2017-03-22 | 2023-12-26 | Novartis Ag | Compositions and methods for immunooncology |
| US11512287B2 (en) * | 2017-06-16 | 2022-11-29 | Sangamo Therapeutics, Inc. | Targeted disruption of T cell and/or HLA receptors |
| EP4327819A3 (en) * | 2017-06-30 | 2024-05-29 | Academisch Ziekenhuis Leiden (H.O.D.N. Leids Universitair Medisch Centrum) | Treatment of haematological malignancies |
| AU2018329741B2 (en) * | 2017-09-08 | 2025-02-20 | Poseida Therapeutics, Inc. | Compositions and methods for chimeric ligand receptor (CLR)-mediated conditional gene expression |
| AU2018357861B2 (en) * | 2017-10-30 | 2024-11-14 | Adoc Ssf, Llc | Primary cell gene editing |
| WO2019136335A1 (en) * | 2018-01-05 | 2019-07-11 | Gencyte Therapeutics, Inc. | Precision molecular adaptor system for car-t immunotherapy |
| CN112334480A (zh) | 2018-04-02 | 2021-02-05 | 派克特制药公司 | 肽-MHC comPACT |
| JP7558151B2 (ja) * | 2018-09-05 | 2024-09-30 | アダプティミューン・リミテッド | T細胞改変 |
| GB201819540D0 (en) * | 2018-11-30 | 2019-01-16 | Adaptimmune Ltd | T cell modification |
| JP7611836B2 (ja) | 2019-02-12 | 2025-01-10 | パクト ファーマ インコーポレイテッド | 抗原特異的t細胞の同定のための組成物と方法 |
| MX2021014552A (es) * | 2019-05-27 | 2022-02-11 | Immatics Us Inc | Vectores viricos y uso de los mismos en terapias celulares adoptivas. |
-
2020
- 2020-04-30 EP EP20798669.6A patent/EP3962938A4/en active Pending
- 2020-04-30 SG SG11202111532SA patent/SG11202111532SA/en unknown
- 2020-04-30 WO PCT/US2020/030818 patent/WO2020223537A1/en unknown
- 2020-04-30 SG SG11202111865UA patent/SG11202111865UA/en unknown
- 2020-04-30 JP JP2021564498A patent/JP2022531231A/ja active Pending
- 2020-04-30 KR KR1020217038746A patent/KR20220004703A/ko active Pending
- 2020-04-30 AU AU2020266579A patent/AU2020266579A1/en active Pending
- 2020-04-30 CN CN202080032593.3A patent/CN113748127B/zh active Active
- 2020-04-30 MX MX2021013225A patent/MX2021013225A/es unknown
- 2020-04-30 EP EP20798347.9A patent/EP3953379A4/en active Pending
- 2020-04-30 CA CA3136740A patent/CA3136740A1/en active Pending
- 2020-04-30 WO PCT/US2020/030704 patent/WO2020223478A1/en unknown
- 2020-04-30 AU AU2020264484A patent/AU2020264484A1/en active Pending
- 2020-04-30 CA CA3151385A patent/CA3151385A1/en active Pending
- 2020-04-30 MX MX2021013218A patent/MX2021013218A/es unknown
- 2020-04-30 JP JP2021564500A patent/JP2022530653A/ja active Pending
- 2020-04-30 KR KR1020217038747A patent/KR20220005050A/ko active Pending
- 2020-05-01 WO PCT/US2020/031007 patent/WO2020223625A1/en active Application Filing
- 2020-11-16 US US17/099,140 patent/US20210085720A1/en active Pending
- 2020-11-20 US US17/100,223 patent/US11304978B2/en active Active
-
2021
- 2021-10-27 IL IL287639A patent/IL287639A/en unknown
- 2021-10-27 IL IL287643A patent/IL287643A/en unknown
-
2022
- 2022-03-10 US US17/691,565 patent/US12247061B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP3962938A1 (en) | 2022-03-09 |
| US20210085721A1 (en) | 2021-03-25 |
| IL287643A (en) | 2021-12-01 |
| WO2020223537A1 (en) | 2020-11-05 |
| US20220193139A1 (en) | 2022-06-23 |
| MX2021013225A (es) | 2022-01-06 |
| JP2022531231A (ja) | 2022-07-06 |
| US12247061B2 (en) | 2025-03-11 |
| AU2020266579A1 (en) | 2021-11-25 |
| KR20220005050A (ko) | 2022-01-12 |
| JP2022530653A (ja) | 2022-06-30 |
| MX2021013218A (es) | 2021-12-10 |
| AU2020264484A1 (en) | 2021-11-04 |
| US11304978B2 (en) | 2022-04-19 |
| SG11202111532SA (en) | 2021-11-29 |
| WO2020223537A8 (en) | 2021-11-11 |
| US20210085720A1 (en) | 2021-03-25 |
| WO2020223478A1 (en) | 2020-11-05 |
| WO2020223625A1 (en) | 2020-11-05 |
| CN113748127A (zh) | 2021-12-03 |
| IL287639A (en) | 2021-12-01 |
| CA3136740A1 (en) | 2020-11-05 |
| SG11202111865UA (en) | 2021-11-29 |
| CA3151385A1 (en) | 2020-11-05 |
| EP3953379A4 (en) | 2023-05-31 |
| CN113748127B (zh) | 2025-01-10 |
| EP3953379A1 (en) | 2022-02-16 |
| EP3962938A4 (en) | 2023-07-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20220004703A (ko) | Cd8 조작된 t 세포 요법을 사용한 암의 치료를 위한 조성물 및 방법 | |
| US12258397B2 (en) | Production of engineered T-cells by sleeping beauty transposon coupled with methotrexate selection | |
| US20220315892A1 (en) | Engineered Artificial Antigen Presenting Cells for Tumor Infiltrating Lymphocyte Expansion | |
| US20230303975A1 (en) | Modified lymphocytes | |
| KR20220038362A (ko) | 재조합 ad35 벡터 및 관련 유전자 요법 개선 | |
| KR20130010121A (ko) | 치료적 단백질을 조건부로 발현하는 벡터,상기 벡터를 포함하는 숙주 세포 및 이의 용도 | |
| JP7642548B2 (ja) | 免疫療法の改善のための遺伝子調節組成物及び遺伝子調節方法 | |
| KR20240037185A (ko) | 키메라 공동자극 수용체, 케모카인 수용체, 및 세포 면역치료에서의 이의 용도 | |
| KR20230010231A (ko) | 생체내 형질도입을 위한 벡터 및 방법 | |
| WO2021050948A1 (en) | Compositions and methods for tcr reprogramming using fusion proteins | |
| US20220041999A1 (en) | Methods to enrich genetically engineered t cells | |
| TW202237823A (zh) | 用於治療癌症之使用經TGFβRII工程化T細胞療法的組合物及方法 | |
| TW202233830A (zh) | 使用下一代工程化t細胞療法治療癌症之組合物及方法 | |
| TW202228728A (zh) | 用於同時調節基因表現之組合物及方法 | |
| EP3630197B1 (en) | Method of selecting genetically modified hematopoietic stem cells | |
| CN115209909A (zh) | 递送组合物和方法 | |
| KR102576635B1 (ko) | Lamp2c 유전자가 녹아웃 된 형질전환 인간 세포주 및 이를 이용한 목적 유전자의 생산 방법 | |
| AU2023353199A1 (en) | Inhibition of genotoxic stress to improve t cell engineering | |
| CN116710108A (zh) | 用于同时调节诸基因表达的组合物和方法 | |
| EA050091B1 (ru) | Рекомбинантные искусственные антиген-презентирующие клетки для увеличения количества опухоль-инфильтрирующих лимфоцитов |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20211126 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application |