KR20210110294A - 통과세포외배출용 전달 구조체 및 관련 방법 - Google Patents
통과세포외배출용 전달 구조체 및 관련 방법 Download PDFInfo
- Publication number
- KR20210110294A KR20210110294A KR1020217017210A KR20217017210A KR20210110294A KR 20210110294 A KR20210110294 A KR 20210110294A KR 1020217017210 A KR1020217017210 A KR 1020217017210A KR 20217017210 A KR20217017210 A KR 20217017210A KR 20210110294 A KR20210110294 A KR 20210110294A
- Authority
- KR
- South Korea
- Prior art keywords
- ser
- leu
- gly
- ile
- glu
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/54—Interleukins [IL]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/642—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent the peptide or protein in the drug conjugate being a cytokine, e.g. IL2, chemokine, growth factors or interferons being the inactive part of the conjugate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/65—Peptidic linkers, binders or spacers, e.g. peptidic enzyme-labile linkers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/107—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length by chemical modification of precursor peptides
- C07K1/113—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length by chemical modification of precursor peptides without change of the primary structure
- C07K1/1136—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length by chemical modification of precursor peptides without change of the primary structure by reversible modification of the secondary, tertiary or quarternary structure, e.g. using denaturating or stabilising agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/14—Extraction; Separation; Purification
- C07K1/16—Extraction; Separation; Purification by chromatography
- C07K1/18—Ion-exchange chromatography
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/28—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Vibrionaceae (F)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
Abstract
본 발명은 담체와 함께 치료용 화물 부분, 예를 들어 IL-22를 포함하는 비-자연적으로 발생하는 융합 분자를 제공한다. 또한, 본 발명은 융합 분자의 제조, 정제, 재접힘, 제형, 및 투여를 위한 방법 및 조성물을 제공한다. 또한, 질환 또는 장애를 치료 및 예방하기 위해 정제된 분자를 사용하는 방법이 본 명세서에서 제공된다.
Description
상호 참조
본 출원은 2018년 11월 7일에 출원된 미국 가출원 번호 제 62/756,889호, 2019년 8월 16일에 출원된 미국 가출원 번호 제 62/888,133호, 및 2019년 8월 16일에 출원된 미국 가출원 번호 제 62/888,238호, 2019년 9월 11일에 출원된 국제 출원 번호 PCT/US2019/050708, 및 2019년 3월 8일에 출원된 국제 출원 번호 PCT/US2019/021474의 이익을 주장하고, 본 출원은 전체 참조로 본 명세서에 포함된다.
본 발명은 통과세포외배출용 전달 구조체 및 관련 방법에 관한 것이다.
단백질은 온전한(intact) 상피 장벽을 가로지르거나 또는 융합막(tight junctions)을 통해 장벽을 가로질러 확산할 수 없기 때문에, 장 상피(gut epithelium)는 단백질과 같은 큰 치료용 분자를 경구 투여하려는 노력을 좌절시켰다. 일단 상피 세포에 의해 흡수되면, 치료용 단백질은 파괴적인 리소좀 트래피킹 경로(trafficking pathway)로 들어갈 수 있거나 또는 장 내강(intestinal lumen)으로 다시 방출될 수 있다. 장 상피를 가로질러 쉽게 수송될 수 없는 이러한 불능은 특히 폴리펩티드-기반 치료제를 위한 상업적으로 실행 가능한 경구 제형을 개발하는데 제한 요인(limiting factor)이 될 수 있다.
정맥 또는 피하 투여와 같은 비경구 투여가 해결책이 될 수 있으나, 이러한 투여 경로는 종종 상당한 부작용을 일으키고, 치료 효능을 낮추며, 순응도에 부정적인 영향을 미칠 수 있는 환자 편의를 감소시킬 수 있다. 상피, 예를 들어, 장 상피를 가로질러 치료제를 수송하기 위한 개선된 조성물 및 방법이 필요하다.
또한, 고수율 및 낮은 내독소 수준으로 올바르게 접히고, 생물학적 활성이며, 안정된 폴리펩티드를 얻기 위하여 생물학적 활성 폴리펩티드의 정제 및 재접힘 (refolding)은 여전히 생물학적 치료제 (예를 들어, 폴리펩티드)의 비용- 및 자원-효율적인 제조를 위한 가장 어려운 측면 중 하나로 간주된다. 따라서, 이러한 생물학적 활성 분자의 개선된 제조 방법 (발효, 재접힘, 정제 및 제형)도 필요하다.
다양한 측면에서, 본 발명은 서열번호: 15 또는 서열번호: 17에 제시된 아미노산 서열, 또는 이와 적어도 90%, 95% 또는 99% 서열 동일성을 갖는 아미노산 서열을 포함하는 전달 구조체를 제공한다.
다양한 측면에서, 본 발명은 서열번호: 7 또는 서열번호: 9에 제시된 아미노산 서열로 이루어진 담체를 포함하는 전달 구조체를 제공한다. 일 예에서, 담체는 이종성 페이로드(heterologous payload)에 결합된다. 일 예에서, 이종성 페이로드는 인간 IL-22이다. 일 예에서, 인간 IL-22는 서열번호: 11에 제시된 아미노산 서열로 이루어진다. 일 예에서, 담체는 IL-22에 공유 또는 비-공유 결합된다. 일 예에서, 담체는 스페이서를 통해 IL-22에 공유 결합된다. 일 예에서, 스페이서는 서열번호: 13에 제시된 아미노산 서열로 이루어진다. 일 예에서, 전달 구조체는 서열번호: 15 또는 서열번호: 17에 제시된 아미노산 서열로 이루어진다.
본 발명은 피험자에서 염증성 질환의 치료 방법을 제공하며, 방법은 유효량의 본 명세서에 기재된 전달 구조체 (예를 들어, 서열번호: 15 또는 서열번호: 17)를 피험자에게 투여하는 단계를 포함한다. 일 예에서, 염증성 질환은 간염, 비만, 지방간 질환, 간 염증. 또는 췌장염, 크론병, 궤양성 대장염, 주머니염 (pouchitis), 직장염(proctitis), 다발성 경화증, 전신 홍반성 루푸스(systemic lupus erythematosus), 이식편 대 숙주 질환(graft versus host disease), 류마티스 관절염 또는 건선이다. 일 예에서, 질환은 크론병 또는 궤양성 대장염이다.
특정 실시예에서, 본 발명은 정제된 비-자연적으로 발생하는 융합 단백질을 얻는 방법을 기재하며, 방법은 비-자연적으로 발생하는 융합 단백질을 포함하는 혼합물에 대해 음이온 교환 크로마토그래피를 수행하여 비-자연적으로 발생하는 융합 단백질을 포함하는 제 1 분획을 얻는 단계를 포함하고; 여기서 비-자연적으로 발생하는 융합 단백질은 IL-22 및 담체를 포함한다. 일 실시예에서, 음이온 교환 크로마토그래피를 수행하는 단계는 음이온성 교환 수지에 비-자연적으로 발생하는 융합 단백질을 결합하고 비-자연적으로 발생하는 융합 단백질의 후속 용리를 위해 증가하는 염 구배를 제공하여 제 1 분획을 얻는 단계를 포함한다. 일 실시예에서, 음이온 교환 크로마토그래피를 수행하는 단계는 혼합물을 아민-작용화된 폴리메타크릴레이트 비드를 포함하는 수지와 접촉시키는 단계를 포함한다. 일 실시예에서, 수지는 NH2-750F 수지이다.
일 실시예에서, 방법은 음이온 교환 크로마토그래피를 수행하기 전에 비-자연적으로 발생하는 융합 단백질을 재접힘하는 단계를 더 포함한다. 일 실시예에서, 비-자연적으로 발생하는 융합 단백질을 재접힘하는 단계는 봉입체(inclusion bodies)로부터의 카오트로프(chaotrope)-가용화된 단백질을 재접힘 용액과 접촉시키는 단계를 포함하며, 여기서 재접힘 용액은 아르기닌 (0.75 M 내지 1.25 M); 글리세롤 (2% 내지 20% v/v); 시스테인 (0.5 mM 내지 10 mm); 및 시스타민 (0.2 mM 내지 10 mM)을 포함하고; 재접힘 용액은 7.5 내지 8.5의 pH를 가진다. 일 실시예에서, 아르기닌은 0.9 M 내지 1.1 M의 농도로 재접힘 용액에 존재하며; 글리세롤은 7% 내지 13% (w/w)의 농도로 재접힘 용액에 존재하고; 시스테인은 1.5 mM 내지 6 mM의 농도로 재접힘 용액에 존재하며; 시스타민은 0.6 mM 내지 3 mM의 농도로 재접힘 용액에 존재하고; 재접힘 용액은 7.8 내지 8.2의 pH를 가진다.
일 실시예에서, 방법은 제 1 분획을 포함하는 시료를 히드록시아파타이트 수지로 처리하여 비-자연적으로 발생하는 융합 단백질을 포함하는 제 2 분획을 얻는 단계를 더 포함한다. 일 실시예에서, 히드록시아파타이트 수지는 CaPure-히드록시아파타이트 수지이다. 일 실시예에서, 방법은 제 1 분획을 포함하는 시료에 대해 양이온 교환 크로마토그래피를 수행하는 단계를 더 포함한다. 일 실시예에서, 양이온 교환 크로마토그래피를 수행하는 단계는 제 1 분획을 포함하는 시료를 설페이트-작용화된 폴리메타크릴레이트 비드를 포함하는 수지와 접촉시키는 단계를 포함한다. 일 실시예에서, 수지는 TOYOPEARL 설페이트-650F 수지이다.
일 실시예에서, 세포와 접촉시, 담체는 비-자연적으로 발생하는 융합 단백질의 세포내이입(endocytosis) 또는 통과세포외배출(transcytosis)을 촉진시킨다. 일 실시예에서, 세포와 접촉시, 담체는 비-자연적으로 발생하는 융합 단백질의 통과세포외배출을 촉진시킨다. 일 실시예에서, 세포는 장 상피 세포이다. 일 실시예에서, 장 상피 세포는 편광 장 상피 세포이다. 일 실시예에서, 담체는 자연적으로 발생하는 또는 비-자연적으로 발생하는 콜릭스 폴리펩티드의 절단된 변이체이다. 일 실시예에서, 담체는 서열번호: 1, 2, 3, 4, 5, 6, 7, 8, 9, 22, 또는 23 중 어느 하나와 적어도 70%, 80%, 85%, 90%, 95%, 98%, 99%, 또는 100% 서열 동일성을 가진다. 일 실시예에서, 비-자연적으로 발생하는 융합 단백질은 서열번호: 14-21 중 어느 하나의 서열과 적어도 70%, 80%, 85%, 90%, 95%, 98%, 99%, 또는 100% 서열 동일성을 가진다. 일 실시예에서, IL-22는 서열번호: 10, 11, 또는 12 중 어느 하나와 적어도 85%, 90%, 95%, 98%, 99% 또는 100% 서열 동일성을 가진다.
일 실시예에서, 담체는 그 자체로 제 1 등전점 (pI)을 가지며, IL-22는 그 자체로 제 2 등전점을 가지며, 여기서 제 1 등전점은 제 2 등전점보다 낮은 적어도 1 pH 단위, 적어도 1.5 pH 단위, 적어도 1.7 pH 단위, 또는 적어도 2 pH 단위이다. 예를 들어, 일 실시예에서, 담체는 4.8 내지 5.4, 4.9 내지 5.3, 5.0 내지 5.2의 pI, 예를 들어 약 5.1의 pI를 가진다. 일 실시예에서, IL-22의 pI는 약 6.8 내지 7.4, 예를 들어 약 6.9 내지 7.3, 약 7.0 내지 7.2, 예를 들어 약 7.1 이다. 일 실시예에서, 비-자연적으로 발생하는 융합 단백질은 본 명세서에 기재된 방법 중 어느 하나에 의해 얻어진다.
특정 실시예에서, 본 발명은 담체 및 IL-22를 포함하는 비-자연적으로 발생하는 융합 단백질을 재접힘하는 방법을 기재하며, 방법은 (i) 비-자연적으로 발생하는 융합 단백질을 포함하는 봉입체를 카오트로픽제를 포함하는 가용화 용액과 접촉시켜 가용성 비-자연적으로 발생하는 융합 단백질을 제조하는 단계; (ii) 비-자연적으로 발생하는 융합 단백질을 재접힘 용액과 접촉시키는 단계를 포함하며, 여기서 재접힘 용액은 아르기닌 (0.75 M 내지 1.25 M); 글리세롤 (2% 내지 20% v/v); 시스테인 (0.5 mM 내지 10 mm); 및 시스타민 (0.2 mM 내지 10 mM)을 포함하고; 재접힘 용액은 7.5 내지 8.5의 pH를 가진다.
일 실시예에서, 아르기닌은 0.9 M 내지 1.1 M의 농도로 재접힘 용액에 존재하며; 글리세롤은 7% 내지 13% (w/w)의 농도로 재접힘 용액에 존재하고; 시스테인은 1.5 mM 내지 6 mM의 농도로 재접힘 용액에 존재하며; 시스타민은 0.6 mM 내지 3 mM의 농도로 재접힘 용액에 존재하고; 재접힘 용액은 7.8 내지 8.2의 pH를 가진다.
참조에 의한 통합
본 명세서에 언급된 모든 간행물, 특허, 및 특허 출원은 각각의 개별 간행물, 특허, 또는 특허 출원이 참조로 포함되는 것으로 구체적이고 개별적으로 나타낸 것과 동일한 정도로, 본 명세서에 참조로 포함된다.
본 발명은 비-자연적으로 발생하는 융합 단백질 (예를 들어, 하나 이상의 이종성 페이로드 분자를 수송할 수 있는 전달 구조체) 및 비-자연적으로 발생하는 융합 단백질의 재접힘 및 정제 방법을 기재한다. 예를 들어, 비-자연적으로 발생하는 융합 단백질은 본 명세서에 기재된 IL-22 전달 구조체일 수 있다.
이하의 용어는 통상의 기술자에 의한 이들 용어의 이해 이외에, 본 명세서에서 사용되는 용어의 의미를 나타내기 위해 논의된다. 본 명세서 및 첨부된 청구범위에서 사용된 바와 같이, 단수 형태 "a", "an" 및 "the"는 문맥이 달리 명확하게 지시하지 않는 한 복수 대상을 포함한다. 청구범위는 임의의 선택적 요소를 제외하도록 작성될 수 있다는 점에 더 유의한다. 이와 같이, 이 진술은 청구범위 요소의 인용과 관련하여 "오로지(solely)", "단지(only)" 등과 같은 배타적 용어의 사용, 또는 "부정적인" 제한의 사용에 대한 선행 근거로 사용하기 위한 것이다.
특정 범위 또는 수는 용어 "약"이 앞에 오는 수치(numerical value)와 함께 본 명세서에서 제공된다. 본 명세서에서 사용되는 용어 "약"은 용어가 나타내는 수의 + 또는 - 1%, 2%, 3%, 4%, 또는 5%를 의미할 것이다. 본 명세서에서 사용된 바와 같이, 용어 "피험자" 및 "개체"는 통용되며, 포유류 (예를 들어, 인간 또는 비-인간 동물)를 포함하는 임의의 동물일 수 있다.
본 명세서에서 사용된 바와 같이, 용어 "치료하다", "치료하는" 또는 "치료", 및 기타 문법적 등가물은, 질환 또는 질병의 하나 이상의 증상의 완화, 경감 또는 개선; 질환 또는 질병의 하나 이상의 추가 증상의 징후, 중증도 또는 빈도의 개선, 예방 또는 감소; 질환 또는 질병의 하나 이상의 증상의 근본적인 원인의 완화 또는 예방; 질환 또는 질병의 저해, 예를 들어, 질환 또는 질병의 발생의 저지, 질환 또는 질병의 완화, 질환 또는 질병의 퇴화 야기, 질환 또는 질병에 의해 야기된 질병의 완화; 또는 질환 또는 질병의 증상의 예방적 및/또는 치료적 저해를 포함한다.
본 명세서에 기재된 바와 같이, 아미노산 서열의 맥락에서, 용어 "퍼센트 (%) 서열 동일성" 및 이와 관련된 용어는, 서열을 정렬하고 필요한 경우 갭을 도입한 후 최대 퍼센트 서열 동일성을 달성하고, 임의의 보존적 치환을 서열 동일성의 일부로 고려하지 않는, 선택된 서열의 아미노산 잔기와 동일한 후보 서열의 아미노산 잔기의 백분율이다. 퍼센트 아미노산 서열 동일성을 결정하기 위한 정렬은 당해 기술분야의 기술 내에 있는 다양한 방식, 예를 들어, Clustal Omega, BLAST, BLAST-2, ALIGN, ALIGN-2 또는 Megalign (DNASTAR) 소프트웨어와 같은 공공용 (publicly available) 컴퓨터 소프트웨어를 이용하여 달성될 수 있다. 통상의 기술자는 비교되는 서열의 전장(full-length)에 걸쳐 최대 정렬을 달성하는데 필요한 임의의 알고리즘을 포함하여, 정렬을 측정하기 위한 적당한 매개변수를 결정할 수 있다.
용어 "폴리펩티드" 및 "단백질"은 아미노산 잔기의 고분자를 나타내기 위해 본 명세서에서 통용된다. 또한, 펩티드는 본질적으로 아미드 결합에 반대되는 에테르에 의해 결합된 아미노산과 같은 펩티드 모방체를 포함하나 이에 한정되지 않는 임의의 폴리아미노산을 포함한다.
페이로드 및 전달 구조체
본 발명은 하나 이상의 이종성 페이로드 분자 (예를 들어, 하나 이상의 치료용 페이로드)를 상피 세포 (예를 들어, 편광 장 상피 세포)를 가로질러 통과세포외배출을 통해 고유판으로 수송할 수 있는 전달 구조체를 제공한다. 전달 구조체는 이종성 페이로드에 결합된 담체를 포함할 수 있다. 전달 구조체는 비-자연적으로 발생하는 융합 단백질일 수 있다. 담체는 내인성 트래피킹 경로를 이용하여 편광 상피 세포 (예를 들어, 편광 장 상피 세포)를 가로질러 이종성 페이로드를 수송할 수 있다. 수동 확산의 이용과 반대로, 내인성 트래피킹 경로의 이용은 담체가 이들 세포의 장벽 기능 또는 이종성 페이로드의 생물학적 활성을 손상시키지 않고 상피 세포를 가로질러 이종성 페이로드를 빠르게 효율적으로 왕복(shuttle)하도록 할 수 있다. 또한, 본 발명은 본 명세서 에 기재된 전달 구조체의 정제 및 재접힘 방법을 제공한다.
본 명세서에서 담체는 박테리아에 의해 분비된 폴리펩티드로부터 유래될 수 있다. 이러한 담체는 비브리오 콜레라(Vibrio cholera) 또는 녹농균(Pseudomonas aeruginosa)으로부터 분비된 폴리펩티드로부터 유래될 수 있다. 비브리오 콜레라에 의해 분비된 폴리펩티드는 콜릭스 폴리펩티드일 수 있다. 콜릭스 폴리펩티드로부터 유래된 담체는 자연적으로 발생하거나 또는 비-자연적으로 발생할 수 있다. 예를 들어, 비-자연적으로 발생하는 콜릭스 폴리펩티드는 서열번호: 1에 제시된 아미노산 서열 (Cholix1-634의 예)로 이루어질 수 있다 (표 1). 콜릭스 폴리펩티드로부터 유래된 담체는 콜릭스로부터 유래된 폴리펩티드의 절단된 및/또는 돌연변이된 변이체일 수 있다. 예를 들어, 담체는 서열번호: 1 또는 서열번호: 26의 아미노산 잔기 1-206, 1-245, 1-251, 1-266 및 1-386을 갖는 아미노산 서열을 포함하거나 또는 이루어질 수 있다. 일 예에서, 이러한 담체는 서열번호: 4의 아미노산 잔기 1-206, 1-245, 1-251, 1-266 및 1-386을 갖는 아미노산 서열을 가진다. 돌연변이(들)은 하나 이상의 치환(들), 결실(들), 및/또는 추가(들)을 포함할 수 있다. 예를 들어, 본 명세서에서 담체는 V1L 치환을 포함할 수 있다. 다르게 서술하면, 일 실시예에서, 콜릭스-관련 담체는 위치 "1"에서 류신 아미노산을 가진다 (위치 1은 N-말단 메티오닌을 갖지 않는 변이체의 첫 번째 아미노산 또는 N-말단 메티오닌을 포함하는 변이체의 두 번째 위치를 나타낸다. 즉, 담체의 길이를 결정할 때, N-말단 메티오닌 (존재하는 경우)은 무시된다.). 일 실시예에서, V1L 치환을 포함하는 담체는 N-말단 아미노산의 감소된 또는 제거된 절단을 경험한다. 일 실시예에서, V1L 치환을 포함하는 담체는 N-말단 아미노산의 감소된 또는 제거된 아세틸화를 경험한다. 본 명세서에 제공된 담체는 자연적으로-발생하는 콜릭스 변이체에 비해 감소된 (예를 들어, 적어도 50% 감소) 또는 제거된 ADP 리보실화 활성 (예를 들어, 신장 인자 (elongation factor) 2의 리보실화)을 가질 수 있다. 일 실시예에서, 담체는 N-말단 메티오닌을 포함할 수 있다. 다른 실시예에서, N-말단 메티오닌은 존재하지 않는다.
절단된 콜릭스 담체는 서열번호: 26에 제시된 서열의 아미노산 잔기 1-386으로 이루어지거나, 본질적으로 이루어지거나, 또는 포함할 수 있다 (FORMULA I). 절단된 콜릭스 담체는 서열번호: 26에 제시된 서열의 아미노산 잔기 1-266으로 이루어지거나, 본질적으로 이루어지거나, 또는 포함할 수 있다 (FORMULA I). 이러한 경우, 담체는 서열번호: 1에 제시된 서열의 아미노산 잔기 1-266으로 이루어지거나, 본질적으로 이루어지거나, 또는 포함할 수 있다. 따라서, 일 예에서, 담체는 서열번호: 2 (Cholix1-386의 예) 또는 서열번호: 3 (Cholix1-266의 예)에 제시된 아미노산 서열로 이루어진다. 일 예에서, 담체는 V1L 치환을 갖는 서열번호: 2로 표시되는 아미노산 서열을 가진다. 따라서, 일 예에서, 담체는 서열번호: 4 (V1L-Cholix1-386의 예) 또는 서열번호: 5 (V1L Cholix1-266의 예)에 제시된 아미노산 서열로 이루어진다. 이들 담체 중 어느 하나는 다양한 미생물 (예를 들어, 박테리아)에서 발현을 위해 이의 N-말단에서 하나 이상의 아미노산, 예를 들어, N-말단 메티오닌을 포함할 수 있다. 이러한 담체는 서열번호: 6-9에 제시된 아미노산 서열을 가질 수 있다.
콜릭스 폴리펩티드는 서열번호: 1-9 또는 서열번호: 22-23 중 어느 하나에 제시된 아미노산 서열과, 적어도 80%, 85%. 90%, 95%, 98%, 또는 99% 서열 동일성을 갖는, 또는 100% 서열 동일성을 갖는 아미노산 서열을 포함하는, 본질적으로 이루어진, 또는 이루어진 단백질일 수 있다. 콜릭스 폴리펩티드의 예는 본 명세서에서 서열번호: 1 또는 서열번호: 22로 제공된다. 또한, 편광 상피 세포 (예를 들어, 편광 장 상피 세포)를 가로질러 페이로드를 수송할 수 있는 절단된 콜릭스 폴리펩티드 변이체가 본 명세서에서 고려된다. 이러한 콜릭스 폴리펩티드는 기준 서열 (reference sequence), 예를 들어, 서열번호: 1, 서열번호: 22, 또는 서열번호: 26, 또는 이와 적어도 80%, 85%, 90%, 95%, 98% 또는 99% 서열 동일성을 갖는 아미노산 서열에 비해, 206 내지 633의 아미노산 위치 중 어느 하나에서 절단될 수 있다.
또한, 상기 서열과 높은 서열 동일성을 갖는 담체를 포함하는 전달 구조체가 본 명세서에서 고려된다. 이러한 높은 서열 동일성은 적어도 90%, 95%, 96%, 97%, 98% 또는 99% 서열 동일성을 포함할 수 있다. 따라서, 일 예에서, 담체는 서열번호: 6-9에 제시된 아미노산 서열과 적어도 90%, 95%, 96%, 97%, 98% 또는 99% 서열 동일성의 서열을 포함한다.
본 명세서에서 고려되는 담체는 페이로드, 에를 들어 이종성 페이로드에 결합될 수 있다. 치료용 페이로드는 사이토카인, 호르몬, 성장 인자, 치료용 항체, 항원, 상기 중 어느 하나의 기능적 단편, 또는 생물학적, 치료적 활성을 갖는 임의의 다른 단백질, 또는 피험자에서 결핍될 수 있는 단백질 (예를 들어, 특정 단백질의 유전적/유전된 결핍(genetic/inherited deficiency))일 수 있다. 본 명세서에서 고려되는 사이토카인은 단량체 케모카인 및 인터루킨 (본 명세서에서 "ILs"로도 약칭됨)을 포함한다. 인터루킨은 IL-22일 수 있다. 인터루킨은 임의의 종 (예를 들어, 인간 또는 설치류)로부터 유래될 수 있다. 인터루킨은 인간 인터루킨일 수 있다. 인간 IL-22는 서열번호: 10 (IL-221-179) 또는 서열번호: 11 (IL-2234-179)에 제시된 아미노산 서열을 가질 수 있다. 본 명세서에서 IL-22는 예를 들어, 이러한 IL-22 단백질이 박테리아로 발현될 때, 이의 N-말단에서 메티오닌을 더 포함할 수 있다. 일 예에서, IL-22는 서열번호: 12 (M+IL-2234-179)에 제시된 아미노산 서열을 가진다. 본 명세서에서 IL-22는 예를 들어, 이러한 IL-22 단백질이 박테리아로 발현될 때, 이의 N-말단에서 메티오닌을 더 포함할 수 있다. 일 예에서, IL-22는 서열번호: 12 (M+IL-2234-179)에 제시된 아미노산 서열을 가진다. IL-22는 서열번호: 10, 또는 이와 적어도 80%, 85%, 90%, 95%, 98% 또는 99% 서열 동일성을 갖는 아미노산 서열 또는 이의 단편을 포함하거나, 본질적으로 이루어지거나, 또는 이루어질 수 있다. IL-22는 IL-22의 분비된 형태인 서열번호: 11 (IL-2234-179), 또는 이와 적어도 80%, 85%, 90%, 95%, 98% 또는 99% 서열 동일성을 갖는 아미노산 서열 또는 이의 단편을 포함하거나, 본질적으로 이루어지거나, 또는 이루어질 수 있다. IL-22는 예를 들어, 이러한 IL-22 단백질이 박테리아로 발현될 때, 이의 N-말단에서 메티오닌을 포함할 수 있다. 이러한 IL-22 단백질은 서열번호: 12 (M+IL-2234-179)에 제시된 아미노산 서열로 이루어지거나, 본질적으로 이루어지거나, 또는 포함할 수 있다.
일 예에서, 본 명세서에서 전달 구조체 중 어느 하나에 사용되는 담체는 상피 (예를 들어, 피험자의 편광 장 상피)를 가로질러 치료용 페이로드를 수송할 수 있는 단백질 또는 다른 유형의 분자일 수 있다. 이러한 수송은 통과세포외배출을 포함할 수 있다. 본 명세서에서 언급된 바와 같이, "통과세포외배출"은 편광 상피 세포를 통한 융합 분자의 트래피킹을 나타낸다. 이러한 트래피킹은 편광 상피 세포의 기저측 막으로부터 생물학적 활성 화물의 방출을 허용한다. 통과세포외배출 과정은 상피 세포 (예를 들어, 편광 장 상피 세포) 내부뿐만 아니라 정점 및/또는 기저 표면(들) 상의 하나 이상의 수용체(들) 및/또는 단백질(들)과 담체의 상호작용(들)을 포함할 수 있다. 담체는 상피, 담체, 및/또는 페이로드의 생물학적 및/또는 치료적 기능을 손상시키지 않고 상피를 가로질러 치료용 페이로드를 수송할 수 있다.
담체는 치료용 페이로드에 공유 또는 비-공유 및 직접 또는 간접적으로 결합될 수 있다. 치료용 페이로드는 담체의 N-말단 또는 C-말단에 직접 결합될 수 있다. 담체가 페이로드에 공유 결합되는 경우, 담체는 스페이서 (본 명세서에서 링커라고도 함)를 통해 이러한 페이로드에 결합될 수 있다. 스페이서는 적어도 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 또는 그 이상의 아미노산 잔기를 포함할 수 있다. 스페이서 아미노산 잔기는 글리신, 세린, 및/또는 트립토판일 수 있다. 스페이서는 절단형 또는 비-절단형 스페이서일 수 있다. 절단형 스페이서는 효소에 의해 또는 pH-의존적 방식으로 절단될 수 있다.
본 명세서에서 고려되는 스페이서의 예는 S, (GS)x , (GGS)x , (GGGS)x (서열번호: 27), (GGGGS)x (서열번호: 28), 또는 (GGGGGS)x (서열번호: 29) (여기서, x = 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 또는 15)와 같은 올리고펩티드 서열을 포함한다. 일부 경우, 스페이서는 서열번호: 13 ((G4S)3), (GGGGSGGGGSGGGGS)에 제시된 서열로 이루어지거나, 본질적으로 이루어지거나, 또는 포함한다. 일부 경우, 스페이서는 서열번호: 31 ((G4S)5), (GGGGSGGGGSGGGGSGGGGSGGGGS)에 제시된 서열로 이루어지거나, 본질적으로 이루어지거나, 또는 포함한다. 일 예에서, 전달 구조체는 (예를 들어, 이온 상호작용, 반데르발스 상호작용, π-π 상호작용 등을 통해) 비-공유 결합된 치료용 페이로드 및 담체를 포함한다. 담체는 이의 N-말단 및/또는 C-말단에 하나 이상의 특징, 요소, 아미노산, 또는 변형을 더 포함할 수 있다. 예를 들어, 일 실시예는 담체의 N-말단에서 N-말단 메티오닌을 포함한다. 이종성 시스템에서의 발현을 위한 변형을 포함하여 다른 변형 (예를 들어, 아세틸화)도 존재할 수 있다.
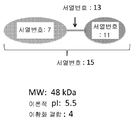
본 명세서에서 전달 구조체는 서열번호: 15 또는 17 (M+Cholix1-266-(G4S)3-IL-2234-179의 예)에 제시된 아미노산 서열을 가질 수 있다 (표 1). 다른 전달 구조체는 (예를 들어, CHO 세포와 같은 포유류 세포에서 발현될 때) 서열번호: 24 또는 25에 제시된 아미노산 서열을 가질 수 있다. 이러한 예시적인 전달 구조체는 온전한 편광 장 상피 세포를 가로질러 고유판으로 IL-22를 수송한다.
다양한 실시예에서, 비-자연적으로 발생하는 융합 단백질은 서열번호: 14-21, 24, 또는 25에 제시된 아미노산 서열, 또는 이와 적어도 80%, 85%, 90%, 95%, 98% 또는 99% 서열 동일성을 갖는 아미노산 서열을 가진다. 서열번호: 15에 제시된 아미노산 서열을 포함하는 비-자연적으로 발생하는 융합 단백질의 담체, 스페이서, 및 페이로드의 개략도는 도 16에 나타낸다.
표 1은 본 명세서에 개시된 방법과 조합하여 사용된 생물학적 활성 분자의 예시적인 아미노산 서열을 나타낸다.
[표 1]
예시적인 아미노산 서열
일 실시예에서, 비-자연적으로 발생하는 융합 단백질은 서열번호: 1-9, 22-23, 및 26에 제시된 서열 중 어느 하나로 이루어진 군으로부터 선택된 담체 및 서열번호: 10-12에 제시된 서열 중 어느 하나로 이루어진 군으로부터 선택된 페이로드를 포함하거나 또는 이루어지며, 여기서 담체 및 페이로드는 서열번호: 13 및 27-29에 제시된 서열 중 어느 하나로 이루어진 군으로부터 선택된 스페이서에 의해 임의로 결합된다.
또한, 본 발명은 전달 구조체 및 하나 이상의 약학적으로 허용가능한 담체를 포함하는 약학 조성물을 제공한다. 일부 경우, 전달 구조체는 서열번호: 15에 제시된 아미노산 서열로 이루어진다. 일부 경우, 전달 구조체는 서열번호: 17에 제시된 아미노산 서열로 이루어진다. 이러한 약학 조성물은 피험자에게 투여하기 위해 제형화될 수 있다. 일 예에서, 약학 조성물은 피험자에게 경구 투여하기 위해 제형화된다.
전달 구조체를 포함하는 약학 조성물은 질환을 치료하기 위해 이를 필요로 하는 피험자 (예를 들어, 인간)에게 투여될 수 있다. 본 발명의 전달 구조체를 이용하여 치료될 수있는 질환은 자가 면역 질환 및 염증성 질환을 포함한다. 일 예에서, 질환은 상피 세포 손상 또는 상피 세포막 (예를 들어, 위장관(GI tract))의 손상이다. 일 예에서, 질환은 간염, 비만, 지방간 질환, 간 염증 또는 췌장염, 크론병 (예를 들어, 누공성 크론병(fistulizing Crohn's disease)), 궤양성 대장염 (예를 들어, 경증에서 중등도(mild-to-moderate) 또는 중등도에서 중증(moderate-to-severe)), 주머니염, 직장염, 다발성 경화증, 전신 홍반성 루푸스, 이식편 대 숙주 질환, 류마티스 관절염 또는 건선이다.
정제 방법 및 조성물
본 발명은 정제된 비-자연적으로 발생하는 융합 단백질을 얻는 방법을 고려한다. 비-자연적으로 발생하는 융합 단백질은 IL-22 및 담체, 임의로 담체에 IL-22를 결합하는 스페이서를 포함할 수 있다. 비-자연적으로 발생하는 융합 단백질은 서열번호: 14-21, 24, 또는 25에 제시된 아미노산 서열과, 적어도 80%, 85%. 90%, 95%, 98%, 또는 99% 서열 동일성을 갖는, 또는 100% 서열 동일성을 갖는 아미노산 서열을 포함하는, 본질적으로 이루어진, 또는 이루어진 단백질일 수 있다. 본 명세서에 기재된 방법 및 조성물의 이점은 정제된 폴리펩티드 또는 단백질의 고순도 및 생물학적 활성을 유지하는 것을 포함한다.
본 명세서에 개시된 방법의 특정 이점은, a) 특별히 개발된 접힘 완충액을 이용한 올바른 접힘으로 인해 비-자연적으로 발생하는 융합 단백질의 높은 생물학적 활성; b) 낮은 독성과 쌍을 이루는 정제된 비-자연적으로 발생하는 융합 단백질의 높은 화학적 순도; c) 정제된 물질의 높은 회수율; d) 신뢰할 수 있는 생산 및 공급을 가능하게 하는 결과의 재현성; e) 임상적 및 상업적 적용을 위한 수-그램 및 수-킬로그램 규모의 제조 가능성 및 확장성; f) 임상적으로 관련된 분자에 대해 비용- 및 논리적으로 효과적인 정제 방법을 제공하는 물질과 자원의 지속가능한 용도;를 포함한다. 또한, 개선된 제조 방법은 이러한 정제된 단백질이 치료용으로 개발될 수 있는 속도를 증가시킬 수 있다 (도 22).
본 명세서에 기재된 비-자연적으로 발생하는 융합 단백질의 예시적인 정제 방법은 도 17에 나타내며, 이는 정제 방법의 각 단계에서 비-자연적으로 발생하는 융합 단백질에 대한 예시적인 순도 및 회수량을 더 나타낸다.
본 명세서에 사용된 바와 같이, "순도"는 바람직하지 않은 단백질 또는 바람직하지 않은 형태의 단백질 (예를 들어, 비-자연적으로 발생하는 융합 단백질의 응집체, 올바르지 않게(incorrectly) 접힌 단백질 또는 이들의 조합)을 포함할 수도 있는 조성물에서 바람직한 단백질 (예를 들어, 비-자연적으로 발생하는 융합 단백질) 또는 바람직한 형태의 단백질 (예를 들어, 비-자연적으로 발생하는 융합 단백질의 단량체, 올바르게 접힌 비-자연적으로 발생하는 융합 단백질, 또는 이들의 조합)의 수준을 나타낸다. 수준은 바람직한 단백질 또는 바람직한 형태의 단백질의 백분율 (%)로 나타낼 수 있다. 예를 들어, 순도는 40%, 50%, 60%, 70%, 80%, 90%, 95%, 또는 99% 이상일 수 있거나, 또는 100% 일 수 있다. 용어 "정제된"은 순도가 증가한 조성물을 나타내기 위해 사용될 수 있다. 순도의 증가는 본 명세서에 기재된 정제 과정, 예를 들어, 음이온 교환 크로마토그래피, 히드록시아파타이트 크로마토그래피, 양이온 교환 크로마토그래피, 또는 이들의 조합으로 인한 것일 수 있다.
일부 경우, 본 발명의 방법 및 조성물은 동시에 수행되는 적어도 2개의 크로마토그래피 컬럼의 사용에 이어 농축/완충액 교환 단계 (용액을 농축하고 완충액 교환을 위한 한외여과(ultrafiltration)/투석여과(diafiltration) (UF/DF))를 포함한다. 크로마토그래피 컬럼은 AKTA Avant 150 컬럼 또는 General Electric (GE)의 AKTA Pilot 컬럼과 같은 저압 크로마토그래피 시스템일 수 있다. 일부 경우, 적어도 하나의 컬럼은 음이온 교환 수지 (예를 들어, NH2-750F 수지)을 함유하고, 적어도 하나의 컬럼은 히드록시아파타이트 수지 (예를 들어, CaPure® 수지)를 함유한다. 일부 경우, 음이온 교환 수지를 함유하는 적어도 하나의 컬럼은 포획 단계에 사용되는 반면, 히드록시아파타이트 수지를 함유하는 적어도 하나의 컬럼은 연마 단계에 사용된다. 일부 경우, 히드록시아파타이트 컬럼 대신 (또는 이외에), 양이온 교환 컬럼이 사용될 수 있다. 예를 들어, 일 실시예에서, 양이온 교환 컬럼은 설페이트-작용화된 폴리메타크릴레이트 수지, 예를 들어 TOYOPEARL 설페이트-650F와 함께 사용된다. 가용화된 단백질의 순도는 UF/DF 후 44%에서 47%로, 음이온 교환 크로마토그래피 후 93%에서 97%로, 히드록시아파타이트 크로마토그래피 후 적어도 99%로 증가할 수 있다. 가용화된 단백질의 회수율은 음이온 교환 크로마토그래피 후 70%에서 73%로, 히드록시아파타이트 크로마토그래피 후 적어도 97%로 증가할 수 있다.
봉입체로부터 비-자연적으로 발생하는 융합 단백질의 분리
일 실시예에서, 정제될 비-자연적으로 발생하는 융합 단백질은 봉입체 (IBs)로부터 분리된다. 본 명세서에 기재된 IBs는 단백질 및 폴리펩티드와 같은 안정된 물질의 핵 또는 세포질 응집체일 수 있다. 일 실시예에서, 발효로부터 비-자연적으로 발생하는 융합 단백질 (예를 들어, 서열번호: 14-21)을 포함하는 이중-세척 봉입체 (double-washed inclusion bodies, DWIB)는 특정 완충 시스템에 재현탁된다 (실시예 6 참조).
일부 경우, DWIB의 농도는 약 0.5 g DWIB/100mL 완충액 내지 약 5 g DWIB/10mL 완충액이다. 일부 경우, DWIB의 농도는 약 2 g DWIB/50mL 완충액 내지 약 5 g DWIB/50mL 완충액이다. 일부 경우, DWIB의 농도는 약 1 g DWIB/20mL 완충액 내지 약 1 g DWIB/10mL 완충액이다. 일부 경우, DWIB의 농도는 적어도 1 g DWIB/100mL 완충액이다. 일부 경우, DWIB의 농도는 적어도 1 g DWIB/10mL 완충액이다.
재현탁용 완충 시스템은 다양한 완충제 및 성분을 포함할 수 있다. 일부 경우, 재현탁용 완충 시스템은 적어도 1M, 적어도 2M, 적어도 4M, 적어도 6M, 적어도 8M의 농도의 구아니딘/HCl (Gu-HCl)을 포함한다. 일부 경우, Gu-HCl의 농도는 약 4 M 내지 약 8 M 이다. 일부 경우, 재현탁용 완충 시스템은 Tris 완충액을 포함하고, 여기서 Tris의 농도는 적어도 50 mM, 적어도 10 mM, 적어도 20 mM, 적어도 50 mM, 또는 적어도 100 mM이다. 일부 경우, Tris 완충액은 약 40 mM 내지 약 60 mM의 농도를 가진다. Tris 완충액은 Tris-HCl일 수 있다. Tris-HCl은 8.0 내지 8.5의 pH를 가질 수 있다. Tris-HCl은 8.2의 pH를 가질 수 있다. 일부 경우, 재현탁용 완충 시스템은 디티오트레이톨 (dithiothreitol, DTT)을 포함한다. DTT는 적어도 7 mM, 8 mM, 9 mM, 10 mM, 20 mM, 30 mM, 40 mM, 50 mM, 60 mM, 또는 70 mM의 농도를 가질 수 있다. DTT는 7 mM 내지 11 mM, 8 mM 내지 10 mM, 또는 9 mM 내지 10 mM의 농도를 가질 수 있다. 일부 경우, 재현탁용 완충 시스템은 에틸렌디아민테트라아세트산 (EDTA)을 포함한다. EDTA는 적어도 1 mM, 1.5 mM, 2 mM, 또는 2.5 mM의 농도를 가질 수 있다. EDTA는 1 mM 내지 2.5 mM 또는 1.9 mM 내지 2.1 mM의 농도를 가질 수 있다. 일 실시예에서, 재현탁용 완충 시스템은 Tris 완충액, Gu-HCl, 및 DTT를 포함하거나, 본질적으로 이루어지거나, 또는 이루어진다. 재현탁에 사용되는 완충 시스템은 약 6 내지 약 10의 pH를 가질 수 있다. 일부 경우, 완충 시스템은 약 7.5 내지 약 8.5의 pH를 가진다. 일부 경우, 완충 시스템의 pH는 적어도 7이다. 일부 경우, 완충 시스템의 pH는 적어도 8이다. 일부 경우, 완충 시스템의 pH는 적어도 8.5이다.
가용화된 비-자연적으로 발생하는 융합 단백질의 환원
환원제를 재현탁 용액에 첨가할 수 있다. 환원제는 디티오트레이톨 (DTT)일 수 있다. 사용된 환원제의 양은 재현탁 용액의 부피와 그 용액에 존재하는 융합 단백질에 따라 달라질 수 있다. 일부 경우, 사용된 환원제의 양은 약 0.025 mM 내지 약 50 mM, 0.5 mM 내지 30 mM, 1mM 내지 10 mM 이다. 일부 경우, 사용된 환원제의 양은 적어도 (또는 그 사이) 2 mM, 3 mM, 4 mM, 5 mM, 6 mM, 7 mM, 8 mM, 9 mM, 또는 10 mM 이다.
가용화된 비-자연적으로 발생하는 융합 단백질 (예를 들어, 서열번호: 14-21) 용액은 약 2℃ 내지 약 40℃ 범위의 다양한 온도에서 배양될 수 있다. 일부 경우, 단백질 용액은 실온 (RT)에서 배양될 수 있다. 용액을 교반하면서 배양을 수행할 수 있다. 용액을 자석 교반-플레이트(magnetic stir-plate)에서 교반한 다음, 원심분리할 수 있다. 약 1,000 xg 내지 약 20,000 xg에서 원심분리를 수행할 수 있다. 일부 경우, 4℃에서 90분 동안 15,970 xg에서 원심분리를 수행할 수 있다. 배양 시간은 성분의 농도, 융합 단백질 (예를 들어, 서열번호: 14-21)의 농도에 따라 약 20분에서 약 180분까지 다양할 수 있다.
본 명세서에 기재된 방법 및 과정을 통해 다양한 용액에서 단백질 농도는 브래드포드 분석(Bradford assay)을 이용하여 수행될 수 있다. 가용화된 비-자연적으로 발생하는 융합 단백질의 농도는 약 1 mg/mL 내지 약 50 mg/mL 일 수 있다. 일부 경우, 가용화된 비-자연적으로 발생하는 융합 단백질의 최종 농도는 약 3 mg/mL 내지 약 30 mg/mL 일 수 있다. 일부 경우, 가용화된 비-자연적으로 발생하는 융합 단백질의 최종 농도는 약 5 mg/mL 내지 약 20 mg/mL 일 수 있다. 일부 경우, 가용화된 비-자연적으로 발생하는 융합 단백질의 최종 농도는 적어도 15 mg/mL 일 수 있다.
비-자연적으로 발생하는 융합 단백질의 재접힘
본 발명의 비-자연적으로 발생하는 융합 단백질은 이들의 특이적인 3-차원 구조 또는 접힘으로 인해 이들의 생물학적 활성을 발휘할 수 있다. 따라서, 이러한 폴리펩티드의 재접힘은 약학 적용을 위해 이러한 폴리펩티드를 개발하는데 중요할 수 있다. 적어도 하나의 담체 및 IL-22를 포함하는 융합 단백질의 바람직한 재접힘은 상동성 자연적으로 발생하는 담체 또는 IL-22 서열의 3차 구조 또는 담체의 바람직한 활성 (예를 들어, 융합 단백질의 통과세포외배출) 및 IL-22의 유지를 야기하는 3차 구조와 유사한 3차 구조로 담체 또는 IL-22의 재접힘을 포함할 수 있다. 본 명세서에 기재된 방법은 가용화된 비-자연적으로 발생하는 융합 단백질을 재접힘하여 재접힌 비-자연적으로 발생하는 융합 단백질을 제조하는 단계를 포함할 수 있다. 재접힘은 음이온 교환 크로마토그래피를 수행하기 전에 발생할 수 있다.
가용화된 단백질 (예를 들어, 서열번호: 14-21)을 재접힘 용액 (재접힘 완충 용액이라고도 함)에 첨가할 수 있다. 사용된 가용화된 단백질의 양은 0.1 mg/mL 내지 1 mg/mL, 1 mg/mL 내지 100 mg/mL, 1 mg/mL 내지 50 mg/mL, 1 mg/mL 내지 10 mg/mL, 5 mg/mL 내지 20 mg/mL, 또는 약 15 mg/mL 일 수 있다. 가용화된 단백질의 양은 적어도 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10 mg/mL 일 수 있다. 가용화된 단백질의 양은 0.1, 0.5, 1, 5, 10, 20, 30, 40, 50, 60, 70, 80, 90, 또는 100 mg/mL 이하일 수 있다. 재접힘 용액은 7.5 내지 8.5, 또는 약 7.0의 pH를 가질 수 있다.
재접힘 완충 용액은 아미노산, 폴리올, 염, 당, 산화환원 시약, 카오트로프, 또는 이들의 조합을 포함할 수 있다. 아미노산은 프롤린, 글리신, 아르기닌, 또는 알라닌일 수 있다. 폴리올은 글리세롤일 수 있다. 염은 염화나트륨 (NaCl), 염화칼륨 (KCl), 또는 염화마그네슘 (MgCl2)일 수 있다. 당은 글루코오스 또는 수크로오스일 수 있다. 산화환원 시약은 시스테인, 시스타민, 글루타티온, 디티오트레이톨 (DTT) 또는 황산구리 (CuSO4)일 수 있다. 일 실시예에서, 재접힘 완충 용액은 Tris-염기, 아르기닌-HCl, 우레아, EDTA, 글리세롤, L-시스테인, 시스타민-2HCl, DTT, Gu-HCl, 또는 이들의 조합을 포함한다. 일 실시예에서, 재접힘 완충액은 Tris pH 8.5, 아르기닌, 글리세롤, 시스테인 및 시스타민을 포함하거나, 본질적으로 이루어지거나, 또는 이루어진다. Tris 완충액의 농도는 약 6 내지 약 9의 범위의 pH를 갖는 약 20 mM 내지 약 200 mM의 범위일 수 있다. 아르기닌-HCl의 농도는 약 0.1 M 내지 약 1.5 M, 약 0.75 M 내지 1.25M, 또는 약 1.0 M의 범위일 수 있다. 우레아의 농도는 약 0.5 M 내지 1.5 M의 범위일 수 있다. EDTA의 농도는 1 mM 내지 3 mM의 범위일 수 있다. 글리세롤의 농도는 약 2 % v/v 내지 약 20 % v/v, 약 8% v/v 내지 약 12% v/v, 또는 약 10% v/v의 범위일 수 있다. 시스테인의 농도는 1 mM 내지 5 mM, 2 mM 내지 4 mM, 또는 약 3 mM 일 수 있다. 시스테인은 L-시스테인일 수 있다. 시스타민의 농도는 약 0.5 mM 내지 약 5 mM, 약 1 mM 내지 약 4 mM, 또는 약 3 mM의 범위일 수 있다. 시스타민은 시스타민-2HCl일 수 있다. DTT의 농도는 약 0.1 mM 내지 약 1 mM의 범위일 수 있다. Gu-HCl의 농도는 약 50 mM 내지 약 500 mM의 범위일 수 있다. 재접힘 완충액은 Tris, L-아르기닌, 우레아, EDTA, 시스테인, 및 시스타민을 포함하거나, 본질적으로 이루어지거나, 또는 이루어질 수 있다. 재접힘 완충액은 100 mM Tris pH 8.5, 1M 아르기닌, 10% (v/v) 글리세롤, 3 mM L-시스테인, 및 1 mM 시스타민-2HCl을 포함하거나, 본질적으로 이루어지거나, 또는 이루어질 수 있다. 가용화된 비-자연적으로 발생하는 융합 단백질을 재접힘 완충액에 첨가하여 재접힘 혼합물을 제조할 수 있다. 재접힘 혼합물에 첨가한 후, 비-자연적으로 발생하는 융합 단백질의 농도는 약 0.1 mg/mL 내지 1.0 mg/mL, 0.5/mL mg 내지 1.5 mg/mL, 0.75 mg/mL 내지 1.25 mg/mL, 또는 약 1 mg/mL 일 수 있다. 재접힘 혼합물에서 비-자연적으로 발생하는 융합 단백질의 농도는 0.5 mg/mL, 0.6 mg/mL, 0.7 mg/mL, 0.8 mg/mL, 0.9 mg/mL 또는 1.0 mg/mL 미만일 수 있다.
다양한 실시예에서, 약 100 mL 내지 약 10,000 L 재접힘 완충액의 부피가 사용된다. 일부 경우, 부피는 약 50 mL 내지 약 1500 L 이다. 일부 경우, 부피는 약 10 L 내지 약 300 L 이다. 일부 경우, 부피는 적어도 200 L 이다.
재접힘 용액은 특정 온도를 가질 수 있다. 예를 들어, 재접힘 용액은 약 2-12℃로 미리-냉각될 수 있다. 일부 경우, 재접힘 용액은 적어도 약 3℃로 미리-냉각된다. 이러한 재접힘 과정은 사용된 단백질 및 적용에 따라 최적화될 수 있다 (도 18).
본 발명의 일 실시예에서, 재접힘 혼합물은 일정 기간 동안 배양된다. 일부 경우, 과정은 약 1시간, 2시간, 4시간, 5시간 또는 20시간일 수 있다. 일부 경우, 재접힘 과정은 약 15 내지 약 25시간이 걸린다. 일부 경우, 연동 펌프(peristaltic pump)를 용액의 구성 (예를 들어, 농도 또는 부피)에 따라 일정한 유속으로 설정하여 가용화된 물질을 재접힘 용액으로 전달한다. 일부 경우, 연동 펌프를 60-80 ml/min의 유속으로 설정한다. 최적화 과정은 15개의 상이한 매트릭스, 12개의 변수 및 200개의 재접힘 반응의 실험 계획법(design of experiments, DOE)을 이용하였다. 제거 과정에 의해 결정을 내렸다.
다양한 실시예에서, 정량 분석을 수행하여 재접힌 비-자연적으로 발생하는 융합 단백질을 포함하는 용액에서 올바르게 접힌 단백질의 양 또는 백분율을 결정할 수 있다. 일부 경우, SEC-HPLC를 수행하여 재접힘 시료에 존재하는 적당히 접힌 비-자연적으로 발생하는 융합 단백질의 양을 결정한다.
재접힌 비-자연적으로 발생하는 융합 단백질의 순도는 45% 내지 65%, 40% 내지 60%, 또는 45% 내지 55% 일 수 있다. 재접힌 비-자연적으로 발생하는 융합 단백질의 순도는 적어도 40%, 45%, 50%, 또는 55% 일 수 있다.
가용화된 IL-22 전달 구조체의 접선 유동 여과 (Tangential flow filtration, TFF)
다양한 실시예에서, 단백질 재접힘은 특정 분자량 컷오프 (MWCOs)와 함께 접선 유동 여과 (TFF) 시스템 (예를 들어, 미공(Millipore)) 및 한외여과/투석여과 (UF/DF) 시스템과 조합하여 또는 이전에 수행된다.
단백질 재접힘 혼합물은 이후에 TFF에 의해 처리되어 용액을 농축하고 완충액을 교환할 수 있다. 일부 경우, 과정은 한외여과/투석여과 (UF/DF)에 의해 수행된다. 한외여과 동안, 용액은 8배 내지 12배, 또는 약 10배로 농축될 수 있다. 한외여과 후 투석여과 완충액으로 투석여과 동안 5배 완충액 교환이 가능하다. UF/DF는 1-2 m2 TFF 평평한 시트 카세트가 있는, 10-20 kDa MWCO Millipore Ultracell Pellican3 여과기의 사용을 포함할 수 있다. 특정 매개변수 (즉, TMP)는 단백질의 분자 특성에 따라 달라질 수 있다. 투석여과 완충액은 약 7 내지 약 8.5의 pH에서 10-25 mM Tris-염기, 및 50-200 mM NaCl을 포함할 수 있다. 특정 매개변수는 단백질의 분자 특성에 따라 달라질 수 있다. UF/DF 과정의 종료시 최종 부피는 약 5 L 내지 약 100 L 일 수 있다. 일부 경우, 최종 부피는 약 10 L 내지 약 50 L의 범위이다. 일부 경우, 최종 부피는 약 80 mL 내지 약 10 L의 범위이다.
유동 여과 시스템을 이용하여 후속 여과를 수행할 수 있다. 일부 경우, 유동 여과 시스템은 AkroPac 여과기 시스템, 및 Cole-Parmer 연동 펌프 및 배관(tubing)이다. 브래드포드 분석을 수행하여 단백질 농도, 수율, 및 단계 회수를 결정할 수 있다.
다양한 실시에에서, 정량 분석을 수행하여 시료 용액에서 올바르게 접힌 단백질의 양 또는 백분율을 결정할 수 있다. 일부 경우, SEC-HPLC를 수행하여 재접힘 UF/DF 시료에 존재하는 적당히 접힌 비-자연적으로 발생하는 융합 단백질의 양을 결정한다.
UF/DF 후 재접힌 비-자연적으로 발생하는 융합 단백질을 포함하는 용액의 순도는 35% 내지 55%, 40% 내지 50%, 또는 43% 내지 47%, 또는 약 45% 일 수 있다. UF/DF 후 재접힌 비-자연적으로 발생하는 융합 단백질을 포함하는 용액의 순도는 적어도 35%, 40%, 또는 45% 일 수 있다. UF/DF 후 가용화된 재접힌 비-자연적으로 발생하는 융합 단백질의 회수율은 87% 내지 97%, 90% 내지 94%, 92% 내지 93%, 또는 약 92.5% 일 수 있다. (기타 농도 및 완충액 교환 시스템도 사용될 수 있다.)
비-자연적으로 발생하는 융합 단백질의 정제 및 회수
앞에 기재된 바와 같이, 동시에 2개의 크로마토그래피 방법, 예를 들어 음이온 교환 크로마토그래피 및 히드록시아파타이트 크로마토그래피 (또는 대안적으로 양이온 교환 크로마토그래피)의 사용은, 용액으로부터 비-자연적으로 발생하는 융합 단백질, 예를 들어 본 명세서에 기재된 IL-22 전달 구조체의 증가된 순도 및 회수를 야기할 수 있다. 본 발명의 다양한 실시예에서, 크로마토그래피 특성 (예를 들어, 컬럼 유형, 수지, 유속, 완충 시스템, 구배, 및 전도도)은 다양한 매개변수 (예를 들어, 정제될 단백질)에 따라 결정되고 최적화된다. 다양한 정제 컬럼이 본 명세서에 기재된 단백질 정제에 사용될 수 있다.
음이온 교환 크로마토그래피
본 명세서에 기재된 방법은 비-자연적으로 발생하는 융합 단백질을 포함하는 혼합물에 대해 음이온 교환 크로마토그래피 (AEX)를 수행하는 단계를 포함할 수 있다. 혼합물은 재접힌 비-자연적으로 발생하는 융합 단백질을 포함하는 용액일 수 있다. 음이온 교환 크로마토그래피를 수행하는 단계는 비-자연적으로 발생하는 융합 단백질을 포함하는 제 1 분획을 제조할 수 있다.
다양한 수지는 본 발명의 방법 및 조성물과 조합하여 사용될 수 있다. 일부 경우, 수지는 아민-작용화된 폴리메틸아크릴레이트 비드를 포함한다. 일부 경우, 음이온 교환 수지 NH2-750F는 단백질 정제에 사용된다. 적어도 15 cm, 20 cm, 25 cm, 또는 30 cm의 층 높이를 갖는 컬럼은 수지로 충전될 수 있다. 10 내지 50 cm의 층 높이를 갖는 컬럼은 적당한 동적 결합 용량(dynamic binding capacity) (예를 들어, >20 g/L)을 촉진시켜 바람직한 양의 단백질의 제조를 가능하게 하는 컬럼 부피를 보장하는 방식으로 수지로 충전될 수 있다. 일부 경우, 컬럼의 동적 결합 용량은 5 g/L 내지 100 g/L, 20 g/L 내지 약 50 g/L, 15 g/L 내지 30 g/L, 또는 20 g/L 내지 25 g/L 이다.
음이온 교환 크로마토그래피에서 용리 (예를 들어, 구배 용리)에 사용되는 완충 시스템은 1개, 2개, 3개 또는 4개의 상이한 완충 용액 (예를 들어, 완충액 A 내지 D)을 포함할 수 있다. 일 실시예에서, 2개의 완충액은 음이온 교환 크로마토그래피에서 사용되며, 본 명세서에서 완충액 A 및 완충액 B라고 한다. 일부 경우, 완충 용액은 Tris (예를 들어, 10-50 mM, pH 7-9), 및/또는 NaCl (예를 들어, 0.1-5 M)을 포함한다. 일부 경우, 완충 용액은 글리세롤을 더 포함한다. 일 실시예에서, 예를 들어 완충액 A 및 완충액 B와 같은 음이온 교환 크로마토그래피에서 사용되는 완충 용액(들)은 Tris pH 7.5 및 NaCl, 및 임의로, 글리세롤을 포함하거나, 본질적으로 이루어지거나, 또는 이루어진다.
완충액 A는 10 mM 내지 30 mM, 15 mM 내지 25 mM, 19 mM 내지 21 mM, 또는 약 20 mM Tris pH 7.5를 포함할 수 있다. 완충액 A는 0.25 M 내지 0.95 M, 0.35 M 내지 0.75M, 0.45 M 내지 0.55 M, 약 0.5 M, 0.65 M 내지 0.75 M, 또는 약 0.7 M NaCl을 포함할 수 있다. 완충액 B는 10 mM 내지 30 mM, 15 mM 내지 25 mM, 19 mM 내지 21 mM, 또는 약 20 mM Tris pH 7.5를 포함할 수 있다. 완충액 B는 1 M 내지 3 M, 1.5 M 내지 2.5 M, 1.9 M 내지 2.1 M, 또는 약 2 M NaCl을 포함할 수 있다. 완충액 A는 8% 내지 12%, 9% 내지 11%, 또는 약 10% (v/v) 글리세롤을 더 포함할 수 있다. 완충액 B는 8% 내지 12%, 9% 내지 11%, 또는 약 10% (v/v) 글리세롤을 더 포함할 수 있다.
서열번호: 15의 음이온 교환 크로마토그래피의 경우, 완충액 A는 20 mM Tris pH 7.5 및 0.5 M NaCl을 포함할 수 있으며, 완충액 B는 20 mM Tris pH 7.5 및 2.0 M NaCl을 포함할 수 있다 (표 4). 서열번호: 17의 음이온 교환 크로마토그래피의 경우, 완충액 A는 20 mM Tris pH 7.5 및 0.5 M NaCl을 포함할 수 있으며, 완충액 B는 20 mM Tris pH 7.5 및 2.0 M NaCl을 포함할 수 있다. 서열번호: 14의 음이온 교환 크로마토그래피의 경우, 완충액 A는 20 mM Tris pH 7.5, 0.7 M NaCl, 및 10% (v/v) 글리세롤을 포함할 수 있으며, 완충액 B는 20 mM Tris pH 7.5, 2.0 M NaCl, 및 10% (v/v) 글리세롤을 포함할 수 있다 (표 5).
일 실시예에서, 특정 부피의 염 용액이 단백질 용액에 첨가된다. 일부 경우, 약 0.1 내지 약 5 M 범위의 농도를 갖는 NaCl 용액이 단백질 용액에 첨가된다.
특정 유속 및 특정 컬럼 체류 시간(residence time)을 관찰하여 단백질 및 고체상 (예를 들어, 수지)의 적당한 상호작용을 보장할 수 있도록 단백질 용액을 컬럼에 로딩할 수 있다. 일부 경우, 컬럼 체류 시간이 약 30초 내지 약 6분, 또는 약 5분이 되도록 유속을 조절한다. 컬럼 체류 시간은 적어도 30초, 또는 1, 2, 3, 4, 또는 5분일 수 있다. 컬럼 체류 시간은 3, 4, 5, 6, 7, 8, 9, 또는 10분 이하일 수 있다. 관류(flow-through)를 수집하고 분석하여 손실로 간주되는 결합되지 않은 단백질이 있는지 확인할 수 있다. 단백질 분석 및 정제를 위해, 약 280 nm에서의 흡광도는 단백질 농도에 대해 결정되고 SEC-HPLC는 단백질 순도에 대해 결정된다.
일 실시예에서, 제 1 완충액의 백분율 (예를 들어, 0-100%) 또는 유속 (예를 들어, 1-10 mL/min)을 제 2 완충액과 조합하여 컬럼 정제 시스템의 특정 최종 유속 (예를 들어, 1-10 mL/min)을 달성한다. 예를 들어, 단백질 정제를 위해 0.0-62.5% B (100-37.5% A)에서 20 컬럼 부피 (CV)의 선형 구배, 이어서 추가 5 CV에 대해 100% B (0% A)로 단계 구배가 수행된다. 일부 경우, 0-75% B (100-25% A) 40 CV, 단계 100% B, 10 CV의 구배는 91-93% 순수한 단백질 및 >90%의 회수율을 나타내는 용리 구배로 수행될 수 있다.
제 1 분획에서 비-자연적으로 발생하는 융합 단백질의 순도는 90% 내지 99% 또는 91% 내지 95% 일 수 있다. 제 1 분획에서 가용화된 비-자연적으로 발생하는 융합 단백질의 순도는 적어도 90%, 91%, 92%, 93%, 94%, 또는 95% 일 수 있다. 제 1 분획에서 가용화된 비-자연적으로 발생하는 융합 단백질의 회수율은 61% 내지 81%, 66% 내지 76%, 또는 71% 내지 72% 일 수 있다.
양이온 교환 크로마토그래피 또는 히드록시아파타이트 크로마토그래피
본 명세서에 기재된 방법은 음이온 교환 크로마토그래피 후에 얻어진 제 1 분획을 양이온 교환 수지로 처리하여 비-자연적으로 발생하는 융합 단백질을 포함하는 제 2 분획을 얻는 단계를 더 포함할 수 있다. 양이온 교환 수지는 설페이트-작용화된 메타크릴레이트 수지일 수 있다. 양이온 교환 수지는 TOYOPEARL® 설페이트-650F 수지일 수 있다.
본 명세서에 기재된 방법은 추가적으로 또는 대안적으로 음이온 교환 크로마토그래피 후에 얻어진 제 1 분획을 히드록시아파타이트 수지로 처리하여 비-자연적으로 발생하는 융합 단백질을 포함하는 제 2 분획을 얻는 단계를 포함할 수 있다. 히드록시아파타이트 수지는 칼슘 친화도를 더 포함하는 양이온 교환 수지일 수 있다. 히드록시아파타이트 수지는 칼슘 포스페이트를 포함할 수 있다. 히드록시아파타이트 수지는 화학식 Ca10(PO4)6(OH)2를 포함할 수 있다. 히드록시아파타이트 수지는 30 μm 내지 50 μm, 35 μm 내지 45 μm, 또는 약 39 μm의 입자 크기를 포함할 수 있다. 히드록시아파타이트 수지는 CaPure® 수지일 수 있다.
CaPure® 수지의 이점은 a) 수용액에서 높은 전도도로 단백질 흡착을 허용하는, 염 내성(salt tolerance); b) 로딩 전에 단백질 (예를 들어, 서열번호: 14-21과 같은 융합 단백질)의 제조가 필요하지 않음; c) 높은 회수율 (>90%)의 야기; d) 높은 결합 용량(binding capacity) (>20 mg/mL 수지); e) 저분자량 (LMW) 불순물의 제거에 의한 순도 증가; 및 f) 내독소 제거 보장 (<1.0 EU/mg)을 포함한다.
양이온 교환 수지 또는 히드록시아파타이트 수지는 크로마토그래피 컬럼을 채우는데 사용될 수 있다. 컬럼은 10 cm 내지 50 cm, 또는 약 20 cm의 층 높이를 포함할 수 있다. 컬럼은 적어도 10 cm, 15 cm, 20 cm, 25 cm, 또는 30 cm의 층 높이를 포함할 수 있다. 컬럼은 20 cm, 30 cm, 40 cm, 또는 50 cm 이하의 층 높이를 포함할 수 있다. 일부 경우, 히드록시아파타이트 혼합-모드 수지 CaPure®는 10-50 cm의 층 높이를 갖는 컬럼을 채우는데 사용되며, 이는 최대 10-100 g/L의 동적 결합 용량을 촉진시켜 바람직한 양의 단백질의 제조를 가능하게 하는 컬럼 부피를 보장한다.
히드록시아파타이트 크로마토그래피에서 용리 (예를 들어, 구배 용리)에 사용되는 완충 시스템은 1개, 2개, 3개 또는 4개의 상이한 완충 용액 (예를 들어, 완충액 A 내지 D)을 포함할 수 있다. 일 실시예에서, 2개의 완충액은 히드록시아파타이트 크로마토그래피에서 사용되며, 본 명세서에서 완충액 A 및 완충액 B라고 한다. 일부 경우, 완충 용액은 Tris (예를 들어, 10-50 mM, pH 7-9), 및/또는 NaCl (예를 들어, 0.1-5 M)을 포함한다. 일부 경우, 완충 용액은 글리세롤을 더 포함한다. 일 실시예에서, 예를 들어 완충액 A와 같은 히드록시아파타이트 크로마토그래피에서 사용되는 제 1 완충 용액은 Tris pH 7.5, NaCl, 및 CaCl2를 포함하거나, 본질적으로 이루어지거나, 또는 이루어진다. 일 실시예에서, 예를 들어 완충액 B와 같은 히드록시아파타이트 크로마토그래피에서 사용되는 제 2 완충 용액은 소듐 포스페이트 pH 7.0, NaCl, 및 CaCl2를 포함하거나, 본질적으로 이루어지거나, 또는 이루어진다.
완충액 A는 10 mM 내지 30 mM, 15 mM 내지 25 mM, 19 mM 내지 21 mM, 또는 약 20 mM Tris pH 7.5를 포함할 수 있다. 완충액 A는 80 mM 내지 120 mM, 90 mM 내지 110 mM, 또는 약 100 mM NaCl을 포함할 수 있다. 완충액 A는 0.5 mM 내지 1.5 mM, 0.75 mM 내지 1.25 mM, 0.9 mM 내지 1.1 mM, 또는 약 1 mM의 CaCl2를 포함할 수 있다. 완충액 B는 150 mM 내지 250 mM, 175 mM 내지 225 mM, 190 mM 내지 210 mM, 또는 약 200 mM 소듐 포스페이트 pH 7.0을 포함할 수 있다. 완충액 B는 50 mM 내지 150 mM, 75 mM 내지 125 mM, 90 mM 내지 110 mM, 또는 약 100 mM NaCl을 포함할 수 있다. 완충액 B는 0.5 mM 내지 1.5 mM, 0.75 mM 내지 1.25 mM, 0.9 mM 내지 1.1 mM, 또는 약 1 mM의 CaCl2를 포함할 수 있다.
서열번호: 15의 히드록시아파타이트 크로마토그래피의 경우, 완충액 A는 20 mM Tris pH 7.5, 100 mM NaCl, 및 1 mM CaCl2를 포함할 수 있으며, 완충액 B는 200 mM 소듐 포스페이트 pH 7.0, 100 mM NaCl, 및 1 mM CaCl2를 포함할 수 있다 (표 6). 서열번호: 17의 히드록시아파타이트 크로마토그래피의 경우, 완충액 A는 20 mM Tris pH 7.5, 100 mM NaCl, 및 1 mM CaCl2를 포함할 수 있으며, 완충액 B는 200 mM 소듐 포스페이트 pH 7.0, 100 mM NaCl, 및 1 mM CaCl2를 포함할 수 있다. 서열번호: 14의 히드록시아파타이트 크로마토그래피의 경우, 완충액 A는 20 mM Tris pH 7.5, 100 mM NaCl, 및 1 mM CaCl2을 포함할 수 있으며, 완충액 B는 200 mM 소듐 포스페이트 pH 7.0, 100 mM NaCl, 및 1 mM CaCl2를 포함할 수 있다 (표 7).
양이온 교환 수지 또는 히드록시아파타이트 수지의 사용 후 가용화된 단백질의 순도는 99% 내지 100% 일 수 있다. 히드록시아파타이트 수지의 사용 후 가용화된 단백질의 순도는 적어도 95%, 96%, 97%, 98%, 99%, 또는 100% 일 수 있다. 히드록시아파타이트 수지의 사용 후 가용화된 단백질의 회수율은 85% 내지 100%, 96% 내지 99%, 또는 97% 내지 98% 일 수 있다. 히드록시아파타이트 수지는 CaPure® 일 수 있다.
정제된 화합물 (예를 들어, 융합 단백질)을 함유하는 컬럼 크로마토그래피 동안 수집된 분획은 투여하기 위해 완충액 교환 또는 투석여과를 이용하여 농축 및 제형화될 수 있다. 예를 들어, CaPure® 동안 수집된 분획은 TFF 시스템 (예를 들어, Pall Corporation)을 이용하여 농축 및 제형화하여 단백질을 농축시킬 수 있다. 단백질은 20 mg/mL의 최종 농도로 농축된 다음, 5배 완충액 교환이 가능하다. 한외여과/투석여과 (UF/DF) 및 10 kDa MWCO Millipore Pellican3, 0.114 m2 TFF 평평한 시트 카세트가 있는 여과기를 이용하여, 여과 과정을 수행할 수 있다. 여과 시스템의 MWCO는 정제될 단백질 (예를 들어, 분자량)에 따라 달라질 수 있다. 투석여과 완충액은 약 pH 7.0에서 10-20 mM 소듐 포스페이트, 50-100 mM NaCl로 이루어질 수 있다. 이후 AkroPac 여과기 및 Cole-Parmer 연동 펌프 및 배관을 사용하는 유동 여과 시스템을 이용하여 제형화된 서열번호: 14-21을 여과할 수 있다. 정제되고 제형화된 단백질은 추가로 사용할 때까지 -80℃에서 분취량으로 저장될 수 있다.
특정 실시예에서, SEC-HPLC에 의해 분석된 단백질은 TSKgel GW3000SWXL, 5μm, 7.8 mm ID x 30.0 cm L 컬럼 (Tosoh Bioscience, 8541)을 이용하여 97% 이상의 순도 (일반적으로 >98%)를 나타낼 수 있다.
단백질 분석
Bio-Rad ChemiDoc™ MP 영상 시스템을 이용한 SDS-PAGE로 상이한 분획의 시료를 분석할 수 있으며, 컬럼 크로마토그래피 동안 수집된 분획은 Thermo Fisher Nanodrop One™을 이용하여 단백질 함량을 분석할 수 있다. 단백질 검출 또는 분석을 위한 일반적인 기법은 겔 전기영동, 형광 현미경, 모세관 전기영동, 질량 분석법, 전기영동 이동성-변화 분석(electrophoretic mobility-shift assay), 또는 핵 자기 공명을 포함한다.
치료 방법
본 발명의 다양한 실시예에서, 본 발명의 융합 분자를 포함하는 약학 조성물은 염증성 질환의 치료 및/또는 예방에 사용하기 위해 제공된다. 이러한 약학 조성물은 경구 전달용으로 제형화될 수 있다. "염증성 질환"은 급성 또는 만성 염증과 관련된 모든 질환을 포함할 수 있다. 급성 염증은 유해한 자극에 대한 신체의 초기 반응이며, 혈장 및 백혈구 (예를 들어, 과립구)가 혈액으로부터 손상된 조직 내로의 증가된 이동에 기인한다. 다수의 생화학적 결과는 국소 혈관계, 면역계, 및 손상된 조직 내의 다양한 세포와 관련된 염증 반응을 증식시키고 성숙시킨다. 장기간 염증은 염증 부위에 존재하는 세포 유형의 점진적인 변화를 야기하는 만성 염증이라고 하고, 염증 과정에서 조직의 동시 파괴 및 치유를 특징으로 한다. 염증성 질환은 화상, 화학적 자극제, 동상, 독소, 병원균에 의한 감염, 신체 상해, 과민성으로 인한 면역 반응, 이온화 방사선, 또는 이물질, 예를 들어, 파편(splinters), 먼지(dirt) 및 잔해(debris)에 의해 야기될 수 있다. 일 실시예에서, 염증성 질환은 상피 세포 손상, 간염, 비만, 지방간 질환, 간 염증, 췌장염, 크론병, 누공성 크론병, 궤양성 대장염, 경증에서 중등도 궤양성 대장염, 중등도에서 중증 궤양성 대장염, 주머니염, 직장염, 다발성 경화증, 전신 홍반성 루푸스, 이식편 대 숙주 질환, 류마티스 관절염, 또는 건선이다.
비-자연적으로 발생하는 융합 단백질을 피험자에게 투여하는 단계를 포함하는, 피험자에서 질환 또는 질병의 치료 방법이 본 명세서에 더 기재된다. 일 실시예에서 질환 또는 질병은 상피 세포 손상, 간염, 비만, 지방간 질환, 간 염증, 췌장염, 크론병, 누공성 크론병, 궤양성 대장염, 경증에서 중등도 궤양성 대장염, 중등도에서 중증 궤양성 대장염, 주머니염, 직장염, 다발성 경화증, 전신 홍반성 루푸스, 이식편 대 숙주 질환, 류마티스 관절염, 또는 건선이다. 비-자연적으로 발생하는 융합 단백질은 피험자에게 경구 투여될 수 있다. 피험자는 인간일 수 있다.
본 발명의 신규한 특징은 첨부된 청구범위에서 구체적으로 제시된다. 본 발명의 특징 및 이점에 대한 더 나은 이해는 본 발명의 원리가 이용되는 예시적인 실시예를 제시하는 하기의 상세한 설명, 및 첨부 도면을 참조하여 얻어질 것이다:
도 1은 상피 세포 단층 위의 정점 챔버(apical chamber) 및 이러한 상피 세포 단층 아래의 기저 챔버(basal chamber)를 포함하는 장치를 개략적으로 나타낸다. 정점에서 기저측(basolateral) 투과도의 경우, 시험 물품 (예를 들어, 전달 구조체, 페이로드 등)을 정점 (A) 측면에 적용하고, 투과된 (예를 들어, 통과세포외배출된) 물질의 양을 기저측 (B) 측면에서 결정하였다.
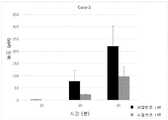
도 2는 스페이서 (서열번호: 13)를 통해 IL-22 (서열번호: 11)에 결합된 담체 (서열번호: 7)를 포함하는 전달 구조체 (서열번호: 15)가 시간-의존적 방식으로 온전한 편광 Caco-2 장 상피 세포 단층을 가로질러 IL-22 페이로드를 수송하였음을 나타낸다 (도 1에서 상기 기재된 바와 같이, 기저측 부위의 단백질의 양은 전달 구조체를 단층의 기저막에 적용한 후 15분, 30분 및 45분에 측정하였다). 자료는 서열번호: 7의 담체 및 IL-22 (서열번호: 11)를 갖는 전달 구조체가 Caco-2 상피 세포에 적용될 때, IL-22 (서열번호: 12)가 담체에 결합되지 않은 경우에 비해 약 2-3 배 더 많은 IL-22가 Caco-2 상피 세포 단층을 통과하였음을 더 나타낸다.
도 3은 전달 구조체 (서열번호: 15)가 시간-의존적 방식으로 온전한 편광 SMI-100 장 상피 세포 단층을 가로질러 IL-22 (서열번호: 11)를 수송하였음을 나타낸다 (기저측 챔버 내의 단백질의 양은 전달 구조체를 단층의 기저막에 적용한 후 15분, 30분 및 45분에 측정하였다). 자료는 IL-22 (서열번호: 11)에 결합된 서열번호: 7의 담체를 포함하는 전달 구조체가 SMI-100 상피 세포에 적용될 때, IL-22 (서열번호: 12)가 담체에 결합되지 않은 경우에 비해 약 2-3 배 더 많은 IL-22가 SMI-100 상피 세포 단층을 통과하였음을 더 나타낸다.
도 4는 스페이서 (서열번호: 13)를 통해 IL-22 (서열번호: 11)에 결합된 담체 (서열번호: 7)를 포함하는 전달 구조체 (서열번호: 15)가 in vivo에서 온전한 편광 장 상피를 가로질러 IL-22를 상당한 양으로 수송하였음을 나타낸다. 장 상피의 정점 부위는 백색 화살표 #1로 강조된다. 고유판(lamina propria)은 "l.p."로 약칭된다. 편광 상피의 외부 기저막은 백색 화살표 #2로 강조된다. IL-22 국소화는 백색 화살표 #3으로 표시된다.
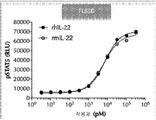
도 5a는 작용제(agonist) 농도 (pM)의 함수로서 쥣과(murine) FL83 B 세포에서 STAT3 인산화를 나타내며, 여기서 작용제는 재조합 인간 IL-22 (rhIL-22, 서열번호: 12) 또는 재조합 쥣과 IL-22 (rmIL-22; MAVLQKSMSFSLMGTLAASCLLLIALWAQE ANALPVNTRCKLEVSNFQQPYIVNRTFMLAKEASLADNNTDVRLIGEKLFRGVSAKDQCYLMKQVLNFTLEDVLLPQSDRFQPYMQEVVPFLTKLSNQLSSCHISGDDQNIQKNVRRLKETVKKLGESGEIKAIGELDLLFMSLRNACV (서열번호: 30))이다. 자료는 rhIL-22 및 rmIL-22가 농도-의존적 방식으로 STAT3 인산화를 유도하였음을 나타내고, 이는 인간 IL-22 단백질이 마우스 IL-22 만큼 효과적으로 마우스 IL-22 수용체를 통해 결합하고 신호 전달(signal transduction)을 유도할 수 있음을 나타낸다.
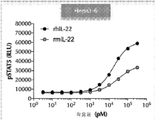
도 5b는 rhIL-22 (서열번호: 12) 및 rmIL-22도 쥣과 Hepa1-6 세포에서 STAT3 인산화를 유도하였음을 나타낸다.
도 6a는 rhIL-22 (서열번호: 12) 및 rmIL-22가 용량-의존적 방식으로 쥣과 FL83 B 세포에서 STAT5 인산화를 유도하였음을 나타내고, 이는 인간 IL-22 단백질이 마우스 IL-22 만큼 효과적으로 마우스 IL-22 수용체를 통해 결합하고 신호 전달을 유도할 수 있음을 나타낸다.
도 6b는 rhIL-22 (서열번호: 12) 및 rmIL-22도 쥣과 Hepa1-6 세포에서 STAT5 인산화를 유도하였음을 나타낸다.
도 7a는 2개의 1일 1회 용량 수준 (1 mg/kg 및 30 mg/kg)에서 서열번호: 15의 전달 구조체의 경구 (peroral; p.o.) 투여, 및 4 mg/kg에서 rhIL-22의 1개의 1일 1회 투여 (복강 내 (intraperitoneal; i.p.))를 비교하기 위한 in vivo 연구 설계 및 시간표의 개요를 나타낸다. 정상 사료-공급된, 8-10 주령, ~23 g, 암컷 C57BL/6 마우스에서 in vivo 연구를 수행하였다. 임의로, 음용수(drinking water) 내 2.5% 덱스트란 설페이트 나트륨 (dextran sulfate sodium, DSS)으로 대장염을 화학적으로 유도하였다. 연구 종료점에는 체중 변화율, 질병 활동 지수(disease activity index), 결장 길이(colon length) 및 무게, 및 조직병리학 (histopathology)을 포함하였다.
도 7b는 도 7a에 기재된 연구에서 사용된 실험군 및 대조군의 특성을 나타낸다.
도 8a는 다양한 실험군 및 대조군의 0일에 비해 연구 10일에 동물의 체중 변화율 (%)을 나타낸다. 비히클에 비해 서열번호: 12의 rhIL-22 또는 서열번호: 15의 전달 구조체에 의한 기준 (0일 대 10일) 체중 변화는 일원 분산분석(1-way ANOVA)에 의해 평가된 바와 같이 유의하지 않았다. 양성 모델 대조군 (시클로스포린) CsA는 일원 분산분석에 의해 평가된 바와 같이 비히클에 비해 상당히 상이하였다.
도 8b는 처음 10일 연구 동안 실험군 및 대조군 동물의 체중 변화를 나타낸다. 이원 분산분석(2-way ANOVA) (*, **, ***)에 의해 평가된 바와 같이, 연구 기간 동안 CsA 군의 평균 체중은 6일부터 10일까지 비히클 대조군에 비해 유의하게 개선되었다. 이원 분산분석 (*)에 의해 평가된 바와 같이, rhIL-22 (i.p.) 체중은 10일에 비히클 대조군에 비해 유의하게 개선되었다. *p<0.05, **p<0.01, ***p<0.001.
도 9는 IL-22 혈장 수준을 결정하기 위한 혈장 ELISA 실험의 결과를 나타낸다. 결과는 혈장 rhIL-22 농도가 용량-의존적 방식으로 서열번호: 15의 전달 구조체의 1 및 30 mg/kg 용량 둘 다의 경구 위관영양(oral gavage) 후 혈장에서 증가된 수준으로의 경향이 있음을 나타낸다 (*p<0.05, **p<0.01, ***p<0.001. ****p<0.0001; 평균 + SEM; n = 2 순진한(Naive), 5 비히클, 5 CsA, 10 기타 (others)).
도 10a는 건강한 CD-1 마우스에서 rhIL-22의 단일 (급성 투여) 후 표적 참여 (target engagement)의 바이오마커(들)을 확인하도록 설계된 단일 용량 in vivo 연구의 개요를 나타낸다.
도 10b는 건강한 CD-1 마우스에서 rhIL-22의 단일 및 다중 투여 후 표적 참여의 바이오마커(들)을 확인하도록 설계된 다중 용량 (아-만성 투여(sub-chronic dosing)) in vivo 연구의 개요를 나타낸다.
도 11a는 rhIL-22의 급성 및 아-만성 투여가 IL-22 농도를 지속적으로 증가 시킴을 나타낸다.
도 11b는 도 11a에 기재된 급성 및 아-만성 투여 실험 동안 측정된 일부 약동학적 매개변수를 나타낸다.
도 12a는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일 및 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 대한 반응으로 유도된 순환 쥣과 C-반응성 단백질 (mCRP) 농도를 나타낸다. 결과는 두 연구군에서 순환 mCRP의 시간-의존적 증가를 나타낸다.
도 12b는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일에 혈장 mCRP 농도의 배수 변화(fold change)를 나타낸다.
도 12c는 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 혈장 mCRP 농도의 배수 변화를 나타낸다.
도 13a는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일 및 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 대한 반응으로 유도된 순환 쥣과 혈청 아밀로이드 단백질 A (mSAA) 농도를 나타낸다. 결과는 두 연구군에서 순환 mSAA의 시간-의존적 증가를 나타내며, 투여 후 약 8시간에 근사치의 혈장 피크 농도를 나타낸다.
도 13b는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일에 혈장 mSAA 농도의 배수 변화를 나타낸다.
도 13c는 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 혈장 mSAA 농도의 배수 변화를 나타낸다.
도 14a는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일 및 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 대한 반응으로 유도된 순환 재생 췌도-유래 단백질 3β (regenerating islet-derived protein 3β, Reg3β)를 나타낸다.
도 14b는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일에 혈장 Reg3β 농도의 배수 변화를 나타낸다.
도 14c는 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 혈장 Reg3β 농도의 배수 변화를 나타낸다.
도 15는 개선된 제조 가능성이 임상 번역을 가능하게 할 수 있는 방법을 나타내는 흐름도를 나타낸다.
도 16은 서열번호: 15가 스페이서 (서열번호: 13)를 통해 인터루킨-22 (IL-22, 서열번호: 11)에 결합된 담체 도메인 (서열번호: 7)을 포함하는 이종성 융합 단백질임을 나타낸다. 이종성 융합 단백질은 E. coli 봉입체 (IB)에서 격리될 수 있으므로 재접힘 및/또는 정제를 필요로 한다.
도 17은 예를 들어 서열번호: 14-21과 같은 본 명세서에 기재된 이종성 융합 단백질, 및 서열번호: 1-9, 22 또는 23의 담체를 포함하는 융합 단백질의 재접힘, 정제 및 제형을 요약하는 흐름도를 나타낸다.
도 18은 서열번호: 15의 구조체의 개선된 재접힘 효율에 대한 반복적 최적화 (iterative optimization)를 나타낸다.
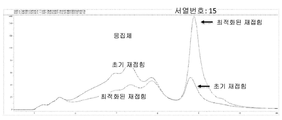
도 19는 최적화된 재접힌 단백질 (서열번호: 15) 및 고분자량을 가지므로 더 낮은 체류 시간을 갖는 단백질 응집체의 신호를 나타내는 크기-배제 크로마토그래프 (SEC)이다.
도 20은 초기 및 최적화된 재접힌 단백질 (서열번호: 15)의 예시적인 SDS-PAGE를 나타낸다.
도 21a-21b는 음이온 교환 수지 NH2-750F를 이용한 서열번호: 15의 제 1 컬럼 정제 후 크기-배제 크로마토그래프를 나타낸다. 도 21a는 10 mL의 컬럼 부피 및 20 cm의 층 높이(bed height)를 갖는 음이온 교환 수지 NH2-750F를 이용한 서열번호: 15의 제 1 컬럼 정제 후 크기-배제 크로마토그래프를 나타낸다. 도 21b는 4.6 L의 컬럼 부피 및 30 cm의 층 높이를 갖는 음이온 교환 수지 NH2-750F를 이용한 서열번호: 15의 제 1 컬럼 정제 후 크기-배제 크로마토그래프를 나타낸다.
도 22a-22b는 히드록시아파타이트 수지 CaPure®를 이용한 서열번호: 15의 제 2 컬럼 정제 후 크기 배제 크로마토그래프를 나타낸다. 도 22a는 5 mL의 컬럼 부피, 10 cm의 층 높이, 및 0-25% B, 25C의 구배를 갖는 히드록시아파타이트 수지 Ca++Pure를 이용한 서열번호: 15의 제 2 컬럼 정제 후 크기 배제 크로마토그래프를 나타낸다. 도 22b는 800 mL의 컬럼 부피, 21 cm의 층 높이, 및 0-25% B, 25CV의 구배를 갖는 히드록시아파타이트 수지 CaPure®를 이용한 서열번호: 15의 제 2 컬럼 정제 후 크기 배제 크로마토그래프를 나타낸다. 각 도면에 대해, CaPure® 수지로부터 용리된 상이한 분획의 시료의 상응하는 SDS-PAGE.
도 23a-23b는 이종성 융합 단백질의 정제 후 액체 크로마토그래피-질량 분광광도계 (LC-MS) 크로마토그래프를 나타낸다. 도 23a는 서열번호: 17의 LC-MS 크로마토그래프를 나타낸다. 피크 1은 올바르게 재접힌 서열번호: 17을 나타낸다. 도 23b는 서열번호: 15의 LC-MS 크로마토그래프를 나타낸다. 피크 1은 올바르게 재접힌 서열번호: 15를 나타낸다. 피크 2는 (서열번호: 20에 의해 나타낸) 절단된 말단 메티오닌을 갖는 서열번호: 15를 나타낸다. 피크 3은 (서열번호: 20에 의해 나타낸) 절단된 말단 메티오닌 및 결과로 생성된 N- 말단 아미노산의 아세틸화를 갖는 서열번호: 15를 나타낸다.
도 24는 구조체의 경구 (본 명세서에서 P.O.로 약칭됨) 전달 후 장 상피를 가로질러 순환으로의 서열번호: 15의 서열을 갖는 전달 구조체의 수송을 평가하기 위한 실시예 16의 연구 개요를 나타낸다.
도 25a-25b는 서열번호: 15의 전달 구조체의 투여 후 시간의 함수로서 IL-22 혈장 농도를 나타내는 그래프를 나타낸다. 도 25a는 서열번호: 15의 전달 구조체의 투여 후 시간의 함수로서 총 IL-22 혈장 농도를 나타낸다. 도 25b는 서열번호: 15의 전달 구조체의 투여 후 시간의 함수로서 IL-22BP 혈장 농도를 나타낸다.
도 26a (비히클) 및 도 26b (서열번호: 15)는 개체 마우스에 대한 시간의 함수로서 IL-22 혈장 농도를 나타내는 그래프이다.
도 27a-27d는 스페이서 길이 및 담체의 N- 또는 C-말단에 페이로드의 결합이 페이로드의 생물학적 활성에 크게 영향을 미치지 않음을 나타낸다. 도 27a는 다양한 아미노산 스페이서의 길이가 IL-22 수용체 이량체화의 유도에 영향을 미치지 않았음을 나타낸다. 도 27b는 담체의 N- 또는 C-말단에 IL-22 페이로드의 결합이 IL-22 수용체 이량체화의 유도에 영향을 미치지 않았음을 나타낸다. 도 27c는 다양한 아미노산 스페이서의 길이가 pSTAT3 활성화의 유도에 영향을 미치지 않았음을 나타낸다. 도 27d는 담체의 N- 또는 C-말단에 IL-22 페이로드의 결합이 pSTAT3 활성화의 유도에 영향을 미치지 않았음을 나타낸다.
도 1은 상피 세포 단층 위의 정점 챔버(apical chamber) 및 이러한 상피 세포 단층 아래의 기저 챔버(basal chamber)를 포함하는 장치를 개략적으로 나타낸다. 정점에서 기저측(basolateral) 투과도의 경우, 시험 물품 (예를 들어, 전달 구조체, 페이로드 등)을 정점 (A) 측면에 적용하고, 투과된 (예를 들어, 통과세포외배출된) 물질의 양을 기저측 (B) 측면에서 결정하였다.
도 2는 스페이서 (서열번호: 13)를 통해 IL-22 (서열번호: 11)에 결합된 담체 (서열번호: 7)를 포함하는 전달 구조체 (서열번호: 15)가 시간-의존적 방식으로 온전한 편광 Caco-2 장 상피 세포 단층을 가로질러 IL-22 페이로드를 수송하였음을 나타낸다 (도 1에서 상기 기재된 바와 같이, 기저측 부위의 단백질의 양은 전달 구조체를 단층의 기저막에 적용한 후 15분, 30분 및 45분에 측정하였다). 자료는 서열번호: 7의 담체 및 IL-22 (서열번호: 11)를 갖는 전달 구조체가 Caco-2 상피 세포에 적용될 때, IL-22 (서열번호: 12)가 담체에 결합되지 않은 경우에 비해 약 2-3 배 더 많은 IL-22가 Caco-2 상피 세포 단층을 통과하였음을 더 나타낸다.
도 3은 전달 구조체 (서열번호: 15)가 시간-의존적 방식으로 온전한 편광 SMI-100 장 상피 세포 단층을 가로질러 IL-22 (서열번호: 11)를 수송하였음을 나타낸다 (기저측 챔버 내의 단백질의 양은 전달 구조체를 단층의 기저막에 적용한 후 15분, 30분 및 45분에 측정하였다). 자료는 IL-22 (서열번호: 11)에 결합된 서열번호: 7의 담체를 포함하는 전달 구조체가 SMI-100 상피 세포에 적용될 때, IL-22 (서열번호: 12)가 담체에 결합되지 않은 경우에 비해 약 2-3 배 더 많은 IL-22가 SMI-100 상피 세포 단층을 통과하였음을 더 나타낸다.
도 4는 스페이서 (서열번호: 13)를 통해 IL-22 (서열번호: 11)에 결합된 담체 (서열번호: 7)를 포함하는 전달 구조체 (서열번호: 15)가 in vivo에서 온전한 편광 장 상피를 가로질러 IL-22를 상당한 양으로 수송하였음을 나타낸다. 장 상피의 정점 부위는 백색 화살표 #1로 강조된다. 고유판(lamina propria)은 "l.p."로 약칭된다. 편광 상피의 외부 기저막은 백색 화살표 #2로 강조된다. IL-22 국소화는 백색 화살표 #3으로 표시된다.
도 5a는 작용제(agonist) 농도 (pM)의 함수로서 쥣과(murine) FL83 B 세포에서 STAT3 인산화를 나타내며, 여기서 작용제는 재조합 인간 IL-22 (rhIL-22, 서열번호: 12) 또는 재조합 쥣과 IL-22 (rmIL-22; MAVLQKSMSFSLMGTLAASCLLLIALWAQE ANALPVNTRCKLEVSNFQQPYIVNRTFMLAKEASLADNNTDVRLIGEKLFRGVSAKDQCYLMKQVLNFTLEDVLLPQSDRFQPYMQEVVPFLTKLSNQLSSCHISGDDQNIQKNVRRLKETVKKLGESGEIKAIGELDLLFMSLRNACV (서열번호: 30))이다. 자료는 rhIL-22 및 rmIL-22가 농도-의존적 방식으로 STAT3 인산화를 유도하였음을 나타내고, 이는 인간 IL-22 단백질이 마우스 IL-22 만큼 효과적으로 마우스 IL-22 수용체를 통해 결합하고 신호 전달(signal transduction)을 유도할 수 있음을 나타낸다.
도 5b는 rhIL-22 (서열번호: 12) 및 rmIL-22도 쥣과 Hepa1-6 세포에서 STAT3 인산화를 유도하였음을 나타낸다.
도 6a는 rhIL-22 (서열번호: 12) 및 rmIL-22가 용량-의존적 방식으로 쥣과 FL83 B 세포에서 STAT5 인산화를 유도하였음을 나타내고, 이는 인간 IL-22 단백질이 마우스 IL-22 만큼 효과적으로 마우스 IL-22 수용체를 통해 결합하고 신호 전달을 유도할 수 있음을 나타낸다.
도 6b는 rhIL-22 (서열번호: 12) 및 rmIL-22도 쥣과 Hepa1-6 세포에서 STAT5 인산화를 유도하였음을 나타낸다.
도 7a는 2개의 1일 1회 용량 수준 (1 mg/kg 및 30 mg/kg)에서 서열번호: 15의 전달 구조체의 경구 (peroral; p.o.) 투여, 및 4 mg/kg에서 rhIL-22의 1개의 1일 1회 투여 (복강 내 (intraperitoneal; i.p.))를 비교하기 위한 in vivo 연구 설계 및 시간표의 개요를 나타낸다. 정상 사료-공급된, 8-10 주령, ~23 g, 암컷 C57BL/6 마우스에서 in vivo 연구를 수행하였다. 임의로, 음용수(drinking water) 내 2.5% 덱스트란 설페이트 나트륨 (dextran sulfate sodium, DSS)으로 대장염을 화학적으로 유도하였다. 연구 종료점에는 체중 변화율, 질병 활동 지수(disease activity index), 결장 길이(colon length) 및 무게, 및 조직병리학 (histopathology)을 포함하였다.
도 7b는 도 7a에 기재된 연구에서 사용된 실험군 및 대조군의 특성을 나타낸다.
도 8a는 다양한 실험군 및 대조군의 0일에 비해 연구 10일에 동물의 체중 변화율 (%)을 나타낸다. 비히클에 비해 서열번호: 12의 rhIL-22 또는 서열번호: 15의 전달 구조체에 의한 기준 (0일 대 10일) 체중 변화는 일원 분산분석(1-way ANOVA)에 의해 평가된 바와 같이 유의하지 않았다. 양성 모델 대조군 (시클로스포린) CsA는 일원 분산분석에 의해 평가된 바와 같이 비히클에 비해 상당히 상이하였다.
도 8b는 처음 10일 연구 동안 실험군 및 대조군 동물의 체중 변화를 나타낸다. 이원 분산분석(2-way ANOVA) (*, **, ***)에 의해 평가된 바와 같이, 연구 기간 동안 CsA 군의 평균 체중은 6일부터 10일까지 비히클 대조군에 비해 유의하게 개선되었다. 이원 분산분석 (*)에 의해 평가된 바와 같이, rhIL-22 (i.p.) 체중은 10일에 비히클 대조군에 비해 유의하게 개선되었다. *p<0.05, **p<0.01, ***p<0.001.
도 9는 IL-22 혈장 수준을 결정하기 위한 혈장 ELISA 실험의 결과를 나타낸다. 결과는 혈장 rhIL-22 농도가 용량-의존적 방식으로 서열번호: 15의 전달 구조체의 1 및 30 mg/kg 용량 둘 다의 경구 위관영양(oral gavage) 후 혈장에서 증가된 수준으로의 경향이 있음을 나타낸다 (*p<0.05, **p<0.01, ***p<0.001. ****p<0.0001; 평균 + SEM; n = 2 순진한(Naive), 5 비히클, 5 CsA, 10 기타 (others)).
도 10a는 건강한 CD-1 마우스에서 rhIL-22의 단일 (급성 투여) 후 표적 참여 (target engagement)의 바이오마커(들)을 확인하도록 설계된 단일 용량 in vivo 연구의 개요를 나타낸다.
도 10b는 건강한 CD-1 마우스에서 rhIL-22의 단일 및 다중 투여 후 표적 참여의 바이오마커(들)을 확인하도록 설계된 다중 용량 (아-만성 투여(sub-chronic dosing)) in vivo 연구의 개요를 나타낸다.
도 11a는 rhIL-22의 급성 및 아-만성 투여가 IL-22 농도를 지속적으로 증가 시킴을 나타낸다.
도 11b는 도 11a에 기재된 급성 및 아-만성 투여 실험 동안 측정된 일부 약동학적 매개변수를 나타낸다.
도 12a는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일 및 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 대한 반응으로 유도된 순환 쥣과 C-반응성 단백질 (mCRP) 농도를 나타낸다. 결과는 두 연구군에서 순환 mCRP의 시간-의존적 증가를 나타낸다.
도 12b는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일에 혈장 mCRP 농도의 배수 변화(fold change)를 나타낸다.
도 12c는 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 혈장 mCRP 농도의 배수 변화를 나타낸다.
도 13a는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일 및 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 대한 반응으로 유도된 순환 쥣과 혈청 아밀로이드 단백질 A (mSAA) 농도를 나타낸다. 결과는 두 연구군에서 순환 mSAA의 시간-의존적 증가를 나타내며, 투여 후 약 8시간에 근사치의 혈장 피크 농도를 나타낸다.
도 13b는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일에 혈장 mSAA 농도의 배수 변화를 나타낸다.
도 13c는 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 혈장 mSAA 농도의 배수 변화를 나타낸다.
도 14a는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일 및 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 대한 반응으로 유도된 순환 재생 췌도-유래 단백질 3β (regenerating islet-derived protein 3β, Reg3β)를 나타낸다.
도 14b는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일에 혈장 Reg3β 농도의 배수 변화를 나타낸다.
도 14c는 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 혈장 Reg3β 농도의 배수 변화를 나타낸다.
도 15는 개선된 제조 가능성이 임상 번역을 가능하게 할 수 있는 방법을 나타내는 흐름도를 나타낸다.
도 16은 서열번호: 15가 스페이서 (서열번호: 13)를 통해 인터루킨-22 (IL-22, 서열번호: 11)에 결합된 담체 도메인 (서열번호: 7)을 포함하는 이종성 융합 단백질임을 나타낸다. 이종성 융합 단백질은 E. coli 봉입체 (IB)에서 격리될 수 있으므로 재접힘 및/또는 정제를 필요로 한다.
도 17은 예를 들어 서열번호: 14-21과 같은 본 명세서에 기재된 이종성 융합 단백질, 및 서열번호: 1-9, 22 또는 23의 담체를 포함하는 융합 단백질의 재접힘, 정제 및 제형을 요약하는 흐름도를 나타낸다.
도 18은 서열번호: 15의 구조체의 개선된 재접힘 효율에 대한 반복적 최적화 (iterative optimization)를 나타낸다.
도 19는 최적화된 재접힌 단백질 (서열번호: 15) 및 고분자량을 가지므로 더 낮은 체류 시간을 갖는 단백질 응집체의 신호를 나타내는 크기-배제 크로마토그래프 (SEC)이다.
도 20은 초기 및 최적화된 재접힌 단백질 (서열번호: 15)의 예시적인 SDS-PAGE를 나타낸다.
도 21a-21b는 음이온 교환 수지 NH2-750F를 이용한 서열번호: 15의 제 1 컬럼 정제 후 크기-배제 크로마토그래프를 나타낸다. 도 21a는 10 mL의 컬럼 부피 및 20 cm의 층 높이(bed height)를 갖는 음이온 교환 수지 NH2-750F를 이용한 서열번호: 15의 제 1 컬럼 정제 후 크기-배제 크로마토그래프를 나타낸다. 도 21b는 4.6 L의 컬럼 부피 및 30 cm의 층 높이를 갖는 음이온 교환 수지 NH2-750F를 이용한 서열번호: 15의 제 1 컬럼 정제 후 크기-배제 크로마토그래프를 나타낸다.
도 22a-22b는 히드록시아파타이트 수지 CaPure®를 이용한 서열번호: 15의 제 2 컬럼 정제 후 크기 배제 크로마토그래프를 나타낸다. 도 22a는 5 mL의 컬럼 부피, 10 cm의 층 높이, 및 0-25% B, 25C의 구배를 갖는 히드록시아파타이트 수지 Ca++Pure를 이용한 서열번호: 15의 제 2 컬럼 정제 후 크기 배제 크로마토그래프를 나타낸다. 도 22b는 800 mL의 컬럼 부피, 21 cm의 층 높이, 및 0-25% B, 25CV의 구배를 갖는 히드록시아파타이트 수지 CaPure®를 이용한 서열번호: 15의 제 2 컬럼 정제 후 크기 배제 크로마토그래프를 나타낸다. 각 도면에 대해, CaPure® 수지로부터 용리된 상이한 분획의 시료의 상응하는 SDS-PAGE.
도 23a-23b는 이종성 융합 단백질의 정제 후 액체 크로마토그래피-질량 분광광도계 (LC-MS) 크로마토그래프를 나타낸다. 도 23a는 서열번호: 17의 LC-MS 크로마토그래프를 나타낸다. 피크 1은 올바르게 재접힌 서열번호: 17을 나타낸다. 도 23b는 서열번호: 15의 LC-MS 크로마토그래프를 나타낸다. 피크 1은 올바르게 재접힌 서열번호: 15를 나타낸다. 피크 2는 (서열번호: 20에 의해 나타낸) 절단된 말단 메티오닌을 갖는 서열번호: 15를 나타낸다. 피크 3은 (서열번호: 20에 의해 나타낸) 절단된 말단 메티오닌 및 결과로 생성된 N- 말단 아미노산의 아세틸화를 갖는 서열번호: 15를 나타낸다.
도 24는 구조체의 경구 (본 명세서에서 P.O.로 약칭됨) 전달 후 장 상피를 가로질러 순환으로의 서열번호: 15의 서열을 갖는 전달 구조체의 수송을 평가하기 위한 실시예 16의 연구 개요를 나타낸다.
도 25a-25b는 서열번호: 15의 전달 구조체의 투여 후 시간의 함수로서 IL-22 혈장 농도를 나타내는 그래프를 나타낸다. 도 25a는 서열번호: 15의 전달 구조체의 투여 후 시간의 함수로서 총 IL-22 혈장 농도를 나타낸다. 도 25b는 서열번호: 15의 전달 구조체의 투여 후 시간의 함수로서 IL-22BP 혈장 농도를 나타낸다.
도 26a (비히클) 및 도 26b (서열번호: 15)는 개체 마우스에 대한 시간의 함수로서 IL-22 혈장 농도를 나타내는 그래프이다.
도 27a-27d는 스페이서 길이 및 담체의 N- 또는 C-말단에 페이로드의 결합이 페이로드의 생물학적 활성에 크게 영향을 미치지 않음을 나타낸다. 도 27a는 다양한 아미노산 스페이서의 길이가 IL-22 수용체 이량체화의 유도에 영향을 미치지 않았음을 나타낸다. 도 27b는 담체의 N- 또는 C-말단에 IL-22 페이로드의 결합이 IL-22 수용체 이량체화의 유도에 영향을 미치지 않았음을 나타낸다. 도 27c는 다양한 아미노산 스페이서의 길이가 pSTAT3 활성화의 유도에 영향을 미치지 않았음을 나타낸다. 도 27d는 담체의 N- 또는 C-말단에 IL-22 페이로드의 결합이 pSTAT3 활성화의 유도에 영향을 미치지 않았음을 나타낸다.
실시예
이들 실시예는 예시적인 목적으로만 제공되며, 본 명세서에 제공된 청구범위의 범위를 제한하지 않는다.
실시예 1
전달 구조체의 발현
이 실시예에서, 콜릭스로부터 유래된 담체 서열, 스페이서 서열 및 치료용 페이로드를 포함하는 단일 아미노산 서열로서 전달 구조체의 제조가 일반적으로 기재된다.
먼저, 서열번호: 15의 전달 구조체를 인코딩하는 핵산 서열을 PCR에 의해 증폭시키고, PCR 산물의 양 끝에서 NdeI 및 EcoRI, PstI 및 PstI, AgeI 및 EcoRI, 또는 PstI 및 EcoRI 부위의 제한 효소 쌍을 통합시켰다. 제한 효소 분해 후, PCR 산물을 세포 발현을 위한 적당한 플라스미드에 클로닝시키고, 이를 상응하는 제한 효소 쌍으로 분해하였다. 플라스미드는 서열번호: 15에 제시된 아미노산 서열을 포함하는 전달 구조체를 인코딩하였다.
전달 구조체는 하기와 같이 발현되었다: E. coli BL21(DE3) pLysS 컴피턴트 세포(competent cells) (Novagen, Madison, Wis.)는 적당한 플라스미드의 존재 하에 표준 열-쇼크 방법을 이용하여 형질전환시켜 암피실린-함유 배지에서 선택된 전달 구조체 발현 세포를 생성하고, 항생제와 함께 루리아-베르타니 배양액(Luria-Bertani broth) (Difco; Becton Dickinson, Franklin Lakes, N.J.)에서 분리 및 성장시킨 다음, OD 0.6에서 1 mM 이소프로필-D-티오갈락토피라노시드 (IPTG)를 첨가하여 단백질 발현을 유도하였다. IPTG 유도 2시간 후, 세포를 10분 동안 5,000 rpm에서 원심분리하여 수확하였다. 세포 용해 후 봉입체를 분리하고, 1g/10mL의 비로 물로 2번 세척하였다. 세포 용해로부터 얻은 펠렛을 물로 재현탁한 다음, 4℃에서 10,000rpm으로 1시간 원심분리하였다. 그 다음, 이 세척을 1회 반복하였다. 이중-세척된 IB (DWIB)를 50 mM Tris-HCl (pH 8.2), 6 M 구아니딘 HCl, 및 10 mM 디티오트레이톨 (DTT)을 함유하는 완충액에 용해시켰다. 그 다음, 가용화된 물질을 0.1 M Tris (4℃에서 pH=8.5), 1.0 M L-아르기닌, 10% 글리세롤, 3 mM L-시스테인, 1 mM 시스타민-2HCl을 함유하는 재접힘 완충액으로 희석시켰다. 서열번호: 15의 재접힌 단백질을 음이온 교환 크로마토그래피 (Q sepharose Ion Exchange) 및 Superdex 200 겔 여과 크로마토그래피 (Amersham Biosciences, Inc., Sweden)로 정제하였다. 단백질의 순도는 SDS-PAGE 및 분석 HPLC (Agilent, Inc. Palo Alto, Calif.)로 평가하였다.
전달 구조체는 이의 예상되는 분자 크기와 관련하여 적당한 접힘을 확인하기 위해 평가되었다. 유도 후, 발현된 단백질을 봉입체로부터 수집하였다. 봉입체를 이용하여, 전달 구조체의 발현 정도를 겔 전기영동으로 확인하고, 겉보기 분자량을 계산된 질량과 비교하였다.
결과는 고 수율 및 순도로 기능성 전달 구조체의 안정적이고 효율적인 제조를 나타내었다.
실시예 2
상피 세포 단층을 가로질러 페이로드의 수송을 평가하는
In
vitro
모델
이 실시예는 본 명세서에 기재된 페이로드 또는 전달 구조체의 수송 특성을 평가하도록 설계된 in vitro 모델을 나타낸다.
도 1은 상피 세포 단층 위의 정점 챔버 및 이러한 상피 세포 단층 아래의 기저 챔버를 포함하는 장치를 개략적으로 나타낸다.
정점에서 기저측 투과도의 경우, 시험 물품 (예를 들어, 전달 구조체, 페이로드 등)을 정점 (A) 측면에 첨가하고, 투과량을 기저측 (B) 측면에서 결정하였다. 기저측에서 정점 투과도의 경우, 시험 물품을 기저측 (B) 측면에 첨가하고, 투과량을 정점 (A) 측면에서 결정하였다.
자료는 하기 방정식에 따라 투과도 (Papp)로 나타낼 수 있다: Papp = (dQ/dt)/ (C0*A). Q/dt는 투과율이며, C0는 시험 물품의 초기 농도이고, A는 단층의 면적이다. 유출 수송비(efflux transport ratio) (Re)는 하기 방정식에 따라 계산될 수 있다: (Re) = Papp(B-A)/Papp(A-B). Re >2는 P-gp 또는 기타 활성 유출 수송체에 대한 잠재적 기질을 나타낼 수 있습니다.
SMI-100 또는 Caco-2 세포를 사용하여 in vitro에서 담체 또는 전달 구조체의 통과세포외배출 기능을 평가할 수 있다.
Caco-2 세포의 경우, ELISA 분석을 수행하여 통과세포외배출을 통해 Caco-2 세포 단층을 가로질러 이동하는 담체 또는 전달 구조체의 능력을 평가하였다. Caco-2 (ATCC HTB-37™) 세포는 완전 배지: 10% 소태아혈청, 2.5 mM 글루타민, 100 U의 페니실린/ml 및 100 μg의 스트렙토마이신/ml으로 보충된 둘베코스 변형된 이글스 배지 F12 (Dulbecco's modified Eagle's medium F12, DMEM F12) (Gibco BRL, Grand Island, N.Y.)에서 37℃에서 5% CO2로 유지시켰다. 세포를 2 내지 3일 마다 이 배지 (완전 배지로 명명됨)로 공급하고, 5 내지 7일 마다 계대배양하였다. 분석을 위해, 세포를 24- 또는 96-웰 플레이트에 씨딩하고 합류(confluence)할 때까지 성장시켰다.
Caco-2 세포를 콜라겐-코팅된 0.4-μm 기공 크기의 폴리카보네이트 막 트랜스웰 지지체 (Corning-Costar, Cambridge, MA) 상에서 합류 단층으로 성장시키고, chopstick Millicell-ERS® 전압계 (Millipore)를 이용하여 측정된 >250 Ω·㎠의 경상피 전기 저항(transepithelial electrical resistance, TER)을 달성한 후 18-25일 동안 사용하였다. 이러한 단층을 가로질러 담체 또는 전달 구조체의 정점에서 기저측 (A→B) 수송은, 37℃에서 전달구조체의 4.7 nM, 23.6 nM 및 236 nM 정점 적용 후 특정 시점 (예를 들어, 15, 30, 및 45분)에서 수송된 단백질의 양을 측정하여 결정되었다. TER 치수 및 10 kDa 형광 덱스트란의 크기 (HPLC 크기 배제 프로토콜을 이용하여 측정됨)를 사용하여 연구 과정 동안 단층 장벽 특성을 확인하였다. 전달 구조체 (예를 들어, 서열번호: 15)의 수송 정도는 세포-기반 세포독성 분석에서 수집된 배지의 적정에 의해 결정되었다. 수송된 전달 구조체는 포획 및 검출용 항체 (예를 들어, 항-담체 또는 항-IL-22 항체와 같은 항-페이로드)를 이용하여 ELISA(enzyme linked immunosorbant assay)로 측정되었다.
세포 배양 삽입물에서 확립된 인간 소장 조직 (SMI-100, MatTek Corporation; Ashland, MA, USA)의 합류 단층을 사용하기 전에 37℃에서 24시간 동안 안정화시켰다. >400 Ω·cm2의 경상피 전기 저항 (TEER)을 갖는 삽입물만 연구에 사용하기에 충분한 단층 무결성(monolayer integrity)을 갖는 것으로 간주되었다. 70 kD 덱스트란 수송의 억제를 평가하여 단층 무결성의 2차 검증을 수행하였다. 챔버를 수송 완충액 (PBS)으로 1회 세척하였다. 20 μg/mL의 농도로 제조된 시험 분자를 100 μL 부피의 삽입물의 정점 표면에 적용하였다. 500 μL PBS의 기저측 부피는 수송 연구를 위해 각 시점에서 교체되었다. 각 실험 조건은 3회 수행되었다.
실시예 3
편광 장 상피 세포 단층을 가로질러 IL-22의 담체-매개 수송
이 실시예는 담체 (서열번호: 7)가 in vitro에서 편광 장 상피 세포를 가로질러 IL-22 페이로드 (서열번호: 11)를 수송할 수 있음을 나타낸다. 이 실시예는 서열번호: 7의 담체가 in vivo에서 편광 장 상피 세포를 가로질러 고유판으로 생물학적 활성 IL-22 페이로드를 수송할 수 있음을 나타낸다.
Caco-2 세포 단층 및 소장 상피 조직 (본 명세서에서 SMI-100이라고도 함)을 가로질러 전달 구조체 (서열번호: 15)의 수송은, 정점 (A)에서 기저 (B)로의 수송을 위해 실시예 2에 따라 및 도 1에 나타낸 바와 같이, 전달 구조체를 상피 세포의 정점 막에 적용하여 시험하였다. 실험을 2회 수행하였으며, 정점 적용 후 15, 30 및 45분에 기저측 챔버로부터의 시료를 수집하여 수송된 단백질의 양을 결정하였다. 실시예 2에 기재된 바와 같이, ELISA 분석을 이용하여 통과세포외배출된 단백질의 양을 측정하였다.
도 2 및 도 3의 자료는 IL-22 (서열번호: 11)에 결합되었을 때 담체 (서열번호: 7)가 시간-의존적 방식으로 Caco-2 (도 2) 및 SMI-100 (도 3) 단층을 가로질러 IL-22 페이로드의 수송을 야기하였으며, 전달 구조체가 담체에 결합되지 않은 IL-22 (서열번호: 12, M+ IL-2234-179) 단독에 비해 상피 세포를 가로질러 약 2-3 배 더 많은 IL-22를 야기하였음을 나타낸다.
in vivo 실험을 위해, 수컷 비스타(Wistar) 랫트를 이용하여 통과세포외배출을 시험하였다. 수컷 비스타 랫트를 12/12 h의 명/암 주기로 케이지 당 3-5 마리 수용하였으며, 연구에 배치되었을 때 약 225-275 g (약 6-8 주령)이었다. 연속 이소플루란 마취를 사용하는 비-회수 프로토콜(non-recovery protocol)을 이용한 광 단계(light phase) 동안 실험을 수행하였다. 중간-공장 부위(mid-jejunum regions)를 노출시킨 4-5 cm 정중선(midline) 복부 절개를 수행하였다. 3.86×10-5 M의 전달 구조체 (서열번호: 15)의 저장 용액(Stock solution)을 인산염 완충 식염수 (PBS)에서 제조하였으며, (250 g 랫트 당) 50 μL을 29-게이지 바늘을 이용하여 관내 주사(intraluminal injection, ILI)로 투여하였다. 그 다음, 주사 부위 장간막 (mesentery)을 영구 마커(permanent marker)로 표시하였다. 연구 종료시, 현미경 평가를 위해 표시된 장 부분을 포획한 3-5 mm 영역을 분리하고 처리하였다.
전달 구조체 (서열번호: 15)의 통과세포외배출 활성의 결과는 도 4에 나타내었으며, 이는 상당한 양의 IL-22 페이로드 (서열번호: 11)가 IL-22에 결합된 콜릭스-유래 담체 (서열번호: 7)를 포함하는 전달 구조체의 일부로 제공될 때 in vivo에서 온전한 편광 장 상피를 가로질렀음을 나타낸다. 이 현미경 영상은 비스타 랫트의 공장에 서열번호: 15의 전달 구조체의 내강 적용한 후 장 상피의 정점 부위 (백색 화살표 #1로 강조됨)에서 상피 세포의 기저 부위 (백색 화살표 #2로 강조됨)로 및 고유판 ( "l.p."로 약칭됨)으로 IL-22 페이로드 (서열번호: 11)의 수송을 나타낸다. 이 영상은 IL-22가 고유판 내부의 세포 및 편광 상피의 외부 기저막에 위치한 IL-22 수용체와 상당한 정도로 상호작용하고 결합하였음을 더 나타낸다 (백색 화살표 #3으로 강조됨). IL-22 국소화는 백색 화살표 #2 및 #3으로 표시된다.
실시예 4
재조합 인간 IL-22는 쥣과 IL-22 수용체에 결합한다
이 실시예는 재조합 인간 IL-22 (rhIL-22, 서열번호: 12)가 재조합 쥣과 IL-22 (rmIL-22)에 필적하는 용량-의존적 방식으로 쥣과 IL-22 수용체에 결합함을 나타낸다.
도 5a는 작용제 농도 (pM)의 함수로서 쥣과 FL83 B 세포에서 STAT3 인산화를 나타내며, 여기서 작용제는 rhIL-22 (서열번호: 12) 또는 rmIL-22이다. 자료는 rhIL-22 및 rmIL-22가 농도-의존적 방식으로 STAT3 인산화를 유도하였음을 나타내고, 이는 인간 IL-22 단백질이 마우스 IL-22 만큼 효과적으로 마우스 IL-22 수용체를 통해 결합하고 신호 전달을 유도할 수 있음을 나타낸다.
도 5b는 rhIL-22 (서열번호: 12) 및 rmIL-22도 쥣과 Hepa1-6 세포에서 STAT3 인산화를 유도하였음을 나타낸다.
도 6a는 rhIL-22 (서열번호: 12) 및 rmIL-22가 용량-의존적 방식으로 쥣과 FL83 B 세포에서 STAT5 인산화를 유도하였음을 나타내고, 이는 인간 IL-22 단백질이 마우스 IL-22에 필적하는 효능으로 마우스 IL-22 수용체를 통해 결합하고 신호 전달을 유도할 수 있음을 나타낸다.
도 6b는 rhIL-22 (서열번호: 12) 및 rmIL-22도 쥣과 Hepa1-6 세포에서 STAT5 인산화를 유도하였으나, 후속 실험에서 추가 용량 범위를 수행해야 할 필요가 있음을 나타낸다.
이러한 자료는 rhIL-22 (예를 들어, 서열번호: 10 또는 11의 전달 구조체에 사용됨)가 쥣과 세포에서 STAT3 및 STAT5를 활성화할 수 있으므로, 쥣과 모델에서 이러한 전달 구조체를 사용하여 IL-22 활성 및 기능을 평가하기 위한 근거를 제공할 수 있는 강력한 증거를 제공한다.
실시예 5
대장염 모델에서 서열번호: 15의 전달 구조체의
In
vivo
효능
이 실시예는 덱스트란 설페이트 나트륨 (DSS) 마우스 모델에서 IL-22 단독 (서열번호: 12)에 비해 서열번호: 13의 링커를 통해 서열번호: 11의 IL-22에 결합된 서열번호: 7의 콜릭스 유래 담체를 포함하는 서열번호: 15의 전달 구조체의 in vivo 효능을 나타낸다.
도 7a는 2개의 1일 1회 용량 수준 (1 mg/kg 및 30 mg/kg)에서 서열번호: 15의 전달 구조체의 경구 (p.o.) 투여, 및 4 mg/kg에서 rhIL-22의 1개의 1일 1회 투여 (복강 내 (i.p.))를 비교하기 위한 in vivo 연구 설계 및 시간표의 개요를 나타낸다. 정상 사료-공급된, 8-10 주령, ~23 g, 암컷 C57BL/6 마우스에서 in vivo 연구를 수행하였다. 임의로, 음용수 내 2.5% 덱스트란 설페이트 나트륨 (DSS)으로 대장염을 화학적으로 유도하였다. 연구 종료점에는 체중 변화율, 질병 활동 지수, 결장 길이 및 무게, 및 조직병리학을 포함하였다.
도 7b는 도 7a에 기재된 연구에서 사용된 실험군 및 대조군의 특성을 나타낸다.
도 8a는 다양한 실험군 및 대조군의 0일에 비해 연구 10일에 동물의 체중 변화율 (%)을 나타낸다. 비히클에 비해 서열번호: 12의 rhIL-22 또는 서열번호: 15의 전달 구조체에 의한 기준 (0일 대 10일) 체중 변화는 일원 분산분석(1-way ANOVA)에 의해 평가된 바와 같이 유의하지 않았다. 양성 모델 대조군 (시클로스포린) CsA는 일원 분산분석에 의해 평가된 바와 같이 비히클에 비해 상당히 상이하였다.
도 8b는 처음 10일 연구 동안 실험군 및 대조군 동물의 체중 변화를 나타낸다. 이원 분산분석(2-way ANOVA) (*, **, ***)에 의해 평가된 바와 같이, 연구 기간 동안 CsA 군의 평균 체중은 6일부터 10일까지 비히클 대조군에 비해 유의하게 개선되었다. 이원 분산분석 (*)에 의해 평가된 바와 같이, rhIL-22 (i.p.) 체중은 10일에 비히클 대조군에 비해 유의하게 개선되었다. *p<0.05, **p<0.01, ***p<0.001.
도 9는 IL-22 혈장 수준을 결정하기 위한 혈장 ELISA 실험의 결과를 나타낸다. 결과는 혈장 rhIL-22 농도가 용량-의존적 방식으로 서열번호: 15의 전달 구조체의 1 및 30 mg/kg 용량 둘 다의 경구 위관영양 후 혈장에서 증가된 수준으로의 경향이 있음을 나타낸다 (*p<0.05, **p<0.01, ***p<0.001. ****p<0.0001; 평균 + SEM; n = 2 순진한, 5 비히클, 5 CsA, 10 기타).
이러한 자료는 서열번호: 15의 전달 구조체가 경구 위관영양을 통한 투여 후 체중 개선을 향한 용량-의존적 경향을 유도하였음을 나타낸다. IL-22는 용량-의존적 방식으로 서열번호: 15의 전달 구조체의 1 및 30 mg/kg 용량 둘 다의 경구 위관영양 후 혈장에서 증가된 수준으로 측정되었다. 이러한 자료는 경구 투여된 서열번호: 15의 전달 구조체가 i.p. 투여된 rhIL-22에 필적하는 DSS 마우스 모델에서 대장염의 증상을 감소시킬 수 있음을 시사한다.
또한, 경구 투여가능한 서열번호: 15의 전달 구조체에 대한 바이오마커는 하기 기재된 바와 같이 CD-1 마우스에 rhIL-22를 투여함으로써 평가되었다.
도 10a는 건강한 CD-1 마우스에서 rhIL-22의 단일 (급성 투여) 후 표적 참여의 바이오마커(들)을 확인하도록 설계된 단일 용량 in vivo 연구의 개요를 나타낸다.
도 10b는 건강한 CD-1 마우스에서 rhIL-22의 단일 및 다중 투여 후 표적 참여의 바이오마커(들)을 확인하도록 설계된 다중 용량 (아-만성 투여) in vivo 연구의 개요를 나타낸다.
도 11a는 rhIL-22의 급성 및 아-만성 투여가 IL-22 농도를 지속적으로 증가 시킴을 나타낸다.
도 11b는 도 11a에 기재된 급성 및 아-만성 투여 실험 동안 측정된 일부 약동학적 매개변수를 나타낸다.
도 12a는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일 및 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 대한 반응으로 유도된 순환 쥣과 C-반응성 단백질 (mCRP) 농도를 나타낸다. 결과는 두 연구군에서 순환 mCRP의 시간-의존적 증가를 나타낸다.
도 12b는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일에 혈장 mCRP 농도의 배수 변화를 나타낸다.
도 12c는 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 혈장 mCRP 농도의 배수 변화를 나타낸다.
도 13a는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일 및 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 대한 반응으로 유도된 순환 쥣과 혈청 아밀로이드 단백질 A (mSAA) 농도를 나타낸다. 결과는 두 연구군에서 순환 mSAA의 시간-의존적 증가를 나타내며, 투여 후 약 8시간에 근사치의 혈장 피크 농도를 나타낸다.
도 13b는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일에 혈장 mSAA 농도의 배수 변화를 나타낸다.
도 13c는 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 혈장 mSAA 농도의 배수 변화를 나타낸다.
도 14a는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일 및 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 대한 반응으로 유도된 순환 재생 췌도-유래 단백질 3β (Reg3β)를 나타낸다.
도 14b는 rhIL-22 (서열번호: 12)의 급성 투여 후 1일에 혈장 Reg3β 농도의 배수 변화를 나타낸다.
도 14c는 rhIL-22 (서열번호: 12)의 아-만성 투여 후 5일에 혈장 Reg3β 농도의 배수 변화를 나타낸다.
이러한 결과는 서열번호: 15 또는 17의 전달 구조체와 같은 전달 구조체의 약력학 (pharmacodynamics, PD)을 평가하는 연구에서 사용될 수 있는 표적 참여의 3개의 잠재적 IL-22 PD 바이오마커: C 반응성 단백질 (CRP), 혈청 아밀로이드 단백질 A (SAA), 및 재생 췌도-유래 단백질 3β (Reg3β)를 나타낸다.
실시예 6
단백질 가용화
서열번호: 15 발효로부터 627 g의 이중-세척 봉입체 (DWIB)를 4500 mL의 8M 구아니딘/HCl (Gu-HCl), 및 pH 8.0에서 50 mM Tris에 재현탁시켰다. 이후, 50 mM Tris pH 8.5를 첨가하여 부피를 6.0 L로 완료하였다. 용액을 교반-플레이트에서 부드럽게 교반하고, 9.225 g의 환원제 디티오트레이톨 (DTT)을 첨가하였다. 6L의 최종 가용화된 단백질 (서열번호: 15) 용액은 6M Gu-HCl, 50 mM Tris pH 8.0, 10mM DTT, 및 ~1g DWIB/10mL 완충액으로 이루어졌다. 가용화된 단백질 (서열번호: 15) 용액을 자석 교반-플레이트에서 교반하면서 실온 (RT)에서 배양한 다음, 4℃에서 90분 동안 15,970×g에서 원심분리하였다. 가용화 된 단백질을 포함하는 상청액을 총 부피가 5520 mL인 새로운 용기로 조심스럽게 옮겼다. 단백질 농도 측정은 브래드포드 분석에 의해 수행되었으며, 15 mg/mL에서 결정되었다.
자료는 단백질 가용화가 상기 과정을 이용하여 수행될 수 있음을 나타낸다.
실시예 7
단백질 재접힘
이 실시예는 도 17의 흐름도에 기재된 정제 과정의 일부로서 단백질 재접힘을 나타낸다.
재접힘 용액을 조심스럽게 연구, 개발 및 최적화하였다 (도 18). 최적화 과정은 15개의 상이한 매트릭스, 12개의 변수 및 200개의 재접힘 반응의 실험 계획법 (DOE)을 이용하였다. 제거 과정에 의해 결정을 내렸다. 초기 재접힘 혼합물 (초기 재접힘 용액 및 재접힌 가용화된 단백질 (서열번호: 15) 함유)은 표 2에 제시되어 있다. 최적화된 재접힘 혼합물 (최적화된 재접힘 용액 및 재접힌 가용화된 단백질 (서열번호: 15) 함유)은 표 3에 제시되어 있다.
| 100 mM Tris pH 8.5 (@ 4℃) |
| 0.5 M 아르기닌 |
| 1 M 우레아 |
| 2 mM EDTA |
| 0.3 mM GSH |
| 1 mM GSSG |
| 0.2 mg/mL 재접힘 농도 |
| 100 mM Tris pH 8.5 (@ 4℃) |
| 1.0 M 아르기닌 |
| 10% 글리세롤 |
| 3 mM L-시스테인 |
| 1 mM 시스타민-2HCl |
| >0.1 mg/mL 재접힘 농도 |
105 L 재접힘 용액을 16시간 동안 4℃에서 배양한 다음, 0.8/0.2 um 막과 Cole-Parmer 연동 펌프 및 배관을 이용한 유동 여과기 (Pall corporation의 AkroPac 또는 Sartorius의 Sartopore 2XLG)를 통해 여과하였다.
실시예 6의 가용화된 단백질 (서열번호: 15) (105 g)을 4℃로 미리냉각시킨 100L의 최적화된 재접힘 용액에 첨가하였다.
이 과정은 73 ml/min으로 설정된 Cole-Parmer 연동 펌프를 이용하여 1시간으로 프로그래밍되었다. 이 과정은 4℃의 냉장실에서 이루어졌다.
최적화된 재접힘 완충 용액은 서열번호: 15의 응집체에 비해 더 많은 양의 서열번호: 15를 제조하였다 (도 19-20). 초기 재접힘 용액의 사용은 약 10%-15% 올바르게 재접힌 서열번호: 15를 제조하였다. 최적화된 재접힘 용액의 사용은 약 45%-55% 올바르게 재접힌 서열번호: 15를 제조하였다.
실시예 8
TFF UF/DF에 의한 단백질 농도 및 완충액 교환
이 실시예는 한외여과/투석여과 (UF/DF) 원리에 기반한 접선 유동 여과 (TFF)를 이용한 단백질 농도 및 완충액 교환을 나타낸다.
(예를 들어, 서열번호: 15의) 재접힌 단백질을 TFF 시스템 (Millipore)으로 처리하여 이를 10배 농축시키고 완충액을 5배 교환하였다. 4개의 10 kDa MWCO Millipore Ultracell Pellican3, 1.14 m2 TFF 평평한 시트 카세트를 이용한 한외여과/투석여과 (UF/DF)에 의해 과정을 수행하였다. 투석여과 완충액은 20 mM Tris-염기 pH 7.5 및 100 mM NaCl로 이루어졌다. UF/DF 과정의 종료시 최종 부피는 10 L 이었다. 이후 이 물질을 Pall corporation의 AkroPac 0.8/0.2 um 여과기 및 Cole-Parmer 연동 펌프 및 배관을 사용하는 유동 여과 시스템을 이용하여 여과하였다. 브래드포드 분석을 수행하여 단백질 농도, 수율, 및 단계 회수를 결정하였다. 이 시점에서, 정량적 SEC-HPLC를 수행하여 재접힘 및 UF/DF 시료에 존재하는 적당히 접힌 서열번호: 15의 단백질의 양을 결정하였다. 브래드포드 분석을 위해 표준 곡선이 생성된 기준 표준으로, 알려진 농도의 시판용 BSA를 사용하였다. Agilent 1100 HPLC 시스템 및 TSKgel SuperSW3000, 4μm, 4.6 mm ID x 30.0 cm L (Tosoh Bioscience, 18675) 컬럼을 사용하였다. 이 정량 분석을 기반으로, 재접힘 효율을 결정하였다.
자료는 완충액 교환 및 TFF UF/DF를 이용하여 단백질 재접힘을 수행할 수 있음을 나타낸다.
실시예 9
포획 단계 NH
2
-750F
®
수지를 이용한 단백질 크로마토그래피
이 실시예는 NH2-750F® 수지를 이용한 단백질 음이온 교환 크로마토그래피의 포획 단계를 나타낸다.
General Electric (GE)의 AKTA Avant 150 또는 AKTA Pilot FPLC 시스템을 단백질 크로마토그래피에 사용하였다. Tosoh 음이온 교환 수지 NH2-750F®를 사용하여, 적어도 20 cm의 최소 층 높이를 갖고 20-25 g/L의 동적 결합 용량을 촉진하는 컬럼 부피를 보장하는 컬럼을 채웠다. 20 mM 소듐 아세테이트, pH 4.5 또는 20 mM 소듐 시트레이트, pH 4.5의 완충액을 사용하여 컬럼을 채웠다. 사용된 완충액은 하기와 같았다: 완충액 A: 20 mM Tris pH 7.5, 0.5 M NaCl; 완충액 B: 20 mM Tris pH 7.5, 2.0 M NaCl. 그 다음, NH2-750F 컬럼을 30분의 접촉 시간으로 0.5 M NaOH 용액으로 세척한 다음, 적어도 3 컬럼 부피 (CV) 동안, 또는 pH 및 전도도가 예상 값 (pH 7.5-pH 7.7, ~49 mS/cm +/- 1 mS/cm)에서 안정된 선에 도달할 때까지, 완충액 A로 평형화하였다.
컬럼에 로딩하기 전에, UF/DF 단백질 (서열번호: 15) 용액에 5 M 저장 용액을 첨가하여 0.4 M NaCl을 보충하였고, 전도도를 측정하여 49 mS/cm +/- 2 mS/cm의 전도도를 보장하였다. 단백질 (서열번호: 15) 용액을 최소 5분의 컬럼 체류 시간의 유속으로 컬럼에 로딩하고, 관류를 수집하였다. 컬럼을 3 CV의 완충액 A로 또는 280 nm에서 흡광도가 돌아올 때까지 세척하였고, 280 nm에서 0.0 mAU에 가까운 기준선에서 안정적이었다. 이 시점에서 0.0-62.5%B에서 20 CV의 선형 구배, 이어서 추가 5 CV에 대해 100%B로 단계 구배를 수행하였다. 분획을 전체적으로 수집하였으며, 이의 부피는 컬럼 부피의 0.5 이하였다. Bio-Rad ChemiDoc™ MP 영상 시스템을 이용한 SDS-PAGE로 상이한 분획의 시료를 분석하였으며, 서열번호: 15의 90% 이상을 함유하는 분획을 풀링하고 NH2-750F-풀로 명명하였다. Thermo Fisher Nanodrop One™를 이용하여 NH2-750F-풀의 단백질 농도를 측정하였으며, 서열번호: 15에 대해 1.22의 흡광 계수 및 260/280 nm 비 <0.6을 고려하여 280 nm (A280)에서 흡광도를 판독하였다. NH2-750F-풀은 약 1.0 M NaCl을 함유한다.
서열번호: 15의 NH2-750F 정제 후 크로마코그램의 예는 20 cm의 층 높이 및 10 mL의 컬럼 부피에 대해 도 21a 및 30 cm의 층 높이 및 4.6L의 컬럼 부피에 대해 도 21b에 나타내었다.
NH2-750F 정제의 요약은 서열번호: 15에 대해 표 4 및 서열번호: 14에 대해 표 5에 나타내었으며, 이는 일반적으로 서열번호: 15와 유사한 방식으로 제조, 재접힘 및 정제되었다.
| 서열번호: 15 | |
| 완충액 A | 20 mM Tris pH 7.5, 0.5M NaCl |
| 완충액 B | 20 mM Tris pH 7.5, 2.0M NaCl |
| 층 높이 | 최소 20 cm |
| 체류 시간 | 5.0 분 |
| 구배 | 0.0 - 62.5%B, 20 CV |
| 결합 용량 | 20-25 g/L (Breakthrough at 40 g/L) |
| 순도 | 93-96% |
| 회수율 | 71-76% |
| 내독소 | < 1.0 EU/mg |
| 서열번호: 14 | |
| 완충액 A | 20 mM Tris pH 7.5, 0.7M NaCl, 10% 글리세롤 |
| 완충액 B | 20 mM Tris pH 7.5, 2.0M NaCl, 10% 글리세롤 |
| 층 높이 | 최소 20 cm |
| 체류 시간 | 5.0 분 |
| 구배 | 0.0 - 62.5%B, 20 CV |
| 결합 용량 | 20-25 g/L |
| 순도 | ≥93-96% |
| 회수율 | 80-93% |
| 내독소 | < 1.0 EU/mg |
실시예 10
CaPure
®
과정을 이용한 단백질 크로마토그래피
이 실시예는 CaPure® 과정을 이용한 단백질 크로마토그래피에서 연마 정제 단계를 나타낸다.
General Electric (GE)의 AKTA Avant 150 또는 AKTA Pilot FPLC 시스템을 서열번호: 15 및 서열번호: 14의 단백질의 단백질 크로마토그래피에 사용하였다. Tosoh 히드록시아파타이드 혼합-모드 수지 CaPure®를 사용하여, 적어도 10 cm의 최소 층 높이를 갖고 최대 20 g/L의 동적 결합 용량을 촉진하는 컬럼 부피를 보장하는 서열번호: 15 및 서열번호: 14 각각에 대한 컬럼을 채웠다. 사용된 완충액은 서열번호: 15에 대해 하기와 같았다: 완충액 A: 20 mM Tris pH 7.5, 100 mM NaCl, 및 1 mM CaCl2; 완충액 B: 200 mM 소듐 포스페이트 pH 7.0, 100 mM NaCl, 및 1 mM CaCl2. 사용된 완충액은 서열번호: 14에 대해 하기와 같았다: 완충액 A: 20 mM Tris pH 7.5, 100 mM NaCl, 및 1 mM CaCl2; 완충액 B: 200 mM 소듐 포스페이트 pH 7.0, 100 mM NaCl, 및 1 mM CaCl2. 그 다음, 각 CaPure® 컬럼을 30분 이상의 접촉 시간으로 0.5 M의 NaOH로 세척한 다음, 적어도 3 컬럼 부피 (CV) 동안, 또는 pH 및 전도도가 예상 값 (pH 7.5-pH 7.7, ~11 mS/cm +/- 1 mS/cm)에서 안정된 선에 도달할 때까지, 완충액 A로 평형화하였다. 컬럼에 로딩하기 전에 NH2-750F-풀을 처리할 필요가 없었다. 이것은 단백질 손실, 시간 및 자원을 크게 감소시켰다. NH2-750F 풀을 최소 5분의 컬럼 체류 시간의 유속으로 컬럼에 로딩하고, 관류를 수집하였다. 컬럼을 3 CV의 완충액 A로 또는 280 nm에서 흡광도가 돌아올 때까지 세척하였고, 0.0 mAU에 가까운 기준선에서 안정적이었다. 이 시점에서 0-25%B에서 25 CV의 선형 구배, 이어서 추가 5 CV에 대해 100%B로 단계 구배를 수행하였다. 분획을 전체적으로 수집하였으며, 이의 부피는 용리 프로파일에 따라 컬럼 부피의 0.36 내지 1.43 범위였다. ChemiDoc™ MP 영상 시스템을 이용한 SDS-PAGE로 상이한 분획의 시료를 분석하였으며, 서열번호: 15 또는 서열번호: 14의 90% 이상을 함유하는 분획을 풀링하고 CaPure-풀로 명명하였다. Thermo Fisher Nanodrop One™를 이용하여 CaPure-풀의 단백질 농도를 측정하였으며, 서열번호: 15에 대해 1.22의 흡광 계수 및 260/280 nm 비 <0.6을 고려하여 280 nm (A280)에서 흡광도를 판독하였다.
서열번호: 15의 CaPure® 정제 후 예시적인 크로마코그램은 10 cm의 층 높이 및 5 mL의 컬럼 부피에 대해 도 22a 및 21 cm의 층 높이 및 800 mL의 컬럼 부피에 대해 도 22b에 나타내었다.
CaPure® 정제의 요약은 서열번호: 15에 대해 표 6 및 서열번호: 14에 대해 표 7에 나타내었다.
| 서열번호: 15 | |
| 완충액 A | 20 mM Tris pH 7.5, 100 mM NaCl, 1 mM CaCl2 |
| 완충액 B | 200 mM 소듐 포스페이트 pH 7.0, 100 mM NaCl, 1 mM CaCl2 |
| 층 높이 | 20 cm |
| 체류 시간 | 5.0 분 |
| 구배 | 0.0 - 25%B, 25 CV |
| 결합 용량 | 20 g/L |
| 순도 | >98% |
| 회수율 | >92% |
| 내독소 | < 1.0 EU/mg |
| 서열번호: 14 | |
| 완충액 A | 20 mM Tris pH 7.5, 100 mM NaCl, 1 mM CaCl2 |
| 완충액 B | 200 mM 소듐 포스페이트 pH 7.0, 100 mM NaCl, 1 mM CaCl2 |
| 층 높이 | 20 cm |
| 체류 시간 | 5.0 분 |
| 구배 | 0.0 - 25%B, 25 CV |
| 결합 용량 | 20 g/L |
| 순도 | >98% |
| 회수율 | >92% |
| 내독소 | < 1.0 EU/mg |
실시예 11
TFF UF/DF에 의한 단백질 농도
이 실시예는 TFF UF/DF 과정에 의한 단백질 제형을 나타낸다.
CaPure® 풀을 TFF 시스템 (Pall corporation)에 의해 최종 농도 20 mg/mL로 농축시킨 다음 5배 완충액 교환을 하였다. 3개의 10 kDa MWCO Millipore Pellican3, 0.114 m2 TFF TFF 평평한 시트 카세트를 이용한 한외여과/투석여과 (UF/DF)에 의해 과정을 수행하였다. 투석여과 완충액은 10 mM 소듐 포스페이트 pH 7.0, 100 mM NaCl로 이루어졌다. 이후 제형화된 서열번호: 15를 Pall corporation의 AkroPac 0.8/0.2 um 여과기 및 Cole-Parmer 연동 펌프 및 배관을 사용하는 유동 여과 시스템을 이용하여 여과하였다. 제형화된 서열번호: 15를 -80℃에서 분취량으로 저장한 다음, 하기의 분석을 수행하여 이의 생물물리학적 품질을 보장하였다: (1) Thermo Fisher Nanodrop One™를 이용하고 1.22의 단백질 흡광 계수를 고려하여 280 nm에서 260/280 비 <0.6으로 흡광도를 측정하여 20 mg/mL의 단백질 (예를 들어, 서열번호: 15) 농도; (2) Charles River Laboratories 장비로 측정된 1.0 Eu/mg 이하의 LAL 내독소 수준; (3) TSKgel GW3000SWXL, 5μm, 7.8 mm ID x 30.0 cm L 컬럼 (Tosoh Bioscience, 8541)을 이용한 97% 이상의 순도 (일반적으로 >98%)의 SEC-HPLC에 의한 순도; (4) Bio-Rad 겔 장치 및 이의 관련된 ChemiDoc™ MP 영상 시스템을 이용한 SDS-PAGE 분석.
실시예 12
정제된 융합 분자의
In Vivo
활성의 평가
이 실시예는 온전한 상피를 가로질러 생물학적 활성 화물을 운반하는 능력과 관련하여 융합 분자의 적당한 접힘을 확인하는 방법을 나타낸다.
서열번호: 15의 융합 단백질은 E coli에 의해 발현되고, 봉입체로부터 수집되며, 상기 실시예 8에 기재된 셔플(shuffle) 교환 완충 시스템을 이용하여 접힌다. 결과로 생성된 물질은 융합 분자의 분자 특성에 따라 실시예 9 및 실시예 10에 기재된 방법 및 예를 들어 표 4-7에 요약된 방법에 따라 정제된다. 제제는 SDS PAGE를 기준으로 ~98%의 단백질 순도를 가진다. 상피 세포는 25 nM 및 250 nM의 농도에서 서열번호: 15를 갖는 융합 분자로 처리된다. 미처리된 일치 세포와 비교하여, 서열번호: 15 처리된 세포는 살아있는/죽은 세포의 유세포 분석에 의해 평가된 용량-의존적 세포 수의 감소를 생성한다. 값은 n=4 ± 표준 편차를 나타낸다.
실시예 13
융합 단백질 정제의 대량화(Scale-up)
이 실시예는 서열번호: 15의 융합 단백질을 이용한 정제 방법의 대량화를 나타낸다 (도 7a 및 7b).
2개의 상이한 규모로 서열번호: 15의 융합 단백질을 정제하였다.
NH2-750F® 수지로 채워진 10 mL의 부피를 갖는 크로마토그래피 컬럼 및 하기의 매개변수: 층 높이: 20 cm, 체류 시간: 5분 (유속: 2 mL/min), 완충액 A: 20 mM Tris pH 7.5, 0.5 M NaCl, 완충액 B: 20 mM Tris pH 7.5, 2 M NaCl을 이용하여, 및 하기의 구배: 20 컬럼 부피 (CVs)에 대해 0.0-62.5% B를 이용하여, 제 1 정제를 수행하였다. 93-96%의 순도, >71%의 회수율, 및 <1.0 EU/mg의 내독소 수준을 갖는 서열번호: 15의 융합 단백질을 얻었다.
NH2-750F® 수지로 채워진 4.6 L의 부피를 갖는 크로마토그래피 컬럼 및 하기의 매개변수: 층 높이: 30 cm, 체류 시간: 11.55분 (유속: 400 mL/min), 완충액 A: 20 mM Tris pH 7.5, 0.5 M NaCl, 완충액 B: 20 mM Tris pH 7.5, 2 M NaCl을 이용하여, 및 하기의 구배: 20 컬럼 부피 (CVs)에 대해 0.0-62.5% B를 이용하여, 제 2 정제를 수행하였다. 93-96%의 순도, >71%의 회수율, 및 <1.0 EU/mg의 내독소 수준을 갖는 서열번호: 15의 융합 단백질을 얻었다.
실시예 14
과정 단계 회수율 사이의 농도
정제 과정을 수행하여 서열번호: 15의 융합 단백질을 4회 (로트 1-4) 정제하였으며, 정제 과정의 각 단계 후에 이 융합 단백질의 회수율을 평가하였다 (표 8). 이들 복제 사이에 융합 단백질의 회수율의 높은 수준의 농도가 있었다.
| 과정 단계 | 과정 설명 | 로트 1 | 로트 2 | 로트 3 | 로트 4 | 평균 (%) |
| 2 | 재접힘 UF/DF | 98.60% | 94% | 92.40% | 85% | 92 |
| 3 | NH2-750F | 68.60% | 66.30% | 76% | 74.50% | 71.35% |
| 4 | CaPure | 99% | 96.40% | 100% | 94.80% | 97.55 |
| 5 | 제형 UF/DF | 97.80% | 100% | 98.75% | 100% | 99.14 |
이러한 자료는 본 발명의 방법 및 조성물이 대규모로 치료용 융합 단백질의 제조 및 정제를 허용하고, 본 명세서에 개시된 방법 및 조성물이 대량화 동안 높은 농도를 제공하였음을 나타낸다.
본 명세서에 개시되고 청구된 모든 방법은 본 발명에 비추어 과도한 실험없이 제조되고 실행될 수 있다. 본 발명의 조성물 및 방법이 바람직한 실시예의 관점에서 기재되었지만, 본 발명의 개념, 사상 및 범위를 벗어나지 않고 본 명세서에 기재된 방법 및 방법의 단계 또는 단계의 순서에 변형이 적용될 수 있다는 것은 통상의 기술자에게 명백할 것이다. 보다 구체적으로, 화학적 및 생리학적으로 관련된 특정 제제가 본 명세서에 기재된 제제로 대체될 수 있는 반면, 동일하거나 유사한 결과가 달성될 수 있음이 명백할 것이다. 통상의 기술자에게 명백한 이러한 모든 유사한 대체 및 변형은 첨부된 청구범위에 의해 정의된 발명의 사상, 범위 및 개념 내에 있는 것으로 간주된다.
실시예 15
서열번호: 15 및 서열번호: 17의 비교
액체 크로마토그래피-질량 분광광도계 (LC-MS)를 서열번호: 15 및 서열번호: 17을 나타내는 정제된 조성물에서 수행하였으며, 결과는 각각 도 23a 및 23b에 나타내었다. 서열번호: 17의 조성물은 서열번호: 15의 조성물과 관련하여 상기 기재된 것과 유사한 방식으로 제조, 재접힘 및 정제되었다.
실시예 16
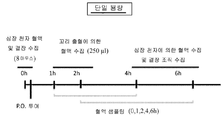
전달 구조체의 In vivo 평가
이 실시예는 비히클과 비교하여 서열번호: 15의 서열을 갖는 전달 구조체의 in vivo 평가를 기재한다.
도 24는 구조체의 경구 (본 명세서에서 P.O.로 약칭됨) 전달 후 장 상피를 가로질러 순환으로의 서열번호: 15의 서열을 갖는 전달 구조체의 수송을 평가하기 위한 (단일-투여) 연구 개요를 나타낸다. 이 실험에 사용된 동물은 금식하지 않은 CD-1 수컷 마우스였다. 1차 연구 종료점은 총 혈장 IL-22 노출이었고, 2차 종료점은 IL-22 결합 단백질 (예를 들어, IL-22BP)을 포함하여 혈장 바이오마커였다.
표 9는 액체 (비제형화) 전달 구조체 및 비히클에 관한 정보를 포함하여 실험 설정에 관한 세부 사항을 제공한다.
| 군 | 시험 물품 | 비히클 | 제형 | 용량 (mpk) | 경로 | N (4/ two TP) |
시점
(시간) |
| 1 | 비히클 | PBS, pH 7 | Aq. bolus | na | P.O. | 4 | 1 |
| 2 | 서열번호: 15 (액체) | PBS, pH 7 | Aq. bolus | 90 | P.O. | 8 (4*2) | 1, 2, 4, 6 |
표 10은 이 실험에서 전달된 서열번호: 15 구조체의 특성을 요약한다.
| 군 | 군 | Cmax (pg/mL) | Tmax (hr) | AUC (0-6hr) |
| 서열번호: 15-액체 | n/a | 24488 | 2 | 58126 |
표 9에 나타낸 각 시점에서 총 혈장 IL-22 노출을 측정하였다. 도 25a는 총 전신 IL-22 노출 (pg/mL)을 나타내며, 도 25b는 혈액 시료 및 측정이 취해진 다양한 시점에서의 IL-22BP 노출 (pg/mL)을 나타낸다. 도 26a - 도 26b는 이 연구에서 시험된 각 군에 대한 개별 측정 및 자료점(data points)을 나타낸다.
서열번호: 15에 제시된 서열을 갖는 경구 투여된 전달 구조체가 혈장에서 IL-22를 제공하였음을 관찰하였다.
실시예 17
스페이서 길이 및 담체의 N- 또는 C-\ 말단에 페이로드의 결합은 페이로드의 생물학적 활성에 크게 영향을 미치지 않는다.
이 실시예는 다양한 길이의 아미노산 링커 및 담체의 N-말단에 이종성 페이로드의 결합이 전달 구조체에 포함될 때 페이로드의 표적 결합 능력에 크게 영향을 미치지 않음을 나타낸다. 시험된 아미노산 링커는 서열번호: 13 (GGGGSGGGGSGGGGS), 서열번호: 28 (GGGGS), 및 서열번호: 31 (GGGGSGGGGSGGGGSGGGGSGGGGS)이었다.
DiscoverX HEK293 세포를 씨딩하고 표시된 농도의 작용제 (IL-22 페이로드를 함유하는 전달 구조체)를 이용하여 16 h (웰당 5,000 세포) 동안 세포를 배양하여, IL-22 수용체 이량체화 분석을 수행하였다. PathHunter® eXpress IL22RA1/IL10RB 이량체화 분석을 이용하여 플레이트 판독기에서 종료점 발광을 판독하였다.
도 27a는 서열번호: 13, 28 및 31의 아미노산 스페이서의 길이가 서열번호: 15, 32 및 33의 전달 구조체에 포함될 때 IL-22 수용체 이량체화를 유도하는 IL-22 (서열번호: 11)의 능력에 영향을 미치지 않았음을 나타낸다. 대조군 재조합 인간 IL-22 (rhIL-22, 서열번호: 12)의 수용체 이량체화의 유도는 검은색 곡선으로 나타낸다.
도 27b는 서열번호: 28의 스페이서를 통해 서열번호: 1의 아미노산 잔기 1-266을 포함하는 담체의 N- 또는 C-말단에 IL-22 페이로드 (서열번호: 11)의 결합이 IL-22 수용체 이량체화를 유도하는 서열번호: 32, 34 및 35의 전달 구조체의 능력을 크게 변화시키지 않았음을 나타낸다. 대조군 재조합 인간 IL-22 (rhIL-22)의 수용체 이량체화의 유도는 검은색 곡선으로 나타낸다.
15분 동안 다양한 농도를 갖는 10 μL의 작용제 (각각의 전달 구조체 또는 IL-22 대조군)와 함께 배양된 Colo205 세포를 이용하여, pSTAT3 활성화 분석을 수행하였다. 그 다음, MSD STAT3 플레이트 (Cat. No. N450SMA-1)를 이용하여 pSTAT3 활성화 정도를 판독하였다.
도 27c는 서열번호: 13, 28 및 31의 아미노산 스페이서의 길이가 서열번호: 15, 32 및 33의 전달 구조체에 포함될 때 pSTAT3 활성화를 유도하는 IL-22 (서열번호: 11)의 능력에 영향을 미치지 않았음을 나타낸다. 대조군 재조합 인간 IL-22 (rhIL-22, 서열번호: 12)의 pSTAT3 활성화는 검은색 곡선으로 나타낸다.
도 27d는 서열번호: 28의 스페이서를 통해 서열번호: 1의 아미노산 잔기 1-266을 포함하는 담체의 N- 또는 C-말단에 IL-22 페이로드 (서열번호: 11)의 결합이 pSTAT3 활성화를 유도하는 서열번호: 32, 34 및 35의 전달 구조체의 능력을 크게 변화시키지 않았음을 나타낸다. 대조군 재조합 인간 IL-22 (rhIL-22)의 pSTAT3 활성화는 검은색 곡선으로 나타낸다.
SEQUENCE LISTING
<110> APPLIED MOLECULAR TRANSPORT INC.
<120> DELIVERY CONSTRUCTS FOR TRANSCYTOSIS AND RELATED METHODS
<130> 40566-716.601
<140> PCT/US2019/060356
<141> 2019-11-07
<150> PCT/US2019/050708
<151> 2019-09-11
<150> 62/888,238
<151> 2019-08-16
<150> 62/888,133
<151> 2019-08-16
<150> PCT/US2019/021474
<151> 2019-03-08
<150> 62/756,889
<151> 2018-11-07
<160> 41
<170> PatentIn version 3.5
<210> 1
<211> 634
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 1
Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala Leu
260 265 270
Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg Ser
275 280 285
Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln Ala
290 295 300
Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser His
305 310 315 320
Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu Val
325 330 335
Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro Gly
340 345 350
Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp Tyr
355 360 365
Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly Ala
370 375 380
Gln Ala Ala Asp Ile Leu Ser Leu Phe Cys Pro Asp Ala Asp Lys Ser
385 390 395 400
Cys Val Ala Ser Asn Asn Asp Gln Ala Asn Ile Asn Ile Glu Ser Arg
405 410 415
Ser Gly Arg Ser Tyr Leu Pro Glu Asn Arg Ala Val Ile Thr Pro Gln
420 425 430
Gly Val Thr Asn Trp Thr Tyr Gln Glu Leu Glu Ala Thr His Gln Ala
435 440 445
Leu Thr Arg Glu Gly Tyr Val Phe Val Gly Tyr His Gly Thr Asn His
450 455 460
Val Ala Ala Gln Thr Ile Val Asn Arg Ile Ala Pro Val Pro Arg Gly
465 470 475 480
Asn Asn Thr Glu Asn Glu Glu Lys Trp Gly Gly Leu Tyr Val Ala Thr
485 490 495
His Ala Glu Val Ala His Gly Tyr Ala Arg Ile Lys Glu Gly Thr Gly
500 505 510
Glu Tyr Gly Leu Pro Thr Arg Ala Glu Arg Asp Ala Arg Gly Val Met
515 520 525
Leu Arg Val Tyr Ile Pro Arg Ala Ser Leu Glu Arg Phe Tyr Arg Thr
530 535 540
Asn Thr Pro Leu Glu Asn Ala Glu Glu His Ile Thr Gln Val Ile Gly
545 550 555 560
His Ser Leu Pro Leu Arg Asn Glu Ala Phe Thr Gly Pro Glu Ser Ala
565 570 575
Gly Gly Glu Asp Glu Thr Val Ile Gly Trp Asp Met Ala Ile His Ala
580 585 590
Val Ala Ile Pro Ser Thr Ile Pro Gly Asn Ala Tyr Glu Glu Leu Ala
595 600 605
Ile Asp Glu Glu Ala Val Ala Lys Glu Gln Ser Ile Ser Thr Lys Pro
610 615 620
Pro Tyr Lys Glu Arg Lys Asp Glu Leu Lys
625 630
<210> 2
<211> 386
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 2
Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala Leu
260 265 270
Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg Ser
275 280 285
Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln Ala
290 295 300
Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser His
305 310 315 320
Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu Val
325 330 335
Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro Gly
340 345 350
Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp Tyr
355 360 365
Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly Ala
370 375 380
Gln Ala
385
<210> 3
<211> 266
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 3
Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly
260 265
<210> 4
<211> 386
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 4
Leu Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala Leu
260 265 270
Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg Ser
275 280 285
Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln Ala
290 295 300
Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser His
305 310 315 320
Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu Val
325 330 335
Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro Gly
340 345 350
Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp Tyr
355 360 365
Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly Ala
370 375 380
Gln Ala
385
<210> 5
<211> 266
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 5
Leu Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly
260 265
<210> 6
<211> 387
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 6
Met Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala
260 265 270
Leu Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg
275 280 285
Ser Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln
290 295 300
Ala Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser
305 310 315 320
His Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu
325 330 335
Val Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro
340 345 350
Gly Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp
355 360 365
Tyr Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly
370 375 380
Ala Gln Ala
385
<210> 7
<211> 267
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 7
Met Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly
260 265
<210> 8
<211> 387
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 8
Met Leu Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala
260 265 270
Leu Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg
275 280 285
Ser Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln
290 295 300
Ala Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser
305 310 315 320
His Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu
325 330 335
Val Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro
340 345 350
Gly Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp
355 360 365
Tyr Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly
370 375 380
Ala Gln Ala
385
<210> 9
<211> 267
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 9
Met Leu Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly
260 265
<210> 10
<211> 179
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 10
Met Ala Ala Leu Gln Lys Ser Val Ser Ser Phe Leu Met Gly Thr Leu
1 5 10 15
Ala Thr Ser Cys Leu Leu Leu Leu Ala Leu Leu Val Gln Gly Gly Ala
20 25 30
Ala Ala Pro Ile Ser Ser His Cys Arg Leu Asp Lys Ser Asn Phe Gln
35 40 45
Gln Pro Tyr Ile Thr Asn Arg Thr Phe Met Leu Ala Lys Glu Ala Ser
50 55 60
Leu Ala Asp Asn Asn Thr Asp Val Arg Leu Ile Gly Glu Lys Leu Phe
65 70 75 80
His Gly Val Ser Met Ser Glu Arg Cys Tyr Leu Met Lys Gln Val Leu
85 90 95
Asn Phe Thr Leu Glu Glu Val Leu Phe Pro Gln Ser Asp Arg Phe Gln
100 105 110
Pro Tyr Met Gln Glu Val Val Pro Phe Leu Ala Arg Leu Ser Asn Arg
115 120 125
Leu Ser Thr Cys His Ile Glu Gly Asp Asp Leu His Ile Gln Arg Asn
130 135 140
Val Gln Lys Leu Lys Asp Thr Val Lys Lys Leu Gly Glu Ser Gly Glu
145 150 155 160
Ile Lys Ala Ile Gly Glu Leu Asp Leu Leu Phe Met Ser Leu Arg Asn
165 170 175
Ala Cys Ile
<210> 11
<211> 146
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 11
Ala Pro Ile Ser Ser His Cys Arg Leu Asp Lys Ser Asn Phe Gln Gln
1 5 10 15
Pro Tyr Ile Thr Asn Arg Thr Phe Met Leu Ala Lys Glu Ala Ser Leu
20 25 30
Ala Asp Asn Asn Thr Asp Val Arg Leu Ile Gly Glu Lys Leu Phe His
35 40 45
Gly Val Ser Met Ser Glu Arg Cys Tyr Leu Met Lys Gln Val Leu Asn
50 55 60
Phe Thr Leu Glu Glu Val Leu Phe Pro Gln Ser Asp Arg Phe Gln Pro
65 70 75 80
Tyr Met Gln Glu Val Val Pro Phe Leu Ala Arg Leu Ser Asn Arg Leu
85 90 95
Ser Thr Cys His Ile Glu Gly Asp Asp Leu His Ile Gln Arg Asn Val
100 105 110
Gln Lys Leu Lys Asp Thr Val Lys Lys Leu Gly Glu Ser Gly Glu Ile
115 120 125
Lys Ala Ile Gly Glu Leu Asp Leu Leu Phe Met Ser Leu Arg Asn Ala
130 135 140
Cys Ile
145
<210> 12
<211> 147
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 12
Met Ala Pro Ile Ser Ser His Cys Arg Leu Asp Lys Ser Asn Phe Gln
1 5 10 15
Gln Pro Tyr Ile Thr Asn Arg Thr Phe Met Leu Ala Lys Glu Ala Ser
20 25 30
Leu Ala Asp Asn Asn Thr Asp Val Arg Leu Ile Gly Glu Lys Leu Phe
35 40 45
His Gly Val Ser Met Ser Glu Arg Cys Tyr Leu Met Lys Gln Val Leu
50 55 60
Asn Phe Thr Leu Glu Glu Val Leu Phe Pro Gln Ser Asp Arg Phe Gln
65 70 75 80
Pro Tyr Met Gln Glu Val Val Pro Phe Leu Ala Arg Leu Ser Asn Arg
85 90 95
Leu Ser Thr Cys His Ile Glu Gly Asp Asp Leu His Ile Gln Arg Asn
100 105 110
Val Gln Lys Leu Lys Asp Thr Val Lys Lys Leu Gly Glu Ser Gly Glu
115 120 125
Ile Lys Ala Ile Gly Glu Leu Asp Leu Leu Phe Met Ser Leu Arg Asn
130 135 140
Ala Cys Ile
145
<210> 13
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 13
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 14
<211> 548
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 14
Met Leu Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala
260 265 270
Leu Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg
275 280 285
Ser Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln
290 295 300
Ala Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser
305 310 315 320
His Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu
325 330 335
Val Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro
340 345 350
Gly Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp
355 360 365
Tyr Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly
370 375 380
Ala Gln Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Ala Pro Ile Ser Ser His Cys Arg Leu Asp Lys Ser Asn Phe
405 410 415
Gln Gln Pro Tyr Ile Thr Asn Arg Thr Phe Met Leu Ala Lys Glu Ala
420 425 430
Ser Leu Ala Asp Asn Asn Thr Asp Val Arg Leu Ile Gly Glu Lys Leu
435 440 445
Phe His Gly Val Ser Met Ser Glu Arg Cys Tyr Leu Met Lys Gln Val
450 455 460
Leu Asn Phe Thr Leu Glu Glu Val Leu Phe Pro Gln Ser Asp Arg Phe
465 470 475 480
Gln Pro Tyr Met Gln Glu Val Val Pro Phe Leu Ala Arg Leu Ser Asn
485 490 495
Arg Leu Ser Thr Cys His Ile Glu Gly Asp Asp Leu His Ile Gln Arg
500 505 510
Asn Val Gln Lys Leu Lys Asp Thr Val Lys Lys Leu Gly Glu Ser Gly
515 520 525
Glu Ile Lys Ala Ile Gly Glu Leu Asp Leu Leu Phe Met Ser Leu Arg
530 535 540
Asn Ala Cys Ile
545
<210> 15
<211> 428
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 15
Met Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Pro Ile Ser Ser His
275 280 285
Cys Arg Leu Asp Lys Ser Asn Phe Gln Gln Pro Tyr Ile Thr Asn Arg
290 295 300
Thr Phe Met Leu Ala Lys Glu Ala Ser Leu Ala Asp Asn Asn Thr Asp
305 310 315 320
Val Arg Leu Ile Gly Glu Lys Leu Phe His Gly Val Ser Met Ser Glu
325 330 335
Arg Cys Tyr Leu Met Lys Gln Val Leu Asn Phe Thr Leu Glu Glu Val
340 345 350
Leu Phe Pro Gln Ser Asp Arg Phe Gln Pro Tyr Met Gln Glu Val Val
355 360 365
Pro Phe Leu Ala Arg Leu Ser Asn Arg Leu Ser Thr Cys His Ile Glu
370 375 380
Gly Asp Asp Leu His Ile Gln Arg Asn Val Gln Lys Leu Lys Asp Thr
385 390 395 400
Val Lys Lys Leu Gly Glu Ser Gly Glu Ile Lys Ala Ile Gly Glu Leu
405 410 415
Asp Leu Leu Phe Met Ser Leu Arg Asn Ala Cys Ile
420 425
<210> 16
<211> 548
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 16
Met Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala
260 265 270
Leu Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg
275 280 285
Ser Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln
290 295 300
Ala Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser
305 310 315 320
His Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu
325 330 335
Val Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro
340 345 350
Gly Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp
355 360 365
Tyr Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly
370 375 380
Ala Gln Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Ala Pro Ile Ser Ser His Cys Arg Leu Asp Lys Ser Asn Phe
405 410 415
Gln Gln Pro Tyr Ile Thr Asn Arg Thr Phe Met Leu Ala Lys Glu Ala
420 425 430
Ser Leu Ala Asp Asn Asn Thr Asp Val Arg Leu Ile Gly Glu Lys Leu
435 440 445
Phe His Gly Val Ser Met Ser Glu Arg Cys Tyr Leu Met Lys Gln Val
450 455 460
Leu Asn Phe Thr Leu Glu Glu Val Leu Phe Pro Gln Ser Asp Arg Phe
465 470 475 480
Gln Pro Tyr Met Gln Glu Val Val Pro Phe Leu Ala Arg Leu Ser Asn
485 490 495
Arg Leu Ser Thr Cys His Ile Glu Gly Asp Asp Leu His Ile Gln Arg
500 505 510
Asn Val Gln Lys Leu Lys Asp Thr Val Lys Lys Leu Gly Glu Ser Gly
515 520 525
Glu Ile Lys Ala Ile Gly Glu Leu Asp Leu Leu Phe Met Ser Leu Arg
530 535 540
Asn Ala Cys Ile
545
<210> 17
<211> 428
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 17
Met Leu Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Pro Ile Ser Ser His
275 280 285
Cys Arg Leu Asp Lys Ser Asn Phe Gln Gln Pro Tyr Ile Thr Asn Arg
290 295 300
Thr Phe Met Leu Ala Lys Glu Ala Ser Leu Ala Asp Asn Asn Thr Asp
305 310 315 320
Val Arg Leu Ile Gly Glu Lys Leu Phe His Gly Val Ser Met Ser Glu
325 330 335
Arg Cys Tyr Leu Met Lys Gln Val Leu Asn Phe Thr Leu Glu Glu Val
340 345 350
Leu Phe Pro Gln Ser Asp Arg Phe Gln Pro Tyr Met Gln Glu Val Val
355 360 365
Pro Phe Leu Ala Arg Leu Ser Asn Arg Leu Ser Thr Cys His Ile Glu
370 375 380
Gly Asp Asp Leu His Ile Gln Arg Asn Val Gln Lys Leu Lys Asp Thr
385 390 395 400
Val Lys Lys Leu Gly Glu Ser Gly Glu Ile Lys Ala Ile Gly Glu Leu
405 410 415
Asp Leu Leu Phe Met Ser Leu Arg Asn Ala Cys Ile
420 425
<210> 18
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 18
Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala Leu
260 265 270
Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg Ser
275 280 285
Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln Ala
290 295 300
Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser His
305 310 315 320
Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu Val
325 330 335
Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro Gly
340 345 350
Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp Tyr
355 360 365
Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly Ala
370 375 380
Gln Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
385 390 395 400
Ser Ala Pro Ile Ser Ser His Cys Arg Leu Asp Lys Ser Asn Phe Gln
405 410 415
Gln Pro Tyr Ile Thr Asn Arg Thr Phe Met Leu Ala Lys Glu Ala Ser
420 425 430
Leu Ala Asp Asn Asn Thr Asp Val Arg Leu Ile Gly Glu Lys Leu Phe
435 440 445
His Gly Val Ser Met Ser Glu Arg Cys Tyr Leu Met Lys Gln Val Leu
450 455 460
Asn Phe Thr Leu Glu Glu Val Leu Phe Pro Gln Ser Asp Arg Phe Gln
465 470 475 480
Pro Tyr Met Gln Glu Val Val Pro Phe Leu Ala Arg Leu Ser Asn Arg
485 490 495
Leu Ser Thr Cys His Ile Glu Gly Asp Asp Leu His Ile Gln Arg Asn
500 505 510
Val Gln Lys Leu Lys Asp Thr Val Lys Lys Leu Gly Glu Ser Gly Glu
515 520 525
Ile Lys Ala Ile Gly Glu Leu Asp Leu Leu Phe Met Ser Leu Arg Asn
530 535 540
Ala Cys Ile
545
<210> 19
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 19
Leu Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala Leu
260 265 270
Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg Ser
275 280 285
Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln Ala
290 295 300
Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser His
305 310 315 320
Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu Val
325 330 335
Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro Gly
340 345 350
Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp Tyr
355 360 365
Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly Ala
370 375 380
Gln Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
385 390 395 400
Ser Ala Pro Ile Ser Ser His Cys Arg Leu Asp Lys Ser Asn Phe Gln
405 410 415
Gln Pro Tyr Ile Thr Asn Arg Thr Phe Met Leu Ala Lys Glu Ala Ser
420 425 430
Leu Ala Asp Asn Asn Thr Asp Val Arg Leu Ile Gly Glu Lys Leu Phe
435 440 445
His Gly Val Ser Met Ser Glu Arg Cys Tyr Leu Met Lys Gln Val Leu
450 455 460
Asn Phe Thr Leu Glu Glu Val Leu Phe Pro Gln Ser Asp Arg Phe Gln
465 470 475 480
Pro Tyr Met Gln Glu Val Val Pro Phe Leu Ala Arg Leu Ser Asn Arg
485 490 495
Leu Ser Thr Cys His Ile Glu Gly Asp Asp Leu His Ile Gln Arg Asn
500 505 510
Val Gln Lys Leu Lys Asp Thr Val Lys Lys Leu Gly Glu Ser Gly Glu
515 520 525
Ile Lys Ala Ile Gly Glu Leu Asp Leu Leu Phe Met Ser Leu Arg Asn
530 535 540
Ala Cys Ile
545
<210> 20
<211> 427
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 20
Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly Gly Gly Gly Gly Ser Gly
260 265 270
Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Pro Ile Ser Ser His Cys
275 280 285
Arg Leu Asp Lys Ser Asn Phe Gln Gln Pro Tyr Ile Thr Asn Arg Thr
290 295 300
Phe Met Leu Ala Lys Glu Ala Ser Leu Ala Asp Asn Asn Thr Asp Val
305 310 315 320
Arg Leu Ile Gly Glu Lys Leu Phe His Gly Val Ser Met Ser Glu Arg
325 330 335
Cys Tyr Leu Met Lys Gln Val Leu Asn Phe Thr Leu Glu Glu Val Leu
340 345 350
Phe Pro Gln Ser Asp Arg Phe Gln Pro Tyr Met Gln Glu Val Val Pro
355 360 365
Phe Leu Ala Arg Leu Ser Asn Arg Leu Ser Thr Cys His Ile Glu Gly
370 375 380
Asp Asp Leu His Ile Gln Arg Asn Val Gln Lys Leu Lys Asp Thr Val
385 390 395 400
Lys Lys Leu Gly Glu Ser Gly Glu Ile Lys Ala Ile Gly Glu Leu Asp
405 410 415
Leu Leu Phe Met Ser Leu Arg Asn Ala Cys Ile
420 425
<210> 21
<211> 427
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 21
Leu Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly Gly Gly Gly Gly Ser Gly
260 265 270
Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Pro Ile Ser Ser His Cys
275 280 285
Arg Leu Asp Lys Ser Asn Phe Gln Gln Pro Tyr Ile Thr Asn Arg Thr
290 295 300
Phe Met Leu Ala Lys Glu Ala Ser Leu Ala Asp Asn Asn Thr Asp Val
305 310 315 320
Arg Leu Ile Gly Glu Lys Leu Phe His Gly Val Ser Met Ser Glu Arg
325 330 335
Cys Tyr Leu Met Lys Gln Val Leu Asn Phe Thr Leu Glu Glu Val Leu
340 345 350
Phe Pro Gln Ser Asp Arg Phe Gln Pro Tyr Met Gln Glu Val Val Pro
355 360 365
Phe Leu Ala Arg Leu Ser Asn Arg Leu Ser Thr Cys His Ile Glu Gly
370 375 380
Asp Asp Leu His Ile Gln Arg Asn Val Gln Lys Leu Lys Asp Thr Val
385 390 395 400
Lys Lys Leu Gly Glu Ser Gly Glu Ile Lys Ala Ile Gly Glu Leu Asp
405 410 415
Leu Leu Phe Met Ser Leu Arg Asn Ala Cys Ile
420 425
<210> 22
<211> 634
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 22
Leu Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala Leu
260 265 270
Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg Ser
275 280 285
Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln Ala
290 295 300
Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser His
305 310 315 320
Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu Val
325 330 335
Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro Gly
340 345 350
Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp Tyr
355 360 365
Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly Ala
370 375 380
Gln Ala Ala Asp Ile Leu Ser Leu Phe Cys Pro Asp Ala Asp Lys Ser
385 390 395 400
Cys Val Ala Ser Asn Asn Asp Gln Ala Asn Ile Asn Ile Glu Ser Arg
405 410 415
Ser Gly Arg Ser Tyr Leu Pro Glu Asn Arg Ala Val Ile Thr Pro Gln
420 425 430
Gly Val Thr Asn Trp Thr Tyr Gln Glu Leu Glu Ala Thr His Gln Ala
435 440 445
Leu Thr Arg Glu Gly Tyr Val Phe Val Gly Tyr His Gly Thr Asn His
450 455 460
Val Ala Ala Gln Thr Ile Val Asn Arg Ile Ala Pro Val Pro Arg Gly
465 470 475 480
Asn Asn Thr Glu Asn Glu Glu Lys Trp Gly Gly Leu Tyr Val Ala Thr
485 490 495
His Ala Glu Val Ala His Gly Tyr Ala Arg Ile Lys Glu Gly Thr Gly
500 505 510
Glu Tyr Gly Leu Pro Thr Arg Ala Glu Arg Asp Ala Arg Gly Val Met
515 520 525
Leu Arg Val Tyr Ile Pro Arg Ala Ser Leu Glu Arg Phe Tyr Arg Thr
530 535 540
Asn Thr Pro Leu Glu Asn Ala Glu Glu His Ile Thr Gln Val Ile Gly
545 550 555 560
His Ser Leu Pro Leu Arg Asn Glu Ala Phe Thr Gly Pro Glu Ser Ala
565 570 575
Gly Gly Glu Asp Glu Thr Val Ile Gly Trp Asp Met Ala Ile His Ala
580 585 590
Val Ala Ile Pro Ser Thr Ile Pro Gly Asn Ala Tyr Glu Glu Leu Ala
595 600 605
Ile Asp Glu Glu Ala Val Ala Lys Glu Gln Ser Ile Ser Thr Lys Pro
610 615 620
Pro Tyr Lys Glu Arg Lys Asp Glu Leu Lys
625 630
<210> 23
<211> 635
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 23
Met Leu Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala
260 265 270
Leu Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg
275 280 285
Ser Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln
290 295 300
Ala Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser
305 310 315 320
His Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu
325 330 335
Val Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro
340 345 350
Gly Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp
355 360 365
Tyr Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly
370 375 380
Ala Gln Ala Ala Asp Ile Leu Ser Leu Phe Cys Pro Asp Ala Asp Lys
385 390 395 400
Ser Cys Val Ala Ser Asn Asn Asp Gln Ala Asn Ile Asn Ile Glu Ser
405 410 415
Arg Ser Gly Arg Ser Tyr Leu Pro Glu Asn Arg Ala Val Ile Thr Pro
420 425 430
Gln Gly Val Thr Asn Trp Thr Tyr Gln Glu Leu Glu Ala Thr His Gln
435 440 445
Ala Leu Thr Arg Glu Gly Tyr Val Phe Val Gly Tyr His Gly Thr Asn
450 455 460
His Val Ala Ala Gln Thr Ile Val Asn Arg Ile Ala Pro Val Pro Arg
465 470 475 480
Gly Asn Asn Thr Glu Asn Glu Glu Lys Trp Gly Gly Leu Tyr Val Ala
485 490 495
Thr His Ala Glu Val Ala His Gly Tyr Ala Arg Ile Lys Glu Gly Thr
500 505 510
Gly Glu Tyr Gly Leu Pro Thr Arg Ala Glu Arg Asp Ala Arg Gly Val
515 520 525
Met Leu Arg Val Tyr Ile Pro Arg Ala Ser Leu Glu Arg Phe Tyr Arg
530 535 540
Thr Asn Thr Pro Leu Glu Asn Ala Glu Glu His Ile Thr Gln Val Ile
545 550 555 560
Gly His Ser Leu Pro Leu Arg Asn Glu Ala Phe Thr Gly Pro Glu Ser
565 570 575
Ala Gly Gly Glu Asp Glu Thr Val Ile Gly Trp Asp Met Ala Ile His
580 585 590
Ala Val Ala Ile Pro Ser Thr Ile Pro Gly Asn Ala Tyr Glu Glu Leu
595 600 605
Ala Ile Asp Glu Glu Ala Val Ala Lys Glu Gln Ser Ile Ser Thr Lys
610 615 620
Pro Pro Tyr Lys Glu Arg Lys Asp Glu Leu Lys
625 630 635
<210> 24
<211> 427
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 24
Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly Gly Gly Gly Gly Ser Gly
260 265 270
Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Pro Ile Ser Ser His Cys
275 280 285
Arg Leu Asp Lys Ser Asn Phe Gln Gln Pro Tyr Ile Thr Asn Arg Thr
290 295 300
Phe Met Leu Ala Lys Glu Ala Ser Leu Ala Asp Asn Asn Thr Asp Val
305 310 315 320
Arg Leu Ile Gly Glu Lys Leu Phe His Gly Val Ser Met Ser Glu Arg
325 330 335
Cys Tyr Leu Met Lys Gln Val Leu Asn Phe Thr Leu Glu Glu Val Leu
340 345 350
Phe Pro Gln Ser Asp Arg Phe Gln Pro Tyr Met Gln Glu Val Val Pro
355 360 365
Phe Leu Ala Arg Leu Ser Asn Arg Leu Ser Thr Cys His Ile Glu Gly
370 375 380
Asp Asp Leu His Ile Gln Arg Asn Val Gln Lys Leu Lys Asp Thr Val
385 390 395 400
Lys Lys Leu Gly Glu Ser Gly Glu Ile Lys Ala Ile Gly Glu Leu Asp
405 410 415
Leu Leu Phe Met Ser Leu Arg Asn Ala Cys Ile
420 425
<210> 25
<211> 427
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 25
Leu Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys Ser
1 5 10 15
Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile Pro
20 25 30
Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser Ile
50 55 60
Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr Val
65 70 75 80
Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe Ala
100 105 110
Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Lys
145 150 155 160
Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn Ile
165 170 175
Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu Gly
180 185 190
Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu Cys
195 200 205
Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln Asn
210 215 220
Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val Ala
225 230 235 240
Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys Pro
245 250 255
Val Glu Gln Arg Ile His Phe Ser Lys Gly Gly Gly Gly Gly Ser Gly
260 265 270
Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Pro Ile Ser Ser His Cys
275 280 285
Arg Leu Asp Lys Ser Asn Phe Gln Gln Pro Tyr Ile Thr Asn Arg Thr
290 295 300
Phe Met Leu Ala Lys Glu Ala Ser Leu Ala Asp Asn Asn Thr Asp Val
305 310 315 320
Arg Leu Ile Gly Glu Lys Leu Phe His Gly Val Ser Met Ser Glu Arg
325 330 335
Cys Tyr Leu Met Lys Gln Val Leu Asn Phe Thr Leu Glu Glu Val Leu
340 345 350
Phe Pro Gln Ser Asp Arg Phe Gln Pro Tyr Met Gln Glu Val Val Pro
355 360 365
Phe Leu Ala Arg Leu Ser Asn Arg Leu Ser Thr Cys His Ile Glu Gly
370 375 380
Asp Asp Leu His Ile Gln Arg Asn Val Gln Lys Leu Lys Asp Thr Val
385 390 395 400
Lys Lys Leu Gly Glu Ser Gly Glu Ile Lys Ala Ile Gly Glu Leu Asp
405 410 415
Leu Leu Phe Met Ser Leu Arg Asn Ala Cys Ile
420 425
<210> 26
<211> 649
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<221> MOD_RES
<222> (1)..(1)
<223> V or L
<220>
<221> MOD_RES
<222> (3)..(3)
<223> E or D
<220>
<221> MOD_RES
<222> (4)..(4)
<223> A or E
<220>
<221> MOD_RES
<222> (6)..(6)
<223> N or K
<220>
<221> MOD_RES
<222> (16)..(16)
<223> S or L
<220>
<221> MOD_RES
<222> (21)..(21)
<223> P or L
<220>
<221> MOD_RES
<222> (24)..(24)
<223> P or Q
<220>
<221> MOD_RES
<222> (30)..(30)
<223> S or F
<220>
<221> MOD_RES
<222> (33)..(33)
<223> S or G
<220>
<221> MOD_RES
<222> (56)..(56)
<223> K or M
<220>
<221> MOD_RES
<222> (59)..(59)
<223> D or G
<220>
<221> MOD_RES
<222> (67)..(67)
<223> I or F
<220>
<221> MOD_RES
<222> (73)..(73)
<223> V or I
<220>
<221> MOD_RES
<222> (81)..(81)
<223> N or S
<220>
<221> MOD_RES
<222> (90)..(90)
<223> H or N
<220>
<221> MOD_RES
<222> (101)..(101)
<223> T or M
<220>
<221> MOD_RES
<222> (104)..(104)
<223> Y or F
<220>
<221> MOD_RES
<222> (108)..(108)
<223> E or D
<220>
<221> MOD_RES
<222> (109)..(109)
<223> G or S
<220>
<221> MOD_RES
<222> (112)..(112)
<223> A or T
<220>
<221> MOD_RES
<222> (114)..(114)
<223> N or H
<220>
<221> MOD_RES
<222> (118)..(118)
<223> P or I
<220>
<221> MOD_RES
<222> (119)..(119)
<223> I or P
<220>
<221> MOD_RES
<222> (131)..(131)
<223> V or I
<220>
<221> MOD_RES
<222> (134)..(134)
<223> L or I
<220>
<221> MOD_RES
<222> (137)..(137)
<223> Q or K
<220>
<221> MOD_RES
<222> (160)..(160)
<223> K or E
<220>
<221> MOD_RES
<222> (161)..(161)
<223> T or N
<220>
<221> MOD_RES
<222> (166)..(166)
<223> S or F
<220>
<221> MOD_RES
<222> (168)..(168)
<223> S or A
<220>
<221> MOD_RES
<222> (174)..(174)
<223> H or Q
<220>
<221> MOD_RES
<222> (175)..(185)
<223> This region may encompass one of the following sequences:
"N", "S", "SIAKQS", or "SIAKQSIAKQS"
<220>
<221> MOD_RES
<222> (196)..(196)
<223> K or N
<220>
<221> MOD_RES
<222> (199)..(199)
<223> Q, E, or H
<220>
<221> MOD_RES
<222> (201)..(201)
<223> E, N, or D
<220>
<221> MOD_RES
<222> (203)..(203)
<223> S or A
<220>
<221> MOD_RES
<222> (210)..(210)
<223> H or N
<220>
<221> MOD_RES
<222> (212)..(212)
<223> H, L, F, or R
<220>
<221> MOD_RES
<222> (214)..(214)
<223> G or T
<220>
<221> MOD_RES
<222> (215)..(215)
<223> L or S
<220>
<221> MOD_RES
<222> (216)..(216)
<223> A or P
<220>
<221> MOD_RES
<222> (217)..(217)
<223> L, E, or K
<220>
<221> MOD_RES
<222> (218)..(218)
<223> C or V
<220>
<221> MOD_RES
<222> (219)..(219)
<223> W, V, or T
<220>
<221> MOD_RES
<222> (221)..(221)
<223> V or absent
<220>
<221> MOD_RES
<222> (222)..(222)
<223> P or absent
<220>
<221> MOD_RES
<222> (223)..(223)
<223> M, I, L, or absent
<220>
<221> MOD_RES
<222> (224)..(224)
<223> D or absent
<220>
<221> MOD_RES
<222> (225)..(225)
<223> A or absent
<220>
<221> MOD_RES
<222> (226)..(226)
<223> I or absent
<220>
<221> MOD_RES
<222> (227)..(227)
<223> Y or C
<220>
<221> MOD_RES
<222> (228)..(228)
<223> N or F
<220>
<221> MOD_RES
<222> (229)..(229)
<223> Y or F
<220>
<221> MOD_RES
<222> (230)..(230)
<223> I or E
<220>
<221> MOD_RES
<222> (231)..(231)
<223> T or D
<220>
<221> MOD_RES
<222> (232)..(232)
<223> Q or P
<220>
<221> MOD_RES
<222> (233)..(233)
<223> Q, E, or A
<220>
<221> MOD_RES
<222> (234)..(234)
<223> N, L, or Q
<220>
<221> MOD_RES
<222> (237)..(237)
<223> L or Y
<220>
<221> MOD_RES
<222> (239)..(239)
<223> D or E
<220>
<221> MOD_RES
<222> (240)..(240)
<223> N or D
<220>
<221> MOD_RES
<222> (242)..(242)
<223> F, H, or Y
<220>
<221> MOD_RES
<222> (245)..(245)
<223> S or A
<220>
<221> MOD_RES
<222> (247)..(247)
<223> E or K
<220>
<221> MOD_RES
<222> (252)..(252)
<223> T or I
<220>
<221> MOD_RES
<222> (254)..(254)
<223> K, E, or G
<220>
<221> MOD_RES
<222> (255)..(255)
<223> V or A
<220>
<221> MOD_RES
<222> (257)..(257)
<223> T or M
<220>
<221> MOD_RES
<222> (262)..(262)
<223> I or M
<220>
<221> MOD_RES
<222> (266)..(266)
<223> P, T, or A
<220>
<221> MOD_RES
<222> (275)..(275)
<223> K, Q, or N
<220>
<221> MOD_RES
<222> (276)..(276)
<223> G or K
<220>
<221> MOD_RES
<222> (279)..(279)
<223> M or I
<220>
<221> MOD_RES
<222> (280)..(280)
<223> S or E
<220>
<221> MOD_RES
<222> (281)..(281)
<223> A or T
<220>
<221> MOD_RES
<222> (298)..(298)
<223> S or G
<220>
<221> MOD_RES
<222> (303)..(303)
<223> D or Y
<220>
<221> MOD_RES
<222> (305)..(305)
<223> T, P, or Q
<220>
<221> MOD_RES
<222> (309)..(309)
<223> S or Q
<220>
<221> MOD_RES
<222> (311)..(311)
<223> A or V
<220>
<221> MOD_RES
<222> (313)..(313)
<223> Q or N
<220>
<221> MOD_RES
<222> (316)..(316)
<223> N or Q
<220>
<221> MOD_RES
<222> (322)..(322)
<223> V or L
<220>
<221> MOD_RES
<222> (326)..(326)
<223> I or M
<220>
<221> MOD_RES
<222> (329)..(329)
<223> S or T
<220>
<221> MOD_RES
<222> (331)..(331)
<223> L or I
<220>
<221> MOD_RES
<222> (334)..(334)
<223> V or I
<220>
<221> MOD_RES
<222> (340)..(340)
<223> D, E, or H
<220>
<221> MOD_RES
<222> (341)..(341)
<223> E or G
<220>
<221> MOD_RES
<222> (343)..(343)
<223> E or A
<220>
<221> MOD_RES
<222> (345)..(345)
<223> E or A
<220>
<221> MOD_RES
<222> (347)..(347)
<223> A or T
<220>
<221> MOD_RES
<222> (351)..(351)
<223> S, D, or T
<220>
<221> MOD_RES
<222> (352)..(352)
<223> D or A
<220>
<221> MOD_RES
<222> (353)..(353)
<223> L or I
<220>
<221> MOD_RES
<222> (355)..(355)
<223> R or Q
<220>
<221> MOD_RES
<222> (359)..(359)
<223> N or D
<220>
<221> MOD_RES
<222> (363)..(363)
<223> M or V
<220>
<221> MOD_RES
<222> (365)..(365)
<223> T or I
<220>
<221> MOD_RES
<222> (370)..(370)
<223> V or I
<220>
<221> MOD_RES
<222> (381)..(381)
<223> H or E
<220>
<221> MOD_RES
<222> (384)..(384)
<223> G or L
<220>
<221> MOD_RES
<222> (386)..(386)
<223> T or I
<220>
<221> MOD_RES
<222> (393)..(393)
<223> G or S
<220>
<221> MOD_RES
<222> (403)..(403)
<223> F or L
<220>
<221> MOD_RES
<222> (404)..(404)
<223> C or Y
<220>
<221> MOD_RES
<222> (407)..(407)
<223> A or T
<220>
<221> MOD_RES
<222> (409)..(409)
<223> K, E, or G
<220>
<221> MOD_RES
<222> (410)..(410)
<223> S, P, or H
<220>
<221> MOD_RES
<222> (414)..(414)
<223> S or L
<220>
<221> MOD_RES
<222> (415)..(415)
<223> N or D
<220>
<221> MOD_RES
<222> (416)..(416)
<223> N or S
<220>
<221> MOD_RES
<222> (423)..(423)
<223> I or V
<220>
<221> MOD_RES
<222> (433)..(433)
<223> P or L
<220>
<221> MOD_RES
<222> (441)..(441)
<223> P or Q
<220>
<221> MOD_RES
<222> (453)..(453)
<223> E or D
<220>
<221> MOD_RES
<222> (454)..(454)
<223> A or T
<220>
<221> MOD_RES
<222> (455)..(455)
<223> T or K
<220>
<221> MOD_RES
<222> (458)..(458)
<223> A or T
<220>
<221> MOD_RES
<222> (461)..(461)
<223> R or Q
<220>
<221> MOD_RES
<222> (463)..(463)
<223> G or D
<220>
<221> MOD_RES
<222> (475)..(475)
<223> V or A
<220>
<221> MOD_RES
<222> (479)..(479)
<223> T, S, or N
<220>
<221> MOD_RES
<222> (485)..(485)
<223> A, S, or T
<220>
<221> MOD_RES
<222> (491)..(491)
<223> N or S
<220>
<221> MOD_RES
<222> (492)..(492)
<223> N or D
<220>
<221> MOD_RES
<222> (495)..(495)
<223> N, S, or K
<220>
<221> MOD_RES
<222> (497)..(497)
<223> E, R, or K
<220>
<221> MOD_RES
<222> (498)..(498)
<223> K, A, or E
<220>
<221> MOD_RES
<222> (502)..(502)
<223> L or V
<220>
<221> MOD_RES
<222> (505)..(505)
<223> A or S
<220>
<221> MOD_RES
<222> (507)..(507)
<223> H or D
<220>
<221> MOD_RES
<222> (509)..(509)
<223> E or S
<220>
<221> MOD_RES
<222> (510)..(510)
<223> V or L
<220>
<221> MOD_RES
<222> (511)..(511)
<223> A or N
<220>
<221> MOD_RES
<222> (512)..(512)
<223> H or Y
<220>
<221> MOD_RES
<222> (513)..(513)
<223> G or R
<220>
<221> MOD_RES
<222> (515)..(515)
<223> A or T
<220>
<221> MOD_RES
<222> (517)..(517)
<223> I or L
<220>
<221> MOD_RES
<222> (518)..(518)
<223> K or Q
<220>
<221> MOD_RES
<222> (519)..(519)
<223> E or K
<220>
<221> MOD_RES
<222> (522)..(522)
<223> G or A
<220>
<221> MOD_RES
<222> (523)..(523)
<223> E, D, or N
<220>
<221> MOD_RES
<222> (524)..(524)
<223> Y, G, A, or N
<220>
<221> MOD_RES
<222> (525)..(525)
<223> G or E
<220>
<221> MOD_RES
<222> (526)..(526)
<223> L or G
<220>
<221> MOD_RES
<222> (527)..(527)
<223> P or L
<220>
<221> MOD_RES
<222> (529)..(529)
<223> R, P, or T
<220>
<221> MOD_RES
<222> (530)..(530)
<223> A or E
<220>
<221> MOD_RES
<222> (531)..(531)
<223> E or K
<220>
<221> MOD_RES
<222> (532)..(532)
<223> R, Q, or K
<220>
<221> MOD_RES
<222> (533)..(533)
<223> D, K, or E
<220>
<221> MOD_RES
<222> (534)..(534)
<223> A, T, or S
<220>
<221> MOD_RES
<222> (540)..(540)
<223> R or K
<220>
<221> MOD_RES
<222> (543)..(543)
<223> I or L
<220>
<221> MOD_RES
<222> (544)..(544)
<223> P or H
<220>
<221> MOD_RES
<222> (545)..(545)
<223> R or Q
<220>
<221> MOD_RES
<222> (554)..(554)
<223> T or I
<220>
<221> MOD_RES
<222> (556)..(556)
<223> T, A, or I
<220>
<221> MOD_RES
<222> (557)..(557)
<223> P or D
<220>
<221> MOD_RES
<222> (560)..(560)
<223> N or K
<220>
<221> MOD_RES
<222> (561)..(561)
<223> A or E
<220>
<221> MOD_RES
<222> (562)..(562)
<223> E, R, or D
<220>
<221> MOD_RES
<222> (563)..(563)
<223> E, N, or R
<220>
<221> MOD_RES
<222> (564)..(564)
<223> H or L
<220>
<221> MOD_RES
<222> (565)..(565)
<223> I or V
<220>
<221> MOD_RES
<222> (566)..(566)
<223> T or E
<220>
<221> MOD_RES
<222> (567)..(567)
<223> Q, R, H, or D
<220>
<221> MOD_RES
<222> (572)..(572)
<223> S or P
<220>
<221> MOD_RES
<222> (583)..(583)
<223> P or T
<220>
<221> MOD_RES
<222> (584)..(584)
<223> E or D
<220>
<221> MOD_RES
<222> (585)..(585)
<223> S, A, or R
<220>
<221> MOD_RES
<222> (586)..(586)
<223> A, E, or V
<220>
<221> MOD_RES
<222> (587)..(587)
<223> G, E, or D
<220>
<221> MOD_RES
<222> (589)..(589)
<223> E or S
<220>
<221> MOD_RES
<222> (590)..(590)
<223> D or N
<220>
<221> MOD_RES
<222> (593)..(593)
<223> V or A
<220>
<221> MOD_RES
<222> (598)..(598)
<223> M or I
<220>
<221> MOD_RES
<222> (601)..(601)
<223> H or Y
<220>
<221> MOD_RES
<222> (602)..(602)
<223> A or G
<220>
<221> MOD_RES
<222> (613)..(613)
<223> A or S
<220>
<221> MOD_RES
<222> (615)..(615)
<223> E or A
<220>
<221> MOD_RES
<222> (616)..(616)
<223> E, A, Q, G, V, or R
<220>
<221> MOD_RES
<222> (618)..(618)
<223> A, P, or T
<220>
<221> MOD_RES
<222> (619)..(619)
<223> I, T, or P
<220>
<221> MOD_RES
<222> (620)..(620)
<223> D or A
<220>
<221> MOD_RES
<222> (624)..(629)
<223> This region may encompass one of the following sequences:
"V" or "VVKEAI"
<220>
<221> MOD_RES
<222> (631)..(631)
<223> K or E
<220>
<221> MOD_RES
<222> (637)..(637)
<223> T, A, or P
<220>
<221> MOD_RES
<222> (644)..(644)
<223> R, Q, or H
<220>
<221> MOD_RES
<222> (645)..(645)
<223> K or absent
<220>
<223> See specification as filed for detailed description of
substitutions and preferred embodiments
<400> 26
Xaa Glu Xaa Xaa Leu Xaa Ile Phe Asp Glu Cys Arg Ser Pro Cys Xaa
1 5 10 15
Leu Thr Pro Glu Xaa Gly Lys Xaa Ile Gln Ser Lys Leu Xaa Ile Pro
20 25 30
Xaa Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr Ile
35 40 45
Asn Asp Glu Gln Asn Asp Ile Xaa Asp Glu Xaa Lys Gly Glu Ser Ile
50 55 60
Ile Thr Xaa Gly Glu Phe Ala Thr Xaa Arg Ala Thr Arg His Tyr Val
65 70 75 80
Xaa Gln Asp Ala Pro Phe Gly Val Ile Xaa Leu Asp Ile Thr Thr Glu
85 90 95
Asn Gly Thr Lys Xaa Tyr Ser Xaa Asn Arg Lys Xaa Xaa Glu Phe Xaa
100 105 110
Ile Xaa Trp Leu Val Xaa Xaa Gly Glu Asp Ser Pro Ala Ser Ile Lys
115 120 125
Ile Ser Xaa Asp Glu Xaa Asp Gln Xaa Arg Asn Ile Ile Glu Val Pro
130 135 140
Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp Xaa
145 150 155 160
Xaa Gln Gly Asn Val Xaa Phe Xaa Val Thr Arg Pro Glu Xaa Xaa Xaa
165 170 175
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Ile Ala Ile Ser Trp Pro Ser
180 185 190
Val Ser Tyr Xaa Ala Ala Xaa Lys Xaa Gly Xaa Arg His Lys Arg Trp
195 200 205
Ala Xaa Trp Xaa Thr Xaa Xaa Xaa Xaa Xaa Xaa Leu Xaa Xaa Xaa Xaa
210 215 220
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Cys Thr Xaa Gly Xaa Xaa
225 230 235 240
Trp Xaa Gly Gly Xaa Tyr Xaa Thr Val Ala Gly Xaa Pro Xaa Xaa Ile
245 250 255
Xaa Val Lys Gln Gly Xaa Glu Gln Lys Xaa Val Glu Gln Arg Ile His
260 265 270
Phe Ser Xaa Xaa Asn Ala Xaa Xaa Xaa Leu Ala Ala His Arg Val Cys
275 280 285
Gly Val Pro Leu Glu Thr Leu Ala Arg Xaa Arg Lys Pro Arg Xaa Leu
290 295 300
Xaa Asp Asp Leu Xaa Cys Xaa Tyr Xaa Ala Gln Xaa Ile Val Ser Leu
305 310 315 320
Phe Xaa Ala Thr Arg Xaa Leu Phe Xaa His Xaa Asp Ser Xaa Phe Thr
325 330 335
Leu Asn Leu Xaa Xaa Gln Xaa Pro Xaa Val Xaa Glu Arg Leu Xaa Xaa
340 345 350
Xaa Arg Xaa Ile Asn Glu Xaa Asn Pro Gly Xaa Val Xaa Gln Val Leu
355 360 365
Thr Xaa Ala Arg Gln Ile Tyr Asn Asp Tyr Val Thr Xaa His Pro Xaa
370 375 380
Leu Xaa Pro Glu Gln Thr Ser Ala Xaa Ala Gln Ala Ala Asp Ile Leu
385 390 395 400
Ser Leu Xaa Xaa Pro Asp Xaa Asp Xaa Xaa Cys Val Ala Xaa Xaa Xaa
405 410 415
Asp Gln Ala Asn Ile Asn Xaa Glu Ser Arg Ser Gly Arg Ser Tyr Leu
420 425 430
Xaa Glu Asn Arg Ala Val Ile Thr Xaa Gln Gly Val Thr Asn Trp Thr
435 440 445
Tyr Gln Glu Leu Xaa Xaa Xaa His Gln Xaa Leu Thr Xaa Glu Xaa Tyr
450 455 460
Val Phe Val Gly Tyr His Gly Thr Asn His Xaa Ala Ala Gln Xaa Ile
465 470 475 480
Val Asn Arg Ile Xaa Pro Val Pro Arg Gly Xaa Xaa Thr Glu Xaa Glu
485 490 495
Xaa Xaa Trp Gly Gly Xaa Tyr Val Xaa Thr Xaa Ala Xaa Xaa Xaa Xaa
500 505 510
Xaa Tyr Xaa Arg Xaa Xaa Xaa Gly Thr Xaa Xaa Xaa Xaa Xaa Xaa Thr
515 520 525
Xaa Xaa Xaa Xaa Xaa Xaa Arg Gly Val Met Leu Xaa Val Tyr Xaa Xaa
530 535 540
Xaa Ala Ser Leu Glu Arg Phe Tyr Arg Xaa Asn Xaa Xaa Leu Glu Xaa
545 550 555 560
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Val Ile Gly His Xaa Leu Pro Leu Arg
565 570 575
Asn Glu Ala Phe Thr Gly Xaa Xaa Xaa Xaa Xaa Gly Xaa Xaa Glu Thr
580 585 590
Xaa Ile Gly Trp Asp Xaa Ala Ile Xaa Xaa Val Ala Ile Pro Ser Thr
595 600 605
Ile Pro Gly Asn Xaa Tyr Xaa Xaa Leu Xaa Xaa Xaa Glu Glu Ala Xaa
610 615 620
Xaa Xaa Xaa Xaa Xaa Ala Xaa Glu Gln Ser Ile Ser Xaa Lys Pro Pro
625 630 635 640
Tyr Lys Glu Xaa Xaa Asp Glu Leu Lys
645
<210> 27
<211> 60
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<221> MISC_FEATURE
<222> (1)..(60)
<223> This sequence may encompass 1-15 "Gly Gly Gly Ser"
repeating units
<400> 27
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
20 25 30
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
35 40 45
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
50 55 60
<210> 28
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 28
Gly Gly Gly Gly Ser
1 5
<210> 29
<211> 90
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<221> MISC_FEATURE
<222> (1)..(90)
<223> This sequence may encompass 1-15 "Gly Gly Gly Gly Gly Ser"
repeating units
<400> 29
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly
1 5 10 15
Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser
35 40 45
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly
50 55 60
Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly
65 70 75 80
Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser
85 90
<210> 30
<211> 179
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 30
Met Ala Val Leu Gln Lys Ser Met Ser Phe Ser Leu Met Gly Thr Leu
1 5 10 15
Ala Ala Ser Cys Leu Leu Leu Ile Ala Leu Trp Ala Gln Glu Ala Asn
20 25 30
Ala Leu Pro Val Asn Thr Arg Cys Lys Leu Glu Val Ser Asn Phe Gln
35 40 45
Gln Pro Tyr Ile Val Asn Arg Thr Phe Met Leu Ala Lys Glu Ala Ser
50 55 60
Leu Ala Asp Asn Asn Thr Asp Val Arg Leu Ile Gly Glu Lys Leu Phe
65 70 75 80
Arg Gly Val Ser Ala Lys Asp Gln Cys Tyr Leu Met Lys Gln Val Leu
85 90 95
Asn Phe Thr Leu Glu Asp Val Leu Leu Pro Gln Ser Asp Arg Phe Gln
100 105 110
Pro Tyr Met Gln Glu Val Val Pro Phe Leu Thr Lys Leu Ser Asn Gln
115 120 125
Leu Ser Ser Cys His Ile Ser Gly Asp Asp Gln Asn Ile Gln Lys Asn
130 135 140
Val Arg Arg Leu Lys Glu Thr Val Lys Lys Leu Gly Glu Ser Gly Glu
145 150 155 160
Ile Lys Ala Ile Gly Glu Leu Asp Leu Leu Phe Met Ser Leu Arg Asn
165 170 175
Ala Cys Val
<210> 31
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 31
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 32
<211> 418
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 32
Met Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly Gly Gly Gly Gly Ser
260 265 270
Ala Pro Ile Ser Ser His Cys Arg Leu Asp Lys Ser Asn Phe Gln Gln
275 280 285
Pro Tyr Ile Thr Asn Arg Thr Phe Met Leu Ala Lys Glu Ala Ser Leu
290 295 300
Ala Asp Asn Asn Thr Asp Val Arg Leu Ile Gly Glu Lys Leu Phe His
305 310 315 320
Gly Val Ser Met Ser Glu Arg Cys Tyr Leu Met Lys Gln Val Leu Asn
325 330 335
Phe Thr Leu Glu Glu Val Leu Phe Pro Gln Ser Asp Arg Phe Gln Pro
340 345 350
Tyr Met Gln Glu Val Val Pro Phe Leu Ala Arg Leu Ser Asn Arg Leu
355 360 365
Ser Thr Cys His Ile Glu Gly Asp Asp Leu His Ile Gln Arg Asn Val
370 375 380
Gln Lys Leu Lys Asp Thr Val Lys Lys Leu Gly Glu Ser Gly Glu Ile
385 390 395 400
Lys Ala Ile Gly Glu Leu Asp Leu Leu Phe Met Ser Leu Arg Asn Ala
405 410 415
Cys Ile
<210> 33
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 33
Met Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
275 280 285
Gly Gly Gly Ser Ala Pro Ile Ser Ser His Cys Arg Leu Asp Lys Ser
290 295 300
Asn Phe Gln Gln Pro Tyr Ile Thr Asn Arg Thr Phe Met Leu Ala Lys
305 310 315 320
Glu Ala Ser Leu Ala Asp Asn Asn Thr Asp Val Arg Leu Ile Gly Glu
325 330 335
Lys Leu Phe His Gly Val Ser Met Ser Glu Arg Cys Tyr Leu Met Lys
340 345 350
Gln Val Leu Asn Phe Thr Leu Glu Glu Val Leu Phe Pro Gln Ser Asp
355 360 365
Arg Phe Gln Pro Tyr Met Gln Glu Val Val Pro Phe Leu Ala Arg Leu
370 375 380
Ser Asn Arg Leu Ser Thr Cys His Ile Glu Gly Asp Asp Leu His Ile
385 390 395 400
Gln Arg Asn Val Gln Lys Leu Lys Asp Thr Val Lys Lys Leu Gly Glu
405 410 415
Ser Gly Glu Ile Lys Ala Ile Gly Glu Leu Asp Leu Leu Phe Met Ser
420 425 430
Leu Arg Asn Ala Cys Ile
435
<210> 34
<211> 418
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 34
Met Ala Pro Ile Ser Ser His Cys Arg Leu Asp Lys Ser Asn Phe Gln
1 5 10 15
Gln Pro Tyr Ile Thr Asn Arg Thr Phe Met Leu Ala Lys Glu Ala Ser
20 25 30
Leu Ala Asp Asn Asn Thr Asp Val Arg Leu Ile Gly Glu Lys Leu Phe
35 40 45
His Gly Val Ser Met Ser Glu Arg Cys Tyr Leu Met Lys Gln Val Leu
50 55 60
Asn Phe Thr Leu Glu Glu Val Leu Phe Pro Gln Ser Asp Arg Phe Gln
65 70 75 80
Pro Tyr Met Gln Glu Val Val Pro Phe Leu Ala Arg Leu Ser Asn Arg
85 90 95
Leu Ser Thr Cys His Ile Glu Gly Asp Asp Leu His Ile Gln Arg Asn
100 105 110
Val Gln Lys Leu Lys Asp Thr Val Lys Lys Leu Gly Glu Ser Gly Glu
115 120 125
Ile Lys Ala Ile Gly Glu Leu Asp Leu Leu Phe Met Ser Leu Arg Asn
130 135 140
Ala Cys Ile Gly Gly Gly Gly Ser Val Glu Glu Ala Leu Asn Ile Phe
145 150 155 160
Asp Glu Cys Arg Ser Pro Cys Ser Leu Thr Pro Glu Pro Gly Lys Pro
165 170 175
Ile Gln Ser Lys Leu Ser Ile Pro Ser Asp Val Val Leu Asp Glu Gly
180 185 190
Val Leu Tyr Tyr Ser Met Thr Ile Asn Asp Glu Gln Asn Asp Ile Lys
195 200 205
Asp Glu Asp Lys Gly Glu Ser Ile Ile Thr Ile Gly Glu Phe Ala Thr
210 215 220
Val Arg Ala Thr Arg His Tyr Val Asn Gln Asp Ala Pro Phe Gly Val
225 230 235 240
Ile His Leu Asp Ile Thr Thr Glu Asn Gly Thr Lys Thr Tyr Ser Tyr
245 250 255
Asn Arg Lys Glu Gly Glu Phe Ala Ile Asn Trp Leu Val Pro Ile Gly
260 265 270
Glu Asp Ser Pro Ala Ser Ile Lys Ile Ser Val Asp Glu Leu Asp Gln
275 280 285
Gln Arg Asn Ile Ile Glu Val Pro Lys Leu Tyr Ser Ile Asp Leu Asp
290 295 300
Asn Gln Thr Leu Glu Gln Trp Lys Thr Gln Gly Asn Val Ser Phe Ser
305 310 315 320
Val Thr Arg Pro Glu His Asn Ile Ala Ile Ser Trp Pro Ser Val Ser
325 330 335
Tyr Lys Ala Ala Gln Lys Glu Gly Ser Arg His Lys Arg Trp Ala His
340 345 350
Trp His Thr Gly Leu Ala Leu Cys Trp Leu Val Pro Met Asp Ala Ile
355 360 365
Tyr Asn Tyr Ile Thr Gln Gln Asn Cys Thr Leu Gly Asp Asn Trp Phe
370 375 380
Gly Gly Ser Tyr Glu Thr Val Ala Gly Thr Pro Lys Val Ile Thr Val
385 390 395 400
Lys Gln Gly Ile Glu Gln Lys Pro Val Glu Gln Arg Ile His Phe Ser
405 410 415
Lys Gly
<210> 35
<211> 538
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 35
Met Val Glu Glu Ala Leu Asn Ile Phe Asp Glu Cys Arg Ser Pro Cys
1 5 10 15
Ser Leu Thr Pro Glu Pro Gly Lys Pro Ile Gln Ser Lys Leu Ser Ile
20 25 30
Pro Ser Asp Val Val Leu Asp Glu Gly Val Leu Tyr Tyr Ser Met Thr
35 40 45
Ile Asn Asp Glu Gln Asn Asp Ile Lys Asp Glu Asp Lys Gly Glu Ser
50 55 60
Ile Ile Thr Ile Gly Glu Phe Ala Thr Val Arg Ala Thr Arg His Tyr
65 70 75 80
Val Asn Gln Asp Ala Pro Phe Gly Val Ile His Leu Asp Ile Thr Thr
85 90 95
Glu Asn Gly Thr Lys Thr Tyr Ser Tyr Asn Arg Lys Glu Gly Glu Phe
100 105 110
Ala Ile Asn Trp Leu Val Pro Ile Gly Glu Asp Ser Pro Ala Ser Ile
115 120 125
Lys Ile Ser Val Asp Glu Leu Asp Gln Gln Arg Asn Ile Ile Glu Val
130 135 140
Pro Lys Leu Tyr Ser Ile Asp Leu Asp Asn Gln Thr Leu Glu Gln Trp
145 150 155 160
Lys Thr Gln Gly Asn Val Ser Phe Ser Val Thr Arg Pro Glu His Asn
165 170 175
Ile Ala Ile Ser Trp Pro Ser Val Ser Tyr Lys Ala Ala Gln Lys Glu
180 185 190
Gly Ser Arg His Lys Arg Trp Ala His Trp His Thr Gly Leu Ala Leu
195 200 205
Cys Trp Leu Val Pro Met Asp Ala Ile Tyr Asn Tyr Ile Thr Gln Gln
210 215 220
Asn Cys Thr Leu Gly Asp Asn Trp Phe Gly Gly Ser Tyr Glu Thr Val
225 230 235 240
Ala Gly Thr Pro Lys Val Ile Thr Val Lys Gln Gly Ile Glu Gln Lys
245 250 255
Pro Val Glu Gln Arg Ile His Phe Ser Lys Gly Asn Ala Met Ser Ala
260 265 270
Leu Ala Ala His Arg Val Cys Gly Val Pro Leu Glu Thr Leu Ala Arg
275 280 285
Ser Arg Lys Pro Arg Asp Leu Thr Asp Asp Leu Ser Cys Ala Tyr Gln
290 295 300
Ala Gln Asn Ile Val Ser Leu Phe Val Ala Thr Arg Ile Leu Phe Ser
305 310 315 320
His Leu Asp Ser Val Phe Thr Leu Asn Leu Asp Glu Gln Glu Pro Glu
325 330 335
Val Ala Glu Arg Leu Ser Asp Leu Arg Arg Ile Asn Glu Asn Asn Pro
340 345 350
Gly Met Val Thr Gln Val Leu Thr Val Ala Arg Gln Ile Tyr Asn Asp
355 360 365
Tyr Val Thr His His Pro Gly Leu Thr Pro Glu Gln Thr Ser Ala Gly
370 375 380
Ala Gln Ala Gly Gly Gly Gly Ser Ala Pro Ile Ser Ser His Cys Arg
385 390 395 400
Leu Asp Lys Ser Asn Phe Gln Gln Pro Tyr Ile Thr Asn Arg Thr Phe
405 410 415
Met Leu Ala Lys Glu Ala Ser Leu Ala Asp Asn Asn Thr Asp Val Arg
420 425 430
Leu Ile Gly Glu Lys Leu Phe His Gly Val Ser Met Ser Glu Arg Cys
435 440 445
Tyr Leu Met Lys Gln Val Leu Asn Phe Thr Leu Glu Glu Val Leu Phe
450 455 460
Pro Gln Ser Asp Arg Phe Gln Pro Tyr Met Gln Glu Val Val Pro Phe
465 470 475 480
Leu Ala Arg Leu Ser Asn Arg Leu Ser Thr Cys His Ile Glu Gly Asp
485 490 495
Asp Leu His Ile Gln Arg Asn Val Gln Lys Leu Lys Asp Thr Val Lys
500 505 510
Lys Leu Gly Glu Ser Gly Glu Ile Lys Ala Ile Gly Glu Leu Asp Leu
515 520 525
Leu Phe Met Ser Leu Arg Asn Ala Cys Ile
530 535
<210> 36
<211> 75
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<221> MISC_FEATURE
<222> (1)..(75)
<223> This sequence may encompass 1-15 "Gly Gly Gly Gly Ser"
repeating units
<400> 36
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
35 40 45
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
50 55 60
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75
<210> 37
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 37
Ser Ile Ala Lys Gln Ser
1 5
<210> 38
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 38
Ser Ile Ala Lys Gln Ser Ile Ala Lys Gln Ser
1 5 10
<210> 39
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 39
Val Val Lys Glu Ala Ile
1 5
<210> 40
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<221> MISC_FEATURE
<222> (1)..(30)
<223> This sequence may encompass 1-15 "Gly Ser"
repeating units
<400> 40
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
1 5 10 15
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
20 25 30
<210> 41
<211> 45
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<221> MISC_FEATURE
<222> (1)..(45)
<223> This sequence may encompass 1-15 "Gly Gly Ser"
repeating units
<400> 41
Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly
1 5 10 15
Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly
20 25 30
Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser
35 40 45
Claims (45)
- 서열번호: 15 또는 서열번호: 17에 제시된 아미노산 서열을 포함하는 전달 구조체.
- 제 1항에 있어서, 전달 구조체는 서열번호: 15에 제시된 아미노산 서열을 포함하는 것을 특징으로 하는, 전달 구조체.
- 제 1항에 있어서, 전달 구조체는 서열번호: 17에 제시된 아미노산 서열을 포함하는 것을 특징으로 하는, 전달 구조체.
- 담체를 포함하는 전달 구조체로서, 담체는
위치 195 내지 347 중 어느 하나에서 이의 C-말단을 가지며;
위치 3에서 글루탐산 및 위치 4에서 알라닌을 갖고;
편광 상피 세포를 가로질러 통과세포외배출할 수 있는 것을 특징으로 하는, 전달 구조체. - 제 4항에 있어서, 담체는 길이가 266 아미노산인 것을 특징으로 하는, 전달 구조체.
- 제 4항 또는 제 5항에 있어서, 담체는 서열번호: 7 또는 서열번호: 9에 제시된 아미노산 서열, 또는 이와 적어도 90%, 95% 또는 99% 서열 동일성을 갖는 아미노산 서열로 이루어지는 것을 특징으로 하는, 전달 구조체.
- 제 6항에 있어서, 담체는 서열번호: 7에 제시된 아미노산 서열로 이루어지는 것을 특징으로 하는, 전달 구조체.
- 제 6항에 있어서, 담체는 서열번호: 9에 제시된 아미노산 서열로 이루어지는 것을 특징으로 하는, 전달 구조체.
- 제 4항 내지 제 8항 중 어느 한 항에 있어서, 담체는 페이로드에 결합되는 것을 특징으로 하는, 전달 구조체.
- 제 9항에 있어서, 페이로드는 IL-22인 것을 특징으로 하는, 전달 구조체.
- 제 10항에 있어서, IL-22는 서열번호: 11에 제시된 아미노산 서열로 이루어지는 것을 특징으로 하는, 전달 구조체.
- 제 9항 내지 제 11항 중 어느 한 항에 있어서, 담체는 IL-22에 비-공유 결합된 것을 특징으로 하는, 전달 구조체.
- 제 9항 내지 제 11항 중 어느 한 항에 있어서, 담체는 IL-22에 공유 결합된 것을 특징으로 하는, 전달 구조체.
- 제 13항에 있어서, 담체는 스페이서를 통해 IL-22에 공유 결합된 것을 특징으로 하는, 전달 구조체.
- 제 14항에 있어서, 스페이서는 서열번호: 13에 제시된 아미노산 서열로 이루어지는 것을 특징으로 하는, 전달 구조체.
- 제 1항 내지 제 15항 중 어느 한 항에 있어서, 전달 구조체는 서열번호: 15 또는 서열번호: 17에 제시된 아미노산 서열로 이루어지는 것을 특징으로 하는, 전달 구조체.
- 피험자에서 염증성 질환의 치료 방법으로서, 방법은 유효량의 제 1항 내지 제 16항 중 어느 한 항의 전달 구조체를 피험자에게 투여하는 단계를 포함하는, 방법.
- 제 17항에 있어서, 염증성 질환은 간염, 비만, 지방간 질환, 간 염증. 또는 췌장염, 크론병, 궤양성 대장염, 주머니염(pouchitis), 직장염(proctitis), 다발성 경화증, 전신 홍반성 루푸스(systemic lupus erythematosus), 이식편 대 숙주 질환 (graft versus host disease), 류마티스 관절염, 또는 건선인 것을 특징으로 하는, 방법.
- 제 18항에 있어서, 질환은 크론병 또는 궤양성 대장염인 것을 특징으로 하는, 방법.
- 정제된 비-자연적으로 발생하는 융합 단백질을 얻는 방법으로서, 방법은
비-자연적으로 발생하는 융합 단백질을 포함하는 혼합물에 대해 음이온 교환 크로마토그래피를 수행하여 비-자연적으로 발생하는 융합 단백질을 포함하는 제 1 분획을 얻는 단계를 포함하고;
여기서 비-자연적으로 발생하는 융합 단백질은 IL-22 및 담체를 포함하는 것을 특징으로 하는, 방법. - 제 20항에 있어서, 음이온 교환 크로마토그래피를 수행하는 단계는 음이온성 교환 수지에 비-자연적으로 발생하는 융합 단백질을 결합하고 비-자연적으로 발생하는 융합 단백질의 후속 용리를 위해 증가하는 염 구배를 제공하여 제 1 분획을 얻는 단계를 포함하는 것을 특징으로 하는, 방법.
- 제 20항 내지 제 21항 중 어느 한 항에 있어서, 음이온 교환 크로마토그래피를 수행하는 단계는 혼합물을 아민-작용화된 폴리메타크릴레이트 비드를 포함하는 수지와 접촉시키는 단계를 포함하는 것을 특징으로 하는, 방법.
- 제 22항에 있어서, 수지는 NH2-750F 수지인 것을 특징으로 하는, 방법.
- 제 20항 내지 제 23항 중 어느 한 항에 있어서, 음이온 교환 크로마토그래피를 수행하기 전에 비-자연적으로 발생하는 융합 단백질을 재접힘하는 단계를 더 포함하는, 방법.
- 제 24항에 있어서, 비-자연적으로 발생하는 융합 단백질을 재접힘하는 단계는 봉입체(inclusion bodies)로부터의 카오트로프(chaotrope)-가용화된 단백질을 재접힘 용액과 접촉시키는 단계를 포함하며,
여기서 재접힘 용액은 아르기닌 (0.75 M 내지 1.25 M); 글리세롤 (2% 내지 20% v/v); 시스테인 (0.5 mM 내지 10 mm); 및 시스타민 (0.2 mM 내지 10 mM)을 포함하고;
재접힘 용액은 7.5 내지 8.5의 pH를 갖는 것을 특징으로 하는, 방법. - 제 25항에 있어서, 아르기닌은 0.9 M 내지 1.1 M의 농도로 재접힘 용액에 존재하며; 글리세롤은 7% 내지 13% (w/w)의 농도로 재접힘 용액에 존재하고; 시스테인은 1.5 mM 내지 6 mM의 농도로 재접힘 용액에 존재하며; 시스타민은 0.6 mM 내지 3 mM의 농도로 재접힘 용액에 존재하고; 재접힘 용액은 7.8 내지 8.2의 pH를 갖는 것을 특징으로 하는, 방법.
- 제 20항 내지 제 26항 중 어느 한 항에 있어서, 제 1 분획을 포함하는 시료를 히드록시아파타이트 수지로 처리하여 비-자연적으로 발생하는 융합 단백질을 포함하는 제 2 분획을 얻는 단계를 더 포함하는, 방법.
- 제 27항에 있어서, 히드록시아파타이트 수지는 CaPure-히드록시아파타이트 수지인 것을 특징으로 하는, 방법.
- 제 20항 내지 제 26항 중 어느 한 항에 있어서, 제 1 분획을 포함하는 시료에 대해 양이온 교환 크로마토그래피를 수행하는 단계를 더 포함하는, 방법.
- 제 29항에 있어서, 양이온 교환 크로마토그래피를 수행하는 단계는 제 1 분획을 포함하는 시료를 설페이트-작용화된 폴리메타크릴레이트 비드를 포함하는 수지와 접촉시키는 단계를 포함하는 것을 특징으로 하는, 방법.
- 제 30항에 있어서, 수지는 TOYOPEARL 설페이트-650F 수지인 것을 특징으로 하는, 방법.
- 제 20항 내지 제 31항 중 어느 한 항에 있어서, 세포와 접촉시, 담체는 비-자연적으로 발생하는 융합 단백질의 세포내이입 또는 통과세포외배출을 촉진시키는 것을 특징으로 하는, 방법.
- 제 32항에 있어서, 세포와 접촉시, 담체는 비-자연적으로 발생하는 융합 단백질의 통과세포외배출을 촉진시키는 것을 특징으로 하는, 방법.
- 제 32항 또는 제 33항에 있어서, 세포는 장 상피 세포인 것을 특징으로 하는, 방법.
- 제 34항에 있어서, 장 상피 세포는 편광 장 상피 세포인 것을 특징으로 하는, 방법.
- 제 20항 내지 제 35항 중 어느 한 항에 있어서, 담체는 자연적으로 발생하는 또는 비-자연적으로 발생하는 콜릭스 폴리펩티드의 절단된 변이체인 것을 특징으로 하는, 방법.
- 제 20항 내지 제 36항 중 어느 한 항에 있어서, 담체는 서열번호: 2, 3, 4, 5, 6, 7, 8, 9, 22, 또는 23 중 어느 하나와 적어도 70%, 80%, 85%, 90%, 95%, 98%, 99%, 또는 100% 서열 동일성을 갖는 것을 특징으로 하는, 방법.
- 제 20항 내지 제 37항 중 어느 한 항에 있어서, 비-자연적으로 발생하는 융합 단백질은 서열번호: 14-21 중 어느 하나의 서열과 적어도 70%, 80%, 85%, 90%, 95%, 98%, 99%, 또는 100% 서열 동일성을 갖는 것을 특징으로 하는, 방법.
- 제 20항 내지 제 38항 중 어느 한 항에 있어서, IL-22는 서열번호: 10, 11, 또는 12 중 어느 하나와 적어도 85%, 90%, 95%, 98%, 99% 또는 100% 서열 동일성을 갖는 것을 특징으로 하는, 방법.
- 제 20항 내지 제 39항 중 어느 한 항에 있어서, 담체는 그 자체로 제 1 등전점 (pI)을 가지며, IL-22는 그 자체로 제 2 등전점을 가지며, 여기서 제 1 등전점은 제 2 등전점보다 낮은 적어도 1 pH 단위, 적어도 1.5 pH 단위, 적어도 1.7 pH 단위, 또는 적어도 2 pH 단위인 것을 특징으로 하는, 방법.
- 제 20항 내지 제 41항 중 어느 한 항의 방법으로 얻어진 비-자연적으로 발생하는 융합 단백질.
- 담체 및 IL-22를 포함하는 비-자연적으로 발생하는 융합 단백질을 재접힘하는 방법으로서, 방법은
(i) 비-자연적으로 발생하는 융합 단백질을 포함하는 봉입체를 카오트로픽제를 포함하는 가용화 용액과 접촉시켜 가용성 비-자연적으로 발생하는 융합 단백질을 제조하는 단계;
(ii) 비-자연적으로 발생하는 융합 단백질을 재접힘 용액과 접촉시키는 단계를 포함하며,
여기서 재접힘 용액은 아르기닌 (0.75 M 내지 1.25 M); 글리세롤 (2% 내지 20% v/v); 시스테인 (0.5 mM 내지 10 mm); 및 시스타민 (0.2 mM 내지 10 mM)을 포함하고; 재접힘 용액은 7.5 내지 8.5의 pH를 갖는 것을 특징으로 하는, 방법. - 제 42항에 있어서, 아르기닌은 0.9 M 내지 1.1 M의 농도로 재접힘 용액에 존재하며; 글리세롤은 7% 내지 13% (w/w)의 농도로 재접힘 용액에 존재하고; 시스테인은 1.5 mM 내지 6 mM의 농도로 재접힘 용액에 존재하며; 시스타민은 0.6 mM 내지 3 mM의 농도로 재접힘 용액에 존재하고; 재접힘 용액은 7.8 내지 8.2의 pH를 갖는 것을 특징으로 하는, 방법.
- 페이로드에 결합된 콜릭스 폴리펩티드를 포함하는 전달 구조체로서,
콜릭스 폴리펩티드는 위치 195 내지 347 중 어느 하나에서 이의 C-말단을 가지며, 편광 상피 세포를 가로질러 통과세포외배출할 수 있는 것을 특징으로 하는, 전달 구조체. - 제 44항에 있어서, 콜릭스 폴리펩티드는 페이로드에 이종 결합된 것을 특징으로 하는, 전달 구조체.
Applications Claiming Priority (11)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862756889P | 2018-11-07 | 2018-11-07 | |
| US62/756,889 | 2018-11-07 | ||
| USPCT/US2019/021474 | 2019-03-08 | ||
| PCT/US2019/021474 WO2019173787A1 (en) | 2018-03-08 | 2019-03-08 | Toxin-derived delivery constructs for oral delivery |
| US201962888133P | 2019-08-16 | 2019-08-16 | |
| US201962888238P | 2019-08-16 | 2019-08-16 | |
| US62/888,238 | 2019-08-16 | ||
| US62/888,133 | 2019-08-16 | ||
| USPCT/US2019/050708 | 2019-09-11 | ||
| PCT/US2019/050708 WO2020096695A1 (en) | 2018-11-07 | 2019-09-11 | Cholix-derived carriers for oral delivery of heterologous payload |
| PCT/US2019/060356 WO2020097394A1 (en) | 2018-11-07 | 2019-11-07 | Delivery constructs for transcytosis and related methods |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20210110294A true KR20210110294A (ko) | 2021-09-07 |
Family
ID=70612266
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020217017210A KR20210110294A (ko) | 2018-11-07 | 2019-11-07 | 통과세포외배출용 전달 구조체 및 관련 방법 |
Country Status (20)
| Country | Link |
|---|---|
| US (2) | US11027020B2 (ko) |
| EP (2) | EP4083058A3 (ko) |
| JP (1) | JP2022506990A (ko) |
| KR (1) | KR20210110294A (ko) |
| CN (1) | CN113423722A (ko) |
| AU (1) | AU2019377117A1 (ko) |
| BR (1) | BR112021009003A2 (ko) |
| CA (1) | CA3119060A1 (ko) |
| CL (1) | CL2021001209A1 (ko) |
| CO (1) | CO2021007402A2 (ko) |
| DK (1) | DK3650037T3 (ko) |
| EA (1) | EA202191280A1 (ko) |
| ES (1) | ES2911075T3 (ko) |
| IL (1) | IL282987B2 (ko) |
| MX (1) | MX2021005346A (ko) |
| PL (1) | PL3650037T3 (ko) |
| PT (1) | PT3650037T (ko) |
| SG (1) | SG11202104721RA (ko) |
| TW (1) | TW202031678A (ko) |
| WO (1) | WO2020097394A1 (ko) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11246915B2 (en) | 2010-09-15 | 2022-02-15 | Applied Molecular Transport Inc. | Cholix toxin-derived fusion molecules for oral delivery of biologically active cargo |
| DK3762009T3 (da) | 2018-03-08 | 2022-06-20 | Applied Molecular Transport Inc | Toxin-afledte indgivelseskonstrukter til oral indgivelse |
| WO2020096695A1 (en) | 2018-11-07 | 2020-05-14 | Applied Molecular Transport Inc. | Cholix-derived carriers for oral delivery of heterologous payload |
| ES2911075T3 (es) | 2018-11-07 | 2022-05-17 | Applied Molecular Transport Inc | Constructos de administración para transcitosis y métodos relacionados |
| CN114599665A (zh) | 2019-08-16 | 2022-06-07 | 应用分子转运公司 | 组合物、制剂及白细胞介素产生和纯化 |
| WO2021252687A2 (en) * | 2020-06-09 | 2021-12-16 | Icosavax, Inc. | Method of making virus-like particle |
| CN117603361A (zh) * | 2022-08-22 | 2024-02-27 | 复旦大学附属儿科医院 | 包含angptl3单抗的融合蛋白 |
Family Cites Families (43)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5668255A (en) | 1984-06-07 | 1997-09-16 | Seragen, Inc. | Hybrid molecules having translocation region and cell-binding region |
| US6022950A (en) | 1984-06-07 | 2000-02-08 | Seragen, Inc. | Hybrid molecules having translocation region and cell-binding region |
| ATE66469T1 (de) | 1985-01-14 | 1991-09-15 | Neorx Corp | Metall-radionuklid markiertes protein fuer diagnose und therapie. |
| US6051405A (en) | 1986-09-24 | 2000-04-18 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Constructs encoding recombinant antibody-toxin fusion proteins |
| US4892827A (en) | 1986-09-24 | 1990-01-09 | The United States Of America As Represented By The Department Of Health And Human Services | Recombinant pseudomonas exotoxins: construction of an active immunotoxin with low side effects |
| ATE412009T1 (de) * | 2000-08-24 | 2008-11-15 | Genentech Inc | Methode zur inhibierung von il-22 induziertem pap1 |
| EP1379273B1 (en) | 2000-11-27 | 2009-09-16 | Powderject Vaccines, Inc. | Nucleic acid adjuvants |
| US6673574B2 (en) | 2000-11-30 | 2004-01-06 | Unigene Laboratories Inc. | Oral delivery of peptides using enzyme-cleavable membrane translocators |
| US20050074462A1 (en) | 2001-05-23 | 2005-04-07 | Duotol Ab | Supression of allergic reactions by transdermal administration of allergens conjugated to cholera toxin or fragments thereof |
| RU2006101702A (ru) * | 2003-06-23 | 2006-09-10 | Дженетикс Инститьют, Ллс (Us) | Антитела против интерлейкина-22 и их применения |
| EP1522585A1 (en) | 2003-10-09 | 2005-04-13 | Plant Research International B.V. | Chimeric carrier molecules for the production of mucosal vaccines |
| US7713737B2 (en) | 2004-10-04 | 2010-05-11 | Trinity Biosystems, Inc. | Methods and compositions for needleless delivery of macromolecules |
| WO2006135428A2 (en) | 2004-10-04 | 2006-12-21 | Trinity Biosystems, Inc. | Methods and compositions for inducing an immune response against multiple antigens |
| WO2007067597A2 (en) | 2005-12-05 | 2007-06-14 | Trinity Biosystems, Inc. | Methods and compositions for needleless delivery of binding partners |
| WO2008011157A2 (en) * | 2006-07-20 | 2008-01-24 | The General Hospital Corporation | Methods, compositions, and kits for the selective activation of protoxins through combinatorial targeting |
| US20090092660A1 (en) | 2006-08-09 | 2009-04-09 | Trinity Biosystems, Inc. | Methods and compositions for needleless delivery of particles |
| WO2008063910A2 (en) | 2006-11-08 | 2008-05-29 | Novavax, Inc. | Method of preparing solid dosage forms of multi-phasic pharmaceutical compositions |
| WO2009014650A2 (en) * | 2007-07-20 | 2009-01-29 | The General Hospital Corporation | Recombinant vibrio cholerae exotoxins |
| CN101361968B (zh) | 2007-08-06 | 2011-08-03 | 健能隆医药技术(上海)有限公司 | 白介素-22在治疗脂肪肝中的应用 |
| WO2009149281A1 (en) | 2008-06-04 | 2009-12-10 | The Government Of The United States Of America, As Represented By The Secretary Of The Department Of Health And Human Services | Immunotoxins and uses thereof |
| NO2344540T3 (ko) | 2008-10-02 | 2018-04-28 | ||
| SG176963A1 (en) * | 2009-06-22 | 2012-02-28 | Amgen Inc | Refolding proteins using a chemically controlled redox state |
| CA2768598A1 (en) | 2009-07-22 | 2011-01-27 | Cenix Bioscience Gmbh | Delivery system and conjugates for compound delivery via naturally occurring intracellular transport routes |
| WO2011031441A1 (en) | 2009-08-28 | 2011-03-17 | The Government Of The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Therapy with a chimeric molecule and a pro-apoptotic agent |
| MX354016B (es) * | 2010-09-15 | 2018-02-07 | J Mrsny Randall | Sistemas y metodos de suministro de agentes bioactivos mediante el uso de secuencias transportadoras derivadas de toxinas. |
| CA2825023A1 (en) | 2011-01-26 | 2012-08-02 | Cenix Bioscience Gmbh | Delivery system and conjugates for compound delivery via naturally occurring intracellular transport routes |
| CN109008910A (zh) | 2011-06-29 | 2018-12-18 | 拉尼医疗有限公司 | 用于使用可吞服药物递送装置递送到肠道内腔中的治疗药剂制剂 |
| TR201809571T4 (tr) | 2013-03-15 | 2018-07-23 | Hoffmann La Roche | Ll-22 polipeptidleri ile ıl-22 fc füzyon proteinleri ve kullanım yöntemleri. |
| CN104623637A (zh) | 2013-11-07 | 2015-05-20 | 健能隆医药技术(上海)有限公司 | Il-22二聚体在制备静脉注射药物中的应用 |
| AU2014346554B2 (en) | 2013-11-07 | 2020-06-04 | Evive Biotechnology (Shanghai) Ltd | Methods of use for IL-22 in the treatment of gastrointestinal graft vs. host disease |
| WO2015086733A1 (en) | 2013-12-13 | 2015-06-18 | Sanofi | Dual glp-1/glucagon receptor agonists |
| RU2016132342A (ru) | 2014-01-09 | 2018-02-14 | Санофи | Стабилизированные фармацевтические составы на основе инсулиновых аналогов и/или инсулиновых производных |
| BR112016025866A2 (pt) | 2014-05-07 | 2017-12-12 | Applied Molecular Transp Llc | composição farmacêutica, método para tratar uma doença anti-inflamatória em um indivíduo, método para tratar uma doença autoimune em um indivíduo, método para tratar um câncer em um indivíduo, uso de uma molécula de fusão que não ocorre naturalmente, método para tratar um distúrbio metabólico em um indivíduo, método para tratar uma doença hepática gordurosa em um indivíduo, método para tratar um distúrbio de deficiência de hormônio de crescimentoem um indivíduo, e, polinucleotídeo que codifica uma molécula de fusão |
| JP6675394B2 (ja) | 2014-10-22 | 2020-04-01 | アルモ・バイオサイエンシーズ・インコーポレイテッド | 疾患及び障害の治療のためにインターロイキン−10を使用する方法 |
| CN107108712A (zh) * | 2014-12-23 | 2017-08-29 | 阿尔莫生物科技股份有限公司 | 提高重组蛋白产量的方法 |
| EP3192805A1 (en) | 2016-01-15 | 2017-07-19 | Humanitas Mirasole S.p.A. | Inhibitors of t cell activation or stimulation and uses thereof |
| JP7084881B2 (ja) | 2016-06-22 | 2022-06-15 | アルカームス インコーポレーテッド | Il-10の免疫刺激特性および抗炎症特性を調節するための組成物および方法 |
| CA3045310A1 (en) | 2016-12-14 | 2018-06-21 | Progenity, Inc. | Treatment of a disease of the gastrointestinal tract with a chemokine/chemokine receptor inhibitor |
| JP2020513280A (ja) | 2016-12-14 | 2020-05-14 | プロジェニティ, インコーポレイテッド | 消化管疾病の免疫抑制剤による治療 |
| WO2019173787A1 (en) * | 2018-03-08 | 2019-09-12 | Applied Molecular Transport Inc. | Toxin-derived delivery constructs for oral delivery |
| ES2911075T3 (es) | 2018-11-07 | 2022-05-17 | Applied Molecular Transport Inc | Constructos de administración para transcitosis y métodos relacionados |
| US20200140511A1 (en) | 2018-11-07 | 2020-05-07 | Applied Molecular Transport Inc. | Delivery constructs for transcytosis and related methods |
| WO2020096695A1 (en) | 2018-11-07 | 2020-05-14 | Applied Molecular Transport Inc. | Cholix-derived carriers for oral delivery of heterologous payload |
-
2019
- 2019-11-07 ES ES19207825T patent/ES2911075T3/es active Active
- 2019-11-07 CN CN201980088287.9A patent/CN113423722A/zh active Pending
- 2019-11-07 BR BR112021009003-7A patent/BR112021009003A2/pt unknown
- 2019-11-07 CA CA3119060A patent/CA3119060A1/en active Pending
- 2019-11-07 WO PCT/US2019/060356 patent/WO2020097394A1/en active Application Filing
- 2019-11-07 PL PL19207825T patent/PL3650037T3/pl unknown
- 2019-11-07 TW TW108140533A patent/TW202031678A/zh unknown
- 2019-11-07 EP EP22159495.5A patent/EP4083058A3/en not_active Withdrawn
- 2019-11-07 DK DK19207825.1T patent/DK3650037T3/da active
- 2019-11-07 EA EA202191280A patent/EA202191280A1/ru unknown
- 2019-11-07 KR KR1020217017210A patent/KR20210110294A/ko unknown
- 2019-11-07 PT PT192078251T patent/PT3650037T/pt unknown
- 2019-11-07 JP JP2021525169A patent/JP2022506990A/ja active Pending
- 2019-11-07 AU AU2019377117A patent/AU2019377117A1/en active Pending
- 2019-11-07 MX MX2021005346A patent/MX2021005346A/es unknown
- 2019-11-07 EP EP19207825.1A patent/EP3650037B1/en active Active
- 2019-11-07 SG SG11202104721RA patent/SG11202104721RA/en unknown
-
2020
- 2020-06-15 US US16/902,256 patent/US11027020B2/en active Active
-
2021
- 2021-04-20 US US17/235,567 patent/US20210338828A1/en not_active Abandoned
- 2021-05-06 IL IL282987A patent/IL282987B2/en unknown
- 2021-05-07 CL CL2021001209A patent/CL2021001209A1/es unknown
- 2021-06-07 CO CONC2021/0007402A patent/CO2021007402A2/es unknown
Also Published As
| Publication number | Publication date |
|---|---|
| IL282987B2 (en) | 2023-02-01 |
| BR112021009003A2 (pt) | 2021-08-17 |
| ES2911075T3 (es) | 2022-05-17 |
| PL3650037T3 (pl) | 2022-06-06 |
| JP2022506990A (ja) | 2022-01-17 |
| US20210338828A1 (en) | 2021-11-04 |
| WO2020097394A1 (en) | 2020-05-14 |
| CO2021007402A2 (es) | 2021-09-30 |
| IL282987B (en) | 2022-10-01 |
| AU2019377117A1 (en) | 2021-06-10 |
| EA202191280A1 (ru) | 2021-12-27 |
| US20200306383A1 (en) | 2020-10-01 |
| EP3650037A1 (en) | 2020-05-13 |
| PT3650037T (pt) | 2022-06-27 |
| US11027020B2 (en) | 2021-06-08 |
| CN113423722A (zh) | 2021-09-21 |
| MX2021005346A (es) | 2021-10-13 |
| CL2021001209A1 (es) | 2021-11-19 |
| IL282987A (en) | 2021-06-30 |
| EP3650037B1 (en) | 2022-03-02 |
| TW202031678A (zh) | 2020-09-01 |
| SG11202104721RA (en) | 2021-06-29 |
| EP4083058A3 (en) | 2023-01-11 |
| DK3650037T3 (da) | 2022-05-02 |
| CA3119060A1 (en) | 2020-05-14 |
| EP4083058A2 (en) | 2022-11-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20210110294A (ko) | 통과세포외배출용 전달 구조체 및 관련 방법 | |
| US20200140511A1 (en) | Delivery constructs for transcytosis and related methods | |
| TWI508736B (zh) | 結合至il-23之以纖維連接蛋白為主之架構域蛋白質 | |
| van Veen et al. | Characterization of recombinant human C1 inhibitor secreted in milk of transgenic rabbits | |
| US10874724B2 (en) | Enzymatic immunomodulation of solid tumors and uses thereof | |
| US20180185455A1 (en) | Preparation comprising factor viii and von willebrand factor peptides | |
| US20240124535A1 (en) | Designed ankyrin repeat domain with improved stability | |
| Binder et al. | PASylated thymosin α1: a long-acting immunostimulatory peptide for applications in oncology and virology | |
| EP3642338B1 (en) | Fusion protein with half-life extending polypeptide | |
| JP6231559B2 (ja) | 高グリコシル化された持続型ヒト成長ホルモンタンパク質の製造方法及び精製方法 | |
| KR20220095204A (ko) | 혈청 알부민과 성장 호르몬의 융합 단백질을 함유하는 수성 의약 조성물 | |
| US20150329606A1 (en) | Method for preparing c1q recombinant protein | |
| EA043603B1 (ru) | Конструкции для доставки для трансцитоза и связанные способы | |
| Collin et al. | The targeting, docking and anti-proteolysis functions of the secretin chaperone PulS | |
| WO2021205150A1 (en) | An enzyme | |
| JPWO2020097394A5 (ko) | ||
| WO2020109978A1 (en) | Lpl-gpihbp1 fusion polypeptides | |
| JP4599028B2 (ja) | 新規な炎症性疾患改善剤 | |
| US20240076345A1 (en) | Human glp-1 polypeptide variant and use thereof | |
| KR20240029769A (ko) | 융합단백질 및 이의 응용 | |
| WO2022195629A1 (en) | Engineered arginase constructs, method of generation and uses thereof | |
| Sadavarte | Biophysical Characterization and Bioprocessing of Proteins | |
| EP2138508A1 (en) | Met agonists | |
| WO2024006563A1 (en) | Il-12 mutants with reduced toxicity, compositions thereof and methods of using the same |