KR20180123731A - 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 - Google Patents
조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 Download PDFInfo
- Publication number
- KR20180123731A KR20180123731A KR1020187032456A KR20187032456A KR20180123731A KR 20180123731 A KR20180123731 A KR 20180123731A KR 1020187032456 A KR1020187032456 A KR 1020187032456A KR 20187032456 A KR20187032456 A KR 20187032456A KR 20180123731 A KR20180123731 A KR 20180123731A
- Authority
- KR
- South Korea
- Prior art keywords
- peptide
- peptides
- amino acid
- seq
- tissue
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1816—Erythropoietin [EPO]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K9/00—Peptides having up to 20 amino acids, containing saccharide radicals and having a fully defined sequence; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/10—Peptides having 12 to 20 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/14—Prodigestives, e.g. acids, enzymes, appetite stimulants, antidyspeptics, tonics, antiflatulents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/02—Drugs for disorders of the urinary system of urine or of the urinary tract, e.g. urine acidifiers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/08—Drugs for genital or sexual disorders; Contraceptives for gonadal disorders or for enhancing fertility, e.g. inducers of ovulation or of spermatogenesis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
- A61P31/06—Antibacterial agents for tuberculosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/02—Antidotes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
- C07K14/505—Erythropoietin [EPO]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/06—Linear peptides containing only normal peptide links having 5 to 11 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Molecular Biology (AREA)
- Zoology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Toxicology (AREA)
- Immunology (AREA)
- Diabetes (AREA)
- Epidemiology (AREA)
- Neurology (AREA)
- Physical Education & Sports Medicine (AREA)
- Urology & Nephrology (AREA)
- Biomedical Technology (AREA)
- Neurosurgery (AREA)
- Cardiology (AREA)
- Endocrinology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Hematology (AREA)
- Rheumatology (AREA)
- Heart & Thoracic Surgery (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Reproductive Health (AREA)
Abstract
본 발명은 잠재적으로 바람직하지 않은 조혈 효과를 거의 또는 전혀 갖지 않으면서 조직 보호 활성을 갖는 펩티드 및 펩티드 유사체를 제공한다. 상기 펩티드 및 펩티드 유사체는 다양한 조직 손상 관련 질환 및 장애의 예방 및 치료에 유용하다.
Description
본 출원은 미국 가출원 제61/062,012호 (2008년 1월 22일자로 출원됨), 제61/062,022호 (2008년 1월 22일자로 출원됨); 제61/062,045호 (2008년 1월 22일자로 출원됨); 제61/133,912호 (2008년 7월 3일자로 출원됨); 및 제61/203,890호 (2008년 12월 30일자로 출원됨)의 우선권 이익을 주장하며, 이로써 이들의 내용은 그 전문이 본원에 참조로 포함된다.
1. 서문
본 발명은 조직 손상과 연관된 질환 또는 장애 및/또는 그의 손상, 영향 또는 증상, 예를 들어 암, 염증, 및 독성제로의 노출 (이들로 한정되지는 않음)의 예방 또는 치료를 위한 조직 보호 펩티드 및 펩티드 유사체를 제공한다. 특히, 본 발명은 전장 리간드의 잠재적으로 바람직하지 않은 조혈 작용이 거의 또는 전혀 없는 I형 사이토킨 수용체 리간드의 단편과 컨센서스 서열을 공유하는 조직 보호 펩티드 및 펩티드 유사체를 제공한다.
상기 펩티드는 또한, 단편, 키메라, 및 조직 보호 수용체 리간드 (예를 들면, EPO)내 핵심 아미노산 잔기들의 공간적 국소화를 모방하도록 설계된 펩티드를 포함한다. 본 발명은 또한, 조직 손상과 연관된 질환 또는 장애의 치료, 예방 또는 개선을 목적으로, 상기 질환 또는 장애로 인한 증상 및/또는 대상체의 반응을 조절하기 위한 방법 및 상기 펩티드의 용도를 제공한다.
또한, 본 발명은 펩티드 및 제약상 허용되는 담체, 부형제 또는 희석제를 포함하는, 조직 손상과 연관된 질환 또는 장애; 또는 그의 손상, 영향 또는 증상, 예를 들어 암, 염증, 및 독성제로의 노출 (이들로 한정되지는 않음)의 치료가 필요한 대상체에서 상기 치료를 위한 제약 조성물을 제공한다.
2. 발명의 배경
조직 손상은, 조직내 세포가 아팝토시스 (apoptosis) 또는 괴사에 의해 파괴되는 허혈성, 외상성, 독성 또는 염증성 손상으로 인한 실질적인 조직 손실에 의해 유발될 수 있다. 조직 손상은 수많은 급성 및 만성의 질환 및 증상에서 발생할 수 있다. 조직 손상이 발생하는 정도는 수많은 인자, 예를 들어 질환 또는 손상의 유형, 질환 또는 손상과 연관된 염증 또는 외상의 수준 또는 중증도, 조직 손상의 위치, 및 조직의 혈관 충분성에 의해 매개된다.
최근 증거에 따르면, 적혈구용적률 (hematocrit)의 유지와 일반적으로 연관된 1형 사이토킨 부류의 구성원인 에리트로포이에틴 (EPO)은 또한, 그의 수용체, 즉 EPOR과의 상호작용을 통해 조직 손상의 감쇠에 있어서 중요할 역할을 할 수 있다 (문헌 [Brines et al., 2004, Proc. Natl. Acad. Sci. USA, 101(41):14907-12]). EPO가, 저산소 세포 환경을 개선하면서 대사성 스트레스에 의해 유발되는 예정된 세포 사멸을 조절하는 기능을 하는 보상적 반응을 제공할 수 있다는 가설이 세워졌지만, 그 기저 분자적 메카니즘은 아직 명확하게 밝혀지지 않았다.
이러한 관측에 기초하여, 연구자들은 각종 적응증에서의 EPO의 용도를 연구하였다. 일례로서, 연구자들은 종양 환자에서의 빈혈의 치료에 사용되는 EPO가 빈혈을 개선할 뿐만 아니라 종양 환자의 웰빙을 증진시킨다는 관측에 기초하여 암에 대한 잠재적 치료제로서의 EPO의 용도를 연구하였다 (미국 특허 제6,579,525호 및 문헌 [Blau C.A., 2007, Stem Cells 25(8):2094-7] 참조). 미국 특허 제6,579,525호 (하란-게라 (Haran-Ghera) 등)는 다발성 골수종의 치료를 위한 재조합 EPO의 용도에 관한 것이며, EPO가 종양에 대한 면역성 반응을 유도한다는 가설을 세운다. 또한, 미국 특허 출원 제11/093,177호 (공개 공보 US 2005/0267027)에는 종양에서 HIF-1α 및/또는 VEGF 발현을 감소시킴으로써 종양에서의 혈관신생 (angiogenesis)을 억제하기 위한 EPO의 용도가 개시되어 있다.
그러나, 잠재적 조직 보호제로서의 EPO는 그의 에리트로포이에틴성 작용으로 인해 심각한 단점을 겪는다. 특히 (예컨대, 암 및 염증과 같은 적응증에서 구상되는) 만성 투여의 경우, EPO의 치료학적 용량의 빈번한 적용은 대상체의 적혈구용적률을 유의하게 증가시킬 수 있고, 이는 고혈압, 발작 및 혈관 혈전증을 초래할 수 있다.
또한, 암과 관련하여, 치료제로서의 EPO의 잠재성은 아직 실현되지 않았다. 여러 유형의 암, 예컨대 유방암이 에리트로포이에틴 수용체를 발현하는 (또한 과발현하는 경향이 있는) 것으로 결정되었다. 이는, 암을 치료하기 위한 EPO의 치료적 사용이 종양 발달의 퇴행에 상반되는 추가의 종양 성장을 초래한다는 우려를 낳았다 (상기 문헌 [Blau, 2007] 및 미국 특허 출원 제10/432,899호 (공개 공보 US 2005/0260580) 참조). 종양 성장 (Blau)으로 인한 사망률의 증가로 인해 다양한 암 적응증에서 EPO의 여러 시도가 중단됨에 따라, 상기 우려는 임상에서 입증되었다. 이러한 부정적인 임상 결과에 비추어, FDA는 승인된 EPO 제품 상에, 미승인 암 적응증에서의 사용을 경고하는 블랙 박스 경고문을 부착하였다
또한, 성숙 인간 EPO 단백질은 질량 분석법에 의해 측정시 약 30.4 kDa의 분자량을 갖는 165개 아미노산 단백질이다. 재조합 단백질은 중국 햄스터 난소 세포에서 고도로 통제된 고비용 및 노동집약적 공정에 의해 제조될 수 있다. 또한, EPO는 그의 활성을 유지하기 위한 엄격한 조건 하에 저장되어야 한다. 이러한 제한들로 인해, EPO는 광범위한 배포를 위해 치료제의 신속한 대량 생산이 요구되는 공중 응급 상황, 예컨대 (산업 재해 또는 테러 활동 또는 전쟁을 통한) 방사선 또는 화학적 작용제와 같은 독성제의 방출에 대처하기 위한 이상적인 후보가 아니다.
따라서, 잠재적으로 유해한 작용이 거의 또는 전혀 없으며 대중이 용이하게 입수할 수 있는 조직 보호 치료제가 요구된다.
3. 요약
본 발명은 반응성 세포, 조직 또는 기관에서 조직 보호 활성을 갖는 단리된 펩티드 및 펩티드 유사체를 제공한다. 특정 실시양태에서, 상기 펩티드 및 펩티드 유사체는 잠재적으로 바람직하지 않은 조혈 작용이 거의 또는 전혀 없다. 특히, 본 발명은 EPO 및 I형 사이토킨 수용체 리간드의 일부와 컨센서스 서열을 공유하는 조직 보호 펩티드 및 펩티드 유사체를 제공한다. 특정 실시양태에서, 단리된 펩티드 또는 펩티드 유사체는 (1) 음전하로 하전된 아미노산 2개 및 (2) 양전하로 하전된 아미노산 1개 및 음전하로 하전된 아미노산 1개로부터 선택된 중심의 (core) 구조적 모티프를 특징으로 하는 9 내지 29-잔기 아미노산 서열을 포함한다. 중심의 하전 아미노산들은 본원에 기재된 바와 같은 7 내지 27개의 아미노산으로 플랭킹된다. 특정 실시양태에서, 중심의 하전 아미노산들은 서로와 바로 인접한다. 특정 실시양태에서, 하전된 아미노산은 1 내지 5개의 아미노산 또는 단일 극성 아미노산으로 분리된다.
특정 측면에서, 본 발명은 하나 이상의 조직 보호 활성을 갖는 단리된 펩티드 및 펩티드 유사체를 제공한다. 예시적인 조직 보호 활성에는 반응성 포유동물 세포, 조직 또는 기관의 기능 또는 생존율을 보호, 유지, 증진 및 회복시키는 것이 포함되나, 이들로 한정되지는 않는다. 따라서, 본 발명의 일면은 반응성 포유동물 세포 및 그와 연관된 세포, 조직 및 기관의 기능 또는 생존율을 보호, 유지, 증진 및 회복시키기 위한 제약 조성물의 제조를 위한, 본 발명의 단리된 펩티드 및 펩티드 유사체의 용도를 제공한다. 관련 실시양태에서, 조성물은 상기 보호, 유지, 증진 및 회복이 필요한 대상체에게 투여하기 위한 것이다.
다른 측면에서, 본 발명의 단리된 펩티드 및 펩티드 유사체는 또한, 에리트로포이에틴 활성을 거의 또는 전혀 갖지 않거나 (예를 들면, 대상체에서의 헤모글로빈 또는 적혈구용적률을 유의하게 증가시키지 않음), 보다 일반적으로는 조혈 활성을 거의 또는 전혀 갖지 않는다 (예를 들면, 적혈구, 림프 및 골수 세포와 같은 혈액 세포 성분을 유의하게 증가시키지 않음). 특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 혈관활성 작용 (예를 들면, 혈관수축), 혈소판의 과활성화, 전구-응고 활성, 및 혈소판 또는 조혈-의존성 세포의 증식 또는 생성의 자극으로부터 선택된 활성을 거의 또는 전혀 갖지 않는다 (문헌 [Coleman et al., 2006, Proc. Natl. Acad. Sci. USA 103:5965-5970] 참조).
본 발명은 또한, 상기 조직 보호 펩티드 및 펩티드 유사체 및 제약상 허용되는 담체, 부형제 또는 희석제를 포함하는 제약 조성물, 및 이러한 조성물의 제조 방법 및 조직 손상과 연관된 질환 및 장애를 치료하기 위한 상기 조성물의 사용 방법을 제공한다. 다른 측면에서, 본 발명은 반응성 조직 손상에 대한 보호 또는 예방, 또는 반응성 조직 또는 반응성 조직 기능의 회복 또는 복원이 필요한 대상체에서의 반응성 조직 손상에 대한 보호 또는 예방, 또는 반응성 조직 또는 반응성 조직 기능의 회복 또는 복원을 위한 제약 조성물을 제조하기 위한, 본원에 기재된 단리된 펩티드 또는 펩티드 유사체의 사용 방법을 제공한다. 한 특정 측면에서, 반응성 포유동물 세포 및 그와 연관된 세포, 조직 또는 기관은 단단한 내피 세포 장벽으로 인해 혈관계로부터 멀어진다. 또다른 특정 측면에서, 세포, 조직, 기관 또는 다른 신체 부분은 포유동물 신체로부터 단리된다 (예컨대, 이식을 위한 것들). 본 발명의 특정 측면에서, 흥분성 조직은 중추신경계 조직, 말초신경계 조직, 심장 조직 또는 망막 조직이다. 또다른 측면에서, 반응성 세포 또는 그와 연관된 세포, 조직 또는 기관은 흥분성 세포, 조직 또는 기관이 아니거나, 또는 이들은 흥분성 세포 또는 조직을 주로 포함하지 않는다.
또다른 실시양태에서, 본 발명은 유효량의 펩티드를 투여함으로써, 염증, 암 또는 신생물성 장애, 또는 독성제로의 노출의 예방, 치료, 개선 또는 관리가 필요한 환자에서 염증, 암 또는 신생물성 장애, 또는 독성제로의 노출을 예방, 치료, 개선 또는 관리하는 방법에 관한 것이다.
특정 실시양태에서, 본 발명은 암, 독성제에 대한 신체 반응, 및 염증의 매개자의 활성을 조절하는 방법에 관한 것이다. 특히, 본 발명은 염증 매개자의 활성을 조절하는 방법에 관한 것이다. 바람직하게는, 본 발명의 펩티드는 하나 이상의 염증 매개자의 작용을 억제할 수 있다.
또다른 실시양태에서, 본 발명은 성장 억제가 필요한 세포를 유효량의 펩티드와 접촉시키는 것을 포함하는, 세포 성장을 억제하는 방법에 관한 것이다.
또다른 실시양태에서, 본 발명은 암 또는 신생물 세포를 유효량의 펩티드와 접촉시키는 것을 포함하는, 암 또는 신생물 세포의 사멸을 일으키는 방법에 관한 것이다.
또다른 실시양태에서, 본 발명은 암 또는 신생물 세포의 혈관 생성을 억제하거나 유사분열 (mitosis) 또는 혈관신생을 일으키는 분자의 생성을 감소시키는 방법에 관한 것이다.
또다른 실시양태에서, 본 발명은 화학요법 또는 방사선 요법과 연관된 부작용의 치료 또는 예방이 필요한 환자에게 유효량의 펩티드를 투여하는 것을 포함하는, 화학요법 또는 방사선 요법과 연관된 부작용을 치료 또는 예방하는 방법에 관한 것이다. 화학요법 또는 방사선 요법과 연관된 부작용에는 악액질, 저혈액량, 구역 (nausea), 설사, 경구 병변 및 탈모가 포함된다.
또다른 실시양태에서, 본 발명은 암 또는 신생물 세포를 유효량의 펩티드와 접촉시키는 것을 포함하는, 환자에서 암 또는 신생물성 질환을 치료 또는 예방하는 방법에 관한 것이다.
또다른 실시양태에서, 본 발명은 암 또는 신생물성 질환의 치료 또는 예방이 필요한 환자에게 유효량의 펩티드를 투여하는 것을 포함하는, 환자에서 암 또는 신생물성 질환을 치료 또는 예방하는 방법에 관한 것이다.
특정 실시양태에서, 본 발명은 암 또는 신생물성 장애의 예방, 치료, 개선 또는 관리가 필요한 대상체에서 암 또는 신생물성 장애를 예방, 치료, 개선 또는 관리하기 위한 제약 조성물의 제조를 위한 펩티드의 용도에 관한 것이다.
또다른 실시양태에서, 본 발명은 염증 또는 염증성 상태와 연관된 증상의 치료 또는 예방을 위한 방법에 관한 것이다. 또다른 실시양태에서, 본 발명은 염증 또는 염증성 상태의 치료 또는 예방이 필요한 환자에서 염증 또는 염증성 상태를 치료 또는 예방하는 방법에 관한 것이다. 본 발명의 방법에 의해 치료가능한 염증성 상태는 특히, 알레르기 및 알레르기성 질환, 류마티스성 질환 및 스포츠 관련 손상이다.
또다른 실시양태에서, 본 발명은 치료가 필요한 인간에서 독성제로의 노출의 작용을 치료, 예방, 개선 또는 관리하는 방법에 관한 것이다. 고려되는 독성제는 특히, 생물학적, 화학적 및 방사성 작용제이다.
특정 실시양태에서, 본 발명은 또한, 상기 단리된 펩티드를 포함하는 제약 조성물의 투여가 필요한 대상체에게 투여하기 위한, 상기 단리된 펩티드를 포함하는 제약 조성물에 관한 것이다. 이 실시양태에 따른 특정 측면에서, 본 발명의 제약 조성물은 제약상 허용되는 담체를 추가로 포함한다. 이러한 제약 조성물은 경구, 비강내, 안구, 흡입, 경피, 직장, 설하, 질내 또는 비경구 투여를 위해 제제화되거나, 생체외에서 세포, 조직 또는 기관의 생존율을 유지하기 위한 관류 용액의 형태로 제제화될 수 있다. 본 발명의 관련 실시양태에서, 대상체는 포유 동물, 바람직하게는 인간이다.
본 발명의 상기 및 여타 특징부, 측면 및 장점은 하기 기재 및 첨부된 청구범위를 통해 보다 잘 이해될 것이다.
4. 약어 및 용어
4.1 약어
본원에서 사용된, 유전학적으로 암호화된 L-거울상이성질체 아미노산들에 대한 약어는 통상적인 약어이며, 다음과 같다.
| 아미노산 | 단일 문자 기호 | 통상의 약어 |
| 알라닌 | A | Ala |
| 아르기닌 | R | Arg |
| 아스파라긴 | N | Asn |
| 아스파르트산 | D | Asp |
| 시스테인 | C | Cys |
| 글루타민 | Q | Gln |
| 글루탐산 | E | Glu |
| 글리신 | G | Gly |
| 히스티딘 | H | His |
| 이소류신 | I | Ile |
| 류신 | L | Leu |
| 라이신 | K | Lys |
| 메티오닌 | M | Met |
| 페닐알라닌 | F | Phe |
| 프롤린 | P | Pro |
| 세린 | S | Ser |
| 트레오닌 | T | Thr |
| 트립토판 | W | Trp |
| 티로신 | Y | Tyr |
| 발린 | V | Val |
| 피로글루타메이트 | U | pGlu (Glp) |
4.2 용어
달리 정의되지 않는다면, 본원에서 사용된 모든 기술 및 과학 용어는 본 발명이 속하는 분야의 기술자가 통상적으로 이해하는 의미를 갖는다. 본원에서 사용된 하기 용어들은 달리 명시되지 않는다면, 이들에 부여된 의미를 갖는다.
(i) 본원에서 사용된 용어 "약" 또는 "대략"은 수와 함께 사용되는 경우, 명시된 수의 1, 5, 10, 15 또는 20% 내에 있는 임의의 수를 나타낸다.
(ii) 본 발명의 방법의 맥락에서 용어 "~와 함께 투여되는"이란, 질환, 장애 또는 상태의 발생 이전에, 그와 동시에 및/또는 그 이후에 화합물을 투여하는 것을 의미한다.
(iii) 용어 "알레르기 항원"은 즉시형 과민성 (알레르기)을 생성할 수 있는 항원성 물질을 나타낸다. 통상적인 알레르기 항원으로는 박테리아, 바이러스, 동물 기생충, 곤충 및 곤충 교상, 화학물질 (라텍스), 먼지, 먼지 진드기, 곰팡이, 동물 비듬, 약물 (예컨대, 항생제, 혈청, 술파제 약물, 항경련제, 인슐린 제제, 국소 마취제, 요오드 및 아스피린), 음식물 (예컨대, 우유, 초콜렛, 딸기, 계란, 콩, 땅콩, 어류, 패류, 밀), 향수, 식물, 꽃가루 및 연기가 포함되나, 이들로 한정되지는 않는다.
(iv) 용어 "알레르기성 질환"은 알레르기에 의해 유발되거나 알레르기와 관련된 상태 또는 질환을 나타낸다. 알레르기성 질환으로는 천식, 과민성 폐 질환, 비염, 부비강염, 아토피성 습진, 접촉성 피부염, 알레르기성 결막염 (간헐성 및 지속성), 춘계 결막염 (건초열), 아토피성 각결막염, 거대 유두상 결막염, 팽진 (두드러기), 맥관부종, 과민성 폐렴, 호산구성 기관지염, 혈관염, 과민성 혈관염, 항호중구 세포질 항체 (ANCA) 연관 혈관염, 베게너 (Wegner) 육아종증, 쳐그 스트라우스 (Churg Strauss) 혈관염, 현미경적 다발성 혈관염, 측두 동맥염, 복강 질환, 비만세포증 및 아나필락시스 (anaphylaxis)가 포함되나, 이들로 한정되지는 않는다.
(v) 용어 "알레르기 증상" 또는 "알레르기성 반응"은 알레르기 항원에 대한 신체 반응을 나타낸다. 알레르기성 반응은 한 영역 (알레르기 항원과 접촉한 피부)으로 국소화되거나 전신화될 수 있다. 알레르기성 반응에는 팽진, 가려움, 두드러기, 부종, 호흡 곤란, 천명, 맥관부종, 연하 곤란, 비내 울혈, 콧물, 숨참, 구역, 위 경련, 복부 동통, 구토 및/또는 저혈압이 포함될 수 있으나, 이들로 한정되지는 않는다.
(vi) 용어 "알레르기"는 특정 항원 (알레르기 항원)으로의 노출에 의해 유발된, 추후 노출시 유해한 면역 반응을 일으키는 과민성 상태를 나타낸다.
(vii) 용어 "아미노산" 또는 특정 아미노산에 대한 임의의 언급은 천연 단백질합성성 (proteogenic) 아미노산 및 비-천연 아미노산, 예컨대 아미노산 유사체를 포함한다. 당업자는 이러한 정의가, 달리 구체적으로 명시되지 않는다면, 천연 단백질합성성 (L)-아미노산, 그의 광학 (D)-이성질체, 화학적으로 변형된 아미노산, 예를 들어 아미노산 유사체, 예컨대 페니실라민 (3-머캅토-D-발린), 천연 비-단백질합성성 아미노산 (예컨대, 노르류신) 및 당업계에 아미노산의 특성인 것으로 알려져 있는 특성을 갖는 화학적으로 합성된 아미노산을 포함한다는 점을 알 것이다. 또한, 용어 "아미노산 등가물"은, 천연 아미노산의 구조로부터는 벗어나지만 실질적으로 아미노산의 구조를 갖는 화합물 (이들은 치환에도 불구하고 그 생물학적 활성을 유지하는 펩티드 내에서 치환될 수 있음)을 나타낸다. 따라서, 예를 들면, 아미노산 등가물은 측쇄 변형 또는 치환을 갖는 아미노산을 포함할 수 있으며, 관련 유기산, 아미드 등도 포함한다. 용어 "아미노산"은 아미노산 등가물을 포함한다. 용어 "잔기"는 아미노산 및 아미노산 등가물 둘 다를 나타낸다. 아미노산은 또한, 당업계에 통상적으로 알려져 있는 바와 같이 다음과 같은 군으로 분류될 수 있다: (1) 산성 = Asp, Glu; (2) 염기성 = Lys, Arg, His; (3) 비-극성 (소수성) = Cys, Ala, Val, Leu, Ile, Pro, Phe, Met, Trp, Gly, Tyr; 및 (4) 비하전 극성 = Asn, Gln, Ser, Thr. 비-극성은 다음과 같이 세분될 수 있다: 고도의 소수성 = Ala, Val, Leu, Ile, Met, Phe; 및 중간 수준의 소수성 = Gly, Pro, Cys, Tyr, Trp. 또다른 방식으로, 아미노산 레퍼토리는 다음과 같이 분류될 수 있다: (1) 산성 = Asp, Glu; (2) 염기성 = Lys, Arg, His, (3) 지방족 = Gly, Ala, Val, Leu, Ile, Ser, Thr (Ser 및 Thr은 임의로, 지방족-히드록실로 개별적으로 분류됨); (4) 방향족 = Phe, Tyr, Trp; (5) 아미드 = Asp, Glu; 및 (6) 황-함유 = Cys 및 Met (예를 들면, 문헌 [Biochemistry, 4th ed., Ed. by L. Stryer, WH Freeman and Co., 1995] 참조 (그 전문이 본원에 참조로 포함됨)).
(viii) 본원에서 사용된 용어 "생물학적 작용제"는 인간, 동물 또는 식물에서 질환을 일으키거나 인간, 동물 또는 식물에게 유해하거나, 물질의 악화를 일으키는 살아있는 유기체 또는 그로부터 유래된 물질 (예컨대, 박테리아, 바이러스, 진균 및 독소)을 나타낸다. 이러한 생물학적 작용제는 자연계에 편재하며, 전쟁 또는 테러 (생화학 테러)에서의 사용을 위해 설계 또는 최적화될 수 있다. 상기 생물학적 작용제는 프리온, 바이러스, 미생물 (박테리아 및 진균) 및 몇몇 단세포 및 다세포 진핵생물 (즉, 기생충)로 구성될 수 있다. 특히, 생물학적 작용제 (이들의 통상적인 명칭, 생물학적 명칭 및 NATO 표준 문자 코드 (가능한 경우)로 식별됨)에는 진균제 (코시디오데스 마이코시스 (Coccidioides mycosis), OC, 코시디오데스 포사다실 (Coccidioides posadasil), 코시디오데스 이미티스 (Coccidioides immitis)), 박테리아제 (안트락스 (anthrax) (피부, 흡입, 위장) (바실루스 안트라시스 (Bacillus anthracis), N 및 TR), 페스트 (림프절형, 폐렴형) (예르시니아 페스티스 (Yersinia pestis), LE), 야토병 (프란시셀라 툴라렌시스 (Francisella tularensis), UL (schu S4), TT (습윤형), ZZ (건조형) 및 SR 및 JT (425)), 콜레라 (비브리오 콜레라 (Vibrio cholerae), HO), 소 브루셀라증 (AB), 돼지 브루셀라증 (US 및 NX), 염소 브루셀라증 (AM 및 BX), 브루셀라 아보르투스 (Brucella abortus), 브루셀라 멜리테니스 (Brucella melitenis), 브루셀라 수이스 (Brucella suis), 박테리아성 이질 (시겔라증, 캄필로박테리아증, 살모넬라증) (Y), 마비저 (부르크홀데리아 말레이 (Burkholderia mallei), LA), 유사비저 (부르크홀데리아 슈도말레이 (Burkholderia pseudomallei), HI), 디프테리아 (코리네박테리움 디프테리아 (Corynebacterium diphtheriae), DK), 리스테리아증 (리스테리아 모노사이토게네스 (Listeria monocytogenes), TQ)), 클라미디아 작용제 (앵무새병 "앵무새 열 (Parrot Fever)" (클라미도필라 시티시 (Chlamydophilia psittici), SI), 리케차 작용제 (록키산 반점열 (리케차 리케치 (Rickettsia rickettsii), RI 및 UY), Q 열 (콕시엘라 부르네티 (Coxiella burnetti), OU, MN (습윤형) 및 NT (건조형)), 인간 티푸스 (리케차 프로와제키 (Rickettsia prowazekii), YE), 뮤린 티푸브 (리케차 타이피 (Rickettsia typhi), AV)), 바이러스 작용제 (황열 (아르보바이러스 플라비비르다 (Arbovirus flavivirdae), OJ, UT 및 LU), 리프트 계곡 열 (RVF 플레보바이러스 부니아비리다 (Phlebovirus bunyaviridae), FA), 알파바이러스 (예: 동부 말 뇌염 (ZX), 서부 말 뇌염, 베네수엘라 말 뇌염 (NU, TD 및 FX)), 천연두 (ZL), 일본 B형 뇌염 (AN), 1형 붉은털원숭이 (Cercopithecine) 헤르페스바이러스 (B형 헤르페스 바이러스), 크리미안-콩고 (Crimean-Congo) 출혈성 열 바이러스, 바이러스성 출혈성 열 (필로비리다 (Filoviridae) (에볼라 및 마르부르크 (Marburg) 바이러스) 및 아레나비리다 (Arenaviridae) (라사 (Lassa) 및 마추포 (Machupo)), 원숭이 천연두 바이러스, 재구성 1918 인플루엔자 바이러스, 남아메리카 출혈성 열 바이러스 (플렉살 (Flexal), 구아나리토 (Guanarito), 주닌 (Junin), 마추포, 사비아 (Sabia)), 진드기-매개 수막뇌염 (TEBV) 바이러스 (중부 유럽 진드기-매개 뇌염, 극동 진드기-매개 뇌염, 키아사누르 포레스트 (Kyasanur Forest) 질환, 옴스크 (Omsk) 출혈성 열, 러시아 봄 및 여름 바이러스), 헨드라 (Hendra) 바이러스, 니파 (Nipah) 바이러스, 한타바이러스 (한국 출혈성 열), 아프리카 말 병 바이러스, 최적화된 돼지 열 바이러스, 아카바네 (Akabane) 바이러스, 새 인플루엔자 바이러스, 블루텅 바이러스, 낙타 천연두 바이러스, 고전 돼지 열 바이러스, 구제역 질환 바이러스, 염소 천연두 바이러스, 피부사상균 질환 바이러스, 악성 카타르성 열 바이러스 (1형 알셀라핀 (Alcelaphine) 헤르페스바이러스), 메낭글 (Menangle) 바이러스, 뉴 캐슬 질환 바이러스, 소 반추 수역 바이러스 (Pestes des petits ruminants virus), 공수병 바이러스, 우역 바이러스, 양 천연두 바이러스, 돼지 수포성 질환 바이러스, 수포성 구내염 바이러스), 독소 (보툴리눔 독소 (클로스트리디움 (Clostridium), X 및 XR), 리신 (ricin) (리시누스 코무니스 (Ricinus communis), W 및 WA), B형 스타필로코쿠스 장독소 (UC 및 PG), 삭시톡신 (마비성 패류 중독) (TZ 및 SS), 테트로도톡신 (PP), 코노톡신, 클로스트리디움 페르프링겐스 엡실론 독소, 트리코테센 마이코톡신 (T-2 독소), 시가톡신) 및 시뮬런트 (몰라시스 레시디움 (Molasis residium) (MR), 바실루스 글로비기 (Bacillus globigii) (BG, BS 및 U), 세라티아 마레센스 (Serratia marescens) (SM 및 P), 아스페르길루스 푸미가투스 (Aspergillus fumigatus) 돌연변이체 C-2 (AF), 이. 콜라이 (EC), 바실루스 투르시디우스 (Bacillus thursidius) (BT), 에르위니아 헤르비콜라 (Erwinia herbicola) (EH), 형광 입자 (FP)), 호밀 맥각병, 나병, 공수병, 장티푸스, 클로스트리디움 페르프링겐스 (가스 괴저), 아플라톡신, 살모넬라 티피무리움 (Salmonella typhimurium), 장독소, 아르헨티나 출혈성 열, 다중-약물 내성 결핵 (MTB), 볼리비아 출혈성 열, 레기오넬라 뉴모필라, 해양 독소, 각기, 말라리아, 펠라그라, 뎅그 열, 스클레로티움 롤포일 (Sclerotium rolfoil), 신경친화성 뇌염, 시겔라 (Y), SEB (UC), 및 마이코톡신, 디아세톡시르페놀, 코우드리아 루미나티움 (Cowdria ruminantium), 마이코플라스마 카프리콜룸 (Mycoplasma capricolum) M.F38/M. 마이코이데스 카프리 (Mycoides capri), 마이코플라스마 마이코이데스 (Mycoplasma mycoides) 마이코이데스, 아브린이 포함될 수 있으나, 이들로 한정되지는 않는다. 생물학적 작용제는 인간 (예를 들면, 천연두, 에볼라 바이러스, 재구성 1918 인플루엔자 바이러스, 리신 등), 동물, 예컨대 가축 (예를 들면, 아프리카 말 병 바이러스, 아프리카 돼지 열 바이러스, 구제역 등) 또는 둘 다 (동부 말 뇌염 바이러스 등)에 대해 표적화될 수 있다. 또한, 비-치명적인 생물학적 작용제라도 위협이 될 수 있으며, 그 이유는 생물학적 무기로서의 사용을 위한 보다 높은 치명성을 높이기 위해 재조작될 수 있기 때문이다. 따라서, 일반 감기를 유발하는 바이러스도 위험이 될 수 있다.
(ix) 본원에서 사용된 용어 "암"은 악성 (malignant) 특성을 나타내는 임의의 비정상적 성장을 나타낸다: (1) 정상 한계와 무관하게 성장 및 분할하고, (2) 인접 조직을 침입 및 파괴하고, (3) 일부 경우에서, 신체의 다른 위치로 확산하는 능력. 암에는 중추신경계, 말초신경계, 위장/소화계, 비뇨생식기계, 부인과, 두경부, 혈액학적/혈액, 근골격/연질 조직, 호흡기 및 유방의 암 또는 신생물성 장애가 포함된다. 암 또는 신생물성 장애의 또다른 예로는 뇌 (별아교세포종, 교모세포종, 신경교종), 척수, 뇌하수체, 유방 (침윤성, 침습-전, 염증성 암, 파제트 (Paget) 질환, 전이성 및 재발성 유방암), 혈액 (호지킨 (Hodgkin) 질환, 백혈병, 다발성 골수종, 림프종), 림프절암, 폐 (선암종, 귀리세포, 비-소세포, 소세포, 편평세포, 중피종), 피부 (흑색종, 기저세포, 편평세포, 카포시 육종), 골암 (유잉 (Ewing) 육종, 골육종, 연골육종), 두경부 (후두, 인두 (비강 및 부비강) 및 식도 암), 경구 (턱, 침샘, 인후, 갑상선, 혀 및 편도선 암), 눈, 부인과 (자궁경부, 자궁내막, 난관, 난소, 자궁, 질 및 음문), 비뇨생식기 (방광, 신장, 음경, 전립선, 고환 및 비뇨기 암), 부신성 (피질 선종, 피질 암종, 크롬친화세포종) 및 위장 (충수, 담도 (간외 담도) 결장, 담낭, 위, 장, 결장, 간, 췌장, 직장 및 위 암)의 암 또는 신생물성 장애, 및 아래 열거된 것들이 포함되나, 이들로 한정되지는 않는다 (이러한 장애의 검토를 위해서는 문헌 [Fishman et al., 1985, Medicine, 2d Ed., J.B. Lippincott Co., Philadelphia] 참조): 백혈병: 급성 백혈병, 급성 림프구성 백혈병, 급성 골수구성 백혈병, 골수모세포성, 전골수구성, 골수단핵구성, 단핵구성 적백혈병, 만성 백혈병, 만성 골수구성 (과립구) 백혈병, 만성 림프구성 백혈병, 진성 적혈구증가증 (polycythemia vera), 위암종, 림프종 (악성 및 비-악성): 호지킨 질환, 비-호지킨 질환, 다발성 골수종, 발덴스트롬 마크로글로불린혈증 (Waldenstrom's macroglobulinemia), 중쇄 질환, 고형 종양, 육종 및 암종: 섬유육종, 점액육종, 지방육종, 연골육종, 골형성 육종, 척삭종, 혈관육종, 내피육종, 림프관육종, 림프관내피육종, 윤활막종, 중피종, 유잉 종양, 평활근육종, 횡문근육종, 결장암종, 췌장암, 유방암, 난소암, 전립선암, 편평세포 암종, 경구 편평세포 암종, 간세포 암종, 기저세포 암종, 선암종, 한선 암종, 피지선 암종, 유두성 암종, 유두성 선암종: 낭선암종, 수질 암종, 기관지원성 암종, 신장 세포 암종, 간암, 담도암종, 융모막암종, 정상피종, 배아 암종, 빌름 (Wilm) 종양, 자궁경부암, 경부 선암종, 자궁암, 고환 종양, 폐 암종, 소세포 폐 암종, 비-소세포 폐 선암종, 방광 암종, 상피성 암종, 신경교종, 악성 신경교종, 교아세포종, 다형 성상세포 교종, 수모세포종, 두개인두종, 상의세포종, 송과체종, 혈관모세포종, 청신경종, 핍지교종, 수막종, 흑색종, 신경아세포종 또는 망막모세포종.
(x) 본원에서 사용된 용어 "화학적 작용제"는 인간 또는 동물에서 심각한 사멸 또는 유해를 일으키는 화학 물질을 나타낸다. 화학적 작용제가 탄약 또는 분산 장치를 이용하여 전달되도록 최적화된 경우, 이러한 작용제는 화학적 무기이다. 일반적으로, 무기로서 사용되는 화학적 작용제는 다음과 같은 작용 방식에 의해 분류될 수 있다: 혈액 작용제, 수포 작용제, 신경 작용제, 폐 작용제 및 무능화 작용제. 하기 각 화학적 작용제는 NATO 표준 문자 코드 (가능한 경우)로 식별된다.
(xi) "혈액 작용제"는 세포가 산소를 사용하는 것을 막는 화학적 작용제를 나타낸다. 이 범주 내의 화학적 작용제에는 아르신 (아담사이트(디페닐아민클로로아르신), 클라크 (Clark) I (디페닐클로로아르신), 클라크 II (디페닐시아노아르신)) 및 시아니드 (시아노겐 클로라이드 (CK), 수소 시아니드 (AC) 등) 화합물이 포함되나, 이들로 한정되지는 않는다. 아르신 화합물은 신부전증을 유발하는 혈관내 용혈을 일으킨다. 시아니드 화합물은 세포가 산소를 사용하는 것을 막으며, 이때 세포가 혐기성 호흡을 하여 과량의 락트산을 생성함에 따라 대사성 산증이 초래된다. 혈액 작용제의 희생자는 두통, 현기증, 구역, 구토, 점막 자극, 호흡곤란, 의식 손상, 혼수, 경련, 빈맥- 및 서맥-부정맥, 저혈압, 심혈관 붕괴 및 청색증 (이들로 한정되지는 않음)을 비롯한 증상을 나타낼 수 있다.
(A) "신경 작용제"는 아세틸콜린스테라제 효소를 불활성화시키는 화학적 작용제를 나타낸다. 희생자 시냅스에서의 신경전달물질 아세틸콜린 축적은 무스카린성 및 니코틴성 작용을 일으킨다. 이 범주 내의 화합물에는 시클로사린 (시클로헥실메틸포스포플루오리데이트, GF), 사린 (이소프로필 메틸포스파노플루오리데이트, GB), 티오사린, 소만 (피나콜릴메틸포스파노플루오리데이트, GC), 타분 (에틸 N,N-디메틸포스포르아미도시아니데이트, GA), VX (O-에틸-[s]-[2-디이소프로필아미노에틸-메틸포스포노티올레이트), VR (N,N-디에틸-2-(메틸-(2-메틸프로폭시)포스포릴)술파닐에탄아민), VE (O-에틸-S-[2-(디에틸아미노)에틸]포스포노티오에이트), VG (O,O-디에틸-S-[2-(디에틸아미노)에틸]포스포로티오에이트), VM (O-에틸-S-[2-(디에틸아미노)에틸]메틸포스포노티오에이트), 에틸 사린 (이소프로필에틸포스포노플루오리데이트, GE), EDMP (에틸-2-디이소프로필아미노에틸메틸포스폰산염), DF (메틸포스포닐 디플루오라이드), 노비초크 작용제, GV (P-[2-(디메틸아미노)에틸]-N,N-디메틸포스포나미딕 플루오라이드), Gd42, Gd83, 타멜린 (Tammelin) 에스테르, 플루오로포스포콜린, 포스포티오클로레이트, DFP 및 살충제 (페노티아진, 유기포스페이트 (디코러스, 말라티온, 파라티온, 펜티온, 아미돈, 파라옥손, 클로로피리포스, 시스톡스, 피로포스페이트, TOCP))가 포함되나, 이들로 한정되지는 않는다. 신경 작용제의 희생자는 서맥, 근종, 침분비 과다, 구토, 설사, 비자발성 배뇨, 근육 속상수축, 최초 탈분극성 이완성 마비, 스파이크 방전 및 경련, 중간형 증후군, 신경독성 에스테라제 억제, 및 유기포스페이트-유발성 지연성 신경병증 (이들로 한정되지는 않음)을 비롯한 증상을 나타낼 수 있다.
(B) "수포 작용제"는 희생자 피부 및 호흡계를 손상시켜 화상 및 호흡성 문제를 일으키는 산-형성 화합물인 작용제를 나타낸다. 이 범주 내의 화학적 작용제에는 황 머스타드 (1,2-비스(2-클로로에틸티오)에탄 (세스퀴머스타드, Q), 1,3-비스(2-클로로에틸티오)-n-프로판, 1,4-비스(2-클로로에틸티오)-n-부탄, 1,5-비스(2-클로로에틸티오)-n-펜탄, 2-클로로에틸클로로메틸술파이드, 비스(2-클로로에틸)술파이드 (HD), 비스(2-클로로에틸티오) 메탄, 비스(2-클로로에틸티오메틸) 에테르, 비스(2-클로로에틸티오에틸) 에테르, 디-2'-클로로에틸술파이드 및 그의 조합물 (HT, HL, HQ)), 질소 머스타드 (비스(2-클로로에틸)에틸아민 (HN1), 비스(2-클로로에틸)메틸아민 (HN2), 트리스(2-클로로에틸)아민 (HN3), 2-클로로-N-(2-클로로에틸)-N-메틸에탄아민-N-옥사이드 히드로클로라이드, 시클로포스파미드, 클로람부실, 우라무스틴, 멜팔란), 루이사이트 (lewisite) (2-클로로비닐디클로로아르신, 비스(2-클로로비닐)클로로아르신, 트리스(2-클로로비닐)아르신, 디클로로(2-클로로비닐)아르신), 에틸디클로로아르신, 메틸디클로로아르신, 페닐디클로로아르신 및 포스겐 옥심 (디클로로포름옥심)이 포함되나, 이들로 한정되지는 않는다. 수포 작용제의 희생자는 홍반, 부종, 괴사 및 소낭, 멜라닌피부증, 기관기관지염, 기관지연축, 기관지 폐쇄, 출혈성 폐 부종, 호흡성 부전증, 박테리아 폐렴, 안구 홍반, 눈물 (lachrymation), 눈의 불편감, 눈의 극심한 동통, 안검연축, 홍채염, 실명, 구역, 구토, 골수 억제, 루이사이트 쇼크, 간 괴사 및 관류 저하 후의 신부전증 (이들로 한정되지는 않음)을 비롯한 증상을 나타낼 수 있다.
(D) "폐 작용제"는 수포 작용제와 유사하나 호흡계 상에 보다 현저한 영향을 미쳐, 호흡계 과부하 및 희생자 질식을 일으키는 작용제를 나타낸다. 이 범주 내의 화학적 작용제에는 아담사이트, 아크롤레인, 비스(클로로메틸)에테르, 염소, 클로로피크린, 디포스포겐, 메틸 클로로술페이트, 주석 클로라이드, 염화수소, 산화질소 및 포스겐이 포함되나, 이들로 한정되지는 않는다. 폐 작용제의 희생자는 화상 감각 (눈, 비인두, 구인두), 눈물 과다, 비루, 기침, 쉰 목소리, 호흡곤란, 연하곤란, 결막염, 각막 손상, 비인두-구인두 손상/부종, 성문 구조의 염증, 분비 및/또는 성대문연축으로 인한 호흡성 고통, 급성 호흡성 증후군, 및 반응성 기도 기능이상 증후군 (이들로 한정되지는 않음)을 비롯한 증상을 나타낼 수 있다.
(E) "무능화 작용제"는 덜 치명적이며 대체로, 생리적 또는 정신적 작용 또는 둘 다를 통해 무능화시키기 위한 작용제를 나타낸다. 통상적인 부류의 무능화 작용제는 최루성 작용제, 즉 눈을 자극하여 눈물, 동통 및 심지어 일시적 실명을 일으키는 화학적 작용제이다. 최루성 작용제로는 a-클로로톨루엔, 벤질 브로마이드, 브로모아세톤 (BA), 브로모벤질시아니드 (CA), 브로모메틸 에틸 케톤, 캅사이신 (OC), 클로르아세토페논 (CN), 클로로메틸 클로로포르메이트, 디벤족사제핀 (CR), 에틸 요오도아세테이트, 오르토-클로로벤질리덴 말로니트릴 (CS), 트리클로로메틸 클로로포르메이트 및 크실릴 브로마이드가 포함되나, 이들로 한정되지는 않는다. 추가적인 무능화 작용제로는 3-퀴누클리디닐 벤질레이트 (환각성; BZ), 히드로시안산 (마비성), 디페닐클로로아르신 (재채기성; DA), 디페닐시아노아르신 (DC), 콜로콜-1 (KOLOKOL-1) (펜타닐 유도체), 다투라 스트라모늄, 헬본, 벨라도나, 히오스사이아무스 팔레즐레즈, 인돌 (리세르그산 디에틸아미드 (LSD-25)), 마리화나 유도체 (DMHP), 암페타민, 코카인, 카페인, 니코틴, 스트리크닌, 메트라졸, 바르비투레이트 (메토헥시탈), 아편유사물질, 항정신병제 (할로페리돌), 벤조디아제핀, 펜타닐류, 사일로사이빈, 이보가인, 하르민, 엑터시, PCP, 아트로핀, 스코폴라민, 옥시부티닌, 디트로판, 항콜린성 항히스타민, 베낙티진 및 신경안정제가 포함되나, 이들로 한정되지는 않는다.
상기 화학물질 중 대다수는 무기로서의 용도를 벗어난 용도를 가지며, 제조업 범주에서 사용된다. 따라서, 제조 공장 또는 화학 공장으로부터 화학적 작용제가 우발적이거나 고의적으로 방출되면, 공장 근로자뿐만 아니라 공장 근방에 거주하는 인구가 위험할 것이다. 독성의 공업 제조용 화학물질의 예에는 암모니아, 아르신, 붕소 트리클로라이드, 붕소 트리플루오라이드, 이황화탄소, 염소, 디보란, 에틸렌 옥사이드, 불소, 포름알데히드, 브롬화수소, 염화수소, 수소 시아니드, 수소 플루오라이드, 수소 술파이드, 질산, 포스겐, 인 트리클로라이드, 이산화황, 황산, 텅스텐 헥사플루오라이드, 아세톤 시아노히드린, 아크롤레인, 아크릴로트릴, 알릴 알코올, 알릴 아민, 알릴 클로로카보네이트, 삼브롬화붕소, 일산화탄소, 카르보닐 술파이드, 클로로아세톤, 클로로아세틸니트릴, 클로로 술폰산, 디케톤, 1,2-디메틸 히드라진, 에틸렌 디브로마이드, 수소 셀레니드, 메탄 술포닐 클로라이드, 메틸 브로마이드, 메틸 클로로포르메이트, 메틸 클로로실란, 메틸 히드라진, 메틸 이소시아네이트, 메틸 메르캅탄, 이산화질소, 포스핀, 인 옥시클로라이드, 인 펜타플루오라이드, 셀레늄 헥사플루오라이드, 실리콘 테트라플루오라이드, 스틸로인 (stiloine), 삼산화황, 술푸릴 클로라이드, 술푸릴 플루오라이드, 텔루륨 헥사플루오라이드, n-옥틸 머캅탄, 티타늄 테트라클로라이드, 트리클로로아세틸 클로라이드, 트리플루오로아세틸 클로라이드, 알릴 이소티오시아네이트, 삼염화비소, 브롬, 브롬 클로라이드, 브롬 펜타 플루오라이드, 브롬 트리플루오라이드, 카르보닐 플루오라이드, 염소 펜타 플루오라이드, 염소 트리플루오라이드, 클로로아세틸알데히드, 클로로아세틸클로라이드, 크로톤알데히드, 시아노겐 클로라이드, 디메틸 술페이트, 디페닐메탄-4,4'-디이소시아네이트, 에틸 클로로포르메이트, 에틸 클로로티오포르메이트, 에틸 포스포노티산 디클로라이드, 에틸 포스폰산 디클로라이드, 에틸렌이민, 헥사클로로시클로펜타디엔, 수소 요오드, 철 펜트카르보닐, 이소부틸 클로로포르메이트, 이소프로필 클로로포르메이트, 이소프로필 이소시아네이트, n-부틸 클로로포르메이트, n-부틸 이소시아네이트, 산화질소, n-프로필 클로로포르메이트, 파라티온, 퍼클로로메틸 머캅탄, sec-부틸 이소시아네이트, tert-부틸 이소시아네이트, 테트라에틸 납, 테트라에틸 피로포스페이트, 테트라 메틸 납, 톨루엔 2,4-디이소시아네이트 및 톨루엔 2,6-디이소시아네이트가 포함되나, 이들로 한정되지는 않는다.
(xi) 본원에서 사용된 "유효량"은 조직 손상과 연관된 임의의 질환 또는 장애 또는 그의 손상, 영향 또는 증상의 조절, 바람직하게는 조직 손상과 연관된 질환 또는 장애에 대한 신체 반응, 예를 들어 암, 염증, 또는 독성제로의 노출에 대한 신체 반응 (이들로 한정되지는 않음)의 유해 작용의 억제, 저해 또는 조절에 충분한 펩티드 양을 포함한다. 또한, "유효량"은 조직 손상과 연관된 임의의 질환 또는 장애를 완화, 개선, 감소 또는 예방하거나 조직 손상과 연관된 질환 또는 장애를 앓는 환자에서 치료적 이익을 제공하기에 충분한 펩티드 양을 포함한다.
(xii) 본원에서 사용된 "에리트로포이에틴 활성"이란, 대상체에서의 헤모글로빈 또는 적혈구용적률 수준의 임의의 유의한 증가를 의미한다. "에리트로포이에틴 활성이 거의 또는 전혀 없음"이란, 대상체의 헤모글로빈 또는 적혈구용적률의 증가된 수준이, 대상체에서의 역효과를 일으키기에 불충분한 증가로서 당업계에서 인정되는 기준을 충족시킴을 의미한다. "유의하게 증가된 에리트로포이에틴 활성"이란, 대조군과 비교한 대상체의 헤모글로빈 또는 적혈구용적률 수준의 차이가 당업계에서 유의한 것으로 인정되는 기준을 충족시킴 (특히, 고혈압, 발작 및 혈관 혈전증의 가능성을 증가시킬 수 있음)을 의미한다.
(xiii) "흥분성 조직"이란, 흥분성 세포를 함유하는 조직을 의미한다. 흥분성 세포는, 전기 자극에 대해 능동적으로 반응하고 세포 막을 통해 차등 전기 전하를 갖는 세포이다. 흥분성 세포는 일반적으로, 잠재적 작용을 겪을 수 있다. 이러한 세포는 전형적으로, 막을 통해 이온 (칼륨, 나트륨, 칼슘, 클로라이드 등)의 유동을 가능하게 하는 채널, 예컨대 전압-개폐, 리간드-개폐 및 신축성 (stretch) 채널을 발현한다. 흥분성 조직에는 뉴런 조직, 근육 조직 및 선 조직이 포함된다. 흥분성 조직에는 뉴런 조직, 예컨대 말초신경계 (귀 및 망막) 및 중추신경계 (뇌 및 척수)의 조직; 심혈관 조직, 예컨대 심장 및 연관 신경의 세포; 및 선 조직, 예컨대 췌장 (T형 칼슘 채널이 세포-세포 간격 접합부와 함께 인슐린 분비에 참여함)이 포함되나, 이들로 한정되지는 않는다. 흥분성 조직의 예시적인 목록에는 신경, 골격근, 평활근, 심근, 자궁, 중추신경계, 척수, 뇌, 망막, 후각계, 청각계 등을 비롯한 기관 및 조직이 포함된다.
(xiv) 용어 "조혈 활성"이란, 적혈구, 림프구 및 골수 세포와 같은 혈액 세포 성분의 임의의 유의한 증가를 의미한다. 조혈 활성은 또한, 단리된 펩티드 또는 펩티드 유사체가 혈관활성 작용 (예를 들면, 혈관수축), 혈소판의 과활성화, 전구-응고 활성, 및 혈소판 또는 에리트로포이에틴-의존성 세포의 증식 또는 생성의 자극으로부터 선택된 활성을 갖는지 여부를 나타낸다.
(xv) 본원에서 사용된 용어 "숙주 세포"는 핵산 분자로 형질감염된 특정 대상체 세포, 및 이러한 세포의 후대세포 또는 잠재적 후대세포를 나타낸다. 돌연변이 또는 환경적 영향이 숙주 세포 게놈으로의 핵산 분자의 통합 또는 계대시에 발생할 수 있기 때문에, 세포의 후대세포는 핵산 분자로 형질감염된 모 세포와 동일하지 않을 수 있다.
(xvi) 본원에서 사용된 용어 "염증성 상태"는 염증성 성분을 갖는, 기계적으로 또는 화학적으로 유도된 각종 질환 또는 외상을 나타낸다. 상기 용어는 뇌, 척수, 결합 조직, 심장, 폐, 신장, 요로, 췌장, 눈 및 전립선 (이들로 한정되지는 않음)을 비롯한, 하나 이상의 기관 또는 조직에서의 염증을 일으키는 상태를 포함한다. 이러한 상태의 비제한적인 예로는 맹장염, 안검염, 기관지염, 윤활낭염, 자궁경부염, 담관염, 담낭염, 융모막염, 결막염, 방광염, 누선염, 피부염, 심내막염, 자궁내막염, 상과염, 부고환염, 섬유조직염, 위염, 치은염, 설염, 화농성 한선염, 홍채염, 후두염, 유방염, 심근염, 근육염, 신장염, 배꼽염, 난소염, 고환염, 골염, 이염, 이하선염, 심장막염, 복막염, 인두염, 늑막염, 정맥염, 폐렴 (폐실질염), 전립선염, 신우신염, 비염, 자궁관염, 부비강염, 구내염, 활막염, 편도염, 포도막염, 요도염, 질염, 음문염, 천식, 전신성 홍반성 루푸스, 중증 근무력증, 건염, 혈관염, 만성 기관지염, 췌장염, 골수염, 관절염 (류마티스성 및 건선성), 사구체신염, 시신경염, 측두동맥염, 뇌염, 수막염, 횡단척수염, 피부근염, 다발성근염, 괴사근막염, 간염, 괴사소장대장염, 골반 염증성 질환, 염증성 장 질환 (궤양성 대장염, 크론병, 회장염 및 장염), 직장염, 혈관염, 혈관 협착증, 재협착, 저혈압, 1형 당뇨병, 가와사키병, 데쿰 (Decum) 질환, 만성 폐쇄성 폐질환, 건선, 죽상동맥경화증, 피부경화증, 쇼그렌 (Sjogren) 증후군, 혼합 결합 조직 질환, 주사, 위궤양, 십이지장궤양, 알츠하이머 질환, 성인 발병성 스틸 (Still) 질환, 급성 망막 색소 상피염, 티체 (Tietze) 증후군, 베체트 (Bechet) 질환, 백반 증후군 (급성 후부 다발성 판상 색소 상피병증, 사행성 맥락막염, 산탄 맥락막병증, 전체포도막염을 동반한 다소성 맥락막염, 범발성 망막하 섬유증 증후군, 점상 내층 맥락막병증, 다발성 소실성 백반 증후군 및 범발성 단안 아급성 신경망막염), 환상 육아종, 과민성 장 증후군, 위장염, 그레이브 (Grave) 질환, 다발성 경화증, 듀피트렌 (Dupuytren) 구축, 이식편 거부 질환 (동종이식 거부반응 및 이식편-대-숙주 질환 포함), 예를 들면 피부 이식편 거부, 고형 기관 이식거부, 골수 이식거부, 염증성 피부병, 바이러스성 피부 병리 (예컨대, 인간 유두종 바이러스, HIV 또는 RLV 감염으로부터 유래된 것들), 박테리아성, 진균성 및/또는 여타 기생충성 피부 병리, 피부 홍반성 루푸스 및 과다 IgG4 질환이 포함되나, 이들로 한정되지는 않는다. "염증성 상태"는 또한, 허혈성 또는 비-허혈성 상태로 인한 염증, 예를 들어 (이들로 한정되지는 않음) 둔상, 타박상, 알레르기 및 알레르기성 질환, 류마티스성 질환 (연소자성 관절염, 류마티스성 관절염, 척-스트라우스 증후군, 섬유조직염, 거대 세포 (측두) 동맥염, 통풍, 헨노흐-쇤린 (Henoch-Schoenlin) 자반증, 과민성 혈관염, 강직성 척추염, 관절낭염, 류마티스성 열, 류마티스성 심장 질환, 전신성 홍반성 루푸스, 류마티스성 다발성근육통, 골관절염 (손, 엉덩이, 무릎 등), 결절성 다발동맥염, 라이터 증후군), 스포츠 관련 손상 (러너스 니 (runner's knee), 테니스 엘보우 (tennis elbow), 동결견 (frozen shoulder), 아킬레스 건염, 족저근막염, 윤활낭염, 오스굿-슐라터 (Osgood-Schlatter) 질환), 반복적 스트레스 손상 (축적성 외상 질환, 국소 긴장이상, 손저림 증후군, 교차 증후군, 반사 교감신경 영양실조 증후군, 협착성 건초염 (드 퀘르뱅 (De Quervain) 증후군, 방아쇠 수지/방아쇠 엄지), 흉곽출구 증후군, 건염, 건초염, 요골 관 증후군, 레이노드 (Raynaud) 질환, 결절종, 게이머 엄지, 위-아이티스 (Wii-itis) 등) 감염 (바이러스성, 진균성 및 박테리아성 포함)을 나타낼 수 있다. "염증성 상태"는 급성 또는 만성일 수 있다.
(xvii) "단리된" 또는 "정제된" 펩티드는, 단백질 또는 펩티드가 유래된 세포 또는 조직 공급원으로부터의 세포 물질 또는 다른 오염 단백질이 실질적으로 없거나, 또는 화학적으로 합성된 경우에 화학적 전구체 또는 다른 화학물질이 없다. 용어 "세포 물질이 실질적으로 없는"은, 펩티드가 단리되거나 재조합 생성되는 세포의 세포 성분으로부터 분리된 펩티드의 제조물을 포함한다. 따라서, 세포 물질이 실질적으로 없는 펩티드는 약 30%, 20%, 10% 또는 5% (건조 중량) 미만의 이종 단백질 (본원에서 "오염 단백질"로도 지칭됨)을 갖는 펩티드 제조물을 포함한다. 펩티드가 재조합 생성되는 경우, 배양 배지가 실질적으로 없는 것이 또한 바림직하다 (즉, 배양 배지는 단백질 제조물의 부피의 약 20%, 10% 또는 5% 미만에 해당함). 펩티드가 화학적 합성에 의해 생성되는 경우, 화학적 전구체 또는 다른 화학물질이 실질적으로 없는 것이 바림직하다 (즉, 단백질 합성에 관여하는 화학적 전구체 또는 다른 화학물질로부터 분리됨). 따라서, 이러한 펩티드 제조물은 관심 펩티드 이외에 약 30%, 20%, 10%, 5% 미만 (건조 중량)의 화학적 전구체 또는 화합물을 갖는다. 바람직한 실시양태에서, 본 발명의 펩티드는 단리되거나 정제된다.
(xviii) "단리된" 핵산 분자는 핵산 분자의 천연 공급원에 존재하는 다른 핵산 분자로부터 분리된 핵산 분자이다. 또한, "단리된" 핵산 분자, 예컨대 cDNA 분자는, 재조합 기술에 의해 생성된 경우에 다른 세포 물질 또는 배양 배지가 실질적으로 없을 수 있거나, 또는 화학적으로 합성된 경우에 화학적 전구체 또는 다른 화학물질이 실질적으로 없을 수 있다. 특정 실시양태에서, 본 발명의 펩티드를 코딩하는 핵산 분자(들)는 단리되거나 정제된다.
(xix) 본원에서 사용된 용어 "관리"는, (한 실시양태에서) 환자가 조직 손상과 연관된 질환 또는 장애의 손상, 영향 또는 증상을 역전시키지 않는 펩티드로부터 얻는 하나 이상의 유익한 부작용의 제공을 포함한다. 특정 실시양태에서, 증상의 진행 또는 악화를 방지하기 위한 목적으로 조직 손상과 연관된 질환 또는 장애의 증상을 "관리"하기 위해 펩티드를 환자에게 투여한다.
(xx) 용어 "조절하다", "조절" 등은 조직 손상과 연관된 질환 또는 장애에 대한 신체 반응의 매개자의 기능 및/또는 발현 (예를 들어, 조절 활성 및/또는 단백질 결합의 전사)을 증가 또는 감소시키는 화합물의 능력을 나타낸다. 본원에 기재된 "조절"은 매개자와 연관된 기능 또는 특성의 직접적이거나 간접적인 억제, 길항작용, 부분적 길항작용, 활성화, 효능작용 또는 부분적 효능작용 및/또는 매개자의 발현의 상향조절 또는 하향조절을 포함한다. 바람직한 실시양태에서, 조절은 직접적이고, 보다 바람직하게는 조절은 매개자의 억제제 또는 길항제, 즉 결합, 자극의 부분 또는 완전 차단, 감소, 예방, 억제, 활성화 지연, 불활성화, 탈감작화 또는 신호 전달의 하향조절을 수행하는 화합물을 통해 이루어진다. 본 발명의 방법에서 유용한 특정 펩티드가 매개자의 기능을 억제하는 능력은 생화학적 검정, 예를 들면 결합 검정, 세포 기재 검정, 예를 들면 일시적 형질감염 검정, 또는 생체내 검정, 예를 들면 뉴런 손상, 암, 염증, 또는 화학적 또는 방사선 손상의 동물 모델 (예컨대, 래트 또는 뮤린 모델)에 의해 입증될 수 있다.
(xxi) 본원에서 펩티드내 구조와 관련하여 사용된 용어 "모티프"는 펩티드 쇄의 아미노산 서열내 일련의 연속적인 아미노산 및/또는 상기 펩티드의 2차 및/또는 3차 구조내 선상으로 또는 공간적으로 인접한 일련의 아미노산을 나타낸다. 모티프는, 전적으로 또는 부분적으로 단백질 접힘으로 인해 형성될 수 있기 때문에, 기재된 모티프의 인접 아미노산들은 펩티드의 선형 아미노산 서열내 0개, 1개 또는 그 이상, 5개 또는 그 이상, 10개 또는 그 이상, 15개 또는 그 이상, 또는 20개 또는 그 이상의 아미노산으로 분리될 수 있다.
(xxii) 본원에서 사용된 용어 "펩티드", "폴리펩티드" 및 "단백질"은 제한된 (즉, 예를 들어 β 턴 또는 β 병풍 구조 (pleated sheet)를 개시하는 아미노산의 존재로서의 일부 구조 요소를 갖거나, 또는 예를 들면, 디술파이드-결합 Cys 잔기의 존재에 의해 고리화된) 아미노산 서열 또는 비제한된 (예를 들면, 선형) 아미노산 서열을 나타내도록 가장 넓은 의미에서 상호교환적으로 사용된다. 특정 실시양태에서, 본 발명의 펩티드는 30개 미만의 아미노산으로 구성된다. 그러나, 당업자는 본 개시를 읽었을 때, 특정 펩티드의 길이가 아니라 조직 보호 수용체 착체에 결합하고/거나 본원에 기재된 펩티드의 결합과 경쟁하는 그의 능력이 본 발명의 방법에 유용한 펩티드를 구별해준다는 점을 인지할 것이다. 용어 "펩티드", "폴리펩티드" 및 "단백질"은 또한, 아미노산 등가물 또는 다른 비-아미노산 기를 함유하며 펩티드 또는 단백질의 바람직한 기능적 활성을 여전히 보유하는 화합물을 나타낸다. 펩티드 등가물은 하나 이상의 아미노산이 관련 유기산 (예컨대, PABA), 아미노산 등가물 등으로 대체된 것에 의해, 또는 측쇄 또는 관능기가 치환 또는 변형된 것에 의해 통상의 펩티드와 구별될 수 있다.
(xxiii) 용어 "조직 손상과 연관된 질환 또는 장애의 손상, 영향 또는 증상의 예방"이란, 이러한 손상, 영향 또는 증상의 개시 지연, 진행 방해, 발생 방해, (그로부터의) 보호, 발생의 억제 또는 제거, 또는 발생 감소를 의미한다. 용어 "예방"이 사용된 경우, 이는 예방적 요법이 투여된 환자 집단의 모든 환자가 예방을 위한 표적인 조직 손상과 연관된 질환 또는 장애에 따른 증상을 전혀 갖지 않거나 그 증상을 전혀 발달시키지 않는다는 것보다는, 환자 집단이 질환 또는 장애의 손상, 영향 또는 증상의 감소를 나타낸다는 점을 의미한다. 예를 들면, 수많은 플루 백신은 백신이 투여된 대상체에서의 플루 예방에 있어서 100% 유효하지는 않다. 당업자는, 예방적 요법이 유익할 환자 및 상황, 예컨대 각종 독성제 또는 외상에 노출될 수 있는 활동에 참여할 개체 (예를 들면, 군사 작전에 참여하는 병사, 화학물질 또는 식품 가공 근로자, 응급 요원 또는 응급처치자 등), 또는 독성제에 노출될 수 있는 개체 (예를 들면, 화학물질, 핵 또는 공장 시설 근방에 거주하는 개체, 또는 군사 또는 테러 공격의 위협 하에 있는 개체) (이들로 한정되지는 않음)를 용이하게 식별할 수 있다.
(xxiv) 본원에서 사용된 "예방적 유효량"은, 조직 손상과 연관된 질환 또는 장애로 인한 손상, 영향 또는 증상의 예방을 달성하기에 충분한 펩티드 양을 나타낸다. 예방적 유효량은 조직 손상과 연관된 질환 또는 장애로 인한 손상, 영향 또는 증상을 예방하기에 충분한 펩티드 양을 나타낼 수 있다. 나아가, 또다른 예방적 작용제와 관련한 예방적 유효량은, 조직 손상과 연관된 질환 또는 장애로 인한 손상, 영향 또는 증상의 예방에 있어서 펩티드와 함께 예방적 이익을 제공하는 예방적 작용제의 양을 의미한다. 용어 "예방적 유효량"은 펩티드의 양과 함께 사용되는 경우, 예방 전반을 개선하거나 또다른 예방적 작용제의 예방적 효능을 증진시키거나 또다른 예방적 작용제와의 상승작용을 제공하는 양을 포함할 수 있다.
(xxv) 용어 "신생물"은 암성 종양의 악성 특성이 결여되어 일반적으로 경증성 및 비-진행성 종양인 비정상적 성장을 나타낸다. 신생물에는 점 (mole), 자궁근종, 갑상선 선종, 부신피질 선종, 뇌하수체 선종 및 기형종 (teratoma)이 포함되나, 이들로 한정되지는 않는다.
(xxvi) 본원에서 사용된 용어 "방사선 작용제"란, 대상체를 사망시키거나 손상시킬 수 있는 임의의 방사성 물질을 의미하며, 도시 또는 국가의 붕괴를 초래하기 위해 사용될 수 있다. 방사선 작용제로의 노출은 무기 (핵 폭탄 (핵분열, 핵융합, 중성자, 증폭 핵분열 또는 솔티드 (salted) 폭탄), 열화 우라늄을 함유하는 폭탄), 테러 장비 ("방사능 오염 폭탄 (dirty bomb)"), 또는 핵 무기의 폭발 또는 원자력 발전소의 고장으로 인한 방사능 낙진의 전개를 통해 발생할 수 있다. 방사성 작용제에는 137Cs, 60Co, 241Am, 252Cf, 192Ir, 238Pu, 90Sr, 226Ra, 91Sr, 92Sr, 95Zr, 99Mo, 106Ru, 131Sb, 132Te, 139Te, 140Ba, 141La, 144Ce, 233U, 235U, 238U, 228P, 229P, 230P, 231P, 232P, 233P, 234P, 235P, 236P, 237P, 238P, 239P, 240P, 241P, 242P, 243P, 244P, 245P, 246P, 247P 및 131I가 포함될 수 있으나, 이들로 한정되지는 않는다. 방사성 작용제로의 노출은 발암, 불임, 백내장 형성, 방사선피부염, 베타 화상, 감마 화상, 세포 손실 (특히, 골수, 소화관 세포), 조혈계, 위장계, 중추신경계, 심혈관계, 피부계 및/또는 생식기계의 손상, 급성 방사선 증후군, 만성 방사선 증후군 및 피부 방사선 증후군을 유발할 수 있다. 급성 방사선 증후군은 일반적으로, 다량의 방사선이 대상체의 신체에 단기간 가해지는 경우로부터 발생한다. 이 증후군은 구역, 구토, 일반 질병 및 피로의 감각과 함께 출발하는 예측가능한 과정 (면역계 우울증, 모발 손실, 제어불가능한 출혈 (입, 피하, 신장), 대량 설사, 섬망 (delirium), 혼수 및 사망)을 갖는다. 피부 방사선 증후군은 급성 방사선 증후군의 아류이며, 피부 상에서의 방사선 작용을 나타내며, 염증, 홍반, 건성 또는 습성 박리, 모발 손실, 수포, 홍조, 궤양, 피지선 및 한선의 손상, 위축, 섬유증, 감소 또는 증가된 피부 색소침착 및 괴사를 포함하나, 이들로 한정되지는 않는다.
(xxvii) 본원에서 사용된 용어 "대상체", "환자" 및 "희생자"는 상호교환적으로 사용된다. 본원에서 사용된 용어 "대상체" 및 "대상체들"은 동물, 바람직하게는 포유동물, 예를 들어 비-영장류 (예를 들면, 소, 돼지, 말, 고양이, 개, 래트 및 마우스) 및 영장류 (예를 들면, 원숭이, 유인원 또는 인간), 보다 바람직하게는 인간을 나타낸다.
(xxviii) 본원에서 사용된 용어 "신생물 또는 암과 연관된 증후군"은 "덩어리 효과 (mass effect)" (종양으로 인한 생명 유지 기관의 압박) 또는 "기능성 종양" (종양을 앓는 기관에 의한 호르몬 과생성)을 통해 종양의 직접적인 작용으로부터 비롯된 증후군을 나타낸다. 이러한 증후군에는 벡위드-위드먼 (Beckwith-Wiedmann) 증후군, SBLA 증후군, 리-프라우메니 (Li-Fraumeni) 증후군, 가족성 선종 폴립증 증후군 (가드너 (Gardner) 증후군), 유전성 비-폴립증성 결장직장암, 터코트 (Turcot) 증후군, 카우덴 (Cowden) 증후군, 카니 트라이어드 (Carney Triad) 증후군, 다발성 내분비계 신생물 증후군 (베르머 (Wermer) (MEN-1), 시플 (Sipple) (MEN-2a, MEN-2b), 폰 히플레-린다우 (Von Hipple-Lindau) 증후군, 쿠싱 (Cushing) 증후군, 애디슨 (Addison) 증후군, 베르너 모리슨 (Verner Morrison) 증후군, 졸링거-엘리슨 (Zollinger-Ellison) 증후군, WDHA 증후군, 췌장 무도병, 아이삭 (Isaac) 증후군, 리플링 (Rippling) 근육 증후군, 스티프먼 (Stiffman) 증후군, 부신생물 운동실조증, Yo 증후군, Tr 증후군, Hu 증후군, CV-2 증후군, CRMP-5 증후군, 안진전/간대성 근경련, Ma 증후군, 모반 (Morvan) 세동성 무도병, 반나얀-라일리-루날카바 (Bannayan-Riley-Runalcaba) 증후군, 포이츠-예거 (Peutz-Jegher) 증후군, 무어-토레 (Muir-Torre) 증후군, 히르쉬프룽 (Hirschsprung) 질환, 린치 (Lynch) 증후군, 램버트-이튼 (Lambert-Eaton) 근무력 증후군, 중증 근무력증, 신경근강직증, 부신생물성 소뇌 변성, 부신생물성 변연엽 뇌염, 스위트 (Sweet) 증후군, 버트-호그-듀브 (Birt-Hogg-Dube) 증후군, 모반양 기저세포 암종 증후군, 범 기저양 소포성 증후군, 과오종 증후군, 바젝스 (Bazex) 증후군, 브룩 스피글러 (Brooke Spiegler) 증후군, 가족성 원주종, 다발성 가족성 모낭상피종, 안드로겐 결핍 증후군, 요법-관련 골수이형성 증후군, 기면 증후군, 걸프전 증후군 및 소마토스타틴종 증후군이 포함되나, 이들로 한정되지는 않는다.
(xxvix) 본원에서 사용된 용어 "조직 보호 활성" 또는 "조직 보호"는 세포, 조직 또는 기관의 손상 또는 사멸을 억제하거나 지연시키는 작용을 나타낸다. 달리 명시되지 않는다면, 세포, 조직 또는 기관의 손상 또는 사멸에서의 "지연"은 본 발명의 펩티드의 부재 하에서의 대조군 상태를 기준으로 평가된다. 조직 보호 활성은 조직 보호 수용체 착체를 발현하는 조직, 세포 및/또는 기관 (즉, 각각 반응성 조직, 세포 및/또는 기관), 예컨대 중추신경계의 조직 (이들로 한정되지는 않음)에 대해 특이적이다. 특정 실시양태에서, 반응성 세포는 적혈구 전구세포가 아니다.
(xxx) 본원에서 사용된 용어 "조직 보호 수용체 착체"란, 하나 이상의 에리트로포이에틴 수용체 서브유닛 및 하나 이상의 통상적인 베타 수용체 서브유닛을 포함하는 착체를 의미한다. 조직 보호 수용체 착체는 다발성 에리트로포이에틴 수용체 서브유닛 및/또는 통상적인 베타 수용체 서브유닛, 및 다른 유형의 수용체 또는 단백질을 함유할 수 있다. WO 2004/096148 (이로써 그 전문이 본원에 참조로 포함됨)을 참조한다
(xxxi) 본원에서 사용된 용어 "독성제"는 앞서 언급된 생물학적, 화학적 및 방사선 작용제를 나타낸다.
(xxxii) 두 아미노산 서열의 동일성 (%)을 측정하기 위해, 최적의 비교를 목적으로 서열을 정렬한다. 이후, 상응하는 아미노산 위치에서의 아미노산 잔기를 비교한다. 제1 서열에서의 위치가, 제2 서열에서의 상응하는 위치의 아미노산 잔기와 동일한 아미노산 잔기에 의해 점유된 경우, 분자들은 그 위치에서 동일하다. 두 서열간의 동일성 (%)은 서열들이 공유하는 동일 위치들의 개수의 함수이다 (즉, 동일성 (%) = 동일 중첩 위치 개수 x 100 / 위치의 총 개수). 한 실시양태에서, 두 서열은 동일한 길이를 갖는다. 또다른 실시양태에서, 서열들이 상이한 길이를 가짐에 따라, 동일성 (%)은 긴 서열의 부분에 대한 짧은 서열의 비교 (상기 부분은 상기 짧은 서열과 동일한 길이를 가짐)를 나타낸다.
(xxxiii) 본원에서 사용된 용어 "치료"는 조직 손상과 연관된 질환 또는 장애 또는 그의 손상, 영향 또는 증상으로 인한 손상, 영향 또는 증상의 제거, 감소, 관리 또는 제어를 포함한다.
본 발명은 반응성 세포, 조직 또는 기관에서 조직 보호 활성을 갖는 단리된 펩티드 및 펩티드 유사체를 제공한다. 상기 펩티드 및 펩티드 유사체는 잠재적으로 바람직하지 않은 조혈 작용이 거의 또는 전혀 없다. 예시적인 조직 보호 활성에는 반응성 포유동물 세포, 조직 또는 기관의 기능 또는 생존율을 보호, 유지, 증진 및 회복시키는 것이 포함되나, 이들로 한정되지는 않는다.
5. 도면의 간단한 설명
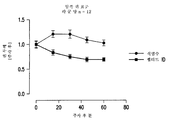
도 1은 EPO 또는 펩티드 ID (서열 282)의 존재 하에서의 UT-7 EPO 세포 증식에 관한 도표이다. 그래프에 나타난 바와 같이, EPO는 UT-7 EPO 세포의 증식을 일으키지만, 펩티드 ID는 모든 용량에서 세포 증식을 일으키지 않으며, 이는 펩티드 ID가 에리트로포이에틴성이 아님을 나타낸다.
도 2는 펩티드 ID가 28일에 걸쳐 하루에 2회 정맥내 투여된 스프라그 돌리 (Sprague Dawley) 래트에서의 헤모글로빈 농도를 나타내는 도표이다. 그래프에 나타난 바와 같이, 펩티드가 투여되지 않은 래트의 헤모글로빈 농도는 펩티드 ID가 투여된 래트의 경우와 동일한 바, 이는 펩티드 ID가 비-조혈성임을 나타낸다.
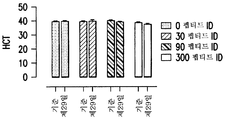
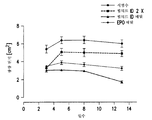
도 3은 다양한 용량의 펩티드 ID가 28일에 걸쳐 하루에 2회 정맥내 투여된 뉴질랜드 백색 토끼로부터 취해진 혈액 샘플에서의 (a) 헤모글로빈 농도, (b) 적혈구용적률 및 (c) 혈소판 수를 나타내는 일련의 막대 그래프이다. 그래프에 나타난 바와 같이, 펩티드 ID의 투여는 모든 용량에서 동물의 헤모글로빈 농도, 적혈구용적률 또는 혈소판 수에 아무런 영향을 미치지 않았다.
도 4는 카인산이 처리된 운동뉴런의 상대 생존율을 나타내는 막대 그래프이다. 그래프에 나타난 바와 같이, 펩티드 B (서열 3) 또는 EPO로 사전 처치된 세포들은 개선된 생존율을 나타냈다.
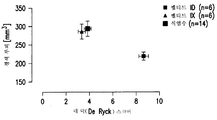
도 5는 중간 뇌동맥 폐색 및 식염수, 펩티드 ID 또는 펩티드 IX (서열 301)의 처치 후에 풋 폴트 (foot fault) 시험이 수행된 래트의 데 릭 (De Ryck) 스코어를 나타내는 표이다. 도표에 나타난 바와 같이, 펩티드 ID는 식염수-처치된 래트 (20.2 ± 0.8 풋 폴트) 및 펩티드 IX-처치된 래트 (20.1 ± 2.1 풋 폴트)에 비해, 풋 폴트 프로토콜에서의 래트 거동을 유의하게 개선하였다 (11.2 ± 1.1 풋 폴트).
도 6은 30분의 양쪽 신장 허혈에 이어 24시간 동안의 재관류가 수행된 마우스 (PBS (대조군), 1분째 1 ㎍/kg의 펩티드 ID, 30분째 1 ㎍/kg의 펩티드 ID, 6시간째 1 ㎍/kg의 펩티드 ID 또는 6시간째 10 ㎍/kg의 펩티드 ID가 재관류로 투여됨)의 혈청에서 크레아티닌 (그래프 A), 우레아 (그래프 B) 및 아스파르테이트 아미노트랜스퍼라제 (AST) (그래프 C)의 농도에 관한 일련의 그래프이다. 각 그래프에 나타난 바와 같이, 6시간째 1 ㎍/kg의 펩티드 ID (재관류) 또는 6시간째 10 ㎍/kg의 펩티드 ID (재관류)의 경우, 신장 기능이상의 생화학적 마커가 감소되었다.
도 7은 30분의 양쪽 신장 허혈에 이어 24시간 동안의 재관류가 수행된 마우스 (다중 용량의 PBS (대조군), 0.1 ㎍/kg의 펩티드 ID, 1 ㎍/kg의 펩티드 ID 또는 10 ㎍/kg의 펩티드 ID가 1분, 6시간 및 12시간째에 재관류로 투여됨)의 혈청에서 크레아티닌 (그래프 A), 우레아 (그래프 B) 및 아스파르테이트 아미노트랜스퍼라제 (AST) (그래프 C)의 농도에 관한 일련의 그래프이다. 각 그래프에 나타난 바와 같이, 1 ㎍/kg의 펩티드 ID 또는 10 ㎍/kg의 펩티드 ID의 경우, 신장 기능이상의 생화학적 마커가 감소되었다.
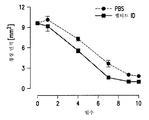
도 8은 펩티드 ID (24 nmol/kg bw)가 매일 피하 투여된 래트에서, 전체 두께 펀치 생검 창상 검정법 (full thickness punch biopsy wound assay)에 따라 처치 기간에 걸친 창상 부위 감소를 나타내는 도표이다. 도표에 나타난 바와 같이, 펩티드 ID가 투여된 래트의 창상은 보다 빠르게 회복되었다.
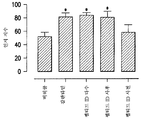
도 9는 식염수, 양성 대조군 갈란타민 (3 mg/kg bw) 또는 펩티드 ID (24 nmol/kg bw)가 다양한 시점에 투여된 성체 위스터 (Wistar) 래트에서 수행된 새로운 물체 인식 시험의 결과를 나타내는 막대 그래프이다. 그래프에 나타난 바와 같이, 갈란타민 및 펩티드 ID는 래트의 새로운 물체 인식을 증가시켰다.
도 10은 시스플라틴, 시스플라틴 및 펩티드 IC (서열 281), 또는 PBS (대조군)로 처치된 래트들에 의해 생성된 요의 부피를 비교하는 그래프이다. 그래프는, 시스플라틴 및 펩티드 IC-처치된 래트의 요 부피가 대조군 (PBS)의 경우와 실질적으로 유사하였음을 나타낸다. 따라서, 그래프는 시스플라틴-유발성 신병증의 래트 모델에서, 펩티드 IC가 5주에 걸쳐 0.4 ㎍/kg의 용량으로 일주일에 3회 투여된 경우, 처치된 래트가 시스플라틴으로 인한 신장 손상으로부터 보호되었음을 나타낸다.
도 11은 시스플라틴, 시스플라틴 + 펩티드 IC, 또는 PBS (대조군)로 처치된 래트에서, 래트가 가열판으로부터 앞발을 거둬들이는 데 걸리는 시간을 비교하는 그래프이다. 그래프는 시스플라틴 및 펩티드 IC로 처치된 래트가 가열판으로부터 앞발을 거둬들이는 데 걸리는 시간이 대조군 (PBS)의 경우와 실질적으로 유사하였음을 나타낸다. 따라서, 그래프는 시스플라틴-유발성 신경병증의 래트 모델에서, 펩티드 IC가 5주에 걸쳐 0.4 ㎍/kg의 용량으로 일주일에 3회 투여된 경우, 처치된 래트가 시스플라틴으로 인한 말초 신경병증으로부터 보호되었음을 나타낸다.
도 12는 문헌 [Lampson L.A. et al., 193, Cancer Res. 53(1):176-82]의 프로토콜에 따라 래트 뇌에 이식된 피질 종양의 상대 부피를 25일 후에 비교한 그래프이다. 그래프에 따르면, 식염수로 처치된 래트의 종양의 상대 부피는 0.4 cm2 약간 넘게 증가되었으나, 이식후 펩티드 ID로 처치된 래트에서는 종양의 상대 부피의 증가가 나타나지 않았다.
도 13은 문헌 [Lampson L.A. et al., 193, Cancer Res. 53(1):176-82]의 프로토콜에 따라 래트 뇌에 이식된 피질 종양의 상대 부피를 25일 후에 비교한 그래프이다. 그래프에 따르면, 식염수로 처치된 래트의 종양의 상대 부피 (이식 2주후 시작)는 약 300 mm2를 넘지만, 펩티드 ID 및 펩티드 IW (반감기가 연장된 펩티드, 서열 305)로 처치한 경우 (이식 2주후 시작), 두 경우 모두에서 종양 크기가 감소되었다. 2주차에서 펩티드 IW를 투여한 경우, 펩티드 ID의 즉시 처치에 의해 달성된 것과 동등한 종양 크기의 감소가 달성되었다.
도 14는 식염수 (매일), 펩티드 ID 또는 펩티드 IW (2주 지연 후)로 처치된 래트에서 피질 종양 크기의 비교도이다. 사진 상의 어두운 영역은 종양의 존재를 나타낸다. 비교 사진은 2주 후의 펩티드 IW 투여가, 종양 이식 직후에 펩티드 ID를 투여한 경우와 유사한 종양 크기 감소를 일으켰음을 명확하게 나타낸다.
도 15는 히스타민 디포스페이트가 피부내 주사된 스프라그 돌리 래트의 귀에서의 귀 두께 차이를 나타낸다. 래트는 펩티드 ID (정맥내) 또는 식염수로 처치하였다. 펩티드 ID로 처치된 래트의 귀는 식염수로 처치된 래트의 귀에 비해 적은 히스타민-유발성 염증을 나타냈다.
도 16은 식염수로 사전 처치된 래트 및 펩티드 ID로 사전 처치된 래트에서, 피부내 투여된 히스타민으로 인한 래트 복부 상의 팽진 (두드러기) 크기의 차이를 나타내는 도표이다. 도표는 히스타민 주사후 24시간까지 펩티드 ID의 항염증성 효과를 나타낸다.
도 17은 EPO로 처치된 래트 및 식염수로 처치된 래트 사이에서, 히스타민으로 인한 팽진 (두드러기) 면적의 차이를 나타내는 도표이다. 15분 후의 팽진 면적은 식염수로 처치된 래트보다 EPO로 처치된 래트에서 더 적었다.
도 18은 히스타민이 투여되고 식염수, 펩티드 IY (서열 304), 펩티드 ID 및 펩티드 IW로 처치된 래트에서 팽진 (두드러기) 크기 (병변 면적)의 차이를 비교한 도표이다. 펩티드 ID 또는 펩티드 IW로 처치된 동물은 식염수 및 펩티드 IY-처치된 동물 상의 병변 면적 (약 .6 cm2)의 거의 절반 (각각, 약 .35 cm2 및 .3 cm2)을 나타냈다.
도 19는 히스타민이 투여되고 식염수, 펩티드 JA (서열 301), 펩티드 IW, 펩티드 IZ (서열 300) 및 펩티드 ID로 처치된 래트에서 팽진 (두드러기) 크기 (병변 면적)의 차이를 비교한 도표이다. 펩티드 IW, IZ 또는 ID로 처치된 동물은 식염수 및 펩티드 JA-처치된 동물 (둘 다 약 .6 cm2)의 경우보다 적은 병변 면적 (각각, .3 cm2, .352 및 .4 cm2)을 나타냈다.
도 20은 압박성 궤양을 겪으며 식염수, 펩티드 ID (2회 투여), 펩티드 ID (매일 투여) 또는 EPO (매일 투여)로 처치된 래트에서 창상 (궤양) 크기 (면적)의 차이를 비교한 도표이다. 도표에 따르면, 펩티드 ID 및 EPO-처치된 래트는 식염수-처치된 래트보다 우수한 창상 치유를 나타냈다. 매일 펩티드 ID로 처치된 동물은 가장 작은 창상 크기를 가졌다.
도 21은 796cGy (A) 또는 831cGy (B)가 방사선 조사된 후에 29일간 매일 펩티드 ID로 피하 처치되거나 (조사 후) 29일간 PBS로 피하 처치된 마우스의 카플란 마이어 (Kaplan Meier) 생존 곡선을 나타낸다. 두 방사선 용량에서, 펩티드 ID는 30일차에 마우스의 전체 생존 시간을 유의하게 증가시켰다 (796cGy: 30일차에 45% 생존율, 831cGy; 30일차에 20% 생존율).
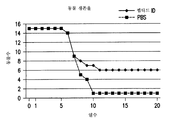
도 22는 15Gy의 부분적인 신체 방사선 조사 후 펩티드 ID (1일차 및 이후 매일) 또는 PBS (1일차 및 이후 매일)로 처치된 마우스의 생존율을 나타내는 도표이다. 도표에 나타난 바와 같이, 20일차까지 생존한 마우스의 수는 PBS가 투여된 마우스에 비해, 펩티드 ID가 투여된 마우스에서 실질적으로 많았다 (6마리의 펩티드-처치된 마우스 대 1마리의 PBS-처치된 마우스).
도 1은 EPO 또는 펩티드 ID (서열 282)의 존재 하에서의 UT-7 EPO 세포 증식에 관한 도표이다. 그래프에 나타난 바와 같이, EPO는 UT-7 EPO 세포의 증식을 일으키지만, 펩티드 ID는 모든 용량에서 세포 증식을 일으키지 않으며, 이는 펩티드 ID가 에리트로포이에틴성이 아님을 나타낸다.
도 2는 펩티드 ID가 28일에 걸쳐 하루에 2회 정맥내 투여된 스프라그 돌리 (Sprague Dawley) 래트에서의 헤모글로빈 농도를 나타내는 도표이다. 그래프에 나타난 바와 같이, 펩티드가 투여되지 않은 래트의 헤모글로빈 농도는 펩티드 ID가 투여된 래트의 경우와 동일한 바, 이는 펩티드 ID가 비-조혈성임을 나타낸다.
도 3은 다양한 용량의 펩티드 ID가 28일에 걸쳐 하루에 2회 정맥내 투여된 뉴질랜드 백색 토끼로부터 취해진 혈액 샘플에서의 (a) 헤모글로빈 농도, (b) 적혈구용적률 및 (c) 혈소판 수를 나타내는 일련의 막대 그래프이다. 그래프에 나타난 바와 같이, 펩티드 ID의 투여는 모든 용량에서 동물의 헤모글로빈 농도, 적혈구용적률 또는 혈소판 수에 아무런 영향을 미치지 않았다.
도 4는 카인산이 처리된 운동뉴런의 상대 생존율을 나타내는 막대 그래프이다. 그래프에 나타난 바와 같이, 펩티드 B (서열 3) 또는 EPO로 사전 처치된 세포들은 개선된 생존율을 나타냈다.
도 5는 중간 뇌동맥 폐색 및 식염수, 펩티드 ID 또는 펩티드 IX (서열 301)의 처치 후에 풋 폴트 (foot fault) 시험이 수행된 래트의 데 릭 (De Ryck) 스코어를 나타내는 표이다. 도표에 나타난 바와 같이, 펩티드 ID는 식염수-처치된 래트 (20.2 ± 0.8 풋 폴트) 및 펩티드 IX-처치된 래트 (20.1 ± 2.1 풋 폴트)에 비해, 풋 폴트 프로토콜에서의 래트 거동을 유의하게 개선하였다 (11.2 ± 1.1 풋 폴트).
도 6은 30분의 양쪽 신장 허혈에 이어 24시간 동안의 재관류가 수행된 마우스 (PBS (대조군), 1분째 1 ㎍/kg의 펩티드 ID, 30분째 1 ㎍/kg의 펩티드 ID, 6시간째 1 ㎍/kg의 펩티드 ID 또는 6시간째 10 ㎍/kg의 펩티드 ID가 재관류로 투여됨)의 혈청에서 크레아티닌 (그래프 A), 우레아 (그래프 B) 및 아스파르테이트 아미노트랜스퍼라제 (AST) (그래프 C)의 농도에 관한 일련의 그래프이다. 각 그래프에 나타난 바와 같이, 6시간째 1 ㎍/kg의 펩티드 ID (재관류) 또는 6시간째 10 ㎍/kg의 펩티드 ID (재관류)의 경우, 신장 기능이상의 생화학적 마커가 감소되었다.
도 7은 30분의 양쪽 신장 허혈에 이어 24시간 동안의 재관류가 수행된 마우스 (다중 용량의 PBS (대조군), 0.1 ㎍/kg의 펩티드 ID, 1 ㎍/kg의 펩티드 ID 또는 10 ㎍/kg의 펩티드 ID가 1분, 6시간 및 12시간째에 재관류로 투여됨)의 혈청에서 크레아티닌 (그래프 A), 우레아 (그래프 B) 및 아스파르테이트 아미노트랜스퍼라제 (AST) (그래프 C)의 농도에 관한 일련의 그래프이다. 각 그래프에 나타난 바와 같이, 1 ㎍/kg의 펩티드 ID 또는 10 ㎍/kg의 펩티드 ID의 경우, 신장 기능이상의 생화학적 마커가 감소되었다.
도 8은 펩티드 ID (24 nmol/kg bw)가 매일 피하 투여된 래트에서, 전체 두께 펀치 생검 창상 검정법 (full thickness punch biopsy wound assay)에 따라 처치 기간에 걸친 창상 부위 감소를 나타내는 도표이다. 도표에 나타난 바와 같이, 펩티드 ID가 투여된 래트의 창상은 보다 빠르게 회복되었다.
도 9는 식염수, 양성 대조군 갈란타민 (3 mg/kg bw) 또는 펩티드 ID (24 nmol/kg bw)가 다양한 시점에 투여된 성체 위스터 (Wistar) 래트에서 수행된 새로운 물체 인식 시험의 결과를 나타내는 막대 그래프이다. 그래프에 나타난 바와 같이, 갈란타민 및 펩티드 ID는 래트의 새로운 물체 인식을 증가시켰다.
도 10은 시스플라틴, 시스플라틴 및 펩티드 IC (서열 281), 또는 PBS (대조군)로 처치된 래트들에 의해 생성된 요의 부피를 비교하는 그래프이다. 그래프는, 시스플라틴 및 펩티드 IC-처치된 래트의 요 부피가 대조군 (PBS)의 경우와 실질적으로 유사하였음을 나타낸다. 따라서, 그래프는 시스플라틴-유발성 신병증의 래트 모델에서, 펩티드 IC가 5주에 걸쳐 0.4 ㎍/kg의 용량으로 일주일에 3회 투여된 경우, 처치된 래트가 시스플라틴으로 인한 신장 손상으로부터 보호되었음을 나타낸다.
도 11은 시스플라틴, 시스플라틴 + 펩티드 IC, 또는 PBS (대조군)로 처치된 래트에서, 래트가 가열판으로부터 앞발을 거둬들이는 데 걸리는 시간을 비교하는 그래프이다. 그래프는 시스플라틴 및 펩티드 IC로 처치된 래트가 가열판으로부터 앞발을 거둬들이는 데 걸리는 시간이 대조군 (PBS)의 경우와 실질적으로 유사하였음을 나타낸다. 따라서, 그래프는 시스플라틴-유발성 신경병증의 래트 모델에서, 펩티드 IC가 5주에 걸쳐 0.4 ㎍/kg의 용량으로 일주일에 3회 투여된 경우, 처치된 래트가 시스플라틴으로 인한 말초 신경병증으로부터 보호되었음을 나타낸다.
도 12는 문헌 [Lampson L.A. et al., 193, Cancer Res. 53(1):176-82]의 프로토콜에 따라 래트 뇌에 이식된 피질 종양의 상대 부피를 25일 후에 비교한 그래프이다. 그래프에 따르면, 식염수로 처치된 래트의 종양의 상대 부피는 0.4 cm2 약간 넘게 증가되었으나, 이식후 펩티드 ID로 처치된 래트에서는 종양의 상대 부피의 증가가 나타나지 않았다.
도 13은 문헌 [Lampson L.A. et al., 193, Cancer Res. 53(1):176-82]의 프로토콜에 따라 래트 뇌에 이식된 피질 종양의 상대 부피를 25일 후에 비교한 그래프이다. 그래프에 따르면, 식염수로 처치된 래트의 종양의 상대 부피 (이식 2주후 시작)는 약 300 mm2를 넘지만, 펩티드 ID 및 펩티드 IW (반감기가 연장된 펩티드, 서열 305)로 처치한 경우 (이식 2주후 시작), 두 경우 모두에서 종양 크기가 감소되었다. 2주차에서 펩티드 IW를 투여한 경우, 펩티드 ID의 즉시 처치에 의해 달성된 것과 동등한 종양 크기의 감소가 달성되었다.
도 14는 식염수 (매일), 펩티드 ID 또는 펩티드 IW (2주 지연 후)로 처치된 래트에서 피질 종양 크기의 비교도이다. 사진 상의 어두운 영역은 종양의 존재를 나타낸다. 비교 사진은 2주 후의 펩티드 IW 투여가, 종양 이식 직후에 펩티드 ID를 투여한 경우와 유사한 종양 크기 감소를 일으켰음을 명확하게 나타낸다.
도 15는 히스타민 디포스페이트가 피부내 주사된 스프라그 돌리 래트의 귀에서의 귀 두께 차이를 나타낸다. 래트는 펩티드 ID (정맥내) 또는 식염수로 처치하였다. 펩티드 ID로 처치된 래트의 귀는 식염수로 처치된 래트의 귀에 비해 적은 히스타민-유발성 염증을 나타냈다.
도 16은 식염수로 사전 처치된 래트 및 펩티드 ID로 사전 처치된 래트에서, 피부내 투여된 히스타민으로 인한 래트 복부 상의 팽진 (두드러기) 크기의 차이를 나타내는 도표이다. 도표는 히스타민 주사후 24시간까지 펩티드 ID의 항염증성 효과를 나타낸다.
도 17은 EPO로 처치된 래트 및 식염수로 처치된 래트 사이에서, 히스타민으로 인한 팽진 (두드러기) 면적의 차이를 나타내는 도표이다. 15분 후의 팽진 면적은 식염수로 처치된 래트보다 EPO로 처치된 래트에서 더 적었다.
도 18은 히스타민이 투여되고 식염수, 펩티드 IY (서열 304), 펩티드 ID 및 펩티드 IW로 처치된 래트에서 팽진 (두드러기) 크기 (병변 면적)의 차이를 비교한 도표이다. 펩티드 ID 또는 펩티드 IW로 처치된 동물은 식염수 및 펩티드 IY-처치된 동물 상의 병변 면적 (약 .6 cm2)의 거의 절반 (각각, 약 .35 cm2 및 .3 cm2)을 나타냈다.
도 19는 히스타민이 투여되고 식염수, 펩티드 JA (서열 301), 펩티드 IW, 펩티드 IZ (서열 300) 및 펩티드 ID로 처치된 래트에서 팽진 (두드러기) 크기 (병변 면적)의 차이를 비교한 도표이다. 펩티드 IW, IZ 또는 ID로 처치된 동물은 식염수 및 펩티드 JA-처치된 동물 (둘 다 약 .6 cm2)의 경우보다 적은 병변 면적 (각각, .3 cm2, .352 및 .4 cm2)을 나타냈다.
도 20은 압박성 궤양을 겪으며 식염수, 펩티드 ID (2회 투여), 펩티드 ID (매일 투여) 또는 EPO (매일 투여)로 처치된 래트에서 창상 (궤양) 크기 (면적)의 차이를 비교한 도표이다. 도표에 따르면, 펩티드 ID 및 EPO-처치된 래트는 식염수-처치된 래트보다 우수한 창상 치유를 나타냈다. 매일 펩티드 ID로 처치된 동물은 가장 작은 창상 크기를 가졌다.
도 21은 796cGy (A) 또는 831cGy (B)가 방사선 조사된 후에 29일간 매일 펩티드 ID로 피하 처치되거나 (조사 후) 29일간 PBS로 피하 처치된 마우스의 카플란 마이어 (Kaplan Meier) 생존 곡선을 나타낸다. 두 방사선 용량에서, 펩티드 ID는 30일차에 마우스의 전체 생존 시간을 유의하게 증가시켰다 (796cGy: 30일차에 45% 생존율, 831cGy; 30일차에 20% 생존율).
도 22는 15Gy의 부분적인 신체 방사선 조사 후 펩티드 ID (1일차 및 이후 매일) 또는 PBS (1일차 및 이후 매일)로 처치된 마우스의 생존율을 나타내는 도표이다. 도표에 나타난 바와 같이, 20일차까지 생존한 마우스의 수는 PBS가 투여된 마우스에 비해, 펩티드 ID가 투여된 마우스에서 실질적으로 많았다 (6마리의 펩티드-처치된 마우스 대 1마리의 PBS-처치된 마우스).
6. 본 발명의 상세한 설명
6.1
단리된
폴리펩티드
본 발명은 조직 손상과 연관된 질환 또는 장애에 대한 신체 반응의 영향을 조절하는 방법을 제공한다. 또한, 본 발명은 에리트로포이에틴 또는 또다른 1형 사이토킨으로부터 유래된 펩티드를 투여함으로써, 조직 손상과 연관된 질환 또는 장애를 앓는 환자에서의 손상, 영향 또는 증상을 예방, 치료, 개선 또는 관리하는 방법을 제공한다. 바람직하게는, 본 발명의 방법에서 사용되는 펩티드는 조직 보호성, 신경보호성, 신경돌기생성성 (neuritogenic) 또는 항아팝토시스성 펩티드이다.
1형 사이토킨, 예컨대 EPO로부터 유래된 여러가지 펩티드가 다음과 같이 당업계에 개시되어 있다: (a) 및 (b) 브라인즈 (Brines) 등의 PCT/US2006/031061 (WO 2007/019545로 공개됨) 및 미국 특허 출원 "Tissue Protective Peptides and Peptide Analogs for Preventing and Treating Diseases and Disorders Associated with Tissue Damage" (2008년 1월 22일자로 출원된 연속 출원 제61/062,012호); "EPO-derived Tissue Protective Peptides and Peptide Analogs for Preventing and Treating Disorders Associated with Tissue Damage" (2008년 1월 22일자로 출원된 연속 출원 제61/062,022호); 및 "Method of Treating Inflammation or Inflammatory Conditions and Symptoms Thereof with Peptides" (2008년 7월 3일자로 출원된 연속 출원 제61/133,912호; "브라인즈"); (c) 보크 (Bock) 등의 PCT 출원 번호 제DK2006/000246호 (WO 2006/119767로 공개됨) 및 WO 2007/071248 ("보크"); (d) 오브라이언 (O'Brien) 등의 미국 특허 제5,571,787호, 제5,700,909호, 제5,696,080호, 제5,714,459호, 제6,590,074호, 제6,559,124호, 제6,271,196호, 제6,268,347호 및 제6,849,602호 ("오브라이언"); (e) 스미스-스윈토스키 (Smith-Swintowsky) 등의 미국 특허 제7,259,146호 및 미국 공개 공보 제20030130197호 ("스미스-스윈토스키"); 및 (f) 유안 (Yuan) 등의 PCT/IB2006/003581 (WO 2007/052154로 공개됨) ("유안") (이들 발명 각각은 이로써 그 전문이 본원에 참조로 포함됨).
상기 모티프들을 논의하기 위한 목적으로, EPO의 3차원 구조는 문헌 [Cheetham et al., 1998, Nat. Struct. Biol. 5; 861-866] (이로써 그의 전문은 본원에 참조로 포함됨)에 기재된 바와 같이, 그리고 서열 1에 기재된 바와 같이 (미국 국립 생물공학 정보 센터의 단백질 데이타 뱅크에 수탁된 데이타로도 입수가능함 (엔트리: "1BUY")) 허용된다.
앞서 기술된 바와 같이, 조직 손상과 연관된 질환 또는 장애에 대한 신체 반응을 조절하는 데 유용하고/거나 조직 손상과 연관된 질환 또는 장애를 앓는 대상체에서의 손상, 영향 또는 증상을 예방, 치료, 개선 및 관리하는 데 유용한 펩티드는, (한 실시양태에서) EPO 단백질의 3차원 구조로부터 유래되고 특히 리간드 결합 부위 및/또는 EPOR 동종이량체의 내부 부분과 방향이 다른 EPO 영역으로부터 유래된, EPO의 아미노산 서열의 단편을 기재로 한 모티프를 갖는다. 이들 단편은 다음과 같은 EPO 구조로부터 유래된다: (1) 헬릭스 B의 N-말단 부분 및 루프 AB (펩티드 A:NITVPDTKVNFYAWKRMEVG, 서열 2, 서열 1의 아미노산 38-57에 상응함); (2) 헬릭스 B의 C-말단 부분 (펩티드 B:QQAVEVWQGLALLSEAVLRGQALLV, 서열 3, 서열 1의 아미노산 58-82에 상응함) 및 (3) 작은 시스테인 루프 및 β-병풍 구조로 이루어진 A-B 루프의 일부 (펩티드 C:GCAEHCSLNENITVPDTKVN, 서열 4, 서열 1의 아미노산 28-47에 상응함).
구체적으로, 상기 모티프는 다음과 같을 수 있다.
(a) 구조적 모티프 A
이 구조적 모티프에서, 조직 손상과 연관된 질환 또는 장애 또는 그로 인한 손상, 영향 또는 증상의 예방, 치료, 개선 또는 관리에 유용한 펩티드는, 소수성 아미노산들로 플랭킹된 5개 이하의 아미노산에 의해 분리될 수 있는 음전하로 하전된 아미노산 2개를 갖는다. 구조적으로, 이는 H1-N1-(X)n-N2-H2 (여기서, n은 0 내지 5임) (서열 5) 또는 별법으로,
(a1) HNNH, 서열 6;
(a2) HNXNH, 서열 7;
(a3) HNXXNH, 서열 8;
(a4) HNXXXNH, 서열 9;
(a5) HNXXXXNH, 서열 10; 또는
(a6) HNXXXXXNH, 서열 11
로 표시될 수 있고, 여기서 H는 소수성 아미노산 (예를 들면, 중간 수준 소수성의 아미노산, 즉 Gly (G), Pro (P), Cys (C), Tyr (Y) 및 Trp (W), 및 바람직하게는 고도 소수성 아미노산, 즉 Ala (A), Val (V), Ile (I), Met (M), Leu (L), Phe (F))을 나타내고, N은 음전하로 하전된 아미노산, 예컨대 Glu (E) 또는 Asp (D)을 나타내고, X는 임의의 아미노산 (바람직하게는 친수성 아미노산)을 나타낸다.
플랭킹 소수성 아미노산 중 하나가 Ser (S), Thr (T), Asn (N) 또는 Gln (Q)과 같은 극성 아미노산으로 대체된, H1-N1-(X)n-N2-L1 (여기서, n은 0 내지 5임) (서열 12) 또는 L1-N1-(X)n-N2-H1 (여기서, n은 0 내지 5임) (서열 13)로 구조적으로 표시되는 구조적 모티프의 한 변형이 개시된다.
상기 모티프의 예는 다음과 같다:
펩티드 D
APPRLICDSRVLERYLLEAKEAE
(서열 14);
펩티드 A
NITVPDTKVNFYAWKRMEVG
(서열 2); 및
펩티드 B
QQAVEVWQGLALLSEAVLRGQALLV
(서열 3).
구조적 모티프 A의 특정 실시양태에서, 조직 손상과 연관된 질환 또는 장애 또는 그로 인한 손상, 영향 또는 증상의 예방, 치료, 개선, 관리에 유용한 단리된 펩티드 및 펩티드 유사체 부류는 하기 화학식 I (서열 15)을 가질 수 있다.
(상기 식에서,
X1은 Cys (C) 또는 Pro (P)이고;
X2는 Asp (D) 또는 Pro (P)이고;
X3은 Ser (S) 또는 Arg (R)이고;
X4는 Arg (R) 또는 Leu (L)이고;
X5는 Val (V) 또는 Ile (I)이고;
X6은 Leu (L) 또는 Cys (C)이고;
X7은 Glu (E) 또는 Asp (D)이고;
X8은 Arg (R) 또는 Ser (S)이고;
X9는 Tyr (Y) 또는 Arg (R)이고;
X10은 Leu (L) 또는 Val (V)이고;
X11은 Leu (L) 또는 Ala (A)이고;
X12는 음전하로 하전된 아미노산이고;
(Z)n은 아미노산이고 (여기서, n은 1 내지 5임);
X13은 음전하로 하전된 아미노산이고;
X14는 Ala (A) 또는 Leu (L)이고;
X15는 Glu (E) 또는 Lys (K)이고;
X16은 Asn (N), Glu (E) 또는 Lys (K)이고;
X17은 Ile (I) 또는 Ala (A)이고;
X18은 Thr (T), Glu (E) 또는 Gly (G)이고;
X19는 Thr (T), Asn (N) 또는 Ala (A)이고;
X20은 Gly (G) 또는 Ile (I)이고;
X21은 Cys (C) 또는 Thr (T)이고;
X22는 Ala (A) 또는 Thr (T)이고;
X23은 Glu (E) 또는 Gly (G)이고;
X24는 His (H) 또는 Cys (C)임)
특정 실시양태에서, 화학식 I의 단리된 펩티드 및 펩티드 유사체는 펩티드 D, 즉 APPRLICDSRVLERYLLEAKEAE (서열 14); 펩티드 A, 즉 NITVPDTKVNFYAWKRMEVG (서열 2); 펩티드 B, 즉 QQAVEVWQGLALLSEAVLRGQALLV (서열 3), 펩티드 C, 즉 GCAEHCSLNENITVPDTKVN (서열 4) 또는 펩티드 E, 즉 RYLLEAKEAENITTGC (서열 303)를 포함하지 않을 수 있다.
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 24개보다 적은 수의 아미노산 잔기를 함유할 수 있다. 실제로, 겨우 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11 또는 심지어 10개의 아미노산 잔기를 함유하는 화학식 I의 절단된 (truncated) 또는 내부 결실 형태는 화학식 I의 단리된 펩티드 및 펩티드 유사체의 전체 특징 및 조직 보호 특성을 실질적으로 보유한다.
본 발명의 특정 실시양태에서, 화학식 I의 단리된 펩티드 및 펩티드 유사체의 내부 잔기에서의 공간적으로 조밀한 전하 배열이 중요한 것으로 추측되기 때문에, 극성이고, 음성 및 양전하로 하전되고, 바로 인접한 아미노산들을 포함하는 잔기는 결실되지 않는다. 따라서, 특정 실시양태에서, 잔기 X11, X12, X13 및 X14는 결실되지 않는다.
화학식 I의 단리된 펩티드 및 펩티드 유사체는 또한, 실질적으로 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성에 실질적으로 지장을 주지 않는 (몇몇 실시양태에서는 심지어 이를 향상시키는) 부가적인 아미노산 잔기에 의해 한쪽 또는 양쪽 말단에서 또는 내부적으로 연장될 수 있다. 실제로, 무려 25, 26, 27, 28 또는 29개의 아미노산 잔기를 함유하는 연장된 중심 펩티드 및 펩티드 유사체는 본 발명의 범주 내에 있는 것으로 간주된다. 바람직하게는, 상기 연장된 펩티드는 화학식 I의 펩티드 유사체의 조직 보호 특성을 실질적으로 보유할 것이다.
화학식 I의 중심 펩티드 및 펩티드 유사체 내의 특정 아미노산 잔기들은 펩티드 및 펩티드 유사체의 활성에 유의하게 유해한 영향을 미치지 않는 (많은 경우에서는 심지어 이를 향상시키는) 다른 아미노산 잔기로 대체될 수 있다. 따라서, 화학식 I의 적어도 하나 내지 최대 8개의 아미노산 잔기가 또다른 아미노산 잔기로 보존적으로 치환된, 화학식 I의 단리된 펩티드 및 펩티드 유사체의 변경되거나 돌연변이된 형태도 본 발명에서 고려된다. 특정 실시양태에서, 7, 6, 5, 4, 3, 2 또는 1개의 아미노산이 보존적으로 치환된다.
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 다음과 같은 아미노산 서열로 이루어진다:
펩티드 F
CDSRVLERYLLEAKEAENITTGCAEH
(서열 16);
펩티드 G
PPRLICDSRVLERYLLEAKEAENITTGC
(서열 17); 및
펩티드 H
ADRELEKIGA
(서열 18).
(b) 구조적 모티프 B
이 구조적 모티프에서, 펩티드는 음성 아미노산 옆에 양성 아미노산을 가지며, 두 하전된 아미노산은 단일 소수성 아미노산들로 플랭킹된다. 구조적으로, 이는 다음과 같이 표시될 수 있다.
(b1) HNPH, 서열 19; 또는
(b2) HPNH, 서열 20
(여기서, P는 양전하로 하전된 아미노산, 예컨대 아르기닌, 라이신 또는 히스티딘을 나타내고, N은 음전하로 하전된 아미노산 글루타메이트 또는 아스파르테이트를 나타냄).
이러한 특정 모티프의 한 변형에서, 음성 및 양성 아미노산은, 예를 들어 다음과 같은 극성 아미노산으로 분리될 수 있다.
(b3) HNLPH, 서열 21;
(b4) HPLNH, 서열 22
(여기서, L은 극성 아미노산, 예컨대 세린, 트레오닌, 아스파라긴 또는 글루타민을 나타냄). 별법으로, 상기 구조적 모티프는 H1-N1-(L)n-P1-H2 (여기서, n은 0 내지 1임) (서열 23) 또는 H1-P1-(L)n-N1-H2 (여기서, n은 0 내지 1임) (서열 24)로 표시될 수 있다. 이러한 모티프의 한 예는 펩티드 C (GCAEHCSLNENITVPDTKVN, 서열 4)이다.
특정 실시양태에서, 이하의 화학식 II 내지 IV에서 개시하는 구조적 모티프 B의 특정 실시양태의 단리된 펩티드 및 펩티드 유사체는 펩티드 D, APPRLICDSRVLERYLLEAKEAE (서열 14); 펩티드 A, NITVPDTKVNFYAWKRMEVG (서열 2); 펩티드 B, QQAVEVWQGLALLSEAVLRGQALLV (서열 3), 펩티드 C, GCAEHCSLNENITVPDTKVN (서열 4) 또는 펩티드 E, RYLLEAKEAENITTGC (서열 303)를 포함하지 않을 수 있다.
구조적 모티프 B의 특정 실시양태에서, 조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 및 관리하는데 유용한 단리된 펩티드 및 펩티드 유사체 군은 하기 화학식 II (서열 25)를 갖는 10 내지 28개의 연속 아미노산 잔기를 포함할 수 있다:
(상기 식에서,
X1은 Ser (S)이고;
X2는 Arg (R)이고;
X3은 Val (V)이고;
X4는 Leu (L)이고;
X5는 Glu (E)이고;
X6은 Arg (R)이고;
X7은 Tyr (Y)이고;
X8은 Leu (L)이고;
X9는 Leu (L)이고;
X10은 Glu (E)이고;
X11은 Ala (A)이고;
X12는 양전하로 하전된 아미노산이고;
X13은 음전하로 하전된 아미노산이고;
X14는 Ala (A)이고;
X15는 Glu (E)이고;
X16은 Asn (N)이고;
X17은 Ile (I)이고;
X18은 Thr (T)이고;
X19는 Thr (T)이고;
X20은 Gly (G)이고;
X21은 Cys (C)이고;
X22는 Ala (A)이고;
X23은 Glu (E)이고;
X24는 His (H)임).
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 24개 미만의 아미노산 잔기를 함유할 수 있다. 실제로, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11개 또는 심지어 10개의 아미노산 잔기 만을 함유하는 화학식 II의 절단된 형태 또는 내부 결실된 형태는 화학식 II의 단리된 펩티드 및 펩티드 유사체의 전반적인 특징 및 조직 보호 특성을 실질적으로 보유한다.
화학식 II의 단리된 펩티드 및 펩티드 유사체의 내부 잔기에서의 공간적으로 조밀한 전하 배열에 대해 예상되는 중요성으로 인하여, 본 발명의 특정 실시양태에서 음전하 및 양전하로 하전된 아미노산 및 바로 인접한 아미노산을 포함하는 잔기는 결실되지 않는다. 즉, 특정 실시양태에서 잔기 X11, X12, X13, 및 X14는 결실되지 않는다.
화학식 II의 단리된 펩티드 및 펩티드 유사체는 또한, 실질적으로 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성에 지장을 주지 않는, 몇몇 실시양태에서는 심지어 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성을 향상시키는 부가적인 아미노산 잔기에 의해 한쪽 또는 양쪽 말단이, 또는 내부가 연장될 수 있다. 실제로, 무려 25, 26, 27, 28 또는 29개의 아미노산 잔기를 함유하는 연장된 중심 펩티드 및 펩티드 유사체는 본 발명의 범위 내에 속하는 것으로 본다. 바람직하게는, 그러한 연장된 펩티드는 화학식 II의 펩티드 유사체의 조직 보호 특성을 실질적으로 보유할 것이다.
화학식 II의 중심 펩티드 및 펩티드 유사체 내의 특정 아미노산 잔기는 펩티드 및 펩티드 유사체의 활성에 유의하게 유해한 영향을 미치지 않는, 많은 경우에서는 심지어 펩티드 및 펩티드 유사체의 활성을 향상시키는 다른 아미노산 잔기로 대체될 수 있다. 따라서, 본 발명에서 또한 고려되는 것은 화학식 내의 적어도 하나, 최대 8개의 아미노산 잔기가 또다른 아미노산 잔기로 보존적으로 치환된, 화학식 II의 단리된 펩티드 및 펩티드 유사체의 변경 또는 돌연변이된 형태이다. 특정 실시양태에서, 7, 6, 5, 4, 3, 2 또는 1개의 아미노산이 보존적으로 치환된다.
특정 실시양태에서, 단리된 펩티드 또는 펩티드 유사체는 다음과 같은 아미노산 서열로 이루어진다:
구조적 모티프 B의 추가의 실시양태에서, 조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 및 관리하는데 유용한 단리된 펩티드 및 펩티드 유사체 군은 하기 화학식 III (서열 27)을 갖는다:
(상기 식에서,
X1은 Pro (P), Lys (K), 또는 Ser (S)이고;
X2는 Pro (P), Glu (E), 또는 Gln (Q)이고;
X3은 Arg (R), Ala (A), 또는 Pro (P)이고;
X4는 Leu (L), Glu (E), 또는 Trp (W)이고;
X5는 Ile (I), Asn (N), 또는 Glu (E)이고;
X6은 Cys (C), Ile (I), 또는 Pro (P)이고;
X7은 Asp (D), Thr (T), Leu (L), 또는 Ala (A)이고;
X8은 Ser (S), Thr (T), Gln (Q), 또는 Asp (D)이고;
X9는 Arg (R), Gly (G), 또는 Leu (L)이고;
X10은 Val (V), Cys (C), His (H), 또는 Glu (E)이고;
X11은 Leu (L), Ala (A), Val (V)이고;
X12는 음전하로 하전된 아미노산이고;
X13은 양전하로 하전된 아미노산이고;
X14는 Tyr (Y), Cys (C), Ala (A), 또는 Ile (I)이고;
X15는 Leu (L), Ser (S), Val (V), 또는 Gly (G)이고;
X16은 Leu (L), Ser (S), 또는 Ala (A)이고;
X17은 Glu (E), Asn (N), 또는 Gly (G)이고;
X18은 Ala (A), Glu (E), 또는 Leu (L)이고;
X19는 Lys (K), Asn (N), 또는 Arg (R)이고;
X20은 Glu (E), Ile (I), 또는 Ser (S)이고;
X21은 Ala (A), Thr (T), 또는 Leu (L)이고;
X22는 Glu (E), Val (V), 또는 Thr (T)이고;
X23은 Asn (N), Pro (P), 또는 Thr (T)이고;
X24는 Ile (I), Asp (D), 또는 Leu (L)임).
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 24개 미만의 아미노산 잔기를 함유할 수 있다. 실제로, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11개 또는 심지어 10개의 아미노산 잔기 만을 함유하는 화학식 III의 절단된 형태 또는 내부 결실된 형태는 화학식 III의 단리된 펩티드 및 펩티드 유사체의 전반적인 특징 및 조직 보호 특성을 실질적으로 보유한다.
화학식 III의 단리된 펩티드 및 펩티드 유사체의 내부 잔기에서의 공간적으로 조밀한 전하 배열에 대해 예상되는 중요성으로 인하여, 본 발명의 특정 실시양태에서는 음전하 및 양전하로 하전된 아미노산 및 바로 인접한 아미노산을 포함하는 잔기는 결실되지 않는다. 즉, 특정 실시양태에서 잔기 X11, X12, X13, 및 X14는 결실되지 않는다.
화학식 III의 단리된 펩티드 및 펩티드 유사체는 또한, 실질적으로 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성에 지장을 주지 않는, 몇몇 실시양태에서는 심지어 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성을 향상시키는 부가적인 아미노산 잔기에 의해 한쪽 또는 양쪽 말단이, 또는 내부가 연장될 수 있다. 실제로, 무려 25, 26, 27, 28 또는 29개의 아미노산 잔기를 함유하는 연장된 중심 펩티드 및 펩티드 유사체는 본 발명의 범위 내에 속하는 것으로 본다. 바람직하게는, 그러한 연장된 펩티드는 화학식 III의 펩티드 유사체의 조직 보호 특성을 실질적으로 보유할 것이다.
화학식 III의 중심 펩티드 및 펩티드 유사체 내의 특정 아미노산 잔기는 펩티드 및 펩티드 유사체의 활성에 유의하게 유해한 영향을 미치지 않는, 많은 경우에서는 심지어 펩티드 및 펩티드 유사체의 활성을 향상시키는 다른 아미노산 잔기로 대체될 수 있다. 따라서, 본 발명에서 또한 고려되는 것은 화학식 내의 적어도 하나, 최대 8개의 아미노산 잔기가 또다른 아미노산 잔기로 보존적으로 치환된, 화학식 III의 단리된 펩티드 및 펩티드 유사체의 변경 또는 돌연변이된 형태이다. 특정 실시양태에서, 7, 6, 5, 4, 3, 2 또는 1개의 아미노산이 보존적으로 치환된다.
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 이하의 펩티드 세트군으로부터 선택된다:
구조적 모티프 B의 또다른 실시양태에서, 조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 및 관리하는데 유용한 단리된 펩티드 및 펩티드 유사체 군은 하기 화학식 IV (서열 31)를 갖는다:
(상기 식에서,
X1은 His (H)이고;
X2는 Cys (C)이고;
X3은 Ser (S)이고;
X4는 Leu (L)이고;
X5는 Ala (A) 또는 Asn (N)이고;
X6은 Pro (P) 또는 Glu (E)이고;
X7은 Pro (P) 또는 Asn (N)이고;
X8은 Arg (R) 또는 Ile (I)이고;
X9는 Leu (L) 또는 Thr (T)이고;
X10은 Ile (I) 또는 Val (V)이고;
X11은 Cys (C) 또는 Pro (P)이고;
X12는 음전하로 하전된 아미노산이고;
X13은 극성 아미노산이고;
X14는 양전하로 하전된 아미노산이고;
X15는 Val (V)이고;
X16은 Leu (L) 또는 Asn (N)이고;
X17은 Glu (E) 또는 Phe (F)이고;
X18은 Arg (R) 또는 Tyr (Y)이고;
X19는 Tyr (Y) 또는 Ala (A)이고;
X20은 Leu (L) 또는 Trp (W)이고;
X21은 Leu (L) 또는 Lys (K)이고;
X22는 Glu (E) 또는 Arg (R)이고;
X23은 Ala (A) 또는 Met (M)이고;
X24는 Lys (K) 또는 Glu (E)이고;
X25는 Glu (E) 또는 Val (V)임).
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 25개 미만의 아미노산 잔기를 함유할 수 있다. 실제로, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11개 또는 심지어 10개의 아미노산 잔기 만을 함유하는 화학식 IV의 절단된 형태 또는 내부 결실된 형태는 화학식 IV의 단리된 펩티드 및 펩티드 유사체의 전반적인 특징 및 조직 보호 특성을 실질적으로 보유한다.
화학식 IV의 단리된 펩티드 및 펩티드 유사체의 내부 잔기에서의 공간적으로 조밀한 전하 배열에 대해 예상되는 중요성으로 인하여, 본 발명의 특정 실시양태에서는 극성, 음전하 및 양전하로 하전된 아미노산 및 바로 인접한 아미노산을 포함하는 잔기는 결실되지 않는다. 즉, 특정 실시양태에서, 잔기 X11, X12, X13, X14, 및 X15는 결실되지 않는다.
화학식 IV의 단리된 펩티드 및 펩티드 유사체는 또한, 실질적으로 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성에 지장을 주지 않는, 몇몇 실시양태에서는 심지어 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성을 향상시키는 부가적인 아미노산 잔기에 의해 한쪽 또는 양쪽 말단이, 또는 내부가 연장될 수 있다. 실제로, 무려 26, 27, 28, 또는 29개의 아미노산 잔기를 함유하는 연장된 중심 펩티드 및 펩티드 유사체는 본 발명의 범위 내에 속하는 것으로 본다. 바람직하게는, 그러한 연장된 펩티드는 화학식 IV의 펩티드 유사체의 조직 보호 특성을 실질적으로 보유할 것이다.
화학식 IV의 중심 펩티드 및 펩티드 유사체 내의 특정 아미노산 잔기는 펩티드 및 펩티드 유사체의 활성에 유의하게 유해한 영향을 미치지 않는, 많은 경우에서는 심지어 펩티드 및 펩티드 유사체의 활성을 향상시키는 다른 아미노산 잔기로 대체될 수 있다. 따라서, 본 발명에서 또한 고려되는 것은 화학식 내의 적어도 하나, 최대 8개의 아미노산 잔기가 또다른 아미노산 잔기로 보존적으로 치환된, 화학식 IV의 단리된 펩티드 및 펩티드 유사체의 변경 또는 돌연변이된 형태이다. 특정 실시양태에서, 7, 6, 5, 4, 3, 2, 또는 1개의 아미노산이 보존적으로 치환된다.
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 이하의 펩티드 세트 군으로부터 선택된다:
당업자는 상기한 바와 같은 구조적 모티프 A 및 B가 본 발명에 있어서 중요하다는 것을 인식할 것이다. 따라서, 당업자는 단리된 펩티드가 서열 1에 나타낸 성숙한 인간 EPO의 아미노산 서열의 임의의 부분과 90% 미만, 85% 미만, 80% 미만, 75% 미만, 70% 미만, 65% 미만, 60% 미만, 55% 미만, 50% 미만, 45% 미만, 40% 미만, 35% 미만, 30% 미만, 또는 20% 미만의 서열 동일성을 가질 수 있음을 인식할 것이다 (이때 상기 EPO 부분은 상기 펩티드와 동일한 수의 아미노산 잔기를 함유함).
본 출원인들은 추가로, 구조적 모티프 A 및 B의 조직 보호 활성이 모티프에 의해 생성된 적절하고 공간적으로 조밀한 전하 배열로 인한 것임을 제안한다. 이러한 전하의 근접은 펩티드 결합에 의해 부여되는 선형 구조를 통해 발생할 수 있거나 (구조는 폴리펩티드 쇄 내의 연속 아미노산에 의해 형성될 수 있음), 또는 이와 달리, 근접은 또한 단백질의 2차 및/또는 3차 구조, 즉 3차원적 구조에 의해 부여되는 EPO 분자 (또는 그밖의 관련 유형 1 사이토킨 분자)의 서로 다른 부분들 사이의 공간적 관계를 통해 발생할 수 있다. 임의의 특정 이론에 구애됨이 없이, 본 출원인들은 일반적으로 이러한 요건이 조직 보호 펩티드가 하전된 아미노산 쌍 (즉, 두 개의 음전하로 하전된 아미노산 및/또는 양전하 및 음전하로 하전된 아미노산)에 요구되는 공간적 위치를 제공하는 분명한 3차 구조 (예를 들어, 헬릭스 또는 병풍 구조)를 갖게 하는데 영향을 준다고 생각한다. 단순한 예외는 아미노산 쌍이 펩티드 골격에 의해 부여된 필요한 강도를 가지면서 서로 바로 인접해 있는 선형 펩티드이다. 따라서, 구조적 모티프 A는 선형의 아미노산 잔기 서열, 예를 들면 H1-N1-N1-H2 (서열 6), 또는 N1 및 N2가 1, 2, 3, 4, 5, 6개 또는 이를 초과하는 개입 잔기에 의해 분리된, 예를 들면 H-N-X-X-X-X-X-N-H (서열 11)의 선형의 아미노산 잔기 서열을 포함한다.
임의의 특정 이론에 구애됨이 없이, 본 출원인들은 조직 보호를 위해서는, 카르바밀 탄소가 약 3 옹스트롬 (Å) 내지 약 5 Å 간격, 바람직하게는 약 4 Å 내지 약 5 Å 간격, 및 보다 바람직하게는 약 4.4 Å 내지 약 4.8 Å 간격으로 떨어지도록 펩티드 내의 하전된 아미노산 쌍이 공간적으로 배향되어야 한다고 생각한다. 이는 예를 들면, 단순한 선형 펩티드에서는 인접한 하전된 아미노산에 의해, 또는 알파 헬릭스를 형성할 수 있는 펩티드의 경우에는 개입 아미노산 잔기에 의해 분리된 하전된 아미노산에 의하는 다수의 방식으로 달성될 수 있다. 3차 구조 (예를 들어, 양친매성 펩티드 내의 알파 헬릭스)는 펩티드가 세포외-세포 표면 막 계면과 같은 특수한 미시환경에 놓였을때에도 부여될 수 있음을 주목한다 (본원에 그 전문이 참조로 포함되는 문헌 [Segrest, 1990, Proteins 8:103-117] 참조).
또한, 조직 보호 활성은 (양전하 및 음전하 또는 두 개의 음전하로) 하전된 측쇄가 서로 약 6.5 Å 내지 약 9 Å 내에 공간적으로 한정되어 있는, 하전된 아미노산의 쌍을 함유하는 펩티드에 대해서도 예상된다. 이는 알파 헬릭스의 경우에서는, 요구되는 만큼 약 6.5 Å 내지 약 9 Å으로 분리된 같은 쪽의 헬릭스에 보다 많거나 적은 전하를 제공할, 1개 또는 2개의 아미노산에 의해 분리된 하전된 쌍에 의해 제공될 수 있다. 당업자는 하전된 아미노산의 적절한 3차원적 위치를 획득하기 위해 일반적으로 요구되는 펩티드의 3차 구조를 고안할 수 있을 뿐 아니라, 펩티드 내에서 전하 분리를 가장하기 위한 소분자의 디자인도 고안할 수 있다.
임의의 두 개의 아미노산의 카르바밀 탄소 사이의 공간적 거리 또는 임의의 두 개의 아미노산의 측쇄 사이의 공간적 거리는 당업계에 공지되어 있거나 본원에서 기재하는 임의의 방법으로 추정할 수 있다. 예를 들면, 단백질의 3차원적 구조가 공지되어 있는 경우, 상기 단백질의 관심 부분 내의 두 개의 측쇄의 전하 분리 또는 두 개의 카르바밀 탄소 사이의 공간적 거리는, 공개되어 있거나 또는 그 밖에 당업계에서 허용되는, 상기 관심 부분 내의 아미노산 잔기의 3차원 좌표에 기초하여 계산할 수 있다. 단백질의 3차원 구조, 및 그에 따른 관심 부분이 공지되지 않은 경우, 또는 본원에서 교시하는 바에 기초하여 3차원 구조가 공지되지 않은 완전한 합성 펩티드가 구축된 경우, 상기 펩티드 내의 두 개의 측쇄의 전하 분리 또는 두 개의 카르바밀 탄소 사이의 공간적 거리는 당업계에 공지되어 있는 단백질 모델링 소프트웨어에 의해 예상되는 3차원 구조를 이용하여 예측할 수 있다. 그러한 소프트웨어의 비제한적인 예로 케미칼 컴퓨팅 그룹 (Chemical Computing Group; 캐나다 퀘백주 소재)의 MOETM 및 아셀리스 (Accelrys; 미국 캘리포니아주 샌 디에고 소재)의 모델러 (Modeler)가 있다. 유사하게, 소분자 디자인 업계에서 뿐만 아니라 당업자에게도 공지되어 있는 상기 언급한 회사로부터 이용가능한 그러한 예측 소프트웨어는, 본원에서 교시하는 바에 기초하여, 개시된 구조적 모티프를 모방한 소분자를 제조할 수 있을 것이다.
c. 구조적 모티프 C.
조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 및 관리하는데 유용한, 펩티드로 표현되는 본 발명의 또다른 구조적 모티프는
이며, 상기 식에서 X1은 하전된 아미노산 잔기이고, X6은 소수성 아미노산 잔기 또는 A이며, X2, X3, X4 및 X5는 임의의 아미노산 잔기이다.
상기 모티프의 X1 위치에서 하전된 잔기, 바람직하게는 음전하로 하전된 잔기가 존재하고, X6 위치에서 소수성 아미노산 잔기, 바람직하게는 Leu (L), Val (V) 또는 Tyr (Y)가 존재하는 것에 더하여, 상기 서열은 모티프의 i) X2 위치에 Ser (S) 및/또는 ii) X2 위치에 소수성 잔기 및/또는 X3 위치에 소수성 잔기를 추가로 포함할 수 있다. 그러한 바람직한 모티프의 예는 서열 (i) R-S-X3-X4-X5-L (서열 35), 및 (ii) R-V-X3-X4-X5-A (서열 36), R-V-L-X4-X5-Y (서열 37), K-A-V-X4-X5-L (서열 38), R-X2-L-X4-X5-L (서열 39), 또는 R-S-L-X4-X5-L (서열 40)일 수 있다. 또한, Ser (S) 또는 Thr (T)는 몇몇 경우에서, X2 위치 및/또는 X3 위치에 소수성 잔기가 존재하는 것과 독립적으로 X4에 위치하는 것이 바람직하다.
구조적 모티프 C를 나타내는, 조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 또는 관리하는데 유용한 펩티드 군은 아래와 같다:
d. 구조적 모티프 D.
조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 또는 관리하는데 유용한 펩티드에 대한 추가의 모티프는 다수의 신경친화성 및 조혈 사이토킨에서 발견되는 신경친화성 펩티드 컨센서스 서열을 기초로 하며, 이는 신경돌기의 성장을 자극하고 프로사포신의 활성을 가장할 것이다. 이러한 컨센서스 서열은 서열 45 (CEFLVKEVTKLIDNNKTEKEIL)의 아미노산 서열을 갖는 사포신 C 유래의 활성 22-량체 펩티드 및 서열 46 (YVKHQGLNKNINLDSVDGVP)의 아미노산 서열을 갖는 20-량체 CNTF 펩티드와, EPO와의 서열 유사성이 밝혀진 다양한 사이토킨 및 성장 인자를 비교한 것으로부터 유래된다.
컨센서스 서열은
이며, 상기 식에서 N은 Asp (N)이고, A는 Leu (L) 또는 Ile (I)이고, X는 독립적으로 임의의 아미노산이고, n은 2 내지 3이고, o는 0 내지 1이고, p는 1 내지 7이고, B는 하나 이상의 하전된 아미노산 (Asp (D), Lys (K), Glu (E), 또는 Arg (R))이고, q는 4 내지 7이고, C는 하나 이상의 소수성 아미노산 (Ala (A), Leu (L), Ile (I) 또는 Val (V))이며, 여기서 C는 제2 아스파라긴 잔기로부터의 6 내지 10 아미노산이다. 구조적 모티프 D를 나타내는 펩티드의 예는 EPO AB-루프로부터 유래된 펩티드 U: AEHCSLNENITVPDTKV (서열 48)이다. 구조적 모티프 D에 따른 추가의 서열은 LIRX1NNX2TX3X4X3X1X1이며, 상기 식에서 X1은 임의의 아미노산이고, X2는 Leu (L) 또는 Arg (R)이 아닌 임의의 아미노산이며, X3은 하전된 아미노산이고, X4가 존재하는 경우 이는 하전된 아미노산이다.
e. 구조적 모티프 E.
또한, X3-X4-X5-G-P-X6-T-W-X7-X8 (서열 49)의 중심 아미노산 서열을 포함하는 펩티드가 본 발명에 따라 조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 또는 관리하는데 유용하며, 상기 식에서 X3은 Cys (C), Glu (E), Ala (A), α-아미노-γ-브로모부티르산, 또는 Hoc (여기서, Hoc은 호모시스테인임)일 수 있고; X4는 Arg (R), His (H), Tyr (Y), Leu (L), 또는 Trp (W)일 수 있거나, 또는 X4는 결합이며; X5는 Met (M), Phe (F), 또는 Ile (I)일 수 있고; X6은 독립적으로 20개의 유전적으로 코딩된 L-아미노산 또는 입체이성질체 D-아미노산 중 어느 하나이고; X7은 Asp (D), Glu (E), Ile(I), Leu (L), 또는 Val (V)일 수 있고; X8은 Cys (C), Lys (K), Ala (A), α-아미노-γ-브로모부티르산, 또는 Hoc (여기서, Hoc은 호모시스테인임)일 수 있으며, 단 X3 또는 X8은 Cys (C) 또는 Hoc이다. 이량체 또는 다량체의 단량체 펩티드 단위가 중심 서열 YX2X3X4X5GPX6TWX7X8 (서열 50)을 포함하는 모티프 변형물을 개시하며, 상기 식에서 X2 및 X6은 독립적으로 20개의 유전적으로 코딩된 L-아미노산으로부터 선택되고; X3은 Cys (C), Glu (E), Ala (A), α-아미노-γ-브로모부티르산, 또는 Hoc (여기서, Hoc은 호모시스테인임)일 수 있고; X4는 Arg (R), His (H), Tyr (Y), Leu (L), 또는 Trp (W)일 수 있거나, 또는 X4는 결합이며; X5는 Met (M), Phe (F), 또는 Ile (I)일 수 있고; X7은 Asp (D), Glu (E), Ile (I), Leu (L), 또는 Val (V)일 수 있고; X8은 Cys (C), Lys (K), Ala (A), α-아미노-γ-브로모부티르산, 또는 Hoc (여기서, Hoc은 호모시스테인임)일 수 있다. 보다 바람직하게는, X3 또는 X8은 Cys (C) 또는 Hoc이다. 추가로, 이량체 또는 다량체의 단량체 펩티드 단위가 아미노산 YX2X3X4X5GPX6TWX7X8 (서열 51)의 중심 서열을 포함하는 모티프 변형물을 개시하며, 상기 식에서 각각의 X2 및 X6은 독립적으로 20개의 유전적으로 코딩된 L-아미노산 중 어느 하나이고; X3은 Cys (C)이고; X8은 Cys (C)이다. 이량체의 단량체 펩티드 단위가 아미노산 X1YX2X3X4X5GPX6TWX7X8X9X10X11 (서열 52)의 중심 서열을 포함하는 또다른 모티프 변형물을 개시하며, 상기 식에서 각각의 X1, X2, X6, X9, X10, 및 X11은 독립적으로 20개의 유전적으로 코딩된 L-아미노산으로부터 선택된다. 특히, X3은 Cys (C), Glu (E), Ala (A)일 수 있으며; X4는 Arg (R), His (H), 또는 Tyr (Y)일 수 있거나, 또는 X4는 결합이며; X5는 Met (M), Phe (F), 또는 Ile (I)일 수 있고; X7은 Asp (D) 또는 Val (V)일 수 있고; X8은 Cys (C), Lys (K), 또는 Ala (A)일 수 있다. 모티프의 또다른 변형물에서, X3 및 X8은 둘 모두 Cys (C)이며, 따라서 이량체의 단량체 펩티드 단위는 아미노산 X1YX2CX4X5GPX6TWX7CX9X10X11 (서열 53)의 중심 서열을 포함한다. 모티프는 또한 아미노산 X1YX2CX4X5GPX6TWX7CX9X10X11 (서열 54)의 중심 서열일 수 있으며, 상기 식에서 X4는 Arg (R) 또는 His (H)일 수 있고; X5는 Phe (F) 또는 Met (M)일 수 있고; X6은 Ile (I), Leu (L), Thr (T), Met (M), 또는 Val (V)일 수 있고; X7은 Asp (D) 또는 Val (V)이고; X9는 Gly (G), Lys (K), Leu (L), Gln (Q), Arg (R), Ser (S), 또는 Thr (T)일 수 있고; X10은 Ala (A), Gly (G),Pro (P), Arg (R), 또는 Tyr (Y)일 수 있다. 또는, 모티프는 아미노산 X1YX2CX4X5GPX6TWX7CX9X10X11 (서열 55)의 중심 서열을 포함할 수 있으며, 상기 식에서 X1은 Asp (D), Glu (E), Leu (L), Asn (N), Ser (S), Thr (T), 또는 Val (V)일 수 있고; X2는 Ala (A), His (H), Lys (K), Leu (L), Met (M), Ser (S), 또는 Thr (T)일 수 있고; X4는 Arg (R) 또는 His (H)이고; X9는 Lys (K), Arg (R), Ser (S), 또는 Thr (T)일 수 있고; X10은 Pro (P)이다. 이와 달리, 모티프는 아미노산 X1YX2CX4X5GPX6TWX7CX9X10X11 (서열 56)의 중심 서열을 포함할 것이며, 상기 식에서 X1은 Asp (D), Glu (E), Leu (L), Asn (N), Ser (S), Thr (T), 또는 Val (V)일 수 있고; X2는 Ala (A), His (H), Lys (K), Leu (L), Met (M), Ser (S), 또는 Thr (T)일 수 있고; X4는 Arg (R) 또는 His (H)이고; X9는 Lys (K), Arg (R), Ser (S), 또는 Thr (T)일 수 있고; X10은 Pro (P)이다.
조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 및 관리하는데 유용한 구조적 모티프 E에 따른 특정 펩티드는 아래와 같다:
f. 구조적 모티프 F.
추가로, EPO의 AB 루프 유래의 펩티드도 역시 고려된다. 이 AB 루프 펩티드는 펩티드의 아미노산 서열의 N-말단의 끝 또는 C-말단의 끝 중 적어도 하나에 작은 비시클릭 분자를 화학적으로 첨가하는 것에 의해 추가로 안정화될 수 있다.
조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 및 관리하는데 유용한 구조적 모티프 F에 따른 특정 펩티드는 아래와 같다:
게다가, 펩티드는 펩티드 서열에 따라서 제1 아미노산 잔기의 술프히드랄 기 및 제2 아미노산 잔기의 술프히드랄 기 사이에 형성된 디술파이드 결합에 의해 안정화될 수 있다. 특정 실시양태의 펩티드는 펩티드 서열 XAEHYS (서열 101)를 갖는 적어도 6개의 아미노산을 가지며, 상기 식에서 X는 술프히드랄 기를 함유하는 제1 아미노산 잔기이고, Y는 술프히드랄 기를 함유하는 제2 아미노산 잔기이며, 여기서 제1 아미노산 잔기의 술프히드랄 기는 제2 아미노산 잔기의 술프히드랄 기로부터 적절한 거리에 위치하여 펩티드 서열 내에서 제2 아미노산 잔기의 술프히드랄 기와 디술파이드 결합을 형성하고, 이로서 펩티드 (화학식 I)를 안정화시킨다.
조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 및 관리하는데 유용한 구조적 모티프 F에 따른 특정 펩티드, 화학식 I은 아래와 같다:
또다른 실시양태에서, 디술파이드 결합으로 안정화된 단리된 EPO-유래의 펩티드는 추가로, 펩티드의 아미노산 서열의 N-말단의 끝 또는 C-말단의 끝 중 적어도 하나에 작은 비시클릭 분자를 화학적으로 첨가하는 것에 의해 안정화된다.
펩티드는 또한, 다음과 같은 펩티드 서열 XAEHYS (서열 111)를 갖는 적어도 7개의 아미노산의 모티프를 나타낼 수 있으며, 상기 식에서 X는 술프히드랄 기를 함유하는 제1 아미노산 잔기이고, Y는 술프히드랄 기를 함유하는 제2 아미노산 잔기이며, 여기서 제1 아미노산 잔기의 술프히드랄 기는 제2 아미노산 잔기의 술프히드랄 기로부터 적절한 거리에 위치하여 펩티드 서열 내에서 제2 아미노산 잔기의 술프히드랄 기와 디술파이드 결합을 형성하고, 이로서 펩티드 (화학식 II)를 안정화시킨다.
조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 또는 관리하는데 유용한 구조적 모티프 F에 따른 특정 펩티드, 화학식 II는 아래와 같다:
G. 다른 EPO 유래의 EPO 펩티드.
상기한 EPO 펩티드 및 EPO 유래의 모티프에 더하여, 미국 특허 제5,106,954호, 동 제5,952,293호, 동 제6,004,758호, 동 제6,346,390호, 동 제6,932,968호, 동 제5,835,382호, 동 제7,037,902호, 동 제7,084,245호, 및 동 제7,272,508호; 미국 특허 출원 제20050191301호; WO2005/021579; 문헌 [Skelton et al. "Amino Acid Determinants of Beta-hairpin Confirmation in Erythropoietin Receptor Agonist Peptides Derived From A Phage Display Library," Journal of Molecular Biology Vol. 316, Issue 8, 2002, pages 1111-1125]; [Livnah et al., Functional Mimcry of a Protein Hormone by a Peptides Agonist: the EPO Receptor Complex at 2Å, Science 26, July 1996 vol. 273, no. 5274, pp. 464-471]; [Johnson and Joliffe, "Erythropoietin Mimetic Peptides and the Future," Nephrol. Dial. Transplant (2000) 15:1274-1277], [Wrighton et al. (1996) Science 273: 458-463]; [Johnson et al. (1998) Biochemistry, 37: 3699-3710]에 개시되어 있는 EPO 펩티드, 단편 또는 모방체도 또한 본 발명의 질환 또는 장애에 대한 신체 반응의 효과를 조정하는 방법에 유용할 수 있다.
6.2 유형 1
사이토킨
단편.
상기의 모티프는 EPO 유래의 펩티드 또는 EPO 효능제 단편 뿐만 아니라, 역시 조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 억제 또는 지연시킬 수 있는 능력을 나타내어, 조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 또는 유지시키는데 있어서 치료상 유효한 유형-1 사이토킨 단편을 확인하는데 유용하다. 유형-1 사이토킨 패밀리에는, 이들로 한정되지는 않지만, 인터류킨 (IL)-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-9, IL-10, 또는 IL-11, 과립구 대식세포-콜로니 자극 인자 (GM-CSF), 렙틴, 과립구 콜로니 자극 인자 (G-CSF), 백혈병 억제 인자 (LIF), 섬모 신경친화성 인자 (CNTF), 트롬보포이에틴 (TPO), 성장 호르몬, 대식세포 콜로니 자극 인자 (M-CSF), 에리트로포이에틴 (EPO) 및 프로락틴이 포함된다.
EPO의 2차 구조를 고려하는 것은 다른 유형-1 사이토킨 수용체 리간드, 예를 들어 다른 것들 중에서도 강력한 신경친화성 및 신경보호 활성을 보유하는 것으로 보이는 (본 출원인들은 이것이 주로 조직 보호 수용체를 자극하는 것에 의한 것이라 생각함) GM-CSF 및 IL-3 (문헌 [Kannan, 2000, Neuroimmunomod. 8:132-141], 본원에 그 전문이 참조로 포함됨) 내에서 동종의 2차 구조 내에 위치하는 동종의 아미노산 유래의 아미노산의 공간적 배열을 통한 후보 펩티드의 제조 지침을 제공한다. 예를 들면, 이들 유형 I 사이토킨의 헬릭스 B를 고려할 경우, 트롬보포이에틴 (TPO; 단백질 데이터 뱅크 (PDB) 등록번호 1V7M) 내의 동종 아미노산은 D62, G65, T68, L69, E72, A76 및 Q80을 포함하고, 여기서 이들 아미노산은 선형의 배열에서 서로 공간적으로 인접하며, 백혈병 억제 인자 (LIF; PDB 등록번호 1EMR) 내의 동종 아미노산은 E61, R64, Y68, S72, N75, 및 D79를 포함하고, 섬모 신경친화성 인자 (CNTF; PDB 등록번호 1CNT) 내의 동종 아미노산은 E71, E75를 포함한다. 이들은 모두 상기한 구조적 모티프 A의 예이며, 이 중 밑줄친 아미노산은 음전하로 하전된 것이다.
이하에서 화학식 V 내지 VI로 개시하는 구조적 모티프 A의 특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 펩티드 BV, WEHVNAIQEARRLL (서열 114); 펩티드 BW, LSKLLRDSHVLH (서열 115); 펩티드 BX, KIRSDLTALTESYVKH (서열 116), 펩티드 BY, GTEKAKLVELYRIVVYL (서열 117) 또는 펩티드 BZ, SIMIDEIIHHLKRPPNPL (서열 118)을 포함하지 않을 수 있다.
구조적 모티프 A의 한 실시양태에서, 유형-1 사이토킨 유래 펩티드 및 펩티드 유사체는 하기 화학식 (V) (서열 119)를 갖는다:
(상기 식에서,
X1은 Trp (W), Val (V), Ala (A), Ile (I), Pro (P), Leu (L), Ser (S), Asp (D), 또는 Thr (T)이고;
X2는 임의의 아미노산이고;
X3은 임의의 아미노산이고;
X4는 임의의 아미노산이고;
X5는 임의의 아미노산이고;
X6은 임의의 아미노산이고;
X7은 임의의 아미노산이고;
X8은 Ile (I), Phe (F), Leu (L), Val (V), Pro (P), Tyr (Y), 또는 Gly (G)이고;
X9는 음전하로 하전된 아미노산이고;
X10은 음전하로 하전된 아미노산이고;
X11은 Ile (I), Leu (L), Ala (A), Gly (G), Phe (F), Val (V), 또는 Pro (P)이고;
X12는 Ile (I), Met (M), Tyr (Y), Ser (S), Val (V), Phe (F), Lys (K), Leu (L), Glu (E), 또는 Asp (D)이고;
X13은 임의의 아미노산이고;
X14는 His (H), Leu (L), Pro (P), Thr (T), Arg (R), Cys (C), Ile (I), Tyr (Y), Gln (Q), 또는 Ala (A)이고;
X15는 Leu (L), Lys (K), Thr (T), Val (V), Phe (F), Ala (A), 또는 Gln (Q)이고;
X16은 Lys (K), Glu (E), Met (M), Gly (G), Asn (N), Gln (Q), Thr (T), 또는 Val (V)이고;
X17은 임의의 아미노산이고;
X18은 Pro (P), Lys (K), Arg (R), Ile (I), Asn (N), Ser (S), Gln (Q), 또는 Phe (F)이고;
X19는 Pro (P), Ile (I), Tyr (Y), Leu (L), Phe (F), Ser (S), Ala (A), Asp (D), Asn (N), 또는 Lys (K)임).
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 19개 미만의 아미노산 잔기를 함유할 수 있다. 실제로, 18, 17, 16, 15, 14, 13, 12, 11개 또는 심지어 10개의 아미노산 잔기 만을 함유하는 화학식 V의 절단된 형태 또는 내부 결실된 형태는 화학식 V의 단리된 펩티드 및 펩티드 유사체의 전반적인 특징 및 조직 보호 특성을 실질적으로 보유한다.
조직 보호 활성에 있어서 화학식 V의 단리된 펩티드 및 펩티드 유사체의 내부 잔기에서의 공간적으로 조밀한 전하 배열에 대해 예상되는 중요성으로 인하여, 본 발명의 특정 실시양태에서는 극성, 음전하 및 양전하로 하전된 아미노산 및 바로 인접한 아미노산을 포함하는 잔기는 결실되지 않는다. 즉, 특정 실시양태에서, 잔기 X8, X9, X10, 및 X11은 결실되지 않는다.
화학식 V의 단리된 펩티드 및 펩티드 유사체는 또한, 실질적으로 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성에 지장을 주지 않는, 몇몇 실시양태에서는 심지어 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성을 향상시키는 부가적인 아미노산 잔기에 의해 한쪽 또는 양쪽 말단이, 또는 내부가 연장될 수 있다. 실제로, 무려 20, 21, 22, 23, 24, 25, 26, 27, 28, 또는 29개의 아미노산 잔기를 함유하는 연장된 중심 펩티드 및 펩티드 유사체는 본 발명의 범위 내에 속하는 것으로 본다. 바람직하게는, 그러한 연장된 펩티드는 화학식 V의 펩티드 유사체의 조직 보호 특성을 실질적으로 보유할 것이다.
화학식 V의 중심 펩티드 및 펩티드 유사체 내의 특정 아미노산 잔기는 펩티드 및 펩티드 유사체의 활성에 유의하게 유해한 영향을 미치지 않는, 많은 경우에서는 심지어 펩티드 및 펩티드 유사체의 활성을 향상시키는 다른 아미노산 잔기로 대체될 수 있다. 따라서, 본 발명에서 또한 고려되는 것은 화학식 내의 적어도 하나, 최대 8개의 아미노산 잔기가 또다른 아미노산 잔기로 보존적으로 치환된, 화학식 V의 단리된 펩티드 및 펩티드 유사체의 변경 또는 돌연변이된 형태이다. 특정 실시양태에서, 7, 6, 5, 4, 3, 2, 또는 1개의 아미노산이 보존적으로 치환된다.
특정 실시양태에서, 화학식 V의 단리된 펩티드 및 펩티드 유사체는 이하의 펩티드 세트 군으로부터 선택된다:
구조적 모티프 A의 또다른 실시양태에서, 유형-1 사이토킨에 기초하고 본 발명의 방법에 유용한 단리된 펩티드 및 펩티드 유사체는 하기 화학식 VI (서열 137)을 갖는다:
(상기 식에서,
X1은 Phe (F), Val (V), Ala (A), Gly (G), Pro (P), Leu (L), Tyr (Y), Ile (I), Cys (C) 또는 Met (M)이고;
X2는 음전하로 하전된 아미노산이고;
(Z)n은 아미노산이며, 여기서 n은 1 내지 5이고;
X3은 음전하로 하전된 아미노산이고;
X4는 Pro (P), Met (M), Val (V), Ile (I), Phe (F), Gly (G), Leu (L), Ala (A), Tyr (Y), 및 Trp (W)임).
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 9개 미만의 아미노산 잔기를 함유할 수 있다. 실제로, 8, 7, 6개 또는 심지어 5개의 아미노산 잔기 만을 함유하는 화학식 VI의 절단된 형태 또는 내부 결실된 형태는 화학식 VI의 단리된 펩티드 및 펩티드 유사체의 전반적인 특징 및 조직 보호 특성을 실질적으로 보유한다.
화학식 VI의 단리된 펩티드 및 펩티드 유사체의 내부 잔기에서의 공간적으로 조밀한 전하 배열에 대해 예상되는 중요성으로 인하여, 본 발명의 특정 실시양태에서는 음전하 및 양전하로 하전된 아미노산 및 바로 인접한 아미노산을 포함하는 잔기는 결실되지 않는다. 즉, 특정 실시양태에서 잔기 X1, X2, X3, 및 X4는 결실되지 않는다.
화학식 VI의 단리된 펩티드 및 펩티드 유사체는 또한, 실질적으로 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성에 지장을 주지 않는, 몇몇 실시양태에서는 심지어 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성을 향상시키는 부가적인 아미노산 잔기에 의해 한쪽 또는 양쪽 말단이, 또는 내부가 연장될 수 있다. 실제로, 무려 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 또는 29개의 아미노산 잔기를 함유하는 연장된 중심 펩티드 및 펩티드 유사체는 본 발명의 범위 내에 속하는 것으로 본다. 바람직하게는, 그러한 연장된 펩티드는 화학식 VI의 펩티드 유사체의 조직 보호 특성을 실질적으로 보유할 것이다.
화학식 VI의 중심 펩티드 및 펩티드 유사체 내의 특정 아미노산 잔기는 펩티드 및 펩티드 유사체의 활성에 유의하게 유해한 영향을 미치지 않는, 많은 경우에서는 심지어 펩티드 및 펩티드 유사체의 활성을 향상시키는 다른 아미노산 잔기로 대체될 수 있다. 따라서, 본 발명에서 또한 고려되는 것은 화학식 내의 적어도 하나, 최대 5개의 아미노산 잔기가 또다른 아미노산 잔기로 보존적으로 치환된, 화학식 VI의 단리된 펩티드 및 펩티드 유사체의 변경 또는 돌연변이된 형태이다. 특정 실시양태에서, 4, 3, 2 또는 1개의 아미노산이 보존적으로 치환된다.
특정 실시양태에서, 화학식 VI의 단리된 펩티드 및 펩티드 유사체는 이하의 펩티드 세트 군으로부터 선택된다:
상기한 구조적 모티프 B를 그 예로 하고 PCT/US2006/031061에 개시되어 있는, 유형-1 사이토킨 유래의 본 발명의 치료 방법에서 유용한 조직 보호 펩티드의 추가의 예에는, 이들로 한정되지는 않지만, GM-CSF 헬릭스 A 단편, 펩티드 BV: WEHVNAIQEARRLL (서열 114); TPO 헬릭스 A 단편, 펩티드 BW: LSKLLRDSHVLH (서열 115); TPO 헬릭스 B 단편: E56, K59; CNTF 헬릭스 A 단편, 펩티드 BX: KIRSDLTALTESYVKH (서열 116); CNTF 헬릭스 B 단편: R89, E92; LIF 헬릭스 B 단편, 펩티드 BY: GTEKAKLVELYRIVVYL (서열 117); 및 인터류킨 3 (IL-3) 헬릭스 A 단편, 펩티드 BZ: SIMIDEIIHHLKRPPNPL (서열 118)이 포함된다.
이하에서 화학식 VII 내지 X로 개시하는 구조적 모티프 B의 특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 펩티드 BV, WEHVNAIQEARRLL (서열 114); 펩티드 BW, LSKLLRDSHVLH (서열 115); 펩티드 BX, KIRSDLTALTESYVKH (서열 116), 펩티드 BY, GTEKAKLVELYRIVVYL (서열 117) 또는 펩티드 BZ, SIMIDEIIHHLKRPPNPL (서열 118)을 포함하지 않을 수 있다.
조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 및 관리하는 본 발명의 방법에서 유용한, 구조적 모티프 B를 나타내는 추가의 유형-1 사이토킨 유래의 펩티드는 하기 화학식 VII (서열 184)로 표현되는 것들이다:
(상기 식에서,
X1은 Leu (L), Ile (I), Gly (G), Val (V), Phe (F), Pro (P), 또는 Ala (A)이고;
X2는 양전하로 하전된 아미노산이고;
X3은 음전하로 하전된 아미노산이고;
X4는 Phe (F), Gly (G), Val (V), Leu (L), Ala (A), 또는 Tyr (Y)임).
본 발명의 한 실시양태에서, 유형-I 사이토킨 유래의 펩티드는 하기 화학식 VII(a)를 갖는다:
(서열 302):
(상기 식에서,
X1은 Leu (L), Ile (I), Gly (G), Val (V), Phe (F), Pro (P), 또는 Ala (A)이고;
X2는 양전하로 하전된 아미노산이고;
X3은 음전하로 하전된 아미노산이고;
X4는 Phe (F), Gly (G), Val (V), Leu (L), Ala (A), 또는 Tyr (Y)이고;
X5는 Arg (R), Asp (D), Glu (E), Asn (N), Ser (S), Thr (T), Phe (F), Val (V), 또는 Tyr (Y)이고;
X6은 His (H), Lys (K), Asp (D), Glu (E), Gln (Q), Asn (N), Ser (S), Leu (L), Trp (W), 또는 Phe (F)임).
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 5개 미만 또는 심지어 4개의 아미노산 잔기를 함유할 수 있다. 실제로, 6개 또는 심지어 5개의 아미노산 잔기 만을 함유하는 화학식 VII 또는 VIIa의 절단된 형태 또는 내부 결실된 형태는 단리된 펩티드 및 펩티드 유사체의 전반적인 특징 및 조직 보호 특성을 실질적으로 보유한다.
화학식 VII 또는 VIIa의 단리된 펩티드 및 펩티드 유사체의 내부 잔기에서의 공간적으로 조밀한 전하 배열에 대해 예상되는 중요성으로 인하여, 본 발명의 특정 실시양태에서는 음전하 및 양전하로 하전된 아미노산 및 바로 인접한 아미노산을 포함하는 잔기는 결실되지 않는다. 즉, 특정 실시양태에서 잔기 X1, X2, X3, 및 X4는 결실되지 않는다.
화학식 VII 및 화학식 IIa의 단리된 펩티드 및 펩티드 유사체는 또한, 실질적으로 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성에 지장을 주지 않는, 몇몇 실시양태에서는 심지어 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성을 향상시키는 부가적인 아미노산 잔기에 의해 한쪽 또는 양쪽 말단이, 또는 내부가 연장될 수 있다. 실제로, 무려 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 또는 29개의 아미노산 잔기를 함유하는 연장된 중심 펩티드 및 펩티드 유사체는 본 발명의 범위 내에 속하는 것으로 본다. 바람직하게는, 그러한 연장된 펩티드는 화학식 VII 또는 화학식 IIa의 펩티드 유사체의 조직 보호 특성을 실질적으로 보유할 것이다.
화학식 VII 또는 화학식 IIa의 중심 펩티드 및 펩티드 유사체 내의 특정 아미노산 잔기는 펩티드 및 펩티드 유사체의 활성에 유의하게 유해한 영향을 미치지 않는, 많은 경우에서는 심지어 펩티드 및 펩티드 유사체의 활성을 향상시키는 다른 아미노산 잔기로 대체될 수 있다. 따라서, 본 발명에서 또한 고려되는 것은 화학식 내의 적어도 하나, 최대 2개의 아미노산 잔기가 또다른 아미노산 잔기로 보존적으로 치환된, 단리된 펩티드 및 펩티드 유사체의 변경 또는 돌연변이된 형태이다.
특정 실시양태에서, 화학식 VII 또는 화학식 IIa의 단리된 펩티드 및 펩티드 유사체는 이하의 펩티드 세트 군으로부터 선택된다:
조직 손상 또는 손상들과 관련된 질환 또는 장애, 그로부터 생성된 영향 또는 증상을 예방, 치료, 개선 또는 관리하는데 유용한 펩티드의 또다른 실시양태에서, 유형-1 사이토킨에서 유래하고 구조적 모티프 B를 나타내는 단리된 펩티드 또는 펩티드 유사체는 하기 화학식 (VIII) (서열 209)을 갖는다:
(상기 식에서,
X1은 Ala (A), Thr (T), Ser (S), Tyr (Y), Leu (L), Val (V), Ile (I), Phe (F), 또는 Glu (E)이고;
X2는 임의의 아미노산이고;
X3은 Ser (S), Gln (Q), Asp (D), Leu (L), Glu (E), Cys (C), Asn (N), Arg (R), 또는 Ala (A)이고;
X4는 Pro (P), Gly (G), Gln (Q), Leu (L), Thr (T), Asn (N), Ser (S), Phe (F), 또는 Ile (I)이고;
X5는 임의의 아미노산이고;
X6은 Pro (P), Ser (S), Cys (C), Val (V), Lys (K), Thr (T), Leu (L), Ile (I), 또는 Gln (Q)이고;
X7은 임의의 아미노산이고;
X8은 Thr (T), Pro (P), Leu (L), Arg (R), Gly (G), Tyr (Y), Gln (Q), Glu (E), Ile (I) 또는 Ala (A)이고;
X9는 임의의 아미노산이고;
X10은 Pro (P), Asn (N), Glu (E), Asp (D), Thr (T), Leu (L), Ile (I), Gln (Q), Phe (F), 또는 Trp (W)이고;
X11은 Trp (W), Leu (L), Ala (A), Met (M), Val (V), Ile (I), Phe (F), 또는 Tyr (Y)이고;
X12는 음전하로 하전된 아미노산이고;
X13은 양전하로 하전된 아미노산이고;
X14는 Val (V), Leu (L), 또는 Ala (A)이고;
X15는 임의의 아미노산이고;
X16은 임의의 아미노산이고;
X17은 임의의 아미노산이고;
X18은 임의의 아미노산이고;
X19는 임의의 아미노산이고;
X20은 임의의 아미노산이고;
X21은 Arg (R), Asp (D), Tyr (Y), Val (V), Ile (I), Leu (L), Lys (K), Ser (S), 또는 Thr (T)이고;
X22는 임의의 아미노산이고;
X23은 임의의 아미노산이고;
X24는 Leu (L), Pro (P), Phe (F), Arg (R), Tyr (Y), Cys (C), Gly (G), Val (V), 또는 Lys (K)임).
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 24개 미만의 아미노산 잔기를 함유할 수 있다. 실제로, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11개 또는 심지어 10개의 아미노산 잔기 만을 함유하는 화학식 VIII의 절단된 형태 또는 내부 결실된 형태는 화학식 VIII의 단리된 펩티드 및 펩티드 유사체의 전반적인 특징 및 조직 보호 특성을 실질적으로 보유한다.
조직 보호 활성에 있어서 화학식 VIII의 단리된 펩티드 및 펩티드 유사체의 내부 잔기에서의 공간적으로 조밀한 전하 배열에 대해 예상되는 중요성으로 인하여, 본 발명의 특정 실시양태에서는 음전하 및 양전하로 하전된 아미노산 및 바로 인접한 아미노산을 포함하는 잔기는 결실되지 않는다. 즉, 특정 실시양태에서 잔기 X11, X12, X13, 및 X14는 결실되지 않는다.
화학식 VIII의 단리된 펩티드 및 펩티드 유사체는 또한, 실질적으로 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성에 지장을 주지 않는, 몇몇 실시양태에서는 심지어 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성을 향상시키는 부가적인 아미노산 잔기에 의해 한쪽 또는 양쪽 말단이, 또는 내부가 연장될 수 있다. 실제로, 무려 25, 26, 27, 28, 또는 29개의 아미노산 잔기를 함유하는 연장된 중심 펩티드 및 펩티드 유사체는 본 발명의 범위 내에 속하는 것으로 본다. 바람직하게는, 그러한 연장된 펩티드는 화학식 VIII의 펩티드 유사체의 조직 보호 특성을 실질적으로 보유할 것이다.
화학식 VIII의 중심 펩티드 및 펩티드 유사체 내의 특정 아미노산 잔기는 펩티드 및 펩티드 유사체의 활성에 유의하게 유해한 영향을 미치지 않는, 많은 경우에서는 심지어 펩티드 및 펩티드 유사체의 활성을 향상시키는 다른 아미노산 잔기로 대체될 수 있다. 따라서, 본 발명에서 또한 고려되는 것은 화학식 내의 적어도 하나, 최대 8개의 아미노산 잔기가 또다른 아미노산 잔기로 보존적으로 치환된, 화학식 VIII의 단리된 펩티드 및 펩티드 유사체의 변경 또는 돌연변이된 형태이다. 특정 실시양태에서, 7, 6, 5, 4, 3, 2 또는 1개의 아미노산이 보존적으로 치환된다.
특정 실시양태에서, 화학식 VIII의 단리된 펩티드 및 펩티드 유사체는 이하의 펩티드 세트 군으로부터 선택된다:
본 발명의 또다른 실시양태에서, 구조적 모티프 B를 나타내는 유형-1 사이토킨에 기초한 단리된 펩티드 및 펩티드 유사체는 하기 화학식 IX (서열 228)를 갖는다:
(상기 식에서,
X1은 Cys (C), Tyr (Y), 또는 Ala (A)이고;
X2는 Ser (S), Leu (L), 또는 Glu (E)이고;
X3은 Arg (R), Gln (Q), 또는 Asn (N)이고;
X4는 Ser (S) 또는 Leu (L)이고;
X5는 Ile (I), Leu (L), 또는 Lys (K)이고;
X6은 Trp (W), Leu (L), 또는 Lys (K)이고;
X7은 Leu (L), Phe (F), 또는 Tyr (Y)이고;
X8은 Ala (A), Asn (N), 또는 Phe (F)이고;
X9는 Arg (R), Pro (P), 또는 Asn (N)이고;
X10은 Lys (K), Leu (L), 또는 Ala (A)이고;
X11은 Ile (I), Val (V), 또는 Gly (G)이고;
X12는 양전하로 하전된 아미노산이고;
X13은 극성 아미노산이고;
X14는 음전하로 하전된 아미노산이고;
X15는 Leu (L), Gly (G), 또는 Val (V)이고;
X16은 Thr (T), Ile (I), 또는 Ala (A)이고;
X17은 Ala (A), Cys (C), 또는 Asp (D)이고;
X18은 Leu (L), Arg (R) 또는 Asn (N)이고;
X19는 Thr (T), Asn (N), 또는 Gly (G)이고;
X20은 Glu(E), Arg (R), 또는 Thr (T)이고;
X21은 Ser (S), Val (V), 또는 Leu (L)이고;
X22는 Tyr (Y), Thr (T), Phe (F)이고;
X23은 Asn (N) 또는 Leu (L)이고;
X24는 Asn (N) 또는 Gly (G)이고;
X25는 Val (V) 또는 Ile (I)임).
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 25개 미만의 아미노산 잔기를 함유할 수 있다. 실제로, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11개 또는 심지어 10개의 아미노산 잔기 만을 함유하는 화학식 IX의 절단된 형태 또는 내부 결실된 형태는 화학식 IX의 단리된 펩티드 및 펩티드 유사체의 전반적인 특징 및 조직 보호 특성을 실질적으로 보유한다.
조직 보호 활성에 있어서 화학식 IX의 단리된 펩티드 및 펩티드 유사체의 내부 잔기에서의 공간적으로 조밀한 전하 배열에 대해 예상되는 중요성으로 인하여, 본 발명의 특정 실시양태에서는 극성, 음전하 및 양전하로 하전된 아미노산 및 바로 인접한 아미노산을 포함하는 잔기는 결실되지 않는다. 즉, 특정 실시양태에서 잔기 X11, X12, X13, X14, 및 X15는 결실되지 않는다.
화학식 IX의 단리된 펩티드 및 펩티드 유사체는 또한, 실질적으로 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성에 지장을 주지 않는, 몇몇 실시양태에서는 심지어 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성을 향상시키는 부가적인 아미노산 잔기에 의해 한쪽 또는 양쪽 말단이, 또는 내부가 연장될 수 있다. 실제로, 무려 26, 27, 28, 또는 29개의 아미노산 잔기를 함유하는 연장된 중심 펩티드 및 펩티드 유사체는 본 발명의 범위 내에 속하는 것으로 본다. 바람직하게는, 그러한 연장된 펩티드는 화학식 XI의 펩티드 유사체의 조직 보호 특성을 실질적으로 보유할 것이다.
화학식 XI의 중심 펩티드 및 펩티드 유사체 내의 특정 아미노산 잔기는 펩티드 및 펩티드 유사체의 활성에 유의하게 유해한 영향을 미치지 않는, 많은 경우에서는 심지어 펩티드 및 펩티드 유사체의 활성을 향상시키는 다른 아미노산 잔기로 대체될 수 있다. 따라서, 본 발명에서 또한 고려되는 것은 화학식 내의 적어도 하나, 최대 8개의 아미노산 잔기가 또다른 아미노산 잔기로 보존적으로 치환된, 화학식 XI의 단리된 펩티드 및 펩티드 유사체의 변경 또는 돌연변이된 형태이다. 특정 실시양태에서, 7, 6, 5, 4, 3, 2, 또는 1개의 아미노산이 보존적으로 치환된다.
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 이하의 펩티드 세트 군으로부터 선택된다:
본 발명의 또다른 실시양태에서, 구조적 모티프 B를 나타내는 유형-1 사이토킨의 단리된 펩티드 및 펩티드 유사체는 하기 화학식 X (서열 233)을 갖는다:
(상기 식에서,
X1은 Leu (L)이고;
X2는 Gly (G)이고;
X3은 Cys (C)이고;
X4는 Val (V)이고;
X5는 Leu (L)이고;
X6은 His (H)이고;
X7은 Arg (R)이고;
X8은 Leu (L)이고;
X9는 Ala (A)이고;
X10은 Asp (D)이고;
X11은 Leu (L)이고;
X12는 음전하로 하전된 아미노산이고;
X13은 극성 아미노산이고;
X14는 양전하로 하전된 아미노산이고;
X15는 Leu (L)이고;
X16은 Pro (P)이고;
X17은 Lys (K)이고;
X18은 Ala (A)이고;
X19는 Gln (Q)이고;
X20은 Asp (D)이고;
X21은 Leu (L)이고;
X22는 Glu (E)이고;
X23은 Arg (R)이고;
X24는 Ser (S)이고;
X25는 Gly (G)임).
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 25개 미만의 아미노산 잔기를 함유할 수 있다. 실제로, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11개 또는 심지어 10개의 아미노산 잔기 만을 함유하는 화학식 X의 절단된 형태 또는 내부 결실된 형태는 화학식 X의 단리된 펩티드 및 펩티드 유사체의 전반적인 특징 및 조직 보호 특성을 실질적으로 보유한다.
조직 보호 활성에 있어서 화학식 X의 단리된 펩티드 및 펩티드 유사체의 내부 잔기에서의 공간적으로 조밀한 전하 배열에 대해 예상되는 중요성으로 인하여, 본 발명의 특정 실시양태에서는 극성, 음전하 및 양전하로 하전된 아미노산 및 바로 인접한 아미노산을 포함하는 잔기는 결실되지 않는다. 즉, 특정 실시양태에서 잔기 X11, X12, X13, X14, 및 X15는 결실되지 않는다.
화학식 X의 단리된 펩티드 및 펩티드 유사체는 또한, 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성에 지장을 주지 않는, 몇몇 실시양태에서는 심지어 펩티드 또는 펩티드 유사체의 구조적 및/또는 기능적 특성을 향상시키는 부가적인 아미노산 잔기에 의해 한쪽 또는 양쪽 말단이, 또는 내부가 연장될 수 있다. 실제로, 무려 26, 27, 28, 또는 29개의 아미노산 잔기를 함유하는 연장된 중심 펩티드 및 펩티드 유사체는 본 발명의 범위 내에 속하는 것으로 본다. 바람직하게는, 그러한 연장된 펩티드는 화학식 X의 펩티드 유사체의 조직 보호 특성을 실질적으로 보유할 것이다.
화학식 X의 중심 펩티드 및 펩티드 유사체 내의 특정 아미노산 잔기는 펩티드 및 펩티드 유사체의 활성에 유의하게 유해한 영향을 미치지 않는, 많은 경우에서는 심지어 펩티드 및 펩티드 유사체의 활성을 향상시키는 다른 아미노산 잔기로 대체될 수 있다. 따라서, 본 발명에서 또한 고려되는 것은 화학식 내의 적어도 하나, 최대 8개의 아미노산 잔기가 또다른 아미노산 잔기로 보존적으로 치환된, 화학식 X의 단리된 펩티드 및 펩티드 유사체의 변경 또는 돌연변이된 형태이다. 특정 실시양태에서, 7, 6, 5, 4, 3, 2 또는 1개의 아미노산이 보존적으로 치환된다.
특정 실시양태에서, 단리된 펩티드 및 펩티드 유사체는 다음과 같은 아미노산 서열로 이루어진다:
본원에 상기 기재된 구조적 모티프 C를 예시하는 유형-1 사이토킨으로부터 유래된 펩티드의 추가의 예로는, 이들로 한정되지는 않지만, 인간 트롬보포이에틴 유래된, 펩티드 GG:DLRVLSKLLRDSHV (서열 235); 펩티드 GH:PTPVLLPAVDFSLGEWKTQM (서열 236); 펩티드 GI:TAHKDPNAIFLSFQHLLRGKVRFL (서열 237); 및 펩티드 GJ:PNRTSGLLETNFTAS (서열 238); GM-CSF 유래된, 펩티드 GK:PSTQPWEHVNAIQEARR (서열 239); 펩티드 GL:NETVEVISE (서열 240); 펩티드 GM:QTRLELYKQGLRGSLTKLKGPLTM (서열 241); 및 펩티드 GN:KDFLLVIPFDCWEPVQE (서열 242); CNFT 유래된, 펩티드 GO:CSRSIWLARKIRSD (서열 243); 펩티드 GP:NKNINLDSADGMPVASTD (서열 244); 펩티드 GQ:LLQVAAFAYQIEELMILLEYK (서열 245); 및 펩티드 GR:ELSQWTVRSIHDLRFISS (서열 246); IL-6 유래된, 펩티드 GS:SERIDKQIRYILDGIS (서열 247); 펩티드 GT:AENNLNLPKMAEKD (서열 248); 펩티드 GU:EEQARAVQMSTKVLIQ (서열 249) 및 펩티드 GV:RSFKEFLQSSLR (서열 250); IL-3 유래된, 펩티드 GW:SCNMIDEIITHLKQ (서열 251); 펩티드 GX:ENNLRRPNLEAFNRAVKS (서열 252); 및 펩티드 GY:HIKDGDWNEFRRKLTFYLKT (서열 253); 인간 인터페론 알파 유래된, 펩티드 GZ:SSCLMDRHDFGFPQEEFDGNQ (서열 254); 펩티드 HA:QQIFNLFTTKDSSAAWDE (서열 255); 및 펩티드 HB:LMNADSILAVKKYFRRITLY (서열 256); 인간 인터페론 베타 유래된, 펩티드 HC:MSYNLLGFLQRSSNFQCQKLLWQLN (서열 257); 펩티드 HD:DRMNFDIPEEIKQLQQFQK (서열 258); 펩티드 HE:KLEKEDFTRGKLMSSLHLKR (서열 259) 및 펩티드 HF:FINRLTGYLRN (서열 260); 인간 인터페론 감마 유래된, 펩티드 HG:CYCQDPYVKEAENLKKYFNA (서열 261); 펩티드 HH:ADNGTLFLGILKNWKEESDR (서열 262); 펩티드 HI:NSNKKKRDDFEKLTNYSVTD (서열 263); 및 펩티드 HJ:ELSPAAKTGKR (서열 264); 인간 줄기 세포 인자 유래된, HK:SLIIGFAAGALYWKKRQPSL (서열 265); HL:RNRVTNNVKDVTKLV (서열 266); 펩티드 HM:DKLVNIVDDLVECVKE (서열 267); 및 펩티드 HN:SETSDCWSSTLSPEKDSRV (서열 268); 및 인간 다중 응고 인자 결핍 단백질 2 유래된, 펩티드 HO:DELINIIDGVLRDDDKNND (서열 269); 펩티드 HP:GLDKNTVHDQEHIMEHLEGV (서열 270); 및 펩티드 HQ:QLHYFKMHDYDGNNLL (서열 271)이 있다.
본원에 상기 기재된 구조적 모티프 D를 예시하는 유형-1 사이토킨으로부터 유래된 펩티드의 추가의 예로는, 이들로 한정되지는 않지만, 사포신 C 유래된, 펩티드 HR:CEFLVKEVTKLIDNNKTEKEIL (서열 45); hCNTF AB 루프 유래된, 펩티드 HS:YVKHQGLNKNINLDSVDGVP (서열 46); hIL-6 AB 루프 유래된 펩티드 HT:EALAENNLNLPKMAG (서열 272), hIL-2 AB 루프 유래된 펩티드 HU:LQMILNGINNYKNPKLT (서열 273), hIL-3 AB 루프 유래된 펩티드 HV:ILMENNLRRPNL (서열 274), hIL-.감마 AB 루프 유래된 펩티드 HW:FYLRNNQLVAGTL (서열 275), hLIF AB 루프 유래된, 펩티드 HX:YTAQGEPFPNNVELKLCAP (서열 276); hIL-1.베타 헬릭스 C 유래된 펩티드 HY:FNKIEINNKLEFESA (서열 277), 및 hONC-M 헬릭스 C 유래된 펩티드 HZ:RPNILGLRNNIYCMAQLL (서열 278)이 있다.
본원에 상기 기재된 구조적 모티프 F를 예시하는 유형-1 사이토킨으로부터 유래된 펩티드의 추가의 예로는, 이들로 한정되지는 않지만, hCNTF 유래된, 펩티드 IA:YVKHQGLNKNINLDSVDGVP-바이오틴 (서열 279) 및 hIL-3 유래된 펩티드 IB: D-바이오틴-ILMENNLRRPNL (서열 280)이 있다.
이들 상기 아미노산은 단지 유형 1 사이토킨 수용체를 통해 신호전달하는 사이토킨 상과의 일부 구성원으로부터의 예이며, 사이토킨 상과의 다른 구성원에서의 상동성 영역이 당업자에 의해 용이하게 확인될 것이다.
6.3
키메라
"키메라" 펩티드 (상기 언급한 구조적 모티프를 나타내는 EPO 분자 또는 다른 유형 I 사이토킨의 외향 아미노산의 비-선형 구조적 요소를 도입하는 선형 아미노산 서열) 또한 본 발명에서 고려된다. 본 발명에 유용한 키메라 펩티드는 별도의 아미노산 서열의 구조적 요소들을 단일 펩티드로 합하는 것으로 이루어질 수 있다. 달리 말하면, 키메라 펩티드는 비-선형이지만 인접한 구조적 요소로부터 유래된 아미노산 서열, 예컨대 서열 1의 아미노산 서열 110-115, 133-136, 및 160-165로부터 유래된 단편으로 구성되며, 이는 헬릭스 C의 C 말단 부분 및 루프 C-D의 N-말단 부분, 루프 C-D의 β-병풍 시트, 및 EPO의 C-말단 부분의 구조적 요소가 단일 펩티드에 함유되도록 할 것이다. 추가로, 키메라 펩티드를 이용하여, 특정한 구조체의 중요한 특징, 예를 들면 특정한 3차 구조체의 외향 아미노산을 선별해 낼 수 있다. 따라서, 본 발명의 방법에 유용한 키메라 펩티드는 헬릭스 B 아미노산 58, 62, 65, 69, 72, 76, 79, 80, 83, 84, 및 85 (예를 들면, 펩티드 IC, QEQLERALNSS, 서열 281), 또는 달리 말하면, PCT/US2006/031061에 개시된 EPO의 헬릭스 B의 모든 외부-제시 아미노산으로 구성된 단편으로 이루어질 수 있다. 첫번째 글루타민이 피로글루타메이트로 교체된 추가의 키메라 펩티드 (예를 들면, 펩티드 ID, UEQLERALNSS, 서열 282) 또한 본 발명에서 고려된다.
추가로, 비-천연 발생 또는 키메라 펩티드는 아미노산의 선형 서열을 통해 본원에서 상기 기재된 에리트로포이에틴 또는 또다른 유형-1 사이토킨에서 임의의 두 아미노산의 카르바밀 탄소 사이의 또는 임의의 두 아미노산의 측쇄 사이의 임계 공간 근접성를 모방하도록 고안될 수 있으며, 다른 단백질로부터 유래된 가능한 조직 보호 키메라를 평가하는데 있어서 지침을 제공할 수 있다. 따라서, 본 발명은 신규한 키메라 조직 보호 펩티드, 예컨대 조직 보호를 촉발시키는 이들 구조적 모티프 및 임계 공간 근접성을 나타내는 것에 관한 것이다.
게다가, 본 발명의 펩티드의 효능은 양친매성 펩티드 헬릭스를 부착시킴으로써 증가될 수 있다. 양친매성 펩티드 헬릭스는 당업계에 널리 공지되어 있으며, 예를 들면 펩티드 리간드를 세포 막에 편재화하는 작용을 하는 클래스 B G-단백질 커플링된 수용체 (예를 들면, 문헌 [Segrest et al., 1990, Proteins 8:103], 이는 그의 전문이 본원에 참조로 포함됨)를 통해 신호전달하는 펩티드로부터의 것이다. 이러한 헬릭스의 예로는, 이들로 한정되지는 않지만, 칼시토닌 (펩티드 IE:ALSILVLLQAGS, 서열 283); 코르티코트로핀 방출 호르몬 (펩티드 IF:VALLPCPPCRA, 서열 284); 베타 엔돌핀 (펩티드 IG:NAIIKNAYKKG, 서열 285); 글루카곤 (펩티드 IH:GSWQRSLQDTE, 서열 286); 세크레틴 (펩티드 II:GGSAARPAPP, 서열 287); 혈관 활동성 장관 펩티드 (펩티드 IJ:NALAENDTPYY, 서열 288); 신경펩티드 Y (펩티드 IK:GALAEAYPSKP, 서열 289); 고나도트로핀 방출 호르몬 (펩티드 IL:GCSSQHWSYGL, 서열 290); 부갑상선 호르몬 (펩티드 IM:VMIVMLAICFL, 서열 291); 췌장 폴리펩티드 (펩티드 IN:LRRYINMLTRP, 서열 292); 및 칼시토닌 유전자 관련 펩티드 (펩티드 IO:LALSILVLYQA, 서열 293) (문헌 [Grace et al., 2004, PNAS 101:12836]에 개시됨, 이는 그의 전문이 본원에 참조로 포함됨)로부터의 고도로 소수성인 영역이 있다. 예를 들면, 본 발명의 방법에 유용한 키메라 펩티드는, PCT/US2006/031061에 개시된 바와 같이, 키메라 펩티드 (펩티드 IP:QEQLERALNSSLRRYINMLTRP, 서열 293)의 경우, 췌장 폴리펩티드 (펩티드 IN:LRRYINMLTRP, 서열 292)의 양친매성 헬릭스로 카르복시 말단에서 연결된 EPO의 헬릭스 B의 표면 전하 모티프를 갖는 펩티드 (펩티드 IC:QEQLERALNSS, 서열 281)로부터 제조될 수 있다. 추가의 변형은 그의 조직 보호 특성에 영향을 미치지 않고 양친매성 헬릭스의 카르복시 말단으로 만들어 질 수 있다. 따라서, 조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상의 치료에 유용한 펩티드의 추가의 예는 서열 TR을 갖는 상기 키메라 펩티드 (펩티드 IQ:QEQLERALNSSLRRYINMLTRTR, 서열 294)의 말단 Pro를 교체함으로써 생성될 수 있다.
추가로, 상기 언급한 헬릭스 대신에, 다른 3차 구조체가 상기 펩티드에 부착될 수 있다. 헬릭스 B 외부-제시 아미노산이 EPO의 AB 루프 내에서 발견되는 베타 병풍 시트 (펩티드 IR:CSLNENI, 서열 295)에 연결되어 서열 펩티드 IS:CSLNENIQEQLERALNSS (서열 296)를 가진 키메라 펩티드를 형성할 수 있다. 추가로, 헬릭스 C의 말단 부분의 제시 아미노산 (펩티드 IT:ALGKA, 서열 297, 서열 1의 아미노산 111, 112, 113, 116, 및 118에 상응함)은 모든 또는 일부 루프 CD-부분 (펩티드 IU:LGAQKEAISPPDAASAAPLRTI, 서열 298, 서열 1의 아미노산 112-133에 상응함)과 합해져서 펩티드 IV:ALGKALGAQKEAISPPDAASAAPLRTI (서열 299)를 형성할 수 있다.
추가로, 상기 개시된 다양한 모티프를 나타내는 단리된 펩티드들 [구조적 모티프 A (예컨대, 화학식 I-IV), 구조적 모티프 B (예컨대, 화학식 V-X), 구조적 모티프 C, 구조적 모티프 D, 구조적 모티프 E 및 구조적 모티프 F]이 합해져서 다양한 키메라 또한 형성할 수 있다. 특정 실시양태에서, 상기 키메라는 펩티드 IC, QEQLERALNSS, 서열 281, 펩티드 IP:QEQLERALNSSLRRYINMLTRP, 서열 293, 펩티드 IQ:QEQLERALNSSLRRYINMLTRTR, 서열 294, 펩티드 IS:CSLNENIQEQLERALNSS, 서열 296, 펩티드 IT:ALGKA, 서열 297, 및 펩티드 IV:ALGKALGAQKEAISPPDAASAAPLRTI, 서열 299를 제외할 것이다.
바람직하게는, 융합된 펩티드들 사이에 연결 아암(arm)이 존재하여, 연결된 펩티드들이 적절한 구조적 배향을 취하여 조직 보호 수용체 복합체와 결합할 수 있도록 가요성을 제공할 것이다. 이러한 융합 펩티드는 개별적인 것과는 대조적으로, 가능하게는 조직 보호 수용체 복합체와의 결합 증진 또는 생물학적 반감기의 증가를 통해 함께 더욱 양호한 조직 보호 효과를 달성하는, 상승작용 효과를 가질 수 있다.
당업자는 본 발명에 따라 독성제에 대한 노출로 인해 생성된 손상, 영향, 또는 증상을 예방, 치료, 개선 또는 관리하는 방법에 있어서 이러한 화합물의 효과를 최대화하기 위해 다양한 목적하는 구조적 요소들을 단일 펩티드로 합하는 것이 이익임을 인식할 것이다. 이러한 키메라는 아미노산 펩티드, 및 비-아미노산 요소, 예컨대 링커 또는 다리 원자 또는 잔기를 포함할 수 있다.
6.4 융합 펩티드
본 발명은 추가로 상기 언급된 펩티드, 유래된 단편 또는 키메라 중 2개 이상이 관련 또는 비관련 단백질, 예컨대 에리트로포이에틴, 알부민 등에 결합할 수 있음을 고려한다. 이러한 융합 펩티드는 상승작용 이익을 달성하거나, 펩티드의 순환 반감기를 증가시키거나, 또는 펩티드가 내피 장벽, 예컨대 혈액-뇌 장벽, 혈액-망막 장벽 등을 통과하거나 또는 그 반대로, 즉 PCT/US01/49479 (WO 2002/053580로 공개되었으며, 그의 전문이 본원에 참조로 포함됨)에 개시된 것과 유사한 수송 메카니즘으로 작용하는 능력을 증가시키기 위해 생성될 수 있다.
6.5 펩티드의 제조
본 발명의 방법에 유용한 펩티드는 당업자에게 널리 공지된 재조합 또는 합성 기술을 이용하여 제조될 수 있다. 특히, 고체 상 단백질 합성은 비교적 짧은 길이의 펩티드에 매우 적절하고, 더욱 일관적인 결과로 더 큰 수율을 제공할 수 있다. 추가로, 고체 상 단백질 합성은 펩티드의 제조에 대하여 추가의 융통성을 제공할 수 있다. 예를 들면, 목적하는 화학적 변형이 합성 단계에서 펩티드에 도입될 수 있으며, 호모시트룰린이 라이신과 대조적으로 펩티드의 합성에 사용되어 합성 이후 펩티드를 카르바밀화할 필요성을 없앨 수 있거나, 또는 보호된 관능기를 가진 아미노산이 합성 동안 펩티드에 남을 수 있다.
합성
본 발명의 방법에 유용한 단리된 펩티드 및 펩티드 유사체는 통상의 단계적 용액 또는 고체 상 합성을 이용하여 제조될 수 있다 (예를 들면, 문헌 [Merrifield, R.B., 1963, J. Am. Chem. Soc. 85:2149-2154]; [Chemical Approaches to the Synthesis of Peptides and Proteins, Williams et al., Eds., 1997, CRC Press, Boca Raton Fla.] 및 그에 인용된 참조 문헌; [Solid Phase Peptide Synthesis: A Practical Approach, Atherton & Sheppard, Eds., 1989, IRL Press, Oxford, England] 및 그에 인용된 참조 문헌을 참조).
별법으로, 본 발명에 유용한 펩티드 및 펩티드 유사체는 예를 들면 문헌 [Liu et al., 1996, Tetrahedron Lett. 37(7):933-936]; [Baca, et al., 1995, J. Am. Chem. Soc. 117:1881-1887]; [Tam et al., 1995, Int. J. Peptide Protein Res. 45:209-216]; [Schnolzer and Kent, 1992, Science 256:221-225]; [Liu and Tam, 1994, J. Am. Chem. Soc. 116(10):4149-4153]; [Liu and Tam, 1994, Proc. Natl. Acad. Sci. USA 91:6584-6588]; [Yamashiro and Li, 1988, Int. J. Peptide Protein Res. 31:322-334]에 기재된 세그먼트 축합에 의해 제조될 수 있다. 이는 특히 Gly (G) 함유 펩티드의 경우이다. 본 발명의 펩티드 및 펩티드 유사체의 합성에 유용한 다른 방법은 문헌 [Nakagawa et al., 1985, J. Am. Chem. Soc. 107:7087-7092]에 기재되어 있다.
재조합 기술
다양한 숙주-발현 벡터 시스템을 이용하여 펩티드 및 펩티드 유사체를 제조할 수 있다. 이러한 숙주-발현 시스템은 관심 펩티드가 그에 의해 제조된 후 정제될 수 있는 비히클을 나타내지만, 적절한 뉴클레오티드 코딩 서열로 형질전환되거나 형질감염되는 경우, 변형된 에리트로포이에틴 유전자 생성물을 동일계내에서 제공할 수 있는 세포 또한 나타낸다. 이들에는 이들로 한정되지는 않지만, 박테리아, 곤충, 식물, 포유동물, 예컨대 인간 숙주 시스템, 예컨대 이들로 한정되지는 않지만, 펩티드 코딩 서열을 함유하는 재조합 바이러스 발현 벡터 (예를 들면, 바쿨로바이러스)로 감염된 곤충 세포 시스템; 재조합 바이러스 발현 벡터 (예를 들면, 콜리플라워 모자이크 바이러스, CaMV; 담배 모자이크 바이러스, TMV)로 감염되거나, 에리트로포이에틴-관련 분자 코딩 서열을 함유하는 재조합 플라스미드 발현 벡터 (예를 들면, Ti 플라스미드)로 형질전환된 식물 세포 시스템; 또는 포유동물 세포의 게놈으로부터 유래된 프로모터, 예를 들면 메탈로티오네인 프로모터, 또는 포유동물 바이러스로부터 유래된 프로모터, 예를 들면 아데노바이러스 후기 프로모터를 함유하는 포유동물 세포 시스템, 예컨대 인간 세포 시스템, 예를 들면 HT1080, COS, CHO, BHK, 293, 3T3, PERC6 함유 재조합 발현 구조물; 우두 바이러스 7.5K 프로모터가 있다.
또한, 삽입된 서열의 발현을 조절하거나, 또는 유전자 생성물을 목적하는 특정 양식으로 변형 및 가공하는 숙주 세포 균주가 선택될 수 있다. 단백질 생성물의 이러한 변형 및 가공은 단백질의 기능에 중요할 수 있다. 당업자에게 공지된 바와 같이, 상이한 숙주 세포는 단백질 및 유전자 생성물의 번역후 가공 및 변형에 대하여 특이적 메커니즘을 갖는다. 적절한 세포주 또는 숙주 시스템을 선택하여 발현된 외래 단백질의 올바른 변형 및 가공을 보장할 수 있다. 이를 위하여, 1차 전사체의 적절한 가공, 유전자 생성물의 글리코실화 및 인산화를 위한 세포 기계를 갖는 진핵 숙주 세포가 사용될 수 있다. 이러한 포유동물 숙주 세포, 예컨대 인간 숙주 세포로는 이들로 한정되지는 않지만, HT1080, CHO, VERO, BHK, HeLa, COS, MDCK, 293, 3T3, 및 WI38이 있다.
재조합 펩티드의 장기간, 고수율의 제조를 위하여, 안정한 발현이 바람직하다. 예를 들어, 재조합 조직 보호 사이토킨 관련 분자의 유전자 생성물을 안정하게 발현하는 세포주를 조작할 수 있다. 바이러스 기원의 복제를 함유하는 발현 벡터를 사용하기보다는, 적절한 발현 제어 요소, 예를 들어 프로모터, 인핸서, 서열, 전사 종결자, 폴리아데닐화 부위 등, 및 선택가능한 마커에 의해 제어된 DNA에 의해 숙주 세포를 형질전환시킬 수 있다. 외래 DNA의 도입 이후, 조작된 세포를 보강 배지 중에서 1 내지 2 일 동안 성장하도록 할 수 있고, 그 후 선택 배지로 교환된다. 재조합 플라스미드 중 선택가능한 마커는 선택에 대한 내성을 부여하고, 세포로 하여금 플라스미드를 이의 염색체에 안정적으로 통합하게 하고, 성장하여 포커스(foci)를 형성하게 하며, 이는 이어서 세포주로 클로닝되고 확장될 수 있다. 상기 방법은 유리하게는 조직-보호 생성물을 발현하는 세포주를 조작하는데 사용될 수 있다. 이러한 조작된 세포주는 EPO 관련 분자 유전자 생성물의 내인성 활성에 영향을 미치는 화합물의 선별 및 평가에 특히 유용할 수 있다.
추가 변형
추가로 변형된 펩티드는 또한 조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상의 예방, 치료, 개선 또는 관리를 위한 본 발명의 방법에 사용될 수 있다. 예를 들어, 상기 언급한 구조적 모티프의 펩티드는 하나 이상의 (D)-아미노산으로 합성될 수 있다. 본 발명의 펩티드에 (L)- 또는 (D)-아미노산을 포함시키는 선택은, 부분적으로, 펩티드의 목적하는 특징에 의존한다. 예를 들어, 하나 이상의 (D)-아미노산의 도입은 시험관내 또는 생체내에서 펩티드에 안정성 증가를 부여할 수 있다. 하나 이상의 (D)-아미노산의 도입은 또한, 예를 들어 본원에 기재된 생물검정, 또는 당업계에 널리 공지된 다른 방법을 이용하여 측정시, 펩티드의 결합 활성을 증가시키거나 감소시킬 수 있다.
(L)-아미노산 서열의 전부 또는 일부를 거울상이성질체 (D)-아미노산의 각 서열로 대체하는 것은 펩티드 쇄의 각 부분에 광학 이성질체 구조를 제공한다. (L)-아미노산 서열의 모든 또는 일부 서열의 역위는 펩티드의 레트로-유사체(retro-analogue)를 제공한다. 거울상이성질체 (L에서 D로, 또는 D에서 L로) 대체 및 서열 역위의 조합은 펩티드의 레트로-인버소-유사체(retro-inverso-analogue)를 제공한다. 거울상이성질체 펩티드, 이의 레트로-유사체, 및 이의 레트로-인버소-유사체는 모 펩티드에 대하여 유의한 위상 관계를 유지하며, 특히 고도의 유사성이 종종 모 펩티드 및 이의 레트로-인버소-유사체에 대하여 얻어진다는 점이 당업자에게 공지되어 있다. 상기 관계 및 유사성은 펩티드의 생화학적 특성, 특히 수용체 단백질에 대한 각 펩티드 및 유사체의 고도의 결합에 반영될 수 있다. 펩티드의 상기 특성의 레트로-인버소-유사체의 합성은, 예를 들어 문헌 [Methods of Organic Chemistry (Houben-Weyl), Synthesis of Peptides and Peptidomimetics - Workbench Edition Volume E22c (Editor-in-chief Goodman M.) 2004 (George Thieme Verlag Stuttgart, New York)], 및 이에 인용된 참조 문헌에 기재되어 있으며, 이들의 전문이 본원에 참조로 포함된다.
아미노산 "변형"은 천연 발생 아미노산을 변경시켜 비-천연 발생 아미노산을 생성하는 것을 말한다. 비-천연 발생 아미노산을 갖는 본 발명의 펩티드의 유도체는, 문헌 [Christopher J. Noren, Spencer J. Anthony-Cahill, Michael C. Griffith, Peter G. Schultz, 1989 Science, 244:182-188] (이는 그의 전문이 본원에 참조로 포함됨)에 기재된 바와 같이, 생합성 동안 비-천연 아미노산을 펩티드로 부위 특이적으로 도입함에 의해 또는 화학적 합성에 의해 생성될 수 있다.
치료적으로 유용한 펩티드와 구조적으로 유사한 펩티드 모방체를 사용하여 동등한 치료 또는 예방 효과를 제공할 수 있다. 일반적으로, 펩티드 모방체는 패러다임 폴리펩티드 (즉, 생화학적 특성 또는 약리 활성을 갖는 폴리펩티드)와 구조적으로 유사하나, 당업계에 공지되어 있고, 각각을 본원에 참조로 포함되는 하기 문헌: [Spatola, A.F. in "Chemistry and Biochemistry of Amino Acids, Peptides, and Proteins," B. Weinstein, eds., Marcel Dekker, New York, p 267 (1983)]; [Spatola, A.F., Vega Data (March 1983), Vol. 1. Issue 3, "Peptide Backbone Modifications"] (일반적 개관); [Morely, J.S., Trends Pharma Sci (1980) pp. 463-468] (일반적 개관); [Hudson, D. et al., (1979) Int J Pept Prot Re 14: 177-185] (--CH2―NH--, --CH2―CH2--); [Spatola, A.F. et al., (1986) Life Sci 38:1243-1249] (--CH2―S); [Hann, M. M., (1982) J Chem Soc Perkin Trans I 307-314] (--CH=CH--, 시스 및 트랜스); [Almquist, R.G. et al., (1980) J Med Chem 23: 1392] (--COCH2--); [Jennings-White, C et al., (1982) Tetrahedron Lett 23:2533] (--COCH2--); [Szelke, M et al., European Appln. EP 45665 (1982) CA:97:39405 (1982)] (--CH(OH)CH2--); [Holladay, M.W. et al., (1983) Tetrahedron Lett 24:4401-4404] (--C(OH)CH2--); 및 [Hruby, V.J., (1982) Life Sci 31:189-199] (--CH2―S--)에 추가로 기재된 방법에 의해, --CH2―NH--, --CH2S--, -CH2―CH2--, --CH=CH-- (시스 및 트랜스), --COCH2--, --CH(OH)CH2--, 및 --CH2SO--로 이루어진 군으로부터 선택되는 결합에 의해 임의로 대체된 하나 이상의 펩티드 결합을 갖는다.
또다른 실시양태에서, 특히 바람직한 비-펩티드 결합은 --CH2NH--이다. 상기 펩티드 모방체는 펩티드 실시양태에 비하여 유의한 이점, 예를 들어 더 경제적 제조, 더 큰 화학적 안정성, 강화된 약리적 특성 (반감기, 흡수성, 효과, 효능 등), 변화된 특이성 (예를 들어, 넓은 범위의 생물학적 활성), 감소된 항원성 등을 가질 수 있다.
펩티드 모방체에 대한 다양한 고안이 가능하다. 예를 들어, 필요한 입체형태가 비-펩티드에 의해 안정화되는 환형 펩티드가 특히 고려되고, 본원에 모두 참조로 포함되는 로블(Lobl) 등의 미국 특허 제5,192,746호, 아베르사(Aversa) 등의 미국 특허 제5,576,423호, 샤수와(Shashoua)의 미국 특허 제5,051,448호, 및 가에타(Gaeta) 등의 미국 특허 제5,559,103호는 상기 화합물을 생성하는 여러 방법을 기재한다. 펩티드 서열을 모방하는 비-펩티드 화합물의 합성도 당업계에 공지되어 있다. 본원에 그 전문이 참조로 포함되는 문헌 [Eldred et al., J. Med. Chem. 37:3882 (1994)]은 펩티드 서열을 모방하는 비-펩티드 길항제를 기재한다. 마찬가지로, 본원에 그 전문이 참조로 포함되는 문헌 [Ku et al., J. Med. Chem 38:9 (1995)]은 일련의 상기 화합물의 합성을 더 설명한다.
합성 이후 추가의 변형이 수행될 수 있다. 예를 들어, 화학적으로 변형된 EPO를 개시하는 미국 특허 출원 제10/188,905호 (2003년 4월 17일에 20030072737-A1로서 공개)에 따라, 그리고 미국 특허 출원 제10/612,665호 (2003년 7월 1일에 출원), 및 미국 특허 출원 제09/753,132호 (2000년 12월 29일에 출원)에 따라 (이들은 그들의 전문이 본원에 참조로 포함됨), 펩티드에 대해 추가의 화학적 변형, 즉 카르바밀화, 아세틸화, 숙시닐화, 구아니딜화, 니트레이트화, 트리니트로페닐화, 아미드화 등이 수행될 수 있다.
추가로, 펩티드는 재조합 펩티드 (뮤테인)로 이루어질 수 있다. 개시되어 있는 돌연변이로서 치환, 결실 (예컨대, 내부 결실), 부가 (예컨대, 융합 펩티드를 제공하는 부가), 또는 아미노산 서열 내부의 및/또는 그에 인접한 아미노산 잔기의 보존적 치환을 들 수 있으나, 이는 PCT/US03/20964 (발명의 명칭 "반응성 세포, 조직, 및 기관의 보호, 회복, 및 강화를 위한 재조합 조직 보호 사이토킨 및 이를 코딩하는 핵산{Recombinant Tissue Protective Cytokines and Encoding Nucleic Acids Thereof for Protection, Restoration, and Enhancement of Responsive Cells, Tissues, and Organs}", 그의 전문이 본원에 참조로 포함됨)에서 앞서 개시된 바와 같이, "침묵적" 변화, 및 비-보존적 아미노산 변화, 및 더 큰 삽입 및 결실을 야기한다.
보존적 또는 비-보존적 아미노산 치환이 하나 이상의 아미노산 잔기에서 이루어질 수 있다. 보존적 및 비-보존적 치환 모두가 이루어질 수 있다. 보존적 대체는 이의 측쇄에서 관련된 아미노산의 패밀리 내부에서 일어나는 것이다. 유전자 코딩된 아미노산은 하기 4 가지 패밀리로 분류될 수 있다: (1) 산성 = Asp (D), Glu (G); (2) 염기성 = Lys (K), Arg (R), His (H); (3) 비극성 (소수성) = Cys (C), Ala (A), Val (V), Leu (L), Ile (I), Pro (P), Phe (F), Met (M), Trp (W), Gly (G), Tyr (Y); 및 (4) 하전되지 않은 극성 = Asn (N), Gln (Q), Ser (S), Thr (T). 비-극성은 하기로 세분될 수 있다: 강한 소수성 = Ala (A), Val (V), Leu (L), Ile (I), Met (M), Phe (F); 및 중간 소수성 = Gly (G), Pro (P), Cys (C), Tyr (Y), Trp (W). 대안적 양식으로, 아미노산 레퍼토리는 하기로 분류될 수 있다: (1) 산성 = Asp (D), Glu (G); (2) 염기성 = Lys (K), Arg (R), His (H), (3) 지방족 = Gly (G), Ala (A), Val (V), Leu (L), Ile (I), Ser (S), Thr (T) (여기서, Ser (S) 및 Thr (T)은 임의로 지방족-히드록실로서 별도로 분류됨); (4) 방향족 = Phe (F), Tyr (Y), Trp (W); (5) 아미드 = Asn (N), Glu (Q); 및 (6) 황 -함유 = Cys (C) 및 Met (M) (예를 들어, 문헌 [Biochemistry, 4th ed., Ed. by L. Stryer, WH Freeman and Co., 1995] 참조, 이는 그의 전문이 본원에 참조로 포함됨).
별법으로, 돌연변이는, 예컨대 포화 돌연변이 유발에 의해 펩티드의 코딩 서열의 전부 또는 일부에 걸쳐 무작위로 도입될 수 있고, 생성되는 돌연변이체를 생물학적 활성에 대하여 선별하여 활성을 보유하는 돌연변이체를 식별할 수 있다. 돌연변이 유발 이후, 코딩된 펩티드는 재조합에 의해 발현될 수 있고, 재조합 펩티드의 활성을 측정할 수 있다.
또다른 실시양태에서, 펩티드의 반감기를 연장하거나 또는 펩티드의 조직 보호 효과를 강화시키기 위한 노력으로, 중합체 (예컨대, 폴리에틸렌 글리콜), 당, 또는 추가의 단백질 (예컨대, 융합 구조체)의 부가를 통해 펩티드를 더 변형할 수 있다. 이러한 변형의 예는 본원에 참조로 포함되는 WO/04022577 A3 및 WO/05025606 A1에 개시되어 있다. 예를 들면, 폴리에틸렌 글리콜 중합체를 펩티드 IC에 부착하여, 펩티드 IW ((서열 305) PEG-QEQLERALNSS)를 생성할 수 있다.
선택된 접합 화학, 및 펩티드에 이미 존재하거나 생성된 반응성 부위의 개수에 따라, 1, 2, 또는 선택된 개수의 중합체를 재현가능한 방식으로 부착시킬 수 있다. PEG, 및 그의 유도체를 펩티드에 부착하는 기본 방식은 펩티드 아미노산 잔기를 통한 비-특이적 결합이다 (예를 들면, 미국 특허 제4,088,538호, 미국 특허 제4,496,689호, 미국 특허 제4,414,147호, 미국 특허 제4,055,635호, 및 PCT WO 87/00056 참조). PEG를 펩티드에 부착하는 또다른 방식은 글리코펩티드 상에서 글리코실 잔기의 비-특이적 산화를 통한 것이다 (예를 들면, WO 94/05332 참조). 이들 비-특이적 방법에서는, PEG가 펩티드 주쇄 상의 반응성 잔기에 랜덤하고 비-특이적 방식으로 부가된다.
7. 펩티드를 시험하기 위한 검정
다양한 검정을 이용하여 본 발명의 치료학적 방법에 사용하는데 있어서 상기 언급된 펩티드의 유용성을 측정할 수 있다. 펩티드 조직 보호 활성은 당업계에 공지되고 미국 특허 출원 제10/554,517호, 제10/612,665호 및 제11/997,898호에 개시된 다양한 검정을 이용하여 확인될 것이다. 추가로, 조혈 활성이 없거나 조혈 활성이 감소된 펩티드는 다양한 시험관내 검정, 예컨대 EPO 의존성 세포주 (UT-7), 마우스 비장 생물검정 (문헌 [Krystal, G. (1983) (a simple microassay for erythropoietin based on 3H-thymidine incorporation into spleen cells for phenylhydrazine treated mice. Exp. Hematol. 11, 649-660)]), 또는 클로날 검정 (문헌 [Spivak, J.L., Seiber, F. (1983). Erythropoietin. Horm. Norm. Abnorm. Hum. Tissues 3, 63-96]), 및 생체내 검정, 예컨대 전-저산소성 적혈구증가증 마우스 검정 (문헌 [Cotes PM, Bangham DR, Bio-assay of erythropoietin in mice made polycythaemic by exposure to air at a reduced pressure, Nature. 1961 Sep 9;191:1065-7])을 이용하여 확인할 것이다. 추가로, 당업자는 조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상를 예방, 완화 또는 치료하는 펩티드의 능력을 시험관내 및 생체내 둘 다의 다양한 검정을 통해 (특정 실시양태에서 생체내 검정이 바람직할 수 있음) 확인할 수 있음을 인식할 것이다.
7.1 조직 보호 검정 및 모델
본 발명의 방법에 이용된 펩티드는 조직 보호 특성, 즉 항-아팝토시스, 신경인성, 신경보호성 등을 나타낸다. 본 발명에 따른 펩티드를 조직 보호 활성, 예를 들어 세포, 조직 또는 기관의 보호에 대하여 시험할 수 있다. 시험관내 및 생체내 검정을 이용하여 보호 활성을 더 시험할 수 있다. 조직 보호 활성을 지시하는 시험관내 시험으로서, 예를 들어 세포 증식 검정, 세포 분화 검정, 또는 조직 보호 수용체 복합체, 예를 들어 조직 보호 사이토킨 수용체 복합체의 활성에 의해 상향조절된 단백질 또는 핵산, 예를 들어 뉴클레올린, 뉴로글로빈, 사이토글로빈, 또는 프라탁신의 존재의 검출을 들 수 있다. 뉴로글로빈은, 예를 들어 산소의 운반 또는 장기간 저장을 용이하게 하는데 수반될 수 있다. 따라서, 산소 운반 또는 저장 검정은 조직 보호 활성을 조절하는 화합물을 식별하거나 선별하기 위한 검정으로서 이용될 수 있다.
뉴로글로빈은 저산소증 또는 허혈에 반응하여 중추 신경계의 세포 및 조직에서 발현되고, 손상으로부터의 보호를 제공할 수 있다 (문헌 [Sun et al. 2001, PNAS 98:15306-15311]; [Schmid et al., 2003, J. Biol. Chem. 276:1932-1935], 이들 각각의 전문이 본원에 참조로 포함됨). 사이토글로빈은 보호에 있어서 유사한 역할을 수행할 수 있으나, 다양한 조직 중 다양한 수준으로 발현된다 (문헌 [Pesce et al, 2002, EMBO 3:1146-1151], 이는 전문이 본원에 참조로 포함됨). 본 발명의 한 실시양태에서, 세포 중 상향조절된 단백질의 수준은 펩티드가 세포에 접촉되기 이전 및 이후에 측정될 수 있다. 특정 실시양태에서, 세포 중 조직 보호 활성과 연관되어 상향조절된 단백질의 존재를 이용하여 펩티드의 조직 보호 활성을 확인할 수 있다.
뉴클레올린은 세포를 손상으로부터 보호할 수 있다. 이는 전사 과정, 서열 특이적 RNA 결합 단백질, 세포질 분열, 핵 생성, 신호 전달, T-세포에 의해 유도된 아팝토시스, 크로마틴 리모델링, 또는 복제의 조절을 비롯하여 세포에서 수많은 역할을 한다. 이는 또한 세포 표면 수용체 DNA/RNA 헬리카제, DNA 의존성 ATPase, 단백질 셔틀, 전사 인자 성분, 또는 전사 억제 인자로서 기능할 수 있다 (문헌 [Srivastava and Pollard, 1999, FASEB J., 13:1911-1922]; 및 [Ginisty et al., 1999, J. Cell Sci., 112:761-772], 이들 각각의 전문이 본원에 참조로 포함됨).
프라탁신은 미토콘드리아의 철 대사에 수반되는 단백질이고, 생체내 및 시험관내 모두에서 EPO에 의해 강하게 상향조절되는 것으로 앞서 밝혀졌다 (문헌 [Sturm et al. (2005) Eur J Clin Invest 35:711], 이는 전문이 본원에 참조로 포함됨).
상향조절된 단백질의 발현은 세포 중 단백질에 해당하는 mRNA 수준을 검출함에 의해 검출될 수 있다. mRNA는 상향조절된 단백질을 코딩하는 핵산에 특이적으로 결합되는 프로브에 하이브리드 형성될 수 있다. 하이브리드 형성은, 예를 들어 노던 블롯, 서던 블롯, 어레이 하이브리드 형성, 친화성 크로마토그래피, 또는 동일계내 하이브리드 형성으로 이루어질 수 있다.
본 발명의 펩티드의 조직 보호 활성은 또한 시험관내 신경 보호 검정의 이용으로 검출될 수 있다. 예를 들어, 1차 신경세포 배양액을 트립신 처리에 의해 새로 태어난 래트 해마로부터 준비하고, 예를 들어 MEM-II 성장 배지 (인비트로겐(Invitrogen), 20 mM의 D-글루코스, 2 mM의 L-글루타민, 10%의 Nu-혈청 (소; 뉴저지주 프랭클린 레이크스 소재의 벡톤 디킨슨(Becton Dickinson)), 2%의 B27 보충제 (인비트로겐), 26.2 mM의 NaHCO3, 100 U/㎖의 페니실린, 및 1 ㎎/㎖의 스트렙타비딘 중 당업계에 공지되어 있고/있거나 본원에 기재된 임의의 방법에 의해 배양할 수 있다 (예를 들어, 문헌 [Leist et al., 2004, Science 305:239-242] 참조, 이는 전문이 본원에 참조로 포함됨). 시딩 후 1 일째, 1 μM의 사이토신아라비노-푸라노사이드를 첨가한다. 그 후, 13 일된 배양액을 관심 펩티드의 투여량을 증가시키면서 (3 내지 3000 pM) 24 시간 동안 예비 인큐베이션한다. 14 일째, 배지를 제거하고 배양액에 실온 (RT)에서 PBS 중 300 μM의 NMDA를 투여한다. 5 분 후, 예비 상태조절된 배지를 배양액으로 반환한 후, 이를 인큐베이터에 24 시간 동안 도로 둔다. 세포를 파라포름알데히드 중에서 고정시키고, 획스트(Hoechst) 33342 (오리건주 유진 소재의 몰리큘러 프로브(Molecular Probes))에 의해 염색하여, 농축된 아팝토시스 핵을 계수할 수 있다. NGF (50 ng/㎖) 및 MK801 (1 μM)을 음성 대조군으로서 포함시킨다.
동물 모델 시스템을 이용하여 화합물의 조직 보호 활성을 증명하거나 상기 기재한 본 발명의 선별 방법에 의해 식별된 화합물의 안정성 및 효능을 증명할 수 있다. 그 후, 동물 모델을 이용하여 검정에서 식별된 화합물을 관심을 갖는 조직 손상, 질환, 상태, 또는 증후군의 유형에 대한 생물학적 활성에 대하여 시험할 수 있다. 이는 기능 판독 시스템에 커플링된 조직 보호 수용체 복합체를 포함하도록 조작된 동물, 예컨대 트랜스제닉 마우스를 포함한다.
식별된 화합물의 세포 또는 조직 보호 활성의 효능을 시험하기 위하여 이용될 수 있는 동물 모델은 당업계에 공지되어 있으며, 예를 들어 루이스(Lewis) 래트에서 급성 실험적 알레르기성 뇌척수염의 발병에 대한 보호, 뇌 외상, 뇌 허혈 ("졸중") 또는 흥분독소에 의해 자극된 발작이 부여된 후 마우스에 있어서 감소된 인지 기능으로부터의 복구 또는 보호 (문헌 [Brines et al., 2000, PNAS, 97:10295-10672], 이는 전문이 본원에 참조로 포함됨), 유도된 망막 허혈로부터의 보호 (문헌 [Rosenbaum et al., 1997, Vis . Res. 37:3443-51], 이는 전문이 본원에 참조로 포함됨), 좌골 신경에 대한 손상으로부터의 보호, 및 심장에 대한 허혈-재관류 손상으로부터의 보호 (시험관내 심근 연구 및 생체내 허혈-재관류 손상, 예를 들어 문헌 [Calvillo et al., 2003, PNAS 100:4802-4806] 및 [Fiordaliso et al., 2005, PNAS 102:2046-2051] 참조, 이들 각각의 전문이 본원에 참조로 포함됨)를 포함한다. 상기 검정은 문헌 [Grasso et al. (2004) Med Sci Monit 10: BR1-3], PCT 공보 WO02/053580 또는 PCT 출원 PCT/US2006/031061에 더 상세히 설명되어 있으며, 이들 각각의 전문이 본원에 참조로 포함된다. 이에 기재된 생체내 방법은 EPO의 투여에 대한 것이나, EPO 대신 투여된 조직 보호 단백질도 유사한 생물학적 활성을 나타내는 것으로 식별되었다 (예를 들어, 문헌 [Leist et al. (2004) Science 305:239-242], 이는 전문이 본원에 참조로 포함됨). 펩티드는 또한 시험을 위해 치환될 수 있다. 펩티드의 조직 보호 활성을 측정하기 위한 기타 검정은 당업자에게 잘 공지되어 있다.
별법으로, 본 발명의 펩티드의 평가를 위하여 세포 결합 검정이 수행될 수 있다. 예를 들어, 관심 펩티드를 검출의 용이함을 위해 바이오마커, 예컨대 형광 또는 방사성 표지된 마커에 결합시키고, EPOR 및/또는 βc 수용체를 발현하는 형질감염된 BaF3 세포에 대한 결합을 시험할 수 있다. 96 웰 플레이트에, 성장 배지 (RPMI 1640, 10%의 우태아 혈청, 1 mM의 나트륨 피루베이트, 2 mM의 L-글루타민) 중 관심 펩티드의 8개의 1:2의 일련의 희석액을, 각 웰 중 최종 부피가 약 100 ㎕가 되도록 플레이팅한다. BaF3 모 세포주 및 EPOR 및/또는 βc 수용체로 형질감염된 BaF3 세포를 성장 배지 (상기 참조)로 3회 세척하고, 펠렛을 성장 배지에 재현탁시키며, 세포를 계수하고 성장 배지에 5,000 세포/100 ㎕까지 희석시킬 수 있다. 그 후, 100 ㎕의 희석된 세포를 각 펩티드 희석액에 첨가한다. 그 후, 검정 플레이트를 37℃의 인큐베이터 내에서 3 내지 4 일 동안 인큐베이션한다. 그 후, 플레이트/세포를 세척하고, 형광 플레이트 판독기 상에서 또는 기타 적절한 방법에 의해 플레이트를 판독하여 관심 펩티드의 생물학적 활성과 관련된 바이오마커의 수준을 검출한다.
유사하게, 경쟁 검정을 이용하여 펩티드가 조직 보호성인지를 측정할 수 있다. 경쟁 검정에서, 조직 보호성인 것으로 공지된 화합물, 예컨대 이들로 한정되지는 않지만, 미국 특허 출원 제10/188,905호 및 제10/185,841호 (이들 각각의 전문이 본원에 참조로 포함함)에 개시된 것과 같은 조직 보호 사이토킨을 적절한 바이오마커에 부착할 수 있다.
96 웰 플레이트에, 적절한 성장 배지 중 공지된 조직 보호 화합물/바이오마커의 8개의 1:2의 일련의 희석액, 및 공지된 조직 보호 화합물/바이오마커 및 과량의 관심 펩티드의 동일한 일련의 희석액을 플레이팅한다. 각 희석액의 최종 부피는 약 100 ㎕가 되어야 한다. 다시, BaF3 세포를 상기 개시한 바와 같이 플레이트에 부착하고 인큐베이션한다. 적절한 시간 이후, 세포를 세척하고, 형광 플레이트 판독기 상에서 또는 당업계에 공지된 임의의 적절한 방법에 의해 플레이트를 판독하여 바이오마커를 검출한다. 공지된 조직 보호 화합물/바이오마커 및 관심 펩티드를 포함하는 플레이트 및/또는 웰의 판독 결과가 오로지 공지된 조직 보호 화합물/바이오마커만을 포함하는 플레이트의 판독 결과 미만인 경우, 관심 펩티드는 조직 보호성이다.
현재까지 발견된 다수의 단백질 인자, 예컨대 모든 공지된 사이토킨은 하나 이상의 인자 의존적 세포 증식 검정에서 활성을 보여주었고, 따라서 상기 검정는 사이토킨 활성을 편리하게 확인하는 기능을 한다. 펩티드의 활성은 세포주, 예컨대 이들로 한정되지는 않지만, 32D, DA2, DA1G, T10, B9, B9/11, BaF3, MC9/G, M+(preB M+), 2E8, RB5, DA1, 123, T1165, HT2, CTLL2, TF-1, Mo7e 및 CMK에 대한 수많은 일상적 인자 의존적 세포 증식 검정 중 임의의 것에 의해 증명될 수 있다. 상기 세포를 조직 보호 펩티드의 존재 또는 부재하에 배양하고, 예를 들어 삼중수소 티미딘의 도입률을 측정함으로써 또는 3-(4,5-디메틸티아졸-2-일)-2,5-디페닐 테트라졸륨 브로마이드 (MTT)의 대사 파괴에 기초한 비색 검정에 의해 세포 증식을 검출한다 (문헌 [Mosman, 1983, J. Immunol. Meth. 65:55-63], 이는 전문이 본원에 참조로 포함됨).
펩티드가 조직 보호 활성을 나타내는 경우, 당업자는 당업자에게 공지된 신경 보호 및 조직 보호 검정, 예컨대 이들로 한정되지는 않지만, P-19 및 PC-12 세포 검정 중 하나를 이용한 결과를 증명하는 것이 유용할 것임을 이해할 것이다. 추가로, 다양한 생체내 모델, 예컨대 척수 손상, 허혈성 뇌졸중, 말초 신경 손상, 상처, 또는 심장, 눈, 신장 등에 대산 손상과 관련된 동물 모델이 펩티드를 더 특징분석하는데 도움이 될 것이다. 적절한 시험관내 및 생체내 검정는 각각의 전문을 본원에 참조로 포함되는 미국 특허 출원 제10/188,905호 및 제10/185,841호에 개시되어 있다.
7.2 특정 징후에 대한 검정
A. 독성제.
본 발명의 방법에서 사용되는 단리된 펩티드는 당업계에 공지되거나 본원에 기재된 다양한 검정을 이용하여 시험관내 또는 생체내에서 독성제에 대한 노출로 인한 손상, 영향 또는 증상을 억제하는 것으로 증명될 수 있다.
본 발명의 방법에 사용되는 추가의 펩티드를, 독성제에 대한 노출로 인한 손상, 영향 또는 증상을 예방, 치료, 개선 또는 관리하는 그들의 능력을 측정하기 위해, 당업계의 다양한 시험관내 검정에서 시험할 수 있다. 일반적으로, 이는 적절한 세포주를 선택하고, 그 세포를 관심 독성제에 가하고, 상기 세포 중 일부를 관심 펩티드로 처리하고, 독성제의 존재하에, 그리고 독성제 및 관심 펩티드의 존재하에 세포 생존 또는 반응을 측정함으로써 달성된다. 세포가 상기 펩티드의 존재하에 개선된 생존, 또는 손상, 영향 또는 증상의 감소를 나타내는 경우, 상기 펩티드는 독성제 노출에 대해 가능한 치료제인 것으로 고려될 수 있다. 추가로, 당업자는 보호제로서 상기 펩티드의 능력이 독성제 시도 이전에 세포를 펩티드로 처리함으로써 평가될 수 있음을 인식할 것이다.
예를 들면, 독성제에 대해 적합한 검정으로는, 이들로 한정되지는 않지만, 화학적 작용제: a) 피부 세포주, 예컨대 J-774 (마우스 대식세포 유래된 세포주), CHO-K1 (차이니즈 햄스터 난소 세포로부터 유래된 상피성 세포주의 균주), 및 HeLa (인간 자궁경부 암종) (문헌 [Sawyer, T. et al., Hypothermia as an adjunct to vesicant-induced skin injury, Eplasty 2008; 8:e25]); b) 발포제에 대한 각막 세포주 (문헌 [Amir, A. et al., The corneal epithelium in sulfur mustard ocular injury - In vitro and ex vivo studies, Proceedings of the U.S. Army Medical Defense Bioscience Review, Aberdeen Proving Ground, MD (2004)]); c) 대식세포 (문헌 [Amir A., et al., Sulfur mustard toxicity in macrophages: effect of dexamethasone, J Appl Toxicol, 20 Suppl 1:S51-8 (2000)]); d) 상기도관 세포주 (문헌 [Andrew, D.J. and C.D. Lindsay, Protection of human upper respiratory tract cell lines against sulphur mustard toxicity by gluthione ester, Hum Exp Toxicol 17(7):387-95 (1998)]; [Calvet et al., Airway epithelial damage and release of inflammatory mediators in human lung parenchyma after sulfur mustard exposure, Hum Exp Toxicol 18(2):77-81(1999)]; [Langford, A. M. et al., The effect of sulphur mustard on glutathione levels in rat lung slices and the influence of treatment with arylthiols and cysteine esters, Hum Exp Toxicol 15(8):619-24]); e) 피부 모델 (문헌 [Blaha et al., Effects of CEES on inflammatory mediators, heat shock protein 70A, histology and ultrastructure in two skin models, J Appl Toxicol 20 Suppl 1:S101-8 (2000)]; [Henemyre-Harris et al., An in vitro wound healing model to screen pharmacological interventions for the effective treatment of cutaneous sulfur mustard injuries, Proceedings of the U.S. Army Medical Defense Bioscience Review, Aberdeen Proving Ground, MD (2004)]) (일반적으로, 적절한 시험관내 연구에 대한 추가의 문헌에 대해서는 www.counteract.rutgers.edu/invitro.html 참조); 방사선 작용제: a) 내피 세포 (문헌 [Abderrahmani, R. et al., Role of plasminogen activator inhibitor type-1 in radiation-induced endothelial cell apoptosis, Radioprotection 2008, vol 43, no. 5]), b) 신경면역성 세포 (구심성 신경, 장의 감각 신경, 비만 세포) (문헌 [Wang, J. et al., Neuroimmune interactions: potential target for mitigating or treating intestinal radiation injury, British Journal of Radiology (2007) 80, S41-S48]), c) 혈액 또는 림프구 배양물 (문헌 [Lloyd DC et al., Phys Med Biol 18(3):421-31 (1973)]; [Lloyd DC et al., Mutat. Res. 179(2):197-208 (1987)]; [Blakely WF et al., Stem Cells 13 (Suppl 1):223-30 (1995)]; [Gotoh E et al., Int. J. Radiation. Biol. 81(1):33-40 (2005)]); 생물학적 작용제: (a) 말초 혈액 단핵 세포 (문헌 [Rasha, H. et al. Modeling of SEB-induced host gene expression to correlate in vitro to in vivo responses: Microarrays for biodefense and environmental applications, Biosensors and Bioelectrics (2004) vol. 20, no. 4, 719-727])가 있다.
추가로, 독성제 노출에 대한 치료제의 효과를 평가하는데 적합한 생체내 검정은 당업계에 공지되어 있다. 래트, 마우스, 기니 피그, 토끼, 돼지, 양, 흰담비, 개 및 비-인간 영장류를 이용하는 동물 모델, 뿐만 아니라 독성제에 특히 민감한 트랜스제닉 동물 (CD46 마우스)이 고려된다. 특히, 당업계에 공지된 검정으로는, 이들로 한정되지는 않지만, 화학적 작용제: (1) 문헌 [Reid, F.M., Sulfur mustard induced skin burns in weanling swine evaluated clinically and histopathologically, Journal of applied toxicology, vol. 20 (S1), pages S153-S160 (2001)]; (2) 문헌 [Isidore, M. A. et al., A dorsal model for cutaneous vesicant injury 2-chloroethyl ethyl sulfate using c57bl/6 mice, Cutaneous and ocular toxicology, Vol. 26 (3), 265-276 (2007)]; (3) 일반적으로, www.counteract.rutgers.edu/animal.html 참조; (4) 문헌 [Kassa J., et al., The Choice: HI-6, pradoxime or Obidoxime against Nerve Agents?], www.asanlte.com/ASANews-97/Antidot-Choice.html, (5) 문헌 [Shih, TM et al., Organophosphorus nerve agents-induced seizures and efficacy of atropine sulfate as anticonvulsant treatment, Pharmacol-Biochem-Behav. 1999 Sep, 64(1), 147-53], (6) 문헌 [Luo, C et al., Comparison of oxime reactivation and aging of the nerve agent-inhibited monkey and human acetylcholinesterases, Chemico-Biological Interactions, 175(1-3), 261-266 (2008)]; 방사선 작용제: (1) 문헌 [W.F. Blakely et al., In Vitro and Animal Models of Partial-Body Dose Exposure: Use of Cytogenic and Molecular Biomarkers for Assesment of Inhomogeneous Dose Exposures and Radiation Injury, PB-Rad-Injury 2008 Workshop, May 5-6, 2008 AFRRI, Bethesda, Maryland]; (2) 문헌 [Augustine, A et al., Meeting Report: Animal Models of Radiation Injury, Protection and Therapy, 방사선 Research 164: 100-109 (2005)]; (3) 문헌 [Houchen, C et al. Prosurvival and Antiapoptotic effects of PGE2 in radiation injury are mediated by EP2 receptor in intestine, Am J Physiol Gastrointest Liver Physiol, 284: G490-G498, 2003]; (4) 문헌 [Jichun Chen, Animal Models for Acquired Bone Marrow Failure Syndromes, Clinical Medicine & Research 3(2): 102-108]: 생물학적 작용제: (1) 문헌 [Biodefense: Research Methodology and Animal Models, James R. Swearengen (editor) 2006 CRC Press]이 있다.
B. 염증
추가로, 염증의 다양한 시험관내 모델을 이용하여 신체에 대한 손상, 증상 또는 영향을 보호 또는 치료하는 펩티드의 능력을 평가할 수 있다. 먼저, 염증 매개인자를 조절하는 펩티드의 능력은, 공지된 방법, 예컨대 이들로 한정되지는 않지만 ELISA, 세포측정 비드 어레이 분석, 고감수성 및 면역혼탁측정 검정에 의해 펩티드로 처리한 후 염증 검정에서 염증 매개인자의 수준을 측정함으로써 확인될 수 있다. 예를 들면, 펩티드가 TNF-α 또는 IL-1을 조절하는지를 측정하기 위해서는, LPS-매개 사이토킨 생성의 뮤린 모델을 수행할 것이다. 뮤린 모델에서 일부 마우스를 관심 펩티드로 사전 처리한 다음, LPS를 시도하는 반면에, 다른 것들은 식염수로 처리할 것이다. 그 후, 혈액을 수집할 것이고, 혈중 TNF-α 및 IL-1 수준을 ELISA 키트 (OPT-EIA 마우스 TNF-α 및 IL-1 ELISA 키트 (비디 바이오사이언시즈(BD Biosciences))에 의해 측정할 수 있다. 처리 동물에서의 TNF-α 수준이 식염수 처리 동물에서의 TNF-α 수준에 비해 낮은 경우, 상기 펩티드는 TNF-α를 조절하는 것으로 고려될 수 있다. 바람직하게는, 상기 펩티드를 1개가 넘는 염증 매개인자를 조절하는 그의 능력에 대해 시험할 것이고, 보다 바람직하게는 TNF-α가 아닌 또는 그 이외의 매개인자일 것이고, 가장 바람직하게는 히스타민일 것이다. 유사하게, 상기 펩티드를 추가의 시험관내 검정, 예컨대 이들로 한정되지는 않지만, 문헌 [Lopata, Andreas L., Specialized in vitro Diagnostic Methods In The Evaluation Of Hypersensitivity - An Overview, Current Allergy & Clinical Immunology, March 2006, Vol. 19, No.1] (히스타민 및 트립신 검정), 및 문헌 [Arulmozhi et al., Pharmacological Investigations of Sapindus trifoliatus in various in vitro and in vivo models of inflammation, Indian Journal of Pharmacology, vol. 37:2, 96-102 (2005)] (5-리폭시게나제 (5-LO), 시클로-옥시게나제 (COX), 류코트린 B4 (LTB4) 및 질산 옥사이드 신타제 (NOS))에서 시험할 수 있다.
추가로, 염증의 생체내 검정은 독성제에 대한 치료제로서의 펩티드 유용성을 평가하는데 유용할 수 있다. 생체내 검정으로는, 예컨대 이들로 한정되지는 않지만, 트랜스제닉 마우스를 이용하는 뮤린 EAE 모델, 예컨대 중증 대장염을 가진 엠디바이오사이언시즈(MDBiosciences) DSS IBD 뮤린 모델, 염증성 장 질환을 가진 엠디바이오사이언시즈 TNBS IBD 뮤린 모델, 미국 특허 제6,437,216호에 개시된 IL-1 녹아웃 마우스와 관련된 모델, 또는 문헌 [Probert et al. Spontaneous inflammatory demyelinating disease in transgenic mice showing CNS-specific expression of tumor necrosis factor α. Proc. Natl. Acad. Sci. 1995 USA 92, 11294-11298], [Kontoyiannis et al. Impaired on/off regulation of TNF biosynthesis in mice lacking TNF AU-rich elements: implications for joint and gut-associated immunopathologies. Immunity 10:387-398, 1999], [Keffer et al. Transgenic mice expressing human tumour necrosis factor: a predictive genetic model of arthritis. EMBO J. 1991 Dec; 10(13):4025-31]에 개시된 TNF-α와 관련된 트랜스제닉 마우스의 모델, 또는 염증을 유도하기 위해 화학적 또는 합성적 시도를 이용하는 모델, 예컨대 문헌 [JPET 307:373-385, 2003]에 개시된 천식 및 만성 폐쇄성 폐질환의 모델, EP 1 777 234에 개시된 아쥬반트 관절염 모델; 뮤린 LPS 쇼크 모델, 뮤린 LPS 폐 모델, 급성 발 염증 모델, 또는 하기에 상세히 개시된 히스티딘 시도 팽진 형성 모델이 있다.
추가로, 널리 공지된 임상 연구, 예컨대 문헌 [Ravensberg et al. "Validated safety predictions of airway responses to house dust mites in asthma," Clinical and Experimental Allergy, 37:100-107 (2007)]에 개시된 피부 단자 시험 및 기관지유발 시험; 문헌 [Diamant et al. "Methods used in clinical development of novel anti-asthma therapies," Respiratory Medicine (2008) 102, 332-338]에 개시된 천식 연구, 또는 문헌 [Boot et al. "Nasal Nitric Oxide: longitudinal reproducibility and the effects of a nasal allergen challenge in patients with allergic rhinitis," Allergy 2007:62:378-384]에 개시된 비강 알레르겐 시도를 이용하여 인간에서 화합물의 효능을 확인할 수 있다.
C. 암.
본 발명의 방법에 사용되는 단리된 펩티드는 당업계에 공지되거나 본원에 기재된 다양한 검정을 이용하여 시험관내 또는 생체내에서 종양 세포 증식, 세포 형질전환 및 종양 발생을 억제하는 것으로 증명될 수 있다. 이러한 검정은 암 세포주의 세포 또는 환자로부터의 세포를 이용할 수 있다. 당업계에 널리 공지된 여러 검정을 이용하여 이러한 생존 및/또는 성장을 평가할 수 있으며, 예를 들면 세포 증식은 3H-티미딘 도입률의 측정에 의해, 직접 세포 계수에 의해, 기지 유전자, 예컨대 원종양유전자 (예를 들면, fos, myc) 또는 세포 주기 마커 (Rb, cdc2, 시클린 A, D1, D2, D3 또는 E)의 전사, 번역 또는 활성에서의 변화를 검출함으로써 검정할 수 있다. 이러한 단백질 및 mRNA의 수준 및 활성은 당업계에 널리 공지된 임의의 방법에 의해 측정될 수 있다. 예를 들면, 단백질은 공지된 면역진단 방법, 예컨대 시판되는 항체 (예를 들면, 여러 세포 주기 마커 항체는 산타 크루즈, 인크.(Santa Cruz, Inc.)로부터의 것임)를 이용하는 웨스턴 블롯팅 또는 면역침강에 의해 정량화될 수 있다. mRNA는 당업계에 널리 보편적으로 공지된 방법, 예를 들면 노던 분석, RNase 보호, 역전사와 관련된 폴리머라제 연쇄 반응 등에 의해 정량화될 수 있다. 세포 생존은 트립판-블루 염색, 또는 당업계에 공지된 다른 세포사 또는 생존 마커를 이용하여 평가할 수 있다. 분화는 형태학 등에서의 변화를 기준으로 가시적으로 평가할 수 있다.
본 발명은 당업계에 공지된 다양한 기술, 예컨대 이들로 한정되지는 않지만 하기 기술에 의한 세포 주기 및 세포 증식 분석을 제공한다:
한 예로서, 증식 세포를 식별하기 위한 검정으로서 브로모데옥시우리딘 ("BRDU") 도입을 이용할 수 있다. BRDU 검정은 새로 합성된 DNA로의 BRDU의 도입에 의해 DNA 합성중인 세포 집단을 식별한다. 그 후, 새로 합성된 DNA는 항-BRDU 항체를 이용하여 검출할 수 있다 (문헌 [Hoshino et al., 1986, Int. J. Cancer 38, 369]; [Campana et al., 1988, J. Immunol. Meth. 107, 79] 참조).
세포 증식은 또한 (3H)-티미딘 도입을 이용하여 실험할 수 있다 (예를 들면, 문헌 [Chen, J., 1996, Oncogene 13:1395 403]; [Jeoung, J., 1995, J. Biol. Chem. 270:18367 73] 참조). 이 검정은 S-상 DNA 합성의 정량적인 특징분석을 가능하게 한다. 이 검정에서, DNA를 합성하는 세포는 3H-티미딘을 새로 합성된 DNA에 도입시킬 것이다. 그 후, 도입률은 당업계의 표준 기술에 의해, 예컨대 섬광 계수기 (예를 들면, 베크만(Beckman) LS 3800 액체 섬광 계수기)에서 방사선동위원소의 계수에 의해 측정할 수 있다.
증식 세포 핵 항원 (PCNA)의 검출 또한 세포 증식의 측정에 이용될 수 있다. PCNA는 증식 세포에서, 특히 세포 주기의 초기 G1 및 S 상에서 그의 발현이 상승되는 36 킬로달톤의 단백질이며, 따라서 증식 세포를 위한 마커로서 기능할 수 있다. 양성 세포는 항-PCNA 항체를 이용한 면역염색에 의해 식별된다 (문헌 [Li et al., 1996, Curr. Biol. 6:189 199]; [Vassilev et al., 1995, J. Cell Sci. 108:1205 15] 참조).
세포 증식은 시간에 걸쳐 세포 집단의 샘플을 계수함으로써 (예를 들면, 매일 세포 계수) 측정할 수 있다. 혈구계수기 및 광학 현미경 (예를 들면, 하이라이트(HyLite) 혈구계수기, 하우저 사이언티픽(Hausser Scientific))을 이용하여 세포를 계수할 수 있다. 관심 집단의 성장 곡선을 얻기 위해 세포 개수를 시간에 대해 플롯팅할 수 있다. 바람직한 실시양태에서, 이 방법에 의해 계수된 세포를 먼저 염료 트립판-블루 (시그마(Sigma))와 혼합하여, 살아있는 세포가 상기 염료를 배제하고, 집단의 생존 구성원으로서 계수되게 한다.
세포의 DNA 함량 및/또는 유사분열 지수는 예를 들면 세포의 DNA 배수체 값을 기준으로 하여 측정될 수 있다. 예를 들면, 세포 주기의 G1 상에 있는 세포는 일반적으로 2N DNA 배수체 값을 함유한다. DNA가 복제되었지만 유사분열을 통해 가공되지 않은 세포 (예를 들면, S-상의 세포)는 2N 초과 4N 이하의 배수체 값의 DNA 함량을 나타낼 것이다. 추가로, 프로피둠 요오다이드 검정을 이용하여 배수체 값 및 세포-주기 동역학을 측정할 수 있다 (예를 들면, 문헌 [Turner, T., et al., 1998, Prostate 34:175 81] 참조). 별법으로, DNA 배수체는 컴퓨터화된 미량밀도측정 염색 시스템 상에서 DNA 포일겐(Feulgen) 염색 (이는 화학량론적 방식으로 DNA에 결합함)의 정량화에 의해 측정될 수 있다 (예를 들면, 문헌 [Bacus, S., 1989, Am. J. Pathol. 135:783 92] 참조). 또다른 실시양태에서, DNA 함량은 염색체 스프레드의 제조에 의해 분석할 수 있다 (문헌 [Zabalou, S., 1994, Hereditas. 120:127 40]; [Pardue, 1994, Meth. Cell Biol. 44:333 351]).
세포-주기 단백질 (예를 들면, CycA, CycB, CycE, CycD, cdc2, Cdk4/6, Rb, p21 또는 p27)의 발현은 세포 또는 세포 집단의 증식 상태와 관련된 중대한 정보를 제공한다. 예를 들면, 항증식 신호전달 경로의 확인은 p21cip1의 유도에 의해 나타날 수 있다. 세포에서 p21 발현 수준이 증가하면, 세포 주기의 G1으로의 진입이 지연된다 (문헌 [Harper et al., 1993, Cell 75:805 816]; [Li et al., 1996, Curr. Biol. 6:189 199]). p21 유도는 시판되는 특이적 항-p21 항체 (예를 들면, 산타 크루즈, 인크.로부터)를 이용하여 면역염색에 의해 확인될 수 있다. 유사하게, 세포-주기 단백질을 시판되는 항체를 이용하여 웨스턴 블롯 분석에 의해 실험할 수 있다. 또다른 실시양태에서, 세포 주기 단백질을 검출하기 전에 세포 집단을 동조화시킨다. 세포-주기 단백질은 또한 관심 단백질에 대한 항체를 이용하여 FACS (형광-활성화된 세포 분별기) 분석에 의해 검출할 수 있다.
본 발명의 펩티드에 의해 세포 증식의 억제를 측정하기 위해 세포 주기의 길이 또는 세포 주기의 속도에서의 변화의 검출을 또한 이용할 수 있다. 한 실시양태에서, 세포 주기의 길이는 (예를 들면, 하나 이상의 본 발명의 펩티드와 접촉하거나 접촉하지 않은 세포를 이용하여) 세포 집단의 배가 시간에 의해 측정된다. 또다른 실시양태에서, FACS 분석을 이용하여 세포 주기 진행의 상을 분석하거나, G1, S, 및 G2/M 분획을 정제한다 (예를 들면, 문헌 [Delia, D. et al., 1997, Oncogene 14:2137 47] 참조).
세포 주기 체크포인트의 경과 및/또는 세포 주기 체크포인트의 유도는 본원에 기재된 방법에 의해 또는 당업계에 공지된 임의의 방법에 의해 실험할 수 있다. 비제한적으로, 세포 주기 체크포인트는 어떤 세포 사건이 특정한 순서로 일어나는 것을 보장하는 메카니즘이다. 체크포인트 유전자는 후기 사건들이 초기 사건의 사전 완료 없이는 일어나지 않게하는 돌연변이로 정의된다 (문헌 [Weinert, T., and Hartwell, L., 1993, Genetics, 134:63 80]). 세포 주기 체크포인트 유전자의 유도 또는 억제는 예를 들면 웨스턴 블롯 분석에 의해 또는 면역염색 등에 의해 검정할 수 있다. 추가로, 세포 주기 체크포인트의 경과는 특정한 사건의 사전 발생 없이 체크포인트를 통한 세포의 진행 (예를 들면, 게놈 DNA가 완전히 복제되지 않고 유사분열로 진행)에 의해 평가될 수 있다.
특정 세포 주기 단백질의 발현의 효과 외에도, 세포 주기와 관련된 단백질의 활성 및 번역후 변형은 세포의 조절 및 증식 상태에 필수적인 역할을 할 수 있다. 본 발명은 당업계에 공지된 임의의 방법에 의해 검출된 번역후 변형 (예를 들면, 인산화)과 관련된 검정을 제공한다. 예를 들면, 인산화된 티로신 잔기를 검출하는 항체는 시판되는 것이며, 웨스턴 블롯 분석에 이용하여 이러한 변형을 가진 단백질을 검출할 수 있다. 또다른 예로, 미리스틸화와 같은 변형은 박층 크로마토그래피 또는 역상 h.p.l.c. 상에서 검출될 수 있다 (예를 들면, 문헌 [Glover, C., 1988, Biochem. J. 250:485 91]; [Paige, L., 1988, Biochem J.; 250:485 91] 참조).
신호전달 및 세포 주기 단백질 및/또는 단백질 복합체의 활성은 종종 키나제 활성에 의해 매개된다. 본 발명은 히스톤 H1 검정과 같은 검정에 의한 키나제 활성의 분석을 제공한다 (예를 들면, 문헌 [Delia, D. et al., 1997, Oncogene 14:213747] 참조).
본 발명의 방법에 사용되는 펩티드는 또한 당업계에 널리 공지된 방법을 이용하여 시험관내에서 배양된 세포에서 세포 증식을 변경시키는 것으로 증명될 수 있다. 세포 배양 모델의 구체적인 예로는, 이들로 한정되지는 않지만, 폐암의 경우 원발성 래트 폐 종양 세포 (문헌 [Swafford et al., 1997, Mol. Cell. Biol., 17:1366 1374]) 및 대세포 미분화된 암 세포주 (문헌 [Mabry et al., 1991, Cancer Cells, 3:53 58); 결장암의 경우 결장직장 세포주 (문헌 [Park and Gazdar, 1996, J. Cell Biochem. Suppl. 24:131 141]); 유방암의 경우 다중으로 수립된 세포주 (문헌 [Hambly et al., 1997, Breast Cancer Res. Treat. 43:247 258]; [Gierthy et al., 1997, Chemosphere 34:1495 1505]; [Prasad and Church, 1997, Biochem. Biophys. Res. Commun. 232:14 19]); 전립선암의 경우 특징이 잘 분석된 수많은 세포 모델 (문헌 [Webber et al., 1996, Prostate, Part 1, 29:386 394; Part 2, 30:58 64; and Part 3, 30:136 142]; [Boulikas, 1997, Anticancer Res. 17:1471 1505]); 비뇨생식기암의 경우 연속 인간 방광암 세포주 (문헌 [Ribeiro et al., 1997, Int. J. Radiat. Biol. 72:11 20]); 전이성 세포 암종의 경우 기관 배양물 (문헌 [Booth et al., 1997, Lab Invest. 76:843 857]) 및 래트 진행 모델 (문헌 [Vet et al., 1997, Biochim. Biophys Acta 1360:39 44]); 및 백혈병 및 림프종의 경우 수립된 세포주 (문헌 [Drexler, 1994, Leuk. Res. 18:919 927, Tohyama, 1997, Int. J. Hematol. 65:309 317])가 있다.
본 발명의 펩티드는 또한 시험관내에서 세포 형질전환 (또는 악성 표현형으로의 진행)을 억제하는 것으로 증명될 수 있다. 이 실시양태에서, 형질전환된 세포 표현형을 가진 세포를 하나 이상의 본 발명의 펩티드와 접촉시키고, 형질전환된 표현형과 관련된 특징 (생체내 종양형성 능력과 연관있는 일련의 시험관내 특징), 예를 들면 이들로 한정되지는 않지만, 연질 한천에서의 콜로니 형성, 더 둥근 세포 형태학, 더 느슨한 기층 부착, 접촉 억제의 소실, 앵커 의존성의 소실, 프로테아제, 예컨대 플라스미노겐 활성화제의 방출, 증가된 당 수송, 감소된 혈청 요건, 또는 태아 항원의 발현 등의 변화에 대해 실험한다 (문헌 [Luria et al., 1978, General Virology, 3d Ed., John Wiley & Sons, New York, pp. 436446] 참조).
침윤성의 소실 또는 감소된 부착을 또한 이용하여 본 발명의 방법에 사용되는 펩티드의 항암 효과를 증명할 수 있다. 예를 들면, 전이성 암 형성의 결정적인 측면은 전암 또는 암 세포가 질환의 원발성 부위로부터 분리되어 속발성 부위에 새로운 성장 콜로니를 수립하는 능력이다. 말초 부위로 침윤하는 세포의 능력은 암 상태에 대한 잠재력을 반영한다. 침윤성의 소실은 당업계에 공지된 다양한 기술, 예를 들면 E-카드헤린-매개 세포--세포 부착의 유도에 의해 측정할 수 있다. 이러한 E-카드헤린-매개 부착에 의해, 표현형 복귀 및 침윤성의 소실이 일어날 수 있다 (문헌 [Hordijk et al., 1997, Science 278:1464 66]).
추가로, 침윤성의 소실은 세포 이동의 억제에 의해 실험할 수 있다. 다양한 2-차원 및 3-차원 세포 매트릭스가 시판된다 (캘리포니아주 샌 디에고 소재의 칼바이오켐-노바바이오켐 코포레이션(Calbiochem-Novabiochem Corp.)). 매트릭스를 가로지르거나 그 안으로의 세포 이동은 현미경, 저속 사진 촬영 또는 비디오 촬영에 의해, 또는 세포 이동의 측정을 가능하게 하는 당업계의 임의의 방법에 의해 실험할 수 있다. 관련 실시양태에서, 침윤성의 소실은 간세포 성장 인자 (HGF)에 대한 반응에 의해 실험한다. HGF-유도된 세포 산란은 마딘-다비(Madin-Darby) 개 신장 (MDCK) 세포와 같은 세포의 침윤성과 상호관련이 있다. 이 검정에 의해, HGF에 반응하는 세포 산란 활성을 소실한 세포 집단을 식별한다 (문헌 [Hordijk et al., 1997, Science 278:1464 66]).
별법으로, 침윤성의 소실은 주화성 챔버 (브리티시 콜롬비아주 밴쿠버 소재의 뉴로프로브/프리시젼 바이오케미컬즈 인크.(Neuroprobe/Precision Biochemicals Inc.))를 통한 세포 이동에 의해 측정할 수 있다. 이러한 검정에서는, 화학유인물질을 챔버의 한 측 (예를 들면, 바닥 챔버)에서 인큐베이션하고, 세포를 반대측 (예를 들면, 상단 챔버)에 떨어져 있는 여과기 상에 플레이팅한다. 세포가 상단 챔버에서 바닥 챔버로 통과하기 위해서는, 세포가 여과기에 있는 작은 구멍을 통해 활발히 이동해야 한다. 그 후, 이동한 세포의 개수에 대한 체커보드 분석은 침윤성과 상호관련있을 수 있다 (예를 들면, 문헌 [Ohnishi, T., 1993, Biochem. Biophys. Res. Commun. 193:518 25]).
본 발명의 방법에 사용되는 펩티드는 또한 생체내에서 종양 형성을 억제하는 것으로 증명될 수 있다. 과다증식 장애, 예컨대 종양 형성 및 전이성 전파의 매우 많은 동물 모델이 당업계에 공지되어 있다 (문헌 ["Principles of Neoplasia," in Harrison's Principles of Internal Medicine, 13th Edition, Isselbacher et al., eds., McGraw-Hill, N.Y., p. 1814]의 챕터 317, 표 317-1, 및 [Lovejoy et al., 1997, J. Pathol. 181:130 135] 참조). 구체적인 예로는 폐암의 경우 래트에게 종양 결절의 이식 (문헌 [Wang et al., 1997, Ann. Thorac. Surg. 64:216 219]) 또는 NK 세포 결핍 SCID 마우스에서 폐암 전이의 수립 (문헌 [Yono and Sone, 1997, Gan To Kagaku Ryoho 24:489 494]); 결장암의 경우 누드 마우스에게 인간 결장암 세포의 결장암 이식 (문헌 [Gutman and Fidler, 1995, World J. Surg. 19:226 234]), 인간 궤양성 대장염의 솜머리 비단원숭이 모델 (문헌 [Warren, 1996, Aliment. Pharmacol. Ther. 10 Supp 12:45 47]) 및 선종성 폴립증 종양 저해제의 돌연변이를 가진 마우스 모델 (문헌 [Polakis, 1997, Biochim. Biophys. Acta 1332:F127 F147]); 유방암의 경우 유방암의 트랜스제닉 모델 (문헌 [Dankort and Muller, 1996, Cancer Treat. Res. 83:71 88]; [Amundadittir et al., 1996, Breast Cancer Res. Treat. 39:119 135]) 및 래트에서 종양의 화학적 유도 (문헌 [Russo and Russo, 1996, Breast Cancer Res. Treat. 39:7-20); 전립선암의 경우 화학적으로 유도된 트랜스제닉 설치류 모델, 및 인간 이종이식편 모델 (문헌 [Royai et al., 1996, Semin. Oncol. 23:35 40]); 비뇨생식기암의 경우 래트 및 마우스에서 유도된 방광 신생물 (문헌 [Oyasu, 1995, Food Chem. Toxicol 33:747 755]) 및 누드 래트에서 인간 전이 세포 암종의 이종이식편 (문헌 [Jarrett et al., 1995, J. Endourol. 9:1 7]); 및 조혈 암의 경우 동물에서 동종 골수 이식 (문헌 [Appelbaum, 1997, Leukemia 11 (Suppl. 4):S15 S17])이 있다. 추가로, 여러 유형의 암에 적용가능한 일반적인 동물 모델, 예컨대 이들로 한정되지는 않지만, p53-결핍 마우스 모델 (문헌 [Donehower, 1996, Semin. Cancer Biol. 7:269 278]), Min 마우스 (문헌 [Shoemaker et al., 1997, Biochem. Biophys. Acta, 1332:F25 F48]), 및 래트에서 종양에 대한 면역 반응 (문헌 [Frey, 1997, Methods, 12:173 188])이 기재되어 있다.
예를 들면, 본 발명의 방법에 사용되는 펩티드를 시험 동물, 한 실시양태에서 소정 유형의 종양이 발전할 소인이 있는 시험 동물에게 투여하고, 후속적으로 본 발명의 펩티드를 투여하지 않은 동물과 비교하여 종양 형성의 감소된 유병률에 대해 시험 동물을 실험할 수 있다. 별법으로, 본 발명의 펩티드를 종양을 가진 시험 동물 (예를 들면, 악성, 신생물성, 또는 형질전환 세포의 도입에 의해, 또는 발암 물질의 투여에 의해 종양이 유도된 동물)에게 투여하고, 후속적으로 본 발명의 펩티드를 투여하지 않은 동물과 비교하여 종양 퇴행에 대해 동물을 실험할 수 있다.
8. 치료학적 용도
A. 신체 반응의 매개인자의 조절
당업자는 본 발명의 펩티드를 사용하여, 조직 손상 관련 질환 또는 장애에 대한 신체 반응의 영향을 조절할 수 있음을 인식할 것이다. 특히, 상기 언급된 펩티드를 사용하여 조절할 수 있는 매개인자의 한 예는 염증 조절제, 예컨대 이들로 한정되지는 않지만, 혈장 유래된 염증 매개인자, 예컨대 브라디키닌, C3, C5a, 인자 XII, 막 공격 복합체, 하게만(Hageman) 인자, 플라스민, 트롬빈, 림포카인 (대식세포 활성화 인자 (MAF), 대식세포 이동 억제 인자 (MMIF), 대식세포 화학주성 인자 (MCF), 백혈구 이동 억제 인자 (LMIF), 히스타민 방출 인자 (HRF), 및 전달 인자 (TF)); 인터류킨 (IL-1, IL-2, IL-3, IL-4, . . . IL-15); 종양 괴사 인자 (TNF-α (카켁틴), TNF-β (림포톡신)); 인터페론 (IFN-α, IFN-β, IFN-γ, IFN-ω, IFN-τ); 콜로니 자극 인자 (과립구 콜로니 자극 인자 (G-CSF), 과립구-대식세포 콜로니 자극 인자 (GM-CSF), 대식세포 콜로니 자극 인자 (M-CSF), 및 다중 콜로니 자극 인자 (IL-3)); 폴리펩티드 성장 인자 (산성 섬유모세포 성장 인자 (aFGF), 염기성 섬유모세포 성장 인자 (bFGF), 표피 성장 인자 (EGF); 신경 성장 인자 (NGF), 혈소판-유래된 성장 인자 (PDGF), 및 혈관 내피 성장 인자 (VEGF)); 전환 성장 인자 (TGF-α 및 TGF-β), α-케모카인 (IL-8, 호중구-활성화 단백질 2 (NAP-2), 혈소판 인자-4 (PF-4), 및 β-트롬보글로불린 (βTG)); β-케모카인 (단핵세포 화학유인물질 단백질 1 (MCP-1), MCP-3, MIP-1α, 대식세포 염증성 단백질 1β (MIP-1β), 발현되고 아마도 분비된 정상 T 활성화시 조절되는 케모카인 (RANTES)) 및 스트레스 단백질 (열 쇼크 단백질 (HSP), 글루코스 관련 단백질 (GSP), 유비퀴틴, 및 수퍼옥사이드 디스무타제 (Mn)), 백혈병 억제 인자 (LIF), 옹코스타틴 (OSM), 섬모 신경친화성 인자 (CNTF), 혈소판 염기성 단백질 (PBP), 라이소좀 과립, 히스타민, 세로토닌, 류코트리엔 B4, 일산화질소, 및/또는 프로스타글란딘이다. 바람직한 실시양태에서, 상기 펩티드는 상기 매개인자의 활성을 억제 또는 저해하고, 보다 바람직하게는 TNF-α, 히스타민, 일산화질소, 및 인터류킨의 활성을 억제한다. 가장 바람직하게는, 상기 펩티드는 2종 이상의 염증 매개인자의 활성을 억제한다.
B. 다양한 질환, 장애, 및 상태의 치료 또는 예방
본 발명의 조직 보호 펩티드 및 펩티드 유사체는 또한 다양한 질환, 장애, 및 상태의 치료 또는 예방을 위한 치료제로서 유용하다. 당업자는 또한 이러한 펩티드 및 펩티드 유사체가 조직 보호 수용체 복합체, 예를 들어 조직 보호 사이토킨 복합체의 조절을 달성하기 위해 사용될 수 있다는 점을 인식할 것이다. 예를 들어, 상기 개시한 본 발명의 검정에 의해 식별된 화합물의 치료학적 적응을 평가하기 위해 이용될 수 있는 시험관내 및 생체내 기술 모두 PCT 출원 PCT/US01/49479, 미국 특허 출원 제10/188,905호 및 제10/185,841호에 개시되어 있다.
본 발명의 상기 조직 보호 펩티드 및 펩티드 유사체는, 주로 신경학적 또는 정신의학적 증상을 갖는 중추 신경계 또는 말초 신경계의 인간 질환 또는 장애, 안구 질환, 심혈관 질환, 심폐 질환, 호흡기 질환, 신장, 비뇨기 및 생식기 질환, 골 질환, 피부 질환, 결합 조직 질환, 위장 질환 및 내분비 및 대사 이상의 예방, 치료적 처치, 또는 예방적 처치에 일반적으로 유용할 수 있다. 용도의 예로는, 이들로 한정되지는 않지만, 외상으로부터 발생하는 손상, 및 뇌 (허혈성 뇌졸중, 둔상, 지주막하 출혈), 척수 (허혈, 둔상), 말초 신경 (좌골 신경 손상, 당뇨병성 신경병증, 수근관 증후군), 망막 (황반 부종, 당뇨병성 망막증, 녹내장), 및 심장 (심근 경색증, 만성 심부전증)에 대한 염증으로부터 발생하는 손상에 대한 보호 및 이의 복구를 들 수 있다. 특히, 이러한 질환, 장애, 및 상태로는 저산소증 상태가 있으며, 이는 반응성 조직, 예컨대 흥분성 조직, 예컨대 이들로 한정되지는 않지만, 섹션 4.2 (xiii)에서 상기 언급된 것, 또는 이들 반응성 세포 조직 또는 기관, 적절한 유형-1 사이토킨 수용체, 예를 들면 EPO-R 수용체 또는 조직 보호 수용체 복합체를 발현하는 것에 불리한 영향을 미친다. 따라서, 본 발명의 조직 보호 펩티드 및 펩티드 유사체는 다양한 상태 및 상황에서의 저산소증 상태로부터 발생하는 반응성 조직에 대한 손상을 치료 또는 예방하기 위해 사용될 수 있다. 상기 상태 및 상황의 비제한적인 예는 본원에서 하기 표에 제공되어 있다.
조직 보호 펩티드 및 펩티드 유사체는 또한 줄기 세포 활성의 조절에 있어서 관심의 대상이다. 조직 보호 활성을 나타내는 사이토킨, 예를 들어 EPO는, 예를 들어 재생적 역할에 있어서 줄기 세포를 동원하여 손상 부위로의 이동을 자극하고 복구 과정을 보조할 수 있는 것으로 정립되었다. 예를 들어, 실험적 뇌졸중에 있어서, EPO는 회복 기간 동안 신경모세포의 허혈 손상 부위로의 동원을 매개하여 신경세포를 재생시킨다 (문헌 [Tsai et al, J. Neurosci (2006) 26:1269-74]). 또다른 예로서, EPO 및 카르바밀화 EPO (CEPO)는 골수로부터 내피 전구 세포를 동원하여 순환시킨다. 그 후, 이들 세포는 먼 부위로 나아가서 새로운 혈관의 형성에 수반된다 (EPO의 효과에 대하여, 예를 들어 문헌 [Bahlmann et al, 2003, Kidney Int. 64:1648-1652] 참조). 임의의 특정 이론에 구애되고자 하는 것은 아니지만, 본원에 개시된 단리된 펩티드 및 펩티드 유사체는 줄기 세포의 동원에 대하여 유사한 효과를 갖는 것으로 여겨진다.
본 발명의 조직 보호 펩티드 및 펩티드 유사체를 이용하여 치료가능하고 예방가능한 뉴런 조직 병리의 보호의 예에 있어서, 이러한 병리는 뉴런 조직의 감소된 산소 공급으로부터 발생한 것을 포함한다. 스트레스, 손상, 및 결국, 뉴런 세포사를 초래하는, 뉴런 조직으로의 산소의 이용가능성을 감소시키는 임의의 상태가 본 발명의 조직 보호 펩티드 및 펩티드 유사체의 이용으로 치료될 수 있다. 일반적으로 저산소증 및/또는 허혈로서 일컬어지는 이들 상태는 뇌졸중, 혈관 폐쇄, 출생전 또는 출생후 산소 부족, 질식, 숨막힘, 익수, 일산화탄소 중독, 연기 흡입, 외상 (예컨대, 수술 및 방사선 요법), 질식, 간질, 저혈당, 만성 폐쇄성 폐질환, 기종, 성인 호흡 곤란 증후군, 혈압강하 쇼크, 패혈성 쇼크, 아나필락시스성 쇼크, 인슐린 쇼크, 겸상 적혈구 빈혈, 심장 마비, 율동 부정, 질소 마취, 저산소혈성 저산소증 (고산병, 고산성 폐 부종, 고산성 뇌 부종, 수면 무호흡, 호흡 저하, 호흡 정지, 단락), 메트헤모글로빈혈증, 조직독성 저산소증, 자궁내 저산소증, 및 심폐 우회 절차에 의해 야기된 신경 결손으로부터 발생하거나 이를 포함하나 이에 국한되는 것은 아니다.
한 실시양태에서, 예를 들어 상기 언급한 검정의 이용으로 식별된 본 발명의 조직 보호 펩티드 및 펩티드 유사체는 수술 절차 또는 의료 절차 이전, 동안, 또는 이후에 손상 또는 조직 손상의 위험으로부터 발생하는 손상 또는 조직 손상을 예방하기 위하여 단독으로 또는 조성물의 일부로서 투여될 수 있다. 예를 들어, 수술 절차는 종양 절제 또는 동맥류 복구를 포함할 수 있고, 의료 절차는 산통 또는 분만을 포함할 수 있다. 본 발명의 조직 보호 펩티드 및 펩티드 유사체를 사용하여 치료가능한, 저혈당에 의해 야기되거나 이로부터 발생하는 기타 병리로서 의원성 고인슐린혈증으로서도 일컬이지는 인슐린 과량복용, 인슐린종, 성장 호르몬 결핍, 코르티솔 저하증, 약물 과량복용, 및 특정 종양을 들 수 있다.
흥분성 뉴런 조직 손상으로부터 발생하는 기타 병리로서 발작 장애, 예컨대 간질, 경련, 또는 만성 발작 장애를 들 수 있다. 치료가능한 기타 상태 및 질환의 예로는, 이들로 한정되지는 않지만, 뇌졸중, 다발성 경화증, 저혈압, 심장 마비, 만성 심부전증, 알츠하이머 질환, 파킨슨 질환, 뇌성 마비, 뇌 또는 척수 외상, AIDS 치매, 노년기 인지 기능 상실, 기억 상실, 근위축성 측삭 경화증, 발작 장애, 알콜 중독, 망막 허혈, 녹내장으로부터 발생하는 눈 신경 손상, 및 뉴런 소실과 같은 질환을 들 수 있다.
본 발명의 특정 조직 보호 펩티드 및 펩티드 유사체를 사용하여 질환 상태 또는 다양한 외상으로부터 발생하는 염증, 예컨대 물리적 또는 화학적으로 유도된 염증을 치료하거나 예방할 수 있다. 조직 보호 펩티드펩티드 및 펩티드 유사체는 또한 하나 이상의 기관 또는 조직, 예컨대 이들로 한정되지는 않지만, 뇌, 척수, 결합 조직, 심장, 폐, 신장 및 요로, 췌장, 눈 및 전립선에서 염증 상태의 치료 및 예방을 위해 고려된다. 상기 외상의 비제한적인 예로는 이들로 한정되지는 않지만 섹션 4.2 (xvi)에 열거된 것들이 있다. 추가로, 조직 보호 펩티드를 사용하여 허혈성 및 비-허혈성 상태, 예컨대 이들로 한정되지는 않지만, 알레르기, 알레르기성 질환, 알레르기성 증상, 류마티스성 질환, 스포츠 관련 손상, 독성제에 대한 노출, 감염 (예컨대, 바이러스, 진균, 및 박테리아)으로부터 발생하는 염증을 치료하거나 예방할 수 있으며, 이러한 상태의 추가로 예는 상기 섹션 4.2(iv), (v) 및 (xvi)에 개시되어 있다. 염증은 급성 또는 만성일 수 있다. 염증 분야에서의 추가의 출원은 2004년 9월 29일에 출원되고 WO 2005/032467로서 공개된 PCT/US2004/031789에 기재되어 있다.
본 발명의 특정 조직 보호 펩티드 및 펩티드 유사체를 사용하여 수초 손상 또는 탈수초로부터 발생하는 중추 신경계 및 말초 신경계 질환을 치료할 수 있다. 이들 질환은 기원을 모르는 염증성 수초 병변을 주로 수반하는 것으로 정의되나, 단 수초형성 결핍 질환, 예컨대 백질이영양증, 및 명백한 원인으로 인한 질환은 예외이다. 다발성 경화증 (MS)은 탈수초성 질환 중 전형적 질환이며, 병리학적으로 이는 변화, 주로 염증성 탈수초, 및 신경아교증으로 특징지어진다. 이의 병인이 공지되어 있지 않으므로, 이의 진단은 임상적 특징, 즉 중추 신경계 병변의 공간적 다중성 및 시간에 걸친 다중성에 기초하여 이루어진다. 더욱이, 급성 파종성 뇌척수염 (ADEM), 염증성 범발성 경화증, 급성 및 아급성 괴사 출혈성 뇌척수염, 및 횡단성 척수염이 탈수초성 질환에 포함된다. 또한, 말초 신경 조직은 수초를 유지하는 슈반 세포에 의존하고, 상기 세포가 손상되는 경우, 말초 탈수초성 질환이 야기된다.
본 발명의 조직 보호 펩티드 및 펩티드 유사체를 사용하여 심장의 상태, 및 이에 대한 손상, 예컨대 심장 및/또는 관련 조직 (예를 들어, 심장막, 대동맥 및 기타 결합 혈관)을 수반하는 만성 또는 급성 병리적 사건, 예컨대 허혈-재관류 손상; 울혈성 심부전증; 심장 마비; 심근 경색증; 아테롬성 동맥경화증, 승모판 누출, 심방조동, 약물 (예를 들어, 독소루비신, 헤르셉틴, 티오리다진 및 시사프라이드)과 같은 화합물에 의해 야기된 심독성; 기생충 감염 (박테리아, 진균, 리케차, 및 바이러스, 예를 들어 매독, 만성 크루스 파동편모충 감염)으로 인한 심장 손상; 전격 심장 아밀로이드증; 심장 수술; 심장 이식; 혈관성형술, 복강경 수술, 외상성 심장 손상 (예를 들어, 관통 또는 심장 둔상, 및 대동맥 판막 파열), 흉부 대동맥류의 수술 복구; 부신 대동맥류; 심근 경색증 또는 심부전증으로 인한 심인성 쇼크; 신경원성 쇼크 및 아나필락시스를 치료하거나 예방할 수 있다. 본 발명의 조직 보호 펩티드 및 펩티드 유사체는 또한 심장 질환, 예컨대 심부전증의 위험이 있는 개인 (즉, 심장이 대사 조직에 의해 요구되는 속도로 혈액을 펌프질할 수 없거나, 또는 심장이 상승된 충만압에 의해서만 그렇게 할 수 있는 경우)을 치료하기 위해 사용될 수 있다. 상기 위험이 있는 환자는 심근 경색증, 관상 동맥 질환, 심근염, 화학요법, 심근병증, 고혈압, 판막성 심질환 (가장 빈번하게는 승모판 폐쇄부전증 및 대동맥 협착증) 및 독소-유도된 심근병증 (예를 들어, 에탄올, 코카인 등) 등을 갖거나 이의 위험을 갖는 환자를 포함할 것이다.
본 발명의 조직 보호 펩티드 및 펩티드 유사체를 사용하여 눈, 예를 들어 망막 조직의 상태, 및 이에 대한 손상을 치료하거나 예방할 수 있다. 이러한 장애의 예로는, 이들로 한정되지는 않지만, 망막 허혈, 황반 변성, 망막 박리, 망막 색소변성증, 동맥경화성 망막증, 고혈압성 망막증, 망막 동맥 차단, 망막 정맥 차단, 망막 부종, 저혈압, 및 당뇨병성 망막증을 들 수 있다.
또다른 실시양태에서, 본 발명의 조직 보호 펩티드 및 펩티드 유사체, 및 본 발명의 원리를 이용하여 독성제에 대한 노출로부터 발생하는 손상, 즉 반응성 조직에 대한 방사선 또는 화학적 손상을 예방하거나 치료할 수 있다. 본 발명의 한 실시양태에서 상기 언급한 펩티드는 독성제에 대한 신체 반응의 매개인자를 조절하기 위한, 바람직하게는 이러한 조절제의 활성을 저해 또는 억제하기 위한 치료제로서 유용하다. 추가로, 상기 언급한 펩티드는 독성제에 대한 노출의 손상, 영향 또는 증상을 치료, 예방, 개선 또는 관리하기 위한 치료제로서 유용하다. 상기 펩티드는 다양한 독성제, 예컨대 생물학적, 화학적 또는 방사선 작용제에 대한 노출을 치료하는데 사용될 수 있다.
이들 펩티드는 생물학적 작용제, 예컨대 프리온, 바이러스, 미생물 (박테리아 및 진균), 및 일부 단세포 및 다세포 진핵생물 (즉, 기생충), 예컨대 이들로 한정되지는 않지만, 섹션 4.2 (viii)에 상기 열거된 생물학적 독소로 인한 손상, 영향 또는 증상을 치료하는데 사용될 수 있다. 추가로 본 발명의 펩티드는 화학적 작용제로 인한 손상, 영향 또는 증상을 예방, 치료, 개선, 또는 관리하는데 사용될 수 있다. 이러한 작용제로는, 이들로 한정되지는 않지만, 혈액 작용제, 블리스터 작용제, 신경 작용제, 폐 작용제, 및 무능화 작용제가 있다. 추가로, 본 발명의 펩티드는 산업용 화학물질, 예컨대 이들로 한정되지는 않지만, 섹션 4.2 (x)에 열거된 것에 대한 독성 노출로 인한 손상, 영향 또는 증상을 예방, 치료, 개선 또는 관리하는데 사용될 수 있다. 방사선 작용제에 대한 노출로 인한 손상, 영향 또는 증상은 본 발명의 펩티드를 이용하여 예방, 치료, 또는 관리 가능하다. 상기 펩티드는 알파, 베타 또는 감마 방사선을 포함하는, 보다 특히 이들로 한정되지는 않지만, 137Cs, 60Co, 241Am, 252Cf, 192Ir, 238Pu, 90Sr, 226Ra, 91Sr, 92Sr, 95Zr, 99Mo, 106Ru, 131Sb, 132Te, 139Te, 140Ba, 141La, 144Ce, 233U, 235U, 238U, 228P, 229P, 230P, 231P, 232P, 233P, 234P, 235P, 236P, 237P, 238P, 239P, 240P, 241P, 242P, 243P, 244P, 245P, 246P, 247P, 및 131I를 포함할 수 있는 방사선활성 작용제로 인한 손상, 영향 또는 증상을 예방, 치료, 개선, 또는 관리할 수 있다. 추가로, 당업자는 상기 펩티드가 또한 이들 독성제의 누적 또는 상승작용 사용 (즉, 희생자가 생물학적 작용제에 더욱 민감하도록, 생물학적 작용제를 분산시키기 전에 방사선활성 작용제를 사용함, 희생자가 피신처 또는 도움을 효과적으로 구하는 것을 방지하기 위해 신경 작용제와 함께 발포제를 투여함, 치유 과정을 억제하거나 복잡하게 만들기 위해 탄환 또는 파편을 생물학적 작용제 또는 방사선활성 작용제로 오염시킴 등)으로 인한 손상, 영향 또는 증상을 예방, 조정, 치료 또는 개선하는데 사용될 수 있음을 인식할 것이다. 바람직하게는, 본 발명의 펩티드는 몇몇 상이한 유형의 세포, 기관, 또는 조직, 예를 들면 하기 중추 신경계, 말초 신경계, 안구, 심혈관, 심폐, 호흡기, 신장, 비뇨기, 생식기, 근골격, 피부, 결합 조직, 위장, 조혈, 내분비, 및 대사 중 두 가지 이상에 대한 독성 효과를 치료, 조정, 개선 또는 예방할 수 있을 것이다. 추가로, 본 발명의 펩티드는 동일한 부류내에서 한 가지가 넘는 독성제 (즉, 화학적, 생물학적 또는 방사선활성 작용제 중 한 가지가 넘는 유형에 대해 - 예를 들면 발포 및 신경 작용제에 대해 예방적임) 또는 상이한 부류의 독성제 (즉, 방사선활성 작용제 및 화학적 작용제에 대한 노출의 치료제)에 대한 치료제 또는 예방제로서 유효할 것이다. 본 발명의 조직 보호 펩티드 및 펩티드 유사체의 추가의 유용성은 화학 요법제의 방사선 노출의 결과로서의 중독, 예컨대 신경독 중독 (예를 들어, 도모산 조개 중독), 독소 (에탄올, 코카인 등); 뉴롤라디리즘(neurolathyrism); 괌(Guam) 질환; 근위축성 측삭 경화증; 및 파킨슨 질환의 치료에 있다.
상기 언급한 바와 같이, 본 발명은 또한 상기 기재한 바와 같은 조직 보호 펩티드의 말초 투여에 의하여 포유동물에서의 반응성 세포, 조직 및 기관의 조직 기능을 강화시키는데 사용하기 위한 본 발명의 조직 보호 펩티드 및 펩티드 유사체에 관한 것이다. 이 방법을 이용하여 다양한 질환 및 상태를 치료할 수 있다. 예를 들어, 이 방법은 심지어 임의의 상태 또는 질환의 부재하에서도 흥분성 조직에서의 기능을 강화시켜 인지 기능의 상승을 야기하는데 유용하다. 또한, 조직 보호 사이토킨은 상처 치유의 질을 개선하고, 치유에 요구되는 시간을 감소시키고, 치유된 조직의 질을 개선하며, 상처로부터 발생하는 유착의 발생률을 감소시키는데 유용하다. 2004년 9월 29일에 출원되고 WO 2005/032467로서 공개된 PCT/US2004/031789를 참조한다. 추가로, 본 발명의 조직 보호 펩티드는 화학적 작용제, 예컨대 블리스터 또는 발포 작용제 또는 산업용 화학물질에 의해 유도된 피부 상의 병변 또는 호흡 경로를 따른 병변을 치료, 예방 또는 관리하는데 유용할 수 있다.
본 발명의 상기 용도는 하기에 더 상세히 기술되어 있고, 인간 및 비-인간 포유동물 모두에서의 습득 및 훈련의 강화를 포함한다.
또다른 실시양태에서, 본 발명의 조직 보호 펩티드 및 펩티드 유사체는 일반적으로 중추 신경계, 말초 신경계, 위장/소화계, 비뇨생식계, 부신, 부인과, 두경부, 혈액학/혈액, 근골격/연질 조직, 호흡기, 및 유방의 다양한 암 또는 신생물성 장애의 예방, 치료적 처치, 예방적 처치 또는 관리에 유용할 수 있다. 용도의 예로는 이들로 한정되지는 않지만, 섹션 4.2(ix) 및 (xxv)에 열거된 암 또는 신생물 장애로부터 발생하는 손상에 대한 보호 및 이의 복구가 있다. 추가로 본 발명의 펩티드는 신생물 또는 암, 예컨대 이들로 한정되지는 않지만 섹션 4.2 (xxviii)에 상기 열거된 것들과 연관된 다양한 증후군의 예방, 치료적 처치, 예방적 처치 또는 관리에 사용될 수 있다. 상기 펩티드는 본 발명의 방법에 따라 상기 언급한 증후군을 다루는데 사용될 수 있다. 예를 들면, 상기 펩티드는, 질환의 신생물 측면의 개시를 지연시키거나, 증후군과 관련된 신생물 성장의 수를 감소시키거나, 일반적으로 이들 상태에 걸린 환자의 삶의 질 또는 장수를 증진시킴으로써, 유전성 증후군, 예컨대 리 프라우메니, 유전성 비용종성 결장직장암, 가족성 선종성 폴립증, 및 폰 히펠-린다우(Von Hippel-Lindau) 증후군을 다루기 위해 투여될 수 있다. 상기 펩티드는 또한 증후군을 예방하거나 증후군의 중증도를 감소시킨다는 희망으로, 특정 치료, 화학요법 또는 방사선 요법과 관련된 증후군, 신생물성 장애 또는 암, 예컨대 안드로겐 결핍 증후군, 골수이형성 증후군 또는 기면 증후군 관련 요법을 다루기 위해 예방적으로 투여될 수 있다.
추가로, 상기 펩티드는 악액질 및 악액질 관련 질환을 치료 또는 예방하는데 사용될 수 있다. 이러한 질환으로는 이들로 한정되지는 않지만, 암 악액질, 식욕부진, 무력증, 빈혈, 결핵, AIDS, 울혈성 심부전증, 신부전증, 간 부전증, 만성 폐쇄성 폐질환, 기종, 근위축증, 당뇨병, 및 내독소증이 있다.
본 발명의 조직 보호 펩티드 및 펩티드 유사체를 중추 신경계에 사용하여 치료가능하거나 예방가능한 상태 및 질환의 예로는, 이들로 한정되지는 않지만, 기분 장애, 불안 장애, 우울증, 자폐증, 주의력 결핍 과잉행동 장애, 및 인지 기능이상을 들 수 있다. 이들 상태는 뉴런 기능의 강화로부터 이익을 얻는다. 본 발명의 교시에 따라 치료가능한 기타 장애로서 수면 장애, 예를 들어 수면 무호흡증 및 여행 관련 장애; 지주막하 및 동맥류 출혈, 저혈압 쇼크, 진탄성 손상, 패혈 쇼크, 아나필락시스성 쇼크, 및 다양한 뇌염 및 수막염, 예를 들어 결합 조직 질환 관련 뇌염, 예컨대 루푸스의 후유증을 들 수 있다. 기타 용도로서 신경독에 의한 중독, 예컨대 도모이산 조개 중독, 뉴롤라디리즘, 및 괌 질환, 근위축성 측삭 경화증, 파킨슨 질환; 색전성 또는 허혈성 손상에 대한 수술 후 치료; 전뇌 조사; 겸상 적혈구 빈혈; 및 자간증의 예방 또는 이로부터의 보호를 들 수 있다.
본 발명의 조직 보호 펩티드 및 펩티드 유사체를 사용하여 치료가능하거나 예방가능한 상태의 추가의 군은 뉴런 손상 및 사망으로 대표되는 다양한 신경 질환의 원인인, 유전성 또는 후천성의 미토콘드리아 기능이상을 포함한다. 예를 들어, 라이병 (아급성 괴사성 뇌병증)은 뉴런 탈락으로 인한 진행성 시각 상실 및 뇌병증, 및 근질환으로 특징지어진다. 이들 경우, 불완전한 미토콘드리아 대사는 흥분성 세포의 대사에 연료를 공급하기에 충분한 고 에너지 기질을 공급하지 못한다. 조직 보호 펩티드 또는 펩티드 유사체는 다양한 미토콘드리아 질환에 있어서 약화되는 기능을 최적화한다. 상기 언급한 바와 같이, 저산소증 상태는 흥분성 조직에 불리한 영향을 미친다. 흥분성 조직으로는, 이들로 한정되지는 않지만, 뉴런 조직, 예컨대 말초 신경계 (귀 및 망막) 및 중추 신경계 (뇌 및 척수)의 조직; 심혈관 조직, 예컨대 심장 및 관련 신경의 세포; 및 샘 조직, 예컨대 세포-대-세포 갭 결합을 따라 T-유형 칼슘 채널이 인슐린 분비에 참여하는 췌장이 있다. 흥분성 조직의 예시적인 목록으로는, 이들로 한정되지는 않지만, 신경, 골격근, 평활근, 심장 근육, 자궁, 중추 신경계, 척수, 뇌, 망막, 후각계, 및 청각계를 포함하는 기관 및 조직이 있다. 상기 기재한 상태에 추가하여, 본 발명의 조직 보호 펩티드 및 펩티드 유사체는 흡입 중독, 예컨대 일산화탄소 및 연기 흡입, 중증 천식, 성인 호흡 곤란 증후군, 및 숨막힘 및 익수의 치료에 유용하다. 저산소증 상태를 발생시키거나 또는 다른 방법에 의해 반응성 조직, 예컨대 흥분성 조직의 손상을 유도하는 추가의 상태로서 인슐린의 부적절한 투여에서, 또는 인슐린을 생성하는 신생물 (인슐린종)에 의해 발생할 수 있는 저혈당을 들 수 있다.
흥분성 조직 손상으로부터 유래하는 것으로 기술되는 다양한 신경심리학적 장애는 본 발명의 조직 보호 펩티드 및 펩티드 유사체의 이용으로 치료가능하다. 뉴런 손상이 수반되고, 본 발명에 의해 그에 치료 또는 예방이 제공되는 만성 장애로서 중추 신경계 및/또는 말초 신경계와 관련된 장애, 예컨대 노년기 인지 기능 상실 및 노인 치매, 만성 발작 장애, 알츠하이머 질환, 파킨슨 질환, 치매, 기억 상실, 근위축성 측삭 경화증, 다발성 경화증, 결절성 경화증, 윌슨(Wilson)병, 대뇌 및 진행성 상핵 마비, 괌 질환, 루이체 치매, 프리온 질환, 예컨대 해면상 뇌병증, 예를 들어 크로이츠펠트-야콥병, 헌팅턴병, 근긴장성 이영양증, 프리드리히(Freidrich) 운동실조증 및 기타 운동실조증, 뿐만 아니라 질 드 라 투렛 증후군(Gilles de la Tourette's syndrome), 발작 장애, 예컨대 간질 및 만성 발작 장애, 뇌졸중, 뇌 또는 척수 외상, AIDS 치매, 알콜 중독, 자폐증, 망막 허혈, 녹내장, 자가면역 기능 장애, 예컨대 고혈압 및 수면 장애, 및 신경정신 장애, 예컨대 이들로 한정되지는 않지만, 정신분열증, 정신분열정동 장애, 주의력 결핍 장애, 기분저하 장애, 주요 우울 장애, 조증, 강박 장애, 정신활성 약물 사용 장애, 불안, 공황 장애, 뿐만 아니라 단극성 및 양극성 정동 장애를 들 수 있다. 추가의 신경정신 및 신경변성 장애로서, 예를 들어 문헌 [American Psychiatric Association's Diagnostic and Statistical Manual of Mental Disorders (DSM)]에 제시된 것을 들 수 있다.
본 발명의 조직 보호 펩티드 및 펩티드 유사체를 사용하여 치료가능하거나 예방가능한 상태의 추가의 군은 신장 질환, 예컨대 급성 및 만성 신부전증을 포함한다. 신장으로의 혈액 공급은 혈류로 침입하는 감염으로부터의 쇼크 (패혈증), 내부 또는 외부 출혈, 중증 설사 또는 화상의 결과로서 신체로부터 체액 손실, 수혈에 대한 반응, 심장 마비 또는 부정맥, 수술 외상 및 신장 이식을 비롯한 여러 원인으로 인하여 차단될 수 있다. 상기 상태로부터 발생하는, 신장으로의 혈액의 감소된 흐름은 급성 신부전증의 발생을 야기할 만큼 충분히 긴 기간 동안 혈류를 위험하게 낮은 수준까지 감소시킬 수 있다. 부진한 혈류는 또한 신장에 있어서 괴사, 또는 조직사를 야기하여 신장 관상 세포를 손상시킨다. 신부전증은 또한 질환 (간질성 및 당뇨병성 신증후군), 감염, 손상 (CPB-유도된), 독소 (조영제-유도된, 화학요법-유도된, 시클로스포린), 자가면역성 염증 (예를 들어, 루푸스, 적혈구 증가증 등)으로부터 발생할 수 있다. 본 발명의 조직 보호 펩티드 및 펩티드 유사체는 상기 손상의 복구 또는 예방을 보조하여 급성 신부전증을 개선하는데 도움을 준다. 추가로, 본 발명의 펩티드는 요로의 질환 또는 장애, 예컨대 이들로 한정되지는 않지만, 요로 감염, 과민성 방광, 및 방광에 대한 외상 또는 방사선 손상을 치료, 예방 또는 개선하는데 사용될 수 있다.
하기 표는 전술한 조직 보호 펩티드에 의해 치료가능한 다양한 상태 및 질환으로서의 추가의 예시적, 비제한적 징후를 열거한다.
<표 I>
조직 보호 펩티드 및 펩티드 유사체에 의해 치료가능한 질환 및 장애
상기 언급한 바와 같이, 이들 질환, 장애 또는 상태는 본 발명의 조직 보호 펩티드 및 펩티드 유사체에 의해 제공되는 이점의 범위를 단지 예시하는 것이다. 따라서, 본 발명은 일반적으로 물리적 외상 또는 인간 질환의 결과의 예방, 치료적 또는 예방적 처치를 제공한다. CNS 및/또는 말초 신경계의 질환, 장애 또는 상태에 대한 예방 또는 치료적 또는 예방적 처치가 고려된다. 정신과적 요소를 갖는 질환, 장애 또는 상태의 예방 또는 치료적 또는 예방적 처치가 제공된다. 안구, 심혈관, 심폐, 호흡기, 신장, 비뇨기, 생식기, 위장, 내분비, 또는 대사 요소를 갖는 것을 포함하나 이에 국한되지 않는 질환, 장애 또는 상태의 예방 또는 치료적 또는 예방적 처치가 제공된다. 상기 펩티드는 조직 손상 관련 질환 또는 장애, 뿐만 아니라 하나 이상의 기관 또는 조직에서, 바람직하게는 적어도 두 가지에서, 예컨대 이들로 한정되지는 않지만, 뇌, 척수, 결합 조직, 피부, 위장관, 생식기 기관, 간, 심장, 폐, 신장, 요로, 췌장, 눈 및 전립선에서 그의 손상, 영향 또는 증상의 예방, 치료적 처치, 예방적 처치 또는 관리에 유용할 수 있다.
특정 실시양태에서, 본 발명의 방법은 본 발명의 펩티드 또는 특징 징후를 제외할 수 있다. 예를 들면, 본 발명의 방법에서 구조적 모티프 C에 따른 펩티드는 WO 2006/119767 및 WO 2007/071248에 개시된 징후, 예컨대 수술후 신경 손상; 외상성 신경 손상; 척수 손상, 신경 섬유의 손상된 수초 형성; 허혈후 손상; 뇌졸중; 파킨슨 질환; 알츠하이머 질환; 헌팅턴 질환; 정신분열증, 치매; 다발성 경화증, 다중경색 치매; 진성 당뇨병 관련 신경 변성; 신경-근육 변성, 생체 시계 또는 신경-근육 결합에 영향을 미치는 장애; 장기 이식; 유전성 또는 외상성 위축성 근육 장애; 생식선, 췌장, 신장, 심장, 간 및 장의 퇴행성 상태; 제I형 또는 제II형 진성 당뇨병; 신장증; 정신병; 신경증 장애; 인격 장애; 성적 도착증 및 장애; 정신 지체; 신경계 및 감각 기관에서의 질환; 인지 이상; 중추 신경계의 염증성 질환; 뇌 변성; 단기 또는 장기 기억의 자극; 추체외로 질환 및 비정상적 운동 장애; 운동 뉴런 질환; 척수의 질환; 자율 신경계의 장애, 말초 신경계의 질환; 신경병증; 눈의 다중 구조체에서 발병한 장애; 귀의 질환 및 유양 돌기; 신생아의 기관 및 연질 조직의 이상; 산통 및 분만시 마취제 또는 다른 진정제 투여의 합병증; 피부의 질환 및 손상; 신경 및 척수에 대한 손상; 약물 중독; 의학적 및 생물학적 물질; 대사성 장애; 내분비선의 장애; 퓨린 및 피리미딘 대사의 장애; 골 장애; 신생물; 암; 뇌의 바이러스 감염; 길랑 바레 증후군; 동통 증후군; 자폐증 및 학습 능력의 자극에서 제외될 수 있다. 또한, 예를 들면, 본 발명의 방법에서 구조적 모티프 D에 따른 펩티드는 미국 특허 제5,571,787호, 제5,700,909호, 제5,696,080호, 제5,714,459호, 제6,590,074호, 제6559,124호, 제6,271,196호, 제6,268,347호, 및 제6,849,602호에 개시된 징후, 예컨대 신경종 (절단, 신경 트랜잭션), 신경 압박 (포착 신경병증, 또는 종양 압박), 신경 외상 (압좌, 신장, 또는 불완전한 절단)으로 인한 신경병증 동통; 진성 당뇨병; 조사, 허혈, 혈관염, 소아마비후 증후군, 알코올, 아밀로이드, 독소, HIV, 갑상선기능저하증, 요독증, 비타민 결핍, 화학요법, ddC (잘시타빈), 파브리(Fabry) 질환, 압박 (디스크, 종양, 반흔 조직), 신결절전 발인손상(root avulsion), 염증 (포진후 신경통), 척수 타박상, 척수 종양, 척수 반측절제술, 및 경색, 뇌간, 시상 또는 피질의 종양 또는 외상; 및 탈수초성 질환, 예컨대 다발성 경화증, 급성 파종성 백질뇌염, 진행성 다소성 백질뇌염, 이염성 백질이영양증, 및 부신성 백질이영양증에서 제외될 수 있다. 또다른 예의 경우, 본 발명의 방법에서 구조적 모티프 E에 따른 펩티드는 미국 특허 제7,259,146호 및 미국 특허 공보 제20030130197호에 개시된 징후, 예컨대 급성 신경변성 장애: 뇌 허혈 또는 경색, 예컨대 색전정 폐색 및 혈전성 폐색; 급성 허혈후 재관류; 주산기 저산소성-허혈성 손상; 심장 마비; 두개내 출혈; 두개내 및 척추내 병변; 및 편타성 진전 유아 증후군; 만성 신경변성 장애: 알츠하이머 질환, 피크(Pick) 질환, 미만성 루이체 질환, 진행성 상핵 마비, 다발계통 변성, 만성 간질 상태, 운동 뉴런 질환, 프리온 질환, 말초 질환과 연관된 신경학 및 정신의학 소견, 예컨대 EPO 결핍, 혈액 손실, 신부전증, 말기 신장 질환, 신장 이식, 및 빈혈과 연관된 다른 질환, 예컨대 혈액학 및 비-혈액학 악성종양/종양, 화학요법 및 다른 약물과 연관된 합병증, 혈액학 장애, 염증성 및 감염성 장애, 만성 전신성 자가면역성 질환, 헤노 쇤라인 자반병, 용혈성 요독증 증후군, 신경계의 화학적, 독성, 감염성, 및 방사선 손상, 및 뇌병증; 신경총병증; 신경병증; 샤르코-마리-투스(Charcot-Marie-Tooth) 질환; 프리드리히 운동실조증; 이염성 백질이영양증; 레프섬(Refsum) 질환; 아드레노미엘로신경병증; 모세관 확장성 운동실조증; 데제린-소타스(Djerine-Sottas) 신경병증; 램버트-이튼 증후군; 및 두개 신경의 장애에서 제외될 수 있다. 추가의 예로, 본 발명의 방법에서 구조적 모티프 F에 따른 펩티드는 WO/2007/052154에 개시된 징후, 예컨대 면역-매개 염증; 자가면역성 질환, 예컨대 하시모토(Hashimoto) 갑상선염, 인슐린 의존성 진성 당뇨병, 전신성 홍반성 루푸스; 탈수초성 질환, 예컨대 다발성 경화증, 횡단척수염, 길랑-바레 증후군, 및 진행성 다소성 백질뇌병증 및 오르가노포스페이트 노출로부터 발생하는 탈수초; 관절염; 급성 뇌혈관 손상; 급성 척수 손상; 급성 뇌 손상; 급성 심혈관 손상; 뇌졸중; 외상성 손상; 이식거부; 및 이식편 거부에서 제외될 수 있다.
C. 질환, 장애 또는 상태의 손상, 영향, 또는 증상의 예방, 치료, 개선, 또는 관리
본 발명의 추가의 실시양태에서, 본 발명의 치료 방법은 상기 언급한 질환 및 장애의 손상, 영향, 또는 증상의 예방, 치료, 개선, 또는 관리에 유용하다. 특히, 현행 치료 방법을 이용하여, 증상, 예컨대 이들로 한정되지는 않지만, 악액질, 발암, 불임, 백내장 형성, 방사선피부염, 베타 화상, 감마 화상, 세포 손실 (특히 골수, 소화관 세포), 조혈, 위장, 중추 신경계, 심혈관, 피부 및/또는 생식계에 대한 손상, 급성 방사선 증후군 (오심감, 구토, 일반병 및 피로, 면역계 우울증, 모발 손실, 제어불가능한 출혈 (입, 피부밑, 신장), 대량 설사, 정신 착란, 혼수상태 및 사망), 만성 방사선 증후군, 피부 방사선 증후군 (염증, 홍반, 건성 또는 습성 표피탈락, 모발 손실, 수포, 발적, 궤양, 피지선 및 한선에 대한 손상, 위축증, 섬유증, 감소된 또는 증가된 피부 색소침착, 및 괴사), 두통, 현기증, 오심, 구토, 점막 자극, 호흡곤란, 손상된 의식, 혼수상태, 경련, 부정빈맥 및 부정서맥, 저혈압, 심혈관 붕괴, 무청색증, 서맥, 축동, 과도한 타액분비, 설사, 비자발적 배뇨, 근육 연축, 초기 탈분극 이완성 마비, 극파 방전 및 경련, 중간형 증후군, 신경독성 에스테라제 억제, 오르가노포스페이트-유도된 지연형 신경병증, 홍반, 부종, 괴사 및 소포, 흑피증, 기관기관지염, 기관지연축, 기관지 폐쇄, 출혈성 폐 부종, 호흡 부전증, 박테리아 폐렴, 눈 홍반, 눈물 흘림, 눈의 불편감, 눈의 중증 동통, 안검경련, 홍채염, 실명, 골수 저해, 루이사이트 쇼크, 간 괴사, 저관류에 대해 속발성인 신부전증, 작열감 (눈, 비인두, 구인두), 누액 과다, 콧물 흘림, 기침 목쉼, 호흡곤란, 연하통, 결막염, 각막 손상, 비강-오로판기알(naso-orophangyal) 손상/부종, 성문 구조의 염증, 분비물 및/또는 후두경련으로 인한 호흡 장애, 급성 호흡 증후군, 방향감각 상실, 거동 변형, 및 반응성 기도 기능이상 증후군을 다룰 수 있다.
상기 언급된 바와 같이, 이들 조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상은 단지 본 발명의 방법에 사용되는 펩티드에 의해 다루어질 수 있는 예시적인 장애의 범위이다. 따라서, 본 발명은 일반적으로 조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상의 예방, 치료적 또는 예방적 처치를 제공한다.
조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상은 유효량의 본 발명의 펩티드의 투여에 의해 치료 또는 예방될 수 있다. 특정 실시양태에서, 본 발명은 본원에 기재된 질환 또는 장애를 가진 대상체에게 상기 질환 또는 장애의 치료 또는 예방에 효과적인 양의 본 발명의 펩티드를 투여하는 단계를 포함하는, 상기 질환 또는 장애의 치료 또는 예방 방법을 제공한다. 한 실시양태에서, 유효량의 하나 이상의 본 발명의 펩티드, 또는 그의 제약상 허용되는 염을 포함하는 조성물을 투여한다.
D. 누적 또는 상승작용 효과를 위한 다른 치료제와 결합된 치료.
특정 실시양태에서, 본 발명은 유효량의 펩티드 및 또다른 적합한 치료제 (각각은 의약에 적합한 섭생에 따라 투여됨)를 이것이 필요한 환자에게 투여하는 것을 포함하는, 조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상의 치료, 조정, 개선 또는 예방 방법을 포괄한다. 이것은 펩티드 및 치료제의 효과의 부가, 상승작용 또는 상쇄 (치료제의 부작용을 중화시킴) 이익을 달성하기 위해 수행될 수 있다. 이것은 펩티드 및 적합한 치료제의 병행, 실질적으로 동시, 또는 비-병행 투여를 포함한다. 펩티드 및 적합한 치료제의 비-병행 투여는 펩티드 및 적합한 치료제의 순차, 교차, 및 단기 대 장기 투여를 포함한다. 또한, 펩티드 및 적합한 치료제는 동일 또는 개별 제약 조성물로 투여될 수 있고, 개별 투여되는 경우, 이들은 동일한 투여 경로 또는 상이한 경로를 통해 투여될 수 있다. 적합한 치료 방법 및 치료제에는, 이들로 한정되지는 않지만, 카르바메이트 (피리도스티그민, 파이소스티그민, 아미노스티그민, 네오스티그민, 시노스티그민, 에파스티그민(Epastigmine), 모밤(Mobam), 데카르보푸란), 항콜린작용제 (트리헥실페니딜, 베낙티진, 비페리덴(Biperidene), 스코폴아민(Scopolamine), 아프로펜, 아트로핀, 히요신, 아디페닌, 카라미펜(Caramiphen), 펜트메토늄, 메카밀아민(Mecamylamine), 트리헥실페니딜(Trihexyphenidyle)) PANPAL, 아미노페놀 (에세롤린), 유기인산염 (TEPP, 파락손(Paraxon), 에틸-4-니트로페닐포스페이트), 타크린, 7-MEO-TA, 후페르진 A, 콜린에스테라제 (BuChE, AChE, 트리에스테라제, 파라옥소나제), 옥심/재생제 (HI-6, PAM, 오비독심(Obidoxime), 트리메독심(Trimedoxime), 메톡심(Methoxime), Hlo-7, BI-6, K048, K033, 프랄리독심 클로라이드 (2-PAM Cl), P2S, TMB4, 2-PAMI), 수라민(Suramine), 벤조디아제핀, 투보쿠린, 메만틴(Memantine), 프로시클리딘(Procyclidine), 니모디핀(Nimodipin), 클로니딘(Clonidine), 프랄리독심, 디아제팜, 엔케팔린스, 페닐메틸술포닐 플루오라이드, 중탄산나트륨, 비타민 E 유사체 (α-토코페롤 숙시네이트, γ-토코트리에놀), 수퍼옥시드 디스뮤타제/카탈라제 모방체 (EUK189), 셀레늄, 벤질 스티릴 술폰, 절단형(truncated) 플라젤린, 스타틴, 게니스테인, 갈란타민, 저체온법, 5-안드로스텐디올, CpG-올리고데옥시뉴클레오티드, 항미생물제, 줄기 세포 이식, 아미포스틴, 템폴(Tempol), 이소플라본, 벤질술폰 유사체, GM-CSF, G-CSF, 요오드화칼륨, 수산화알루미늄, 프루시안 블루(Prussian blue), 킬레이트제 (디에틸렌트리아민펜타아세테이트 (Ca-DTPA), 아연 디에틸렌트리아민펜타아세테이트 (Zn-DTPA)), 케라틴 형성세포 성장 인자, 장 펩티드 호르몬, 베타 글루칸, 옥트레오티드, 펜톡시필린, 안지오텐신 전환 효소 억제제, 안지오텐신 II 수용체 차단제, 메테모글로빈 구성인자 (아질산아밀, 아질산나트륨), 나트륨 티오술페이트, 코발트 화합물 (히드록시코발라민 (비타민 B12a), 톡소이드, 항독소, 백신, 수동 항체, 화학요법제, 예컨대 이들로 한정되지는 않지만, 메토트렉세이트, 탁솔, 머캅토퓨린, 티오구아닌, 히드록시우레아, 시타라빈, 시클로포스파미드, 이포스파미드, 니트로소우레아, 시스플라틴, 카르보플라틴, 미토마이신, 다카르바진, 프로카르비진, 에토포시드, 캄파테신, 블레오마이신, 독소루비신, 이다루비신, 다우노루비신, 닥티노마이신, 플리카마이신, 미톡산트론, 아스파라기나제, 빈블라스틴, 빈크리스틴, 비노렐빈, 파클리탁셀 및 도세탁셀; 방사선: γ-방사선; 알킬화제; 질소 머스타드: 시클로포스파미드, 이포스파미드, 트로포스파미드, 클로람부실(Chlorambucil); 니트로소우레아: 카르무스틴 (BCNU), 로무스틴(Lomustine) (CCNU), 알킬술포네이트 부술판, 트레오술판(Treosulfan); 트리아젠(Triazene): 다카르바진(Dacarbazine); 백금 함유 화합물: 시스플라틴, 카르보플라틴, 식물 알칼로이드; 빈카(Vinca) 알칼로이드: 빈크리스틴, 빈블라스틴, 빈데신, 비노렐빈; 탁소이드(Taxoid): 파클리탁셀, 도세탁솔(Docetaxol); DNA 토포이소머라제 억제제 에피포도필린(Epipodophyllin): 에토포시드, 테니포시드(Teniposide), 토포테칸(Topotecan), 9-아미노캄프토테신 이리노테칸 (캄프토.(Campto.)RTM.), 크리스나톨; 미토마이신(Mytomycin): 미토마이신 C, 미토마이신 C; 항대사물질, 항엽산: DHFR 억제제: 메토트렉세이트, 트리메트렉세이트(Trimetrexate); IMP 데히드로게나제 억제제: 미코페놀산, 티아조푸린(Tiazofurin), 리바비린(Ribavirin) EICAR; 리보뉴클레오티드 리덕타제 억제제: 히드록시우레아; 데페록사민; 피리미딘 유사체: 우라실 유사체, 5-플루오로우라실, 플록수리딘(Floxuridine), 독시플루리딘(Doxifluridine), 라티트렉세드(Ratitrexed); 사이토신(Cytosine) 유사체: 시타라빈 (ara C), 사이토신 아라비노시드 플루다라빈; 퓨린 유사체: 머캅토퓨린, 티오구아닌; 호르몬 요법; 수용체 길항제: 항에스트로겐제, 타목시펜(Tamoxifen), 랄록시펜(Raloxifene), 메게스트롤; LHRH 효능제: 고세렐린, 류프롤리드(Leuprolide) 아세테이트; 항안드로겐제: 플루타미드, 비칼루타미드; 레티노이드(Retinoid)/델토이드(Deltoid) 비타민 D3 유사체: EB 1089, CB 1093, KH 1060; 광역학적 요법: 베르토포르핀 (BPD-MA), 프탈로시아닌 광감작제, Pc4 데메톡시-히포크렐린 A (2BA-2-DMHA), 사이토킨: 인터페론-α, 인터페론-γ, 종양 괴사 인자; 이소프레닐화 억제제: 로바스타틴; 도파민작용성 신경독: 1-메틸-4-페닐피리디늄 이온; 세포 주기 억제제: 스타우로스포린; 악티노마이신(Actinomycin): 악티노마이신 D, 닥티노마이신(Dactinomycin); 블레오마이신(Bleomycin): 블레오마이신 A2, 블레오마이신 B2, 펩플로마이신(Peplomycin); 안트라사이클린(Anthracycline): 다우노루비신, 독소루비신 (아드리아마이신), 이다루비신(Idarubicin), 에피루비신(Epirubicin), 피라루비신(Pirarubicin), 조루비신(Zorubicin), 미톡산트론(Mitoxantrone); MDR 억제제: 베라파밀; Ca2 + ATPase 억제제: 타프시가르긴; TNF-a 억제제/탈리도미드 혈관신생 억제제 3-(3,4-디메톡시-페닐)-3-(1-옥소-1,3-디히드로-이소인돌-2-일)-프로피온아미드 (SelCID™), ImiD™, 레블리미드(Revlimid)™, 악티미드(Actimid)™가 포함된다. 본 발명의 또다른 측면에서, 본 발명에 따른 제약 조성물은 제제 중의 펩티드를 조직 보호 기능을 나타내는 하나 이상의 소분자와 함께 포함할 수 있다. 적합한 소분자에는, 이들로 한정되지는 않지만, 스테로이드 (예를 들어, 라자로이드 및 글루코코르티코이드), 항산화제 (예를 들어, 조효소 Q10, 알파 리포산 및 NADH), 항이화작용 효소 (예를 들어, 글루타티온 퍼옥시다제, 수퍼옥시드 디뮤타제, 카탈라제, 합성 촉매 스캐빈저, 및 또한 모방체), 인돌 유도체 (예를 들어, 인돌아민, 카르바졸 및 카르볼린), 질산 중성화제, 아데노신/아데노신 효능제, 식물성 화학물질 (플라보노이드), 허브 추출물 (은행나무 및 심황), 비타민 (비타민 A, E 및 C), 옥시다제 전자 받개 억제제 (예를 들어, 크산틴 옥시다제 전자 억제제), 미네랄 (예를 들어, 구리, 아연 및 마그네슘), 비-스테로이드성 소염 약물 (예를 들어, 아스피린, 나프록센 및 이부프로펜), 및 그의 조합물이 포함된다. 추가적으로 이러한 작용제로는, 이들로 한정되지는 않지만, 소염제 (예를 들어, 코르티코스테로이드, 프레드니손 및 히드로코르티손), 글루코코르티코이드, 스테로이드, 비-스테로이드성 소염 약물 (예를 들어, 아스피린, 이부프로펜, 디클로페낙 및 COX-2 억제제), 베타-효능제, 항콜린작용제 및 메틸 크산틴), 면역 조절제 (예를 들어, 유기 소분자, T 세포 수용체 조절제, 사이토킨 수용체 조절제, T-세포 고갈제, 사이토킨 길항제, 모노킨 길항제, 림프구 억제제 또는 항암제), 금 주사제, 술파살리진, 페니실라민, 항혈관신생제 (예를 들어, 안지오스타틴), TNF-α 길항제 (예를 들어, 항-TNFα 항체) 및 엔도스타틴), 답손, 프소랄렌 (예를 들어, 메톡살렌 및 트리옥살렌), 항말라리아제 (예를 들어, 히드록시클로로퀸), 항바이러스제, 항히스타민제 및 항생제 (예를 들어, 에리트로마이신 및 페니실린)은 본 발명의 제약 조성물과 함께 사용될 수 있다.
다른 실시양태에서, 조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상에 대한 본 발명의 치료, 조정, 개선 또는 예방 방법은 추가로 치료 방법, 예컨대 화학요법, 방사선 요법 (x-선 방사선, 고-에너지 메가볼트 (1 MeV 에너지 초과의 방사선), 전자 빔, 오르토전압 x-선 방사선, 감마-선 방출 방사성 동위원소 (라듐, 코발트 및 다른 원소의 방사성 동위원소)), 고압 챔버, 심장 우회기, 혈관형성술, 저체온법, 수술, 혈관형성술 등과 함께 펩티드를 투여하여, 펩티드 및 치료 방법의 효과의 부가적, 상승작용적 또는 상쇄적 (치료 방법의 부작용을 중화시킴) 이익을 달성할 수 있다. 그 예로서, 특정 실시양태에서, 펩티드는 화학요법 또는 방사선 요법과 병행하여 암 치료로서의 수술을 경험한 환자에게 투여될 수 있다. 또다른 특정 실시양태에서, 화학요법제 또는 방사선 요법은 펩티드 투여 전후에, 바람직하게는 적어도 1시간, 5시간, 12시간, 1일, 1주일, 1개월 전후에, 보다 바람직하게는 수 개월 (예를 들어, 3개월 이하) 전후에 투여된다. 추가적으로, 본 발명은 화학요법 또는 방사선 요법 (여기서, 상기 화학요법 또는 방사선 요법은 너무 독성이어서, 예를 들어 치료되는 환자에 대해 허용되지 않거나 또는 견딜 수 없는 부작용을 생성하는 것으로 입증된 바 있거나 입증될 수 있음)에 대한 대안으로서 펩티드를 사용하여 암 또는 신생물성 질환을 치료하는 방법을 제공한다. 별법으로, 본 발명은, 치료 방법의 독성 부작용을 예방 또는 개선하려는 노력에서 화학요법 또는 방사선을 이용하는 치료 이전에, 이러한 치료와 동시에 또는 이러한 치료 이후에 펩티드를 투여하는 치료 방법을 제공한다. 실시예 2에서 입증된 바와 같이, 본 발명의 방법에 따라 투여되는 펩티드는 공지된 시스-백금 화학요법의 부작용을 개선할 수 있다. 비록, 상기 예는 암 치료에 관련된 것이지만, 펩티드가 조직 손상 관련 질환 또는 장애, 및 그로부터 발생하는 손상, 영향 또는 증상, 예컨대 염증 및 독성제로의 노출에 대한 당업계의 다른 치료 방법과 연합으로 투여되어, 상승작용, 부가 또는 상쇄 결과를 달성할 수 있음을 이해한다.
E. 펩티드의 제제화 및 투여
한 실시양태에서, 본 발명의 방법은 펩티드를 포함하는 제약 조성물을 전신으로 투여하여, 표적 세포, 조직 또는 기관을 보호하거나 또는 치료할 수 있음을 제공한다. 상기 투여는 흡입을 통해 비경구적으로, 또는 점막관통으로, 예를 들어, 경구적으로, 구강으로, 비내로, 직장으로, 질내로, 설하로, 안구로, 점막하로 또는 경피적으로 이루어질 수 있다. 바람직하게는, 투여는, 예를 들어, 정맥내 또는 복막내 주사를 통한 비경구적인 것이고, 또한 이들로 한정되지는 않지만, 동맥내, 근육내, 진피내 및 피하 투여를 포함한다.
관류액의 사용, 기관으로의 주사, 또는 기타 국소 투여에 의한 것과 같은 기타 투여 경로에 있어서, 상기 기재된 바와 유사한 수준의 펩티드를 생성하는 제약 조성물이 제공될 것이다. 약 15 pM 내지 30 nM의 수준이 바람직하다.
본 발명의 제약 조성물은 치료 유효량의 화합물 및 제약상 허용되는 담체를 포함할 수 있다. 특정 실시양태에서, 용어 "제약상 허용되는"은 동물, 및 보다 구체적으로 인간에게 사용하기 위해, 연방 또는 주 정부의 관리 당국에 의해 승인되거나, 또는 미국 약전 또는 기타 일반적으로 인정되는 외국 약전에 열거된 것을 의미한다. 용어 "담체"는 치료제와 함께 투여되는 희석제, 보조제, 부형제 또는 비히클을 지칭한다. 상기 제약 담체는 멸균 액체, 예컨대 석유, 동물, 식물 또는 합성 기원의 것을 비롯한 오일, 예컨대 땅콩유, 대두유, 광유, 참깨유 등 및 물 중의 식염수 용액일 수 있다. 제약 조성물이 정맥내로 투여되는 경우에는 식염수 용액이 바람직한 담체이다. 또한, 식염수 용액 및 수성 덱스트로스 및 글리세롤 용액은 특히 주사가능한 용액제를 위한 액체 담체로서 사용될 수 있다. 적합한 제약 부형제로는 전분, 글루코스, 락토스, 수크로스, 젤라틴, 맥아, 쌀, 밀가루, 호분, 실리카겔, 나트륨 스테아레이트, 글리세롤 모노스테아레이트, 활석, 염화나트륨, 건조 탈지유, 글리세롤, 프로필렌 글리콜, 물, 에탄올 등이 포함된다. 조성물은, 바람직한 경우, 또한 부수적인 양의 습윤제 또는 유화제, 또는 pH 완충제도 함유할 수 있다. 상기 조성물은 용액제, 현탁액제, 에멀젼제, 정제, 환제, 캡슐제, 산제, 서방형 제제 등의 형태를 취할 수 있다. 조성물은 통상의 결합제 및 담체, 예컨대 트리글리세리드와 함께 좌제로서 제제화될 수 있다. 본 발명의 화합물은 중성 또는 염 형태로서 제제화될 수 있다. 제약상 허용되는 염은 유리 아미노기와 형성된 염, 예컨대 염산, 인산, 아세트산, 옥살산, 타르타르산 등으로부터 유래된 염, 및 유리 카르복실기와 형성된 염, 예컨대 나트륨, 칼륨, 암모늄, 칼슘, 수산화제2철, 이소프로필아민, 트리에틸아민, 2-에틸아미노 에탄올, 히스티딘, 프로카인 등으로부터 유래된 염을 포함한다. 적합한 제약 담체의 예는 그 전문이 본원에 참조로 포함되는 문헌 ["Remington's Pharmaceutical Sciences" by E.W. Martin]에 기재되어 있다. 상기 조성물은 치료 유효량의 화합물을, 바람직하게는 정제된 형태로 적합한 양의 담체와 함께 함유하여, 환자에게 적절한 투여형을 제공할 것이다. 제형은 투여 방식에 적합해야 한다.
펩티드, 예컨대 지속형 펩티드의 점막관통 흡수성을 증가시키기 위한 제제가 또한 본 발명에 의해 고려된다. 경구 투여에 적합한 제약 조성물은 캡슐제 또는 정제로서; 산제 또는 과립제로서; 용액제, 시럽제 또는 현탁액제 (수성 또는 비-수성 액제)로서; 식용 폼(foam) 또는 휩(whip)으로서; 또는 에멀젼제로서 제공될 수 있다. 정제 또는 경질 젤라틴 캡슐제는 락토스, 전분 또는 이의 유도체, 마그네슘 스테아레이트, 나트륨 사카린, 셀룰로스, 탄산마그네슘, 스테아르산 또는 이의 염을 포함할 수 있다. 연질 젤라틴 캡슐제는 식물성유, 밀랍, 지방, 반-고체 또는 액체 폴리올 등을 포함할 수 있다. 용액제 및 시럽제는 물, 폴리올 및 당을 포함할 수 있다.
경구 투여용으로 의도된 활성제는 위장관 내의 활성제의 붕해 및/또는 흡수를 지연시키는 물질로 코팅되거나 또는 이와 혼합될 수 있다 (예를 들어, 글리세롤 모노스테아레이트 또는 글리세롤 디스테아레이트가 사용될 수 있음). 따라서, 활성제의 서방성이 장시간에 걸쳐 달성될 수 있으며, 필요에 따라, 활성제는 위 내부에서 분해되는 것으로부터 보호될 수 있다. 경구 투여용 제약 조성물을 제제화하여, 특정 pH 또는 효소 조건으로 인하여 특정 위장 위치에서 활성제가 방출되는 것을 용이하게 할 수 있다.
경피 투여에 적합한 제약 조성물은 연장된 기간 동안 수용자의 표피와 긴밀하게 접촉되어 유지되는 개별 패치제로서 제공될 수 있다. 국소 투여에 적합한 제약 조성물은 연고제, 크림제, 현탁액제, 로션제, 산제, 용액제, 페이스트제, 겔제, 분무제, 에어로졸제 또는 오일로서 제공될 수 있다. 피부, 입, 눈 또는 기타 외부 조직에 대한 국소 투여를 위해, 국소 연고제 또는 크림제가 바람직하게 사용된다. 연고제로 제제화되는 경우, 활성 성분은 파라핀계 또는 수혼화성 연고 기제와 함께 사용될 수 있다. 별법으로, 활성 성분은 수중유 기재 또는 유중수 기제와 함께 크림제로 제제화될 수 있다. 눈에 국소 투여하기에 적합한 제약 조성물로는 점안제가 포함된다. 상기 조성물에서, 활성 성분은 적합한 담체, 예를 들어, 수성 용매 중에 용해되거나 현탁될 수 있다. 입에 국소 투여하기에 적합한 제약 조성물로는 로젠지제, 파스틸지제 및 구강세정제가 포함된다.
비내 및 폐 투여에 적합한 제약 조성물은 고체 담체, 예컨대 산제 (바람직하게는 입도가 20 내지 500 ㎛ 범위임)를 포함할 수 있다. 산제는 코로 들이쉬는 방식으로, 즉, 코에 가까이 위치된 분말 용기로부터 코를 통하여 빠르게 흡입함으로써 투여될 수 있다. 별법으로, 비내 투여용으로 채택된 조성물은 액체 담체, 예를 들어, 비내 분무제 또는 점비제를 포함할 수 있다. 별법으로, 화합물의 폐 내로의 직접 흡입은 인두 중앙부로의 마우스피스를 통한 설비 또는 깊은 흡입에 의해 달성될 수 있다. 상기 조성물은 활성 성분의 수용액 또는 오일 용액을 포함할 수 있다. 흡입에 의한 투여용 조성물은, 활성 성분의 예정된 투여량을 제공하도록 구성될 수 있는, 특별히 개조된 장치, 예컨대 이들로 한정되지 않지만, 가압 에어로졸, 네불라이저 또는 취입기로 공급될 수 있다. 바람직한 실시양태에서, 본 발명의 제약 조성물은 비강 내로 직접 투여되거나, 또는 비강 또는 인두 중앙부를 통해 폐 내로 투여된다.
직장 투여에 적합한 제약 조성물은 좌제 또는 관장제로서 제공될 수 있다. 질 투여에 적합한 제약 조성물은 페서리, 탐폰, 크림, 겔, 페이스트, 포말 또는 분무 제제로서 제공될 수 있다.
비경구 투여에 적합한 제약 조성물은 항산화제, 완충제, 정균제, 및 조성물이 목적 수용자 혈액과 실질적으로 등장성이 되게 하는 용질을 함유할 수 있는, 수성 및 비-수성 멸균 주사가능한 용액제 또는 현탁액제를 포함한다. 상기 조성물 중에 존재할 수 있는 기타 성분으로는, 예를 들어, 물, 알콜, 폴리올, 글리세린 및 식물성유가 포함된다. 비경구 투여에 적합한 조성물은 단위-용량 또는 다중-용량 용기, 예를 들어, 밀봉된 앰플 및 바이알에 존재할 수 있고, 사용 직전에 단지 멸균 액체 담체, 예를 들어, 주사용 멸균 식염수 용액의 첨가만을 필요로 하는 동결 건조 상태로 저장될 수 있다. 즉석 주사 용액 및 현탁액은 멸균 산제, 과립제 및 정제로부터 제조될 수 있다. 한 실시양태에서, 주사가능한 펩티드 용액을 포함하는 자동주사기는 구급차, 응급실 및 전장 상황에 따른 긴급 사용을 위해, 및 심지어 가정 환경, 특히 잔디 깎는 기계의 경솔한 사용에 의한 것과 같은 외상성 절단이 발생할 수 있는 가능성이 존재하는 경우에서의 자가 투여를 위해 제공될 수 있다. 절단된 발 또는 발가락의 세포 및 조직이 재부착 후 생존할 가능성은, 실행가능한 즉시, 심지어 의료 인력이 현장에 도착하기 이전에, 또는 절단된 발가락으로 인해 고통받는 사람이 안내되어 응급실에 도착하기 이전에, 펩티드를 절단된 부분의 여러 부위에 투여함으로써 증가시킬 수 있다.
바람직한 실시양태에서, 조성물은 통상의 절차에 따라 인간에게 정맥내 투여하기에 적합한 제약 조성물로서 제제화된다. 전형적으로, 정맥내 투여용 조성물은 멸균 등장성 수성 완충액 중의 용액제이다. 필요에 따라, 조성물은 또한 주사 부위에서의 통증을 완화시키기 위해 가용화제 및 국소 마취제, 예컨대 리도카인을 포함할 수 있다. 일반적으로, 성분은 단위 투여형으로, 예를 들어, 활성제의 양을 나타내는 앰플 또는 사세(sachette)와 같은 기밀 용기 중 건조된 동결건조 분말 또는 무수 농축물로서 개별적으로 또는 함께 혼합되어 공급된다. 조성물이 주입에 의해 투여되는 경우, 이는 제약 등급의 멸균수 또는 멸균 식염수를 함유하는 주입용 병을 이용하여 분배될 수 있다. 조성물이 주사에 의해 투여되는 경우, 멸균 식염수의 앰플을 제공하여, 성분이 투여 전에 혼합될 수 있도록 할 수 있다.
좌제는 일반적으로 활성 성분을 0.5 중량% 내지 10 중량% 범위로 함유하고; 경구 제제는 바람직하게는 10% 내지 95%의 활성 성분을 함유한다.
관류 조성물은 제자리 관류에 사용하기 위해 제공될 수 있다. 상기 제약 조성물은 개체에게 단기 또는 장기의, 국소성 또는 전신성 투여에 적합하지 않은 펩티드의 수준 또는 펩티드의 형태를 포함할 수 있으나, 기관 조(organ bath), 기관 관류액, 또는 제자리 관류액 중에서 본원에서 의도된 기능을 수행한 후, 여기에 함유된 펩티드의 수준을 감소시키거나 제거하고, 그 후 치료된 기관 또는 조직을 정상적 순환에 노출시키거나 복귀시킨다.
본 발명은 또한 본 발명의 제약 조성물의 1종 이상의 성분으로 채워진 하나 이상의 용기를 포함하는 제약 팩 또는 키트를 제공한다. 상기 용기(들)와 관련하여 임의로는 제약 또는 생물학적 제품의 제조, 사용 또는 판매를 규제하는 정부 당국에 의해 처방된 형식의 공지문이 제공될 수 있고, 상기 공지문은 인간 투여를 위한 제조, 사용 또는 판매 당국에 의한 승인을 반영한다.
또다른 실시양태에서, 예를 들어, 펩티드는 제어 방출형 시스템으로 전달될 수 있다. 예를 들어, 펩티드는 정맥내 주입, 매몰식 삼투성 펌프, 경피 패치, 리포솜, 또는 기타 투여 방식을 이용하여 투여될 수 있다. 한 실시양태에서, 펌프가 사용될 수 있다 (각각 그의 전문이 본원에 참조로 포함되는 문헌 [Langer, 상동]; [Sefton, 1987, CRC Crit. Ref. Biomed. Eng. 14:201]; [Buchwald et al., 1980, Surgery 88:507]; [Saudek et al., 1989, N. Engl. J. Med. 321:574] 참조). 또다른 실시양태에서, 화합물은 소포, 특히 리포솜으로 전달될 수 있다 (문헌 [Langer, Science 249:1527-1533 (1990)]; [Treat et al., Liposomes in the Therapy of Infectious Disease and Cancer, Lopez-Berestein and Fidler (eds.), Liss, New York, pp. 353-365 (1989)]; WO 91/04014; 미국 특허 제4,704,355호; [Lopez-Berestein, 동 문헌, pp. 317-327] 참조; 일반적으로 동 문헌 참조). 또다른 실시양태에서, 중합성 물질이 사용될 수 있다 (문헌 [Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Press: Boca Raton, Florida, 1974]; [Controlled Drug Bioavailability, Drug Product Design and Performance, Smolen and Ball (eds.), Wiley: New York (1984)]; [Ranger and Peppas, J. Macromol. Sci. Rev. Macromol. Chem. 23:61, 1953] 참조; 또한 문헌 [Levy et al., 1985, Science 228:190]; [During et al., 1989, Ann. Neurol. 25:351]; [Howard et al., 1989, J. Neurosurg. 71:105] 참조 (상기 각각은 그 전문이 본원에서 참조로 포함됨)).
또다른 실시양태에서, 제어 방출형 시스템은 치료 표적, 즉, 표적 세포, 조직 또는 기관에 근접하게 위치하여, 이에 따라 전신 용량의 단지 일부만을 필요로 할 수 있다 (예를 들어, 그 전문이 본원에 참조로 포함되는 문헌 [Goodson, pp. 115-138 in Medical Applications of Controlled Release, vol. 2, 상동, 1984] 참조). 기타 제어 방출형 시스템은 그 전문이 본원에 참조로 포함되는 문헌 [Langer (1990), Science 249:1527-1533]의 개관에 개시되어 있다.
또다른 실시양태에서, 적절하게 제제화된 펩티드는 비내, 구강, 경구, 직장, 질, 안구, 경피, 비경구, 흡입 또는 설하 투여에 의해 투여될 수 있다.
특정 실시양태에서, 본 발명의 펩티드를 치료가 필요한 영역에 국소적으로 투여하는 것이 바람직할 수 있고; 이는, 예를 들어, 이에 한정되지 않지만, 수술 동안의 국부 주입, 수술 후, 예를 들어 창상 드레싱과 함께 국소 적용에 의해, 주사에 의해, 카테터에 의해, 좌제에 의해, 또는 이식물에 의해 달성될 수 있고, 상기 이식물은 다공성, 비-다공성, 또는 젤라틴 물질, 예컨대 실라스틱(silastic) 막과 같은 막, 또는 섬유이다. 상기 실시양태의 비제한적인 예는 혈관구조, 맥관 등의 일부에 이식되는, 본 발명의 펩티드로 코팅된 스텐트 또는 기타 스캐폴딩(scaffolding)일 것이다.
바람직한 유효량의 선택은 당업자에게 공지되어 있을 여러 인자를 고려하여 해당 숙련자에 의해 용이하게 결정될 것이다. 상기 인자로는 펩티드의 특정 형태, 및 이의 약동학적 파라미터, 예컨대 생체이용률, 대사, 반감기 등을 들 수 있고, 이는 제약 화합물에 대한 규제 승인을 얻는 데 전형적으로 이용된 통상의 개발 절차 동안 확립되었을 것이다. 용량에 고려되는 추가의 인자는 치료될 상태 또는 질환, 또는 정상 개체에서 달성될 이점, 환자의 체질량, 투여 경로, 투여가 단기인지 또는 장기인지의 여부, 부수적인 투약, 및 투여된 제약 제제의 효능에 영향을 미치는 것으로 잘 알려져 있는 기타 인자를 포함한다. 따라서 정확한 투여량은, 전문가의 판단 및 각 환자의 상황, 예를 들어, 개별 환자의 상태 및 면역 상태에 따라, 그리고 표준 임상 기술에 따라 결정되어야 한다.
본 발명의 또다른 측면에서, 관류액 또는 관류 용액이 이식용 기관의 관류 및 저장을 위해 제공되고, 상기 관류 용액은 반응성 세포 및 결합 세포, 조직 또는 기관을 보호하기에 효과적인 양의 펩티드 또는 펩티드 유사체를 포함한다. 이식에는, 이들로 한정되지는 않지만, 타가이식 {여기서, 기관 (예컨대, 세포, 조직 또는 기타 신체 부분)는 한 기증자로부터 적출되어, 상이한 수혜자에게 이식되며, 여기서 양쪽은 동일한 종임}; 자가이식 {여기서, 기관을 신체의 한 부분으로부터 취하여 또다른 부분에 대체함 (예컨대, 기관을 적출하고, 생체외에서, 예컨대 종양 제거를 위하여 절제하거나, 회복시키거나 또는 달리 조작한 후에, 본래 위치에 복귀시킬 수 있는 벤치(bench) 수술 절차} 또는 이종이식 (여기서, 조직 또는 기관은 종 간에 이식됨)을 들 수 있다. 한 실시양태에서, 관류 용액은 위스콘신 대학 (UW) 용액이고 (그 전문이 본원에 참조로 포함되는 미국 특허 제4,798,824호), 이는 5% 히드록시에틸 전분 (분자량이 약 200,000 내지 약 300,000이고, 에틸렌 글리콜, 에틸렌 클로로히드린, 염화나트륨 및 아세톤을 실질적으로 함유하지 않음); 25 mM KH2PO4; 3 mM 글루타티온; 5 mM 아데노신; 10 mM 글루코스; 10 mM HEPES 완충액; 5 mM 마그네슘 글루코네이트; 1.5 mM CaCl2; 105 mM 나트륨 글루코네이트; 페니실린 200,000 유닛; 인슐린 40 유닛; 덱사메타손 16 ㎎; 페놀 레드(Phenol Red) 12 ㎎을 함유하며; 7.4 내지 7.5의 pH 및 약 320 mOsm/ℓ의 삼투압을 갖고, 적절한 양의 본 발명의 펩티드로 보충된다. 상기 특정 관류액은 유효량의 펩티드를 포함하여 본 발명의 용도에 적합할 수 있는 여러가지 그러한 용액을 단순히 예시한 것이다. 추가의 실시양태에서, 관류 용액은 약 1 내지 약 500 ng/ml의 펩티드, 또는 약 40 내지 약 320 ng/ml의 펩티드를 함유한다. 상기 언급한 바와 같이, 임의의 형태의 펩티드가 본 발명의 상기 측면에 사용될 수 있다.
본원 전체의 목적을 위한 펩티드의 바람직한 수용자는 인간이지만, 본원의 방법은 기타 포유동물, 특히 길들여진 동물, 가축, 반려동물 및 동물원 동물에게도 동일하게 적용된다. 그러나, 본 발명은 제한적인 것이 아니며, 그러한 이점은 어떠한 포유동물에게도 적용될 수 있다.
생체외 발명의 추가의 측면에서, 임의의 펩티드, 예컨대 이들로 한정되지는 않지만, 상기 기재된 것이 사용될 수 있다.
본 발명의 또다른 측면에서, 내피 세포 장벽에 의해 혈관계로부터 단리되지 않은 세포, 조직 또는 기관에서의 조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상의 예방, 치료 또는 관리를 위한 방법 및 조성물은, 세포, 조직 또는 기관을 펩티드를 함유하는 제약 조성물에 직접 노출시키거나, 또는 펩티드를 함유하는 제약 조성물을 조직 또는 기관의 혈관계에 투여하거나 접촉시킴으로써 제공된다.
에리트로포이에틴 기재의 기타 조직 보호 화합물과 유사하게, 본 발명의 펩티드가, 내피 세포 치밀 이음부를 갖는 기관, 예를 들어, 뇌, 망막 및 정소의 모세관의 내피 세포의 관강 표면으로부터 기저막 표면으로 운반될 수 있는 것이 가능하다. 따라서, 장벽을 가로지르는 세포 상에서 조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상의 결과는 치료될 수 있다. 임의의 특정 이론에 구속되고자 하는 것은 아니지만, 펩티드의 트랜스사이토시스 이후, 이는 세포, 예를 들어, 신경세포, 눈 (예를 들어, 망막), 지방, 결합, 모발, 치아, 점막, 췌장, 내분비, 귀, 상피, 피부, 근육, 심장, 폐, 간, 신장, 소장, 부신 (예를 들어, 부신 피질, 부신 수질), 모세관, 내피, 정소, 난소, 줄기 또는 자궁내막 세포 상의 조직-보호 수용체와 상호작용할 수 있고, 수용체 결합은 반응성 세포 또는 조직 내부의 유전자 발현 프로그램의 활성화를 야기하는 신호 전달 연쇄 반응을 개시하여, 세포 또는 조직, 또는 기관을, 예컨대 독소, 염증, 저산소증 등에 대한 노출에 의한 손상으로부터 보호할 수 있다. 또다른 실시양태에서, 펩티드는 본원에 참조로 포함되는 PCT 공보 제PCT/USO1/49479호, 미국 특허 출원 제10/188,905호 및 10/185,841호의 교시에 따라 장벽을 가로지를 수 있는 화합물, 예컨대 CEPO에 가교되어, 장벽을 가로질러 운반될 수 있다.
따라서, 조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상으로부터 조직을 보호하는 방법은 본원에서 하기에 상세히 기재되어 있다.
본 발명의 한 실시양태의 실행에 있어서, 포유동물 환자는, 일반적으로 신경, 폐, 심장, 난소 또는 정소 손상과 같은 악영향을 미치는, 암 치료를 위한 전신 화학요법, 예컨대 방사선 요법을 경험한다. 상기 기재된 바와 같은 조직 보호 펩티드 또는 펩티드 유사체를 포함하는 제약 조성물의 투여는 화학요법 및/또는 방사선 요법 이전에 및 그 동안에 수행하여, 각종 조직 및 기관을 화학요법제에 의한 손상으로부터 보호하며, 예컨대 정소를 보호한다. 이러한 치료는 화학요법제의 순환 수준이 포유동물 신체에 대한 잠재적 위험 수준 미만으로 떨어질 때까지 계속될 수 있다.
본 발명의 또다른 실시양태의 실행에 있어서, 각종 기관은 자동차 사고의 희생자로부터 적출되어 수많은 수혜자에게 이식되도록 계획되며, 이 중 일부는 장거리 및 장기간 동안의 운송을 필요로 한다. 기관 적출 이전에, 기증자에게 본원에 기재된 바와 같은 조직 보호 펩티드 및 펩티드 유사체를 포함하는 제약 조성물을 주입한다. 수송을 위해 적출된 기관은 본원에 기재된 바와 같은 조직 보호 펩티드 또는 펩티드 유사체를 함유하는 관류액으로 관류시키고, 조직 보호 펩티드 또는 펩티드 유사체를 포함하는 기관 조 내에 저장한다. 특정 기관은 본 발명에 따른 조직 보호 펩티드 및 펩티드 유사체를 함유하는 관류액을 사용하는 박동성 관류 장치에 의해 계속 관류시킨다. 운송 동안, 및 제자리 기관 이식 및 재관류 시에 최소한의 기관 기능 악화가 발생한다.
본 발명의 또다른 실시양태에서, 개체를 독성제에 노출시키는 위험한 활동 중인 참가자는, 독성제에 대한 노출 효과의 예방 (즉, 발병 지연, 억제 또는 중단), 이에 대한 보호 또는 이의 완화에 충분한 펩티드를 함유한 제약 조성물의 용량을 취할 수 있다. 특히, 상기 치료 방법은 독성제와의 접촉이 포함되는 다양한 직업, 예컨대 광부, 화학물질 제조업자, 군사 인력 (군인, 낙하산병), 응급 인력 (경찰, 소방관, EMS 및 재난 구조 인력), 건설 인부, 식품 가공업자, 및 발전소 고용인에 적용될 수 있다.
본 발명의 또다른 실시양태에서, 심장 판막을 복구하는 수술 절차는 일시적 심장 마비 및 동맥 폐쇄를 필요로 한다. 수술 전에, 환자에게 조직 보호 펩티드 또는 펩티드 유사체를 주입한다. 상기 치료는, 특히 재관류 이후 저산소성 허혈 세포 손상을 예방한다. 추가로, 본 발명의 제약 조성물은, 수술 절차와 관련된 외상을 제한하거나 또는 수술 절차로부터 개체의 회복을 돕기 위한 노력으로 예방적으로 사용되어 개체를 수술에 대해 준비시킬 수 있다. 조직 보호 펩티드 및 펩티드 유사체를 함유하는 제약 조성물을 사용하는 본 발명의 치료 방법은 수술 절차에 대한 예방 용도를 제공하며, 이는 임시적 허혈 사건을 유도하는 절차, 예컨대, 이들로 한정되지는 않지만, 바이패스 절차 (관상동맥 바이패스), 혈관형성 절차, 절단 및 이식, 및 또한 반응성 세포, 조직 또는 기관에 직접 수행되는 절차, 예컨대 뇌 및 척수 수술, 및 개심 절차에 특히 유용할 것이다. 상기 절차는 심폐 (심장 폐) 바이패스의 이용을 수반할 수 있다.
본 발명의 또다른 실시양태에서, 임의의 수술 절차, 예컨대 심폐 바이패스 수술에 있어서, 본 발명의 조직 보호 펩티드 또는 펩티드 유사체가 사용될 수 있다. 한 실시양태에서, 상기 기재된 바와 같은 조직 보호 펩티드 및 펩티드 유사체를 포함하는 제약 조성물의 투여가 바이패스 절차 이전에, 그 동안에 및/또는 그 이후에 수행되어, 뇌, 심장 및 기타 기관의 기능을 보호한다.
생체외 적용 또는 생체내 적용에 펩티드를 사용하여, 조직 손상 관련 질환 또는 장애, 또는 그로부터 발생하는 손상, 영향 또는 증상을 치료하는 전술한 예에서, 본 발명은 약 .01 pg 내지 30 mg, .5 pg 내지 25 mg, 1 pg 내지 20 mg, 500 pg 내지 10 mg, 1 ng 내지 10 mg, 500 ng 내지 10 mg, 1 ㎍ 내지 10 mg, 500 ㎍ 내지 10 mg, 또는 1 mg 내지 10 mg 범위 내의 펩티드의 양, 및 제약상 허용되는 담체를 포함하는, 독성제에 대한 노출의 손상 및 효과 또는 그의 증상의 예방, 치료 또는 관리에 적절한 단위 투여형의 제약 조성물을 제공한다. 바람직한 실시양태에서, 펩티드의 양은 약 .5 pg 내지 1 ㎎의 범위 내에 있다. 바람직한 실시양태에서, 제제는 비-적혈구 조혈성인 펩티드를 함유한다.
게다가, 본 발명의 상기 회복 측면은 세포, 조직 또는 기관의 기능이상의 회복을 위한 제약 조성물의 제조를 위한 본원의 임의의 펩티드의 용도에 관한 것이고, 여기서 상기 치료는 기능이상의 원인이 되는 초기 손상 이후, 및 상당히 이후에 개시된다. 게다가, 본 발명의 펩티드를 사용하는 치료는 급성기 뿐만 아니라 만성기 동안의 질환 또는 상태의 과정에 걸친 것일 수 있다.
본 발명의 펩티드는 투여 당, 약 1 ng 내지 약 300 ㎍/체중 ㎏, 바람직하게는 약 5 내지 150 ㎍/체중 ㎏, 가장 바람직하게는 약 10 내지 100 ㎍/체중 ㎏의 투여량으로 전신 투여될 수 있다. 예를 들어, 투여는, 임상적으로 필요한 한, 매시간, 매일, 또는 적절한 간격 이후, 예를 들어, 1 내지 12시간마다, 바람직하게는 6 내지 12시간 마다; 2 내지 6일마다, 바람직하게는 2 내지 4일마다; 1 내지 12주마다, 바람직하게는 1 내지 3주마다 반복될 수 있다. 한 실시양태에서, 유효량의 펩티드 및 제약상 허용되는 담체는 단일 용량 바이알 또는 기타 용기에 포장될 수 있다. 또다른 실시양태에서, 본원에 기재된 활성을 나타낼 수 있으나 헤모글로빈 농도 또는 적혈구 용적률의 증가를 야기하지 않는 펩티드가 사용된다. 상기 펩티드는 본 발명의 방법이 장기간 제공될 목적인 경우에 바람직하다.
<실시예>
실시예
1. 펩티드 합성 방법
A. 펩티드 A (서열 2, EPO 아미노산 서열 38-57에 해당함) 및 펩티드 B (서열 3, EPO 아미노산 서열 58-82에 해당함)의 합성.
EPO의 단편인 펩티드 A (서열 2) 및 펩티드 B (서열 3)를 문헌 [Band, D., Chopra, N and Kent, S., "Total Synthesis of Crambin," J. AM. CHEM. SOC. 2004, 126, 1377-1383] (본원에 그 전문이 참조로 포함됨)에 기재된 바와 같은 Boc 화학 단계식 고체상 펩티드 합성법에서의 "제자리 중화"를 이용하여 합성하였다. 간단하게는, EPO 아미노산 서열 38-57 (펩티드 A, , 서열 2) 및 EPO 아미노산 서열 58-82 (펩티드 B, , 서열 3)에 해당하는 2개의 단편을 -OCH2-Pam-수지 (유리 α카르복시 펩티드) 또는 HSCH2CH2CO-Leu-OCH2-Pam-수지 (α티오에스테르 펩티드) 상에서 합성하였다. 합성 동안, 각종 아미노산의 측쇄를 하기와 같이 보호하였다: Arg(Tos), Asn(Xan), Asp(OcHex), Cys(4-CH3Bzl) 또는 Cys(ACM), Glu(OcHex), Lys(2-Cl-Z), Ser(Bzl), Thr(Bzl), Tyr(Br-Z). 펩티드 사슬을 어셈블링시킨 후, 펩티드를 탈보호하고, 동시에 p-크레솔을 함유하는 무수 HF (90:10, v/v)로 0℃에서 1시간 동안 처리하여 수지 지지체로부터 절단하였다. 감압 하에 HF를 증발시킨 후, 조 생성물을 침전시키고, 냉각된 디에틸 에테르로 연화처리하며(triturated), 펩티드를 0.1% TFA를 함유하는 50% 수성 아세토니트릴 중에 용해시키고, 정제용 HPLC 시스템에 의해 정제하였다. LC-MS를 이용하여 펩티드 조성을 확인하였다.
펩티드 ID (, 서열 282)는 보호된 N-말단 (피로글루탐산의 5원 고리 구조에 의해 보호됨), 및 C-말단의 유리 카르복실 기를 갖는 11-아미노산 선형 펩티드이다. 그의 분자량은 1257 달톤이다. 이것을 왕(Wang) 수지 상에서 표준 Fmoc 고체상 펩티드 합성법을 이용하여 합성하고, 정제용 HPLC 및 이온-교환 크로마토그래피로 정제하고, 동결건조시켰다. 아세테이트 및 암모늄은 펩티드 분자의 염기성 기 및 산성 기에 이온 형태로 결합하여 혼합 염을 형성한다.
실시예
2. 조직 보호 펩티드 및 펩티드 유사체는 비-적혈구
조혈성임
.
A.
시험관내
평가
UT-7epo (인간 에리트로포이에틴-의존성 백혈병 세포주)를 펩티드의 적혈구 조혈 효능의 측정을 위해 사용하였다. UT-7epo 세포 (도이체 잠루크 본 미크로오르가니스멘 운트 첼쿨투렌(Deutsche Sammlung von Mikroorganismen und Zellkulturen, DSMZ). cat. No. ACC 363)를 10% FBS 및 5 ng/ml 에리트로포이에틴을 함유한 완전 RPMI-1640 배지 중에서 성장시켰다. 에리트로포이에틴에 노출된 세포의 증식/생존 (= 생존력 증가) 반응은 고전적인 적혈구형 에리트로포이에틴 수용체에 의해 매개되며, 이는 고전적인 에리트로포이에틴 수용체를 자극하는 에리트로포이에틴 변이체의 능력의 정량적 측정치이다.
UT-7epo 세포를 10% 기증자 태아 혈청, 4 mM L-글루타민을 함유하고 5 ng/ml 재조합 인간 에리트로포이에틴이 보충된 신선한 완전 RPMI 1640 배지에 옮겼다. 세포를 플라스크 당 배지 20 ml를 채운 75 ㎠ 플라스크 중에서 5% CO2를 갖는 가습 인큐베이터 내 37℃에서 48시간 동안 유지시켰다. 검정 제2일, 즉, 48시간에, 세포를 플라스크로부터 50 ml의 원뿔 튜브로 옮기고, 실온에서 5분 동안 1,000 rpm에서 원심분리하였다. 상청액을 따라버리고, 세포를 기아 배지 10 ml (3% 기증자 태아 혈청, 4 mM L-글루타민)로 2회 세척하였다. 그 후, 피펫의 상하 운동을 이용하여 세포를 기아 배지 중에 재현탁시켜 단세포 현탁액을 얻었다. 재현탁된 세포를 기아 배지로 희석하여 4×105 세포/ml의 밀도를 얻고, 25 ㎠ 플라스크 당 총 배양 부피 10 ml로 플레이팅하였다. 4시간의 인큐베이션 후에, 세포를 다시 50 ml 원뿔 튜브로 옮겼다. 대조군 세포를 5 ng/ml rhu-에리트로포이에틴과 함께 처음부터 끝까지 유지시켰다.
세포를 기아 배지 중에 200,000개 세포/ml로 희석시키고, 96웰 플레이트에 100 ㎕/웰로 플레이팅하며, 각종 농도의 에리트로포이에틴 및 펩티드 ID (서열 282)에 노출시켰다. 3% 혈청을 함유하는 RPMI 1640 배지 중에서 일련의 10배 희석액을 사용하여 5 pM 내지 50 nM의 시험 화합물 농도를 생성하였다. 추가 48시간의 인큐베이션 후에, WST-1 세포 증식 시약 (로쉐, Roche) 15 ml의 용액을 각 웰에 첨가하고, CO2 중 37℃에서 1시간 동안 인큐베이션하였다. 1분 동안 혼합한 후에, 플레이트을 플레이트 판독기에서 판독하였다 (650 nm에서의 백그라운드 흡수로부터 감해진, 450 nm에서의 흡수). 도 1에 나타낸 바와 같이, 펩티드 ID는 EPO의 강한 적혈구 조혈 효과와 비교하여 용량 범위에 걸쳐 적혈구 조혈 활성을 갖지 않았다. 이것은 비-적혈구 조혈 펩티드 또는 펩티드 유사체가 1 ㎍/ml 미만의 용량, 더 바람직하게는 10 ㎍/ml 미만의 용량에 대하여 적혈구 조혈 활성을 갖지 않을 것이라는 예측을 하기에 나타냈다.
B.
생체내
평가
조직 보호 펩티드 및 펩티드 유사체의 적혈구 조혈 활성을 평가하기 위해, 펩티드 ID를 28일 동안 스프라구에 다울레이 래트에게 1일 2회씩 정맥내로 투여하였다. 9마리 수컷 및 9마리 암컷 래트를 1 내지 4군으로 배정하여, 투여 당 PBS 중 펩티드 ID 0, 60, 180 및 600 ㎍/kg (각각 0, 48, 143 및 477 nmol/kg)를 볼루스(bolus) 정맥내 투여에 의해 제1일 내지 제28일에 투여하고, 혈액학적 변수의 검정을 위한 혈액 샘플을 제29일에 수집하였다. 헤모글로빈 농도는 자동화 분석기 (케스카 코포레이션(Keska Corporation))를 이용하여 측정하였다. 도 2에 나타낸 바와 같이, 어떠한 군에서도 헤모글로빈 농도에서의 차이는 존재하지 않았다.
추가로, 펩티드 ID의 적혈구 조혈 및 혈액생성 효과를 토끼에서 평가하였다. 연구를 개시하기 이전에 모든 토끼에서 혈액 샘플을 채취하여, 동물에 대한 혈액학적 기준을 확립하였다. 펩티드 ID를 뉴질랜드 백색 토끼에게 28일 동안 1일 2회씩 i.v. 투여하였다. 이 연구를 위해, 6마리 수컷 및 암컷을 1군 및 4군에 배정하고, 4마리 수컷 및 4마리 암컷을 2군 및 3군에 배정하였다. 볼루스 i.v. 투여에 의해 투여 당 PBS 중 펩티드 ID를, 1군에는 0을 투여하고, 2군에는 30 ㎍ (24 nmol/kg bw)을 투여하고, 3군에는 90 ㎍/kg (72 nmol/kg bw)을 투여하고; 4군에는 300 ㎍/kg (240 nmol/kg bw)을 투여하였다. 혈액학적 변수의 검정을 위한 혈액 샘플을 제29일에 수집하였다. 기준 대 제29일의 혈액학적 파라미터를 비교했을 때 헤모글로빈 농도, 적혈구용적 또는 혈소판수에서는 차이를 나타내지 않았다 (도 3a. b. 및 c.).
실시예
3. 펩티드 또는 펩티드 유사체는
시험관내
검정에서 조직 보호성임.
펩티드 및 펩티드 유사체를 임의의 여러가지 시험관내 검정을 이용하여 조직 보호성에 대하여 용이하게 평가할 수 있다. 예를 들어, 흥분독성으로부터의 보호는 마우스 운동뉴런의 카이닛-유도성 사멸을 이용하여 측정될 수 있다. 종래에 기재되어 있는 바와 같이 (본원에 그 전문이 참조로 포함되는 문헌 [Siren et al., 2001, Proc. Natl. Acad Sci. ISA, 98:4044]), 15-일령 스프라구에-다울레이 래트 태아로부터 척수를 얻었다. 전각을 트립신 처리하고, 300×g에서 10분 동안 4% BSA 쿠션(cushion)을 통해 원심분리하였다. 세포 (뉴런-신경교세포 혼합 배양액을 나타냄)를 폴리-DL 오르니틴 및 라미닌으로 미리 코팅된 24 mm 웰 플레이트에 2,000개 세포/㎠의 밀도로 시딩하였다. 운동뉴런를 면역패닝(immunopanning)에 의해 더 정제하고, 폴리-DL 오르니틴 및 라미닌으로 미리 코팅되고 완전 배양 배지 [뉴로베이살(Neurobasal)/B27 (2%); 0.5 mM L-글루타민; 2% 말 혈청; 25 mM 2 머캅토에탄올; 25 mM 글루타메이트; 1% 페니실린 및 스트렙토마이신; 1 ng/ml BDNF]를 함유하는 24 mm 웰 플레이트 상에 상기 세포를 저밀도 (20,000 세포/㎠)로 시딩하였다. 배지 (글루타메이트 무함유)를 제4일 및 제6일에 배양액에 재첨가하였다. 카인산 (뉴런-신경교세포 혼합 배양액에 대하여 5 mM; 정제된 배양액에 대하여 50 mM)과 함께 48시간 동안 인큐베이션함으로써 배양액 중에서 제6일에 세포 사멸을 유도하였다. 세포 사멸 유도 72시간 전에, 펩티드 B (5 ng/ml, 1.8 nM), EPO (3.3 nM) 또는 비히클을 배양액에 첨가하고, 48시간 동안 계속 처리하였다. 그 후, 배지를 따라버리고, 세포를 PBS 중 4% (부피/부피) 파라포름알데히드로 40분 동안 고정시키고, 0.2% 트리톤 X-100으로 투과시키고, PBS 중 10% (부피/부피) FCS로 차단하고, 비-인산화 신경세사 (SMI-32; 1:9,000)에 대한 항체와 함께 밤새 인큐베이션하고, 디아미노벤지딘을 사용한 아비딘-비오틴 방법을 이용하여 가시화하였다. 커버 슬립의 4개 측면 전역의 SMI-32 양성 세포를 카운팅하여 운동뉴런의 생존력을 형태상으로 평가하고, 아팝토시스체의 염색을 H33258을 사용하여 수행하였다. 도 4에 나타낸 바와 같이, 펩티드 B는 카인산에 대한 글루타메이트 수용체의 신경독성 효과에 대해 세포를 보호하였다.
실시예
4. 중간 대뇌 동맥 폐쇄 모델
스프라구에-다울레이 (군 당 8마리)를 다음의 MCAO 프로토콜에 적용하고, 문헌 [Brines et al, 2000, PNAS USA 97:10526-10531] (본원에 그의 전문이 참조로 포함됨)의 교시에 따라 수술을 수행하였다. 간단하게는, 클로랄 히드레이트 (400 ㎎/㎏-bw, i.p.)로 래트를 마취시키고, 경동맥을 가시화하며, 우측 경동맥을 2개 봉합에 의해 폐쇄하고 절단하였다. 우측 안와에 인접하고 문측에 위치한 천두공은, 코 동맥으로의 원위부를 소작시킨 중간 대뇌 동맥 ("MCA")의 가시화를 허용하였다. 상기 고정된 MCA 병변 주위에 반암부 (경계 구역)을 생성하기 위하여, 대측성 경동맥을 미세 핀셋에 의해 제공되는 수축을 이용하여 1시간 동안 폐쇄시킨 후 재개방하였다.
재관류 시 식염수, 단일 i.v. 용량으로서의 펩티드 ID (2 ㎍/kg bw), 또는 단일 i.v. 용량으로서의 펩티드 IX (, 서열 301, 펩티드 B, 서열 3의 스크램블(scrambled) 버젼)(2 ㎍/kg bw)을 래트에게 투여한 후에, 2-시간 간격으로 3회 더 주사하였다. 손상을 평가하기 위하여, 래트를 행동 시험에 적용하거나, 또는 앞서 기재한 프로토콜에 따라 수술 후 24시간에 뇌 구획의 테트라졸륨 착색을 수행하여 병변 부피를 측정하였다.
(a) 병변 부피
이어서, 병변 부피는 수술 후 24시간에 뇌 구획의 테트라졸륨 착색을 수행하여 측정하였다. 펩티드 ID가 식염수 처치된 래트 (291 ± 23 mm3)와 비교하여 24시간에 경색 부피 (225 ± 20 mm3)의 유의한 감소를 입증하였다.
(b) 행동 시험
래트를 또한 풋 폴트(foot fault) 행동 프로토콜로 시험하였다. 문헌 [Markgraf et al., 1992, Brain Research 575:238-246] (본원에 그 전문이 참조로 포함됨)의 프로토콜에 따라, 격자 크기가 30 mm인 30 ㎝ x 30 ㎝의 올려놓은 스테인리스 스틸 격자 바닥에서 래트를 시험하였다. 격자 상에 위치시킨 경우, 래트는 주위를 돌아다려고 하고, 때때로 발을 격자 상에 위치시키기보다 격자 틈을 통해서 위치시킬 것이다 ("풋 폴트"). 풋 폴트 횟수를 1분 간격으로 측정하였다.
풋 폴트 횟수는 MCAO로 인한 래트의 인지 손상의 지표이고, 풋 폴트 횟수가 적을수록 인지 손상이 덜 된 것이다. 도 5에 나타난 바와 같이, 식염수 처치된 래트 (20.2 ± 0.8 풋 폴트) 및 펩티드 IX 처치된 래트 (20.1 ± 2.1 풋 폴트)에 비해, 펩티드 ID가 풋 폴트 프로토콜에서의 래트 동작을 유의하게 개선하였다 (11.2 ± 1.1 풋 폴트).
실시예
5: 양측 신장 허혈 검정
60마리 수컷 C57/BL6 마우스 (약 25 g; 찰스 리버 래버레이토리스(Charles River Laboratories))를 케타민 (150 mg/kg) 및 크실라진 (15 mg/kg) i.p.로 마취시켰다. 각각의 동물을 37℃에서 설정된 항온 블랭킷에 넣고, 중간선 개복 후에, 비외상성 혈관 클램프를 사용하여 신장경을 30분 동안 클램핑하였다. 재관류 후 1분, 6시간 및 12시간에 i.p. 주사를 통해 소정량의 펩티드 ID를 투여하였다. 단일 용량 연구에서, 대조군 (PBS), 1분에 펩티드 IG 1 ㎍/kg, 30분에 펩티드 IG 1 ㎍/kg, 6시간에 펩티드 ID 1 ㎍/kg 또는 6시간에 펩티드 ID 10 ㎍/kg (군 당 12마리 마우스)을 마우스에게 투여하였다. 다중 용량 연구에서, 1분, 6시간 및 12시간에 대조군 (PBS), 펩티드 ID 0.1 ㎍/kg, 펩티드 ID 1 ㎍/kg 또는 펩티드 ID 10 ㎍/kg의 다중 용량을 재관류 내로 마우스에게 투여하였다.
24시간 후에, 마우스를 재마취시키고, 심장 천자에 의해 혈액을 취하였다. 혈장 우레아 및 크레아틴을 신장 기능이상의 지표로 사용하고, 아스파르테이트 아미노트랜스퍼라제를 신장 손상의 지표로 사용하였다. ANOVA 이후 두넷(Dunnett) 시후 시험 비교를 이용하여 데이타를 분석하였다.
각각의 그래프로 나타낸 바와 같은 도 6 및 도 7에 나타낸 바와 같이, 펩티드 ID 1 ㎍/kg 또는 펩티드 ID 10 ㎍/kg은 신장 기능이상 시 상기 생화학적 마커의 감소를 야기하였다.
실시예
6: 창상 치유
창상 치유의 전층 펀치 생검(punch biopsy) 모델을 사용하여 펩티드 ID를 평가하였다. 이 실험에서, 면도하고 털을 제거한 스프라구에-다울레이 래트의 견갑골 부위의 3 cm-너비의 정사각형 코너에 3.5 mm-직경의 전층 피부 창상을 위치시켰다. 펩티드 ID (24 nmol/kg bw, 9 마리 래트) 또는 PBS (9마리 래트)를 10일 동안 매일 피하로 투여하였다. 연속의 디지털 사진으로부터 맹검법으로 측정된 개방 창상 면적은 도 8에 나타낸 바와 같이 펩티드 ID를 투여한 동물에서 더 빠른 치유를 나타냈다.
실시예
7: 인지 향상
래트에서의 신규한 물체 인지 패러다임을 이용하여 이미 경험한 물체에 대한 이들의 회상력을 평가하였다. 구체적으로, 성체 위스타(Wistar) 래트를 신규한 시험 물체에 노출시킨 다음, 24시간 후에 상기 물체에 다시 노출시켰다. 동물을 다음을 투여하는 5개의 군으로 구분하였다: (1) 비히클 투여, (2) 시험 1시간 전에 양성 대조군으로서 갈란타민 (3 mg/kg i.p.) 투여, (3) 신규한 물체에 대한 1차 노출 3시간 후에 펩티드 ID (24 nmol/kg bw i.p.) 투여, (4) 훈련 전 5일 동안 및 훈련 후 바로 다음날까지 계속 1일 2회씩 펩티드 ID (24 nmol/kg bw i.p.) 투여, 및 (5) 신규한 물체에 대한 1차 노출 1시간 전에 펩티드 ID (24 nmol/kg bw i.p.) 투여.
도 9에 나타낸 바와 같이, 2군 내지 4군의 래트는 1군 및 5군의 래트와 비교하여 시험에서 신규한 물체에 대한 개선된 인지를 나타냈다. 상기 결과는 펩티드 ID가 기억 획득의 통합기에 영향을 미칠 수 있음을 시사한다.
실시예
8:
시스플라틴
유도성
신병증
암 화학요법제, 예컨대 시스플라틴 (CDDT)은 다른 독성 중에서도 신장 손상을 유도하는 것으로 알려져 있다. 시스플라틴-유도성 신병증으로부터 래트를 보호하는 펩티드 IC의 능력은 5주 동안 주 2회씩 CDDT 2 mg/kg을 복막내 투여함으로써 평가하였다. 동시에, 펩티드 IC는 5주 동안 1주 3회씩 0.4 ㎍/kg의 용량으로 투여하였다. 신장 기능은 요 생성 부피를 측정함으로써 평가하였다. 도 10에 나타낸 바와 같이, 펩티드 IC와의 병행 치료는 CDDT로 인한 신장 기능이상에 대해 보호하였다.
또한, CDDT는 다른 독성 중에서도 말초 신경병증을 유도하는 것으로 알려져 있다. 신장 기능에 대해 상기 기재된 실험 디자인에 따라, 말초 신경병증에 대해 보호하는 펩티드 IC의 능력을 또한 평가하였다. CDDT 2 mg/kg을 5주 동안 주 2회씩 복막내 투여하였다. 동시에, 펩티드 IC는 5주 동안 주 3회씩 0.4 ㎍/kg의 용량으로 투여하였다. 신경병증은 래트의 발을 따뜻한 표면에 접촉시킨 후 발을 움츠리기까지의 지체 기간인 가열판 잠재기(hotplate latency)에 따라 평가하였다. 도 11에 나타낸 바와 같이, 병행 치료는 말초 신경병증의 출현을 예방하였다.
실시예
9: 피질 종양 이식
피질 종양 이식 연구는 문헌 [Lampson et al. Cancer Res. 53:176-82:1993]의 프로토콜에 따라 수행하여 종양 성장에 있어서 펩티드 ID의 효과를 측정하였다.
상기 프로토콜에 따라, 수컷 CD 피셔(fisher) 래트를 마취시키고, 이들의 오른쪽 두피를 면도하고, 소독제로 세척하였다. 이어서, 우측두 뇌성 피질 위에 있는 두피에 작은 절개를 만들었다. 경질막은 천공하지 않으면서 두개관을 통해 1 mm 구멍을 뚫었다. 무균 조건 하에, 5 ㎕ 중의 살아있는 50,000개 9L/LacZ 신경교육종 세포를 정밀 해밀톤(Hamilton) 시린지에 부착된 22게이지 니들을 통해 천천히 주사하였다. 이어서, 골 왁스를 천공 부위에 도포하고, 피부를 봉합하고, 예방 용량의 항셍제를 i.p. 투여하였다. 대조군 래트에게 매일 i.p. 식염수 주사를 제공하였다. 펩티드 ID로 처치된 래트에게는 25일 동안 매일 30 ㎍/kg i.p. 주사를 투여하였다. 이식 후 25일에, 동물을 마취시키고, 뇌를 2% 파라포름알데히드로 관류-고정시켰다. 이어서, 뇌를 적출하고, 뇌 매트릭스 장치 상에서 관상면을 1 mm 두께로 절단하고, 종양 매스 크기를 면적측정 방법으로 측정하였다.
도 12는 펩티드 ID가 상기 모델에서 피질 종양의 추가 성장을 억제하였음을 입증한다. 식염수 처치된 래트에서의 종양의 상대 부피는 0.4 ㎤ 초과로 성장한 반면, 펩티드 ID 처치된 래트에서의 종양은 종양 부피에 있어서 성장을 경험하지 않았다.
실시예
10: 9L
신경교육종
이식 모델.
상기 기재된 문헌 [Lampson et al. Cancer Res. 53:176-82:1993]의 프로토콜에 따라, 해밀톤 시린지를 사용하여 LacZ 유전자로 형질감염된 9L 신경교육종 세포를 CD 피셔 래트에 이식하였다. 10 마이크로리터 중 100,000개 세포를 우측 미상 내에 주사하였다.
이식 후 2주에, 동물들을 일일 복막내 주사를 위해 3개의 군으로 나누었다: 하나의 군에는 짧은 혈장 반감기를 갖는 펩티드 ID를 투여하고, 또다른 군에는 펩티드 IW (펩티드 IC의 peg화된 형태)를 투여하고, 제3 군에는 식염수를 투여하였다. 펩티드를 25 nmole/체중 kg의 용량으로 제공하였다. 3주 후에, 동물들을 희생시키고, 연속 1 mm 두께의 관상면을 뇌를 통해 절단하고, 5-브로모-4-클로로-3-인돌릴-[베타]-D-갈락토피라노시드 (Xgal)와 함께 인큐베이션하였다. 종양 세포 (LacZ 유전자 함유)는 Xgal을 진청색 착색으로 대사시켰고, 이는 종양 범위에 제한되었다. 고해상도 디지털 영상이 얻어지고, 청색이 착색된 면적을 면적측정 방법을 이용하여 측정하였다. 데이타는 종양 침윤의 총 면적으로 표현된다.
그 결과, 도 13에 나타낸 바와 같이, 반감기가 더 긴 펩티드 (펩티드 IW)로 처치된 군에서 종양 크기가, 반감기가 짧은 펩티드 (펩티드 ID)로 이식일부터 시작하여 희생 시까지 매일 계속적으로 동물들을 매일 처치하는 경우에 얻어지는 것과 동일한 총 면적까지 현저하게 감소됨이 나타났다. 한편, 이식 후 2주에는 더 짧게 작용하는 펩티드 (펩티드 ID)를 투여한 군의 평균 면적이 식염수 군에서보다 더 작기는 하지만, 이것은 유의하게 상이하지는 않았다.
추가로, 도 14는 식염수, 펩티드 ID 및 펩티드 IW 처치된 래트의 뇌의 비교 사진을 제시한다. 명확하게 볼 수 있는 바와 같이, 가장 큰 종양 (암부)은 식염수 처치된 래트에서 나타난다. 매일 펩티드 ID로 처치된 래트는 상당히 더 작은 종양을 갖지만, 2주 후에는 펩티드 IW로 처치된 래트가 최선의 결과를 나타냈다.
이러한 발견은 9L 신경교육종 세포주의 퇴화를 야기하는 펩티드의 능력과 일치한다.
실시예
11: (예측성) 암 악액질에서의 치료.
암의 악액질 증후를 처리하기 위한 펩티드의 능력은 다음의 프로토콜에 따라 입증할 수 있다.
체중이 약 200 g인 래트에게 108 AH-130 간암 세포를 복막내로 접종할 것이다. 동시에, 1군의 래트를 약 .10 내지 2.0 ㎍/kd/일의 치료 유효 범위 내에 있을 용량으로 관심 펩티드, 예컨대 펩티드 ID 또는 펩티드 IW로 처치할 것이다. 제2 군은 플라시보로 처치할 것이다. 제16일에, 래트를 희생시킬 것이다. 대상체 래트의 음식 섭취 및 보행 활성은 접종 이전에 및 제11일에 평가할 것이다. 체중 및 체성분은 제0일 및 제16일 희생 후에 NMR-스캔으로 평가할 것이다.
플라시보 처치된 래트와 비교하여, 제1 군은 본 발명의 방법에 따른 펩티드로 처치되어 지방 및 근육량 소모가 더 적게 나타날 것으로 기대될 것이다. 또한, 펩티드 처치된 래트의 음식 섭취 및 보행 활성이 개선될 것이다.
실시예
12: 히스타민 유도성 귀 염증.
히스타민의 전-염증성 영향을 길항시키는, 본 발명의 치료 방법에 유용한 펩티드의 능력을 문헌 [Brand et al. "Tea tree oil reduces histamine-induced oedema in murine ears," Inflamm. Res. 51 (2002) 283-289]에 개시된 히스타민-유도성 부종의 마우스 모델에서 평가하였다. 간단하게는, 24마리 스프라구에 다울레이 래트 (수컷, 250 gm)를 연구에 사용하였다. 히스타민 유발시험 이전에, 각각의 래트를 마취시키고, 래트 귀의 두께를 스프링 하중식 마이크로미터를 이용하여 측정하였다. 히스타민 디포스페이트 60 mg/ml 용액 20 ul를 래트의 귀에 진피내로 주사하고, 30초 후에 래트에게 (1) 30 ㎍/kg 펩티드 ID IV (12마리 래트) 또는 (2) 식염수 IV (12마리 래트)를 투여하였다. 이어서, 히스타민 디포스페이트 60 mg/ml 용액 20 ul를 래트의 다른쪽 귀에 진피내로 주사하였다. 이 후, 래트 귀의 두께를 히스타민 유발시험 후 15, 30, 45 및 60분에 캘리퍼(caliper)를 이용하여 측정하였다.
도 15에서 볼 수 있는 바와 같이, 펩티드 ID는 식염수에 비해 히스타민 유발시험과 관련된 부종의 양을 감소시켰다.
실시예
13: 히스타민 유도성
팽진
형성
진피내 히스타민 투여에 의해 유도되는 혈장 혈관외유출 (팽진)을 감소시키는 펩티드 ID의 능력을 래트에서 평가하였다. 가시적인 혈관 누출 마커를 제공하기 위해 동물에게 에반스 블루(Evans Blue) 염료 (알부민에 단단하게 결합함)를 미리 투여하였다. 펩티드 IG 활성의 지속성을 측정하기 위해, 펩티드 ID 투여 (30 ㎍/kg, 정맥내로 투여함) 후 다양한 시점에서, 진피내 용량의 히스타민 0.12 ㎍을 투여하고, 염료 누출 범위는 히스타민 배치 후 15분 (팽진 표면 면적이 가장 큰 시점)에 얻어진 디지털 사진 상에서 수행되는 면적측정법에 의해 정량화하였다. 각각의 동물은, 히스타민 투여가 후속 반응에 영향을 미치는 것을 피하기 위해 단일 시점에서만 시험하였다. 단일-용량 펩티드 ID 투여는 팽진 형성을 저해하는 것으로 밝혀졌고, 이러한 저해 효과는 단일 투여 후 24시간 내에 검출가능하였으며, 도 16에 나타낸 바와 같이, 식염수 대 펩티드 ID-처치된 동물의 면적에 있어서의 차이를 나타냈다.
실시예
14: 히스타민 유도성
팽진
형성
이소플루란 마취 하에, 12마리 스프라구에-다울레이 래트의 복부를 면도하고 털을 제거하였다. 이어서, 에반스 블루의 희석 용액 (식염수 중 30 mg/ml, 1 ml/kg bw)을 각각의 래트에게 정맥내로 (내경정맥을 통해) 주사하였다. 5분 후에, 6개의 소용량의 히스타민 (히스타민 디포스페이트, 20 마이크로리터를 진피내로 투여)을 각 래트의 복부 상에서 직사각형 패턴으로 진피내로 투여하였다. 15분 후, 팽진이 그의 최대 크기에 도달할 때, 상기 팽진의 사진을 찍고, 수포 면적을 디지털 면적측정법으로 측정하였다. 각종 펩티드의 효능을 시험하기 위해, 히스타민 주사 직후에, 관심 펩티드를 래트에게 정맥내로 투여하였다. 펩티드를 시험하고, 그 결과를 하기에 기록하였다.
A.
에리트로포이에틴.
히스타민 유발시험 시에 식염수 또는 EPO 10 ㎍m/kg을 래트에게 투여하였다. 도 17은 EPO 처치된 래트의 팽진 면적 (병변 면적) (약 .4 ㎠)이 식염수 처치된 동물의 병변 면적 (약 .8 ㎠)의 절반이었음을 도시한다.
히스타민 유발시험 시에 식염수, 펩티드 IY (30 ㎍/kg), 펩티드 ID (30 ㎍/kg) 또는 펩티드 IW (30 ㎍/kg)를 래트에게 투여하였다. 도 18은 펩티드 ID 및 펩티드 IW 처치된 래트의 팽진 면적 (병변 면적) (각각 약 .35 ㎠ 및 .3 ㎠)이 식염수 및 펩티드 IY 처치된 동물의 병변 면적 (각각 약 .6 ㎠)의 절반이었음을 도시한다. 이것은 히스타민 및 히스타민 관련 염증성 반응의 조절에서의 펩티드 ID 및 IW의 효능을 입증할 뿐만 아니라, 펩티드 IY가 소염 활성을 나타내지 않기 때문에 펩티드의 효능에 있어서 상기-개시된 모티프의 중요성을 또한 입증한다.
C. 펩티드 IW, 레트로 인버소(Retro Inverso) 펩티드 IC (펩티드 IZ, 서열 300, ), 펩티드 ID 및 스크램블 펩티드 IZ (펩티드 JA (서열 301) ).
히스타민 유발시험 시에 식염수, 펩티드 JA (30 ㎍/kg), 펩티드 IZ (30 ㎍/kg), 펩티드 IW (30 ㎍/kg) 또는 펩티드 ID (30 ㎍/kg)를 래트에게 투여하였다. 도 19는 펩티드 IW, ID 및 IZ 처치된 래트의 팽진 면적 (병변 면적) (각각 약 .3 ㎠, .35 ㎠ 및 .4 ㎠)이 식염수 및 펩티드 JA 처치된 동물의 병변 면적 (각각 약 .6 ㎠)보다 더 작음을 도시한다.
실시예
15:
욕창성
궤양 검정
욕창성 궤양 (욕창) 검정은 문헌 [Pierce et al., Selective A2A adenosine receptor activation reduces skin pressure ulcer formation and inflammation, Am J Physiol Heart Circ Physiol 281:67-74, 2001]의 개시에 따라 24마리 성체 스프라구에-다울레이 래트에서 수행하였다. 간단하게는, 강자성 스틸판을 래트 피부의 배측부(dorsal region) 하에 이식하였다. 직사각형의 영구 자석을, 상기 판이 그 아래에 이식되어 있는 피부 영역에 적용하여, 판과 자석 사이의 피부를 압착하였다. 이러한 압착은 피부로의 혈류를 감소시켜 허혈을 야기하였다. 래트를 72-시간 동안 허혈-재관류 주기 (2시간 허혈 + .5시간 재관류)에 적용하였다. 각 래트에 있는 창상 면적을 측정하고, 이후에 래트를 식염수로 처치하하거나, 펩티드 ID 30 ㎍/kg을 sc로 2회 투여하거나 (1회째는 첫번째 허열 기간에 시작하고, 2회째는 24시간 이후에 시작함), 펩티드 ID 30 ㎍/kg을 매일 sc로 투여하거나, 또는 EPO를 매일 투여하였다. 각각의 래트에 있는 창상 면적을 12일 동안 매일 측정하였다. 도 20은 펩티드 ID 및 EPO가 창상 크기를 감소시키고, 펩티드 IG의 매일 투여가 창상 크기를 가장 작게 하였음을 입증한다.
실시예
16 (예측
실시예
): 피부 단자 시험
초기 히스타민 피부 단자 시험은 기준을 결정하기 위해 수행하였다. 피부 단자 시험은 반횡와위의 환자에서 양쪽 전완의 수장 측면 (손목의 원위 피부선 위 5 cm 초과)에서 수행하였다. 전완을 알코올로 세정하고 건조시켰다. 펜을 사용하여, 히스타민 및 음성 대조군을 위한 피부 시험 예측 부위를 적어도 서로 2 cm 떨어도록 표시하고 표지하였다. 한 방울의 히스타민 디히드로클로라이드 (10 mg/ml) 또는 음성 대조군을 적절한 표시에 넣고, 그 후 멸균 란셋을 각각의 방울을 통해 90° 각도로 도입하고 회수하였다. 이어서, 투여 15분 후에 홍반 및 팽진 형성의 존재에 대해 상기 부위를 관찰하였다. 팽진 사진을 찍었고, 이후 팽진 크기는 디지털 면적측정법으로 측정하였다.
상기 프로토콜을 이용하여, 적어도 3시간 후의 시점에 피부 단자 시험을 다시 수행하였다. 상기 언급된 펩티드 중 하나를 히스타민 유발시험 투여 전 15분 내지 2시간에, 히스타민 유발시험 투여 시에, 또는 히스타민 유발시험 후 1 내지 60분에 환자에게 투여하여, 히스타민 유도성 염증을 예방, 관리/개선 또는 치료하는 펩티드의 능력을 각각 측정할 수 있다. 예를 들어, 히스타민 단자 시에, 환자에게 해당 용량의 펩티드 ID를 IV 또는 sc 주사에 의해 제공할 수 있다. 펩티드 ID로의 처치 후 팽진 면적이 약 50% 감소할 것으로 예상된다.
실시예
17: 혈액생성 스크리닝 검정에서의 방사성 완화 활성
혈액생성계에서 방사능 제제의 효과를 완화시키는, 본 발명의 치료 방법에 유용한 펩티드의 능력은 방사선 손상된 쥣과동물 모델에서 평가하였다. 간단하게는, 80마리 C57BL/6 마우스 (50% 암컷 및 50% 수컷, 15 내지 28 gm)를 2개의 군으로 나누어 본 연구에 사용하였다.
2개의 군 모두에서, 137C 방사선 공급원 (감마세포(GammaCell) 40; 캐나다 온타리오주 카나타 소재의 노르디온 인터내셔널(Nordion International))으로부터의 감마 방사선의 단일한 균일 전신 선량으로서 노출 속도 65-69 cGy/분 +/- 2.5 cGy으로 마우스에게 방사선을 조사하였다.
A 군에는 LD70/30 선량의 방사선 (796 cGy)을 수용시키며, 그때 마우스 중 20마리에게는 방사선 조사 후 24시간에 펩티드 ID (30 ug/kg 피하로)를 투여한 다음, 29일 동안 1일 1회씩 투여하였다. 나머지 20마리의 마우스 (대조군)에는 방사선 조사 후 24시간에 PBS (피하)를 투여한 다음, 29일 동안 1일 1회씩 투여하였다.
B 군에는 LD90/30 선량의 방사선 (831 cGy)을 수용시키며, 그때 마우스 중 20마리에게는 방사선 조사 후 24시간에 펩티드 ID (30 ug/kg 피하로)를 투여한 다음, 29일 동안 1일 1회씩 투여하였다. 나머지 20마리의 마우스 (대조군)에는 조사 후 24시간에 PBS (피하)를 투여한 다음, 29일 동안 1일 1회씩 투여하였다.
조기 안락사 징후가 나타날 때까지 1일 1회, 그 이후 제30일까지는 2회/1일로 상기 마우스의 생존을 모니터링하였다.
도 21에 나타낸 바와 같이, 피하 투여된 펩티드 ID를 투여한 마우스의 30-일 생존율 및 총 생존 시간이, PBS를 투여한 마우스에 비해 유의하게 증가하였다. 특히, 796 cGy에서 처치군 마우스는 대조군의 10% 생존율에 비해 45% 생존율을 나타내고, 831 cGy에서 처치군 마우스는 대조군의 5% 생존율에 비해 20% 생존율을 나타냈다.
실시예
18: 위장 스크리닝 검정에서의 방사성 완화 활성
위장계에서 방사능 제제의 효과를 완화시키는, 본 발명의 치료 방법에 유용한 펩티드의 능력은 방사선 손상된 쥣과동물 모델에서 평가하였다. 간단하게는, 30마리 C57BL/6 마우스 (수컷, 20 내지 30 gm)를 본 연구에 사용하였다.
300 kV, 10 mA에서 작동하는 판탁(Pantak) HF320 X-선 (영국 리딩 소재의 아그파 NDT 엘티디.(Agfa NDT Ltd.))을 이용하여 마우스에게 방사선을 조사하였다. X-선 튜브를 추가로 여과하여 2.3 mm Cu 반가층 (HVL)의 방사선질을 제공하였다. 마우스의 머리, 흉부 및 앞다리를 차폐하여 이들의 골수를 보호하여 GI 반응을 선별하였다. 마우스를 지그(jig)에 감금하고, X-선 튜브의 초점으로부터 초점이 모이는 700 mm 거리에 위치시켰다. 마우스를 방사선 15 Gy에 노출시키기에 충분한 기간 동안 75.5 cGy/분 (차폐되지 않음) 및 70.0 cGy/분 (차폐됨)의 선량율로 방사선을 전달하였다.
방사선 조사 후 24시간에, 마우스 중 15마리에게 펩티드 ID (30 ug/kg 피하)를 투여한 다음, 연구 기간 동안 1일 1회씩 투여하고, 나머지 15마리의 마우스 (대조군)에게는 PBS (피하)를 투여한 다음, 연구 기간 동안 1일 1회씩 투여하였다.
설사 및 조기 안락사 징후가 나타날 때까지는 1일 1회, 그 이후에는 1일 2회씩 마우스의 체중을 측정하고 모니터링하였다.
도 22에 나타낸 바와 같이, 피하로 투여된 펩티드 ID를 수용한 마우스의 20일 생존율은 PBS를 수용한 마우스보다 유의하게 더 컸다 (처치군의 6마리 마우스 대 대조군에서 1마리).
본 발명은 본 발명의 개별 측면에 대한 단일 예시로서 의도된 기재된 특정 실시양태에 의해 그 범위가 제한되지 않고, 기능적으로 동일한 방법 및 성분이 본 발명의 범위 내에 있다. 실제, 본원에 도시되고 기재된 것 이외에도, 본 발명의 각종 변형이 전술한 설명 및 첨부되는 도면으로부터 당업자에게 명백할 것이다. 상기 변형은 첨부된 특허청구범위 내에 있는 것으로 의도된다.
본원에 인용된 모든 참조 문헌은 모든 목적을 위해 그 전문이 본원에 참조로 포함된다.
SEQUENCE LISTING
<110> ARAIM PHARMACEUTICALS, INC.
<120> TISSUE PROTECTIVE PEPTIDES AND PEPTIDE ANALOGS FOR PREVENTING AND
TREATING DISEASES AND DISORDERS ASSOCIATED WITH TISSUE DAMAGE
<130> 12110-007-228
<140> PCT/US2009/000424
<141> 2009-01-22
<150> US 61/062,012
<151> 2008-01-22
<150> US 61/062,022
<151> 2008-01-22
<150> US 61/062,045
<151> 2008-01-22
<150> US 61/133,912
<151> 2008-07-03
<150> US 61/203,890
<151> 2008-12-30
<160> 305
<170> PatentIn version 3.5
<210> 1
<211> 166
<212> PRT
<213> Artificial Sequence
<220>
<223> Recombinant human erythropoietin (EPO) comprising mutations N24K,
N38K, N83K
<220>
<221> misc_feature
<222> (166)..(166)
<223> Xaa is any amino acid
<400> 1
Ala Pro Pro Arg Leu Ile Cys Asp Ser Arg Val Leu Glu Arg Tyr Leu
1 5 10 15
Leu Glu Ala Lys Glu Ala Glu Lys Ile Thr Thr Gly Cys Ala Glu His
20 25 30
Cys Ser Leu Asn Glu Lys Ile Thr Val Pro Asp Thr Lys Val Asn Phe
35 40 45
Tyr Ala Trp Lys Arg Met Glu Val Gly Gln Gln Ala Val Glu Val Trp
50 55 60
Gln Gly Leu Ala Leu Leu Ser Glu Ala Val Leu Arg Gly Gln Ala Leu
65 70 75 80
Leu Val Lys Ser Ser Gln Pro Trp Glu Pro Leu Gln Leu His Val Asp
85 90 95
Lys Ala Val Ser Gly Leu Arg Ser Leu Thr Thr Leu Leu Arg Ala Leu
100 105 110
Gly Ala Gln Lys Glu Ala Ile Ser Pro Pro Asp Ala Ala Ser Ala Ala
115 120 125
Pro Leu Arg Thr Ile Thr Ala Asp Thr Phe Arg Lys Leu Phe Arg Val
130 135 140
Tyr Ser Asn Phe Leu Arg Gly Lys Leu Lys Leu Tyr Thr Gly Glu Ala
145 150 155 160
Cys Arg Thr Gly Asp Xaa
165
<210> 2
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> EPO structures: (1) loop AB and N-terminal portion of helix B
<400> 2
Asn Ile Thr Val Pro Asp Thr Lys Val Asn Phe Tyr Ala Trp Lys Arg
1 5 10 15
Met Glu Val Gly
20
<210> 3
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> EPO structures: (2) C-terminal portion of helix B
<400> 3
Gln Gln Ala Val Glu Val Trp Gln Gly Leu Ala Leu Leu Ser Glu Ala
1 5 10 15
Val Leu Arg Gly Gln Ala Leu Leu Val
20 25
<210> 4
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> EPO structures: (3) a portion of the A-B loop consisting of a
small cysteine loop and a Beta-pleated sheet
<400> 4
Gly Cys Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val Pro Asp
1 5 10 15
Thr Lys Val Asn
20
<210> 5
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural Motif A
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(7)
<223> Xaa is any amino acid or a bond
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is a hydrophobic amino acid
<400> 5
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 6
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural Motif A
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(3)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is a hydrophobic amino acid
<400> 6
Xaa Xaa Xaa Xaa
1
<210> 7
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural Motif A
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is a hydrophobic amino acid
<400> 7
Xaa Xaa Xaa Xaa Xaa
1 5
<210> 8
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural Motif A
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(4)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is negatively charged amino acid
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is a hydrophobic amino acid
<400> 8
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 9
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural Motif A
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(5)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (7)..(7)
<223> Xaa is a hydrophobic amino acid
<400> 9
Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 10
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural Motif A
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(6)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (7)..(7)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is a hydrophobic amino acid
<400> 10
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 11
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural Motif A
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(7)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is a hydrophobic amino acid
<400> 11
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 12
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Variation of structural motif A
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(7)
<223> Xaa is any amino acid or a bond
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is a polar amino acid
<400> 12
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 13
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Variation of structural motif
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a polar amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(7)
<223> Xaa is any amino acid or a bond
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is a hydrophobic amino acid
<400> 13
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 14
<211> 23
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide D
<400> 14
Ala Pro Pro Arg Leu Ile Cys Asp Ser Arg Val Leu Glu Arg Tyr Leu
1 5 10 15
Leu Glu Ala Lys Glu Ala Glu
20
<210> 15
<211> 29
<212> PRT
<213> Artificial Sequence
<220>
<223> Formula I of structural motif A
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Cys (C) or Pro (P)
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is Asp (D) or Pro (P)
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Ser (S) or Arg (R)
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Arg (R) or Leu (L)
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Val (V) or Ile (I)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is Leu (L) or Cys (C)
<220>
<221> misc_feature
<222> (7)..(7)
<223> Xaa is Glu (E) or Asp (D)
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is Arg (R) or Ser (S)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is Tyr (Y) or Arg (R)
<220>
<221> misc_feature
<222> (10)..(10)
<223> Xaa is Leu (L) or Val (V)
<220>
<221> misc_feature
<222> (11)..(11)
<223> Xaa is Leu (L) or Ala (A)
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (13)..(13)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (14)..(17)
<223> Xaa is any amino acid or a bond
<220>
<221> misc_feature
<222> (18)..(18)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (19)..(19)
<223> Xaa is Ala (A) or Leu (L)
<220>
<221> misc_feature
<222> (20)..(20)
<223> Xaa is Glu (E) or Lys (K)
<220>
<221> misc_feature
<222> (21)..(21)
<223> Xaa is Asn (N), Glu (E), or Lys (K)
<220>
<221> misc_feature
<222> (22)..(22)
<223> Xaa is Ile (I) or Ala (A)
<220>
<221> misc_feature
<222> (23)..(23)
<223> Xaa is Thr (T), Glu (E), or Gly (G)
<220>
<221> misc_feature
<222> (24)..(24)
<223> Xaa is Thr (T), Asn (N), or Ala (A)
<220>
<221> misc_feature
<222> (25)..(25)
<223> Xaa is Gly (G) or Ile (I)
<220>
<221> misc_feature
<222> (26)..(26)
<223> Xaa is Cys (C) or Thr (T)
<220>
<221> misc_feature
<222> (27)..(27)
<223> Xaa is Ala (A) or Thr (T)
<220>
<221> misc_feature
<222> (28)..(28)
<223> Xaa is Glu (E) or Gly (G)
<220>
<221> misc_feature
<222> (29)..(29)
<223> Xaa is His (H) or Cys (C)
<400> 15
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
20 25
<210> 16
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide F
<400> 16
Cys Asp Ser Arg Val Leu Glu Arg Tyr Leu Leu Glu Ala Lys Glu Ala
1 5 10 15
Glu Asn Ile Thr Thr Gly Cys Ala Glu His
20 25
<210> 17
<211> 28
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide G
<400> 17
Pro Pro Arg Leu Ile Cys Asp Ser Arg Val Leu Glu Arg Tyr Leu Leu
1 5 10 15
Glu Ala Lys Glu Ala Glu Asn Ile Thr Thr Gly Cys
20 25
<210> 18
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide H
<400> 18
Ala Asp Arg Glu Leu Glu Lys Ile Gly Ala
1 5 10
<210> 19
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif B
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is a hydrophobic amino acid
<400> 19
Xaa Xaa Xaa Xaa
1
<210> 20
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif B
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is a hydrophobic amino acid
<400> 20
Xaa Xaa Xaa Xaa
1
<210> 21
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Variation of Structural motif B
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is a polar amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is a hydrophobic amino acid
<400> 21
Xaa Xaa Xaa Xaa Xaa
1 5
<210> 22
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Variation of Structural motif B
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is a polar amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is a hydrophobic amino acid
<400> 22
Xaa Xaa Xaa Xaa Xaa
1 5
<210> 23
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif B
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is a polar amino acid or a bond
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is a hydrophobic amino acid
<400> 23
Xaa Xaa Xaa Xaa Xaa
1 5
<210> 24
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif B
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a hydrophobic amino acid
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is a polar amino acid or a bond
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is hydrophobic amino acid
<400> 24
Xaa Xaa Xaa Xaa Xaa
1 5
<210> 25
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural Motif B
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Ser (S)
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is Arg (R)
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Val (V)
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Leu (L)
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Glu (E)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is Arg (R)
<220>
<221> misc_feature
<222> (7)..(7)
<223> Xaa is Tyr (Y)
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is Leu (L)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is Leu (L)
<220>
<221> misc_feature
<222> (10)..(10)
<223> Xaa is Glu (E)
<220>
<221> misc_feature
<222> (11)..(11)
<223> Xaa is Ala (A)
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (13)..(13)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (14)..(14)
<223> Xaa is Ala (A)
<220>
<221> misc_feature
<222> (15)..(15)
<223> Xaa is Glu (E)
<220>
<221> misc_feature
<222> (16)..(16)
<223> Xaa is Asn (N)
<220>
<221> misc_feature
<222> (17)..(17)
<223> Xaa is Ile (I)
<220>
<221> misc_feature
<222> (18)..(18)
<223> Xaa is Thr (T)
<220>
<221> misc_feature
<222> (19)..(19)
<223> Xaa is Thr (T)
<220>
<221> misc_feature
<222> (20)..(20)
<223> Xaa is Gly (G)
<220>
<221> misc_feature
<222> (21)..(21)
<223> Xaa is Cys (C)
<220>
<221> misc_feature
<222> (22)..(22)
<223> Xaa is Ala (A)
<220>
<221> misc_feature
<222> (23)..(23)
<223> Xaa is Glu (E)
<220>
<221> misc_feature
<222> (24)..(24)
<223> Xaa is His (H)
<400> 25
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
20
<210> 26
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif B, Peptide I
<400> 26
Ser Arg Val Leu Glu Arg Tyr Leu Leu Glu Ala Lys Glu Ala Glu Asn
1 5 10 15
Ile Thr Thr Gly Cys Ala Glu His
20
<210> 27
<211> 23
<212> PRT
<213> Artificial Sequence
<220>
<223> Formula III of structural motif B
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Pro (P), Lys (K), or Ser (S)
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is Pro (P), Glu (E), or Gln (Q)
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Arg (R), Ala (A), or Pro (P)
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Leu (L), Glu (E), or Trp (W)
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Ile (I), Asn (N), or Glu (E)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is Cys (C), Ile (I), or Pro (P)
<220>
<221> misc_feature
<222> (7)..(7)
<223> Xaa is Asp (D), Thr (T), Leu (L), or Ala (A)
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is Ser (S), Thr (T), Gln (Q), or Asp (D)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is Arg (R), Gly (G), or Leu (L)
<220>
<221> misc_feature
<222> (10)..(10)
<223> Xaa is Val (V), Cys (C), His (H), or Glu (E)
<220>
<221> misc_feature
<222> (11)..(11)
<223> Xaa is Leu (L), Ala (A), Val (V)
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (13)..(13)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (14)..(14)
<223> Xaa is Tyr (Y), Cys (C), Ala (A), or Ile (I)
<220>
<221> misc_feature
<222> (15)..(15)
<223> Xaa is Leu (L), Ser (S), Val (V), or Gly (G)
<220>
<221> misc_feature
<222> (16)..(16)
<223> Xaa is Leu (L), Ser (S), or Ala (A)
<220>
<221> misc_feature
<222> (17)..(17)
<223> Xaa is Glu (E), Asn (N), or Gly (G)
<220>
<221> misc_feature
<222> (18)..(18)
<223> Xaa is Ala (A), Glu (E), or Leu (L)
<220>
<221> misc_feature
<222> (19)..(19)
<223> Xaa is Lys (K), Asn (N), or Arg (R)
<220>
<221> misc_feature
<222> (20)..(20)
<223> Xaa is Glu (E), Ile (I), or Ser (S)
<220>
<221> misc_feature
<222> (21)..(21)
<223> Xaa is Ala (A), Thr (T), or Leu (L)
<220>
<221> misc_feature
<222> (22)..(22)
<223> Xaa is Glu (E), Val (V), or Thr (T)
<220>
<221> misc_feature
<222> (23)..(23)
<223> Xaa is Asn (N), Pro (P), or Thr (T)
<220>
<221> misc_feature
<222> (24)..(24)
<223> Xaa is Ile (I), Asp (D), or Leu (L)
<400> 27
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa Xaa
20
<210> 28
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif B, Peptide J
<400> 28
Pro Pro Arg Leu Ile Cys Asp Ser Arg Val Leu Glu Arg Tyr Leu Leu
1 5 10 15
Glu Ala Lys Glu Ala Glu Asn Ile
20
<210> 29
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif B, Peptide K
<400> 29
Lys Glu Ala Glu Asn Ile Thr Thr Gly Cys Ala Glu His Cys Ser Leu
1 5 10 15
Asn Glu Asn Ile Thr Val Pro Asp
20
<210> 30
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif B, Peptide L
<400> 30
Ser Gln Pro Trp Glu Pro Leu Gln Leu His Val Asp Lys Ala Val Ser
1 5 10 15
Gly Leu Arg Ser Leu Thr Thr Leu
20
<210> 31
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Formula IV of structural motif B
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is His (H)
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is Cys (C)
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Ser (S)
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Leu (L)
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Ala (A) or Asn (N)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is Pro (P) or Glu (E)
<220>
<221> misc_feature
<222> (7)..(7)
<223> Xaa is Pro (P) or Asn (N)
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is Arg (R) or Ile (I)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is Leu (L) or Thr (T)
<220>
<221> misc_feature
<222> (10)..(10)
<223> Xaa is Ile (I) or Val (V)
<220>
<221> misc_feature
<222> (11)..(11)
<223> Xaa is Cys (C) or Pro (P)
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (13)..(13)
<223> Xaa is a polar amino acid
<220>
<221> misc_feature
<222> (14)..(14)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (15)..(15)
<223> Xaa is Val (V)
<220>
<221> misc_feature
<222> (16)..(16)
<223> Xaa is Leu (L) or Asn (N)
<220>
<221> misc_feature
<222> (17)..(17)
<223> Xaa is Glu (E) or Phe (F)
<220>
<221> misc_feature
<222> (18)..(18)
<223> Xaa is Arg (R) or Tyr (Y)
<220>
<221> misc_feature
<222> (19)..(19)
<223> Xaa is Tyr (Y) or Ala (A)
<220>
<221> misc_feature
<222> (20)..(20)
<223> Xaa is Leu (L) or Trp (W)
<220>
<221> misc_feature
<222> (21)..(21)
<223> Xaa is Leu (L) or Lys (K)
<220>
<221> misc_feature
<222> (22)..(22)
<223> Xaa is Glu (E) or Arg (R)
<220>
<221> misc_feature
<222> (23)..(23)
<223> Xaa is Ala (A) or Met (M)
<220>
<221> misc_feature
<222> (24)..(24)
<223> Xaa is Lys (K) or Glu (E)
<220>
<221> misc_feature
<222> (25)..(25)
<223> Xaa is Glu (E) or Val (V)
<400> 31
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
20 25
<210> 32
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif B, Peptide M
<400> 32
Ala Pro Pro Arg Leu Ile Cys Asp Ser Arg Val Leu Glu Arg Tyr Leu
1 5 10 15
Leu Glu Ala Lys Glu
20
<210> 33
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif B, Peptide N
<400> 33
His Cys Ser Leu Asn Glu Asn Ile Thr Val Pro Asp Thr Lys Val Asn
1 5 10 15
Phe Tyr Ala Trp Lys Arg Met Glu Val
20 25
<210> 34
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif C
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is a charged amino acid residue
<220>
<221> misc_feature
<222> (2)..(5)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is a hydrophobic amino acid residue or Ala
<400> 34
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 35
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif C
<220>
<221> misc_feature
<222> (3)..(5)
<223> Xaa is any amino acid
<400> 35
Arg Ser Xaa Xaa Xaa Leu
1 5
<210> 36
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif C
<220>
<221> misc_feature
<222> (3)..(5)
<223> Xaa is any amino acid
<400> 36
Arg Val Xaa Xaa Xaa Ala
1 5
<210> 37
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif C
<220>
<221> misc_feature
<222> (4)..(5)
<223> Xaa is any amino acid
<400> 37
Arg Val Leu Xaa Xaa Tyr
1 5
<210> 38
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif C
<220>
<221> misc_feature
<222> (4)..(5)
<223> Xaa is any amino acid
<400> 38
Lys Ala Val Xaa Xaa Leu
1 5
<210> 39
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif C
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (4)..(5)
<223> Xaa is any amino acid
<400> 39
Arg Xaa Leu Xaa Xaa Leu
1 5
<210> 40
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif C
<220>
<221> misc_feature
<222> (4)..(5)
<223> Xaa is any amino acid
<400> 40
Arg Ser Leu Xaa Xaa Leu
1 5
<210> 41
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif C, Peptide O
<400> 41
Asp Ser Arg Val Leu Glu Arg Tyr Leu Leu Glu Ala Lys Glu
1 5 10
<210> 42
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif C, Peptide P
<400> 42
Asn Glu Asn Ile Thr Val Pro Asp Thr Lys Val Asn Phe Tyr Ala Trp
1 5 10 15
Lys Arg
<210> 43
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif C, Peptide Q
<400> 43
Gln Leu His Val Asp Lys Ala Val Ser Gly Leu Arg Ser Leu Thr Thr
1 5 10 15
Leu Leu Arg Ala
20
<210> 44
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif C, Peptide R
<400> 44
Arg Val Tyr Ser Asn Phe Leu Arg Gly Lys Leu Lys Leu Tyr Thr Gly
1 5 10 15
Glu Ala
<210> 45
<211> 22
<212> PRT
<213> Artificial Sequence
<220>
<223> Peptide derived from saposin C, Peptide HR
<400> 45
Cys Glu Phe Leu Val Lys Glu Val Thr Lys Leu Ile Asp Asn Asn Lys
1 5 10 15
Thr Glu Lys Glu Ile Leu
20
<210> 46
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> hCNTF AB loop derived Peptide HS
<400> 46
Tyr Val Lys His Gln Gly Leu Asn Lys Asn Ile Asn Leu Asp Ser Val
1 5 10 15
Asp Gly Val Pro
20
<210> 47
<211> 23
<212> PRT
<213> Artificial Sequence
<220>
<223> Neurotrophic peptide consensus sequence of structural motif D
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Leu (L) or Ile (I)
<220>
<221> misc_feature
<222> (2)..(3)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is any amino acid or bond
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Asn (N)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is any amino acid or bond
<220>
<221> misc_feature
<222> (7)..(7)
<223> Xaa is Asn (N)
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (9)..(14)
<223> Xaa is any amino acid or bond
<220>
<221> misc_feature
<222> (15)..(15)
<223> Xaa is Asp (D), Lys (K), Glu (E), or Arg (R)
<220>
<221> misc_feature
<222> (16)..(19)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (20)..(22)
<223> Xaa is any amino acid or bond
<220>
<221> misc_feature
<222> (23)..(23)
<223> Xaa is Ala (A), Leu (L), Ile (I) or Val (V)
<400> 47
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa Xaa
20
<210> 48
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif D, Peptide U
<400> 48
Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val Pro Asp Thr Lys
1 5 10 15
Val
<210> 49
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Cys (C), Glu (E), Ala (A), alpha-amino-gamma-bromobutyric
acid, or homocysteine
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is Arg (R), His (H), Tyr (Y), Leu (L), or Trp (W), or a bond
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Met (M), Phe (F), or Ile (I)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is Asp (D), Glu (E), Ile (I), Leu (L), or Val (V)
<220>
<221> misc_feature
<222> (10)..(10)
<223> Xaa is Cys (C), Lys (K), Ala (A), alpha-amino-gamma-bromobutyric
acid, or homocysteine
<400> 49
Xaa Xaa Xaa Gly Pro Xaa Thr Trp Xaa Xaa
1 5 10
<210> 50
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Cys (C), Glu (E), Ala (A), alpha-amino-gamma-bromobutyric
acid, or homocysteine
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Arg (R), His (H), Tyr (Y), Leu (L), or Trp (W), or a bond
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Met (M), Phe (F), or Ile (I)
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (11)..(11)
<223> Xaa is Asp (D), Glu (E), Ile (I), Leu (L), or Val (V)
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is Cys (C), Lys (K), Ala (A), alpha-amino-gamma-bromobutyric
acid, or homocysteine
<400> 50
Tyr Xaa Xaa Xaa Xaa Gly Pro Xaa Thr Trp Xaa Xaa
1 5 10
<210> 51
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Cys (C)
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Arg (R), His (H), Tyr (Y), Leu (L), or Trp (W), or a bond
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Met (M), Phe (F), or Ile (I)
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (11)..(11)
<223> Xaa is Asp (D), Glu (E), Ile (I), Leu (L), or Val (V)
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is Cys (C)
<400> 51
Tyr Xaa Xaa Xaa Xaa Gly Pro Xaa Thr Trp Xaa Xaa
1 5 10
<210> 52
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Cys (C), Glu (E), Ala (A)
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Arg (R), His (H), Tyr (Y), or a bond
<220>
<221> misc_feature
<222> (6)..(6)
<223> Met (M), Phe (F), or Ile
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is Asp (D) or Val (V)
<220>
<221> misc_feature
<222> (13)..(13)
<223> Xaa is Cys (C), Lys (K), or Ala (A)
<220>
<221> misc_feature
<222> (14)..(16)
<223> Xaa is any amino acid
<400> 52
Xaa Tyr Xaa Xaa Xaa Xaa Gly Pro Xaa Thr Trp Xaa Xaa Xaa Xaa Xaa
1 5 10 15
<210> 53
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Arg (R), His (H), Tyr (Y), or a bond
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is Met (M), Phe (F), or Ile (I)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is Asp (D) or Val (V)
<220>
<221> misc_feature
<222> (14)..(16)
<223> Xaa is any amino acid
<400> 53
Xaa Tyr Xaa Cys Xaa Xaa Gly Pro Xaa Thr Trp Xaa Cys Xaa Xaa Xaa
1 5 10 15
<210> 54
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Arg (R) or His (H)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is Phe (F) or Met (M)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is Ile (I), Leu (L), Thr (T), Met (M), or Val (V)
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is Asp (D) or Val (V)
<220>
<221> misc_feature
<222> (14)..(14)
<223> Xaa is Gly (G), Lys (K), Leu (L), Gln (Q), Arg (R), Ser (S), or
Thr (T)
<220>
<221> misc_feature
<222> (15)..(15)
<223> Xaa is Ala (A), Gly (G), Pro (P), Arg (R), or Tyr (Y)
<220>
<221> misc_feature
<222> (16)..(16)
<223> Xaa is any amino acid
<400> 54
Xaa Tyr Xaa Cys Xaa Xaa Gly Pro Xaa Thr Trp Xaa Cys Xaa Xaa Xaa
1 5 10 15
<210> 55
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Asp (D), Glu (E), Leu (L), Asn (N), Ser (S), Thr (T), or
Val (V)
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Ala (A), His (H), Lys (K), Leu (L), Met (M), Ser (S), or
Thr (T)
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Arg (R) or His (H)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is Met (M), Phe (F) or Ile (I)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is Asp (D) or Val (V)
<220>
<221> misc_feature
<222> (14)..(14)
<223> Xaa is Lys (K), Arg (R), Ser (S), or Thr (T)
<220>
<221> misc_feature
<222> (15)..(15)
<223> Xaa is Pro (P)
<220>
<221> misc_feature
<222> (16)..(16)
<223> Xaa is any amino acid
<400> 55
Xaa Tyr Xaa Cys Xaa Xaa Gly Pro Xaa Thr Trp Xaa Cys Xaa Xaa Xaa
1 5 10 15
<210> 56
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Asp (D), Glu (E), Leu (L), Asn (N), Ser (S), Thr (T), or
Val (V)
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Ala (A), His (H), Lys (K), Leu (L), Met (M), Ser (S), or
Thr (T)
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Arg (R) or His (H)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is Met (M), Phe (F), or Ile (I)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is Asp (D), or Val (V)
<220>
<221> misc_feature
<222> (14)..(14)
<223> Xaa is Lys (K), Arg (R), Ser (S), or Thr (T)
<220>
<221> misc_feature
<222> (15)..(15)
<223> Xaa is Pro (P)
<220>
<221> misc_feature
<222> (16)..(16)
<223> Xaa is any amino acid
<400> 56
Xaa Tyr Xaa Cys Xaa Xaa Gly Pro Xaa Thr Trp Xaa Cys Xaa Xaa Xaa
1 5 10 15
<210> 57
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide S
<400> 57
Gly Gly Leu Tyr Leu Cys Arg Phe Gly Pro Val Thr Trp Asp Cys Gly
1 5 10 15
Tyr Lys Gly Gly
20
<210> 58
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide T
<400> 58
Gly Gly Thr Tyr Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 59
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide U
<400> 59
Gly Gly Asp Tyr His Cys Arg Met Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Leu Gly Gly
20
<210> 60
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide V
<400> 60
Val Gly Asn Tyr Met Cys His Phe Gly Pro Ile Thr Trp Val Cys Arg
1 5 10 15
Pro Gly Gly Gly
20
<210> 61
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide W
<400> 61
Gly Gly Val Tyr Ala Cys Arg Met Gly Pro Ile Thr Trp Val Cys Ser
1 5 10 15
Pro Leu Gly Gly
20
<210> 62
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide X
<400> 62
Val Gly Asn Tyr Met Ala His Met Gly Pro Ile Thr Trp Val Cys Arg
1 5 10 15
Pro Gly Gly
<210> 63
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide Y
<400> 63
Gly Gly Thr Tyr Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln
<210> 64
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide Z
<400> 64
Gly Gly Leu Tyr Ala Cys His Met Gly Pro Met Thr Trp Val Cys Gln
1 5 10 15
Pro Leu Arg Gly
20
<210> 65
<211> 22
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AA
<400> 65
Thr Ile Ala Gln Tyr Ile Cys Tyr Met Gly Pro Glu Thr Trp Glu Cys
1 5 10 15
Arg Pro Ser Pro Lys Ala
20
<210> 66
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AB
<400> 66
Tyr Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10
<210> 67
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AC
<400> 67
Tyr Cys His Phe Gly Pro Leu Thr Trp Val Cys
1 5 10
<210> 68
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AD
<400> 68
Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10
<210> 69
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AE
<400> 69
Gly Gly Thr Ala Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 70
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AF
<400> 70
Gly Gly Thr Tyr Ser Cys His Phe Ala Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 71
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AG
<400> 71
Gly Gly Thr Tyr Ser Cys Phe Gly Pro Leu Thr Trp Val Cys Lys Pro
1 5 10 15
Gln Gly Gly
<210> 72
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AH
<400> 72
Thr Tyr Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys Pro Gln
1 5 10 15
Gly Gly
<210> 73
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AI
<400> 73
Thr Tyr Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys Pro Gln
1 5 10 15
<210> 74
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AJ
<400> 74
Tyr Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys Pro
1 5 10
<210> 75
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AK
<400> 75
Tyr Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys
1 5 10
<210> 76
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AL
<400> 76
Tyr Ser Cys His Phe Gly Ala Leu Thr Trp Val Cys Lys
1 5 10
<210> 77
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AM
<400> 77
Gly Gly Cys Arg Ile Gly Pro Ile Thr Trp Val Cys Gly Gly
1 5 10
<210> 78
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AN
<400> 78
His Phe Gly Pro Leu Thr Trp Val
1 5
<210> 79
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AO
<400> 79
Gly Gly Thr Thr Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 80
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AP
<400> 80
Gly Gly Thr Phe Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 81
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AQ
<400> 81
Gly Gly Thr Tyr Ser Cys His Phe Gly Ala Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 82
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AR
<400> 82
Gly Gly Thr Tyr Ser Cys His Phe Gly Pro Ala Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 83
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AS
<400> 83
Gly Gly Thr Tyr Ser Cys His Phe Gly Pro Leu Ala Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 84
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AT
<400> 84
Gly Gly Thr Tyr Ser Cys His Phe Gly Pro Leu Thr Ala Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 85
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AU
<400> 85
Gly Gly Thr Tyr Ser Cys His Phe Gly Pro Leu Thr Phe Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 86
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AV
<400> 86
Gly Gly Thr Tyr Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Ala Gln Gly Gly
20
<210> 87
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AW
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is any amino acid
<400> 87
Gly Gly Thr Xaa Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 88
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AX
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is any amino acid
<400> 88
Gly Gly Thr Xaa Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 89
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AY
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is p-NH2-Phe
<400> 89
Gly Gly Thr Xaa Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 90
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide AZ
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is p-F-Phe
<400> 90
Gly Gly Thr Xaa Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 91
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide BA
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is p-I-Phe
<400> 91
Gly Gly Thr Xaa Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 92
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide BB
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is 3,5-dibromo-Tyr
<400> 92
Gly Gly Thr Xaa Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 93
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide BC
<220>
<221> MOD_RES
<222> (1)..(1)
<223> ACETYLATION, N-terminal
<400> 93
Gly Gly Thr Tyr Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 94
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide BD
<400> 94
Gly Gly Leu Tyr Ala Cys His Met Gly Pro Met Thr Trp Val Cys Gln
1 5 10 15
Pro Leu Gly Gly
20
<210> 95
<211> 22
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide BE
<400> 95
Leu Gly Arg Lys Tyr Ser Cys His Phe Gly Pro Leu Thr Trp Val Cys
1 5 10 15
Gln Pro Ala Lys Lys Asp
20
<210> 96
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif E, Peptide BF
<400> 96
Gly Gly Thr Tyr Ser Glu His Phe Gly Pro Leu Thr Trp Val Lys Lys
1 5 10 15
Pro Gln Gly Gly
20
<210> 97
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BG
<220>
<221> MOD_RES
<222> (1)..(1)
<223> N-terminal D-biotin
<400> 97
Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val Pro Asp Thr Lys
1 5 10 15
Val
<210> 98
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BH
<220>
<221> MOD_RES
<222> (1)..(1)
<223> N-terminal D-biotin
<400> 98
Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val Pro
1 5 10
<210> 99
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BI
<220>
<221> MOD_RES
<222> (17)..(17)
<223> C-terminal biotin
<400> 99
Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val Pro Asp Thr Lys
1 5 10 15
Lys
<210> 100
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BJ
<220>
<221> MOD_RES
<222> (13)..(13)
<223> C-terminal D-biotin
<400> 100
Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val Pro
1 5 10
<210> 101
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Formula I of structural motif F
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is any amino acid containing a sulfhydral group
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is a any amino acid containing a sulfhydral group
<400> 101
Xaa Ala Glu His Xaa Ser
1 5
<210> 102
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BK
<400> 102
Thr Thr Gly Cys Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val
1 5 10 15
Pro Asp Thr Lys
20
<210> 103
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BL
<400> 103
Cys Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val Pro Asp Thr
1 5 10 15
Lys Val
<210> 104
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BM
<400> 104
Cys Ala Glu His Cys Ser
1 5
<210> 105
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BN
<400> 105
Gly Cys Ala Glu His Cys Ser Leu
1 5
<210> 106
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BO
<400> 106
Gly Cys Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val Pro Asp
1 5 10 15
Thr Lys Val
<210> 107
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BP
<400> 107
Cys Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val Pro
1 5 10
<210> 108
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BQ
<400> 108
Thr Thr Gly Cys Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val
1 5 10 15
Pro Asp Thr Lys Val
20
<210> 109
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BR
<400> 109
Thr Thr Gly Cys Ala Glu His Cys Ser Leu Asn Glu Asn Ile Thr Val
1 5 10 15
Pro
<210> 110
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BS
<400> 110
Cys Ala Glu His Cys Ser Leu Asn Lys Asn Ile Asn Leu Asp Ser Val
1 5 10 15
Asp Gly Val Pro
20
<210> 111
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Formula II of structural motif F
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is any amino acid containing a sulfhydral group
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is any amino acid containing a sulhydral group
<400> 111
Xaa Ala Glu His Xaa Ser
1 5
<210> 112
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BT
<400> 112
Ala Glu His Cys Ser Leu Met Glu Asn Asn Leu Arg Arg Pro Asn Leu
1 5 10 15
<210> 113
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif F, Peptide BU
<220>
<221> MOD_RES
<222> (1)..(1)
<223> N-terminal D-biotin
<400> 113
Ala Glu His Cys Ser Leu Met Glu Asn Asn Leu Arg Arg Pro Asn Leu
1 5 10 15
<210> 114
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide BV
<400> 114
Trp Glu His Val Asn Ala Ile Gln Glu Ala Arg Arg Leu Leu
1 5 10
<210> 115
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide BW
<400> 115
Leu Ser Lys Leu Leu Arg Asp Ser His Val Leu His
1 5 10
<210> 116
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide BX
<400> 116
Lys Ile Arg Ser Asp Leu Thr Ala Leu Thr Glu Ser Tyr Val Lys His
1 5 10 15
<210> 117
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide BY
<400> 117
Gly Thr Glu Lys Ala Lys Leu Val Glu Leu Tyr Arg Ile Val Val Tyr
1 5 10 15
Leu
<210> 118
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide BZ
<400> 118
Ser Ile Met Ile Asp Glu Ile Ile His His Leu Lys Arg Pro Pro Asn
1 5 10 15
Pro Leu
<210> 119
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Formula V of structural motif A
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Try (W), Val (V), Ala (A), Ile (I), Pro (P), Leu (L), Ser
(S), Asp (D), or Thr (T)
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (7)..(7)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is Ile (I), Phe (F), Leu (L), Val (V), Pro (P), Tyr (Y), or
Gly (G)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (10)..(10)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (11)..(11)
<223> Xaa is Ile (I), Leu (L), Ala (A), Gly (G), Phe (F), Val (V), or
Pro (P)
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is Ile (I), Met (M), Tyr (Y), Ser (S), Val (V), Phe (F), Lys
(K), Leu (L), Glu (E), or Asp (D)
<220>
<221> misc_feature
<222> (13)..(13)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (14)..(14)
<223> Xaa is His (H), Leu (L), Pro (P), Thr (T), Arg (R), Cys (C), Ile
(I), Tyr (Y), Gln (Q), or Ala (A)
<220>
<221> misc_feature
<222> (15)..(15)
<223> Xaa is Leu (L), Lys (K), Thr (T), Val (V), Phe (F), Ala (A), or
Gln (Q)
<220>
<221> misc_feature
<222> (16)..(16)
<223> Xaa is Lys (K), Glu (E), Met (M), Gly (G), Asn (N), Gln (Q), Thr
(T), or Val (V)
<220>
<221> misc_feature
<222> (17)..(17)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (18)..(18)
<223> Xaa is Pro (P), Lys (K), Arg (R), Ile (I), Asn (N), Ser (S), Gln
(Q), or Phe (F)
<220>
<221> misc_feature
<222> (19)..(19)
<223> Xaa is Pro (P), Ile (I), Tyr (Y), Leu (L), Phe (F), Ser (S), Ala
(A), Asp (D), Asn (N), or Lys (K)
<400> 119
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa
<210> 120
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CA
<400> 120
Lys Thr Ser Trp Val Asn Cys Ser Asn Met Ile Asp Glu Ile Ile Thr
1 5 10 15
His Leu Lys Gln Pro Pro Leu Pro
20
<210> 121
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CB
<400> 121
Leu Leu Gln Val Ala Ala Phe Ala Tyr Gln Ile Glu Glu Leu Met Ile
1 5 10 15
Leu Leu Glu Tyr Lys Ile Pro Arg
20
<210> 122
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CC
<400> 122
His Gln Leu Ala Phe Asp Thr Tyr Gln Glu Phe Glu Glu Ala Tyr Ile
1 5 10 15
Pro Lys Glu Gln Lys Tyr Ser Phe
20
<210> 123
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CD
<400> 123
Asp Ser Asn Val Tyr Asp Leu Leu Lys Asp Leu Glu Glu Gly Ile Gln
1 5 10 15
Thr Leu Met Gly Arg Leu Glu Asp
20
<210> 124
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CE
<400> 124
Glu Glu Gly Ile Gln Thr Leu Met Gly Arg Leu Glu Asp Gly Ser Pro
1 5 10 15
Arg Thr Gly Gln Ile Phe Lys Gln
20
<210> 125
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CF
<400> 125
Ser Asn Val Asp Lys Glu Thr Gly Glu Asp Gly
1 5 10
<210> 126
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CG
<400> 126
Tyr Ser Ile Ile Asp Lys Leu Val Asn Ile Val Asp Asp Leu Val Glu
1 5 10 15
Cys Val Lys Glu Asn Ser Ser Lys
20
<210> 127
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CH
<400> 127
Phe Lys Ser Pro Glu Pro Arg Leu Phe Thr Pro Glu Glu Phe Phe Arg
1 5 10 15
Ile Phe Asn Arg Ser Ile Asp Ala
20
<210> 128
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CI
<400> 128
Leu Asp Asn Leu Leu Leu Lys Glu Ser Leu Leu Glu Asp Phe Lys Gly
1 5 10 15
Tyr Leu Gly Cys Gln Ala Leu Ser
20
<210> 129
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CJ
<400> 129
Gln Ala Leu Ser Glu Met Ile Gln Phe Tyr Leu Glu Glu Val Met Pro
1 5 10 15
Gln Ala Glu Asn Gln Asp Pro Asp
20
<210> 130
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CK
<400> 130
Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn
1 5 10 15
Leu Ala Gln Ser Lys Asn Phe His
20
<210> 131
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CL
<400> 131
Ala Gln Asp Leu Glu Arg Ser Gly Leu Asn Ile Glu Asp Leu Glu Lys
1 5 10 15
Leu Gln Met Ala Arg Pro Asn Ile
20
<210> 132
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CM
<400> 132
Val Pro Pro Ser Thr Ala Leu Arg Glu Leu Ile Glu Glu Leu Val Asn
1 5 10 15
Ile Thr Gln Asn Gln Lys Ala Pro
20
<210> 133
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CN
<400> 133
Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu Met Gln
1 5 10 15
Ala Leu Asn Phe Asn Ser Glu Thr
20
<210> 134
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CO
<400> 134
Asn Ser Glu Thr Val Pro Gln Lys Ser Ser Leu Glu Glu Pro Asp Phe
1 5 10 15
Tyr Lys Thr Lys Ile Lys Leu Cys
20
<210> 135
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CP
<400> 135
Phe Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met
1 5 10 15
Tyr Gln Val Glu Phe Lys Thr Met
20
<210> 136
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CQ
<400> 136
Cys Leu Lys Asp Arg Met Asn Phe Asp Ile Pro Glu Glu Ile Lys Gln
1 5 10 15
Leu Gln Gln Phe Gln Lys Glu Asp
20
<210> 137
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Formula IV of structural motif A
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Phe (F), Val (V), Ala (A), Gly (G), Pro (P), Leu (L), Tyr
(Y), Ile (I), Cys (C) or Met (M)
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (4)..(7)
<223> Xaa is any amino acid or a bond
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is Pro (P), Met (M), Val (V), Ile (I), Phe (F), Gly (G), Leu
(L), Ala (A), Tyr (Y), and Trp (W)
<400> 137
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 138
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CR
<400> 138
Asn Glu Thr Val Glu Val Ile Ser Glu Met Phe Asp Leu Gln Glu Pro
1 5 10 15
Thr Cys Leu Gln Thr Arg Leu Glu Leu Tyr
20 25
<210> 139
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CS
<400> 139
Asn Leu Lys Asp Phe Leu Leu Val Ile Pro Phe Asp Cys Trp Glu Pro
1 5 10 15
Val Gln Glu
<210> 140
<211> 27
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CT
<400> 140
Arg Asp Thr Ala Ala Glu Met Asn Glu Thr Val Glu Val Ile Ser Glu
1 5 10 15
Met Phe Asp Leu Gln Glu Pro Thr Cys Leu Gln
20 25
<210> 141
<211> 29
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CU
<400> 141
Arg Leu Leu Asn Leu Ser Arg Asp Thr Ala Ala Glu Met Asn Glu Thr
1 5 10 15
Val Glu Val Ile Ser Glu Met Phe Asp Leu Gln Glu Pro
20 25
<210> 142
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CV
<400> 142
Leu Pro Leu Leu Asp Phe Asn Asn Leu Asn Gly Glu Asp Gln Asp Ile
1 5 10 15
Leu Met Glu Asn Asn Leu Arg Arg Pro Asn
20 25
<210> 143
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CW
<400> 143
Pro Thr Arg His Pro Ile His Ile Lys Asp Gly Asp Trp Asn Glu Phe
1 5 10 15
Arg Arg Lys Leu Thr Phe Tyr Leu Lys Thr
20 25
<210> 144
<211> 28
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CX
<400> 144
His Val Gly His Val Asp Val Thr Tyr Gly Pro Asp Thr Ser Gly Lys
1 5 10 15
Asp Val Phe Gln Lys Lys Lys Leu Gly Cys Gly Leu
20 25
<210> 145
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CY
<400> 145
Lys His Gln Gly Leu Asn Lys Asn Ile Asn Leu Asp Ser Ala Asp Gly
1 5 10 15
Met Pro Val Ala Ser Thr Asp Gln Trp Ser
20 25
<210> 146
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide CZ
<400> 146
Trp Ser Glu Leu Thr Ala Glu Gln Glu Leu Gln Arg Val Ala Arg Glu
1 5 10 15
Val His
<210> 147
<211> 27
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DA
<400> 147
Leu Arg Ala His Arg Leu His Gln Leu Ala Phe Asp Thr Tyr Gln Glu
1 5 10 15
Phe Glu Glu Ala Tyr Ile Pro Lys Glu Gln Lys
20 25
<210> 148
<211> 27
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DB
<400> 148
Leu Val Tyr Gly Ala Ser Asp Ser Asn Val Tyr Asp Leu Leu Lys Asp
1 5 10 15
Leu Glu Glu Gly Ile Gln Thr Leu Met Gly Arg
20 25
<210> 149
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DC
<400> 149
Ser Asn Val Asp Lys Glu Thr Gly Glu Asp Gly
1 5 10
<210> 150
<211> 27
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DD
<400> 150
Gln Glu Glu Arg Arg Arg Val Asn Gly Phe Leu Asp Tyr Leu Gln Glu
1 5 10 15
Phe Leu Gly Val Met Asn Thr Glu Trp Ile Ile
20 25
<210> 151
<211> 27
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DE
<400> 151
Glu Glu Phe Phe Arg Ile Phe Asn Arg Ser Ile Asp Ala Phe Lys Asp
1 5 10 15
Phe Val Val Ala Ser Glu Thr Ser Asp Cys Val
20 25
<210> 152
<211> 27
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DF
<400> 152
Ser Arg Asn Val Ile Gln Ile Ser Asn Asp Leu Glu Asn Leu Arg Asp
1 5 10 15
Leu Leu His Val Leu Ala Phe Ser Lys Ser Cys
20 25
<210> 153
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DG
<400> 153
Tyr Ser Thr Val Ser Gly Asp Trp Gln Leu Asp Leu
1 5 10
<210> 154
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DH
<400> 154
Gln Phe Tyr Leu Glu Glu Val Met Pro Gln Ala Glu Asn Gln Asp Pro
1 5 10 15
Asp Ile Lys Ala His Val Asn Ser Leu Gly
20 25
<210> 155
<211> 28
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DI
<400> 155
Gln Phe Tyr Leu Glu Glu Val Met Pro Gln Ala Glu Asn Gln Asp Pro
1 5 10 15
Asp Ile Lys Ala His Val Asn Ser Leu Gly Glu Asn
20 25
<210> 156
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DJ
<400> 156
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
1 5 10 15
Pro Leu Glu Glu Val Leu Asn Leu Ala
20 25
<210> 157
<211> 28
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DK
<400> 157
Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu
1 5 10 15
Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr
20 25
<210> 158
<211> 28
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DL
<400> 158
Phe Lys Asp Asp Gln Ser Ile Gln Lys Ser Val Glu Thr Ile Lys Glu
1 5 10 15
Asp Met Asn Val Lys Phe Phe Asn Ser Asn Lys Lys
20 25
<210> 159
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DM
<400> 159
Val Glu Ile Glu Glu Gln Thr Lys Arg Leu Leu Glu Gly Met Glu Leu
1 5 10 15
Ile Val Ser Gln Val His Pro Glu Thr Lys
20 25
<210> 160
<211> 28
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DN
<400> 160
Gly Met Glu Leu Ile Val Ser Gln Val His Pro Glu Thr Lys Glu Asn
1 5 10 15
Glu Ile Tyr Pro Val Trp Ser Gly Leu Pro Ser Leu
20 25
<210> 161
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DO
<400> 161
Pro Glu Ala Ile Val Glu Glu Arg Glu Leu Ser Gln Val
1 5 10
<210> 162
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DP
<400> 162
His Lys Cys Asp Ile Thr Leu Gln Glu Ile Ile Lys Thr Leu Asn Ser
1 5 10 15
Leu Thr Glu Gln
20
<210> 163
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DQ
<400> 163
Ala Glu Asn Asn Leu Asn Leu Pro Lys Met Ala Glu Lys Asp Gly Cys
1 5 10 15
Phe Gln Ser Gly Phe Asn Glu Glu Thr
20 25
<210> 164
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DR
<400> 164
Thr Cys Leu Val Lys Ile Ile Thr Gly Leu Leu Glu Phe Glu Val Tyr
1 5 10 15
Leu Glu Tyr Leu Gln Asn Arg Phe Glu
20 25
<210> 165
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DS
<400> 165
Val Pro Pro Gly Glu Asp Ser Lys Asp Val Ala Ala Pro His Arg Gln
1 5 10 15
Pro Leu Thr Ser
20
<210> 166
<211> 27
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DT
<400> 166
Arg Lys Glu Thr Cys Asn Lys Ser Asn Met Cys Glu Ser Ser Lys Glu
1 5 10 15
Ala Leu Ala Glu Asn Asn Leu Asn Leu Pro Lys
20 25
<210> 167
<211> 27
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DU
<400> 167
Leu Val Lys Ile Ile Thr Gly Leu Leu Glu Phe Glu Val Tyr Leu Glu
1 5 10 15
Tyr Leu Gln Asn Arg Phe Glu Ser Ser Glu Glu
20 25
<210> 168
<211> 29
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DV
<400> 168
Thr Cys Leu Val Lys Ile Ile Thr Gly Leu Leu Glu Phe Glu Val Tyr
1 5 10 15
Leu Glu Tyr Leu Gln Asn Arg Phe Glu Ser Ser Glu Glu
20 25
<210> 169
<211> 29
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DW
<400> 169
Ile Gln Phe Leu Gln Lys Lys Ala Lys Asn Leu Asp Ala Ile Thr Thr
1 5 10 15
Pro Asp Pro Thr Thr Asn Ala Ser Leu Leu Thr Lys Leu
20 25
<210> 170
<211> 29
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DX
<400> 170
Arg Asn Asn Ile Tyr Cys Met Ala Gln Leu Leu Asp Asn Ser Asp Thr
1 5 10 15
Ala Glu Pro Thr Lys Ala Gly Arg Gly Ala Ser Gln Pro
20 25
<210> 171
<211> 28
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DY
<400> 171
Pro Leu Pro Thr Pro Val Leu Leu Pro Ala Val Asp Phe Ser Leu Gly
1 5 10 15
Glu Trp Lys Thr Gln Met Glu Glu Thr Lys Ala Gln
20 25
<210> 172
<211> 29
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide DZ
<400> 172
Asp Phe Ser Leu Gly Glu Trp Lys Thr Gln Met Glu Glu Thr Lys Ala
1 5 10 15
Gln Asp Ile Leu Gly Ala Val Thr Leu Leu Leu Glu Gly
20 25
<210> 173
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide EA
<400> 173
Leu Glu Trp Lys Thr Gln Thr Asp Gly Leu Glu Gly Ala Ala Gly Gln
1 5 10 15
<210> 174
<211> 28
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide EB
<400> 174
Thr Val Ala Gly Ser Lys Met Gln Gly Leu Leu Glu Arg Val Asn Thr
1 5 10 15
Glu Ile His Phe Val Thr Lys Cys Ala Phe Gln Pro
20 25
<210> 175
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide EC
<400> 175
Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp His Glu Asp Ile
1 5 10 15
Thr Lys Asp Lys Thr Ser Thr Val Glu Ala
20 25
<210> 176
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide ED
<400> 176
Asn Ser Glu Thr Val Pro Gln Lys Ser Ser Leu Glu Glu Pro Asp Phe
1 5 10 15
Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
20 25
<210> 177
<211> 29
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide EE
<400> 177
Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu Pro
1 5 10 15
Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg
20 25
<210> 178
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide EF
<400> 178
Thr Thr Asn Asp Val Pro His Ile Gln Cys Gly Asp Gly Cys Asp Pro
1 5 10 15
Gln Gly Leu Arg Asp Asn Ser Gln Phe Cys
20 25
<210> 179
<211> 27
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide EG
<400> 179
Ala Trp Ser Ala His Pro Leu Val Gly His Met Asp Leu Arg Glu Glu
1 5 10 15
Gly Asp Glu Glu Thr Thr Asn Asp Val Pro His
20 25
<210> 180
<211> 29
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide EH
<400> 180
Leu Val Gly His Met Asp Leu Arg Glu Glu Gly Asp Glu Glu Thr Thr
1 5 10 15
Asn Asp Val Pro His Ile Gln Cys Gly Asp Gly Cys Asp
20 25
<210> 181
<211> 29
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide EI
<400> 181
Leu Gln Arg Ile His Gln Gly Leu Ile Phe Tyr Glu Lys Leu Leu Gly
1 5 10 15
Ser Asp Ile Phe Thr Gly Glu Pro Ser Leu Leu Pro Asp
20 25
<210> 182
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide EJ
<400> 182
Asn His Leu Lys Thr Val Leu Glu Glu Lys Leu Glu Lys Glu Asp Phe
1 5 10 15
Thr Arg Gly Lys Leu Met Ser Ser Leu His
20 25
<210> 183
<211> 27
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, Peptide EK
<400> 183
Leu Glu Tyr Cys Leu Lys Asp Arg Met Asn Phe Asp Ile Pro Glu Glu
1 5 10 15
Ile Lys Gln Leu Gln Gln Phe Gln Lys Glu Asp
20 25
<210> 184
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Leu (L), Ile (I), Gly (G), Val (V), Phe (F), Pro (P), or
Ala (A)
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Phe (F), Gly (G), Val (V), Leu (L), Ala (A), or Tyr (Y)
<400> 184
Xaa Xaa Xaa Xaa
1
<210> 185
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EL
<400> 185
Ile Ile Thr Phe Glu Ser Phe Lys Glu Asn Leu Lys Asp Phe Leu Leu
1 5 10 15
Val Ile Pro Phe Asp Cys Trp Glu
20
<210> 186
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EM
<400> 186
Thr Ala Ala Pro Thr Arg His Pro Ile His Ile Lys Asp Gly Asp Trp
1 5 10 15
Asn Glu Phe Arg Arg Lys Leu Thr
20
<210> 187
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EN
<400> 187
Val Asp Val Thr Tyr Gly Pro Asp Thr Ser Gly Lys Asp Val Phe Gln
1 5 10 15
Lys Lys Lys Leu Gly Cys Gln Leu
20
<210> 188
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EO
<400> 188
Ser Gly Lys Asp Val Phe Gln Lys Gln Gly Gln Ser Val Gln
1 5 10
<210> 189
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EP
<400> 189
Gln Glu Leu Ser Gln Trp Thr Val Arg Ser Ile His Asp Leu Arg Phe
1 5 10 15
Ile Ser Ser His Gln Thr Gly Ile
20
<210> 190
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EQ
<400> 190
Trp Ser Glu Leu Thr Ala Glu Gln Glu Leu Gln Arg Val Ala Arg Glu
1 5 10 15
Val His
<210> 191
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide ER
<400> 191
Gly Ala Ser Asp Ser Asn Val Tyr Asp Leu Leu Lys Asp Leu Glu Glu
1 5 10 15
Gly Ile Gln Thr Leu Met Gly Arg
20
<210> 192
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide ES
<400> 192
Gly Ile Cys Arg Asn Arg Val Thr Asn Asn Val Lys Asp Val Thr Lys
1 5 10 15
Leu Val Ala Asn Leu Pro Lys Asp
20
<210> 193
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide ET
<400> 193
Phe Arg Ile Phe Asn Arg Ser Ile Asp Ala Phe Lys Asp Phe Val Val
1 5 10 15
Ala Ser Glu Glu Thr Ser Asp Cys Val
20 25
<210> 194
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EU
<400> 194
Val Ile Gln Ile Ser Asn Asp Leu Glu Asn Leu Arg Asp Leu Leu His
1 5 10 15
Val Leu Ala Phe Ser Lys Ser Cys
20
<210> 195
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EV
<400> 195
Thr His Phe Pro Gly Asn Leu Pro Asn Met Leu Arg Asp Leu Arg Asp
1 5 10 15
Ala Phe Ser Arg Val Lys Thr Phe
20
<210> 196
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EW
<400> 196
Pro Gly Asn Leu Pro Asn Met Leu Arg Asp Leu Arg Asp Ala Phe Ser
1 5 10 15
Arg Val Lys Thr Phe Phe Gln Met
20
<210> 197
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EX
<400> 197
Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser
1 5 10 15
Asn Ile Asn Val Ile Val Leu Glu
20
<210> 198
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EY
<400> 198
Gln Asp Pro Tyr Val Lys Glu Ala Glu Asn Leu Lys Lys Tyr Phe Asn
1 5 10 15
Ala Gly
<210> 199
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide EZ
<400> 199
Val Thr Asp Leu Asn Val Gln Arg Lys Ala Ile His Glu Leu Ile Gln
1 5 10 15
Val Met Ala Glu Leu Ser Pro Ala
20
<210> 200
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FA
<400> 200
Pro Gly Gly Ala Ala Arg Cys Gln Val Thr Leu Arg Asp Leu Phe Asp
1 5 10 15
Arg Ala Val Val Leu Ser His Tyr
20
<210> 201
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FB
<400> 201
Trp Gly Leu Ala Gly Leu Asn Ser Cys Pro Val Lys Glu Ala Asn Gln
1 5 10 15
Ser Thr Leu Glu Asn Phe Leu Glu
20
<210> 202
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FC
<400> 202
Asp Met Thr Thr His Leu Ile Leu Arg Ser Phe Lys Glu Phe Leu Gln
1 5 10 15
Ser Ser Leu Arg Ala Leu Arg Gln
20
<210> 203
<211> 22
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FD
<400> 203
Gly Pro Val Pro Pro Ser Thr Ala Leu Arg Glu Leu Ile Glu Glu Leu
1 5 10 15
Val Asn Ile Thr Gln Asn
20
<210> 204
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FE
<400> 204
Lys Asp Leu Leu Leu His Leu Lys Lys Leu Phe Arg Glu Gly Arg Phe
1 5 10 15
Asn
<210> 205
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FF
<400> 205
Arg Asp Thr Lys Ile Glu Val Ala Gln Phe Val Lys Asp Leu Leu Leu
1 5 10 15
His Leu Lys Lys Leu Phe Arg Glu
20
<210> 206
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FG
<400> 206
Leu Asp Gln Ile Pro Gly Tyr Leu Asn Arg Ile His Glu Leu Leu Asn
1 5 10 15
Gly Thr Arg Gly Leu Phe Pro Gly
20
<210> 207
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FH
<400> 207
Ser Pro Ile Ser Ser Asp Phe Ala Val Lys Ile Arg Glu Leu Ser Asp
1 5 10 15
Tyr Leu Leu Gln Asp Tyr Pro Val
20
<210> 208
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FI
<400> 208
Tyr Tyr Gly Arg Ile Leu His Tyr Leu Lys Ala Lys Glu Tyr Ser His
1 5 10 15
Cys Ala Trp Thr Ile Val Arg Val
20
<210> 209
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
structural formula VIII
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Ala (A), Thr (T), Ser (S), Tyr (Y), Leu (L), Val (V), Ile
(I), Phe (F), or Glu (E)
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Ser (S), Gln (Q), Asp (D), Leu (L), Glu (E), Cys (C), Asn
(N), Arg (R), or Ala (A)
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Pro (P), Gly (G), Gln (Q), Leu (L), Thr (T), Asn (N), Ser
(S), Phe (F), or Ile (I)
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is Pro (P), Ser (S), Cys (C), Val (V), Lys (K), Thr (T), Leu
(L), Ile (I), or Gln (Q)
<220>
<221> misc_feature
<222> (7)..(7)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is Thr (T), Pro (P), Leu (L), Arg (R), Gly (G), Tyr (Y), Gln
(Q), Glu (E), Ile (I) or Ala (A)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (10)..(10)
<223> Xaa is Pro (P), Asn (N), Glu (E), Asp (D), Thr (T), Leu (L), Ile
(I), Gln (Q), Phe (F), or Trp (W)
<220>
<221> misc_feature
<222> (11)..(11)
<223> Xaa is Trp (W), Leu (L), Ala (A), Met (M), Val (V), Ile (I), Phe
(F), or Tyr (Y)
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (13)..(13)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (14)..(14)
<223> Xaa is Val (V), Leu (L), or Ala (A)
<220>
<221> misc_feature
<222> (15)..(20)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (21)..(21)
<223> Xaa is Arg (R), Asp (D), Tyr (Y), Val (V), Ile (I), Leu (L), Lys
(K), Ser (S), or Thr (T)
<220>
<221> misc_feature
<222> (22)..(23)
<223> Xaa is any amino acid
<220>
<221> misc_feature
<222> (24)..(24)
<223> Xaa is Leu (L), Pro (P), Phe (F), Arg (R), Tyr (Y), Cys (C), Gly
(G), Val (V), or Lys (K)
<400> 209
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
20
<210> 210
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokines derived peptides exhibiting structural motifl B,
Peptide FJ
<400> 210
Ala Arg Ser Pro Ser Pro Ser Thr Gln Pro Trp Glu His Val Asn Ala
1 5 10 15
Ile Gln Glu Ala Arg Arg Leu Leu
20
<210> 211
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FK
<400> 211
Ile Thr Phe Glu Lys Leu Val Ile Pro
1 5
<210> 212
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FL
<400> 212
Thr Ala Gln Gly Glu Pro Phe Pro Asn Asn Leu Asp Lys Leu Cys Gly
1 5 10 15
Pro Asn Val Thr Asp Phe Pro Pro
20
<210> 213
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FM
<400> 213
Ser Thr Asp Gln Trp Ser Glu Leu Thr Glu Ala Glu Arg Leu Gln Glu
1 5 10 15
Asn Leu Gln Ala Tyr Arg Thr Phe
20
<210> 214
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FN
<400> 214
Tyr Gly Leu Leu Tyr Cys Phe Arg Lys Asp Met Asp Lys Val Glu Thr
1 5 10 15
Phe Leu Arg Ile Val Gln Cys Arg
20
<210> 215
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FO
<400> 215
Leu Glu Ser Gln Thr Val Gln Gly Gly Thr Val Glu Arg Leu Phe Lys
1 5 10 15
Asn Leu Ser Leu Ile Lys Lys Tyr
20
<210> 216
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FP
<400> 216
Val Gln Leu Ser Asp Ser Leu Thr Asp Leu Leu Asp Lys Phe Ser Asn
1 5 10 15
Ile Ser Glu Gly Leu Ser Asn Tyr
20
<210> 217
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FQ
<400> 217
Ile Ser Glu Gly Leu Ser Asn Tyr Ser Ile Ile Asp Lys Leu Val Asn
1 5 10 15
Ile Val Asp Asp Leu Val Glu Cys
20
<210> 218
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FR
<400> 218
Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu
1 5 10 15
Asp Leu Gln Met Ile Leu Asn Gly
20
<210> 219
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FS
<400> 219
Phe Asn Ser Asn Lys Lys Lys Arg Asp Asp Phe Glu Lys Leu Thr Asn
1 5 10 15
Tyr Ser Val Thr Asp Leu Asn Val
20
<210> 220
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FT
<400> 220
Ala Arg Cys Gln Val Thr Leu Arg Asp Leu Phe Asp Arg Ala Val Val
1 5 10 15
Leu Ser His Tyr Ile His Asn Leu
20
<210> 221
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FU
<400> 221
Leu Asp Arg Val Tyr Asn Glu Glu Lys Arg Tyr Thr His
1 5 10
<210> 222
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FV
<400> 222
Glu Ala Asn Gln Ser Thr Leu Glu Asn Phe Leu Glu Arg Leu Lys Thr
1 5 10 15
Ile Met Arg Glu Lys Tyr Ser Lys
20
<210> 223
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FW
<400> 223
Leu Glu Arg Ser Gly Leu Asn Ile Glu Asp Leu Glu Lys Leu Gln Met
1 5 10 15
Ala Arg Pro Asn Ile Leu Gly Leu
20
<210> 224
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FX
<400> 224
Leu Trp Arg Leu Val Leu Ala Gln Arg Trp Met Glu Arg Leu Lys Thr
1 5 10 15
Val Ala Gly Ser Lys Met Gln Gly
20
<210> 225
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FY
<400> 225
Thr Val Ala Gly Ser Lys Met Gln Gly Leu Leu Glu Arg Val Asn Thr
1 5 10 15
Glu Ile His Phe Val Thr Lys Cys
20
<210> 226
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide FZ
<400> 226
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
1 5 10 15
Tyr Leu Asn Ala Ser
20
<210> 227
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide GA
<400> 227
Leu Gln Arg Ile His Gln Gly Leu Ile Phe Tyr Glu Lys Leu Leu Gly
1 5 10 15
Ser Asp Ile Phe Thr Gly Glu Pro
20
<210> 228
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Formula IX
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Cys (C), Tyr (Y), or Ala (A)
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is Ser (S), Leu (L), or Glu (E)
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Arg (R), Gln (Q), or Asn (N)
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Ser (S) or Leu (L)
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Ile (I), Leu (L), or Lys (K)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is Trp (W), Leu (L), or Lys (K)
<220>
<221> misc_feature
<222> (7)..(7)
<223> Xaa is Leu (L), Phe (F), or Tyr (Y)
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is Ala (A), Asn (N), or Phe (F)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is Arg (R), Pro (P), or Asn (N);
<220>
<221> misc_feature
<222> (10)..(10)
<223> Xaa is Lys (K), Leu (L), or Ala (A);
<220>
<221> misc_feature
<222> (11)..(11)
<223> Xaa is Ile (I), Val (V), or Gly (G)
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (13)..(13)
<223> Xaa is a polar amino acid
<220>
<221> misc_feature
<222> (14)..(14)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (15)..(15)
<223> Xaa is Leu (L), Gly (G), or Val (V)
<220>
<221> misc_feature
<222> (16)..(16)
<223> Xaa is Thr (T), Ile (I), or Ala (A)
<220>
<221> misc_feature
<222> (17)..(17)
<223> Xaa is Ala (A), Cys (C), or Asp (D)
<220>
<221> misc_feature
<222> (18)..(18)
<223> Xaa is Leu (L), Arg (R) or Asn (N)
<220>
<221> misc_feature
<222> (19)..(19)
<223> Xaa is Thr (T), Asn (N), or Gly (G)
<220>
<221> misc_feature
<222> (20)..(20)
<223> Xaa is Glu (E), Arg (R), or Thr (T)
<220>
<221> misc_feature
<222> (21)..(21)
<223> Xaa is Ser (S), Val (V), or Leu (L)
<220>
<221> misc_feature
<222> (22)..(22)
<223> Xaa is Tyr (Y), Thr (T), Phe (F)
<220>
<221> misc_feature
<222> (23)..(23)
<223> Xaa is Asn (N) or Leu (L)
<220>
<221> misc_feature
<222> (24)..(24)
<223> Xaa is Asn (N) or Gly (G)
<220>
<221> misc_feature
<222> (25)..(25)
<223> Xaa is Val (V) or Ile (I)
<400> 228
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
20 25
<210> 229
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide GB
<400> 229
Cys Ser Arg Ser Ile Trp Leu Ala Arg Lys Ile Arg Ser Asp Leu Thr
1 5 10 15
Ala Leu Thr Glu Ser Tyr Val Lys His
20 25
<210> 230
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide GC
<400> 230
Glu Leu Met Ile Leu Leu Glu Tyr Lys Ile Pro Arg Asn Glu Ala Asp
1 5 10 15
Gly Met Pro Ile Asn Val Gly Asp Gly
20 25
<210> 231
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide GD
<400> 231
Tyr Leu Gln Leu Leu Leu Phe Asn Pro Leu Val Lys Thr Glu Gly Ile
1 5 10 15
Cys Arg Asn Arg Val Thr Asn Asn Val
20 25
<210> 232
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
Peptide GE
<400> 232
Ala Glu Asn Leu Lys Lys Tyr Phe Asn Ala Gly His Ser Asp Val Ala
1 5 10 15
Asp Asn Gly Thr Leu Phe Leu Gly Ile
20 25
<210> 233
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptides exhibiting structural motif B,
structural formula X
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Leu (L)
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is Gly (G)
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is Cys (C)
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Val (V)
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Leu (L)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is His (H)
<220>
<221> misc_feature
<222> (7)..(7)
<223> Xaa is Arg (R)
<220>
<221> misc_feature
<222> (8)..(8)
<223> Xaa is Leu (L)
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa is Ala (A)
<220>
<221> misc_feature
<222> (10)..(10)
<223> Xaa is Asp (D)
<220>
<221> misc_feature
<222> (11)..(11)
<223> Xaa is Leu (L)
<220>
<221> misc_feature
<222> (12)..(12)
<223> Xaa is negatively charged amino acid
<220>
<221> misc_feature
<222> (13)..(13)
<223> Xaa is a polar amino acid
<220>
<221> misc_feature
<222> (14)..(14)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (15)..(15)
<223> Xaa is Leu (L)
<220>
<221> misc_feature
<222> (16)..(16)
<223> Xaa is Pro (P)
<220>
<221> misc_feature
<222> (17)..(17)
<223> Xaa is Lys (K)
<220>
<221> misc_feature
<222> (18)..(18)
<223> Xaa is Ala (A)
<220>
<221> misc_feature
<222> (19)..(19)
<223> Xaa is Gln (Q)
<220>
<221> misc_feature
<222> (20)..(20)
<223> Xaa is Asp (D)
<220>
<221> misc_feature
<222> (21)..(21)
<223> Xaa is Leu (L)
<220>
<221> misc_feature
<222> (22)..(22)
<223> Xaa is Glu (E)
<220>
<221> misc_feature
<222> (23)..(23)
<223> Xaa is Arg (R)
<220>
<221> misc_feature
<222> (24)..(24)
<223> Xaa is Ser (S)
<220>
<221> misc_feature
<222> (25)..(25)
<223> Xaa is Gly (G)
<400> 233
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
20 25
<210> 234
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokines derived peptides exhibiting structural motif B,
Peptide GF
<400> 234
Leu Gly Cys Val Leu His Arg Leu Ala Asp Leu Glu Gln Arg Leu Pro
1 5 10 15
Lys Ala Gln Asp Leu Glu Arg Ser Gly
20 25
<210> 235
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Human thrombopoietin derived Peptide GG
<400> 235
Asp Leu Arg Val Leu Ser Lys Leu Leu Arg Asp Ser His Val
1 5 10
<210> 236
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Human thrombopoietin derived Peptide GH
<400> 236
Pro Thr Pro Val Leu Leu Pro Ala Val Asp Phe Ser Leu Gly Glu Trp
1 5 10 15
Lys Thr Gln Met
20
<210> 237
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> Human Thrombopoietin derived Peptide GI
<400> 237
Thr Ala His Lys Asp Pro Asn Ala Ile Phe Leu Ser Phe Gln His Leu
1 5 10 15
Leu Arg Gly Lys Val Arg Phe Leu
20
<210> 238
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Human thromboietin derived Peptide GJ
<400> 238
Pro Asn Arg Thr Ser Gly Leu Leu Glu Thr Asn Phe Thr Ala Ser
1 5 10 15
<210> 239
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> GM-CSF derived Peptide GK
<400> 239
Pro Ser Thr Gln Pro Trp Glu His Val Asn Ala Ile Gln Glu Ala Arg
1 5 10 15
Arg
<210> 240
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> GM-CSF derived Peptide GL
<400> 240
Asn Glu Thr Val Glu Val Ile Ser Glu
1 5
<210> 241
<211> 24
<212> PRT
<213> Artificial Sequence
<220>
<223> GM-CSF derived Peptide GM
<400> 241
Gln Thr Arg Leu Glu Leu Tyr Lys Gln Gly Leu Arg Gly Ser Leu Thr
1 5 10 15
Lys Leu Lys Gly Pro Leu Thr Met
20
<210> 242
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> GM-CSF derived Peptide GN
<400> 242
Lys Asp Phe Leu Leu Val Ile Pro Phe Asp Cys Trp Glu Pro Val Gln
1 5 10 15
Glu
<210> 243
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> CNFT derived Peptide GO
<400> 243
Cys Ser Arg Ser Ile Trp Leu Ala Arg Lys Ile Arg Ser Asp
1 5 10
<210> 244
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> CNFT derived Peptide GP
<400> 244
Asn Lys Asn Ile Asn Leu Asp Ser Ala Asp Gly Met Pro Val Ala Ser
1 5 10 15
Thr Asp
<210> 245
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<223> CNFT derived Peptide GQ
<400> 245
Leu Leu Gln Val Ala Ala Phe Ala Tyr Gln Ile Glu Glu Leu Met Ile
1 5 10 15
Leu Leu Glu Tyr Lys
20
<210> 246
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> CNFT derived Peptide GR
<400> 246
Glu Leu Ser Gln Trp Thr Val Arg Ser Ile His Asp Leu Arg Phe Ile
1 5 10 15
Ser Ser
<210> 247
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> IL-6 derived Peptide GS
<400> 247
Ser Glu Arg Ile Asp Lys Gln Ile Arg Tyr Ile Leu Asp Gly Ile Ser
1 5 10 15
<210> 248
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> IL-6 derived Peptide GT
<400> 248
Ala Glu Asn Asn Leu Asn Leu Pro Lys Met Ala Glu Lys Asp
1 5 10
<210> 249
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> IL-6 derived Peptide GU
<400> 249
Glu Glu Gln Ala Arg Ala Val Gln Met Ser Thr Lys Val Leu Ile Gln
1 5 10 15
<210> 250
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> IL-6 derived Peptide GV
<400> 250
Arg Ser Phe Lys Glu Phe Leu Gln Ser Ser Leu Arg
1 5 10
<210> 251
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> IL-3 derived Peptide GW
<400> 251
Ser Cys Asn Met Ile Asp Glu Ile Ile Thr His Leu Lys Gln
1 5 10
<210> 252
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> IL-3 derived Peptide GX
<400> 252
Glu Asn Asn Leu Arg Arg Pro Asn Leu Glu Ala Phe Asn Arg Ala Val
1 5 10 15
Lys Ser
<210> 253
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> IL-3 derived Peptide GY
<400> 253
His Ile Lys Asp Gly Asp Trp Asn Glu Phe Arg Arg Lys Leu Thr Phe
1 5 10 15
Tyr Leu Lys Thr
20
<210> 254
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<223> Human interferon alpha derived Peptide GZ
<400> 254
Ser Ser Cys Leu Met Asp Arg His Asp Phe Gly Phe Pro Gln Glu Glu
1 5 10 15
Phe Asp Gly Asn Gln
20
<210> 255
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Human interferon alpha derived Peptide HA
<400> 255
Gln Gln Ile Phe Asn Leu Phe Thr Thr Lys Asp Ser Ser Ala Ala Trp
1 5 10 15
Asp Glu
<210> 256
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Human interferon alpha derived Peptide HB
<400> 256
Leu Met Asn Ala Asp Ser Ile Leu Ala Val Lys Lys Tyr Phe Arg Arg
1 5 10 15
Ile Thr Leu Tyr
20
<210> 257
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Human interferon beta derived Peptide HC
<400> 257
Met Ser Tyr Asn Leu Leu Gly Phe Leu Gln Arg Ser Ser Asn Phe Gln
1 5 10 15
Cys Gln Lys Leu Leu Trp Gln Leu Asn
20 25
<210> 258
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Human interferon beta derived Peptide HD
<400> 258
Asp Arg Met Asn Phe Asp Ile Pro Glu Glu Ile Lys Gln Leu Gln Gln
1 5 10 15
Phe Gln Lys
<210> 259
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Human interferon beta derived Peptide HE
<400> 259
Lys Leu Glu Lys Glu Asp Phe Thr Arg Gly Lys Leu Met Ser Ser Leu
1 5 10 15
His Leu Lys Arg
20
<210> 260
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Human interferon beta derived Peptide HF
<400> 260
Phe Ile Asn Arg Leu Thr Gly Tyr Leu Arg Asn
1 5 10
<210> 261
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Human interferon gamma derived Peptide HG
<400> 261
Cys Tyr Cys Gln Asp Pro Tyr Val Lys Glu Ala Glu Asn Leu Lys Lys
1 5 10 15
Tyr Phe Asn Ala
20
<210> 262
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Human interferon gamma derived Peptide HH
<400> 262
Ala Asp Asn Gly Thr Leu Phe Leu Gly Ile Leu Lys Asn Trp Lys Glu
1 5 10 15
Glu Ser Asp Arg
20
<210> 263
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Human interferon gamma derived Peptide HI
<400> 263
Asn Ser Asn Lys Lys Lys Arg Asp Asp Phe Glu Lys Leu Thr Asn Tyr
1 5 10 15
Ser Val Thr Asp
20
<210> 264
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Human interferon gamma derived Peptide HJ
<400> 264
Glu Leu Ser Pro Ala Ala Lys Thr Gly Lys Arg
1 5 10
<210> 265
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Human stem cell factor derived Peptide HK
<400> 265
Ser Leu Ile Ile Gly Phe Ala Ala Gly Ala Leu Tyr Trp Lys Lys Arg
1 5 10 15
Gln Pro Ser Leu
20
<210> 266
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Human stem cell factor derived Peptide HL
<400> 266
Arg Asn Arg Val Thr Asn Asn Val Lys Asp Val Thr Lys Leu Val
1 5 10 15
<210> 267
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Human stem cell factor derived Peptide HM
<400> 267
Asp Lys Leu Val Asn Ile Val Asp Asp Leu Val Glu Cys Val Lys Glu
1 5 10 15
<210> 268
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Human stem cell factor derived Peptide HN
<400> 268
Ser Glu Thr Ser Asp Cys Trp Ser Ser Thr Leu Ser Pro Glu Lys Asp
1 5 10 15
Ser Arg Val
<210> 269
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Human multiple coagulation factor deficiency protein 2 derived
Peptide HO
<400> 269
Asp Glu Leu Ile Asn Ile Ile Asp Gly Val Leu Arg Asp Asp Asp Lys
1 5 10 15
Asn Asn Asp
<210> 270
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Human multiple coagulation factor deficiency protein 2 derived
Peptide HP
<400> 270
Gly Leu Asp Lys Asn Thr Val His Asp Gln Glu His Ile Met Glu His
1 5 10 15
Leu Glu Gly Val
20
<210> 271
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Human multiple coagulation factor deficiency protein 2 derived
Peptide HQ
<400> 271
Gln Leu His Tyr Phe Lys Met His Asp Tyr Asp Gly Asn Asn Leu Leu
1 5 10 15
<210> 272
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> hIL-6 AB loop derived Peptide HT
<400> 272
Glu Ala Leu Ala Glu Asn Asn Leu Asn Leu Pro Lys Met Ala Gly
1 5 10 15
<210> 273
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> hIL-2 AB loop derived Peptide HU
<400> 273
Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu
1 5 10 15
Thr
<210> 274
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> hIL-3 AB loop derived Peptide HV
<400> 274
Ile Leu Met Glu Asn Asn Leu Arg Arg Pro Asn Leu
1 5 10
<210> 275
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> hIL-gamma AB loop derived Peptide HW
<400> 275
Phe Tyr Leu Arg Asn Asn Gln Leu Val Ala Gly Thr Leu
1 5 10
<210> 276
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> hLIF AB loop derived Peptide HX
<400> 276
Tyr Thr Ala Gln Gly Glu Pro Phe Pro Asn Asn Val Glu Leu Lys Leu
1 5 10 15
Cys Ala Pro
<210> 277
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> hIL-1.beta helix C derived Peptide HY
<400> 277
Phe Asn Lys Ile Glu Ile Asn Asn Lys Leu Glu Phe Glu Ser Ala
1 5 10 15
<210> 278
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> hONC-M helix C derived Peptide HZ
<400> 278
Arg Pro Asn Ile Leu Gly Leu Arg Asn Asn Ile Tyr Cys Met Ala Gln
1 5 10 15
Leu Leu
<210> 279
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> hCNTF derived Peptide IA
<220>
<221> MOD_RES
<222> (19)..(19)
<223> C-terminal biotin
<400> 279
Tyr Val Lys His Gln Gly Leu Asn Lys Asn Ile Asn Leu Asp Ser Val
1 5 10 15
Asp Gly Val
<210> 280
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> hIL-3 derived Peptide IB
<220>
<221> MOD_RES
<222> (1)..(1)
<223> N-terminal D-biotin
<400> 280
Ile Leu Met Glu Asn Asn Leu Arg Arg Pro Asn Leu
1 5 10
<210> 281
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Helix B amino acids derived Peptide IC
<400> 281
Gln Glu Gln Leu Glu Arg Ala Leu Asn Ser Ser
1 5 10
<210> 282
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Helix B amino acids derived Peptide ID
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is pyroglutamate
<400> 282
Xaa Glu Gln Leu Glu Arg Ala Leu Asn Ser Ser
1 5 10
<210> 283
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Calcitonin derived Peptide IE
<400> 283
Ala Leu Ser Ile Leu Val Leu Leu Gln Ala Gly Ser
1 5 10
<210> 284
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Corticotropin releasing hormone derived Peptide IF
<400> 284
Val Ala Leu Leu Pro Cys Pro Pro Cys Arg Ala
1 5 10
<210> 285
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Beta endorphin derived Peptide IG
<400> 285
Asn Ala Ile Ile Lys Asn Ala Tyr Lys Lys Gly
1 5 10
<210> 286
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Glucagon derived Peptide IH
<400> 286
Gly Ser Trp Gln Arg Ser Leu Gln Asp Thr Glu
1 5 10
<210> 287
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Secretin derived Peptide II
<400> 287
Gly Gly Ser Ala Ala Arg Pro Ala Pro Pro
1 5 10
<210> 288
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Vasointestinal peptide derived Peptide IJ
<400> 288
Asn Ala Leu Ala Glu Asn Asp Thr Pro Tyr Tyr
1 5 10
<210> 289
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Neuropeptide Y derived Peptide IK
<400> 289
Gly Ala Leu Ala Glu Ala Tyr Pro Ser Lys Pro
1 5 10
<210> 290
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Gonadotropin releasing hormone derived Peptide IL
<400> 290
Gly Cys Ser Ser Gln His Trp Ser Tyr Gly Leu
1 5 10
<210> 291
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Parathyroid hormone derived Peptide IM
<400> 291
Val Met Ile Val Met Leu Ala Ile Cys Phe Leu
1 5 10
<210> 292
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Pancreatic polypeptide derived Peptide IN
<400> 292
Leu Arg Arg Tyr Ile Asn Met Leu Thr Arg Pro
1 5 10
<210> 293
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Calcitonin gene related peptide derived Peptide IO
<400> 293
Leu Ala Leu Ser Ile Leu Val Leu Tyr Gln Ala
1 5 10
<210> 294
<211> 23
<212> PRT
<213> Artificial Sequence
<220>
<223> Carboxy terminus of the amphipathic helix; sequence TR derived
Peptide IQ
<400> 294
Gln Glu Gln Leu Glu Arg Ala Leu Asn Ser Ser Leu Arg Arg Tyr Ile
1 5 10 15
Asn Met Leu Thr Arg Thr Arg
20
<210> 295
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Helix-B exterior-presenting amino acids linked to the beta
pleated sheet derived Peptide IR
<400> 295
Cys Ser Leu Asn Glu Asn Ile
1 5
<210> 296
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Chimeric peptide derived Peptide IS
<400> 296
Cys Ser Leu Asn Glu Asn Ile Gln Glu Gln Leu Glu Arg Ala Leu Asn
1 5 10 15
Ser Ser
<210> 297
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Terminal portion of Helix C derived Peptide IT
<400> 297
Ala Leu Gly Lys Ala
1 5
<210> 298
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Loop CD-partial derived Peptide IU
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is PEG-Q
<400> 298
Xaa Glu Gln Leu Glu Arg Ala Leu Asn Ser Ser
1 5 10
<210> 299
<211> 27
<212> PRT
<213> Artificial Sequence
<220>
<223> Peptide IV
<400> 299
Ala Leu Gly Lys Ala Leu Gly Ala Gln Lys Glu Ala Ile Ser Pro Pro
1 5 10 15
Asp Ala Ala Ser Ala Ala Pro Leu Arg Thr Ile
20 25
<210> 300
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Retro inverso peptide IZ
<400> 300
Ser Ser Asn Leu Ala Gln Arg Glu Leu Gln Glu Gln
1 5 10
<210> 301
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Scrambled peptide IX
<400> 301
Leu Ser Glu Gln Ala Arg Asn Gln Ser Glu Leu
1 5 10
<210> 302
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Type-1 cytokine derived peptide, structural formula VII(a)
<220>
<221> misc_feature
<222> (1)..(1)
<223> Xaa is Leu (L), Ile (I), Gly (G), Val (V), Phe (F), Pro (P), or
Ala (A)
<220>
<221> misc_feature
<222> (2)..(2)
<223> Xaa is a positively charged amino acid
<220>
<221> misc_feature
<222> (3)..(3)
<223> Xaa is a negatively charged amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa is Phe (F), Gly (G), Val (V), Leu (L), Ala (A), or Tyr (Y)
<220>
<221> misc_feature
<222> (5)..(5)
<223> Xaa is Arg (R), Asp (D), Glu (E), Asn (N), Ser (S), Thr (T), Phe
(F), Val (V), or Tyr (Y)
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa is His (H), Lys (K), Asp (D), Glu (E), Gln (Q), Asn (N), Ser
(S), Leu (L), Trp (W), or Phe (F)
<400> 302
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 303
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Structural motif A, derived Peptide E
<400> 303
Arg Tyr Leu Leu Glu Ala Lys Glu Ala Glu Asn Ile Thr Thr Gly Cys
1 5 10 15
<210> 304
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Scrambled peptide, Peptide IY
<220>
<221> MOD_RES
<222> (3)..(3)
<223> N-terminal phosphate
<400> 304
Gly Leu Leu Ser Glu Ala Arg Asn Gln Ser Glu Leu
1 5 10
<210> 305
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Polyethylene glycol polymer, Peptide IW
<220>
<221> MOD_RES
<222> (1)..(1)
<223> 5-terminal polyethylene glycol
<400> 305
Gln Glu Gln Leu Glu Arg Ala Leu Asn Ser Ser
1 5 10
Claims (1)
- 조직 보호 활성을 나타내는 단리된 펩티드의 치료적 용도.
Applications Claiming Priority (11)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US6201208P | 2008-01-22 | 2008-01-22 | |
| US6202208P | 2008-01-22 | 2008-01-22 | |
| US6204508P | 2008-01-22 | 2008-01-22 | |
| US61/062,022 | 2008-01-22 | ||
| US61/062,045 | 2008-01-22 | ||
| US61/062,012 | 2008-01-22 | ||
| US13391208P | 2008-07-03 | 2008-07-03 | |
| US61/133,912 | 2008-07-03 | ||
| US20389008P | 2008-12-30 | 2008-12-30 | |
| US61/203,890 | 2008-12-30 | ||
| PCT/US2009/000424 WO2009094172A2 (en) | 2008-01-22 | 2009-01-22 | Tissue protective peptides and peptide analogs for preventing and treating diseases and disorders associated with tissue damage |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020187010703A Division KR20180041269A (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20180123731A true KR20180123731A (ko) | 2018-11-19 |
Family
ID=40810017
Family Applications (7)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020157033078A KR101768792B1 (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| KR1020187010703A KR20180041269A (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| KR1020207017687A KR20200075044A (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| KR1020197020103A KR20190085187A (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| KR1020107018602A KR101572286B1 (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| KR1020177011116A KR101850908B1 (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| KR1020187032456A KR20180123731A (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
Family Applications Before (6)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020157033078A KR101768792B1 (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| KR1020187010703A KR20180041269A (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| KR1020207017687A KR20200075044A (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| KR1020197020103A KR20190085187A (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| KR1020107018602A KR101572286B1 (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| KR1020177011116A KR101850908B1 (ko) | 2008-01-22 | 2009-01-22 | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
Country Status (15)
| Country | Link |
|---|---|
| US (4) | US8853358B2 (ko) |
| EP (2) | EP2933264A3 (ko) |
| JP (5) | JP5542064B2 (ko) |
| KR (7) | KR101768792B1 (ko) |
| CN (4) | CN111346213A (ko) |
| AU (1) | AU2009206748B2 (ko) |
| CA (1) | CA2712757A1 (ko) |
| ES (1) | ES2539124T3 (ko) |
| HK (2) | HK1143822A1 (ko) |
| IL (1) | IL207155A (ko) |
| MX (3) | MX2010008050A (ko) |
| NZ (3) | NZ587105A (ko) |
| PL (1) | PL2245056T4 (ko) |
| SG (3) | SG10202011946PA (ko) |
| WO (1) | WO2009094172A2 (ko) |
Families Citing this family (54)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9585932B2 (en) | 2005-04-29 | 2017-03-07 | Peter C. Dowling | Use of EPO-derived peptide fragments for the treatment of neurodegenerative disorders |
| US9345745B2 (en) * | 2005-04-29 | 2016-05-24 | Bo Wang | Methods for treating inflammatory disorders and traumatic brain injury using stabilized non-hematopoietic EPO short peptides |
| US8653028B2 (en) | 2005-04-29 | 2014-02-18 | Rui Rong Yuan | Erythropoietin-derived short peptide and its mimics as immuno/inflammatory modulators |
| CA3079319A1 (en) | 2005-08-05 | 2007-02-15 | Araim Pharmaceuticals, Inc. | Tissue protective peptides and uses thereof |
| SG10202011946PA (en) | 2008-01-22 | 2020-12-30 | Araim Pharmaceuticals Inc | Tissue protective peptides and peptide analogs for preventing and treating diseases and disorders associated with tissue damage |
| WO2011127144A1 (en) | 2010-04-06 | 2011-10-13 | Synedgen Inc. | Methods and compositions for treating wounds utilizing chitosan compounds |
| US9999702B2 (en) * | 2010-04-09 | 2018-06-19 | Kci Licensing Inc. | Apparatuses, methods, and compositions for the treatment and prophylaxis of chronic wounds |
| US9526648B2 (en) | 2010-06-13 | 2016-12-27 | Synerz Medical, Inc. | Intragastric device for treating obesity |
| US10010439B2 (en) | 2010-06-13 | 2018-07-03 | Synerz Medical, Inc. | Intragastric device for treating obesity |
| US8628554B2 (en) | 2010-06-13 | 2014-01-14 | Virender K. Sharma | Intragastric device for treating obesity |
| US10420665B2 (en) | 2010-06-13 | 2019-09-24 | W. L. Gore & Associates, Inc. | Intragastric device for treating obesity |
| WO2012069474A2 (en) | 2010-11-24 | 2012-05-31 | H. Lundbeck A/S | A method for reducing potential virus burden in a sample by cyanate treatment |
| US20130288373A1 (en) * | 2010-12-20 | 2013-10-31 | Kenneth Verstraete | Crystal structure of flt3 ligand-receptor complex |
| WO2012174028A2 (en) * | 2011-06-13 | 2012-12-20 | The Board Of Trustees Of The University Of Illinois | Peptide compositions and methods for treating lung injury, asthma, anaphylaxis, angioedema, systemic vascular permeability syndromes, and nasal congestion |
| FR2978964B1 (fr) * | 2011-08-09 | 2015-02-20 | Conservatoire Nat Arts | Composition vaccinale anti-il-6 |
| CN105012313B (zh) * | 2014-04-25 | 2018-03-16 | 广州市赛普特医药科技股份有限公司 | 5α‑雄甾‑3β,5,6β‑三醇及其类似物在预防或治疗低压缺氧引起的高原病中的应用 |
| JP6426001B2 (ja) * | 2011-11-17 | 2018-11-21 | グリア エスピー ゼット.オー.オー. | 神経膠腫を治療するための組成物および方法 |
| EP2897622B1 (en) | 2012-09-20 | 2021-04-21 | Synedgen, Inc. | Methods for treatment or prevention of damage resulting from radiation |
| US9895399B2 (en) | 2013-01-31 | 2018-02-20 | The Trustees Of The University Of Pennsylvania | Repair of peripheral nerve injury |
| US20160222084A1 (en) | 2013-03-15 | 2016-08-04 | The Board Of Regents Of The University Of Oklahoma | Compositions Comprising D-Amino Acid Peptides and Methods of Production and Use Thereof for Inhibiting Autoantibodies |
| SG11201600294QA (en) * | 2013-07-17 | 2016-02-26 | Araim Pharmaceuticals Inc | Tissue protective peptides and peptide analogs for preventing and treating diseases and disorders associated with tissue damage |
| KR101510743B1 (ko) * | 2013-07-23 | 2015-04-10 | (주)케어젠 | 파골 세포 분화 억제용 펩타이드 및 이의 용도 |
| PT3104939T (pt) | 2014-02-10 | 2024-07-17 | Fred Hutchinson Cancer Center | Tratamento de ataque cardíaco e lesão isquémica com iodeto de sódio |
| US9314457B2 (en) | 2014-06-19 | 2016-04-19 | The University Of Utah Research Foundation | Methods of treating and preventing vascular instability diseases |
| GB2539161A (en) * | 2014-11-26 | 2016-12-14 | Neuro-Bio Ltd | Neurodegenerative disorders |
| US20180292390A1 (en) * | 2015-04-23 | 2018-10-11 | Rowan University | Novel slice cultures and methods for diagnosing neuronal degeneration diseases |
| CN105233256A (zh) * | 2015-10-28 | 2016-01-13 | 中国人民解放军第三军医大学 | 促红细胞生成素及其衍生物在制备治疗疾病中促进凋亡细胞清除的药物中的应用 |
| RU2613308C1 (ru) * | 2015-11-23 | 2017-03-15 | Федеральное государственное бюджетное учреждение "Ростовский научно-исследовательский онкологический институт" Министерства здравоохранения Российской Федерации | Способ прогнозирования предрасположенности к послеоперационному кровотечению при раке головки поджелудочной железы |
| JP7235509B2 (ja) | 2016-04-14 | 2023-03-08 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | 植え込み可能な生きた電極およびその製造方法 |
| US10779980B2 (en) | 2016-04-27 | 2020-09-22 | Synerz Medical, Inc. | Intragastric device for treating obesity |
| EP3448415A4 (en) * | 2016-04-29 | 2019-11-06 | Araim Pharmaceuticals, Inc. | TISSUE PROTECTIVE PEPTIDES FOR PREVENTING AND TREATING DISEASES AND DISORDERS ASSOCIATED WITH TISSUE INJURY |
| CN106075392B (zh) * | 2016-07-18 | 2020-07-07 | 滨州医学院 | 促红细胞生成素衍生物在听力保护上的应用 |
| IL247369B (en) * | 2016-08-18 | 2018-08-30 | B G Negev Tech And Applications Ltd | Polypeptides derived from CSF-m and their uses |
| US11390654B2 (en) * | 2016-09-02 | 2022-07-19 | Christopher Joseph Soares | Use of CGRP receptor antagonists in neuroprotection and neurological disorders |
| BR112019009246B1 (pt) | 2016-11-10 | 2023-01-17 | Asc Regenity Ltd | Formulações cosméticas contendo moléculas derivadas de eritropoietina, polipeptídeo isolado e uso do mesmo |
| CN110475786A (zh) * | 2017-02-27 | 2019-11-19 | 大邱庆北科学技术院 | 红细胞生成素衍生肽通过其对预防细胞损伤的作用的用途 |
| JP6450999B2 (ja) * | 2017-03-31 | 2019-01-16 | 国立大学法人群馬大学 | B型ボツリヌス毒素を用いたレイノー現象の治療 |
| WO2018204847A2 (en) * | 2017-05-05 | 2018-11-08 | Trefoil Therapeutics, Inc. | Recombinant modified fibroblast growth factors and therapeutic uses thereof |
| CN110590919B (zh) * | 2017-05-24 | 2022-05-24 | 中国海洋大学 | 含鸟氨酸的短肽及其应用 |
| EP3668532A4 (en) * | 2017-08-19 | 2021-09-01 | Ohio State Innovation Foundation | INNOVATIVE PEPTIDE BASED CANCER IMAGING AGENTS |
| US20200223894A1 (en) * | 2017-09-19 | 2020-07-16 | Auckland Uniservices Limited | Peptides for the treatment of conditions associated with adiponectin dysfunction |
| CN107880109B (zh) * | 2017-11-01 | 2019-08-30 | 复旦大学附属中山医院 | 一种促红细胞生成素来源肽及其制备方法和用途 |
| US10975124B2 (en) | 2018-02-23 | 2021-04-13 | The Board Of Regents Of The University Of Oklahoma | Methods and compositions for treating diseases and conditions associated with gonadotropin releasing hormone receptor |
| KR102167641B1 (ko) * | 2018-08-27 | 2020-10-19 | 주식회사 사이루스 | 에리스로포이에틴 유래 펩티드를 함유하는 세포증식 촉진용 조성물 |
| CA3112382A1 (en) | 2018-09-10 | 2020-03-19 | Cold Spring Harbor Laboratory | Methods for treating pancreatitis |
| KR20200080179A (ko) * | 2018-12-26 | 2020-07-06 | 아미코젠주식회사 | 아세틸콜린 수용체 저해 펩타이드 및 이의 용도 |
| WO2021137932A1 (en) * | 2019-11-04 | 2021-07-08 | Faraday Pharmaceuticals, Inc. | Use of iodide compounds for the treatment and prevention of chemotherapy-associated cachexia and cardiotoxicity |
| EP4100692A4 (en) | 2020-02-06 | 2024-03-06 | Austin Star Detonator Company | INTEGRATED IGNITION SENSORS |
| WO2021245677A1 (en) * | 2020-06-05 | 2021-12-09 | Digestix Bioscience Inc. | Compositions and methods for treating dysplastic and early-stage neoplastic conditions |
| CN111863118B (zh) * | 2020-07-20 | 2023-09-05 | 湖南莱博赛医用机器人有限公司 | 基于tct制片进行tct和dna倍体分析的方法 |
| CN112557347B (zh) * | 2020-11-12 | 2023-10-24 | 渤海大学 | 一种黏液层中乳糜粒子迁移模型的制备及检测方法 |
| WO2023000038A1 (en) * | 2021-07-23 | 2023-01-26 | Lateral IP Pty Ltd | Peptide compositions capable of binding lanthionine synthetase c-like protein (lancl) and uses thereof |
| CN114606317B (zh) * | 2022-03-22 | 2022-12-02 | 中山大学附属第一医院 | 一种预测胃癌淋巴结转移的菌群标志物及其应用 |
| CN117106057A (zh) * | 2022-08-19 | 2023-11-24 | 南京汉欣医药科技有限公司 | 一种高纯的人促肾上腺皮质激素或其类似物及其规模化制备方法 |
Family Cites Families (61)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1479268A (en) | 1973-07-05 | 1977-07-13 | Beecham Group Ltd | Pharmaceutical compositions |
| CH596313A5 (ko) | 1975-05-30 | 1978-03-15 | Battelle Memorial Institute | |
| NO812612L (no) | 1980-08-06 | 1982-02-08 | Ferring Pharma Ltd | Enzym-inhibitorer. |
| US4414147A (en) | 1981-04-17 | 1983-11-08 | Massachusetts Institute Of Technology | Methods of decreasing the hydrophobicity of fibroblast and other interferons |
| US4558006A (en) | 1983-02-04 | 1985-12-10 | Kirin-Amgen, Inc. | A.T.C.C. HB8209 and its monoclonal antibody to erythropoietin |
| US4496689A (en) | 1983-12-27 | 1985-01-29 | Miles Laboratories, Inc. | Covalently attached complex of alpha-1-proteinase inhibitor with a water soluble polymer |
| US5051448A (en) | 1984-07-24 | 1991-09-24 | The Mclean Hospital Corporation | GABA esters and GABA analog esters |
| US4704355A (en) | 1985-03-27 | 1987-11-03 | New Horizons Diagnostics Corporation | Assay utilizing ATP encapsulated within liposome particles |
| EP0229108B1 (en) | 1985-06-26 | 1990-12-27 | Cetus Corporation | Solubilization of proteins for pharmaceutical compositions using polymer conjugation |
| US4798824A (en) | 1985-10-03 | 1989-01-17 | Wisconsin Alumni Research Foundation | Perfusate for the preservation of organs |
| US6932968B1 (en) | 1989-07-26 | 2005-08-23 | Dade Behring Marburg Gmbh | Erythropoietin (EPO) peptides and antibodies directed against these |
| DE3924746A1 (de) * | 1989-07-26 | 1991-01-31 | Behringwerke Ag | Erythropoietin (epo)-peptide und dagegen gerichtete antikoerper |
| AU6501390A (en) | 1989-09-21 | 1991-04-18 | Synergen, Inc. | Method for transporting compositions across the blood brain barrier |
| US5192746A (en) | 1990-07-09 | 1993-03-09 | Tanabe Seiyaku Co., Ltd. | Cyclic cell adhesion modulation compounds |
| WO1994005332A2 (en) | 1992-09-01 | 1994-03-17 | Berlex Laboratories, Inc. | Glycolation of glycosylated macromolecules |
| US5559103A (en) | 1993-07-21 | 1996-09-24 | Cytel Corporation | Bivalent sialyl X saccharides |
| US5571787A (en) | 1993-07-30 | 1996-11-05 | Myelos Corporation | Prosaposin as a neurotrophic factor |
| US5700909A (en) | 1993-07-30 | 1997-12-23 | The Regents Of The University Of California | Prosaposin and cytokine-derived peptides |
| WO1995021919A2 (en) | 1994-02-14 | 1995-08-17 | Kirin Brewery Company, Limited | Protein having tpo activity |
| US5576423A (en) | 1994-12-02 | 1996-11-19 | Schering Corporation | Antibodies to the slam protein expressed on activated T cells |
| US6849602B1 (en) | 1996-03-05 | 2005-02-01 | The Regents Of The University Of California | Compositions for alleviating neuropathic pain with prosaposin receptor agonists |
| US6271196B1 (en) | 1996-03-05 | 2001-08-07 | Regents Of The University Of Ca | Methods of alleviating neuropathic pain using prosaposin-derived peptides |
| US6346390B1 (en) | 1996-03-08 | 2002-02-12 | Receptron, Inc. | Receptor derived peptides involved in modulation of response to ligand binding |
| US5952293A (en) | 1996-03-08 | 1999-09-14 | Receptron | Receptor derived peptides involved in inhibition of receptor internalization in response to ligand binding |
| US5835382A (en) | 1996-04-26 | 1998-11-10 | The Scripps Research Institute | Small molecule mimetics of erythropoietin |
| US6437216B1 (en) | 1997-11-13 | 2002-08-20 | Interleukin Genetics Inc. | Transgenic models of inflammatory disease |
| IL124015A0 (en) | 1998-04-08 | 1999-01-26 | Yeda Res & Dev | Pharmaceutical compositions comprising a protein |
| US6307024B1 (en) * | 1999-03-09 | 2001-10-23 | Zymogenetics, Inc. | Cytokine zalpha11 Ligand |
| NZ533098A (en) | 1999-04-13 | 2006-04-28 | Kenneth S | Modulation of excitable tissue function by peripherally administered erythropoietin at high doses |
| AU2001252650A1 (en) | 2000-04-28 | 2001-11-12 | Effector Cell Institute | Novel derivative of cell chemotactic factor |
| US7259146B2 (en) | 2000-05-26 | 2007-08-21 | Ortho-Mcneil Pharmaceutical, Inc. | Neuroprotective peptides |
| AU7490401A (en) * | 2000-05-26 | 2001-12-11 | Ortho Mcneil Pharm Inc | Neuroprotective peptides |
| WO2002043572A2 (en) | 2000-11-30 | 2002-06-06 | Henry M. Jackson Foundation | Erythropoietin and erythropoietin receptor expression in human cancer |
| PA8536201A1 (es) | 2000-12-29 | 2002-08-29 | Kenneth S Warren Inst Inc | Protección y mejoramiento de células, tejidos y órganos que responden a la eritropoyetina |
| US20030072737A1 (en) | 2000-12-29 | 2003-04-17 | Michael Brines | Tissue protective cytokines for the protection, restoration, and enhancement of responsive cells, tissues and organs |
| US7205275B2 (en) | 2001-10-11 | 2007-04-17 | Amgen Inc. | Methods of treatment using specific binding agents of human angiopoietin-2 |
| CA2490411A1 (en) | 2002-06-28 | 2004-01-08 | Centocor, Inc. | Mammalian epo mimetic ch1 deleted mimetibodies, compositions, methods and uses |
| EP1552298A4 (en) | 2002-07-01 | 2006-11-08 | Kenneth S Warren Inst Inc | RECOMBINANT TISSUE-PROOFING CYTOKINS AND NUCLEIC ACIDS COORDINATING THEREOF FOR THE PROTECTION, RECOVERY AND IMPROVEMENT OF CELLS, TISSUE AND ORGANS THEREOF |
| US7037902B2 (en) | 2002-07-03 | 2006-05-02 | Receptron, Inc. | Affinity small molecules for the EPO receptor |
| EP1545586A4 (en) | 2002-09-09 | 2007-09-26 | Warren Pharmaceuticals Inc | LONG-ACTING ERYTHROPOIETINES THAT MAINTAIN THE PROTECTIVE ACTIVITY OF THE TISSUE OF ENDOGENEURY ERYTHROPOIETIN |
| JP2004305006A (ja) | 2003-04-01 | 2004-11-04 | Japan Science & Technology Agency | 人工調製肺サーファクタント |
| US7718363B2 (en) | 2003-04-25 | 2010-05-18 | The Kenneth S. Warren Institute, Inc. | Tissue protective cytokine receptor complex and assays for identifying tissue protective compounds |
| CA2525568C (en) | 2003-05-12 | 2017-07-25 | Affymax, Inc. | Novel peptides that bind to the erythropoietin receptor |
| JP2007512001A (ja) | 2003-08-28 | 2007-05-17 | バイオレクシス ファーマシューティカル コーポレイション | Epoミメティックペプチドおよび融合タンパク質 |
| BRPI0409650A (pt) | 2003-09-09 | 2006-04-25 | Warren Pharmaceuticals Inc | métodos para regular o nìvel hematócrito e humanos, produtos de eritropoietina artificial, métodos para preparar um produto de eritropoietina e pra tratar anemia em pacientes em risco de dano no tecido, e, composição farmacêutica |
| EP1670492A4 (en) | 2003-09-29 | 2009-07-08 | Warren Pharmaceuticals Inc | FABRIC PROTECTION CYTOKINES FOR THE TREATMENT AND PREVENTION OF SEPTICEMIA AND THE FORMATION OF ADHESIONS |
| US20050090551A1 (en) | 2003-10-27 | 2005-04-28 | Board Of Trustees Of Southern Illinois University | Therapeutic use of methionine for the treatment or prevention of mucositis |
| ME02251B (me) | 2004-02-02 | 2015-12-31 | Engeneic Molecular Delivery Pty Ltd | Kompozicije i postupci in vitro i in vivo, ciljanog oslobađanja leka u ćelijama sisara, preko intaktnih minićelija izvedenih iz bakterija |
| US20080227696A1 (en) * | 2005-02-22 | 2008-09-18 | Biosurface Engineering Technologies, Inc. | Single branch heparin-binding growth factor analogs |
| EP1740530B8 (en) | 2004-03-16 | 2017-03-01 | Temple University - Of The Commonwealth System of Higher Education | Substituted phenoxy- and phenylthio-derivatives for treating proliferative disorders |
| US20050267027A1 (en) | 2004-04-05 | 2005-12-01 | Lounsbury Karen M | Use of erythropoietin for treatment of cancer |
| WO2007010552A2 (en) | 2005-03-17 | 2007-01-25 | Serum Institute Of India Limited | N- terminal peg conjugate of erythropoietin |
| US8653028B2 (en) | 2005-04-29 | 2014-02-18 | Rui Rong Yuan | Erythropoietin-derived short peptide and its mimics as immuno/inflammatory modulators |
| US9345745B2 (en) | 2005-04-29 | 2016-05-24 | Bo Wang | Methods for treating inflammatory disorders and traumatic brain injury using stabilized non-hematopoietic EPO short peptides |
| EP2377884A1 (en) | 2005-05-10 | 2011-10-19 | Neoloch Aps | Neuritogenic peptides |
| EP1736481A1 (en) | 2005-05-13 | 2006-12-27 | Charite Universitätsmedizin-Berlin | Erythropoietin variants |
| EP1888098A2 (en) | 2005-05-25 | 2008-02-20 | Neose Technologies, Inc. | Glycopegylated erythropoietin formulations |
| CA3079319A1 (en) | 2005-08-05 | 2007-02-15 | Araim Pharmaceuticals, Inc. | Tissue protective peptides and uses thereof |
| WO2007071248A2 (en) | 2005-12-20 | 2007-06-28 | Copenhagen University | Neuritogenic and neuronal survival promoting peptides derived from the family of s-100 proteins |
| JP2010513309A (ja) | 2006-12-18 | 2010-04-30 | アルタス ファーマシューティカルズ インコーポレイテッド | ヒト成長ホルモン製剤 |
| SG10202011946PA (en) | 2008-01-22 | 2020-12-30 | Araim Pharmaceuticals Inc | Tissue protective peptides and peptide analogs for preventing and treating diseases and disorders associated with tissue damage |
-
2009
- 2009-01-22 SG SG10202011946PA patent/SG10202011946PA/en unknown
- 2009-01-22 KR KR1020157033078A patent/KR101768792B1/ko active IP Right Grant
- 2009-01-22 MX MX2010008050A patent/MX2010008050A/es active IP Right Grant
- 2009-01-22 NZ NZ587105A patent/NZ587105A/xx not_active IP Right Cessation
- 2009-01-22 NZ NZ621196A patent/NZ621196A/en not_active IP Right Cessation
- 2009-01-22 JP JP2010544332A patent/JP5542064B2/ja not_active Expired - Fee Related
- 2009-01-22 CN CN202010159339.1A patent/CN111346213A/zh active Pending
- 2009-01-22 WO PCT/US2009/000424 patent/WO2009094172A2/en active Application Filing
- 2009-01-22 CN CN200980110883.9A patent/CN102066413B/zh not_active Expired - Fee Related
- 2009-01-22 EP EP15157182.5A patent/EP2933264A3/en not_active Withdrawn
- 2009-01-22 CN CN201510002352.5A patent/CN104689298A/zh active Pending
- 2009-01-22 KR KR1020187010703A patent/KR20180041269A/ko not_active Application Discontinuation
- 2009-01-22 ES ES09703197.5T patent/ES2539124T3/es active Active
- 2009-01-22 KR KR1020207017687A patent/KR20200075044A/ko not_active Application Discontinuation
- 2009-01-22 KR KR1020197020103A patent/KR20190085187A/ko not_active Application Discontinuation
- 2009-01-22 AU AU2009206748A patent/AU2009206748B2/en not_active Ceased
- 2009-01-22 KR KR1020107018602A patent/KR101572286B1/ko active IP Right Grant
- 2009-01-22 SG SG10201604530SA patent/SG10201604530SA/en unknown
- 2009-01-22 US US12/863,973 patent/US8853358B2/en active Active
- 2009-01-22 PL PL09703197T patent/PL2245056T4/pl unknown
- 2009-01-22 MX MX2014004271A patent/MX356129B/es unknown
- 2009-01-22 CA CA2712757A patent/CA2712757A1/en not_active Abandoned
- 2009-01-22 NZ NZ601868A patent/NZ601868A/en not_active IP Right Cessation
- 2009-01-22 KR KR1020177011116A patent/KR101850908B1/ko active IP Right Grant
- 2009-01-22 EP EP09703197.5A patent/EP2245056B1/en active Active
- 2009-01-22 SG SG2013011762A patent/SG188161A1/en unknown
- 2009-01-22 CN CN201810587683.3A patent/CN108743916A/zh active Pending
- 2009-01-22 KR KR1020187032456A patent/KR20180123731A/ko not_active Application Discontinuation
-
2010
- 2010-07-22 MX MX2019011592A patent/MX2019011592A/es unknown
- 2010-07-22 IL IL207155A patent/IL207155A/en active IP Right Grant
- 2010-11-05 HK HK10110367.2A patent/HK1143822A1/xx not_active IP Right Cessation
-
2014
- 2014-05-02 JP JP2014094974A patent/JP6309815B2/ja not_active Expired - Fee Related
- 2014-09-30 US US14/502,735 patent/US9580465B2/en active Active
-
2016
- 2016-03-30 HK HK16103640.0A patent/HK1215713A1/zh unknown
- 2016-06-08 JP JP2016114592A patent/JP2017002040A/ja active Pending
-
2017
- 2017-01-30 US US15/419,963 patent/US20170232066A1/en not_active Abandoned
-
2019
- 2019-02-25 JP JP2019031123A patent/JP2019123715A/ja active Pending
- 2019-12-20 US US16/723,499 patent/US20200360476A1/en not_active Abandoned
-
2021
- 2021-02-04 JP JP2021016186A patent/JP2021073281A/ja active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101850908B1 (ko) | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 | |
| US20210107942A1 (en) | Tissue protective peptides and peptide analogs for preventing and treating diseases and disorders associated with tissue damage | |
| US10864253B2 (en) | Tissue protective peptides for preventing and treating diseases and disorders associated with tissue damage | |
| AU2014203195B2 (en) | Tissue protective peptides and peptide analogs for preventing and treating diseases and disorders associated with tissue damage | |
| AU2016203452B2 (en) | Tissue protective peptides and peptide analogs for preventing and treating diseases and disorders associated with tissue damage | |
| CERAMI et al. | Patent 2712757 Summary |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A107 | Divisional application of patent | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |