JP2010513309A - ヒト成長ホルモン製剤 - Google Patents
ヒト成長ホルモン製剤 Download PDFInfo
- Publication number
- JP2010513309A JP2010513309A JP2009541592A JP2009541592A JP2010513309A JP 2010513309 A JP2010513309 A JP 2010513309A JP 2009541592 A JP2009541592 A JP 2009541592A JP 2009541592 A JP2009541592 A JP 2009541592A JP 2010513309 A JP2010513309 A JP 2010513309A
- Authority
- JP
- Japan
- Prior art keywords
- hgh
- preparation
- crystals
- tris
- suspension
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/27—Growth hormone [GH] (Somatotropin)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/645—Polycationic or polyanionic oligopeptides, polypeptides or polyamino acids, e.g. polylysine, polyarginine, polyglutamic acid or peptide TAT
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/06—Drugs for disorders of the endocrine system of the anterior pituitary hormones, e.g. TSH, ACTH, FSH, LH, PRL, GH
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
- C07K14/61—Growth hormones [GH] (Somatotropin)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/34—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyesters, polyamino acids, polysiloxanes, polyphosphazines, copolymers of polyalkylene glycol or poloxamers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0021—Intradermal administration, e.g. through microneedle arrays, needleless injectors
Abstract
Description
本願は、2006年12月18日に出願された米国特許出願第60/870,605号に対する優先権を主張する。米国特許出願第60/870,605号の内容は、その全体が、本明細書中に参考として援用される。
本開示は、タンパク質治療剤の製剤に関し、より詳しくは、ヒト成長ホルモンの製剤に関する。
ソマトトロピンあるいは成長ホルモン(「GH」)は、内分泌系の主要な腺である腺性下垂体によって脳内で合成および分泌される刺激ホルモンの一類型を構成する哺乳動物のタンパク質である。腺性下垂体によるGHおよび他の刺激性ホルモンの分泌により、体全体の他の内分泌腺および組織内の細胞の活性が調節される。具体的には、GHは、下垂体前葉の成長ホルモン分泌細胞によって分泌され、肝臓および他の組織を刺激してIGF−1を合成および分泌する機能を果たす。IGF−1は、細胞分裂を制御し、代謝プロセスを調節し、遊離状態で存在するか、またはIGFBP−1〜6で指定される6つの他のタンパク質の1つに結合するタンパク質である。この分泌プロセスそれ自体は、ソマトリベリン(GH放出を促進)およびソマトスタチン(GH放出を阻害)の作用に対抗することによりモジュレートされる。
本開示は、改善された安定性を有する結晶性hGHの製剤を提供する。さらに、本開示は、かかる製剤の調製方法およびかかる製剤を用いた治療方法を提供する。
本明細書に記載のhGH調製物を提供すること、および
例えば、注射によって、2、3、4、5、6、7、8、9または10日に1回以下で投与すること
を含む。
該関係者に、本明細書に記載の調製物の成分を含むhGH調製物が所定の期間および/または所定の条件で安定であることを指示することを含む(includes comprising)。
hGH調製物、例えば本明細書に記載のhGH調製物が所定の期間および/または所定の条件で安定であることのエビデンスを提供すること、または安定であると明示すること
を含む。
約−30℃〜約10℃の一次乾燥サイクル
を含む。
該調製物(例えば、該凍結乾燥物を再懸濁した後)を、例えば注射によって前記患者に、例えば、2、3、4、5、6、7、8、9または10日に1回以下で投与すること
を含む。
概論:結晶性hGHの安定性
経時的に、結晶性hGHの懸濁液では、可溶性タンパク質の凝集体が現れることがあり得、hGHが酸化、脱アミド化、化学分解および結晶形態の変化を受けることがあり得、hGHが溶液中に溶解することがあり得る。
ヒト成長ホルモン
用語「成長ホルモン(GH)」は、一般的に、哺乳動物の下垂体によって分泌される成長ホルモンをいう。網羅的列挙ではないが、哺乳動物の例としては、ヒト、類人猿、サル、ラット、ブタ、イヌ、ウサギ、ネコ、ウシ、ウマ、マウス、ラットおよびヤギが挙げられる。本開示の好ましい実施形態によれば、哺乳動物はヒトである。
最も好ましい実施形態において、一価のカチオンはナトリウムである。最も好ましい実施形態において、ヒト成長ホルモンまたはヒト成長ホルモン誘導体は、ヒト成長ホルモンまたはヒト成長ホルモン誘導体のモノマーまたはモノマー鎖1つあたり約1〜約500個の一価のカチオン分子を含む。
液状懸濁剤製剤
製剤化ビヒクル
ポリArg複合体型hGH結晶を懸濁させるpH、緩衝液、塩、懸濁化剤、ヒアルロン酸(「HA」)および/または保存料の配合物を「製剤化ビヒクル」と称することがあり得る。該ビヒクルの各成分は、個々に、または組合せで種々であり得、所望の特性、例えば安定性が増大した複合体型hGH結晶の懸濁液がもたらされるように最適化され得る。
pH
懸濁液のpHは、hGH複合体型結晶(ポリArg複合体型hGH結晶の懸濁液)の安定性に影響を及ぼす主な因子であり得る。例えば、該懸濁液のpHは、hGH複合体型結晶の脱アミド化と酸化に影響を及ぼし得る。ある実施形態において、約7.0または7.5(他の製剤化条件に応じて)より上のpHにより、タンパク質の(図1)と酸化の両方の増大が引き起こされ得る。脱アミド化は、例えば、カチオン交換HPLC(CEX−HPLC)によって測定され得る。酸化は、例えば、逆相HPLC(RP−HPLC)によって測定され得る。約5.5または約5.0より下のpHでは、例えば、該懸濁液の他の特性にもよるが、タンパク質の混濁がもたらされ得る。濁度は、例えば、320nmで読み取りが行なわれるUV吸光度によって測定され得る。
緩衝液
懸濁液を作製するために使用される緩衝液は、hGH複合体型結晶(ポリArg複合体型hGH結晶の懸濁液)の安定性に影響を及ぼす主な因子であり得る。例えば、該懸濁液の緩衝液は、hGH複合体型結晶の懸濁液の結晶の大きさと濁度(例えば、不溶性凝集体による)に影響を及ぼし得る。濁度は、例えば、320nmで読み取りが行なわれるUV吸光度によって測定され得る。結晶の大きさは、例えば、顕微鏡法およびレーザー回折粒径計測器によって評価され得る。
好ましい実施形態では、緩衝液は、ヒスチジン緩衝液、クエン酸緩衝液、またはTris緩衝液である。より好ましい実施形態では、緩衝液はリン酸緩衝液である。また、緩衝液の濃度は種々であり得、例えば、緩衝液成分、例えば、リン酸塩、グリシン、ヒスチジン、クエン酸塩、酢酸塩、またはTrisの濃度は、種々であり得る。
塩
懸濁液に使用される塩は、hGH複合体型結晶(ポリArg複合体型hGH結晶の懸濁液)の安定性に影響を及ぼす主な因子であり得、例えば、該懸濁液中の塩の含有量は、脱アミド化速度および/または懸濁液中のhGH複合体型結晶のレベルに影響を及ぼし得る。一例として、塩の含有量が高い(例えば、イオン強度が増大する)ほど、もたらされ得る脱アミド化は少なくなる。脱アミド化は、例えば、カチオン交換HPLC(CEX−HPLC)によって測定され得る。
懸濁化剤
懸濁液に使用される懸濁化剤は、hGH複合体型結晶(ポリArg複合体型hGH結晶の懸濁液)の安定性に影響を及ぼす主な因子であり得る。例えば、該懸濁液中の懸濁化剤は、化学分解速度および/または脱アミド化速度および/または懸濁液中のhGH複合体型結晶のレベルに影響を及ぼし得る。懸濁化剤がないか、または少量だと、該懸濁液のケーキングがもたらされ得る。化学分解は、例えば、RP−HPLCによって測定され得る。脱アミド化は、例えば、カチオン交換HPLC(CEX−HPLC)によって測定され得る。
hGHの濃度
懸濁液中のポリArg複合体型結晶の濃度は、hGH複合体型結晶(ポリArg複合体型hGH結晶の懸濁液)の安定性に影響を及ぼす別の因子であり得る。例えば、高濃度では、該懸濁液は粘稠性となり得る。タンパク質の安定性は、RP−HPLCにより、酸化のレベルまたは速度に関してアッセイされ得る。また、安定性は、カチオン交換HPLC(CEX−HPLC)により、脱アミド化のレベルまたは速度に関して測定され得る。
hGH対ポリArg比
懸濁液中の該複合体型結晶におけるポリArgに対するhGHの比は、該結晶の安定性に影響を及ぼす別の因子であり得る。例えば、ポリArgに対するhGHの比が小さいと、ポリArgに対するhGHの比が大きい(例えば、比(ration)が7)ときより分解レベルが高くなり得ることが考えられ得る。分解は、例えば逆相HPLC(RP−HPLC)によって測定され得る。
保存容器および容器の閉鎖部
懸濁液を保存するために使用する容器の選択および/または容器の閉鎖部の選択は、hGH複合体型結晶(ポリArg複合体型hGH結晶の懸濁液)の安定性に影響を及ぼし得る。例えば、容器および/または閉鎖部の選択は、用量の一貫性または製剤の減損に影響を及ぼし得る。例えば、結晶は、バイアルのボトルネック部に蓄積されることがあり得、あるいは閉鎖部(例えば、閉鎖部の壁面上)に蓄積されることがあり得る。さらに、容器および/またはその閉鎖部の形状もまた、用量の一貫性に影響を及ぼし得る。用量の一貫性は、例えば、回収されたhGH濃縮物の量を測定することにより、または例えば試料の撹拌後の抽出可能重量を測定することにより測定され得る。
上部空間
最後に、容器の上部空間もまたタンパク質の安定性に影響を及ぼし得る。例えば、容器の閉鎖部の上部空間は、送達用量の一貫性に対して有意な影響を有し得る。
保存料
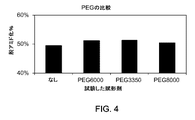
保存料は、例えば抗菌性保存料が、反復用量医薬製剤の調製物に使用され得る。懸濁液状のポリArg複合体型結晶製剤における保存料の任意選択的な添加およびその濃度は、hGH複合体型結晶(ポリArg複合体型hGH結晶の懸濁液)の安定性に影響を及ぼす因子であり得る。例えば、保存料の存在は、該複合体型hGHの安定性、結晶構造および/または有効性(例えば、放出プロフィール)に影響を及ぼし得る。結晶構造は、顕微鏡法によってアッセイされ得る。放出プロフィールは、製剤の上清み中のhGHの濃度をアッセイすること、または製剤中の遊離hGHの割合を計算することにより測定され得る。
ヒアルロン酸
ヒアルロン酸(「HA」)もまた、本明細書に記載の製剤に含めることがあり得る。本開示においては、HAとその塩の両方の使用が想定される。例えば、HAにより、結晶の過剰な電荷が緩和され得、それにより、HAを使用しない場合は複合体型hGH結晶製剤の投与によって引きこされ得る注射部位での反応の可能性が低減され得る。他の利点としては、被検体(例えば、ヒト)への投与後の複合体型結晶の徐放プロフィールへの寄与、微細ゲージ(fine gauged)(例えば、非常に微細なゲージ、例えば30ゲージ)針での注射が可能、複合体の結晶化度および完全性の経時的な保持が挙げられ得る。ある実施形態では、HAの使用により、hGHの放出プロフィールまたはインビボ有効性は改変されない。
凍結乾燥製剤
hGH結晶の凍結乾燥製剤
凍結乾燥されたhGHまたはhGH誘導体タンパク質製剤(例えば、ポリArgと複合体形成されたもの)(例えば、凍結乾燥調製物の再構成後)では、hGH製剤の安定性が増大され得る。例えば、本明細書に記載の凍結乾燥製剤は、冷蔵温度または室温で約24ヶ月以上の化学安定性が得られることが予測される。
解析方法
製剤の開発は、以下の特徴:種々の温度での保存安定性、用量の一貫性の関数としての容器と閉鎖部の適合性、付着の可能性、製剤の投与の容易さ、および容器の閉鎖部に対するロスによって評価され得る。安定性の試験方法およびその適用を以下の表1に示す。
アレニウスプロット反応速度論を使用し、短期安定性データ(例えば、50℃、40℃、35℃、30℃および25℃などの高い保存温度でストレス負荷した試料から得られたもの)を用いて、2〜8℃での化学分解速度が予測され得る。2〜8℃の外挿データを用いて、提案貯蔵寿命または有効期限が確立され得る。
hGH含有量
ポリArgと複合体形成されたhGH結晶を含む懸濁液のhGH含有量は、UV分光測光法によって測定され得る。ポリArgと複合体形成されたhGH結晶の懸濁液を50mMグリシン、pH2.6に溶解させ、280nmにおける吸光度を測定する。HGHの濃度は、測定された吸光度値に希釈率を乗算し、次いで、rhGHの吸光係数0.75mL・mg−1・cm−1で除算することにより計算される。
濁度
ポリArgと複合体形成されたhGH結晶の懸濁液の濁度は、UV分光測光法によって測定され得る。ポリArgと複合体形成されたhGH結晶の懸濁液を50mMグリシン、pH2.6に溶解させ、320nmにおける吸光度を測定する。
粒径分布
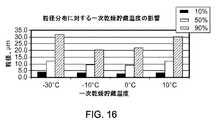
粒径分布を値を求めると、ポリArgと複合体形成されたhGH結晶を含む懸濁液の製造プロセスの一貫性が評価され得る。粒径分布は、微小容量モジュールを備えたCoulter LS 230 Particle Size Analyzer (Coulter Corp.,Miami、Florida)を使用し、レーザー回折によって測定され得る。試料を、試料緩衝液または1×PBSまたは製剤化ビヒクル中に希釈し、8〜12%の不透明性の機能範囲を得る。各試料を3連で解析し、フラウンホーファー光学モデルを用いてデータ解析を行なう。10%(dl10)、50%(メジアン)および90%(dl90)の累積分布限界を表す容量を報告する。この試験方法は、製剤安定性試験でも同様に行なわれ得る(すなわち、保存時の粒子分布の変化の可能性を評価するため)。
RP−HPLC(酸化のパーセンテージ、およびポリ−L−アルギニン含有量)
これらの解析には、同じ移動相とカラムが使用され得る。ポリLアルギニン(ポリArg)定量のための方法は、214nmで行なわれ得、hGHの定量は280nmで行なわれ得る。ポリLアルギニンおよびhGHの量を用いて、上清みおよび総ポリ−L−アルギニン含有量に対する遊離hGHを計算し、報告する。HGH/ポリArg比(質量対質量)は、消散係数0.75を用い、OD280から誘導される総hGH濃度を用いて計算され得る。ポリ−L−アルギニンの定量は、ポリ−L−アルギニン標準の較正曲線を使用することにより行なわれ得る。試験試料中のポリL−アルギニンの濃度は、ポリ−L−アルギニン標準の線形回帰直線に基づいて測定され得る。C5 Supelco Discovery Bio Wide Poreカラム(5cm×4.6mm、3μm粒径、300A細孔径)が使用され得る。HPLC解析用のhGH試料は、50mMグリシン緩衝液、pH2.6での溶解によって調製され得る。rhGHの溶出は、1.0mL/分の流速で、移動相A(0.1%トリフルオロ酢酸を含む水)および移動相B(0.1%トリフルオロ酢酸を含むアセトニトリル)で構成される移動相勾配を使用し、以下のとおりに行なわれる:95%A/5%Bで0〜2分間保持、2〜8分間で50%A/50%Bに線形変更、8〜20分間で30%A/70%Bに線形変更、20〜22分間で10%A/90%Bに線形変更、10%A/90%Bで22〜25分間保持した後、初期条件95%A/5%Bに戻す。酸化型rhGHのピーク面積を計算し、非酸化型rhGHのものと比較する。純度を、rhGHに関連するすべてのピークの総面積に対する酸化型のピークのピーク面積の割合として計算する。
可溶性凝集体(高分子量の%)
rhGHの高分子量の可溶性凝集体はrhGHモノマーから、サイズ排除HPLCによって分離され得る。Phenomenex BioSep−SEC−S 2000(7.8mm内径×60cm)カラムが使用され得る。HPLC解析用のhGH試料は、pH2.6の50mMグリシン緩衝液での溶解によって調製され得る。rhGHの溶出は、0.4mL/分の流速で、60mMリン酸ナトリウム、3%イソプロパノール、pH7.0からなる移動相を用いて定組成的に行なわれる。rhGHモノマーおよび凝集体の検出は、280nmで行なわれる。凝集rhGHのピーク面積を測定し、rhGHモノマーピークのものと比較する。rhGHのメインピークより前のピークはrhGHの凝集種である。凝集体の割合を、rhGHタンパク質のすべてのピークの総面積に対する凝集体のピークのピーク面積の割合として計算する。
脱アミド化および他の分解
脱アミド化型rhGHのピークは非脱アミド化型rhGHから、カチオン交換HPLC(CEX−HPLC)によって分離され得る。PolyLC PolySULFOETHYL A(4.6mm×50mm、5μm、300Å)カラムが使用され得る。HPLC解析用のhGH試料は、50mMグリシン緩衝液、pH2.6での溶解によって調製され得る。rhGHの溶出は、1.0mL/分の流速で、移動相A(50mMの酢酸ナトリウム、pH4.6)および移動相B(50mMの酢酸ナトリウム、250mMの塩化ナトリウム、pH4.6)で構成される漸増塩濃度の移動相勾配を用いて、以下のとおりに行なわれる:100%A/0%Bで開始、0 5分間で80%A/20%Bに線形変更、5〜40分間で40%A/60%Bに線形変更、4〜45分間で0%A/100%Bに線形変更、そして5分で初期条件(100%A)に戻す。脱アミド化型および非脱アミド化型rhGHの検出は、280nmで行なった。ストレス負荷試料におけるrhGHのメインピークより前のピークは、おそらく脱アミド化型および分解されたrhGH種である。脱アミド化型rhGHのピーク面積を計算し、非脱アミド化型rhGHのものと比較する。純度を、rhGHに関連するすべてのタンパク質ピークの総面積に対する分解された種のピークのピーク面積の割合として計算する。
溶解プロフィール
hGH結晶の溶解試験を開発し、適当な緩衝液中へのポリLアルギニンコートhGH結晶の溶解が行なわれている際の関連パラメータをモニターする。溶解緩衝液として、クエン酸塩、pH5.0が使用され得る。複合体型hGHの溶解速度を、一定mgのhGH結晶、クエン酸塩(pH5.0)媒体中、一定の攪拌速度および37℃の条件下で測定する。最初に分散を行なった後、遠心分離により上清みを除去し、次いで生理学的条件と類似した新たな媒体を補給する。この手順を15分毎に1時間まで繰り返し、次いで溶解速度を計算する。
生体活性およびpKプロフィール
インビボ評価に使用される種は、ドブネズミ(Rattus norvegicus)(ウィスターラット、下垂体を切除したもの)であり得る。処置群は、適合週用量レベルで結晶性hGHと市販のhGH製剤との同等性が測定されるように設計する。希釈した試験品を、脊椎の両側の胸腰領域にゆっくりと皮下注射する。針を脊椎から遠いところに指向し、中心(hub)まで挿入した後、いずれかの物質を注射した。注射部位は、注射を容易にする必要性に応じて、投与3日前および投与後に剃毛し、印をつける。
用量はすべて、300μL容シリンジ(BDパーツ番号BD 320438)に装着した30ゲージ×8mmの針を用いて投与する。シリンジ上に印が付けられた各単回単位は、10μLに相当する。懸濁液または溶液の均一性を確実にするため、希釈した対照および試験品を、シリンジ内に吸引する前に気泡が発生しないように注意深く反転させる。この実験は、下垂体を切除した雄ウィスターラットに投与した場合のhGH製剤の生体活性を比較するための方法を提供する。比較が行なわれる対象の対照hGH製剤の選択は、一部、標準的なラット体重増加アッセイで既に確立された有効性に基づいて行なわれ得る。試験物質または対照物質を、下垂体を切除した雄ウィスターラット(9ラット/群)に皮下(SC)注射によって投与する。例えば、5.6mg/kgの対照製剤および試験製剤の単回SC注射を受けた後の下垂体を切除したラットの成長が比較され得る。別の例として、0.8mg/kgの市販の可溶性rhGH(例えば、Nutropin AQ)のSC注射を毎日7日間(すなわち、5.6mg/kg/週)が、対照として使用され得る。投与開始前毎週および第−7日から(投与前の7日間)第8日の観察期間の最後まで毎日、体重を測定する。また、別個の試験におけるpKプロフィールアッセイでの血中hGHレベルの測定のための血液が採取され得る。血中hGHレベルは、ELISAによって測定され得る。
医薬製剤
本明細書に記載の結晶性タンパク質製剤、例えば、ポリArg複合体型hGH結晶は、治療用途のため、例えば、hGHの不足または欠乏に苦しむ被検体を治療するための医薬製剤に製剤化され得る。
哺乳動物において、GHは、組織を刺激してタンパク質IGF−1を合成および分泌させ、このタンパク質は、次いで細胞分裂および代謝プロセスにある役割を果たす。当業者には認識されるように、血清hGHおよびIGF−1レベルは、多くの因子、例えば、生理学的および処置関連因子に依存する。かかる因子としては、限定されないが、生理学的因子、例えば、実年齢および骨年齢、性別、体重、発達段階(例えば、思春期の成長レベル)ならびに処置関連因子、例えば、用量、投与速度(動態)および投与経路など、ならびに患者の診断および病歴などが挙げられる。また、当業者には、種々の患者集団に対して種々のhGHレベルおよびIGF−1レベルが、安全性と有効性の両方の観点から有益であり得ることが認識される。
キット
ポリArg複合体型結晶性hGHを含有する製剤と、使用説明書と、任意選択で、該製剤を投与するためのデバイスとを含むキットもまた、本開示の一部である。製剤は、適当な容器内(例えば、バイアル、プレフィルドシリンジなど)に存在させ得る。使用説明書には、任意の形態、例えば、パンフレットもしくはシート、または使用説明書が得られるサイトへのワールドワイドウェブのアドレスが採用され得る。使用説明書には、例えば、保存および/または投与のための使用説明が含まれ得る。
概論:結晶性タンパク質製剤のための無針注射システム
本開示は、さらに、被検体への投与のためのニードルフリー(ジェット式)注射器での使用のための治療用タンパク質の結晶性懸濁液の分野に関する。本開示はまた、無針(needless)注射に適した結晶性タンパク質製剤の調製方法を特徴とする。
BioJector 2000:BioJector 2000は、2つの構成要素:手持ち型の再度使用可能なジェット式注射器と、滅菌された単回使用の使い捨てプラスチック製シリンジからなる。BioJector 2000には、動力供給源として使い捨て二酸化炭素カートリッジが使用されている。この二酸化炭素ガスが、一貫した確実な圧力を使い捨てシリンジのプランジャーに供給し、それにより適用薬物が組織内に推進される。
VetJetおよびVitajet:VetJetは、獣医学的市場における使用のための改良型Vitajetである。VetJetもまた携帯型注射器ユニットおよび使い捨てシリンジの2つの構成要素で構成されている。VetJetはバネによって動力供給される。
ニードルフリー注射器は、液状の非結晶性タンパク質製剤の投与に使用されている。結晶性タンパク質の懸濁液に対するニードルフリーデバイスの報告例がない考えられ得る理由は、タンパク質結晶が懸濁液中で微粒子状を呈し、これによりニードルフリーデバイスによる注射が困難となり得るため、または結晶性製剤に物理的変化が引き起こされ、それにより該製剤の治療作用が害され得るためである。
− 結晶性タンパク質懸濁製剤の投与のためのニードルフリー(ジェット式)注射デバイスの使用;
− 前記結晶性製剤の治療作用の保持;および
− ニードルフリー(ジェット式)注射器使用時の注射時の痛みの軽減
が挙げられる。:
本明細書に示したように、無針注射器の使用可能性に影響を及ぼす因子としては、
− 結晶性タンパク質の沈降速度、および
− 粒子(すなわち、結晶)の大きさ
が挙げられる。
粒径
結晶性タンパク質の粒径は、例えば、レーザー回折(例えば、微小容量モジュールを備えたCoulter LS 230 Particle Size Analyzer(Coulter Corp.,Miami、Florida)を使用)によって測定され得る。粒径(例えば、最大寸法)がオリフィスサイズより小さい(例えば、約1/2より小さい)場合、特に、粒径がオリフィスの直径の約1/3より小さい場合、
該製剤は、無針投与に適したものであり得る。
得る)が、結晶の大きさに影響を及ぼすように最適化され得る。
沈降速度
沈降速度は、結晶性タンパク質の無針投与に対する好適性に影響を及ぼし得る。沈降速度が高い場合、被検体に送達される用量は、一貫性がなくなることがあり得る。結晶性懸濁液の高い沈降速度は、用量調製および投与に必要とされる時間中にニードルフリーデバイス内で用量の再分布させる速度、例えば、水平位置でのデバイスの1時間の定温放置後、約90%再分布させる速度と定義され得る。低い沈降速度は、実質的な用量の再分布なく用量の調製および投与を可能にする速度と定義され得る。一実施形態では、高い沈降速度は、水平位置でニードルフリーデバイスを定温放置すると、注射されるのが用量の90%未満となる速度と定義され得る。一部のある実施形態では、低い沈降速度は、任意の位置での1時間を越える定温放置後、均一な用量(例えば、用量の再分布が最小限またはなし;例えば、約35%未満、約30%、約25%、約20%、約15%、約10%、約9%、約8%、約7%、約6%、約5%、約4%、約3%、約2%、約1%)を可能にする速度と定義され得る。
使用方法
無針注射システムを用いて、結晶性タンパク質を含有する製剤が被検体に投与され得る。例えば、被検体は該結晶性タンパク質での処置を必要とする患者であり得、例えば、該結晶性タンパク質は結晶性hGHであり得、患者は、hGHの欠乏に苦しむ患者であり得る。用量および用量投与スケジュールは、さまざまな因子に基づいて決定される。かかる因子としては、限定されないが、生理学的因子、例えば、実年齢および骨年齢、性別、体重、発達段階(例えば、思春期の成長レベル)ならびに処置関連因子、例えば、用量、投与速度(動態)および投与経路など、ならびに患者の診断および病歴が挙げられる。
キット
結晶性タンパク質を含有する製剤および無針投与における使用説明書、ならびに任意選択で無針投与のためのデバイスを含むキットもまた、本開示の一部である。製剤は、適当な容器内(例えば、バイアル、プレフィルドシリンジなど)に存在させ得る。使用説明書には、任意の形態、例えば、パンフレットもしくはシート、または使用説明書が得られるサイトへのワールドワイドウェブのアドレスが採用され得る。使用説明書には、例えば、保存および/または投与のための使用説明が含まれ得る。
解析方法
結晶性タンパク質の無針投与に対する好適性の評価に使用され得る解析方法としては、以下のものが挙げられる。
注射
結晶性製剤は、1S021シリンジを備えたBioJector 2000システム、および0.0062インチノズルシリンジRef# K7000、30G×1/2インチ針(BDパーツ番号 328466)が予め装着されたBD 0.5ccシリンジ、30G×1/2インチ(BDパーツ番号305106)、25G×5/8インチ(BDパーツ番号305122)、18G×1.5インチ(BDパーツ番号305196 )(1mL容シリンジに対するルアーロック(BDパーツ番号 309628)が取り付けられている)を備えたVetJetシステムの使用を伴って注射される。0.25mLの試料を2連で試験する。BioJector 2000システムおよびVetJetシステムは、BioJectorの推奨に従って使用する。
SE−HPLC
SE−HPLC(サイズ排除HPLC)法を用いて純度を測定するためには、Phenomenex BioSep SEC−S−2000カラムを使用する。10マイクロリットルの2mg/mL濃度の試料をカラム内に注入する。泳動バッファーは、3%IPAおよび60mMリン酸ナトリウム、pH7.0で構成する。流速を0.6mL/分に設定し、泳動時間を30分間とする。検出は214nmで行なう。得られたクロマトグラムを手作業で積分する。純度割合(モノマー)は、ピーク面積に基づいて計算した。
RP−HPLC
RP−HPLCは、純度の試験に使用する。タンパク質の純度をRP−HPLC法を用いて測定するためには、C5 Supelco Discovery Bio Wide Pore Column(5cm×4.6mm、3μm粒径、30nm細孔径)を使用する。カラムのサーモスタット温度を37℃に設定する。10マイクロリットルの試料を2mg/mL濃度で注入する。溶出は、1.0mL/分の流速で、移動相A(0.1%TFA含有水)および移動相B(0.8%TFA含有MeCN)によって提示される勾配系を用いて行なわれる。勾配系は、0分から2.5分で5%Bから50%Bに、次いで2.5分から15.5分で50%から70%Bに、次いで15.5分から17分で70%から90%に変化させ、この直後に再度5%Bを確立させる。その後3分保持した後、次の泳動を開始する。検出は214nmで行なう。得られたクロマトグラムを手作業で積分する。純度割合をピーク面積に基づいて計算する。
SCX−HPLC(強カチオン交換)クロマトグラフィー
SCX−HPLC法は、安定性の試験において脱アミド化特異的測定のために使用する。IEX−HPLC法を用いてタンパク質の純度を測定するため、PolyLC(NEST Groupカタログ番号P054SE0503)カラムを使用した。カラムのサーモスタット温度を30℃に設定した。20マイクロリットルの試料を2mg/mL濃度で注入した。溶出は、1mL/分の流速で、移動相A(50mMの酢酸Na、pH4.6)および移動相B(50mMの酢酸Na、pH4.6 250mMのNaCl)によって提示される勾配系を用いて行なわれる。勾配系は、0分から5分で0%Bから20%Bに、次いで5分から25分で20%から70%Bに、次いで25分から25.1分で70%から100%に変化させ、100%Bを27分まで維持した後、27.1分から再度0%Bを確立させた後、5分間置く。検出は、214nmおよび280nmで行なう。得られたクロマトグラムを手作業で積分した。純度割合は、ピーク面積に基づいて計算した。
粒径分布(PSD)
PSDは、微小容量モジュールを備えたCoulter LS 230 Particle Size Analyzer(Coulter Corp.,Miami、Florida)を用いて、レーザー回折によって測定される。試料を試料緩衝液中に希釈し、8〜12%の不透明性の機能範囲を得る。データ解析は、フラウンホーファー光学モデルを用いて行なう。10%(dl10)、50%(メジアン)および90%(dl90)の累積分布限界を表す粒径(単位:μm)の割合を報告する。
3−pH溶解試験
この試験は、タンパク質試料における溶解プロフィールの変化を評価するために使用する。
粒子表面の変化
粒子表面の変化は、Zetasizer Nano−Z(Malvern Instruments Ltd.UK)を用いて測定される。泳動バッファーは、20mMのTris、pH7.5とした。ゼータ電位変換標準(Zeta Potential Transfer Standard)を用いて、機器(Malvernカタログ番号DTS 1050)を較正する。各試料に対し、12μlの結晶性アリコート(濃度10〜30mg/ml)を588μlの泳動バッファーに添加し、室温で3回の測定値を得る。
顕微鏡像
結晶性試験品の顕微鏡像を評価し、注射による試験品の関連する変化を検出する。
制御放出プロフィールを有する長期作用性hGHを作製するためのhGHの結晶化および複合体形成のプロセスが開発されている(米国特許出願公開公報第2004/0209804号)。ポリArg複合体形成は、裸の(bare)hGH結晶が市販の日常注射製剤と同じ性能を示すため、制御放出プロフィールの寄与において重要である。ポリArg複合体型hGH結晶もしくはhGH誘導体、またはこれらをを含有する組成物もしくは製剤は、いくつかの利点、例えば、週1回の送達が可能であること、使用の準備ができた結晶性懸濁液形態であること、安全性、有効性、純度、安定性および一定期間にわたる注射針通過可能性を有する。該複合体型hGH薬物の送達方法は、ポリマーまたは融合タンパク質を使用せず、注射を少なくするため、および被検体に対してよりユーザーフレンドリーな処置選択肢がもたらされるように設計される。この結晶化技術の特異性は、上清み中に存在する遊離hGHが限定的であるため、可溶性凝集体の増加が観察されないことである。
6〜7のpH範囲の緩衝液(好ましくは、リン酸塩)、塩(好ましくは、塩化ナトリウムまたは酢酸ナトリウム)、および懸濁化剤(好ましくはポリエチレングリコール6000または8000)を用いて調製される。このような製剤と適合する容器の閉鎖部系は、10mm未満の上部空間を有するシリコーン処理されたプレフィルドシリンジ、または上部空間のないバイアルである。
プレフィルドシリンジ/ニードルステイクおよび10mm未満の上部空間は、タンパク質結晶非経口製剤に、より好適である。
実施例2
5±3℃(冷蔵)で約18〜約24ヶ月および室温25±2℃(使用時)条件で少なくとも1週間安定である目標のポリArg複合体型結晶製剤性hGHの懸濁液を調製するための試験を行なった。
室温での分解速度の推定
室温での当該新規製剤の安定性の解析により、同じ改善された安定性製剤#55−01Nが得られた(表24)。冷蔵保存条件で最適と特定された他の製剤は、室温で保存した場合も対照製剤よりも良好な安定性を有した。
インビボ結果:下垂体を切除したラットでの試験
これらの実験は、最適化された安定性製剤ビヒクルにおけるポリアルギニン複合体型hGH結晶の治療作用が、対照製剤のhGH放出プロフィールと同等であるか否かを調べるために行なった。下垂体を切除した雄ウィスターラットにおいて、対照ロットと最適化された安定性製剤ロット番号299−35−06(10mMのクエン酸Na、0.2%のTween20、0.25%のフェノール、150mMのNaCl pH6.0)間で、治療作用に有意差は観察されなかった。
標準的なラット体重増加アッセイにおける有効性の確認は、hGH製剤の臨床的開発および商品開発のための重要な工程である。試験物質または対照物質を、下垂体を切除した雄ウィスターラット(9ラット/群)にSC(皮下)注射により投与した。この試験では、5.6mg/kgの単回用量および反復用量の対照および当該新規製剤の単回SC注射、または0.8mg/kgの市販の可溶性rhGH(Nutropin AQ)の毎日のSC注射を7日間(すなわち、5.6mg/kg/週)受けた後の、下垂体を切除したラットの成長を比較した。投与開始前および第−7日から毎日(投与前の7日間)第8日の観察期間の最後まで毎日、体重を毎週測定した。この下垂体を切除したラットモデルにおいて、日常rhGH注射製剤、対照、および最適化された安定性製剤間で、体重増加に有意差は観察されなかった。平均体重変化は、それぞれ18±3%、18±2%、および16±4%であった。
結論
これらの試験により、製剤化ビヒクル中にポリアルギニンでコーティングされたhGH結晶含む懸濁液用の製剤化ビヒクルが特定された。該製剤は、
a)安定性の改善をもたらす
b)該複合体において対照製剤と同等の結晶化度を維持する
c)29以下のゲージ針での投与を可能にする
このような製剤は、以下のものを提供する
a)高分子電解質でコートされたhGH結晶の懸濁液、ここで、該結晶性hGHの濃度は、
5〜100mg/mL、好ましくは10〜50mg/mLの範囲、より好ましくは20〜30mg/mLの範囲である。
b)5.0〜8.0の範囲pHでhGH複合体の結晶化度を維持する生物学的に適合性の緩衝液で構成された製剤化ビヒクル中の懸濁液。緩衝塩濃度は、濃度1〜150mMの範囲である。好ましくは、2〜50mM;より好ましくは10mM濃度である。緩衝塩の例としては、酢酸塩、トリエタノールアミン、イミダゾール、リン酸塩、クエン酸塩、Tris−HClが挙げられる。好ましい緩衝液は、5.8〜7.0、好ましくは6.0〜6.5のpH範囲のリン酸ナトリウムである。緩衝液の組合せ、例えば、リン酸ナトリウムとクエン酸ナトリウムの緩衝液、例えば、2mMのクエン酸Na塩と8mMのリン酸Na塩が使用され得る。
c)hGH複合体の結晶化度を維持または増大させる成分。一例(as example)は中性塩、例えば、酢酸Naまたはポリエチレングリコール(PEG3350〜PEG8000)などである。好ましいPEG濃度は、1〜25w/v%、より好ましくは2〜10w/v%;より好ましくは4〜6w/v%の範囲である。フェノールは、0.1〜0.5%の濃度で使用され得る。
d)組成物の総重量オスモル濃度が、250〜450mOsm/kg、好ましくは270〜350mOsm/kg、より好ましくは280〜330mOsm/kgの範囲となるようにする張度調整剤。例としては、塩化ナトリウム、酢酸ナトリウム、Tris−HClなどの中性塩が挙げられる。作用緩衝pH範囲外の緩衝塩も中性塩として使用され得る。好ましい塩は、酢酸ナトリウムまたは塩化ナトリウムである。アミノ酸の塩も、緩衝pH範囲外のpH範囲で中性塩として使用され得る。好ましいアミノ酸の塩は、グリシンナトリウム塩である。マンニトール、ソルビトールなどのポリオールもまた、張度調整剤として使用され得る。ポリエチレングリコールも張度調整剤として使用され得る。
e)任意選択で、約0.25%w/vの濃度の保存料、例えばフェノール。好ましいフェノール濃度範囲は0.2〜0.3%である。
f)任意選択で、前記製剤の化学安定性を増大させる成分、例えば、メチオニン、EDTAなど。
リード製剤化ビヒクルの具体例:
10mMのリン酸Na、25mMのTris、100mMのNaAc、5%のPEG6000、pH6.5
10mMのリン酸Na、0.25%のフェノール、150mMのNaCl、5%のPEG6000 pH6.0
10mMのクエン酸Na、0.2%のTween20、0.25%のフェノール、150mMのNaCl、pH6.0
30mMのトリエタノールアミン、100mMの酢酸Na、5%のPEG6000 pH6.8
25mMのトリエタノールアミン、10mMのメチオニン、100mMのNaCl、2%のPEG3350 pH6.8
25mMのイミダゾール、100mMの酢酸Na、5%のPEG6000 pH6.5
潜在的に有益な製剤化ビヒクルの具体例:
2mMのクエン酸Na塩、8mMのリン酸Na塩、120mMのNaCl、0.3%のフェノール pH6.0
10mMのリン酸Na、100mMのグリシン、0.3%のフェノール、pH6.0
10mMのリン酸Na、100mMのNaCl、0.3%のフェノール、pH6.0
10mMのリン酸Na、100mMの酢酸Na塩、5%のPEG6000、pH6.0
10mMのリン酸Na、100mMのNaCl、5%のPEG6000、pH6.0
10mMのリン酸Na、100mMのNaCl、5%のPEG6000、pH6.5
2mMのクエン酸Na塩、8mMのリン酸Na塩、120mMのNaCl、0.3%のフェノール pH5.4
10mMのリン酸Na塩、100mMのNaCl、10%w/vのPEG3350 pH6.0
10mMのクエン酸Na塩、80mMのNa グリシン、10%w/vのPEG6000 pH5.4
10mMの酢酸Na塩、120mMのNaCl、10%w/vのPEG6000 pH5.6
前記製剤の調製:プロトコル
(1)ポリアルギニン複合体型hGH結晶、25mg/mlの作製(Govardhanら,2004:WO2004/060310)
(2)工程1生成物の遠心分離、3,5000rpm、15分、4℃
(3)上清みの除去、容量記録
(4)同容量の製剤化ビヒクルの添加
(5)ペレットの再懸濁
(6)工程3を反復、次いで、再懸濁時に所望のhGH濃度が得られる容量の製剤化ビヒクルの添加、再懸濁
(7)最終懸濁液を2〜8℃で保存
試料を低pH勾配RP−HPLC法により解析し、化学分解をモニターして脱アミド化を排除する;脱アミド化は、カチオン交換HPLCの使用により検出する;最後に、化学分解を、RP−HPLCおよびIEX−HPLCで得られた不純物数を合わせることにより示す。SE−HPLCを用いて凝集をモニターする。遊離ポリアルギニンに対する結合ポリアルギニンの比を、RP−HPLCで測定された上清み中に存在する総ポリアルギニン濃度に基づいて計算する。結晶化度は、RP−HPLC較正により、製剤の結晶性相中のhGH濃度に対する上清み中のhGH濃度の比として求める。
HPLC解析用の試料調製:RP−、IEX−およびSE−HPLC解析を行なうために、結晶を溶解させる。結晶を遠心分離し、上清みを除去する;結晶性ペレットをpH2.8の酢酸水溶液に、2mg/mL濃度となるように溶解させる。2分間の定温放置後、溶液を、12000rpmで4分間遠心分離する。次いで、HPLCを用いて試料を解析する。
RP−HPLC:RP−HPLCは、RP−HPLC法を用いてhGHの純度を調べるために使用する。C5 Supelco Discovery Bio Wide Pore Column(5cm×4.6mm、3μm粒径、30nm細孔径)を使用する。カラムのサーモスタット温度を37℃に設定する。10μLの試料を2mg/mL濃度で注入する。溶出は、1.0mL/分の流速で、移動相A(0.1%TFA含有水)および移動相B(0.1%TFA含有MeCN)によって提示される勾配系を用いて行なわれる。
勾配系は、0分から2.5分で5%Bから50%Bに、次いで2.5分から15.5分で50%から70%Bに、次いで15.5分から17分で70%から90%に変化させる。この直後、再度5%Bを確立させ、その後3分保持する。検出は214nmで行なう。得られたクロマトグラムを手作業で積分する。純度割合をピーク面積に基づいて計算する。
IEX−HPLC弱アニオン交換クロマトグラフィー:WAX−hGH法は、特に時間点0での安定性の試験における脱アミド化を測定するために使用する。WAX法を用いてhGHの純度を測定するためには、PolyMA WAX(Supelcoカタログ番号59602−U)を使用する。カラムのサーモスタット温度を37℃に設定する。5μLの試料を2mg/mL濃度で注入する。溶出は、0.5mL/分の流速で、移動相A(50mMのTRIS、pH8.0)および移動相B(50mMのTRIS、pH8.0 500mMのNaCl)によって提示される勾配系を用いて行なわれる。勾配系は、0分から30分で5%Bから30%Bに、次いで30分から40分で30%から50%Bに、次いで40分から42分で50%から95%に変化させ、45分まで95%Bで維持した後、再度50%Bを確立させ、その後3分保持する。検出は、214nmおよび280nmで行なう。得られたクロマトグラムを手作業で積分する。純度割合をピーク面積に基づいて計算する。
IEX−HPLC強カチオン交換クロマトグラフィー:SCX−hGH法は、安定性の試験において脱アミド化特異的に使用する。IEX−HPLC法を用いてhGHの純度を測定するためには、PolyLC(NEST Groupカタログ番号P054SE0503)を使用する。カラムのサーモスタット温度を30℃に設定する。20μLの試料を2mg/mL濃度で注入する。溶出は、1mL/分の流速で、移動相A(50mMの酢酸Na、pH4.6)および移動相B(50mMの酢酸Na、pH4.6 250mMのNaCl)によって提示される勾配系を用いて行なわれる。勾配系は、0分から5分で0%Bから20%Bに、次いで5分から25分で20%〜70%Bに、次いで25分から25.1分で70%から100%に変化させ、100%Bを27分まで維持した後、27.1分から再度0%Bを確立させた後、5分間置く。検出は、214nmおよび280nmで行なう。得られたクロマトグラムを手作業で積分する。純度割合をピーク面積に基づいて計算する。
SE−HPLC:試料中の凝集体の含有量を測定するために使用する。SE−HPLC Phenomenex BioSep SEC−S−2000カラムを使用する。10μlの2mg/mL濃度の試料をカラム内に注入する。泳動バッファーは、3%IPAおよび60mMリン酸ナトリウム、pH7.0で構成する。流速を0.6mL/分に設定し、泳動時間を30分間とする。検出は214nmで行なう。得られたクロマトグラムを手作業で積分する。純度割合をピーク面積に基づいて計算する。
結晶化度:結晶化度は、試料中の総hGH濃度に対する上清み中のhGH濃度(RP−HPLC較正に基づいたもの)の比として計算する。
実施例3
本開示は、高分子電解質と複合体形成されたhGH結晶の徐放性反復用量懸濁液の分野に関する。
この実験は、ポリアルギニンと複合体形成されたhGH結晶の懸濁液中の遊離hGHの含有量に対するクエン酸塩およびリン酸緩衝液の影響を評価するために行なった。対照として、既知hGH(対照)製剤を使用した。さらに2種類の試料を、ポリアルギニンと複合体形成されたhGH結晶のペレットを、界面活性剤、塩およびフェノールも含むクエン酸緩衝液系製剤化ビヒクルまたはリン酸緩衝液系製剤化ビヒクルに再懸濁させることにより、調製した。
ポリアルギニンと複合体形成されていないhGH結晶(すなわち、裸のhGH結晶)の懸濁液中の遊離hGHの含有量に対するクエン酸緩衝液およびリン酸緩衝液の影響を示すための実験を行なった。対照として、既存の(対照)複合体型hGH製剤の基準製剤化ビヒクルを使用した。さらに2種類の試料を、裸の結晶のペレットを、界面活性剤、塩およびフェノールも含有するクエン酸またはリン酸緩衝液系製剤化ビヒクルに再懸濁することにより調製した。
次の実験は、ポリアルギニンと複合体形成されたhGH結晶の対照製剤化ビヒクルまたはリン酸ナトリウム低pH製剤化ビヒクルでの懸濁液中の遊離hGHおよびポリアルギニンの含有量に対する、種々の濃度の種々の保存料の影響を示すために行なった。対照として、保存料の添加なしの製剤化ビヒクルを使用した。試料の上清み中の遊離hGHおよびポリアルギニンの含有量を、室温で1ヶ月間定温放置後に解析した。
この実験は、ポリアルギニンと複合体形成されたhGH結晶の対照製剤化ビヒクルおよびリン酸ナトリウム低pH製剤化ビヒクルでの懸濁液中のhGHの化学安定性に対する、種々の濃度の種々の保存料の影響を示すために行なった。対照として、保存料の添加なしの対照ビヒクルおよびリン酸ナトリウム低pH製剤化ビヒクルを使用した。hGH分解生成物の含有量の増加を、室温で1ヶ月間定温放置後に解析した。
この実験は、種々の製剤化ビヒクル中のポリアルギニンと複合体形成されたhGH結晶の形態構造に対する抗菌性保存料の影響を評価するために行なった。対照として、保存料の添加なしの対照ビヒクルおよびおよびリン酸ナトリウム低pH製剤化ビヒクルを使用した。室温で1ヶ月間定温放置後に、顕微鏡観察を行なった。抗菌性保存料無含有で0.5%のフェノールと0.3%のメタ−クレゾールを含む対照製剤化ビヒクル(右)の懸濁液中のポリアルギニンでコーティングされたhGH結晶の顕微鏡像を調べた。また、抗菌性保存料無含有で0.2%のフェノールと0.2%のメタ−クレゾールを含む低pHリン酸系製剤化ビヒクル(10mMのNaHPO4、100mMのNaCl、5%のPEG6000、pH6.0)の懸濁液中のポリアルギニンでコーティングされたhGH結晶の顕微鏡像も調べた。
インビボ結果:下垂体を切除したラットでの試験
この実験は、反復用量製剤化ビヒクル(保存料を含む)でのポリアルギニン複合体型hGH結晶の放出プロフィールが、単回用量の対照hGH製剤のhGH放出プロフィールと同等であるか否かを評価するために行なった。下垂体を切除した雄ウィスターラットにおいて、保存料なしの対照緩衝液中の複合体型hGHの単回用量製剤と、フェノールを含む対照緩衝液中の複合体型hGHの反復用量製剤間で、薬力学的プロフィールに有意差は観察されなかった。
標準的なラット体重増加アッセイにおける有効性の確認は、hGH製剤の臨床的開発および商品開発のための重要な工程である。試験物質または対照物質を、下垂体を切除した雄ウィスターラット(9ラット/群)にSC(皮下)注射により投与した。この試験では、5.6mg/kgの単回用量および反復用量の対照緩衝液中(保存料を含む)のhGH製剤の単回SC注射、または0.8mg/kgの市販の可溶性rhGH(Nutropin AQ)の毎日のSC注射を7日間(すなわち、5.6mg/kg/週)受けた後の、下垂体を切除したラットの成長を比較した。投与開始前および第−7日から毎日(投与前の7日間)第8日の観察期間の最後まで毎日、体重を毎週測定した。この下垂体を切除したラットモデルにおいて、日常rhGH対照、単回用量製剤および反復用量製剤間で、体重増加に有意差は観察されなかった。平均体重変化は、それぞれ18±3%、18±2%、および16±4%であった。
インビボ結果:下垂体を切除したラットでの試験
この実験は、反復用量製剤化ビヒクル(保存料を含む)でのポリアルギニン複合体型hGH結晶の放出プロフィールが、単回用量の対照hGH製剤のhGH放出プロフィールと同等であるか否かを評価するために行なった。下垂体を切除した雄ウィスターラットにおいて、保存料なしの対照緩衝液中の複合体型hGHの単回用量製剤と、フェノールを含む対照緩衝液中の複合体型hGHの反復用量製剤間で、PDプロフィールに有意差は観察されなかった。試験物質または対照物質を、下垂体を切除した雄ウィスターラット(9ラット/群)にSC(皮下)注射により投与した。この試験では、5.6mg/kgの単回用量および反復用量の製剤を受けた後の、下垂体を切除したラットの成長を比較した。
投与開始前および第−7日から毎日(投与前の7日間)第8日の観察期間の最後まで毎日、体重を毎週測定した。この下垂体を切除したラットモデルにおいて、単回用量製剤と反復用量製剤間で、体重増加に有意差は観察されなかった。平均体重変化は、それぞれ15±2%および16±1%(平均±SE)であった。
前記製剤の調製:プロトコル:
(1)ポリアルギニン複合体型hGH結晶、25mg/mlの作製
(Govardhanら,2004−WO2004/060310)
(2)工程1生成物の遠心分離、3,5000rpm、15分、4℃
(3)上清みの除去、容量記録
(4)同容量の反復用量製剤化ビヒクルの添加
(5)ペレットの再懸濁
(6)工程3を反復、次いで、
再懸濁時に所望のhGH濃度が得られる容量の製剤化ビヒクルの添加、再懸濁
(7)最終懸濁液を2〜8℃で保存
解析方法
RP−HPLCは、脱アミド化hGH以外のすべてのhGH関連不純物を検出するために使用され(脱アミド化はIEX−HPLCの使用により測定される、下記参照)、C5 Supelco Discovery Bio Wide Pore Column(5cm×4.6mm、3um粒径、30nm細孔径)において行なわれる。サーモスタットの温度は37℃である。溶出は、移動相A(0.1%TFA含有H2O)および移動相B(0.1%TFA含有MeCN)によって提示される勾配系を用いて行なわれる。勾配系は、0分から2.5分で5%Bから50%Bに、次いで2.5分から15.5分で50%から70%Bに、次いで1.5分で70%から90%に変化させ、この直後に再度5%Bを確立させる。その後3分保持した後、次の泳動を開始する。流速は1.0ml/分である。注入容量は、2mg/ml濃度のhGH試料で10μlである。検出は214nmで行なう。純度割合をピーク面積に基づいて計算する。
IEX−HPLCは、脱アミド化特異的アッセイとして使用する。hGHの純度を測定するためには、PolyLC(NEST Groupカタログ番号P054SE0503)を使用する。カラムのサーモスタット温度を30℃に設定する。20μLの試料を2mg/mL濃度で注入する。溶出は、1mL/分の流速で、移動相A(50mMの酢酸Na、pH4.6)および移動相B(50mMの酢酸Na、pH4.6 250mMのNaCl)によって提示される勾配系を用いて行なわれる。勾配系は、0分から5分で0%Bから20%Bに、次いで5分から25分で20%〜70%Bに、次いで25分から25.1分で70%から100%に変化させ、100%Bを27分まで維持した後、27.1分から再度0%Bを確立させた後、5分間置く。検出は280nmで行なう。純度割合をピーク面積に基づいて計算する。
実施例4
これらの実験は、ニードルフリー(ジェット式)注射器での投与での使用のための治療用タンパク質の結晶性懸濁液の分野に関する。液状可溶性製剤の医薬品の投与には、種々のデバイス、例えばニードルフリー(ジェット式)注射器デバイスを使用する。このようなデバイスは、薬物投与の容易性を改善すること、注射回数を減らすこと、および場合によっては、注射時の痛みを軽減することにより、患者のコンプライアンスの増大を補助する。
結晶性懸濁液を投与できる可能性を、ニードルフリージェット式注射器を用いて評価した。ニードルフリー注射器に使用され得る結晶性懸濁液に対する制限を特定した。しかしながら、適切に製剤化および選択された結晶性製剤は、ニードルフリー(ジェット式)注射システムを用いて投与され得る。
結晶性hGHの懸濁液に対する剪断応力の考えられ得る影響を試験するため、注射前および注射後の試料を、結晶性hGHの懸濁液の上清み中の遊離hGHおよびポリアルギニンの含有量について解析した。対照懸濁液ALTU−238は、ポリアルギニンでコーティングまたはポリアルギニンと複合体形成されたhGH結晶の製剤化ビヒクルでの既知懸濁液である。剪断応力により、前記製剤の放出特性が変化し得る。ALTU−238は、典型的な範囲の遊離hGHおよびポリアルギニンを含む。これらのパラメータの変化は、懸濁液中の結晶に対する前記注射システムの有害な影響の表示であり得、hGH放出プロフィールに影響を及ぼし得る。注射は3連で行なった。対照試料ならびに種々の注射システムを使用した後の試料の上清みを、hGHおよびポリアルギニンの含有量について解析した。3回の連続操作の遊離hGHおよびポリアルギニンの平均含有量を表36に示す。
この実験では、結晶性hGHの懸濁液(ALTU−238)の粒径に対するBioJector 2000ジェット式注射の影響を調べた。粒径は、Coulter LS 230粒径測定装置を用いて、注射前ならびに1回目および反復注射後に測定した。フラウンホーファー光学モデルを用いてデータを解析した。起こり得る結晶形態構造の変化の検出には、顕微鏡観察を使用した。
ポリアルギニンでコーティングされたhGH結晶のヒアルロン酸を含有する製剤化ビヒクルでの懸濁液HA−ALTU−238を使用し、この結晶性タンパク質懸濁製剤でのジェット式注射器の使用の実現可能性を試験した。この実験では、hGH凝集に対する種々の注射システムの影響を調べた。注射は2連で行なった。注射後、結晶を溶解させ、可溶性hGHを凝集についてSE−HPLCによって解析した。
この実験では、結晶性hGHの懸濁液(HA−ALTU−238)の粒径に対するBioJector 2000ジェット式注射の影響。粒径は、Coulter LS 230粒径測定装置を用いて、注射前ならびに1回目の注射後および反復注射後に測定した。フラウンホーファー光学モデルを用いてデータを解析した。起こり得る結晶形態構造の変化の検出には、顕微鏡観察を使用した。
可溶性hGH製剤に対するジェット式注射器の影響を試験するため、Nutropin AQ試料を使用した。30G×1/2針による注射前または注射後のNutropin AQ試料では、微粒状物質の形成は観察されなかった。しかしながら、BioJector 2000およびVetJet注射器での注射後のNutropin AQ試料では微粒状物質の形成が観察された。この微粒状物質は、おそらくジェット式注射器の使用の結果形成されたものである。これらのデータは、Nutropin AQ製剤がニードルフリー注射システムには適切でないかもしれないことを示し、タンパク質製剤に対するニードルフリー注射器の良好な使用には適切な製剤開発が必要とされ得るという考えを確証するものである。
ALTU−238は、ポリアルギニンでコーティングされたhGH結晶の懸濁液である。該結晶は、約10〜20μmの長さおよび約1〜2μmの厚みの針状形態を有する。該懸濁液自体は安定である。先の試験では、結晶の有意な沈降は少なくとも6ヶ月の保存期間の間、観察されなかった。しかしながら、結晶が高速で沈降する傾向がある一例として、市販のインスリン懸濁製剤がある。
同じ実験を、ALTU−238製剤を用いて行なった。製剤をBioJectorのシリンジ内に負荷し、水平、まっすぐ垂直または逆さまの位置に1時間保持した後、注射した。これらの保持試料を、製剤をジェット式注射器のシリンジに負荷したほぼ直後に注射された試料と比較した。注射後、注射分中のhGHの量とシリンジ内部に残留した量を測定し、シリンジ内に負荷された物質を100%とみなしてパーセンテージで表示した。
次に、結晶が大粒径および六角形の形態構造を有する他のモデル結晶性タンパク質懸濁液の特性に対するジェット式注射システムの影響を調べた。この実験では、約30μmの中粒径を有する六角形BC−Lipase結晶の懸濁液に対するジェット式注射システムの影響を調べた。注射の際に結晶形態構造の変化は検出されず、体積基準分布に有意な変化は検出されなかった(表45)。
結晶がさらに大きく六角形の形態構造を有する他のモデル結晶性タンパク質懸濁液の特性に対するジェット式注射システムの影響を調べた。この実験では、約80μmの中粒径を有する大きな結晶を有するひし形の3次元BC−Lipase結晶の懸濁液に対するジェット式注射システムの影響を調べた。
方法プロトコル
注射:結晶性製剤は、1S021シリンジを備えたBioJector 2000システム、および0.0062インチノズルシリンジRef# K7000、30G×1/2インチ針(BDパーツ番号 328466)が予め装着されたBD 0.5ccシリンジ、30G×1/2インチ(BDパーツ番号305106)、25G×5/8インチ(BDパーツ番号305122)、18G×1.5インチ(BDパーツ番号 305196)(1mL容シリンジに対するルアーロック(BDパーツ番号 309628)が取り付けられている)を備えたVetJetシステムを用いて注射される。0.25mLの試料を2連で試験する。BioJector 2000システムおよびVetJetシステムは、BioJectorの推奨に従って使用する。
SE−HPLC:SE−HPLC法を用いて純度を測定するためには、Phenomenex BioSep SEC−S−2000カラムを使用する。10マイクロリットルの2mg/mL濃度の試料をカラム内に注入する。泳動バッファーは、3%IPAおよび60mMリン酸ナトリウム、pH7.0で構成する。流速を0.6mL/分に設定し、泳動時間を30分間とする。検出は214nmで行なう。得られたクロマトグラムを手作業で積分する。純度割合(モノマー)は、ピーク面積に基づいて計算した。
RP−HPLC:RP−HPLCは、純度の試験に使用する。hGHの純度をRP−HPLC法を用いて測定するためには、C5 Supelco Discovery Bio Wide Pore Column(5cm×4.6mm、3μm粒径、30nm細孔径)を使用する。カラムのサーモスタット温度を37℃に設定する。10マイクロリットルの試料を2mg/mL濃度で注入する。溶出は、1.0mL/分の流速で、移動相A(0.1%TFA含有水)および移動相B(0.8%TFA含有MeCN)によって提示される勾配系を用いて行なわれる。勾配系は、0分から2.5分で5%Bから50%Bに、次いで2.5分から15.5分で50%から70%Bに、次いで15.5分から17分で70%から90%に変化させ、この直後に再度5%Bを確立させる。その後3分保持した後、次の泳動を開始する。検出は214nmで行なう。得られたクロマトグラムを手作業で積分する。純度割合をピーク面積に基づいて計算する。
IEX−HPLC(強カチオン交換)クロマトグラフィー:SCX−hGHは、安定性の試験において脱アミド化特異的に使用する。IEX−HPLC法を用いてhGHの純度を測定するため、PolyLC(NEST Groupカタログ番号P054SE0503)カラムを使用する。カラムのサーモスタット温度を30℃に設定する。20マイクロリットルの試料を2mg/mL濃度で注入する。溶出は、1mL/分の流速で、移動相A(50mMの酢酸Na、pH4.6)および移動相B(50mMの酢酸Na、pH4.6 250mMのNaCl)によって提示される勾配系を用いて行なわれる。勾配系は、0分から5分で0%Bから20%Bに、次いで5分から25分で20%から70%Bに、次いで25分から25.1分で70%から100%に変化させ、100%Bを27分まで維持した後、27.1分から再度0%Bを確立させた後、5分間置く。検出は、214nmおよび280nmで行なう。得られたクロマトグラムを手作業で積分する。純度割合は、ピーク面積に基づいて計算する。
粒径分布(PSD):粒径分布は、微小容量モジュールを備えたCoulter LS 230 Particle Size Analyzer(Coulter Corp.,Miami、Florida)を用いて、レーザー回折によって測定される。試料を試料緩衝液(結晶性タンパク質3用の製剤化ビヒクル)中に希釈し、8〜12%の不透明性の機能範囲を得る。データ解析は、フラウンホーファー光学モデルを用いて行なう。10%(dl10)、50%(メジアン)および90%(dl90)の累積分布限界を表す粒径(単位:μm)の割合を報告する。
3−pH溶解試験:3−pH溶解試験は、ALTU−238試料における溶解プロフィールの変化を評価するために使用する。
粒子表面の変化:粒子表面の変化は、Zetasizer Nano−Z(Malvern Instruments Ltd.UK)を用いて測定される。泳動バッファーは、20mMのTris、pH7.5とする。ゼータ電位変換標準(Zeta Potential Transfer Standard)を用いて、機器(Malvernカタログ番号DTS 1050)を較正する。各試料に対し、12μlの結晶性アリコート(濃度10〜30mg/ml)を588μlの泳動バッファーに添加し、室温で3回の測定値を得る。
顕微鏡像:結晶性試験品の外観を顕微鏡によって評価し、注射による試験品の関連する変化を検出する。
実施例5
ALTU−238は、長期作用性のポリアルギニン(ポリArg)コート結晶性ヒト成長ホルモン(ソマトロピン)である。さらなる開発として、凍結乾燥形態および再構成凍結乾燥製剤を開発した。再構成凍結乾燥製剤では、再懸濁後、2〜8℃で24ヶ月以上の化学安定性が得られることが予測される。
1.約20〜約50mg/mLのhGH結晶の懸濁液
2.緩衝液として、Trisまたはリン酸塩とTrisもしくはヒスチジンいずれかとの併用緩衝液
3.7〜9のpH範囲
4.塩:50mM〜100mMの範囲の塩化ナトリウムまたは酢酸ナトリウム
5.懸濁化剤およびケーキング剤として、2.5%〜10%の範囲のポリエチレングリコール6000または8000
6.シリコーン処理されたバイアルまたはコーティングされたバイアル、例えば、Schott I型+ガラス製バイアル、または表面コートされた容器の閉鎖部
7.溶解サイクルパラメータとして、−50℃〜−60℃の凍結貯蔵温度、−30℃〜10℃の一次乾燥貯蔵温度、および20℃〜40℃の二次乾燥
を含む。
これらの成分および量は、凍結乾燥前の製剤に適したものであり、また、凍結乾燥hGHを再構成させた後の製剤にも適したものである。
表48に列挙した試験方法の1つ以上を用いて、再構成凍結乾燥形態の製剤の安定性が評価される。該試験方法を実施するための詳細は、当該技術分野で知られており、本明細書に記載している。
製剤を改善するため、以下の試験は、緩衝液種の選択および緩衝液濃度を中心として行なった。Tris含有prelyo懸濁液では、TrisがこのpHで最大緩衝能を有するため;および/または再構成させると、緩衝液成分の1つとしてリン酸塩を添加によりリン酸塩がpH7.5で緩衝し得るため、pHを約8まで上げた。ヒスチジンを第2の緩衝液として選択する考えは、凍結乾燥プロセス中、リン酸塩の存在のためpHが低い方にシフトし過ぎ、結晶溶解がもたらされるのを抑制するためであった。0.2mLおよび1.0mLの薬物製剤を送達するのに、2つの充填容積:0.5mLおよび1.2mLを評価した。本発明者らの目的が達成され得る3つの緩衝液系を、Tris、pH8.0;ヒスチジン(リン酸塩を有する)pH7.5において製剤化した。興味深い観察結果の1つは、Tris、pH8.6において製剤化した試料で、pHが8.0に低下したことであり、これにより、複合体型hGH結晶の最適緩衝液範囲は8あたりであるばずという説が確認された。これらのすべての結果に基づき、pH8のTrisを用いた緩衝液;ならびにヒスチジンとリン酸塩またはTris/リン酸塩を含有する2つの緩衝液組合せを、ポリArg複合体型hGH結晶に選択する。
a.凍結速度 1℃/分
b.−50℃〜−60℃で凍結
c.一次乾燥貯蔵温度範囲 −30℃〜10℃
d.二次乾燥貯蔵温度 20℃〜40℃
である。
リード製剤の一例の安定性の結果を以下の表にまとめる。データはすべて、これらの2つのサイクルで作製した試料と比較した場合、同等である。
Claims (125)
- 高分子電解質複合体型組換えヒト成長ホルモンまたはヒト成長ホルモン誘導体(hGH)結晶;
塩緩衝液;
60〜200mMのナトリウムイオン濃度範囲を有するナトリウム塩;および
懸濁化剤
の1種類以上を含むhGH調製物。 - 前記懸濁化剤がポリエチレングリコールである、請求項1に記載のhGH調製物。
- 前記懸濁化剤が2.5〜20%w/vのポリエチレングリコールである、請求項1に記載のhGH調製物。
- 前記hGHまたはhGH誘導体が所定の期間または所定の条件で安定である、請求項1に記載のhGH調製物。
- 前記hGHまたはhGH誘導体が所定の期間安定であり、前記期間が少なくとも6ヶ月である、請求項4に記載の方法。
- 前記hGHまたはhGH誘導体が所定の期間安定であり、前記期間が少なくとも12ヶ月である、請求項4に記載の方法。
- pHがpH6〜7である、請求項1に記載のhGH調製物。
- リン酸緩衝液を含み、pHが6〜7のpHを有する、請求項1に記載のhGH調製物。
- ポリアルギニン複合体型hGH結晶の濃度が5mg/mL〜50mg/mLである、請求項1に記載のhGH調製物。
- 該ポリアルギニン複合体型hGH結晶が約2〜約100μmの粒径分布を有する、請求項1に記載のhGH調製物。
- ポリアルギニンに対するhGHの比が約3〜約15である、請求項1に記載のhGH調製物。
- シリンダー型のシリコーン処理された容器内の上部空間がないか、または10mmまでの上部空間を有する容器内に配置された、請求項1に記載のhGH調製物。
- 前記容器が、テフロン(登録商標)コートされた栓またはゴム配合物4432のいずれかである閉鎖部を含む、請求項12に記載のhGH調製物。
- 反復用量を収容する容器内に配置された、請求項1に記載のhGH調製物。
- 単回用量を収容する容器内に配置された、請求項1に記載のhGH調製物。
- 0.2mL〜1.0mLの充填容積を有する容器内に配置された、請求項1に記載のhGH調製物。
- 送達デバイス内に配置された、請求項1に記載のhGH調製物。
- 29ゲージ以下の針を有するシリンジ内に配置された、請求項1に記載のhGH調製物。
- ニードルフリー注射器内に配置された、請求項1に記載のhGH調製物。
- 前記hGHが5〜100mg/mlで存在する、請求項1に記載のhGH調製物。
- さらに抗菌剤を含む、請求項1に記載のhGH調製物。
- さらにヒアルロン酸を含む、請求項1に記載の調製物。
- 前記調製物が懸濁剤以外のポリマーを含まない、請求項1に記載のhGH調製物。
- 前記調製物がヒスチジン緩衝液を含まない、請求項1に記載のhGH調製物。
- さらに保存料を含む、請求項1に記載のhGH調製物。
- 前記保存料がフェノールである、請求項25に記載のhGH調製物。
- 5〜50mg/mlのポリアルギニン複合体型組換えヒト成長ホルモンまたはヒト成長ホルモン誘導体(hGH)結晶;
6.1〜6.8のpHのリン酸緩衝液;
60〜200mMの塩化ナトリウムまたは酢酸ナトリウム;
2.5〜20%のポリエチレングリコール
を含み;
10mm以下の上部空間を有するシリコーン処理されたプレフィルドシリンジ内に;
0.2〜1.0mlの容量で、
配置されたhGH調製物。 - 前記シリンジが29ゲージ以下の針を有する、請求項27に記載のhGH調製物。
- ニードルフリー注射器内に配置された、請求項27に記載のhGH調製物。
- 高分子電解質でコートされたhGH結晶の懸濁液であって、該結晶性hGHの濃度が5〜100mg/mLである懸濁液;
前記複合体の結晶化度を、好ましくはpH範囲5.0〜8.0に維持する生物学的に適合性の緩衝液;
前記複合体の結晶化度を維持または増大させる結晶化度促進剤;および
前記組成物の総重量オスモル濃度が250〜450mOsm/kgの範囲内となるようにする張度調整剤
の1種類以上を含むhGH調製物。 - さらに保存料を含む、請求項30に記載のhGH調製物。
- 前記保存料がフェノールである、請求項30に記載のhGH調製物。
- 前記フェノールが0.2〜0.3%w/vの濃度である、請求項32に記載のhGH調製物。
- さらに化学的安定剤を含む、請求項30に記載のhGH調製物。
- 前記生物学的に適合性の緩衝液が1〜150mMの範囲の緩衝塩濃度を有する、請求項30に記載のhGH調製物。
- 前記緩衝塩が、酢酸塩、トリエタノールアミン、イミダゾール、リン酸塩、クエン酸塩およびTris−HClからなる群より選択される、請求項35に記載のhGH調製物。
- 前記生物学的に適合性の緩衝液がリン酸ナトリウムである、請求項30に記載のhGH調製物。
- 前記生物学的に適合性の緩衝液がリン酸ナトリウム緩衝液とクエン酸ナトリウム緩衝液を含む、請求項30に記載のhGH調製物。
- 前記複合体の結晶化度を維持または増大させる前記結晶化度促進剤が酢酸ナトリウムまたはポリエチレングリコールを含む、請求項30に記載のhGH調製物。
- 前記複合体の結晶化度を維持または増大させる前記結晶化度促進剤が1〜25w/v%のPEGを含む、請求項30に記載のhGH調製物。
- 前記複合体の結晶化度を維持または増大させる結晶化度促進剤がフェノールを含む、請求項30に記載のhGH調製物。
- 前記張度調整剤が、中性塩、塩化ナトリウム、酢酸ナトリウム、Tris−HCL、その作用緩衝pH範囲外の緩衝塩、その緩衝pH範囲外のpH範囲内のアミノ酸の塩、グリシンナトリウム塩、ポリオール、およびポリエチレングリコールからなる群より選択される、請求項30に記載のhGH調製物。
- 反復用量を収容する容器内に配置された、請求項30に記載のhGH調製物。
- 単回用量を収容する容器内に配置された、請求項30に記載のhGH調製物。
- 前記容器が、テフロン(登録商標)コートされた栓またはゴム配合物4432のいずれかである閉鎖部を含む、請求項44に記載のhGH調製物。
- 0.2mL〜1.0mLの充填容積を有する容器内に配置された、請求項30に記載のhGH調製物。
- 送達デバイス内に配置された、請求項30に記載のhGH調製物。
- ニードルフリー注射器内に配置された、請求項30に記載のhGH調製物。
- さらにヒアルロン酸を含む、請求項30に記載の調製物。
- 請求項1に記載の調製物の成分を合わせることを含む、hGH調製物の作製方法。
- 請求項30に記載の調製物の成分を合わせることを含む、hGH調製物の作製方法。
- 請求項1または請求項30の調製物の成分を容器内に0.2〜1.0mlの充填容積まで配置することを含み、前記容器がシリンジである、hGH調製物のパッケージング方法。
- 請求項1または請求項30の調製物の成分を容器内に0.2〜1.0mlの反復用量を収容する充填容積まで配置することを含む、hGH調製物のパッケージング方法。
- 請求項1または請求項30のhGH調製物を提供すること、および該調製物を患者に投与することを含む、hGH調製物を患者に送達する方法。
- 関係者に、 請求項1または請求項30の調製物の成分を含むhGH調製物が所定の期間または所定の条件で安定であることを指示することを含む、hGH調製物またはhGH調製物に関する情報を関係者に提供する方法。
- 該調製物が所定の期間安定であり、前記期間が少なくとも6ヶ月である、請求項55に記載の方法。
- 該調製物が所定の期間安定であり、前記期間が少なくとも12ヶ月である、請求項55に記載の方法。
- 該調製物が所定の条件で安定であり、前記条件が温度である、請求項55に記載の方法。
- 該調製物が所定の条件で安定であり、前記条件が室温である、請求項55に記載の方法。
- hGH調製物が所定の期間または所定の条件で安定であることのエビデンスを提供すること、または安定であると明示することを含む、標準を満たす方法。
- 該調製物が所定の期間安定であり、前記期間が少なくとも6ヶ月である、請求項60に記載の方法。
- 該調製物が所定の期間安定であり、前記期間が少なくとも12ヶ月である、請求項60に記載の方法。
- 該調製物が所定の条件で安定であり、前記条件が温度である、請求項60に記載の方法。
- 該調製物が所定の条件で安定であり、前記条件が室温である、請求項60に記載の方法。
- 内部に結晶化タンパク質の調製物が配置されたニードルフリー注射器。
- 前記調製物が結晶の溶液である、請求項65に記載のニードルフリー注射器。
- 前記結晶は架橋されたものである、請求項65に記載のニードルフリー注射器。
- 前記結晶が高分子電解質との複合体型である、請求項65に記載のニードルフリー注射器。
- 前記調製物がhGHまたはhGH誘導体のものである、請求項65に記載のニードルフリー注射器。
- 前記調製物が、請求項1または請求項30のhGHまたはhGH誘導体調製物である、請求項65に記載のニードルフリー注射器。
- 前記調製物がワクチンではない、請求項65に記載のニードルフリー注射器。
- 前記調製物中の結晶が、注射器の送達オリフィスの直径の0.5以下の平均最大寸法を有する、請求項65に記載のニードルフリー注射器。
- 前記調製物が、さらにヒアルロン酸を含む、請求項65に記載のニードルフリー注射器。
- 前記調製物中のタンパク質の濃度が約100mg/ml未満である、請求項65に記載のニードルフリー注射器。
- 結晶化タンパク質調製物をニードルフリー注射器内に配置して供給すること、および前記薬物を前記被検体に注射することを含む、結晶化タンパク質調製物を被検体に送達する方法。
- 前記調製物が結晶の溶液である、請求項75に記載の方法。
- 前記結晶は架橋されたものである、請求項75に記載の方法。
- 前記結晶が高分子電解質との複合体型である、請求項75に記載の方法。
- 前記調製物がhGHまたはhGH誘導体のものである、請求項75に記載の方法。
- 前記調製物が、請求項1または請求項30のhGHまたはhGH誘導体調製物である、請求項75に記載の方法。
- 前記調製物がワクチンではない、請求項75に記載の方法。
- 前記調製物中の結晶が、注射器の送達オリフィスの直径の0.5以下の平均最大寸法を有する、請求項75に記載の方法。
- 前記調製物が、さらにヒアルロン酸を含む、請求項75に記載の方法。
- 前記調製物中のタンパク質の濃度が約100mg/ml未満である、請求項75に記載の方法。
- 再懸濁させると、
hGHまたはhGH誘導体結晶の懸濁液、
緩衝液、
塩および
ポリエチレングリコール
を含む懸濁液をもたらすhGHまたはhGH誘導体の凍結乾燥調製物。 - 該結晶の懸濁液が約20〜約50mg/mlの量で存在する、請求項85に記載の調製物。
- 緩衝液がTrisを含む、請求項85に記載の調製物。
- 緩衝液がリン酸塩を含む、請求項87に記載の調製物。
- 緩衝液が、さらにTrisまたはヒスチジンを含む、請求項88に記載の調製物。
- 該懸濁液のpHが約7〜約9である、請求項85に記載の調製物。
- 前記塩が塩化ナトリウムまたは酢酸ナトリウムを含む、請求項85に記載の調製物。
- 前記塩が約50mM〜約100mMの量で存在する、請求項91に記載の調製物。
- 前記ポリエチレングリコールが、ポリエチレングリコール3350、6000または8000を含む、請求項85に記載の調製物。
- 前記ポリエチレングリコールが約2.5%〜約10%の量で存在する、請求項93に記載の調製物。
- 該懸濁液が、
約20〜約50mg/mLのhGH結晶の懸濁液;
Trisまたはリン酸塩とTrisもしくはヒスチジンいずれかとの併用緩衝液;
約7〜約9のpH;
約50mM〜約100mMの量の塩化ナトリウムまたは酢酸ナトリウム;および
約2.5%〜約10%の量のポリエチレングリコール3350、6000または8000
を含む、請求項85に記載の調製物。 - さらに保存料を含む、請求項85に記載の調製物。
- 前記保存料がフェノール、m−クレゾール、クロロブタノール、またはベンジルアルコールである、請求項96に記載の調製物。
- 該懸濁液が、シリコーン処理されたバイアルまたは表面コートされた容器閉鎖部内に配置される、請求項85に記載の調製物。
- 約−30℃〜約10℃の一次乾燥サイクル
を含む、凍結乾燥された結晶性hGHの作製方法。 - さらに、約20℃〜約40℃の二次乾燥サイクルを含む、請求項99に記載の方法。
- 請求項99に記載の方法によってもたらされる生産物。
- 25mg/mLのポリArg複合体型hGH結晶、25mMのTris、100mMの酢酸Na、5%のPEG6000、pH7.5
を含むhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのTris、100mMの酢酸Na、5%のPEG6000、pH7.5
からなるhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのTris、0.2%のHA、100mMの酢酸Na、5%のPEG6000、pH7.5
を含むhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのTris、0.2%のHA、100mMの酢酸Na、5%のPEG6000、pH7.5
からなるhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、5%のPEG6000、pH7.0
を含むhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、5%のPEG6000、pH7.0
からなるhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、5%のPEG6000、pH7.5
を含むhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、5%のPEG6000、pH7.5
からなるhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、5%のPEG8000、pH7.5
を含むhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、5%のPEG8000、pH7.5
からなるhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、5%のPEG3350、pH7.5
を含むhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、5%のPEG3350、pH7.5
からなるhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、100mMのNaCl、5%のPEG6000、pH7.5
を含むhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、100mMのNaCl、5%のPEG6000、pH7.5
からなるhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、100mMのNaCl、5%のPEG8000、pH7.5
を含むhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、100mMのNaCl、5%のPEG8000、pH7.5
からなるhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、100mMのNaCl、5%のPEG3350、pH7.5
を含むhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、100mMのNaCl、5%のPEG3350、pH7.5
からなるhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのヒスチジン、100mMのNaCl、5%のPEG6000、pH7.0
を含むhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのヒスチジン、100mMのNaCl、5%のPEG6000、pH7.0
からなるhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、1%のスクロース、5%のPEG6000、pH7.5
を含むhGHの凍結乾燥調製物。 - 25mg/mLのポリArg複合体型hGH結晶、25mMのtris、1%のスクロース、5%のPEG6000、pH7.5
からなるhGHの凍結乾燥調製物。 - 再懸濁させた請求項85に記載の凍結乾燥物。
- 請求項85または124に記載のhGH調製物を提供すること、および
患者に投与すること
を含む、hGH調製物を患者に送達する方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US87060506P | 2006-12-18 | 2006-12-18 | |
| PCT/US2007/087417 WO2008076819A2 (en) | 2006-12-18 | 2007-12-13 | Human growth hormone formulations |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015153650A Division JP6106722B2 (ja) | 2006-12-18 | 2015-08-03 | ヒト成長ホルモン製剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010513309A true JP2010513309A (ja) | 2010-04-30 |
| JP2010513309A5 JP2010513309A5 (ja) | 2011-01-27 |
Family
ID=39402753
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009541592A Pending JP2010513309A (ja) | 2006-12-18 | 2007-12-13 | ヒト成長ホルモン製剤 |
| JP2015153650A Expired - Fee Related JP6106722B2 (ja) | 2006-12-18 | 2015-08-03 | ヒト成長ホルモン製剤 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015153650A Expired - Fee Related JP6106722B2 (ja) | 2006-12-18 | 2015-08-03 | ヒト成長ホルモン製剤 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US8071544B2 (ja) |
| EP (2) | EP2486916B1 (ja) |
| JP (2) | JP2010513309A (ja) |
| AU (1) | AU2007333959A1 (ja) |
| CA (1) | CA2672284C (ja) |
| DK (1) | DK2486916T3 (ja) |
| WO (1) | WO2008076819A2 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012511009A (ja) * | 2008-12-05 | 2012-05-17 | アルコン リサーチ, リミテッド | 薬学的懸濁物 |
| JP2014508174A (ja) * | 2011-03-15 | 2014-04-03 | バイオジェン・アイデック・インコーポレイテッド | 速い用量調節の漸増投与レジメンを用いた、インターフェロンの筋肉内投与に伴うインフルエンザ様症状を軽減するための方法 |
| JPWO2015064591A1 (ja) * | 2013-10-28 | 2017-03-09 | テルモ株式会社 | タンパク質水性懸濁剤 |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20190085187A (ko) | 2008-01-22 | 2019-07-17 | 아라임 파마슈티칼즈, 인크. | 조직 손상 관련 질환 및 장애를 예방 및 치료하기 위한 조직 보호 펩티드 및 펩티드 유사체 |
| US8912236B2 (en) | 2009-03-03 | 2014-12-16 | Alcon Research, Ltd. | Pharmaceutical composition for delivery of receptor tyrosine kinase inhibiting (RTKi) compounds to the eye |
| CN102361632A (zh) * | 2009-03-30 | 2012-02-22 | 弗·哈夫曼-拉罗切有限公司 | 避免玻璃雾化的方法 |
| US20120183531A1 (en) * | 2009-07-14 | 2012-07-19 | Biogen Idee Ma Inc | Methods for Inhibiting Yellow Color Formation in a Composition |
| US20110059079A1 (en) * | 2009-09-04 | 2011-03-10 | Xoma Technology Ltd. | Antibody Coformulations |
| FR2966044B1 (fr) | 2010-10-18 | 2012-11-02 | Sanofi Pasteur | Procede de conditionnement d'un vaccin contenant un adjuvant d'aluminium |
| WO2013014196A1 (en) | 2011-07-25 | 2013-01-31 | Sandoz Ag | Aqueous formulation comprising at least a neutral salt and a biopharmaceutical protein |
| US20140294977A1 (en) * | 2011-11-23 | 2014-10-02 | Durect Corporation | Radiation-Sterilized Biodegradable Drug Delivery Composition |
| EP2949336B1 (en) | 2013-01-28 | 2018-09-05 | National University Corporation Kumamoto University | Stabilized protein gel preparation |
| EP3079668A1 (en) | 2013-12-09 | 2016-10-19 | Durect Corporation | Pharmaceutically active agent complexes, polymer complexes, and compositions and methods involving the same |
| CN113425835B (zh) * | 2020-03-23 | 2024-03-19 | 常州健益生物制药有限公司 | 一种生长激素原料药溶液、水针剂及其制备方法 |
| CN112494638B (zh) * | 2020-12-22 | 2023-12-19 | 深圳科兴药业有限公司 | 一种人生长激素注射剂组合物及其制备方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1992000998A1 (en) * | 1990-07-13 | 1992-01-23 | Novo Nordisk A/S | Growth hormone crystals and a process for production of these gh-crystals |
| WO1993012812A1 (en) * | 1991-12-20 | 1993-07-08 | Novo Nordisk A/S | A stabilized pharmaceutical formulation comprising growth hormone and histidine |
| JP2006512416A (ja) * | 2002-12-31 | 2006-04-13 | アルタス ファーマシューティカルズ インコーポレイテッド | ヒト成長ホルモンの結晶およびその調製方法 |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4342832A (en) | 1979-07-05 | 1982-08-03 | Genentech, Inc. | Method of constructing a replicable cloning vehicle having quasi-synthetic genes |
| US5618697A (en) | 1982-12-10 | 1997-04-08 | Novo Nordisk A/S | Process for preparing a desired protein |
| NL9000634A (nl) * | 1990-03-20 | 1991-10-16 | Catharina Ziekenhuis Stichting | Suspensie-injectiepreparaat op waterbasis, werkwijze voor de bereiding daarvan en toepassing van dit preparaat voor pijnbestrijding. |
| IL106524A (en) * | 1992-07-31 | 2000-08-31 | Genentech Inc | Human growth hormone aqueous formulation |
| WO1994019020A1 (en) * | 1993-02-23 | 1994-09-01 | Genentech, Inc. | Excipient stabilization of polypeptides treated with organic solvents |
| US5439643A (en) * | 1993-11-03 | 1995-08-08 | Liebert; Richard T. | Method and apparatus for terminal sterilization |
| DE69420872T2 (de) * | 1994-06-17 | 2000-01-13 | Applied Research Systems | Hgh enthaltende pharmazeutische zubereitungen |
| US7276251B2 (en) * | 1997-04-01 | 2007-10-02 | Lg Life Sciences, Ltd., Inc. | Sustained-release composition of drugs encapsulated in microparticles of hyaluronic acid |
| US20020077461A1 (en) * | 1996-04-24 | 2002-06-20 | Soren Bjorn | Pharmaceutical formulation |
| US6541606B2 (en) * | 1997-12-31 | 2003-04-01 | Altus Biologics Inc. | Stabilized protein crystals formulations containing them and methods of making them |
| US7582311B1 (en) * | 1999-10-15 | 2009-09-01 | Genentech, Inc. | Injection vehicle for polymer-based formulations |
| US6699504B2 (en) * | 2000-01-28 | 2004-03-02 | Pelias Technologies, Inc. | Slow release protein polymers |
| NZ571243A (en) | 2002-12-31 | 2010-04-30 | Altus Pharmaceuticals Inc | Complexes of protein crystals and ionic polymers comprising human growth hormone and protamine |
| AU2006330833A1 (en) * | 2005-12-23 | 2007-07-05 | Altus Pharmaceuticals Inc. | Compositions comprising polycation-complexed protein crystals and methods of treatment using them |
-
2007
- 2007-12-13 DK DK11010051.8T patent/DK2486916T3/en active
- 2007-12-13 AU AU2007333959A patent/AU2007333959A1/en not_active Abandoned
- 2007-12-13 EP EP11010051.8A patent/EP2486916B1/en not_active Not-in-force
- 2007-12-13 US US12/519,720 patent/US8071544B2/en not_active Expired - Fee Related
- 2007-12-13 WO PCT/US2007/087417 patent/WO2008076819A2/en active Application Filing
- 2007-12-13 JP JP2009541592A patent/JP2010513309A/ja active Pending
- 2007-12-13 EP EP07869230A patent/EP2120869A2/en not_active Withdrawn
- 2007-12-13 CA CA2672284A patent/CA2672284C/en not_active Expired - Fee Related
-
2011
- 2011-10-10 US US13/270,136 patent/US20120088724A1/en not_active Abandoned
-
2015
- 2015-08-03 JP JP2015153650A patent/JP6106722B2/ja not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1992000998A1 (en) * | 1990-07-13 | 1992-01-23 | Novo Nordisk A/S | Growth hormone crystals and a process for production of these gh-crystals |
| WO1993012812A1 (en) * | 1991-12-20 | 1993-07-08 | Novo Nordisk A/S | A stabilized pharmaceutical formulation comprising growth hormone and histidine |
| JP2006512416A (ja) * | 2002-12-31 | 2006-04-13 | アルタス ファーマシューティカルズ インコーポレイテッド | ヒト成長ホルモンの結晶およびその調製方法 |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012511009A (ja) * | 2008-12-05 | 2012-05-17 | アルコン リサーチ, リミテッド | 薬学的懸濁物 |
| JP2014508174A (ja) * | 2011-03-15 | 2014-04-03 | バイオジェン・アイデック・インコーポレイテッド | 速い用量調節の漸増投与レジメンを用いた、インターフェロンの筋肉内投与に伴うインフルエンザ様症状を軽減するための方法 |
| JP2018030847A (ja) * | 2011-03-15 | 2018-03-01 | バイオジェン・エムエイ・インコーポレイテッドBiogen MA Inc. | 速い用量調節の漸増投与レジメンを用いた、インターフェロンの筋肉内投与に伴うインフルエンザ様症状を軽減するための方法 |
| US10500254B2 (en) | 2011-03-15 | 2019-12-10 | Biogen Ma Inc. | Method for reducing flu-like symptoms associated with intramuscular administration of interferon using a fast titration escalating dosing regimen |
| JPWO2015064591A1 (ja) * | 2013-10-28 | 2017-03-09 | テルモ株式会社 | タンパク質水性懸濁剤 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2672284C (en) | 2014-08-26 |
| WO2008076819A2 (en) | 2008-06-26 |
| JP2015214573A (ja) | 2015-12-03 |
| AU2007333959A1 (en) | 2008-06-26 |
| EP2120869A2 (en) | 2009-11-25 |
| US20120088724A1 (en) | 2012-04-12 |
| CA2672284A1 (en) | 2008-06-26 |
| US8071544B2 (en) | 2011-12-06 |
| EP2486916A1 (en) | 2012-08-15 |
| EP2486916A8 (en) | 2013-03-27 |
| EP2486916B1 (en) | 2015-04-01 |
| US20100216705A1 (en) | 2010-08-26 |
| DK2486916T3 (en) | 2015-06-15 |
| JP6106722B2 (ja) | 2017-04-05 |
| WO2008076819A3 (en) | 2009-03-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6106722B2 (ja) | ヒト成長ホルモン製剤 | |
| CN1273187C (zh) | 稳定性提高的无锌或低锌胰岛素制剂 | |
| JP6522711B2 (ja) | Fshの安定化 | |
| JP5941496B2 (ja) | 成長ホルモン製剤 | |
| RU2357750C2 (ru) | Кристаллы человеческого гормона роста и способы их получения | |
| WO2008098212A2 (en) | Extended release formulations of glucagon and other peptides and proteins | |
| WO2002067989A1 (en) | Crystallisation-resistant aqueous growth hormone formulations | |
| Maggio | Use of excipients to control aggregation in peptide and protein formulations | |
| WO2005014034A1 (en) | Stabilized formulation of parathyroid hormone | |
| US20090023629A1 (en) | Compositions comprising polycation-complexed protein crystals and methods of treatment using them | |
| CN101659701B (zh) | 人生长激素晶体和制备它们的方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101126 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20101126 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111114 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120926 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20121225 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130107 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130125 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130201 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130225 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131016 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140115 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140122 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140212 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20140212 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20140212 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20141119 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20141119 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20150123 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20150403 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20150603 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150609 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20150603 |