KR20150115881A - Hiv 성숙 억제 활성을 갖는 c-19 변형된 트리테르페노이드 - Google Patents
Hiv 성숙 억제 활성을 갖는 c-19 변형된 트리테르페노이드 Download PDFInfo
- Publication number
- KR20150115881A KR20150115881A KR1020157023907A KR20157023907A KR20150115881A KR 20150115881 A KR20150115881 A KR 20150115881A KR 1020157023907 A KR1020157023907 A KR 1020157023907A KR 20157023907 A KR20157023907 A KR 20157023907A KR 20150115881 A KR20150115881 A KR 20150115881A
- Authority
- KR
- South Korea
- Prior art keywords
- alkyl
- mmol
- group
- pentamethyl
- substituted
- Prior art date
Links
- 0 CC(C)([C@@]1CC2)C(**)=CC[C@]1(C)[C@@](CC1)[C@]2(C)[C@](C)(CC2)[C@]1[C@@](C1(CC1)CC1)[C@@]21C(*)=O Chemical compound CC(C)([C@@]1CC2)C(**)=CC[C@]1(C)[C@@](CC1)[C@]2(C)[C@](C)(CC2)[C@]1[C@@](C1(CC1)CC1)[C@@]21C(*)=O 0.000 description 7
- NICIHZYGEQHDPN-UHFFFAOYSA-N NCCN(CC1)CCS1(=O)=O Chemical compound NCCN(CC1)CCS1(=O)=O NICIHZYGEQHDPN-UHFFFAOYSA-N 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N C1NCCOC1 Chemical compound C1NCCOC1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 1
- LZJAGQDVCQGYHN-KWRQCDRVSA-N C=C/C=C(/N=N)\O Chemical compound C=C/C=C(/N=N)\O LZJAGQDVCQGYHN-KWRQCDRVSA-N 0.000 description 1
- LVPOLVGXWHPBGK-ZYUAVXSTSA-N CC(C)(C)OC(N[C@@](CC[C@H]1C(CO)=C)(CC2)[C@H]1[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@]1(C)[C@@H]2C(C)(C)C(c(cc2)cc(F)c2C(O)=O)=CC1)=O Chemical compound CC(C)(C)OC(N[C@@](CC[C@H]1C(CO)=C)(CC2)[C@H]1[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@]1(C)[C@@H]2C(C)(C)C(c(cc2)cc(F)c2C(O)=O)=CC1)=O LVPOLVGXWHPBGK-ZYUAVXSTSA-N 0.000 description 1
- KLIWIBVFVIHXCA-GXZXMBCKSA-N CC(C)(C)OC(N[C@@](CC[C@H]1C2(C)OC2)(CC2)[C@H]1[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@]1(C)[C@@H]2C(C)(C)C(c(cc2)cc(F)c2C(OC)=O)=CC1)=O Chemical compound CC(C)(C)OC(N[C@@](CC[C@H]1C2(C)OC2)(CC2)[C@H]1[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@]1(C)[C@@H]2C(C)(C)C(c(cc2)cc(F)c2C(OC)=O)=CC1)=O KLIWIBVFVIHXCA-GXZXMBCKSA-N 0.000 description 1
- KRZINFAVQOBLON-VSSLKDAESA-N CC(C)(C)OC(c(cc1)ccc1C(C(C)(C)[C@@H]1CC2)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(CNC)=C)[C@@]21C(O)=O)=O Chemical compound CC(C)(C)OC(c(cc1)ccc1C(C(C)(C)[C@@H]1CC2)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(CNC)=C)[C@@]21C(O)=O)=O KRZINFAVQOBLON-VSSLKDAESA-N 0.000 description 1
- HVHZEKKZMFRULH-UHFFFAOYSA-N CC(C)(C)c1nc(C(C)(C)C)cc(C)c1 Chemical compound CC(C)(C)c1nc(C(C)(C)C)cc(C)c1 HVHZEKKZMFRULH-UHFFFAOYSA-N 0.000 description 1
- GNNMVHCMBNFUJP-PCTVEBQMSA-N CC(C)(C1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)C(CC1)[C@]2(C)[C@](C)(CC2)[C@H]1C(CCC1)[C@@]21NCCN(CC1)CCS1(=O)=O Chemical compound CC(C)(C1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)C(CC1)[C@]2(C)[C@](C)(CC2)[C@H]1C(CCC1)[C@@]21NCCN(CC1)CCS1(=O)=O GNNMVHCMBNFUJP-PCTVEBQMSA-N 0.000 description 1
- JVQBAVCNMSUQNH-ZCGYYAQBSA-N CC(C)(C1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)C(CC1)[C@]2(C)[C@](C)(CC2)[C@H]1C1[IH]CC[C@]21NCCN(CC1)CCS1(=O)=O Chemical compound CC(C)(C1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)C(CC1)[C@]2(C)[C@](C)(CC2)[C@H]1C1[IH]CC[C@]21NCCN(CC1)CCS1(=O)=O JVQBAVCNMSUQNH-ZCGYYAQBSA-N 0.000 description 1
- NVCQZQJHKMJEER-CCSYMGPDSA-N CC(C)([C@@H]1CC2)C(c(cc3)cc(F)c3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(CO)=C)[C@@]21N Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)cc(F)c3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(CO)=C)[C@@]21N NVCQZQJHKMJEER-CCSYMGPDSA-N 0.000 description 1
- ZTUOUKBKQDCATR-CTSUHPALSA-N CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H](C(CC1)NC(c3ccc(C4(C(F)(F)F)N=N4)cc3)=O)[C@@]21NCCN(CC1)CCS1(=O)=O Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H](C(CC1)NC(c3ccc(C4(C(F)(F)F)N=N4)cc3)=O)[C@@]21NCCN(CC1)CCS1(=O)=O ZTUOUKBKQDCATR-CTSUHPALSA-N 0.000 description 1
- IDBJONSAWSZKTR-PQBBHEMQSA-N CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(CN(C)C)=C)[C@@]21C(NCCN(C)C)=O Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(CN(C)C)=C)[C@@]21C(NCCN(C)C)=O IDBJONSAWSZKTR-PQBBHEMQSA-N 0.000 description 1
- JEWLKFOMDBJPHI-PIHDDTHSSA-N CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(CN(C)CCN(C)C)=C)[C@@]21C(NCCN(C)C)=O Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(CN(C)CCN(C)C)=C)[C@@]21C(NCCN(C)C)=O JEWLKFOMDBJPHI-PIHDDTHSSA-N 0.000 description 1
- DAAHTUVWCHRHGT-IVTMKUIASA-N CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(CNCCN(C)C)=C)[C@@]21C(NCCC(O)=O)=O Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(CNCCN(C)C)=C)[C@@]21C(NCCC(O)=O)=O DAAHTUVWCHRHGT-IVTMKUIASA-N 0.000 description 1
- AZIRGVYKTUMEJU-SPNMLRJJSA-N CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC[C@@](CC2)([C@@H]3[C@@H]2C(NC)=O)NCCN(CC2)CCS2(=O)=O)[C@]13N Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(O)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC[C@@](CC2)([C@@H]3[C@@H]2C(NC)=O)NCCN(CC2)CCS2(=O)=O)[C@]13N AZIRGVYKTUMEJU-SPNMLRJJSA-N 0.000 description 1
- LAETYLPBBQNMHC-PVXWTIBUSA-N CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)C2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(O)=O)C21NCCN(CC1)CCS1(=O)=O Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)C2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(O)=O)C21NCCN(CC1)CCS1(=O)=O LAETYLPBBQNMHC-PVXWTIBUSA-N 0.000 description 1
- QDILYWBUTPXRCC-LMEOTBJMSA-N CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)C1[C@@H]([C@H](COCNC)CC1)[C@@]21NCCN(CC1)CCS1(=O)=O Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)C1[C@@H]([C@H](COCNC)CC1)[C@@]21NCCN(CC1)CCS1(=O)=O QDILYWBUTPXRCC-LMEOTBJMSA-N 0.000 description 1
- QSMYCGZKJDUPEJ-ZTESCHFWSA-N CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(C)=O)[C@@]21NCCN(CC1)CCS1(=O)=O Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(C)=O)[C@@]21NCCN(CC1)CCS1(=O)=O QSMYCGZKJDUPEJ-ZTESCHFWSA-N 0.000 description 1
- PDPMVNIDYNWYLT-GURKVXKLSA-N CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)NC(NC)=O)[C@@]21NCCN(CC1)CCS1(=O)=O Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)NC(NC)=O)[C@@]21NCCN(CC1)CCS1(=O)=O PDPMVNIDYNWYLT-GURKVXKLSA-N 0.000 description 1
- XZWHVWJLYQOPCD-GURKVXKLSA-N CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)NC(OC)=O)[C@@]21NCCN(CC1)CCS1(=O)=O Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)NC(OC)=O)[C@@]21NCCN(CC1)CCS1(=O)=O XZWHVWJLYQOPCD-GURKVXKLSA-N 0.000 description 1
- PDOCHRGNTWZUGP-FBTRDPLWSA-N CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)NC(c3ccc(C4(C(F)(F)F)N=N4)cc3)=O)[C@@]21NCCN(CC1)CCS1(=O)=O Chemical compound CC(C)([C@@H]1CC2)C(c(cc3)ccc3C(OC)=O)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)NC(c3ccc(C4(C(F)(F)F)N=N4)cc3)=O)[C@@]21NCCN(CC1)CCS1(=O)=O PDOCHRGNTWZUGP-FBTRDPLWSA-N 0.000 description 1
- HAXFWDWDVVVAEU-GYLRQWMPSA-N CC(C1)([C@H](CC2)[C@H]([C@@H](CC3)[C@@](C)(CC4)[C@](C)(CC5)[C@H]3[C@]3(C)[C@@H]5C(C)(C)C(c(cc5)ccc5C(OC)=O)=CC3)[C@]24C(OCc2ccccc2)=O)C1(Br)Br Chemical compound CC(C1)([C@H](CC2)[C@H]([C@@H](CC3)[C@@](C)(CC4)[C@](C)(CC5)[C@H]3[C@]3(C)[C@@H]5C(C)(C)C(c(cc5)ccc5C(OC)=O)=CC3)[C@]24C(OCc2ccccc2)=O)C1(Br)Br HAXFWDWDVVVAEU-GYLRQWMPSA-N 0.000 description 1
- NGEHAGHBIPWJLL-KHYSSXOOSA-N CC(COC(C)=O)([C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)[C@]13N)O Chemical compound CC(COC(C)=O)([C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)[C@]13N)O NGEHAGHBIPWJLL-KHYSSXOOSA-N 0.000 description 1
- FITCIOSTABKWSJ-VIJPSQODSA-N CC(COC)([C@](C)(CC[C@]1(C)CC2)[C@@H]1[C@@](C)(CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@]1(C)[C@@H]2C(C)(C)C(c(cc2)ccc2C(OC)=O)=CC1)O Chemical compound CC(COC)([C@](C)(CC[C@]1(C)CC2)[C@@H]1[C@@](C)(CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@]1(C)[C@@H]2C(C)(C)C(c(cc2)ccc2C(OC)=O)=CC1)O FITCIOSTABKWSJ-VIJPSQODSA-N 0.000 description 1
- WAMDUJUYVYARFQ-OTVPSICSSA-N CC([C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(O)=O)=CC2)[C@]13NCCN(CC1)CCS1(=O)=O)N(C)C Chemical compound CC([C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(O)=O)=CC2)[C@]13NCCN(CC1)CCS1(=O)=O)N(C)C WAMDUJUYVYARFQ-OTVPSICSSA-N 0.000 description 1
- BYXRQVFSJUSUMD-CNKHNCKHSA-N CC([C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)[C@]13NCCN(CC1)CCS1(=O)=O)NC(C)=O Chemical compound CC([C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)[C@]13NCCN(CC1)CCS1(=O)=O)NC(C)=O BYXRQVFSJUSUMD-CNKHNCKHSA-N 0.000 description 1
- KFFBXIJPIJNJHN-MCUNVQSMSA-N CC([C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)[C@]13NCCN(CC1)CCS1(=O)=O)NC(OC)=O Chemical compound CC([C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)[C@]13NCCN(CC1)CCS1(=O)=O)NC(OC)=O KFFBXIJPIJNJHN-MCUNVQSMSA-N 0.000 description 1
- OZXBZJGOQYNLKS-WLSCIQAGSA-N CC([C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)[C@]13NCCN(CC1)CCS1(=O)=O)O Chemical compound CC([C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)[C@]13NCCN(CC1)CCS1(=O)=O)O OZXBZJGOQYNLKS-WLSCIQAGSA-N 0.000 description 1
- VZZKSCFNKPGVNM-CVDRROQNSA-N CC1(CC1)[C@H](CC1)C([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)C13NCCN(CC1)CCS1(=O)=O Chemical compound CC1(CC1)[C@H](CC1)C([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)C13NCCN(CC1)CCS1(=O)=O VZZKSCFNKPGVNM-CVDRROQNSA-N 0.000 description 1
- OJQBJLJDBLBTPG-LKRYTKLXSA-N CC1(CC1)[C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)C2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(O)=O)=CC2)C13NCCN(CC1)CCS1(=O)=O Chemical compound CC1(CC1)[C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)C2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)ccc4C(O)=O)=CC2)C13NCCN(CC1)CCS1(=O)=O OJQBJLJDBLBTPG-LKRYTKLXSA-N 0.000 description 1
- BEWTTWZGPIEIIB-FXVJZSOJSA-N CC1(CC1)[C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)C4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)[C@]13N Chemical compound CC1(CC1)[C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)C4C(C)(C)C(c(cc4)ccc4C(OC)=O)=CC2)[C@]13N BEWTTWZGPIEIIB-FXVJZSOJSA-N 0.000 description 1
- MDPXUMHLXBGVGR-CVWBOJHWSA-N CC1([C@H](CC2)[C@H]([C@@H](CC3)[C@@](C)(CC4)[C@](C)(CC5)[C@H]3[C@]3(C)[C@@H]5C(C)(C)C(c(cc5)cc(F)c5C(O)=O)=CC3)[C@]24NCCN(CC2)CCS2(=O)=O)OC1 Chemical compound CC1([C@H](CC2)[C@H]([C@@H](CC3)[C@@](C)(CC4)[C@](C)(CC5)[C@H]3[C@]3(C)[C@@H]5C(C)(C)C(c(cc5)cc(F)c5C(O)=O)=CC3)[C@]24NCCN(CC2)CCS2(=O)=O)OC1 MDPXUMHLXBGVGR-CVWBOJHWSA-N 0.000 description 1
- BNOSBNIKTGTBRR-ZMCUKCJTSA-N CC1C([C@H](CC2)[C@H]([C@@H](CC3)[C@@](C)(CC4)[C@](C)(CC5)[C@H]3[C@]3(C)[C@@H]5C(C)(C)C(c(cc5)cc(F)c5C(OC)=O)=CC3)[C@]24N)OC1 Chemical compound CC1C([C@H](CC2)[C@H]([C@@H](CC3)[C@@](C)(CC4)[C@](C)(CC5)[C@H]3[C@]3(C)[C@@H]5C(C)(C)C(c(cc5)cc(F)c5C(OC)=O)=CC3)[C@]24N)OC1 BNOSBNIKTGTBRR-ZMCUKCJTSA-N 0.000 description 1
- QXJXWZXXJNRSBI-BOYVBGEHSA-N CCC/C=C(\C(C)(C)[C@H](CC1)C[C@@H](CC2)[C@]1(C)[C@](C)(CC[C@@H]1C(CCC3)NCCN(CC4)CCS4(=O)=O)[C@H]2[C@H]1[C@@H]3C(N1CCOCC1)=O)/c(cc1)ccc1C(O)=O Chemical compound CCC/C=C(\C(C)(C)[C@H](CC1)C[C@@H](CC2)[C@]1(C)[C@](C)(CC[C@@H]1C(CCC3)NCCN(CC4)CCS4(=O)=O)[C@H]2[C@H]1[C@@H]3C(N1CCOCC1)=O)/c(cc1)ccc1C(O)=O QXJXWZXXJNRSBI-BOYVBGEHSA-N 0.000 description 1
- MOKPMRQMILJRDS-SFJBONAQSA-N CCOC(C(CC1)CC=C1C(C(C)(C)[C@@H]1CC2)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(C)(C)O)[C@@]21NCCN1C(C2)COC2C1)=O Chemical compound CCOC(C(CC1)CC=C1C(C(C)(C)[C@@H]1CC2)=CC[C@]1(C)[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@@H]([C@@H](CC1)C(C)(C)O)[C@@]21NCCN1C(C2)COC2C1)=O MOKPMRQMILJRDS-SFJBONAQSA-N 0.000 description 1
- ZGDVFKSOCBPKJN-CNNHIXBDSA-N CCOC(CCNC([C@@](CC[C@H]1C(CN(C)C(CCC(OC)=O)=O)=C)(CC2)[C@H]1[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@]1(C)[C@@H]2C(C)(C)C(c(cc2)ccc2C(O)=O)=CC1)=O)=O Chemical compound CCOC(CCNC([C@@](CC[C@H]1C(CN(C)C(CCC(OC)=O)=O)=C)(CC2)[C@H]1[C@@H](CC1)[C@]2(C)[C@](C)(CC2)[C@H]1[C@]1(C)[C@@H]2C(C)(C)C(c(cc2)ccc2C(O)=O)=CC1)=O)=O ZGDVFKSOCBPKJN-CNNHIXBDSA-N 0.000 description 1
- LIQWOTZFKVPZQW-QODWSZOGSA-N CC[C@H](CC[C@H]([C@H]([C@H](CC1)CCCC2)[C@@H]2C(N2CCOCC2)=O)[C@]1(C)CCC1)[C@]2(C)[C@@H]1C(C)(C)C(c(cc1)ccc1C(OC)=O)=CC2 Chemical compound CC[C@H](CC[C@H]([C@H]([C@H](CC1)CCCC2)[C@@H]2C(N2CCOCC2)=O)[C@]1(C)CCC1)[C@]2(C)[C@@H]1C(C)(C)C(c(cc1)ccc1C(OC)=O)=CC2 LIQWOTZFKVPZQW-QODWSZOGSA-N 0.000 description 1
- GRYGYTHJJDDQPF-ORPINSSNSA-N CC[C@](CC1)([C@H]([C@@H](C)C(C)NC(C(F)(F)F)=O)[C@@H](CC2)[C@]1(C)[C@](C)(CC1)[C@H]2[C@]2(C)[C@@H]1C(C)(C)C(c(cc1)ccc1C(OC)=O)=CC2)NCCN(CC1)CCS1(=O)=O Chemical compound CC[C@](CC1)([C@H]([C@@H](C)C(C)NC(C(F)(F)F)=O)[C@@H](CC2)[C@]1(C)[C@](C)(CC1)[C@H]2[C@]2(C)[C@@H]1C(C)(C)C(c(cc1)ccc1C(OC)=O)=CC2)NCCN(CC1)CCS1(=O)=O GRYGYTHJJDDQPF-ORPINSSNSA-N 0.000 description 1
- ORXZBRUPYUINKK-SJPCBVBISA-N CC[C@](CC1)([C@H]([C@@H](C)C(C)O)[C@@H](CC2)[C@]1(C)[C@](C)(CC1)[C@H]2[C@]2(C)[C@@H]1C(C)(C)C(c(cc1)ccc1C(OC)=O)=CC2)NCCN(CC1)CCS1(=O)=O Chemical compound CC[C@](CC1)([C@H]([C@@H](C)C(C)O)[C@@H](CC2)[C@]1(C)[C@](C)(CC1)[C@H]2[C@]2(C)[C@@H]1C(C)(C)C(c(cc1)ccc1C(OC)=O)=CC2)NCCN(CC1)CCS1(=O)=O ORXZBRUPYUINKK-SJPCBVBISA-N 0.000 description 1
- UNFUCESBTFMGPZ-RCIDGYDTSA-N CC[C@](CC1)([C@H]([C@H](C(C)(COC)O)I)[C@@](C)(CC2)[C@]1(C)[C@](C)(CC1)[C@H]2[C@]2(C)[C@@H]1C(C)(C)C(c(cc1)ccc1C(O)=O)=CC2)NCCN(CC1)CCS1(=O)=O Chemical compound CC[C@](CC1)([C@H]([C@H](C(C)(COC)O)I)[C@@](C)(CC2)[C@]1(C)[C@](C)(CC1)[C@H]2[C@]2(C)[C@@H]1C(C)(C)C(c(cc1)ccc1C(O)=O)=CC2)NCCN(CC1)CCS1(=O)=O UNFUCESBTFMGPZ-RCIDGYDTSA-N 0.000 description 1
- FIUWFUHNMQKYJE-BGYKLINNSA-N CC[C@](CNCCN(CC1)CCS1(=O)=O)(CC[C@](C)([C@@H]1CC2)[C@](C)(CC3)[C@H]2[C@]2(C)[C@@H]3C(C)(C)C(c(cc3)ccc3C(OC)=O)=CC2)[C@@H]1C(C)(C)C(C)(CO)O Chemical compound CC[C@](CNCCN(CC1)CCS1(=O)=O)(CC[C@](C)([C@@H]1CC2)[C@](C)(CC3)[C@H]2[C@]2(C)[C@@H]3C(C)(C)C(c(cc3)ccc3C(OC)=O)=CC2)[C@@H]1C(C)(C)C(C)(CO)O FIUWFUHNMQKYJE-BGYKLINNSA-N 0.000 description 1
- OIRDBPQYVWXNSJ-UHFFFAOYSA-N COS(C(F)(F)F)(=O)=O Chemical compound COS(C(F)(F)F)(=O)=O OIRDBPQYVWXNSJ-UHFFFAOYSA-N 0.000 description 1
- UVYBTWCKLAREPZ-KLULTHIGSA-N C[C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)cc(F)c4C(OC)=O)=CC2)[C@]13NCCN(CC1)CCS1(=O)=O Chemical compound C[C@H](CC1)[C@H]([C@@H](CC2)[C@@](C)(CC3)[C@](C)(CC4)[C@H]2[C@]2(C)[C@@H]4C(C)(C)C(c(cc4)cc(F)c4C(OC)=O)=CC2)[C@]13NCCN(CC1)CCS1(=O)=O UVYBTWCKLAREPZ-KLULTHIGSA-N 0.000 description 1
- AYPYZGQQOPBYLB-UHFFFAOYSA-N O=S1(CCN(CC=[ClH])CC1)=O Chemical compound O=S1(CCN(CC=[ClH])CC1)=O AYPYZGQQOPBYLB-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J63/00—Steroids in which the cyclopenta(a)hydrophenanthrene skeleton has been modified by expansion of only one ring by one or two atoms
- C07J63/008—Expansion of ring D by one atom, e.g. D homo steroids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/58—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Virology (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Tropical Medicine & Parasitology (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- AIDS & HIV (AREA)
- Steroid Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
Description
관련 출원에 대한 상호 참조
본원은 2013년 2월 6일에 출원된 미국 가출원 일련 번호 61/761,403을 우선권 주장하며, 이는 본원에 참조로 포함된다.
발명의 분야
본 발명은 HIV에 대해 유용한 신규 화합물, 및 보다 특히 HIV 성숙 억제제로서 유용한, 베툴린산으로부터 유도된 화합물 및 다른 구조적으로 관련된 화합물, 및 그를 함유하는 제약 조성물, 뿐만 아니라 그의 제조 방법에 관한 것이다.
HIV-1 (인간 면역결핍 바이러스 -1) 감염은 2010년 말에 전세계적으로 4500-5000만명으로 추정되는 사람들을 감염시킨 주요 의료 문제로 남아있다. HIV 및 AIDS (후천성 면역결핍 증후군) 사례의 수는 빠르게 증가하고 있다. 2005년에, 대략 500만건의 새로운 감염이 보고되었고, 310만명의 사람들이 AIDS로 인해 사망하였다. HIV의 치료를 위해 현재 이용가능한 약물은 뉴클레오시드 역전사효소 (RT) 억제제 또는 승인된 단일 환제 조합을 포함한다: 지도부딘 (또는 AZT 또는 레트로비르(RETROVIR)®), 디다노신 (또는 비덱스(VIDEX)®), 스타부딘 (또는 제리트(ZERIT)®), 라미부딘 (또는 3TC 또는 에피비르(EPIVIR)®), 잘시타빈 (또는 DDC 또는 히비드(HIVID)®), 아바카비르 숙시네이트 (또는 지아겐(ZIAGEN)®), 테노포비르 디소프록실 푸마레이트 염 (또는 비리어드(VIREAD)®), 엠트리시타빈 (또는 FTC - 엠트리바(EMTRIVA)®), 콤비비르(COMBIVIR)® (-3TC 플러스 AZT 함유), 트리지비르(TRIZIVIR)® (아바카비르, 라미부딘 및 지도부딘 함유), 엡지콤(EPZICOM)® (아바카비르 및 라미부딘 함유), 트루바다(TRUVADA)® (비리어드® 및 엠트리바® 함유); 비-뉴클레오시드 역전사효소 억제제: 네비라핀 (또는 비라뮨(VIRAMUNE)®), 델라비르딘 (또는 리스크립터(RESCRIPTOR)®) 및 에파비렌즈 (또는 수스티바(SUSTIVA)®), 아트리플라(ATRIPLA)® (트루바다® + 수스티바®), 및 에트라비린, 및 펩티드모방체 프로테아제 억제제 또는 승인된 제제: 사퀴나비르, 인디나비르, 리토나비르, 넬피나비르, 암프레나비르, 로피나비르, 칼레트라(KALETRA)® (로피나비르 및 리토나비르), 다루나비르, 아타자나비르 (레야타즈(REYATAZ)®) 및 티프라나비르 (압티부스(APTIVUS)®) 및 코비시스타트, 및 인테그라제 억제제, 예컨대 랄테그라비르 (이센트레스(ISENTRESS)®), 및 진입 억제제, 예컨대 엔푸비르티드 (T-20) (푸제온(FUZEON)®) 및 마라비록 (셀젠트리(SELZENTRY)®)을 포함한다.
각각의 이들 약물은 단독으로 사용되는 경우에 바이러스 복제를 단지 일시적으로만 저지할 수 있다. 그러나, 조합하여 사용되는 경우에, 이들 약물은 바이러스혈증 및 질환 진행에 대해 엄청난 영향을 미친다. 실제로, AIDS 환자 중에서의 사망률의 유의한 감소가 조합 요법의 광범위한 적용의 결과로서 최근에 기록되었다. 그러나, 이러한 인상적인 결과에도 불구하고, 환자 중 30 내지 50%는 궁극적으로 조합 약물 요법에 실패할 수 있다. 특정 세포 유형 내에서의 불충분한 약물 효력, 비-순응성, 제한된 조직 침투 및 약물-특이적 한계 (예를 들어, 대부분의 뉴클레오시드 유사체는 휴지기 세포에서 인산화될 수 없음)는 감수성 바이러스의 불완전 억제를 설명할 수 있다. 또한, 돌연변이의 빈번한 혼입과 조합된 HIV-1의 높은 복제율 및 신속한 교체는, 준최적 약물 농도가 존재하는 경우에 약물-내성 변이체의 출현 및 치료 실패를 유발한다. 따라서, 뚜렷한 내성 패턴, 및 바람직한 약동학 뿐만 아니라 안전성 프로파일을 나타내는 신규 항-HIV 작용제가 보다 많은 치료 옵션을 제공하기 위해 필요하다. 개선된 HIV 융합 억제제 및 HIV 진입 보조수용체 길항제는 다수의 연구자에 의해 추가로 연구된 새로운 클래스의 항-HIV 작용제 중 2개의 예이다.
HIV 부착 억제제는 HIV 표면 당단백질 gp120에 결합하고, 표면 단백질 gp120과 숙주 세포 수용체 CD4 사이의 상호작용을 방해하는 추가 하위부류의 항바이러스 화합물이다. 따라서, 이들은 HIV 생활 주기의 제1 단계에서 HIV가 인간 CD4 T-세포에 부착되는 것을 방지하고, HIV 복제를 차단한다. HIV 부착 억제제의 특성은 항바이러스제로서의 최대화된 유용성 및 효능을 갖는 화합물을 얻기 위한 노력으로 개선되어 왔다. 특히, US 7,354,924 및 US 7,745,625는 HIV 부착 억제제의 예시이다.
HIV의 치료를 위한 또 다른 신생 부류의 화합물은 HIV 성숙 억제제로 불린다. 성숙은 HIV 복제 또는 HIV 생활 주기의 10개 이상만큼의 많은 단계 중 마지막이고, 여기서 HIV는 궁극적으로 캡시드 (CA) 단백질의 방출을 발생시키는 gag 단백질에서의 여러 HIV 프로테아제-매개 절단 사건의 결과로서 감염성이 된다. 성숙 억제제는 HIV 캡시드가 적절히 조립되고 성숙되는 것, 보호성 외부 코트를 형성하는 것, 또는 인간 세포로부터 출현하는 것을 방지한다. 대신에, 비-감염성 바이러스가 생성되고, HIV 감염의 후속 주기를 방지한다.
베툴린산의 특정 유도체는 현재 HIV 성숙 억제제로서 강력한 항-HIV 활성을 나타내는 것으로 밝혀졌다. 예를 들어, US 7,365,221은 모노아실화 베툴린 및 디히드로베툴린 유도체, 및 항-HIV 작용제로서의 그의 용도를 개시하고 있다. '221 참고문헌에서 논의된 바와 같이, 특정 치환된 아실 기, 예컨대 3',3'-디메틸글루타릴 및 3',3'-디메틸숙시닐 기와의 베툴린산 (1)의 에스테르화로, 증진된 활성을 갖는 유도체를 생성하였다 (Kashiwada, Y., et al., J. Med. Chem. 39:1016-1017 (1996)). 강력한 항-HIV 작용제인 아실화 베툴린산 및 디히드로베툴린산 유도체가 또한 미국 특허 번호 5,679,828에 기재되어 있다. 베툴린의 3 탄소에서의 히드록실의 숙신산과의 에스테르화로, HIV-1 활성을 억제할 수 있는 화합물을 또한 생성하였다 (Pokrovskii, A. G., et al., Khimiya y Interesakh Ustoichivogo Razvitiya, Vol. 9, No. 3, pp. 485-491 (2001)).
HIV 감염을 베툴린산으로부터 유도된 화합물로 치료하는 용도에 대한 다른 참고문헌은 US 2005/0239748 및 US 2008/0207573, 뿐만 아니라 WO2006/053255, WO2009/100532 및 WO2011/007230을 포함한다.
개발 중이었던 1종의 HIV 성숙 화합물은 화학식 C36H56O6 및 IUPAC 명칭 3β-(3-카르복시-3-메틸-부타노일옥시) 루프-20(29)-엔-28-산을 갖는 베비리마트 또는 PA-457로서 확인되었다.
브리스톨-마이어스 스큅(Bristol-Myers Squibb)에 의해 2011년 6월 2일에 출원된 발명의 영문 명칭 "MODIFIED C-3 BETULINIC ACID DERIVATIVES AS HIV MATURATION INHIBITORS"의 USSN 13/151,706 (현재 US 2012-0142707) 및 2011년 6월 2일에 출원된 발명의 영문 명칭 "C-28 AMIDES OF MODIFIED C-3 BETULINIC ACID DERIVATIVES AS HIV MATURATION INHIBITORS"의 USSN 13/151,722 (현재 US 2012-0142653) 출원을 또한 본원에서 참조한다. 2012년 1월 27일에 출원된 발명의 영문 명칭 "C-28 AMINES OF C-3 MODIFIED BETULINIC ACID DERIVATIVES AS HIV MATURATION INHIBITORS"의 USSN 13/359,680 (현재 U.S. 2013-0029954) 출원을 또한 참조한다. 또한, 2012년 1월 27일에 출원된 발명의 영문 명칭 "C-17 AND C-3 MODIFIED TRITERPENOIDS WITH HIV MATURATION INHIBITORY ACTIVITY"의 USSN 13/359,727 (현재 U.S. 2013-0035318) 출원, 및 2013년 3월 13일에 출원된 발명의 영문 명칭 "C-17 BICYCLIC AMINES OF TRITERPENOIDS WITH HIV MATURATION INHIBITORY ACTIVITY"의 USSN 13/799,479 (현재 U.S. 2013-0296554) 출원을 참조한다.
현재 관련 기술분야에 필요한 것은 HIV 성숙 억제제로서 유용한 신규 화합물, 뿐만 아니라 이들 화합물을 함유하는 신규 제약 조성물이다.
본 발명은 하기 화학식 I 및 II의 화합물 (그의 제약상 허용되는 염 포함), 그의 제약 제제, 및 바이러스, 예컨대 HIV에 감염되었거나 또는 이에 감염되기 쉬운 환자에서의 그의 용도를 제공한다. 화학식 I 및 II의 화합물은 특히 HIV의 억제제로서 효과적인 항바이러스제이다. 이들은 HIV 및 AIDS의 치료에 유용하다.
본 발명의 한 실시양태는 하기 화학식 I의 화합물; 및 하기 화학식 II의 화합물의 군으로부터 선택된, 그의 제약상 허용되는 염을 포함하는 화합물에 관한 것이다.
<화학식 I>
<화학식 II>
상기 식에서, X는 페닐, 헤테로아릴 고리, C4-8 시클로알킬, C4-8 시클로알케닐, C4-9 스피로시클로알킬, C4-9 스피로시클로알케닐, C4-8 옥사시클로알킬, C4-8 디옥사시클로알킬, C6-8 옥사시클로알케닐, C6-8 디옥사시클로알케닐, C6 시클로디알케닐, C6 옥사시클로디알케닐, C6-9 옥사스피로시클로알킬 및 C6-9 옥사스피로시클로알케닐 고리의 군으로부터 선택되고;
추가로 여기서 X는 A로 치환되고, 여기서 A는 -H, -할로, -히드록실, -C1-6 알킬, -C1-6 알콕시, -C1-6 알킬-Q1, -알킬치환된 C1-6 알킬-Q1, -CN, -CF2Q1, -NR2R2, -COOR2 및 -CONR2R2의 군으로부터 선택된 적어도 1개의 구성원이고;
여기서 Q1은 아릴, 헤테로아릴, 치환된 헤테로아릴, -OR2, -COOR3, -NR2R2, -SO2R7, -CONHSO2R3, 및 -CONHSO2NR2R2의 군으로부터 선택되고;
Y는 -COOR2, -C(O)NR2SO2R3, -C(O)NHSO2NR2R2, -NR2SO2R2, -SO2NR2R2, -C3-6 시클로알킬-COOR2, -C2-6 알케닐-COOR2, -C2-6 알키닐-COOR2, -C1-6 알킬-COOR2, -알킬치환된 C1-6 알킬, -COOR2, CF2-COOR2, -NHC(O)(CH2)n-COOR2, -SO2NR2C(O)R2, -테트라졸, 및 -CONHOH의 군으로부터 선택되고,
여기서 n=1-6이고;
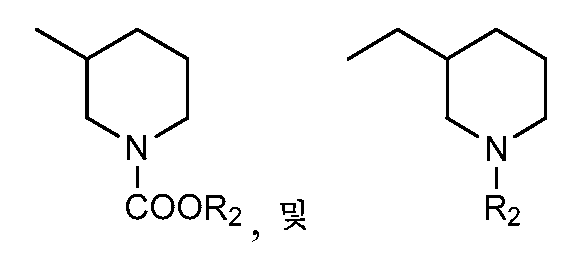
R1은
의 군으로부터 선택되고;
W는 부재하거나, 또는 -CH2 또는 -CO이고;
Z는 -NR28R29, -OR30, -COOR2, -CONR18R19, F, Cl, Br, 및 I의 군으로부터 선택되고;
U는 -NR28R29, -OR30, -COOR2, -CONR18R19, F, Cl, Br, I, 아릴 및 헤테로아릴의 군으로부터 선택되고;
R2는 -H, 벤질, -C1-6 알킬, -알킬치환된 C1-6 알킬 및 -아릴치환된 C1-6 알킬의 군으로부터 선택되고;
R3은 벤질, -C1-6 알킬 또는 -알킬치환된 C1-6 알킬이고;
R4는 -H, -C1-6 알킬, -C1-6 알킬-C(OR3)2-C3-6 시클로알킬, -C1-6 치환된 알킬, -C1-6 알킬-C3-6 시클로알킬, -C1-6 알킬-Q2, -C1-6 알킬-C3-6 시클로알킬-Q2, 아릴, 헤테로아릴, 치환된 헤테로아릴, -COR6, -COCOR6, -SO2R7, -SO2NR2R2,의 군으로부터 선택되고,
여기서 Q2는 헤테로아릴, 치환된 헤테로아릴, F, Cl, Br, I, -CF3, -OR2, -COOR2, -NR8R9, -CONR10R11 및 -SO2R7의 군으로부터 선택되고;
R5는 -H, -C1-6 알킬, -C3-6 시클로알킬, -C1-6 알킬치환된 알킬, -C1-6 알킬-NR8R9, -COR6, -COCOR6, -SO2R7 및 -SO2NR2R2의 군으로부터 선택되며;
단 W가 CO인 경우에 R4 또는 R5는 -COR6 또는 -COCOR6일 수 없고;
추가로 단 R4 또는 R5 중 오직 1개가 -COR6, -COCOR6, -SO2R7 및 -SO2NR2R2의 군으로부터 선택될 수 있거나;
R6은 -C1-6 알킬, -C1-6 알킬-치환된알킬, -C3-6 시클로알킬, -C3-6 치환된시클로알킬-Q3, -C1-6 알킬-Q3, -C1-6 알킬-치환된알킬-Q3, -C3-6 시클로알킬-Q3, 아릴-Q3, -NR13R14, 및 -OR15의 군으로부터 선택되고;
여기서 Q3은 아릴, 헤테로아릴, 치환된 헤테로아릴, -OR2, -COOR2, -NR8R9, SO2R7, -CONHSO2R3, 및 -CONHSO2NR2R2의 군으로부터 선택되고;
R7은 -C1-6 알킬, -C1-6 치환된 알킬, -C3-6 시클로알킬, -CF3, 아릴, 및 헤테로아릴의 군으로부터 선택되고;
R8 및 R9는 독립적으로 -H, -C1-6 알킬, -C1-6 치환된 알킬, 아릴, 헤테로아릴, 치환된 아릴, 치환된 헤테로아릴, 및 -C1-6 알킬-Q2의 군으로부터 선택되고;
R8은 또한 -COOR3일 수 있고;
또는 R8 및 R9는 인접한 N과 함께
의 군으로부터 선택된 사이클을 형성하고;
V는 -CR24R25, -SO2, -O 및 -NR12의 군으로부터 선택되고;
M은 -CHR24R25, -NR26R27, -SO2R7, -SO2NR3R3 및 -OH의 군으로부터 선택되고;
R10 및 R11은 독립적으로 -H, -C1-6 알킬, -C1-6 치환된 알킬 및 -C3-6 시클로알킬의 군으로부터 선택되거나,
R12는 -C1-6 알킬, -C1-6 알킬-OH; -C1-6 알킬, -C1-6 치환된 알킬, -C3-6 시클로알킬, -COR7, -COONR18R19, -SOR7, 및 -SONR20R21의 군으로부터 선택되고;
R13 및 R14는 독립적으로 -H, -C1-6 알킬, -C3-6 시클로알킬, -C1-6 치환된 알킬, -C1-6 알킬-Q4, -C1-6 알킬-C3-6 시클로알킬-Q4, -C1-6 치환된 알킬-Q4 및 의 군으로부터 선택되거나,
또는 R13 및 R14는 인접한 N과 함께
의 군으로부터 선택된 사이클을 형성하고;
R15는 -C1-6 알킬, -C3-6 시클로알킬, -C1-6 치환된 알킬, -C1-6 알킬-Q4, -C1-6 알킬-C3-6 시클로알킬-Q4 및 -C1-6 치환된 알킬-Q4의 군으로부터 선택되고;
Q4는 헤테로아릴, 치환된 헤테로아릴, -NR2R2, -CONR2R2, -COOR2, -OR2, 및 -SO2R3의 군으로부터 선택되고;
R16은 -H, -C1-6 알킬, -NR2R2, 및 -COOR3의 군으로부터 선택되고;
R17은 -H, -C1-6 알킬, -COOR3, 및 아릴의 군으로부터 선택되고;
R18 및 R19는 독립적으로 H, -C1-6 알킬, -C1-6 치환된 알킬, 및 -C1-6 시클로알킬의 군으로부터 선택되고;
R18은 또한 -COOR3일 수 있거나;
R20 및 R21은 독립적으로 H, -C1-6 알킬, -C1-6 치환된 알킬, -C1-6 알킬-Q5, -C1-6 시클로알킬, 아릴, 치환된 아릴, 헤테로아릴, 및 치환된 헤테로아릴의 군으로부터 선택되고,
Q5는 할로겐 및 SO2R3의 군으로부터 선택되고;
R24 및 R25는 독립적으로 -H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -SO2R3, -SO2NR2R2 또는 -OH, -NR2R2, -NR2SO2R3, -NR2COR3 및 -NR2CONR2R2의 군으로부터 선택되며;
단 R24 및 R25 중 오직 1개가 -OH, -NR2R2, -NR2SO2R3, -NR2COR3 및 -NR2CONR2R2의 군으로부터 선택될 수 있고;
R26 및 R27은 독립적으로 -H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -C1-3 알킬아릴, C1- 3알킬헤테로아릴, -CO2R2 및 -SO2R7의 군으로부터 선택되며;
단 R26 및 R27 중 오직 1개가 -CO2R2 또는 -SO2R7의 군으로부터 선택될 수 있고;
R28 및 R29는 독립적으로 -H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -C3-6 시클로알킬, -C1-6 알킬-Q6, -COC1-6 알킬-Q6, -COOR3; -COCF3의 군으로부터 선택되고;
R28은 또한 -COOR3 및 -CONR18R19로부터 선택될 수 있거나;
또는 R28 및 R29는 인접한 N과 함께
의 군으로부터 선택된 사이클을 형성하고;
R30은 H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -C3-6 시클로알킬, 및 -C1-6 알킬-Q6의 군으로부터 선택되고;
여기서 Q6은 H, -OR2, -COOR2, -COCOOR2, 및 -NR31R32의 군으로부터 선택되고;
R31 및 R32는 독립적으로 -H, -C1-6 알킬, -C1-6 치환된 알킬, -C1-6 치환된 알킬-OR2, 및 -COR3의 군으로부터 선택되거나,
R33은 -H, -C1-6 알킬, -C1-6 치환된 알킬, 및 -C1-6 치환된 알킬-Q7의 군으로부터 선택되고,
여기서 Q7은 -COOR2 및 -COONR2R2의 군으로부터 선택된다.
추가 실시양태에서, 바이러스, HIV인 바이러스에 감염된 포유동물에게 항바이러스 유효량의 상기 화학식 I 및 II의 화합물의 군으로부터 선택된 화합물, 및 1종 이상의 제약상 허용되는 담체, 부형제 또는 희석제를 투여하는 것을 포함하는, 상기 포유동물을 치료하는 방법이 제공된다. 임의로, 화학식 I 및/또는 II의 화합물은 항바이러스 유효량의, (a) AIDS 항바이러스제; (b) 항감염제; (c) 면역조절제; 및 (d) 다른 HIV 진입 억제제의 군으로부터 선택된 또 다른 AIDS 치료제와 조합하여 투여될 수 있다.
본 발명의 또 다른 실시양태는 항바이러스 유효량의 화학식 I 및 II의 화합물의 군으로부터 선택된 화합물, 및 1종 이상의 제약상 허용되는 담체, 부형제 및 희석제를; 항바이러스 유효량의, (a) AIDS 항바이러스제; (b) 항감염제; (c) 면역조절제; 및 (d) 다른 HIV 진입 억제제의 군으로부터 선택된 또 다른 AIDS 치료제와 임의로 조합하여 포함하는 제약 조성물이다.
본 발명의 또 다른 실시양태에서 본원의 화학식 I 및 II의 화합물을 제조하는 1종 이상의 방법이 제공된다.
또한 본원의 화학식 I 및 II의 화합물을 제조하는데 유용한 중간체 화합물이 본원에 제공된다.
본 발명은 이들 뿐만 아니라 하기 기재된 다른 중요한 목적에 관한 것이다.
본 발명의 화합물이 비대칭 중심을 보유하고, 따라서 부분입체이성질체 및 거울상이성질체의 혼합물로서 발생할 수 있기 때문에, 본 개시내용은 화학식 I 및 II의 화합물의 혼합물에 더하여, 그의 개별 부분입체이성질체 및 거울상이성질체 형태를 포함한다.
정의
본원에서 다른 곳에 달리 구체적으로 제시되지 않는 한, 하기 용어 중 1개 이상이 본원에 사용될 수 있고, 하기 의미를 가질 것이다:
"H"는 수소 (그의 동위원소, 예컨대 중수소 포함)를 지칭한다.
본원 및 청구범위에 사용된 용어 "C1-6 알킬"은 (달리 명시되지 않는 한) 직쇄 또는 분지쇄 알킬 기, 예컨대 메틸, 에틸, 프로필, 이소프로필, 부틸, 이소부틸, t-부틸, 아밀, 헥실 등을 의미한다.
"C1-C4 플루오로알킬"은, 적어도 1개의 H 원자가 F 원자로 치환되고, 각각의 H 원자가 독립적으로 F 원자에 의해 치환될 수 있는 것인, F-치환된 C1-C4 알킬을 지칭한다.
"할로겐"은 염소, 브로민, 아이오딘 또는 플루오린을 지칭한다.
"아릴" 또는 "Ar" 기는 완전 공액 파이-전자계를 갖는, 모든 탄소 모노시클릭 또는 융합-고리 폴리시클릭 (즉, 인접한 탄소 원자 쌍을 공유하는 고리) 기를 지칭한다. 아릴 기의 예는 비제한적으로 페닐, 나프탈레닐 및 안트라세닐이다. 아릴 기는 치환 또는 비치환될 수 있다. 치환되는 경우에, 치환기(들)는 바람직하게는 알킬, 시클로알킬, 아릴, 헤테로아릴, 헤테로지환족, 히드록시, 알콕시, 아릴옥시, 헤테로아릴옥시, 헤테로알리시클로옥시, 티오히드록시, 티오아릴옥시, 티오헤테로아릴옥시, 티오헤테로알리시클로옥시, 시아노, 할로겐, 니트로, 카르보닐, O-카르바밀, N-카르바밀, C-아미도, N-아미도, C-카르복시, O-카르복시, 술피닐, 술포닐, 술폰아미도, 트리할로메틸, 우레이도, 아미노 및 -NRxRy (여기서, Rx 및 Ry는 독립적으로 수소, 알킬, 시클로알킬, 아릴, 카르보닐, C-카르복시, 술포닐, 트리할로메틸, 및 조합된 5- 또는 6-원 헤테로지환족 고리의 군으로부터 선택됨)로부터 선택된 1개 이상이다.
본원에 사용된 "헤테로아릴" 기는, 고리(들) 내에 질소, 산소 및 황의 군으로부터 선택된 1개 이상의 원자를 갖고, 또한 완전 공액 파이-전자계를 갖는, 모노시클릭 또는 융합된 고리 (즉, 인접한 원자 쌍을 공유하는 고리) 기를 지칭한다. 달리 나타내지 않는 한, 헤테로아릴 기는 헤테로아릴 기 내의 탄소 또는 질소 원자에 부착될 수 있다. 용어 헤테로아릴은, 모 헤테로아릴의 N-옥시드가 관련 기술분야에 공지되어 있는 바와 같이 화학적으로 실현가능한 경우에, 이러한 N-옥시드를 포괄하는 것으로 의도됨을 주목해야 한다. 헤테로아릴 기의 예는 비제한적으로 푸릴, 티에닐, 벤조티에닐, 티아졸릴, 이미다졸릴, 옥사졸릴, 옥사디아졸릴, 티아디아졸릴, 벤조티아졸릴, 트리아졸릴, 테트라졸릴, 이속사졸릴, 이소티아졸릴, 피롤릴, 피라닐, 테트라히드로피라닐, 피라졸릴, 피리딜, 피리미디닐, 퀴놀리닐, 이소퀴놀리닐, 퓨리닐, 카르바졸릴, 벤족사졸릴, 벤즈이미다졸릴, 인돌릴, 이소인돌릴, 피라지닐, 디아지닐, 피라진, 트리아지닐, 테트라지닐, 및 테트라졸릴이다. 치환되는 경우에, 치환기(들)는 바람직하게는 알킬, 시클로알킬, 아릴, 헤테로아릴, 헤테로지환족, 히드록시, 알콕시, 아릴옥시, 헤테로아릴옥시, 헤테로알리시클로옥시, 티오알콕시, 티오히드록시, 티오아릴옥시, 티오헤테로아릴옥시, 티오헤테로알리시클로옥시, 시아노, 할로겐, 니트로, 카르보닐, O-카르바밀, N-카르바밀, C-아미도, N-아미도, C-카르복시, O-카르복시, 술피닐, 술포닐, 술폰아미도, 트리할로메틸, 우레이도, 아미노, 및 -NRxRy (여기서, Rx 및 Ry는 상기 정의된 바와 같음)로부터 선택된 1개 이상이다.
본원에 사용된 "헤테로지환족" 기는 고리(들) 내에 질소, 산소 및 황의 군으로부터 선택된 1개 이상의 원자를 갖는, 모노시클릭 또는 융합된 고리 기를 지칭한다. 고리는 결합의 안정한 배열을 제공하는 것들로부터 선택되고, 존재하지 않을 시스템을 포괄하는 것으로 의도되지 않는다. 고리는 또한 1개 이상의 이중 결합을 가질 수 있다. 그러나, 고리는 완전 공액 파이-전자계를 갖지 않는다. 헤테로지환족 기의 예는 비제한적으로 아제티디닐, 피페리딜, 피페라지닐, 이미다졸리닐, 티아졸리디닐, 3-피롤리딘-1-일, 모르폴리닐, 티오모르폴리닐 및 테트라히드로피라닐이다. 치환되는 경우에, 치환기(들)는 바람직하게는 알킬, 시클로알킬, 아릴, 헤테로아릴, 헤테로지환족, 히드록시, 알콕시, 아릴옥시, 헤테로아릴옥시, 헤테로알리시클로옥시, 티오히드록시, 티오알콕시, 티오아릴옥시, 티오헤테로아릴옥시, 티오헤테로알리시클로옥시, 시아노, 할로겐, 니트로, 카르보닐, 티오카르보닐, O-카르바밀, N-카르바밀, O-티오카르바밀, N-티오카르바밀, C-아미도, C-티오아미도, N-아미도, C-카르복시, O-카르복시, 술피닐, 술포닐, 술폰아미도, 트리할로메탄술폰아미도, 트리할로메탄술포닐, 실릴, 구아닐, 구아니디노, 우레이도, 포스포닐, 아미노 및 -NRxRy (여기서, Rx 및 Ry는 상기 정의된 바와 같음)로부터 선택된 1개 이상이다.
"알킬" 기는 직쇄 및 분지쇄 기를 포함하는 포화 지방족 탄화수소를 지칭한다. 바람직하게는, 알킬 기는 1 내지 20개의 탄소 원자 (수치 범위; 예를 들어, "1-20"이 본원에 언급되는 경우마다, 이는 기, 이 경우에 알킬 기가 1개의 탄소 원자, 2개의 탄소 원자, 3개의 탄소 원자 등 내지 20개 이하의 탄소 원자를 함유할 수 있는 것을 의미함)를 갖는다. 보다 바람직하게는, 이는 1 내지 10개의 탄소 원자를 갖는 중간 크기 알킬이다. 가장 바람직하게는, 이는 1 내지 4개의 탄소 원자를 갖는 저급 알킬이다. 알킬 기는 치환 또는 비치환될 수 있다. 치환되는 경우에, 치환기(들)는 바람직하게는 트리할로알킬, 시클로알킬, 아릴, 헤테로아릴, 헤테로지환족, 히드록시, 알콕시, 아릴옥시, 헤테로아릴옥시, 헤테로알리시클로옥시, 티오히드록시, 티오알콕시, 티오아릴옥시, 티오헤테로아릴옥시, 티오헤테로알리시클로옥시, 시아노, 할로, 니트로, 카르보닐, 티오카르보닐, O-카르바밀, N-카르바밀, O-티오카르바밀, N-티오카르바밀, C-아미도, C-티오아미도, N-아미도, C-카르복시, O-카르복시, 술피닐, 술포닐, 술폰아미도, 트리할로메탄술폰아미도, 트리할로메탄술포닐, 및 조합된 5- 또는 6-원 헤테로지환족 고리로부터 개별적으로 선택된 1개 이상이다.
"시클로알킬" 기는 모든-탄소 모노시클릭 또는 융합된 고리 (즉, 인접한 탄소 원자 쌍을 공유하는 고리) 기를 지칭하며, 여기서 1개 이상의 고리는 완전 공액 파이-전자계를 갖지 않는다. 시클로알킬 기의 예는 비제한적으로 시클로프로판, 시클로부탄, 시클로펜탄, 시클로펜텐, 시클로헥산, 시클로헥센, 시클로헵탄, 시클로헵텐 및 아다만탄이다. 시클로알킬 기는 치환 또는 비치환될 수 있다. 치환되는 경우에, 치환기(들)는 바람직하게는 알킬, 아릴, 헤테로아릴, 헤테로지환족, 히드록시, 알콕시, 아릴옥시, 헤테로아릴옥시, 헤테로알리시클로옥시, 티오히드록시, 티오알콕시, 티오아릴옥시, 티오헤테로아릴옥시, 티오헤테로알리시클로옥시, 시아노, 할로, 니트로, 카르보닐, 티오카르보닐, O-카르바밀, N-카르바밀, O-티오카르바밀, N-티오카르바밀, C-아미도, C-티오아미도, N-아미도, C-카르복시, O-카르복시, 술피닐, 술포닐, 술폰아미도, 트리할로- 메탄술폰아미도, 트리할로메탄술포닐, 실릴, 아미디노, 구아니디노, 우레이도, 포스포닐, 아미노 및 -NRxRy (여기서, Rx 및 Ry는 상기 정의된 바와 같음)로부터 개별적으로 선택된 1개 이상이다.
"알케닐" 기는 적어도 2개의 탄소 원자 및 적어도 1개의 탄소-탄소 이중 결합을 갖는, 본원에 정의된 바와 같은 알킬 기를 지칭한다.
"알키닐" 기는 적어도 2개의 탄소 원자 및 적어도 1개의 탄소-탄소 삼중 결합을 갖는, 본원에 정의된 바와 같은 알킬 기를 지칭한다.
"히드록시" 기는 -OH 기를 지칭한다.
"알콕시" 기는 본원에 정의된 바와 같은, -O-알킬 및 -O-시클로알킬 기 둘 다를 지칭한다.
"아릴옥시" 기는 본원에 정의된 바와 같은, -O-아릴 및 -O-헤테로아릴 기 둘 다를 지칭한다.
"헤테로아릴옥시" 기는 헤테로아릴이 본원에 정의된 바와 같은 것인 헤테로아릴-O- 기를 지칭한다.
"헤테로알리시클로옥시" 기는 헤테로지환족이 본원에 정의된 바와 같은 것인 헤테로지환족-O- 기를 지칭한다.
"티오히드록시" 기는 -SH 기를 지칭한다.
"티오알콕시" 기는 본원에 정의된 바와 같은, S-알킬 및 -S-시클로알킬 기 둘 다를 지칭한다.
"티오아릴옥시" 기는 본원에 정의된 바와 같은, -S-아릴 및 -S-헤테로아릴 기 둘 다를 지칭한다.
"티오헤테로아릴옥시" 기는 헤테로아릴이 본원에 정의된 바와 같은 것인 헤테로아릴-S- 기를 지칭한다.
"티오헤테로알리시클로옥시" 기는 헤테로지환족이 본원에 정의된 바와 같은 것인 헤테로지환족-S- 기를 지칭한다.
"카르보닐" 기는 R"가 수소, 알킬, 알케닐, 알키닐, 시클로알킬, 아릴, 헤테로아릴 (고리 탄소를 통해 결합됨) 및 헤테로지환족 (고리 탄소를 통해 결합됨)의 군으로부터 선택되며, 이들 각각이 본원에 정의된 바와 같은 것인 -C(=O)-R" 기를 지칭한다.
"알데히드" 기는 R"가 수소인 카르보닐 기를 지칭한다.
"티오카르보닐" 기는 R"가 본원에 정의된 바와 같은 것인 -C(=S)-R" 기를 지칭한다.
"케토" 기는 C=O의 어느 한쪽 또는 양쪽 상의 탄소가 알킬, 시클로알킬, 아릴, 또는 헤테로아릴 또는 헤테로지환족 기의 탄소일 수 있는 것인 -CC(=O)C- 기를 지칭한다.
"트리할로메탄카르보닐" 기는 Z가 할로겐인 Z3CC(=O)- 기를 지칭한다.
"C-카르복시" 기는 R"가 본원에 정의된 바와 같은 것인 -C(=O)O-R" 기를 지칭한다.
"O-카르복시" 기는 R"가 본원에 정의된 바와 같은 것인 R"C(-O)O- 기를 지칭한다.
"카르복실산" 기는 R"가 수소인 C-카르복시 기를 지칭한다.
"트리할로메틸" 기는 Z가 본원에 정의된 바와 같은 할로겐 기인 -CZ3 기를 지칭한다.
"트리할로메탄술포닐" 기는 Z가 상기 정의된 바와 같은 것인 Z3CS(=O)2- 기를 지칭한다.
"트리할로메탄술폰아미도" 기는 Z가 상기 정의된 바와 같고, Rx가 H 또는 (C1-6)알킬인 Z3CS(=O)2NRx- 기를 지칭한다.
"술피닐" 기는 R"가 (C1- 6)알킬인 -S(=O)-R" 기를 지칭한다.
"술포닐" 기는 R"가 (C1- 6)알킬인 -S(=O)2R" 기를 지칭한다.
"S-술폰아미도" 기는 RX 및 RY가 독립적으로 H 또는 (C1- 6)알킬인 -S(=O)2NRXRY를 지칭한다.
"N-술폰아미도" 기는 Rx가 H 또는 (C1- 6)알킬인 R"S(=O)2NRX- 기를 지칭한다.
"O-카르바밀" 기는 RX 및 RY가 독립적으로 H 또는 (C1- 6)알킬인 -OC(=O)NRxRy 기를 지칭한다.
"N-카르바밀" 기는 Rx 및 Ry가 독립적으로 H 또는 (C1- 6)알킬인 RxOC(=O)NRy 기를 지칭한다.
"O-티오카르바밀" 기는 Rx 및 Ry가 독립적으로 H 또는 (C1- 6)알킬인 -OC(=S)NRxRy 기를 지칭한다.
"N-티오카르바밀" 기는 Rx 및 Ry가 독립적으로 H 또는 (C1- 6)알킬인 RxOC(=S)NRy- 기를 지칭한다.
"아미노" 기는 -NH2 기를 지칭한다.
"C-아미도" 기는 Rx 및 Ry가 독립적으로 H 또는 (C1- 6)알킬인 -C(=O)NRxRy 기를 지칭한다.
"C-티오아미도" 기는 Rx 및 Ry가 독립적으로 H 또는 (C1- 6)알킬인 -C(=S)NRxRy 기를 지칭한다.
"N-아미도" 기는 Rx 및 Ry가 독립적으로 H 또는 (C1- 6)알킬인 RxC(=O)NRy- 기를 지칭한다.
"우레이도" 기는 Rx, Ry, 및 Ry2가 독립적으로 H 또는 (C1- 6)알킬인 -NRxC(=O)NRyRy2 기를 지칭한다.
"구아니디노" 기는 Rx, Ry, 및 Ry2가 독립적으로 H 또는 (C1- 6)알킬인 -RxNC(=N)NRyRy2 기를 지칭한다.
"아미디노" 기는 Rx 및 Ry가 독립적으로 H 또는 (C1- 6)알킬인 RxRyNC(=N)- 기를 지칭한다.
"시아노" 기는 -CN 기를 지칭한다.
"실릴" 기는 R"가 (C1- 6)알킬 또는 페닐인 -Si(R")3을 지칭한다.
"포스포닐" 기는 Rx가 (C1- 6)알킬인 P(=O)(ORx)2를 지칭한다.
"히드라지노" 기는 Rx, Ry, 및 Ry2가 독립적으로 H 또는 (C1- 6)알킬인 -NRxNRyRy2 기를 지칭한다.
임의의 2개의 인접한 R 기는 조합되어, 이러한 R 기가 처음에 보유한 고리에 융합된, 추가의 아릴, 시클로알킬, 헤테로아릴 또는 헤테로시클릭 고리를 형성할 수 있다.
헤테로아릴계 내 질소 원자는 "헤테로아릴 고리 이중 결합에 참여"할 수 있고, 이는 5-원 고리 헤테로아릴 기를 포함하는 2종의 호변이성질체 구조에서의 이중 결합 형태를 지칭하는 것으로 관련 기술분야에 공지되어 있다. 이는 관련 기술분야의 화학자에 의해 익히 이해되는 바와 같이 질소가 치환될 수 있는지의 여부를 지시한다. 본 개시내용 및 본 개시내용의 청구범위는 화학 결합의 공지된 일반적 원리에 기초한다. 청구범위는 문헌에 기초하여 불안정하거나 존재할 수 없는 것으로 공지된 구조를 포괄하지 않는 것으로 이해된다.
본원에 개시된 화합물의 제약상 허용되는 염 및 전구약물은 본 발명의 범주 내이다. 본원 및 청구범위에 사용된 용어 "제약상 허용되는 염"은 비독성 염기 부가염을 포함하는 것으로 의도된다. 적합한 염은 유기 및 무기 산, 예컨대 비제한적으로 염산, 브로민화수소산, 인산, 황산, 메탄술폰산, 아세트산, 타르타르산, 락트산, 술핀산, 시트르산, 말레산, 푸마르산, 소르브산, 아코니트산, 살리실산, 프탈산 등으로부터 유도된 것들을 포함한다. 본원에 사용된 용어 "제약상 허용되는 염"은 또한 산성 기의 염, 예컨대 카르복실레이트, 암모늄과 같은 반대이온과의 염, 알칼리 금속 염, 특히 나트륨 또는 칼륨 염, 알칼리 토금속 염, 특히 칼슘 또는 마그네슘 염, 및 적합한 유기 염기, 예컨대 저급 알킬아민 (메틸아민, 에틸아민, 시클로헥실아민 등) 또는 치환된 저급 알킬아민 (예를 들어, 히드록실-치환된 알킬아민, 예컨대 디에탄올아민, 트리에탄올아민 또는 트리스(히드록시메틸)-아미노메탄)과의 염, 또는 피페리딘 또는 모르폴린과 같은 염기와의 염을 포함하는 것으로 의도된다.
상기 언급된 바와 같이, 본 발명의 화합물은 또한 "전구약물"을 포함한다. 본원에 사용된 용어 "전구약물"은 용어 "전구약물 에스테르" 및 용어 "전구약물 에테르" 둘 다를 포괄한다.
용어 "C-19" 및 "C-3"은 IUPAC 규칙에 따라 넘버링된 트리테르펜 코어의 특정 위치 (예시적 트리테르펜: 베툴린에 대해 하기 도시된 위치)를 지칭한다.
상기 제시된 바와 같이, 본 발명은 하기 화학식 I의 화합물; 및 하기 화학식 II의 화합물의 군으로부터 선택된, 그의 제약상 허용되는 염을 포함하는 화합물에 관한 것이다.
<화학식 I>
<화학식 II>
상기 식에서, X는 페닐, 헤테로아릴 고리, C4-8 시클로알킬, C4-8 시클로알케닐, C4-9 스피로시클로알킬, C4-9 스피로시클로알케닐, C4-8 옥사시클로알킬, C4-8 디옥사시클로알킬, C6-8 옥사시클로알케닐, C6-8 디옥사시클로알케닐, C6 시클로디알케닐, C6 옥사시클로디알케닐, C6-9 옥사스피로시클로알킬 및 C6-9 옥사스피로시클로알케닐 고리의 군으로부터 선택되고;
추가로 여기서 X는 A로 치환되고, 여기서 A는 -H, -할로, -히드록실, -C1-6 알킬, -C1-6 알콕시, -C1-6 알킬-Q1, -알킬치환된 C1-6 알킬-Q1, -CN, -CF2Q1, -NR2R2, -COOR2 및 -CONR2R2의 군으로부터 선택된 적어도 1개의 구성원이고;
여기서 Q1은 아릴, 헤테로아릴, 치환된 헤테로아릴, -OR2, -COOR3, -NR2R2, -SO2R7, -CONHSO2R3, 및 -CONHSO2NR2R2의 군으로부터 선택되고;
Y는 -COOR2, -C(O)NR2SO2R3, -C(O)NHSO2NR2R2, -NR2SO2R2, -SO2NR2R2, -C3-6 시클로알킬-COOR2, -C2-6 알케닐-COOR2, -C2-6 알키닐-COOR2, -C1-6 알킬-COOR2, -알킬치환된 C1-6 알킬, -COOR2, CF2-COOR2, -NHC(O)(CH2)n-COOR2, -SO2NR2C(O)R2, -테트라졸, 및 -CONHOH의 군으로부터 선택되고,
여기서 n=1-6이고;
R1은
의 군으로부터 선택되고;
W는 부재하거나, 또는 -CH2 또는 -CO이고;
Z는 -NR28R29, -OR30, -COOR2, -CONR18R19, F, Cl, Br, 및 I의 군으로부터 선택되고;
U는 -NR28R29, -OR30, -COOR2, -CONR18R19, F, Cl, Br, I, 아릴 및 헤테로아릴의 군으로부터 선택되고;
R2는 -H, 벤질, -C1-6 알킬, -알킬치환된 C1-6 알킬 및 -아릴치환된 C1-6 알킬의 군으로부터 선택되고;
R3은 벤질, -C1-6 알킬 또는 -알킬치환된 C1-6 알킬이고;
R4는 -H, -C1-6 알킬, -C1-6 알킬-C(OR3)2-C3-6 시클로알킬, -C1-6 치환된 알킬, -C1-6 알킬-C3-6 시클로알킬, -C1-6 알킬-Q2, -C1-6 알킬-C3-6 시클로알킬-Q2, 아릴, 헤테로아릴, 치환된 헤테로아릴, -COR6, -COCOR6, -SO2R7, -SO2NR2R2, 의 군으로부터 선택되고,
여기서 Q2는 헤테로아릴, 치환된 헤테로아릴, F, Cl, Br, I, -CF3, -OR2, -COOR2, -NR8R9, -CONR10R11 및 -SO2R7의 군으로부터 선택되고;
R5는 -H, -C1-6 알킬, -C3-6 시클로알킬, -C1-6 알킬치환된 알킬, -C1-6 알킬-NR8R9, -COR6, -COCOR6, -SO2R7 및 -SO2NR2R2의 군으로부터 선택되며;
단 W가 CO인 경우에 R4 또는 R5는 COR6 또는 COCOR6일 수 없고;
추가로 단 R4 또는 R5 중 오직 1개가 -COR6, -COCOR6, -SO2R7 및 -SO2NR2R2의 군으로부터 선택될 수 있거나;
R6은 -C1-6 알킬, -C1-6 알킬-치환된알킬, -C3-6 시클로알킬, -C3-6 치환된시클로알킬-Q3, -C1-6 알킬-Q3, -C1-6 알킬-치환된알킬-Q3,-C3-6 시클로알킬-Q3, 아릴-Q3, -NR13R14, 및 -OR15의 군으로부터 선택되고;
여기서 Q3은 아릴, 헤테로아릴, 치환된 헤테로아릴, -OR2, -COOR2, -NR8R9, SO2R7, -CONHSO2R3, 및 -CONHSO2NR2R2의 군으로부터 선택되고;
R7은 -C1-6 알킬, -C1-6 치환된 알킬, -C3-6 시클로알킬, -CF3, 아릴, 및 헤테로아릴의 군으로부터 선택되고;
R8 및 R9는 독립적으로 -H, -C1-6 알킬, -C1-6 치환된 알킬, 아릴, 헤테로아릴, 치환된 아릴, 치환된 헤테로아릴, -C1 -6 알킬-Q2, 및 -COOR3의 군으로부터 선택되고:
R8은 또한 -COOR3일 수 있고;
또는 R8 및 R9는 인접한 N과 함께
의 군으로부터 선택된 사이클을 형성하고;
V는 -CR24R25, -SO2, -O 및 -NR12의 군으로부터 선택되고;
M은 -CHR24R25, -NR26R27, -SO2R7, -SO2NR3R3 및 -OH의 군으로부터 선택되고;
R10 및 R11은 독립적으로 -H, -C1-6 알킬, -C1-6 치환된 알킬 및 -C3-6 시클로알킬의 군으로부터 선택되거나,
R12는 -C1-6 알킬, -C1-6 알킬-OH; -C1-6 알킬, -C1-6 치환된 알킬, -C3-6 시클로알킬, -COR7, -COONR18R19, -SOR7, 및 -SONR20R21의 군으로부터 선택되고;
R13 및 R14는 독립적으로 -H, -C1-6 알킬, -C3-6 시클로알킬, -C1-6 치환된 알킬, -C1-6 알킬-Q4, -C1-6 알킬-C3-6 시클로알킬-Q4, -C1-6 치환된 알킬-Q4 및 의 군으로부터 선택되거나,
또는 R13 및 R14는 인접한 N과 함께
의 군으로부터 선택된 사이클을 형성하고;
R15는 -C1-6 알킬, -C3-6 시클로알킬, -C1-6 치환된 알킬, -C1-6 알킬-Q4, -C1-6 알킬-C3-6 시클로알킬-Q4 및 -C1-6 치환된 알킬-Q4의 군으로부터 선택되고;
Q4는 헤테로아릴, 치환된 헤테로아릴, -NR2R2, -CONR2R2, -COOR2, -OR2, 및 -SO2R3의 군으로부터 선택되고;
R16은 -H, -C1-6 알킬, -NR2R2, 및 -COOR3의 군으로부터 선택되고;
R17은 -H, -C1-6 알킬, -COOR3, 및 아릴의 군으로부터 선택되고;
R18 및 R19는 독립적으로 H, -C1-6 알킬, -C1-6 치환된 알킬, 및 -C1-6 시클로알킬의 군으로부터 선택되고;
R18은 또한 -COOR3일 수 있거나;
R20 및 R21은 독립적으로 H, -C1-6 알킬, -C1-6 치환된 알킬, -C1-6 알킬-Q5, -C1-6 시클로알킬, 아릴, 치환된 아릴, 헤테로아릴, 및 치환된 헤테로아릴의 군으로부터 선택되고,
Q5는 할로겐 및 SO2R3의 군으로부터 선택되고;
R24 및 R25는 독립적으로 -H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -SO2R3, -SO2NR2R2 또는 -OH, -NR2R2, -NR2SO2R3, -NR2COR3 및 -NR2CONR2R2의 군으로부터 선택되며;
단 R24 및 R25 중 오직 1개가 -OH, -NR2R2, -NR2SO2R3, -NR2COR3 및 -NR2CONR2R2의 군으로부터 선택될 수 있고;
R26 및 R27은 독립적으로 -H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -C1-3 알킬아릴, C1- 3알킬헤테로아릴, -CO2R2 및 -SO2R7의 군으로부터 선택되며;
단 R26 및 R27 중 오직 1개가 -CO2R2 또는 -SO2R7의 군으로부터 선택될 수 있고;
R28 및 R29는 독립적으로 H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -C3-6 시클로알킬, -C1-6 알킬-Q6, -COC1 -6 알킬-Q6, -COOR3; -COCF3의 군으로부터 선택되고;
R28은 또한 -COOR3 및 -CONR18R19로부터 선택될 수 있거나;
또는 R28 및 R29는 인접한 N과 함께
의 군으로부터 선택된 사이클을 형성하고;
R30은 H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -C3-6 시클로알킬, 및 -C1-6 알킬-Q6의 군으로부터 선택되고;
여기서 Q6은 H, -OR2, -COOR2, -COCOOR2, 및 -NR31R32의 군으로부터 선택되고;
R31 및 R32는 독립적으로 -H, -C1-6 알킬, -C1-6 치환된 알킬, -C1-6 치환된 알킬-OR2, 및 -COR3의 군으로부터 선택되거나,
R33은 -H, -C1-6 알킬, -C1-6 치환된 알킬, 및 -C1-6 치환된 알킬-Q7의 군으로부터 선택되고,
여기서 Q7은 -COOR2 및 -COONR2R2의 군으로부터 선택된다.
특히, X가 페닐인 화학식 I 및 II의 화합물이 바람직하다.
A가 -H 또는 할로, 특히 -F인 화합물이 또한 바람직하다.
Y가 -COOR2인 화합물이 추가로 바람직하다. R2가 -H인 것이 또한 바람직하다.
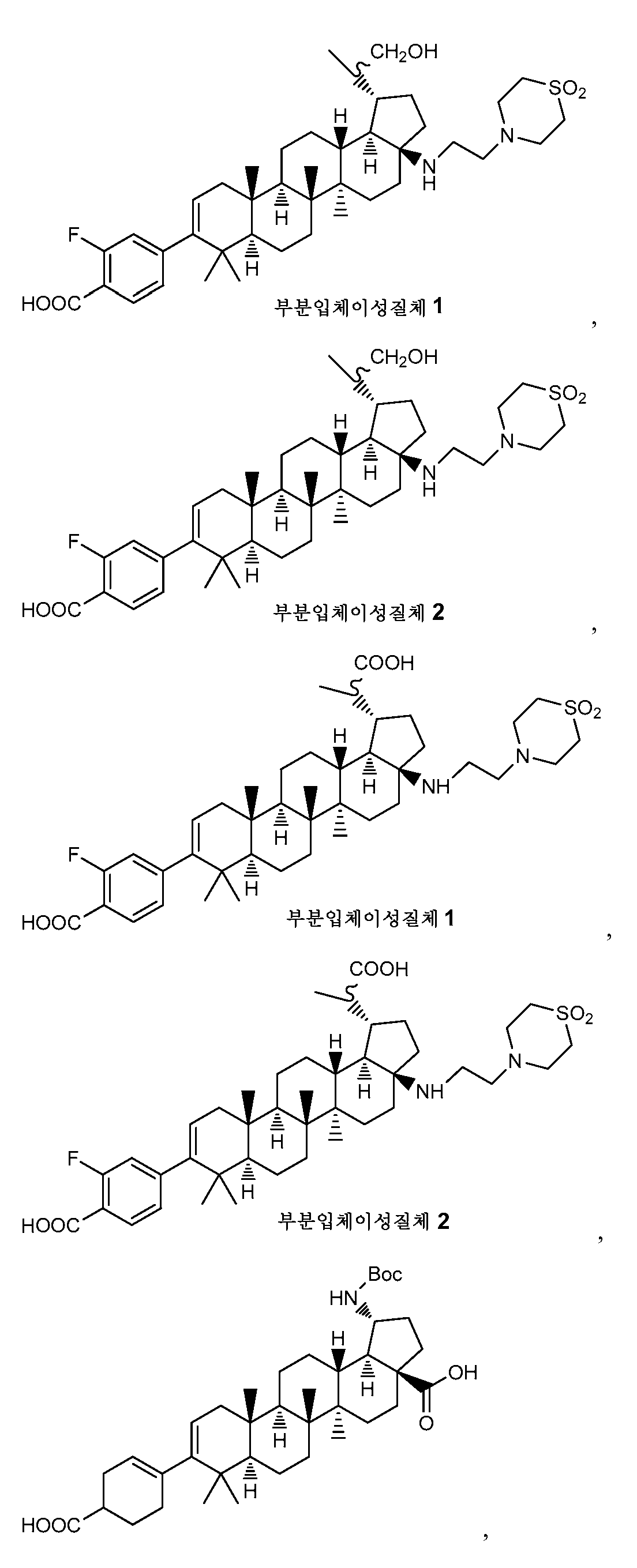
다음의 군으로부터 선택된, 그의 제약상 허용되는 염을 포함하는 화합물이 또한 바람직하다.
상기 기재된 모든 다양한 실시양태에 따른 본 발명의 화합물은 경구로, 비경구로 (피하 주사, 정맥내, 근육내, 흉골내 주사 또는 주입 기술 포함), 흡입 스프레이에 의해, 또는 직장으로, 및 다른 수단에 의해, 통상의 기술자에게 이용가능한 비-독성 제약상 허용되는 담체, 부형제 및 희석제를 함유하는 투여 단위 제제로 투여될 수 있다. 1종 이상의 아주반트가 또한 포함될 수 있다.
따라서, 본 발명에 따라, 바이러스 감염, 예컨대 HIV 감염 및 AIDS를 치료하기 위한 치료 방법 및 제약 조성물이 추가로 제공된다. 치료는 항바이러스 유효량의 1종 이상의 화학식 I 및 II의 화합물을 1종 이상의 제약상 허용되는 담체, 부형제 또는 희석제와 함께 함유하는 제약 조성물을 이러한 치료를 필요로 하는 환자에게 투여하는 것을 포함한다. 본원에 사용된 용어 "항바이러스 유효량"은, 의미있는 환자 이익, 즉 HIV 감염의 억제를 특징으로 하는 급성 상태의 억제, 개선 또는 치유를 나타내기에 충분한 조성물 및 방법의 각각의 활성 성분의 총량을 의미한다. 단독으로 투여되는 개별 활성 성분에 적용되는 경우에, 상기 용어는 그 성분 단독의 양을 지칭한다. 조합에 적용되는 경우에, 상기 용어는 조합으로, 연속적으로 또는 동시에 투여되는지의 여부와 관계없이, 치료 효과를 발생시키는 활성 성분들의 조합된 양을 지칭한다. 본원 및 청구범위에 사용된 용어 "치료하다, 치료하는, 치료"는 HIV 감염과 연관된 질환의 예방, 개선 또는 치유를 의미한다.
본 발명의 제약 조성물은 경구로 투여가능한 현탁액 또는 정제; 뿐만 아니라 비강 스프레이, 멸균 주사가능한 제제, 예를 들어 멸균 주사가능한 수성 또는 유성 현탁액 또는 좌제로서의 형태일 수 있다. 제약상 허용되는 담체, 부형제 또는 희석제는 제약 조성물에 이용될 수 있고, 제약 제제 분야에서 이용되는 것들이다.
현탁액으로서 경구로 투여되는 경우에, 이들 조성물은 제약 제제 기술분야에 전형적으로 공지된 기술에 따라 제조되고, 벌크를 부여하기 위한 미세결정질 셀룰로스, 현탁화제로서의 알긴산 또는 알긴산나트륨, 점도 증진제로서의 메틸셀룰로스, 및 관련 기술분야에 공지된 감미제/향미제를 함유할 수 있다. 즉시 방출 정제로서, 이들 조성물은 관련 기술분야에 공지된 미세결정질 셀룰로스, 인산이칼슘, 전분, 스테아르산마그네슘 및 락토스 및/또는 다른 부형제, 결합제, 연장제, 붕해제, 희석제 및 윤활제를 함유할 수 있다.
주사가능한 용액 또는 현탁액은 공지된 기술에 따라, 적합한 비-독성, 비경구로 허용되는 희석제 또는 용매, 예컨대 만니톨, 1,3-부탄디올, 물, 링거액 또는 등장성 염화나트륨 용액, 또는 적합한 분산화제 또는 습윤제 및 현탁화제, 예컨대 합성 모노- 또는 디글리세리드를 비롯한 멸균, 배합, 고정 오일, 및 올레산을 비롯한 지방산을 사용하여 제제화될 수 있다.
본원에 제시된 화합물은, 통상적으로 연장된 기간, 예컨대 수일, 수주, 수개월, 또는 심지어 수년에 걸쳐, 인간에게 약 1 내지 100 mg/kg 체중의 투여량 범위의 분할 용량으로 경구 투여될 수 있다. 한 바람직한 투여량 범위는 경구로 약 1 내지 10 mg/kg 체중의 분할 용량이다. 또 다른 바람직한 투여량 범위는 약 1 내지 20 mg/kg 체중의 분할 용량이다. 그러나, 임의의 특정한 환자를 위한 구체적인 용량 수준 및 투여 빈도는 달라질 수 있으며, 이는 사용되는 구체적 화합물의 활성, 그 화합물의 대사 안정성 및 작용 기간, 연령, 체중, 전반적 건강, 성별, 식이, 투여 방식 및 시간, 배출 속도, 약물 조합, 특정한 상태의 중증도, 및 요법을 받는 숙주를 비롯한 다양한 인자에 의존적일 것으로 이해될 것이다.
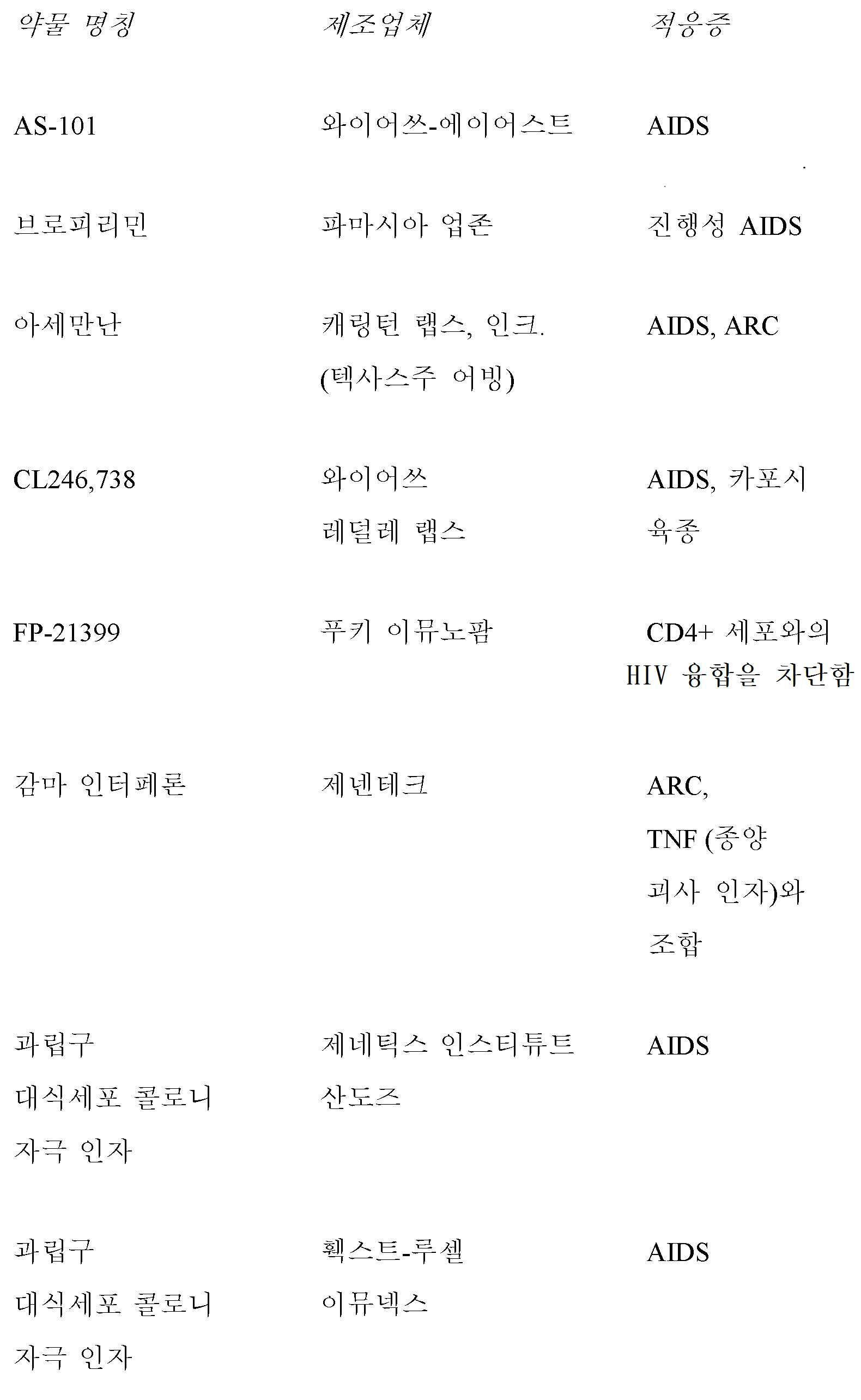
또한 본원에 제시된 화학식 I 및 II의 화합물과 함께 AIDS의 치료에 유용한 1종 이상의 다른 작용제와의 조합이 본원에서 고려된다. 예를 들어, 본 개시내용의 화합물은 노출전 및/또는 노출후의 기간에 관계없이, 유효량의 AIDS 항바이러스제, 면역조절제, 항감염제 또는 백신, 예컨대 하기 비제한적 표에 있는 것들과 조합하여 효과적으로 투여될 수 있다.
항바이러스제
면역조절제
항감염제
추가로, 본원에 제시된 본 개시내용의 화합물은 HIV 진입 억제제와 조합하여 사용될 수 있다. 이러한 HIV 진입 억제제의 예는 문헌 [DRUGS OF THE FUTURE 1999, 24(12), pp. 1355-1362; CELL, Vol. 9, pp. 243-246, Oct. 29, 1999; 및 DRUG DISCOVERY TODAY, Vol. 5, No. 5, May 2000, pp. 183-194 및 Inhibitors of the entry of HIV into host cells, Meanwell, Nicholas A.; Kadow, John F. Current Opinion in Drug Discovery & Development (2003), 6(4), 451-461]에 논의되어 있다. 구체적으로 상기 화합물은 CCR5 또는 CXCR4 보조수용체 둘 중 하나를 표적으로 하는 부착 억제제, 융합 억제제 및 케모카인 수용체 길항제와 조합하여 이용될 수 있다. HIV 부착 억제제는 또한 US 7,354,924 및 US 2005/0209246에 제시되어 있다.
본원의 화합물과 AIDS 항바이러스제, 면역조절제, 항감염제, HIV 진입 억제제 또는 백신과의 조합의 범주는 상기 표에 있는 목록에 제한되지는 않고, 원칙적으로 AIDS의 치료에 유용한 임의의 제약 조성물과의 임의의 조합을 포함하는 것으로 이해될 것이다.
바람직한 조합은 본 개시내용의 화합물 및 HIV 프로테아제의 억제제 및/또는 HIV 역전사효소의 비-뉴클레오시드 억제제를 사용하는 동시 또는 교대 치료이다. 조합에서의 임의적인 제4 성분은 HIV 역전사효소의 뉴클레오시드 억제제, 예컨대 AZT, 3TC, ddC 또는 ddI이다. 바람직한 HIV 프로테아제의 억제제는 레야타즈® (활성 성분 아타자나비르)이다. 전형적으로 300 내지 600mg의 용량이 1일 1회 투여된다. 이는 저용량의 리토나비르 (50 내지 500mg)와 공-투여될 수 있다. 또 다른 바람직한 HIV 프로테아제의 억제제는 칼레트라®이다. 또 다른 유용한 HIV 프로테아제의 억제제는 N-(2(R)-히드록시-1-(S)-인다닐)-2(R)-페닐메틸-4-(S)-히드록시-5-(1-(4-(3-피리딜-메틸)-2(S)-N'-(t-부틸카르복스아미도)-피페라지닐))-펜탄아미드 에탄올레이트의 술페이트 염이고, U.S. 5,413,999에 따라 합성되는, 인디나비르이다. 인디나비르는 일반적으로 800 mg의 투여량으로 1일 3회 투여된다. 다른 바람직한 프로테아제 억제제는 넬피나비르 및 리토나비르이다. 또 다른 바람직한 HIV 프로테아제의 억제제는 600 또는 1200 mg tid 투여량으로 투여되는 사퀴나비르이다. 바람직한 HIV 역전사효소의 비-뉴클레오시드 억제제는 에파비렌즈를 포함한다. 이들 조합은 HIV 감염의 확산 및 정도를 제한하는 것에 대해 예상치 못한 효과를 가질 수 있다. 바람직한 조합은 하기 (1) 인디나비르와 에파비렌즈, 및 임의로, AZT 및/또는 3TC 및/또는 ddI 및/또는 ddC; (2) 인디나비르, 및 AZT 및/또는 ddI 및/또는 ddC 및/또는 3TC 중 임의의 것, 특히 인디나비르 및 AZT 및 3TC; (3) 스타부딘 및 3TC 및/또는 지도부딘; (4) 테노포비르 디소프록실 푸마레이트 염 및 엠트리시타빈과의 조합을 포함한다.
이러한 조합에서 본 발명의 화합물 및 다른 활성제는 개별적으로 또는 함께 투여될 수 있다. 또한, 1종의 성분은 다른 작용제(들)의 투여 전에, 동시에, 또는 투여 후에 투여될 수 있다.
약어:
NBS = N-브로모숙신이민
TBDMS =tert-부틸디메틸실란
PTFE = 폴리테트라플루오로에틸렌
NMO = 4-메틸모르폴린-N-옥시드
THF = 테트라히드로푸란
TLC = 박층 크로마토그래피
DCM = 디클로로메탄
DCE = 디클로로에탄
TFA = 트리플루오로아세트산
LCMS = 액체 크로마토그래피 질량 분광분석법
Prep = 정제용
HPLC = 고성능 액체 크로마토그래피
DAST = (디에틸아미노)황 트리플루오라이드
TEA = 트리에틸아민
DIPEA = N,N-디이소프로필에틸아민
HATU = [O-(7-아자벤조트리아졸-1-일)-1,1,3,3-테트라메틸우로늄 헥사플루오로포스페이트]
DMAP = 디메틸아미노피리딘
TMS = 트리메틸실릴
NMR = 핵 자기 공명
DPPA = 디페닐 포스포릴 아지드
AIBN = 아조비스이소부티로니트릴
TBAF = 테트라부틸암모늄 플루오라이드
DMF = 디메틸포름아미드
TBTU = O-(벤조트리아졸-1-일)-N,N,N',N'-테트라메틸우로늄 테트라플루오로보레이트
min = 분
h = 시간
sat. = 포화
TEA = 트리에틸아민
EtOAc = 에틸 아세테이트
TFA = 트리플루오로아세트산
PCC = 피리디늄 클로로크로메이트
TLC = 박층 크로마토그래피
Tf2NPh = (트리플루오로메틸술포닐)메탄술폰아미드
디옥산 = 1,4-디옥산
PG = 보호기
atm = 대기압
mol = 몰
mmol = 밀리몰
mg = 밀리그램
μg = 마이크로그램
μl = 마이크로리터
μm= 마이크로미터
mm = 밀리미터
실시예
하기 실시예는 상기 일반적으로 기재된 바와 같은 화학식 I 및 II의 화합물의 전형적인 합성을 예시한다. 이들 실시예는 단지 예시적이며, 어떠한 방식으로도 본 개시내용을 제한하도록 의도되지 않는다. 시약 및 출발 물질은 통상의 기술자가 용이하게 입수가능하다.
화학
선택된 실시예의 전형적 절차 및 특성화:
달리 언급되지 않는 한, 용매 및 시약은 상업적 공급원으로부터 입수된 대로 직접 사용하였고, 반응은 질소 분위기 하에 수행하였다. 플래쉬 크로마토그래피는 실리카 겔 60 (0.040-0.063 입자 크기; EM 사이언스(EM Science) 공급) 상에서 수행하였다. 1H NMR 스펙트럼은 500 MHz에서 브루커(Bruker) DRX-500f (또는 언급된 바와 같이 브루커 AV 400 MHz, 300 MHz에서 브루커 DPX-300B 또는 배리안 제미니(Varian Gemini) 300) 상에서 기록하였다. 화학적 이동은 δTMS = 0에 대한 δ 스케일 상에서 ppm으로 보고하였다. 하기 내부 참조는 하기 용매 중 잔류 양성자에 대해 사용하였다: CDCl3 (δH 7.26), CD3OD (δH 3.30), 아세트산-d4 (아세트산 d4) (δH 11.6, 2.07), DMSO 믹스 또는 DMSO-D6_CDCl3 (δH 2.50 및 8.25) (비 75%:25%), 및 DMSO-D6 (δH 2.50).
표준 두문자어는 다중도 패턴을 기재하기 위해 사용하였다: s (단일선), br. s (넓은 단일선), d (이중선), t (삼중선), q (사중선), m (다중선), b (넓은), app (명백한). 커플링 상수 (J)는 헤르츠 단위이다. 모든 액체 크로마토그래피 (LC) 데이터는 전기분무 방식의 LC를 위한 마이크로매스 플랫폼(Micromass Platform)을 사용하여 결정된 질량 분광측정법 (MS) 데이터와 함께 SPD-10AV UV-Vis 검출기를 사용하여 시마즈(Shimadzu) LC-10AS 액체 크로마토그래프 상에서 기록하였다.
LC/MS 방법:
방법 1
출발%B = 0, 최종%B = 100, 2분에 걸친 구배, 100%B에서 유지
유량 = 4 mL / 분
파장 = 220 nm
용매 A = 95% 물, 5% 메탄올, 10 mM 아세트산암모늄
용매 B = 5% 물, 95% 메탄올, 10 mM 아세트산암모늄
칼럼 = 엑스브리지(Xbridge) C18 5μm 4.6 x 50 mm
방법 2
출발%B = 0, 최종%B = 100, 2분에 걸친 구배, 100%B에서 유지
유량 = 4 mL / 분
파장 = 220 nm
용매 A = 95% 물, 5% 메탄올, 10 mM 아세트산암모늄
용매 B = 5% 물, 95% 메탄올, 10 mM 아세트산암모늄
칼럼 = 페노메넥스 루나(Phenomenex Luna) C18, 5 μm, 3.0 x 50 mm
방법 3
출발%B = 0, 최종%B = 100, 2분에 걸친 구배, 100%B에서 유지
유량 = 1 mL/분
파장 = 220 nm
용매 A = 95% 물, 5% 아세토니트릴, 10mM 아세트산암모늄
용매 B = 5% 물, 95% 아세토니트릴, 10mM 아세트산암모늄
칼럼 = 페노메넥스 루나 C18, 3 μm, 2.0 x 30 mm
방법 4
출발%B = 0, 최종%B = 100, 2분에 걸친 구배, 100%B에서 유지
유량 = 1 mL / 분
파장 = 220 nm
용매 A = 95% 물, 5% 메탄올, 10 mM 아세트산암모늄
용매 B = 5% 물, 95% 메탄올, 10 mM 아세트산암모늄
칼럼 = 페노메넥스 루나 C18, 3 μm, 2.0 x 30 mm
방법 5
출발%B = 0, 최종%B = 100, 2분에 걸친 구배, 100%B에서 유지
유량 = 1 mL / 분
파장 = 220 nm
용매 A = 90% 물, 10% 메탄올, 0.1% TFA
용매 B = 10% 물, 90% 메탄올, 0.1% TFA
칼럼 = 페노메넥스 루나 C18, 3 μm, 2.0 x 30 mm
방법 6
출발%B = 0, 최종%B = 100, 2분에 걸친 구배, 100%B에서 유지
유량 = 1 mL / 분
파장 = 220 nm
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 아세토니트릴, 90% 물, 0.1% TFA
칼럼 = 페노메넥스 루나 C18, 3 μm, 2.0 x 30 mm
정제용 HPLC 방법:
정제용 HPLC 방법 1
출발 %B = 25 최종 %B = 100, 10분에 걸친 구배, 100%B에서 유지
유량 = 25 mL/분
용매 A = 5% MeOH - 95% H2O - 10 mM 아세트산암모늄
용매 B = 95% MeOH - 5% H2O - 10 mM 아세트산암모늄
칼럼 = 엑스브리지 페닐(XBridge Phenyl) 19x100 mm S5
정제용 HPLC 방법 2
출발%B = 0, 최종%B = 100, 20분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어(Waters Sunfire) C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 3
출발%B = 0, 최종%B = 100, 15분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 4
출발%B = 15, 최종%B = 100, 20분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 5
출발%B = 15, 최종%B = 100, 10분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 6
출발%B = 15, 최종%B = 100, 30분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 7
출발%B = 15, 최종%B = 100, 20분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 95% 물, 5% 아세토니트릴, 10 mM 아세트산암모늄
용매 B = 5% 물, 95% 아세토니트릴, 10 mM 아세트산암모늄
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 8
출발%B = 15, 최종%B = 100, 30분에 걸친 구배, 100%B에서 15분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 9
출발 %B = 25 최종 %B = 100, 10분에 걸친 구배, 100%B에서 유지
용매 A = 5% MeOH - 95% H2O - 10 mM 아세트산암모늄
유량 = 25 mL/분
용매 B = 95% MeOH - 5% H2O - 10 mM 아세트산암모늄
칼럼 = 워터스-선파이어 OBD 19x100 mm S5
정제용 HPLC 방법 10
출발%B = 20, 최종%B = 100, 20분에 걸친 구배, 100%B에서 5분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 11
출발%B = 20, 최종%B = 100, 30분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 12
출발%B = 0, 최종%B = 100, 20분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 95% 물, 5% 아세토니트릴, 10 mM 아세트산암모늄
용매 B = 5% 물, 95% 아세토니트릴, 10 mM 아세트산암모늄
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 13
출발%B = 0, 최종%B = 100, 15분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 95% 물, 5% 아세토니트릴, 10 mM 아세트산암모늄
용매 B = 5% 물, 95% 아세토니트릴, 10 mM 아세트산암모늄
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 14
출발%B = 0, 최종%B = 100, 10분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 15
출발%B = 0, 최종%B = 100, 20분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 엑스브리지 페닐, 5 μm, 30 x 100 mm
정제용 HPLC 방법 16
출발%B = 0, 최종%B = 100, 30분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 17
출발%B = 0, 최종%B = 100, 30분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 95% 물, 5% MeOH, 10 mM 중탄산암모늄
용매 B = 5% 물, 95% MeOH, 10 mM 중탄산암모늄
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 18
출발 %B = 20 최종 %B = 60, 10분에 걸친 구배, 100%B에서 5분 동안 유지
유량 = 20 mL/분
용매 A = 물 - 20 mM 아세트산암모늄
용매 B = 95% 아세토니트릴 - 5% H2O - 20 mM 아세트산암모늄
칼럼 = 엑스브리지 페닐 C18 19 x 200 mm S5
정제용 HPLC 방법 19
출발%B = 0, 최종%B = 100, 40분에 걸친 구배, 100%B에서 4분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 150 mm
정제용 HPLC 방법 20
출발 %B = 30 최종 %B = 100, 15분에 걸친 구배, 100%B에서 유지
유량 = 25 mL/분
용매 A = 5% MeOH - 95% H2O - 10 mM 아세트산암모늄
용매 B = 95% MeOH - 5% H2O - 10 mM 아세트산암모늄
칼럼 = 엑스브리지 페닐 19x100 mm S5
정제용 HPLC 방법 21
출발 %B = 15 최종 %B = 90, 20분에 걸친 구배, 100%B에서 유지
유량 = 40 mL/분
용매 A = 90% 물 - 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물 - 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μM, 30 x 100 mm
정제용 HPLC 방법 22
출발 %B = 25 최종 %B = 90, 15분에 걸친 구배, 100%B에서 유지
유량 = 40 mL/분
용매 A = 90% 물 - 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물 - 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μM, 30 x 100 mm
정제용 HPLC 방법 23
출발%B = 30, 최종%B = 100, 20분에 걸친 구배, 100%B에서 10분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 100 mm
정제용 HPLC 방법 24
출발%B = 30, 최종%B = 100, 12분에 걸친 구배, 100%B에서 8분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 선파이어 C18, 5 μm, 30 x 100 mm
정제용 HPLC 방법 25
출발%B = 20, 최종%B = 100, 15분에 걸친 구배, 100%B에서 5분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 엑스브리지 페닐, 5 μm, 30 x 100 mm
정제용 HPLC 방법 26
출발%B = 20, 최종%B = 100, 10분에 걸친 구배, 100%B에서 15분 동안 유지
유량 = 50 mL / 분
용매 A = 90% 물, 10% 아세토니트릴, 0.1% TFA
용매 B = 10% 물, 90% 아세토니트릴, 0.1% TFA
칼럼 = 워터스 엑스브리지 페닐, 5 μm, 30 x 100 mm
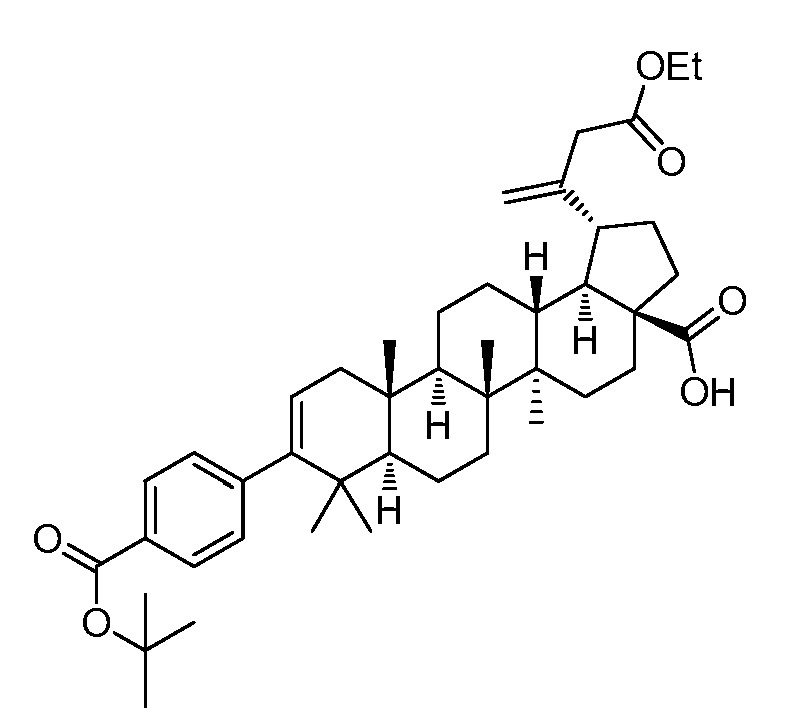
주요 중간체의 제조:
중간체 1-4는 하기 반응식에 제시된 바와 같이 제조할 수 있다:
(1R,3aS,5aR,5bR,7aR,9S,11aR,11bR,13aR,13bR)-벤질 9-히드록시-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조.
DMF (150 mL) 중 베툴린산 (12 g, 26.3 mmol) 및 탄산칼륨 (7.26 g, 52.6 mmol)의 현탁액에 벤질 브로마이드 (3.28 mL, 27.6 mmol)를 첨가하였다. 혼합물을 60℃로 3.5시간 동안 가열한 다음, 이를 실온으로 냉각시켰다. 냉각시 고체가 침전되기 시작하였다. 혼합물을 물 (200 mL)로 희석하고, 형성된 고체를 여과에 의해 수집하여 표제 화합물 (13.92 g, 25.5 mmol, 97% 수율)을 백색 고체로서 수득하였다.
(1R,3aS,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 5a,5b,8,8,11a-펜타메틸-9-옥소-1-(프로프-1-엔-2-일)이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조.
디클로로메탄 (100 mL) 중 (1R,3aS,5aR,5bR,7aR,9S,11aR,11bR,13aR,13bR)-벤질 9-히드록시-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (7.1 g, 12.98 mmol)의 용액에 PCC (4.20 g, 19.48 mmol)를 첨가하였다. 5분 동안 교반한 후, 혼합물은 짙은 진홍색으로 변하였다. 혼합물을 5.5시간 동안 추가로 교반하였다. 혼합물을 셀라이트 및 실리카 겔의 패드를 통해 여과하고, 이를 디클로로메탄으로 세척한 다음, 에틸 아세테이트: 헥산의 1:1 혼합물로 세척하였다. 여과물을 감압 하에 농축시켜 표제 화합물 (6.92 g, 12.7 mmol, 98% 수율)을 백색 발포체로서 수득하였다.
(1R,3aS,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-9-(트리플루오로메틸술포닐옥시)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조. 중간체 1
THF (200 mL) 중 (1R,3aS,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 5a,5b,8,8,11a-펜타메틸-9-옥소-1-(프로프-1-엔-2-일)이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (29.0 g, 53.2 mmol)의 용액을 -78℃로 냉각시켰다. 용액에 KHMDS (톨루엔 중 0.5 M) (213 mL, 106 mmol)를 첨가하였다. 황색 용액을 -78℃에서 25분 동안 교반하고, THF (70 mL) 및 톨루엔 (30 mL) 중 1,1,1-트리플루오로-N-페닐-N-(트리플루오로메틸)술포닐 메탄술폰아미드 (20.92 g, 58.6 mmol)의 용액을 캐뉼라를 통해 첨가하였다. 용액을 -78℃에서 3시간 동안 교반하였다. 이어서, 추가의 1,1,1-트리플루오로-N-페닐-N-(트리플루오로메틸)술포닐 메탄술폰아미드 1.0 g을 첨가하고, 혼합물을 -78℃에서 교반하였다. 1시간 동안 교반한 후, 혼합물을 물 (300 mL)로 켄칭하고, 혼합물을 에틸 아세테이트 (3 x 200 mL)로 추출하였다. 합한 유기 층을 MgSO4로 건조시켰다. 건조제를 여과에 의해 제거하고, 여과물을 감압 하에 농축시켜 표제 화합물 (40.0 g, 59.1 mmol)을 황색 고체로서 수득하였다. 생성물 Rf = 실리카 겔 TLC, 헥산 중 5% EtOAc에 의해 0.57, 하네시안 염색을 사용하여 가시화함.
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조.
디옥산 (25 mL) 중 (1R,3aS,5aR,5bR,7aR,11aR,11bR,13bR)-벤질 5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-9-(트리플루오로메틸술포닐옥시)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (6.21 g, 9.18 mmol)의 용액에 2-프로판올 (25 mL) 및 물 (15 mL)에 이어서 탄산나트륨 1수화물 (3.42 g, 27.5 mmol), 4-메톡시카르보닐페닐보론산 (2.478 g, 13.77 mmol), 및 테트라키스(트리페닐포스핀)팔라듐(0) (0.318 g, 0.275 mmol)을 첨가하였다. 플라스크를 환류 응축기에 부착하고, N2로 플러싱하고, 밤새 환류 가열하였다. 이어서, 혼합물을 실온으로 냉각시키고, 물 (75 mL)로 희석하였다. 혼합물을 에틸 아세테이트 (3 x 75 mL)로 추출하고, 염수 (75 mL)로 세척하였다. 합한 유기 층을 MgSO4로 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 실리카 겔에 흡착시키고, 실리카 겔 플래쉬 크로마토그래피에 의해 헥산 중 0-20% 에틸 아세테이트 구배를 사용하여 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 표제 화합물 (4.16 g, 6.28 mmol, 68.4% 수율)을 백색 발포체로서 수득하였다.
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-tert-부틸디메틸실릴 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조. 중간체 2
디클로로에탄 (100 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (3.82 g, 5.76 mmol)의 용액에 트리에틸아민 (1.285 mL, 9.22 mmol), tert-부틸디메틸실란 (1.912 mL, 11.52 mmol), 및 아세트산팔라듐 (II) (0.647 g, 2.88 mmol)을 첨가하였다. 혼합물을 N2로 플러싱하고, 60℃로 가열하였다. 2시간 후, 반응을 실온으로 냉각시키고, 고체를 제거하기 위해 셀라이트 및 실리카 겔의 패드를 통해 여과하고, 이를 헥산 중 25% EtOAc로 세척하였다. 여과물을 감압 하에 농축시키고, 아세트산 (25 mL), THF (10 mL) 및 물 (3 mL)로 처리하였다. 1시간 동안 교반한 후, 형성된 고체를 여과에 의해 수집하고, 물로 세척하여 표제 화합물 (3.62 g, 5.27 mmol, 91% 수율)을 백색 고체로서 수득하였다.
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조.
디옥산 (25 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR, 13aR,13bR)-tert-부틸디메틸실릴 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (3.12 g, 4.54 mmol)의 용액에 TBAF (물 중 75 중량%) (2.375 g, 6.81 mmol)를 첨가하고, 혼합물을 실온에서 4시간 동안 교반하였다. 반응 혼합물을 1N HCl (25 mL) 및 물 (5 mL)로 희석하고, 디클로로메탄 (3 x 100 mL)으로 추출하였다. 합한 유기 층을 Na2SO4 상에서 건조시키고 여과하고, 감압 하에 약 10 mL 부피로 부분적으로 농축시켰다. 부분적으로 농축된 혼합물에 1N HCl (50 mL)을 첨가하였다. 형성된 고체를 여과에 의해 수집하고, 물로 세척하여 표제 화합물 (2.58 g, 4.50 mmol, 99% 수율)을 백색 고체로서 수득하였다. LCMS: m/e 571.47 (M-H)-, 3.60분 (방법 2).
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-이소시아네이토-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
1,4-디옥산 (200 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (10 g, 17.46 mmol)의 슬러리에 트리에틸아민 (4.38 mL, 31.4 mmol)에 이어서 디페닐 포스포릴 아지드 (5.82 mL, 26.2 mmol)를 첨가하였다. 생성된 백색 슬러리를 100℃로 가열하였다. 5시간 후, 반응물이 실온으로 냉각되도록 한 다음, EtOAc로 희석하고, 1N NaOH (2 x 70 mL)로 세척하였다. 합한 수성 층을 EtOAc (2 x 150 mL)로 추출하였다. 합한 유기 층을 Na2SO4 상에서 건조시키고, 여과하고, 슬러리 (75 mL)로 농축시키고, 이를 냉장고에서 밤새 보관하였다. 슬러리를 여과하고, 백색 고체 생성물을 Et2O로 세척하였다. 액체 여과물을 황색 슬러리로 농축시키고, 이를 여과하고, Et2O로 세척하여 보다 더 백색의 고체 생성물을 수득하였다. 2개의 배치의 백색 고체를 합하고, 진공 하에 건조시켜 표제 화합물 (8.6 g, 15.09 mmol, 86% 수율)을 백색 고체로서 수득하였다.
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조. 중간체 3
THF (100 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-이소시아네이토-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (5.47 g, 9.60 mmol)의 탁한 용액에 진한 염산 (19.83 mL, 240 mmol)을 첨가하였다. 생성된 균질 혼합물을 실온에서 72시간 동안 교반하고, 반응 혼합물을 농축 건조시켜 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트, HCl (4.98 g, 8.58 mmol, 89% 수율)을 백색 고체로서 수득하였다. LCMS: m/e 544.5 (M+H)+, 3.26분 (방법 3).
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도-4-티오모르폴리닐)에틸)아미노)-1-이소프로페닐-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조. 중간체 4
아세토니트릴 (50 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-1-이소프로페닐-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (600 mg, 1.10 mmol), 4-(2-클로로에틸)티오모르폴린 1,1-디옥시드 (600 mg, 2.56 mmol) (WO2002045652에 기재된 바와 같이 제조됨), 무수 인산칼륨 (3.00 g, 14.1mmol) 및 아이오딘화칼륨 (10 mg, 0.060 mmol)의 혼합물을 150 mL 에이스글래스(AceGlass) 재밀봉가능한 압력 용기에 넣었다. 백색 현탁액을 질소로 덮었다. 용기를 밀봉하고, 115-125℃로 48시간 동안 가온하였다. 조 반응물을 실리카 겔의 짧은 베드를 통해 여과하고, 에틸 아세테이트로 세척하였다. 여과물을 진공 하에 농축시키고, 실리카 겔 크로마토그래피에 의해 에틸 아세테이트 및 헥산 (0-50%)으로 용리시키면서 정제하여 표제 화합물을 무색 발포체 (566 mg, 73%)로서 수득하였다.
LCMS: m/e 705.51 (M+H)+, 3.01분 (방법 4).
중간체 5는 하기 반응식에 제시된 바와 같이 제조하였다:
단계 1: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
1,4-디옥산 (100 mL) 중 (1R,3aS,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-9-(트리플루오로메틸술포닐옥시)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (17.2 g, 25.4 mmol)의 현탁액에 2-프로판올 (100 mL), 물 (40 mL), 탄산나트륨, 1수화물 (9.45 g, 76 mmol), 4-tert-부톡시카르보닐페닐보론산 (8.46 g, 38.1 mmol), 및 테트라키스(트리페닐포스핀)팔라듐(0) (0.881 g, 0.762 mmol)을 첨가하였다. 혼합물을 함유하는 플라스크를 환류 응축기에 부착하고, 질소로 플러싱하고, 환류 가열 (90℃ 오일 조 온도)하였다. 가열시, 혼합물 중에 용해된 고체, 및 혼합물이 진홍색이 되었다. 3.5시간 가열한 후, 혼합물을 실온으로 냉각시켰다. 냉각시킨 후, 결정이 형성되었으며, 이를 여과에 의해 수집하고, 물로 세척하였다. 결정을 DCM 및 EtOH 중에 용해시키고, 감압 하에 농축시켰다. 잔류물을 DCM 중에 용해시키고, 셀라이트 및 실리카 겔의 플러그를 통해 통과시켰다. 여과물을 감압 하에 농축시켜 목적 생성물, (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (13.8 g, 19.57 mmol, 77% 수율)를 담회색 발포체로서 수득하였다.
단계 2: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-tert-부틸디메틸실릴 9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조. 중간체 5
DCE (200 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (13.8 g, 19.57 mmol)의 용액에 트리에틸아민 (4.37 mL, 31.3 mmol), tert-부틸디메틸실란 (6.49 mL, 39.1 mmol), 및 아세트산팔라듐 (II) (1.099 g, 4.89 mmol)을 첨가하였다. 혼합물을 질소로 플러싱하고, 60℃로 가열하였다. 3.5시간 가열한 후, 혼합물을 실온으로 냉각시키고, 실리카 겔 및 셀라이트의 패드를 통해 여과하고, 이를 디클로로메탄에 이어서 헥산 중 25% 에틸 아세테이트로 세척하였다. 여과물을 감압 하에 농축시켰다. 혼합물을 물 200 mL로 희석하고, 디클로로메탄 (3 x 200 mL)으로 추출하였다. 합한 유기 층을 황산나트륨으로 건조시키고, 여과하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-tert-부틸디메틸실릴 9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (13.75 g, 18.86 mmol, 96% 수율)를 백색 발포체로서 수득하였다.
중간체 6은 하기 반응식에 제시된 바와 같이 제조하였다:
단계 1. (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(3-플루오로-4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조.
1,4-디옥산 (24 mL) 및 물 (6 mL) 중 (1R,3aS,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-9-(트리플루오로메틸술포닐옥시)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (4.0 g, 5.91 mmol), 3-플루오로-4-(메톡시카르보닐)페닐보론산 (1.287 g, 6.50 mmol), 탄산나트륨 1수화물 (2.198 g, 17.73 mmol), 및 Pd(PPh3)4 (0.205 g, 0.177 mmol)의 현탁액을 N2로 플러싱하고, 혼합물을 환류 가열하였다. 2시간 가열한 후, 혼합물을 실온으로 냉각시켰다. 혼합물을 물 (40 mL)로 희석하고, 디클로로메탄 (3 x 40 mL)으로 추출하였다. 합한 유기 층을 Na2SO4로 건조시켰다. 건조제를 여과에 의해 제거하고, 여과물을 감압 하에 농축시켰다. 잔류물을 DCM 중에 용해시키고, 헥산 중 25% EtOAc 용액으로 세척하면서 셀라이트 및 실리카 겔의 패드를 통해 여과하였다. 여과물을 감압 하에 농축시켜 표제 화합물 (3.59 g, 5.27 mmol, 89% 수율)을 암회색 발포체로서 수득하였다. 조 생성물을 추가 정제 없이 후속 단계에 사용하였다.
단계 2. (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-9-(3-플루오로-4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조.
DCE (25 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(3-플루오로-4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (3.59 g, 5.27 mmol)의 용액에 TEA (1.176 mL, 8.44 mmol), t-부틸디메틸실란 (1.749 mL, 10.54 mmol), 및 아세트산팔라듐 (II) (0.118 g, 0.527 mmol)을 첨가하였다. 혼합물을 N2로 플러싱하고, 60℃로 1시간 동안 가열하였다. 혼합물을 실온으로 냉각시키고, 셀라이트 및 실리카 겔의 플러그를 통해 여과하였다 (헥산 중 25% EtOAc로 세척함). 여과물을 감압 하에 농축시켰다. 잔류물을 디옥산 25 mL로 희석하고, TBAF (물 중 75%) (2.76 g, 7.91 mmol)를 첨가하였다. 혼합물을 실온에서 30분 동안 교반한 다음, 1N HCl 50 mL로 희석하였다. 형성된 고체를 여과에 의해 수집하고, 물로 세척하여 표제 화합물 (2.95 g, 4.99 mmol, 95% 수율)을 백색 고체로서 수득하였다.
단계 3. 메틸 2-플루오로-4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-이소시아네이토-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
톨루엔 (50 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-9-(3-플루오로-4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (2.95 g, 4.99 mmol) 및 TEA (1.39 mL, 9.99 mmol)의 용액에 디페닐 포스포르아지데이트 (1.614 mL, 7.49 mmol)를 첨가하고, 혼합물을 환류 가열하였다. 3시간 후, 반응 혼합물을 감압 하에 농축시키고, 실리카 겔에 흡착시키고, 플래쉬 크로마토그래피에 의해 헥산 중 0-10% EtOAc 구배를 사용하여 정제하여 표제 화합물을 백색 고체로서 수득하였다. 물질을 추가 정제 없이 후속 단계에 사용하였다.
단계 4. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 디히드로클로라이드의 제조. 중간체 6.
THF (35 mL) 중 조 메틸 2-플루오로-4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-이소시아네이토-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (2.93 g, 4.99 mmol)의 용액에 12N HCl (10 mL, 121 mmol)을 첨가하였다. 혼합물을 24시간 동안 교반한 후, 혼합물을 고체가 침전될 때까지 물 (100 mL)로 희석하였다. 고체를 여과에 의해 수집하고, 물로 세척하여 표제 화합물 (2.75 g, 4.33 mmol, 87% 수율)을 회백색 고체로서 수득하였으며, 이를 추가 정제 없이 후속 단계에 사용하였다. LCMS: m/e 562 (M+H)+, 1.96분 (방법 5).
C-30 아민의 제조를 위한 반응식 (실시예 1-6).
실시예 1-6은 중간체 2 또는 5 중 어느 하나로부터 하기 반응식을 따라 제조하였다:
실시예 1
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에틸아미노)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
단계 1: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-tert-부틸디메틸실릴 1-(3-브로모프로프-1-엔-2-일)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
CCl4 (5 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-tert-부틸디메틸실릴 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.315 g, 0.458 mmol)의 용액에 NBS (0.102 g, 0.573 mmol)를 첨가하였다. 혼합물을 실온에서 16시간 동안 교반한 다음, 셀라이트의 패드를 통해 여과하고 (DCM으로 세척함), 여과물을 감압 하에 농축시켰다. 잔류물을 12g 실리카 겔 칼럼 상에 로딩하고, 플래쉬 크로마토그래피에 의해 헥산 중 0-10% 에틸 아세테이트 구배를 사용하여 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-tert-부틸디메틸실릴 1-(3-브로모프로프-1-엔-2-일)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.205 g, 0.268 mmol, 58.4% 수율)를 백색 발포체로서 수득하였다. LCMS: m/e 765, 767.5 (M+H)+, 4.78분 (방법 1).
단계 2: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에틸아미노)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조.
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-tert-부틸디메틸실릴 1-(3-브로모프로프-1-엔-2-일)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (26 mg, 0.034 mmol)를 함유하는 플라스크에 2-모르폴리노에틸아민 (0.056 mL, 0.430 mmol)을 첨가하였다. 형성된 슬러리를 DCE (1 mL) 중에 용해시키고, 실온에서 밤새 교반하였다. 혼합물을 실온에서 18.5시간 교반한 후, 이를 질소의 스트림 하에 농축시키고, 역상 정제용 HPLC (방법 1)에 의해 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에틸아미노)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (17.6 mg, 0.025 mmol, 74.0% 수율)을 백색 발포체로서 수득하였다. LCMS: m/e 701.6 (M+H)+, 2.37분 (방법 1).
단계 3: 보호기 제거
1,4-디옥산 (1 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에틸아미노)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (17.6 mg, 0.025 mmol)의 용액에 1N NaOH (0.126 mL, 0.126 mmol)를 첨가하였다. 혼합물을 75℃로 19.5시간 동안 가열한 다음, 실온으로 냉각시켰다. 혼합물에 1N HCl 5 mL를 첨가하고, 혼합물을 감압 하에 농축시켰다. 잔류물을 정제용 HPLC (방법 1)에 의해 정제하여 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에틸아미노)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (6.4 mg, 9.32 μmol, 37.1% 수율)을 회백색 고체로서 수득하였다. LCMS: m/e 687.5 (M+H)+, 1.99분 (방법 1).
실시예 2
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-1-(3-(2-히드록시에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
단계 1: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-tert-부틸디메틸실릴 1-(3-브로모프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
CCl4 (10 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-tert-부틸디메틸실릴 9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (2.0 g, 2.74 mmol)의 용액에 NBS (0.57 g, 3.20 mmol)를 1시간에 걸쳐 조금씩 첨가하였다. 혼합물을 실온에서 6시간 동안 교반하였다. 혼합물을 셀라이트의 패드를 통해 여과하고 (DCM으로 세척함), 감압 하에 농축시켰다. 잔류물을 90g 실리카 겔 칼럼 상에 로딩하고, 플래쉬 크로마토그래피에 의해 헥산 중 0-10% 에틸 아세테이트 구배를 사용하여 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 표제 화합물 (1.29 g, 1.60 mmol, 58.4% 수율)을 백색 발포체로서 수득하였다. LCMS: m/e 807, 809.4 (M+H)+, 6.31분 (방법 1).
단계 2: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(2-히드록시에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
DCE (2 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-tert-부틸디메틸실릴 1-(3-브로모프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.125 g, 0.155 mmol)의 용액에 에탄올아민 (0.093 mL, 1.547 mmol)을 첨가하였다. 혼합물을 실온에서 20.5시간 동안 교반한 다음, 감압 하에 농축시키고, 정제용 HPLC (방법 1)에 의해 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 표제 화합물 (56 mg, 0.083 mmol, 53.7% 수율)을 백색 발포체로서 수득하였다. LCMS: m/e 674.4 (M+H)+, 2.45분 (방법 1).
단계 3: 보호기의 제거
DCM (0.5 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(2-히드록시에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (0.025 g, 0.037 mmol)의 용액에 TFA (0.1 mL, 1.298 mmol)를 첨가하였다. 혼합물을 실온에서 16.25시간 동안 교반한 다음, 질소의 스트림 하에 농축시켰다. 잔류물을 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-1-(3-(2-히드록시에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (8.0 mg, 0.013 mmol, 34.9% 수율)을 백색 고체로서 수득하였다. LCMS: m/e 618.3 (M+H)+, 2.00분 (방법 1).
실시예 3
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-1-(3-(디메틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
단계 2: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(디메틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
DCE (1 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-tert-부틸디메틸실릴 1-(3-브로모프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.125 g, 0.155 mmol)의 용액에 디메틸아민 (THF 중 2M) (0.773 mL, 1.547 mmol)을 첨가하였다. 혼합물을 실온에서 21시간 교반한 후, 이를 감압 하에 농축시키고, 정제용 HPLC (방법 1)에 의해 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(디메틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (74 mg, 0.112 mmol, 72.7% 수율)을 백색 발포체로서 수득하였다. LCMS: m/e 658.6 (M+H)+, 2.75분 (방법 1).
단계 3: DCM (0.5 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(디메틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (25 mg, 0.038 mmol)의 용액에 TFA (0.1 mL, 1.298 mmol)를 첨가하였다. 혼합물을 실온에서 16.5시간 동안 교반한 다음, 질소의 스트림 하에 농축시켰다. 잔류물을 메탄올 및 디옥산 중에 용해시키고, 정제용 HPLC에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-1-(3-(디메틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (5.8 mg, 9.64 μmol, 25.4% 수율)을 백색 고체로서 수득하였다. LCMS: m/e 602.4 (M+H)+, 2.05분 (방법 1).
실시예 4
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
단계 2: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
DCE (2 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-tert-부틸디메틸실릴 1-(3-브로모프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.125 g, 0.155 mmol)의 용액에 N,N,N'-트리메틸에틸렌디아민 (0.201 mL, 1.547 mmol)을 첨가하였다. 혼합물을 실온에서 20시간 동안 교반한 다음, 감압 하에 농축시키고, 정제용 HPLC (방법 1)에 의해 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (64 mg, 0.090 mmol, 57.9% 수율)을 백색 발포체로서 수득하였다. LCMS: m/e 713.5 (M-H)-, 2.76분 (방법 1).
단계 3: DCM (0.5 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (0.025 g, 0.035 mmol)의 용액에 TFA (0.1 mL, 1.298 mmol)를 첨가하였다. 혼합물을 실온에서 16.5시간 동안 교반한 다음, 질소의 스트림 하에 농축시켰다. 잔류물을 메탄올 및 디옥산 중에 용해시키고, 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (17.8 mg, 0.027 mmol, 77% 수율)을 백색 고체로서 수득하였다. LCMS: m/e 657.4 (M-H)-, 2.16분 (방법 1).
실시예 5
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-1-(3-(2-(디메틸아미노)에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
단계 2: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(2-(디메틸아미노)에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
DCE (2 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-tert-부틸디메틸실릴 1-(3-브로모프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.125 g, 0.155 mmol)의 용액에 N,N-디메틸에틸렌디아민을 첨가하였다. 혼합물을 실온에서 21시간 동안 교반한 다음, 감압 하에 농축시키고, 정제용 HPLC (방법 1)에 의해 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(2-(디메틸아미노)에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (78 mg, 0.111 mmol, 71.9% 수율)을 백색 발포체로서 수득하였다. LCMS: m/e 699.5 (M-H)-, 2.53분 (방법 1).
단계 3: DCM (0.5 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(2-(디메틸아미노)에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (25 mg, 0.036 mmol)의 용액에 TFA (0.1 mL, 1.298 mmol)를 첨가하였다. 혼합물을 실온에서 15.5시간 동안 교반한 다음, 질소의 스트림 하에 농축시키고, 잔류물을 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켰다. 생성물, (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-1-(3-(2-(디메틸아미노)에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (4.7 mg, 7.29 μmol, 20% 수율)을 백색 고체로서 단리시켰다. LCMS: m/e 643.4 (M-H)-, 2.08분 (방법 1).
실시예 6
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-(2-카르복시에틸아미노)프로프-1-엔-2-일)-9-(4-카르복시페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
단계 2: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(3-에톡시-3-옥소프로필아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
DCE (2 mL) 및 트리에틸아민 (0.216 mL, 1.547 mmol) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-tert-부틸디메틸실릴 1-(3-브로모프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.125 g, 0.155 mmol)의 용액에 베타-알라닌, 에틸 에스테르 히드로클로라이드 (0.238 g, 1.547 mmol)를 첨가하였다. 혼합물을 실온에서 22시간 동안 교반한 다음, 40℃로 가온하고, 추가로 6시간 동안 교반하였다. 혼합물을 실온으로 냉각시키고, 실온에서 90시간 동안 교반한 다음, 감압 하에 농축시켰다. 잔류물을 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(3-에톡시-3-옥소프로필아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (73 mg, 0.100 mmol, 64.6% 수율)을 회백색 고체로서 수득하였다. LCMS: m/e 728.5 (M-H)-, 2.57분 (방법 1).
단계 3: DCM (0.5 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(3-에톡시-3-옥소프로필아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (0.035 g, 0.048 mmol)의 용액에 TFA (0.1 mL, 1.298 mmol)를 첨가하였다. 혼합물을 실온에서 21.5시간 동안 교반한 다음, 용매를 질소의 스트림 하에 제거하였다. 조 생성물을 디옥산 0.5 mL 중에 용해시키고, 1N NaOH 0.4 mL를 혼합물에 첨가하였다. 이를 75℃로 18.25시간 동안 가온한 다음, 실온으로 냉각시켰다. 혼합물을 메탄올 1 mL로 희석하고, 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-(2-카르복시에틸아미노)프로프-1-엔-2-일)-9-(4-카르복시페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (11 mg, 0.017 mmol, 35.5% 수율)을 백색 고체로서 수득하였다. LCMS: m/e 644.4 (M-H)-, 1.91분 (방법 1).
실시예 7
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(디메틸아미노)에틸카르바모일)-1-(3-(디메틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조
단계 1: tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(디메틸아미노)에틸카르바모일)-1-(3-(디메틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(디메틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (50 mg, 0.076 mmol)을 함유하는 바이알에 옥살릴 클로라이드 (DCM 중 2M) (2 mL, 4.00 mmol)를 첨가하였다. 혼합물을 실온에서 2시간 동안 교반한 다음, 감압 하에 농축시켰다. 잔류물을 DCM 중에 용해시키고, 감압 하에 추가로 2회 농축시켰다. 조 생성물을 DCE (2 mL) 및 DIEA (0.066 mL, 0.380 mmol)로 희석하고, N,N-디메틸에틸렌디아민 (0.022 mL, 0.204 mmol), 및 DMAP (1 mg, 8.19 μmol)를 첨가하였다. 혼합물을 실온에서 18.5시간 동안 교반한 다음, 감압 하에 농축시켰다. 조 생성물을 추가 정제 없이 후속 단계에 사용하였다. LCMS: m/e 726.6 (M-H)-, 2.87분 (방법 1).
단계 2: DCM (1 mL) 중 tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(디메틸아미노)에틸카르바모일)-1-(3-(디메틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (55.3 mg, 0.076 mmol)의 용액에 TFA (0.1 mL, 1.298 mmol)를 첨가하였다. 혼합물을 실온에서 15시간 동안 교반한 다음, 질소의 스트림 하에 농축시키고, 잔류물을 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켰다. 목적 생성물, 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(디메틸아미노)에틸카르바모일)-1-(3-(디메틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (24.8 mg, 0.037 mmol, 48.6% 수율)을 백색 고체로서 단리시켰다. LCMS: m/e 672.4 (M+H)+, 2.10분 (방법 1).
실시예 8
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-3a-(2-(디메틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조
단계 1: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
DCE (2 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-tert-부틸디메틸실릴 1-(3-브로모프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.125 g, 0.155 mmol)의 용액에 N,N,N'-트리메틸에틸렌디아민 (0.201 mL, 1.547 mmol)을 첨가하였다. 혼합물을 실온에서 20시간 동안 교반한 다음, 감압 하에 농축시키고, 정제용 HPLC (방법 1)에 의해 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (64 mg, 0.090 mmol, 57.9% 수율)을 백색 발포체로서 수득하였다. LCMS: m/e 713.5 (M-H)-, 2.76분 (방법 1).
단계 2: tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-3a-(2-(디메틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (0.037 g, 0.052 mmol)을 함유하는 바이알에 옥살릴 클로라이드 (DCM 중 2M) (2 mL, 4.00 mmol)를 첨가하였다. 혼합물을 실온에서 2.5시간 동안 교반하고, 감압 하에 농축시켰다. 잔류물을 DCM 중에 용해시키고 추가로 2회 농축시켰다. 조 잔류물을 DCE (2 mL) 및 DIEA (0.045 mL, 0.259 mmol)로 희석하였다. N,N-디메틸아미노에틸아민 (0.011 mL, 0.103 mmol) 및 DMAP (1 mg, 8.19 μmol)를 첨가하고, 혼합물을 18.5시간 동안 교반한 다음, 감압 하에 농축시켜 조 생성물을 수득하였으며, 이를 추가 정제 없이 후속 단계에 직접 사용하였다. LCMS: m/e 786.65 (M+H)+, 2.77분 (방법 1).
단계 3: DCM (1 mL) 중 tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-3a-(2-(디메틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (40.8 mg, 0.052 mmol)의 용액에 TFA (0.1 mL, 1.298 mmol)를 첨가하였다. 혼합물을 실온에서 15시간 동안 교반한 다음, 질소의 스트림 하에 농축시키고, 잔류물을 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-((2-(디메틸아미노)에틸)(메틸)아미노)프로프-1-엔-2-일)-3a-(2-(디메틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (27 mg, 0.037 mmol, 71.2% 수율)을 백색 고체로서 수득하였다. LCMS: m/e 729.64 (M+H)+, 2.14분 (방법 1).
실시예 9
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-카르복시에틸카르바모일)-1-(3-(2-(디메틸아미노)에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조
단계 1: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-(tert-부톡시카르보닐(2-(디메틸아미노)에틸)아미노)프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
1,4-디옥산 (2 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(2-(디메틸아미노)에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (45 mg, 0.064 mmol)의 용액에 수산화나트륨 (1N) (0.25 mL, 0.250 mmol) 및 Boc2O (0.030 mL, 0.128 mmol)를 첨가하였다. 혼합물을 실온에서 17.5시간 동안 교반한 다음, 물 (4 mL)로 희석하고, 디클로로메탄 (3 x 5 mL)으로 추출하였다. 합한 유기 층을 황산나트륨으로 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 1,4-디옥산 (1 mL) 중에 용해시키고, 1N 수산화나트륨 (0.2 mL, 0.2 mmol)으로 처리하였다. 혼합물을 97시간 동안 교반한 다음, 메탄올로 희석하고, 정제용 HPLC에 의해 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-(tert-부톡시카르보닐(2-(디메틸아미노)에틸)아미노)프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산을 백색 고체로서 수득하였다. LCMS: m/e 799.6 (M-H)-, 2.76분 (방법 1).
단계 2: tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-(tert-부톡시카르보닐(2-(디메틸아미노)에틸)아미노)프로프-1-엔-2-일)-3a-(3-에톡시-3-옥소프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-(tert-부톡시카르보닐(2-(디메틸아미노)에틸)아미노)프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (26 mg, 0.024 mmol)을 함유하는 플라스크에 옥살릴 클로라이드 (DCM 중 2M) (1 mL, 2.000 mmol)를 첨가하였다. 혼합물을 실온에서 2시간 동안 교반한 다음, 감압 하에 농축시켰다. 잔류물을 DCM 중에 용해시키고, 추가로 2회 농축시켰다. 조 생성물을 DCE (1 mL) 및 DIEA (0.021 mL, 0.122 mmol), 베타-알라닌, 에틸 에스테르 히드로클로라이드 (7.48 mg, 0.049 mmol) 중에 용해시키고, DMAP (0.5 mg, 4.09 μmol)를 첨가하였다. 혼합물을 실온에서 2.5시간 동안 교반한 다음, 반응물을 물 (5 mL)로 켄칭하고, 디클로로메탄 (3 x 5 mL)으로 추출하였다. 합한 유기 층을 황산나트륨으로 건조시키고, 여과하고, 감압 하에 농축시켜 조 생성물을 수득하였으며, 이를 추가 정제 없이 후속 단계에 사용하였다. LCMS: m/e 898.7 (M-H)-, 2.75분 (방법 1).
단계 3: 3-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-(tert-부톡시카르보닐(2-(디메틸아미노)에틸)아미노)프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복스아미도)프로판산의 제조
1,4-디옥산 (1 mL) 중 tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-(tert-부톡시카르보닐(2-(디메틸아미노)에틸)아미노)프로프-1-엔-2-일)-3a-(3-에톡시-3-옥소프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.022 g, 0.024 mmol)의 용액에 NaOH (1N) (0.120 mL, 0.120 mmol)를 첨가하였다. 혼합물을 75℃로 87시간 동안 가열한 다음, 실온으로 냉각시키고, 감압 하에 농축시켰다. 조 생성물을 추가 정제 없이 후속 단계에 사용하였다. LCMS: m/e 870.6 (M-H)-, 2.46분 (방법 1).
단계 4: BOC 탈보호: 디클로로메탄 (2 mL) 중 3-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-(tert-부톡시카르보닐(2-(디메틸아미노)에틸)아미노)프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복스아미도)프로판산 (20.93 mg, 0.024 mmol)의 용액에 TFA (0.25 mL, 3.24 mmol)를 첨가하였다. 혼합물을 실온에서 16.5시간 동안 교반한 다음, 질소의 스트림 하에 농축시켰다. 잔류물을 디옥산 및 메탄올 중에 용해시키고, 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켰다. 불순물을 함유하는 잔류물을 정제용 HPLC (방법 9)에 의해 재정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-카르복시에틸카르바모일)-1-(3-(2-(디메틸아미노)에틸아미노)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (6.2 mg, 8.66 μmol, 4 단계에 걸쳐 13.5% 수율)을 백색 고체로서 수득하였다. LCMS: m/e 714.5 (M-H)-, 1.93분 (방법 1).
실시예 10
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-(3-카르복시-N-메틸프로판아미도)프로프-1-엔-2-일)-3a-(2-카르복시에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(메틸아미노)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
DCE (1 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-tert-부틸디메틸실릴 1-(3-브로모프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.125 g, 0.155 mmol)의 용액에 메틸아민 (THF 중 2M) (0.773 mL, 1.547 mmol)을 첨가하였다. 혼합물을 실온에서 20시간 동안 교반한 다음, 추가의 메틸아민 (THF 중 2M) 0.8 mL를 첨가하고, 혼합물을 실온에서 1시간 동안 교반한 다음, 40℃로 가온하고, 추가로 8시간 동안 교반하였다. 혼합물을 감압 하에 농축시키고, 생성물을 메탄올, 1,4-디옥산, 및 물의 용액으로부터 결정화하여 조 생성물을 회백색 고체 (85 mg, 0.132 mmol, 85% 수율)로서 수득하였다. LC/MS: m/e 644.4 (M+H)+, 2.44분 (방법 1).
단계 2: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(4-메톡시-N-메틸-4-옥소부탄아미도)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
DCE (2 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(메틸아미노)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (0.04 g, 0.062 mmol)의 용액에 DIEA (0.054 mL, 0.311 mmol), 메틸 4-클로로-4-옥소부티레이트 (0.038 mL, 0.311 mmol), 및 DMAP (1 mg, 8.19 μmol)를 첨가하였다. 혼합물을 실온에서 3시간 동안 교반한 다음, 물 2 mL 및 1N HCl 6 mL로 희석하고, 디클로로메탄 (3 x 7 mL)으로 추출하였다. 합한 유기 층을 황산나트륨으로 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 플래쉬 크로마토그래피에 의해, 혼합물에 첨가된 0.1% 아세트산을 함유하는 헥산 중 0-100% 에틸 아세테이트 구배를 사용하여 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 목적 생성물을 백색 고체 (0.047g, 0.062 mmol, 50% 수율)로서 수득하였다. LC/MS: m/e 758.4 (M+H)+, 2.57분 (방법 1).
단계 3: tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-에톡시-3-옥소프로필카르바모일)-1-(3-(4-메톡시-N-메틸-4-옥소부탄아미도)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(4-메톡시-N-메틸-4-옥소부탄아미도)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (0.047 g, 0.062 mmol)을 함유하는 바이알에 옥살릴 클로라이드 (디클로로메탄 중 2M) (1 mL, 2.0 mmol)를 첨가하였다. 용액을 실온에서 2시간 동안 교반한 다음, 감압 하에 농축시켰다. 잔류물을 디클로로메탄 중에 용해시키고, 추가로 2회 농축시킨 다음, 하우스 진공 하에 1시간 동안 건조시켰다. 잔류물을 DCE (1 mL) 중에 용해시키고, 휘니그의 염기 (0.032 mL, 0.186 mmol)를 첨가하고, 이어서 베타-알라닌, 에틸 에스테르 히드로클로라이드 (0.014 g, 0.093 mmol)를 첨가하였다. 혼합물을 실온에서 17시간 동안 교반한 다음, 질소의 스트림 하에 농축시키고, 플래쉬 크로마토그래피에 의해 헥산 중 0-50% 에틸 아세테이트 구배 및 12g 실리카 겔 칼럼을 사용하여 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켰다. 목적 생성물을 백색 고체 (15 mg, 0.017 mmol, 28% 수율)로서 단리시켰다. LC/MS: m/e 857.5 (M+H)+, 2.57분 (방법 1).
단계 4: 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-에톡시-3-옥소프로필카르바모일)-1-(3-(4-메톡시-N-메틸-4-옥소부탄아미도)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
디클로로메탄 (1 mL) 중 tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-에톡시-3-옥소프로필카르바모일)-1-(3-(4-메톡시-N-메틸-4-옥소부탄아미도)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.015 g, 0.017 mmol)의 용액에 TFA (0.05 mL, 0.649 mmol)를 첨가하였다. 혼합물을 실온에서 23시간 동안 교반한 다음, 감압 하에 농축시키고, 추가 정제 없이 후속 단계에 사용하였다. LC/MS: m/e 801.4 (M+H)+, 2.11분 (방법 1).
단계 5: 1,4-디옥산 (1 mL) 중 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-에톡시-3-옥소프로필카르바모일)-1-(3-(4-메톡시-N-메틸-4-옥소부탄아미도)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (0.017 mmol)의 용액에 수산화나트륨 (1N) (0.1 mL, 0.100 mmol)을 첨가하였다. 혼합물을 75℃로 72시간 동안 가열한 다음, 정제용 HPLC에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켰다. 잔류물을 아세트산 중에 용해시키고, 감압 하에 농축시켜 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(3-(3-카르복시-N-메틸프로판아미도)프로프-1-엔-2-일)-3a-(2-카르복시에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (3.0 mg, 0.0037 mmol, 22% 수율)을 투명한 무색 필름으로서 수득하였다. LC/MS: m/e 759.4 (M+H)+, 1.74분 (방법 1).
실시예 11
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
단계 1: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-벤질 1-(3-브로모프로프-1-엔-2-일)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
사염화탄소 (25 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (3.25 g, 4.90 mmol)의 용액에 N-브로모숙신이미드 (1.00 g, 5.62 mmol)를 첨가하였다. 혼합물을 실온에서 1시간 동안 교반하고, 추가로 N-브로모숙신이미드 0.25g을 첨가하였다. 혼합물을 실온에서 18시간 동안 교반한 후, 이를 셀라이트의 패드를 통해 여과하고 (DCM으로 세척함), 여과물을 감압 하에 농축시켰다. 잔류물을 플래쉬 크로마토그래피에 의해 160 실리카 겔 칼럼 및 헥산 중 0-10% 에틸 아세테이트 구배를 사용하여 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 목적 생성물 1.44g을 백색 고체로서 수득하였다. 보다 덜 순수한 여러 분획을 합하고, 농축시키고, 플래쉬 크로마토그래피 (헥산 중 0-5% 에틸 아세테이트, 90g 실리카 겔 칼럼)에 의해 재정제하였다. 단리물을 합하여 생성물 (2.1 g, 2.83 mmol, 57.7% 수율)을 백색 고체로서 수득하였다. LC/MS: m/e 741, 743.2 (M+H)+, 4.13분 (방법 1).
단계 2: 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(벤질옥시카르보닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조
1,4-디옥산 (3 mL) 중 NaH (60% 미네랄 오일 분산액) (0.135 g, 3.37 mmol)의 현탁액에 4-(2-히드록시에틸)모르폴린 (0.204 mL, 1.685 mmol) 및 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-벤질 1-(3-브로모프로프-1-엔-2-일)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.25 g, 0.337 mmol)를 첨가하였다. 혼합물을 실온에서 교반한 다음, 50℃로 20시간 동안 가열하였다. 반응물을 실온으로 냉각시키고, 물 (10 mL)로 켄칭한 다음, 디클로로메탄 (3 x 20 mL)으로 추출하였다. 합한 유기 층을 황산나트륨으로 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 플래쉬 크로마토그래피에 의해 디클로로메탄 중 0-10% MeOH 구배 및 12g 실리카 겔 칼럼을 사용하여 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 표제 화합물 (0.133 g, 0.171 mmol, 50.7% 수율)을 백색 발포체로서 수득하였다. LC/MS: m/e 778.4 (M+H)+, 2.44분 (방법 1).
단계 3: DCE (2 mL) 중 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(벤질옥시카르보닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (0.078 g, 0.00 μmol)의 용액에 트리에틸아민 (0.022 mL, 0.160 mmol), tert-부틸디메틸실란 (0.033 mL, 0.200 mmol), 및 아세트산팔라듐 (II) (0.011 g, 0.050 mmol)을 첨가하였다. 혼합물을 질소로 플러싱하고, 60℃로 5.5시간 동안 가열한 다음, 실온으로 냉각시키고, 밤새 교반하였다. 혼합물을 셀라이트의 패드를 통해 여과하여 고체를 제거하고 (디클로로메탄으로 세척함), 여과물을 감압 하에 농축시켰다. 잔류물을 THF (2 mL) 중에 용해시키고, 테트라부틸암모늄 플루오라이드 수화물 (0.042 g, 0.150 mmol)로 처리하였다. 1.25시간 후, 혼합물을 물 (5 mL)로 희석하고, 디클로로메탄 (3 x 7 mL)으로 추출하였다. 합한 유기 층을 황산나트륨으로 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 고온의 디옥산 및 물로부터 결정화하여 정제하였다. 냉각시 형성된 고체를 여과에 의해 수집하고, 물로 세척하였다. 수집된 고체를 고온의 에탄올, 디옥산으로부터 재결정화하고, 물을 천천히 첨가하였다. 형성된 고체를 여과에 의해 수집하고, 에탄올로 세척하여 생성물 (10 mg, 0.0145 mmol, 14.5% 수율)을 회백색 고체로서 수득하였다. LC/MS: m/e 688.4 (M+H)+, 2.18분 (방법 1).
실시예 12
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-카르복시에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조
단계 1: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-벤질 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
톨루엔 (3 mL) 및 메탄올 (0.75 mL) 중 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(벤질옥시카르보닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (0.38 g, 0.488 mmol)의 탁한 용액을 0℃로 냉각시키고, TMS-디아조메탄 (헥산 중 2M) (0.317 mL, 0.635 mmol)을 적가하였다. 용액을 5분 동안 격렬히 버블링한 다음, 버블링을 중지하였다. 혼합물을 실온으로 가온하고, 교반하였다. 4시간 동안 교반한 후, 추가의 2N TMS-디아조메탄 용액 0.1 mL를 첨가하고, 혼합물을 실온에서 1시간 동안 교반하였다. 혼합물을 에틸 아세테이트 20 mL로 희석하고, 포화 중탄산나트륨에 이어서 포화 염화나트륨으로 세척하였다. 유기 층을 황산나트륨으로 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 플래쉬 크로마토그래피에 의해 디클로로메탄 중 0-5% MeOH 구배 및 25g 실리카 겔 칼럼을 사용하는 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (0.295 g, 0.350 mmol, 71.7% 수율)을 백색 발포체로서 수득하였다. LC/MS: m/e 792.4 (M+H)+, 3.51분 (방법 1).
단계 2: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
DCE (3.5 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-벤질 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.288 g, 0.364 mmol)의 용액에 TEA (0.081 mL, 0.582 mmol), tert-부틸디메틸실란 (0.121 mL, 0.727 mmol), 및 아세트산팔라듐 (0.020 g, 0.091 mmol)을 첨가하였다. 혼합물을 N2로 플러싱하고, 60℃로 가열하였다. 2.5시간 후, 혼합물을 실온으로 냉각시키고, 셀라이트의 패드를 통해 여과하여 고체를 제거한 다음, 감압 하에 농축시켰다. 잔류물을 THF 5 mL로 희석하고, 탁한 용액에 테트라부틸암모늄 플루오라이드 수화물 (0.152 g, 0.545 mmol)을 첨가하였다. 혼합물을 실온에서 2시간 동안 교반하고, 물 (15 mL)로 희석하고, 에틸 아세테이트 (3 x 15 mL)로 추출하였다. 합한 유기 층을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 플래쉬 크로마토그래피에 의해 디클로로메탄 중 0-5% 메탄올 구배 및 25g 실리카 겔 칼럼을 사용하여 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (0.188 g, 0.268 mmol, 73.7% 수율)을 백색 고체로서 수득하였다. LC/MS: m/e 702.4 (M+H)+, 2.66분 (방법 1).
단계 3: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-에톡시-3-옥소프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (0.188 g, 0.268 mmol)을 함유하는 플라스크에 옥살릴 클로라이드 (DCM 중 2M) (3 mL, 6.00 mmol)를 첨가하였다. 용액 (옥살릴 클로라이드의 첨가시 수분 동안 버블링함)을 실온에서 2시간 동안 교반한 다음, 감압 하에 농축시켰다. 잔류물을 DCM 중에 용해시키고, 추가로 2회 농축시켜 임의의 잔류 옥살릴 클로라이드를 제거하였다. 조 산 클로라이드 생성물을 추가 정제 없이 후속 단계에 사용하였다.
DCE (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(클로로카르보닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (32.2 mg, 0.0447 mmol)의 현탁액에 베타-알라닌, 에틸 에스테르 히드로클로라이드 (10.30 mg, 0.067 mmol) 및 디이소프로필에틸아민 (0.023 mL, 0.134 mmol)을 첨가하였다. 혼합물을 실온에서 5시간 동안 교반한 다음, 플래쉬 크로마토그래피에 의해, 혼합물에 첨가된 0.1% 아세트산암모늄을 함유하는 DCM 중 0-5% MeOH 구배를 사용하여 직접 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (32 mg, 0.040 mmol, 89% 수율)을 백색 발포체로서 수득하였다. LC/MS: m/e 801.4 (M+H)+, 2.66분 (방법 1).
단계 4: 1,4-디옥산 (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-에톡시-3-옥소프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.032 g, 0.040 mmol)의 용액에 NaOH (1N) (0.199 mL, 0.199 mmol)를 첨가하였다. 혼합물을 75℃로 15시간 동안 가열한 다음, 실온으로 냉각시키고, 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (18 mg, 0.024 mmol, 59.6% 수율)을 백색 고체로서 수득하였다. LC/MS: m/e 759.4 (M+H)+, 1.99분 (방법 1).
실시예 13-17
C-30 에틸 모르폴리노 에테르를 함유하는 C-28 아미드의 제조를 위한 반응식
실시예 13
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(2-히드록시에틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조
단계 1: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(2-히드록시에틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
DCE (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(클로로카르보닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (32.2 mg, 0.0447 mmol) (메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-에톡시-3-옥소프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조에 상기 기재된 합성)의 현탁액에 2-(2-아미노에틸아미노)에탄올 (16 μL, 0.158 mmol)을 첨가하였다. 혼합물을 실온에서 밤새 교반하였다. 16시간 교반한 후, 혼합물에 디이소프로필에틸아민 (0.023 mL, 0.134 mmol)을 첨가하였다. 혼합물을 실온에서 1시간 동안 교반한 다음, 플래쉬 크로마토그래피에 의해, 혼합물에 첨가된 0.1% 수산화암모늄을 함유하는 디클로로메탄 중 0-10% 메탄올 구배를 사용하여 직접 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (19 mg, 0.024 mmol, 53.9% 수율)을 백색 발포체로서 수득하였다. LC/MS: m/e 788.4 (M+H)+, 2.52분 (방법 1).
단계 2: 1,4-디옥산 (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(2-히드록시에틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.019 g, 0.024 mmol)의 용액에 1N NaOH (0.121 mL, 0.121 mmol)를 첨가하였다. 혼합물을 75℃로 23시간 동안 가열한 다음, 실온으로 냉각시키고, 추가로 63시간 동안 교반하였다. 반응물에 추가의 1N NaOH 0.1 mL를 첨가하고, 혼합물을 75℃로 23시간 동안 가열한 다음, 실온으로 냉각시키고, 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (15 mg, 0.019 mmol, 80% 수율)을 백색 고체로서 수득하였다. LC/MS: m/e 774.6 (M+H)+, 2.07분 (방법 1).
실시예 14
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(디메틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(디메틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
DCE (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(클로로카르보닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (40 mg, 0.056 mmol) (메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-에톡시-3-옥소프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조에 상기 기재된 합성)의 현탁액에 N,N-디메틸아미노에틸아민 (7.34 mg, 0.083 mmol)을 첨가하였다. 혼합물을 실온에서 16시간 동안 교반한 다음, 혼합물에 디이소프로필에틸아민 (0.023 mL, 0.134 mmol)을 첨가하였다. 이를 실온에서 추가로 2시간 동안 교반한 다음, 플래쉬 크로마토그래피에 의해, 혼합물에 첨가된 0.1% 수산화암모늄을 함유하는 DCM 중 0-10% MeOH 구배 및 12g 실리카 겔 칼럼을 사용하여 직접 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 목적 생성물 (38.4 mg, 0.050 mmol, 90% 수율)을 백색 발포체로서 수득하였다. LC/MS: m/e 772.5 (M+H)+, 2.68분 (방법 1).
단계 2: 1,4-디옥산 (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(디메틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (38.4 mg, 0.050 mmol)의 용액에 1N NaOH (0.249 mL, 0.249 mmol)를 첨가하였다. 혼합물을 75℃로 15시간 동안 가열한 다음, 정제용 HPLC (방법 1)에 의해 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (14 mg, 0.018 mmol, 37% 수율)을 백색 고체로서 수득하였다. LC/MS: m/e 758.6 (M+H)+, 2.14분 (방법 1).
실시예 15
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-3a-(3-(2-옥소피롤리딘-1-일)프로필카르바모일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조
단계 1: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-3a-(3-(2-옥소피롤리딘-1-일)프로필카르바모일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
DCE (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(클로로카르보닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (32.2 mg, 0.0447 mmol) 메틸 (4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-에톡시-3-옥소프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조에 상기 기재된 합성)의 현탁액에 1-(3-아미노프로필)-2-피롤리디논 (9.40 μL, 0.067 mmol)을 첨가하였다. 혼합물을 실온에서 16시간 동안 교반한 다음, 디이소프로필에틸아민 (0.023 mL, 0.134 mmol)을 혼합물에 첨가하고, 이를 실온에서 추가로 1시간 동안 교반하였다. 혼합물을 플래쉬 크로마토그래피에 의해, 혼합물에 첨가된 0.1% 아세트산암모늄을 함유하는 디클로로메탄 중 0-5% 메탄올 구배 및 12g 실리카 겔 칼럼을 사용하여 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (36.4 mg, 0.044 mmol, 99% 수율)을 백색 발포체로서 수득하였다. LC/MS: m/e 826.5 (M+H)+, 2.59분 (방법 1).
단계 2: 1,4-디옥산 (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-3a-(3-(2-옥소피롤리딘-1-일)프로필카르바모일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.0364 g, 0.044 mmol)의 용액에 1N NaOH (0.220 mL, 0.220 mmol)를 첨가하였다. 혼합물을 75℃로 15시간 동안 가열한 다음, 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (31 mg, 0.035 mmol, 81% 수율)을 백색 고체로서 수득하였다. LC/MS: m/e 812.5 (M+H)+, 2.11분 (방법 1).
실시예 16
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-(1H-이미다졸-1-일)프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-(1H-이미다졸-1-일)프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
DCE (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(클로로카르보닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (25 mg, 0.035 mmol) (메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-에톡시-3-옥소프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조에 상기 기재된 합성)의 현탁액에 1-(3-아미노프로필)이미다졸 (8 μL, 0.067 mmol)을 첨가하였다. 혼합물을 실온에서 16시간 동안 교반한 다음, 디이소프로필에틸아민 (0.023 mL, 0.132 mmol)을 첨가하였다. 혼합물을 실온에서 30분 동안 교반한 다음, 플래쉬 크로마토그래피에 의해, 첨가된 0.1% 수산화암모늄을 함유하는 디클로로메탄 중 0-5% 메탄올 구배 및 12g 실리카 겔 칼럼을 사용하여 직접 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (10.8 mg, 0.013 mmol, 38.5% 수율)을 백색 발포체로서 수득하였다. LC/MS: m/e 809.4 (M+H)+, 2.55분 (방법 1).
단계 2: 1,4-디옥산 (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-(1H-이미다졸-1-일)프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.0108 g, 0.013 mmol)의 용액에 1N NaOH (0.067 mL, 0.067 mmol)를 첨가하였다. 혼합물을 75℃로 15시간 동안 가열한 다음, 혼합물을 실온으로 냉각시켰다. 추가의 1N NaOH 0.067 μL를 혼합물에 첨가하고, 이를 75℃로 가열하였다. 8시간 가열한 후, 혼합물을 실온으로 냉각시키고, 실온에서 추가로 63시간 동안 교반하였다. 혼합물을 정제용 HPLC에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (9 mg, 10.19 μmol, 76% 수율)을 백색 고체로서 수득하였다. LC/MS: m/e 795.5 (M+H)+, 2.09분 (방법 1).
실시예 17
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(카르복시메틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조
단계 1: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(2-메톡시-2-옥소에틸아미노)에틸카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
DCE (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(클로로카르보닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (32.2 mg, 0.0447 mmol) (메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(3-에톡시-3-옥소프로필카르바모일)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조에 상기 기재된 합성)의 현탁액에 메틸 2-(2-아미노에틸아미노)아세테이트 (8.86 mg, 0.067 mmol)를 첨가하였다. 혼합물을 실온에서 16시간 동안 교반하였다. 혼합물에 디이소프로필에틸아민 (0.023 mL, 0.134 mmol)을 첨가하고, 혼합물을 실온에서 3.5시간 동안 교반하였다. 추가로 메틸 2-(2-아미노에틸아미노)아세테이트 10 mg을 첨가하고, 반응물을 실온에서 추가로 19시간 동안 교반하였다. 혼합물에 추가의 메틸 2-(2-아미노에틸아미노)아세테이트 10 mg을 첨가하고, 추가로 실온에서 교반하였다. 혼합물을 실온에서 추가로 60시간 동안 교반한 후, 이를 플래쉬 크로마토그래피에 의해, 혼합물에 첨가된 0.1% 수산화암모늄을 함유하는 디클로로메탄 중 0-10% 메탄올 구배 및 12g 실리카 겔 칼럼을 사용하여 직접 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (31 mg, 0.027 mmol, 59.5% 수율)을 백색 발포체로서 수득하였다. LC/MS: m/e 816.5 (M+H)+, 2.57분 (방법 1).
단계 2: 1,4-디옥산 (1 mL) 중 2-(2-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(3-(2-모르폴리노에톡시)프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복스아미도)에틸아미노)아세트산 (30 mg, 0.026 mmol)의 용액에 1N NaOH (0.2 mL, 0.200 mmol)를 첨가하였다. 혼합물을 75℃로 15시간 동안 가열한 다음, 실온으로 냉각시키고, 정제용 HPLC (방법 1)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (10 mg, 0.013 mmol, 48.5% 수율)을 백색 고체로서 수득하였다. LC/MS: m/e 788.5 (M+H)+, 2.01분 (방법 1).
실시예 18
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(디메틸아미노)에틸카르바모일)-1-(3-(4-메톡시-N-메틸-4-옥소부탄아미도)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조
단계 1: tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(디메틸아미노)에틸카르바모일)-1-(3-(4-메톡시-N-메틸-4-옥소부탄아미도)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-(tert-부톡시카르보닐)페닐)-1-(3-(4-메톡시-N-메틸-4-옥소부탄아미도)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (0.1 g, 0.132 mmol)을 함유하는 바이알에 옥살릴 클로라이드 (DCM 중 2M) (2 mL, 4.00 mmol)를 첨가하였다. 용액을 실온에서 2.5시간 동안 교반하고, 감압 하에 농축시켰다. 잔류물을 DCM 중에 용해시키고, 추가로 2회 농축시켜 잔류 옥살릴 클로라이드를 제거하였다. 잔류물을 진공 하에 건조시킨 후, 이를 DCE (2 mL) 중에 용해시키고, 디이소프로필에틸아민 (0.069 mL, 0.396 mmol)을 첨가하고, 이어서 N1,N1-디메틸에탄-1,2-디아민 (0.022 mL, 0.198 mmol)을 첨가하였다. 혼합물을 실온에서 67시간 동안 교반한 다음, 물 7 mL로 희석하고, 디클로로메탄 (3 x 7 mL)으로 추출하였다. 합한 유기 층을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 플래쉬 크로마토그래피에 의해 디클로로메탄 중 0-10% 메탄올 구배 및 12g 실리카 겔 칼럼을 사용하여 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (73.4 mg, 0.089 mmol, 67% 수율)을 회백색 발포체로서 수득하였다. LC/MS: m/e 828.6 (M+H)+, 2.54분 (방법 1).
단계 2: DCM (1 mL) 중 tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-(2-(디메틸아미노)에틸카르바모일)-1-(3-(4-메톡시-N-메틸-4-옥소부탄아미도)프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (73 mg, 0.088 mmol)의 용액에 TFA (0.1 mL, 1.298 mmol)를 첨가하였다. 혼합물을 실온에서 16시간 동안 밤새 교반한 다음, 질소의 스트림 하에 농축시켰다. 잔류물을 1,4-디옥산 (2 mL)으로 희석하고, 75℃로 가열하였다. 22시간 가열한 후, 혼합물을 실온으로 냉각시켰다. 이어서, 이를 1N HCl로 산성화시키고, 열선총으로 가열하고, 실온에서 밤새 정치되도록 하였다. 어떠한 결정도 형성되지 않은 경우에, 혼합물을 정제용 HPLC (방법 1)에 의해 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켰다. 잔류물을 동일한 HPLC 방법을 사용하여 2회 재정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (14 mg, 0.018 mmol, 21% 수율)을 백색 고체로서 수득하였다. LC/MS: m/e 772.5 (M+H)+, 2.05분 (방법 1).
실시예 19-21
4-((1R,3aS,5aR,5bR,7aS,9S,11aS,11bR,13aR,13bR)-1-(1-카르복시프로프-1-엔-2-일)-3a-((2-(디메틸아미노)에틸)카르바모일)-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (실시예 19), 4-((1S,3aS,5aR,5bR,7aS,9S,11aS,11bR,13aR,13bR)-1-(1-카르복시프로판-2-일)-3a-((2-(디메틸아미노)에틸)카르바모일)-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-9-일)벤조산, 이성질체 1 (실시예 20), 및 4-((1S,3aS,5aR,5bR,7aS,9S,11aS,11bR,13aR,13bR)-1-(1-카르복시프로판-2-일)-3a-((2-(디메틸아미노)에틸)카르바모일)-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-9-일)벤조산, 이성질체 2 (실시예 21)의 제조
단계 1: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-벤질 1-(3-브로모프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
CCl4 (50 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (3.02 g, 4.29 mmol)의 용액에 NBS (0.954g, 5.36 mmol)를 첨가하였다. 혼합물을 실온에서 15.5시간 동안 교반한 다음, 셀라이트의 패드를 통해 여과하여 고체를 제거하고, 여과물을 감압 하에 농축시켰다. 잔류물을 플래쉬 크로마토그래피에 의해 160g 실리카 겔 칼럼 및 헥산 중 0-10% 에틸 아세테이트 구배를 사용하여 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 2.22g을 백색 발포체 (70% 순도)로서 수득하였으며, 이를 추가 정제 없이 후속 단계에 사용하였다.
단계 2: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(tert-부톡시카르보닐)페닐)-1-(4-에톡시-4-옥소부트-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
1,4-디옥산 (20 mL) 및 에탄올 (10 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-벤질 1-(3-브로모프로프-1-엔-2-일)-9-(4-(tert-부톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (1.5 g, 1.339 mmol)의 용액을 함유하는 가압가능한 용기에 탄산칼륨 (0.370 g, 2.68 mmol)을 첨가하였다. 혼합물을 질소로 버블링하여 10분 동안 탈기시키고, 팔라듐 테트라키스 (0.077 g, 0.067 mmol)를 첨가하였다. 혼합물을 배기시키고, 질소로 3회 재충전한 다음, 일산화탄소로 충전하고, 2회 배기시킨 다음, 최종적으로 85 psi의 일산화탄소로 채우고, 오일 조에서 85℃로 가열하였다. 24시간 가열한 후, 혼합물을 실온으로 냉각시킨 후, 물 25 mL로 희석하고, 에틸 아세테이트 (3 x 25 mL)로 추출하였다. 합한 유기 층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 플래쉬 크로마토그래피에 의해 헥산 중 0-10% EtOAc 구배 및 90g 실리카 겔 칼럼을 사용하여 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 주요 및 부차적 생성물, 표제 화합물인 주요 생성물 (0.591g, 0.761 mmol, 57% 수율)을 수득하였다. LC/MS: m/e 794.5 (M+18), 4.08분 (방법 1).
단계 3: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-tert-부틸디메틸실릴 9-(4-(tert-부톡시카르보닐)페닐)-1-(4-에톡시-4-옥소부트-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
DCE (7 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(tert-부톡시카르보닐)페닐)-1-(4-에톡시-4-옥소부트-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.588 g, 0.757 mmol)의 용액에 트리에틸아민 (0.169 mL, 1.211 mmol), tert-부틸디메틸실란 (0.251 mL, 1.513 mmol), 및 아세트산팔라듐 (II) (0.042 g, 0.189 mmol)을 첨가하였다. 혼합물을 질소로 플러싱하고, 60℃로 가열하였다. 5시간 가열한 후, 혼합물을 실온으로 냉각시킨 후, 셀라이트의 패드를 통해 여과하여 고체를 제거하고, 감압 하에 농축시켰다. 조 물질을 추가 정제 없이 후속 단계에 사용하였다.
단계 4: (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-9-(4-(tert-부톡시카르보닐)페닐)-1-(4-에톡시-4-옥소부트-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
THF (10 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-tert-부틸디메틸실릴 9-(4-(tert-부톡시카르보닐)페닐)-1-(4-에톡시-4-옥소부트-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.607 g, 0.757 mmol)의 용액에 테트라부틸암모늄 플루오라이드 수화물 (0.317 g, 1.136 mmol)을 첨가하였다. 황색 용액을 실온에서 3.5시간 동안 교반한 다음, 물 20 mL 및 1N HCl 10 mL로 희석하고, 디클로로메탄 (3 x 30 mL)으로 추출하였다. 합한 유기 층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 플래쉬 크로마토그래피에 의해 헥산 중 0-50% 에틸 아세테이트 구배 및 40g 실리카 겔 칼럼을 사용하여 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 생성물 (0.485 g, 0.706 mmol, 93% 수율)을 백색 고체로서 수득하였다. LC/MS: m/e 685.5 (M-H)-, 2.90분 (방법 1).
단계 5: tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-(2-(디메틸아미노)에틸카르바모일)-1-(4-에톡시-4-옥소부트-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트, HCl의 제조
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-9-(4-(tert-부톡시카르보닐)페닐)-1-(4-에톡시-4-옥소부트-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (0.15 g, 0.218 mmol)을 함유하는 오븐-건조된 둥근바닥 플라스크에 옥살릴 클로라이드 (DCM 중 2M) (5 mL, 10.00 mmol)를 첨가하였다. 혼합물을 실온에서 2.5시간 동안 교반하고, 감압 하에 농축시켰다. 잔류물을 DCM 중에 용해시키고, 추가로 2회 농축시켜 임의의 과량의 옥살릴 클로라이드를 제거하였다. 조 생성물을 DCE (2 mL) 중에 용해시키고, 디이소프로필에틸아민 (0.114 mL, 0.655 mmol)을 첨가하고, 이어서 N,N-디메틸에틸렌디아민 (0.036 mL, 0.328 mmol) 및 DMAP (1 mg, 8.19 μmol)를 첨가하였다. 혼합물을 실온에서 20시간 동안 교반한 다음, 물 (10 mL)로 희석하고, 디클로로메탄 (3 x 10 mL)으로 추출하였다. 합한 유기 층을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 플래쉬 크로마토그래피에 의해 디클로로메탄 중 0-10% 메탄올 구배 및 12g 실리카 겔 칼럼을 사용하여 정제하였다. 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 표제 화합물 (0.12 g, 0.151 mmol, 69.3% 수율)을 백색 고체로서 수득하였다. LC/MS: m/e 757.6 (M+H)+, 2.29분 (방법 6).
단계 6: 1,4-디옥산 (2 mL) 중 tert-부틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-(2-(디메틸아미노)에틸카르바모일)-1-(4-에톡시-4-옥소부트-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.115 g, 0.145 mmol)의 용액에 1N NaOH (0.725 mL, 0.725 mmol)를 첨가하였다. 혼합물을 85℃로 39시간 동안 가열하였다. NaOH (10N, 0.1 mL)를 혼합물에 첨가하고, 이를 85℃로 다시 가열하였다. 22시간 가열한 후, 혼합물을 실온으로 냉각시키고, 1N HCl을 사용하여 pH = 1로 산성화시켰다. 형성된 고체를 여과에 의해 수집하여 생성물의 혼합물 85 mg을 수득하였으며, 이를 추가 정제 없이 후속 단계에 직접 사용하였다. 생성물의 혼합물을 함유하는 바이알에 1,4 디옥산 중 4N HCl 3mL를 첨가하였다. 혼합물을 실온에서 2.5시간 동안 교반한 다음, 질소의 스트림 하에 농축시켰다. 잔류물을 정제용 HPLC (방법 1)에 의해 정제하였다. 생성물의 혼합물을 함유하는 분획을 합하고, 감압 하에 농축시켰다. 생성물의 혼합물을 아세트산 (2 mL) 및 메탄올 (4 mL) 중에 용해시키고, 질소로 탈기시키고, 10% Pd/C 20 mg을 혼합물에 첨가하였다. 혼합물을 1ATM의 H2 하에 3시간 동안 교반한 다음, 추가의 Pd/C 100 mg을 첨가하고, 혼합물을 1ATM의 H2 하에 교반하였다. 21시간 동안 교반한 후, 혼합물을 셀라이트의 플러그를 통해 여과하고, 감압 하에 농축시켰다. 잔류물을 정제용 HPLC (방법 1)에 의해 정제하였다. 3개의 주요 피크를 제1 정제용 HPLC 정제로 분리하였다. 일수소화 생성물을 함유하는 분획을 합하고, 농축시키고, 정제용 HPLC (방법 10)에 의해 재정제하였다. 각각의 다른 2종의 생성물을 농축시켜 비스-히드록실화 생성물의 2종의 부분입체이성질체를 수득하였다.
실시예 19: (단리물 1) 4-((1R,3aS,5aR,5bR,7aS,9S,11aS,11bR,13aR,13bR)-1-(1-카르복시프로프-1-엔-2-일)-3a-((2-(디메틸아미노)에틸)카르바모일)-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (4.0 mg, 0.006 mmol, 4% 수율)
LC/MS: m/e 675.5 (M+H)+, 2.05분 (방법 1).
실시예 20: (단리물 2) 4-((1S,3aS,5aR,5bR,7aS,9S,11aS,11bR,13aR,13bR)-1-(1-카르복시프로판-2-일)-3a-((2-(디메틸아미노)에틸)카르바모일)-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-9-일)벤조산, 이성질체 1 (6.5 mg, 0.010 mmol, 7% 수율)
LC/MS: m/e 677.6 (M+H)+, 2.19분 (방법 1).
실시예 21: (단리물 3) 4-((1S,3aS,5aR,5bR,7aS,9S,11aS,11bR,13aR,13bR)-1-(1-카르복시프로판-2-일)-3a-((2-(디메틸아미노)에틸)카르바모일)-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-9-일)벤조산, 이성질체 2 (5.5 mg, 0.008 mmol, 5.5% 수율)
LC/MS: m/e 677.5 (M+H)+, 2.04분 (방법 1).
실시예 22
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실산의 제조
단계 1: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실레이트의 제조
톨루엔 (2 mL) 및 메탄올 (0.5 mL) 중 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실산 (WO13123019에 기재된 바와 같이 제조됨) (0.1 g, 0.144 mmol)의 용액을 0℃로 냉각시켰다. 용액에 TMS-디아조메탄 (에테르 중 2M) (0.086 mL, 0.173 mmol)을 적가하였다. 기체 발생이 중지된 후, 혼합물을 실온으로 가온하고, 황색 용액을 실온에서 2시간 동안 교반하였다. 혼합물을 아세트산 1 mL를 조심스럽게 첨가하여 산성으로 만든 다음, 감압 하에 농축시켰다. 잔류물을 포화 수성 중탄산나트륨 (15 mL)으로 희석하고, 디클로로메탄 (3 x 10 mL)으로 추출하였다. 합한 유기 층을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 표제 생성물 (0.086 g, 0.121 mmol, 84% 수율)을 회백색 발포체로서 수득하였다.
단계 2: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실레이트의 제조
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실레이트 (0.086 g, 0.121 mmol)를 함유하는 플라스크에 아세틸아세톤 코발트(II) 염 (0.062 g, 0.243 mmol)을 첨가하였다. 혼합물을 THF (2 mL)로 희석하고, 페닐실란 (0.060 mL, 0.485 mmol)을 첨가하였다. 혼합물을 질소로 퍼징한 다음, 산소의 풍선 하에 두었다. 1.5시간 후, 혼합물을 디클로로메탄으로 희석하고, 4g 실리카 겔 칼럼을 통해 여과하였다 (DCM 중 10% MeOH로 세척함). 여과물을 감압 하에 농축시켰다. 잔류물을 디클로로메탄 중 0-8% MeOH 구배 및 12g 실리카 겔 칼럼을 사용하여 재정제하였다. 주요 단리물을 함유하는 분획을 합하고, 감압 하에 농축시켜 담녹색 고체 56 mg을 수득하였으며, 이를 추가 정제 없이 후속 단계에 사용하였다.
단계 3: 1,4-디옥산 (2 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실레이트 (0.056 g, 0.077 mmol)의 용액에 NaOH (1N) (0.385 mL, 0.385 mmol)를 첨가하고, 혼합물을 70℃로 가열하였다. 혼합물을 18시간 동안 가열한 후, 이를 실온으로 냉각시킨 후, 정제용 HPLC (방법 21)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실산, TFA (9.2 mg, 11.1 μmol, 14% 수율)를 백색 고체로서 수득하였다. LC/MS: m/e 713.6 (M+H)+, 1.44분 (방법 6).
실시예 23
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(2-옥사-5-아자비시클로[2.2.1]헵탄-5-일)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실산의 제조
단계 1: 에틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(2-옥사-5-아자비시클로[2.2.1]헵탄-5-일)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실레이트의 제조
WO13169578에 기재된 바와 같이 제조된 에틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(2-옥사-5-아자비시클로[2.2.1]헵탄-5-일)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실레이트 (46.5 mg, 0.068 mmol)를 함유하는 플라스크에 아세틸아세톤 코발트(II) 염 (34.8 mg, 0.135 mmol)을 첨가하였다. 혼합물을 THF (2 mL)로 희석하고, 페닐실란 (0.033 mL, 0.271 mmol)을 첨가하였다. 혼합물을 질소로 퍼징한 다음, 산소의 풍선 하에 두었다. 4.5시간 동안 교반한 후, 혼합물을 디클로로메탄으로 희석하고, 디클로로메탄 중 0-10% MeOH 구배 및 12g 실리카 겔 칼럼을 사용하여 직접 정제하였다. 2종의 주요 단리물을 함유하는 분획을 감압 하에 농축시켜 표제 화합물 (7.5 mg, 0.011 mmol, 16% 수율)을 담녹색 고체로서 수득하였다. LC/MS: m/e 705.7 (M+H)+, 1.76분 (방법 6).
단계 2: 1,4-디옥산 (0.5 mL) 중 에틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(2-옥사-5-아자비시클로[2.2.1]헵탄-5-일)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실레이트 (7.5 mg, 11 μmol)의 용액에 NaOH (1N) (0.074 mL, 0.074 mmol)를 첨가하였다. 혼합물을 75℃로 3시간 동안 가온한 다음, 실온으로 냉각시키고, 정제용 HPLC (방법 22)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 감압 하에 농축시켜 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(2-옥사-5-아자비시클로[2.2.1]헵탄-5-일)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실산, TFA (1.8 mg, 2.3 μmol, 22% 수율)를 투명한 무색 필름으로서 수득하였다. LC/MS: m/e 677.7 (M+H)+, 1.40분 (방법 6).
실시예 A1
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((tert-부톡시카르보닐)아미노)-1-(3-히드록시프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조산의 제조
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((tert-부톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
WO201206190에 기재된 바와 같이 제조된 THF (30 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (1.5 g, 2.67 mmol) 및 트리에틸아민 (0.744 mL, 5.34 mmol)의 용액에 디-tert-부틸 디카르보네이트 (0.930 mL, 4.00 mmol)를 첨가하였다. 반응 혼합물을 실온에서 15시간 동안 교반하였다. 이어서, 반응 혼합물을 증류수 (15 mL)로 켄칭하고, 디클로로메탄 (2 x15 mL)으로 추출하였다. 유기 상을 합하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 목적 생성물을 무색 오일 (1.8 g, 100%)로서 수득하였다. LCMS: m/e 662.42 (M+H)+, 3.39분 (방법 4).
단계 2. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((tert-부톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2-메틸옥시란-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
0℃에서 디클로로메탄 (20 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((tert-부톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (1800 mg, 2.72 mmol)의 용액에 3-클로로벤조퍼옥시산 (670 mg, 2.99 mmol)을 첨가하였다. 반응 혼합물을 0℃에서 2시간 동안 교반한 다음, 실온으로 2시간 동안 가온하였다. 이어서, 반응 혼합물을 포화 수성 Na2S2O3 (25mL)으로 켄칭하고, 디클로로메탄 (2 x 30 mL)으로 추출하고, 유기 상을 합하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 목적 생성물을 무색 오일로서 수득하였다. 잔류물을 실리카 겔 상에서 0-30% 에틸 아세테이트/헥산을 사용하여 정제하여 목적 생성물을 백색 고체 (1.0 g, 54%)로서 수득하였다. LCMS: m/e 678.39 (M+H)+, 3.69분 (방법 4).
단계 3. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((tert-부톡시카르보닐)아미노)-1-(3-히드록시프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
THF (2 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((tert-부톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2-메틸옥시란-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (200 mg, 0.295 mmol) 및 HCl (0.516 mL, 2.065 mmol)의 혼합물을 LCMS가 출발 물질이 소모되었다는 것을 나타낼 때까지 2시간 동안 교반하였다. 반응 혼합물을 감압 하에 농축시키고, 잔류물을 아세토니트릴 (1 mL) 중에 용해시키고, HPLC에 의해 정제하여 목적 생성물을 백색 고체 (30 mg, 15%)로서 수득하였다. LCMS: m/e 578.5 (M+H)+, 1.93분 (방법 6).
단계 4: 디옥산 (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((tert-부톡시카르보닐)아미노)-1-(3-히드록시프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (30 mg, 0.044 mmol) 및 1 N NaOH (0.443 mL, 0.443 mmol)의 혼합물을 78℃에서 3시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시킨 후 침전시켰다. 백색 고체를 여과하고, 물 (2 mL) 및 아세토니트릴 (2 mL)로 세척하여 목적 생성물 (19 mg, 61%)을 수득하였다. LCMS: m/e 664.5 (M+H)+, 2.55분 (방법 6).
실시예 A2
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-아미노-1-(3-히드록시프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조산의 제조
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-아미노-1-(3-히드록시프로프-1-엔-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (6 mg, 10.38 μmol) 및 1 N NaOH (0.104 mL, 0.104 mmol)의 혼합물을 78℃에서 3시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시킨 다음, 1 N HCl을 사용하여 pH~4-6으로 중화시키고, 백색 침전물을 여과하고, 증류수로 세척하여 목적 생성물을 백색 고체 (4 mg, 65%)로서 수득하였다. LCMS: m/e 564.18 (M+H)+, 2.44분 (방법 4).
실시예 A3
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2-메틸옥시란-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조산의 제조
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(2-메틸옥시란-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
THF (3 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((tert-부톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2-메틸옥시란-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (150 mg, 0.221 mmol) 및 염화수소 (1.106 mL, 4.43 mmol)의 혼합물을 30시간 동안 교반하였다. 반응을 중단하고, 증류수 (4 mL)로 켄칭하고, 디클로로메탄 (3x 2 mL)으로 추출하고, 합한 유기 상을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 표제 화합물을 무색 오일 (100 mg, 78%)로서 수득하였다. LCMS: m/e 578.2 (M+H)+, 1.98분 (방법 4).
단계 2. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2-메틸옥시란-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
아세토니트릴 (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(2-메틸옥시란-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (68.4 mg, 0.346 mmol), 인산칼륨 (110 mg, 0.519 mmol) 및 아이오딘화칼륨 (28.7 mg, 0.173 mmol)의 혼합물을 120℃에서 2시간 동안 가열하였다. 반응 혼합물을 증류수 (3 mL)로 켄칭하고, 디클로로메탄 (3 x 2 mL)으로 추출하고, 합한 유기 상을 Na2SO4 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 조 물질을 황색 오일로서 수득하였다. 조 물질을 정제용 HPLC에 의해 정제하여 표제 화합물을 무색 오일 (20 mg, 16%)로서 수득하였다. LCMS: m/e 739.55 (M+H)+, 2.09분 (방법 6).
단계 3. 디옥산 (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2-메틸옥시란-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (20 mg, 0.027 mmol) 및 1 N NaOH (0.271 mL, 0.271 mmol)의 혼합물을 78℃에서 3시간 동안 가열하였다. 반응 혼합물을 여과하고, 정제용 HPLC에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2-메틸옥시란-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조산을 무색 오일 (10 mg, 50%)로서 수득하였다. LCMS: m/e 725.55 (M+H)+, 2.67분 (방법 6).
실시예 A4 및 실시예 A5
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조산 (부분입체이성질체 1 및 부분입체이성질체 2)의 제조
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
실온에서 THF (50mL) 및 물 (50 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (2000 mg, 3.56 mmol) 및 탄산나트륨 (1509 mg, 14.24 mmol)의 혼합물에 THF (5 mL) 중 (9H-플루오렌-9-일)메틸 카르보노클로리데이트 (1105 mg, 4.27 mmol)를 첨가하였다. 반응 혼합물을 2시간 동안 교반하고, 증류수 (10 mL)로 켄칭하고, 에틸 아세테이트 (3 x 6 mL)로 추출하고, 합한 유기 상을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 조 물질을 0-30% 에틸 아세테이트/헥산을 이동상으로서 사용하는 실리카 겔을 사용하여 정제하여 목적 생성물을 백색 고체 (2.3 g, 81%)로서 수득하였다. LCMS: m/e 784.3 (M+H)+, 4.7분 (방법 4).
단계 2. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2-메틸옥시란-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
0℃에서 디클로로메탄 (4 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (950 mg, 1.212 mmol)의 용액에 3-클로로벤조퍼옥시산 (326 mg, 1.454 mmol)을 첨가하였다. 반응 혼합물을 18시간 동안 교반하고, 포화 Na2S2O3 (25 mL)으로 켄칭하고, 디클로로메탄 (2x30mL)으로 추출하였다. 합한 유기 상을 중탄산나트륨의 포화 수용액으로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 생성된 황색 오일을 0-30% 에틸 아세테이트/헥산을 이동상으로서 사용하는 실리카 겔을 사용하여 정제하여 목적 생성물을 백색 고체 (780 mg, 80%)로서 수득하였다. LCMS: m/e 800.29 (M+H)+, 3.21분 (방법 4).
단계 3. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-옥소프로판-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
실온에서 THF (30 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2-메틸옥시란-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (780 mg, 0.975 mmol)의 용액에 BF3.OEt2 (0.247 mL, 1.950 mmol)를 첨가하였다. 반응 혼합물을 실온에서 2시간 동안 교반하고, 증류수 (40 mL)로 켄칭하고, 디클로로메탄 (2 x 30 mL)으로 추출하였다. 합한 유기 상을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 조 물질을 0-35% 에틸 아세테이트/헥산을 이동상으로서 사용하는 실리카 겔을 사용하여 정제하여 표제 화합물을 부분입체이성질체의 혼합물 (백색 고체, 480 mg, 62%)로서 수득하였다. LCMS: m/e 800.6 (M+H)+, 3.40/3.61분 (방법 6).
단계 4. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
실온에서 THF (2 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-옥소프로판-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (60 mg, 0.075 mmol)의 용액에 수소화붕소나트륨 (5.67 mg, 0.150 mmol)을 첨가하였다. 반응 혼합물을 실온에서 2시간 동안 교반한 다음, 증류수 (2 mL)로 켄칭하고, 디클로로메탄 (2 x 2 mL)으로 추출하였다. 합한 유기 상을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 표제 화합물을 부분입체이성질체의 혼합물 (백색 고체, 50 mg, 83%)로서 수득하였다. LCMS: m/e 802.6/802.6 (M+H)+, 2.98/3.41분 (방법 6).
단계 5. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
20℃에서 THF (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (50 mg, 0.062 mmol)의 용액에 피페리딘 (106 mg, 1.247 mmol)을 첨가하였다. 반응 혼합물을 20℃에서 2시간 동안 교반한 다음, 감압 하에 농축시켰다. 잔류물을 아세토니트릴 (2 mL) 중에 용해시키고, 정제용 HPLC에 의해 정제하여 표제 화합물의 2종의 부분입체이성질체: 부분입체이성질체 1 (12 mg, 33%) 및 부분입체이성질체 2 (20 mg, 55%)를 백색 고체로서 수득하였다. LCMS: m/e 580.5/580.6(M+H)+, 1.56/1.60분 (방법 6).
단계 6. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
아세토니트릴 (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 1), 4-(2-클로로에틸)티오모르폴린 1,1-디옥시드 (20.46 mg, 0.103 mmol), 인산칼륨 (21.97 mg, 0.103 mmol) 및 아이오딘화칼륨 (5.73 mg, 0.034 mmol)의 혼합물을 120℃에서 15시간 동안 가열하였다. 반응 혼합물을 물 (2 mL)로 켄칭하고, 디클로로메탄 (2 x 2 mL)으로 추출하였다. 합한 유기 상을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 1)를 백색 고체 (9 mg, 35%)로서 수득하였다. LCMS: m/e 741.44 (M+H)+, 2.00분 (방법 4).
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 2)는 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 2)를 출발 물질로서 사용하여, 부분입체이성질체 1에 대해 상기 기재된 동일한 방법을 따라 제조하였다. 생성물을 백색 고체 (22 mg, 86%)로서 단리시켰다. LCMS: m/e 741.4(M+H)+, 2.24분 (방법 4).
단계 7. 아세토니트릴 (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 1) (9 mg, 0.012 mmol) 및 수산화나트륨 (0.297 mL, 0.297 mmol)의 혼합물을 80℃에서 2시간 동안 가열하였다. 반응 혼합물을 여과하고, 정제용 HPLC에 의해 정제하여 제공하였다.
실시예 A4: 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조산 (부분입체이성질체 1)을 백색 고체 (5 mg, 22%)로서 수득하였다. LCMS: m/e 727.6 (M+H)+, 1.34분 (방법 6).
실시예 A5: 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조산 (부분입체이성질체 2)은 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 2)를 출발 물질로서 사용하여, 부분입체이성질체 1에 대해 상기 기재된 방법을 따라 제조하였다. 생성물을 백색 고체 (13 mg, 57%)로서 단리시켰다. LCMS: m/e 727.6(M+H)+, 1.93분 (방법 6).
실시예 A6 및 실시예 A7
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-(1-카르복시에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조산 (부분입체이성질체 1 및 부분입체이성질체 2)의 제조
단계 1. 2-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-9-(3-플루오로-4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-일)프로판산의 제조
20℃에서 tBuOH (4 mL) 및 THF (8 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-옥소프로판-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 혼합물) (150 mg, 0.187 mmol)의 용액에 물 (5 mL) 중 인산이수소나트륨 (202 mg, 1.687 mmol) 및 아염소산나트륨 (115 mg, 1.275 mmol)의 용액을 0.5-1시간에 걸쳐 첨가하였다. 반응 혼합물을 20℃에서 추가로 1시간 동안 교반하고, 물 (10 mL)로 켄칭하고, 디클로로메탄 (2 x 10 mL)으로 추출하였다. 합한 유기 상을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 표제 화합물을 부분입체이성질체의 혼합물 (백색 고체, 100 mg, 65%)로서 수득하였다. LCMS: m/e 816.3 (M+H)+, 2.68분 (방법 4).
단계 2. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트의 제조
20℃에서 디클로로메탄 (2 mL) 중 2-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-9-(3-플루오로-4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-일)프로판산 (100 mg, 0.123 mmol)의 용액에 티오닐 클로라이드 (0.045 mL, 0.613 mmol)를 첨가하였다. 반응 혼합물을 20℃에서 2시간 동안 교반한 다음, 감압 하에 농축시켜 갈색 잔류물을 수득하였다. 메탄올 (4 mL)을 잔류물에 천천히 첨가하고, 혼합물을 추가로 10 분 동안 교반하였다. 이어서, 반응 혼합물을 감압 하에 농축시켜 표제 화합물을 부분입체이성질체의 혼합물 (갈색 고체, 96 mg, 94%)로서 수득하였다. LCMS: m/e 830.35/830.34 (M+H)+, 3.59/3.83분 (방법 4).
단계 3. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 1 및 부분입체이성질체 2)의 제조
20℃에서 THF (1mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (96 mg, 0.116 mmol)의 용액에 피페리딘 (197 mg, 2.313 mmol)을 첨가하였다. 반응 혼합물을 1시간 동안 교반한 다음, 감압 하에 농축시켰다. 잔류물을 아세토니트릴 (1 mL) 중에 용해시키고, 투명한 용액을 정제용 HPLC에 의해 정제하여 2종의 부분입체이성질체의 표제 화합물: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 1)를 백색 고체 (12 mg, 17%)로서 수득하였다. LCMS: m/e 607.24 (M)+/591.25(M-NH2)+, 1.88분 (방법 4). 및 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 2)를 백색 고체 (23 mg, 33%)로서 수득하였다. LCMS: m/e 607.24 (M)+/591.25(M-NH2)+, 2.00분 (방법 4).
단계 4. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 1 및 부분입체이성질체 2)의 제조
아세토니트릴 (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 1) (12 mg, 0.020 mmol), 인산칼륨 (24.10 mg, 0.114 mmol), 4-(2-클로로에틸)티오모르폴린 1,1-디옥시드 (22.44 mg, 0.114 mmol) 및 아이오딘화칼륨 (6.28 mg, 0.038 mmol)의 혼합물을 120℃에서 15시간 동안 가열하였다. 반응 혼합물을 물 (2 mL)로 켄칭하고, 디클로로메탄 (2 x 2 mL)으로 추출하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 1)를 백색 고체 (10 mg, 34%)로서 수득하였다. LCMS: m/e 769.33 (M+H)+, 2.24분 (방법 4).
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 2)는 메틸 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 2)를 출발 물질로서 사용하여, 부분입체이성질체 1의 합성에 대해 상기 기재된 방법을 따라 제조하였다. 생성물을 백색 고체 (16 mg, 55%)로서 단리시켰다. LCMS: m/e 769.33(M+H)+, 2.26분 (방법 4).
단계 5. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 1) (10 mg, 0.013 mmol) 및 수산화나트륨 (0.130 mL, 0.130 mmol)의 혼합물을 80℃에서 2시간 동안 가열하였다. 반응 혼합물을 여과하고, 정제용 HPLC에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-(1-카르복시에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조산 (부분입체이성질체 1)을 백색 고체 (4 mg, 39%)로서 수득하였다. LCMS: m/e 741.25 (M+H)+, 1.55분 (방법 4).
실시예 A7: 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-(1-카르복시에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조산 (부분입체이성질체 2)은 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-메톡시-1-옥소프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조에이트 (부분입체이성질체 2)를 출발 물질로서 사용하여, 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-(1-카르복시에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)-2-플루오로벤조산 (부분입체이성질체 1)의 합성에 대해 상기 기재된 방법을 따라 제조하였다. 표제 화합물을 백색 고체 (7 mg, 69%)로서 단리시켰다. LCMS: m/e 741.5(M+H)+, 2.21분 (방법 4).
실시예 A8
(1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-((tert-부톡시카르보닐)아미노)-9-(4-카르복시시클로헥스-1-엔-1-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
단계 1. (1R,3aS,5aR,5bR,7aR,9S,11aR,11bR,13aR,13bS)-벤질 1-아세틸-9-히드록시-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
DMF (10 mL) 중 (1R,3aS,5aR,5bR,7aR,9S,11aR,11bR,13aR,13bS)-1-아세틸-9-히드록시-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (1.6 g, 3.49 mmol), 탄산칼륨 (0.964 g, 6.98 mmol) 및 (브로모메틸)벤젠 (0.435 mL, 3.66 mmol)의 혼합물을 60℃에서 18시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 100 mL 물을 첨가하였다. 백색 침전물을 수집하고, 진공 하에 건조시켜 목적 생성물을 백색 고체 (1.7 g, 89%)로서 수득하였다. LCMS: m/e 549.3 (M+H)+, 2.54분 (방법 4).
단계 2. (1R,3aS,5aR,5bR,7aR,9S,11aR,11bR,13aR,13bS)-3a-((벤질옥시)카르보닐)-9-히드록시-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-1-카르복실산의 제조
물 (30 mL) 중 수산화나트륨 (1.749 g, 43.7 mmol)의 용액에 디브로민 (0.789 mL, 15.31 mmol)을 0℃에서 천천히 첨가하고, 반응 혼합물을 0℃에서 20분 동안 교반하고, 이 새로 제조된 오렌지 용액을 디옥산 (40 mL) 중 (1R,3aS,5aR,5bR,7aR,9S,11aR,11bR,13aR,13bS)-벤질 1-아세틸-9-히드록시-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (1.2 g, 2.187 mmol)의 용액에 천천히 첨가하였다. 반응 혼합물을 0℃에서 4시간 동안 교반한 다음, 실온으로 가온하고, 15시간 동안 교반하였다. 이어서, 반응 혼합물을 진한 HCl에 의해 pH=3-4로 중화시키고, 디클로로메탄 (2 x 40 mL)으로 추출하였다. 합한 유기 상을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 조 물질을 0-60% 에틸 아세테이트/헥산을 이동상으로서 사용하는 실리카 겔을 사용하여 정제하여 목적 생성물을 백색 고체 (1.1 g, 91%)로서 수득하였다. LCMS: m/e 549.18 (M-H)-, 2.26분 (방법 4).
단계 3. (1R,3aR,5aR,5bR,7aR,9S,11aR,11bR,13aR,13bR)-벤질 1-((아지도카르보닐)아미노)-9-히드록시-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
디옥산 (30 mL) 중 (1R,3aS,5aR,5bR,7aR,9S,11aR,11bR,13aR,13bS)-3a-((벤질옥시)카르보닐)-9-히드록시-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-1-카르복실산 (1100 mg, 1.997 mmol), 디페닐 포스포르아지데이트 (1.076 mL, 4.99 mmol) 및 트리에틸아민 (0.835 mL, 5.99 mmol)의 혼합물을 TLC가 sm이 소모되었음을 나타낼 때까지 75℃에서 2시간 동안 가열하였다. 반응 혼합물을 감압 하에 농축시키고, 잔류물을 0-42% 에틸 아세테이트/헥산을 이동상으로서 사용하는 실리카 겔을 사용하여 정제하여 표제 화합물을 백색 고체 (1.2 g, 100%)로서 수득하였다. LCMS: m/e 589.29 (M-H)-, 2.40분 (방법 4).
단계 4. (1R,3aR,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 1-((아지도카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-9-옥소이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
THF (20 mL) 중 (1R,3aR,5aR,5bR,7aR,9S,11aR,11bR,13aR,13bR)-벤질 1-((아지도카르보닐)아미노)-9-히드록시-5a,5b,8,8,11a-펜타메틸이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (1.2 g, 2.031 mmol) 및 PCC (1.095 g, 5.08 mmol)의 혼합물을 20℃에서 17시간 동안 교반하였다. 반응 혼합물을 감압 하에 농축시키고, 잔류물을 실리카 겔 상에서 0-35% 에틸 아세테이트/헥산을 이동상으로서 사용하여 정제하여 생성물을 무색 오일 (1.15 g, 96%)로서 수득하였다. LCMS: m/e 589.29 (M+H)+, 2.48분 (방법 4).
단계 5. (1R,3aR,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 1-아미노-5a,5b,8,8,11a-펜타메틸-9-옥소이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
THF (20 mL) 중 (1R,3aR,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 1-((아지도카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-9-옥소이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (1.15 g, 1.953 mmol)의 용액에 1N 수산화나트륨 (9.77 mL, 9.77 mmol)을 첨가하였다. 반응 혼합물을 sm이 소모될 때까지 1시간 동안 교반하였다. 반응 혼합물에 HCl (0.593 mL, 19.53 mmol)을 첨가하고, 반응 혼합물을 추가로 2시간 동안 교반하고, 디클로로메탄 (3 x 15 mL)으로 추출하고, 합한 유기 상을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 표제 화합물을 연황색 고체 (1.0 g, 96%)로서 수득하였다. LCMS: m/e 520.28 (M+H)+, 2.30분 (방법 4).
단계 6. (1R,3aR,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 1-((tert-부톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-9-옥소이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
THF (10 mL) 중 (1R,3aR,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 1-아미노-5a,5b,8,8,11a-펜타메틸-9-옥소이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트(97055-013, 011) (1.05 g, 2.020 mmol), 디-tert-부틸 디카르보네이트 (0.704 mL, 3.03 mmol) 및 트리에틸아민 (0.845 mL, 6.06 mmol)의 혼합물을 20℃에서 48시간 동안 교반하였다. 반응 혼합물을 증류수 (15 mL)로 켄칭하고, 디클로로메탄 (2 x 15 mL)으로 추출하고, 유기 층을 합하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 조 물질을 수득하였으며, 조 물질을 0-40% 에틸 아세테이트/헥산을 이동상으로서 사용하는 실리카 겔을 사용하여 정제하여 생성물을 백색 고체 (0.83 g, 66%)로서 수득하였다.
단계 7. (1R,3aR,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 1-((tert-부톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-9-(((트리플루오로메틸)술포닐)옥시)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
THF (10 mL) 중 (1R,3aR,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 1-((tert-부톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-9-옥소이코사히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (0.83 g, 1.339 mmol)의 용액에 -78℃에서 포타슘 비스(트리메틸실릴)아미드 (2.94 mL, 2.68 mmol)를 첨가하였다. 반응 혼합물을 -78℃에서 15분 동안 교반하고, 4 mL THF 중 1,1,1-트리플루오로-N-페닐-N-((트리플루오로메틸)술포닐)메탄술폰아미드 (0.526 g, 1.473 mmol)를 첨가하였다. 반응 혼합물을 -78℃에서 2시간 동안 교반하였다. 반응 혼합물을 증류수 (20 mL)로 켄칭하고, 에틸 아세테이트 (2 x 20 mL)로 추출하였다. 유기 상을 합하고, 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 물질을 이동상으로서 0-33% 에틸 아세테이트/헥산을 함유하는 실리카 겔을 사용하여 정제하여 표제 화합물을 무색 오일로서 수득하였으며, 이를 진공 하에 건조시켜 백색 발포체 고체 (0.5 g, 50%)를 수득하였다.
단계 8. (1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 1-((tert-부톡시카르보닐)아미노)-9-(4-(에톡시카르보닐)시클로헥스-1-엔-1-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조
디옥산 (5 mL) 및 물 (5 mL) 중 에틸 4-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)시클로헥스-3-엔카르복실레이트 (149 mg, 0.532 mmol), (1R,3aR,5aR,5bR,7aR,11aR,11bR,13aR,13bR)-벤질 1-((tert-부톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-9-(((트리플루오로메틸)술포닐)옥시)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (200 mg, 0.266 mmol), 테트라키스(트리페닐포스핀)팔라듐(0) (15.37 mg, 0.013 mmol) 및 중탄산나트륨 (112 mg, 1.330 mmol)의 혼합물을 76℃에서 3시간 동안 가열하였다. 반응 혼합물을 증류수 (10 mL)로 켄칭하고, 에틸 아세테이트 (3 x 10 mL)로 추출하였다. 추출물을 합하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 조 물질을 0-25% 에틸 아세테이트/헥산을 이동상으로서 사용하는 실리카 겔을 사용하여 정제하여 표제 화합물을 무색 오일 (0.15 g, 75%)로서 수득하였다. LCMS: m/e 778.65 (M+Na)+, 3.77분 (방법 6).
단계 9. (1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-((tert-부톡시카르보닐)아미노)-9-(4-(에톡시카르보닐)시클로헥스-1-엔-1-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조
디클로로에탄 (2 mL) 중 (1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 1-((tert-부톡시카르보닐)아미노)-9-(4-(에톡시카르보닐)시클로헥스-1-엔-1-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (80 mg, 0.106 mmol), tert-부틸디메틸실란 (24.61 mg, 0.212 mmol), 아세트산팔라듐 (II) (11.88 mg, 0.053 mmol) 및 트리에틸아민 (0.044 mL, 0.317 mmol)의 혼합물을 60℃에서 3시간 동안 가열하였다. 이어서, 혼합물을 실리카 겔의 패드를 통해 여과하여 Pd 촉매를 제거하고, 여과물을 감압 하에 농축시켜 조 물질을 황색 오일로서 수득하였다. 이 황색 오일을 2 mL THF 중에 용해시키고, TBAF (111 mg, 0.317 mmol)로 처리하였다. 혼합물을 출발 물질이 소모될 때까지 2시간 동안 교반하였다. 반응 혼합물을 pH 4에 도달할 때까지 1 N HCl로 처리하였다. 물 (2 mL)을 첨가하고, 백색 침전물이 형성되었다. 침전물을 수집하고, 건조시켜 표제 화합물을 백색 고체 (45 mg, 64%)로서 수득하였다. LCMS: m/e 688.6 (M+Na)+, 2.71분 (방법 6).
단계 10. 아세토니트릴 (1 mL) 중 (1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-((tert-부톡시카르보닐)아미노)-9-(4-(에톡시카르보닐)시클로헥스-1-엔-1-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (6 mg, 9.01 μmol) 및 수산화나트륨 (0.090 mL, 0.090 mmol)의 용액을 80℃에서 3시간 동안 가열하였다. 반응 혼합물을 여과하고, HPLC에 의해 정제하여 (1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-((tert-부톡시카르보닐)아미노)-9-(4-카르복시시클로헥스-1-엔-1-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산을 백색 고체 (1.5 mg, 25%)로서 수득하였다. LCMS: m/e 636.23 (M-H)-, 2.28분 (방법 4).
실시예 A9
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-((tert-부톡시카르보닐)아미노)-3a-((2-(디메틸아미노)에틸)카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실산의 제조
단계 1. 에틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-((tert-부톡시카르보닐)아미노)-3a-((2-(디메틸아미노)에틸)카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실레이트의 제조
디클로로메탄 (1 mL) 중 (1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-((tert-부톡시카르보닐)아미노)-9-(4-(에톡시카르보닐)시클로헥스-1-엔-1-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (10 mg, 0.015 mmol)의 용액에 실온에서 옥살릴 디클로라이드 (0.015 mL, 0.030 mmol)를 첨가하고, 반응 혼합물을 출발 물질이 소모될 때까지 1시간 동안 교반하였다. 반응 혼합물을 감압 하에 농축시키고, 진공 하에 2시간 동안 건조시켜 중간체 산 클로라이드를 황색 오일로서 수득하였다. 디클로로메탄 (1 mL) 중 N1,N1-디메틸에탄-1,2-디아민 (1.986 mg, 0.023 mmol) 및 휘니그의 염기 (5.25 μL, 0.030 mmol)의 용액에 사전에 제조한 디클로로메탄 (1 mL) 중 산 클로라이드를 첨가하고, 반응 혼합물을 16시간 동안 교반하고, 증류수 (2 mL)로 켄칭하고, 디클로로메탄 (2 x 2 mL)으로 추출하고, 합한 유기 상을 염수 (3 mL)로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 표제 화합물을 갈색 오일 (6 mg, 54%)로서 수득하였다. LCMS: m/e 736.6 (M+H)+, 3.02분 (방법 3).
단계 2. 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-((tert-부톡시카르보닐)아미노)-3a-((2-(디메틸아미노)에틸)카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실산의 제조
디옥산 (1 mL) 중 에틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-1-((tert-부톡시카르보닐)아미노)-3a-((2-(디메틸아미노)에틸)카르바모일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)시클로헥스-3-엔카르복실레이트 (6 mg, 8.15 μmol) 및 NaOH (0.082 mL, 0.082 mmol)의 혼합물을 80℃에서 2시간 동안 가열하였다. 반응 혼합물을 여과하고, HPLC에 의해 정제하여 목적 생성물을 무색 오일 (1.1 mg, 18%)로서 수득하였다. LCMS: m/e 708.5 (M+H)+, 1.76분 (방법 6).
실시예 B1
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시-1-메톡시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 및 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2의 제조.
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도-4-티오모르폴리닐)에틸)아미노)-1-이소프로페닐-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (1.11 g, 1.57 mmol), 시트르산 1수화물 (0.662 g, 3.15 mmol) 및 4-메틸모르폴린 N-옥시드 (0.203 g, 1.73 mmol)의 혼합물에 tert-부탄올 (30 mL)에 이어서 물 (30 mL)을 첨가하였다. 이어서, tert-부탄올 중 사산화오스뮴, 2.5% (0.800 g, 0.988 mL, 0.079 mmol)를 첨가하고, 생성된 혼합물을 실온에서 27시간 동안 교반하였다. 올리브 녹색 용액을 진공 하에 잔류물로 농축시킨 다음, THF (150 mL) 중에 재용해시켰다. 용액을 염수 (75 mL)로 세척한 다음, 유기물을 염수 (50 mL) 및 1N 수성 NaOH (10 mL)의 혼합물로 2회 세척한 다음, 염수 (50 mL)로 1회 더 세척하였다. 합한 수성 추출물을 THF (75 mL)로 역추출하고, 유기 상을 합하였다. 유기물에 실리카 겔 (11 g)을 첨가하고, 혼합물을 진공 하에 자유 유동 분말로 농축시키고, 이를 진공 오븐에 50℃에서 16시간 동안 두었다. 자유 유동 분말을 80g 실리카 겔 칼럼의 상부 상에 로딩하였다. 용리 구배 100% DCM에서 9:1 DCM:MeOH로 2종의 부분입체이성질체의 표제 화합물을 분리하였다. 칼럼으로부터 용리된 표제 화합물의 2종의 이성질체 중 첫 번째를 이성질체 1 (0.232 g, 20% 수율) 및 칼럼으로부터 용리된 표제 화합물의 2종의 이성질체 중 두 번째를 이성질체 2 (0.476 g, 41% 수율)로 표지하였다.
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1에 대한 분석 데이터: LCMS: m/e 739.7 (M+H)+, 2.12분 (방법 5).
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2에 대한 분석 데이터: LCMS: m/e 739.7 (M+H)+, 2.13분 (방법 5).
단계 2: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시-1-메톡시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
클로로포름 (0.5 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2 (0.020 g, 0.027 mmol) 및 2,6-디-tert-부틸-4-메틸피리딘 (0.028 g, 0.135 mmol)의 교반 혼합물에 메틸 트리플루오로메탄술포네이트 (0.022 g, 0.135 mmol)를 첨가하였다. 상기 용액을 함유하는 바이알을 밀봉하고, 70℃로 18시간 동안 가열하였다. 추가의 메틸 트리플루오로메탄술포네이트 (0.022 g, 0.135 mmol)를 첨가하고, 혼합물을 70℃로 30분 동안 다시 가열하였다. 혼합물을 클로로포름 (2 mL)으로 희석하고, 포화 수성 염화암모늄 (3 x 1 mL)으로 세척하였다. 유기 상을 질소 스트림을 통해 농축시키고, 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 표제 화합물 (0.0094 g, 35.4% 수율)을 비스-TFA 염으로서 수득하였다. LCMS: m/e 753.8 (M+H)+, 2.31분 (방법 5).
단계 3: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시-1-메톡시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.094 g, 0.0096 mmol), 수산화리튬 1수화물 (0.0040 g, 0.096 mmol), 메탄올 (0.3 mL), THF (0.3 mL) 및 물 (0.3 mL)의 혼합물을 교반하면서 75℃로 80분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하여 표제 화합물 (0.0104 g, >100% 수율)을 비스-TFA 염으로서 수득하였다.
LCMS: m/e 739.6 (M+H)+, 2.08분 (방법 5).
실시예 B2
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디메톡시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조
단계 1: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디메톡시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
클로로포름 (0.5 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2 (0.020 g, 0.027 mmol) 및 2,6-디-tert-부틸-4-메틸피리딘 (0.056 g, 0.271 mmol)의 교반 혼합물에 메틸 트리플루오로메탄술포네이트 (0.058 g, 0.352 mmol)를 첨가하였다. 상기 용액을 함유하는 바이알을 밀봉하고, 70℃로 4시간 동안 가열하였다. 혼합물을 클로로포름 (1.5 mL)으로 희석하고, 포화 수성 염화암모늄 (1 mL)으로 세척하였다. 수성 세척을 클로로포름 (2 x 1 mL)으로 역추출하고, 유기 상을 합하였다. 합한 유기 상을 질소 스트림을 통해 농축시키고, 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 표제 화합물 (0.010 g, 48.2% 수율)을 수득하였다. LCMS: m/e 767.7 (M+H)+, 2.34분 (방법 5).
단계 2: 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디메톡시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디메톡시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.0155 g, 0.016 mmol), 수산화리튬 1수화물 (0.0065 g, 0.156 mmol), 메탄올 (0.3 mL), THF (0.3 mL) 및 물 (0.3 mL)의 혼합물을 교반하면서 75℃로 80분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하여 표제 화합물 (0.0118 g, 76% 수율)을 수득하였다. LCMS: m/e 753.6 (M+H)+, 2.19분 (방법 5).
실시예 B3
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
건조 THF (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도-4-티오모르폴리닐)에틸)아미노)-1-이소프로페닐-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.050 g, 0.071 mmol) 및 코발트 (II) 아세틸아세토네이트 (3.7 mg, 0.014 mmol)의 교반 혼합물에 페닐실란 (0.015 g, 0.142 mmol)을 첨가하였다. 혼합물을 산소로 덮고, 바이알을 밀봉하고, 혼합물을 70℃로 69시간 동안 가열하였다. 혼합물을 열로부터 제거하였다. 추가의 코발트 (II) 아세틸아세토네이트 (24 mg, 0.11 mmol) 및 페닐실란 (0.015 g, 0.142 mmol)을 첨가하고, 바이알을 산소 기체의 풍선을 장착하고, 혼합물을 실온에서 3시간 동안 교반하였다. 역상 정제용 HPLC (정제용 HPLC 방법 4)에 의해 정제하여 표제 화합물 (0.0196 g, 29% 수율)을 비스-TFA 염으로서 수득하였다. LCMS: m/e 723.6 (M+H)+, 2.20분 (방법 5).
단계 2: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.0195 g, 0.021mmol), 수산화리튬 1수화물 (0.0103 g, 0.246 mmol), 메탄올 (0.3 mL), THF (0.3 mL) 및 물 (0.3 mL)의 혼합물을 교반하면서 75℃로 80분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하여 표제 화합물 (0.0186 g, 96% 수율)을 비스-TFA 염으로서 수득하였다. LCMS: m/e 709.6 (M+H)+, 2.01분 (방법 5).
실시예 B4
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-메톡시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-메톡시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
클로로포름 (0.5 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.020 g, 0.021 mmol) 및 2,6-디-tert-부틸-4-메틸피리딘 (0.043 g, 0.210 mmol)의 교반 혼합물에 메틸 트리플루오로메탄술포네이트 (0.035 g, 0.210 mmol)를 첨가하였다. 상기 용액을 함유하는 바이알을 밀봉하고, 70℃로 80분 동안 가열하였다. 조 혼합물을 질소 스트림을 통해 농축시키고, 역상 정제용 HPLC (정제용 HPLC 방법 4)에 의해 정제하여 표제 화합물 (0.0164 g, 81% 수율)을 비스-TFA 염으로서 수득하였다. LCMS: m/e 737.7 (M+H)+, 2.34분 (방법 5).
단계 2: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-메톡시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.0162 g, 0.017 mmol), 수산화리튬 1수화물 (0.0084 g, 0.201 mmol), 메탄올 (0.35 mL), THF (0.35 mL) 및 물 (0.2 mL)의 혼합물을 교반하면서 70℃로 20분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 5)에 의해 정제하여 표제 화합물 (0.0151 g, 91% 수율)을 비스-TFA 염으로서 수득하였다. LCMS: m/e 723.7 (M+H)+, 2.18분 (방법 5).
실시예 B5
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 1의 제조.
THF (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도-4-티오모르폴리닐)에틸)아미노)-1-이소프로페닐-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.100 g, 0.142 mmol)의 용액을 빙조에서 냉각시키고, THF 중 보란-테트라히드로푸란 착물, 1.0M (0.340 mL, 0.340 mmol)으로 천천히 처리하였다. 혼합물을 실온에서 16시간 동안 교반한 다음, 70℃에서 30분 동안 교반하였다. 혼합물을 빙조에서 다시 냉각시키고, 여기에 에탄올 (0.180 mL, 3.1 mmol) 및 포화 수성 아세트산나트륨 (0.066 mL)을 첨가하고, 이어서 30% 과산화수소 (0.092 mL, 0.90 mmol)를 천천히 첨가하였다. 생성된 혼합물을 실온에서 3시간 동안 교반하였다. 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 4)에 의해 정제하여 반응의 주요 이성질체 생성물을 함유하는 백색 고체 (56.7 mg)를 수득하였다. 부차적 이성질체는 단리되지 않았다. 이 고체의 부분 (20.0 mg, 총 회수된 양의 35.3%)을 MeOH (0.25 mL) 및 THF (0.25 mL)의 혼합물 중에 용해시키고, 70℃에서 1.0M 수성 LiOH (0.252 mL, 0.252 mmol)로 45분 동안 처리하였다. 이 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 4)에 의해 정제하고, 이어서 생성물 분획을 1M 수성 HCl로 처리하고, 후속적으로 진공 하에 농축시켜 이성질체 1 표제 화합물 비스 HCl 염을 백색 고체 (0.0138 g, 33.9% 전체 수율)로서 수득하였다. LCMS: m/e 709.7 (M+H)+, 1.95분 (방법 5).
실시예 B6
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 2의 제조.
THF (10 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도-4-티오모르폴리닐)에틸)아미노)-1-이소프로페닐-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (1.00 g, 1.42 mmol)의 용액을 빙조에서 냉각시키고, THF 중 보란-테트라히드로푸란 착물, 1.0M (3.40 mL, 3.40 mmol)으로 천천히 처리하였다. 혼합물을 실온에서 16시간 동안 교반한 다음, 70℃에서 30분 동안 교반하였다. 혼합물을 빙조에서 다시 냉각시키고, 여기에 에탄올 (0.90 mL, 15.4 mmol) 및 포화 수성 아세트산나트륨 (0.33 mL)을 첨가하고, 이어서 30% 과산화수소 (0.46 mL, 4.5 mmol)를 천천히 첨가하였다. 생성된 혼합물을 실온에서 2.5시간 동안 교반하였다. 유기물에 실리카 겔 (11 g)을 첨가하고, 혼합물을 진공 하에 자유 유동 분말로 농축시키고, 이를 진공 오븐에 50℃에서 16시간 동안 두었다. 자유 유동 분말을 160g 실리카 겔 칼럼의 상부 상에 로딩하였다. 용리 구배 100% DCM에서 9:1 DCM:MeOH로 2종의 부분입체이성질체를 분리하였다. 반응으로부터의 주요 이성질체 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1은 칼럼으로부터 첫 번째로 용리되었다 (0.458 g, 44.6% 수율). LCMS: m/e 723.6 (M+H)+, 2.14분 (방법 5).
반응 중에 형성된 2종의 이성질체 중 부차적인 것은 칼럼으로부터 주요 이성질체 이후에 용리되었고, 불순물과 혼합되었다. 부차적 이성질체를 함유하는 이들 불순물 분획을 역상 정제용 HPLC (정제용 HPLC 방법 6)에 의해 재정제하여 고체 (53.8 mg)를 수득하였다. 이 고체의 부분 (25 mg, 총량의 46.5%)을 MeOH (0.3 mL) 및 THF (0.3 mL)의 혼합물 중에 용해시키고, 1.0M 수성 LiOH (0.263 mL, 0.263 mmol)로 70℃에서 45분 동안 처리하였다. 이 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 7)에 의해 정제하여 이성질체 2 표제 화합물을 백색 고체 유리 염기 (0.0115 g, 5.2% 전체 수율)로서 수득하였다. LCMS: m/e 710.5 (M+H)+, 2.18분 (방법 5).
실시예 B7
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-메톡시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
THF (1 mL) 중 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도-4-티오모르폴리닐)에틸)아미노)-1-이소프로페닐-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.100 g, 0.142 mmol)의 용액을 빙조에서 냉각시키고, THF 중 보란-테트라히드로푸란 착물, 1.0M (0.340 mL, 0.340 mmol)으로 천천히 처리하였다. 혼합물을 실온에서 16시간 동안 교반한 다음, 70℃에서 30분 동안 교반하였다. 혼합물을 빙조에서 다시 냉각시키고, 여기에 에탄올 (0.180 mL, 3.1 mmol) 및 포화 수성 아세트산나트륨 (0.066 mL)을 첨가하고, 이어서 30% 과산화수소 (0.092 mL, 0.90 mmol)를 천천히 첨가하였다. 생성된 혼합물을 실온에서 3시간 동안 교반하였다. 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 6)에 의해 정제하여 반응의 주요 이성질체 생성물을 함유하는 백색 고체 (56.7 mg)를 수득하였다. 부차적 이성질체는 단리되지 않았다. 이 고체의 부분 (30.0 mg, 총 회수된 양의 52.9%)을 클로로포름 (0.5 mL) 중에 용해시키고, 2,6-디-tert-부틸-4-메틸피리딘 (0.065 g, 0.315 mmol) 및 메틸 트리플루오로메탄술포네이트 (0.052 g, 0.315 mmol)로 처리하였다. 혼합물을 실온에서 16시간 동안 교반한 다음, 70℃에서 30분 동안 교반하였다. 이 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하여 표제 화합물 비스 TFA 염을 무색 유리질 고체 (0.0177 g, 24.0% 전체 수율)로서 수득하였다. LCMS: m/e 737.7 (M+H)+, 2.34분 (방법 5).
실시예 B8
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-플루오로프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1의 제조.
THF (10 mL) 중 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도-4-티오모르폴리닐)에틸)아미노)-1-이소프로페닐-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (1.00 g, 1.42 mmol)의 용액을 빙조에서 냉각시키고, THF 중 보란-테트라히드로푸란 착물, 1.0M (3.40 mL, 3.40 mmol)으로 천천히 처리하였다. 혼합물을 실온에서 16시간 동안 교반한 다음, 70℃에서 30분 동안 교반하였다. 혼합물을 빙조에서 다시 냉각시키고, 여기에 에탄올 (0.90 mL, 15.4 mmol) 및 포화 수성 아세트산나트륨 (0.33 mL)을 첨가하고, 이어서 30% 과산화수소 (0.46 mL, 4.5 mmol)를 천천히 첨가하였다. 생성된 혼합물을 실온에서 2.5시간 동안 교반하였다. 유기물에 실리카 겔 (11 g)을 첨가하고, 혼합물을 진공 하에 자유 유동 분말로 농축시키고, 이를 진공 오븐에 50℃에서 16시간 동안 두었다. 자유 유동 분말을 160g 실리카 겔 칼럼의 상부 상에 로딩하였다. 용리 구배 100% DCM 에서 9:1 DCM:MeOH로 2종의 부분입체이성질체를 분리하였다. 반응으로부터의 주요 이성질체 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1은 칼럼으로부터 첫 번째로 용리되었다 (0.458 g, 44.6% 수율). LCMS: m/e 723.6 (M+H)+, 2.14분 (방법 5).
단계 2: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-플루오로프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
DCM (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 (0.025 g, 0.035 mmol)의 용액을 -78℃로 냉각시키고, DAST (0.0078 g, 0.048 mmol)로 처리하였다. 혼합물이 실온으로 가온되도록 하고, 21시간 동안 교반하였다. 반응 혼합물을 농축시키고, 역상 정제용 HPLC (정제용 HPLC 방법 8)에 의해 정제하여 표제 화합물 (0.0097 g, 29% 수율)을 비스-TFA 염으로서 수득하였다. LCMS: m/e 725.6 (M+H)+, 2.35분 (방법 5).
단계 3: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-플루오로프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.0095 g, 0.010 mmol), 1.0M 수성 수산화리튬 1수화물 (0.100 mL, 0.100 mmol), 메탄올 (0.3 mL) 및 THF (0.3 mL)의 혼합물을 교반하면서 70℃로 45분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 표제 화합물 (0.0152 g, >100% 수율)을 비스-TFA 염으로서 수득하였다. LCMS: m/e 711.4 (M+H)+, 2.19분 (방법 5).
실시예 B9
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산, 이성질체 1의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
중간체 3 (4.00 g, 6.89 mmol)을 함유하는 플라스크에 중탄산나트륨 (2.90 g, 34.5 mmol)을 첨가하였다. 혼합물을 THF (80 mL) 및 물 (25 mL)로 희석한 다음, 9-플루오레닐메톡시카르보닐-클로라이드 (2.140 g, 8.27 mmol)를 첨가하고, 혼합물을 실온에서 교반하였다. 2시간 교반한 후, TLC는 반응이 완결되었음을 나타내었다. 혼합물을 EtOAc 350 mL로 희석하고, 물 (3 x 100 mL)로 세척하였다. 유기물을 MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물 (대략 5.5 g 회백색 유리질 고체)을 실리카 겔 크로마토그래피 (10 칼럼 부피에 걸쳐 용리 구배 96:4 헥산:EtOAc에서 65:35 헥산:EtOAc)에 의해 정제하여 생성물을 백색 고체로서 수득하였다. 총 회수 = 4.25 g (80% 수율).
단계 2. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1,2-디히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 및 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1,2-디히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2의 제조.
PTFE 스크류마개 및 교반막대를 갖는 20 mL 섬광 바이알에서 THF (60 mL) 및 물 (10 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (2.50 g, 3.26 mmol)와 NMO (0.765 g, 6.53 mmol)를 합하였다. 이어서, 고체 사산화오스뮴 (0.415 g, 1.632 mmol)을 도입하였다. 혼합물을 질소로 플러싱하고, 밀봉하고, 실온에서 7일 동안 교반하였다. 황색 혼합물을 에틸 아세테이트 (700 mL) 및 물 (300 mL)로 희석하고, 진탕시키고, 상을 분리하였다. 유기물을 물 (2 x 250 mL)로 세척한 다음, 염수 (50 mL)로 세척하였다. 유기물을 황산나트륨 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 갈색 고체를 수득하였다. 조 고체를 실리카 크로마토그래피 (용리 구배 100% 헥산에서 헥산 중 40% EtOAc, 4 칼럼 부피 동안 헥산 중 40% EtOAc 유지, 이어서 헥산 중 50% EtOAc)에 의해 정제하였다. 2종의 생성물을 단리시켰다. 부차적 생성물 (이성질체 2)은 칼럼으로부터 용리된 2종의 이성질체 중 첫 번째였다. 이성질체 2는 회색 고체 (0.183 g, 7.0% 수율)로서 단리시켰다.
주요 생성물 (이성질체 1)은 실리카 칼럼으로부터 단리된 2종의 이성질체 중 두 번째였다. 이성질체 1은 회색 고체 (1.165 g, 44.6% 수율)로서 단리시켰다.
단계 3. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1-아세톡시-2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1의 제조.
PTFE 스크류마개를 갖는 20 mL 섬광 바이알에서 클로로포름 (5 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1,2-디히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 (0.30 g, 0.375 mmol)을 용해시켰다. 혼합물에 피리딘 (0.243 mL, 3.00 mmol)을 첨가하고, 이어서 아세틸 클로라이드 (0.133 mL, 1.875 mmol)를 첨가하였다. 발열이 관찰되었다. TLC로 반응이 5분 내에 완결되었음을 확인하였다. 조 혼합물을 최소의 CHCl3 중에 용해시키고, 실리카 겔 크로마토그래피 (6칼럼 부피에 걸쳐 용리 구배 100% 헥산에서 헥산 중 50% EtOAc, 6 칼럼 부피 동안 헥산 중 50% EtOAc 유지)에 의해 정제하였다. 따라서 주요 생성물을 백색 고체로서 단리시켰다. 총 회수 = 0.260 g (82% 수율).
단계 4. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세톡시-2-히드록시프로판-2-일)-3a-아미노-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1의 제조.
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1-아세톡시-2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 (0.260 g, 0.309 mmol)을 클로로포름 (5 mL) 중에 용해시키고, 피페리딘 (0.5 mL, 5.05 mmol)을 첨가하였다. 혼합물을 실온에서 18시간 동안 교반하였다. 반응물을 진공 하에 농축시키고, 조 잔류물을 실리카 겔 크로마토그래피 (6 칼럼 부피에 걸쳐 용리 구배 100% DCM에서 9:1 DCM:MeOH, 6 칼럼 부피 동안 9:1 DCM:MeOH 유지)에 의해 정제하였다. 유사 생성물 분획을 합하고, 진공 하에 농축시켜 미황색 발포성 고체 0.1809 g (95% 수율)을 수득하였다.
단계 5. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세톡시-2-히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1의 제조.
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세톡시-2-히드록시프로판-2-일)-3a-아미노-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 (0.180 g, 0.290 mmol)을 함유하는 75 mL 중압 용기에 4-(2-클로로에틸)티오모르폴린 1,1-디옥시드 (0.150 g, 0.759 mmol), 인산, 칼륨 염 (0.229 g, 1.079 mmol) 및 KI (0.110 g, 0.663 mmol)를 첨가하였다. 혼합물을 아세토니트릴 (12 mL)로 희석하였다. 이어서, 용기를 N2로 플러싱하고, 밀봉하고, 오일 조에서 110℃로 16시간 동안 가열하였다. 혼합물을 EtOAc (100 mL) 및 물 (50 mL)로 희석하고, 진탕시키고, 상을 분리하였다. 유기 상을 MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 잔류물을 수득하였다. 조 잔류물을 실리카 겔 크로마토그래피 (6 칼럼 부피에 걸쳐 용리 구배 100%DCM에서 9:1 DCM:MeOH, 6 칼럼 부피 동안 9:1 DCM:MeOH 유지)에 의해 정제하여 황색 오일 (0.297 g)을 수득하였으며, 이를 추가 정제 없이 직접 후속 단계로 이행하였다. LCMS: m/z = 781.7 (M+H)+, 2.21분 (방법 5).
단계 6: 20 mL 섬광 바이알에서 조 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세톡시-2-히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 (0.227 g, 0.290 mmol) 및 수산화리튬 1수화물 (0.085 g, 2.030 mmol)과 테트라히드로푸란 (4 mL), MeOH (3 mL) 및 물 (2 mL)을 합하였다. 바이알을 PTFE 스크류마개로 캡핑하고, 혼합물을 교반하면서 75℃로 2시간 동안 가열하였다. 추가의 수산화리튬 1수화물 (36 mg, 0.857 mmol)을 첨가하고, 혼합물을 75℃로 추가로 45분 동안 재가열하였다. 혼합물을 역상 정제용 HPLC에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산, 이성질체 1 (0.173 g, 61.2% 수율)을 백색 분말 TFA 염으로서 수득하였다. LCMS: m/z = 725.6 (M+H)+, 1.94분 (방법 5).
실시예 B10
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산, 이성질체 2의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1-아세톡시-2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2의 제조.
20 mL 섬광 바이알에서 클로로포름 (5 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1,2-디히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2 (0.169, 0.211 mmol)를 용해시켰다. 혼합물에 피리딘 (0.137 mL, 1.690 mmol)을 첨가하였다. 혼합물을 빙조에서 냉각시키고, 아세틸 클로라이드 (0.075 mL, 1.056 mmol)를 천천히 첨가하였다. PTFE 스크류마개를 바이알에 부착하고, 혼합물을 실온에서 10분 동안 교반하였다. 이어서, 혼합물을 진공 하에 농축시켰다. 조 혼합물을 실리카 겔 크로마토그래피 (10 칼럼 부피에 걸쳐 용리 구배 100% 헥산에서 헥산 중 40% EtOAc, 10 칼럼 부피 동안 헥산 중 40% EtOAc 유지)에 의해 정제하여 미황색 고체, 0.1386 g (78% 수율)을 수득하였다.
단계 2. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세톡시-2-히드록시프로판-2-일)-3a-아미노-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2의 제조.
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((((9H-플루오렌-9-일)메톡시)카르보닐)아미노)-1-(1-아세톡시-2-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2 (0.135 g, 0.160 mmol)를 클로로포름 (5 mL) 중에 용해시키고, 피페리딘 (0.5 mL, 5.05 mmol)을 첨가하였다. 혼합물을 실온에서 18시간 동안 교반하였다. 혼합물을 질소 스트림을 통해 농축시킨 다음, 실리카 겔 크로마토그래피 (8 칼럼 부피에 걸쳐 용리 구배 100% DCM에서 9:1 DCM:MeOH, 6 칼럼 부피 동안 9:1 DCM:MeOH 유지)에 의해 정제하여 미황색 고체 (0.0848 g, 85% 수율)를 수득하였다.
단계 3. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세톡시-2-히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2의 제조.
15 mL 중압 용기에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세톡시-2-히드록시프로판-2-일)-3a-아미노-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2 (0.082 g, 0.132 mmol), 4-(2-클로로에틸)티오모르폴린 1,1-디옥시드 (0.065 g, 0.331 mmol), 인산, 칼륨 염 (0.098 g, 0.463 mmol) 및 KI (0.055 g, 0.331 mmol)를 합하였다. 혼합물을 아세토니트릴 (6 mL)로 희석하였다. 이어서, 용기를 N2로 플러싱하고, 밀봉하고, 오일 조에서 110℃로 밤새 가열하였다. 혼합물을 클로로포름 (50 mL)으로 희석하고, 여과하여 고체를 제거하였다. 조 혼합물을 실리카 겔 크로마토그래피 (6 칼럼 부피에 걸쳐 용리 구배 100%DCM에서 9:1 DCM:MeOH, 6 칼럼 부피 동안 9:1 DCM:MeOH 유지)에 의해 정제하여 매우 미황색 오일 (0.099 g, 96% 수율)을 수득하였다. LCMS: m/z = 781.6 (M+H)+, 2.16분 (방법 5).
단계 4: 1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세톡시-2-히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2 (0.025 g, 0.032 mmol) 및 수산화리튬 1수화물 (0.016 g, 0.384 mmol)과 테트라히드로푸란 (0.4 mL), MeOH (0.4 mL) 및 물 (0.4 mL)을 합하였다. 바이알을 PTFE 스크류마개로 캡핑하고, 혼합물을 교반하면서 75℃로 2시간 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산, 이성질체 2 (0.026 g, 84% 수율)를 백색 유리질 고체 TFA 염으로서 수득하였다. LCMS: m/z = 725.6 (M+H)+, 1.95분 (방법 5).
실시예 B11 및 B12
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-((R)-1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 1 및 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-((R)-1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 2의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.280 g, 0.379 mmol)의 두 이성질체 및 과아이오딘산나트륨 (0.324 g, 1.515 mmol)의 혼합물을 THF (10 mL) 및 물 (2 mL)의 혼합물 중에 용해시켰다. 혼합물을 1시간 동안 교반한 다음, THF (75 mL) 및 염수 (30 mL)로 희석하고, 생성된 혼합물을 진탕시키고, 상을 분리하였다. 수층을 THF (2 x 50 mL)로 추출한 다음, 클로로포름 (2 x 50 mL)으로 추출하였다. 유기물을 합하고, 탁한 생성물을 대략 30 mL로 농축시켰다. 메탄올을 유기물이 완전한 용액이 될 때까지 첨가한 다음, 실리카 겔 (3 g)을 첨가하고, 혼합물을 자유 유동 분말로 농축시키고, 이를 진공 오븐에 밤새 두었다. 분말을 DCM 선-평형화시킨 25 g 실리카 겔 카트리지의 상부 상에 로딩하였다. 용리 (구배 100% DCM에서 DCM:MeOH의 9:1 혼합물 40%)하여 생성물 (0.2462 g, 92% 수율)을 미회백색 유리질 고체로서 수득하였다. LCMS: m/z = 707.6 (M+H)+, 2.25분 (방법 5).
단계 2. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
PTFE 스크류마개를 갖는 1 드램 바이알에서 무수 에탄올 (1 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.020 g, 0.028 mmol)와 수소화붕소나트륨 (0.00535 g, 0.141 mmol)을 합하였다. 혼합물을 실온에서 30분 동안 교반하였지만, 혼합물이 완전히 용해되지는 않았다. THF (1 mL)를 첨가하고, 이제 완전한 용액을 실온에서 16시간 동안 교반하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 4)에 의해 부분적으로 정제하여 TFA 염 물질 0.026 g을 부분입체이성질체의 혼합물로서 수득하였으며, 이를 추가 조작 없이 후속 단계로 이행하였다. LCMS: m/z = 709.5 (M+H)+, 2.14분 (방법 5).
단계 3: PTFE 스크류마개를 갖는 1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-((R)-1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 TFA 염 (0.026 g, 0.014 mmol)을 함유하는 단계 2로부터의 물질과 수산화리튬 1수화물, 1.0M 수용액 (0.280 mL, 0.28 mmol) 및 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 스크류마개로 캡핑하고, 혼합물을 교반하면서 70℃로 45분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하였다. 2종의 분리된 생성물을 단리시켰다. 용리된 제1 물질이 주요 생성물이었고, 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 1 (0.0169 g, 61.5% 수율 백색 분말 TFA 염)로 표지하였다. 부차적 생성물은 두 번째로 용리되었고, 이를 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 2 (0.0051 g, 18.6% 수율 백색 분말 TFA 염)로 표지하였다.
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 1에 대한 분석 데이터: LCMS: m/z = 695.4 (M+H)+, 1.95분 (방법 5).
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 2에 대한 분석 데이터: LCMS: m/z = 695.4 (M+H)+, 2.01분 (방법 5).
실시예 B13
4-((3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-에틸리덴-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 및 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2의 제조.
고무 격막을 갖는 7 mL 섬광 바이알에서 질소 분위기 하에 에탄올 (2 mL) 및 건조 THF (2 mL)의 혼합물 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.100 g, 0.141 mmol)와 수소화붕소나트륨 (0.021 g, 0.566 mmol)을 합하였다. 혼합물을 실온에서 2시간 동안 교반하였다. 버블링이 중지될 때까지 혼합물에 포화 염화암모늄을 적가하였다. 혼합물을 소량의 THF로 희석하고, 여과하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 10)에 의해 정제하였다. 용리된 제1 물질은 주요 생성물이었고; 이 주요 생성물을 이성질체 1로 표지하고, 백색 분말 (0.0547 g, 41.3% 수율) TFA 염으로서 단리시켰다. 용리된 제2 물질은 부차적 생성물이었고; 이 부차적 생성물을 이성질체 2로 표지하고, 백색 분말 (0.0219 g, 16.5% 수율) TFA 염으로서 단리시켰다. 미반응 출발 물질 (0.0328 g, 24.8%)의 부분은 용리된 제3 물질이었다.
이성질체 1을 DCM 및 메탄올의 1:1 혼합물 중에 용해시키고, 1 그램 워터스 오아시스(Waters Oasis) MCX 양이온 교환 카트리지 상에 로딩하였다. 카트리지를 1:1 DCM:MeOH (20 mL)로 헹군 다음, MeOH (10 mL)로 헹구었다. 이어서, 이성질체 1 물질을 메탄올 중 2.0M 암모니아 (20 mL)를 사용하여 카트리지로부터 용리하였다. 따라서 이성질체 1을 미회백색 고체로서의 유리 염기 물질로서 정량적으로 회수하였다.
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1에 대한 분석 데이터: LCMS: m/z = 709.4 (M+H)+, 2.18분 (방법 5).
단계 2. 메틸 4-((3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-에틸리덴-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
고무 마개를 갖는 1 드램 바이알에, DCM (1 mL) 중 유리 염기 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-((R)-1-히드록시에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 (0.025 g, 0.035 mmol)을 두었다. 혼합물을 드라이 아이스/아세톤 조에서 -78℃로 냉각시키고, 교반 혼합물에 DAST (6.99 μl, 0.053 mmol)를 첨가하였다. 냉각 조를 제거하고, 혼합물을 실온에서 2시간 동안 교반하였다. 혼합물을 질소 스트림 하에 잔류물로 농축시키고, 이를 최소의 THF:MeOH 혼합물 (대략 4 대 1) 중에 재용해시키고, 역상 정제용 HPLC (정제용 HPLC 방법 11)에 의해 정제하였다. 따라서 생성물을 백색 고체 (0.0139 g, 43% 수율) TFA 염으로서 단리시켰다. LCMS: m/z = 691.3 (M+H)+, 2.31분 (방법 5).
단계 3: 1 드램 바이알에서 메틸 4-((3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-에틸리덴-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트, TFA 염 (0.0139 g, 0.015 mmol)과 수산화리튬 1수화물, 1.0M 수용액 (0.151 mL, 0.151 mmol) 및 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 캡핑하고, 혼합물을 70℃로 35분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 4)에 의해 정제하여 4-((3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-에틸리덴-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 고체 (0.0092 g, 61.8% 수율) TFA 염으로서 수득하였다. LCMS: m/z = 677.4 (M+H)+, 2.17분 (방법 5).
실시예 B14 및 실시예 B15
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(히드록시이미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 1 및 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(히드록시이미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 2의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(히드록시이미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
PTFE 스크류마개를 갖는 1 드램 바이알에서 건조 메탄올 (2.3 mL) 및 테트라히드로푸란 (1.5 mL)의 혼합물 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.028 g, 0.040 mmol)와 히드록실아민 히드로클로라이드 (0.028 g, 0.396 mmol) 및 아세트산나트륨 (0.049 g, 0.594 mmol)을 합하였다. 현탁액을 5일 동안 신속히 교반한 다음, 질소 스트림 하에 농축시켰다. 혼합물을 최소량의 THF 및 메탄올의 혼합물 중에 재용해시키고, 역상 정제용 HPLC (정제용 HPLC 방법 12)에 의해 정제하였다. 따라서 생성물을 백색 고체 (0.0248 g, 87% 수율)로서 수득하였다. LCMS: m/z = 722.4 (M+H)+, 2.15분 (방법 5).
단계 2: 1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-((E)-1-(히드록시이미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.020 g, 0.028 mmol)와 수산화리튬 1수화물, 1.0M 수용액 (0.277 mL, 0.277 mmol), 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 캡핑하고, 혼합물을 교반하면서 70℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 12)에 의해 정제하였다. 2개의 피크를 수집하였다. 정제용 HPLC로부터 용리된 제1 물질을 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(히드록시이미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 1 (0.0041 g, 20.7% 수율)로 표지하고, 주요 이성질체 2 생성물로 오염되었다. 정제용 HPLC로부터 용리된 제2 물질은 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(히드록시이미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 2로 표지된 주요 생성물이고, 백색 분말 (0.0119 g, 60.1% 수율)로서 깨끗이 단리시켰다.
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(히드록시이미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산, 이성질체 1에 대한 분석 데이터: HPLC는 이 물질이 이성질체 1 옥심 대 이성질체 2 옥심의 73:27 혼합물임을 나타내었다. LCMS: m/z = 708.4 (M+H)+, 1.95분 (방법 5).
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(히드록시이미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산, 이성질체 2에 대한 분석 데이터: HPLC는 이 물질이 깨끗한 단일 화합물임을 나타내었다. LCMS: m/z = 708.4 (M+H)+, 1.99분 (방법 5).
실시예 B16
4-((1S,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-모르폴리노프로판-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1S,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-모르폴리노프로판-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
고무 격막 및 교반막대를 갖는 1 드램 바이알에서 건조 클로로포름 (1 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 (0.025 g, 0.035 mmol) 및 2,6-디-tert-부틸-4-메틸피리딘 (0.021 g, 0.104 mmol)을 합하였다. 교반 용액에 트리플루오로메탄술폰산 무수물 (0.013 g, 0.045 mmol)을 실온에서 적가하였다. 혼합물을 실온에서 1시간 동안 교반한 다음, 혼합물에 모르폴린 (0.030 mL, 0.346 mmol)을 첨가하고, 생성된 용액을 실온에서 30분 동안 교반한 다음, 60℃로 90분 동안 가열하였다. 반응 혼합물을 질소 스트림 하에 농축시키고, 최소량의 THF 및 MeOH의 혼합물 중에 재용해시켰다. 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하여 목적 생성물을 백색 분말 (0.0199 g, 50.7% 수율) TFA 염으로서 수득하였다. LCMS: m/z = 792.7 (M+H)+, 1.97분 (방법 5).
단계 2: 1 드램 바이알에서 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL) 중에 메틸 4-((1S,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-모르폴리노프로판-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트, TFA 염 (0.0192 g, 0.019 mmol)과 수산화리튬 1수화물, 1.0M 수용액 (0.188 mL, 0.188 mmol)을 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 캡핑하고, 혼합물을 교반하면서 70℃로 40분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하여 4-((1S,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-모르폴리노프로판-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0139 g, 73% 수율)으로서 수득하였다. LCMS: m/z = 778.7 (M+H)+, 1.75분 (방법 5).
실시예 B17
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(3-옥소프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
75 mL 켐글래스 압력 용기에서 중간체 4 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (1.50 g, 2.13 mmol)와 이산화셀레늄 (0.295 g, 2.66 mmol) 및 아세트산 (30 mL)을 합하였다. 용기를 밀봉하고, 혼합물을 100℃로 45분 동안 가열하였다. 혼합물이 실온으로 냉각되도록 하고, 추가의 0.25 당량의 이산화셀레늄 (0.059 g, 0.67 mmol)을 첨가하였다. 용기를 100℃로 15분 동안 재가열하였다. 혼합물을 미세 소결 깔때기를 통해 여과하여 미세 흑색 고체를 제거하고, 여과물을 진공 하에 오렌지색 발포성 잔류물로 농축시켰다. 조 혼합물을 실리카 겔 크로마토그래피 (6 칼럼 부피에 걸쳐 용리 구배 100% 헥산에서 3:1 헥산:아세톤, 6 칼럼 부피 동안 3:1 헥산:아세톤 유지)에 의해 정제하였다. 생성물 분획을 합하고, 농축시켜 생성물을 회백색 고체: 0.747 g (48.8% 수율)으로서 수득하였다. LCMS: m/z = 719.6 (M+H)+, 2.56분 (방법 3).
단계 2. (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산의 제조.
고무 마개로 밀봉된 100 mL 둥근 바닥 플라스크에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(3-옥소프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.590 g, 0.821 mmol)와 시트르산 1수화물 (0.345 g, 1.64 mmol)을 합하였다. 이어서, tert-부탄올 (18 mL)을 첨가하고, 이어서 물 (15 mL)을 첨가하였다. 교반 혼합물에 NMO, 물 중 50 중량% 용액 (0.374 mL, 1.81 mmol)에 이어서 t-부탄올 중 사산화오스뮴, 2.5% (0.515 mL, 0.041 mmol)를 첨가하였다. 혼합물을 실온에서 30.5시간 동안 교반하였다. 혼합물에 고체 과아이오딘산나트륨 (1.229 g, 5.74 mmol)을 첨가하였다. 고체를 용액으로부터 5분 내로 침전시키기 시작하였다. 90분 동안 교반한 후, 반응 혼합물을 물 125 mL로 희석하고, 이로 인해 무거운 미세 침전물이 발생하였다. 현탁액을 여과하여 미세 회색빛 고체를 단리시켰으며, 이를 역상 정제용 HPLC (정제용 HPLC 방법 13)에 의해 정제하여 회백색 분말: 0.2386 g (41.0% 수율)을 수득하였다. LCMS: m/z = 709.5 (M+H)+, 1.68분 (방법 3).
단계 3: 1 드램 바이알에서 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산 (0.020 g, 0.028 mmol)과 수산화리튬 1수화물, 1.0M 수용액 (0.282 mL, 0.282 mmol), 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 캡핑하고, 혼합물을 70℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하였다. 생성물 분획을 합하고, 진공 하에 농축시켜 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-9-(4-카르복시페닐)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산을 백색 분말 TFA 염 (0.0212 mg, 80% 수율)으로서 수득하였다. LCMS: m/z = 695.4 (M+H)+, 1.93분 (방법 5).
실시예 B18
4-((1S,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(1,1-디옥시도티오모르폴리노)프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1S,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(1,1-디옥시도티오모르폴리노)프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
고무 격막 및 교반막대를 갖는 1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-히드록시프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 (0.150 g, 0.207 mmol) 및 건조 클로로포름 (2 mL)을 합하였다. 혼합물을 얼음/염 조에서 냉각시키고, -10℃ 교반 슬러리에 트리플루오로메탄술폰산 무수물 (0.046 mL, 0.270 mmol)을 첨가하였다. 생성된 혼합물을 -10C에서 1시간 동안 교반한 다음, 혼합물에 티오모르폴린 1,1-디옥시드 (0.280 g, 2.075 mmol)를 첨가하고, 혼합물을 교반하면서 70℃로 가열하였다. 조 혼합물을 농축시키고, 최소량의 THF 및 MeOH 중에 재용해시키고, 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하였다. 따라서 생성물을 백색 유리질 고체 TFA 염 (0.0105 g, 4.3% 수율)으로서 단리시켰다. LCMS: m/z = 840.6 (M+H)+, 2.16분 (방법 5).
단계 2: 1 드램 바이알에서 테트라히드로푸란 (0.5 mL) 및 MeOH (0.5 mL) 중에 메틸 4-((1S,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(1,1-디옥시도티오모르폴리노)프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트, TFA 염 (0.0106 g, 9.92 μmol)과 수산화리튬 1수화물, 1.0M 수용액 (0.099 mL, 0.099 mmol)을 합하였다. 혼합물을 교반하면서 70℃로 60분 동안 가열하였다. 조 반응 혼합물을 질소 스트림을 통해 농축시킨 다음, 아세토니트릴/메탄올 중에 재용해시키고, 여과하고, 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 4-((1S,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(1,1-디옥시도티오모르폴리노)프로판-2-일)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0080 g, 65.6% 수율)으로서 수득하였다. LCMS: m/z = 826.6 (M+H)+, 1.94분 (방법 5).
실시예 B19
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 1의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1의 제조.
20 mL 섬광 바이알에서 에탄올 (1 mL) 중에 3% HCl 중 염화티타늄 (III) (0.766 mL, 1.21 mmol), 20 중량% 용액 및 아세트산나트륨 (0.099 g, 1.212 mmol)을 합하였다. 생성된 라벤더 색 용액을 빙조에서 냉각시키고, THF (2 mL)를 첨가하고, 이어서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-(히드록시이미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.175 g, 0.242 mmol)를 첨가하였다. 바이알을 PTFE 라이닝된 스크류마개로 캡핑하고, 생성된 현탁액을 실온에서 30분 동안 교반한 다음, 질소 스트림 하에 고체로 농축시키고, 고진공 하에 실온에서 밤새 두었다. THF (2 mL) 및 에탄올 (1 mL)을 첨가한 다음, 고체 수소화붕소나트륨 (0.092 g, 2.424 mmol)을 천천히 첨가하여, 반응 혼합물로부터 상당한 기체방출이 발생하였다. t=130분에서, 과량의 수소화붕소나트륨을 첨가 (스패튤라를 통해, 대략 추가로 10 당량 또는 그 초과)하여 상당한 기체방출이 즉시 발생하였고, 혼합물을 실온에서 총 16시간 동안 교반하였다. 반응 혼합물에 수성 염화암모늄을 천천히 첨가하여 반응을 켄칭하였다. 혼합물을 질소 스트림 하에 잔류물로 농축시킨 다음, 최소의 아세토니트릴/메탄올/물 중에 재용해시키고, 여과하고, 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 목적 물질을 단일 이성질체 베이지색 고체 TFA 염 (0.079 g, 31% 수율)으로서 수득하였다. LCMS: m/z = 708.5 (M+H)+, 2.06분 (방법 5).
단계 2: 1 드램 바이알에서 테트라히드로푸란 (0.5 mL) 및 MeOH (0.5 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-((R)-1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 TFA 염 (0.040 g, 0.038 mmol)과 수산화리튬 1수화물, 1.0M 수용액 (0.381 mL, 0.381 mmol)을 합하였다. 혼합물을 교반하면서 70℃로 30분 동안 가열하였다. 조 반응 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 1을 백색 분말 TFA 염 (0.040 g, 99% 수율)으로서 수득하였다. LCMS: m/z = 694.5 (M+H)+, 1.83분 (방법 5).
실시예 B20
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-모르폴리노에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-모르폴리노에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
20 mL 섬광 바이알에서 1,4-디옥산 (0.5 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.020 g, 0.019 mmol)과 1-브로모-2-(2-브로모에톡시)에탄 (0.00883 g, 0.038 mmol) 및 트리에틸아민 (0.016 mL, 0.114 mmol)을 합하였다. 혼합물을 85℃로 30분 동안 가열하였고, 이는 어떠한 반응도 발생시키지 않았다. 혼합물을 5 mL 마이크로웨이브 용기로 옮기고, 건조 아세토니트릴 (2 mL)로 희석하였다. 혼합물에 추가의 1-브로모-2-(2-브로모에톡시)에탄 (추가로 10 당량; 0.0445 g, 0.190 mmol) 뿐만 아니라 2,6-디-tert-부틸-4-메틸피리딘 (0.023 g, 0.114 mmol)을 첨가하였다. 생성된 혼합물을 마이크로웨이브에서 120℃로 90분 동안 가열하였다. 용기의 내용물을 질소 스트림 하에 농축시키고, 소량의 THF, 아세토니트릴 및 메탄올의 혼합물로 재용해시키고, 여과하고, 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하였다. 따라서 목적 생성물을 백색 고체로서 수득하고, 후속 단계로 직접 이행하였다. LCMS: m/z = 778.6 (M+H)+, 2.13분 (방법 5).
단계 2: 1 드램 바이알에서 테트라히드로푸란 (0.5 mL) 및 MeOH (0.5 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-모르폴리노에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.021 g, 0.019 mmol)과 수산화리튬 1수화물, 1.0M 수용액 (0.190 mL, 0.190 mmol)을 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 70℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 14)에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-모르폴리노에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0182 g, 2 단계에 걸쳐 86% 수율)으로서 수득하였다. LCMS: m/z = 764.6 (M+H)+, 1.85분 (방법 5).
실시예 B21
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세트아미도에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세트아미도에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
PTFE라이닝된 스크류마개 및 교반막대를 갖는 1 드램 바이알에서 건조 클로로포름 (1 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.019 g, 0.018 mmol)과 TEA (0.025 mL, 0.181 mmol)를 합하였다. 이어서, 아세틸 클로라이드 (1.930 μl, 0.027 mmol)를 한번에 첨가하고, 용액을 실온에서 30분 동안 교반하였다. 반응 혼합물을 질소 스트림 하에 농축시키고, 정제 없이 후속 단계로 직접 이행하였다. LCMS: m/z = 750.5 (M+H)+, 2.17분 (방법 5).
단계 2: PTFE 라이닝된 스크류마개를 갖는 1 드램 바이알에서 테트라히드로푸란 (0.5 mL) 및 MeOH (0.5 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세트아미도에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.014 g, 0.018 mmol)와 수산화리튬 1수화물, 1.0M 수용액 (0.180 mL, 0.180 mmol)을 함유하는 조 혼합물을 합하였다. 혼합물을 교반하면서 70℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 1회 주입으로 정제하였다. 따라서 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아세트아미도에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0108 g, 61.6% 수율)으로서 수득하였다. LCMS: m/z = 736.5 (M+H)+, 1.94분 (방법 5).
실시예 B22 및 실시예 B23
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-((메톡시카르보닐)아미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 및 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(2,2,2-트리플루오로아세트아미도)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-((메톡시카르보닐)아미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 및 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(2,2,2-트리플루오로아세트아미도)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
교반막대를 갖는 20 mL 섬광 바이알에서 건조 클로로포름 (1 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.019 g, 0.018 mmol)과 TEA (0.025 mL, 0.181 mmol)를 두었다. 혼합물에 메틸 클로로포르메이트 (2.102 μl, 0.027 mmol)를 첨가하고, 용액을 실온에서 15분 동안 교반하였다. 조 반응 혼합물을 질소 스트림 하에 잔류물로 농축시키고, 이를 후속 단계로 직접 이행하였다. LCMS: m/z = 766.5 (M+H)+, 2.24분 및 804.5 (M+H)+, 2.32분 (방법 5).
단계 2: PTFE 스크류마개를 갖는 1 드램 바이알에서 테트라히드로푸란 (0.5 mL) 및 MeOH (0.5 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-((메톡시카르보닐)아미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 및 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(2,2,2-트리플루오로아세트아미도)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (총 0.018 mmol)와 수산화리튬 1수화물, 1.0M 수용액 (0.180 mL, 0.180 mmol)을 함유하는 조 혼합물을 합하였다. 혼합물을 교반하면서 70℃로 25분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하였다. 따라서 2종의 표제 화합물을 단리시켰다:
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(1-((메톡시카르보닐)아미노)에틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산: 백색 분말 TFA 염 (0.0039 g, 21.9% 수율)으로서 단리됨. LCMS: m/z = 752.5 (M+H)+, 2.03분 (방법 5).
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(2,2,2-트리플루오로아세트아미도)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산: 백색 분말 TFA 염 (0.0066 g, 35.7% 수율)으로서 단리됨. LCMS: m/z = 790.5 (M+H)+, 2.12분 (방법 5).
실시예 B24 및 실시예 B25
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2-(술피노옥시)아세틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 및 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시아세틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
교반막대를 갖는 1 드램 바이알에 수산화나트륨, 3.0M 수성 (0.471 mL, 1.414 mmol)을 두었다. 바이알을 얼음/아세톤 조에서 -10℃로 냉각시켰다. 교반 용액에 브로민 (0.026 mL, 0.495 mmol)을 2분에 걸쳐 적가하였다. 생성된 황색/녹색 용액을 냉각 조에서 10분 동안 교반한 다음, 1,4-디옥산 (0.30 mL)을 매우 천천히 적가하고, 생성된 황색 용액을 추가로 5분 동안 차갑게 교반하였다. 차가운 황색 하이포브롬산 용액을 1,4-디옥산 (1.15 mL) 및 물 (0.20 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.050 g, 0.071 mmol)의 0℃ 차가운 동결 현탁액에 적가하였다. 생성된 황색 현탁액이 실온으로 즉시 가온되도록 하고, 실온에서 80분 동안 교반하였다. 혼합물에 포화 수성 아황산나트륨 용액 0.2 mL를 첨가하고, 혼합물을 80℃로 25분 동안 가열하였다. 혼합물을 질소 스트림 하에 고체 잔류물로 농축시켰다. 잔류물에 THF (2 mL), 메탄올 (0.5 mL), 물 (0.3 mL) 및 아세토니트릴 (0.3 mL)을 첨가하였다. 바이알을 진탕시키고, 내용물을 여과하여 고체를 제거하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하였다. 목적 화합물을 함유하는 분획을 합하고, 역상 정제용 HPLC (정제용 HPLC 방법 12)에 의해 재정제하였다. 따라서 2종의 표제 화합물을 단리시켰다:
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2-(술피노옥시)아세틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산: 백색 분말 (0.0091 g, 12.6% 수율)로서 단리됨. LCMS: m/z = 773.4 (M+H)+, 2.03분 (방법 5).
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-히드록시아세틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산: 백색 분말 (0.0042 g, 6.2% 수율)로서 단리됨. LCMS: m/z = 709.4 (M+H)+, 1.96분 (방법 5).
실시예 B26
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-((메톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-((메톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
1 드램 바이알에서 건조 1,4-디옥산 (0.5 mL) 중에 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산 (0.025 g, 0.035 mmol)과 트리에틸아민 (8.85 μl, 0.063 mmol) 및 디페닐포스포릴 아지드 (0.011 mL, 0.053 mmol)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 100℃로 75분 동안 밀봉하였다. 실온에서 혼합물에 메탄올 중 소듐 메톡시드, 0.5M 용액 (0.705 mL, 0.353 mmol)을 첨가하였다. 1시간 후, 반응 혼합물을 질소 스트림을 통해 농축시키고, 조 잔류물을 후속 단계 내의 에스테르의 가수분해로 이행하였다. LCMS: m/z = 738.7 (M+H)+, 2.25분 (방법 3).
단계 2: 1 드램 바이알에서 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-((메톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.026 g, 0.035 mmol)와 수산화리튬 1수화물, 1.0M 수용액 (0.352 mL, 0.352 mmol) 및 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 스크류마개로 캡핑하고, 혼합물을 교반하면서 70℃로 20분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-((메톡시카르보닐)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트를 백색 분말 TFA 염 (0.0113 g, 32.7% 수율)으로서 수득하였다. LCMS: m/z = 724.4 (M+H)+, 1.96분 (방법 3).
실시예 B27
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(모르폴린-4-카르보닐)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(모르폴린-4-카르보닐)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
1 드램 바이알에서 클로로포름 (1 mL) 중에 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산 (0.025 g, 0.035 mmol)과 모르폴린 (3.99 μl, 0.046 mmol), HATU (0.017 g, 0.046 mmol) 및 DIPEA (0.020 mL, 0.113 mmol)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 실온에서 밤새 교반하였다. 혼합물을 질소 스트림 하에 농축시킨 다음, 최소량의 아세토니트릴 및 메탄올의 혼합물 중에 재용해시켰다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 5)에 의해 정제하여 생성물을 백색 고체 TFA 염 (0.0276 g)으로서 수득하였다. LCMS: m/z = 778.5 (M+H)+, 2.26분 (방법 5).
단계 2: 1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(모르폴린-4-카르보닐)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.027 g, 0.027 mmol)과 수산화리튬 1수화물, 1.0M 수용액 (0.134 mL, 0.134 mmol) 및 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라 이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 60℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(모르폴린-4-카르보닐)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0323 g, 2 단계에 걸쳐 92% 수율)으로서 수득하였다. LCMS: m/z = 764.5 (M+H)+, 2.06분 (방법 5).
실시예 B28
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸카르바모일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸카르바모일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸카르바모일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트는, THF 중 메틸아민, 2.0M (0.176 mL, 0.353 mmol)을 모르폴린 대신 사용한 것을 제외하고는 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(모르폴린-4-카르보닐)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조에 대해 기재된 바와 유사한 절차에 의해 제조하였다. 또한, 정제용 HPLC 정제 후 물질을 상이한 조건 (정제용 HPLC 방법 12)을 사용하여 재정제해야하며, 이로써 목적 생성물을 백색 분말 (0.0142 g, 55.8% 수율)로서 수득하였다. LCMS: m/z = 722.6 (M+H)+, 2.02분 (방법 3).
단계 2: 1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸카르바모일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.0142 g, 0.020 mmol)와 수산화리튬 1수화물, 1.0M 수용액 (0.197 mL, 0.197 mmol) 및 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 60℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸카르바모일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0171 mg, 92% 수율)으로서 수득하였다. LCMS: m/z = 708.4 (M+H)+, 1.98분 (방법 5).
실시예 B29
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(3-메틸우레이도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-((아지도카르보닐)아미노)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
1 드램 바이알에서 건조 1,4-디옥산 (2 mL) 중에 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산 (0.085 g, 0.120 mmol)과 트리에틸아민 (0.030 mL, 0.216 mmol) 및 디페닐포스포릴 아지드 (0.028 mL, 0.132 mmol)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 실온에서 100분 동안 교반한 다음, 100℃로 가열하고, 2시간 동안 교반하였다. 혼합물에 추가의 디페닐포스포릴 아지드 (0.028 mL, 0.132 mmol)를 첨가하고, 혼합물을 100℃로 재가열하고, 1시간 동안 교반하였다. 조 혼합물을 추가 정제 없이 직접 후속 단계로 이행하였다. LCMS: m/z = 749.6 (M+H)+, 2.30분 (방법 3).
단계 2. 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(3-메틸우레이도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
1 드램 바이알에서 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-((아지도카르보닐)아미노)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.030 g, 0.040 mmol)와 THF 중 메탄아민, 1.0M (0.400 mL, 0.400 mmol)을 합하였다. 혼합물을 실온에서 1시간 동안 교반하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 목적 생성물을 백색 분말 TFA 염 (0.0193 g, 2 단계에 걸쳐 50% 수율)으로서 수득하였다. LCMS: m/z = 737.4 (M+H)+, 2.14분 (방법 5).
단계 3: 1 드램 바이알에서 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(3-메틸우레이도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.019 g, 0.020 mmol)과 수산화리튬 1수화물, 1.0M 수용액 (0.197 mL, 0.197 mmol) 및 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 60℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(3-메틸우레이도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0203 g, 106% 수율)으로서 수득하였다. LCMS: m/z = 723.4 (M+H)+, 1.93분 (방법 5).
실시예 B30
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(피롤리딘-1-카르복스아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(피롤리딘-1-카르복스아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
1 드램 바이알에서 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-((아지도카르보닐)아미노)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.030 g, 0.040 mmol)과 피롤리딘 (0.033 mL, 0.400 mmol)을 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 실온에서 1시간 동안 교반하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하였다. 따라서 목적 생성물을 백색 분말 TFA 염 (0.0178 g, 44.3% 수율)으로서 수득하였다. LCMS: m/z = 777.5 (M+H)+, 2.16분 (방법 5).
단계 2: 1 드램 바이알에서 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(피롤리딘-1-카르복스아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.019 g, 0.019 mmol)과 수산화리튬 1수화물, 1.0M 수용액 (0.189 mL, 0.189 mmol) 및 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 60℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(피롤리딘-1-카르복스아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0163 g, 85% 수율)으로서 수득하였다. LCMS: m/z = 763.4 (M+H)+, 2.04분 (방법 5).
실시예 B31
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1,3,4-옥사디아졸-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-포르밀히드라진카르보닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
1 드램 바이알에서 클로로포름 (1 mL) 중에 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산 (0.050 g, 0.071 mmol)과 포름산 히드라지드 (8.47 mg, 0.141 mmol), HATU (0.035 g, 0.092 mmol) 및 DIPEA (0.039 mL, 0.226 mmol)를 합하였다. 혼합물을 실온에서 26시간 동안 교반하였다. 혼합물을 질소 스트림을 통해 농축시킨 다음, 최소량의 아세토니트릴/MeOH의 혼합물 중에 재용해시키고, 여과하고, 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하였다. 따라서 목적 생성물을 백색 고체 TFA 염 (0.0396 g, 57.4% 수율)으로서 단리시켰다. LCMS: m/z = 751.4 (M+H)+, 2.11분 (방법 5).
단계 2. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1,3,4-옥사디아졸-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(2-포르밀히드라진카르보닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.020 g, 0.020 mmol) 및 DIPEA (0.036 mL, 0.204 mmol)와 아세토니트릴 (0.5 mL)을 합하였다. 혼합물에 p-톨루엔술포닐 클로라이드 (0.031 g, 0.163 mmol)를 첨가하였다. 혼합물을 실온에서 1시간 동안 교반하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 12)에 의해 정제하였다. 따라서 목적 생성물 (0.0084 g, 56.1% 수율)을 수득하였다. LCMS: m/z = 733.7 (M+H)+, 2.32분 (방법 3).
단계 3: 1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1,3,4-옥사디아졸-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.0084 g, 0.011 mmol)와 수산화리튬 1수화물, 1.0M 수용액 (0.115 mL, 0.115 mmol) 및 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 70℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1,3,4-옥사디아졸-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0106 g, 97% 수율)으로서 수득하였다. LCMS: m/z = 719.4 (M+H)+, 1.92분 (방법 5).
실시예 B32
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(2-옥소피롤리딘-1-일)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(2-옥소피롤리딘-1-일)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
5mL 마이크로웨이브 바이알에서 아세토니트릴 (0.5 mL) 및 1,4-디옥산 (0.5 mL)의 혼합물 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.025 g, 0.035 mmol)와 4-클로로부타노일 클로라이드 (5.94 μl, 0.053 mmol) 및 2,6-디-tert-부틸-4-메틸피리딘 (0.029 g, 0.141 mmol)을 합하였다. 혼합물을 실온에서 5분 동안 교반한 다음, 마이크로웨이브 반응기에서 120℃로 1시간 동안 가열하였다. 혼합물이 실온으로 냉각되도록 한 다음, 미네랄 오일 중 수소화나트륨 60% NaH 분산액 (과량, 대략 20 mg)을 혼합물에 첨가하여 상당한 기체방출을 야기하였다. 혼합물을 실온에서 24시간 동안 교반하였다. 조 혼합물을 추가 조작 없이 후속 단계로 이행하였다. LCMS: m/z = 776.5 (M+H)+, 2.18분 (방법 5).
단계 2: THF 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(2-옥소피롤리딘-1-일)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.027 g, 0.035 mmol) 및 과량의 수소화나트륨을 함유하는 조 반응 혼합물을 물 (1 mL)을 천천히 첨가하여 켄칭하여 동적인 기체방출을 발생시켰다. 이어서, 메탄올 (1 mL)을 첨가하고, 생성된 혼합물을 60℃로 30분 동안 가열하였다. 혼합물을 질소 스트림을 통해 대략 0.5 mL로 농축시키고, 아세토니트릴 (1 mL) 및 메탄올 (1 mL)로 희석한 다음, 여과하고, 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(2-옥소피롤리딘-1-일)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0270 g, 2 단계에 걸쳐 76% 수율)으로서 수득하였다. LCMS: m/z = 762.5 (M+H)+, 1.98분 (방법 5).
실시예 B33
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아미노-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
20 mL 섬광 바이알에서 건조 1,4-디옥산 (5 mL) 중에 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산, 트리에틸암모늄 염 (0.100 g, 0.123 mmol)과 디페닐포스포릴 아지드 (0.080 mL, 0.370 mmol) 및 트리에틸아민 (0.034 mL, 0.247 mmol)을 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 80℃로 2시간 동안 가열하였다. 혼합물이 실온으로 냉각되도록 하고, 실온에서 1.5시간 동안 정치시켰다. 신속하게 교반하는 혼합물에 수산화나트륨, 1.0M 수성 (4.93 mL, 4.93 mmol)을 한번에 첨가하였다. 생성된 탁한 혼합물을 실온에서 30분 동안 신속히 교반하였다. 혼합물을 질소 스트림을 통해 농축시키고, 역상 정제용 HPLC (정제용 HPLC 방법 15)에 의해 정제하였다. 따라서 목적 생성물을 백색 고체 TFA 염 (0.0739 g, 59.5% 수율)으로서 단리시켰다. LCMS: m/z = 666.3 (M+H)+, 1.79분 (방법 5).
실시예 B34
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(디메틸아미노)-3a-((2-((2-((2-메톡시에틸)술포닐)에틸)(메틸)아미노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아미노-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조
1 드램 바이알에서 건조 1,4-디옥산 (2 mL) 중에 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산 (0.150 g, 0.212 mmol)과 디페닐포스포릴 아지드 (0.114 mL, 0.529 mmol) 및 트리에틸아민 (0.118 mL, 0.846 mmol)을 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 80℃로 45분 동안 가열하였다. 추가의 디페닐포스포릴 아지드 (0.057 mL, 0.265 mmol)를 첨가하고, 혼합물을 85℃로 추가로 20분 동안 가열하였다. 혼합물을 열로부터 제거하고, 실온으로 냉각되도록 하고, 여기에 수산화나트륨, 3.0M 수성 (1.41 mL, 4.23 mmol)을 첨가하였다. 45분 교반한 후, 혼합물을 빙조에서 냉각시키고, 여기에 염산, 12M (0.353 mL, 4.23 mmol)을 천천히 첨가하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하였다. 목적 생성물을 백색 분말 TFA 염 (0.0558 g, 25.8% 수율)으로서 단리시켰다. LCMS: m/z = 680.4 (M+H)+, 1.93분 (방법 5).
단계 2. 4-(2-(((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(디메틸아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-일)아미노)에틸)-4-메틸티오모르폴린-4-윰 1,1-디옥시드의 제조.
1 드램 바이알에서 클로로포름 (0.5 mL) 중에 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아미노-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.021 g, 0.021 mmol)과 2,6-디-tert-부틸-4-메틸피리딘 (0.042 g, 0.205 mmol)을 합하였다. 이 교반 혼합물에 메틸 트리플루오로메탄술포네이트 (0.011 mL, 0.103 mmol)를 첨가하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 70℃에서 30분 동안 교반하였다. 추가로 5 당량의 메틸 트리플루오로메탄술포네이트 (0.011 mL, 0.103 mmol)를 첨가하고, 혼합물을 70℃로 추가로 105분 동안 재가열하였다. 혼합물을 질소 스트림을 통해 농축시키고, 최소의 메탄올과 첨가된 소량의 THF 중에 재용해시켰다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하였다. 따라서 단리된 생성물을 후속 단계로 직접 이행하였다. LCMS: m/z = 722.4 (M+H)+, 2.04분 (방법 5).
단계 3: 1 드램 바이알에서 4-(2-(((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(디메틸아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-일)아미노)에틸)-4-메틸티오모르폴린-4-윰 1,1-디옥시드 (0.010 g, 9.12 μmol)와 1.0M 수성 수산화리튬 수화물 (0.091 mL, 0.091 mmol) 및 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 70℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하여 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(디메틸아미노)-3a-((2-((2-((2-메톡시에틸)술포닐)에틸)(메틸)아미노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0048 g, 2 단계에 걸쳐 20% 수율)으로서 수득하였다. LCMS: m/z = 740.4 (M+H)+, 1.88분 (방법 5).
실시예 B35
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(메틸아미노)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(메틸아미노)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
1 드램 바이알에서 클로로포름 (0.5 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.020 g, 0.028 mmol)와 2,6-디-tert-부틸-4-메틸피리딘 (0.029 g, 0.141 mmol)을 합하였다. 이 교반 혼합물에 메틸 트리플루오로메탄술포네이트 (4.98 μl, 0.045 mmol)를 첨가하고, PTFE 라이닝된 스크류마개를 설치하고, 혼합물을 실온에서 45분 동안 교반하였다. 혼합물에 추가의 메틸 트리플루오로메탄술포네이트 (7 μl, 대략 0.063 mmol, 2.25 당량)를 첨가하고, 실온에서 1.5시간 동안 교반하였다. 혼합물에 THF 중 1.0M 암모니아를 첨가한 다음, 혼합물을 질소 스트림 하에 잔류물로 농축시키고, 최소량의 1:1 THF/MeOH 혼합물 중에 재용해시키고, 역상 정제용 HPLC (정제용 HPLC 방법 12)에 의해 정제하였다. 목적 생성물을 함유하는 분획을 합하고, 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 재정제하여 목적 생성물을 백색 분말 TFA 염 (0.0123 g, 40.9% 수율)으로서 수득하였다. LCMS: m/z = 722.3 (M+H)+, 2.01분 (방법 5).
단계 2: 1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(메틸아미노)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.0093 g, 8.74 μmol)과 1.0M 수성 수산화리튬 수화물 (0.087 mL, 0.087 mmol), 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 70℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 16)에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-(메틸아미노)에틸)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 유리질 고체 TFA 염 (0.0078 g, 80% 수율)으로서 수득하였다. LCMS: m/z = 708.4 (M+H)+, 1.79분 (방법 5).
실시예 B36
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세트아미도-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
1 드램 바이알에서 건조 1,4-디옥산 (1 mL) 중에 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산 (0.020 g, 0.028 mmol)과 디페닐포스포릴 아지드 (0.015 mL, 0.071 mmol) 및 트리에틸아민 (0.016 mL, 0.113 mmol)을 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 80℃로 20분 동안 가열하였다. 이어서, 반응 혼합물을 피펫을 통해 수산화나트륨, 3.0M 수성 (0.235 mL, 0.705 mmol)을 함유하는 80℃ 바이알로 직접 첨가하였다. 혼합물을 1분 후에 열로부터 제거하였다. 혼합물을 아세트산 무수물 (0.135 g, 1.33 mmol)로 처리하고, 생성된 혼합물을 70℃로 10분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 16)에 의해 정제하여 목적 생성물을 무색 고체 TFA 염 (0.0149 g, 54% 수율)으로서 수득하였다. LCMS: m/z = 708.3 (M+H)+, 1.92분 (방법 5).
실시예 B37 및 실시예 B38
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸아미노)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 및 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(디메틸아미노)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸아미노)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 및 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(디메틸아미노)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
2개의 개별 단계 1 및 단계 2 실험을 수행하였다. 두 실험으로부터의 단계 2 반응 혼합물 후의 최종 생성된 조 물질을 합하고, 정제하여 표제 화합물을 수득하였다:
실험 1: 1 드램 바이알에서 클로로포름 (0.5 mL) 중에 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아미노-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.021 g, 0.021 mmol)과 2,6-디-tert-부틸-4-메틸피리딘 (0.042 g, 0.205 mmol)을 합하였다. 이 교반 혼합물에, 메틸 트리플루오로메탄술포네이트 (0.011 mL, 0.103 mmol)를 첨가하였다. PTFE라이닝된 스크류마개를 설치하고, 혼합물을 실온에서 밤새 교반하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 16)에 의해 정제하였다. 따라서 2종의 목적 생성물의 혼합물을 정제용 HPLC로부터 TFA 염 (0.0123 g)으로서 수득하였다. 물질을 후속 단계 (단계 2 실험 1)로 직접 이행하였다. LCMS: m/z = 694.6 (M+H)+, 1.92분 및 708.6 (M+H)+, 2.07분 (방법 3).
실험 2: 1 드램 바이알에서 클로로포름 (0.5 mL) 중에 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아미노-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.021 g, 0.021 mmol)과 2,6-디-tert-부틸-4-메틸피리딘 (0.042 g, 0.205 mmol)을 합하였다. 이 교반 혼합물에 메틸 트리플루오로메탄술포네이트 (0.011 mL, 0.103 mmol)를 첨가하였다. PTFE라이닝된 스크류마개를 설치하고, 혼합물을 70℃로 30분 동안 가열하였다. 추가의 메틸 트리플루오로메탄술포네이트 (0.011 mL, 0.103 mmol)를 첨가하고, 혼합물을 70℃로 105분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하였다. 따라서 2종의 목적 생성물의 혼합물을 정제용 HPLC로부터 TFA 염 (0.010 g)으로서 수득하였다. 물질을 후속 단계 (단계 2 실험 2)로 직접 이행하였다.
단계 2:
실험 1: 1 드램 바이알에서 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸아미노)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 및 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(디메틸아미노)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.0123 g, 0.012 mmol)을 함유하는 단계 1, 실험 1로부터의 혼합물과 1M 수성 수산화리튬 수화물 (0.117 mL, 0.117 mmol), 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 70℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 16)에 의해 정제하였다.
실험 2: 1 드램 바이알에서 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸아미노)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 및 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(디메틸아미노)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.010 g, 9.52 μmol)을 함유하는 단계 1, 실험 2로부터의 혼합물과 수산화리튬 수화물 (0.095 mL, 0.095 mmol), 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 70℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하였다.
단계 2 실험 1 및 단계 2 실험 2로부터의 합한 잔류물의 재정제: 단계 2 실험 1 및 단계 2 실험 2로부터의 정제용 HPLC 정제로부터의 생성물을 함유하는 분획을 합하고, 역상 정제용 HPLC (정제용 HPLC 방법 17)에 의해 재정제하였다. 농축된 유사 생성물 분획을 88% 아세토니트릴, 10% 물, 2%TFA의 혼합물로 처리하고, 이어서 진공 하에 재농축시켜 TFA 염으로 전환시켰다. 따라서 분리된 목적 생성물을 TFA 염으로서 수득하였다.
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸아미노)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (실시예 B37): 이 물질을 무색 고체 TFA 염 (0.0086 g, 2 단계에 걸쳐 18% 합한 수율)으로서 회수하였다. LCMS: m/z = 680.4 (M+H)+, 1.73분 (방법 5).
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(디메틸아미노)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (실시예 B38): 이 물질을 무색 고체 TFA 염 (0.0097 g, 2 단계에 걸쳐 21% 합한 수율)으로서 회수하였다. LCMS: m/z = 694.4 (M+H)+, 1.76분 (방법 5).
실시예 B39
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-(디메틸아미노)에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 1의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-(디메틸아미노)에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 및 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-(디메틸아미노)에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2의 제조.
15 mL 압력 용기에서, MeOH (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.100 g, 0.141 mmol)의 용액을 THF 중 디메틸아민, 2.0M (1.061 mL, 2.122 mmol), 아세트산 (0.121 mL, 2.122 mmol) 및 소듐 시아노보로히드라이드 (0.019 g, 0.283 mmol)로 처리하였다. 용기를 밀봉하고, 혼합물을 오일 조에서 110℃로 6일 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 16)에 의해 정제하였다. 따라서 목적 생성물을 단리시켰다:
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-(디메틸아미노)에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1은 주요 생성물이고, 백색 고체 TFA 염 (0.0246 g, 16.1% 수율)으로서 회수하였다. LCMS: m/z = 736.4 (M+H)+, 2.05분 (방법 5).
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-(디메틸아미노)에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2는 부차적 생성물이고, 백색 점착성 고체 TFA 염 (0.0116 g, 7.6% 수율)으로서 회수하였다.
단계 2: 1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-((R)-1-(디메틸아미노)에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 TFA 염 (0.0246 g, 0.023 mmol)과 1M 수성 수산화리튬 수화물 (0.228 mL, 0.228 mmol), 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 80℃로 20분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 16)에 의해 정제하였다. 필수적으로 생성물 분획을 합하고, 역상 정제용 HPLC (정제용 HPLC 방법 15)에 의해 재정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-(디메틸아미노)에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 1을 백색 유리 고체 TFA 염 (0.0151 g, 62.2% 수율)으로서 수득하였다. LCMS: m/z = 722.4 (M+H)+, 1.80분 (방법 5).
실시예 B40
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-(디메틸아미노)에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 2의 제조.
1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-((R)-1-(디메틸아미노)에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2 TFA 염 (0.0116 g, 10.76 μmol)과 1M 수성 수산화리튬 수화물 (0.108 mL, 0.108 mmol), 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 80℃로 20분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 3)에 의해 정제하였다. 목적 생성물을 점착성 검 TFA 염 (0.0053 g, 46.3% 수율)으로서 단리시켰다. LCMS: m/z = 722.4 (M+H)+, 1.82분 (방법 5).
실시예 B41
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 2의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1 및 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2의 제조.
MeOH (0.5 mL) 및 THF (0.5 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.050 g, 0.071 mmol)의 용액에 아세트산암모늄 (0.055 g, 0.707 mmol) 및 소듐 시아노보로히드라이드 (7.02 mg, 0.106 mmol)를 첨가하였다. 반응 혼합물을 실온에서 24시간 동안 교반한 다음, 70℃로 6일 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 16)에 의해 정제하여 목적 생성물을 수득하였다:
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 1: 무색 고체 TFA 염 (0.0233 g, 31.4% 수율)으로서 단리됨. LCMS: m/z = 708.4 (M+H)+, 2.01분 (방법 5).
메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2: 무색 고체 TFA 염 (0.0090 g, 12.1% 수율)으로서 단리됨. LCMS: m/z = 708.4 (M+H)+, 2.06분 (방법 5).
단계 2. 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 이성질체 2의 제조.
1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-((R)-1-아미노에틸)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 이성질체 2 TFA 염 (0.0081 g, 7.71 μmol)과 1M 수성 수산화리튬 수화물 (0.077 mL, 0.077 mmol), 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 80℃로 20분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 16)에 의해 정제하였다. 목적 화합물을 백색 유리질 고체 TFA 염 (0.0076 g, 93% 수율)으로서 단리시켰다. LCMS: m/z = 694.4 (M+H)+, 1.83분 (방법 5).
실시예 B42
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(히드록시메틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. (에틸 탄산) (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산 무수물의 제조.
1 드램 바이알에서 건조 클로로포름 중에 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산, 트리에틸암모늄 염 (0.020 g, 0.025 mmol)과 에틸 클로로포르메이트 (0.014 ml, 0.148 mmol) 및 트리에틸아민 (6.87 μl, 0.049 mmol)을 합하였다. 혼합물을 실온에서 10분 동안 교반하였다. 조 반응 혼합물을 후속 단계에 직접 사용하였다. LCMS: m/z = 781.4 (M+H)+, 2.30분 (방법 5).
단계 2. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(히드록시메틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
클로로포름 (1 mL) 중 (에틸 탄산) (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-1-카르복실산 무수물 (0.020 g, 0.025 mmol)을 함유하는 조 혼합물을 THF (0.75 mL)로 희석하고, 수소화붕소나트륨 (9.46 mg, 0.250 mmol)으로 처리하였다. 5분 후, 어떠한 기체 발생도 명백하지 않았고, 남은 고체 수소화붕소나트륨이 혼합물 중에 부유하였다. 혼합물에 건조 메탄올 (0.75 mL)을 첨가하였고, 발포가 즉시 발생하였다. 15분 후, 추가의 수소화붕소나트륨 (9.46 mg, 0.250 mmol)을 첨가하고, 혼합물을 질소 하에 밤새 교반하였다. 조 혼합물을 질소 스트림 하에 농축시킨 다음, 최소량의 MeOH 및 THF의 혼합물 중에 재용해시키고, 역상 정제용 HPLC (정제용 HPLC 방법 12)에 의해 정제하였다. 목적 생성물을 백색 유리 고체 (0.0080 g, 93% 수율)로서 수득하였다. LCMS: m/z = 695.4 (M+H)+, 2.20분 (방법 5).
단계 3: 1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(히드록시메틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.008 g, 0.012 mmol)와 1M 수성 수산화리튬 수화물 (0.115 mL, 0.115 mmol), 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 80℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 18)에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-1-(히드록시메틸)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (0.0055 g, 52.6% 수율)을 수득하였다. LCMS: m/z = 681.6 (M+H)+, 1.99분 (방법 5).
실시예 B43 및 실시예 B44
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2,2,2-트리플루오로아세트아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 및 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2,2,2-트리플루오로-N-메틸아세트아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아미노-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 및 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸아미노)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
100 mL 둥근 바닥 플라스크에서 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아미노-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 TFA 염 (0.410 g, 0.407 mmol)과 건조 DCM (15 mL) 및 메탄올 (15 mL)을 합하였다. 용액에 TMS-디아조메탄 (1.424 mL, 2.85 mmol)을 첨가하였다. 대략 절반의 디아조메탄 용액을 첨가한 후, 약간의 발열 및 상당한 기체방출이 뒤따랐다. 혼합물을 실온에서 3시간 동안 교반한 다음, 진공 하에 고체 잔류물로 농축시켰다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 4)에 의해 정제하였다. 따라서 2종의 목적 생성물의 혼합물을 미황색 고체 TFA 염 (0.259 g, 70.2% 수율)으로서 수득하였다. 혼합물을 후속 단계로 직접 이행하였다. LCMS: m/z = 680.5 (M+H)+ 및 694.6 (M+H)+, 2.04분 (방법 5).
단계 2. 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2,2,2-트리플루오로아세트아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 및 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2,2,2-트리플루오로-N-메틸아세트아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
건조 THF (1 mL) 중 옥살릴 디클로라이드 (14.0 mg; 0.110 mmol)의 표준 용액을 제조하였다. 1 드램 바이알에서 건조 THF (0.5 mL) 중에 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아미노-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 및 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(메틸아미노)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (0.020 g, 0.022 mmol)을 함유하는 단계 1로부터의 혼합물과 DIPEA (0.019 mL, 0.110 mmol)를 합하였다. 이 혼합물에, 옥살릴 디클로라이드 (1.396 mg, 0.011 mmol)를 함유하는 표준 옥살릴 디클로라이드/THF 용액 0.1 mL를 첨가하고, 생성된 혼합물을 실온에서 3시간 동안 교반하였다. 이 혼합물에 추가 당량의 옥살릴 디클로라이드 (1.396 mg, 0.011 mmol) (표준 용액 0.1 mL)를 첨가하였다. 혼합물을 실온에서 1시간 동안 교반한 다음, 추가 당량의 옥살릴 디클로라이드 (1.396 mg, 0.011 mmol) (표준 용액 0.1 mL)를 첨가하고, 실온에서 30분 동안 교반하였다. 혼합물을 질소 스트림 하에 농축시키고, 조 잔류물을 후속 단계로 그대로 직접 이행하였다. LCMS: m/z = 776.5 (M+H)+, 2.28분 및 m/z = 790.6 (M+H)+, 2.47분 (방법 5).
단계 3: 1 드램 바이알에서 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2,2,2-트리플루오로아세트아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 및 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2,2,2-트리플루오로-N-메틸아세트아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.017 g, 0.022 mmol)를 함유하는 단계 2로부터의 조 반응 혼합물을 1M 수성 수산화리튬 수화물 (0.176 mL, 0.176 mmol)로 처리하고, MeOH (0.3 mL)를 첨가하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 70℃로 30분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 6)에 의해 정제하였다. 따라서 2종의 목적 생성물을 수득하였다.
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2,2,2-트리플루오로아세트아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산은 정제용 HPLC로부터 용리된 제1 화합물이었다. 이 생성물을 백색 분말 TFA 염 (0.0110 g, 50% 수율)으로서 단리시켰다. LCMS: m/z = 762.4 (M+H)+, 2.11분 (방법 5).
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(2,2,2-트리플루오로-N-메틸아세트아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산은 정제용 HPLC로부터 용리된 제2 화합물이었다. 이 생성물을 백색 분말 TFA 염 (0.0042 g, 18% 수율)으로서 단리시켰다. LCMS: m/z = 776.5 (M+H)+, 2.13분 (방법 5).
실시예 B45
4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(4-(3-(트리플루오로메틸)-3H-디아지린-3-일)벤즈아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(4-(3-(트리플루오로메틸)-3H-디아지린-3-일)벤즈아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
1 드램 바이알에서 클로로포름 (1 mL) 중에 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아미노-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.025 g, 0.037 mmol) 및 4-(3-(트리플루오로메틸)-3H-디아지린-3-일)벤조산 (11.00 mg, 0.048 mmol)과 HATU (0.022 g, 0.059 mmol) 및 DIPEA (0.019 mL, 0.110 mmol)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 알루미늄 호일로 감싸고, 내용물을 실온에서 밤새 교반하였다. 조 혼합물을 질소 스트림 하에 잔류물로 농축시킨 다음, 혼합물을 최소량의 메탄올 중에 재용해시켰다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 16)에 의해 정제하였다. 목적 생성물을 백색 고체 TFA 염 (0.0290 g, 80% 수율)으로서 단리시켰다. LCMS: m/z = 892.6 (M+H)+, 2.41분 (방법 5).
단계 2: 1 드램 바이알에서 메틸 4-((1R,3aR,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(4-(3-(트리플루오로메틸)-3H-디아지린-3-일)벤즈아미도)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.0295 g, 0.033 mmol)를 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)의 혼합물 중에 용해시킨 다음, 혼합물을 1M 수성 수산화리튬 수화물 (0.132 mL, 0.132 mmol)로 처리하였다. 빛의 진입을 차단하기 위해 바이알을 알루미늄 호일로 감싸고, PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 70℃로 45분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 19)에 의해 정제하여 목적 생성물을 백색 고체 TFA 염 (0.0190 g, 53.9% 수율)으로서 수득하였다. LCMS: m/z = 878.6 (M+H)+, 2.25분 (방법 5).
실시예 B46
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-아미노-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-아미노-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
혼합물 디올 부분입체이성질체 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-(1,2-디히드록시프로판-2-일)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (12.26 g, 16.59 mmol)를 THF (450 mL) 및 물 (150 mL)의 혼합물 중에 용해시키고, 생성된 용액을 빙조에서 냉각시켰다. 과아이오딘산나트륨 (7.10 g, 33.2 mmol)을 첨가하였다. 투명한 용액은 빠르게 탁해졌고, 백색 솜털모양의 고체가 침전되었다. 혼합물을 실온에서 30분 동안 교반한 다음, 클로로포름 (1200 mL) 및 물 (500 mL)로 희석하고, 생성된 혼합물을 진탕시키고, 상을 분리하였다. 수층을 클로로포름 (2 x 400 mL)으로 다시 추출하였다. 유기물을 합하고, 황산나트륨 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 칼럼 크로마토그래피 (300 g 실리카, 6 칼럼 부피에 걸쳐 용리 구배 100% DCM에서 20:1 DCM:MeOH, 8 칼럼 부피 동안 20:1 DCM:MeOH 유지)에 의해 정제하여 목적 생성물을 백색 고체 (1.70 g, 18.8% 수율)로서 수득하였다. LCMS: m/z = 546.4 (M+H)+, 2.36분 (방법 5).
단계 2: 1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-아미노-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.035 g, 0.064 mmol)와 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)의 혼합물을 합한 다음, 혼합물을 1M 수성 수산화리튬 수화물 (0.257 mL, 0.257 mmol)로 처리하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 70℃로 45분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 16)에 의해 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-아미노-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 백색 분말 TFA 염 (0.0253 g, 60% 수율)으로서 수득하였다. LCMS: m/z = 532 (M+H)+, 2.11분 (방법 5).
실시예 B47
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
1 드램 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-1-아세틸-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (0.0262 g, 0.028 mmol)와 수산화리튬 1수화물, 1.0M 수용액 (0.249 mL, 0.249 mmol), 테트라히드로푸란 (0.3 mL) 및 MeOH (0.3 mL)를 합하였다. 바이알을 PTFE 라이닝된 스크류마개로 밀봉하고, 혼합물을 교반하면서 70℃로 35분 동안 가열하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 2)에 의해 정제하여 표제 화합물을 백색 분말 TFA 염 (0.0208 g, 80% 수율)으로서 수득하였다. LCMS: m/z = 693.6 (M+H)+, 2.16분 (방법 5).
실시예 B48
(1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-9-(4-카르복시페닐)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조.
단계 1. (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-벤질 1-((S)-2,2-디브로모-1-메틸시클로프로필)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조.
브로모포름 (29.0 mL, 332 mmol) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(프로프-1-엔-2-일)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (11.0 g, 16.6 mmol) 및 N-벤질-N,N-디에틸에탄아미늄 브로마이드 (0.903 g, 3.32 mmol)의 용액을 신속히 교반하고, 수산화나트륨 (13.3 g, 332 mmol)의 수성 (50 mL) 용액으로 천천히 처리하였다. 생성된 2상 혼합물을 신속히 교반하면서 63℃로 가열하였다. 추가의 브로모포름 (29.0 mL, 332 mmol) 및 수성 (50 mL) NaOH (13.3 g, 332 mmol)를 첨가하고, 혼합물을 63℃에서 60시간 동안 신속히 교반하였다. 혼합물을 물 (700 mL)로 천천히 희석하고, DCM (3 x 200 mL)으로 세척하였다. 유기 추출물을 합하고, 진공 하에 담갈색 오일로 농축시켰다. 실리카 겔 칼럼 크로마토그래피 (구배 100% 헥산에서 30:1 헥산:EtOAc)로 정제하여 백색 고체 6.85 g (49.5% 수율)을 수득하였다.
단계 2. (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조.
톨루엔 (100 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bS)-벤질 1-((S)-2,2-디브로모-1-메틸시클로프로필)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (6.82 g, 8.17 mmol)의 용액을 트리-n-부틸주석 히드라이드 (14.3 g, 13.1 mL, 49.0 mmol)에 이어서 AIBN (0.067 g, 0.409 mmol)으로 처리하였다. 혼합물을 교반하면서 100℃에서 18시간 동안 가열하였다. 혼합물을 진공 하에 농축시키고, 실리카 겔 칼럼 크로마토그래피 (구배 100% 헥산에서 25:1 헥산:EtOAc)에 의해 정제하였다. 생성물 분획을 합하고, 진공 하에 농축시킨 다음, 잔류물을 DCM 중에 재용해시키고, 90% 실리카 및 10 중량% KF로 구성된 칼럼을 통해 DCM을 용리액으로서 사용하여 통과시켰다.
진공 하에 농축시켜 백색 발포체 고체 5.48 g (99%)을 수득하였다.
단계 3. (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-tert-부틸디메틸실릴 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트의 제조.
1,2-디클로로에탄 (100 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-벤질 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (5.34 g, 7.89 mmol)의 용액에 트리에틸아민 (1.76 mL, 12.6 mmol), tert-부틸디메틸실란 (2.62 mL, 1.84 g, 15.8 mmol) 및 아세트산팔라듐 (II) (0.443 g, 1.97 mmol)을 첨가하였다. 혼합물을 60℃로 22시간 동안 가열하였다. 조 반응 혼합물을 실리카 겔/셀라이트 플러그를 통해 10:1 헥산:EtOAc를 용리액으로서 사용하여 통과시켰다. 진공 하에 농축시켜 백색 고체 6.34 g (>100% 수율)을 수득하였으며, 이를 추가 정제 없이 후속 단계로 이행하였다.
단계 4. (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산의 제조.
1,4-디옥산 (100 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-tert-부틸디메틸실릴 9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실레이트 (5.53 g, 7.89 mmol)의 용액에 THF 중 TBAF (11.8 mL, 11.8 mmol), 1.0M을 첨가하였다. 혼합물을 2.5시간 동안 교반한 다음, 1M 수성 HCl 400 mL를 첨가하고, 백색 고체의 생성된 현탁액을 실온에서 10분 동안 교반하였다. 고체 침전물을 여과에 의해 단리시키고, 건조시켜 표제 화합물을 백색 분말 (4.43 g, 96% 수율)로서 수득하였다. LCMS: m/e 587.4 (M+H)+, 4.58분 (방법 5).
단계 5: 20 mL 섬광 바이알에서 THF (1 mL), 메탄올 (1 mL) 및 물 (0.5 mL) 중에 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (0.080 g, 0.136 mmol)과 수산화리튬 1수화물 (0.023 g, 0.545 mmol)을 합하였다. 현탁 혼합물을 60℃로 1시간 동안 가온하였다. 조 혼합물을 역상 정제용 HPLC (정제용 HPLC 방법 26)에 의해 정제하였다. 목적 생성물을 백색 분말 (0.042 g, 51.6% 수율)로서 수득하였다. LCMS: m/e 571.7 (M-H)-, 2.35분 (방법 3).
실시예 B49
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-이소시아네이토-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
1,4-디옥산 (60 mL) 중 (1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-9-(4-(메톡시카르보닐)페닐)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-3a-카르복실산 (3.50 g, 5.96 mmol)의 슬러리에 트리에틸아민 (1.50 mL, 10.7 mmol) 및 디페닐포스포릴 아지드 (1.93 mL, 2.46 g, 8.95 mmol)를 첨가하였다. 생성된 슬러리를 100℃로 5시간 동안 가열하였다. 혼합물을 실온으로 냉각시키고, EtOAc로 희석하고, 1N NaOH (2 x 70 mL)로 세척한 다음, 염수 (25 mL)로 세척하였다. 고체가 유기 상으로부터 석출되었고, 여과에 의해 단리시켰다. 여과물을 농축시켜 또 다른 수확 침전물을 수득하였다. 2종의 초기 침전물은 둘 다 동일한 물질이었고, 백색 분말 (2.25 g, 64.6% 수율)로 건조시켰다.
단계 2. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 히드로클로라이드의 제조.
THF (40 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-이소시아네이토-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 (2.24 g, 3.84 mmol)의 용액을 진한 HCl (7.93 mL, 96 mmol)로 처리하였다. 생성된 용액을 실온에서 48시간 동안 교반하였다. 혼합물을 여과하여 고체를 제거한 다음, 여과물을 진공 하에 백색 분말 (2.30 g, 100% 수율)로 농축시켰다. LCMS: m/e 559 (M+H)+, 2.12분 (방법 6).
단계 3: 밀봉된 바이알에서 THF (0.8 mL) 및 MeOH (0.8 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 히드로클로라이드 (0.050 g, 0.090 mmol) 및 수산화리튬 1수화물, 1.0M 수성 (0.359 mL, 0.359 mmol)의 혼합물을 75℃로 가온하여 균질 용액을 수득하였다. 혼합물을 1시간 후에 열로부터 제거하였다. 조 혼합물을 역상 정제용 HPLC에 의해 정제용 HPLC 방법 24를 사용하여 정제하여 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 미황색 분말 (48.5 mg, 79% 수율)로서 수득하였다. LCMS: m/e 544.7 (M+H)+, 1.94분 (방법 6).
실시예 B50
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-5a,5b,8,8,11a-펜타메틸-3a-(메틸아미노)-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-5a,5b,8,8,11a-펜타메틸-3a-(메틸아미노)-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
밀봉된 바이알에서 DMF (1 mL) 중에 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 히드로클로라이드 (50 mg, 0.084 mmol) 및 탄산칼륨 (23.3 mg, 0.168 mmol)의 혼합물을 메틸 아이오다이드 (0.016 mL, 0.036 g, 0.25 mmol)로 처리하고, 75℃로 3시간 동안 가열하였다. 혼합물을 THF 및 염수로 희석하였다. 혼합물을 진탕시키고, 상을 분리하였다. 유기물을 진공 하에 잔류물로 농축시켰다. 생성물을 정제용 HPLC 방법 25를 사용하여 역상 정제용 HPLC 정제한 후, 유리질 백색 고체 (57.2 mg, 99% 수율) 모노 TFA 염으로서 수득하였다. LCMS: m/e 572.6 (M+H)+, 2.18분 (방법 6).
단계 2: 밀봉된 바이알에서 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-5a,5b,8,8,11a-펜타메틸-3a-(메틸아미노)-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 TFA 염 (57 mg, 0.083 mmol), 1.0M 수성 LiOH (0.417 mL, 0.417 mmol), THF (0.8 mL) 및 메탄올 (0.8 mL)의 혼합물을 75℃로 1시간 동안 가온한 다음, 60℃에서 18시간 동안 가온하였다. 표제 화합물, 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-5a,5b,8,8,11a-펜타메틸-3a-(메틸아미노)-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 정제용 HPLC 방법 24를 사용하여 역상 정제용 HPLC 정제한 후, 백색 고체 (44.1 mg, 69% 수율) 모노 TFA 염으로서 단리시켰다. LCMS: m/e 558.7 (M+H)+, 1.98분 (방법 6).
실시예 B51
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-(2-(1,1-디옥시도티오모르폴리노)아세트아미도)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-(2-(1,1-디옥시도티오모르폴리노)아세트아미도)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
DCM (1 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 히드로클로라이드 (50 mg, 0.084 mmol) 및 2-(1,1-디옥시도티오모르폴리노)아세트산 (0.023 g, 0.117 mmol)의 혼합물을 HATU (0.044 g, 0.117 mmol) 및 DIPEA (0.063 mL, 0.359 mmol)로 처리하였다. 혼합물을 실온에서 3시간 동안 교반하였다. 혼합물을 질소 스트림 하에 잔류물로 농축시킨 다음, 메탄올 및 THF의 혼합물 중에 재용해시켰다. 생성물을 정제용 HPLC 방법 25를 사용하여 역상 정제용 HPLC 정제한 후, 유리질 회백색 고체 (44.9 mg, 59% 수율) 모노 TFA 염으로서 단리시켰다. LCMS: m/e 733.6 (M+H)+, 2.66분 (방법 6).
단계 2: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-(2-(1,1-디옥시도티오모르폴리노)아세트아미도)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 트리플루오로아세트산 염 (0.0449 g, 0.053 mmol) 및 1M 수성 수산화리튬 (0.265 mL, 0.265 mmol)과 THF (0.5 mL) 및 MeOH (0.5 mL)의 혼합물을 밀봉된 바이알에서 75℃로 1시간 동안 가열하였다. 표제 화합물, 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-(2-(1,1-디옥시도티오모르폴리노)아세트아미도)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 정제용 HPLC 방법 24를 사용하여 역상 정제용 HPLC 정제한 후, 백색 고체 (37.6 mg, 83% 수율) 모노 TFA 염으로서 단리시켰다. LCMS: m/e 719.7 (M+H)+, 2.32분 (방법 6).
실시예 B52
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
단계 1. 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트의 제조.
아세토니트릴 (3 mL) 중 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 히드로클로라이드 (100 mg, 0.168 mmol), 4-(2-클로로에틸)티오모르폴린 1,1-디옥시드 히드로클로라이드 (0.122 mg, 0.522 mmol) (WO1002045652에 기재된 바와 같이 제조됨), 인산칼륨, 삼염기성 (0.157 g, 0.740 mmol) 및 아이오딘화칼륨 (0.075 g, 0.454 mmol)을 함유하는 압력 용기를 밀봉하고, 120℃로 64시간 동안 가열하였다. 조 혼합물을 THF로 희석하고, 여과하여 고체를 제거하였다. 여과물을 농축시키고, 생성물을 정제용 HPLC 방법 25를 사용하여 역상 정제용 HPLC 정제한 후, 백색 고체 (0.0982 mg, 61.6% 수율)를 비스 TFA 염으로서 단리시켰다. LCMS: m/e 719.7 (M+H)+, 2.10분 (방법 6).
단계 2: 메틸 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조에이트 트리플루오로아세트산 염 (0.098 g, 0.118 mmol) 및 1M 수성 수산화리튬 (0.588 mL, 0.588 mmol)과 THF (1 mL) 및 MeOH (1 mL)의 혼합물을 밀봉된 바이알에서 75℃로 1시간 동안 가열하였다. 표제 화합물, 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산을 정제용 HPLC 방법 24를 사용하여 역상 정제용 HPLC 정제한 후, 백색 고체 (89.9 mg, 79% 수율)를 비스 TFA 염으로서 단리시켰다. LCMS: m/e 705.8 (M+H)+, 1.93분 (방법 6).
실시예 B53
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-3a-(2-(4-(메틸술포닐)피페리딘-1-일)에틸아미노)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
표제 화합물은, 단계 1에서 1-(2-클로로에틸)-4-(메틸술포닐)피페리딘 (0.152 g, 0.673 mmol)을 4-(2-클로로에틸)티오모르폴린 1,1-디옥시드 히드로클로라이드 대신 사용하였다는 점을 제외하고는 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조에 사용된 동일 2 단계 방법에 의해 제조하였다. 표제 화합물을 정제용 HPLC 방법 24를 사용하여 단계 2 반응 혼합물을 역상 정제용 HPLC 정제한 후, 백색 고체 (70.5 mg, 71.5% 수율)를 비스 TFA 염으로서 단리시켰다. LCMS: m/e 733.6 (M+H)+, 2.28분 (방법 5).
실시예 B54
4-((1R,3aS,5aR,5bR,7aS,9S,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)이코사히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (0.036 g, 0.055 mmol) 및 에틸 아세테이트 (2 mL)의 혼합물을 질소 기체로 덮은 다음, 탄소 상 10% 팔라듐 (0.023 g, 0.022 mmol)을 첨가하였다. 플라스크에 수소 기체의 풍선을 장착하고, 혼합물을 수소 분위기 하에 18시간 동안 신속히 교반하였다. 혼합물을 여과하여 촉매를 제거하고, 진공 하에 농축시켰다. 표제 화합물을 정제용 HPLC 방법 24를 사용하여 반응 혼합물을 역상 정제용 HPLC 정제한 후, 백색 고체 (13.1 mg, 36.4% 수율) 모노 TFA 염으로서 단리시켰다. LCMS: m/e 546.7 (M+H)+, 1.95분 (방법 6).
실시예 B55
4-((1R,3aS,5aR,5bR,7aS,9S,11aS,11bR,13aR,13bR)-5a,5b,8,8,11a-펜타메틸-3a-(메틸아미노)-1-(1-메틸시클로프로필)이코사히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
표제 화합물은, 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-5a,5b,8,8,11a-펜타메틸-3a-(메틸아미노)-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 (0.034 g, 0.051 mmol)을 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산 대신에 사용하였다는 점을 제외하고는 4-((1R,3aS,5aR,5bR,7aS,9S,11aS,11bR,13aR,13bR)-3a-아미노-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)이코사히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 합성에 대해 기재된 바와 같은 동일한 절차를 따라 제조하였다. 조 혼합물을 역상 정제용 HPLC에 의해 정제용 HPLC 방법 23을 사용하여 정제하여 표제 화합물을 백색 고체 (25.5 mg, 63.6% 수율) 모노 TFA 염으로서 수득하였다. LCMS: m/e 560.8 (M+H)+, 2.14분 (방법 6).
실시예 B56
4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-3a-(2-(4-(메틸술포닐)피페라진-1-일)에틸아미노)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조.
표제 화합물을, 단계 1에서 1-(2-클로로에틸)-4-(메틸술포닐)피페라진 (0.118 g, 0.522 mmol)을 4-(2-클로로에틸)티오모르폴린 1,1-디옥시드 히드로클로라이드 대신에 사용하였다는 점을 제외하고는 4-((1R,3aS,5aR,5bR,7aR,11aS,11bR,13aR,13bR)-3a-((2-(1,1-디옥시도티오모르폴리노)에틸)아미노)-5a,5b,8,8,11a-펜타메틸-1-(1-메틸시클로프로필)-2,3,3a,4,5,5a,5b,6,7,7a,8,11,11a,11b,12,13,13a,13b-옥타데카히드로-1H-시클로펜타[a]크리센-9-일)벤조산의 제조에 사용된 동일한 2 단계 방법에 의해 제조하였다. 표제 화합물을 정제용 HPLC 방법 4를 사용하여 단계 2 반응 혼합물을 역상 정제용 HPLC 정제한 후, 백색 고체 (58.7 mg, 59.2% 수율)를 비스 TFA 염으로서 정제시켰다.
LCMS: m/e 734.4 (M+H)+, 2.30분 (방법 5).
실시예에 대한 생물학 데이터
ㆍ "μM"은 마이크로몰을 의미하고;
ㆍ "mL"은 밀리리터를 의미하고;
ㆍ "μl"은 마이크로리터를 의미하고;
ㆍ "mg"는 밀리그램을 의미하고;
ㆍ "μg"는 마이크로그램을 의미하고;
표 1에 보고된 결과를 얻기 위해 사용된 물질 및 실험 절차는 하기 기재되어 있다.
HIV 세포 배양 검정 - MT-2 세포 및 293T 세포를 NIH AIDS 연구 및 참조 시약 프로그램으로부터 입수하였다. MT-2 세포를 10% 열 불활성화 태아 소 혈청, 100 μg/ml 페니실린 G 및 100 유닛/ml까지의 스트렙토마이신으로 보충된 RPMI 1640 배지 중에 번식시켰다. 293T 세포를 10% 열 불활성화 태아 소 혈청 (FBS), 100 유닛/ml 페니실린 G 및 100 μg/ml 스트렙토마이신으로 보충된 DMEM 배지 중에 번식시켰다. NL4-3의 프로바이러스 DNA 클론을 NIH AIDS 연구 및 참조 시약 프로그램으로부터 입수하였다. NL4-3으로부터의 nef 유전자의 섹션이 레닐라(Renilla) 루시페라제 유전자로 대체된 것인 재조합 NL4-3 바이러스를 참조 바이러스로서 사용하였다. 또한, 잔기 Gag P373을 P373S로 전환시켰다. 간략하게, 재조합 바이러스를 NL4-3의 변경된 프로바이러스 클론의 형질감염에 의해 제조하였다. 형질감염은 인비트로젠(Invitrogen) (캘리포니아주 칼스배드)으로부터의 리포펙타민 플러스(LipofectAMINE PLUS)를 제조업체의 지침을 따라 사용하여 293T 세포에서 수행하였다. 루시페라제 효소 활성을 마커로서 사용하여 MT-2 세포에서 바이러스를 적정하였다. 프로메가(Promega) (위스콘신주 매디슨)로부터의 이중 루시페라제 키트를 제조업체의 프로토콜을 변형시켜 사용함으로써 루시페라제를 정량화하였다. 희석된 수동성 용해 용액을 재현탁된 루시페라제 검정 시약 및 재현탁된 스톱 & 글로(Stop & Glo) 기질과 예비-혼합 (2:1:1 비)하였다. 혼합물 50 μL를 검정 플레이트 상의 각각의 흡인 웰에 첨가하고, 루시페라제 활성을 왈락 트리룩스(Wallac TriLux) (퍼킨-엘머(Perkin-Elmer)) 상에서 즉시 측정하였다. 억제제의 연속 희석물의 존재 하에 NLRluc 재조합체로 4-5일 동안 감염시킨 세포에서 루시페라제 활성을 측정함으로써, 재조합 바이러스에 대한 억제제의 항바이러스 활성을 정량화하였다. 화합물에 대한 EC50 데이터는 표 1에 제시되어 있다.
<표 1>
상기 기재는 단지 예시적이고, 어떠한 방식으로도 본 발명의 범주 또는 근본 원리를 제한하는 것으로 이해되어서는 안 된다. 실제로, 본원에 제시되고 기재된 것에 더하여, 본 발명의 다양한 변형이 하기 실시예 및 상기 설명으로부터 통상의 기술자에게 명백해질 것이다. 이러한 변형은 또한 첨부된 청구범위의 범주 내인 것으로 의도된다.
Claims (12)
- 하기 화학식 I의 화합물; 및 하기 화학식 II의 화합물의 군으로부터 선택된, 그의 제약상 허용되는 염을 포함하는 화합물.
<화학식 I>
<화학식 II>
상기 식에서, X는 페닐, 헤테로아릴 고리, C4-8 시클로알킬, C4-8 시클로알케닐, C4-9 스피로시클로알킬, C4-9 스피로시클로알케닐, C4-8 옥사시클로알킬, C4-8 디옥사시클로알킬, C6-8 옥사시클로알케닐, C6-8 디옥사시클로알케닐, C6 시클로디알케닐, C6 옥사시클로디알케닐, C6-9 옥사스피로시클로알킬 및 C6-9 옥사스피로시클로알케닐 고리의 군으로부터 선택되고;
추가로 여기서 X는 A로 치환되고, 여기서 A는 -H, -할로, -히드록실, -C1-6 알킬, -C1-6 알콕시, -C1-6 알킬-Q1, -알킬치환된 C1-6 알킬-Q1, -CN, -CF2Q1, -NR2R2, -COOR2 및 -CONR2R2의 군으로부터 선택된 적어도 1개의 구성원이고;
여기서 Q1은 아릴, 헤테로아릴, 치환된 헤테로아릴, -OR2, -COOR3, -NR2R2, -SO2R7, -CONHSO2R3, 및 -CONHSO2NR2R2의 군으로부터 선택되고;
Y는 -COOR2, -C(O)NR2SO2R3, -C(O)NHSO2NR2R2, -NR2SO2R2, -SO2NR2R2, -C3-6 시클로알킬-COOR2, -C2-6 알케닐-COOR2, -C2-6 알키닐-COOR2, -C1-6 알킬-COOR2, -알킬치환된 C1-6 알킬, -COOR2, CF2-COOR2, -NHC(O)(CH2)n-COOR2, -SO2NR2C(O)R2, -테트라졸, 및 -CONHOH의 군으로부터 선택되고,
여기서 n=1-6이고;
R1은
의 군으로부터 선택되고;
W는 부재하거나, 또는 -CH2 또는 -CO이고;
Z는 -NR28R29, -OR30, -COOR2, -CONR18R19, F, Cl, Br, 및 I의 군으로부터 선택되고;
U는 -NR28R29, -OR30, -COOR2, -CONR18R19, F, Cl, Br, I, 아릴 및 헤테로아릴의 군으로부터 선택되고;
R2는 -H, 벤질, -C1-6 알킬, -알킬치환된 C1-6 알킬 및 -아릴치환된 C1-6 알킬의 군으로부터 선택되고;
R3은 벤질, -C1-6 알킬 또는 -알킬치환된 C1-6 알킬이고;
R4는 -H, -C1-6 알킬, -C1-6 알킬-C(OR3)2-C3-6 시클로알킬, -C1-6 치환된 알킬, -C1-6 알킬-C3-6 시클로알킬, -C1-6 알킬-Q2, -C1-6 알킬-C3-6 시클로알킬-Q2, 아릴, 헤테로아릴, 치환된 헤테로아릴, -COR6, -COCOR6, -SO2R7, -SO2NR2R2,의 군으로부터 선택되고,
여기서 Q2는 헤테로아릴, 치환된 헤테로아릴, F, Cl, Br, I, -CF3, -OR2, -COOR2, -NR8R9, -CONR10R11 및 -SO2R7의 군으로부터 선택되고;
R5는 -H, -C1-6 알킬, -C3-6 시클로알킬, -C1-6 알킬치환된 알킬, -C1-6 알킬-NR8R9, -COR6, -COCOR6, -SO2R7 및 -SO2NR2R2의 군으로부터 선택되며;
단 W가 CO인 경우에 R4 또는 R5는 -COR6 또는 -COCOR6일 수 없고;
추가로 단 R4 또는 R5 중 오직 1개가 -COR6, -COCOR6, -SO2R7 및 -SO2NR2R2의 군으로부터 선택될 수 있거나;
또는 W가 부재하거나 또는 CH2인 경우에, R4 및 R5는 인접한 N과 함께를 형성할 수 있고;
R6은 -C1-6 알킬, -C1-6 알킬-치환된알킬, -C3-6 시클로알킬, -C3-6 치환된시클로알킬-Q3, -C1-6 알킬-Q3, -C1-6 알킬-치환된알킬-Q3, -C3-6 시클로알킬-Q3, 아릴-Q3, -NR13R14, 및 -OR15의 군으로부터 선택되고;
여기서 Q3은 아릴, 헤테로아릴, 치환된 헤테로아릴, -OR2, -COOR2, -NR8R9, SO2R7, -CONHSO2R3, 및 -CONHSO2NR2R2의 군으로부터 선택되고;
R7은 -C1-6 알킬, -C1-6 치환된 알킬, -C3-6 시클로알킬, -CF3, 아릴, 및 헤테로아릴의 군으로부터 선택되고;
R8 및 R9는 독립적으로 -H, -C1-6 알킬, -C1-6 치환된 알킬, 아릴, 헤테로아릴, 치환된 아릴, 치환된 헤테로아릴, -C1-6 알킬-Q2, 및 -COOR3의 군으로부터 선택되고;
R8은 또한 -COOR3일 수 있고;
R8 및 R9는 또한 독립적으로의 군으로부터 선택될 수 있거나,
또는 R8 및 R9는 인접한 N과 함께
의 군으로부터 선택된 사이클을 형성하고;
V는 -CR24R25, -SO2, -O 및 -NR12의 군으로부터 선택되고;
M은 -CHR24R25, -NR26R27, -SO2R7, -SO2NR3R3 및 -OH의 군으로부터 선택되고;
R10 및 R11은 독립적으로 -H, -C1-6 알킬, -C1-6 치환된 알킬 및 -C3-6 시클로알킬의 군으로부터 선택되거나,
또는 R10 및 R11은 인접한 N과 함께 사이클, 예컨대 를 형성하고;
R12는 -C1 -6 알킬, -C1 -6 알킬-OH; -C1 -6 알킬, -C1 -6 치환된 알킬, -C3 -6 시클로알킬, -COR7, -COONR18R19, -SOR7, 및 -SONR20R21의 군으로부터 선택되고;
R13 및 R14는 독립적으로 -H, -C1-6 알킬, -C3-6 시클로알킬, -C1-6 치환된 알킬, -C1-6 알킬-Q4, -C1-6 알킬-C3-6 시클로알킬-Q4, -C1-6 치환된 알킬-Q4 및 의 군으로부터 선택되거나,
또는 R13 및 R14는 인접한 N과 함께
의 군으로부터 선택된 사이클을 형성하고;
R15는 -C1-6 알킬, -C3-6 시클로알킬, -C1-6 치환된 알킬, -C1-6 알킬-Q4, -C1-6 알킬-C3-6 시클로알킬-Q4 및 -C1-6 치환된 알킬-Q4의 군으로부터 선택되고;
Q4는 헤테로아릴, 치환된 헤테로아릴, -NR2R2, -CONR2R2, -COOR2, -OR2, 및 -SO2R3의 군으로부터 선택되고;
R16은 -H, -C1-6 알킬, -NR2R2, 및 -COOR3의 군으로부터 선택되고;
R17은 -H, -C1-6 알킬, -COOR3, 및 아릴의 군으로부터 선택되고;
R18 및 R19는 독립적으로 H, -C1-6 알킬, -C1-6 치환된 알킬, 및 -C1-6 시클로알킬의 군으로부터 선택되고;
R18은 또한 -COOR3일 수 있거나;
또는 R18 및 R19는 인접한 N과 함께 의 군으로부터 선택된 사이클을 형성하고;
R20 및 R21은 독립적으로 H, -C1 -6 알킬, -C1 -6 치환된 알킬, -C1 -6 알킬-Q5, -C1 -6 시클로알킬, 아릴, 치환된 아릴, 헤테로아릴, 및 치환된 헤테로아릴의 군으로부터 선택되고,
Q5는 할로겐 및 SO2R3의 군으로부터 선택되고;
R24 및 R25는 독립적으로 -H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -SO2R3, -SO2NR2R2 또는 -OH, -NR2R2, -NR2SO2R3, -NR2COR3 및 -NR2CONR2R2의 군으로부터 선택되며;
단 R24 및 R25 중 오직 1개가 -OH, -NR2R2, -NR2SO2R3, -NR2COR3 및 -NR2CONR2R2의 군으로부터 선택될 수 있고;
R26 및 R27은 독립적으로 -H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -C1-3 알킬아릴, -C1- 3알킬헤테로아릴, -CO2R2 및 -SO2R7의 군으로부터 선택되며;
단 R26 및 R27 중 오직 1개가 -CO2R2 또는 -SO2R7의 군으로부터 선택될 수 있고;
R28 및 R29는 독립적으로 -H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -C3-6 시클로알킬, -C1-6 알킬-Q6, -COC1 -6 알킬-Q6, -COOR3; -COCF3의 군으로부터 선택되고;
R28은 또한 -COOR3 및 -CONR18R19로부터 선택될 수 있거나;
또는 R28 및 R29는 인접한 N과 함께
의 군으로부터 선택된 사이클을 형성하고;
R30은 H, -C1-6 알킬, -알킬치환된 C1-6 알킬, -C3-6 시클로알킬, 및 -C1-6 알킬-Q6의 군으로부터 선택되고;
여기서 Q6은 H, -OR2, -COOR2, -COCOOR2, 및 -NR31R32의 군으로부터 선택되고;
R31 및 R32는 독립적으로 -H, -C1-6 알킬, -C1-6 치환된 알킬, -C1-6 치환된 알킬-OR2, 및 -COR3의 군으로부터 선택되거나,
또는 R31 및 R32는 인접한 N과 함께 의 군으로부터 선택된 사이클을 형성하고;
R33은 -H, -C1-6 알킬, -C1-6 치환된 알킬, 및 -C1-6 치환된 알킬-Q7의 군으로부터 선택되고,
여기서 Q7은 -COOR2 및 -COONR2R2의 군으로부터 선택된다. - 제1항에 있어서, X가 페닐인 화합물.
- 제2항에 있어서, A가 -H인 화합물.
- 제1항에 있어서, Y가 -COOR2인 화합물.
- 제4항에 있어서, Y가 -COOH인 화합물.
- 항바이러스 유효량의 제1항에 청구된 바와 같은 화합물 중 1종 이상을 1종 이상의 제약상 허용되는 담체, 부형제 또는 희석제와 함께 포함하는 제약 조성물.
- 제7항에 있어서, 항바이러스 유효량의, (a) AIDS 항바이러스제; (b) 항감염제; (c) 면역조절제; 및 (d) 또 다른 HIV 진입 억제제의 군으로부터 선택된 AIDS 치료제를 추가로 포함하는, HIV에 의한 감염을 치료하는데 유용한 제약 조성물.
- HIV 바이러스에 감염된 포유동물에게 항바이러스 유효량의 제1항에 청구된 바와 같은 화합물, 및 1종 이상의 제약상 허용되는 담체, 부형제 또는 희석제를 투여하는 것을 포함하는, 상기 포유동물을 치료하는 방법.
- 항바이러스 유효량의 제6항에 청구된 바와 같은 화합물 중 1종 이상을 1종 이상의 제약상 허용되는 담체, 부형제 또는 희석제와 함께 포함하는 제약 조성물.
- 제10항에 있어서, 항바이러스 유효량의, (a) AIDS 항바이러스제; (b) 항감염제; (c) 면역조절제; 및 (d) 또 다른 HIV 진입 억제제의 군으로부터 선택된 AIDS 치료제를 추가로 포함하는, HIV에 의한 감염을 치료하는데 유용한 제약 조성물.
- HIV 바이러스에 감염된 포유동물에게 항바이러스 유효량의 제10항에 청구된 바와 같은 화합물, 및 1종 이상의 제약상 허용되는 담체, 부형제 또는 희석제를 투여하는 것을 포함하는, 상기 포유동물을 치료하는 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361761403P | 2013-02-06 | 2013-02-06 | |
| US61/761,403 | 2013-02-06 | ||
| PCT/US2014/014647 WO2014123889A1 (en) | 2013-02-06 | 2014-02-04 | C-19 modified triterpenoids with hiv maturation inhibitory activity |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20150115881A true KR20150115881A (ko) | 2015-10-14 |
Family
ID=50150818
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020157023907A KR20150115881A (ko) | 2013-02-06 | 2014-02-04 | Hiv 성숙 억제 활성을 갖는 c-19 변형된 트리테르페노이드 |
Country Status (15)
| Country | Link |
|---|---|
| US (1) | US20140221361A1 (ko) |
| EP (1) | EP2953960A1 (ko) |
| JP (1) | JP6186010B2 (ko) |
| KR (1) | KR20150115881A (ko) |
| CN (1) | CN105121454A (ko) |
| AR (1) | AR094684A1 (ko) |
| AU (1) | AU2014215468B2 (ko) |
| BR (1) | BR112015018491A2 (ko) |
| CA (1) | CA2900124A1 (ko) |
| EA (1) | EA027371B1 (ko) |
| IL (1) | IL240289A0 (ko) |
| MX (1) | MX2015010003A (ko) |
| SG (1) | SG11201505639SA (ko) |
| TW (1) | TW201443073A (ko) |
| WO (1) | WO2014123889A1 (ko) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8906889B2 (en) * | 2012-02-15 | 2014-12-09 | Bristol-Myers Squibb Company | C-3 cycloalkenyl triterpenoids with HIV maturation inhibitory activity |
| AU2016298669A1 (en) | 2015-07-28 | 2018-02-22 | Glaxosmithkline Intellectual Property (No.2) Limited | Betuin derivatives for preventing or treating HIV infections |
| CA2993758A1 (en) | 2015-07-28 | 2017-02-02 | Glaxosmithkline Intellectual Property (No.2) Limited | Betuin derivatives for preventing or treating hiv infections |
| WO2017025901A1 (en) * | 2015-08-11 | 2017-02-16 | Hetero Research Foundation | Novel c28-analogues with c3-modifications of triterpene derivatives as hiv inhibitors |
| AU2016327169A1 (en) | 2015-09-24 | 2018-04-12 | Glaxosmithkline Intellectual Property (No.2) Limited | Compounds with hiv maturation inhibitory activity |
| US20190023733A1 (en) | 2016-01-20 | 2019-01-24 | Glaxosmithkline Intellectual Property (No.2) Limited | Amine derivatives of lupanes with hiv maturation inhibitory activity |
| AR107512A1 (es) * | 2016-02-04 | 2018-05-09 | VIIV HEALTHCARE UK Nº 5 LTD | Triterpenoides modificados en c-3 y c-17 como inhibidores del vih-1 |
| WO2017149518A1 (en) * | 2016-03-04 | 2017-09-08 | Hetero Labs Limited | C-3 novel triterpene with c-17 amine derivatives as hiv inhibitors |
| JP6936820B2 (ja) * | 2016-06-30 | 2021-09-22 | ヴィーブ ヘルスケア ユーケー(ナンバー5)リミテッド | ヒト免疫不全ウイルス複製の阻害剤としてのアザデカリン誘導体 |
| WO2018044853A1 (en) * | 2016-08-31 | 2018-03-08 | Viiv Healthcare Conpany | Combinations and uses and treatments thereof |
| US20190183901A1 (en) * | 2016-08-31 | 2019-06-20 | Viiv Healthcare Company | Combinations and uses and treatments thereof |
| ES2970042T3 (es) | 2018-04-24 | 2024-05-24 | Viiv Healthcare Uk No 5 Ltd | Compuestos con actividad inhibidora de la maduración del VIH |
| AU2019292599B2 (en) * | 2018-06-29 | 2022-03-03 | Dfh Therapeutics | Triterpene amine derivatives |
| ES2965305T3 (es) | 2019-02-11 | 2024-04-12 | Hetero Labs Ltd | Nuevos derivados de triterpeno como inhibidores del VIH |
Family Cites Families (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2694048B2 (ja) * | 1991-05-09 | 1997-12-24 | 日立建機株式会社 | 建設機械の油圧駆動装置 |
| US5413999A (en) | 1991-11-08 | 1995-05-09 | Merck & Co., Inc. | HIV protease inhibitors useful for the treatment of AIDS |
| FR2683531B1 (fr) * | 1991-11-13 | 1993-12-31 | Rhone Poulenc Rorer Sa | Nouveaux derives du lupane, leur preparation et les compositions pharmaceutiques qui les contiennent. |
| US5679828A (en) | 1995-06-05 | 1997-10-21 | Biotech Research Labs, Inc. | Betulinic acid and dihydrobetulinic acid derivatives and uses therefor |
| US20020137755A1 (en) | 2000-12-04 | 2002-09-26 | Bilodeau Mark T. | Tyrosine kinase inhibitors |
| US20040110785A1 (en) | 2001-02-02 | 2004-06-10 | Tao Wang | Composition and antiviral activity of substituted azaindoleoxoacetic piperazine derivatives |
| US7365221B2 (en) | 2002-09-26 | 2008-04-29 | Panacos Pharmaceuticals, Inc. | Monoacylated betulin and dihydrobetulin derivatives, preparation thereof and use thereof |
| US7745625B2 (en) | 2004-03-15 | 2010-06-29 | Bristol-Myers Squibb Company | Prodrugs of piperazine and substituted piperidine antiviral agents |
| US20050239748A1 (en) | 2004-03-17 | 2005-10-27 | Panacos Pharmaceuticals, Inc. | Pharmaceutical salts of 3-O-(3',3'-dimethylsuccinyl) betulinic acid |
| TW200628161A (en) | 2004-11-12 | 2006-08-16 | Panacos Pharmaceuticals Inc | Novel betulin derivatives, preparation thereof and use thereof |
| US20110144069A1 (en) | 2006-10-16 | 2011-06-16 | Myriad Genetics, Incorporated | Compounds for treating viral infections |
| WO2009100532A1 (en) | 2008-02-14 | 2009-08-20 | Virochem Pharma Inc. | NOVEL 17ß LUPANE DERIVATIVES |
| US9067966B2 (en) | 2009-07-14 | 2015-06-30 | Hetero Research Foundation, Hetero Drugs Ltd. | Lupeol-type triterpene derivatives as antivirals |
| BR112012030810A2 (pt) * | 2010-06-04 | 2019-09-24 | Bristol-Myers Squibb Company | "c-28 amidas de derivados de ácido c-3 betulínico modificados como inibidores de maturação de hiv" |
| ES2612452T3 (es) * | 2010-06-04 | 2017-05-17 | VIIV Healthcare UK (No.5) Limited | Derivados de ácido betulínico C-3 modificados como inhibidores de la maduración del VIH |
| US8897303B2 (en) | 2010-06-29 | 2014-11-25 | Futurewei Technologies, Inc. | Delegate gateways and proxy for target hosts in large layer 2 and address resolution with duplicated internet protocol addresses |
| PL2670764T3 (pl) * | 2011-01-31 | 2016-02-29 | Bristol Myers Squibb Co | C-28 aminy zmodyfikowanych C-3 pochodnych kwasu betulinowego jako inhibitory dojrzewania HIV |
| CA2826113C (en) * | 2011-01-31 | 2018-09-04 | Bristol-Myers Squibb Company | C-17 and c-3 modified triterpenoids with hiv maturation inhibitory activity |
| US8906889B2 (en) | 2012-02-15 | 2014-12-09 | Bristol-Myers Squibb Company | C-3 cycloalkenyl triterpenoids with HIV maturation inhibitory activity |
| US20150119373A1 (en) * | 2012-04-24 | 2015-04-30 | Hetero Research Foundation | Novel betulinic acid derivatives as hiv inhibitors |
| US8889854B2 (en) | 2012-05-07 | 2014-11-18 | Bristol-Myers Squibb Company | C-17 bicyclic amines of triterpenoids with HIV maturation inhibitory activity |
-
2014
- 2014-02-04 US US14/172,389 patent/US20140221361A1/en not_active Abandoned
- 2014-02-04 SG SG11201505639SA patent/SG11201505639SA/en unknown
- 2014-02-04 EA EA201591406A patent/EA027371B1/ru not_active IP Right Cessation
- 2014-02-04 JP JP2015556998A patent/JP6186010B2/ja not_active Expired - Fee Related
- 2014-02-04 AU AU2014215468A patent/AU2014215468B2/en not_active Ceased
- 2014-02-04 MX MX2015010003A patent/MX2015010003A/es unknown
- 2014-02-04 CN CN201480019576.0A patent/CN105121454A/zh active Pending
- 2014-02-04 EP EP14705662.6A patent/EP2953960A1/en not_active Withdrawn
- 2014-02-04 WO PCT/US2014/014647 patent/WO2014123889A1/en active Application Filing
- 2014-02-04 KR KR1020157023907A patent/KR20150115881A/ko not_active Application Discontinuation
- 2014-02-04 BR BR112015018491A patent/BR112015018491A2/pt not_active Application Discontinuation
- 2014-02-04 CA CA2900124A patent/CA2900124A1/en not_active Abandoned
- 2014-02-05 TW TW103103839A patent/TW201443073A/zh unknown
- 2014-02-06 AR ARP140100400A patent/AR094684A1/es unknown
-
2015
- 2015-08-02 IL IL240289A patent/IL240289A0/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| CN105121454A (zh) | 2015-12-02 |
| EA201591406A1 (ru) | 2015-12-30 |
| MX2015010003A (es) | 2015-10-30 |
| BR112015018491A2 (pt) | 2017-07-18 |
| AR094684A1 (es) | 2015-08-19 |
| WO2014123889A1 (en) | 2014-08-14 |
| US20140221361A1 (en) | 2014-08-07 |
| SG11201505639SA (en) | 2015-08-28 |
| AU2014215468B2 (en) | 2017-05-18 |
| CA2900124A1 (en) | 2014-08-14 |
| IL240289A0 (en) | 2015-09-24 |
| JP6186010B2 (ja) | 2017-08-23 |
| EA027371B1 (ru) | 2017-07-31 |
| AU2014215468A1 (en) | 2015-09-24 |
| EP2953960A1 (en) | 2015-12-16 |
| TW201443073A (zh) | 2014-11-16 |
| JP2016507558A (ja) | 2016-03-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20150115881A (ko) | Hiv 성숙 억제 활성을 갖는 c-19 변형된 트리테르페노이드 | |
| KR101886467B1 (ko) | Hiv 성숙 억제 활성을 갖는 c-17 및 c-3 변형 트리테르페노이드 | |
| JP6155285B2 (ja) | Hiv成熟阻害活性のあるc−3シクロアルケニルトリテルペノイド | |
| JP6186012B2 (ja) | C−3アルキルおよびアルケニル修飾ベツリン酸誘導体 | |
| JP5755731B2 (ja) | Hiv成熟阻害剤としての修飾c−3ベツリン酸誘導体のc−28アミド | |
| KR20150013157A (ko) | Hiv 성숙 억제 활성을 갖는 트리테르페노이드의 c-17 비시클릭 아민 | |
| JP6100786B2 (ja) | 抗ウイルス活性を有する新規ベツリン酸誘導体 | |
| KR102411082B1 (ko) | 할로알킬 치환기를 지니는 비방향족 고리에 의해 위치 3에서 치환된,hiv 성숙화 억제 활성을 갖는 트리테르페노이드 | |
| ES2957767T3 (es) | Triterpenoides modificados en C-3 y C-17 como inhibidores del VIH-1 | |
| AU2015346303B2 (en) | Oxolupene derivatives | |
| JP2017533934A (ja) | C17アリール置換ベツリン酸類似体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| N231 | Notification of change of applicant | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |