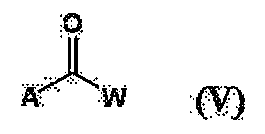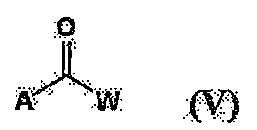KR20130028126A - 시스테인 유도체 - Google Patents
시스테인 유도체 Download PDFInfo
- Publication number
- KR20130028126A KR20130028126A KR1020127033919A KR20127033919A KR20130028126A KR 20130028126 A KR20130028126 A KR 20130028126A KR 1020127033919 A KR1020127033919 A KR 1020127033919A KR 20127033919 A KR20127033919 A KR 20127033919A KR 20130028126 A KR20130028126 A KR 20130028126A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- alkyl group
- methylthiazolidine
- dicarboxylic acid
- acetyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 150000001944 cysteine derivatives Chemical class 0.000 title claims abstract description 93
- 150000003839 salts Chemical class 0.000 claims abstract description 47
- 239000002537 cosmetic Substances 0.000 claims abstract description 27
- -1 2-ethyl Chemical group 0.000 claims description 123
- 125000000217 alkyl group Chemical group 0.000 claims description 87
- 150000001875 compounds Chemical class 0.000 claims description 68
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 65
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 49
- CMLMTPHQDNAMKO-UHFFFAOYSA-N 3-acetyl-2-methyl-1,3-thiazolidine-2,4-dicarboxylic acid Chemical group CC(=O)N1C(C(O)=O)CSC1(C)C(O)=O CMLMTPHQDNAMKO-UHFFFAOYSA-N 0.000 claims description 41
- LLPCTYVJIFDZPF-UHFFFAOYSA-N 3-acetyl-2-ethoxycarbonyl-2-methyl-1,3-thiazolidine-4-carboxylic acid Chemical compound CCOC(=O)C1(C)SCC(C(O)=O)N1C(C)=O LLPCTYVJIFDZPF-UHFFFAOYSA-N 0.000 claims description 37
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims description 32
- 125000003545 alkoxy group Chemical group 0.000 claims description 32
- 125000006615 aromatic heterocyclic group Chemical group 0.000 claims description 27
- 239000013078 crystal Substances 0.000 claims description 27
- 125000000539 amino acid group Chemical group 0.000 claims description 26
- 125000003282 alkyl amino group Chemical group 0.000 claims description 22
- 125000001424 substituent group Chemical group 0.000 claims description 22
- SBUXRMKDJWEXRL-ZWKOTPCHSA-N trans-body Chemical compound O=C([C@@H]1N(C2=O)[C@H](C3=C(C4=CC=CC=C4N3)C1)CC)N2C1=CC=C(F)C=C1 SBUXRMKDJWEXRL-ZWKOTPCHSA-N 0.000 claims description 19
- 239000003795 chemical substances by application Substances 0.000 claims description 15
- 238000000034 method Methods 0.000 claims description 15
- 230000002087 whitening effect Effects 0.000 claims description 13
- VFTAQENJCWXWIP-UHFFFAOYSA-N 8-acetyl-5-methyl-3-oxa-6-thia-8-azabicyclo[3.2.1]octane-2,4-dione Chemical compound O=C1OC(=O)C2(C)SCC1N2C(=O)C VFTAQENJCWXWIP-UHFFFAOYSA-N 0.000 claims description 8
- 150000007530 organic bases Chemical class 0.000 claims description 8
- 125000005843 halogen group Chemical group 0.000 claims description 6
- 238000002844 melting Methods 0.000 claims description 5
- 230000008018 melting Effects 0.000 claims description 5
- 239000002253 acid Substances 0.000 claims description 3
- ZVQOOHYFBIDMTQ-UHFFFAOYSA-N [methyl(oxido){1-[6-(trifluoromethyl)pyridin-3-yl]ethyl}-lambda(6)-sulfanylidene]cyanamide Chemical compound N#CN=S(C)(=O)C(C)C1=CC=C(C(F)(F)F)N=C1 ZVQOOHYFBIDMTQ-UHFFFAOYSA-N 0.000 claims 1
- 230000008099 melanin synthesis Effects 0.000 abstract description 14
- 230000002401 inhibitory effect Effects 0.000 abstract description 5
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 111
- 230000015572 biosynthetic process Effects 0.000 description 76
- 238000003786 synthesis reaction Methods 0.000 description 76
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 54
- 230000002829 reductive effect Effects 0.000 description 51
- 239000000243 solution Substances 0.000 description 49
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 46
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 42
- 238000006243 chemical reaction Methods 0.000 description 42
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 41
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 36
- 235000013350 formula milk Nutrition 0.000 description 35
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 30
- 239000000203 mixture Substances 0.000 description 30
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 29
- 229960002433 cysteine Drugs 0.000 description 27
- 239000007787 solid Substances 0.000 description 25
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 24
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 24
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 22
- 239000000126 substance Substances 0.000 description 21
- 239000013256 coordination polymer Substances 0.000 description 20
- 238000005481 NMR spectroscopy Methods 0.000 description 19
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 18
- 235000019441 ethanol Nutrition 0.000 description 18
- 229940024606 amino acid Drugs 0.000 description 17
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 17
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 16
- 235000001014 amino acid Nutrition 0.000 description 16
- 238000001914 filtration Methods 0.000 description 16
- 235000018417 cysteine Nutrition 0.000 description 15
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 15
- 238000002360 preparation method Methods 0.000 description 15
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical class O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 15
- 150000001413 amino acids Chemical class 0.000 description 14
- 238000004519 manufacturing process Methods 0.000 description 14
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 14
- HDDMIKXHZLVXSA-UHFFFAOYSA-N 2-ethoxycarbonyl-2-methyl-1,3-thiazolidine-4-carboxylic acid Chemical compound CCOC(=O)C1(C)NC(C(O)=O)CS1 HDDMIKXHZLVXSA-UHFFFAOYSA-N 0.000 description 13
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 13
- 238000012360 testing method Methods 0.000 description 13
- 239000004201 L-cysteine Substances 0.000 description 12
- 235000013878 L-cysteine Nutrition 0.000 description 12
- XUMBMVFBXHLACL-UHFFFAOYSA-N Melanin Chemical compound O=C1C(=O)C(C2=CNC3=C(C(C(=O)C4=C32)=O)C)=C2C4=CNC2=C1C XUMBMVFBXHLACL-UHFFFAOYSA-N 0.000 description 12
- SJRJJKPEHAURKC-UHFFFAOYSA-N N-Methylmorpholine Chemical compound CN1CCOCC1 SJRJJKPEHAURKC-UHFFFAOYSA-N 0.000 description 12
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 12
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 12
- 238000013112 stability test Methods 0.000 description 12
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 11
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 11
- SBUXRMKDJWEXRL-ROUUACIJSA-N cis-body Chemical compound O=C([C@H]1N(C2=O)[C@H](C3=C(C4=CC=CC=C4N3)C1)CC)N2C1=CC=C(F)C=C1 SBUXRMKDJWEXRL-ROUUACIJSA-N 0.000 description 11
- 239000002904 solvent Substances 0.000 description 11
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 10
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 10
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 10
- 238000004128 high performance liquid chromatography Methods 0.000 description 10
- 239000000463 material Substances 0.000 description 10
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 10
- JCAKCGQZNBEITC-UHFFFAOYSA-N 2-methyl-1,3-thiazolidine-2,4-dicarboxylic acid Chemical compound OC(=O)C1(C)NC(C(O)=O)CS1 JCAKCGQZNBEITC-UHFFFAOYSA-N 0.000 description 9
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 9
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 9
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 9
- 125000002950 monocyclic group Chemical group 0.000 description 9
- 239000011541 reaction mixture Substances 0.000 description 9
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 8
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 8
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 8
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 description 8
- 239000012346 acetyl chloride Substances 0.000 description 8
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 8
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 8
- 125000004076 pyridyl group Chemical group 0.000 description 8
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 7
- 238000003756 stirring Methods 0.000 description 7
- 238000003860 storage Methods 0.000 description 7
- 229910052717 sulfur Inorganic materials 0.000 description 7
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 6
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- YASYEJJMZJALEJ-UHFFFAOYSA-N Citric acid monohydrate Chemical compound O.OC(=O)CC(O)(C(O)=O)CC(O)=O YASYEJJMZJALEJ-UHFFFAOYSA-N 0.000 description 6
- 239000012300 argon atmosphere Substances 0.000 description 6
- 239000000843 powder Substances 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 239000004471 Glycine Substances 0.000 description 5
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 5
- 125000003275 alpha amino acid group Chemical group 0.000 description 5
- 239000003814 drug Substances 0.000 description 5
- 239000003480 eluent Substances 0.000 description 5
- 239000000706 filtrate Substances 0.000 description 5
- 150000007529 inorganic bases Chemical class 0.000 description 5
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 5
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 5
- 125000002958 pentadecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 5
- 229910000027 potassium carbonate Inorganic materials 0.000 description 5
- 238000010898 silica gel chromatography Methods 0.000 description 5
- XHFLOLLMZOTPSM-UHFFFAOYSA-M sodium;hydrogen carbonate;hydrate Chemical compound [OH-].[Na+].OC(O)=O XHFLOLLMZOTPSM-UHFFFAOYSA-M 0.000 description 5
- 239000011593 sulfur Substances 0.000 description 5
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 5
- DMULYRUQGZZSDA-UHFFFAOYSA-N 2-ethoxycarbonyl-3-hexadecanoyl-2-methyl-1,3-thiazolidine-4-carboxylic acid Chemical compound CCCCCCCCCCCCCCCC(=O)N1C(C(O)=O)CSC1(C)C(=O)OCC DMULYRUQGZZSDA-UHFFFAOYSA-N 0.000 description 4
- FVYCWQHIHPMASV-UHFFFAOYSA-N 3-decanoyl-2-ethoxycarbonyl-1,3-thiazolidine-4-carboxylic acid Chemical compound CCCCCCCCCC(=O)N1C(C(O)=O)CSC1C(=O)OCC FVYCWQHIHPMASV-UHFFFAOYSA-N 0.000 description 4
- OKWVYHBTQAJGRQ-UHFFFAOYSA-N 3-decanoyl-2-ethoxycarbonyl-2-methyl-1,3-thiazolidine-4-carboxylic acid Chemical compound CCCCCCCCCC(=O)N1C(C(O)=O)CSC1(C)C(=O)OCC OKWVYHBTQAJGRQ-UHFFFAOYSA-N 0.000 description 4
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 4
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 4
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- 238000010521 absorption reaction Methods 0.000 description 4
- 229960003767 alanine Drugs 0.000 description 4
- 235000004279 alanine Nutrition 0.000 description 4
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 4
- 210000004027 cell Anatomy 0.000 description 4
- 229920001429 chelating resin Polymers 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 4
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 4
- 235000019341 magnesium sulphate Nutrition 0.000 description 4
- 230000014759 maintenance of location Effects 0.000 description 4
- 239000002245 particle Substances 0.000 description 4
- 239000013077 target material Substances 0.000 description 4
- 125000004213 tert-butoxy group Chemical group [H]C([H])([H])C(O*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 4
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 4
- QKENWXNAIAEMIY-UHFFFAOYSA-N 3-acetyl-2-[3-hydroxy-5-(hydroxymethyl)-2-methylpyridin-4-yl]-1,3-thiazolidine-4-carboxylic acid Chemical compound CC(=O)N1C(C(O)=O)CSC1C1=C(CO)C=NC(C)=C1O QKENWXNAIAEMIY-UHFFFAOYSA-N 0.000 description 3
- BNXIAIVVCIFJDT-UHFFFAOYSA-N 3-acetyl-2-ethoxycarbonyl-1,3-thiazolidine-4-carboxylic acid Chemical compound CCOC(=O)C1SCC(C(O)=O)N1C(C)=O BNXIAIVVCIFJDT-UHFFFAOYSA-N 0.000 description 3
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 3
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 150000001370 alpha-amino acid derivatives Chemical class 0.000 description 3
- 230000009435 amidation Effects 0.000 description 3
- 238000007112 amidation reaction Methods 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 125000004432 carbon atom Chemical group C* 0.000 description 3
- 230000032050 esterification Effects 0.000 description 3
- 238000005886 esterification reaction Methods 0.000 description 3
- 150000002148 esters Chemical class 0.000 description 3
- IDGUHHHQCWSQLU-UHFFFAOYSA-N ethanol;hydrate Chemical compound O.CCO IDGUHHHQCWSQLU-UHFFFAOYSA-N 0.000 description 3
- NTNZTEQNFHNYBC-UHFFFAOYSA-N ethyl 2-aminoacetate Chemical compound CCOC(=O)CN NTNZTEQNFHNYBC-UHFFFAOYSA-N 0.000 description 3
- 210000004209 hair Anatomy 0.000 description 3
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 229910052739 hydrogen Inorganic materials 0.000 description 3
- 230000007062 hydrolysis Effects 0.000 description 3
- 238000006460 hydrolysis reaction Methods 0.000 description 3
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 3
- JMMWKPVZQRWMSS-UHFFFAOYSA-N isopropanol acetate Natural products CC(C)OC(C)=O JMMWKPVZQRWMSS-UHFFFAOYSA-N 0.000 description 3
- 229940011051 isopropyl acetate Drugs 0.000 description 3
- GWYFCOCPABKNJV-UHFFFAOYSA-N isovaleric acid Chemical compound CC(C)CC(O)=O GWYFCOCPABKNJV-UHFFFAOYSA-N 0.000 description 3
- DWKPPFQULDPWHX-VKHMYHEASA-N l-alanyl ester Chemical compound COC(=O)[C@H](C)N DWKPPFQULDPWHX-VKHMYHEASA-N 0.000 description 3
- 230000007774 longterm Effects 0.000 description 3
- LHECNLDHYYGZDL-UHFFFAOYSA-N methyl 3-acetyl-2-(1,2,3,4,5-pentahydroxypentyl)-1,3-thiazolidine-4-carboxylate Chemical compound COC(=O)C1CSC(C(O)C(O)C(O)C(O)CO)N1C(C)=O LHECNLDHYYGZDL-UHFFFAOYSA-N 0.000 description 3
- KQSSATDQUYCRGS-UHFFFAOYSA-N methyl glycinate Chemical compound COC(=O)CN KQSSATDQUYCRGS-UHFFFAOYSA-N 0.000 description 3
- 239000012046 mixed solvent Substances 0.000 description 3
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 238000010992 reflux Methods 0.000 description 3
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 125000003548 sec-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 3
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 3
- 229940124597 therapeutic agent Drugs 0.000 description 3
- WQZGKKKJIJFFOK-SVZMEOIVSA-N (+)-Galactose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-SVZMEOIVSA-N 0.000 description 2
- 125000004890 (C1-C6) alkylamino group Chemical group 0.000 description 2
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 2
- PJUPKRYGDFTMTM-UHFFFAOYSA-N 1-hydroxybenzotriazole;hydrate Chemical compound O.C1=CC=C2N(O)N=NC2=C1 PJUPKRYGDFTMTM-UHFFFAOYSA-N 0.000 description 2
- JEPVUMTVFPQKQE-UHFFFAOYSA-N 2-(1,2,3,4,5-pentahydroxypentyl)-1,3-thiazolidin-3-ium-4-carboxylate Chemical compound OCC(O)C(O)C(O)C(O)C1NC(C(O)=O)CS1 JEPVUMTVFPQKQE-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- CDNKRUFYOOECEU-UHFFFAOYSA-N 2-[3-hydroxy-5-(hydroxymethyl)-2-methylpyridin-4-yl]-1,3-thiazolidine-4-carboxylic acid Chemical compound CC1=NC=C(CO)C(C2SCC(N2)C(O)=O)=C1O CDNKRUFYOOECEU-UHFFFAOYSA-N 0.000 description 2
- CUHKNSQDMNYEFA-UHFFFAOYSA-N 2-ethoxycarbonyl-1,3-thiazolidine-4-carboxylic acid Chemical compound CCOC(=O)C1NC(C(O)=O)CS1 CUHKNSQDMNYEFA-UHFFFAOYSA-N 0.000 description 2
- QHNSMFVRVKNCAM-UHFFFAOYSA-N 3-acetyl-2-(1,2,3,4,5-pentahydroxypentyl)-1,3-thiazolidine-4-carboxylic acid Chemical compound CC(=O)N1C(C(O)C(O)C(O)C(O)CO)SCC1C(O)=O QHNSMFVRVKNCAM-UHFFFAOYSA-N 0.000 description 2
- HUNTVLOXOOTOCV-UHFFFAOYSA-N 3-acetyl-2-methoxycarbonyl-2-methyl-1,3-thiazolidine-4-carboxylic acid Chemical compound COC(=O)C1(C)SCC(C(O)=O)N1C(C)=O HUNTVLOXOOTOCV-UHFFFAOYSA-N 0.000 description 2
- AERPJPSICHEUPD-UHFFFAOYSA-N 3-decanoyl-1,3-thiazolidine-2,4-dicarboxylic acid Chemical compound CCCCCCCCCC(=O)N1C(C(O)=O)CSC1C(O)=O AERPJPSICHEUPD-UHFFFAOYSA-N 0.000 description 2
- OZFNZYJZIHYRFL-UHFFFAOYSA-N 3-decanoyl-2-methyl-1,3-thiazolidine-2,4-dicarboxylic acid Chemical compound CCCCCCCCCC(=O)N1C(C(O)=O)CSC1(C)C(O)=O OZFNZYJZIHYRFL-UHFFFAOYSA-N 0.000 description 2
- VKKSWGYSMDXWDU-UHFFFAOYSA-N 3-hexadecanoyl-2-methyl-1,3-thiazolidine-2,4-dicarboxylic acid Chemical compound CCCCCCCCCCCCCCCC(=O)N1C(C(O)=O)CSC1(C)C(O)=O VKKSWGYSMDXWDU-UHFFFAOYSA-N 0.000 description 2
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- ZRALSGWEFCBTJO-UHFFFAOYSA-N Guanidine Chemical compound NC(N)=N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 2
- 150000008065 acid anhydrides Chemical class 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 235000008206 alpha-amino acids Nutrition 0.000 description 2
- 230000002862 amidating effect Effects 0.000 description 2
- 125000003277 amino group Chemical group 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- 229910052786 argon Inorganic materials 0.000 description 2
- 239000012267 brine Substances 0.000 description 2
- 125000004106 butoxy group Chemical group [*]OC([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 2
- 125000006309 butyl amino group Chemical group 0.000 description 2
- 239000012295 chemical reaction liquid Substances 0.000 description 2
- 238000009833 condensation Methods 0.000 description 2
- 230000005494 condensation Effects 0.000 description 2
- 238000002425 crystallisation Methods 0.000 description 2
- 230000008025 crystallization Effects 0.000 description 2
- IPIVAXLHTVNRBS-UHFFFAOYSA-N decanoyl chloride Chemical compound CCCCCCCCCC(Cl)=O IPIVAXLHTVNRBS-UHFFFAOYSA-N 0.000 description 2
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000006612 decyloxy group Chemical group 0.000 description 2
- VGIFWOHNNTUGHN-UHFFFAOYSA-N diethyl 3-decanoyl-2-methyl-1,3-thiazolidine-2,4-dicarboxylate Chemical compound CCCCCCCCCC(=O)N1C(C(=O)OCC)CSC1(C)C(=O)OCC VGIFWOHNNTUGHN-UHFFFAOYSA-N 0.000 description 2
- QIUBALRFZKEMNA-UHFFFAOYSA-N diethyl 3-hexadecanoyl-2-methyl-1,3-thiazolidine-2,4-dicarboxylate Chemical compound CCCCCCCCCCCCCCCC(=O)N1C(C(=O)OCC)CSC1(C)C(=O)OCC QIUBALRFZKEMNA-UHFFFAOYSA-N 0.000 description 2
- KNMSOMGVNLBQJC-UHFFFAOYSA-N dimethyl 1,3-thiazolidine-2,4-dicarboxylate;hydrochloride Chemical compound Cl.COC(=O)C1CSC(C(=O)OC)N1 KNMSOMGVNLBQJC-UHFFFAOYSA-N 0.000 description 2
- BNBKDVANJHYGEH-UHFFFAOYSA-N dimethyl 3-acetyl-1,3-thiazolidine-2,4-dicarboxylate Chemical compound COC(=O)C1CSC(C(=O)OC)N1C(C)=O BNBKDVANJHYGEH-UHFFFAOYSA-N 0.000 description 2
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000004494 ethyl ester group Chemical group 0.000 description 2
- 125000000031 ethylamino group Chemical group [H]C([H])([H])C([H])([H])N([H])[*] 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 235000019634 flavors Nutrition 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- HHLFWLYXYJOTON-UHFFFAOYSA-N glyoxylic acid Chemical compound OC(=O)C=O HHLFWLYXYJOTON-UHFFFAOYSA-N 0.000 description 2
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000001245 hexylamino group Chemical group [H]N([*])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 2
- 125000003707 hexyloxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- 125000006316 iso-butyl amino group Chemical group [H]N(*)C([H])([H])C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 125000002510 isobutoxy group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])O* 0.000 description 2
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 239000006210 lotion Substances 0.000 description 2
- 125000000250 methylamino group Chemical group [H]N(*)C([H])([H])[H] 0.000 description 2
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 description 2
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 125000000913 palmityl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000004115 pentoxy group Chemical group [*]OC([H])([H])C([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 2
- 125000004894 pentylamino group Chemical group C(CCCC)N* 0.000 description 2
- 239000002304 perfume Substances 0.000 description 2
- 239000008363 phosphate buffer Substances 0.000 description 2
- 230000001766 physiological effect Effects 0.000 description 2
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 229940002612 prodrug Drugs 0.000 description 2
- 239000000651 prodrug Substances 0.000 description 2
- 125000002572 propoxy group Chemical group [*]OC([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 2
- 125000006308 propyl amino group Chemical group 0.000 description 2
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 230000035484 reaction time Effects 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- RPACBEVZENYWOL-XFULWGLBSA-M sodium;(2r)-2-[6-(4-chlorophenoxy)hexyl]oxirane-2-carboxylate Chemical compound [Na+].C=1C=C(Cl)C=CC=1OCCCCCC[C@]1(C(=O)[O-])CO1 RPACBEVZENYWOL-XFULWGLBSA-M 0.000 description 2
- 150000005846 sugar alcohols Polymers 0.000 description 2
- 125000004434 sulfur atom Chemical group 0.000 description 2
- 125000006318 tert-butyl amino group Chemical group [H]N(*)C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 125000003396 thiol group Chemical group [H]S* 0.000 description 2
- 125000002889 tridecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- 229960004441 tyrosine Drugs 0.000 description 2
- 125000002948 undecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- JWZZKOKVBUJMES-UHFFFAOYSA-N (+-)-Isoprenaline Chemical compound CC(C)NCC(O)C1=CC=C(O)C(O)=C1 JWZZKOKVBUJMES-UHFFFAOYSA-N 0.000 description 1
- TXTWXQXDMWILOF-UHFFFAOYSA-N (2-ethoxy-2-oxoethyl)azanium;chloride Chemical compound [Cl-].CCOC(=O)C[NH3+] TXTWXQXDMWILOF-UHFFFAOYSA-N 0.000 description 1
- YEDNBEGNKOANMB-REOHCLBHSA-N (2r)-2-amino-3-sulfanylpropanamide Chemical compound SC[C@H](N)C(N)=O YEDNBEGNKOANMB-REOHCLBHSA-N 0.000 description 1
- LLPCTYVJIFDZPF-GMSGAONNSA-N (2r,4s)-3-acetyl-2-ethoxycarbonyl-2-methyl-1,3-thiazolidine-4-carboxylic acid Chemical compound CCOC(=O)[C@@]1(C)SC[C@H](C(O)=O)N1C(C)=O LLPCTYVJIFDZPF-GMSGAONNSA-N 0.000 description 1
- CMLMTPHQDNAMKO-SVGQVSJJSA-N (2r,4s)-3-acetyl-2-methyl-1,3-thiazolidine-2,4-dicarboxylic acid Chemical compound CC(=O)N1[C@@H](C(O)=O)CS[C@]1(C)C(O)=O CMLMTPHQDNAMKO-SVGQVSJJSA-N 0.000 description 1
- QIJRTFXNRTXDIP-YBBRRFGFSA-N (2s)-2-amino-3-sulfanylpropanoic acid;hydrate;hydrochloride Chemical compound O.Cl.SC[C@@H](N)C(O)=O QIJRTFXNRTXDIP-YBBRRFGFSA-N 0.000 description 1
- LLPCTYVJIFDZPF-XVKPBYJWSA-N (2s,4r)-3-acetyl-2-ethoxycarbonyl-2-methyl-1,3-thiazolidine-4-carboxylic acid Chemical compound CCOC(=O)[C@]1(C)SC[C@@H](C(O)=O)N1C(C)=O LLPCTYVJIFDZPF-XVKPBYJWSA-N 0.000 description 1
- CMLMTPHQDNAMKO-XNCJUZBTSA-N (2s,4r)-3-acetyl-2-methyl-1,3-thiazolidine-2,4-dicarboxylic acid Chemical compound CC(=O)N1[C@H](C(O)=O)CS[C@@]1(C)C(O)=O CMLMTPHQDNAMKO-XNCJUZBTSA-N 0.000 description 1
- IZZZHEKMOXCDPJ-YFKPBYRVSA-N (5r)-5-acetamido-2,4-dioxo-6-sulfanylhexanoic acid Chemical compound CC(=O)N[C@@H](CS)C(=O)CC(=O)C(O)=O IZZZHEKMOXCDPJ-YFKPBYRVSA-N 0.000 description 1
- 125000004512 1,2,3-thiadiazol-4-yl group Chemical group S1N=NC(=C1)* 0.000 description 1
- 125000001607 1,2,3-triazol-1-yl group Chemical group [*]N1N=NC([H])=C1[H] 0.000 description 1
- 125000001359 1,2,3-triazol-4-yl group Chemical group [H]N1N=NC([*])=C1[H] 0.000 description 1
- 125000003626 1,2,4-triazol-1-yl group Chemical group [*]N1N=C([H])N=C1[H] 0.000 description 1
- 125000001305 1,2,4-triazol-3-yl group Chemical group [H]N1N=C([*])N=C1[H] 0.000 description 1
- 125000004507 1,2,5-oxadiazol-3-yl group Chemical group O1N=C(C=N1)* 0.000 description 1
- 125000004509 1,3,4-oxadiazol-2-yl group Chemical group O1C(=NN=C1)* 0.000 description 1
- 125000004521 1,3,4-thiadiazol-2-yl group Chemical group S1C(=NN=C1)* 0.000 description 1
- MNDORKXIPQABFE-UHFFFAOYSA-N 1-(2-methyl-1,3-thiazolidin-3-yl)ethanone Chemical compound CC1SCCN1C(C)=O MNDORKXIPQABFE-UHFFFAOYSA-N 0.000 description 1
- 125000004173 1-benzimidazolyl group Chemical group [H]C1=NC2=C([H])C([H])=C([H])C([H])=C2N1* 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- HFDFBFAJJPZBNS-UHFFFAOYSA-N 2-ethoxycarbonyl-2-methyl-3-[(2-methylpropan-2-yl)oxycarbonyl]-1,3-thiazolidine-4-carboxylic acid Chemical compound CCOC(=O)C1(C)SCC(C(O)=O)N1C(=O)OC(C)(C)C HFDFBFAJJPZBNS-UHFFFAOYSA-N 0.000 description 1
- 125000002941 2-furyl group Chemical group O1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- BSKHPKMHTQYZBB-UHFFFAOYSA-N 2-methylpyridine Chemical compound CC1=CC=CC=N1 BSKHPKMHTQYZBB-UHFFFAOYSA-N 0.000 description 1
- TYEYBOSBBBHJIV-UHFFFAOYSA-M 2-oxobutanoate Chemical compound CCC(=O)C([O-])=O TYEYBOSBBBHJIV-UHFFFAOYSA-M 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 125000000389 2-pyrrolyl group Chemical group [H]N1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000003682 3-furyl group Chemical group O1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000001397 3-pyrrolyl group Chemical group [H]N1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- 125000001541 3-thienyl group Chemical group S1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- KDDQRKBRJSGMQE-UHFFFAOYSA-N 4-thiazolyl Chemical group [C]1=CSC=N1 KDDQRKBRJSGMQE-UHFFFAOYSA-N 0.000 description 1
- 125000004539 5-benzimidazolyl group Chemical group N1=CNC2=C1C=CC(=C2)* 0.000 description 1
- CWDWFSXUQODZGW-UHFFFAOYSA-N 5-thiazolyl Chemical group [C]1=CN=CS1 CWDWFSXUQODZGW-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- XUJNEKJLAYXESH-UWTATZPHSA-N D-Cysteine Chemical compound SC[C@@H](N)C(O)=O XUJNEKJLAYXESH-UWTATZPHSA-N 0.000 description 1
- XBPCUCUWBYBCDP-UHFFFAOYSA-N Dicyclohexylamine Chemical compound C1CCCCC1NC1CCCCC1 XBPCUCUWBYBCDP-UHFFFAOYSA-N 0.000 description 1
- 229930195710 D‐cysteine Natural products 0.000 description 1
- 239000004129 EU approved improving agent Substances 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- XXRCUYVCPSWGCC-UHFFFAOYSA-N Ethyl pyruvate Chemical compound CCOC(=O)C(C)=O XXRCUYVCPSWGCC-UHFFFAOYSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 102000011782 Keratins Human genes 0.000 description 1
- 108010076876 Keratins Proteins 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- QIJRTFXNRTXDIP-JIZZDEOASA-N L-cysteine hydrochloride hydrate Chemical compound O.Cl.SC[C@H](N)C(O)=O QIJRTFXNRTXDIP-JIZZDEOASA-N 0.000 description 1
- 150000008538 L-cysteines Chemical class 0.000 description 1
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- CHJJGSNFBQVOTG-UHFFFAOYSA-N N-methyl-guanidine Natural products CNC(N)=N CHJJGSNFBQVOTG-UHFFFAOYSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- 206010042496 Sunburn Diseases 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- 102000004142 Trypsin Human genes 0.000 description 1
- 108090000631 Trypsin Proteins 0.000 description 1
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 1
- CLTRPFHGRORABV-UHFFFAOYSA-N [4-(8-acetyl-2-oxo-3-oxa-6-thia-8-azabicyclo[3.2.1]octan-4-yl)-2,3,4-triacetyloxybutyl] acetate Chemical compound CC(=O)OCC(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C1OC(=O)C2CSC1N2C(C)=O CLTRPFHGRORABV-UHFFFAOYSA-N 0.000 description 1
- VLSOAXRVHARBEQ-UHFFFAOYSA-N [4-fluoro-2-(hydroxymethyl)phenyl]methanol Chemical compound OCC1=CC=C(F)C=C1CO VLSOAXRVHARBEQ-UHFFFAOYSA-N 0.000 description 1
- 239000006096 absorbing agent Substances 0.000 description 1
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 125000003368 amide group Chemical group 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000003862 amino acid derivatives Chemical class 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 229940035676 analgesics Drugs 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 229940121363 anti-inflammatory agent Drugs 0.000 description 1
- 230000001166 anti-perspirative effect Effects 0.000 description 1
- 230000001153 anti-wrinkle effect Effects 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 239000003213 antiperspirant Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 125000002511 behenyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- JUHORIMYRDESRB-UHFFFAOYSA-N benzathine Chemical compound C=1C=CC=CC=1CNCCNCC1=CC=CC=C1 JUHORIMYRDESRB-UHFFFAOYSA-N 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000003354 benzotriazolyl group Chemical group N1N=NC2=C1C=CC=C2* 0.000 description 1
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 150000001576 beta-amino acids Chemical class 0.000 description 1
- 239000007844 bleaching agent Substances 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 238000013329 compounding Methods 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 238000010908 decantation Methods 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 210000003298 dental enamel Anatomy 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 235000015872 dietary supplement Nutrition 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- AUAHSDLXVCLXIZ-UHFFFAOYSA-N diethyl 3-acetyl-2-methyl-1,3-thiazolidine-2,4-dicarboxylate Chemical compound CCOC(=O)C1CSC(C)(C(=O)OCC)N1C(C)=O AUAHSDLXVCLXIZ-UHFFFAOYSA-N 0.000 description 1
- JUZYXMMUJLZZRP-UHFFFAOYSA-N diethyl 3-decanoyl-1,3-thiazolidine-2,4-dicarboxylate Chemical compound CCCCCCCCCC(=O)N1C(C(=O)OCC)CSC1C(=O)OCC JUZYXMMUJLZZRP-UHFFFAOYSA-N 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- SWSQBOPZIKWTGO-UHFFFAOYSA-N dimethylaminoamidine Natural products CN(C)C(N)=N SWSQBOPZIKWTGO-UHFFFAOYSA-N 0.000 description 1
- 229940078469 dl- cysteine Drugs 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- YVKSGVDJQXLXDV-BYPYZUCNSA-N ethyl (2r)-2-amino-3-sulfanylpropanoate Chemical compound CCOC(=O)[C@@H](N)CS YVKSGVDJQXLXDV-BYPYZUCNSA-N 0.000 description 1
- OAYLNYINCPYISS-UHFFFAOYSA-N ethyl acetate;hexane Chemical compound CCCCCC.CCOC(C)=O OAYLNYINCPYISS-UHFFFAOYSA-N 0.000 description 1
- 230000006203 ethylation Effects 0.000 description 1
- 238000006200 ethylation reaction Methods 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 210000004709 eyebrow Anatomy 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000000417 fungicide Substances 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 235000013402 health food Nutrition 0.000 description 1
- 125000005446 heptyloxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- 241000411851 herbal medicine Species 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- ARBOVOVUTSQWSS-UHFFFAOYSA-N hexadecanoyl chloride Chemical compound CCCCCCCCCCCCCCCC(Cl)=O ARBOVOVUTSQWSS-UHFFFAOYSA-N 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- COQRGFWWJBEXRC-UHFFFAOYSA-N hydron;methyl 2-aminoacetate;chloride Chemical compound Cl.COC(=O)CN COQRGFWWJBEXRC-UHFFFAOYSA-N 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 1
- 125000000593 indol-1-yl group Chemical group [H]C1=C([H])C([H])=C2N([*])C([H])=C([H])C2=C1[H] 0.000 description 1
- 125000002249 indol-2-yl group Chemical group [H]C1=C([H])C([H])=C2N([H])C([*])=C([H])C2=C1[H] 0.000 description 1
- 125000000814 indol-3-yl group Chemical group [H]C1=C([H])C([H])=C2N([H])C([H])=C([*])C2=C1[H] 0.000 description 1
- 125000004531 indol-5-yl group Chemical group [H]N1C([H])=C([H])C2=C([H])C(*)=C([H])C([H])=C12 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 125000005956 isoquinolyl group Chemical group 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 125000002960 margaryl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 229960003194 meglumine Drugs 0.000 description 1
- 229940087646 methanolamine Drugs 0.000 description 1
- IYUKFAFDFHZKPI-DFWYDOINSA-N methyl (2s)-2-aminopropanoate;hydrochloride Chemical compound Cl.COC(=O)[C@H](C)N IYUKFAFDFHZKPI-DFWYDOINSA-N 0.000 description 1
- CWKLZLBVOJRSOM-UHFFFAOYSA-N methyl pyruvate Chemical compound COC(=O)C(C)=O CWKLZLBVOJRSOM-UHFFFAOYSA-N 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- 125000006611 nonyloxy group Chemical group 0.000 description 1
- 125000005447 octyloxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- 125000001117 oleyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])/C([H])=C([H])\C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000001715 oxadiazolyl group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 210000004694 pigment cell Anatomy 0.000 description 1
- 230000019612 pigmentation Effects 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 235000011056 potassium acetate Nutrition 0.000 description 1
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 125000004307 pyrazin-2-yl group Chemical group [H]C1=C([H])N=C(*)C([H])=N1 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000002206 pyridazin-3-yl group Chemical group [H]C1=C([H])C([H])=C(*)N=N1 0.000 description 1
- 125000004940 pyridazin-4-yl group Chemical group N1=NC=C(C=C1)* 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- FCHXJFJNDJXENQ-UHFFFAOYSA-N pyridoxal hydrochloride Chemical compound Cl.CC1=NC=C(CO)C(C=O)=C1O FCHXJFJNDJXENQ-UHFFFAOYSA-N 0.000 description 1
- RADKZDMFGJYCBB-UHFFFAOYSA-N pyridoxal hydrochloride Natural products CC1=NC=C(CO)C(C=O)=C1O RADKZDMFGJYCBB-UHFFFAOYSA-N 0.000 description 1
- 125000000246 pyrimidin-2-yl group Chemical group [H]C1=NC(*)=NC([H])=C1[H] 0.000 description 1
- 125000004527 pyrimidin-4-yl group Chemical group N1=CN=C(C=C1)* 0.000 description 1
- 125000004528 pyrimidin-5-yl group Chemical group N1=CN=CC(=C1)* 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 239000002453 shampoo Substances 0.000 description 1
- 230000037384 skin absorption Effects 0.000 description 1
- 231100000274 skin absorption Toxicity 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 239000000344 soap Substances 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 125000004079 stearyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 150000003463 sulfur Chemical class 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 210000004243 sweat Anatomy 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- DYHSDKLCOJIUFX-UHFFFAOYSA-N tert-butoxycarbonyl anhydride Chemical compound CC(C)(C)OC(=O)OC(=O)OC(C)(C)C DYHSDKLCOJIUFX-UHFFFAOYSA-N 0.000 description 1
- 125000004523 tetrazol-1-yl group Chemical group N1(N=NN=C1)* 0.000 description 1
- 125000004299 tetrazol-5-yl group Chemical group [H]N1N=NC(*)=N1 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 150000003548 thiazolidines Chemical class 0.000 description 1
- 125000001984 thiazolidinyl group Chemical group 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 229930192474 thiophene Natural products 0.000 description 1
- DZLNHFMRPBPULJ-UHFFFAOYSA-N thioproline Chemical compound OC(=O)C1CSCN1 DZLNHFMRPBPULJ-UHFFFAOYSA-N 0.000 description 1
- DAXBISKSIDBYEU-UHFFFAOYSA-N tidiacic Chemical compound OC(=O)C1CSC(C(O)=O)N1 DAXBISKSIDBYEU-UHFFFAOYSA-N 0.000 description 1
- 239000000606 toothpaste Substances 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 239000012588 trypsin Substances 0.000 description 1
- 239000004474 valine Substances 0.000 description 1
- 229940124549 vasodilator Drugs 0.000 description 1
- 239000003071 vasodilator agent Substances 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229920003169 water-soluble polymer Polymers 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/04—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
- C07D277/06—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having no double bonds between ring members or between ring members and non-ring members with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/49—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing heterocyclic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/49—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing heterocyclic compounds
- A61K8/4906—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing heterocyclic compounds with one nitrogen as the only hetero atom
- A61K8/4926—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing heterocyclic compounds with one nitrogen as the only hetero atom having six membered rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q1/00—Make-up preparations; Body powders; Preparations for removing make-up
- A61Q1/02—Preparations containing skin colorants, e.g. pigments
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q15/00—Anti-perspirants or body deodorants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q17/00—Barrier preparations; Preparations brought into direct contact with the skin for affording protection against external influences, e.g. sunlight, X-rays or other harmful rays, corrosive materials, bacteria or insect stings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/02—Preparations for care of the skin for chemically bleaching or whitening the skin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D513/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00
- C07D513/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00 in which the condensed system contains two hetero rings
- C07D513/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K5/00—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof
- C07K5/04—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof containing only normal peptide links
- C07K5/06—Dipeptides
- C07K5/06139—Dipeptides with the first amino acid being heterocyclic
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Dermatology (AREA)
- Epidemiology (AREA)
- Birds (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Cosmetics (AREA)
- Thiazole And Isothizaole Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Abstract
Description
도 2는 CP, N-Ac-CP, CP2Et 및 N-Ac-CP2Et의 pH 5, 그리고 70℃에 있어서의 경시적 안정성 시험의 결과를 나타낸다.
도 3은 CP, N-Ac-CP 및 N-Ac-CP2Et의 pH 6, 그리고 70℃에 있어서의 경시적 안정성 시험의 결과를 나타낸다.
도 4는 CP, N-Ac-CP 및 N-Ac-CP2Et의 pH 7, 그리고 70℃에 있어서의 경시적 안정성 시험의 결과를 나타낸다.
Claims (13)
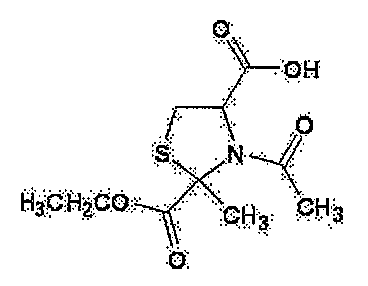
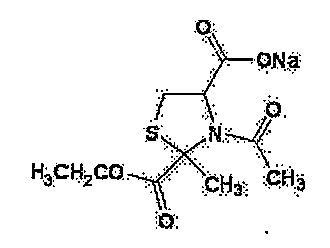
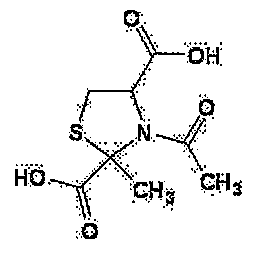
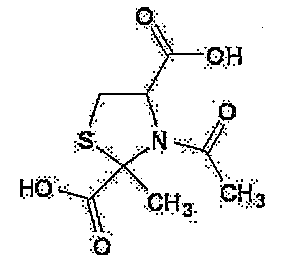
- 제1항에 있어서, 시스테인 유도체가, N-아세틸-2-메틸티아졸리딘-2,4-디카르복실산 및 N-아세틸-2-메틸티아졸리딘-2,4-디카르복실산-2-에틸에스테르와, 이들의 염으로부터 선택되는 1종 또는 2종 이상인 화장료.
- 제1항에 있어서, 시스테인 유도체가, N-아세틸-2-메틸티아졸리딘-2,4-디카르복실산의 트랜스체 및 N-아세틸-2-메틸티아졸리딘-2,4-디카르복실산-2-에틸에스테르의 트랜스체와, 이들의 염으로부터 선택되는 1종 또는 2종 이상인 화장료.
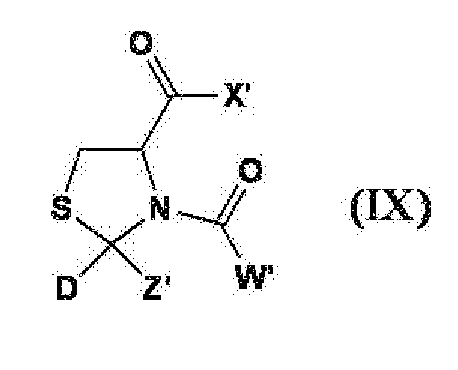
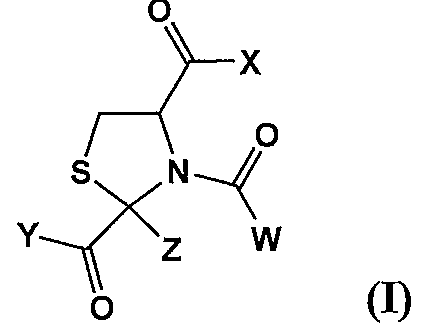
- 하기 화학식으로 표시되는 시스테인 유도체 또는 그의 염을 함유하는 화장료.
[상기 식에서,
X'는 OR1, NHR2(식 중, R1 및 R2는 각각 독립적으로 수소 원자 또는 C1-22 알킬기를 나타냄), 또는 수식되어 있어도 좋은 아미노산 잔기를 나타내고;
D는,
(1) (i) 수산기, 및
(ii) 수산기로 치환되어 있어도 좋은 C1-6 알킬기
로부터 선택되는 치환기로 치환되어 있어도 좋은 방향족 복소환기, 또는
(2) 수산기로 치환되어 있어도 좋은 C1-22 알킬기를 나타내며;
Z'는 수소 원자 또는 C1-22 알킬기를 나타내고;
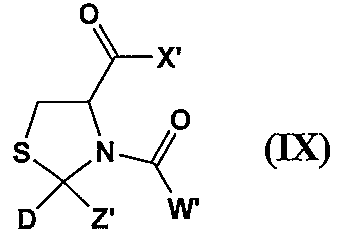
W'는 C1-22 알킬기, C1-22 알콕시기 또는 C1-22 알킬아미노기를 나타낸다.] - 하기 화학식으로 표시되는 시스테인 유도체 또는 그의 염을 함유하는 미백제.
[상기 식에서,
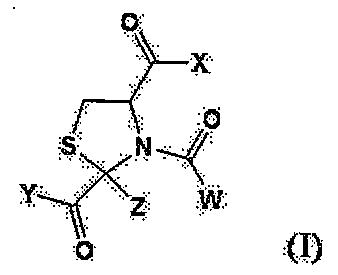
X 및 Y는 각각 독립적으로 OR1, NHR2(식 중, R1 및 R2는 각각 독립적으로 수소 원자 또는 C1-22 알킬기를 나타냄), 또는 수식되어 있어도 좋은 아미노산 잔기를 나타내거나, 혹은, X와 Y가 함께 -O-를 형성하여도 좋고;
Z는 수소 원자 또는 C1-22 알킬기를 나타내며;
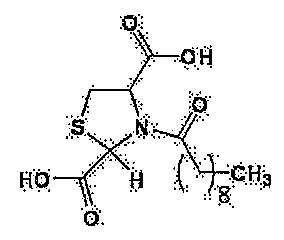
W는 C1-22 알킬기, C1-22 알콕시기 또는 C1-22 알킬아미노기를 나타낸다.] - 하기 화학식으로 표시되는 시스테인 유도체(단, N-아세틸-2-메틸티아졸리딘-2,4-디카르복실산 및 N-아세틸-2-메틸티아졸리딘-2,4-디카르복실산 무수물을 제외함) 또는 그의 염.
[상기 식에서,
X 및 Y는 각각 독립적으로 OR1, NHR2(식 중, R1 및 R2는 각각 독립적으로 수소 원자 또는 C1-22 알킬기를 나타냄), 또는 수식되어 있어도 좋은 아미노산 잔기를 나타내거나, 혹은, X와 Y가 함께 -O-를 형성하여도 좋고;
Z는 수소 원자 또는 C1-22 알킬기를 나타내며;
W는 C1-22 알킬기, C1-22 알콕시기 또는 C1-22 알킬아미노기를 나타낸다.] - 하기 화학식으로 표시되는 시스테인 유도체 또는 그의 염.
[상기 식에서,
X'는 OR1, NHR2(식 중, R1 및 R2는 각각 독립적으로 수소 원자 또는 C1-22 알킬기를 나타냄), 또는 수식되어 있어도 좋은 아미노산 잔기를 나타내고;
D는,
(1) (i) 수산기, 및
(ii) 수산기로 치환되어 있어도 좋은 C1-6 알킬기
로부터 선택되는 치환기로 치환되어 있어도 좋은 방향족 복소환기, 또는
(2) 수산기로 치환되어 있어도 좋은 C1-22 알킬기를 나타내며;
Z'는 수소 원자 또는 C1-22 알킬기를 나타내고;
W'는 C1-22 알킬기, C1-22 알콕시기 또는 C1-22 알킬아미노기를 나타낸다.] - N-아세틸-2-메틸티아졸리딘-2,4-디카르복실산의 트랜스체 또는 그의 염.
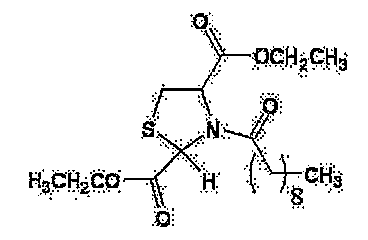
- N-아세틸-2-메틸티아졸리딘-2,4-디카르복실산-2-에틸에스테르의 트랜스체 또는 그의 염.
- 제9항에 있어서, 결정의 형태인 트랜스체.
- 제10항에 있어서, 융점이 138℃~141℃인 트랜스체.
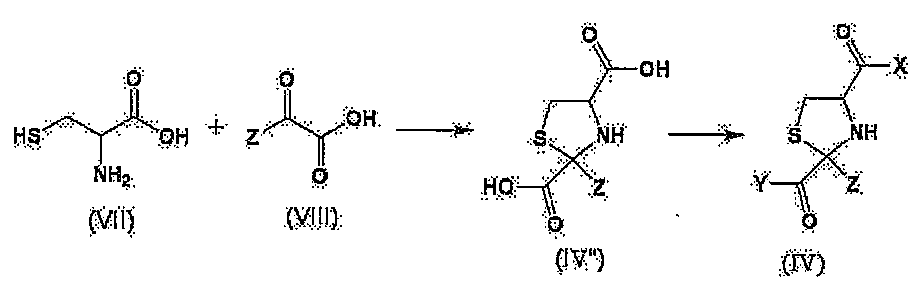
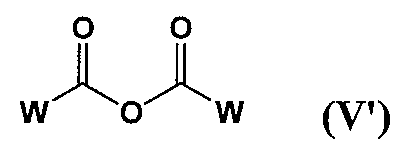
- 화학식 (IV)로 표시되는 화합물을 화학식 (V)로 표시되는 화합물 또는 화학식 (V')로 표시되는 화합물과 반응시켜 화학식 (I)로 표시되는 시스테인 유도체(단, N-아세틸-2-메틸티아졸리딘-2,4-디카르복실산 및 N-아세틸-2-메틸티아졸리딘-2,4-디카르복실산 무수물을 제외함)를 제조하는 방법.
[상기 식에서,
X 및 Y는 각각 독립적으로 OR1, NHR2(식 중, R1 및 R2는 각각 독립적으로 수소 원자 또는 C1-22 알킬기를 나타냄), 또는 수식되어 있어도 좋은 아미노산 잔기를 나타내거나, 혹은, X와 Y가 함께 -O-를 형성하여도 좋고;
Z는 수소 원자 또는 C1-22 알킬기를 나타낸다.]
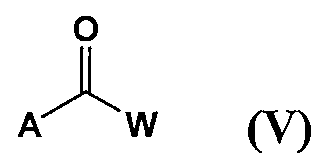
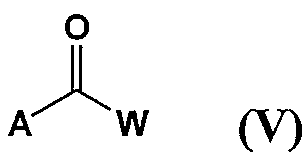
[상기 식에서, A는 할로겐 원자를 나타내고; W는 C1-22 알킬기, C1-22 알콕시기 또는 C1-22 알킬아미노기를 나타낸다.]
[상기 식에서, W는 상기와 동일한 의미를 나타낸다.]
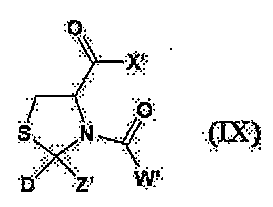
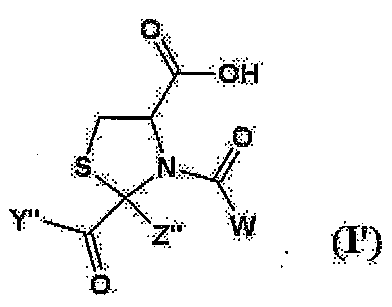
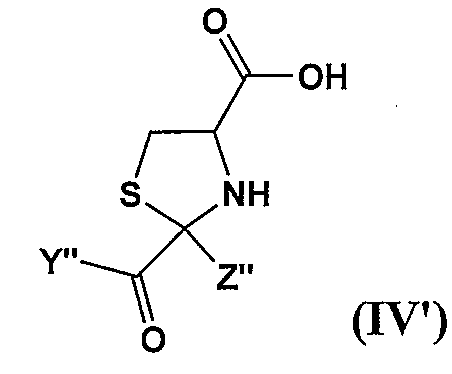
[상기 식에서, 각 기호는 상기와 동일한 의미를 나타낸다.] - 화학식 (IV')로 표시되는 화합물을, 유기 염기의 존재 하에 화학식 (V)로 표시되는 화합물과 반응시키거나, 또는 염기의 비존재 하에 화학식 (V')로 표시되는 화합물과 반응시켜 화학식 (I')로 표시되는 시스테인 유도체 또는 그의 염의 트랜스체를 선택적으로 제조하는 방법.
[상기 식에서, Y''는 C1-22 알콕시기를 나타내고; Z''는 C1-22 알킬기를 나타낸다.]
[상기 식에서, A는 할로겐 원자를 나타내고; W는 C1-22 알킬기, C1-22 알콕시기 또는 C1-22 알킬아미노기를 나타낸다.]
[상기 식에서, 각 기호는 상기와 동일한 의미를 나타낸다.]
[상기 식에서, 각 기호는 상기와 동일한 의미를 나타낸다.]
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JPJP-P-2010-123169 | 2010-05-28 | ||
| JP2010123169 | 2010-05-28 | ||
| PCT/JP2011/062293 WO2011149093A1 (ja) | 2010-05-28 | 2011-05-27 | システイン誘導体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20130028126A true KR20130028126A (ko) | 2013-03-18 |
| KR101496795B1 KR101496795B1 (ko) | 2015-03-02 |
Family
ID=45004075
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020127033919A Active KR101496795B1 (ko) | 2010-05-28 | 2011-05-27 | 시스테인 유도체 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US9212154B2 (ko) |
| EP (1) | EP2578203B1 (ko) |
| JP (1) | JP5327384B2 (ko) |
| KR (1) | KR101496795B1 (ko) |
| CN (1) | CN102917685B (ko) |
| WO (1) | WO2011149093A1 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20220159866A (ko) * | 2021-05-26 | 2022-12-05 | 경북대학교 산학협력단 | 시스테인 유도체의 피부 미백 용도 |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013081193A1 (ja) * | 2011-11-30 | 2013-06-06 | 味の素株式会社 | システイン誘導体およびアルコールを含有する化粧料 |
| JP5979154B2 (ja) * | 2011-11-30 | 2016-08-24 | 味の素株式会社 | システイン誘導体および界面活性剤を含有する化粧料 |
| JP5994789B2 (ja) * | 2011-11-30 | 2016-09-21 | 味の素株式会社 | シワ防止化粧料 |
| KR101628589B1 (ko) * | 2011-11-30 | 2016-06-08 | 아지노모토 가부시키가이샤 | 미백 화장료 |
| JP6852261B2 (ja) * | 2016-01-21 | 2021-03-31 | 味の素株式会社 | アシル塩基性アミノ酸誘導体および生理活性物質を含むマルチラメラベシクル製剤 |
| KR20220154694A (ko) * | 2020-03-16 | 2022-11-22 | 아지노모토 가부시키가이샤 | 동물 세포의 배양 방법 |
| EP4153605A4 (en) * | 2020-05-21 | 2024-10-02 | Changzhou Syntheall Pharmaceuticals Co., Ltd. | COMPOSITIONS CONTAINING DICHLOROACETIC ACID, PROCESSES FOR THE PREPARATION THEREOF AND USES THEREOF |
| CN114057790B (zh) * | 2021-11-18 | 2023-10-24 | 万华化学集团股份有限公司 | 一种高全反式异构体含量的维生素a三苯基膦盐的制备方法 |
| WO2025109193A1 (en) * | 2023-11-24 | 2025-05-30 | Sanofi | Synthesized thiazolidines as a cysteine delivery method in cell culture feed |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB811816A (en) * | 1954-07-16 | 1959-04-15 | Farmaceutici Italia | Heterocyclic hydrazides |
| JPS4815938B1 (ko) | 1970-10-24 | 1973-05-18 | ||
| FR2356423A1 (fr) * | 1976-07-01 | 1978-01-27 | Oeriu Simion | Derives de l'acide thiazolidinecarboxylique, leur preparation et leur application comme medicaments |
| ATE411281T1 (de) * | 1998-06-29 | 2008-10-15 | Hoffmann La Roche | Verfahren zur herstellung von s-aryl-cystein |
| CN101332157B (zh) * | 1998-10-09 | 2012-01-11 | 味之素株式会社 | 半胱氨酸衍生物 |
| FR2816838B1 (fr) | 2000-11-17 | 2004-12-03 | Oreal | Utilisation de derives de l'acide 2-oxothiazolidine- 4-carboxylique comme agents prodesquamants |
| US20030095959A1 (en) * | 2000-11-21 | 2003-05-22 | Access Business Group International Llc. | Topical skin composition |
| CA2709784A1 (en) * | 2007-12-21 | 2009-07-09 | University Of Rochester | Method for altering the lifespan of eukaryotic organisms |
| JP5439849B2 (ja) * | 2008-02-28 | 2014-03-12 | 味の素株式会社 | システイン誘導体 |
| JP5378713B2 (ja) | 2008-06-19 | 2013-12-25 | 日本理化学薬品株式会社 | 外用組成物 |
-
2011
- 2011-05-27 KR KR1020127033919A patent/KR101496795B1/ko active Active
- 2011-05-27 EP EP11786790.3A patent/EP2578203B1/en active Active
- 2011-05-27 JP JP2012517348A patent/JP5327384B2/ja active Active
- 2011-05-27 CN CN201180026582.5A patent/CN102917685B/zh active Active
- 2011-05-27 WO PCT/JP2011/062293 patent/WO2011149093A1/ja not_active Ceased
-
2012
- 2012-11-27 US US13/686,384 patent/US9212154B2/en active Active
-
2015
- 2015-11-06 US US14/934,596 patent/US10144717B2/en active Active
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20220159866A (ko) * | 2021-05-26 | 2022-12-05 | 경북대학교 산학협력단 | 시스테인 유도체의 피부 미백 용도 |
Also Published As
| Publication number | Publication date |
|---|---|
| US9212154B2 (en) | 2015-12-15 |
| EP2578203A1 (en) | 2013-04-10 |
| JPWO2011149093A1 (ja) | 2013-07-25 |
| EP2578203A4 (en) | 2013-07-24 |
| US10144717B2 (en) | 2018-12-04 |
| KR101496795B1 (ko) | 2015-03-02 |
| JP5327384B2 (ja) | 2013-10-30 |
| CN102917685B (zh) | 2015-11-25 |
| US20160060234A1 (en) | 2016-03-03 |
| WO2011149093A1 (ja) | 2011-12-01 |
| EP2578203B1 (en) | 2015-04-01 |
| CN102917685A (zh) | 2013-02-06 |
| US20130095048A1 (en) | 2013-04-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20130028126A (ko) | 시스테인 유도체 | |
| JP3635703B2 (ja) | 化粧品における給湿剤としてのエクトインおよびエクトイン誘導体 | |
| JP5439849B2 (ja) | システイン誘導体 | |
| EP2117499B1 (en) | Use of sinapic acid in non-therapeutic cosmetic and/or topical compositions | |
| JP6167908B2 (ja) | 両性イオン型塩基性アミノ酸誘導体 | |
| JP2003528122A (ja) | 皮膚におけるストレスタンパク質を保護するためのエクトインまたはエクトイン誘導体の使用 | |
| JP5994789B2 (ja) | シワ防止化粧料 | |
| KR102068635B1 (ko) | 3,4,5-트리메톡시 신남산 에스테르 유도체와 그 제조방법 및 이를 포함하는 피부 미백용 조성물 | |
| JP5979155B2 (ja) | システイン誘導体およびアルコールを含有する化粧料 | |
| JP4070357B2 (ja) | 皮膚外用剤 | |
| JP5979154B2 (ja) | システイン誘導体および界面活性剤を含有する化粧料 | |
| KR102939875B1 (ko) | 신규 화합물을 포함하는 화장료 조성물 | |
| KR102463238B1 (ko) | 신규 히드록시 피라논 화합물, 이의 제조방법 및 이를 포함하는 화장료 조성물 | |
| KR101969345B1 (ko) | 펩타이드가 결합된 안정한 아스코르빈산 유도체를 포함하는 피부 염증 완화용 조성물 | |
| KR102463237B1 (ko) | 살리실산 유도체와 그 제조방법 및 이를 함유하는 미백용 화장료 조성물 | |
| KR101491728B1 (ko) | 비타민 c와 비타민 b3의 컨쥬게이트 및 그를 포함하는 항산화제 | |
| CN102964283A (zh) | 4-氨基硫脲缩甲醛基苯甲(氨基酸)酰胺化合物及其应用 | |
| KR20180095852A (ko) | 화장품 용도를 위한 (r)-n-(아다만틸-2-일)피롤리딘-2-카복스아미드 유도체 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0105 | International application |
Patent event date: 20121227 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20121227 Comment text: Request for Examination of Application |
|
| PG1501 | Laying open of application | ||
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20140331 Patent event code: PE09021S01D |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
Patent event code: PE07011S01D Comment text: Decision to Grant Registration Patent event date: 20141222 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
Comment text: Registration of Establishment Patent event date: 20150223 Patent event code: PR07011E01D |
|
| PR1002 | Payment of registration fee |
Payment date: 20150224 End annual number: 3 Start annual number: 1 |
|
| PG1601 | Publication of registration | ||
| FPAY | Annual fee payment |
Payment date: 20180219 Year of fee payment: 4 |
|
| PR1001 | Payment of annual fee |
Payment date: 20180219 Start annual number: 4 End annual number: 4 |
|
| FPAY | Annual fee payment |
Payment date: 20190218 Year of fee payment: 5 |
|
| PR1001 | Payment of annual fee |
Payment date: 20190218 Start annual number: 5 End annual number: 5 |
|
| FPAY | Annual fee payment |
Payment date: 20200218 Year of fee payment: 6 |
|
| PR1001 | Payment of annual fee |
Payment date: 20200218 Start annual number: 6 End annual number: 6 |
|
| PR1001 | Payment of annual fee |
Payment date: 20210218 Start annual number: 7 End annual number: 7 |
|
| PR1001 | Payment of annual fee |
Payment date: 20220119 Start annual number: 8 End annual number: 8 |
|
| PR1001 | Payment of annual fee |
Payment date: 20240119 Start annual number: 10 End annual number: 10 |
|
| PR1001 | Payment of annual fee |
Payment date: 20250108 Start annual number: 11 End annual number: 11 |