KR20080069710A - 위치규칙성 폴리셀레노펜 - Google Patents
위치규칙성 폴리셀레노펜 Download PDFInfo
- Publication number
- KR20080069710A KR20080069710A KR1020087015194A KR20087015194A KR20080069710A KR 20080069710 A KR20080069710 A KR 20080069710A KR 1020087015194 A KR1020087015194 A KR 1020087015194A KR 20087015194 A KR20087015194 A KR 20087015194A KR 20080069710 A KR20080069710 A KR 20080069710A
- Authority
- KR
- South Korea
- Prior art keywords
- polymer
- independently
- alkyl
- mmol
- formula
- Prior art date
Links
- 0 C*(*)c1cc(*)c(-c2ccc(-c3c(*)cc(*(C)N)[s]3)[s]2)[s]1 Chemical compound C*(*)c1cc(*)c(-c2ccc(-c3c(*)cc(*(C)N)[s]3)[s]2)[s]1 0.000 description 5
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
- C08G61/122—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides
- C08G61/123—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G79/00—Macromolecular compounds obtained by reactions forming a linkage containing atoms other than silicon, sulfur, nitrogen, oxygen, and carbon with or without the latter elements in the main chain of the macromolecule
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06K—GRAPHICAL DATA READING; PRESENTATION OF DATA; RECORD CARRIERS; HANDLING RECORD CARRIERS
- G06K19/00—Record carriers for use with machines and with at least a part designed to carry digital markings
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
- H10K85/113—Heteroaromatic compounds comprising sulfur or selene, e.g. polythiophene
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2323/00—Functional layers of liquid crystal optical display excluding electroactive liquid crystal layer characterised by chemical composition
- C09K2323/02—Alignment layer characterised by chemical composition
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Abstract
본 발명은 위치규칙성 폴리셀레노펜, 광학, 전기광학 또는 전자 장치에서 반도체 또는 전하 수송 물질로서의 그들의 용도, 및 그들을 포함하는 광학, 전기광학 또는 전자장치에 관한 것이다.
Description
본 발명은 위치규칙성 폴리셀레노펜, 광학, 전기광학 또는 전자 장치에서 반도체 또는 전하 수송 물질로서의 그들의 용도, 및 그들을 포함하는 광학, 전기광학 또는 전자장치에 관한 것이다.
최근 몇년 동안, 전자분야에서 중합체를 사용하는 데에 대한 관심이 증가되어 왔다. 한가지 중요한 특정 분야는 유기 광전지(OPV; organic photovoltaics)이다. 중합체가 OPV에서 그 용도를 찾았으며, 중합체들을 사용하면 장치들이 용액-가공 기술(예: 스핀 캐스팅, 딥 코팅 또는 잉크 젯 인쇄)에 의해 제조될 수 있기 때문이다. 용액 가공은 무기 박막 장치 제조에 사용되는 증발 기술에 비해 더 싸고 더 큰 규모로 실행될 수 있다. 현재, 중합체계 장치는 4 내지 5% 효율을 달성하고 있다(예를 들면 K. M. Coakley 및 M. D. McGehee, Chem . Mater . 2004, 16, 4533-4542 참조). 이는 일반적으로 25% 이하인, 무기 장치에 의해 달성될 수 있는 효율보다 훨씬 낮은 것이다.
현재 OPV 장치에서 가장 높은 효율을 달성하는 중합체의 부류는 폴리(3-알킬 -티오펜)(P3AT)이다. 가장 통상적으로 사용된 예는 폴리(3-헥실-티오펜)(P3HT)이며, 이용가능성이 넓고 흡수성이 우수하기 때문이다. P3HT는 480 내지 650 nm에 걸쳐 강하게 흡수하고, 최대 피크 흡수도는 560 nm에서이다. 이는 햇빛에 의해 방출된 상당 부분이 흡수되지 않음을 의미한다.
OPV 장치의 효율을 향상시키기 위해, 태양 스펙트럼의 더 긴 파장 영역(650 내지 800nm)으로부터 더욱 많은 빛을 흡수하는 중합체가 요구된다. 이러한 목적으로는, 낮은 밴드 갭, 바람직하게는 1.9 eV 미만의 밴드 갭을 갖는 중합체가 바람직하지만, 예를 들면 P3HT는 약 2.0 eV의 밴드 갭을 갖는다.
OPV 장치 이외에, 유기 물질이 또한 유기계 박막 트랜지스터 및 유기 전계 효과 트랜지스터(TFT, OFET)에서 활성 층으로서 전망을 나타냈다(참조: H. E. Katz, Z. Bao 및 S. L. Gilat, Acc. Chem. Res., 2001, 34, 5, 359). 이러한 장치는 스마트 카드, 보안 태그 및 플랫 패널 디스플레이에서의 스위칭 부재에 잠재적 용도를 갖는다. 유기 물질은 용액으로부터 침착될 수 있다면, 그들의 실리콘 유사체에 비해 비용면에서 상당한 장점을 갖는 것으로 파악되며, 이는 신속하고 큰 면적의 제작 경로를 가능하게 하기 때문이다.
장치의 성능은 원칙적으로 반도체 물질의 전하 운반체 이동성 및 전류 온/오프 비율을 기준으로 하며, 따라서 이상적인 반도체는 오프 상태에서 낮은 전도성과 함께 높은 전하 운반체 이동성(> 1 x 10-3 cm2 V-1 s-1)을 가져야 한다. 또한, 반도체 물질이 산화에 대해 비교적 안정한 것, 즉 높은 이온화 포텐셜을 갖는 것이 중 요한데, 산화가 장치 성능의 감소를 유도하기 때문이다.
위치규칙성 헤드-투-테일 P3HT는 1 x 10-5 내지 4.5 x 10-2 cm2V-1s-1의 전하 운반체 이동성을 갖지만, 10 내지 103의 오히려 낮은 전류 온/오프 비율을 갖는다[참조: Z. Bao 등., Appl . Pys . Lett ., 1996, 69, 4108]. 이러한 낮은 온/오프 전류는 부분적으로는 중합체의 낮은 이온화 포텐셜에 기인하고, 이는 주변 조건에서 중합체의 산소 도핑, 및 후속적인 높은 오프 전류를 유도할 수 있다[참조: H. Sirringhaus 등, Adv . Solid State Phys ., 1999, 39, 101 ].
높은 위치규칙성은 향상된 팩킹 및 최적 미세구조를 유도할 수 있고, 향상된 전하 운반체 이동성을 유도할 수 있다[참조: H. Sirringhaus 등, Science, 1998, 280, 1741-1744; H. Sirringhaus 등, Nature, 1999, 401, 685-688; 및 H. Sirringhaus 등, Synthetic Metals, 2000, 111-112, 129-132]. 일반적으로, P3AT는 향상된 용해도를 나타내고 넓은 면적 필름을 제작하기 위해 용액 가공될 수 있다. 그러나, P3AT는 상대적으로 낮은 이온화 포텐셜을 갖고 공기중에서 도핑될 여지가 있다.
본 발명의 목적은 합성하기 용이하고, 높은 전하 이동성을 갖고, 양호한 가공성 및 산화 안정성을 갖는, 특히 OPV 및 OFET 장치에 사용하기 위한 반도체 또는 전하수송 물질로서 사용하기 위한 신규 물질을 제공하는 것이다. 본 발명의 또 다른 목적은 신규한 반도체 및 전하 수송 성분, 및 이들 성분을 포함하는 신규하고 향상된 전기광학적, 전자 및 발광 장치를 제공하는 것이다. 본 발명의 또 다른 목 적은 하기 상세한 설명으로부터 당해 기술분야의 숙련인에게 바로 자명할 것이다.
본 발명의 발명자들은 본 발명에 청구된 바와 같은 위치규칙성 폴리셀레노펜을 제공함으로써 이러한 목적이 달성될 수 있다는 것을 발견하였다. 특히, 위치규칙성 폴리(3-알킬)셀레노펜(P3AS), 및 주쇄에 셀레노펜만을 함유하는 다른 중합체가 1.9eV보다 낮은 밴드갭을 가지면서 높은 정공 운반체 수송, 용액 가공성 및 높은 광학 흡수계수와 같은 바람직한 성질을 유지한다는 것을 발견하였다.
위치불규칙성 폴리(3-알킬)셀레노펜은 3-알킬 셀레노펜 전구체의 전기화학적 중합에 의해(C. Mahatsekake 등, Phosphorus , Sulfur and Silicon, 1990, 47, 35-41) 또는 FeCl3을 사용하는 산화적인 화학적 경로에 의해(Y. Katsumi 등, Japanese Journal Appl. Physics. Part 2, 1989, 28, L138-L140 ; C. G. Andrieu 등, Sulfur Letters, 1996, 19, 261-266) 이전에 합성되었다. 양쪽 제조방법 모두 알킬 측쇄의 위치결정과 관련하여 낮은 위치규칙성의 물질을 제공하였다. 가츠미(Katsumi) 및 동료들에 의해 보고된 위치불규칙성 폴리(3-알킬)셀레노펜은 위치불규칙성 폴리(3-알킬)티오펜보다 큰 밴드갭(2.4 eV vs 2.2 eV)을 갖는 것으로 보고되었다(Y. Katsumi 등 Japanese Journal Appl . Physics . Part 2, 1989, 28, L138-L140). 이는 알킬 측쇄와, 황과 비교하여 더 큰 이온 반경을 갖는 셀레늄 사이의 증가된 입체 상호작용, 이러한 입체 상호작용이 중합체 주쇄의 평면성, 따라서 밴드갭을 감소시킨다는 것에 의해 합리화된다. 전계 효과 트랜지스터에서 이들 물질의 전하 운반체 이동성 또는 유기 광전지 장치에서의 성능은 앞서 보고된 바 없었다.
유럽 특허 공개공보 제 EP-A-1 439 590 호에는 모노-, 올리고- 및 폴리-비스(티에닐) 아릴렌이 개시되어 있지만, 본 발명의 중합체를 기재하지는 않는다. 다음 문헌에서는 폴리-비스(3-옥틸-티오펜-2-일) 셀레노펜이 개시되어 있지만, 본 발명의 중합체가 개시되어 있지는 않다[참조: S. Tierney, M. Heeney 및 I. McCulloch, Synth Met ., 148(2), 195-198,(2005)] .
발명의 요약
본 발명은 3- 및/또는 4-위치에서 선택적으로 치환된 2,5-셀레노펜의 위치규칙성 중합체에 관한 것이다.
본 발명은 또한 반도체, 전하 수송 또는 발광 물질로서 본 발명에 따른 중합체의 용도에 관한 것이다.
본 발명은 또한 본 발명에 따른 하나 이상의 중합체를 포함하는 반도체, 전기발광 또는 전하 수송 물질, 부품 또는 장치에 관한 것이다.
본 발명은 또한 광학, 전기광학 또는 전자부품 또는 장치, 유기 전계 효과 트랜지스터(OFET), 집적회로(IC), 박막 트랜지스터(TFT), 플랫 패널 디스플레이, 무선주파수 식별(RFID) 태그, 전기발광 또는 발광 장치 또는 부품, 유기 발광 다이오드(OLED), 디스플레이의 백라이트, 광전지 또는 센서 장치, 전하 주입층, 쇼트키(Schottky) 다이오드, 평면화층, 정전기방지층, 전도성 기판 또는 패턴, 배터리에서 전극 물질, 광전도체, 전자사진 분야, 전자사진 기록, 유기 메모리 장치, 얼라인먼트 층, 미용 또는 약제학적 조성물, 바이오센서, 바이오칩에서 전하수송, 반 도체, 전기전도성, 광전도성 또는 발광 물질로서, 또는 DNA 서열을 검출하고 검사하기 위한 본 발명에 따른 중합체의 용도에 관한 것이다.
본 발명은 또한 본 발명에 따른 중합체, 반도체 또는 전하 수송 물질, 부품 또는 장치를 포함하는 광학, 전기광학 또는 전자 장치, FET, 집적 회로(IC), TFT, OLED 또는 얼라인먼트 층에 관한 것이다.
본 발명은 또한 본 발명에 따른 중합체, 반도체 또는 전하 수송 물질, 부품 또는 장치 또는 FET, IC, TFT 또는 OLED를 포함하는 플랫 패널 디스프레이를 위한 TFT 또는 TFT 어레이, 무선주파수 식별(RFID) 태그, 전기발광 디스플레이 또는 백라이트에 관한 것이다.
본 발명은 또한 본 발명에 따른 FET 또는 RFID 태그를 포함하는 보안 마킹 또는 장치에 관한 것이다.
도 1은 클로로벤젠(a)중에 그리고 박막(b)으로서 본 발명에 따른 위치규칙성 폴리(3-헥실)셀레노펜(P3HS)의 고형 상태 UV 스펙트럼을 클로로벤젠(c)중에 그리고 박막(d)으로서 위치규칙성 폴리(3-헥실)티오펜(P3HT)과 비교하여 나타낸다.
도 2는 본 발명에 따른 위치규칙성 P3HS의 고형 상태 UV 스펙트럼을 나타낸다.
도 3은 본 발명에 따른 P3HS를 포함하는 트랜지스터 장치의 전류(I)-전압(V) 이동 특성(3a) 및 출력 특성(3b)을 나타낸다.
용어 "위치규칙성"이란 85% 이상의 위치규칙성을 갖는 중합체를 의미한다. "위치규칙성"이란 중합체 안에서 단량체 단위의 헤드-투-테일 커플링의 수를 총 커플링 수로 나눈 값을 의미하고, 백분율로 표시된다. 90% 이상, 매우 바람직하게는 95% 이상, 더욱 바람직하게는 96 내지 100% 이상, 가장 바람직하게는 98 내지 100%의 위치규칙성을 갖는 중합체가 특히 바람직하다.
달리 언급되지 않는 한, 분자량은 수평균분자량 Mn 또는 중량평균 분자량 Mw로서 주어지고, 폴리스티렌 표준물질에 대한 겔 투과 크로마토그래피(GPC)에 의해 측정된다. 중합도(n)는 수평균 중합도를 의미하고, n = Mn/Mu로서 주어지며, 여기서 Mu는 단일 반복단위의 분자량이다(통상 화학식 I1의 R9 및 R10과 같이, 반복단위의 일부가 아닌 중합체의 말단기는 고려하지 않음).
본 발명의 중합체는 3- 및/또는 4-위치에서 선택적으로 치환된 2,5-셀레노펜-다이일 단위로만 이루어진다.
종래 기술분야에 개시된 중합체와 대조적으로, 본 발명에 따른 위치규칙성 P3AS는 위치규칙성 P3AT에 비해 감소된 밴드갭을 갖는 것으로 밝혀졌다. 이는 본 발명의 폴리셀레노펜을 특히 광전지 장치에 사용하기 위한 반도체 물질로서 인기있는 후보로 만들었다. 이러한 결과는 놀라운 것이고 종래 기술분야에서 기대할 수 없었던 것인데, 왜냐하면 종래 기술분야에서는, 위치불규칙성 P3HS가 위치불규칙성 P3HT보다 더 큰 밴드갭을 갖는다고 교시하기 때문이다(참조: Y. Katsumi 등 Japanese Journal Appl . Physics . Part 2, 1989, 28, L138-L140). 따라서, 위치규칙성 P3AS는 또한 위치규칙성 P3AT보다 더 큰 밴드갭을 갖고, 따라서 광전지를 위한 매력적인 후보가 아닐 것이라는 예측을 할 것이다. 이러한 예상치 못한 큰 밴드갭 감소 및 위치규칙성의 향상은 자명하지 않다.
또한, 본 발명에 따른 중합체에서 높은 위치규칙성은 헤드-헤드 및 테일-테일 커플링에 의해 야기된 입체 상호작용을 감소시키고, 따라서 중합체가 고도로 평면성이고 정렬된 층상 구조로 변하게 할 수 있다. 또한, 본 발명의 중합체는 유사한 모든-티오펜 시스템에 필적하는 더 높은 전하 운반체 이동성을 나타내기 때문에 유리하다. 황(88pm; 피코미터)에 비해 증가된 세레늄의 원자 반경(103 pm)은 중합체 쇄 사이의 분자 겹침을 향상시키고, 전하 도약 과정(charge hopping process)을 촉진시킨다.
본 발명에 따른 중합체는 특히 OPV 또는 OFET 장치에서 전하 수송 또는 반도체 물질로서 특히 유용하다. 셀레노펜기 안으로 알킬 측쇄가 도입되어 중합체의 용해도 및 용액 가공성을 향상시킨다.
본 발명에 따른 중합체는 단독중합체 또는 공중합체일 수 있다. 하기 화학식 I로부터 선택된 중합체가 특히 바람직하다:
상기 식에서,
R1 -8은 서로 독립적으로 그리고 복수일 경우에도 서로 독립적으로 H, 할로겐, 선택적으로 치환된 아릴 또는 헤테로아릴, P-Sp-, P*-Sp-, 또는 탄소원자수 1 내지 40의 직쇄, 분지쇄 또는 사이클릭 알킬(이는 F, Cl, Br, I 또는 CN에 의해 선택적으로 단일치환되거나 다중치환되고, 하나 이상의 비인접한 CH2기는 각각의 경우 서로 독립적으로 -O-, -S-, -NH-, -NR0-, -SiR0R00-, -CO-, -COO-, -OCO-, -O-CO-O-, -S-CO-, -CO-S-, -CX1=CX2- 또는 -C≡C-에 의해 O 및/또는 S 원자가 서로에 직접 연결되지 않는 방식으로 선택적으로 치환된다)이고,
R0 및 R00는 서로 독립적으로 H, 탄소원자수 1 내지 12의 선택적으로 치환된 아릴 또는 알킬이고,
X1 및 X2는 서로 독립적으로 H, F, Cl 또는 CN이고,
P는 중합가능한 기이고,
P*는 중합가능한 기 P로 전환되거나 P에 의해 치환될 수 있는 기이고,
Sp는 스페이서기 또는 단일 결합이고,
a, b, c 및 d는 서로 독립적으로 0, 1, 2 또는 3이고, a + b + c + d ≥ 1이고,
n은 1보다 큰 정수이고,
여기서 반복단위는 동일하거나 상이하다.
하기 화학식 I1의 중합체가 특히 바람직하다:
상기 식에서,
R1 -8, a, b, c, d 및 n은 화학식 I의 의미를 갖고,
R9 및 R10은 서로 독립적으로 R1의 의미중 하나를 갖거나 또는 -Sn(R0)3, -B(OR')(OR"), -CH2Cl, -CHO, -CH=CH2 또는 -SiR0R00R000이고,
R0, R00, R000는 서로 독립적으로 H, 탄소원자수 1 내지 12의 선택적으로 치환된 아릴 또는 알킬이고,
R' 및 R"는 서로 독립적으로 H 또는 탄소원자수 1 내지 12의 알킬이거나, 또는 OR' 및 OR"는 붕소 원자와 함께 탄소원자수 2 내지 20을 갖는 사이클릭 기를 형성한다.
특히 바람직한 것은
- n이 2 내지 5,000, 바람직하게는 10 내지 5,000, 매우 바람직하게는 100 내지 1000의 정수이고,
- 폴리스티렌 표준물질에 대해 GPC에 의해 측정한 분자량(Mw)이 5,000 내지 300,000, 특히 20,000 내지 200,000이고,
- a = 1 , b = c = d = 0이고,
- a = 1 , b = c = d = 0이고, R1 및 R2중 하나 또는 모두는 H와 상이하고,
- a = b = c = 1 , d = 0이고,
- a = b = c = 1 , d = 0, R1 및 R5는 H와 상이하고, R2, R3, R4, R6은 H이고,
- a = b = c = d = 1이고,
- a = b = c = d = 1 , R1 및 R7은 H와 상이하고, R2, R3, R4, R5, R6, R8은 H이고,
- R1 -8은 서로 독립적으로 할로겐, 선택적으로 치환된 아릴 또는 헤테로아릴, P-Sp-, P*-Sp-, 또는 탄소원자수 6 내지 30의 직쇄, 분지쇄 또는 사이클릭 알킬(이는 F, Cl, Br, I 또는 CN에 의해 선택적으로 단일- 또는 다중치환되고 하나 이상의 비인접한 CH2기는 각각의 경우 서로 독립적으로 -O-, -S-, -NH-, -NR0-, -SiR0R00-, -CO-, -COO-, -OCO-, -O-CO-O-, -S-CO-, -CO-S-, -CX1=CX2- 또는 -C≡C-에 의해 O 및/또는 S 원자가 서로에 직접 연결되지 않는 방식으로 선택적으로 치환된다)이고,
- R1 -8은 C1-C20-알킬, C1-C20-알콕시, C2-C20-알케닐, C2-C20-알키닐, C1-C20-티오알킬, C1-C20-실릴, C1-C20-에스터, C1-C20-아미노, C1-C20-플루오로알킬, 및 선택적으로 치환된 아릴 또는 헤테로아릴, 매우 바람직하게는 C1-C20-알킬 또는 C1-C20-플루오로알킬로부터 선택되고,
- P*는 -OH 또는 -0-Si-R0R00R000이고, 바람직하게는 R0, R00 및 R000는 선택적으로 치환된 아릴 또는 C1 -12-알킬, 바람직하게는 C1-C6-알킬, 예를 들면 메틸, 에틸, 이소프로필, t-부틸 또는 페닐로부터 선택된 동일하거나 상이한 기이고,
- R9 및 R10은 H, 할로겐, Sn(R0)3, -B(OR')(OR"), CH2Cl, CHO, CH=CH2, SiR0R00R000 및 선택적으로 치환된 아릴 또는 헤테로아릴로부터 선택되고,
- R1, R2, R3, R4, R5 및 R6중 하나 이상은 P-Sp-이고,
- R9 및 R10중 하나 또는 모두는 P-Sp- 또는 P*-Sp-인 화학식 I 및 I1의 중합체이다.
다음 화학식 Ia, Ib 및 Ic의 중합체가 특히 바람직하다:
상기 식에서,
n은 화학식 I의 의미를 갖고 R은 화학식 I에서 R1의 의미를 갖거나 상기 정의한 바와 같고, 이는 H와 상이하다.
R1 -8중 하나가 아릴 또는 헤테로아릴이면, 바람직하게는 탄소원자수 25 이하의 모노-, 바이- 또는 트라이사이클릭 방향족 또는 헤테로방향족 기이고, 여기서 고리들은 융합될 수 있다. 헤테로방향족 기는 N, O 및 S로부터 바람직하게 선택된 하나 이상의 헤테로고리 원자를 함유한다. 방향족 또는 헤테로방향족 기는 하나 이상의 기 L로 선택적으로 치환된다.
L은 F, Cl, Br, I, CN 또는 탄소원자수 1 내지 20의 직쇄, 분지쇄 또는 사이클릭 알킬(이는 비치환되거나 F, Cl, Br, I, -CN 또는 -OH에 의해 단일- 또는 다중치환되고 하나 이상의 비인접한 CH2기는 각각의 경우 서로 독립적으로 -O-, -S-, -NH-, -NR0-, -SiR0R00-, -CO-, -COO-, -OCO-, -OCO-O-, -S-CO-, -CO-S-, -CH=CH- 또는 -C≡C-에 의해, O 및/또는 S 원자가 서로에 직접 연결되지 않는 방식으로 선택적으로 치환된다)이다.
특히 바람직한 아릴 및 헤테로아릴 기는 페닐, 플루오르화 페닐, 피리딘, 피리미딘, 바이페닐, 나프탈렌, 선택적으로 플루오르화 또는 알킬화 또는 플루오로알킬화된 벤조[1,2-b:4,5-b']다이티오펜, 선택적으로 플루오르화 또는 알킬화 또는 플루오로알킬화된 티에노[3,2-b]티오펜, 선택적으로 플루오르화 또는 알킬화 또는 플루오로알킬화된 2,2-다이티오펜, 티아졸 및 옥사졸이고, 이들 모두는 치환되지 않거나, 상기 정의한 바와 같이 L로 단일- 또는 다중치환된다.
R1 -8중 하나가 알킬 또는 알콕시 라디칼이면, 즉 말단 CH2기가 -O-에 의해 치환되면, 직쇄이거나 분지쇄일 수 있다. 이는 바람직하게는 직쇄이고, 2 내지 8개의 탄소원자를 갖고 따라서 바람직하게는 예를 들면 에틸, 프로필, 부틸, 펜틸, 헥실, 헵틸, 옥틸, 에톡시, 프로폭시, 부톡시, 펜톡시, 헥실옥시, 헵톡시 또는 옥톡시, 또한 메틸, 노닐, 데실, 운데실, 도데실, 트라이데실, 테트라데실, 펜타데실, 노녹시, 데콕시, 운데콕시, 도데콕시, 트라이데콕시 또는 테트라데콕시이다.
플루오로알킬 또는 플루오르화 알킬 또는 알콕시는 바람직하게는 직쇄(O)CiF2i+i이고, 여기서 i는 1 내지 20의 정수, 특히 1 내지 15, 바람직하게는 (O)CF3, (O)C2F5, (O)C3F7, (O)C4F9, (O)C5F11, (O)C6F13, (O)C7F15 또는 (O)C8F17, 가장 바람직하게는 (O)C6F13이다.
CX1=CX2는 바람직하게는 -CH=CH-, -CH=CF-, -CF=CH-, -CF=CF-, - CH=C(CN)- 또는 -C(CN)=CH-이다.
할로겐은 바람직하게는 F, Br 또는 Cl이다.
헤테로원자는 바람직하게는 N, O 및 S로부터 선택된다.
중합가능한 기 P는 중합반응, 예를 들면 라디칼 또는 이온성 쇄 중합, 중부가 또는 중축합에 참여할 수 있는 기, 또는 예를 들면 축합 또는 부가에 의해 중합체 유사 반응에서 중합체 주쇄로 그라프트될 수 있는 기이다. 라디칼, 양이온 또는 음이온 중합과 같이 쇄 중합반응을 위한 중합가능한 기가 특히 바람직하다. C-C 이중결합 또는 삼중결합을 포함하는 중합가능한 기 또는 고리-개방 반응에 의해 중합할 수 있는 중합가능한 기, 예를 들면 옥세탄 또는 에폭사이드가 매우 바람직하다.
매우 바람직하게는, 중합가능한 기 P는 CH2=CW1-COO-, CH2=CW1-CO-, , , CH2=CW2-(O)k1-, CH3-CH=CH-O-, (CH2=CH)2CH-OCO-, (CH2=CH-CH2)2CH-OCO-, (CH2=CH)2CH-O-, (CH2=CH-CH2)2N-, (CH2=CH- CH2)2N-CO-, HO-CW2W3-, HS-CW2W3-, HW2N-, HO-CW2W3-NH-, CH2=CW1-CO-NH-, CH2=CH-(COO)k1-Phe-(O)k2-, CH2=CH-(CO)k1-Phe-(O)k2-, Phe-CH=CH-, HOOC-, OCN-, 및 W4W5W6Si-으로부터 선택되고, W1는 H, Cl, CN, CF3, 페닐 또는 탄소원자수 1 내지 5의 알킬이고, 특히 H, Cl 또는 CH3, W2 및 W3는 각각 서로 독립적으로 H 또는 탄소원자수 1 내지 5의 알킬이고, 특히 H, 메틸, 에틸 또는 n-프로필이고, W4, W5 및 W6은 각각 서로 독립적으로 Cl, 탄소원자수 1 내지 5의 옥사알킬 또는 옥사카보닐알킬이고, W7 및 W8은 각각 서로 독립적으로 H, Cl 또는 탄소원자수 1 내지 5의 알킬이고, Phe는 상기 정의된 바와 같은 하나 이상의 기 L에 의해 선택적으로 치환된 1,4-페닐렌이고, k1 및 k2는 각각 서로 독립적으로 0 또는 1이다.
특히 바람직한 기 P는 CH2=CH-COO-, CH2=C(CH3)-COO-, CH2=CH-, CH2=CH-O-, (CH2=CH)2CH-OCO-, (CH2=CH)2CH-O-, 및 이다.
아크릴레이트 및 옥세탄기는 매우 바람직하다. 옥세탄은 중합시(가교결합) 수축이 덜 발생하고, 이는 필름 안에 응력을 덜 발전시키고, 정렬성을 더 높게 보유하고 더 적은 결함을 유도한다. 옥세탄 가교결합은 또한 양이온성 개시제를 필요로 하고, 자유 라디칼 개시제와는 달리 산소에 대해 불활성이다.
스페이서 기 Sp로서, 당해 기술분야의 숙련인들에게 이러한 목적을 위해 공지된 모든 기를 사용할 수 있다. 스페이서 기 Sp는 바람직하게는 식 Sp'-X로 구성되고, 따라서 P-Sp-는 P-Sp'-X-이고 P*-Sp-는 P*-Sp'-X-이고, 여기서
Sp'는 비치환되거나 F, Cl, Br, I 또는 CN에 의해 단일 또는 다중치환될 수 있는 탄소원자수 20 이하의 알킬렌(하나 이상의 비인접한 CH2기는 각각의 경우 서로 독립적으로 -O-, -S-, -NH-, -NR0-, -SiR0R00-, -CO-, -COO-, -OCO-, -OCO-O-, -S-CO-, -CO-S-, -CH=CH- 또는 -C≡C-에 의해, O 및/또는 S 원자가 서로에 직접 연결되지 않도록 선택적으로 치환될 수 있다)이고,
X는 -O-, -S-, -CO-, -COO-, -OCO-, -O-COO-, -CO-NR0-, -NR0-CO-, -CO-NR0-CO-, -OCH2-, -CH2O-, -SCH2-, -CH2S-, -CF2O-, -OCF2-, - CF2S-, -SCF2-, -CF2CH2-, -CH2CF2-, -CF2CF2-, -CH=N-, -N=CH-, -N=N-, -CH=CR0-, -CX1=CX2-, -C≡C-, -CH=CH-COO-, -OCO-CH=CH- 또는 단일결합이고,
R0, R00, X1 및 X2는 상기 주어진 의미중 하나를 갖는다.
X는 바람직하게는 -O-, -S-, -OCH2-, -CH2O-, -SCH2-, -CH2S-, -CF2O-, -OCF2-, -CF2S-, -SCF2-, -CH2CH2-, -CF2CH2-, -CH2CF2-, -CF2CF2-, -CH=N-, -N=CH-, -N=N-, -CH=CR0-, -CX1=CX2-, 또는 단일결합이고, 특히 -O-, -S-, -C≡C-, -CX1=CX2- 또는 단일결합이고, 매우 바람직하게는 공액 시스템을 형성할 수 있는 기, 예를 들면 -C≡C- 또는 -CX1=CX2-, 또는 단일결합이다.
일반적인 기 Sp'는 예를 들면 -(CH2)p-, -(CH2CH2O)q-CH2CH2-, -CH2CH2-S-CH2CH2- 또는 -CH2CH2-NH-CH2CH2- 또는 -(SiR0R00-O)p-이고, p는 2 내지 12의 정수이고, q는 1 내지 3의 정수이고, R0 및 R00는 위에서 정의한 의미를 갖는다.
바람직한 기 Sp'는 예를 들면 에틸렌, 프로필렌, 부틸렌, 펜틸렌, 헥실렌, 헵틸렌, 옥틸렌, 노닐렌, 데실렌, 운데실렌, 도데실렌, 옥타데실렌, 에틸렌옥시에틸렌, 메틸렌옥시부틸렌, 에틸렌-티오에틸렌, 에틸렌-N-메틸-이미노에틸렌, 1-메틸알킬렌, 에테닐렌, 프로페닐렌 및 부테닐렌이다.
하나 또는 두개의 기 P-Sp- 또는 P*-Sp-(여기서, Sp는 단일결합이다)를 갖는 화합물이 또한 바람직하다.
각각 두개의 기 P-Sp- 또는 P*-Sp-를 갖는 화합물의 경우, 기 P 또는 P* 각각 및 스페이서 기 Sp는 동일하거나 상이할 수 있다.
또 다른 바람직한 실시태양은 하나 이상의 기 P*-Sp-를 포함하는 화합물에 관한 것이고, 여기서 P*는 위에서 정의된 바와 같은 중합가능한 기 P로 전환되거나 P에 의해 치환될 수 있는 기이다. 바람직하게는 P*는 예를 들면 자발성 중합에 대 해 P보다 덜 반응성인 기이다. 이들 화합물은 예를 들면 하나 이상의 P기를 갖는 화학식 I의 중합성 화합물의 합성에서 중간체로서 사용되거나 긴 시간동안 저장되거나 수송되기에는 반응성이 너무 큰 중합성 화합물을 위한 전구체 물질로서 사용될 수 있다. 기 P*는 바람직하게는 공지된 방법에 의해 기 P로 용이하게 변형되거나 P에 의해 치환될 수 있도록 선택된다. 예를 들면, 이는 기 P의 보호된 형태일 수 있다. 추가의 바람직한 기 P*는 예를 들면 중합성(메트)아크릴레이트 말단기 안으로 반응될 수 있는 -OH 또는, -O-Si-R0R00R000과 같은 실릴기(예: -O-Si(CH3)3, -O-Si-(이소프로필)3, -O-Si-(페닐)3, -O-Si-(CH3)2(페닐), -O-Si(CH3)2(t-부틸) 등)이다.
중합 또는 공중합에 의해 본 발명의 화합물 또는 혼합물로부터 수득된 SCLCP는 중합가능한 기 P에 의해 형성된 주쇄를 갖는다.
본 발명의 중합체는 당해 기술분야의 숙련인에게 공지되고 문헌에 기술된 방법에 따라 또는 그와 유사한 방법에 따라 합성될 수 있다. 다른 제조방법은 실시예로부터 채택될 수 있다. 몇가지 바람직한 방법이 아래 기술된다(여기서, R은 R1의 의미중 하나를 갖고, X는 위에 주어진 바와 같이, X1의 의미중 하나를 갖는다).
위치규칙성 폴리(3-알킬)셀레노펜의 제조방법이 하기 반응식 1에 예시적으로 묘사되어 있다.
3-헥실셀레노펜을 다음 문헌 절차에 따라 제조한다(참조: C. Mahatsekake 등, Phosphorus , Sulfur and Silicon, 1990, 47, 35-41). 이 물질을 THF중 NBS로 처리하여 2,5-위치에서 브롬화한다. 생성된 2,5-다이브로모-3-헥실셀레노펜을 1 당량의 알킬 그리냐르 시약(예를 들면, 이소-프로필 마그네슘 클로라이드)으로 처리하여 그리냐르 치환 반응을 통해 용액중 2-브로모-5-클로로마그네슘-3-헥실셀레노펜 및 2-클로로마그네슘-5-브로모-3-헥실셀레노펜의 혼합물을 형성한다. 생성된 혼합물을 전이 금속 촉매를 첨가하여 바로 중합하여 입체규칙성 폴리(3-헥실)셀레노펜을 수득한다. 바람직한 전이 금속 촉매는 2자리 리간드, 예를 들면 1,3-다이페닐포스피노프로판(dppp)과 같은 포스핀 리간드의 존재하에 Ni(II) 염, 예를 들면 Ni(dppp)Cl2(1,3-비스(다이페닐포스피노프로판) 니켈(II) 클로라이드), Ni(dppe)Cl2(1,2-비스(다이페닐포스피노)에탄 니켈(II) 클로라이드) 또는 Ni(dppf)Cl2(다이클로로[1,1'-비스(다이페닐포스피노)페로센] 니켈(II)), 또는 Ni(O) 촉매, 예를 들면 비스(1,5-사이클로옥타다이엔)니켈(0) [Ni(COD)2]이다.
t- 또는 테트라-셀레노펜 중합체의 제조방법은 하기 반응식 2에 예시적으로 설명한다.
3-알킬셀레노펜을 5-위치에서 장애 리튬 염기(예를 들면 리튬 다이이소프로필아미드)로 리튬화시키고, 생성된 오가노리튬 중간체는 구리(II) 클로라이드와 같은 산화제로 처리하여 산화적으로 이량체화시켜 4,4'-다이알킬-2,2'-바이셀레노펜을 수득한다. 이는 THF중 NBS로 처리하여 브롬화한다. 생성된 바이셀레노펜을 이어서 2개의 경로중 하나에 의해 중합할 수 있다. 전이금속 촉매[선택적으로 부가적인 포스핀 리간드의 존재하에 바람직한 촉매는 팔라듐(0) 촉매, 예를 들면 Pd(PPh3)4(테트라키스(트라이페닐포스핀)팔라듐(O)) 또는 Pd2(dba)3(트리스(다이벤질리덴아세톤)다이팔라듐(O)) 또는 팔라듐(II) 전구체, 예를 들면 Pd(PPh3)Cl2(다이클로로비스(트라이페닐포스핀)팔라듐(II)), 또는 Pd(dppf)Cl2(다이클로로[1,1'-비스(다이페닐포스피노)페로센]팔라듐(II)이다]의 존재하에, 2,5-비스(트라이메틸스태닐)셀레노펜 또는 5,5'-비스(트라이메틸스태닐)-[2,2']바이셀레노펜과 반응하여 의 도하는 중합체를 수득한다. 선택적으로, 이러한 중합체는 전이 금속 촉매 및 염기의 존재하에, 5,5'-다이브로모-4,4'-다이알킬-2,2'-바이셀레노펜과 비스(보론)산 또는 셀레노펜 및 바이셀레노펜의 에스터(스즈키(Suzuki) 중합)와의 반응에 의해 제조될 수 있다.
중합체는 또한 반응식 3에 예시적으로 묘사된 바와 같이, 산화적 커플링을 통해 미리 형성된 트라이- 또는 테트라셀레노펜 단량체를 중합하여 제조될 수 있다.
3-알킬티오펜과 1 당량의 NBS의 브롬화에 의해 2-브로모-3-알킬셀레노펜을 수득한다. 마그네슘 금속과 이의 반응으로 그리냐르 시약을 수득하고, 이어서 전이 금속 촉매의 존재하에 2,5-다이브로모셀레노펜 또는 5,5'-다이브로모-2,2'-비스 셀레노펜과 가교결합하여 각각 트라이- 및 테트라셀레노펜을 수득한다. 이들 단량체를 철(lll) 클로라이드로 용매중에 처리하여 중합체를 수득한다.
위에서 그리고 아래 기술한 바와 같이 위치규칙성 폴리셀레노펜의 신규한 제조방법은 본 발명의 또 다른 양태이다.
본 발명의 추가의 양태는 본 발명에 따른 화합물 및 물질의 산화된 형태 및 환원된 형태 모두에 관한 것이다. 전자의 손실 또는 획득은 고도로 비편재된 이온성 형태를 형성하고, 이는 높은 전도성을 갖는다. 이는 통상적인 도판트에 대해 노출될 수 있다. 적절한 도판트 및 도핑 방법이 예를 들면 유럽 특허 제 0 528 662 호, 미국 특허 제 5,198,153 호 또는 국제 특허 공개공보 제 WO 96/21659 호로부터 당해 기술분야의 숙련인에게 공지되어 있다.
도핑 방법은 일반적으로 반도체 물질을 산화환원반응중 산화제 또는 환원제로 처리하여 물질중 비편재된 이온 중심을 형성하는 것을 포함하고, 상응하는 반대이온은 적용된 도판트로부터 유래된다. 적절한 도핑 방법은 예를 들면 주변 압력 또는 감소된 압력에서 도핑 증기에 노출시키고, 도판트를 함유하는 용액중에서 전기화학적으로 도핑하고, 도판트를 열적으로 확산될 반도체 물질과 접촉하게 하고, 반도체 물질로 도판트를 이온-주입하는 것을 포함한다.
전자가 운반체로서 사용될 때, 적절한 도판트는 예를 들면 할로겐(예를 들면, I2, Cl2, Br2, ICl, ICl3, IBr 및 IF), 루이스 산(예를 들면, PF5, AsF5, SbF5, BF3, BCl3, SbCl5, BBr3 및 SO3), 프로톤산(protonic acid), 유기산 또는 아미노산 (예를 들면, HF, HCl, HNO3, H2SO4, HClO4, FSO3H 및 ClSO3H), 전이금속 화합물(예를 들면, FeCl3, FeOCl, Fe(ClO4)3, Fe(4-CH3C6H4SO3)3, TiCl4, ZrCl4, HfCl4, NbF5, NbCl5, TaCl5, MoF5, MoCl5, WF5, WCl6, UF6 및 LnCl3(여기서, Ln은 란타노이드이다), 음이온(예를 들면, Cl-, Br-, I-, I3 -, HSO4 -, SO4 2 -, NO3 -, ClO4 -, BF4 -, PF6 -, AsF6 -, SbF6 -, FeCl4 -, Fe(CN)6 3-, 및 다양한 설폰산의 음이온, 예를 들면 아릴-SO3 -)이다. 정공이 운반체로서 사용될 때, 도판트의 예는 양이온(예를 들면, H+, Li+, Na+, K+, Rb+ 및 Cs+), 알칼리 금속(예를 들면, Li, Na, K, Rb, 및 Cs), 알칼리-토금속(예를 들면, Ca, Sr, 및 Ba), O2, XeOF4, (NO2 +)(SbF6 -), (NO2 +)(SbCl6 -), (NO2 +)(BF4 -), AgClO4, H2IrCl6, La(NO3)3·6H2O, FSO2OOSO2F, Eu, 아세틸콜린, R4N+(R은 알킬기이다), R4P+(R은 알킬기이다), R6As+(R은 알킬기이다), 및 R3S+(R은 알킬기이다)이다.
본 발명의 화합물 및 물질의 전도성 형태는 응용분야에서, 예를 들면 비제한적으로 유기 발광 다이오드 응용에서 전하 주입 층 및 ITO 평면화 층, 플랫 패널 디스플레이 및 터치 스크린을 위한 필름, 인쇄 회로 기판과 같은 전자 분야에서 정전기방지 필름, 인쇄 전도성 기판, 패턴 또는 트랙, 및 응축기에서 유기 "금속"으로서 사용될 수 있다.
본 발명의 바람직한 실시태양은 메소젠성 또는 액정성인 화학식 I 및 I1의 화합물, 및 바람직한 그들의 하위 화학식의 화합물에 관한 것이고, 매우 바람직하게는 하나 이상의 중합가능한 기를 포함한다. 이러한 유형의 매우 바람직한 물질은 화학식 I 또는 I1 및 그들의 바람직한 하위 화학식(여기서, n은 >1 내지 15의 정수이고, R9 및/또는 R10은 P-Sp-이다)의 올리고머이다.
이들 물질은 반도체 또는 전하 수송 물질로서 특히 유용한데, 이들이 공지된 기술에 의해 액정 상에서 균일하게 고도로 정렬된 배향으로 정렬될 수 있고, 따라서 더 높은 정도의 정렬을 나타내어 특히 높은 전하 운반체 이동성을 유도하기 때문이다. 고도로 정렬된 액정 상태는 동일 반응계 중합 또는 가교결합에 의해 기 P를 통해 고정되어, 높은 전하 운반체 이동성 및 높은 열적, 기계적 및 화학적 안정성을 갖는 중합체 필름을 수득한다.
예를 들면, 장치가 중합성 액정 물질로부터 동일자리 중합반응에 의해 제조되면, 액정 물질은 바람직하게는 하나 이상의 화학식 I1의 화합물 및 그의 바람직한 하위 화학식(R9 및 R10중 하나 이상은 P-Sp-이다)을 포함한다. 액정 중합체가 용액중 중합에 의해 먼저 제조되고 분리된 중합체가 장치를 제조하기 위해 사용되면, 중합체는 바람직하게는 화학식 I1, 및 그의 바람직한 하위 화학식의 하나 이상의 화합물(여기서, R9 및 R10중 하나는 P-Sp-이다)을 포함하는 액정 물질로부터 제조된다.
본 발명에 따라 중합성 화합물을 선행 기술분야에 공지된 다른 중합성 메소 젠성 또는 액정 화합물과 함께 공중합하여 액정 상 거동을 유도하거나 향상시킬 수 있다.
따라서, 본 발명의 또 다른 양태는 하나 이상의 중합가능한 기를 포함하는 상기 그리고 아래에 기술한 바와 같은 본 발명의 하나 이상의 화합물을 포함하고 선택적으로 하나 이상의 추가의 중합성 화합물을 포함하는 중합성 액정 물질에 관한 것이고, 여기서 본 발명의 중합성 화합물 및/또는 추가의 중합성 화합물중 하나 이상은 메소젠성 또는 액정성이다.
특히 바람직한 것은 네마틱 및/또는 스멕틱 상을 갖는 액정 물질이다. FET 용도의 경우, 스멕틱 물질이 특히 바람직하다. OLED 용도의 경우, 네마틱 또는 스멕틱 물질이 특히 바람직하다. 특히 바람직한 것은 스멕틱 A(SA) 상, 또한 고도로 정렬된 스멕틱 상, 예를 들면 SB, SE, SG 및 SF 상이다.
본 발명의 또 다른 양태는 상기 정의한 바와 같은 중합성 액정 물질로부터 수득할 수 있는 전하 수송 성질을 갖는 비등방성 중합체 필름에 관한 것으로, 이는 그 액정 상태에서 거시적으로 균일한 배향으로 정렬되고 중합되거나 가교결합되어 그 배향된 상태를 고정시킨다.
바람직하게는, 중합은 본 발명의 반도체 물질을 포함하는 전기장치 또는 광학 장치의 제작동안 물질의 코팅된 층의 동일반응계 중합으로서 수행된다. 액정 물질의 경우, 바람직하게는 중합 전 그 액정 상태에서 수직 배향(homeotropic orientation)으로 정렬되고, 여기서 공액 파이-전자 시스템은 전하 수송의 방향에 대해 수직이다. 이로써 분자간 거리는 최소화되고 따라서 분자간 전하 수송에 요구되는 에너지가 최소화된다. 이어서 분자는 중합되거나 가교결합되어 액정 상태의 균일한 배향을 고정시킨다. 정렬 및 경화는 액정 상태로 수행되거나 물질의 메소상태로 수행된다. 이러한 기술은 당해 기술분야에 공지되어 있고, 일반적으로 예를 들면 다음 문헌에 개시된다(참조: D.J. Broer, 등., Angew. Makromol. Chem. 183,(1990), 45-66).
액정 물질의 정렬은 예를 들면 물질이 코팅되어 있는 기판을, 코팅중 또는 코팅 후 물질을 깎거나, 자기장 또는 전기장을 코팅된 물질에 적용하거나, 또는 표면-활성 화합물을 액정 물질에 첨가하는 처리를 하여 달성될 수 있다. 정렬 기술에 관한 개론은 예를 들면 다음 문헌에 개시되어 있다[참조: I. Sage, "Thermotropic Liquid Crystals", G. W. Gray에 의해 편집, John Wiley & Sons, 1987, p. 75-77, 및 T. Uchida 및 H. Seki, "Liquid Crystals - Applications and Uses Vol. 3", B. Bahadur에 의해 편집, World Scientific Publishing, Singapore 1992, p. 1-63]. 얼라인먼트 소재 및 기술은 다음 문헌을 참조한다[참조: J. Cognard, Mol. Cryst. Liq. Cryst. 78, Supplement 1(1981), p. 1-77].
중합은 열 또는 화학 방사선에 노출되어 발생한다. 화학 방사선은 빛, 예를 들면 UV 광, IR 광 또는 가시 광, X-선 또는 감마 선을 사용한 조사 또는 높은 에너지 입자, 예를 들면 이온 또는 전자를 사용한 조사를 의미한다. 바람직하게는 중합은 비-흡수성 파장에서 UV 조사에 의해 수행된다. 예를 들면 화학 방사선의 공급원으로서, 단일 UV 램프 또는 UV 램프의 세트가 사용될 수 있다. 높은 램프 전력을 사용할 때, 경화 시간이 감소될 수 있다. 또 다른 가능한 화학 방사선을 위한 공급원은 레이저이고, 예를 들면 UV 레이저, IR 레이저 또는 가시 레이저이다.
중합은 바람직하게는 화학 방사선의 파장에서 흡수하는 개시제의 존재하에 수행된다. 예를 들면, UV 광에 의해 중합할 때, 광 개시제가 사용되어 UV 조사하에 분해되어 유리 라디칼 또는 이온을 생성하고 중합 반응을 개시한다. 아크릴레이트 또는 메타크릴레이트기로 중합성 물질을 경화할 때, 바람직하게는 라디칼 광개시제가 사용되고, 중합성 물질을 비닐, 에폭사이드 및 옥세탄 기로 경화할 때, 바람직하게는 양이온성 광개시제가 사용된다. 가열시 분해되어 중합을 개시하는 자유 라디칼 또는 이온을 생성하는 중합 개시제를 사용하는 것이 또한 가능하다. 라디칼 중합을 위한 광개시제로서 예를 들면, 시판되는 이가큐어(Irgacure) 651 , 이가큐어 184, 다로큐어(Darocure) 1173 또는 다로큐어 4205(모두 시바 가이기 아게(Ciba Geigy AG)로부터 시판됨)가 사용될 수 있는 한편, 양이온성 광중합의 경우 시판되는 UVI 6974(유니온 카바이드(Union Carbide))가 사용될 수 있다.
중합성 물질은 부가적으로 예를 들면 촉매, 감광제, 안정화제, 억제제, 쇄-전달제, 공-반응 단량체, 계면활성 화합물, 윤활제, 습윤제, 분산제, 소수성화제, 접착제, 유동 개선제, 소포제, 공기제거제, 희석제, 반응 희석제, 보조제, 착색제, 염료, 안료 또는 나노입자로부터 선택된 하나 이상의 다른 적절한 성분 또는 첨가제를 포함할 수 있다.
하나 이상의 P-Sp- 기를 포함하는 화합물은 또한 중합성 메소젠성 화합물과 공중합하여 액정 상 거동을 유도하거나 향상시킨다. 공단량체로서 적절한 중합성 메소젠성 화합물은 종래 기술분야에 공지되어 있고, 예를 들면 국제 특허 공개공보 제 WO 93/22397 호; 유럽 특허 제 EP 0,261,712 호; 독일 특허 제 DE 195,04,224 호; 제 WO 95/22586 호 및 제 WO 97/00600 호에 개시되어 있다.
본 발명의 또 다른 양태는 중합 또는 중합유사 반응에 의해 상기 정의한 바와 같은 중합성 액정 물질로부터 수득된 액정 측쇄 중합체(SCLCP)에 관한 것이다. 특히 바람직한 것은 화학식 I1 및 그의 바람직한 하위 화학식(여기서, n은 1 내지 15의 정수이고 R9 및 R10중 하나 또는 모두, 바람직하게는 하나는 중합성 또는 반응성기이다)의 하나 이상의 화합물로부터, 또는 하나 이상의 상기 화합물들을 포함하는 중합성 혼합물로부터 수득된 SCLCP이다.
본 발명의 또 다른 양태는 화학식 I1 및 그의 바람직한 하위 화학식(여기서, n은 1 내지 15이고 R9 및 R10중 하나 또는 모두는 중합성 또는 반응성기이다)의 하나 이상의 화합물로부터, 또는 위에서 정의한 바와 같은 중합성 액정 혼합물로부터, 또는 하나 이상의 부가적 메소젠성 또는 비-메소젠성 공단량체와 함께 공중합 또는 공중합유사 반응에 의해 수득된 SCLCP에 관한 것이다.
측쇄 액정 중합체 또는 공중합체(SCLCP)는, 반도체 성분이 펜단트기로서 위치되고 지방족 스페이서 기에 의해 가요성 주쇄로부터 분리되어 고도로 정렬된 박판형 형태학을 수득할 가능성을 제공한다. 이러한 구조는 밀접하게 팩킹된 공액 방향족 메소젠으로 구성되고, 여기서 매우 밀접한(일반적으로 <4Å) 파이-파이 스 택킹이 발생할 수 있다. 이러한 스택킹은 분자간 전하 수송이 더욱 용이하게 발생하여 높은 전하 운반체 이동성을 유도하게 한다. SCLCP는 가공전에 용이하게 합성되고 이어서 예를 들면 유기 용매중 용액으로부터 가공되기 때문에 특정 용도에 유리하다. SCLCP가 용액중 사용되면, 적절한 표면상에 코팅될 때 자발적으로 배향할 수 있고, 그들의 메소상 온도일 때, 큰 면적의 고도로 정렬된 도메인을 생성할 수 있다.
SCLCP는 상기 기술한 방법에 의해 본 발명에 따른 중합성 화합물 또는 혼합물로부터, 또는 당해 기술분야의 숙련인에게 공지된 종래의 중합 기술(예를 들면 라디칼, 음이온성 또는 양이온성 쇄 중합, 중부가 또는 중축합을 포함함)에 의해 제조될 수 있다. 중합은 예를 들면 코팅 및 사전 정렬, 또는 동일반응계에서 중합의 필요없이 용액중 중합으로서 수행될 수 있다. 적절한 반응기 또는 그들의 혼합물을 갖는 본 발명에 따른 화합물을 중합유사 반응에서 미리 합성된 등방성 또는 비등방성 중합체 주쇄에 그라프팅하여 SCLCP를 형성할 수 있다. 예를 들면, 말단 하이드록시기를 갖는 화합물은 측방향 카복실산 또는 에스터기를 갖는 중합체 주쇄에 부착될 수 있고, 말단 이소시아네이트기를 갖는 화합물은 자유 하이드록시기를 갖는 주쇄에 부가될 수 있고, 말단 비닐 또는 비닐옥시 기를 갖는 화합물은 Si-H 기를 갖는 폴리실록산 주쇄에 첨가될 수 있다. 본 발명의 화합물과 종래의 메소젠성 또는 비 메소젠성 공단량체의 공중합 또는 중합유사반응에 의해 SCLCP를 형성할 수 있다. 적절한 공단량체는 당해 기술분야의 숙련인에게 공지되어 있다. 원칙적으로, 의도하는 중합체-형성 반응을 경험할 수 있는 반응성 또는 중합가능한 기(예 를 들면, 상기 정의한 바와 같이 중합성 또는 반응성 기 P)를 수반하는 당해 기술분야에 공지된 모든 종래의 공단량체를 사용할 수 있다. 일반적인 메소젠성 공단량체는 예를 들면 국제 특허 공개공보 제 WO 93/22397 호, 유럽 특허 제 EP 0 261 712 호, 독일 특허 제 DE 195 04 224 호, 제 WO 95/22586 호, 제 WO 97/00600 호 및 영국 특허 제 GB 2 351 734 호에 언급된 것이다. 일반적인 비-메소젠성 공단량체는 예를 들면 탄소원자수 1 내지 20의 알킬기를 갖는 알킬 아크릴레이트 또는 알킬 메타크릴레이트, 예를 들면 메틸 아크릴레이트 또는 메틸 메타크릴레이트이다.
본 발명의 화합물은 광학, 전자 및 반도체 물질로서, 특히 전계 효과 트랜지스터(FET)에서 전하 수송 물질로서, 예를 들면 집적 회로, ID 태그 또는 TFT 용도를 위한 성분으로서 유용하다. 선택적으로, 전기발광 디스플레이 용도에서 유기 발광 다이오드(OLED)에서 또는 예를 들면 액정 디스플레이의 백라이트로서, 전자사진 기록을 위한 광전지 또는 센서 물질로서 그리고 다른 반도체 용도로서 사용될 수 있다.
특히 본 발명에 따른 올리고머 및 중합체는 유리한 용해도를 나타내고 따라서 이들 화합물의 용액을 사용한 제조방법이 허용된다. 따라서, 층들 및 코팅들을 포함하는 필름은 낮은 비용의 생산 기술, 예를 들면 스핀 코팅에 의해 제조할 수 있다. 적절한 용매 또는 용매 혼합물은 알칸 및/또는 방향족, 특히 그들의 불소화 유도체를 포함한다.
본 발명의 물질은 광학, 전자 및 반도체 물질로서, 특히 전계 효과 트랜지스(FET)에서 전하 수송 물질로서, 전자사진 기록을 위한 광전지 또는 센서 물질로 서, 그리고 다른 반도체 용도로서 유용하다. 유기 반도체 물질이 게이트-유전 및 드레인 및 소스 전극 사이의 필름으로서 정렬되어 있는 이러한 FET 일반적으로 미국 특허 제 US 5,892,244 호, 국제 특허 공개공보 제 WO 00/79617 호, 제 US 5,998,804 호, 및 배경기술 및 선행 기술 챕터에서 인용된 문헌 및 아래 열거된 문헌에 공지되어 있다. 본 발명에 따른 화합물의 용해도 성질을 사용하는 낮은 비용의 생산 및 그에 따른 대규모 표면의 가공성과 같은 장점 덕분에, 이들 FET의 바람직한 용도는 집적 회로, TFT-디스플레이 및 보안 용도와 같은 것이다.
보안 용도에서, 전계 효과 트랜지스터 및 다른 반도체 물질을 갖는 장치, 예를 들면 트랜지스터 또는 다이오드는 ID 태그 또는 보안 마킹을 위해 사용되어 은행어음, 신용 카드 또는 ID 카드, 국가 ID 문서, 라이센스 또는 화폐 가치를 갖는 임의의 제품, 예를 들면 우표, 티켓, 주식, 수표와 같은 유가 문서의 위조를 감정하거나 방지할 수 있다.
선택적으로, 본 발명에 따른 화합물은 유기 발광 장치 또는 다이오드(OLED), 예를 들면 디스플레이 분야 또는 예를 들면 액정 디스플레이의 백라이트로서 사용될 수 있다. 통상적인 OLED는 다층 구조물을 사용하여 실현된다. 방출층은 일반적으로 하나 이상의 전자-수송 및/또는 정공-수송 층 사이에 샌드위치된다. 전압을 가함으로써, 전자 및 정공은 전하 운반체로서 방출층으로 이동하고, 여기서 그들의 재조합은 여기(excitation)로 이어지고 방출층 안에 함유된 발광체 단위의 발생으로 이어진다. 본 발명의 화합물, 물질 및 필름은 그들의 전기 및/또는 광학 성질에 상응하게, 하나 이상의 전하 수송 층 및/또는 발광층 안에 사용될 수 있다. 또한, 발광층 안에서의 그들의 용도는 본 발명에 따른 상기 화합물, 물질 및 필름이 전기발광 성질 자체를 나타내거나 전기발광 기 또는 화합물을 포함하면, 특히 유리하다. OLED에 사용하기 위한 적절한 단량체, 올리고머 및 중합체 화합물 또는 물질의 선택, 특성화 뿐만 아니라 가공은 일반적으로 당해 기술분야의 숙련인에게 공지되어 있고, 다음 문헌 및 본원에 인용된 문헌을 참조한다[참조: Meerholz, Synthetic Materials, 111-112, 2000, 31-34, Alcala, J. Appl. Phys., 88, 2000, 7124-7128].
또 다른 용도에 따르면, 본 발명의 화합물, 물질 또는 필름, 특히 발광 특성을 나타내는 것들을 예를 들면 다음 문헌에 개시된 디스플레이 장치의 광 공급원 물질로서 사용할 수 있다[유럽 특허 제 EP 0 889 350 A1 호 또는 C. Weder 등., Science, 279, 1998, 835-837].
또 다른 용도에 따르면, 본 발명의 화합물, 물질 또는 필름은 미국 특허출원 제 US 2003/0021913 호에 개시된 바와 같이, LCD 또는 OLED 장치 안에 또는 여기서 얼라인먼트 층으로서 단독으로 또는 다른 물질과 함께 사용될 수 있다. 본 발명에 따른 전하 수송 화합물의 용도는 얼라인먼트 층의 전기전도성을 증가시킬 수 있다. LCD에서 사용될 때, 증가된 전기 전도성은 스위칭할 수 있는 LCD 셀 안에 역 잔사성 dc 효과를 감소시키고 예를 들면 강유전체의 LCD에서 이미지 스틱킹을 억제하고, 강유전체성 LC의 자발성 편극화 전하의 스위칭에 의해 생성된 잔사성 전하를 감소시킬 수 있다. 얼라인먼트 층 상으로 제공된 발광 물질을 포함하는 OLED 장치에서 사용될 때, 이러한 증가된 전기전도성은 발광 물질의 전기발광성을 증가시킬 수 있다. 메소젠성 또는 액정 성질을 갖는 본 발명에 따른 화합물 또는 물질은 상기 기술된 바와 같이 배향된 비등방성 필름을 형성할 수 있고, 이는 상기 비등방성 필름 상으로 제공된 액정 매질 내의 얼라인먼트를 유도하거나 향상시키기 위한 얼라인먼트 층으로서 특히 유용하다. 본 발명에 따른 물질은 또한 미국 특허출원 제 US 2003/0021913 호에 개시된 바와 같이, 광얼라인먼트 층에 또는 광얼라인먼트 층으로서 사용하기 위한 광학 이성질체성 화합물 및/또는 발색단과 조합될 수 있다.
또 다른 용도에 따르면, 본 발명에 따른 화합물 및 물질, 특히 그들의 수용성 유도체(예를 들면, 극성 또는 이온성 측쇄기) 또는 이온성으로 도핑된 형태가 DNA 서열을 검출하고 검사하기 위한 화학적 센서 또는 물질로서 사용될 수 있다. 이러한 용도가 예를 들면 다음 문헌에 개시되어 있다[참조: L. Chen, D. W. McBranch, H. Wang, R. Helgeson, F. Wudl 및 D. G. Whitten, Proc. Natl. Acad. Sci. U.S.A. 1999, 96, 12287; D. Wang, X. Gong, P. S. Heeger, F. Rininsland, G. C. Bazan 및 A. J. Heeger, Proc. Natl. Acad. Sci. U.S.A. 2002, 99, 49; N. DiCesare, M. R. Pinot, K. S. Schanze 및 J. R. Lakowicz, Langmuir 2002, 18, 7785; D. T. McQuade, A. E. Pullen, T. M. Swager, Chem. Rev. 2000, 100, 2537].
본 발명에 따른 화합물 및 물질은, 또한 유럽 특허 제 1 498 112 A2 호에 개시된 바와 같이, 미용 또는 약제학적 조성물, 예를 들면 헤어 트리트먼트를 위한 미용 조성물에서 사용될 수 있다.
아래 실시예는 제한없이 본 발명을 설명하는 역할을 한다. 상기 및 아래 설명에 있어서, 달리 설명되지 않으면, 모든 온도는 ℃로 주어지고 모든 백분율은 중 량 기준이다.
실시예
1
중합체 1은 하기 반응식 1에 개시된 바와 같이 제조된다:
반응식 1
2.5- 다이브로모 -3- 헥실셀레노펜:
0℃에서 THF(20 ml)중 3-헥실셀레노펜 [문헌(C. Mahatsekake 등, Phosphorus, Sulfur and Silicon, 1990, 47, 35-41)에 개시된 바와 같이 제조됨; 1.0 g, 4.64 mmol]의 용액에 N-브로모숙신이미드(1.66 g, 9.3 mmol)을 40분 동안 6번에 걸쳐 첨가한다. 생성된 용액을 16 내지 18℃의 온도에서 16시간 동안 암실에서 교반한다. 용매를 감압하에 제거하고 생성된 잔사를 에틸 아세테이트(50 ml)중에 용해하고 물로 세척하였다(2 x 30 ml). 수성 세척물을 합치고 에틸 아세테이트로 추출하였다. 합쳐진 유기물을 포화 소듐 클로라이드로 세척하고 건조하고(소듐 설페이트), 여과하고 감압하에 농축하였다. 생성된 흐린 황색 오일을 실리카를 통해 여과하고(용리액:가솔린 40-60℃) 무색 오일을 수득한다(1.39 g, 80%). 1H NMR(300 MHz, CDCl3) δ 6.98(s, 1H), 2.48(t, 2H, J = 7.8 Hz), 1.53(m, 2H), 1.29(m, 6H), 0.89(t, 3H, J = 6.6 Hz). 13C NMR(75 MHz, CDCl3) δ 144.9, 134.2, 113.5, 111.0, 31.6, 30.7, 29.5, 28.8, 22.6, 14.1. MS(El) 374(t). 실측치 C, 32.4; H, 3.9. C10H14Br2Se1에 대한 계산치: C, 32.2; H, 3.78.
폴리(3-헥실)셀레노펜
(
1
):
무수 THF(10 ml)중 2,5-다이브로모-3-헥실셀레노펜(0.75 g, 2 mmol)의 용액에 18℃에서 이소프로필 마그네슘 클로라이드(THF중 1.05 ml의 2M 용액, 2.1 mmol)를 첨가하였다. 생성된 용액을 18℃에서 20분 동안 교반하고 20분 동안 가열하여 환류시켰다. 1,3-비스(다이페닐포스피노프로판) 니켈(II) 클로라이드(10.8 mg, 0.02 mmol)를 고형물로서 1회 첨가하고 6시간 동안 반응을 환류하였다. 뜨거운 용액을 잘 교반된 메탄올 안으로 침전시키고 생성된 현탁액을 20분 동안 교반하였다. 고형물을 여과하고 메탄올(8 시간), 아세톤(16 시간) 및 이소헥산(16 시간)으로 세척한다(속실렛(Soxhlet)). 잔사를 뜨거운 클로로포름 안에 용해하고 여과하고 60℃에서 메탄올로 침전시켰다. 여과하여 중합체를 어두운 분말(0.24 g)로서 수득하였다. GPC(C6H5Cl, 6O℃) Mn 55,000, Mw 108,000 g/mol. 1H NMR(300 MHz, CDCl3, 5O℃) δ 7.11(s, 1H), 2.73(t, 1.9H), 2.55(br m, 0.1H) 1.69(m, 2H), 1.5-1.25(m, 6H), 0.91(t, 3H)(위치규칙성 = 95%). λmax(고형 필름) 630, 695(sh) nm. λ max(CHCl3) 499 nm
폴리(3-헥실)셀레노펜
(
1
)의 선택적 제조방법:
실온에서 무수 THF(50 ml)중 2,5-다이브로모-3-헥실셀레노펜(5.22 g, 14 mmol)의 용액에 n-부틸 마그네슘 클로라이드(THF중 6.3 ml의 2M 용액, 12.6 mmol)를 첨가하였다. 생성된 용액을 실온에서 50분 동안 교반하고 1시간 동안 가열하여 환류시켰다. 가열을 그만하고, 1,2-(비스(다이페닐포스피노)에탄)다이클로로니켈(II)(41 mg, 0.078 mmol)을 고형물로서 한번에 첨가한다. 일단 생성된 발열이 가라앉으면, 반응을 21시간 동안 환류시킨다. 반응을 실온까지 냉각하고 메탄올 안으로 침전시키고 생성된 현탁액을 20분 동안 교반한다. 고형물을 여과하고 메탄올(20시간), 아세톤(24시간) 및 THF(24시간)으로 세척한다(속실렛). 잔사를 뜨거운 클로로벤젠중에 용해하고 여과하고 메탄올 안으로 침전시킨다. 여과하여 중합체를 진한 적색 분말(2.51 g)로서 수득하였다. GPC(C6H5Cl, 60℃) Mn 81,000, Mw 147,000 g/mol. 1H NMR(300 MHz, C6D5C, 70℃) δ 7.27(s, 1H), 2.79(t, 2H), 1.70(오중선, 2H), 1.41(m, 2H), 1.29(br m, 4H), 0.87(t, 3H)(위치규칙성 >97%). 13C NMR(75 MHz, C6D5Cl, 70℃) δ 141.61, 140.28, 138.48, 132.46, 31.72, 30.84, 30.66, 29.33, 22.61, 13.87. 실측치 C, 56.5; H, 6.6. (C10H14Se)n에 대한 계산치: C, 56.3; H, 6.6.
도 1은 클로로벤젠(a)중에서 그리고 얇은 필름(b)으로서 중합체 1(제 1 방법 에 따라 제조됨)의 UV-가시스펙트럼을 나타낸다. 클로로벤젠(c)중에서 그리고 얇은 필름(d)으로서 위치규칙성 폴리(3-헥실)티오펜은 비교를 위해 나타낸다. P3HT는 96%의 위치규칙성을 갖고 알드리치 케미칼 캄파니(Aldrich chemical company)로부터 입수가능하다. P3HS는 최대 흡수치 및 흡수 개시점 모두에서 P3HT에 비해 적색 이동을 나타내고, 이는 P3HS가 P3HT보다 더 작은 밴드갭을 가짐을 지시한다.
실시예
2
중합체 2는 하기 반응식 4와 같이 제조된다:
단계 2-1: 2,5-
다이브로모
-3-
옥틸셀레노펜
0℃에서 THF(80 ml)중 3-옥틸셀레노펜(문헌(C. Mahatsekake 등, Phosphorus , Sulfur and Silicon, 1990, 47, 35-41)에 개시된 바와 같이 제조됨; 7.43 g, 30.5 mmol)의 용액에 N-브로모숙신이미드(10.88 g, 61.1 mmol)을 1시간에 걸쳐 여러번에 나누어 첨가하였다. 생성된 용액을 16 내지 18℃ 사이의 온도에서 암실에서 교반한다. 이어서 물을 첨가하고 혼합물을 에틸 아세테이트(3 x 100 ml)로 추출한다. 결합된 추출물을 물 및 염수로 세척하고 Na2SO4상에서 건조시킨다. 용매를 감압하에 제거한다. 잔사를 실리카상에서 가솔린으로 용리하면서 칼럼 크로마토그래피에 의해 정제하고 무색 오일(11.38 g, 93%)을 수득한다. 1H NMR(300 MHz, CDCl3): δ(ppm) 6.95(s, 1H, Ar-H), 2.47(t, J = 7.6 Hz, 2H, CH2), 1.51(m, 2H, CH2), 1.27(m, 1OH, CH2), 0.88(t, J = 6.8 Hz, 3H, CH3). 13C NMR(75MHz, CDCl3): δ(ppm) 144.8, 134.1, 113.6, 111.0, 31.9, 30.6, 29.5, 29.4, 29.2, 29.1, 22.7, 14.2. MS(El) 402(t, M+).
단계 2-2:
폴리
-3-
옥틸셀레노펜
무수 THF(60ml)중 2,5-다이브로모-3-옥틸셀레노펜(5.98 g, 14.9 mmol)의 교반된 용액에 n-부틸마그네슘 클로라이드(7.3 ml의 2.0 M 용액/THF, 14.6 mmol)를 16 내지 18℃에서 서서히 첨가한다. 완전히 첨가한 후, 혼합물을 또 다른 30분 동안 교반하고, 1시간 동안 가열하여 환류시킨다. 가열을 멈추고 1,2-비스(다이페닐포스피노)에탄니켈 클로라이드(27 mg, 0.05 mmol)를 고형물로서 첨가한다. 생성된 반응 혼합물을 21시간 동안 환류시키고, 실온까지 냉각시키고 교반된 메탄올 안으로 서서히 첨가하여 침전시킨다. 침전물을 여거하고 아세톤으로 세척하여 자주색 고형물을 수득한다. 이러한 조질 생성물을 22시간 동안 메탄올로, 20 시간 동안 아세톤으로 그리고 20 시간 동안 THF로 속실렛 추출을 통해 세척하고, 뜨거운 클로로벤젠중 용해한다. 이러한 용액을 메탄올에 적가하고, 형성된 침전물을 여과에 의해 수집하고 아세톤으로 세척하고, 이어서 진공 건조하여 자주빛 중합체를 수득 하였다(3.3Og, 91%). GPC(C6H5Cl, 60℃): Mn = 138,000, Mw 218,000 g/mol. 1H NMR(300 MHz, C6D5C1 70℃) δ(ppm) 7.28(s, 1H)1 2.80(t, 2H), 1.72(m, 2H), 1.45(m, 2H), 1.25(m, 8H), 0.88(t, 3H). RR(위치규칙성) > 97%.
실시예
3
중합체 3은 하기 반응식 5와 제조한다:
단계 3.1: 2,5-
다이브로모셀레노펜
:
3-데실셀레노펜(0.92 g, 3.4 mmol)을 THF(20 ml)중 용해하고, 0℃에서 N-브로모숙신이미드(1.2 g, 6.7 mmol)를 10분 동안 여러번에 나눠 첨가하였다. 완전히 첨가한 후, 혼합물을 16 내지 18℃까지 가열되도록 하고 질소하에 암실에서 밤새 교반한다(약 16시간). 이어서 물을 첨가하고 혼합물을 에틸 아세테이트로 추출한다(3 x 50 ml). 합한 추출물을 물 및 염수로 세척하고 Na2SO4상에서 건조시킨다. 용매를 감압하에 제거한다. 잔사를 실리카상에서 가솔린으로 용리하면서 칼럼 크로마토그래피에 의해 정제하여 흐린 노란색 오일(1.27 g, 87%)을 수득한다. MS(El) 430(t, M+). 1H NMR(300 MHz, CDCl3): δ(ppm) 6.95(s, 1H), 2.47(t, J= 7.5 Hz, 2H), 1.51(m, 2H), 1.26(m, 14H), 0.88(t, 3H).
단계 3.2:
폴리(3-데실)셀레노펜
:
무수 THF(10 ml)중 2,5-다이브로모-3-데실셀레노펜(0.98g, 2.3mmol)의 교반된 용액에 16 내지 18℃에서 n-부틸마그네슘 클로라이드(THF중 1.0 ml의 2.0 M 용액, 2.0 mmol)를 서서히 첨가하였다. 완전히 첨가한 후, 혼합물을 추가로 50분 동안 교반하고 1시간 동안 환류하에 가열한다. 가열을 멈추고 1,2-비스(다이페닐포스피노)에탄니켈 클로라이드(5 mg, 0.01 mmol)를 고형물로서 첨가한다. 생성된 반응 혼합물을 22시간 동안 환류하고, 이어서 실온까지 냉각하고 교반된 메탄올 안으로 서서히 첨가한다. 침전물을 여과 제거하고 아세톤으로 세척하여 자주색 고형물을 수득한다. 이러한 조질 생성물은 또한 18시간 동안 메탄올로, 8시간 동안 아세톤으로, 24시간 동안 이소-헥산으로 속실렛 추출하여 세척함으로써 정제하고, 이어서 뜨거운 클로로벤젠중에 용해했다. 이러한 용액을 메탄올에 적가하고, 형성된 침전물을 여과에 의해 모으고 아세톤으로 세척하고 이어서 진공하에 건조하여 자주색 중합체(0.48 g, 77%)를 수득한다. GPC(C6H5Cl 6O℃): Mn 90,000, Mw 131,000 g/mol. 1H NMR(300 MHz, C6D5Cl): δ(ppm) 7.28(s, 1H), 2.81(t, 2H, J = 7.1 Hz), 1.73(m, 2H), 1.44(m, 2H) 1.28(m, 12H), 0.88(t, 3H). RR(위치규칙성) > 96%.
실시예
4
중합체 4는 하기 반응식 6에 개시된 바와 같이 제조된다:
4.1 2,5-
비스(트라이메틸스태닐)셀레노펜
:
질소하에 0℃에서 무수 헥산(90 ml) 및 TMEDA(17.4 g, 150 mmol)의 용액중 셀레노펜(7.4 g, 56.5 mmol)의 용액에 n-BuLi(헥산중 55 ml의 2.5M 용액, 137.5 mmol)의 용액을 5분 동안 적가하였다. 생성된 용액을 30분 동안 환류하고 이어서 0℃까지 냉각하고 트라이메틸주석 클로라이드(25.6 g, 129 mmol)를 고형물로서 한번에 첨가한다. 생성된 용액을 실온까지 가온하고 20시간 동안 이 온도에서 교반한다. 이 용액을 물(100 ml)로 급랭하고, 에틸 아세테이트(100 ml)를 첨가한다. 층들을 분리하고 유기층을 추가로 물(4 x 100 ml), 염수(100 ml)로 세척하고, 건조하고(Na2SO4), 여과하고 감압하에 농축한다. 생성된 고형물을 아세토니트릴로부터 4회 재결정화하고 생성물을 백색 침상으로서 수득한다(25.8 g, 83%). M/Z 클러스터 는 456(M+)에 중심이 있음. 실측치 C, 26.3; H, 4.6. Cl0H20SeSn2에 대한 계산치 C, 26.3; H, 4.2. 1H NMR(300 MHz, CDCl3) δ 7.68(s, 2H), 0.37(s, 18H). 13C NMR(75 MHz, CDCl3) δ 150.2, 138.7, -7.7.
4.2. 4,4'-
비스
(
헥실
)-2,2'-
바이셀레노펜
:
-40℃에서 무수 THF(25ml)중 3-헥실셀레노펜(4.30 g, 20 mmol) 및 N,N,N', N'- 테트라메틸에틸렌다이아민(2.44 g, 21 mmol)의 용액에 n-BuLi(헥산중 8.5 ml의 2.5M 용액, 21.3 mmol)을 첨가한다. 이 용액을 25℃까지 30분 동안 가온하고 25℃에서 45분 동안 교반한다. 생성된 용액을 -20℃까지 냉각하고 구리(II) 클로라이드(2.96 g, 22 mmol)를 고형물로서 한번에 첨가한다. 반응을 25℃에서 추가로 16시간 동안 교반하고 5% HCl(50 ml)을 첨가하여 급랭한다. 유기물을 에틸 아세테이트로 추출한다(3 x 50 ml). 합쳐진 유기물을 5% HCl(2 x 50 ml), 물(50 ml) 및 포화 소듐 클로라이드(50 ml)로 세척하고, 건조시키고(Na2SO4), 여과하고 감압하에 농축한다. 생성된 오일을 실리카상에서 칼럼 크로마토그래피에 의해 추가로 정제한다(용리액: 가솔린 40 내지 60℃). 처음 분획은 3-헥실셀레노펜을 함유하고 제 2 분획은 생성물을 함유한다. -70℃에서 THF/아세토니트릴로부터 재결정화하여 생성물을 백색 고형물(2.1 g, 49%)로서 수득한다. Mpt 34-35.5℃. M/Z 430(M+). 1H NMR(300 MHz, CDCl3) δ 7.36(s, 2H), 7.11(s, 2H)1 2.52(t, 4H), 1.60(오중선, 4H), 1.30(m, 12H), 0.89(t, 6H). 13C NMR(75 MHz, CDCl3) δ 145.9, 144.0, 128.3, 122.9, 32.3, 31.7, 30.2, 29.0, 22.7, 14.2. 실측치 C, 56.3; H, 7.2. C20H30Se2는 C, 56.1 ; H, 7.1를 요구한다.
4.3 5.5'-
다이브로모
-4,4'-
비스
(
헥실
)-2,2'-
바이셀레노펜
:
암실에서 25℃에서 테트라하이드로푸란(25mL)중 4,4'-비스(헥실)-2,2'-바이셀레노펜(1.0g, 2.33mmol)의 용액에 N-브로모석신이미드(0.84 g, 4.72 mmol)를 30분에 걸쳐 2번에 나눠 첨가하였다. 생성된 용액을 6시간 동안 교반한다. 용매를 감압하에 제거하고 잔사를 에틸 아세테이트(50 ml)중 용해하고 물(2 x 30 ml) 및 포화 소듐 클로라이드(30 ml)로 세척하고, 여과하고 감압하에 농축하였다. 생성된 조질 생성물을 실리카 마개를 통해 여과하고(용리액: 가솔린 40 내지 60℃) 감압하에 농축한다. 에탄올로부터 재결정화하여 생성물(0.75 g, 55%)을 백색 결정으로서 수득한다. Mpt. 57-58 ℃. M/Z 삼중선은 456에 중심이 있음(M+). 1H NMR(300 MHz, CDCl3) δ 6.84(s, 2H), 2.48(t, 4H), 1.55(오중선, 4H), 1.3(m, 12H), 0.89(t, 6H). 13C NMR(75 MHz, CDCl3) δ 145.3, 142.9, 127.7, 110.3, 31.6, 30.9, 29.7, 29.6, 22.6, 14.2. 실측치 C, 41.1; H, 4.7. C20H30Se2Br2는 C, 41.0; H, 4.8를 요구함.
폴리
(2,5-
비스(3-헥실셀로펜-2-일)셀레노펜
) [
4
]:
10 ml 유리 바이알에 교반 바, 5,5'-다이브로모-4,4'- 비스(헥실)-2,2'-바이셀레노펜(150 mg, 0.256 mmol), 2,5-비스-트라이메틸스태닐셀레노펜(116.9 mg, 0.256 mmol), 트리스(다이벤질리덴아세톤)다이팔라듐(0)(4.7 mg, 0.005 mmol, 4 mol % Pd), 트라이(o-톨릴)포스핀(6.2 mg, 0.02 mmol, 8 mol %) 및 클로로벤젠(5 ml)을 충전한다. 유리 바이알에 질소를 퍼징하고 안전하게 밀봉한다. 유리 바이알을 마이크로웨이브 반응기 안에 두고(Emrys Creator, Personal Chemistry Ltd) 140℃까지 2분 동안 순차적으로 가열하고, 2분 동안 160℃까지 및 15분 동안 180℃까지 가열한다. 실온까지 냉각한 후, 반응 혼합물을 메탄올(50 ml) 및 37% 염화수소산(5 mL)의 혼합물 안으로 침전시키고 14시간 동안 교반한다. 중합체를 여과하고, 메탄올(6시간), 아세톤(24시간) 및 이소헥산(24시간)으로 세척한다(속실렛 추출을 통해). 생성된 중합체를 뜨거운 클로로포름중 용해시키고 메탄올 안으로 침전시켜 생성물(90 mg)을 수득한다. GPC(클로로벤젠, 6O℃) Mn(10,500 g/mol), Mw(26,000 g/mol). λmax(고형 필름) 564, 596, 659(sh) nm. λmax(C6H5Cl1, 60℃) 508 nm. 1H NMR(300 MHz, 60℃, 1,2-C6D4Cl2) δ 7.26(s, 2H), 용매 피크에 의해 뚜렷하지 않은 다른 방향족 양자, 2.79(br t, 4H), 1.73(m, 4H), 1.40(m, 4H), 1.27(m, 8H), 0.89(t, 6H).
실시예
5
중합체 5는 하기 반응식 7에 기술한 바와 같이 제조된다:
5.1. 4,4'-
비스
(
옥틸
)-2,2'-
바이셀레노펜
:
-40℃에서 무수 THF(40 ml)중 3-옥틸셀레노펜(7.30 g, 30 mmol) 및 N,N,N',N'-테트라메틸에틸렌다이아민(3.72 g, 32 mmol)의 용액에 n-BuLi(12.8 ml의2.5M 용액/헥산, 32 mmol)을 첨가한다. 상기 용액을 30분 동안 25℃까지 가온하고, 25℃에서 30분 동안 교반한다. 생성된 용액을 -20℃까지 냉각하고 구리(II) 클로라이드(4.57 g, 34 mmol)를 고형물로서 한번에 첨가한다. 반응을 추가로 16시간 동안 25℃에서 교반하고, 5% HCl(50 ml)를 첨가하여 급랭한다. 유기물을 에틸 아세테이트(3 x 100 ml)로 추출한다. 합쳐진 유기물을 5% HCl(2 x 80 ml), 물(80 ml) 및 포화 소듐 클로라이드(80 ml)로 세척하고, 건조하고(Na2SO4), 여과하고 감압하에 농축한다. 생성된 오일을 실리카상에서 칼럼 크로마토그래피로 추가로 정제 한다(용리액: 가솔린 40-60℃). 첫번째 분획은 3-옥틸셀레노펜을 함유하고 두번째 분획은 생성물을 함유한다. 다이에틸 에터로부터 재결정화하여 생성물을 백색 고형물로 수득한다(2.92 g, 40%). M/Z 486(M+). 1H NMR(300 MHz, CDCl3) δ 7.35(s, 2H), 7.11(s, 2H), 2.52(t, 4H), 1.60(오중선, 4H), 1.30(m, 20H)1 0.88(t, 6H). 13C NMR(75 MHz, CDCl3) δ 146.0, 144.0, 128.4, 122.9, 32.3, 31.9, 30.3, 29.5, 29.4, 29.3, 22.7, 14.2. 실측치 C, 59.1; H, 8.1. C24H38Se2는 C, 59.5; H, 7.9를 요구한다.
5.2: 5,5'- 다이브로모 -4.4'- 비스 ( 옥틸 )-2.2'-바이 셀레노펜:
0℃에서 테트라하이드로푸란(40 ml)중 4,4'-비스(옥틸)-2,2'-바이셀레노펜(2.5 g, 5.16 mmol)의 용액에 N-브로모석신이미드(1.84 g, 10.32 mmol)을 암실에서 1시간 동안 여러번 나누어 첨가한다. 생성된 용액을 4시간 동안 교반한다. 용매를 감압하에 제거하고 에틸 아세테이트(100 ml)중 용해된 잔사를 물(2 x 30 ml) 및 포화 소듐 클로라이드(30 ml)로 세척하고, 여과하고 감압하에 농축한다. 생성된 조질 생성물을 실리카 마개를 통해 여과하고(용리액: 가솔린 40 내지 60℃) 감압하에 농축한다. 에탄올로부터 재결정화하여 생성물을 백색 결정으로서 수득한다(2.1 g, 63%). M/Z 삼중선은 642에 중심이 있음 642(M+). 1H NMR(300 MHz, CDCl3) δ 6.84(s, 2H), 2.48(t, 4H), 1.56(오중선, 4H), 1.3(m, 20H), 0.88(t, 6H). 13C NMR(75 MHz, CDCl3) δ 145.3, 142.9, 127.7, 110.3, 31.9, 30.9, 29.6, 29.4, 29.3(3C), 22.7, 14.2. 실측치 C, 44.8; H, 5.7. C24H36Se2Br2는 C, 44.9; H, 5.7을 요구한다.
5.3 폴리(2,5-
비스(3-옥틸셀로펜-2-일)셀레노펜
)[
5
]:
10 ml 용량의 유리 바이알에 교반 바, 5,5'-다이브로모-4,4'-비스(헥실)-2,2'-바이셀레노펜(328.7 mg, 0.512 mmol), 2,5-비스-트라이메틸스태닐셀레노펜(233.7 mg, 0.512 mmol), 트리스(다이벤질리덴아세톤)다이팔라듐(0)(9.37 mg, 0.01 mmol, 4 mol % Pd), 트라이(o-톨릴)포스핀(12.46 mg, 0.04 mmol, 8 mol %) 및 클로로벤젠(8 ml)을 충전한다. 유리 바이알을 질소로 퍼징하고 안전하게 밀봉한다. 유리 바이알을 마이크로웨이브 반응기 안에 두고(Emrys Creator, Personal Chemistry Ltd) 2분 동안 140℃까지 순차적으로 가열하고, 2분 동안 160℃까지 가열하고 마지막으로 15분 동안 180℃까지 가열한다. 실온까지 냉각한 후, 반응 혼합물을 메탄올(50 ml) 및 37% 염화수소산(5 mL)의 혼합물 안으로 침전시키고 14시간 동안 교반한다. 중합체를 여과하고, 메탄올(6 시간), 아세톤(24 시간) 및 이소헥산(24 시간)으로 세척한다(속실렛 여과를 통해). 생성된 중합체를 뜨거운 클로로포름 안에 용해하고 메탄올 안으로 침전시켜 생성물을 수득한다(180 mg). GPC(클로로벤젠, 60℃) Mn(17,200 g/mol), Mw(38,700 g/mol). λmax(고형 필름) 600, 655(sh) nm. λmax(C6H5Cl1) 514 nm. 1H NMR(300 MHz, 6O℃, 1,2-C6D4Cl2) δ 7.27(s, 2H), 용매 피크에 의해 뚜렷하지 않은 다른 방향족 양자, 2.77(br t, 4H), 1.74(m, 4H), 1.40(m, 4H), 1.27(m, 16H), 0.88(t, 6H)
실시예
6
중합체 6은 아래 반응식 8에 기술한 바와 같이 제조한다:
6.1. 4,4'-
비스
(데실)-2.2'-
바이셀레노펜
:
3-데실셀레노펜을 공개된 절차에 따라 제조한다(참조: C. Mahatsekake 등, Phosphorus, Sulfur and Silicon, 1990, 47, 35-41; 1.0 g, 4.64 mmol). 무수 THF(25mL)중 3-데실셀레노펜(5.0 g, 18.4 mmol) 및 N,N,N',N'-테트라메틸에틸렌다이아민(2.56 g, 22 mmol)의 용액에 -40℃에서 n-BuLi(헥산중 8 ml의 2.5M 용액, 20 mmol)을 첨가한다. 용액을 45분에 걸쳐 25℃까지 가온하고, 10분 동안 40℃에서 교반한다. 생성된 용액을 -20℃까지 냉각하고 구리(II) 클로라이드(2.96 g, 22 mmol)를 고형물로서 한번에 첨가한다. 반응을 추가로 16시간 동안 25℃에서 교반하고, 5% HCl(50 ml)를 첨가하여 급랭한다. 유기물을 에틸 아세테이트(3 x 100 ml)로 추출한다. 결합된 유기물을 5% HCl(2 x 80 ml), 물(80 ml) 및 포화 소듐 클로라이드(80 ml)로 세척하고, 건조하고(Na2SO4), 여과하고 감압하에 농축한다. 생성된 오일을 실리카상에서 칼럼 크로마토그래피로 추가로 정제한다(용리액: 가솔린 40 내지 60℃). 첫번째 분획은 3-데실셀레노펜을 함유하고 두번째 분획은 생성물을 함유하였다. 다이에틸 에터로부터 재결정화하여 생성물을 백색 고형물로서 수득한다(2.6 g, 52%). Mpt 56.5-57.O℃. M/Z 542(M+). 1H NMR(300 MHz, CDCl3) δ 7.35(s, 2H), 7.10(s, 2H), 2.52(t, 4H), 1.60(오중선, 4H), 1.30(m, 28H), 0.88(t, 6H). 13C NMR(75 MHz, CDCl3) δ 145.9, 144.0, 128.4, 122.9, 32.3, 32.0, 30.3, 29.7, 29.65, 29.5, 29.4, 29.35, 22.7, 14.2. 실측치 C, 62.2; H, 9.0. C28H46Se2는 C, 62.2; H, 8.6을 요구한다.
6.2: 5,5'-
다이브로모
-4,4'-
비스
(데실)-2,2'-
비스셀레노펜
:
암실에서 테트라하이드로푸란(40 ml)중 4,4'-비스(데실)-2,2'-바이셀레노펜(2.4 g, 4.44 mmol)의 용액에 0℃에서 N-브로모석신이미드(1.84 g, 10.32 mmol)를 1시간에 걸쳐 여러번 나누어 첨가한다. 생성된 용액을 4시간 동안 교반한다. 용매를 감압하에 제거하고 잔사를 에틸 아세테이트(100 ml)중 용해하고 물(2 x 30 ml) 및 포화 소듐 클로라이드(30 ml)로 세척하고, 여과하고 감압하에 농축한다. 생성된 조질 생성물을 실리카 마개를 통해 여과하고(용리액: 가솔린 40-60℃) 감압하에 농축한다. 다이에틸 에터로부터 재결정화하여 생성물(2.92 g, 94%)을 백색 결정으로서 수득한다. M/Z 삼중선의 중심은 698(M+)에 있음. 1H NMR(300 MHz, CDCl3) δ 6.84(s, 2H)1 2.48(t, 4H), 1.56(오중선, 4H), 1.3(m, 28H), 0.88(t, 6H). 13C NMR(75 MHz, CDCl3) δ 145.3, 142.9, 127.7, 110.3, 31.9, 30.9, 29.7, 29.6(2C), 29.5, 29.4, 29.3, 22.7, 14.2. 실측치 C, 48.1 ; H, 6.4. C24H36Se2Br2는 C, 48.2 H, 6.4를 요구함.
6.3
폴리
(2,5-
비스(3-데실셀로펜-2-일)셀레노펜
) [
6
]:
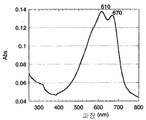
10 ml용량 유리 바이알에 교반 바, 5,5'-다이브로모-4,4'-비스(데실)-2,2'-바이셀레노펜(400 mg, 0.573 mmol), 2,5-비스-트라이메틸스태닐셀레노펜(261.5 mg, 0.573 mmol), 트리스(다이벤질리덴아세톤)다이팔라듐(0)(10.5 mg, 0.011 mmol, 4 mol % Pd), 트라이(o-톨릴)포스핀(13.95 mg, 0.046 mmol, 8 mol %) 및 클로로벤젠(7 ml)을 충전한다. 유리 바이알을 질소로 퍼징하고 안전하게 밀봉한다. 유리 바이알을 마이크로웨이브 반응기(Emrys Creator, Personal Chemistry Ltd) 안에 두고 2분 동안 140℃까지 순차적으로 가열하고, 이어서 2분 동안 160℃까지 가열하고 최종적으로 15분 동안 180℃까지 가열한다. 50℃까지 냉각한 후, 반응 혼합물을 메탄올(80 mL) 및 37% 염화수소산(20 mL)의 혼합물 안에 침전시키고 2시간 동안 교반하였다. 중합체를 여과하고, 메탄올(16 시간), 아세톤(16 시간) 및 이소헥산(16 시간)으로 세척한다(속실렛 추출을 통해). 생성된 중합체를 뜨거운 클로로벤젠 안에 용해하고 실리카 0.4 g상에서 교반하고, 아세톤으로 여과하여 생성물(380 mg)을 수득한다. GPC(클로로벤젠, 6O℃) Mn(30,000 g/mol), Mw(67,600 g/mol). λmax(고형물 필름) 610, 670(sh) nm. λmax(C6H5Cl1, 6O℃) 514 nm. 1H NMR(300 MHz, 6O℃, 1,2-C6D4Cl2) δ 7.25(s, 2H), 용매 피크에 의해 뚜렷하지 않은 다른 방향족 양자, 2.77(br t, 4H), 1.72(m, 4H), 1.40(m, 4H), 1.27(m, 24H), 0.89(t, 6H) . 실측치 C, 57.4; H, 6.9. (C32H46Se3)n에 대한 계산치 C, 57.8; H, 7.0.
도 2는 중합체 6의 고형 상태 UV 스펙트럼을 나타낸다.
실시예
7
중합체 7은 아래 반응식 9에 기술한 바와 같이 제조한다:
7.1 5,5'-
비스
-
트라이메틸스태닐
-2,2'-
바이셀레노펜
:
헥산중 BuLi의 용액(10.6 ml의 1.6 M 용액, 17 mmol)을 THF(50 ml) 및 TMEDA(1.98 g, 17 mmol)중 2,2'-바이셀레노펜(2.00 g, 7.7 mmol)의 냉각된(-78℃) 용액에 적가한다. BuLi를 첨가하면 즉시 색상 변화가 관찰된다(암적색). 20분 동안 교반한 후, 반응 혼합물은 암황색을 나타냈다. 혼합물을 6시간 동안 교반하고 16 내지 18℃까지 가온되게 한다. 가온중, 반응 혼합물은 겉모양이 초록색 현탁액으로 변했다. 이어서 반응 혼합물을 -70℃까지 냉각한다. 트라이메틸스태닐 클로라이드(3.38 g, 17 mmol)를 고형물로서 반응 혼합물에 첨가한다. 10분 후, 반응 혼합물은 갈색이 되었다. 반응 혼합물을 실온까지 밤새 가온되도록 한다. 반응을 물(100 mL)로 급랭하고 혼합물을 1시간 동안 교반한다. 에틸아세테이트(100 mL)를 혼합물에 첨가한다. 층들을 분리한다. 합쳐진 유기 추출물을 물, 염수로 세척하고 이어서 건조한다(Na2SO4). 여과 후, 조질 생성물을 농축하여 갈색 오일을 수득한다. MeCN을 첨가하고 혼합물을 5분 동안 교반한다. 혼합물을 아세토니트릴로부터 3회 재결정화한다. 물질을 추가의 정제없이 사용한다. MS(El) 588(M+).
7.2 폴리[4.4'-
다이데실
-(2.2';5',2";5",2")
쿼터셀레노펜
]
7
:
10 ml용량의 유리 바이알에 교반 바, 5,5'-다이브로모-4,4'-비스(데실)-2,2'-바이셀레노펜(298.2 mg, 0.427 mmol), 5,5'-비스-트라이메틸스태닐-2,2'-바이셀레노펜(250.0 mg, 0.427 mmol), 트리스(다이벤질리덴아세톤)다이팔라듐(0)(7.82 mg, 0.01 mmol, 4 mol % Pd), 트라이(o-톨릴)포스핀(10.40 mg, 0.034 mmol, 8 mol %) 및 클로로벤젠(5 ml)을 충전한다. 유리 바이알을 질소로 퍼징하고 안전하게 밀봉한다. 유리 바이알을 마이크로웨이브 반응기 안에 놓고(Emrys Creator, Personal Chemistry Ltd) 2분 동안 140℃까지 순차적으로 가열하고, 이어서 2분 동안 160℃까지, 마지막에는 15분 동안 180℃까지 가열한다. 실온까지 냉각한 후, 반응 혼합물을 메탄올(50 ml) 및 37% 염화수소산(5 ml)의 혼합물 안으로 침전시키고, 1.5시간 동안 교반한다. 중합체를 여과하고, 아세톤(6 시간), 및 이소헥산(24 시간)으로 세척한다(속실렛 추출을 통해). 생성된 중합체를 뜨거운 클로로포름중에 용해하고 메탄올 안으로 침전시켜 생성물(120 mg)을 수득한다. GPC(클로로벤젠, 60℃) Mn(10,000 g/mol), Mw(16,500 g/mol). λmax(필름) 605, 665(sh) nm.
실시예
8 - 용도
실시예
트랜지스터 제작 및 측정
박막 유기 전계-효과 트랜지스터(OFET)를 열적으로 성장한 실리콘 옥사이드(SiO2) 절연 층으로 고도로 도핑된 실리콘 기판상에서 제작하고, 여기서 기판은 공통 게이트 전극으로서 기능한다. 트랜지스터 소스-드레인 금 전극은 SiO2 층상에서 사진석판기술로 한정된다. 유기 반도체 침착 전, FET 기판을 실릴화제 헥사메틸다이실라잔(HMDS) 또는 옥틸트라이클로로실란(OTS)으로 처리한다. 이어서 얇은 반도체 필름을 FET 기판상에 클로로포름, 크실렌, 클로로벤젠 또는 다이클로로벤젠(0.4-1.0 중량%)중 스핀-코팅 중합체 용액에 의해 침착한다. 트랜지스터 장치의 전기적 특성화는 컴퓨터 제어된 아질런트 4155 C 세미컨덕터 파라미터 애널라이 저(Agilent 4155C Semiconductor Parameter Analyser)를 사용하여 질소 분위기하에 수행된다.
트랜지스터 특성은 스핀 코팅에 의해 제조된 필름상에서 측정한다. 필름을 10분 동안 100℃까지 질소하에 가열하여 잔사성 용매를 제거하고, 이어서 실온까지 냉각하여 트랜지스터 특성을 측정한다.
도 3a는 20 마이크론 채널 길이 및 20,000 마이크론 채널 폭을 갖는 트랜지스터 장치에서 중합체 1의 전류(I)-전압(V) 이동 특성(실시예 1에서 제 1 방법에 따라 제조됨)을 나타낸다. 트랜지스터 게이트 전압(Vg)은 소스-드래인 전압(Vsd)의 2개의 상이한 세팅에 대해 40 및 -60 볼트 사이에서 다양하다. Isd가 각각 Vsd=-5V(라인 a) 및 -60V(라인 b)에 있어서 Vg에 대해 도시된다. 도식은 순방향 및 역방향 스위프를 나타낸다. 도 3b는 동일한 트랜지스터에 대해 출력 특성을 나타내고, 여기서 게이트 전압은 15 볼트 간격으로 0V 및 -60V 사이에서 다양하고, 소스-드레인 전압은 0 내지 -60V에서 스위핑된다.
장치는 양호한 전류 모듈레이션 및 명확한 선형 및 포화 형태를 갖는 전형적인 p-유형 거동을 나타낸다. 전계 효과 이동성은 하기 수학식 1을 사용하여 포화 형태(Vd>(Vg-V0))로 계산된다:
상기 식에서,
W는 채널 폭이고, L은 채널 길이이고, Ci는 절연층의 캐패시탄스이고, Vg는 게이트 전압이고, Vd는 드레인 전압이고, Id는 드레인 전류이고, V0는 턴-온(turn-on) 전압이고 μsat는 포화 전하 운반체 이동성이다. 턴-온 전압(V0)은 소스-드레인 전류의 개시점으로서 측정된다(도 1). 화합물 1, 2, 3 & 6의 이동성 값은 표 1에 요약된다:
| 중합체 1, 2, 3 & 6의 전기 데이타 요약 | |||
| 화합물 | μsat(㎠/Vs) | μlin(㎠/Vs) | 온/오프 |
| 1 | 1.8-2 | 1.5-2 | 106 |
| 2 | 2.0-2 | 1.4-2 | 106 |
| 3 | 3.0-2 | 2.2-2 | 106 |
| 6 | 6.0-2 | 4.2-2 | 106 |
Claims (11)
- 3- 및/또는 4-위치에서 선택적으로 치환된 2,5-셀레노펜의 위치규칙성 중합체.
- 제 1 항에 있어서,하기 화학식 I로부터 선택된 것을 특징으로 하는 중합체:화학식 I상기 식에서,R1 -8은 서로 독립적으로, 복수일 경우에 서로 독립적으로, H, 할로겐, 선택적으로 치환된 아릴 또는 헤테로아릴, P-Sp-, P*-Sp-, 또는 탄소원자수 1 내지 40의 직쇄, 분지쇄 또는 사이클릭 알킬(F, Cl, Br, I 또는 CN에 의해 선택적으로 단일치환되거나 다중치환되고, 하나 이상의 비인접한 CH2기는 각각의 경우 서로 독립적으로 -O-, -S-, -NH-, -NR0-, -SiR0R00-, -CO-, -COO-, -OCO-, -O-CO-O-, -S-CO-, -CO-S-, -CX1=CX2- 또는 -C≡C-에 의해 O 및/또는 S 원자가 서로에 직접 연결되지 않도록 선택적으로 치환된다)이고,R0 및 R00는 서로 독립적으로 H, 탄소원자수 1 내지 12의 선택적으로 치환된 아릴 또는 알킬이고,X1 및 X2는 서로 독립적으로 H, F, Cl 또는 CN이고,P는 중합가능한 기이고,P*는 중합가능한 기 P로 전환되거나 P에 의해 치환될 수 있는 기이고,Sp는 스페이서기 또는 단일 결합이고,a, b, c 및 d는 서로 독립적으로 0, 1, 2 또는 3이고, a + b + c + d ≥ 1이고,n은 1보다 큰 정수이고,여기서 반복단위는 동일하거나 상이하다.
- 제 1 항 또는 제 2 항에 있어서,하기 화학식 I1로부터 선택된 것을 특징으로 하는 중합체:화학식 I1상기 식에서,R1 -6, a, b, c, d 및 n은 화학식 I의 의미를 갖고,R7 및 R8은 서로 독립적으로 R1의 의미중 하나를 갖거나 -Sn(R0)3, -B(OR')(OR"), -CH2Cl, -CHO, -CH=CH2 또는 -SiR0R00R000이고,R0, R00, R000는 서로 독립적으로 H, 탄소원자수 1 내지 12의 선택적으로 치환된 아릴 또는 알킬이고,R' 및 R"는 서로 독립적으로 H 또는 탄소원자수 1 내지 12의 알킬이거나, 또는 OR' 및 OR"는 붕소 원자와 함께 탄소원자수 2 내지 20을 갖는 사이클릭 기를 형성한다.
- 제 1 항 내지 제 4 항중 어느 한 항에 있어서,R1 -8이 C1-C20-알킬, C1-C20-알콕시, C1-C20-알케닐, C1-C20-알키닐, C1-C20-티오알킬, C1-C20-실릴, C1-C20-에스터, C1-C20-아미노 및 C1-C20-플루오로알킬로 이루어진 군으로부터 선택된 것임을 특징으로 하는 중합체.
- 제 1 항 내지 제 5 항중 어느 한 항에 있어서,n이 2 내지 5000의 정수인 것을 특징으로 하는 중합체.
- 제 1 항 내지 제 6 항중 어느 한 항에 있어서,R9 및 R10중 하나 또는 모두가 할로겐, -Sn(R0)3, -B(OR')(OR"), -CH2Cl, -CHO, -CH=CH2 또는 -SiR0R00R000인 것을 특징으로 하는 중합체.
- 제 1 항 내지 제 7 항중 어느 한 항에 따른 하나 이상의 중합체를 포함하는 반도체 또는 전하 수송 물질, 부품 또는 장치.
- 광학, 전기광학 또는 전자부품 또는 장치, 유기 전계 효과 트랜지스터(OFET), 집적회로(IC), 박막 트랜지스터(TFT), 플랫 패널 디스플레이, 무선주파수 식별(RFID) 태그, 전기발광 또는 발광 장치 또는 부품, 유기 발광 다이오드(OLED), 디스플레이의 백라이트, 광전지 또는 센서 장치, 전하 주입층, 쇼트키(Schottky) 다이오드, 평면화층, 정전기방지 필름, 전도성 기판 또는 패턴, 배터리에서 전극 물질, 광전도체, 전자사진 분야, 전자사진 기록, 유기 메모리 장치, 얼라인먼트 층에서 전하수송, 반도체, 전기전도성, 광전도성 또는 발광 물질로서 사용되거나, 또는 DNA 서열을 검출하고 검사하기 위한 제 1 항 내지 제 8 항중 어느 한 항에 따른 중합체의 용도.
- 제 1 항 내지 제 8 항중 어느 한 항에 따른 중합체, 반도체 또는 전하 수송 물질, 부품 또는 장치를 포함하는, 광학, 전기광학 또는 전자 장치, FET, IC, TFT, OLED 또는 RFID 태그.
- 2,5-다이할로-3-치환된 셀레노펜을 알킬 그리냐르 시약으로 처리하고 생성된 중간체 혼합물을 전이 금속 촉매를 첨가하여 중합함으로써, 제 1 항 내지 제 7 항중 하나 이상의 항에 따른 중합체를 제조하는 방법.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP05025621.3 | 2005-11-24 | ||
| EP05025621 | 2005-11-24 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20080069710A true KR20080069710A (ko) | 2008-07-28 |
Family
ID=37758571
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020087015194A KR20080069710A (ko) | 2005-11-24 | 2006-10-30 | 위치규칙성 폴리셀레노펜 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US8431682B2 (ko) |
| EP (1) | EP1951787B1 (ko) |
| JP (1) | JP2009520044A (ko) |
| KR (1) | KR20080069710A (ko) |
| CN (1) | CN101316876A (ko) |
| AT (1) | ATE499398T1 (ko) |
| DE (2) | DE112006002690T5 (ko) |
| GB (1) | GB2445514B (ko) |
| TW (1) | TW200738778A (ko) |
| WO (1) | WO2007059849A1 (ko) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5570818B2 (ja) * | 2007-01-31 | 2014-08-13 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 位置規則性ポリマーの調製方法 |
| JP2011517701A (ja) * | 2007-09-10 | 2011-06-16 | エダ リサーチ アンド ディベロップメント カンパニー,リミティド | セレノフェンおよびセレノフェン系重合体、それらの調製物、およびその使用 |
| KR101040216B1 (ko) * | 2009-01-14 | 2011-06-16 | 아주대학교산학협력단 | 릴레이 노드 배치방법, 릴레이 노드 배치 장치 및 컴퓨터로읽을 수 있는 기록매체 |
| JP5589821B2 (ja) * | 2010-12-20 | 2014-09-17 | 株式会社豊田中央研究所 | 蓄電デバイス及び電極活物質の製造方法 |
| JP2015513573A (ja) * | 2012-02-15 | 2015-05-14 | メルク パテント ゲーエムベーハー | 共役ポリマー |
| JP5937382B2 (ja) * | 2012-03-06 | 2016-06-22 | 国立大学法人東京工業大学 | 有機半導体用有機ヘテロ高分子及びそれを用いた半導体デバイス |
| CN113429575A (zh) * | 2021-06-17 | 2021-09-24 | 华南理工大学 | 一种含硒/碲杂环类聚合物及其制备方法和转化方法 |
Family Cites Families (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07116277B2 (ja) * | 1985-02-22 | 1995-12-13 | 三井東圧化学株式会社 | セレノフェン重合体の製造方法 |
| EP0261712A1 (en) | 1986-09-04 | 1988-03-30 | Koninklijke Philips Electronics N.V. | Picture display cell, method of forming an orientation layer on a substrate of the picture display cell and monomeric compounds for use in the orientation layer |
| US5892244A (en) | 1989-01-10 | 1999-04-06 | Mitsubishi Denki Kabushiki Kaisha | Field effect transistor including πconjugate polymer and liquid crystal display including the field effect transistor |
| US5198153A (en) | 1989-05-26 | 1993-03-30 | International Business Machines Corporation | Electrically conductive polymeric |
| JP2844122B2 (ja) * | 1990-11-01 | 1999-01-06 | 株式会社巴川製紙所 | 高分子示温材料 |
| JP3224829B2 (ja) | 1991-08-15 | 2001-11-05 | 株式会社東芝 | 有機電界効果型素子 |
| DE69325555D1 (de) | 1992-04-27 | 1999-08-12 | Merck Patent Gmbh | Elektrooptisches fluessigkristallsystem |
| DE4405316A1 (de) | 1994-02-19 | 1995-08-24 | Basf Ag | Neue polymerisierbare flüssigkristalline Verbindungen |
| DE19504224A1 (de) | 1994-02-23 | 1995-08-24 | Merck Patent Gmbh | Flüssigkristallines Material |
| JP3246189B2 (ja) * | 1994-06-28 | 2002-01-15 | 株式会社日立製作所 | 半導体表示装置 |
| WO1996021659A1 (en) | 1995-01-10 | 1996-07-18 | University Of Technology, Sydney | Organic semiconductor |
| DE19532408A1 (de) | 1995-09-01 | 1997-03-06 | Basf Ag | Polymerisierbare flüssigkristalline Verbindungen |
| EP0889350A1 (en) | 1997-07-03 | 1999-01-07 | ETHZ Institut für Polymere | Photoluminescent display devices (I) |
| US5998804A (en) | 1997-07-03 | 1999-12-07 | Hna Holdings, Inc. | Transistors incorporating substrates comprising liquid crystal polymers |
| EP0902043A3 (de) * | 1997-09-10 | 1999-08-11 | Basf Aktiengesellschaft | Polyselenophene, Verfahren zu deren Herstellung, und deren Verwendung |
| DE19739774A1 (de) * | 1997-09-10 | 1999-03-11 | Basf Ag | Polyselenophene als Materialien mit nichtlinear optischen Eigenschaften |
| US6166172A (en) * | 1999-02-10 | 2000-12-26 | Carnegie Mellon University | Method of forming poly-(3-substituted) thiophenes |
| BR0011888A (pt) | 1999-06-21 | 2004-03-09 | Univ Cambridge Tech | Processo para formar um dispositivo eletrônico, dispositivo eletrônico, circuito lógico, visor de matriz ativa, e, transistor de polímero |
| US6514578B1 (en) | 1999-06-30 | 2003-02-04 | Merck Patent Gesellschaft Mit Beschrankter Haftung | Polymerizable mesogenic tolanes |
| JP2001261796A (ja) * | 2000-03-14 | 2001-09-26 | Japan Science & Technology Corp | アルコキシポリチオフェンとアルコキシチオフェン |
| US20030021913A1 (en) | 2001-07-03 | 2003-01-30 | O'neill Mary | Liquid crystal alignment layer |
| US6770904B2 (en) * | 2002-01-11 | 2004-08-03 | Xerox Corporation | Polythiophenes and electronic devices generated therefrom |
| EP1852922A3 (en) | 2002-12-04 | 2010-03-10 | Merck Patent GmbH | Mono-, oligo- and poly-bis(thienyl)arylenes and their use as charge transport materials |
| FR2858222A1 (fr) | 2003-07-16 | 2005-02-04 | Oreal | Composition comprenant un polymere conducteur et un agent oxydant,procede de deformation permanente la mettant en oeuvre |
| EP1654298B1 (en) * | 2003-08-06 | 2008-10-01 | MERCK PATENT GmbH | Process of preparing regioregular polymers |
-
2006
- 2006-10-30 US US12/094,895 patent/US8431682B2/en not_active Expired - Fee Related
- 2006-10-30 KR KR1020087015194A patent/KR20080069710A/ko not_active Application Discontinuation
- 2006-10-30 DE DE112006002690T patent/DE112006002690T5/de not_active Withdrawn
- 2006-10-30 EP EP06828886A patent/EP1951787B1/en not_active Not-in-force
- 2006-10-30 DE DE602006020322T patent/DE602006020322D1/de active Active
- 2006-10-30 WO PCT/EP2006/010421 patent/WO2007059849A1/en active Application Filing
- 2006-10-30 JP JP2008541612A patent/JP2009520044A/ja active Pending
- 2006-10-30 AT AT06828886T patent/ATE499398T1/de not_active IP Right Cessation
- 2006-10-30 CN CNA2006800441760A patent/CN101316876A/zh active Pending
- 2006-10-30 GB GB0807844A patent/GB2445514B/en not_active Expired - Fee Related
- 2006-11-21 TW TW095143082A patent/TW200738778A/zh unknown
Also Published As
| Publication number | Publication date |
|---|---|
| JP2009520044A (ja) | 2009-05-21 |
| GB0807844D0 (en) | 2008-06-04 |
| EP1951787A1 (en) | 2008-08-06 |
| TW200738778A (en) | 2007-10-16 |
| WO2007059849A1 (en) | 2007-05-31 |
| GB2445514A (en) | 2008-07-09 |
| CN101316876A (zh) | 2008-12-03 |
| EP1951787B1 (en) | 2011-02-23 |
| ATE499398T1 (de) | 2011-03-15 |
| US8431682B2 (en) | 2013-04-30 |
| GB2445514B (en) | 2010-01-13 |
| DE112006002690T5 (de) | 2008-10-23 |
| DE602006020322D1 (de) | 2011-04-07 |
| US20090227764A1 (en) | 2009-09-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5301698B2 (ja) | モノ、オリゴおよびポリチエノ[2,3−b]チオフェン | |
| US7470377B2 (en) | Monomers, oligomers and polymers comprising thiophene and selenophene | |
| KR101355305B1 (ko) | 티에노 (3,4-d) 티아졸의 단량체, 올리고머 및 중합체 | |
| JP5474299B2 (ja) | チエノ[2,3−b]チオフェンのモノマー、オリゴマーおよびポリマー | |
| JP2008504370A (ja) | 重合性チエノ[3,2−b]チオフェン類 | |
| KR20090033909A (ko) | 치환 벤조디티오펜 및 벤조디셀레노펜 | |
| JP2004339193A (ja) | フルオレンおよびアリール基を含むモノマー、オリゴマーおよびポリマー | |
| EP1279689B1 (en) | Mono-, Oligo and Poly-3-(1,1-difluoroalkyl)thiophenes and their use as charge transport materials | |
| EP1951787B1 (en) | Regioregular polyselenophenes | |
| EP1477504A1 (en) | Mono-, oligo- and polymers comprising dithienotiophene and aryl groups | |
| EP1398336B1 (en) | Mono-, Oligo- and Poly(3-alkynylthiophenes) and their Use as Charge Transport Materials | |
| EP1300430A1 (en) | Mono-, oligo- and polymers of benzo[b]thiophene and 2,2'-bisbenzo[b]thiophene and their use as charge transport materials | |
| EP1279690A1 (en) | Mono-oligo- and poly-3-substituted-4-fluorothiophenes and their use as charge transport materials | |
| EP1475401A2 (en) | Mono-, oligo- and polymers comprising fluorene and aryl groups |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |