JP7586835B2 - ミトコンドリア標的化及び抗癌治療のためのアルキルtpp化合物 - Google Patents
ミトコンドリア標的化及び抗癌治療のためのアルキルtpp化合物 Download PDFInfo
- Publication number
- JP7586835B2 JP7586835B2 JP2021561710A JP2021561710A JP7586835B2 JP 7586835 B2 JP7586835 B2 JP 7586835B2 JP 2021561710 A JP2021561710 A JP 2021561710A JP 2021561710 A JP2021561710 A JP 2021561710A JP 7586835 B2 JP7586835 B2 JP 7586835B2
- Authority
- JP
- Japan
- Prior art keywords
- tpp
- cancer
- cells
- metabolic
- mitochondrial
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
- A61K31/662—Phosphorus acids or esters thereof having P—C bonds, e.g. foscarnet, trichlorfon
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
- A61K31/167—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide having the nitrogen of a carboxamide group directly attached to the aromatic ring, e.g. lidocaine, paracetamol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/365—Lactones
- A61K31/375—Ascorbic acid, i.e. vitamin C; Salts thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4375—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a six-membered ring having nitrogen as a ring heteroatom, e.g. quinolizines, naphthyridines, berberine, vincamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/60—Salicylic acid; Derivatives thereof
- A61K31/609—Amides, e.g. salicylamide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/65—Tetracyclines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7004—Monosaccharides having only carbon, hydrogen and oxygen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7048—Compounds having saccharide radicals and heterocyclic rings having oxygen as a ring hetero atom, e.g. leucoglucosan, hesperidin, erythromycin, nystatin, digitoxin or digoxin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pain & Pain Management (AREA)
- Oncology (AREA)
- Hematology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
本出願は、2019年4月16日出願の米国仮特許出願第62/834,932号、及び2019年5月3日出願の米国仮特許出願第62/842,893号の利益を主張するものであり、これらはいずれも、参照によりその全体が本出願に援用される。
Claims (8)
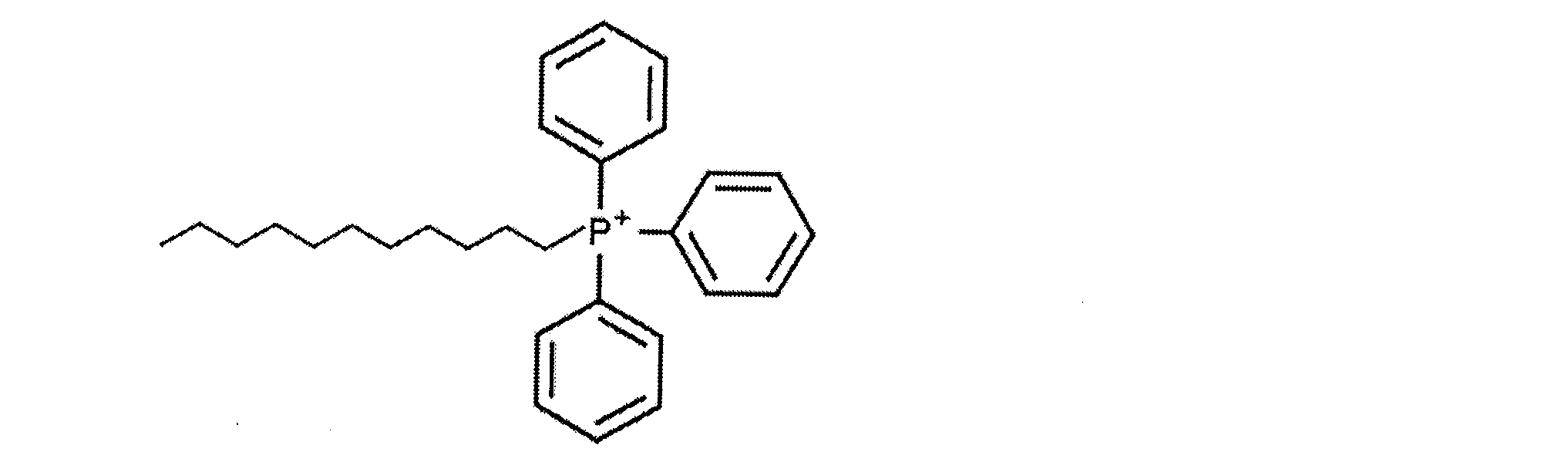
- 9~18個の炭素原子を含む飽和直鎖型アルキル鎖を有するアルキルトリフェニルホスホニウム(A‐TPP)化合物と、ドキシサイクリン、アジスロマイシン、ニクロサミド及び塩化ベルベリンよりなる群から選択されるOXPHOS阻害剤化合物とを含む、癌療法用組成物。
- 前記A‐TPP化合物はドデシルTPP(d‐TPP)を含む、請求項1に記載の組成物。
- ビタミンC及び2‐デオキシ‐グルコースよりなる群から選択される解糖阻害剤化合物を更に含む、請求項2に記載の組成物。
- 前記解糖阻害剤化合物はビタミンCを含む、請求項3に記載の組成物。
- 前記解糖阻害剤化合物は2‐デオキシ‐グルコースを含む、請求項3に記載の組成物。
- 前記OXPHOS阻害剤化合物はドキシサイクリンを含む、請求項1に記載の組成物。
- 前OXPHOS阻害剤化合物はニクロサミドを含む、請求項1に記載の組成物。
- 前記OXPHOS阻害剤化合物は塩化ベルベリンを含む、請求項1に記載の組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2024195137A JP7854213B2 (ja) | 2019-04-16 | 2024-11-07 | ミトコンドリア標的化及び抗癌治療のためのアルキルtpp化合物 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962834932P | 2019-04-16 | 2019-04-16 | |
| US62/834,932 | 2019-04-16 | ||
| US201962842893P | 2019-05-03 | 2019-05-03 | |
| US62/842,893 | 2019-05-03 | ||
| PCT/US2020/028414 WO2020214754A1 (en) | 2019-04-16 | 2020-04-16 | Alkyl-tpp compounds for mitochondria targeting and anti-cancer treatments |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024195137A Division JP7854213B2 (ja) | 2019-04-16 | 2024-11-07 | ミトコンドリア標的化及び抗癌治療のためのアルキルtpp化合物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022529949A JP2022529949A (ja) | 2022-06-27 |
| JP7586835B2 true JP7586835B2 (ja) | 2024-11-19 |
Family
ID=72837603
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021561710A Active JP7586835B2 (ja) | 2019-04-16 | 2020-04-16 | ミトコンドリア標的化及び抗癌治療のためのアルキルtpp化合物 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20220211728A1 (ja) |
| EP (1) | EP3955935B1 (ja) |
| JP (1) | JP7586835B2 (ja) |
| KR (1) | KR20210152500A (ja) |
| CN (1) | CN114025769A (ja) |
| CA (1) | CA3136811A1 (ja) |
| SG (1) | SG11202111450QA (ja) |
| WO (1) | WO2020214754A1 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022265178A1 (ko) * | 2021-06-15 | 2022-12-22 | 주식회사 스마틴바이오 | Trap1 억제제 및 이의 용도 |
| KR20230066947A (ko) | 2021-11-08 | 2023-05-16 | 현대모비스 주식회사 | 차량용 램프 |
| AU2022422771A1 (en) * | 2021-12-22 | 2024-07-04 | Lunella Biotech, Inc. | Mitochondrial atp inhibitors targeting the gamma subunit prevent metastasis |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013019975A1 (en) | 2011-08-03 | 2013-02-07 | University Of Iowa Research Foundation | Compositions and methods of treating cancer |
| EP3124027A1 (en) | 2015-07-28 | 2017-02-01 | Centrum Badan Molekularnych I Makromolekularnych Polskiej Akademii Nauk | Triphenylphosphonium salts for use in cancer threapy |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SI2563375T1 (sl) * | 2010-04-28 | 2014-09-30 | Alcon Research, Ltd. | Farmacevtski sestavki s fosfonijevimi antimikrobnimi sredstvi |
| US20150366884A1 (en) * | 2013-02-08 | 2015-12-24 | University Of Iowa Research Foundation | Compositions and methods for cancer therapy |
| PT2989110T (pt) * | 2013-04-24 | 2018-11-15 | Jira Neuzil | Derivados de tamoxifeno para o tratamento de doenças neoplásicas, especialmente com nível elevado de proteína her2 |
| EP3328372A4 (en) * | 2015-07-28 | 2019-03-20 | University Of Iowa Research Foundation | COMPOSITIONS AND METHOD FOR THE TREATMENT OF CANCER |
| BR112019019109B1 (pt) * | 2017-03-15 | 2023-11-07 | Lunella Biotech, Inc | Compostos mitorriboscina, composição farmacêutica compreendendo os mesmos, e seus usos direcionados para células cancerosas, bactérias e levedura patogênica |
| EP3612539A1 (en) * | 2017-04-20 | 2020-02-26 | Rising Tide Foundation | Phosphonium-ion tethered tetracycline drugs for treatment of cancer |
| EP3612540A1 (en) * | 2017-04-20 | 2020-02-26 | Rising Tide Foundation | Triphenylphosphonium-tethered tetracycyclines for use in treating cancer |
| US12006553B2 (en) | 2017-05-19 | 2024-06-11 | Lunella Biotech, Inc. | Companion diagnostics for mitochondrial inhibitors |
| US10980821B2 (en) | 2017-11-24 | 2021-04-20 | Lunella Biotech, Inc. | Triphenylphosphonium-derivative compounds for eradicating cancer stem cells |
| US20220365069A1 (en) * | 2019-09-13 | 2022-11-17 | Lunella Biotech, Inc. | Atp-based cell sorting and hyperproliferative cancer stem cells |
-
2020
- 2020-04-16 CA CA3136811A patent/CA3136811A1/en active Pending
- 2020-04-16 WO PCT/US2020/028414 patent/WO2020214754A1/en not_active Ceased
- 2020-04-16 EP EP20791432.6A patent/EP3955935B1/en active Active
- 2020-04-16 SG SG11202111450QA patent/SG11202111450QA/en unknown
- 2020-04-16 JP JP2021561710A patent/JP7586835B2/ja active Active
- 2020-04-16 US US17/604,651 patent/US20220211728A1/en active Pending
- 2020-04-16 KR KR1020217035882A patent/KR20210152500A/ko active Pending
- 2020-04-16 CN CN202080043979.4A patent/CN114025769A/zh active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013019975A1 (en) | 2011-08-03 | 2013-02-07 | University Of Iowa Research Foundation | Compositions and methods of treating cancer |
| EP3124027A1 (en) | 2015-07-28 | 2017-02-01 | Centrum Badan Molekularnych I Makromolekularnych Polskiej Akademii Nauk | Triphenylphosphonium salts for use in cancer threapy |
Non-Patent Citations (1)
| Title |
|---|
| Fedor F. Severin et al.,"Penetrating cation/fatty acid anion pair as a mitochondria-targeted protonophore",Proceedings of the National Academy of Sciences,2010年,Vol.107, No.2,p.663-668,DOI: 10.1073/pnas.0910216107 |
Also Published As
| Publication number | Publication date |
|---|---|
| SG11202111450QA (en) | 2021-11-29 |
| WO2020214754A1 (en) | 2020-10-22 |
| EP3955935B1 (en) | 2026-03-18 |
| KR20210152500A (ko) | 2021-12-15 |
| CN114025769A (zh) | 2022-02-08 |
| JP2025024030A (ja) | 2025-02-19 |
| EP3955935A4 (en) | 2023-01-18 |
| JP2022529949A (ja) | 2022-06-27 |
| CA3136811A1 (en) | 2020-10-22 |
| EP3955935A1 (en) | 2022-02-23 |
| US20220211728A1 (en) | 2022-07-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6046702B2 (ja) | 脳腫瘍の処置用のcsf−1r阻害剤 | |
| KR20210084555A (ko) | 신경모세포종의 치료에 사용하기 위한 오로라 a 키나제 억제제 | |
| AU2016234924B2 (en) | Compounds for the treatment of mTOR pathway related diseases | |
| JP7586835B2 (ja) | ミトコンドリア標的化及び抗癌治療のためのアルキルtpp化合物 | |
| CN102427814A (zh) | 激酶蛋白结合抑制剂 | |
| US20180252717A1 (en) | Methods and panels of compounds for characterization of glioblastoma multiforme tumors and cancer stem cells thereof | |
| WO2023104151A1 (zh) | 治疗肿瘤的药物组合及用途 | |
| EP4467140A1 (en) | Pharmaceutical combination for treating tumors and use thereof | |
| Gallardo et al. | Macrocyclic lactones block melanoma growth, metastases development and potentiate activity of anti–BRAF V600 inhibitors | |
| JP2020508290A (ja) | ゴシポールおよびフェンホルミンを有効成分として含む膵臓癌予防および治療用薬学的組成物 | |
| JP2022539074A (ja) | ミトコンドリアの標的化及び癌幹細胞の根絶のためのカルボシアニン化合物 | |
| WO2012151541A1 (en) | Csf-1r inhibitors for treatment of brain tumors | |
| JP7854213B2 (ja) | ミトコンドリア標的化及び抗癌治療のためのアルキルtpp化合物 | |
| KR102939983B1 (ko) | 1,1-다이에톡시에떼인을 유효성분으로 포함하는 항암제 | |
| US11286236B2 (en) | Compound, agent and composition for the suppression of cancer growth | |
| KR20230092999A (ko) | 감마 하위단위 예방 전이를 표적화하는 미토콘드리아 atp 억제제 | |
| JP2025500434A (ja) | γサブユニットを標的とするミトコンドリアATP阻害剤は転移を予防する | |
| WO2025059579A1 (en) | Methods of treating mat2a related diseases | |
| WO2017023277A1 (en) | Methods and compositions for characterization of glioblastoma multiforme tumors and cancer stem cells | |
| HK1241730A1 (en) | Composition for treating cancer stem cells |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230324 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240507 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240807 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240920 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241008 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241107 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7586835 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |