JP7279727B2 - ギ酸回収方法 - Google Patents
ギ酸回収方法 Download PDFInfo
- Publication number
- JP7279727B2 JP7279727B2 JP2021038072A JP2021038072A JP7279727B2 JP 7279727 B2 JP7279727 B2 JP 7279727B2 JP 2021038072 A JP2021038072 A JP 2021038072A JP 2021038072 A JP2021038072 A JP 2021038072A JP 7279727 B2 JP7279727 B2 JP 7279727B2
- Authority
- JP
- Japan
- Prior art keywords
- formic acid
- recovering
- aqueous solution
- solution containing
- dcm
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
Landscapes
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
R1R2R3N (1)
(式(1)において、R1~R3のうち少なくとも2つは独立して炭素数6以上12以下のアルキル基であり、残りは水素原子を示す。)
R1R2R3N (1)
(式(1)において、R1~R3のうち少なくとも2つは独立して炭素数6以上12以下のアルキル基であり、残りは水素原子を示す。)
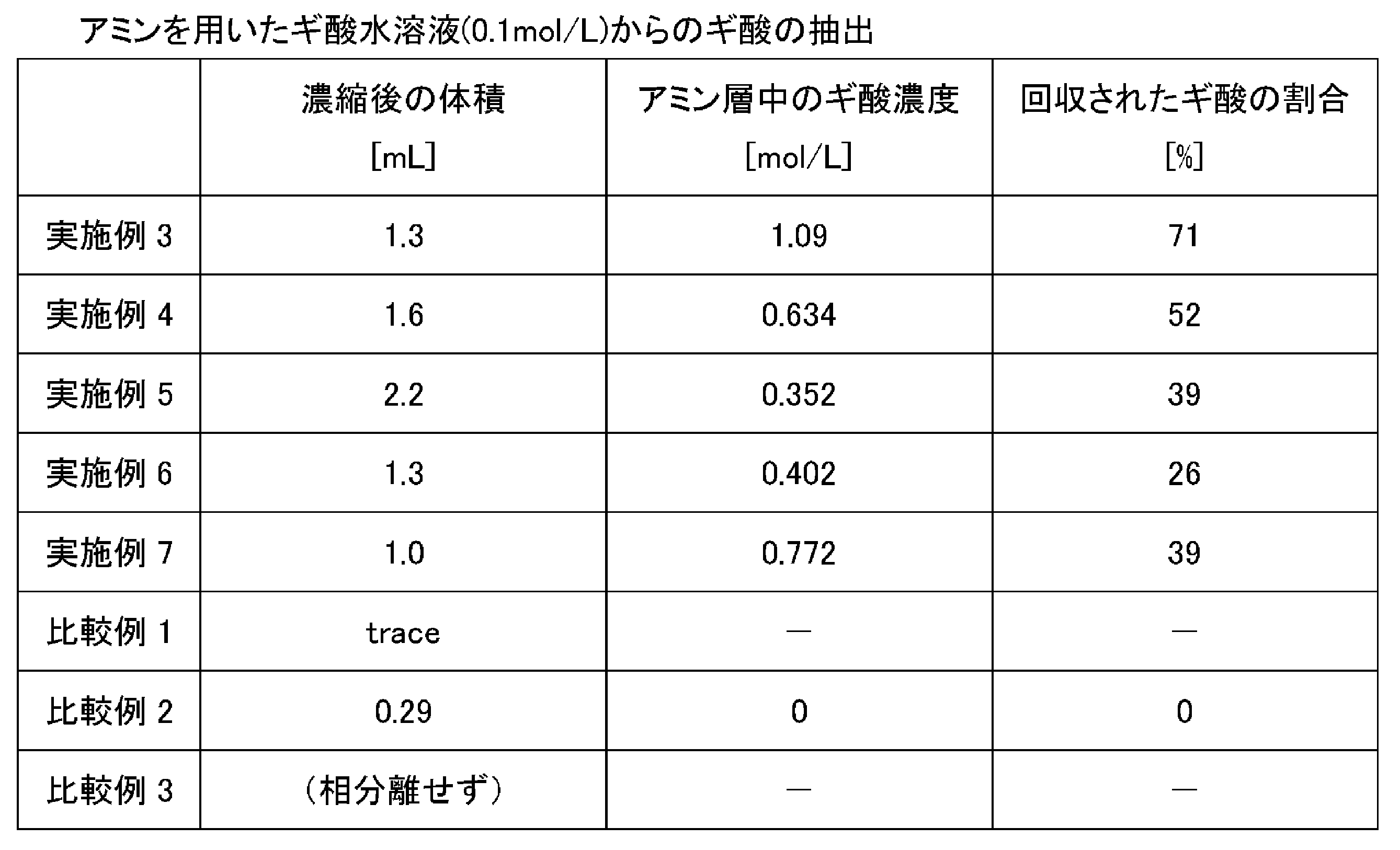
以下に示す方法で、トリ-n-オクチルアミン(TOA)(炭素数の合計は24)を用いてギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)と、ジクロロメタン(DCM、ナカライテスク株式会社、10mL)、トリ-n-オクチルアミン(TOA、東京化成株式会社製、1.75mL)(ギ酸の物質量に対して2.0当量)とを分液漏斗で、室温で1分間撹拌し、ギ酸をDCM層に抽出した。
(3)静置後、DCM層を分取し、メスシリンダーで分取量を確認した。
(4)エバポレーターでDCMを減圧留去し(40℃、200tor)、それぞれ濃縮した。
(5)重水素化クロロホルム(CDCl3、シグマアルドリッチ社製、4mL)に内部標準として1,2-ジクロロエタン(DCE、富士フィルム和光純薬株式会社製、8μL)を添加した。
(6)(5)の1mLに対して(4)のDCM層残渣から0.25mLを添加し、さらにCDCl3を加えて2.0mLとした。
(7)(6)の一部をNMR試料管に取って、1H-NMR測定装置(日本電子株式会社製、JNM-ECX400P)を用いて1H-NMRを測定した。
以下に示す方法で、トリス(2-エチルヘキシル)アミン(TEHA)(炭素数の合計は24)を用いてギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)と、DCM(10mL)と、トリス(2-エチルヘキシル)アミン(TEHA、東京化成株式会社製、1.73mL)(ギ酸の物質量に対して2.0当量)とを分液漏斗で、室温で1分間撹拌し、ギ酸をDCM層に抽出した。
(3)静置後、DCM層を分取し、メスシリンダーで分取量を確認した。
(4)エバポレーターでDCMを減圧留去し(40℃、200tor)、それぞれ濃縮した。
(5)CDCl3(5mL)に内部標準としてDCE(10μL)を添加した。
(6)(5)の1mLに対して(4)のDCM層残渣から0.25mLを添加し、さらにCDCl3を加えて2.0mLとした。
(7)(6)の一部をNMR試料管に取って、1H-NMRを測定した。
以下に示す方法で、ジ-n-オクチルアミン(DOA)(炭素数の合計は16)を用いてギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)を水で10倍に希釈したもの(0.01mol/L、200mL)と、DCM(10mL)と、ジ-n-オクチルアミン(DOA、東京化成株式会社製、1.21mL)(ギ酸の物質量に対して2.0当量)とを分液漏斗で、室温で1分間撹拌し、ギ酸をDCM層に抽出した。
(3)静置後、DCM層を分取し、メスシリンダーで分取量を確認した。
(4)エバポレーターでDCMを減圧留去し(40℃、200tor)、それぞれ濃縮した。
(5)CDCl3(4mL)に内部標準としてDCE(8μL)を添加した。
(6)(5)の1mLに対して(4)のDCM層残渣から0.25mLを添加し、さらにCDCl3を加えて2.0mLとした。
(7)(6)の一部をNMR試料管に取って、1H-NMRを測定した。
以下に示す方法で、トリヘプチルアミン(THpA)(炭素数の合計は21)を用いてギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)を水で10倍に希釈したもの(0.01mol/L、200mL)と、DCM(10mL)と、トリヘプチルアミン(THpA、東京化成株式会社製、1.54mL)(ギ酸の物質量に対して2.0当量)とを分液漏斗で、室温で1分間撹拌し、ギ酸をDCM層に抽出した。
(3)静置後、DCM層を分取し、メスシリンダーで分取量を確認した。
(4)エバポレーターでDCMを減圧留去し(40℃、200tor)、それぞれ濃縮した。
(5)CDCl3(4mL)に内部標準としてDCE(8μL)を添加した。
(6)(5)の1mLに対して(4)のDCM層残渣から0.25mLを添加し、さらにCDCl3を加えて2.0mLとした。
(7)(6)の一部をNMR試料管に取って、1H-NMRを測定した。
以下に示す方法で、トリドデシルアミン(TDdA)(炭素数の合計は36)を用いてギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)を水で10倍に希釈したもの(0.01mol/L、200mL)と、DCM(10mL)と、トリドデシルアミン(TDdA、東京化成株式会社製、2.53mL)(ギ酸の物質量に対して2.0当量)とを分液漏斗で、室温で1分間撹拌し、ギ酸をDCM層に抽出した。
(3)静置後、DCM層を分取し、メスシリンダーで分取量を確認した。
(4)エバポレーターでDCMを減圧留去し(40℃、200tor)、それぞれ濃縮した。
(5)CDCl3(4mL)に内部標準としてDCE(8μL)を添加した。
(6)(5)の1mLに対して(4)のDCM層残渣から0.25mLを添加し、さらにCDCl3を加えて2.0mLとした。
(7)(6)の一部をNMR試料管に取って、1H-NMRを測定した。
以下に示す方法で、トリヘキシルアミン(THexA)(炭素数の合計は18)を用いてギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)を水で10倍に希釈したもの(0.01mol/L、200mL)と、DCM(10mL)と、トリヘキシルアミン(THexA、東京化成株式会社製、1.35mL)(ギ酸の物質量に対して2.0当量)とを分液漏斗で、室温で1分間撹拌し、ギ酸をDCM層に抽出した。
(3)静置後、DCM層を分取し、メスシリンダーで分取量を確認した。
(4)エバポレーターでDCMを減圧留去し(40℃、200tor)、それぞれ濃縮した。
(5)CDCl3(4mL)に内部標準としてDCE(8μL)を添加した。
(6)(5)の1mLに対して(4)のDCM層残渣から0.25mLを添加し、さらにCDCl3を加えて2.0mLとした。
(7)(6)の一部をNMR試料管に取って、1H-NMRを測定した。
以下に示す方法で、N-メチル-ジ-n-オクチルアミン(MDOA)(炭素数の合計は17)を用いてギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)を水で10倍に希釈したもの(0.01mol/L、200mL)と、DCM(10mL)と、N-メチル-ジ-n-オクチルアミン(MDOA、東京化成株式会社製、1.28mL)(ギ酸の物質量に対して2.0当量)とを分液漏斗で、室温で1分間撹拌し、ギ酸をDCM層に抽出した。
(3)静置後、DCM層を分取し、メスシリンダーで分取量を確認した。
(4)エバポレーターでDCMを減圧留去し(40℃、200tor)、それぞれ濃縮した。
(5)CDCl3(4mL)に内部標準としてDCE(8μL)を添加した。
(6)(5)の1mLに対して(4)のDCM層残渣から0.25mLを添加し、さらにCDCl3を加えて2.0mLとした。
(7)(6)の一部をNMR試料管に取って、1H-NMRを測定した。
以下に示す方法で、ジイソプロピルエチルアミン(DiPrEA)(炭素数の合計は8)を用いてギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)を水で10倍に希釈したもの(0.01mol/L、200mL)と、DCM(10mL)と、ジイソプロピルエチルアミン(DiPrEA、東京化成株式会社製、0.68mL)(ギ酸の物質量に対して2.0当量)とを分液漏斗で、室温で1分間撹拌した。
(3)静置後、DCM層を分取し、メスシリンダーで分取量を確認した。
(4)エバポレーターでDCMを減圧留去し(40℃、200tor)、それぞれ濃縮した。
(5)CDCl3(4mL)に内部標準としてDCE(8μL)を添加した。
(6)(5)の1mLに対して(4)のDCM層残渣から0.25mLを添加し、さらにCDCl3を加えて2.0mLとした。
(7)(6)の一部をNMR試料管に取って、1H-NMRを測定した。
以下に示す方法で、オクチルアミン(OA)(炭素数の合計は8)を用いてギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)を水で10倍に希釈したもの(0.01mol/L、200mL)と、DCM(10mL)と、オクチルアミン(OA、東京化成株式会社製、0.66mL)(ギ酸の物質量に対して2.0当量)とを分液漏斗で、室温で1分間撹拌した。
(3)静置後、DCM層を分取し、メスシリンダーで分取量を確認した。
(4)エバポレーターでDCMを減圧留去し(40℃、200tor)、それぞれ濃縮した。
(5)CDCl3(4mL)に内部標準としてDCE(8μL)を添加した。
(6)(5)の1mLに対して(4)のDCM層残渣から0.25mLを添加し、さらにCDCl3を加えて2.0mLとした。
(7)(6)の一部をNMR試料管に取って、1H-NMRを測定した。
以下に示す方法で、ドデシルアミン(DdA)(炭素数の合計は12)を用いてギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)を水で10倍に希釈したもの(0.01mol/L、200mL)と、DCM(10mL)と、ドデシルアミン(DdA、東京化成株式会社製、0.74mL)(ギ酸の物質量に対して2.0当量)とを分液漏斗で、室温で1分間撹拌した。
(3)終夜(16時間)静置した。
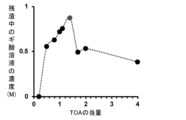
以下に示す方法で、トリ-n-オクチルアミン(TOA)を用い、TOAの使用量を変えて、ギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)と、DCM(10mL)と、トリ-n-オクチルアミン(TOA、東京化成株式会社製)0.175mL(ギ酸の物質量に対して0.20当量)、0.438mL(同0.50当量)、0.700mL(同0.80当量)、0,875mL(同1.0当量)、0.963mL(同1.1当量)、1.23mL(同1.4当量)、1.49mL(同1.7当量)、3.50mL(同4.0当量)とをそれぞれ分液漏斗で、室温で1分間撹拌し、ギ酸をDCM層に抽出した。
(3)静置後、DCM層を分取し、メスシリンダーで分取量を確認した。
(4)エバポレーターでDCMを減圧留去し(40℃、200tor)、それぞれ濃縮した。
(5)CDCl3(1mL)に内部標準としてDCE(2μL)を添加した。
(6)(5)の1mLに対して(4)のDCM層残渣から0.25mLを添加し、さらにCDCl3を加えて2.0mLとした。
(7)(6)の一部をNMR試料管に取って、1H-NMRを測定した。
以下に示す方法で、トリ-n-オクチルアミン(TOA)を用い、ジクロロメタン(DCM)の使用量を変えて、ギ酸水溶液からギ酸を回収した。
(2)(1)のギ酸水溶液(20mL)と、DCM(5,10,50,100mL)と、トリ-n-オクチルアミン(TOA、東京化成株式会社製、1.75mL)(ギ酸の物質量に対して2.0当量)とをそれぞれ分液漏斗で、室温で1分間撹拌し、ギ酸をDCM層に抽出した。
(3)静置後、DCM層を分取し、メスシリンダーで分取量を確認した。
(4)エバポレーターでDCMを減圧留去し(40℃、200tor)、それぞれ濃縮した。
(5)CDCl3(1mL)に内部標準としてDCE(2μL)を添加した。
(6)(5)の1mLに対して(4)のDCM層残渣から0.25mLを添加し、さらにCDCl3を加えて2.0mLとした。
(7)(6)の一部をNMR試料管に取って、1H-NMRを測定した。
Claims (8)
- ギ酸を含む水溶液から、下記式(1)で示すアルキルアミンと有機溶媒とを用いて、ギ酸を回収する回収工程と、
前記回収工程で得られたギ酸を含む有機溶媒層から有機溶媒を減圧または常圧にて留去する留去工程と、
を含むことを特徴とするギ酸回収方法。
R1R2R3N (1)
(式(1)において、R1~R3のうち少なくとも2つは独立して炭素数6以上12以下のアルキル基であり、残りは水素原子を示す。) - 請求項1に記載のギ酸回収方法であって、
R1~R3は、すべて独立して炭素数6以上12以下のアルキル基であることを特徴とするギ酸回収方法。 - 請求項1または2に記載のギ酸回収方法であって、
R1~R3の炭素数の合計は、12以上であることを特徴とするギ酸回収方法。 - 請求項1~3のいずれか1項に記載のギ酸回収方法であって、
用いる前記アルキルアミンの当量は、前記ギ酸を含む水溶液中のギ酸の物質量に対して0.5当量以上10当量以下の範囲であることを特徴とするギ酸回収方法。 - 請求項1~4のいずれか1項に記載のギ酸回収方法であって、
前記ギ酸を含む水溶液は、電気化学セル(太陽電池で駆動するものも含む)から生成したギ酸を含む水溶液であることを特徴とするギ酸回収方法。 - 請求項1~5のいずれか1項に記載のギ酸回収方法であって、
前記ギ酸を含む水溶液のpHは、7以下であることを特徴とするギ酸回収方法。 - 請求項1~6のいずれか1項に記載のギ酸回収方法であって、
前記有機溶媒の沸点は、80℃以下であることを特徴とするギ酸回収方法。 - 請求項1~7のいずれか1項に記載のギ酸回収方法であって、
用いる前記有機溶媒の量は、前記ギ酸を含む水溶液中のギ酸の濃度に対してアミンの濃度が1~100倍の範囲となる量であることを特徴とするギ酸回収方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021038072A JP7279727B2 (ja) | 2021-03-10 | 2021-03-10 | ギ酸回収方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021038072A JP7279727B2 (ja) | 2021-03-10 | 2021-03-10 | ギ酸回収方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022138278A JP2022138278A (ja) | 2022-09-26 |
| JP7279727B2 true JP7279727B2 (ja) | 2023-05-23 |
Family
ID=83400101
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021038072A Active JP7279727B2 (ja) | 2021-03-10 | 2021-03-10 | ギ酸回収方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7279727B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7758023B2 (ja) * | 2023-07-18 | 2025-10-22 | 株式会社豊田中央研究所 | 電気化学リアクタおよび人工光合成装置 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007522136A (ja) | 2004-01-29 | 2007-08-09 | ズィーケム インコーポレイテッド | 有機酸の回収 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3428319A1 (de) * | 1984-08-01 | 1986-02-13 | Hüls AG, 4370 Marl | Verfahren zur gewinnung wasserfreier bzw. weitgehendwasserfreier ameisensaeure |
| JP7372069B2 (ja) * | 2018-09-18 | 2023-10-31 | 日東電工株式会社 | ギ酸回収方法 |
-
2021
- 2021-03-10 JP JP2021038072A patent/JP7279727B2/ja active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007522136A (ja) | 2004-01-29 | 2007-08-09 | ズィーケム インコーポレイテッド | 有機酸の回収 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022138278A (ja) | 2022-09-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7044880B2 (ja) | ビニルスルホン酸無水物、その製造方法、及びビニルスルホニルフルオリドの製造方法 | |
| CN106854195B (zh) | 一种高纯度氟代碳酸乙烯酯的制备方法 | |
| JP7279727B2 (ja) | ギ酸回収方法 | |
| CN109264682B (zh) | 一种高纯度二氟磺酰亚胺的制备方法 | |
| JP5694576B2 (ja) | ジフルオロアセトニトリル及びその誘導体の製造方法 | |
| CN106146246A (zh) | 2,3,3,3‑四氟丙烯的纯化方法 | |
| CN102391072A (zh) | 从二氯丙醇氯化氢混合水溶液中分离二氯丙醇油相的方法 | |
| JP7335267B2 (ja) | パーフルオロ(2-メチレン-4-メチル-1,3-ジオキソラン)の製造方法 | |
| CN101768045B (zh) | 强酸性离子液体制备卤代烃方法 | |
| JP2008088135A (ja) | 第四級イミダゾリウムテトラフルオロボレートの精製方法及び該方法により精製した第四級イミダゾリウムテトラフルオロボレートを用いた電気二重層キャパシタ | |
| CN111809195B (zh) | α-二硫醚二羧酸类化合物的电化学催化氧化偶联合成方法 | |
| US9221847B2 (en) | Ionic liquid | |
| WO2010013685A1 (ja) | フルオロアルケン化合物の製造方法 | |
| JP2009084193A (ja) | チアゾリウム塩 | |
| CN115747846A (zh) | 一种五氟丙酰氟的制备方法 | |
| US8115018B2 (en) | Process for brominating alkylthiophenes | |
| JP2022138277A (ja) | ギ酸回収方法 | |
| JP4993262B2 (ja) | 第四級アンモニウムテトラフルオロボレートの精製方法及びそれを用いた電気二重層キャパシタ | |
| JP2005232019A (ja) | イオン性液体及びその製造方法 | |
| CN106810423B (zh) | 一种五氟苯酚的制备方法 | |
| JP6850070B2 (ja) | 組成物及びその製造方法 | |
| JP2021038188A (ja) | 含フッ素(メタ)アクリル酸エステル類の製造方法 | |
| KR20150119372A (ko) | 이온성 액체의 제조 공정 | |
| CN1745198A (zh) | 制备溴化羟基芳族化合物的方法 | |
| JP2020100618A (ja) | 4−メチル−5−ノナノン及び4−メチル−5−ノナノールの製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220324 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20230308 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230411 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230424 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7279727 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |