JP6541173B2 - 細胞死誘導ベクター及びそれを有する部位特異的細胞死誘導カイコ系統 - Google Patents
細胞死誘導ベクター及びそれを有する部位特異的細胞死誘導カイコ系統 Download PDFInfo
- Publication number
- JP6541173B2 JP6541173B2 JP2015022652A JP2015022652A JP6541173B2 JP 6541173 B2 JP6541173 B2 JP 6541173B2 JP 2015022652 A JP2015022652 A JP 2015022652A JP 2015022652 A JP2015022652 A JP 2015022652A JP 6541173 B2 JP6541173 B2 JP 6541173B2
- Authority
- JP
- Japan
- Prior art keywords
- cell death
- promoter
- gene
- site
- silkworm
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; CARE OF BIRDS, FISHES, INSECTS; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New breeds of animals
- A01K67/033—Rearing or breeding invertebrates; New breeds of invertebrates
- A01K67/04—Silkworms
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
Description
(2)前記プロアポトーシスタンパク質がBaxタンパク質又はBakタンパク質である、(1)に記載の細胞死誘導ベクター。
(3)部位特異的プロモーター及び該プロモーターの下流にプロアポトーシスタンパク質又はその活性断片をコードするDNAを機能的に連結した、(1)又は(2)に記載の細胞死誘導ベクター。
(4)部位特異的プロモーター及び該プロモーターの下流に機能的に連結した転写調節因子をコードする遺伝子を含む第1発現ユニット、及び該転写調節因子の標的プロモーター及び該標的プロモーターの下流に機能的に連結したプロアポトーシスタンパク質又はその活性断片をコードするDNAを含む第2発現ユニットから構成される、(1)又は(2)に記載の細胞死誘導ベクター。
(5)前記転写調節因子をコードする遺伝子がGAL4遺伝子であり、該転写調節因子の標的プロモーターがUASプロモーターである、(4)に記載の細胞死誘導ベクター。
(6)(3)に記載の細胞死誘導ベクターを含む部位特異的細胞死誘導カイコ系統。
(7)(4)又は(5)に記載の第2発現ユニットを含む部位特異的細胞死誘導カイコ系統。
(8)(4)又は(5)に記載の第1発現ユニットを有する遺伝子組換えカイコ系統と(7)に記載の部位特異的細胞死誘導カイコ系統とを交配させる工程、及び前記第1及び第2発現ユニットを有する部位特異的細胞死誘導カイコを選択する工程を含む部位特異的細胞死誘導カイコの作出方法。
1−1.概要
本発明の第1の態様は、細胞死誘導ベクターである。本発明の細胞死誘導ベクターは、発現ベクターであり、部位特異的プロモーターとその制御下にある脊椎動物由来、好ましくは哺乳動物由来のプロアポトーシスタンパク質、又はその活性断片をコードするDNAを含むことを特徴とする。本発明の細胞死誘導ベクターによれば、宿主であるチョウ目昆虫に導入することで、プロモーターが活性化される細胞又は組織において、細胞死を自在に誘導することができる。
「チョウ目昆虫」とは、分類学上のチョウ目(鱗翅目:Lepidoptera)に属する昆虫であって、チョウ又はガをいう。チョウには、タテハチョウ科(Nymphalidae)、アゲハチョウ科(Papilionidae)、シロチョウ科(Pieridae)、シジミチョウ科(Lycaenidae)、及びセセリチョウ科(Hesperiidae)に属する昆虫が含まれる。ガには、ヤママユガ科(Saturniidae)、カイコガ科(Bombycidae)、イボタガ科(Brahmaeidae)、オビガ科(Eupterotidae)、カレハガ科(Lasiocampidae)、ミノガ科(Psychidae)、シャクガ科(Geometridae)、ヒトリガ科(Archtiidae)、ヤガ科(Noctuidae)、メイガ科(Pyralidae)、スズメガ科(Sphingidae)等に属する昆虫が含まれる。例えば、ガであれば、Bombyx属、Samia属、Antheraea属、Saturnia属、Attacus属、Rhodinia属に属する種、具体的には、カイコ、クワコ(Bombyx mandarina)、シンジュサン(Samia cynthia;エリサンSamia cynthia ricini及びシンジュサンとエリサンの交配種を含む)、ヤママユガ(Antheraea yamamai)、サクサン(Antheraea pernyi)、ヒメヤママユ(Saturnia japonica)、オオミズアオ(Actias gnoma)等が挙げられる。
1−3−1.細胞死誘導ベクターの構成要素
本発明の細胞死誘導ベクターは、宿主の特定の細胞内で目的の遺伝子等を発現できるように構成されている。
「部位特異的プロモーター」とは、発現ベクターを導入した宿主個体の特定の細胞又は組織において、下流(3’末端側)に配置された遺伝子の発現を制御することのできるプロモーターである。本明細書では、宿主個体全体での発現を制御するユビキタスなプロモーター(全身性プロモーター)に対応する用語として使用する。
本発明の細胞死誘導ベクターは、目的の遺伝子等として、プロアポトーシスタンパク質又はその活性断片をコードするDNA(本明細書では、しばしば「プロアポトーシス遺伝子等」と表記する)を含む。
「標識遺伝子」は、選抜マーカーとも呼ばれる標識タンパク質をコードする遺伝子である。「標識タンパク質」とは、その活性に基づいて標識遺伝子の発現の有無を判別することのできるポリペプチドをいう。標識遺伝子は、細胞死誘導ベクターを保有する宿主、すなわち形質転換体を判別する目的、及び/又は細胞死誘導ベクターから発現した目的のタンパク質等をモニタリングする目的で用いられるが、本発明の細胞死誘導ベクターではいずれの目的で使用してもよい。いずれの場合にも、標識タンパク質の活性に基づいて形質転換体の判別や目的のタンパク等をモニタリングすることができる。ここで「活性に基づいて」とは、活性の検出結果に基づいて、という意味である。活性の検出は、標識タンパク質の活性そのものを直接的に検出するものであってもよいし、色素のような標識タンパク質の活性によって発生する代謝物を介して間接的に検出するものであってもよい。検出は、生物学的検出(抗体、アプタマー等のペプチドや核酸の結合による検出を含む)、化学的検出(酵素反応的検出を含む)、物理的検出(行動分析的検出を含む)、又は検出者の感覚的検出(視覚、触覚、嗅覚、聴覚、味覚による検出を含む)のいずれであってもよい。
「トランスポゾンの逆位末端反復配列(ITRs:inverted terminal repeat sequence)」は、本発明の細胞死誘導ベクターをゲノムDNAに相同組換え可能な発現ベクターとする場合に含まれ得る選択構成要素である。逆位末端反復配列は、通常は2個1組で使用され、トランスポゾンとしては、piggyBac、mariner、minos等を用いることができる(Shimizu,K. et al., 2000, Insect Mol. Biol., 9, 277-281;Wang W. et al.,2000, Insect Mol Biol 9(2):145-55)。
「5’UTR及び3’UTR」は、いずれもそれ自身がタンパク質やその断片、又は機能性核酸をコードしない非翻訳領域からなるポリヌクレオチドである。各UTRを構成する塩基配列は、限定はしないがプロアポトーシス遺伝子に由来する5’UTR及び3’UTRであることが好ましい。細胞死誘導ベクターにおいて5’UTRは、前記プロアポトーシス遺伝子等の開始コドンの上流(5’末端側)に配置され、3’UTRは、プロアポトーシス遺伝子等の終止コドンの下流(3’末端側)に配置される。なお、3’UTRは、ポリAシグナルを含むことができる。
「ターミネーター」は、本発明の細胞死誘導ベクターにおいて、プロアポトーシス遺伝子等の3’末端側、好ましくは終止コドンの下流に配置される塩基配列で、プロアポトーシス遺伝子等の転写を終結できる塩基配列で構成されている。例えば、配列番号28で示す塩基配列からなるhsp70ターミネーターや配列番号29で示す塩基配列からなるSV40ターミネーターが挙げられる。
「エンハンサー」は、本発明の細胞死誘導ベクターにおいて、部位特異的プロモーターの制御によるプロアポトーシス遺伝子等の発現をさらに増強することができる塩基配列からなる。
「インスレーター」は、周囲の染色体のクロマチンによる影響を受けることなく、その配列に挟まれた遺伝子の転写を、安定的に制御できる塩基配列である。例えば、ニワトリのcHS4配列やショウジョウバエのgypsy配列などが挙げられる。
「マルチクローニングサイト」は、複数のクローニング用制限酵素部位からなるクラスター配列である。マルチクローニングサイトを構成する塩基配列や包含する制限酵素部位の種類及び数については、特に制限はしない。また、細胞死誘導ベクターにおけるマルチクローニングサイトの数や配置される位置についても、制限はしないが、前記部位特異的プロモーターの制御領域範囲内に配置することが好ましい。そのような位置に配置することで、プロアポトーシス遺伝子等を本発明の細胞死誘導ベクター内に容易に挿入できるからである。
「転写調節因子の遺伝子」は、後述する第1発現ユニットの必須構成要素である。本明細書でいう「転写調節因子」とは、後述する標的プロモーターに結合して、その標的プロモーターを活性化することのできるタンパク質因子をいう。例えば、酵母のガラクトース代謝活性化タンパク質であるGAL4タンパク質、及びテトラサイクリン制御性トランス活性化因子であるtTA及びその変異体等が挙げられる。
「転写調節因子の標的プロモーター」とは、後述する第2発現ユニットの必須要素であって、第1発現ユニットにコードされた転写調節因子が結合することによって、その制御下にある遺伝子発現を活性化することのできるプロモーターをいう。前記転写調節因子とその標的プロモーターは、前記転写調節因子とは対応関係にあり、通常は、転写調節因子が定まれば、その標的プロモーターも必然的に定まる。例えば、転写調節因子がGAL4タンパク質の場合には、UAS(Upstream Activating Sequence)が使用される。
細胞死誘導ベクターは、1つの遺伝子発現ユニットで構成される場合と、2つの遺伝子発現ユニットで構成される場合がある。以下、それぞれの場合について説明をする。
細胞死誘導ベクターは、宿主細胞内でプロアポトーシス遺伝子等を発現させるのに必要な全ての構成要素を1つの細胞死誘導ベクター内に含む。具体的には、必須の構成要素である部位特異的プロモーター及びそのプロモーターの下流に発現可能な状態で配置されたプロアポトーシス遺伝子等を含む。
細胞死誘導ベクターが第1発現ユニット及び第2発現ユニットの2つの遺伝子発現ユニットで構成される場合、プロアポトーシス遺伝子等の発現に必須の構成要素は各ユニットに分割されて存在する。本構成では、第1及び第2発現ユニットが宿主細胞内に併存してはじめて1つの細胞死誘導ベクターとして機能する。すなわち、同一細胞内で第1発現ユニットに含まれるプロモーターの活性化により第1発現ユニットから転写調節因子が発現し、それが第2発現ユニットの標的プロモーターを活性化することによって目的のプロアポトーシス遺伝子等を発現することができる。第1及び第2発現ユニットは、以下の構成を有する。
本発明の細胞死誘導発現ベクターは、アポトーシスエフェクター因子をコードする発現ベクターであり、チョウ目昆虫の宿主、特にカイコに導入することによって、所望する細胞又は組織において、細胞死を自在に誘導することができる。
2−1.概要
本発明の第2の態様は、部位特異的細胞死誘導カイコ系統である。本態様のカイコ系統は、第1態様に記載の細胞死誘導ベクターを有するカイコ及びその後代である。本系統を用いることで、細胞死によって任意の細胞又は組織を壊滅させたカイコ系統を自在かつ容易に作出することができる。
本発明の「部位特異的細胞死誘導カイコ系統」は、第1態様に記載の細胞死誘導発現ベクターを有し、特定の細胞又は組織において細胞死を誘導する潜在性を有する継代可能な遺伝子組換え体又はその後代をいう。特定の細胞又は組織においてプロアポトーシスタンパク質等が発現しているか否かは問わない。
本発明の部位特異的細胞死誘導カイコ系統の作出方法は、細胞死誘導ベクターを宿主であるカイコに導入することで達成し得る。細胞死誘導ベクターのカイコ導入方法について以下で具体的に説明をする。
本発明の遺伝子組換えカイコ系統によれば、特定の細胞又は組織を細胞死によって壊滅させる部位特異的細胞死誘導カイコを容易に作出でき、また継代管理することができる。
3−1.概要
本発明の第3の態様は、部位特異的細胞死誘導カイコの作出方法である。本方法によれば、細胞死によって特定の細胞又は組織を壊滅させた部位特異的細胞死誘導カイコを作出することができる。
前述のように、細胞死誘導ベクターが1つの遺伝子発現ユニットで構成される場合には、細胞死誘導ベクターを有する部位特異的細胞死誘導カイコ系統が、同時に部位特異的細胞死誘導カイコとなる。また、細胞死誘導ベクターが第1及び第2発現ユニットの2つの遺伝子発現ユニットで構成される場合、両遺伝子発現ユニットを1個体内に有する遺伝子組換えカイコも部位特異的細胞死誘導カイコである。
「交配工程」とは、第1発現ユニットを有する遺伝子組換えカイコ系統と第2発現ユニットを有する部位特異的細胞死誘導カイコ系統とを交配させる工程である。交配は、二つのカイコ系統を常法に基づいて交配させればよい。2つの発現ユニットを有する遺伝子組換えカイコは、予め兄妹交配又は同系交配を行い、各発現ユニットに関してホモ接合体にしておくことが好ましい。
(目的)
本発明の細胞死誘導ベクターの構築に使用するプロアポトーシス遺伝子をクローニングし、その遺伝子がコードするタンパク質の細胞内局在を確認する。
プロアポトーシス遺伝子として、マウス由来のBax遺伝子(mBax遺伝子)を選択した。mBax遺伝子をクローニングするために、マウス3T3-L1細胞から総RNAを抽出した。抽出は、Trizol(life technologies)を用いて行った。具体的な手順は、キットに添付のプロトコルに従った。得られた総RNAの2μgを鋳型としてHigh-Capacity cDNA Reverse Transcription Kit(Roche-diagnostics)を用いて逆転写反応を行い、cDNAを合成した。具体的な手順は、キットに添付のプロトコルに従った。作製したcDNAライブラリを鋳型にmBax-F(配列番号30)及びmBax-R(配列番号31)のプライマーペアを用いてmBax遺伝子をPCRで増幅した。PCRは、KOD plus(TOYOBO)を用いて行い、反応液組成は、添付のプロトコルに記載されたスタンダードな方法に従った。PCRサイクルの条件は、94℃15秒、55℃30秒、68℃40秒を1サイクルとして、35サイクル行った。得られた増幅産物を、Bgl II制限酵素で消化した後、pEF-BOS-T7 vector (Kasashima et al., 1999, Genes Cells 4: 667-683.)のBamHIサイトへ挿入してクローニングを行い、哺乳細胞発現用ベクター「pEF-BOS-T7-mBax」を構築した。
図1に結果を示す。図1は、pBOS-T7-mBaxをトランスフェクションしたHeLa細胞の抗体染色図である。細胞内で発現したT7-mBaxは、抗T7抗体(αT7-tag; A)によって緑色蛍光(図中、白点で示される)として検出された。同時に、抗シトクロムc抗体(αcytoC; B)も反応させ、ミトコンドリアを赤色蛍光(図中、白点で示される)で標識した。Cは、AとBを重ねた図で、AとBの蛍光が一致した部位が存在すれば白点となって現れる。図1CからT7-mBaxタンパク質とシトクロムcの局在が一致していることがわかる。この結果から、T7タグを融合したT7-mBaxタンパク質もミトコンドリアに局在することが確認された。
(目的)
本発明の細胞死誘導ベクターを構築する。
本実施例では、第1発現ユニットと第2発現ユニットの2つの遺伝子発現ユニットからなる細胞死誘導ベクターを構築した。
(目的)
実施例2で構築した細胞死誘導ベクターを用いて本発明の部位特異的細胞死誘導カイコ系統を作出する。
実施例2で構築した細胞死誘導ベクターの第2発現ユニットpUAS-T7-mBaxとその対照用第2発現ユニットpUAS-EGFPを、Qiagen Plasmid Midi Kit (Qiagen)を用いて精製した。具体的な生成方法は、キットに添付のプロトコルに従った。精製後のpUAS-T7-mBaxとpUAS-UASを、それぞれトランスポゾン転移酵素をコードするpiggyBacヘルパープラスミドpHA3PIG(Tamura T. et al., 2000, Nature Biotechnology, 18, 81-84)と1:1の割合で混合し、非休眠系統であるカイコw1, pnd系統の産卵後4〜8時間の卵に顕微注入した(Tamura et al. 2000;前述)。注入後の卵は、加湿状態下、25℃で孵化するまでインキュベートした。孵化後、12時間明期と12時間暗期の光条件で25℃の飼育室にて、全齢を人工飼料(シルクメイト原種1-3齢S、日本農産工)で飼育した。人工飼料は2〜3日毎に交換した(Uchino K. et al., 2006;前述)。羽化後、兄妹交配を行い、得られたF1卵を孵化させた後、3xP3-EGFPマーカーによる眼の蛍光の有無で選抜して目的の遺伝子組換えカイコ系統を得た。遺伝子組換えカイコ系統は、休眠系統であるw-cと交配させて系統を維持した。
pUAS-T7-mBaxが染色体に組込まれた部位特異的細胞死誘導カイコ系統として「4-3D系統」及び「4-4A系統」の2系統を得た。この2系統について、pUAS-T7-mBaxの染色体への挿入は、サザンブロッティングにより確認した。その結果、いずれの系統もゲノム中への挿入は1コピーであることが明らかになった(図示せず)。また、4-3D系統と4-4A系統における細胞死誘導ベクターのゲノム挿入位置をインバースPCRによって検証したところ、4-3D系統は16番染色体に順方向で、また4-4A系統は26番染色体に逆方向で挿入されていることが明らかとなった。どちらも遺伝子間領域であり、ゲノム内の遺伝子を破壊する等といった挿入による影響はないと考えられた。
(目的)
本発明の部位特異的細胞死誘導カイコ系統を用いて作出された部位特異的細胞死誘導カイコにおいて、部位特異的プロモーターが活性化される細胞又は組織で細胞死が誘導されることを検証する。
実施例3で樹立した4-4A系統のヘテロオス個体を、Ser1系統(MSG-GAL4系統)、AyFib431a系統(PSG-GAL4系統)、及びSS19-1系統(30K-GAL4系統)のヘテロメス個体とそれぞれ交配させてF1個体を得た。ここで、MSG-GAL4系統は中部絹糸腺特異的なプロモーターを含む第1発現ユニットpMSG-GAL4を染色体に組込んだ遺伝子組換えカイコ系統(Tatematsu et al., 2010, Transgenic Res. 19: 473-487)であり、PSG-GAL4系統は後部絹糸腺特異的なプロモーターを含む第1発現ユニットpAyfib-GAL4を染色体に組込んだ遺伝子組換えカイコ系統(文献名Tsubota et al., 2014, G3. 4: 1347-1357)であり、そして30K-GAL4系統は脂肪体特異的なプロモーターを含む第1発現ユニットp30K-GAL4を染色体に組込んだ遺伝子組換えカイコ系統(文献名H. Sezutsu, personal communication)である。さらに対照用として、UAS-EGFP系統のヘテロオス個体をMSG-GAL4系統、PSG-GAL4系統、及び30K-GAL4系統のヘテロメス個体とそれぞれ交配させてF1個体を得た。
図2〜4に結果を示す。図2及び図3は絹糸腺を、図4は脂肪体を示している。
図2Aは、第1発現ユニットを含むMSG-GAL4系統と第2発現ユニットを含む4-4A系統を交配させて得られたF1個体のうち、第1発現ユニットと第2発現ユニットを包含する個体(MSG-GAL4/UAS-T7-mBax個体)の絹糸腺を示している。この図が示すように中部絹糸腺でmBax遺伝子を発現させた場合、中部絹糸腺(矢印)の退縮が観察された。一方、図2B及びCは、MSG-GAL4系統と対照用のUAS-EGFP系統を交配させて得られたF1個体のうち第1発現ユニットと対照用第2発現ユニットを有する個体(MSG-GAL4/UAS-EGFP個体)の絹糸腺を示している。図2Cの蛍光図で示すように、このF1個体では、中部絹糸腺(矢印)でEGFP遺伝子が発現しているが、中部絹糸腺の退縮は認められなかった。また、図2Dは、第2サブユニットのみを有し、mBaxタンパク質の発現が誘導されない4-4A系統の絹糸腺を示している。この個体も中部絹糸腺の退縮は認められなかった。
(目的)
本発明の細胞誘導ベクターによる部位特異的細胞死誘導カイコでの部位特異的細胞死がアポトーシスによる細胞死であることを検証する。
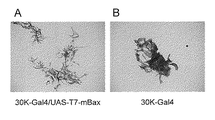
アポトーシスによる細胞死は、ゲノムが断片化する特徴がある。そこで、細胞死を誘導した組織のゲノムが断片化されていることを電気泳動法により確認した。30K-GAL4/UAS-T7-mBaxカイコ、及び対照区の30K-GAL4系統のカイコの5齢2日目幼虫及び4日目幼虫から脂肪体を摘出し、その脂肪体からフェノール法によりゲノムDNAを抽出した。抽出したゲノムDNAを1.8%のアガロースゲルで電気泳動を行い、30 K-GAL4/UAS-T7-mBaxと対照区の30K-GAL4間でゲノムDNAのサイズについて確認した。
図5に結果を示す。この図は脂肪体から抽出したカイコゲノムDNAのアガロース電気泳動の結果を示す図である。図5Aは5齢2日目幼虫由来の、また図5Bは5齢4日目幼虫由来の、カイコゲノムDNAの電気泳動を示す。
(目的)
本発明の部位特異的細胞死誘導カイコによる細胞死誘導が成虫段階でも可能か否かを検証する。
細胞死を誘導する細胞として、触角に存在するフェロモン受容細胞を選択した。フェロモン受容細胞では、成虫の体形成がほぼ完了した羽化3日前からBmOR1遺伝子の発現が始まる。BmOR1タンパク質は、カイコフェロモン物質ボンビコール(BOL)の受容体である。そこで、フェロモン受容細胞で細胞死を誘導させて、カイコ成虫の雄個体におけるフェロモンに対する応答行動(羽ばたき行動)に異常を生じるか否かを検証した。
図7にオスカイコの羽ばたき行動の結果を、図8にオス触角におけるBmOR1の発現量の結果を示す。グラフの縦軸は反応した個体の割合(%)、横軸はボンビコール濃度を示す。図中、sumi4-4A/1bはBmOR1-GAL4/UAS-T7-mBax系統を、1bはpBmOR1-GAL4系統を、そしてw1,pndはバックグラウンド系統を示している。対照区の系統(1b及びw1,pnd)のどちらも0.1ngの濃度で反応する個体が見られ、10ngの濃度では、ほとんどすべての個体が反応した。一方、BmOR1-GAL4/UAS-T7-mBax系統のsumi4-4A/1bでは反応を示した個体の出現が1 ngであった。さらに、1000ngの暴露を行っても、一部の個体は全く反応しなかった。以上の結果からフェロモン受容細胞でmBaxを発現させたオスカイコ個体では、ボンビコールに対する反応性が著しく低下することが明らかとなった。
(目的)
部位特異的プロモーターに代えて全身性プロモーターを有する第1発現ユニットを用いた場合、個体全体でも細胞死を誘導できるか否かを検証する。
全身性プロモーターであるアクチン3プロモーター(配列番号39)とその下流に発現可能な状態でGAL4遺伝子を連結したpBac[Actin3-GAL4: 3xP3-DsRed](Uchino et al., 2006, J. Insect Biotechnol. Sericology 75: 89-97)(「pActin3-GAL4」と略称する)を第1発現ユニットとした。この第1発現ユニットのみを染色体に組込んだ遺伝子組換えカイコ系統であるActin3-GAL4系統(Uchino et al., 2008, Insect Biochem. Mol. Biol. 38: 116-1173)のヘテロメス個体を、実施例4と同様に第2発現ユニットのみを含む4-4A系統のヘテロオス個体と交配させて、得られたF1胚の選択マーカーを確認し、発現ユニットの有無や保有する発現ユニットの種類によってF1胚を分類した。なお、pUAS-mBaxは眼におけるEGFP遺伝子が、pActin3-GAL4はDsRed遺伝子が、個体の選択マーカー遺伝子である。
図9に結果を示す。「GFP」はpUAS-mBaxのみを、「Red」はpActin3-GAL4のみを有する胚を示す。「double」は第1発現ユニットpActin3-GAL4と第2発現ユニットpUAS-mBaxの両方を有する胚である。「lethal」は初期胚で致死となった胚を、また「Negative」はpActin3-GAL4及びpUAS-mBaxのいずれも有さない胚を示す。
Claims (8)
- 部位特異的プロモーター、及び哺乳動物由来のBaxタンパク質又はBakタンパク質をコードするDNAをカイコ細胞内で発現可能な状態で含み、
前記DNAは、前記プロモーターによる直接的又は間接的な発現制御を受けるように配置されている細胞死誘導ベクター。 - 部位特異的プロモーター、及び該プロモーターの下流に前記タンパク質をコードするDNAを機能的に連結した、請求項1に記載の細胞死誘導ベクター。
- 部位特異的プロモーター及び該プロモーターの下流に機能的に連結した転写調節因子をコードする遺伝子を含む第1発現ユニット、及び
該転写調節因子の標的プロモーター及び該標的プロモーターの下流に機能的に連結した前記タンパク質をコードするDNAを含む第2発現ユニットから構成される、請求項1に記載の細胞死誘導ベクター。 - 前記転写調節因子をコードする遺伝子がGAL4遺伝子であり、該転写調節因子の標的プロモーターがUASプロモーターである、請求項3に記載の細胞死誘導ベクター。
- 請求項2に記載の細胞死誘導ベクターを含む部位特異的細胞死誘導カイコ系統。
- 転写調節因子の標的プロモーター及び該標的プロモーターの下流に機能的に連結した哺乳動物由来のBaxタンパク質又はBakタンパク質をコードするDNAを含む第2発現ユニットを含む部位特異的細胞死誘導カイコ系統。
- 前記転写調節因子をコードする遺伝子がGAL4遺伝子であり、該転写調節因子の標的プロモーターがUASプロモーターである、請求項6に記載の部位特異的細胞死誘導カイコ系統。
- 部位特異的プロモーター及び該プロモーターの下流に機能的に連結した転写調節因子をコードする遺伝子を含む第1発現ユニットを有する遺伝子組換えカイコ系統と請求項6に記載の部位特異的細胞死誘導カイコ系統とを交配させる工程、及び
前記第1及び第2発現ユニットを有する部位特異的細胞死誘導カイコを選択する工程
を含む部位特異的細胞死誘導カイコの作出方法。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015022652A JP6541173B2 (ja) | 2015-02-06 | 2015-02-06 | 細胞死誘導ベクター及びそれを有する部位特異的細胞死誘導カイコ系統 |
| PCT/JP2016/053468 WO2016125885A1 (ja) | 2015-02-06 | 2016-02-05 | 細胞死誘導ベクター及びそれを有する部位特異的細胞死誘導カイコ系統 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015022652A JP6541173B2 (ja) | 2015-02-06 | 2015-02-06 | 細胞死誘導ベクター及びそれを有する部位特異的細胞死誘導カイコ系統 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016144416A JP2016144416A (ja) | 2016-08-12 |
| JP6541173B2 true JP6541173B2 (ja) | 2019-07-10 |
Family
ID=56564223
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015022652A Active JP6541173B2 (ja) | 2015-02-06 | 2015-02-06 | 細胞死誘導ベクター及びそれを有する部位特異的細胞死誘導カイコ系統 |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP6541173B2 (ja) |
| WO (1) | WO2016125885A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7029898B2 (ja) * | 2017-07-27 | 2022-03-04 | 日機装株式会社 | 光照射装置 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20060123489A1 (en) * | 2004-12-03 | 2006-06-08 | Envivo Pharmaceuticals, Inc. | Sex-specific automated sorting of non-human animals |
| JPWO2007046439A1 (ja) * | 2005-10-18 | 2009-04-23 | 独立行政法人農業生物資源研究所 | 抗体を産生するトランスジェニックカイコとその製造方法 |
| CN102242147B (zh) * | 2011-05-13 | 2012-11-21 | 浙江同点生物科技有限公司 | 家蚕中部丝腺细胞合成分泌狂犬病病毒核蛋白的方法 |
| CN104903445B (zh) * | 2012-12-25 | 2017-09-12 | 国立研究开发法人农业生物资源研究所 | 后部绢丝腺基因表达单元及具有其的转基因绢丝虫 |
| JP6332585B2 (ja) * | 2013-07-11 | 2018-05-30 | 国立研究開発法人農業・食品産業技術総合研究機構 | トランスジェニックカイコを用いた非天然アミノ酸含有タンパク質の製造方法 |
-
2015
- 2015-02-06 JP JP2015022652A patent/JP6541173B2/ja active Active
-
2016
- 2016-02-05 WO PCT/JP2016/053468 patent/WO2016125885A1/ja active Application Filing
Also Published As
| Publication number | Publication date |
|---|---|
| WO2016125885A1 (ja) | 2016-08-11 |
| JP2016144416A (ja) | 2016-08-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10844402B2 (en) | Expression systems | |
| Smith et al. | Testis‐specific expression of the β2 tubulin promoter of Aedes aegypti and its application as a genetic sex‐separation marker | |
| JP6326703B2 (ja) | 外因性遺伝子発現増強剤 | |
| JP6497605B2 (ja) | 雌蚕致死カイコ系統 | |
| EP3395949A1 (en) | Biocontrol | |
| JP6990413B2 (ja) | 遺伝子組換えミノムシ絹糸 | |
| JPWO2014104269A1 (ja) | 後部絹糸腺遺伝子発現ユニット及びそれを有する遺伝子組換え絹糸虫 | |
| US20220098597A1 (en) | Self-Limiting Noctuids | |
| Du et al. | Identification and functional characterization of doublesex gene in the testis of Spodoptera litura | |
| Zhao et al. | Regulation of the gut-specific carboxypeptidase: a study using the binary Gal4/UAS system in the mosquito Aedes aegypti | |
| Sumitani et al. | Establishment of a specific cell death induction system in Bombyx mori by a transgene with the conserved apoptotic regulator, mouse Bcl‐2‐associated X protein (mouse Bax) | |
| Soulavie et al. | hemingway is required for sperm flagella assembly and ciliary motility in Drosophila | |
| Duan et al. | Cre-mediated targeted gene activation in the middle silk glands of transgenic silkworms (Bombyx mori) | |
| Hosoya et al. | A modified Tet‐ON system minimizing leaky expression for cell‐type specific gene induction in medaka fish | |
| Mlih et al. | Integrin–ECM interactions and membrane-associated Catalase cooperate to promote resilience of the Drosophila intestinal epithelium | |
| JP6541173B2 (ja) | 細胞死誘導ベクター及びそれを有する部位特異的細胞死誘導カイコ系統 | |
| Mazock et al. | Transgene rescue identifies an essential function for Drosophila β spectrin in the nervous system and a selective requirement for ankyrin-2–binding activity | |
| JP6436908B2 (ja) | 外因性遺伝子発現ベクター、形質転換体判別マーカー及び形質転換体 | |
| Tsubota et al. | Establishment of transgenic silkworms expressing GAL4 specifically in the haemocyte oenocytoid cells | |
| Long et al. | Highly efficient and inducible DNA excision in transgenic silkworms using the FLP/FRT site-specific recombination system | |
| JP6964843B2 (ja) | バイナリー遺伝子発現システム | |
| Liu et al. | A fluorescent sex-sorting technique for insects with the demonstration in Drosophila melanogaster | |
| KR102114194B1 (ko) | 킬러레드 단백질을 발현하는 실크를 생산하는 형질전환 누에 | |
| Kim et al. | Utilization of the B ombyx mori heat shock protein 70 promoter for screening transgenic silkworms | |
| Yu et al. | Mutation of a palmitoyltransferase ZDHHC18-like gene is responsible for the minute wing mutation in the silkworm (Bombyx mori) |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A712 Effective date: 20160428 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20160824 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170927 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180925 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20181126 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190124 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190312 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190513 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20190528 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20190513 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20190606 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6541173 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |