JP6044540B2 - 保存安定性に優れたs−アデノシル−l−メチオニン含有組成物 - Google Patents
保存安定性に優れたs−アデノシル−l−メチオニン含有組成物 Download PDFInfo
- Publication number
- JP6044540B2 JP6044540B2 JP2013528937A JP2013528937A JP6044540B2 JP 6044540 B2 JP6044540 B2 JP 6044540B2 JP 2013528937 A JP2013528937 A JP 2013528937A JP 2013528937 A JP2013528937 A JP 2013528937A JP 6044540 B2 JP6044540 B2 JP 6044540B2
- Authority
- JP
- Japan
- Prior art keywords
- same
- composition
- methionine
- adenosyl
- additive
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P13/00—Preparation of nitrogen-containing organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid or pantothenic acid
- A61K31/198—Alpha-amino acids, e.g. alanine or edetic acid [EDTA]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7076—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines containing purines, e.g. adenosine, adenylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/06—Fungi, e.g. yeasts
- A61K36/062—Ascomycota
- A61K36/064—Saccharomycetales, e.g. baker's yeast
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/42—Proteins; Polypeptides; Degradation products thereof; Derivatives thereof, e.g. albumin, gelatin or zein
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/146—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1652—Polysaccharides, e.g. alginate, cellulose derivatives; Cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1658—Proteins, e.g. albumin, gelatin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/19—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles lyophilised, i.e. freeze-dried, solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/20—Hypnotics; Sedatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P13/00—Preparation of nitrogen-containing organic compounds
- C12P13/04—Alpha- or beta- amino acids
- C12P13/12—Methionine; Cysteine; Cystine
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/26—Preparation of nitrogen-containing carbohydrates
- C12P19/28—N-glycosides
- C12P19/38—Nucleosides
- C12P19/40—Nucleosides having a condensed ring system containing a six-membered ring having two nitrogen atoms in the same ring, e.g. purine nucleosides
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12R—INDEXING SCHEME ASSOCIATED WITH SUBCLASSES C12C - C12Q, RELATING TO MICROORGANISMS
- C12R2001/00—Microorganisms ; Processes using microorganisms
- C12R2001/645—Fungi ; Processes using fungi
- C12R2001/85—Saccharomyces
- C12R2001/865—Saccharomyces cerevisiae
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- Natural Medicines & Medicinal Plants (AREA)
- Mycology (AREA)
- Genetics & Genomics (AREA)
- General Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Inorganic Chemistry (AREA)
- Alternative & Traditional Medicine (AREA)
- Medical Informatics (AREA)
- Botany (AREA)
- Psychiatry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pain & Pain Management (AREA)
- Immunology (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Vascular Medicine (AREA)
Description
酵素的合成法については、微生物より単離精製したSAMe合成酵素(メチオニンアデノシルトランスフェラーゼ)を用い、アデノシン5’−三リン酸(ATP)とL−メチオニンを基質としてSAMeを酵素的に合成する方法である。この方法は、醗酵法と比べ、SAMeの生成量が多く、菌体からのSAMe抽出操作が必要ないなどの利点がある。しかしながら、酵素の調製が煩雑であること、得られる酵素の活性が微弱であること、ATP分解酵素等の妨害物質を除去する必要があること、さらには、基質であるATPが極めて高価であるなど様々な問題を有し、必ずしも実用的な方法とは成り得なかった。
また、近年の遺伝子工学の発展により、クローン化したSAMe合成酵素遺伝子を用いることによって該酵素の調製がより簡便になり、酵素調製の問題は解決されつつある。しかしながら、依然として高価なATPを基質として使用する必要があるなど、他の実用上の問題は解決されていない。
そこで、本発明者等は、SAMe含有抽出物を利用し、SAMeを高濃度に含有し、かつ安定な状態で長期間保存できる性能的に優れた組成物、及び該組成物を経済的に生産できる方法について鋭意検討した結果、以下に示す項目によって、解決できることを見出し、本発明を完成するに至った。
〔2〕前記微生物が、サッカロマイセス属に属する微生物である、前記〔1〕に記載の組成物。
〔3〕前記サッカロマイセス属に属する微生物がサッカロマイセス・セレビジエである、前記〔2〕に記載の組成物。
〔4〕前記組成物が固体である、前記〔1〕〜〔3〕のいずれかに記載の組成物。
〔5〕前記〔4〕に記載の組成物を用いて成型された成型体。
〔6〕S−アデノシル−L−メチオニンと、カルボキシメチルセルロース、ヒドロキシプロピルセルロース、大豆多糖類、カゼインナトリム及びツェインから選ばれる少なくとも1種の添加物とを含有する組成物の製造方法であって、S−アデノシル−L−メチオニン生産能を有する微生物を培養して得られたS−アデノシル−L−メチオニン含有菌体から抽出されたS−アデノシル−L−メチオニン含有抽出液に、該添加物を、該S−アデノシル−L−メチオニン含有抽出液中のS−アデノシル−L−メチオニンに対する質量比として0.05〜15倍量の範囲で混合し、得られた混合物を乾燥させる、組成物の製造方法。
また、本発明により得られる該SAMe含有組成物は、生体吸収性にも優れる。
以下、本発明について詳細に説明する。
なお、SAMeを含む組成物には、5'−ヌクレオチド、遊離アミノ酸、抗酸化作用を有し肝機能改善に役立つグルタチオン、免疫力の増進作用や整腸作用を有するβ−グルカンや食物繊維などの有用成分が多く含まれており、健康食品等として広く利用されている。
微生物を培養する際に使用する炭素源は、微生物が資化し得るものであれば特に制限はなく、例えば、グルコース、蔗糖、澱粉、廃糖蜜等の炭水化物、エタノール等のアルコール、又は酢酸等の有機酸が挙げられる。窒素源も、使用する微生物が資化し得るものであれば特に制限はなく、例えば、アンモニア、硝酸、尿素等の無機体窒素化合物、又は微生物エキス、麦芽エキス等の有機体窒素化合物を含むものが挙げられる。また、無機塩類としては、リン酸、カリウム、ナトリウム、マグネシウム、カルシウム、鉄、亜鉛、マンガン、コバルト、銅、モリブデン等の塩が用いられる。さらには、SAMeの骨格構成にあずかるメチオニン、アデニン、アデノシルリボヌクレオシドを添加し培養することもできる。
また、菌体内のSAMe含量を高めるには、好気的に培養することが好ましい。培養槽は、通気可能で必要に応じ攪拌できるものであればよく、例えば、機械的攪拌培養槽、エアーリフト式培養槽及び気泡塔型培養槽等を利用することができる。
培地の供給方法は、炭素源、窒素源、各種無機塩類、各種添加剤等を、一括若しくは個別に連続的又は間欠的に供給する。例えば、蔗糖、エタノール等の基質は他の培地成分との混合物として培養槽に供給してもよく、また他の培地成分とは別に独立して培養槽に供給してもよい。
培養液のpH制御は、酸、アルカリ溶液によって行われる。アルカリとしては窒素源として使用されるアンモニア、尿素、又は非窒素系塩基、例えば、苛性ソーダ、苛性カリ等を用いてpH制御するのが望ましい。酸としては無機酸、例えば、リン酸、硫酸、硝酸、又は有機酸が用いられる。なお、無機塩類であるリン酸塩、カリウム塩、ナトリウム塩、硝酸塩等を用いてpH制御することもできる。
SAMeを含有する抽出液を得る方法としては、分離した微生物菌体の分離濃縮物に対して、タンパク質分解酵素、細胞壁溶解酵素などを添加して抽出する方法、微生物中の酵素を利用して自己消化により抽出する方法、高圧分散処理等の高圧粉砕により抽出する方法、鉱酸、有機酸を添加する混合する方法、加熱処理する方法等が挙げられる。
SAMeを含有する抽出液は、SAMeを含有する微生物菌体と比べて、固形分が少なく、水に分散、溶解させ易く、食品、調味料などへ容易に添加することができる。また、SAMe成分の濃縮が可能である。
大豆多糖類は、ヘミセルロースを主成分とする水溶性多糖類であり、ガラクトース、アラビノース、ガラクツロン酸、キシロース、フコース、ラムノース等の糖から構成された多糖類あり、具体的にはフロイント産業株式会社製の市販品(商品名「ヘミロース」)を好適に用いることができる。ツェインとは、トウモロコシ由来のタンパク質であり、該タンパク質加水分解物又はナトリウム塩やカリウム塩等の塩を使用してもよい。本発明において、特定の添加物を用いることで、組成物中のSAMeの保存安定性が向上し、さらにはSAMeの生体吸収性が向上する。本発明で使用する添加物は、食品、化粧品、医薬品用途で汎用されており、安全に使用することができる。これらの添加物は、適宜合成したものを使用してもよいし、市販品を使用してもよい。
乾燥条件としては、噴霧乾燥法では、入口温度210℃以下、出口温度110℃以下にて乾燥させることが望ましい。凍結乾燥法では、最終棚温度30℃以下にて乾燥させることが望ましい。本発明の乾燥組成物は、保存安定性の観点から、その水分含量が5.0質量%以下、好ましくは3.0質量%以下、より好ましくは1.0質量%以下になるようにすることが望ましい。
組成物中のSAMeの含有量としては、組成物の乾燥質量に対して1質量%以上であることが好ましく、3質量%以上であることがより好ましく、8質量%以上であることが更に好ましい。
(a)微生物菌体の培養
前述した公知の培養法に従って、L−メチオニン含有培地(Shiozaki S.,et all, J. Biotechnology, 4, 345-354 (1986))にサッカロマイセス属に属する微生物サッカロマイセス・セレビジエIFO2346を接種し、培養温度27〜29℃で好気的に通気攪拌通気拌しながら6日間培養した。その結果、菌体濃度3.5質量%,SAMe含量205mg/gの微生物菌体培養液18Lを得た。
(b)微生物菌体の集菌
上記の微生物菌体培養液18Lを連続ロータリー型遠心分離器(日立HIMAC CENTRIFUGE CR10B2)で処理し、菌体濃度が乾物換算で18質量%に相当する液状の微生物菌体濃縮物3.4kgを得た。
(c)微生物菌体濃縮物からSAMeを含有する抽出液の抽出
上記の微生物菌体濃縮物3.4kgに50質量%硫酸を添加してpHを3.5に調整した。該微生物菌体濃縮物を50℃に30分間加熱撹拌後、直ちに遠心管に移し替え、遠心分離器(日立HIMAC CENTRIFUGE CR10B2)にて冷却遠心分離処理後、上清液をSAMe含有抽出液として回収した。
上記のSAMe含有抽出液にヒドロキシプロピルセルロース(和光純薬工業株式会社製)(以下、HPCと略す)を、表1に示すように乾燥前SAMe含有抽出液中SAMeに対しての質量比として0.19、1.92、13.46倍量加えて、室温にて30分間攪拌混合し、HPCを添加した液状のSAMe含有組成物を得た。
上記のHPCを添加した液状のSAMe含有組成物を凍結乾燥器(日本真空技術株式会社製)の凍結乾燥用ステンレストレーに流し込み−50℃で凍結した後、最終棚段温度25℃の条件で36時間凍結乾燥した。得られた乾燥組成物(固体)をさらに粉砕することによって、SAMe及びHPCを含有する粉末状の乾燥組成物を得た。
得られた乾燥組成物を密閉ガラス容器中に詰め、40℃、RH75%での加速試験条件下で保存安定性試験を行った。表1に40℃、RH75%での加速保存安定性試験結果を示した。なお、SAMe残存率は、乾燥組成物より過塩素酸を用いた公知の方法でSAMeを抽出し、液体クロマトグラフィーを用いた比較定量法にて実施した。保存後の臭気の有無については5名のパネラーによる官能検査にて求めた。
本発明のSAMe測定では、以下の条件の液体クロマトグラフィーを使用した。
用いられた分析条件:
カラム:ナカライテスク(nacalai tesque)株式会社製、商品名COSMOSIL、4.6φ×100mm
溶離液:0.2M KH2PO4水溶液/メタノール=95/5(質量比)
流速:0.7mL/分、検出器:UV(260nm)、SAMe保持時間:約150秒
SAMe含有抽出液へ添加するHPCを、乾燥前SAMe含有抽出液中SAMeに対しての質量比として0.02倍量加えた以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経て、SAMe及びHPCを含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表1に示す。
実施例1−1〜1−3の(a)から(c)と同様にして得られたSAMe含有抽出液について、(d)の操作にてHPCを該抽出液中SAMeに対する質量比として0.19倍量加える操作を行い、室温にて30分間攪拌混合し、HPCを添加した液状のSAMe含有組成物を得た。
得られたHPCを添加した液状のSAMe含有組成物を微粒子化装置として二流体ノズルを有するミニスプレードライヤBー290(メトローム社製)を用いて、乾燥室の入口温度135℃、出口温度80℃、通液速度1.2g/分の条件にて噴霧乾燥し、SAMe及びHPCを含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表2に示す。
SAMe含有抽出液へ添加する添加物としてカルボキシメチルセルロースを乾燥前SAMe含有抽出液中SAMeに対しての添加物の質量比として0.19倍量加えた以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経て、SAMe及びカルボキシメチルセルロースを含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表1に示す。
SAMe含有抽出液へ添加する添加物を大豆多糖類(フロイント産業社製、製品名「ヘミロース」)に変更した以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経て、SAMe及び大豆多糖類を含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表1、及び表2に示す。
SAMe含有抽出液へ添加する大豆多糖類(フロイント産業社製、製品名「ヘミロース」)を乾燥前SAMe含有抽出液中SAMeに対しての添加物の質量比として0.02倍量加えた以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経て、SAMe及び大豆多糖類を含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表1に示す。
SAMe含有抽出液へ添加する添加物を大豆多糖類(フロイント産業社製、製品名「ヘミロース」)に変更した以外は、実施例1−4と同様に処理して、噴霧乾燥を経て、SAMe及び大豆多糖類を含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表2に示す。
SAMe含有抽出液へ添加物を添加しなかったこと以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経てSAMeを含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び得られた該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表1に示す。
SAMe含有抽出液へ添加物を添加しなかったこと以外は、実施例1−4と同様に処理して、噴霧乾燥を経て、SAMeを含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表2示す。
SAMe含有抽出液へ添加する添加物を、それぞれ表1に示すトレハロース、クエン酸、EDTA、DL−リンゴ酸、ガラクトース又はγ-シクロデキストリンに変更し、該添加物を乾燥前SAMe含有抽出液中SAMeに対しての添加物の質量比として2.31倍量加えた以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経て、SAMe及び添加物を含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表1に示す。
SAMe含有抽出液へ添加する添加物をそれぞれ表1に示すセルロース、ヒドロキシプロピルメチルセルロース、タマリンドガム、又はシェラックに変更し、該添加物を乾燥前SAMe含有抽出液中SAMeに対しての添加物の質量比として0.19倍量加えた以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経て、SAMe及び添加物を含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び密閉ガラス容器中、40℃、RH75%の加速条件下での該組成物の保存安定性試験の結果、官能検査の結果を表1に示す。
SAMe含有抽出液へ添加する添加物をカゼインナトリウムに変更した以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経て、SAMe及びカゼインナトリウムを含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び得られた該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表3、4に示す。
SAMe含有抽出液へ添加するカゼインナトリウムを乾燥前SAMe含有抽出液中SAMeに対しての添加物の質量比として0.02倍量加えた以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経て、SAMe及びカゼインナトリウムを含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表3に示す。
SAMe含有抽出液へ添加する添加物をカゼインナトリウムに変更した以外は、実施例1−4と同様に処理して、噴霧乾燥を経て、SAMe及びカゼインナトリウムを含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表4に示す。
SAMe含有抽出液へ添加する添加物を微結晶性ツェイン(小林香料株式会社製、商品名:小林ツェインDP)に変更した以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経て、SAMe及びツェインを含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び得られた該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表3、4に示す。
SAMe含有抽出液へ添加する微結晶性ツェイン(小林香料株式会社製、商品名:小林ツェインDP)を乾燥前SAMe含有抽出液中SAMeに対しての添加物の質量比として0.02倍量加えた以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経て、SAMe及びツェインを含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表3に示す。
SAMe含有抽出液へ添加する添加物を微結晶性ツェイン(小林香料株式会社製、商品名:小林ツェインDP)に変更した以外は、実施例1−4と同様に処理して、噴霧乾燥を経て、SAMe及びツェインを含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表4に示す。
SAMe含有抽出液へ添加するタ添加物を、それぞれ表3に示す、カゼイン、ゼラチン、ダイズタンパク又はエンドウタンパクに変更し、該添加物を該抽出液中SAMeに対する質量比として2.31倍量加えた以外は、実施例1−1〜1−3と同様に処理して、凍結乾燥を経て、SAMe及び添加物を含有する粉末状の乾燥組成物を得た。該組成物中のSAMe含量、及び該組成物の密閉ガラス容器中、40℃、RH75%の加速条件下での保存安定性試験の結果、官能検査の結果を表3に示す。
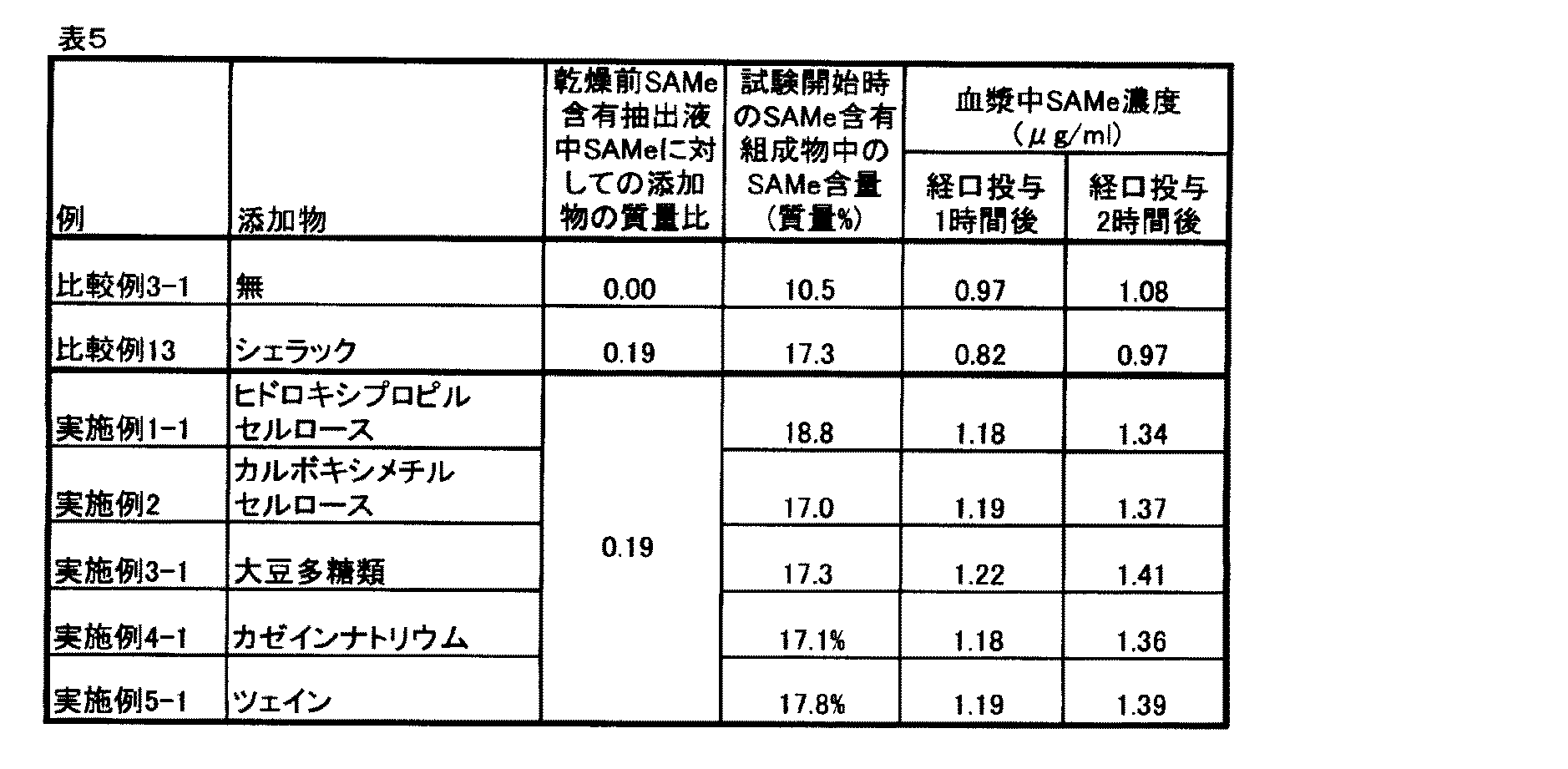
実施例1−1、実施例2、実施例3−1、実施例4−1、実施例5−1、及び比較例13で得られた、SAMe及び添加物を含有する粉末状の乾燥組成物、並びに比較例3−1で得られた、SAMeを含有する粉末状の乾燥組成物について、文献(J of Chromatography B,863,94-100(2008))記載の方法と同様にSD系ラット(雄、8週齢、動物数:各群n=3)を用いて、生体吸収性試験を実施した。
ラットへの粉末状の乾燥組成物の投与量は、SAMeとして300mg/kg−ラットの投与量になる様に粉末状の乾燥組成物を蒸留水へ分散した状態でラットに経口投与し、経口投与後0.5、1、2、3及び5時間後のラットの血液を採取した。採取した血液は速やかに遠心分離し、血漿成分の分離、過塩素酸を用いたSAMe成分の抽出、LC−MS−MS法(Liquid chromatography coupled with mass spectrometry)により分析した。
生体吸収性試験の結果、経口投与2時間後の血漿中SAMe濃度が最も高かった。各粉末状の乾燥組成物の経口投与1時間後及び2時間後の生体吸収性試験の結果を表5に示す。
(LC-MS-MS法)
LC-MS-MS装置:Thermo社製 Accela、LTQ orbitrap Discovery
(HPLC条件)
カラム:ジーエルサイエンス社製 Intersil ODS-3(4.6mm×150mm)
流速:0.5mL/min、カラムオーブン:40℃、検出器:UV(260nm)、SAMe保持時間:約145秒、注入量:10μL
溶離液: 2mmol/Lヘプタフルオロ酪酸水溶液:アセトニトリル=30:70
(MS条件)
Ion Source:ESI
Ion Polarity Mode: Positive
Scan Mode Type:FTフルマス
Resolution:30000
Mass Range:m/z 360−410
Claims (6)
- S−アデノシル−L−メチオニンと、ヒドロキシプロピルセルロース、大豆多糖類、カゼインナトリム及びツェインから選ばれる少なくとも1種の添加物とを含有する組成物であり、S−アデノシル−L−メチオニンが、S−アデノシル−L−メチオニン生産能を有する微生物を培養して得られたS−アデノシル−L−メチオニン含有菌体から抽出されたものであり、該組成物中の該添加物の含有量が、該組成物中のS−アデノシル−L−メチオニンに対する質量比として0.05〜15倍量の範囲である、組成物。
- 前記微生物が、サッカロマイセス属に属する微生物である、請求項1に記載の組成物。
- 前記サッカロマイセス属に属する微生物がサッカロマイセス・セレビジエである、請求項2に記載の組成物。
- 前記組成物が固体である、請求項1〜3のいずれかに記載の組成物。
- 請求項4に記載の組成物を用いて成型された成型体。
- S−アデノシル−L−メチオニンと、ヒドロキシプロピルセルロース、大豆多糖類、カゼインナトリム及びツェインから選ばれる少なくとも1種の添加物とを含有する組成物の製造方法であって、S−アデノシル−L−メチオニン生産能を有する微生物を培養して得られたS−アデノシル−L−メチオニン含有菌体から抽出されたS−アデノシル−L−メチオニン含有抽出液に、該添加物を、該S−アデノシル−L−メチオニン含有抽出液中のS−アデノシル−L−メチオニンに対する質量比として0.05〜15倍量の範囲で混合し、得られた混合物を乾燥させる、組成物の製造方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011176921 | 2011-08-12 | ||
| JP2011176921 | 2011-08-12 | ||
| JP2011176922 | 2011-08-12 | ||
| JP2011176922 | 2011-08-12 | ||
| PCT/JP2012/068492 WO2013024663A1 (ja) | 2011-08-12 | 2012-07-20 | 保存安定性に優れたs-アデノシル-l-メチオニン含有組成物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2013024663A1 JPWO2013024663A1 (ja) | 2015-03-05 |
| JP6044540B2 true JP6044540B2 (ja) | 2016-12-14 |
Family
ID=47714988
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013528937A Active JP6044540B2 (ja) | 2011-08-12 | 2012-07-20 | 保存安定性に優れたs−アデノシル−l−メチオニン含有組成物 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US9700629B2 (ja) |
| EP (1) | EP2742943B1 (ja) |
| JP (1) | JP6044540B2 (ja) |
| KR (1) | KR101645619B1 (ja) |
| CN (1) | CN103841977B (ja) |
| AU (1) | AU2012295986B2 (ja) |
| TW (1) | TW201317249A (ja) |
| WO (1) | WO2013024663A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ITMI20130426A1 (it) * | 2013-03-20 | 2014-09-21 | Gnosis Spa | S-adenosilmetionina sterile ad alto contenuto di isomero attivo per soluzioni iniettabili e procedimento per ottenerla |
| US9884437B2 (en) | 2014-06-20 | 2018-02-06 | Palo Alto Research Center Incorporated | Integral vasculature |
| IT201700074957A1 (it) | 2017-07-04 | 2019-01-04 | Gnosis Spa | Sale di (ss)-adenosil metionina con inositolo esafosfato e procedimento per ottenerlo |
| CN117099949B (zh) * | 2023-08-01 | 2025-07-15 | 百色学院 | 米根霉发酵制备富含s-腺苷甲硫氨酸食品的方法与应用 |
| IT202300027237A1 (it) | 2023-12-19 | 2025-06-19 | Lesaffre & Cie | Formulazioni orosolubili stabili a base di s-adenosil metionina |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4025659A (en) * | 1975-06-06 | 1977-05-24 | Ralston Purina Company | Soy protein/casein coffee whitener composition |
| IT1200589B (it) * | 1985-02-14 | 1989-01-27 | Gibipharma Spa | Derivati naturali attivita farmagologica |
| WO1994005299A1 (fr) | 1992-09-04 | 1994-03-17 | Fuji Kagaku Kogyo Kabushiki Kaisha | Compositions medicinales |
| EP0970948B1 (en) * | 1997-06-25 | 2005-03-09 | Teijin Limited | Vitamin d 3? derivatives and remedies for inflammatory respiratory diseases prepared from the same |
| JP4242475B2 (ja) * | 1998-05-13 | 2009-03-25 | 丸善製薬株式会社 | ビタミンk1組成物およびその製造法 |
| US20030069202A1 (en) * | 2000-06-02 | 2003-04-10 | Kern Kenneth Norman | Compositions, kits, and methods for promoting defined health benefits |
| JP3549197B2 (ja) * | 2001-08-10 | 2004-08-04 | 日清ファルマ株式会社 | ユビキノン含有製剤 |
| JP4592260B2 (ja) | 2003-05-29 | 2010-12-01 | 雪印乳業株式会社 | ラクトフェリン組成物 |
| NZ526350A (en) * | 2003-06-09 | 2004-10-29 | A | Anti-aging compositions comprising an amino acid, vitamin B complex, metal salt and an amino alcohol |
| CN1217002C (zh) | 2003-06-12 | 2005-08-31 | 北京凯因生物技术有限公司 | 酶催化生产腺苷甲硫氨酸的方法 |
| JP2005229812A (ja) | 2004-02-17 | 2005-09-02 | Kohjin Co Ltd | 安定化されたsamを含有する乾燥微生物又は微生物抽出物、及びその製造方法 |
| US20050272687A1 (en) * | 2004-06-08 | 2005-12-08 | Hebert Rolland F | Stable S-adenosyl-l-methionine |
| JP2008012464A (ja) | 2006-07-07 | 2008-01-24 | Fujifilm Corp | S−アデノシルメチオニンの抽出方法 |
| JPWO2008072532A1 (ja) * | 2006-12-07 | 2010-03-25 | 第一三共株式会社 | 貯蔵安定性が改善された医薬組成物 |
| US9200250B2 (en) | 2007-01-25 | 2015-12-01 | Mitsubishi Gas Chemical Company, Inc. | Method for production of dry yeast containing S-adenosyl-L-methionine and having excellent storage stability, product produced by the method, and molded composition of the dry yeast |
| US20090088404A1 (en) * | 2007-01-31 | 2009-04-02 | Methylation Sciences International Srl | Extended Release Pharmaceutical Formulations of S-Adenosylmethionine |
| WO2009081833A1 (ja) | 2007-12-20 | 2009-07-02 | Kaneka Corporation | 安定化された(ss)-s-アデノシル-l-メチオニンを含有する微生物乾燥菌体又は微生物エキス、及びその製造方法 |
| IT1393331B1 (it) | 2009-02-09 | 2012-04-20 | Graal S R L | Composizioni orosolubili e/o effervescenti contenenti almeno un sale di s-adenosilmetionina (same) |
| JP2013503352A (ja) | 2009-08-31 | 2013-01-31 | エムバイオ ダイアグノスティクス,インコーポレイティド | 統合されたサンプル調製及び検体検出 |
| EP2557151B1 (en) | 2010-04-07 | 2017-10-04 | Mitsubishi Gas Chemical Company, Inc. | S-adenosyl-l-methionine-containing dry yeast composition with excellent storage stability and process for producing same |
-
2012
- 2012-07-20 US US14/238,029 patent/US9700629B2/en active Active
- 2012-07-20 EP EP12824083.5A patent/EP2742943B1/en not_active Not-in-force
- 2012-07-20 KR KR1020147003560A patent/KR101645619B1/ko active Active
- 2012-07-20 JP JP2013528937A patent/JP6044540B2/ja active Active
- 2012-07-20 AU AU2012295986A patent/AU2012295986B2/en not_active Ceased
- 2012-07-20 CN CN201280039382.8A patent/CN103841977B/zh active Active
- 2012-07-20 WO PCT/JP2012/068492 patent/WO2013024663A1/ja not_active Ceased
- 2012-08-03 TW TW101127983A patent/TW201317249A/zh unknown
Also Published As
| Publication number | Publication date |
|---|---|
| EP2742943A1 (en) | 2014-06-18 |
| EP2742943A4 (en) | 2015-01-28 |
| US20140213542A1 (en) | 2014-07-31 |
| AU2012295986B2 (en) | 2016-12-01 |
| JPWO2013024663A1 (ja) | 2015-03-05 |
| WO2013024663A1 (ja) | 2013-02-21 |
| US9700629B2 (en) | 2017-07-11 |
| CN103841977A (zh) | 2014-06-04 |
| TWI563000B (ja) | 2016-12-21 |
| CN103841977B (zh) | 2016-04-20 |
| KR101645619B1 (ko) | 2016-08-05 |
| EP2742943B1 (en) | 2016-11-16 |
| AU2012295986A1 (en) | 2014-03-06 |
| KR20140063596A (ko) | 2014-05-27 |
| TW201317249A (zh) | 2013-05-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4479932B2 (ja) | 保存安定性に優れたs−アデノシル−l−メチオニン含有乾燥酵母の製造方法、その製造物及びその成型された組成物 | |
| JP6044540B2 (ja) | 保存安定性に優れたs−アデノシル−l−メチオニン含有組成物 | |
| JP5974891B2 (ja) | 保存安定性に優れたs−アデノシル−l−メチオニン含有乾燥酵母組成物及びその製造方法 | |
| CN101437934B (zh) | 含s-腺苷-l-甲硫氨酸的干燥酵母的制备方法以及口服用组合物 | |
| JP5136409B2 (ja) | 保存安定性に優れたs−アデノシル−l−メチオニン含有乾燥酵母の製造方法、その製造物及び経口摂取用組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150508 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20150508 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160315 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20160510 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20161018 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20161031 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 6044540 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |