JP5864262B2 - 化学および/または生化学反応のための光学システム - Google Patents
化学および/または生化学反応のための光学システム Download PDFInfo
- Publication number
- JP5864262B2 JP5864262B2 JP2011544920A JP2011544920A JP5864262B2 JP 5864262 B2 JP5864262 B2 JP 5864262B2 JP 2011544920 A JP2011544920 A JP 2011544920A JP 2011544920 A JP2011544920 A JP 2011544920A JP 5864262 B2 JP5864262 B2 JP 5864262B2
- Authority
- JP
- Japan
- Prior art keywords
- light
- reaction vessel
- reaction
- spectrum
- excitation
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000006243 chemical reaction Methods 0.000 title claims description 154
- 230000003287 optical effect Effects 0.000 title claims description 59
- 238000005842 biochemical reaction Methods 0.000 title claims description 14
- 239000000126 substance Substances 0.000 title claims description 14
- 230000005284 excitation Effects 0.000 claims description 86
- 238000001228 spectrum Methods 0.000 claims description 81
- 230000000873 masking effect Effects 0.000 claims description 33
- 238000001514 detection method Methods 0.000 claims description 30
- 238000003752 polymerase chain reaction Methods 0.000 claims description 30
- 230000005855 radiation Effects 0.000 claims description 20
- 150000007523 nucleic acids Chemical class 0.000 claims description 18
- 239000000523 sample Substances 0.000 claims description 16
- 108020004707 nucleic acids Proteins 0.000 claims description 15
- 102000039446 nucleic acids Human genes 0.000 claims description 15
- 239000003153 chemical reaction reagent Substances 0.000 claims description 14
- 238000000034 method Methods 0.000 claims description 12
- 239000007850 fluorescent dye Substances 0.000 claims description 8
- 108020005187 Oligonucleotide Probes Proteins 0.000 claims description 4
- 230000000694 effects Effects 0.000 claims description 4
- 239000002751 oligonucleotide probe Substances 0.000 claims description 4
- 230000008569 process Effects 0.000 claims description 4
- 108091028043 Nucleic acid sequence Proteins 0.000 claims description 3
- 108060002716 Exonuclease Proteins 0.000 claims description 2
- 238000003491 array Methods 0.000 claims description 2
- 102000013165 exonuclease Human genes 0.000 claims description 2
- 238000012546 transfer Methods 0.000 claims description 2
- 239000000835 fiber Substances 0.000 description 59
- 239000006185 dispersion Substances 0.000 description 18
- 239000013307 optical fiber Substances 0.000 description 16
- 238000010586 diagram Methods 0.000 description 12
- 239000000975 dye Substances 0.000 description 11
- 230000003595 spectral effect Effects 0.000 description 11
- 238000005259 measurement Methods 0.000 description 10
- 238000004458 analytical method Methods 0.000 description 9
- 230000003321 amplification Effects 0.000 description 8
- 238000003199 nucleic acid amplification method Methods 0.000 description 8
- 238000010438 heat treatment Methods 0.000 description 7
- 239000011541 reaction mixture Substances 0.000 description 5
- 230000004044 response Effects 0.000 description 5
- 230000008901 benefit Effects 0.000 description 4
- 239000011521 glass Substances 0.000 description 4
- 230000008859 change Effects 0.000 description 3
- 238000012937 correction Methods 0.000 description 3
- 239000012530 fluid Substances 0.000 description 3
- 238000012545 processing Methods 0.000 description 3
- 108020004414 DNA Proteins 0.000 description 2
- 238000000137 annealing Methods 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 238000009833 condensation Methods 0.000 description 2
- 230000005494 condensation Effects 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 238000004925 denaturation Methods 0.000 description 2
- 230000036425 denaturation Effects 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 238000010222 PCR analysis Methods 0.000 description 1
- 208000034809 Product contamination Diseases 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 238000007664 blowing Methods 0.000 description 1
- 230000005465 channeling Effects 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 238000000695 excitation spectrum Methods 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- 238000005286 illumination Methods 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 238000009830 intercalation Methods 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 238000003909 pattern recognition Methods 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000013139 quantization Methods 0.000 description 1
- 238000005057 refrigeration Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000035939 shock Effects 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 229910052724 xenon Inorganic materials 0.000 description 1
- FHNFHKCVQCLJFQ-UHFFFAOYSA-N xenon atom Chemical compound [Xe] FHNFHKCVQCLJFQ-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J19/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J19/0046—Sequential or parallel reactions, e.g. for the synthesis of polypeptides or polynucleotides; Apparatus and devices for combinatorial chemistry or for making molecular arrays
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/25—Colour; Spectral properties, i.e. comparison of effect of material on the light at two or more different wavelengths or wavelength bands
- G01N21/251—Colorimeters; Construction thereof
- G01N21/253—Colorimeters; Construction thereof for batch operation, i.e. multisample apparatus
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/6452—Individual samples arranged in a regular 2D-array, e.g. multiwell plates
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/08—Optical fibres; light guides
- G01N2201/0826—Fibre array at source, distributing
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/08—Optical fibres; light guides
- G01N2201/0833—Fibre array at detector, resolving
Landscapes
- Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Pathology (AREA)
- Immunology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Investigating Or Analysing Materials By The Use Of Chemical Reactions (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Description
PCRの間に、反応混合物に存在する核酸を比較的高温(例えば95℃)で変性し(変性)、次に、短いオリゴヌクレオチドプライマーが一本鎖の標的核酸に結合する温度(例えば55℃)に反応混合物を冷却する(アニーリング)というステップからなるサイクルを一連繰り返すことにより、特定の標的核酸が増幅される。その後、プライマーを、例えば72℃でポリメラーゼ酵素を使用して伸長させ(伸長)、元の核酸配列を複製する。変性、アニーリングおよび伸長のサイクルを繰り返した結果、サンプルの中に存在する標的核酸の量が指数関数的に増加する。
合わせる概念は、「リアルタイム」PCRとして知られるようになっている。
光分散装置は、プリズムまたは回折格子のような光発散装置であってもよい。
1実施形態では、光検出装置は、開口からの光の分散スペクトルが生成される平面と、分散スペクトル内の特定のスペクトルを検出する1または複数の検出器とを備える。
装置は、マスキング要素の小開口からの光を光検出装置まで案内する複数の光導波管を備えてもよい。
光導波管と、光検出装置の異なる部分の間との間にはフィルタが配置され、各フィルタは、光の異なるスペクトルを、光検出装置のそれぞれの部分へ通過させる。
第2態様によれば、本発明は、複数の反応容器のうちの少なくとも1つの反応容器で起こる化学または生化学反応から生じた光のスペクトルを検出する装置であって、
各反応容器は、光が発出し得る放射領域を有する受容部分を備え、
前記装置は、
光が通過可能な、各反応容器に隣接する開口を備えたマスキング要素と、
マスキング要素の開口からの光を、各導波管からの光を分散スペクトルへ分散する光分散装置まで案内する複数の光導波管と、
光の分散スペクトルの複数のスペクトルをほぼ同時に検出する光検出装置と、
を備えた装置を提供する。
装置はさらに、光分散装置に隣接して所定のアレイに配列された複数の出力開口を有する出力アレイ要素を備えてもよく、各光導波管は、マスキング要素のそれぞれの開口からの光を受け取るように拘束された第1の端部と、光を光分散装置へ向けるようにアレイ要素中のそれぞれの開口で拘束された第2端部とを備える。
任意の実施形態の装置は、各反応容器に隣接するマスキング要素中のさらなる小開口と、励起光源からの励起光を各反応容器まで案内する励起光源との間に配置された各反応容器に対するさらなる光導波管をさらに備えてもよい。
好ましくは、放射領域は受容部分の上部にあるが、受容部分の側部または受容部分の底部にあってもよい。
別の態様では、本発明は、複数の反応容器のアレイの複数の反応容器で起こる化学または生化学反応から生じた光のスペクトルを検出する装置であって、
各反応容器は、光が発出し得る放射領域を有する受容部分を備え、
前記装置は、前記放射領域からの光を、導波管から分散スペクトルへと光を分散させる光分散装置まで案内する、各反応容器に対する少なくとも1つの光導波管と、
前記光の分散スペクトル中の複数の複数のスペクトルをほぼ同時に検出する光検出装置と、
励起光を反応容器の受容部分へ提供する少なくとも1つの励起装置と、
を備える装置を提供する。
励起装置は、反応容器の受容部分内または反応容器の受容部分に隣接して配置された励起光源を有する。
光分散装置は、プリズムまたは回折格子を備えてよい。
好ましくは、放射領域は、受容部分の上部、および/または受容部分の側部、および/または受容部分の底部にある。
複数の反応容器が、48、96または384ウェルプレートのようなマルチウェルプレート内に含まれてもよい。
特定のスペクトルは反応容器内の特定の試薬または特定の試薬の状態の特性であってもよく、および/または反応中に存在する蛍光団の単一の種に由来してもよい。
挿入染料等の、核酸が間に挿入された蛍光団、
標識されたハイブリダイゼーションプローブ等の、核酸とハイブリダイズする蛍光団、
標識された消化プローブ等の、PCRプロセスにより修飾される蛍光団、
蛍光性の標識プローブ等の、自身の間の蛍光エネルギー伝達を提供する蛍光団、および
他の蛍光プローブ、
からなる群から選択された1または複数の蛍光団であってよい。
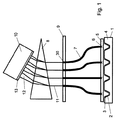
まず図1に目を向けると、反応容器3が中に設けられた多くのウェル2を備えたマルチウェルからなるアレイ1が示される。アレイ1は従来のそのようなアレイと同様に、任意の数のウェル、例えば48個、96個または384個のウェルを有してよい。アレイ1は、当業者に周知のように、サーマルサイクラーのヒータブロック4に収容されてもよい。
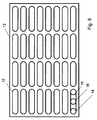
各反応容器からの光を案内し、これをプリズム8に向かって所定の配列で誘導することは明白である。図5に最も良く示されるように、開口30の所定の配列の配置は、反応容器3の幅が長さとほぼ同じである場合には概ね正方形である大きな配列からの光の配列を、ファイバの端部が別の寸法(図5では水平)よりもある寸法(図5では垂直)に共に密接に詰まるような配列に、効果的に再配置する。所望の場合、抵抗素子を通じて電流を流すことにより加熱されるマスキングプレート5を提供してもよく、したがって、所望の場合、マスキングプレート5は加熱蓋として機能する。この場合、ファイバは好ましくは、加熱蓋に要求される温度に対して耐性であるように選択される。
、例えば、4×の利得がイメージの偶数列に使用され、8×の利得設定が奇数列に使用される場合、スペクトル画像は、より低い利得画像が飽和でより高い最大の光源レベルを有し、より高い利得画像が低い光レベルでより高い精度を提供する、異なる利得レベルの2つの半分の解像度画像として有効に得られる。別の例は、Aptina/Micron MT9V024イメージセンサであり、このセンサでは画像を多くの長方形領域に分割することが可能であり、各長方形領域は個々のデジタル利得および利得制御設定を有することが可能である。領域はスペクトル画像と一致するように配置され、スペクトルの異なる領域に対して異なる利得設定を与え、従って異なる波長領域に対して異なる利得設定を与える場合があるため、スペクトル画像は異なる領域に異なる利得を有するセンサに特に適している。これを用いて、各領域に対して最良のSNRと最小の量子化ノイズを与えるように異なる強さのレベルを有するスペクトルの領域を得ることが可能である。
レイと検出器の間に配置され、上に説明したように発せられた光が再配置される場合、生じるイメージは直接画像よりも小さく、このため画像全体(すなわちアレイ中のすべての容器からの光)がプリズムの中および検出器の上を通過することが可能となる。これは、ウェルのスペクトルが重なりなく分散されるのに必要な空間を残すために、生じた画像の示す発光がより少ない場合であっても当てはまる(例えば、システムは照射領域の約10分の1しか実際に有しないかもしれない)。
1は、励起受容端で一つに結合されてよく、これにより光を励起ファイバ31の中に誘導することがより容易になる。これは穿孔プレート35であってもよいが、単にファイバを略六角形に詰めた束にまとめる方がより容易であることが多いため、穿孔プレート35は必ずしも必要ではない。
33であってもよい。LED 32および33はLED 32および33の両方からの励起光を組み合わせて、かつそれをホモジナイザ36(ほぼ六角形のプリズムまたはガラスシリンダ)に向けるようにダイクロイックミラー34の両側に配置される。ダイクロイックミラー34は、LED 32からの青色光を伝達し、LED 33からの緑信号をホモジナイザへ反射させ、ホモジナイザ内で励起光を複数回反射することにより各励起導波管のより一様な照射を生じる。この組み合わせにより、励起ファイバ束の研摩された端部の空間的に均質な照明が生じ、その結果、反応容器3はかなり等しい励起を受け取る。ダイクロイックミラー34を両方のLEDからの光をファイバに向ける他の手段と取り替えてもよく、それは例えばY字型導波管であってもよいし、あるいは両方の光に対して角度をなした複数のLEDを単に備えてファイバの中に角度をなして光を向けることでもよいことに留意すべきである、
1実施形態は、1つのフェルール当たり1つの励起および1つの発光を有する複数の円筒形の金属フェルールに装着された、16対の放射/励起ファイバを有してもよい。その場合、フェルールは、使用のために従来の加熱蓋の孔に配置することが可能である。約110℃の加熱蓋との接触に耐えるよう、ファイバは耐熱性プラスチックから形成される。
おけるスペクトル自体に対する強度を与える。種々の変換手段があるが、単純で適切な方法は、スペクトル領域の各垂直カラムのピクセルをすべて平均して、垂直方向でスペクトルの中心のより明るいピクセルにより重きを置くことである。その後、各カラム平均がそのカラムの強度(すなわち読み取り値のチャネル)になる。補正の最終段階は、画像のそのカラムに分散された実際の波長にチャネルをマッピングすることであろう。これは、プリズムの分散する挙動のモデル化か既知のスペクトルの測定により行うことが可能であるが、スペクトルは波長ではなくチャネルで比較することができるため、これは必ずしも必要だとは限らない。
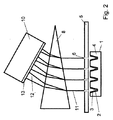
減少する。図12の実施形態に示されるように、隣接する各毛細管40に隣接して、適当な励起光の発光ダイオード(LED)44が提供されてもよい。図13に示される他の実施形態では、励起光が先の実施形態と同じ方法で提供され、励起光32および33の1または複数の供給源から毛細管40に励起光をもたらすために励起ファイバ31が使用される。
、ファイバがブロック4を垂直方向に通過しているが、場合により、ファイバの垂直方向の部分はブロックの外部にあるようにすることが可能であることが理解される。例えば、複数のウェルからなる1つの列を有するブロックでは、途中に他のウェルがないため、ファイバは単にブロックの「側面」からウェルを水平に通過すればよい。複数のウェルからなる2つの列を備えた取付部も明らかに同様に配置されることができ、ファイバは取付部の2つのより長い垂直方向の側面から入る。
Claims (17)
- 少なくとも1つの反応容器で起こる化学または生化学反応から生じた光のスペクトルを検出する装置であって、
前記装置は、複数の反応容器と、マスキング要素と、複数の光導波管と、光検出装置と、さらなる複数の光導波管とを備え、
前記複数の反応容器の各反応容器は、内部空間を有する受容部分を備え、前記内部空間において前記化学または生化学反応が起こるとともに該反応が起こるときに前記内部空間において前記光が生成され、該反応容器は、前記反応が起こるときに密閉されるとともに、生成された光が発出し得る放射領域を有しており、
前記マスキング要素は、前記放射領域のそれぞれを通じて発出される生成された光が通過可能な少なくとも1つの開口が各反応容器に隣接して配置される複数の開口のアレイを備え、各開口は、前記反応容器のそれぞれの前記放射領域よりも小さく、
前記複数の光導波管は、各反応容器に対し少なくとも1つの光導波管を含んでおり、各光導波管は、前記マスキング要素の前記複数の開口のアレイのそれぞれの開口からの光を案内するものであり、
前記光検出装置は、光が内部で生成される全ての反応容器に対する前記複数の光導波管により案内される光を同時に受け取るとともに該受け取った光の複数のスペクトルの少なくとも一部を検出するものであり、
前記さらなる複数の光導波管の各さらなる光導波管は、各反応容器に隣接する前記マスキング要素中のさらなる開口と励起光源との間において各反応容器に対し配置され、前記励起光源からの励起光を前記各反応容器の前記内部空間に案内するものである、装置。 - マスキング要素は、1つの反応容器当たり少なくとも2つの開口を有し、複数の光導波管の各々は、前記生成された光をそれぞれの開口から光検出装置まで案内し、1つの反応容器当たり1つの導波管が、前記生成された光の1つの特定のスペクトルの検出のために光検出装置のある部分まで前記生成された光を案内し、1つの反応容器当たりの別の導波管が、前記生成された光の1つの特定のスペクトルの検出のために光検出装置の別の部分まで前記生成された光を案内する、請求項1に記載の装置。
- 光検出装置の異なる部分と前記光導波管との間に配置されたフィルタをさらに備え、各フ
ィルタは、光の異なるスペクトルを、光検出装置のそれぞれの部分へ通過させる請求項2に記載の装置。 - 同じであっても異なっていてもよいスペクトルの励起光を提供可能な複数の励起光源を備え、各励起光源からの励起光は、1または複数のさらなる光導波管を通じて反応容器の各々に案内される請求項1〜3のいずれか1項に記載の装置。
- 前記少なくとも1つの反応容器が概ねテーパ形状に形成されている請求項1〜3のいずれか1項に記載の装置。
- 前記少なくとも1つの反応容器が毛細管により形成される請求項1〜3のいずれか1項に記載の装置。
- 前記放射領域が受容部分の上部にある請求項1〜3のいずれか1項に記載の装置。
- 前記放射領域が受容部分の側部にある請求項1〜3のいずれか1項に記載の装置。
- 前記放射領域が受容部分の底部にある請求項1〜3のいずれか1項に記載の装置。
- 前記マスキング要素が、反応容器のアレイが装着されるヒータブロックにより提供される請求項9に記載の装置。
- 光検出装置はCCDまたはCMOS検出器を有する請求項1〜3のいずれか1項に記載の装置。
- 複数の反応容器がマルチウェルプレート内に含まれる請求項1〜3のいずれか1項に記載の装置。
- 前記マルチウェルプレートを保持するヒータブロックを有するサーマルサイクラーをさらに備える請求項12に記載の装置。
- 特定のスペクトルは反応容器内の特定の試薬または特定の試薬の状態の特性である請求項1または2に記載の装置。
- 特定のスペクトルは、反応中に存在する蛍光団の単一の種に由来する請求項1または2に記載の装置。
- 化学または生化学反応は少なくとも1つの蛍光団の存在下で行われたポリメラーゼ連鎖反応(PCR)であり、該少なくとも1つの蛍光団は、
核酸の間に挿入された蛍光団、
核酸とハイブリダイズする蛍光団、
PCRプロセスにより修飾される蛍光団、
自身の間の蛍光エネルギー伝達を提供する蛍光団、および
他の蛍光プローブ、
からなる群から選択された1または複数の蛍光団であってよい請求項1〜3のいずれか1項に記載の装置。 - 前記蛍光団は、PCRの標的核酸配列に特異的にハイブリダイズする第1のオリゴヌクレオチドプローブに取り付けられた蛍光標識であり、
第1のオリゴヌクレオチドプローブは、プローブ上で同時に存在する場合に前記蛍光標
識と蛍光エネルギーを交換可能な第2の蛍光団を備え、
反応の伸長期の間に標的核酸に結合した任意の第1のプローブを消化するために、5’−3’エキソヌクレアーゼ活性を有するポリメラーゼがPCRに使用される、請求項16に記載の装置。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US14339109P | 2009-01-08 | 2009-01-08 | |
| US61/143,391 | 2009-01-08 | ||
| PCT/GB2010/000028 WO2010079338A2 (en) | 2009-01-08 | 2010-01-08 | Optical system for chemical and/or biochemical reactions |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015251451A Division JP2016095315A (ja) | 2009-01-08 | 2015-12-24 | 化学および/または生化学反応のための光学システム |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012514747A JP2012514747A (ja) | 2012-06-28 |
| JP2012514747A5 JP2012514747A5 (ja) | 2013-02-28 |
| JP5864262B2 true JP5864262B2 (ja) | 2016-02-17 |
Family
ID=42316903
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011544920A Active JP5864262B2 (ja) | 2009-01-08 | 2010-01-08 | 化学および/または生化学反応のための光学システム |
| JP2015251451A Pending JP2016095315A (ja) | 2009-01-08 | 2015-12-24 | 化学および/または生化学反応のための光学システム |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015251451A Pending JP2016095315A (ja) | 2009-01-08 | 2015-12-24 | 化学および/または生化学反応のための光学システム |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US10029227B2 (ja) |
| EP (3) | EP2376896B1 (ja) |
| JP (2) | JP5864262B2 (ja) |
| CN (1) | CN102341694B (ja) |
| CA (1) | CA2749247A1 (ja) |
| DE (1) | DE202010018011U1 (ja) |
| DK (1) | DK2584344T3 (ja) |
| ES (2) | ES2875831T3 (ja) |
| WO (1) | WO2010079338A2 (ja) |
Families Citing this family (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2875831T3 (es) | 2009-01-08 | 2021-11-11 | It Is Int Ltd | Sistema óptico para reacciones químicas y/o bioquímicas |
| DE102010010741A1 (de) * | 2010-03-09 | 2011-09-15 | Beckman Coulter, Inc. | Lichtleitervorrichtung zum Abstrahlen und Empfangen von Licht, System, Verfahren und Computerprogrammprodukt |
| GB201005704D0 (en) * | 2010-04-06 | 2010-05-19 | It Is Internat Ltd | Improvements in systems for chemical and/or biochemical reactions |
| EP3151015A1 (en) * | 2010-11-15 | 2017-04-05 | F. Hoffmann-La Roche AG | Instrument and method for the automated thermal treatment of liquid samples |
| CN102645276A (zh) * | 2011-02-16 | 2012-08-22 | 台湾超微光学股份有限公司 | 光谱感测设备、系统及方法 |
| EP2525211B1 (en) | 2011-05-16 | 2018-01-03 | F. Hoffmann-La Roche AG | Instrument and method for detecting analytes |
| JP5883314B2 (ja) * | 2011-09-02 | 2016-03-15 | 日本インスツルメンツ株式会社 | 還元気化水銀測定装置 |
| EP2581728B1 (en) * | 2011-10-10 | 2013-09-18 | CYCLERtest B.V. | Calibration device for a thermal cycler |
| US9551030B2 (en) * | 2012-06-17 | 2017-01-24 | Pacific Biosciences Of California, Inc. | Filter architecture for analytical devices |
| TWI458828B (zh) * | 2012-07-18 | 2014-11-01 | Univ Nat Pingtung Sci & Tech | Droplet type high throughput thermal cycling system |
| EP2883039A1 (en) * | 2012-08-10 | 2015-06-17 | Streck Inc. | Real-time optical system for polymerase chain reaction |
| CN105008878B (zh) * | 2012-12-05 | 2017-09-19 | 吉恩波克公司 | 光学探询器件 |
| SG11201506481QA (en) | 2013-02-22 | 2015-09-29 | Life Technologies Corp | Optical systems and methods for biological analysis |
| CA2916990C (en) | 2013-06-28 | 2023-05-23 | Streck, Inc. | Devices for real-time polymerase chain reaction |
| SG11201602873XA (en) | 2013-10-14 | 2016-05-30 | Agency Science Tech & Res | Non-motorized optical multiplexing for the simultaneous detection of dna target amplicons in a polymerase chain reaction solution |
| GB2594163B (en) * | 2014-04-04 | 2022-01-12 | It Is International Ltd | Biochemical reaction system |
| GB2591198B (en) | 2014-04-04 | 2021-10-27 | It Is Int Ltd | Biochemical reaction system |
| CN105092544A (zh) * | 2014-05-12 | 2015-11-25 | 绍兴安尼特微电子科技有限公司 | 一种荧光定量pcr检测仪光学激发和检测系统 |
| US10908083B2 (en) | 2015-02-02 | 2021-02-02 | Hitachi High-Tech Corporation | Multicolor fluorescence analysis device |
| DE102015003019A1 (de) | 2015-03-06 | 2016-09-08 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Verfahren und Vorrichtung zur optischen Detektion einer Bewegung in einer biologischen Probe mit räumlicher Ausdehnung |
| DE102016200271A1 (de) | 2016-01-13 | 2017-07-13 | Institut Dr. Foerster Gmbh & Co. Kg | Vorrichtung zur Erzeugung und Messung einer Emission |
| US20170266668A1 (en) * | 2016-03-15 | 2017-09-21 | Abbott Laboratories | Nucleic Acid Amplification and Detection Devices, Systems and Methods |
| FR3051251B1 (fr) * | 2016-05-10 | 2018-06-15 | Commissariat A L'energie Atomique Et Aux Energies Alternatives | Systeme d'observation d'une plaque a puits |
| SE539770C2 (en) * | 2016-06-10 | 2017-11-21 | Bomill Ab | A detector system comprising a plurality of light guides and a spectrometer comprising the detector system |
| CH712735A1 (de) * | 2016-07-22 | 2018-01-31 | Tecan Trading Ag | Pipettiervorrichtung mit einem Flüssigkeitsvolumensensor und Flüssigkeitsbearbeitungssystem. |
| JP6747192B2 (ja) * | 2016-09-07 | 2020-08-26 | 株式会社島津製作所 | 遺伝子増幅装置 |
| CN106770086A (zh) * | 2016-11-24 | 2017-05-31 | 北京旌准医疗科技有限公司 | 一种实时荧光定量pcr仪的荧光检测方法及系统 |
| US20180156717A1 (en) * | 2016-12-05 | 2018-06-07 | Bill & Melinda Gates Foundation | Multi-test assay systems and methods of using the same |
| DE102016225817B4 (de) * | 2016-12-21 | 2019-07-04 | Bayer Pharma Aktiengesellschaft | Verfahren und System für Messungen im Hochdurchsatz-Screening mit hoher Zeitauflösung |
| JP6904131B2 (ja) * | 2017-07-21 | 2021-07-14 | 株式会社島津製作所 | 遺伝子測定装置 |
| CN107741400B (zh) * | 2017-11-15 | 2024-01-26 | 苏州雅睿生物技术股份有限公司 | 一种ivd体外检测设备的样本检测系统 |
| CN108007564B (zh) * | 2017-11-17 | 2018-10-26 | 浙江大学 | 一种大动态范围光电信号测量系统及测量方法 |
| DE102017223851B4 (de) * | 2017-12-28 | 2020-08-06 | Biochip Systems GmbH | Sensoranordnung zur Detektion wenigstens einer stofflichen Eigenschaft einer Probe sowie Mikrotiter-Platte mit einer Vielzahl von Sensoranordnungen |
| CN108181239B (zh) * | 2018-02-07 | 2023-09-12 | 张哲夫 | 一种多通道荧光定量pcr仪的光学系统 |
| DE102018202588A1 (de) * | 2018-02-21 | 2019-08-22 | Robert Bosch Gmbh | Optische Sensorvorrichtung sowie ein Verfahren zur Herstellung einer optischen Sensorvorrichtung |
| SG10201801853WA (en) * | 2018-03-02 | 2019-10-30 | Delta Electronics Int’L Singapore Pte Ltd | Portable multi-color fluorescence detection device |
| US10935492B2 (en) | 2018-04-13 | 2021-03-02 | Applied Materials, Inc. | Metrology for OLED manufacturing using photoluminescence spectroscopy |
| DE102018111033A1 (de) * | 2018-05-08 | 2019-11-14 | Byonoy Gmbh | Transmissionsvorrichtung zur Untersuchung von Proben in Kavitäten einer Mikrotiterplatte und Verfahren zum Untersuchen von Proben in Kavitäten einer Mikrotiterplatte mittels Transmission |
| JP6688342B2 (ja) * | 2018-07-06 | 2020-04-28 | 日本板硝子株式会社 | 反応処理装置 |
| CN112423883A (zh) | 2018-07-12 | 2021-02-26 | 卢米耐克斯公司 | 用于进行可变样品制备和分析过程的系统和方法 |
| DE102018212489A1 (de) * | 2018-07-26 | 2020-01-30 | Implen GmbH | Vorrichtung für eine lichtspektroskopische Analyse |
| TWI674413B (zh) * | 2018-10-31 | 2019-10-11 | 致茂電子股份有限公司 | 探針對準設備 |
| JP7497186B2 (ja) * | 2019-09-03 | 2024-06-10 | Tianma Japan株式会社 | 蛍光偏光測定システム |
| CN110967324A (zh) * | 2019-10-14 | 2020-04-07 | 广东省测试分析研究所(中国广州分析测试中心) | 一种多通道实时荧光检测仪的光学检测装置 |
| WO2021074970A1 (ja) * | 2019-10-15 | 2021-04-22 | 株式会社日立ハイテク | 核酸試料処理装置および核酸試料処理方法 |
| DE102019128546A1 (de) * | 2019-10-22 | 2021-04-22 | Byonoy Gmbh | Transmissionsvorrichtung zur Untersuchung von Proben in Kavitäten einer Mikrotiterplatte und Verfahren zum Untersuchen von Proben in Kavitäten einer Mikrotiterplatte mittels Transmission |
| JP7233385B2 (ja) * | 2020-01-20 | 2023-03-06 | 日本板硝子株式会社 | 反応処理装置 |
| DE102020108957B4 (de) | 2020-03-31 | 2021-10-07 | Otto-Von-Guericke-Universität Magdeburg | Vorrichtung, Verfahren und Computerprogramm zur Fluoreszenzmessung |
| WO2021232135A1 (en) * | 2020-05-19 | 2021-11-25 | S.M. Research Inc. | A random access real-time quantitative polymerase chain reaction (qpcr) reactor system |
| CN112945869B (zh) * | 2021-02-01 | 2021-11-16 | 杭州赛基生物科技有限公司 | 智慧医院液体试样检测试剂盒用膜载体、试剂盒及膜载体制造方法 |
| CN113607676B (zh) * | 2021-08-04 | 2022-04-05 | 淮北师范大学 | 基于异形比色皿和近红外图像的牛奶成分快速检测方法 |
| CN114480111A (zh) * | 2022-02-15 | 2022-05-13 | 深圳阿斯克医疗有限公司 | 一种实时荧光定量pcr仪 |
| DE102023104746A1 (de) | 2023-02-27 | 2024-08-29 | Deutsches Zentrum für Luft- und Raumfahrt e.V. | Detektorvorrichtung zum erfassen von fluoreszenzlicht |
Family Cites Families (48)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US615674A (en) * | 1898-12-13 | Richard beasley browne | ||
| JPH0619321B2 (ja) | 1986-06-27 | 1994-03-16 | 東ソー株式会社 | マイクロプレ−ト用吸光度測定装置 |
| JP2622567B2 (ja) | 1986-11-26 | 1997-06-18 | リシュブルーク・ジョン | 高感度光学的イメージ装置 |
| JPS63298137A (ja) | 1987-05-29 | 1988-12-05 | Soken:Kk | イメ−ジファイバを用いた検体分析装置 |
| KR100236506B1 (ko) | 1990-11-29 | 2000-01-15 | 퍼킨-엘머시터스인스트루먼츠 | 폴리머라제 연쇄 반응 수행 장치 |
| US5994056A (en) | 1991-05-02 | 1999-11-30 | Roche Molecular Systems, Inc. | Homogeneous methods for nucleic acid amplification and detection |
| US5670113A (en) | 1991-12-20 | 1997-09-23 | Sibia Neurosciences, Inc. | Automated analysis equipment and assay method for detecting cell surface protein and/or cytoplasmic receptor function using same |
| US5210590A (en) | 1992-02-18 | 1993-05-11 | L. T. Industries, Inc. | Rapid scanning spectrographic analyzer |
| US5401465A (en) * | 1992-05-05 | 1995-03-28 | Chiron Corporation | Luminometer with reduced sample crosstalk |
| CA2100020C (en) | 1992-07-17 | 2001-09-11 | Walter Blumenfeld | Methods and apparatus for detecting bacterial growth by spectrophotometric sampling of a fiber-optic array |
| JPH0634546A (ja) | 1992-07-17 | 1994-02-08 | Tosoh Corp | 蛍光検出器 |
| JP2909216B2 (ja) * | 1994-04-29 | 1999-06-23 | パーキン‐エルマー コーポレイション | 核酸増幅生成物のリアルタイム検出装置 |
| US5589351A (en) | 1994-12-06 | 1996-12-31 | Nps Pharmaceuticals, Inc. | Fluorescence detection apparatus |
| IT1280954B1 (it) | 1995-10-05 | 1998-02-11 | Sorin Biomedica Cardio Spa | Procedimento e sistema per rilevare parametri chimico-fisici. |
| JPH10170444A (ja) | 1996-12-06 | 1998-06-26 | Hamamatsu Photonics Kk | 光測定装置 |
| JPH10197449A (ja) * | 1997-01-07 | 1998-07-31 | Hamamatsu Photonics Kk | 光測定装置 |
| JPH10281994A (ja) * | 1997-04-08 | 1998-10-23 | Hamamatsu Photonics Kk | 蛍光測定装置 |
| JPH10318929A (ja) * | 1997-05-19 | 1998-12-04 | Toa Medical Electronics Co Ltd | 発光反応測定方法 |
| US6469311B1 (en) | 1997-07-16 | 2002-10-22 | Molecular Devices Corporation | Detection device for light transmitted from a sensed volume |
| US6043880A (en) | 1997-09-15 | 2000-03-28 | Becton Dickinson And Company | Automated optical reader for nucleic acid assays |
| US6982431B2 (en) * | 1998-08-31 | 2006-01-03 | Molecular Devices Corporation | Sample analysis systems |
| DK0953379T3 (da) | 1998-05-01 | 2004-11-22 | Hoffmann La Roche | Apparat til samtidig overvågning af reaktioner, der finder sted i en flerhed af reaktionsbeholdere |
| EP0953837A1 (en) * | 1998-05-01 | 1999-11-03 | F. Hoffmann-La Roche Ag | Fluorescence light measuring device and an apparatus wherein such a device is used |
| EP0953838A1 (en) | 1998-05-01 | 1999-11-03 | F. Hoffmann-La Roche Ag | Apparatus for simultaneously monitoring reactions taking place in a plurality of reaction vessels |
| GB9815702D0 (en) * | 1998-07-21 | 1998-09-16 | Cambridge Imaging Ltd | Improved imaging system for fluorescence assays |
| US6569631B1 (en) | 1998-11-12 | 2003-05-27 | 3-Dimensional Pharmaceuticals, Inc. | Microplate thermal shift assay for ligand development using 5-(4″dimethylaminophenyl)-2-(4′-phenyl)oxazole derivative fluorescent dyes |
| US6838680B2 (en) | 1999-05-12 | 2005-01-04 | Aclara Biosciences, Inc. | Multiplexed fluorescent detection in microfluidic devices |
| WO2001001112A1 (en) | 1999-06-26 | 2001-01-04 | Packard Instrument Company, Inc. | Microplate reader |
| US6657169B2 (en) | 1999-07-30 | 2003-12-02 | Stratagene | Apparatus for thermally cycling samples of biological material with substantial temperature uniformity |
| CA2399908A1 (en) * | 2000-02-10 | 2001-08-16 | Todd Dickinson | Array of individual arrays as substrate for bead-based simultaneous processing of samples and manufacturing method therefor |
| US6690467B1 (en) | 2000-05-05 | 2004-02-10 | Pe Corporation | Optical system and method for optically analyzing light from a sample |
| JP2002098696A (ja) * | 2000-09-26 | 2002-04-05 | Inst Of Physical & Chemical Res | 集積型生体分子センサー |
| EP1511990B1 (en) * | 2002-05-17 | 2015-03-25 | Life Technologies Corporation | Instrument for detecting and measuring fluorescence including an excitation source |
| GB0221167D0 (en) * | 2002-09-12 | 2002-10-23 | Quanta Biotech Ltd | Control apparatus |
| US7148043B2 (en) | 2003-05-08 | 2006-12-12 | Bio-Rad Laboratories, Inc. | Systems and methods for fluorescence detection with a movable detection module |
| JP2005077260A (ja) | 2003-09-01 | 2005-03-24 | Fuji Photo Film Co Ltd | 化学発光検出方法およびシステム |
| US7177023B2 (en) | 2004-03-19 | 2007-02-13 | Applera Corporation | Fluorescent light detection |
| EP1758981A4 (en) | 2004-05-28 | 2013-01-16 | Wafergen Inc | APPARATUS AND METHODS FOR PERFORMING MULTIPLEX ANALYZES |
| US7136550B2 (en) * | 2004-10-28 | 2006-11-14 | Corning Incorporated | Single-fiber launch/receive system for biosensing applications |
| EP1877585A2 (en) * | 2005-04-28 | 2008-01-16 | Merck & Co., Inc. | Real-time hpv pcr assays |
| RU2304277C2 (ru) | 2005-06-23 | 2007-08-10 | Яков Игоревич Алексеев | Устройство для одновременного контроля в реальном масштабе времени множества амплификаций нуклеиновой кислоты |
| US20070098594A1 (en) | 2005-11-03 | 2007-05-03 | Roche Molecular Systems, Inc. | Analytical multi-spectral optical detection system |
| US7715001B2 (en) | 2006-02-13 | 2010-05-11 | Pacific Biosciences Of California, Inc. | Methods and systems for simultaneous real-time monitoring of optical signals from multiple sources |
| DE102006036171B4 (de) | 2006-07-28 | 2008-10-09 | Analytik Jena Ag | Anordnung und Verfahren zur mehrkanaligen Fluoreszenzmessung in PCR-Proben |
| JP2008089321A (ja) * | 2006-09-29 | 2008-04-17 | Fujifilm Corp | バイオセンサ検出装置 |
| EP2193356B1 (en) * | 2007-08-29 | 2014-07-23 | Eppendorf Ag | Device and method for radiometric measurement of a plurality of samples |
| EP2108942A1 (en) | 2008-04-09 | 2009-10-14 | F. Hoffmann-Roche AG | Reference light source device |
| ES2875831T3 (es) | 2009-01-08 | 2021-11-11 | It Is Int Ltd | Sistema óptico para reacciones químicas y/o bioquímicas |
-
2010
- 2010-01-08 ES ES10726151T patent/ES2875831T3/es active Active
- 2010-01-08 DE DE202010018011U patent/DE202010018011U1/de not_active Expired - Lifetime
- 2010-01-08 WO PCT/GB2010/000028 patent/WO2010079338A2/en active Application Filing
- 2010-01-08 EP EP10726151.3A patent/EP2376896B1/en active Active
- 2010-01-08 CA CA2749247A patent/CA2749247A1/en not_active Abandoned
- 2010-01-08 ES ES13151696T patent/ES2892342T3/es active Active
- 2010-01-08 EP EP13151696.5A patent/EP2584344B1/en active Active
- 2010-01-08 US US13/143,720 patent/US10029227B2/en active Active
- 2010-01-08 EP EP21169538.2A patent/EP3889586A1/en active Pending
- 2010-01-08 JP JP2011544920A patent/JP5864262B2/ja active Active
- 2010-01-08 DK DK13151696.5T patent/DK2584344T3/da active
- 2010-01-08 CN CN201080011733.5A patent/CN102341694B/zh active Active
-
2013
- 2013-09-06 US US14/019,687 patent/US9089828B2/en active Active
-
2015
- 2015-12-24 JP JP2015251451A patent/JP2016095315A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| US9089828B2 (en) | 2015-07-28 |
| EP2584344A3 (en) | 2013-07-31 |
| WO2010079338A2 (en) | 2010-07-15 |
| EP2584344B1 (en) | 2021-06-30 |
| US20120014835A1 (en) | 2012-01-19 |
| CN102341694A (zh) | 2012-02-01 |
| US20140005078A1 (en) | 2014-01-02 |
| JP2012514747A (ja) | 2012-06-28 |
| WO2010079338A3 (en) | 2010-11-18 |
| EP3889586A1 (en) | 2021-10-06 |
| DE202010018011U1 (de) | 2013-07-10 |
| CN102341694B (zh) | 2018-03-23 |
| EP2376896A2 (en) | 2011-10-19 |
| JP2016095315A (ja) | 2016-05-26 |
| CA2749247A1 (en) | 2010-07-15 |
| EP2584344A2 (en) | 2013-04-24 |
| ES2875831T3 (es) | 2021-11-11 |
| DK2584344T3 (da) | 2021-10-04 |
| EP2376896B1 (en) | 2021-05-19 |
| US10029227B2 (en) | 2018-07-24 |
| ES2892342T3 (es) | 2022-02-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5864262B2 (ja) | 化学および/または生化学反応のための光学システム | |
| US7295316B2 (en) | Fluorescent detector with automatic changing filters | |
| CN104136914B (zh) | 用于光学测量试样中核酸的荧光的装置及该装置的使用 | |
| US20070098594A1 (en) | Analytical multi-spectral optical detection system | |
| KR101802460B1 (ko) | 유전자 진단 장치 | |
| KR20120012468A (ko) | rtPCR 반응을 모니터링하기 위한 광학 검출 시스템 | |
| EP1984670A2 (en) | Methods and systems for simultaneous real-time monitoring of optical signals from multiple sources | |
| JP2017510796A (ja) | 熱サイクリック生化学処置のための装置及び方法 | |
| US20180252646A1 (en) | Optical structure and optical light detection system | |
| EP1721146B1 (en) | Apparatus and method for fluorescent detection in biological samples | |
| KR100818351B1 (ko) | 다채널 바이오 칩 스캐너 | |
| JP2024534844A (ja) | 病原体又は遺伝的変異を特定するためのスクリーニングシステム | |
| TWI498562B (zh) | 生化反應之檢測裝置及其方法 | |
| EP1951912B1 (en) | Method of thermal cycling comprising measuring signals in different wells at different temperatures | |
| US20090155919A1 (en) | High throughput drug screening method |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130108 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130108 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20140115 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140121 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140404 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140411 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140718 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150106 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20150403 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150703 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20151124 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20151224 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5864262 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |