JP5840855B2 - 胚性幹細胞から心筋シートを製造する方法 - Google Patents
胚性幹細胞から心筋シートを製造する方法 Download PDFInfo
- Publication number
- JP5840855B2 JP5840855B2 JP2011076235A JP2011076235A JP5840855B2 JP 5840855 B2 JP5840855 B2 JP 5840855B2 JP 2011076235 A JP2011076235 A JP 2011076235A JP 2011076235 A JP2011076235 A JP 2011076235A JP 5840855 B2 JP5840855 B2 JP 5840855B2
- Authority
- JP
- Japan
- Prior art keywords
- cells
- sheet
- cardiomyocytes
- flk
- myocardial
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/34—Muscles; Smooth muscle cells; Heart; Cardiac stem cells; Myoblasts; Myocytes; Cardiomyocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/44—Vessels; Vascular smooth muscle cells; Endothelial cells; Endothelial progenitor cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/38—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells
- A61L27/3804—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells characterised by specific cells or progenitors thereof, e.g. fibroblasts, connective tissue cells, kidney cells
- A61L27/3834—Cells able to produce different cell types, e.g. hematopoietic stem cells, mesenchymal stem cells, marrow stromal cells, embryonic stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/38—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells
- A61L27/3886—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells comprising two or more cell types
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/54—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0657—Cardiomyocytes; Heart cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0697—Artificial constructs associating cells of different lineages, e.g. tissue equivalents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/412—Tissue-regenerating or healing or proliferative agents
- A61L2300/414—Growth factors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2430/00—Materials or treatment for tissue regeneration
- A61L2430/20—Materials or treatment for tissue regeneration for reconstruction of the heart, e.g. heart valves
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/01—Modulators of cAMP or cGMP, e.g. non-hydrolysable analogs, phosphodiesterase inhibitors, cholera toxin
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/04—Immunosuppressors, e.g. cyclosporin, tacrolimus
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/165—Vascular endothelial growth factor [VEGF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/13—Coculture with; Conditioned medium produced by connective tissue cells; generic mesenchyme cells, e.g. so-called "embryonic fibroblasts"
- C12N2502/1329—Cardiomyocytes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/13—Coculture with; Conditioned medium produced by connective tissue cells; generic mesenchyme cells, e.g. so-called "embryonic fibroblasts"
- C12N2502/1347—Smooth muscle cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/28—Vascular endothelial cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/02—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from embryonic cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Cell Biology (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Biotechnology (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Developmental Biology & Embryology (AREA)
- Pharmacology & Pharmacy (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- Dermatology (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Transplantation (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Cardiology (AREA)
- Vascular Medicine (AREA)
- Immunology (AREA)
- Virology (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- Botany (AREA)
- Rheumatology (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Heart & Thoracic Surgery (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Description
[1]以下の工程(a)および(b):
(a)胚性幹細胞からFlk/KDR陽性細胞、心筋細胞、内皮細胞および壁細胞をそれぞれ製造する工程、および
(b)当該Flk/KDR陽性細胞へ当該心筋細胞、内皮細胞および壁細胞を混合することによりシートを形成させる工程
を含む、胚性幹細胞由来の心筋細胞、内皮細胞および壁細胞からシートを製造する方法。
[2]前記Flk/KDR陽性細胞が、胚性幹細胞をゼラチン被覆培養器材上で培養することにより誘導される、[1]に記載の方法。
[3]前記工程(a)において、心筋細胞が、シクロスポリンAの存在下で前記Flk/KDR陽性細胞を培養することにより製造される、[1]または[2]に記載の方法。
[4]前記工程(a)において、内皮細胞および壁細胞が、VEGFおよびcAMPの存在下で前記Flk/KDR陽性細胞を培養することにより製造される、[1]または[2]に記載の方法。
[5]前記工程(b)において、Flk/KDR陽性細胞を1〜7日間、好ましくは3日間培養した後に、心筋細胞、内皮細胞および壁細胞を混合させる、[1]〜[4]のいずれかに記載の方法。
[6]前記工程(b)において、温度応答性ポリマーを被覆した培養器材を用いてシートを形成させる、[1]〜[5]のいずれかに記載の方法。
[7]前記工程(b)において、混合後VEGFの存在下でさらに培養することによりシートを形成させる、[1]〜[6]のいずれかに記載の方法。
[8]前記シートを積層化する工程をさらに含む、[1]〜[7]のいずれかに記載の方法。
[9]前記積層化が3層である、[8]に記載の方法。
[10][1]〜[9]のいずれかに記載の方法で得られた心筋シートを含む心疾患治療剤。
ES細胞は、ヒトやマウスなどの哺乳動物の初期胚(例えば胚盤胞)の内部細胞塊から樹立された、多能性と自己複製による増殖能を有する幹細胞である。
心筋シートを製造するためのFlk/KDR陽性細胞(Flk+細胞ともいう)、心筋細胞、内皮細胞および壁細胞の製造に使用される分化培地の例を以下に記載する。
本発明においてFlk/KDR陽性細胞とは、少なくともFlk/KDRを発現している細胞であり、ここでFlk/KDRとは、Flk1またはKDRを意味し、血管内皮細胞増殖因子(VEGF)の受容体である。Flk1は、NCBIのaccession番号NM_010612が例示され、KDRは、NCBIのaccession番号NM_002253が例示される。
本発明において心筋細胞とは、少なくとも心筋トロポニン(cTnT)またはαMHCを発現している細胞を意味する。cTnTは、ヒトの場合NCBIのaccession番号NM_000364が例示され、マウスの場合、NM_001130174が例示される。αMHCは、ヒトの場合NCBIのaccession番号NM_002471が例示され、マウスの場合、NM_001164171が例示される。
本発明において内皮細胞とは、少なくともPE-CAM、VE-cadherinおよびフォン-ウィルブラント因子(vWF)のいずれか一つを発現している細胞を意味する。また、壁細胞とは、少なくともSmooth muscle actin(SMA)を発現している細胞を意味する。ここで、PE-CAMは、ヒトの場合NCBIのaccession番号NM_000442が例示され、マウスの場合、NM_001032378が例示される。VE-cadherinは、ヒトの場合NCBIのaccession番号NM_001795が例示され、マウスの場合、NM_009868が例示される。vWFは、ヒトの場合NCBIのaccession番号NM_000552が例示され、マウスの場合、NM_011708が例示される。SMAは、ヒトの場合NCBIのaccession番号NM_001141945が例示され、マウスの場合、NM_007392が例示される。
心筋シートとは、心臓または血管を形成する各種細胞から成り、細胞間結合により細胞同士が連結されたシート状の細胞集合体である。ここで、心臓または血管を形成する各種細胞とは上述の心筋細胞、内皮細胞および壁細胞が例示される。
・少なくとも、心筋細胞、内皮細胞および壁細胞を含み、心筋シートを構成する細胞構成比は、以下のものに限定されないが、例えば、心筋細胞35〜50%、内皮細胞0.5〜7%、壁細胞45〜63%である。
・内皮細胞が心筋細胞と心筋細胞の間に散在している。
・VEGFを発現し分泌する。
本発明で提供する心筋シートは、動物(好ましくはヒト)の心疾患の治療剤として用いることができる。心疾患の治療方法は、心筋シートを、所望の部分を覆うように配置することによって達成される。ここで、所望の部分を覆うように配置することは、当該分野において周知技術を用いて行うことができる。配置に際し、所望の部分が大きい場合は、組織を取り巻くように配置してもよい。また、心筋シートの配置は、所望の効果を得るため、同部分へ数回の配置を行うこともできる。数回の配置を行う場合、心筋シートが組織へ生着し、血管新生を行うために十分な時間をおいて行うことが望ましい。
Yamashita JK, et al. FASEB J. 19:1534-6, 2005に記載のaMHCプロモーターによりEGFPの発現が制御されるよう操作されたマウスES細胞株(EMG7)を用いた。
上述のようにEMG7より作製した心筋シートを0.25%トリプシンを用いて単離し、PE(phycoerythrin)結合の抗CD31抗体にて標識し、FACSを用いてGFP(FITC)およびPEの陽性率により心筋細胞(CM), 内皮細胞(EC), 壁細胞(MC)の割合について定量した結果を図1に示す。その結果、CM: 43.4±6.2%, EC: 3.3±2.6%, MC: 53.3±8.2%と計算された。
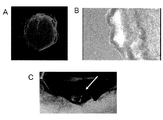
組織学的評価を行うため、EMG7より作製した心筋シートを4%PFA(paraformaldehyde)を用いて固定し、1%スキムミルクにてブロッキング後、抗体(一次抗体:mouse anti-cTnT, rat anti-VE-Cadherin、二次抗体:anti-mouse Alexa Flour 546, anti-rat AlexaFlour 488)を用いてCM, ECを標識し、DAPI (4',6-diamino-2-phenylindole) を用いて核染色した後、多光子レーザー顕微鏡(LSM 510, Carl-Zeiss)または蛍光顕微鏡(BZ-9000, Keyence)により観察した(図2BおよびC)。さらに、4%PFAにて固定し、脱水・脱脂・脱アルコールののち、パラフィン浸透ののち包埋した。6μmの切片をヘマトキシリン・エオジン染色、シリウスレッド染色あるいは前述と同様にcTnTに対する免疫染色(HRP/DAB発光)した(図2A)。その結果、細胞外マトリクス(図2A上段、シリウスレッド染色)が保持されたままシートが回収されていることが示された。シートは3-4層の細胞で成り立っていることが示された。またCMは細胞シートの主な構成成分であるが、その間にECが散在している様子が観察された。
電気生理学的評価を行うため、0.1%ゼラチンにてコーティングした電極付き培養皿(MED64 system, アルファメッド・サイエンス)の電極上にEMG7より作製した心筋シートを静置した。続いて、培地を吸引し37℃にて30分インキュベートすることにより電極とシートを固定し、それぞれの電極の電位を測定することにより、シート上での電位の伝導を記録した。その結果を図3に示す。細胞外電位測定により、拍動が電気的に連続して一方向性に伝導することを確認した(図3C)。
EMG7より作製した心筋シートの形成中(Condition 1)および完成後(Condition 2)の培養上清のサイトカイン量をELISA(enzyme-linked immunosorbent assay)を用いてTNFα、IGF-1、VEGF、IL-6、bFGF、IFNγ、EGF、LeptinおよびHGFを測定した(HGF: mouse HGF EIA kit, IIM, それ以外: mouse angiogenesis ELISA strip, Signosis)。その結果を図4に示す。心筋シートの形成中および完成後のいずれにおいても、angiogenesisに関わるサイトカイン(TNFα, IGF-1, VEGF, IL-6, bFGF, IFNγ, EGF, Leptin, HGF)のうち、VEGFが非常に多く産生されることが示された。
・Condition 2: ゼラチンコーティングディッシュ上に上述の方法で作製した心筋シートを広げたて静置し、培地を吸引し培養皿とシートを固定後、培地を加えて37℃にて30分インキュベートする。別の心筋シートを広げてディッシュに固定したシートの上へ静置し、培地を吸引して積層させた。同様に3層分繰り返す。2,3層目は元のシートから少しずつ位置をずらして積層化させた。続いて、ピペットマンを用いて培養皿底面を沿わせるように培地を流し、積層化された細胞シートを培養皿からはがした(図5)。このように積層化した心筋シートを無血清培地を用いて2回洗浄し、無血清培地にて培養を継続し、3時間後培養上清を回収し、サイトカイン量の測定に用いた。
上述のように作製した心筋シートをRNeasy mini (QIAGEN) を用いてRNAを抽出し、vegf164の発現量を定量性RT-PCRにて測定した(Step One Plus, Appliedbiosystems、vegf164のforward primer: 5’-CCAGCACATAGGAGAGATGAGCTT-3’(配列番号1)およびreverse primer: 5’-CAAGGCTCACAGTGATTTTCTGG-3’(配列番号2)、b-actinのforward primer: 5’-CATCCGTAAAGACCTCTATGCCAAC-3’(配列番号3)およびreverse primer: 5’-ATGGAGCCACCGATCCACA-3’(配列番号4))。この時、対照として、マウス新生仔由来心線維芽細胞(CF)を用いて作成した細胞シートを用いた。その結果を図6Aに示す。EMG7より作製した心筋シートがCFシートに比べvegf164を極めて多く発現することが示された。さらに、上述の心筋シート作製過程において心筋細胞を添加したシート(CM(+))と添加しなかったシート(CM(-))をそれぞれ回収前(室温に下げる前)に培養上清を吸引し、無血清培地にて2回洗浄した後、無血清培地にて3時間培養後の上清を回収し、VEGFの量を測定した(Quantikine mouse VEGF, R&D)。その結果を図6Bに示す。CM(+)シートがCM(-)シートに比べVEGFを極めて多く分泌することが示された。
心筋シートを回収後にゼラチンコーティングディッシュ上に静置し、培地を吸引し37℃にて30分インキュベートすることによりデイッュとシートを固定した。次のように3群に分け、各群3枚ずつ作成し、4%PFAによる固定後、%スキムミルクにてブロッキングし、抗体(一次:mouse anti-Oct 3/4, rabbit anti-Nanog、二次:anti-mouse Alexa Flour 488, anti-rat Alexa Flour 546)を用いてNanogまたはOct3/4陽性細胞を標識し、蛍光顕微鏡を用いて計測した。結果を図7に示す。回収直後のシート内(Group1)に未分化細胞の小コロニーが混入していることを確認した。また、LIF(+)の環境下でのシート継続培養(Group2)では混入未分化コロニーのサイズが増大するが、LIF(-)(Group3)ではその増大は抑えられることを確認した。
・Group 2: 心筋シートを回収後、LIF(白血病阻害因子)を添加したES細胞用培地(Yamashita J, et al. Nature. 408:92-6, 2000)にて3日間継続培養後、蛍光免疫染色を行う。
・Group 3: LIFを添加しないES細胞用培地にて3日間継続培養後、蛍光免疫染色を行う。
10-13週齢、250〜330gの無胸腺免疫不全ラット(F344/N Jcl-rnu/rnu)(日本クレア)より次の方法で亜急性期心筋梗塞(MI)モデル作成した。当該ラットをラット用人工呼吸器にて呼吸管理し、イソフルラン吸引により麻酔した。続いて、少量の酸素による人工呼吸下で左肋間開胸による心膜切開より心臓を露出後、前下行枝を第一中隔枝末梢で6-0ポリプロピレン糸にて結紮した。末梢灌流領域の収縮低下および色調変化を確認(それらを認めない場合再度結紮を施行)した後、4-0ポリプロピレン糸にて閉創した。6日後に心臓超音波検査(Vivid7, GE横河メディカル)にてMIの有無を確認した。左室内径短縮率(FS)が40%を超えるものは不適モデルとして除外した。
移植後2週および4週に心臓超音波検査および移植後4週に左室容量圧曲線測定検査(心臓カテーテル検査:MIKRO-TIP catheter system, Millar instruments)により心機能を測定した。治療群とSham群についてそれぞれ評価し比較した。
経時的なグラフト細胞の生着、生着細胞の局在の評価およびグラフト由来心筋細胞形態の変化(成熟)の評価を移植後1日、3日、1週、4週において次の方法により行った。ジエチルエーテルにて麻酔導入後、ラット用人工呼吸器にて呼吸管理し、イソフルランにて麻酔維持した。正中にて開胸し上大静脈・左上大静脈および下大静脈を確保し遮断した。心尖部に23G針を刺入し、生理的食塩水注入にて左室内血液を流出させると同時に右心房を開放し心臓の過拡張および浮腫を防止した。右心房から生理的食塩水のみ流出することを確認した後、45分間、4%PFAを同様に注入し組織を固定した(灌流固定法)。続いて、心臓を摘出し4%PFAに浸潤、4℃over nightの後、15%スクロース液に浸潤させた(4℃、2回交換、計24時間)。イソペンタンにドライアイスを加えた溶液およびOCTコンパウンドを用いて凍結包埋を行った。さらに、梗塞部位の中心部にて6μm切片を作成し、ブロッキング剤(Protein Block Serum-Free, DAKO)によりブロッキングを行った後、抗体(一次抗体:mouse anti-cTnT, rabbit anti-GFPおよび二次抗体:anti-mouse AlexaFlour 546またはanti-rat AlexaFlour 488)を用いてGFP陽性心筋細胞を標識し、蛍光顕微鏡(BZ-9000, Keyence)を用いて観察した。
移植4週後に、梗塞中心部より50μm間隔で6μm厚にて各個体あたり5枚の切片を作成し、シリウスレッドにより染色し蛍光顕微鏡観察を行った。心室内腔長と梗塞部位長を測定し、梗塞部位の割合を計算した。また、梗塞部位面積を梗塞部位長で割り、梗塞部位平均壁厚を計算した。治療群とSham群でそれぞれ行い(各5個体ずつ)、比較した。その結果、治療群がSham群に比べ梗塞領域が限定され、梗塞部位の壁菲薄化が抑えられることが示された(図13)。これらは治療群において梗塞後左室リモデリングが抑制されているためと示唆された。
移植後1日、3日、1週、4週に、前述と同様の方法で作製した切片を用いてvWFに対する免疫染色(1:500)とFISHを同時に行った。4週目での治療群とSham群における新生血管数(capillary density)につき、梗塞部位を中心部(Central-MI)と周辺部(Peri-MI)に分けて計測し比較した(各3個体につき、無作為5視野ずつ)。この時、中心部と周辺部を図示するために、治療群の1例についてはマッソン・トリクローム染色を行った。治療群については1日、3日、1週の段階での新生血管の分布(グラフト由来心筋細胞生着部での血管新生の有無等)を観察した。移植後1日目にはグラフト部位の内部にvWF陽性細胞が散在しており、3日目にはグラフト部位の心筋細胞塊を内側から囲むようにvWF陽性細胞の集積が認められたが、これらは明らかな管腔構造は示していなかった。マウスのシグナルも示していないので、レシピエント(ラット)側からの集積と考えられる。移植後7日目には、3日目に示された集積はすでに認められなかった。さらに高倍率にて3日目の状態を観察すると、グラフト心筋細胞塊の中に一部vWF陽性の管腔構造を認め、またその内部に赤血球を認め、血流を伴った新生血管がグラフト内に増生していることを示した。また同部位にてFISHとvWF免疫染色を同時に行うことにより、その新生血管の一部にマウス由来細胞が取り込まれていることが示された。新生血管形成にはレシピエント細胞のみならずグラフト由来細胞も寄与していることが考えられた(図14)。移植後4週では前述のように、グラフト由来細胞の生着自体はかなり減少しているが、capillary densityの測定により、血管新生は治療群において有意に促進されていることが示された。またその血管新生は治療群において、梗塞周辺部でより多く起こっていることが示された(図15)。
Claims (8)
- 以下の工程(a)から工程(e)を順番に含むことを特徴とする、心筋細胞、内皮細胞および壁細胞を含む心筋シートを製造する方法。
(a)内皮細胞および壁細胞の混合細胞を用意する工程
(b)心筋細胞を用意する工程
(c)Flk/KDR陽性細胞を用意する工程
(d)前記工程(a)で用意した内皮細胞および壁細胞の混合細胞と前記工程(b)で用意した心筋細胞を細胞数で1:1の比率で混合し、前記工程(c)で用意したFlk/KDR陽性細胞と混合する工程
(e)前記工程(d)で得られた混合細胞を温度応答性ポリマーを被覆した培養器材上でVEGFを含む培地中で培養することによりシートを形成させる工程 - 前記工程(a)の混合細胞または前記工程(b)の心筋細胞がFlk/KDR陽性細胞から得られる、請求項1に記載の方法。
- 前記Flk/KDR陽性細胞が、多能性と自己複製による増殖能を有する幹細胞をゼラチン被覆培養器材上で培養することにより得られる、請求項1または2に記載の方法。
- 前記工程(a)の混合細胞が、Flk/KDR陽性細胞をVEGFおよび8−ブロモ−cAMPの存在下で培養する工程を含む方法によって得られる、請求項2または3に記載
の方法。 - 前記工程(b)の心筋細胞が、Flk/KDR陽性細胞を、シクロスポリンAの存在下で培養する工程を含む方法によって得られる、請求項2または3に記載の方法。
- 前記Flk/KDR陽性細胞を1〜7日間培養した後に、心筋細胞、ならびに、内皮細胞および壁細胞の混合細胞を混合させる、請求項1〜5のいずれか1項に記載の方法。
- 前記工程(e)で得られたシートを積層化する工程をさらに含む、請求項1〜6のいずれか1項に記載の方法。
- 前記積層化が3層である、請求項7に記載の方法。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011076235A JP5840855B2 (ja) | 2011-03-30 | 2011-03-30 | 胚性幹細胞から心筋シートを製造する方法 |
| US14/009,018 US9623052B2 (en) | 2011-03-30 | 2012-03-30 | Method for producing myocardial sheet from embryonic stem cell |
| EP12763936.7A EP2692859B1 (en) | 2011-03-30 | 2012-03-30 | Method for producing cardiomyocyte sheet from embryonic stem cells |
| PCT/JP2012/059427 WO2012133945A1 (ja) | 2011-03-30 | 2012-03-30 | 胚性幹細胞から心筋シートを製造する方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011076235A JP5840855B2 (ja) | 2011-03-30 | 2011-03-30 | 胚性幹細胞から心筋シートを製造する方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012210156A JP2012210156A (ja) | 2012-11-01 |
| JP2012210156A5 JP2012210156A5 (ja) | 2014-05-15 |
| JP5840855B2 true JP5840855B2 (ja) | 2016-01-06 |
Family
ID=46931617
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011076235A Expired - Fee Related JP5840855B2 (ja) | 2011-03-30 | 2011-03-30 | 胚性幹細胞から心筋シートを製造する方法 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US9623052B2 (ja) |
| EP (1) | EP2692859B1 (ja) |
| JP (1) | JP5840855B2 (ja) |
| WO (1) | WO2012133945A1 (ja) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010044417A1 (ja) | 2008-10-14 | 2010-04-22 | 株式会社セルシード | 温度応答性細胞培養器材、及びその製造方法 |
| US9764063B2 (en) | 2012-03-15 | 2017-09-19 | Iheart Japan Corporation | Method for producing mixed cell population of cardiomyocytes and vascular cells from induced pluripotent stem cell |
| US10159766B2 (en) | 2013-05-31 | 2018-12-25 | Iheart Japan Corporation | Layered cell sheet incorporating hydrogel |
| JP6248617B2 (ja) * | 2013-12-25 | 2017-12-20 | 大日本印刷株式会社 | 細胞シートの製造方法 |
| JP5924750B2 (ja) * | 2014-05-01 | 2016-05-25 | iHeart Japan株式会社 | Cd82陽性心筋前駆細胞 |
| JP7180965B2 (ja) * | 2014-11-12 | 2022-11-30 | テルモ株式会社 | 心筋細胞シート |
| US10711247B2 (en) | 2015-08-31 | 2020-07-14 | Tokyo Women's Medical University | Method for reducing pluripotent stem cells, method for producing cell population having reduced pluripotent stem cells |
| JP6420933B2 (ja) | 2016-12-02 | 2018-11-07 | タカラバイオ株式会社 | 内皮細胞の製造方法 |
| US12018281B2 (en) | 2018-03-30 | 2024-06-25 | Kyoto University | Cardiomyocyte maturation promoter |
| SG11202009314XA (en) | 2018-03-30 | 2020-10-29 | Univ Kyoto | Heterocyclic compound |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5843780A (en) | 1995-01-20 | 1998-12-01 | Wisconsin Alumni Research Foundation | Primate embryonic stem cells |
| DE60143892D1 (de) | 2000-07-21 | 2011-03-03 | Cellseed Ind | Herzmuskel-ähnliche zellschicht, dreidimensionales konstrukt, herzmuskel-ähnliches gewebe und verfahren zur herstellung |
| EP2266499B1 (en) | 2003-08-01 | 2015-06-10 | Cellseed Inc. | Three-dimensional tissue structure |
| CN1863904B (zh) | 2003-10-03 | 2014-05-28 | 福田惠一 | 由干细胞分化诱导心肌细胞的方法 |
| EP1785482B1 (en) | 2004-08-27 | 2017-10-04 | Daiichi Sankyo Company, Limited | A method of selecting a cardiomyocyte using intracellular mitochondria as an indicator |
| KR101529317B1 (ko) | 2005-06-22 | 2015-06-16 | 아스테리아스 바이오세라퓨틱스, 인크. | 영장류 다능성 줄기 세포의 심근세포 계통 세포로의 분화 |
| KR101455144B1 (ko) | 2006-01-31 | 2014-10-27 | 다이이찌 산쿄 가부시키가이샤 | 줄기세포 및 태아에서 유래된 심근세포 및 예정 심근세포의 제조방법 |
| AU2007244226B2 (en) | 2006-04-28 | 2012-09-20 | Daiichi Sankyo Company, Limited | Method for inducing differentiation of pluripotent stem cells into cardiomyocytes |
| US8765465B2 (en) * | 2008-03-26 | 2014-07-01 | Kyoto University | Efficient production and use of highly cardiogenic progenitors and cardiomyocytes from embryonic and induced pluripotent stem cells |
| JP5387294B2 (ja) | 2009-09-29 | 2014-01-15 | ブラザー工業株式会社 | サーバに接続されるプリンタ及びサーバ |
| JP5654786B2 (ja) | 2010-06-28 | 2015-01-14 | 株式会社セルシード | アクリルアミド誘導体および該誘導体を含む重合体 |
-
2011
- 2011-03-30 JP JP2011076235A patent/JP5840855B2/ja not_active Expired - Fee Related
-
2012
- 2012-03-30 WO PCT/JP2012/059427 patent/WO2012133945A1/ja active Application Filing
- 2012-03-30 EP EP12763936.7A patent/EP2692859B1/en not_active Not-in-force
- 2012-03-30 US US14/009,018 patent/US9623052B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP2692859B1 (en) | 2016-12-28 |
| US9623052B2 (en) | 2017-04-18 |
| EP2692859A1 (en) | 2014-02-05 |
| WO2012133945A1 (ja) | 2012-10-04 |
| US20140056859A1 (en) | 2014-02-27 |
| JP2012210156A (ja) | 2012-11-01 |
| EP2692859A4 (en) | 2015-01-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5840855B2 (ja) | 胚性幹細胞から心筋シートを製造する方法 | |
| JP5671670B2 (ja) | 間葉系幹細胞を含む細胞シート | |
| Du et al. | Induced pluripotent stem cell-derived hepatocytes and endothelial cells in multi-component hydrogel fibers for liver tissue engineering | |
| Wanjare et al. | Perivascular cells in blood vessel regeneration | |
| Yeh et al. | Cardiac repair with injectable cell sheet fragments of human amniotic fluid stem cells in an immune-suppressed rat model | |
| JP6832049B2 (ja) | 心臓神経堤細胞、及びその使用方法 | |
| JP5862915B2 (ja) | ハイドロゲルを組み込んだ積層化細胞シート | |
| JP2020000245A (ja) | シート状細胞培養物の製造方法 | |
| Kim et al. | Hepatic patch by stacking patient-specific liver progenitor cell sheets formed on multiscale electrospun fibers promotes regenerative therapy for liver injury | |
| Forte et al. | Human cardiac progenitor cell grafts as unrestricted source of supernumerary cardiac cells in healthy murine hearts | |
| EP1490476A2 (en) | Endothelial cells derived from human embryonic stem cells | |
| US11666604B2 (en) | Multilayered cell sheet of cardiac stem cells and method of preparing the same | |
| US20130171213A1 (en) | Method for manufacturing multilayered cell sheet, multilayered cell sheet having vascular network obtained thereby, and method of use thereof | |
| US20120100110A1 (en) | Physiological methods for isolation of high purity cell populations | |
| US20170035939A1 (en) | Adipocyte sheet, three-dimensional structure thereof, and method for producing the same | |
| Belmokhtar et al. | Regeneration of three layers vascular wall by using BMP2-treated MSC involving HIF-1α and Id1 expressions through JAK/STAT pathways | |
| KR20110024660A (ko) | 인간 배아줄기세포 또는 인간 유도만능줄기세포의 혈관내피세포로의 혈청 및 이종 비함유 분화방법 | |
| KR101477016B1 (ko) | 인간 배아줄기세포 유래 혈관주위 전구세포의 제조방법 및 이를 포함하는 세포치료 조성물 | |
| JP2016096732A (ja) | シート状細胞培養物の製造方法 | |
| Rahimi et al. | Comparative effectiveness of three-dimensional scaffold, differentiation media and co-culture with native cardiomyocytes to trigger in vitro cardiogenic differentiation of menstrual blood and bone marrow stem cells | |
| JP7471069B2 (ja) | 移植片の活性を高める方法 | |
| US20200095557A1 (en) | Cell spheroids containing capillary structures and methods of using same | |
| Di Baldassarre et al. | Induced Pluripotent Stem Cells Technology and Cardiomyocyte Generation: Progress, Uncertainties and Challenges in the Biological Features and Clinical Applications | |
| Song | Probing the spatiotemporal dynamics of cell-cell interactions in engineered tissues | |
| Glaser | Defining the Microenvironment for Directing Embryonic Stem Cells into Endothelial Cells |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140325 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20140325 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150519 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150630 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20151020 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20151112 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5840855 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |