JP5730882B2 - シアノピリジンの水溶液の製造方法およびデバイス - Google Patents
シアノピリジンの水溶液の製造方法およびデバイス Download PDFInfo
- Publication number
- JP5730882B2 JP5730882B2 JP2012533518A JP2012533518A JP5730882B2 JP 5730882 B2 JP5730882 B2 JP 5730882B2 JP 2012533518 A JP2012533518 A JP 2012533518A JP 2012533518 A JP2012533518 A JP 2012533518A JP 5730882 B2 JP5730882 B2 JP 5730882B2
- Authority
- JP
- Japan
- Prior art keywords
- cyanopyridine
- column
- gas phase
- heat exchanger
- aqueous solution
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000000034 method Methods 0.000 title claims description 107
- FFNVQNRYTPFDDP-UHFFFAOYSA-N 2-cyanopyridine Chemical compound N#CC1=CC=CC=N1 FFNVQNRYTPFDDP-UHFFFAOYSA-N 0.000 title claims description 105
- 239000007864 aqueous solution Substances 0.000 title claims description 57
- 239000012071 phase Substances 0.000 claims description 80
- 238000010521 absorption reaction Methods 0.000 claims description 63
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 41
- 229910001868 water Inorganic materials 0.000 claims description 32
- 239000007795 chemical reaction product Substances 0.000 claims description 24
- 239000007788 liquid Substances 0.000 claims description 23
- 238000010791 quenching Methods 0.000 claims description 17
- 230000000171 quenching effect Effects 0.000 claims description 13
- 239000007787 solid Substances 0.000 claims description 13
- 238000004140 cleaning Methods 0.000 claims description 11
- 238000005915 ammonolysis reaction Methods 0.000 claims description 8
- 230000001590 oxidative effect Effects 0.000 claims description 8
- 239000008346 aqueous phase Substances 0.000 claims description 7
- 238000004519 manufacturing process Methods 0.000 claims description 7
- 238000005406 washing Methods 0.000 claims description 6
- GZPHSAQLYPIAIN-UHFFFAOYSA-N 3-pyridinecarbonitrile Chemical group N#CC1=CC=CN=C1 GZPHSAQLYPIAIN-UHFFFAOYSA-N 0.000 claims description 5
- ITQTTZVARXURQS-UHFFFAOYSA-N 3-methylpyridine Chemical group CC1=CC=CN=C1 ITQTTZVARXURQS-UHFFFAOYSA-N 0.000 claims description 4
- 238000010992 reflux Methods 0.000 claims description 3
- 230000003134 recirculating effect Effects 0.000 claims 1
- 239000007789 gas Substances 0.000 description 95
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 description 17
- DFPAKSUCGFBDDF-UHFFFAOYSA-N Nicotinamide Chemical compound NC(=O)C1=CC=CN=C1 DFPAKSUCGFBDDF-UHFFFAOYSA-N 0.000 description 17
- 239000000047 product Substances 0.000 description 15
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 14
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 9
- 239000003054 catalyst Substances 0.000 description 9
- 238000006243 chemical reaction Methods 0.000 description 9
- 235000005152 nicotinamide Nutrition 0.000 description 9
- 239000011570 nicotinamide Substances 0.000 description 9
- 229960003512 nicotinic acid Drugs 0.000 description 9
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 8
- 229960003966 nicotinamide Drugs 0.000 description 8
- 235000001968 nicotinic acid Nutrition 0.000 description 8
- 239000011664 nicotinic acid Substances 0.000 description 8
- 239000001301 oxygen Substances 0.000 description 8
- 229910052760 oxygen Inorganic materials 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- BSKHPKMHTQYZBB-UHFFFAOYSA-N 2-methylpyridine Chemical compound CC1=CC=CC=N1 BSKHPKMHTQYZBB-UHFFFAOYSA-N 0.000 description 7
- 229910021529 ammonia Inorganic materials 0.000 description 7
- 230000007062 hydrolysis Effects 0.000 description 7
- 238000006460 hydrolysis reaction Methods 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 5
- -1 heterocyclic aromatic nitriles Chemical class 0.000 description 5
- 239000003960 organic solvent Substances 0.000 description 5
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 239000006227 byproduct Substances 0.000 description 4
- 238000001816 cooling Methods 0.000 description 4
- 238000011049 filling Methods 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 4
- AURDEEIHMPRBLI-UHFFFAOYSA-N 3-methylpyridine Chemical compound CC1=CC=CN=C1.CC1=CC=CN=C1 AURDEEIHMPRBLI-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 238000013461 design Methods 0.000 description 3
- 239000007791 liquid phase Substances 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- OISVCGZHLKNMSJ-UHFFFAOYSA-N 2,6-dimethylpyridine Chemical compound CC1=CC=CC(C)=N1 OISVCGZHLKNMSJ-UHFFFAOYSA-N 0.000 description 2
- 239000006096 absorbing agent Substances 0.000 description 2
- 239000001569 carbon dioxide Substances 0.000 description 2
- 229910002092 carbon dioxide Inorganic materials 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 238000001704 evaporation Methods 0.000 description 2
- LELOWRISYMNNSU-UHFFFAOYSA-N hydrogen cyanide Chemical compound N#C LELOWRISYMNNSU-UHFFFAOYSA-N 0.000 description 2
- 239000003595 mist Substances 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 238000012856 packing Methods 0.000 description 2
- 150000003222 pyridines Chemical class 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- 239000012808 vapor phase Substances 0.000 description 2
- 235000019156 vitamin B Nutrition 0.000 description 2
- 239000002912 waste gas Substances 0.000 description 2
- 239000002351 wastewater Substances 0.000 description 2
- LTKMTXLIAZLQHS-UHFFFAOYSA-N 1-methylpyridine Chemical group CN1C=CC=C=C1 LTKMTXLIAZLQHS-UHFFFAOYSA-N 0.000 description 1
- GRRJLVAHCMYTEP-UHFFFAOYSA-N 2h-pyridine-1-carbonitrile Chemical group N#CN1CC=CC=C1 GRRJLVAHCMYTEP-UHFFFAOYSA-N 0.000 description 1
- 229930003270 Vitamin B Natural products 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- 150000001491 aromatic compounds Chemical class 0.000 description 1
- 235000011089 carbon dioxide Nutrition 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 238000000151 deposition Methods 0.000 description 1
- HPYNZHMRTTWQTB-UHFFFAOYSA-N dimethylpyridine Natural products CC1=CC=CN=C1C HPYNZHMRTTWQTB-UHFFFAOYSA-N 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000013505 freshwater Substances 0.000 description 1
- 239000008246 gaseous mixture Substances 0.000 description 1
- 239000011491 glass wool Substances 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 238000003842 industrial chemical process Methods 0.000 description 1
- 238000009776 industrial production Methods 0.000 description 1
- 239000012442 inert solvent Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 239000000543 intermediate Substances 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- VUZPPFZMUPKLLV-UHFFFAOYSA-N methane;hydrate Chemical compound C.O VUZPPFZMUPKLLV-UHFFFAOYSA-N 0.000 description 1
- 239000012450 pharmaceutical intermediate Substances 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- OENLEHTYJXMVBG-UHFFFAOYSA-N pyridine;hydrate Chemical compound [OH-].C1=CC=[NH+]C=C1 OENLEHTYJXMVBG-UHFFFAOYSA-N 0.000 description 1
- 239000012495 reaction gas Substances 0.000 description 1
- 239000008234 soft water Substances 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 239000011720 vitamin B Substances 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D3/00—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping
- B01D3/009—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping in combination with chemical reactions
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/78—Carbon atoms having three bonds to hetero atoms, with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/84—Nitriles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/78—Carbon atoms having three bonds to hetero atoms, with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/84—Nitriles
- C07D213/85—Nitriles in position 3
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Epidemiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pyridine Compounds (AREA)
Description
シアノピリジンは医薬品中間体および他の化合物の製造にとって重要な出発原料である。3−メチルピリジン(3−ピコリン)は、ビタミンB−複合体の必須ビタミン(ビタミンB3)であるニコチン酸アミドおよびニコチン酸の工業生産の中間体である。
発明の基礎を成す課題は、上述の欠点を克服する、シアノピリジンの調製方法を提供することである。
驚くべきことに、発明の基礎を成す課題は特許請求の範囲に記載した方法およびデバイスによって解決される。さらなる発明の実施形態をこの説明を通じて開示する。
(A)シアノピリジンを含む気体反応生成物をリアクタ内で製造し、
(B)この気体反応生成物をカラム内で水でクエンチし、シアノピリジンの少なくとも一部が減少した気相を得て、
(C)この気相を凝縮器に移し、ここで凝縮物を得て、前記気相から前記水の少なくとも一部を減少させ、
(D)凝縮器からの気相を少なくとも1つの熱交換器に通す
方法である。
(a)吸収セクションおよびストリッピングセクションを含むカラムであって、吸収セクションは、この吸収セクションを通過した液体がストリッピングセクションに入るようにストリッピングセクションの上方に位置しているカラムを用意することと、
(b)シアノピリジンを含む気体反応生成物をカラムに供給することと、
(c)吸収セクションにおいて前記気相を水溶液に接触させて、シアノピリジンの少なくとも一部をこの水溶液に溶解させることと、
(d)ストリッピングセクションにおいて、工程(c)で吸収セクションから得られた水溶液をストリッピングガスでストリッピングすることと、
(e)水溶液をカラムの底部から抜き出すことと
を含む。
(i)シアノピリジンを含む気体反応生成物を製造するリアクタと、
(ii)気体反応生成物を水でクエンチして、それによりシアノピリジンの少なくとも一部が減少した気相を得るカラムと、
(iii)前記カラムから得られた気相から水の少なくとも一部を減少させて凝縮物を得る凝縮器と、
(iv)凝縮器から得られた気相が通る、少なくとも1つの熱交換器と
を含むデバイスである。
吸収セクションおよびストリッピングセクションであって、吸収セクションは、この吸収セクションを通過した液体がストリッピングセクションに入るようにストリッピングセクションの上方に位置している吸収セクションおよびストリッピングセクションと、
シアノピリジンを含む気体反応生成物をカラムに供給する手段であって、
吸収セクションは、前記気相を水溶液に接触させて、それによりシアノピリジンの少なくとも一部を水溶液に溶解させるように適合されており、
ストリッピングセクションは、吸収セクションから得られた前記水溶液をストリッピングガスでストリッピングするように適合されている
手段と、
カラムの底部にある、前記水溶液を抜き出す手段と
を含む。
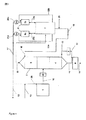
発明の方法を図1に示した部材を有する工業的デバイスで行った。リアクタにおいて、シアノピリジンをメチルピリジンからアンモ酸化反応で製造した。デバイス内の成分、温度、質量流量および圧力を表1に示すように各区画について調節した。熱交換器はスイッチ(24)によって動作モードから洗浄モードへ切り替えた。洗浄されていない熱交換器を通る質量流量は、他の熱交換器の洗浄中に、全体的な連続流が保持されるように調節する。表の見出しは、図1に示しかつ上述の対応する記載で説明した各連結部分の番号を示している。たとえば、流れ第14は最終生成物流である。この例から発明は非常に純粋なシアノピリジンを効率的な連続方法で製造することを可能にすることがわかる。
[1]シアノピリジンの製造方法であって、
(A)シアノピリジンを含む気体反応生成物をリアクタ(1)内で製造し、
(B)前記気体反応生成物をカラム(2)内で水を用いてクエンチし、前記シアノピリジンの少なくとも一部が減少した気相を得て、
(C)前記気相を凝縮器(7)に移し、ここで凝縮物を得て、前記気相は前記水の少なくとも一部が減少し、
(D)前記凝縮器(7)からの気相を少なくとも1つの熱交換器(9)に通す
方法。
[2]工程(D)において、前記少なくとも1つの熱交換器(9)は80℃〜350℃の温度を有する[1]に記載の方法。
[3]少なくとも1つの熱交換器(9)に蓄積する固体凝縮物の量をモニタし、予め定めた量の固体が蓄積したときに前記少なくとも1つの熱交換器(9)を洗浄する[1]および[2]の少なくとも一に記載の方法。
[4]前記洗浄を水または前記方法中に得られる水溶液を用いて行う[1]〜[3]の少なくとも一に記載の方法。
[5]前記気相を前記凝縮器(7)から前記少なくとも1つの熱交換器(9)に1分未満で移す[1]〜[4]の少なくとも一に記載の方法。
[6]工程(D)において、前記気相を並列に配置した少なくとも2つの熱交換器に通す[1]〜[5]の少なくとも一に記載の方法。
[7]少なくとも1つの熱交換器(9a)の洗浄中、少なくとも1つの熱交換器(9b)を洗浄しない[6]に記載の方法。
[8]工程(C)で得られた前記凝縮物を前記カラム(2)に供給するおよび/または工程(D)で前記少なくとも1つの熱交換器(9)を通過した前記気相の少なくとも一部を前記リアクタ(1)に供給する[1]〜[7]の少なくとも一に記載の方法。
[9]前記リアクタ(1)内で、アルキルピリジンの酸化性アンモノリシスを行う[1]〜[8]の少なくとも一に記載の方法。
[10]前記アルキルピリジンは3−メチルピリジンであり、前記シアノピリジンは3−シアノピリジンである[1]〜[9]の少なくとも一に記載の方法。
[11]前記方法は閉鎖式プロセスであり、工程(e)で前記カラム(2)から抜き出されない水相を還流する、および/または前記気相の少なくとも一部、好ましくは50体積%超を還流する[1]〜[10]の少なくとも一に記載の方法。
[12]工程(B)は
(a)吸収セクション(3)およびストリッピングセクション(4)を含むカラム(2)であって、前記吸収セクションは、前記吸収セクション(3)を通過した液体が前記ストリッピングセクション(4)に入るように前記ストリッピングセクションの上方に位置しているカラム(2)を用意することと、
(b)シアノピリジンを含む気体反応生成物を前記カラム(2)に供給することと、
(c)前記吸収セクション(3)において前記気相を水溶液に接触させて、前記シアノピリジンの少なくとも一部を前記水溶液に溶解させることと、
(d)前記ストリッピングセクション(4)において、工程(c)で前記吸収セクション(3)から得られた水溶液をストリッピングガスでストリッピングすることと、
(e)前記水溶液を前記カラム(2)の底部から抜き出すことと
を含む[1]〜[11]の少なくとも一に記載の方法。
[13]シアノピリジンの製造デバイスであって、
(i)シアノピリジンを含む気体反応生成物を製造するリアクタ(1)と、
(ii)前記気体反応生成物を水を用いてクエンチして、それにより前記シアノピリジンの少なくとも一部が減少した気相を得るカラム(2)と、
(iii)前記カラム(2)から得られた前記気相から前記水の少なくとも一部を減少させて凝縮物を得る凝縮器と、
(iv)前記凝縮器から得られた気相が通る、少なくとも1つの熱交換器(9)と
を含むデバイス。
[14]前記カラム(2)は
吸収セクション(3)およびストリッピングセクション(4)であって、前記吸収セクション(3)は、前記吸収セクション(3)を通過した液体が前記ストリッピングセクション(4)に入るように前記ストリッピングセクション(4)の上方に位置している吸収セクション(3)およびストリッピングセクション(4)と、
シアノピリジンを含む前記気体反応生成物を前記カラム(2)に供給する手段であって、
前記吸収セクション(3)は、前記気相を水溶液に接触させて、それにより前記シアノピリジンの少なくとも一部を前記水溶液に溶解させるように適合されており、
前記ストリッピングセクション(4)は、前記吸収セクション(3)から得られた前記水溶液をストリッピングガスでストリッピングするように適合している
手段と、
前記カラム(2)の底部にある、前記水溶液を抜き出す手段(11、14)と
を含む[13]に記載のデバイス。
[15]前記凝縮器(7)は含水凝縮物を前記凝縮器(7)から前記カラム(2)の前記吸収セクション(3)に供給する手段(16)、および/または前記少なくとも1つの熱交換器(9)を通過した気相を前記リアクタ(1)に移す手段(20、25)を含む[13]または[14]に記載のデバイス。
Claims (14)
- シアノピリジンの製造方法であって、
(A)シアノピリジンを含む気体反応生成物を、リアクタ(1)内でアルキルピリジンの酸化性アンモノリシスを行うことによって製造し、
(B)前記気体反応生成物をカラム(2)内で水を用いてクエンチし、前記シアノピリジンの少なくとも一部が減少した気相を得て、
(C)前記気相を凝縮器(7)に移し、ここで凝縮物を得て、前記気相は前記水の少なくとも一部が減少し、
(D)前記凝縮器(7)からの気相を少なくとも1つの熱交換器(9)に通す
方法。 - 工程(D)において、前記少なくとも1つの熱交換器(9)は80℃〜350℃の温度を有する請求項1に記載の方法。
- 少なくとも1つの熱交換器(9)に蓄積する固体凝縮物の量をモニタし、予め定めた量の固体が蓄積したときに前記少なくとも1つの熱交換器(9)を洗浄する請求項1または2に記載の方法。
- 前記洗浄を水または前記方法中に得られる水溶液を用いて行う請求項3に記載の方法。
- 前記気相を前記凝縮器(7)から前記少なくとも1つの熱交換器(9)に1分未満で移す請求項1〜4の何れか1項に記載の方法。
- 工程(D)において、前記気相を並列に配置した少なくとも2つの熱交換器に通す請求項1〜5の何れか1項に記載の方法。
- 少なくとも1つの熱交換器(9a)の洗浄中、少なくとも1つの熱交換器(9b)を洗浄しない請求項3または6に記載の方法。
- 工程(C)で得られた前記凝縮物を前記カラム(2)に供給するおよび/または工程(D)で前記少なくとも1つの熱交換器(9)を通過した前記気相の少なくとも一部を前記リアクタ(1)に供給する請求項1〜7の何れか1項に記載の方法。
- 前記アルキルピリジンは3−メチルピリジンであり、前記シアノピリジンは3−シアノピリジンである請求項1〜8の何れか1項に記載の方法。
- 工程(B)は
(a)吸収セクション(3)およびストリッピングセクション(4)を含むカラム(2)であって、前記吸収セクションは、前記吸収セクション(3)を通過した液体が前記ストリッピングセクション(4)に入るように前記ストリッピングセクションの上方に位置しているカラム(2)を用意することと、
(b)シアノピリジンを含む気体反応生成物を前記カラム(2)に供給することと、
(c)前記吸収セクション(3)において前記気相を水溶液に接触させて、前記シアノピリジンの少なくとも一部を前記水溶液に溶解させることと、
(d)前記ストリッピングセクション(4)において、工程(c)で前記吸収セクション(3)から得られた水溶液をストリッピングガスでストリッピングすることと、
(e)前記水溶液を前記カラム(2)の底部から抜き出すことと
を含む請求項1〜9の何れか1項に記載の方法。 - 前記方法は閉鎖式プロセスであり、工程(e)で前記カラム(2)から抜き出されない水相を還流する、および/または前記気相の少なくとも一部を還流する請求項10に記載の方法。
- 前記方法は閉鎖式プロセスであり、工程(e)で前記カラム(2)から抜き出されない水相を還流する、および/または前記気相の50体積%超を還流する請求項10に記載の方法。
- シアノピリジンの製造デバイスであって、
(i)シアノピリジンを含む気体反応生成物を、アルキルピリジンの酸化性アンモノリシスを行うことによって製造するリアクタ(1)と、
(ii)前記気体反応生成物を水を用いてクエンチして、それにより前記シアノピリジンの少なくとも一部が減少した気相を得るカラム(2)と、
(iii)前記カラム(2)から得られた前記気相から前記水の少なくとも一部を減少させて凝縮物を得る凝縮器と、
(iv)前記凝縮器から得られた気相が通る、少なくとも1つの熱交換器(9)と
を含み、
前記カラム(2)は
吸収セクション(3)およびストリッピングセクション(4)であって、前記吸収セクション(3)は、前記吸収セクション(3)を通過した液体が前記ストリッピングセクション(4)に入るように前記ストリッピングセクション(4)の上方に位置している吸収セクション(3)およびストリッピングセクション(4)と、
シアノピリジンを含む前記気体反応生成物を前記カラム(2)に供給する手段であって、
前記吸収セクション(3)は、前記気相を水溶液に接触させて、それにより前記シアノピリジンの少なくとも一部を前記水溶液に溶解させるように適合されており、
前記ストリッピングセクション(4)は、前記吸収セクション(3)から得られた前記水溶液をストリッピングガスでストリッピングするように適合している
手段と、
前記カラム(2)の底部にある、前記水溶液を抜き出す手段(11、14)と
を含むデバイス。 - 前記凝縮器(7)は含水凝縮物を前記凝縮器(7)から前記カラム(2)の前記吸収セクション(3)に供給する手段(16)、および/または前記少なくとも1つの熱交換器(9)を通過した気相を前記リアクタ(1)に移す手段(20、25)を含む請求項13に記載のデバイス。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US25237309P | 2009-10-16 | 2009-10-16 | |
| EP09013113.7 | 2009-10-16 | ||
| US61/252,373 | 2009-10-16 | ||
| EP09013113A EP2319834A1 (en) | 2009-10-16 | 2009-10-16 | Methods and devices for the production of aqueous solutions of cyanopyridines |
| PCT/EP2010/006204 WO2011045015A1 (en) | 2009-10-16 | 2010-10-12 | Methods and devices for the production of aqueous solutions of cyanopyridines |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2013507406A JP2013507406A (ja) | 2013-03-04 |
| JP2013507406A5 JP2013507406A5 (ja) | 2013-11-28 |
| JP5730882B2 true JP5730882B2 (ja) | 2015-06-10 |
Family
ID=41693013
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012533518A Expired - Fee Related JP5730882B2 (ja) | 2009-10-16 | 2010-10-12 | シアノピリジンの水溶液の製造方法およびデバイス |
Country Status (17)
| Country | Link |
|---|---|
| US (2) | US8680287B2 (ja) |
| EP (2) | EP2319834A1 (ja) |
| JP (1) | JP5730882B2 (ja) |
| KR (1) | KR101775887B1 (ja) |
| CN (1) | CN102648181B (ja) |
| AU (1) | AU2010306144B2 (ja) |
| BR (1) | BR112012012143A2 (ja) |
| CA (1) | CA2775025C (ja) |
| DK (1) | DK2488499T3 (ja) |
| EA (1) | EA020721B1 (ja) |
| ES (1) | ES2449915T3 (ja) |
| HK (1) | HK1169406A1 (ja) |
| IN (1) | IN2012DN02614A (ja) |
| MX (1) | MX2012004464A (ja) |
| MY (1) | MY156176A (ja) |
| PL (1) | PL2488499T3 (ja) |
| WO (1) | WO2011045015A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2319833A1 (en) * | 2009-10-16 | 2011-05-11 | Lonza Ltd. | Methods and devices for the production of aqueous solutions of cyanopyridines |
| CN103360304A (zh) * | 2013-07-27 | 2013-10-23 | 新乡市博科精细化工有限公司 | 2-甲基吡啶的加工生产装置 |
Family Cites Families (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2861299A (en) | 1958-11-25 | Apparatus for and method of cleaning lint cotton | ||
| GB790937A (en) * | 1955-08-23 | 1958-02-19 | Distillers Co Yeast Ltd | Process for the recovery of cyanopyridines |
| US2929811A (en) * | 1958-11-28 | 1960-03-22 | Bernard T Hofreiter | Starch products of stable viscosity |
| US3929811A (en) | 1973-11-15 | 1975-12-30 | Lummus Co | Production of pyridine nitriles and carboxylic acids |
| US4603207A (en) * | 1985-10-24 | 1986-07-29 | The Standard Oil Company | Conversion of a mixture of 3-methylpyridine and 3-methylpiperidine to 3-cyanopyridine |
| JPH0692368B2 (ja) * | 1986-02-06 | 1994-11-16 | 広栄化学工業株式会社 | ピリジン塩基の合成方法 |
| US4810794A (en) * | 1986-02-06 | 1989-03-07 | Koei Chemical Co., Ltd. | Process for producing pyridine bases |
| JP4161119B2 (ja) * | 1994-05-23 | 2008-10-08 | ロンザ リミテッド | アルキルピリジンの酸化アンモノリシス |
| JP3941121B2 (ja) * | 1994-05-23 | 2007-07-04 | ロンザ リミテッド | アルキルピリジンの酸化アンモノリシスのための触媒組成物 |
| CN1086311C (zh) | 1994-05-23 | 2002-06-19 | 隆萨股份公司 | 烷基吡啶的氧化氨解 |
| DE19504283A1 (de) | 1995-02-09 | 1996-08-14 | Degussa | Verfahren zur Herstellung von Cyanopyridinen und dafür geeignete Katalysatoren |
| ZA968485B (en) * | 1995-11-01 | 1997-05-20 | Lonza Ag | Process for preparing nicotinamide |
| JPH09136876A (ja) * | 1995-11-14 | 1997-05-27 | Nitto Chem Ind Co Ltd | 2−シアノ−3−メチルピリジンの回収法 |
| JP3712739B2 (ja) * | 1995-12-14 | 2005-11-02 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー | ポリエステルプレポリマーの合成方法 |
| US6118003A (en) * | 1998-01-29 | 2000-09-12 | Reilly Industries, Inc. | Processes for producing 3-cyanopyridine from 2-methyl-1,5-pentanediamine |
| US7608719B2 (en) * | 2001-09-07 | 2009-10-27 | Jubilant Organosys Limited | Process for the production of heteroaromatic nitriles improved catalyst therefor and a process for the production of said improved catalyst |
| DE10305650A1 (de) | 2003-02-12 | 2004-08-26 | Reilly Industries, Inc., Indianapolis | Verfahren zur Regenerierung von Mischoxidkatalysatoren |
| DE10335454A1 (de) | 2003-08-02 | 2005-02-24 | Reilly Industries, Inc., Indianapolis | Verfahren zur Herstellung von Cyanopyridinen und dafür geeignete Katalysatoren |
| CN100532361C (zh) | 2006-03-27 | 2009-08-26 | 中国石油化工股份有限公司上海石油化工研究院 | 3-氰基吡啶吸收方法 |
| JP5303463B2 (ja) * | 2006-08-08 | 2013-10-02 | ダウ アグロサイエンシィズ エルエルシー | シアノピリジンを含有する気体反応生成物を急冷するためのプロセス |
| EP2319833A1 (en) * | 2009-10-16 | 2011-05-11 | Lonza Ltd. | Methods and devices for the production of aqueous solutions of cyanopyridines |
-
2009
- 2009-10-16 EP EP09013113A patent/EP2319834A1/en not_active Ceased
-
2010
- 2010-10-12 IN IN2614DEN2012 patent/IN2012DN02614A/en unknown
- 2010-10-12 EP EP10768872.3A patent/EP2488499B1/en not_active Not-in-force
- 2010-10-12 ES ES10768872.3T patent/ES2449915T3/es active Active
- 2010-10-12 AU AU2010306144A patent/AU2010306144B2/en not_active Ceased
- 2010-10-12 MX MX2012004464A patent/MX2012004464A/es active IP Right Grant
- 2010-10-12 DK DK10768872.3T patent/DK2488499T3/da active
- 2010-10-12 JP JP2012533518A patent/JP5730882B2/ja not_active Expired - Fee Related
- 2010-10-12 KR KR1020127012206A patent/KR101775887B1/ko active IP Right Grant
- 2010-10-12 CA CA2775025A patent/CA2775025C/en not_active Expired - Fee Related
- 2010-10-12 MY MYPI2012001386A patent/MY156176A/en unknown
- 2010-10-12 EA EA201200596A patent/EA020721B1/ru not_active IP Right Cessation
- 2010-10-12 WO PCT/EP2010/006204 patent/WO2011045015A1/en active Application Filing
- 2010-10-12 BR BR112012012143A patent/BR112012012143A2/pt not_active Application Discontinuation
- 2010-10-12 CN CN201080046250.9A patent/CN102648181B/zh not_active Expired - Fee Related
- 2010-10-12 PL PL10768872T patent/PL2488499T3/pl unknown
- 2010-10-13 US US12/903,270 patent/US8680287B2/en not_active Expired - Fee Related
-
2012
- 2012-10-15 HK HK12110159.2A patent/HK1169406A1/zh not_active IP Right Cessation
-
2014
- 2014-01-27 US US14/165,219 patent/US9155977B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| ES2449915T3 (es) | 2014-03-21 |
| EP2319834A1 (en) | 2011-05-11 |
| EA201200596A1 (ru) | 2012-12-28 |
| US20140140901A1 (en) | 2014-05-22 |
| EA020721B1 (ru) | 2015-01-30 |
| WO2011045015A1 (en) | 2011-04-21 |
| CA2775025A1 (en) | 2011-04-21 |
| CN102648181B (zh) | 2015-11-25 |
| CA2775025C (en) | 2017-09-05 |
| IN2012DN02614A (ja) | 2015-09-04 |
| PL2488499T3 (pl) | 2014-05-30 |
| KR20120087150A (ko) | 2012-08-06 |
| BR112012012143A2 (pt) | 2015-09-08 |
| CN102648181A (zh) | 2012-08-22 |
| MY156176A (en) | 2016-01-15 |
| AU2010306144A1 (en) | 2012-05-10 |
| MX2012004464A (es) | 2012-05-08 |
| US20110092709A1 (en) | 2011-04-21 |
| KR101775887B1 (ko) | 2017-09-19 |
| JP2013507406A (ja) | 2013-03-04 |
| AU2010306144B2 (en) | 2016-03-31 |
| HK1169406A1 (zh) | 2013-01-25 |
| US9155977B2 (en) | 2015-10-13 |
| US8680287B2 (en) | 2014-03-25 |
| DK2488499T3 (da) | 2014-03-24 |
| EP2488499B1 (en) | 2013-12-18 |
| EP2488499A1 (en) | 2012-08-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5730882B2 (ja) | シアノピリジンの水溶液の製造方法およびデバイス | |
| JP5784615B2 (ja) | シアノピリジンの製造方法およびデバイス | |
| JP5364884B2 (ja) | (メタ)アクリロニトリルの製造方法 | |
| JP4426869B2 (ja) | 蒸留塔の洗浄方法 | |
| JP4147015B2 (ja) | 気体の凝縮方法 | |
| RU2647593C2 (ru) | Способ отделения акролеина от технологического газа, образующегося при гетерогенно-катализируемом окислении пропена | |
| RU2599247C1 (ru) | Способ непрерывного промышленного получения глиоксаля | |
| JP2013507406A5 (ja) | ||
| TW201035007A (en) | Process for production of p-dichlorobenzene | |
| EA005130B1 (ru) | Способ получения меламина из мочевины | |
| JP2005298384A (ja) | (メタ)アクリル酸又は/かつ(メタ)アクロレインを含む反応ガスの冷却方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131010 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20131010 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20141104 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150204 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150310 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150408 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5730882 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |