JP4937587B2 - 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 - Google Patents
液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 Download PDFInfo
- Publication number
- JP4937587B2 JP4937587B2 JP2006008538A JP2006008538A JP4937587B2 JP 4937587 B2 JP4937587 B2 JP 4937587B2 JP 2006008538 A JP2006008538 A JP 2006008538A JP 2006008538 A JP2006008538 A JP 2006008538A JP 4937587 B2 JP4937587 B2 JP 4937587B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- alkyl group
- structural unit
- carbon atoms
- polymer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/039—Macromolecular compounds which are photodegradable, e.g. positive electron resists
- G03F7/0392—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition
- G03F7/0395—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition the macromolecular compound having a backbone with alicyclic moieties
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/039—Macromolecular compounds which are photodegradable, e.g. positive electron resists
- G03F7/0392—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition
- G03F7/0397—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition the macromolecular compound having an alicyclic moiety in a side chain
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/20—Exposure; Apparatus therefor
- G03F7/2041—Exposure; Apparatus therefor in the presence of a fluid, e.g. immersion; using fluid cooling means
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S430/00—Radiation imagery chemistry: process, composition, or product thereof
- Y10S430/1053—Imaging affecting physical property or radiation sensitive material, or producing nonplanar or printing surface - process, composition, or product: radiation sensitive composition or product or process of making binder containing
- Y10S430/1055—Radiation sensitive composition or product or process of making
- Y10S430/106—Binder containing
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S430/00—Radiation imagery chemistry: process, composition, or product thereof
- Y10S430/1053—Imaging affecting physical property or radiation sensitive material, or producing nonplanar or printing surface - process, composition, or product: radiation sensitive composition or product or process of making binder containing
- Y10S430/1055—Radiation sensitive composition or product or process of making
- Y10S430/106—Binder containing
- Y10S430/111—Polymer of unsaturated acid or ester
Landscapes
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- General Physics & Mathematics (AREA)
- Materials For Photolithography (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Exposure Of Semiconductors, Excluding Electron Or Ion Beam Exposure (AREA)
- Exposure And Positioning Against Photoresist Photosensitive Materials (AREA)
Description
レジストとしては、高解像性が達成される上に、放射線の照射により発生した酸の触媒反応、連鎖反応が利用でき、量子収率が1以上で、しかも高感度が達成できる化学増幅型レジストが注目され、盛んに開発が行われている。
これまで、化学増幅型レジストのベース樹脂としては、KrFエキシマレーザー(248nm)に対する透明性が高いポリヒドロキシスチレン(PHS)やその水酸基を酸解離性の溶解抑制基で保護した樹脂(PHS系樹脂)や、ArFエキシマレーザー(193nm付近)に対する透明性に優れる(メタ)アクリル酸エステルから誘導される構成単位を主鎖に有する樹脂(アクリル系樹脂)のカルボキシ基を酸解離性溶解抑制基で保護した樹脂などが一般的に用いられている。なお、「(メタ)アクリル酸エステル」とは、α位に水素原子が結合したアクリル酸エステルと、α位にメチル基が結合したメタクリル酸エステルの一方あるいは両方を意味する。
また、酸解離性溶解抑制基としては、たとえば、エトキシエチル基等のアセタール基、tert−ブチル基等の3級アルキル基、tert−ブトキシカルボニル基、tert−ブトキシカルボニルメチル基などが知られている。たとえば、従来ArFレジスト組成物の樹脂成分中の酸解離性溶解抑制基を有する構成単位としては、下記特許文献1に示されるように、2−アルキル−2−アダマンチル(メタ)アクリレート等の(メタ)アクリル酸の3級エステル化合物から誘導される構成単位が一般的に用いられている。
しかし、光源波長の短波長化は高額な新たな露光装置が必要となる。また、高NA化では、解像度と焦点深度幅がトレードオフの関係にあるため、解像度を上げても焦点深度幅が低下するという問題がある。
このような液浸露光によれば、同じ露光波長の光源を用いても、より短波長の光源を用いた場合や高NAレンズを用いた場合と同様の高解像性を達成でき、しかも焦点深度幅の低下もないといわれている。また、液浸露光は、既存の露光装置を用いて行うことができる。そのため、液浸露光は、低コストで、高解像性で、かつ焦点深度幅にも優れるレジストパターンの形成を実現できると予想され、多額な設備投資を必要とする半導体素子の製造において、コスト的にも、解像度等のリソグラフィー特性的にも、半導体産業に多大な効果を与えるものとして大変注目されている。現在、液浸媒体としては、主に水が検討されている。
物質溶出を抑制する手段として、たとえば、レジスト膜の液浸媒体に対する耐性(液浸媒体耐性)を高めることが考えられる。現在、液浸媒体としては、主に水等の水性溶剤が検討されていることから、レジスト膜の疎水性を高めることが液浸媒体耐性向上に有効ではないかと推測される。
しかしながら、レジスト膜の疎水性を高めるためにレジストの組成を変更することは、通常、リソグラフィー特性を悪化させてしまう。そのため、物質溶出の抑制とリソグラフィー特性との両立は困難である。
本発明は、上記事情に鑑みてなされたものであって、浸漬露光時の物質溶出の抑制とリソグラフィー特性とを両立できる液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法を提供することを目的とする。
すなわち、本発明の第一の態様は、酸解離性溶解抑制基を有し、酸の作用によりアルカリ可溶性が増大する樹脂成分(A)と、露光により酸を発生する酸発生剤成分(B)とを含む液浸露光用ポジ型レジスト組成物であって、
前記樹脂成分(A)が、主鎖環状型重合体(A1)と、α位の炭素原子にハロゲン原子、炭素原子数1〜5のアルキル基または炭素原子数1〜5のハロゲン化アルキル基が結合していてもよく、カルボキシ基の水素原子が有機基で置換されていてもよいアクリル酸から誘導される構成単位(a)を主鎖に有する非主鎖環状型重合体(A2)とを含有し、
前記非主鎖環状型重合体(A2)が、α位の炭素原子にハロゲン原子、炭素原子数1〜5のアルキル基または炭素原子数1〜5のハロゲン化アルキル基が結合していてもよいアクリル酸エステルから誘導される構成単位であって下記一般式(p1)で表される酸解離性溶解抑制基(p1)を有する構成単位(a1)を有することを特徴とする液浸露光用ポジ型レジスト組成物である。
「アルキル基」は、特に断りがない限り、直鎖状、分岐鎖状および環状の1価の飽和炭化水素基を包含するものとする。
「低級アルキル基」は、炭素原子数1〜5のアルキル基である。
「脂肪族」とは、芳香族に対する相対的な概念であって、芳香族性を持たない基、化合物等を意味するものと定義する。「脂肪族環式基」は、芳香族性を持たない単環式基または多環式基であることを示す。
「露光」は放射線の照射全般を含む概念とする。
≪液浸露光用ポジ型レジスト組成物≫
本発明の液浸露光用ポジ型レジスト組成物は、酸解離性溶解抑制基を有し、酸の作用によりアルカリ可溶性が増大する樹脂成分(A)(以下、(A)成分という)と、露光(放射線の照射)により酸を発生する酸発生剤成分(以下、(B)成分という)とを含むものである。
(A)成分は、酸解離性溶解抑制基を有するため、露光前はアルカリ不溶性であり、露光により前記(B)成分から発生した酸が作用すると、酸解離性溶解抑制基が解離し、これによって(A)成分全体のアルカリ可溶性が増大する。そのため、レジストパターンの形成において、レジストに対して選択的露光を行うと、または露光に加えて露光後加熱(PEB)を行うと、露光部はアルカリ可溶性へ転じる一方で、未露光部はアルカリ不溶性のまま変化しないので、アルカリ現像することによりポジ型のレジストパターンが形成できる。
(A)成分は、主鎖環状型重合体(A1)(以下、重合体(A1)ということがある)と、アクリル酸から誘導される構成単位(a)を主鎖に有する非主鎖環状型重合体(A2)(以下、重合体(A2)ということがある)とを含有する。
以下、各重合体について詳細に説明する。
本発明において、「主鎖環状型重合体」とは、該重合体を構成する構成単位が、単環または多環式の環構造を有し、該環構造の環上の少なくとも1つ、好ましくは2つ以上の炭素原子が主鎖を構成する構成単位(以下、主鎖環状型構成単位という)を有することを意味する。
かかる構造の重合体(A1)を含有することにより、液浸露光時の溶出が抑制されることに加えて、さらに、レジストとした際のエッチング耐性が向上する。これは、主鎖環状型構成単位を有することにより、炭素密度が高くなっているためと推測される。
ポリシクロオレフィンは、多環式の炭化水素環上に1個の二重結合(オレフィン二重結合)を有するものであり、「ポリシクロオレフィンから誘導される構成単位」とは、当該オレフィン二重結合が開裂して構成される構成単位を意味する。
ポリシクロオレフィンにおける炭化水素環は、炭素数が6〜12であることが好ましく、炭素数7〜12であることがさらに好ましく、炭素数7〜10が最も好ましい。
ポリシクロオレフィンにおける炭化水素環は、置換基を有していてもよいし、有していなくてもよい。該置換基としては、炭素数1〜5の低級アルキル基、フッ素原子、フッ素原子で置換された炭素数1〜5のフッ素化低級アルキル基、酸素原子(=O)等が挙げられる。
炭化水素環の具体例としては、例えば、置換基を有していてもよく、有していなくてもよいビシクロアルカン、トリシクロアルカン、テトラシクロアルカンなどのポリシクロアルカンなどを例示できる。具体的には、アダマンタン、ノルボルナン、イソボルナン、トリシクロデカン、テトラシクロドデカンなどが挙げられる。特に、エッチング耐性の高さ、入手の容易さ等の点で、ノルボルナン、テトラシクロドデカンが好ましい。
置換基の数は、1〜3が好ましく、1が特に好ましい。
置換基の結合位置は、主鎖を構成する炭素原子から最も離れた位置の炭素原子が好ましく、たとえばa”が0である場合、置換基は、その環骨格(ビシクロ[2.2.1]−2−ヘプタン(ノルボルナン))の5位および/または6位に結合していることが好ましく、a”が1である場合、置換基は、その環骨格(テトラシクロ[4.4.0.12.5.1.7.10]−3−ドデカン)の8位および/または9位に結合していることが好ましい。
フッ素原子を有する重合体としては、上記一般式(a’)で表される基本骨格を構成する炭素原子に結合した水素原子の一部がフッ素原子またはフッ素原子を有する基で置換された構成単位を有するものが挙げられる。
フッ素原子を有する基としては、たとえば、水素原子の一部または全部がフッ素原子で置換されたアルキル基;後述する構成単位(a’3)においてR64(アルカリ可溶性基を有する有機基)として例示したもののうち、フッ素原子を含む基(たとえば後述する一般式(a’31)で表される基)等が例示できる。
酸解離性溶解抑制基は、解離前は重合体(A1)全体をアルカリ不溶とするアルカリ溶解抑制性を有するとともに、解離後はこの重合体(A1)全体をアルカリ可溶性へ変化させるものであれば、これまで、化学増幅型レジスト用のベース樹脂の酸解離性溶解抑制基として提案されているものを使用することができ、一般的には、カルボキシ基と環状または鎖状の第3級アルキルエステルを形成する基;後述する一般式(p1)で表される基などが広く知られている。
なお、前記鎖状または環状のアルキル基は置換基を有していてもよい。
以下、カルボキシ基と第3級アルキルエステルを構成することにより、酸解離性となっている基を、便宜上、「第3級アルキルエステル型酸解離性溶解抑制基」という。
第3級アルキルエステル型酸解離性溶解抑制基としては、たとえば、脂肪族分岐鎖状酸解離性溶解抑制基、脂肪族環式基を含有する酸解離性溶解抑制基が挙げられる。
脂肪族分岐鎖状酸解離性溶解抑制基としては、炭素数4〜8の第3級アルキル基が好ましく、具体的にはtert−ブチル基、tert−アミル、tert−ヘプチル基、基等が挙げられる。
「脂肪族環式基を含有する酸解離性溶解抑制基」としては、後述する一般式(p1)におけるYの「脂肪族環式基」として例示するものと同様の脂肪族環式基の環骨格上に第3級炭素原子を有する基(たとえば1−メチル−1−シクロヘキシル基、1−エチル−1−シクロヘキシル基、2−メチル−2−アダマンチル基、2−エチル−2−アダマンチル基等);脂肪族環式基に、第3級炭素原子を有する分岐鎖状アルキレン基(好ましくは炭素数3〜15の分岐鎖状アルキレン基)が結合した基(たとえばジアルキルメチレン基に1−アダマンチル基が結合した基等)などが挙げられる。
「環状または鎖状のアルコキシアルキルエステル」とは、カルボキシ基の水素原子がアルコキシアルキル基で置換されることによりエステルを形成しており、そのカルボニルオキシ基(−C(O)−O−)の末端の酸素原子に前記アルコキシアルキル基が結合している構造を示す。
かかるアセタール型酸解離性溶解抑制基においては、酸が作用すると、アセタール型酸解離性溶解抑制基と、当該アセタール型酸解離性溶解抑制基が結合した酸素原子との間で結合が切断される。
中でも、本発明の効果に優れることから、重合体(A1)は、下記構成単位(a’1)を有することが好ましい。
構成単位(a’1)は、下記一般式(a’1)で表される構成単位である。
a”は0または1であり、工業上入手が容易であることを考慮すると、0であることが好ましい。
b”は1〜3の整数であり、合成上、および工業上入手が容易であることを考慮すると、1又は2であることが好ましい。
本発明においては、特に、式(a’1)におけるR61がエチル基であり、b”が2であることが好ましい。すなわち、酸解離性溶解抑制基として、1−エチル−1−シクロヘキシル基を有することが、上記効果に特に優れるため、好ましい。
重合体(A1)中、構成単位(a’1)の割合は、重合体(A1)を構成する全構成単位の合計に対して、5〜80モル%が好ましく、10〜50モル%がより好ましく、10〜30モル%がさらに好ましい。下限値以上とすることによって、レジスト組成物とした際にパターンを得ることができ、上限値以下とすることにより他の構成単位とのバランスをとることができる。
重合体(A1)は、上記構成単位(a’1)に加えて、さらに下記一般式(a’2)で表される構成単位(a’2)を有することが好ましい。
重合体(A1)が構成単位(a’2)を有することにより、解像性等のリソグラフィー特性が向上する。これは、構成単位(a’2)により重合体(A1)全体の親水性が高まり、重合体(A1)をレジスト組成物とした際に、該レジスト組成物を用いて得られるレジスト膜とアルカリ現像液との親和性が高まるためと推測される。
式(a’2)中、a”は上記式(a’1)におけるa”と同様である。
R62およびR63は、それぞれ独立に、水素原子または低級アルキル基であり、工業上入手が容易であること等を考慮すると、水素原子が好ましい。
R62およびR63の低級アルキル基としては、直鎖でも分岐でもよく、炭素数1〜5のアルキル基が好ましく、たとえばメチル基、エチル基、プロピル基、イソプロピル基、n−ブチル基、イソブチル基、ペンチル基、イソペンチル基、ネオペンチル基等が挙げられる。
重合体(A1)中、構成単位(a’2)の割合は、重合体(A1)の全構成単位の合計に対して、5〜80モル%が好ましく、10〜50モル%がより好ましく、10〜30モル%がさらに好ましい。下限値以上とすることにより構成単位(a’2)を有する効果に優れ、上限値以下とすることにより他の構成単位とのバランスをとることができる。
重合体(A1)は、上記構成単位(a’1)および(a’2)に加えて、さらに下記一般式(a’3)で表される構成単位(a’3)を有することが好ましい。構成単位(a’3)を有することにより、浸漬露光時の溶出抑制効果がさらに向上する。これは、アルカリ可溶性基、特にフッ素原子を含むアルカリ可溶性基を有することにより、後述する接触角及び後退角がいっそう向上するするためと考えられる。また、構成単位(a’3)を有することにより、解像性、基板密着性等も向上する。
R64はアルカリ可溶性基を有する有機基である。
ここで、本明細書および特許請求の範囲において、有機基は、少なくとも炭素原子を含む基を意味する。
アルカリ可溶性基は、当該重合体のアルカリ溶解性を高める基であり、フェノール性水酸基と同程度の、比較的小さいpKa(Kaは酸解離定数)を有する基が好ましく、特に限定するものではないが、pKaが6〜12の範囲内の基が好適である。
アルカリ可溶性基として、より具体的には、水酸基(フェノール性水酸基、アルコール性水酸基)、カルボキシ基等の、末端に−OHを有する基が挙げられる。好ましいアルカリ可溶性基としては、例えば、アルコール性水酸基;ヒドロキシアルキル基において水酸基が結合した炭素原子(α位の炭素原子)に結合した水素原子が電子吸引性基で置換された基(電子吸引性基置換ヒドロキシアルキル基);カルボキシ基等が挙げられる。中でも、電子吸引性基置換ヒドロキシアルキル基またはカルボキシ基が好ましい。
ヒドロキシ基の数は特に限定するものではないが、1つであることが好ましい。
電子吸引性基としては、ハロゲン原子またはハロゲン化アルキル基等が挙げられる。
ハロゲン原子としては、フッ素原子、塩素原子等が挙げられ、フッ素原子が好ましい。
ハロゲン化アルキル基において、ハロゲンは前記ハロゲン原子と同様であり、アルキル基は、炭素数が例えば1〜5程度の低級アルキル基が好ましく、より好ましくはメチル基またはエチル基、最も好ましくはメチル基である。ハロゲン化アルキル基として、具体的には、例えばトリフルオロメチル基、ジフルオロメチル基、モノフルオロメチル基、パーフルオロエチル基等が挙げられ、特にトリフルオロメチル基が好ましい。
電子吸引性基の数は、1または2であり、好ましくは2である。
ここでのハロゲン原子、又はハロゲン化アルキル基とは前記したものと同様であり、アルキル基としては、メチル基、エチル基、プロピル基などの低級アルキル基が挙げられる。
これらの中でも、電子吸引性基がフッ素原子又はフッ素化アルキル基である基(フッ素化されたヒドロキシアルキル基)が好ましく、特にはR71及びR72がともにフッ素化アルキル基であるものが好ましく、アルキル基の水素原子の全部がフッ素で置換されたパーフルオロアルキル基が好ましい。
R64としては、特に、浸漬露光時の物質溶出の抑制効果に優れることから、下記一般式(a’31)で表される基が好ましい。
また、d”およびe”は、それぞれ独立して、1〜5の整数であり、より好ましくは1〜3の整数であり、特にd”およびe”が1であるものが、合成上、及び効果において優れており、好ましい。
本発明の重合体(A1)中、構成単位(a’3)の割合は、重合体(A1)の全構成単位の合計に対して、10〜90モル%が好ましく、20〜80モル%がより好ましく、50〜70モル%がさらに好ましい。下限値以上とすることにより、構成単位(a’3)を有する効果に優れ、上限値以下とすることにより他の構成単位とのバランスをとることができる。
重合体(A1)は、本発明の効果を損なわない範囲で、前記構成単位(a’1)〜(a’3)以外の構成単位(a’4)を含んでいてもよい。
構成単位(a’4)としては、上述の構成単位(a’1)〜(a’3)に分類されない他の構成単位であって、構成単位(a’1)〜(a’3)を誘導するモノマーと共重合可能なモノマーから誘導される構成単位であれば特に限定するものではない。
かかる構成単位(a’4)としては、公知のエチレン性二重結合を有する化合物から誘導される構成単位を目的に応じて任意に用いることができる。
また、置換基として多環の脂環式基を有するポリシクロオレフィンから誘導される構成単位としては、上記置換基を有さないポリシクロオレフィンから誘導される構成単位の環上に、置換基として、例えば、トリシクロデカニル基、アダマンチル基、テトラシクロドデカニル基等の多環式基を有する構成単位が挙げられる。
重合体(A1)が構成単位(a’1)および構成単位(a’3)を含み、かつ構成単位(a’2)を含まない二元系の重合体(ただし構成単位(a’4)を含んでもよい)である場合、各構成単位の割合(モル比)は、本発明の効果および重合体の合成における制御がしやすい点で、重合体(A1)を構成する全構成単位に対し、構成単位(a’1)が5〜80モル%であることが好ましく、10〜60モル%であることがより好ましく、構成単位(a’3)が5〜95モル%であることが好ましく、10〜60モル%であることがより好ましい。
また、重合体(A1)が構成単位(a’1)〜(a’3)を含む三元系の重合体(ただし構成単位(a’4)を含んでもよい)である場合、各構成単位の割合(モル比)は、重合体(A1)を構成する全構成単位に対し、構成単位(a’1)が5〜80モル%であることが好ましく、10〜50モル%であることがより好ましく、構成単位(a’2)が5〜80モル%であることが好ましく、10〜50モル%であることがより好ましく、構成単位(a’3)が10〜90モル%であることが好ましく、20〜80モル%であることがより好ましい。これにより、エッチング耐性およびレジストパターン形状に優れ、さらに解像性等のリソグラフィー特性にも優れたものとなる。
また、重合体(A1)には、上記重合の際に、たとえばHS−CH2−CH2−CH2−C(CF3)2−OHのような連鎖移動剤を併用して用いることにより、末端に−C(CF3)2−OH基を導入してもよい。このように、アルキル基の水素原子の一部がフッ素原子で置換されたヒドロキシアルキル基が導入された共重合体は、現像欠陥の低減やLER(ラインエッジラフネス:ライン側壁の不均一な凹凸)の低減に有効である。
下限値は、特に限定するものではないが、解像性、有機溶剤への溶解性等を考慮すると、3000以上が好ましく、5000以上がより好ましい。
重合体(A2)は、アクリル酸から誘導される構成単位(a)を主鎖に有する非主鎖環状型重合体である。
ここで、本明細書および特許請求の範囲において、「非主鎖環状型重合体」とは、該重合体が、上述した「主鎖環状型重合体」ではないことを意味する。すなわち、非主鎖環状型重合体の主鎖を構成する炭素原子として、環を構成する炭素原子が含まれないことを意味する。
「アクリル酸」は、狭義のアクリル酸(CH2=CHCOOH)、及びその水素原子の一部または全部が他の基または原子で置換された誘導体を含む概念とする。
アクリル酸の誘導体としては、たとえば、狭義のアクリル酸のα位の炭素原子に置換基(水素原子以外の原子または基)が結合しているα置換アクリル酸、これらのアクリル酸のカルボキシ基の水素原子が有機基で置換されたアクリル酸エステル等が挙げられる。
アクリル酸のα位(α位の炭素原子)とは、特に断りがない限り、カルボニル基が結合している炭素原子のことである。
α置換アクリル酸の置換基としては、ハロゲン原子、低級アルキル基、ハロゲン化低級アルキル基等が挙げられる。
α位の置換基としてのハロゲン原子としては、フッ素原子、塩素原子、臭素原子、ヨウ素原子等が挙げられ、特にフッ素原子が好ましい。
α位の置換基としての低級アルキル基として、具体的には、メチル基、エチル基、プロピル基、イソプロピル基、n−ブチル基、イソブチル基、tert−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基などの低級の直鎖状または分岐状のアルキル基が挙げられる。
アクリル酸のα位に結合しているのは、水素原子、ハロゲン原子、低級アルキル基またはハロゲン化低級アルキル基であることが好ましく、水素原子、フッ素原子、低級アルキル基またはフッ素化低級アルキル基であることがより好ましく、工業上の入手の容易さから、水素原子またはメチル基であることが最も好ましい。
「アクリル酸から誘導される構成単位」とは、アクリル酸のエチレン性二重結合が開裂して構成される構成単位を意味する。
「アクリル酸エステルから誘導される構成単位」とは、アクリル酸エステルのエチレン性二重結合が開裂して構成される構成単位を意味する。
構成単位(a)としては、下記一般式(a)で表される構成単位が挙げられる。
Xの有機基としては、特に限定されず、たとえば後述する構成単位(a1)〜(a4)等において挙げた構成単位において、アクリル酸エステルのエステル側鎖部に結合した基(酸解離性溶解抑制基、ラクトン環を有する基、極性基含有脂肪族炭化水素基、多環式の脂肪族炭化水素基等)が挙げられる。
ここで、「構成単位(a)のみからなる」とは、重合体(A2)の主鎖が、構成単位(a)のみから構成されており、他の構成単位を含まないことを意味する。
重合体(A2)は、下記一般式(p1)で表される酸解離性溶解抑制基(p1)を有するアクリル酸エステルから誘導される構成単位(a1)を有する必要がある。かかる構成単位を有することにより、良好なリソグラフィー特性が得られる。
R1’,R2’の低級アルキル基としては、上記Rの低級アルキル基と同様のものが挙げられ、メチル基またはエチル基が好ましく、メチル基が最も好ましい。
本発明においては、R1’,R2’のうち少なくとも1つが水素原子であることが好ましい。すなわち、酸解離性溶解抑制基(p1)が、下記一般式(p1−1)で表される基であることが好ましい。
Yの脂肪族環式基としては、従来ArFレジスト等において多数提案されている単環又は多環式の脂肪族環式基の中から適宜選択して用いることができる。
脂肪族環式基は、飽和又は不飽和のいずれでもよいが、飽和であることが好ましい。
脂肪族環式基としては、例えば、炭素数5〜8の単環式基、炭素数6〜16の多環式基が挙げられる。炭素数5〜8の脂肪族単環式基としては、モノシクロアルカンから1個以上の水素原子を除いた基が例示でき、具体的には、シクロペンタン、シクロヘキサンなどから1個以上の水素原子を除いた基などが挙げられる。炭素数6〜16の脂肪族多環式基としては、ビシクロアルカン、トリシクロアルカン、テトラシクロアルカンなどから1個以上の水素原子を除いた基などを例示でき、具体的には、アダマンタン、ノルボルナン、イソボルナン、トリシクロデカン、テトラシクロドデカンなどのポリシクロアルカンから1個以上の水素原子を除いた基などが挙げられる。これらの中でも、脂肪族多環式基が好ましく、工業上、アダマンチル基、ノルボルニル基、テトラシクロドデカニル基が好ましく、特にアダマンチル基が好ましい。
脂肪族環式基は、置換基を有していてもよく、有していなくてもよい。該置換基としては、炭素数1〜5の低級アルキル基、フッ素原子、フッ素原子で置換された炭素数1〜5のフッ素化低級アルキル基、酸素原子(=O)等が挙げられる。脂肪族環式基は、上記の中でも、置換基として、炭素数1〜5の低級アルキル基を有することが好ましく、メチル基を有することが特に好ましい。
脂肪族環式基は、置換基を除いた基本の環が、炭素及び水素のみで構成される炭化水素基(脂環式基)であってもよく、脂環式基の環を構成する炭素原子の一部がヘテロ原子(酸素原子、窒素原子等)で置換された複素環式基であってもよく、好ましくは脂環式基である。
Yの脂肪族環式基として、具体的には、下記化学式で示される構造のものが例示できる。
酸解離性溶解抑制基(p1)は、通常、アクリル酸のカルボキシ基末端の水素原子と置換して(カルボニルオキシ基(−C(O)−O−)末端の酸素原子に結合して)エステルを形成している。
構成単位(a1)としては、下記一般式(a1−0−1)で表される構成単位と、下記一般式(a1−0−2)で表される構成単位からなる群から選ばれる1種以上が好ましい。
X1は、酸解離性溶解抑制基(p1)である。
Y2は好ましくは炭素数1〜4のアルキレン基又は2価の脂肪族環式基である。
Y2は2価の脂肪族環式基である場合、水素原子が2個以上除かれた基が用いられる以外は、前記「脂肪族環式基」の説明と同様のものを用いることができる。
構成単位(a1)としては、特に前記一般式(a1−2)で表される構成単位が好ましく、式(a1−2−36)〜(a1−2−39)で表される構成単位がより好ましく、式(a1−2−36)または(a1−2−37)で表される構成単位が最も好ましい。
重合体(A2)は、構成単位(a1)に加えて、ラクトン含有環式基を含むアクリル酸エステルから誘導される構成単位(a2)を有することが好ましい。
ここで、ラクトン含有環式基とは、−O−C(O)−構造を含むひとつの環(ラクトン環)を含有する環式基を示す。ラクトン環をひとつの目の環として数え、ラクトン環のみの場合は単環式基、さらに他の環構造を有する場合は、その構造に関わらず多環式基と称する。
構成単位(a2)のラクトン環式基は、重合体(A2)をレジスト膜の形成に用いた場合に、レジスト膜の基板への密着性を高めたり、現像液との親水性を高めたりするうえで有効なものである。
具体的には、ラクトン含有単環式基としては、γ−ブチロラクトンから水素原子1つを除いた基が挙げられる。また、ラクトン含有多環式基としては、ラクトン環を有するビシクロアルカン、トリシクロアルカン、テトラシクロアルカンから水素原子一つを除いた基が挙げられる。
R’の低級アルキル基としては、前記構成単位(a1)におけるRの低級アルキル基と同じである。
一般式(a2−1)〜(a2−5)中、R’は、工業上入手が容易であること等を考慮すると、水素原子が好ましい。
以下に、前記一般式(a2−1)〜(a2−5)の具体的な構成単位を例示する。
重合体(A2)中の構成単位(a2)の割合は、重合体(A2)を構成する全構成単位の合計に対して、5〜70モル%が好ましく、10〜60モル%がより好ましく、20〜60モル%がさらに好ましい。下限値以上とすることにより構成単位(a2)を含有させることによる効果が充分に得られ、上限値以下とすることにより他の構成単位とのバランスをとることができる。
重合体(A2)は、構成単位(a1)に加えて、または構成単位(a1)および(a2)に加えて、極性基含有脂肪族炭化水素基を含むアクリル酸エステルから誘導される構成単位(a3)を有することが好ましい。構成単位(a3)を有することにより、重合体(A2)の親水性が高まり、現像液との親和性が高まって、露光部でのアルカリ溶解性が向上し、解像性の向上に寄与する。
極性基としては、水酸基、シアノ基、カルボキシ基、アルキル基の水素原子の一部がフッ素原子で置換されたヒドロキシアルキル基等が挙げられ、特に水酸基が好ましい。
脂肪族炭化水素基としては、炭素数1〜10の直鎖状または分岐状の炭化水素基(好ましくはアルキレン基)や、多環式の脂肪族炭化水素基(多環式基)が挙げられる。該多環式基としては、例えばArFエキシマレーザー用レジスト組成物用の樹脂において、多数提案されているものの中から適宜選択して用いることができる。該多環式基の炭素数は7〜30であることが好ましい。
その中でも、水酸基、シアノ基、カルボキシ基、またはアルキル基の水素原子の一部がフッ素原子で置換されたヒドロキシアルキル基を含有する脂肪族多環式基を含むアクリル酸エステルから誘導される構成単位がより好ましい。該多環式基としては、ビシクロアルカン、トリシクロアルカン、テトラシクロアルカンなどから1個以上の水素原子を除いた基などを例示できる。具体的には、アダマンタン、ノルボルナン、イソボルナン、トリシクロデカン、テトラシクロドデカンなどのポリシクロアルカンから1個以上の水素原子を除いた基などが挙げられる。これらの多環式基の中でも、アダマンタンから2個以上の水素原子を除いた基、ノルボルナンから2個以上の水素原子を除いた基、テトラシクロドデカンから2個以上の水素原子を除いた基が工業上好ましい。
jは1であることが好ましく、特に水酸基がアダマンチル基の3位に結合しているものが好ましい。
重合体(A2)中、構成単位(a3)の割合は、当該重合体(A2)を構成する全構成単位に対し、5〜50モル%であることが好ましく、5〜40モル%がより好ましく、5〜25モル%がさらに好ましい。
重合体(A2)は、本発明の効果を損なわない範囲で、上記構成単位(a1)〜(a3)以外の他の構成単位を含んでいてもよい。かかる構成単位としては、主鎖環状型構成単位ではなく、かつ上述の構成単位(a1)〜(a3)に分類されない他の構成単位であれば特に限定するものではなく、ArFエキシマレーザー用、KrFエキシマレーザー用(好ましくはArFエキシマレーザー用)等のレジスト用樹脂に用いられるものとして従来から知られている多数のものが使用可能である。
構成単位(a4)における多環式基としては、例えば、前記の構成単位(a1)の場合に例示したものと同様のものを例示することができ、ArFエキシマレーザー用、KrFエキシマレーザー用(好ましくはArFエキシマレーザー用)等のレジスト組成物の樹脂成分に用いられるものとして従来から知られている多数のものが使用可能である。
特にトリシクロデカニル基、アダマンチル基、テトラシクロドデカニル基、イソボルニル基、ノルボルニル基から選ばれる少なくとも1種以上であると、工業上入手し易いなどの点で好ましい。これらの多環式基は、炭素数1〜5の直鎖又は分岐状のアルキル基で置換されていてもよい。
構成単位(a4)として、具体的には、下記一般式(a4−1)〜(a4−5)の構造のものを例示することができる。
また、重合体(A2)には、上記重合の際に、たとえばHS−CH2−CH2−CH2−C(CF3)2−OHのような連鎖移動剤を併用して用いることにより、末端に−C(CF3)2−OH基を導入してもよい。このように、アルキル基の水素原子の一部がフッ素原子で置換されたヒドロキシアルキル基が導入された共重合体は、現像欠陥の低減やLER(ラインエッジラフネス:ライン側壁の不均一な凹凸)の低減に有効である。
また分散度(Mw/Mn)は1.0〜5.0が好ましく、1.0〜3.0がより好ましく、1.2〜2.5が最も好ましい。なお、Mnは数平均分子量を示す。
(B)成分としては、特に限定されず、これまで化学増幅型レジスト用の酸発生剤として提案されているものを使用することができる。このような酸発生剤としては、これまで、ヨードニウム塩やスルホニウム塩などのオニウム塩系酸発生剤、オキシムスルホネート系酸発生剤、ビスアルキルまたはビスアリールスルホニルジアゾメタン類、ポリ(ビススルホニル)ジアゾメタン類などのジアゾメタン系酸発生剤、ニトロベンジルスルホネート系酸発生剤、イミノスルホネート系酸発生剤、ジスルホン系酸発生剤など多種のものが知られている。
前記直鎖若しくは分岐鎖状のアルキル基としては、炭素数1〜10であることが好ましく、炭素数1〜8であることがさらに好ましく、炭素数1〜4であることが最も好ましい。
前記環状のアルキル基としては、炭素数4〜12であることが好ましく、炭素数5〜10であることがさらに好ましく、炭素数6〜10であることが最も好ましい。
前記フッ素化アルキル基としては、炭素数1〜10であることが好ましく、炭素数1〜8であることがさらに好ましく、炭素数1〜4であることが最も好ましい。また、該フッ化アルキル基のフッ素化率(アルキル基中全水素原子の個数に対する置換したフッ素原子の個数の割合)は、好ましくは10〜100%、さらに好ましくは50〜100%であり、特に水素原子をすべてフッ素原子で置換したものが、酸の強度が強くなるので好ましい。
R51としては、直鎖状のアルキル基またはフッ素化アルキル基であることが最も好ましい。
R52において、ハロゲン原子としては、フッ素原子、臭素原子、塩素原子、ヨウ素原子などが挙げられ、フッ素原子が好ましい。
R52において、アルキル基は、直鎖または分岐鎖状であり、その炭素数は好ましくは1〜5、特に1〜4、さらには1〜3であることが望ましい。
R52において、ハロゲン化アルキル基は、アルキル基中の水素原子の一部または全部がハロゲン原子で置換された基である。ここでのアルキル基は、前記R52における「アルキル基」と同様のものが挙げられる。置換するハロゲン原子としては上記「ハロゲン原子」について説明したものと同様のものが挙げられる。ハロゲン化アルキル基において、水素原子の全個数の50〜100%がハロゲン原子で置換されていることが望ましく、全て置換されていることがより好ましい。
R52において、アルコキシ基としては、直鎖状または分岐鎖状であり、その炭素数は好ましくは1〜5、特に1〜4、さらには1〜3であることが望ましい。
R52としては、これらの中でも水素原子が好ましい。
置換基としては、水酸基、低級アルキル基(直鎖または分岐鎖状であり、その好ましい炭素数は5以下であり、特にメチル基が好ましい)などを挙げることができる。
R53のアリール基としては、置換基を有しないものがより好ましい。
u”は1〜3の整数であり、2または3であることが好ましく、特に3であることが望ましい。
R1”〜R3”のアリール基としては、特に制限はなく、例えば、炭素数6〜20のアリール基であって、該アリール基は、その水素原子の一部または全部がアルキル基、アルコキシ基、ハロゲン原子等で置換されていてもよく、されていなくてもよい。アリール基としては、安価に合成可能なことから、炭素数6〜10のアリール基が好ましい。具体的には、たとえばフェニル基、ナフチル基が挙げられる。
前記アリール基の水素原子が置換されていても良いアルキル基としては、炭素数1〜5のアルキル基が好ましく、メチル基、エチル基、プロピル基、n−ブチル基、tert−ブチル基であることが最も好ましい。
前記アリール基の水素原子が置換されていても良いアルコキシ基としては、炭素数1〜5のアルコキシ基が好ましく、メトキシ基、エトキシ基が最も好ましい。
前記アリール基の水素原子が置換されていても良いハロゲン原子としては、フッ素原子であることが好ましい。
R1”〜R3”のアルキル基としては、特に制限はなく、例えば炭素数1〜10の直鎖状、分岐状または環状のアルキル基等が挙げられる。解像性に優れる点から、炭素数1〜5であることが好ましい。具体的には、メチル基、エチル基、n−プロピル基、イソプロピル基、n−ブチル基、イソブチル基、n−ペンチル基、シクロペンチル基、ヘキシル基、シクロヘキシル基、ノニル基、デカニル基等が挙げられ、解像性に優れ、また安価に合成可能なことから好ましいものとして、メチル基を挙げることができる。
これらの中で、R1”〜R3”は、それぞれ、フェニル基またはナフチル基であることが最も好ましい。
前記直鎖または分岐のアルキル基としては、炭素数1〜10であることが好ましく、炭素数1〜8であることがさらに好ましく、炭素数1〜4であることが最も好ましい。
前記環状のアルキル基としては、前記R1”で示したような環式基であって、炭素数4〜15であることが好ましく、炭素数4〜10であることがさらに好ましく、炭素数6〜10であることが最も好ましい。
前記フッ素化アルキル基としては、炭素数1〜10であることが好ましく、炭素数1〜8であることがさらに好ましく、炭素数1〜4であることが最も好ましい。また、該フッ化アルキル基のフッ素化率(アルキル基中のフッ素原子の割合)は、好ましくは10〜100%、さらに好ましくは50〜100%であり、特に水素原子をすべてフッ素原子で置換したものが、酸の強度が強くなるので好ましい。
R4”としては、直鎖または環状のアルキル基、またはフッ素化アルキル基であることが最も好ましい。
R5”〜R6”のアリール基としては、R1”〜R3”のアリール基と同様のものが挙げられる。
R5”〜R6”のアルキル基としては、R1”〜R3”のアルキル基と同様のものが挙げられる。
これらの中で、R5”〜R6”はすべてフェニル基であることが最も好ましい。
式(b−2)中のR4”としては上記式(b−1)のR4”と同様のものが挙げられる。
Y”、Z”は、それぞれ独立に、少なくとも1つの水素原子がフッ素原子で置換された直鎖状または分岐状のアルキル基であり、該アルキル基の炭素数は1〜10であり、好ましくは炭素数1〜7、より好ましくは炭素数1〜3である。
X”のアルキレン基の炭素数またはY”、Z”のアルキル基の炭素数は、上記炭素数の範囲内において、レジスト溶媒への溶解性も良好である等の理由により、小さいほど好ましい。
また、X”のアルキレン基またはY”、Z”のアルキル基において、フッ素原子で置換されている水素原子の数が多いほど、酸の強度が強くなり、また200nm以下の高エネルギー光や電子線に対する透明性が向上するので好ましい。該アルキレン基またはアルキル基中のフッ素原子の割合、すなわちフッ素化率は、好ましくは70〜100%、さらに好ましくは90〜100%であり、最も好ましくは、全ての水素原子がフッ素原子で置換されたパーフルオロアルキレン基またはパーフルオロアルキル基である。
R31の有機基としては、直鎖、分岐または環状のアルキル基またはアリール基が好ましい。これらのアルキル基、アリール基は置換基を有していても良い。該置換基としては、特に制限はなく、たとえばフッ素原子、炭素数1〜6の直鎖、分岐または環状のアルキル基等が挙げられる。ここで、「置換基を有する」とは、アルキル基またはアリール基の水素原子の一部または全部が置換基で置換されていることを意味する。
アルキル基としては、炭素数1〜20が好ましく、炭素数1〜10がより好ましく、炭素数1〜8がさらに好ましく、炭素数1〜6が特に好ましく、炭素数1〜4が最も好ましい。アルキル基としては、特に、部分的または完全にハロゲン化されたアルキル基(以下、ハロゲン化アルキル基ということがある)が好ましい。なお、部分的にハロゲン化されたアルキル基とは、水素原子の一部がハロゲン原子で置換されたアルキル基を意味し、完全にハロゲン化されたアルキル基とは、水素原子の全部がハロゲン原子で置換されたアルキル基を意味する。ハロゲン原子としては、フッ素原子、塩素原子、臭素原子、ヨウ素原子等が挙げられ、特にフッ素原子が好ましい。すなわち、ハロゲン化アルキル基は、フッ素化アルキル基であることが好ましい。
アリール基は、炭素数4〜20が好ましく、炭素数4〜10がより好ましく、炭素数6〜10が最も好ましい。アリール基としては、特に、部分的または完全にハロゲン化されたアリール基が好ましい。なお、部分的にハロゲン化されたアリール基とは、水素原子の一部がハロゲン原子で置換されたアリール基を意味し、完全にハロゲン化されたアリール基とは、水素原子の全部がハロゲン原子で置換されたアリール基を意味する。
R31としては、特に、置換基を有さない炭素数1〜4のアルキル基、または炭素数1〜4のフッ素化アルキル基が好ましい。
R32としては、特に、シアノ基、置換基を有さない炭素数1〜8のアルキル基、または炭素数1〜8のフッ素化アルキル基が好ましい。
R33としては、ハロゲン化アルキル基が好ましく、フッ素化アルキル基がより好ましい。
R33におけるフッ素化アルキル基は、アルキル基の水素原子が50%以上フッ素化されていることが好ましく、より好ましくは70%以上、さらに好ましくは90%以上フッ素化されていることが好ましい。
R34のアリール基は、炭素数1〜10のアルキル基、ハロゲン化アルキル基、アルコキシ基等の置換基を有していても良い。該置換基におけるアルキル基またはハロゲン化アルキル基は、炭素数が1〜8であることが好ましく、炭素数1〜4がさらに好ましい。また、該ハロゲン化アルキル基は、フッ素化アルキル基であることが好ましい。
R35としては、ハロゲン化アルキル基が好ましく、フッ素化アルキル基がより好ましく、部分的にフッ素化されたアルキル基が最も好ましい。
R35におけるフッ素化アルキル基は、アルキル基の水素原子が50%以上フッ素化されていることが好ましく、より好ましくは70%以上、さらに好ましくは90%以上フッ素化されていることが、発生する酸の強度が高まるため好ましい。最も好ましくは、水素原子が100%フッ素置換された完全フッ素化アルキル基である。
R37の2または3価の芳香族炭化水素基としては、上記R34のアリール基からさらに1または2個の水素原子を除いた基が挙げられる。
R38の置換基を有さないアルキル基またはハロゲン化アルキル基としては、上記R35の置換基を有さないアルキル基またはハロゲン化アルキル基と同様のものが挙げられる。
p’’は好ましくは2である。
また、特開平9−208554号公報(段落[0012]〜[0014]の[化18]〜[化19])に開示されているオキシムスルホネート系酸発生剤、WO2004/074242A2(65〜85頁目のExample1〜40)に開示されているオキシムスルホネート系酸発生剤も好適に用いることができる。
また、好適なものとして以下のものを例示することができる。
また、特開平11−035551号公報、特開平11−035552号公報、特開平11−035573号公報に開示されているジアゾメタン系酸発生剤も好適に用いることができる。
また、ポリ(ビススルホニル)ジアゾメタン類としては、例えば、特開平11−322707号公報に開示されている、1,3−ビス(フェニルスルホニルジアゾメチルスルホニル)プロパン、1,4−ビス(フェニルスルホニルジアゾメチルスルホニル)ブタン、1,6−ビス(フェニルスルホニルジアゾメチルスルホニル)ヘキサン、1,10−ビス(フェニルスルホニルジアゾメチルスルホニル)デカン、1,2−ビス(シクロヘキシルスルホニルジアゾメチルスルホニル)エタン、1,3−ビス(シクロヘキシルスルホニルジアゾメチルスルホニル)プロパン、1,6−ビス(シクロヘキシルスルホニルジアゾメチルスルホニル)ヘキサン、1,10−ビス(シクロヘキシルスルホニルジアゾメチルスルホニル)デカンなどを挙げることができる。
本発明においては、中でも(B)成分としてフッ素化アルキルスルホン酸イオンをアニオンとするオニウム塩を用いることが好ましい。
本発明の液浸露光用ポジ型レジスト組成物における(B)成分の含有量は、(A)成分100質量部に対し、0.5〜30質量部、好ましくは1〜10質量部とされる。上記範囲とすることでパターン形成が充分に行われる。また、均一な溶液が得られ、保存安定性が良好となるため好ましい。
本発明の液浸露光用ポジ型レジスト組成物には、レジストパターン形状、引き置き経時安定性などを向上させるために、さらに任意の成分として、含窒素有機化合物(D)(以下、(D)成分という)を配合することができる。
この(D)成分は、既に多種多様なものが提案されているので、公知のものから任意に用いれば良いが、環式アミン、脂肪族アミン、特に第2級脂肪族アミンや第3級脂肪族アミンが好ましい。
脂肪族アミンとしては、アンモニアNH3の水素原子の少なくとも1つを、炭素数12以下のアルキル基またはヒドロキシアルキル基で置換したアミン(アルキルアミンまたはアルキルアルコールアミン)が挙げられる。その具体例としては、n−ヘキシルアミン、n−ヘプチルアミン、n−オクチルアミン、n−ノニルアミン、n−デシルアミン等のモノアルキルアミン;ジエチルアミン、ジ−n−プロピルアミン、ジ−n−ヘプチルアミン、ジ−n−オクチルアミン、ジシクロヘキシルアミン等のジアルキルアミン;トリメチルアミン、トリエチルアミン、トリ−n−プロピルアミン、トリ−n−ブチルアミン、トリ−n−ヘキシルアミン、トリ−n−ペンチルアミン、トリ−n−ヘプチルアミン、トリ−n−オクチルアミン、トリ−n−ノニルアミン、トリ−n−デカニルアミン、トリ−n−ドデシルアミン等のトリアルキルアミン;ジエタノールアミン、トリエタノールアミン、ジイソプロパノールアミン、トリイソプロパノールアミン、ジ−n−オクタノールアミン、トリ−n−オクタノールアミン等のアルキルアルコールアミン等が挙げられる。
これらの中でも、アルキルアルコールアミン及びトリアルキルアミンが好ましく、アルキルアルコールアミンが最も好ましい。アルキルアルコールアミンの中でもトリエタノールアミンやトリイソプロパノールアミンが最も好ましい。
環式アミンとしては、たとえば、ヘテロ原子として窒素原子を含む複素環化合物が挙げられる。該複素環化合物としては、単環式のもの(脂肪族単環式アミン)であっても多環式のもの(脂肪族多環式アミン)であってもよい。
脂肪族単環式アミンとして、具体的には、ピペリジン、ピペラジン等が挙げられる。
脂肪族多環式アミンとしては、炭素数が6〜10のものが好ましく、具体的には、1,5−ジアザビシクロ[4.3.0]−5−ノネン、1,8−ジアザビシクロ[5.4.0]−7−ウンデセン、ヘキサメチレンテトラミン、1,4−ジアザビシクロ[2.2.2]オクタン等が挙げられる。
これらは単独で用いてもよいし、2種以上を組み合わせて用いてもよい。
(D)成分は、(A)成分100質量部に対して、通常0.01〜5.0質量部の範囲で用いられる。
有機カルボン酸としては、例えば、マロン酸、クエン酸、リンゴ酸、コハク酸、安息香酸、サリチル酸などが好適である。
リンのオキソ酸若しくはその誘導体としては、リン酸、リン酸ジ−n−ブチルエステル、リン酸ジフェニルエステルなどのリン酸又はそれらのエステルのような誘導体、ホスホン酸、ホスホン酸ジメチルエステル、ホスホン酸−ジ−n−ブチルエステル、フェニルホスホン酸、ホスホン酸ジフェニルエステル、ホスホン酸ジベンジルエステルなどのホスホン酸及びそれらのエステルのような誘導体、ホスフィン酸、フェニルホスフィン酸などのホスフィン酸及びそれらのエステルのような誘導体が挙げられる。
(E)成分は、(A)成分100質量部当り0.01〜5.0質量部の割合で用いられる。
(S)成分としては、使用する各成分を溶解し、均一な溶液とすることができるものであればよく、従来、化学増幅型レジストの溶剤として公知のものの中から任意のものを1種または2種以上適宜選択して用いることができる。
例えば、γ−ブチロラクトン等のラクトン類;
アセトン、メチルエチルケトン、シクロヘキサノン、メチル−n−アミルケトン、メチルイソアミルケトン、2−ヘプタノンなどのケトン類;
エチレングリコール、ジエチレングリコール、プロピレングリコール、ジプロピレングリコールなどの多価アルコール類及びその誘導体;
エチレングリコールモノアセテート、ジエチレングリコールモノアセテート、プロピレングリコールモノアセテート、またはジプロピレングリコールモノアセテート等のエステル結合を有する化合物、前記多価アルコール類または前記エステル結合を有する化合物のモノメチルエーテル、モノエチルエーテル、モノプロピルエーテル、モノブチルエーテル等のモノアルキルエーテルまたはモノフェニルエーテル等のエーテル結合を有する化合物等の多価アルコール類の誘導体;
ジオキサンのような環式エーテル類や、乳酸メチル、乳酸エチル(EL)、酢酸メチル、酢酸エチル、酢酸ブチル、ピルビン酸メチル、ピルビン酸エチル、メトキシプロピオン酸メチル、エトキシプロピオン酸エチルなどのエステル類;
アニソール、エチルベンジルエーテル、クレジルメチルエーテル、ジフェニルエーテル、ジベンジルエーテル、フェネトール、ブチルフェニルエーテル、エチルベンゼン、ジエチルベンゼン、アミルベンゼン、イソプロピルベンゼン、トルエン、キシレン、シメン、メシチレン等の芳香族系有機溶剤などを挙げることができる。
これらの有機溶剤は単独で用いてもよく、2種以上の混合溶剤として用いてもよい。
中でも、プロピレングリコールモノメチルエーテルアセテート(PGMEA)、プロピレングリコールモノメチルエーテル(PGME)、ELが好ましい。
また、PGMEAと極性溶剤とを混合した混合溶媒は好ましい。その配合比(質量比)は、PGMEAと極性溶剤との相溶性等を考慮して適宜決定すればよいが、好ましくは1:9〜9:1、より好ましくは2:8〜8:2の範囲内とすることが好ましい。
より具体的には、極性溶剤としてELを配合する場合は、PGMEA:ELの質量比は、好ましくは1:9〜9:1、より好ましくは2:8〜8:2である。また、極性溶剤としてPGMEを配合する場合は、PGMEA:PGMEの質量比は、好ましくは1:9〜9:1、より好ましくは2:8〜8:2、さらに好ましくは3:7〜7:3である。
また、(S)成分として、その他には、PGMEA及びELの中から選ばれる少なくとも1種とγ−ブチロラクトンとの混合溶剤も好ましい。この場合、混合割合としては、前者と後者の質量比が好ましくは70:30〜95:5とされる。
(S)成分の使用量は特に限定しないが、基板等に塗布可能な濃度で、塗布膜厚に応じて適宜設定されるものであるが、一般的にはレジスト組成物の固形分濃度が2〜20質量%、好ましくは5〜15質量%の範囲内となる様に用いられる。
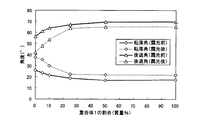
浸漬露光時の物質溶出を抑制できる理由は、明らかではないが、(A)成分として、重合体(A1)と重合体(A2)とを含有することにより、たとえば重合体(A2)を単独で用いる場合に比べ、得られるレジスト膜の後退角が増大すること、および転落角が減少することが主な要因の1つと考えられる。すなわち、本発明の液浸露光用ポジ型レジスト組成物を用いて形成されるレジスト膜は、(A)成分としてたとえば樹脂(A2)のみを用いた場合に比べ、水に対する動的接触角(レジスト膜を傾斜させていった際に水滴が転落しはじめたときの接触角。水滴の転落方向前方の端点における接触角(前進角)と、転落方向後方の端点における接触角(後退角)とがある。)、転落角(レジスト膜を傾斜させていった際に水滴が転落しはじめたときのレジスト膜の傾斜角度)が変化する。たとえば後退角は大きくなり、一方、転落角は小さくなる。液浸露光においては、上述のように、浸漬露光時にレジスト膜が水等の液浸溶媒に接触することになる。したがって、物質溶出は、レジスト膜表面の特性(たとえば親水性・疎水性等)により影響を受けると推測される。本発明においては、特定の(A)成分を用いることにより、これらの特性が変化し、それによって物質溶出が生じにくく、しかも良好なリソグラフィー特性が得られるレジスト膜が形成されていると推測される。
まず、直径6インチのシリコン基板の上に、レジスト組成物溶液をスピンコートした後、90℃の温度条件で90秒間加熱してレジスト膜を形成する。
次に、上記レジスト膜に対して、AUTO SLIDING ANGLE:SA−30DM(協和界面科学社製)、AUTO DISPENSER:AD−31(協和界面科学社製)等の市販の測定装置を用いて測定することができる。
また、本発明の液浸露光用ポジ型レジスト組成物は、当該ポジ型レジスト組成物を用いて得られるレジスト膜における転落角の測定値が36度以下であることが好ましく、10〜36度であることがより好ましく、12〜30度であることが特に好ましく、15〜25度であることが最も好ましい。転落角が36度以下であると、浸漬露光時の物質溶出抑制効果が向上する。また、転落角が10度以上であると、リソグラフィー特性等が良好である。
そのため、レジスト膜の変質や、液浸溶媒の屈折率の変化も抑制できる。したがって、液浸溶媒の屈折率の変化が抑制される等により、形成されるレジストパターンのうねりやLERが低減され、形状等のリソグラフィー特性が良好となる。
また、露光装置のレンズの汚染を低減でき、そのため、これらに対する保護対策を行わなくてもよく、プロセスや露光装置の簡便化に貢献できる。
また、本発明の液浸露光用ポジ型レジスト組成物によれば、高解像性、たとえば120nm以下の寸法のレジストパターンを形成できる。
さらに、プロセスマージンも大きい。たとえば、ベーク温度の変化に対するレジストーパターンの寸法変化量が小さく、ベーク温度マージンが大きい。また、マスクリニアリティ(マスク再現性)が良好で、たとえば同じ露光量で、寸法やピッチが異なる多様なマスクに忠実なレジストパターンを形成できる。
これらのリソグラフィー特性が良好な理由は、定かではないが、物質溶出が抑制されるためレジストの変質が抑制されること、本発明において用いられる重合体(A2)が、いわゆるアセタール型の酸解離性溶解抑制基を有しており、かかる酸解離性溶解抑制基は、たとえば第3級アルキルエステル型酸解離性溶解抑制基に比べて低い活性化エネルギーによる解離が可能であるため、露光部において酸解離性溶解抑制基が解離しやすく、露光部と未露光部とのアルカリ溶解性の差(コントラスト)が大きくなりやすいこと、また、その解離の度合いが、露光量やベーク温度の影響を受けにくいこと等が考えられる。
次に、本発明のレジストパターン形成方法について説明する。
本発明のレジストパターン形成方法は、上記本発明の液浸露光用ポジ型レジスト組成物を用いて基板上にレジスト膜を形成する工程、前記レジスト膜を浸漬露光する工程、前記レジスト膜を現像しレジストパターンを形成する工程を含む。
まず、シリコンウェーハ等の基板上に、本発明の液浸露光用レジスト組成物をスピンナーなどで塗布した後、プレベーク(ポストアプライベーク(PAB)処理)を行うことにより、レジスト膜を形成する。
このとき、基板とレジスト組成物の塗布層との間に、有機系または無機系の反射防止膜を設けて2層積層体とすることもできる。
また、レジスト膜上にさらに有機系の反射防止膜を設けて2層積層体とすることもでき、さらにこれに下層の反射防止膜を設けた3層積層体とすることもできる。
レジスト膜上に設ける反射防止膜はアルカリ現像液に可溶であるものが好ましい。
ここまでの工程は、周知の手法を用いて行うことができる。操作条件等は、使用する液浸露光用ポジ型レジスト組成物の組成や特性に応じて適宜設定することが好ましい。
露光に用いる波長は、特に限定されず、ArFエキシマレーザー、KrFエキシマレーザー、F2レーザーなどの放射線を用いて行うことができる。本発明にかかるレジスト組成物は、KrFまたはArFエキシマレーザー、特にArFエキシマレーザーに対して有効である。
このとき、液浸媒体としては、空気の屈折率よりも大きく、かつ液浸露光用ポジ型レジスト組成物を用いて形成されるレジスト膜の有する屈折率を有する溶媒が好ましい。かかる溶媒の屈折率としては、前記範囲内であれば特に制限されない。
空気の屈折率よりも大きく、かつレジスト膜の屈折率よりも小さい屈折率を有する溶媒としては、例えば、水、フッ素系不活性液体、シリコン系溶剤等が挙げられる。
フッ素系不活性液体としては、特に、アルキル基の水素原子が全てフッ素原子で置換されたパーフロオロアルキル化合物が好ましい。パーフロオロアルキル化合物としては、具体的には、パーフルオロアルキルエーテル化合物やパーフルオロアルキルアミン化合物を挙げることができる。
さらに、具体的には、前記パーフルオロアルキルエーテル化合物としては、パーフルオロ(2−ブチル−テトラヒドロフラン)(沸点102℃)を挙げることができ、前記パーフルオロアルキルアミン化合物としては、パーフルオロトリブチルアミン(沸点174℃)を挙げることができる。
以下の実施例および比較例で用いた重合体を下記に示す。
表1に示す各成分を混合し、溶解してポジ型レジスト組成物溶液を調製した。
(B)−1:トリフェニルスルホニウムノナフルオロブタンスルホネート。
(D)−1:トリエタノールアミン。
(S)−1:PGMEA/EL=8/2(質量比)の混合溶剤。
<後退角および転落角の測定>
得られたポジ型レジスト組成物溶液を、スピンナーを用いて直径8インチのシリコンウェーハ上に塗布し、ホットプレート上で110℃、90秒間プレベークして、乾燥させることにより、膜厚200nmのレジスト膜を形成した。該レジスト膜上に純水を1滴(50μl)滴下させた後、以下に示す装置及び条件で後退角および転落角を測定した(露光前の後退角および転落角)。
<装置名>
AUTO SLIDING ANGLE:SA−30DM(協和界面科学社製)
AUTO DISPENSER:AD−31(協和界面科学社製)
<解析ソフト(装置に付属のもの)>
FAMAS
これらの結果に示すように、重合体(A1)に相当する重合体1と、重合体(A2)に相当する重合体2とを併用した実施例1〜4は、重合体2を単独で用いた比較例1に比べて、露光前・露光後ともに転落角が小さくなり、後退角が大きくなっていた。また、露光前後の転落角の差、および露光前後の後退角の差が、比較例1に比べて小さくなっていた。
上記と同様にしてポジ型レジスト組成物溶液を用いてレジスト膜を形成した。次に、VRC310S(エス・イー・エス株式会社製)を用いて、純水一滴(150μl)を室温下で、ウェーハの中心から円を描くように等線速で液滴を移動させた(液滴が接触したレジスト膜の総接触面積221.56cm2)。その後、その液滴を採取して、分析装置Agilent−HP1100 LC−MSD(Agilent Technologies社製)により分析して、(B)成分のカチオン部(PAG+)およびアニオン部(PAG−)の溶出量(mol/cm2)を求めた。
次に、露光されたレジスト膜を上記と同様に分析して、(B)成分のカチオン部(PAG+)およびアニオン部(PAG−)の溶出量(mol/cm2)を求めた
これらの結果を表3に示す。
上記評価において、露光前の溶出量は、選択的露光を施してレジストパターンを形成する際の未露光部における溶出量を評価するためのものであり、露光後の溶出量は、露光部における溶出量を評価するためのものである。したがって、露光前と露光後の両方において、液浸媒体(水)への物質溶出が少なかったことから、実施例1〜4のポジ型レジスト組成物が、浸漬露光する工程を含むレジストパターン形成方法に用いる液浸露光用として好適に使用できることが確認できた。
実施例1〜3及び比較例2で得られたポジ型レジスト組成物溶液を用いてリソグラフィー特性を評価した。
8インチシリコンウェーハ上に、有機系反射防止膜組成物「ARC−29A」(商品名、ブリュワーサイエンス社製)を、スピンナーを用いて塗布し、ホットプレート上で205℃、60秒間焼成して乾燥させることにより、膜厚77nmの有機系反射防止膜を形成した。そして、ポジ型レジスト組成物溶液を、スピンナーを用いて反射防止膜上に塗布し、ホットプレート上で、表4に示すPAB温度で60秒間のPAB処理を行い、乾燥することにより、膜厚150nmのレジスト膜を形成した。
ついで、ArF露光装置NSR−S302(ニコン社製;NA(開口数)=0.60,2/3輪帯照明)により、ArFエキシマレーザー(193nm)を、マスクパターンを介して選択的に照射した。そして、表4に示すPAB温度で60秒間のPEB処理を行い、さらに23℃にて2.38質量%テトラメチルアンモニウムヒドロキシド(TMAH)水溶液で30秒間現像し、その後30秒間、純水を用いて水リンスし、振り切り乾燥を行って、120nmの孤立スペースパターン(以下、Isoスペースパターンという)を形成した。
このようにして得られたIsoスペースパターンを走査型電子顕微鏡(SEM)により観察した。その結果を表4に示す。
Claims (11)
- 酸解離性溶解抑制基を有し、酸の作用によりアルカリ可溶性が増大する樹脂成分(A)と、露光により酸を発生する酸発生剤成分(B)とを含む液浸露光用ポジ型レジスト組成物であって、
前記樹脂成分(A)が、主鎖環状型重合体(A1)と、α位の炭素原子にハロゲン原子、炭素原子数1〜5のアルキル基または炭素原子数1〜5のハロゲン化アルキル基が結合していてもよく、カルボキシ基の水素原子が有機基で置換されていてもよいアクリル酸から誘導される構成単位(a)を主鎖に有する非主鎖環状型重合体(A2)とを含有し、
前記非主鎖環状型重合体(A2)が、α位の炭素原子にハロゲン原子、炭素原子数1〜5のアルキル基または炭素原子数1〜5のハロゲン化アルキル基が結合していてもよいアクリル酸エステルから誘導される構成単位であって下記一般式(p1)で表される酸解離性溶解抑制基(p1)を有する構成単位(a1)を有することを特徴とする液浸露光用ポジ型レジスト組成物。
- 前記主鎖環状型重合体(A1)が、ポリシクロオレフィンから誘導される構成単位を主鎖に有する重合体である請求項1記載の液浸露光用ポジ型レジスト組成物。
- 前記非主鎖環状型重合体(A2)が、さらに、α位の炭素原子にハロゲン原子、炭素原子数1〜5のアルキル基または炭素原子数1〜5のハロゲン化アルキル基が結合していてもよいアクリル酸エステルから誘導される構成単位であってラクトン含有環式基を含む構成単位(a2)を有する請求項6記載の液浸露光用ポジ型レジスト組成物。
- 前記非主鎖環状型重合体(A2)が、さらに、α位の炭素原子にハロゲン原子、炭素原子数1〜5のアルキル基または炭素原子数1〜5のハロゲン化アルキル基が結合していてもよいアクリル酸エステルから誘導される構成単位であって極性基含有脂肪族炭化水素基を含む構成単位(a3)を有する請求項6または7記載の液浸露光用ポジ型レジスト組成物。
- 前記主鎖環状型重合体(A1)と前記非主鎖環状型重合体(A2)との質量比が99:1〜1:99の範囲内である請求項1〜8のいずれか一項に記載の液浸露光用ポジ型レジスト組成物。
- さらに含窒素有機化合物(D)を含有する請求項1〜9のいずれか一項に記載の液浸露光用ポジ型レジスト組成物。
- 請求項1〜10のいずれか一項に記載の液浸露光用ポジ型レジスト組成物を用いて基板上にレジスト膜を形成する工程、前記レジスト膜を浸漬露光する工程、前記レジスト膜を現像しレジストパターンを形成する工程を含むレジストパターン形成方法。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006008538A JP4937587B2 (ja) | 2006-01-17 | 2006-01-17 | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 |
| PCT/JP2006/324550 WO2007083458A1 (ja) | 2006-01-17 | 2006-12-08 | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 |
| US12/160,957 US7968269B2 (en) | 2006-01-17 | 2006-12-08 | Positive resist composition for immersion exposure and method of forming resist pattern |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006008538A JP4937587B2 (ja) | 2006-01-17 | 2006-01-17 | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2007192876A JP2007192876A (ja) | 2007-08-02 |
| JP4937587B2 true JP4937587B2 (ja) | 2012-05-23 |
Family
ID=38287415
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006008538A Expired - Fee Related JP4937587B2 (ja) | 2006-01-17 | 2006-01-17 | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US7968269B2 (ja) |
| JP (1) | JP4937587B2 (ja) |
| WO (1) | WO2007083458A1 (ja) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5012073B2 (ja) * | 2006-02-15 | 2012-08-29 | 住友化学株式会社 | フォトレジスト組成物 |
| JP5481768B2 (ja) * | 2006-09-08 | 2014-04-23 | Jsr株式会社 | 感放射線性樹脂組成物及びそれを用いたレジストパターン形成方法 |
| JP2008065282A (ja) * | 2006-09-11 | 2008-03-21 | Tokyo Ohka Kogyo Co Ltd | ポジ型レジスト組成物およびレジストパターン形成方法 |
| JP5537829B2 (ja) * | 2009-03-31 | 2014-07-02 | 富士フイルム株式会社 | 感活性光線性または感放射線性樹脂組成物、及び該組成物を用いたパターン形成方法 |
| JP5586294B2 (ja) | 2009-03-31 | 2014-09-10 | 富士フイルム株式会社 | 感活性光線性または感放射線性樹脂組成物、及び該組成物を用いたパターン形成方法 |
| JP2012150501A (ja) * | 2012-03-21 | 2012-08-09 | Jsr Corp | 感放射線性樹脂組成物及びそれを用いたレジストパターン形成方法 |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3380128B2 (ja) | 1996-11-29 | 2003-02-24 | 富士通株式会社 | レジスト材料及びレジストパターンの形成方法 |
| US6200725B1 (en) | 1995-06-28 | 2001-03-13 | Fujitsu Limited | Chemically amplified resist compositions and process for the formation of resist patterns |
| JP3798458B2 (ja) | 1996-02-02 | 2006-07-19 | 東京応化工業株式会社 | オキシムスルホネート化合物及びレジスト用酸発生剤 |
| JP3980124B2 (ja) | 1997-07-24 | 2007-09-26 | 東京応化工業株式会社 | 新規ビススルホニルジアゾメタン |
| JP3854689B2 (ja) | 1997-07-24 | 2006-12-06 | 東京応化工業株式会社 | 新規な光酸発生剤 |
| JP3865473B2 (ja) | 1997-07-24 | 2007-01-10 | 東京応化工業株式会社 | 新規なジアゾメタン化合物 |
| US5945517A (en) | 1996-07-24 | 1999-08-31 | Tokyo Ohka Kogyo Co., Ltd. | Chemical-sensitization photoresist composition |
| US6187504B1 (en) * | 1996-12-19 | 2001-02-13 | Jsr Corporation | Radiation sensitive resin composition |
| JP3935267B2 (ja) | 1998-05-18 | 2007-06-20 | 東京応化工業株式会社 | 新規なレジスト用酸発生剤 |
| US6153733A (en) | 1998-05-18 | 2000-11-28 | Tokyo Ohka Kogyo Co., Ltd. | (Disulfonyl diazomethane compounds) |
| JP4131062B2 (ja) | 1998-09-25 | 2008-08-13 | 信越化学工業株式会社 | 新規なラクトン含有化合物、高分子化合物、レジスト材料及びパターン形成方法 |
| JP4307663B2 (ja) | 1998-12-16 | 2009-08-05 | 東京応化工業株式会社 | ポジ型レジスト組成物およびそれに用いる重合体、並びにレジストパターン形成方法 |
| JP2001318465A (ja) * | 2000-05-11 | 2001-11-16 | Fuji Photo Film Co Ltd | ポジ型フォトレジスト組成物 |
| KR100795112B1 (ko) * | 2001-02-05 | 2008-01-17 | 후지필름 가부시키가이샤 | 포지티브 레지스트 조성물 |
| JP4560507B2 (ja) | 2003-02-19 | 2010-10-13 | チバ ホールディング インコーポレーテッド | ハロゲン化オキシム誘導体及び潜在的酸としてのそれらの使用 |
| JP4530751B2 (ja) | 2003-07-24 | 2010-08-25 | 富士フイルム株式会社 | ポジ型感光性組成物及びそれを用いたパターン形成方法 |
| EP1505439A3 (en) | 2003-07-24 | 2005-04-20 | Fuji Photo Film Co., Ltd. | Positive photosensitive composition and method of forming resist pattern |
| WO2005075446A1 (ja) * | 2004-02-04 | 2005-08-18 | Daicel Chemical Industries, Ltd. | 不飽和カルボン酸ヘミアセタールエステル、高分子化合物及びフォトレジスト用樹脂組成物 |
| JP4651283B2 (ja) * | 2004-02-04 | 2011-03-16 | ダイセル化学工業株式会社 | 不飽和カルボン酸ヘミアセタールエステル、高分子化合物及びフォトレジスト用樹脂組成物 |
| JP4365236B2 (ja) | 2004-02-20 | 2009-11-18 | 富士フイルム株式会社 | 液浸露光用レジスト組成物及びそれを用いたパターン形成方法 |
| JP2006096965A (ja) | 2004-02-20 | 2006-04-13 | Tokyo Ohka Kogyo Co Ltd | 高分子化合物、該高分子化合物を含有するフォトレジスト組成物、およびレジストパターン形成方法 |
| JP4424500B2 (ja) * | 2004-04-09 | 2010-03-03 | 信越化学工業株式会社 | ポジ型レジスト材料及びパターン形成方法 |
| KR100864147B1 (ko) | 2004-04-09 | 2008-10-16 | 신에쓰 가가꾸 고교 가부시끼가이샤 | 포지티브형 레지스트 재료 및 패턴 형성 방법 |
| TWI291473B (en) | 2004-06-08 | 2007-12-21 | Tokyo Ohka Kogyo Co Ltd | Polymer, positive resist composition, and method for forming resist pattern |
| JP4942925B2 (ja) * | 2004-06-18 | 2012-05-30 | 東京応化工業株式会社 | 高分子化合物、ポジ型レジスト組成物及びレジストパターン形成方法 |
| US7799883B2 (en) | 2005-02-22 | 2010-09-21 | Promerus Llc | Norbornene-type polymers, compositions thereof and lithographic process using such compositions |
| JP4524207B2 (ja) * | 2005-03-02 | 2010-08-11 | 富士フイルム株式会社 | 液浸露光用ポジ型レジスト組成物及びそれを用いたパターン形成方法 |
| JP2006301435A (ja) * | 2005-04-22 | 2006-11-02 | Fuji Photo Film Co Ltd | 液浸露光用ポジ型レジスト組成物及びそれを用いたパターン形成方法 |
-
2006
- 2006-01-17 JP JP2006008538A patent/JP4937587B2/ja not_active Expired - Fee Related
- 2006-12-08 WO PCT/JP2006/324550 patent/WO2007083458A1/ja not_active Ceased
- 2006-12-08 US US12/160,957 patent/US7968269B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| WO2007083458A1 (ja) | 2007-07-26 |
| JP2007192876A (ja) | 2007-08-02 |
| US7968269B2 (en) | 2011-06-28 |
| US20100196823A1 (en) | 2010-08-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4717640B2 (ja) | 液浸露光用レジスト組成物およびレジストパターン形成方法 | |
| KR101032019B1 (ko) | 액침 노광용 레지스트 조성물 및 레지스트 패턴 형성 방법 | |
| JP4757766B2 (ja) | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP4597655B2 (ja) | レジストパターン形成方法 | |
| JP2008096743A (ja) | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 | |
| KR101088929B1 (ko) | 액침노광용 레지스트 조성물 및 레지스트 패턴 형성 방법 | |
| JP4937587B2 (ja) | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP2007212990A (ja) | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP4633648B2 (ja) | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP5010995B2 (ja) | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP2008145667A (ja) | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP2008292580A (ja) | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP4980040B2 (ja) | レジスト被覆膜形成用材料およびレジストパターン形成方法 | |
| JP2008102276A (ja) | 液浸露光用レジスト組成物およびレジストパターン形成方法 | |
| JP2007334278A (ja) | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP5225555B2 (ja) | 液浸露光用レジスト組成物およびレジストパターン形成方法 | |
| JP5073839B2 (ja) | 液浸露光用レジスト組成物およびレジストパターン形成方法 | |
| US7910285B2 (en) | Positive resist composition for immersion exposure and method of forming resist pattern | |
| JP4717732B2 (ja) | ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP2008051967A (ja) | 液浸露光用レジスト組成物およびレジストパターン形成方法 | |
| JP5112563B2 (ja) | レジスト被覆膜形成用材料およびレジストパターン形成方法 | |
| JP4472586B2 (ja) | ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP2008015162A (ja) | ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP2008096817A (ja) | 液浸露光用ポジ型レジスト組成物およびレジストパターン形成方法 | |
| JP2007316507A (ja) | 液浸露光用レジスト組成物およびレジストパターン形成方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20081024 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110920 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111114 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20111115 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120214 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120222 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150302 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4937587 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |