下記の詳細な説明は、図面を参照して読まれるべきであり、異なる図面において類似の要素は同一の参照番号で示す。図面は、必ずしも縮尺されておらず、選択された実施形態を示し、および本発明の範囲を限定するよう意図されていない。詳細な説明は、本発明の原理を一例として明らかにし、限定としては示さない。この説明は、当業者は本発明を明確に作製および使用することができ、および、本発明を実施するための最良の形態と現在考えられているものを含む本発明のいくつかの実施形態、適合、変法、代替例および使用を記載する。
定義
別に定義されない限り、本明細書で用いられるすべての技術用語および科学用語は、本発明が属する分野の当業者に一般的に理解される意味を有する。ここでは、下記の用語は、別に規定されない限り、与えられた意味を有する。
「分析物」とは、試料の望ましくは検出される成分をいう。その語は、試料中の単一の成分または複数の成分をいうことができる。
「試料」とは、試料提示器具の表面上に提示された、生物学的または非生物学的起源に由来する任意の物質をいう。試料は、元の未処理の形で、および/または、修飾、分画、抽出、および濃縮を含むがそれらに限定されない処理後に、試料提示器具に加えることができる。本発明の試料は液体または非液体試料であることができる。
「基材」とは、表面を提示または支持することができる材料をいう。
「表面」とは、物体または基材の外側または上側の境界をいう。
「実質的に非結合性」または「結合抵抗性」または「分析物結合抵抗性」とは、分析物に対する認識可能なアフィニティまたは結合を示さない、本発明の試料提示器具に関連して用いられるある表面の特性をいう。いくらかの結合が起こりうる一方、これらの表面は、使用する分析法の検出限界を下回るレベルへ結合を最小化するように特に設計される。
「表面張力」とは、表面付近の不均等な分子凝集力のため、表面上に付けられた液滴が可能な最小の接触面積へ収縮する傾向がある液体の特性をいう。
「湿潤性」とは、固体表面が液体試料によって濡れる程度をいう。特記されない限り、液体試料は本質的に水性である。
「接触角」とは、固体表面の平面と、三相接触(固体/液体/気体)の点に始まる液滴境界との接線との間の角度をいう。
「マトリクス」とは、MALDI−MSまたはSELDI−MSといった質量分析技術に用いられる、レーザーのエネルギーを吸収およびそのエネルギーを分析物分子へ移動し、不安定な高分子のイオン化を可能にするための材料をいう。SELDI−MSでは、マトリクスは「EAM」または「エネルギー吸収分子」と呼ばれる。生物学的分析物の検出のためのマトリクスとしてよく用いられる試薬は、トランス−3,5−ジメトキシ−4−ヒドロキシ桂皮酸(シナピン酸、SA)、α−シアノ−4−ヒドロキシ桂皮酸(HCCA)および2,5−ジヒドロキシ安息香酸(DHBA)を含むがそれらに限定されない。他の適当なマトリクスは当業者に公知である。
「SAM」とは自己組織化単分子膜をいう。SAMは界面活性剤の有機溶媒溶液への適当な基材の浸漬によって自然に形成される分子集合体である。
本明細書および付属の請求項では、文脈で明らかにそうでないと指示されない限り、単数形「a」、「an」および「the」は複数の対象物を含むことに注意する。したがって、たとえば、「分子(a compound)」は一個の分子または分子の組み合わせを意味することが意図され、「液体(a fluid)」は一種類以上の液体、またはその混合物を意味することが意図される。
試料提示器具の説明
本発明の試料提示器具の下記の説明は、発明の要旨で上記説明されたよりも、より詳細な理解を提供する。しかし、本発明の試料提示器具は、それぞれは下記に詳細に説明される、図面、本発明の試料提示器具を製造する方法、および本発明の試料提示器具の使用および用途を参照することによってさらに説明される。
上述のとおり、本発明の試料提示器具は、化学的および生物学的存在物の同定のために用いられるさまざまな分析方法に用いられる既知の試料提示器具に対する魅力的な代替を提供する。さらに本発明は、試料提示器具を作成する方法および液体試料中に含まれる分析物の幅広い分析測定を実施する方法を提供する。本発明の試料提示器具の独自の性質は、既知の分析技術およびそれに関連して用いられる試料提示器具または容器に伴う(上記背景の節に記載された)欠点の多数を扱う。
より具体的には、本発明の試料提示器具は、幅広い分析方法に用いられる既知の試料提示器具に対する魅力的な代替を提供する。それらはたとえば、液体試料中の分析物を、最大100μLまでの容量でバイオチップの表面上に選択的に保持されおよび濃縮されるといった追加的な利点を有する。さらに、分析物は、実質的に非結合性または結合抵抗性であるように設計された試料提示器具の部分から検出されるため、バイオチップに基づくアフィニティ捕捉器具の表面上の直接的な検出、または器具の表面が分析物に対して大きなアフィニティを有する他の試料提示器具と比較して、高感度で分析物が検出される。
本試料提示器具は好ましい実施形態ではわずか一回の液体操作を必要とするため、本発明は、一つの表面から他の表面への分析物の移動に関連する損失の可能性をさらに最小化する。これは、試料提示器具表面の分析物抵抗性と組み合わせて、結果として目的の分析物の損失の低減をきたす。
さらに分析物は、たとえば、SELDI−MSバイオチップのように、アフィニティ捕捉器具に結合しないため、液体試料は、本発明の試料提示器具の表面上で制御された態様で操作および移動することができる。これによって、分析物の試料提示器具の表面への実質的な結合がない分析ゾーンへの試料の濃縮を可能にする。さらにこれによって、分析物を含む試料を、各ゾーン分析物に関して異なる性質を有する表面上の異なるゾーンに移動させることができ、これによって検出前に分析物の精製、単離および/または修飾を可能にする。
本発明は、試料取り扱い中に分析物に関する表面の性質が操作できるよう、さまざまな化学的または物理的刺激(たとえば、熱、紫外線)に反応して表面のさまざまな部分の性質が変化しうる試料提示器具を含む。そのような表面性質への変化は、可逆性または非可逆性であるよう設計してもよい。
したがって本発明は、分析測定の実施に有用である試料提示器具に関する。一実施形態では本発明は、さまざまな分析すべき試料に関して湿潤性の異なる一つ以上のゾーンのある表面を有する、試料提示器具を含む。これら湿潤性の異なるゾーンによって、液体試料中の分析物の保持、濃縮、および移動する能力の異なるゾーンが結果として生じる。これらゾーンは、さまざまな形状およびサイズであってもよく、およびたがいに対して連続性または不連続性であってもよい。本発明の試料提示器具は、それぞれが湿潤性の異なる二つ以上のゾーンを有する、二次元または三次元表面を含んでもよい。
本発明の試料提示器具は、たとえば、ガラス、ケイ酸塩、半導体、金属、ポリマー(たとえば、プラスチック)、および他の水酸化材料、たとえば、ケイ素上のSiO2、アルミニウム上のAl2O3、などを含むがそれらに限定されない、さまざまな材料から成りうる基材を含む。好ましくは、基材は金のような金属、またはケイ素のような半導体である。本発明の試料提示器具はさらに基材の表面上にさまざまなゾーンを作成するために、当業者に知られている方法によって表面修飾された基材を含み、前記ゾーンは湿潤性に関する異なる性質を有する。そのような表面修飾は、自己組織化単分子膜(SAM)、ポリマー(線状および分岐)、およびラングミュア−ブロジェット組織の基材への添加を含むがそれらに限定されない。一例としてSAMを用いると、基材に添加される際に、SAMは液体試料が曝露しうる試料提示器具の表面を作成する。用いられる特定のSAMの組成に応じて、本発明の試料提示器具の表面は、液体試料中の分析物に対して湿潤性の点でおよびアフィニティ(またはその欠如)の点で異なる性質を持ってもよい。SAMは、性質が特定のゾーンに用いられるSAMを反映する別個のゾーンを作成する態様で、本発明の試料提示器具に添加してもよい。当業者に公知の他の表面修飾技術もまた本発明に含まれる。
本発明の試料提示器具は、うち一つが液体試料の保持に関して最適な別個のゾーンから成ってもよい。本発明の試料提示器具は、うち一つが分析物の高感度検出に関して最適な、湿潤性の異なる別個のゾーンをさらに含んでもよい。
試料提示器具の表面が含みうるゾーンの種類に関して、それらは分析すべき試料に関して異なる湿潤性の効用によって主として特徴付けられ、この結果、液体試料中の分析物を保持または結合する能力の異なるゾーンを生じる。これらゾーンは、「境界ゾーン」「液体保持ゾーン」および「分析ゾーン」と広く呼ばれている。本発明は二種類のゾーンの存在を必要とするだけであるが、二種類を超えるゾーンを含むことも意図されている。本発明はそれぞれの種類の二つ以上のゾーンも含みうる。たとえば試料提示器具は、それぞれが液体試料および/またはそこに含まれる分析物に関して異なる性質を持ちうる複数の液体保持ゾーンを含んでもよい。さまざまなゾーンは、たとえば質量分析器具といったさまざまな分析機器上での高処理量の自動化を円滑にしまたは適合するために、精密に位置決めすることができる。
「境界ゾーン」は、分析すべき試料に関して実質的に非湿潤性であるゾーンを含む。境界ゾーンは、それ以外のゾーンと比較して、試料に関して最高の接触角を有するゾーンである。
「液体保持ゾーン」は、分析すべき試料に関して境界ゾーンと比較して相対的により湿潤性である(および下記の分析ゾーンよりも相対的に湿潤性が低い)。液体保持ゾーンは境界ゾーンの接触角よりも相対的に低い接触角(および下記の分析ゾーンよりも相対的に高い接触角)を有する。液体保持ゾーンはまた、最初は分析ゾーンと等しいかまたはより低い接触角を有しうるが、しかし化学的または物理的刺激のために、液体保持ゾーンは化学的または物理的刺激の前の分析ゾーンよりも高い接触角を取ることができ、この結果として液体試料が他のゾーンよりも優先的に一つのゾーンへ導かれる。さらに、液体保持ゾーンは二種類の亜型(subtype)でありうる。一つの亜型では、液体保持ゾーンは液体試料保持目的のために作用するように設計され、その一方で実質的に分析物結合抵抗性である。別の亜型では、液体保持ゾーンは液体試料を保持するように、しかしまた実質的に液体試料中で分析物を結合するように設計され、およびしたがってそれが分析物を捕捉する点で「捕捉ゾーン」と呼ぶことができる。この第二の亜型はまた、実質的に分析物結合性であるがたとえば、紫外線、電気、または熱といった化学的または物理的刺激に供される際に実質的に非結合性になる表面も含みうる。
「分析ゾーン」は、それ以外のゾーンと比較して分析する試料に関して最も湿潤性の高い(および最も低い接触角を有する)ゾーンである。分析ゾーンは、分析物結合抵抗性であるように設計される。分析ゾーンは、目的の抽出物の分析感度を向上させるために、サイズ、形状、および表面性質に関して最適化することができる。
他の利点の中でも、本発明の試料提示器具は、ゾーン間の湿潤性の差を理由に、試料取り扱いに用いられる他のバイオチップよりも大量の液体試料容量を保持および取り扱うことができる。一方、本発明の試料提示器具の液体の能力は、ゾーンのサイズに依存する。3mmの直径の円形ゾーンの場合、液体の能力は最大約100μlまで、少なくとも約70μLでありうる。試料提示器具は、物理的境界、貯蔵容器、またはウェルの必要性なしにこの量の液体試料を含むことができる。
本発明の試料提示器具の別の一実施形態では、試料提示器具は「標的チップ」と呼ぶことができ、およびTnと略され、ここで「n」は試料提示器具の表面上の別個のゾーンの数を表す数表示であり、「n」は2ないし無限の任意の数でありうる。したがって、たとえば、T2標的チップは二個のゾーンを有し、T3標的チップは三個のゾーンを有するなどである。本発明は、2または3ゾーンよりずっと多数を含む試料提示器具を考慮し、および決して特定数のゾーンに限定されない。ゾーンの数が増加するにつれ、全体の効果は勾配に近づく。標的チップは、分析物結合に対して抵抗性であるように設計された一つ以上のゾーンから成る試料提示器具である。T2標的チップに関して、たとえば、試料提示器具は二つのゾーン−すなわち境界ゾーンおよび分析ゾーンを含む。液体試料に接触するゾーンの表面は分析物結合抵抗性であるよう設計されている。すなわち、分析ゾーンは分析物結合抵抗性である。液体試料に接触するゾーンの表面は、分析前の乾燥段階中に分析物を効果的に閉じ込める。T3標的チップに関して、試料提示器具は三つのゾーン−すなわち境界ゾーン、液体保持ゾーン、および分析ゾーンを含む。液体試料に接触するゾーンの表面は、分析物結合抵抗性であるよう設計されている。すなわち、液体保持ゾーンおよび分析ゾーンは分析物結合抵抗性である。液体試料に接触するゾーンの表面は、乾燥段階中に効果的に分析物を分析ゾーンに濃縮する。したがって本発明の試料提示器具は、それぞれが分析物に関して極小の吸着を示す別個のゾーンを含んでもよい。
本発明の試料提示器具の別の一実施形態では、試料提示器具は「捕捉チップ」または「捕捉/濃縮チップ」と呼ぶことができ、およびXnと略され、ここで「n」は試料提示器具の表面上のゾーンの数を表す数表示であり、ここで「n」は2ないし無限の任意の数でありうる。したがって、たとえば、X2捕捉チップは二個のゾーンを有し、X3捕捉チップは三個のゾーンを有するなどである。本発明は、2または3ゾーンよりずっと多数を含む試料提示器具を考慮し、および決して特定数のゾーンに限定されない。ゾーンの数が増加するにつれ、全体の効果は勾配に近づく。捕捉チップおよび捕捉/濃縮チップは、分析物を結合するよう設計された一つ以上のゾーンから成る試料提示器具である。分析物を捕捉する責任を有する部分は、典型的には捕捉ゾーン際立った特徴として設計された特異的な表面修飾を含む。これら表面修飾は、分析物と特異的に(モノクローナル抗体、など)または非特異的に(静電気引力に基づいて結合する荷電基、など)またはそのような引力の任意の組み合わせで結合する生物学的および化学的部分を含んでもよい。目的の分析物を捕捉する能力に加えて、これら表面修飾は、液体試料中に分析物を保持することによってその後の修飾を許容してもよい。そのため、たとえば、表面修飾がモノクローナル抗体である捕捉ゾーンを含む本発明の試料提示器具は、液体試料からの相補的抗原を結合し、およびその抗原を保持する一方、液体試料の残りが物理的な移動または湿潤性の差のどちらかによって器具表面の他の部分へと移動してもよい。保持された抗原は、試料提示器具の捕捉ゾーン上への他の化合物の添加(たとえば、抗原の一部を開裂する酵素の添加)によって修飾してもよい。修飾された抗原は次いでさらなる取り扱いのために試料提示器具の他の部分に移動する、または既知の技術による分析のために器具から除去することができる。
X2捕捉チップに関して、たとえば、試料提示器具は二つのゾーン−すなわち境界ゾーンおよび捕捉ゾーンを含む。液体試料に接触するゾーンの表面は、分析物を捕捉するよう設計されているすなわち、捕捉ゾーンの表面の化学的または生物学的性質に基づいて、捕捉ゾーンは分析物と結合する。液体試料に接触するゾーンの表面は、分析前の乾燥段階中に分析物を効果的に閉じ込める。X3捕捉/濃縮チップに関して、試料提示器具が三つのゾーン-すなわち境界ゾーン、捕捉ゾーン、および分析ゾーンを含む。境界ゾーンは、実質的に非湿潤性であるように設計される。捕捉ゾーンは、分析物を捕捉および結合するように設計される。分析ゾーンは、分析物結合抵抗性であるように設計される。分析物は捕捉ゾーンと分析ゾーンとの間を移動し、さまざまな既知の分析的検出方法のうち一つによる分析の前に行われる。液体試料を含む分析ゾーンの表面は、分析前の乾燥段階中に分析物を効果的に閉じ込める。捕捉ゾーンから分析ゾーンへの液体試料の移動は、捕捉ゾーンの表面の性質の効用によって達成されうる。すなわち、捕捉ゾーンが分析ゾーンよりも低い程度の湿潤性を有するならば、物理的介入なしに液体試料は捕捉ゾーンから分析ゾーンへと移動する。代替的に、捕捉ゾーンは、その性質が化学的または物理的刺激(たとえば、熱、紫外線)に反応して変化することができ、捕捉ゾーンが分析ゾーンよりも低い程度の湿潤性を有し、およびしたがって液体試料を捕捉ゾーンから分析ゾーンへと移動させるよう設計しうる。
本発明の試料提示器具の別の一実施形態では、試料提示器具は、上述の標的および捕捉チップの組み合わせでありうる。この実施形態では、試料提示器具は、異なる機能を有する表面から成る。これらの種類の試料提示器具は、機械的手段(たとえばピペッティングによって)またはその他(たとえばゾーン間の湿潤性の差によって)による、一つのゾーンから別のゾーンへの液体試料の移動を含みうる。一例として、「捕捉−移動−濃縮チップ」、略してX2−移動−T3は、二つのゾーン(すなわち、境界ゾーンおよび捕捉ゾーン)から成るX2チップ、および三つのゾーン(すなわち、境界ゾーン、液体保持ゾーン、および分析ゾーン)から成るT3チップの両方から成る試料提示器具である。分析物の移動(機械的またはその他)は、X2チップの捕捉ゾーンとT3チップの液体保持ゾーンとの間で起こる。
これら試料提示器具は、表面が一つ以上の分析物との結合アフィニティを示しうるよう、二つ以上の「捕捉ゾーン」を含みうる。液体試料が一つのゾーンから別のゾーンへと試料提示器具の表面上を移動する際に、分析物を順次結合する能力は、機械的介入を用いて物理的に画分を分離する必要無しに液体試料の多くの異なる画分の分析を円滑にするという本発明の特徴である。その代わりに、本発明の試料提示器具の異なる湿潤性性質は、異なる捕捉ゾーンと結合する分析物を放置する工程中で液体試料を器具の異なるゾーンへと導くことができ、およびこれによって液体試料を逐次処理する。
より具体的には、捕捉ゾーンおよび液体保持ゾーンの組み合わせを含む試料提示器具の実施形態は、検出前に液体試料中の分析物を単離、濃縮、精製、および修飾するために組み合わせた態様で用いることができる。そのため、たとえば、試料中の分析物が分析ゾーンに閉じ込められるように液体試料をT2チップ上に置くことができる。次いでその試料を、境界ゾーン、捕捉ゾーン、および分析ゾーンを含むX3チップへ移動させることができる。この例では、試料がX3チップに用いられる際に境界ゾーンから捕捉ゾーン(より高い程度の湿潤性を有する)へ移動し、試料中の脂質部分が捕捉ゾーンの表面に結合し、および残りの試料が分析ゾーンへ移動する(分析ゾーンが最高度の湿潤性を有するため)ように、捕捉ゾーンを、液体試料に由来する脂質部分を結合(およびそのようにして除去)するように設計しうる。この例では、分析ゾーンから分析される最終試料が濃縮されおよび脂質を除去精製されるように、液体試料はT2チップ上に閉じ込められ、および次いで脂質がX3チップ上で移動する。捕捉ゾーンは多数の異なる分析物を結合するように設計することができるため、およびこれらのゾーンのうち任意のもののさまざまな組み合わせを用いることができるため、広汎な範囲の精製、濃縮、単離、および修飾能力(一つ以上の分析物に対する)を有する試料提示器具を作製することができる。
一つの試料提示器具から他への液体試料の移動の機構は異なってもよい。上記の例を用いて、T2からの濃縮された試料を機械的に除去して(たとえば、ピペッティングによって)および分離されたX3試料提示器具に載せてもよい。代替的に、T2およびX3試料提示器具はゾーンによって接続されてもよく、その湿潤性は化学的または物理的刺激(たとえば、紫外線)に反応して変化してもよく、その結果、それらの間のゾーンの紫外線への曝露の結果、T2器具の分析ゾーンよりも高いがしかしX3器具の捕捉ゾーンよりも低い湿潤性が生じ、試料がT2からX3へと移動する際に、T2試料提示器具の分析ゾーンにおける濃縮された試料が、X3器具の捕捉ゾーンの上に移動してもよい。ここでもまた、多数の表面(異なる湿潤性および分析物結合性質を有する)およびその構造を有するため、広範な範囲の精製、濃縮、単離、および修飾能力(一つ以上の分析物に対する)試料提示器具を作製することができる。
本発明の試料提示器具は、上記の実施形態のそれぞれにおいて異なる形状またはパターンを有する異なる湿潤性のゾーンをさらに提供してもよい(いくつかの例を図に示す)。たとえば一実施形態では、試料提示器具は、中心ゾーンが分析ゾーンであり、液体保持ゾーンによって囲まれ、境界ゾーンによって囲まれた同心円形状のゾーンを有してもよい。ゾーンは、さまざまな光パターン化技術を用いて作製することができるため、既知の光パターン化技術は結果として生じるパターンに莫大なばらつきを提供するため、および、さまざまなゾーンの広範な範囲の可能な形状、パターン、および構成がある。さらに、湿潤性の異なるゾーンのさまざまな性質は、分析物を表面上の一つ以上の指示されたまたは事前に決定された位置(たとえば、アドレス可能な部位、レーン、またはフィールド)へと導くことができる試料提示器具の作製を可能にする。この文脈における「アドレス可能な」は、それら指示された位置に保持された液体試料または分析物が、目的の分析物を測定する分析器具によって処理できるよう、事前に決定された位置、レーンまたはフィールドが、本発明の試料提示器具と連携して作用する自動処理器具によって指示できることを単に意味する。さらに、これら事前に決定された位置にある液体試料または分析物は、他の試料提示器具によるその後の取り扱いまたは操作(たとえば、修飾、精製、濃縮、など)のために、試料提示器具から除去してもよい。
本発明の試料提示器具は、生物学的および非生物学的液体試料の両方の取り扱いに適している。それらはまた、たとえば、質量分析法、さまざまなクロマトグラフィー法、免疫蛍光分光法、および液体試料中の分析物を検出および測定する他の既知の分析方法含むが、それらに限定されない、幅広い分析物検出方法にも適している。
上述の変法のそれぞれが、既知の方法よりも検出および分析のための分析物を提示する能力が向上した試料提示器具の設計および使用に最大の柔軟性を与えるように設計される。したがって、本発明の試料提示器具は、分析物の高感度検出を向上させるよう設計された分析ゾーンへと分析物を導く能力を有する。したがって本発明の試料提示器具は、改善した分析物の付着を与える。
本発明の試料提示器具は、最大約100μL、および少なくとも約70μLの容量の液体試料受けおよび保持することができる器具をさらに含んでもよい。本発明の試料提示器具は、分析物の付着物を約2平方ミリメートル(2mm2)未満、および好ましくは約lmm2未満と測定された表面積へと分析物を導く試料位置決め器具として使用してもよい。約1mm未満と測定された表面積へと分析物の付着物を導くことによって、分析物の付着の改善を円滑にし、自動データ取り込みおよび検出感度の両方の簡便さを増加させる。結果として、本発明の試料提示器具は、液体保持能力および分析物の制御された付着の両方に関して、実質的な有用性を示す表面を提供する。好ましい実施形態では、この属性の組み合わせは、既知の試料担体と比較して約4倍から約100倍を上回る検出感度を与える。
一実施形態では、本発明の試料提示器具は基材から成り、基材の表面は同心配置に組織された三つの隣接するゾーンからさらに成り、中央分析ゾーンは液体保持ゾーンに囲まれ、および液体保持ゾーンは境界ゾーンに囲まれる。代替的に、本発明の試料提示器具は基材から成ってもよく、表面は隣接する配置に組織された三つの隣接するゾーンからさらに成り、分析ゾーンの一部および液体保持ゾーンの一部は互いに隣接しており、および互いに連続していない分析ゾーンおよび液体保持ゾーンのそれら部分が共通の境界ゾーンに囲まれている。
本発明の試料提示器具の実施形態では、分析ゾーンの表面は好ましくは約40°未満の、より好ましくは約30°未満の、および最も好ましくは約20°未満の接触角を有する。分析ゾーンの表面は、好ましくは分析物に関して極小のアフィニティまたは結合を示す。液体保持ゾーンの表面は、好ましくは約40°から約95°の範囲の、より好ましくは約60°から約95°の範囲の、最も好ましくは約80°から約95°の範囲の接触角を有し、およびさらに好ましくは分析物に関して極小のアフィニティまたは結合を示す。境界ゾーンの表面は、好ましくは約95°より大きく、より好ましくは約105°より大きく、最も好ましくは約115°より大きい接触角を有し、およびさらに好ましくは液体試料に関して極小の湿潤性を示す。
本発明の試料提示器具の別の一実施形態では、分析ゾーンの接触角は、液体保持ゾーンの接触角よりも、少なくとも約10°、好ましくは少なくとも約20°、より好ましくは少なくとも約30°、および最も好ましくは少なくとも約40°少なく、液体保持ゾーンの接触角は、境界ゾーンの接触角よりも、好ましくは少なくとも約10°、より好ましくは少なくとも約15°、および最も好ましくは少なくとも約20°少ない。本発明の試料提示器具の実施形態では、液体保持ゾーンの表面積は、分析ゾーンの表面積よりも、好ましくは少なくとも約4倍大きく、より好ましくは少なくとも約10倍大きく、および最も好ましくは少なくとも約50倍大きく、および分析ゾーンの表面積は、好ましくは約1mm2未満であり、より好ましくは約0.2mm2から約0.8mm2の範囲にあり、および最も好ましくは約0.4mm2から約0.6mm2の範囲にある。
本発明の試料提示器具は、さらに基材から成ってもよく、基材の表面は、対の分析ゾーンおよび液体保持ゾーンは同心性の対または隣接する対のどちらかとして配置され、および対の分析および液体保持ゾーンは共通の境界ゾーンに囲まれており、1から1536対の分析ゾーンおよび液体保持ゾーンからさらに成ってもよいがそれらに限定されない。複数の対の分析ゾーンおよび液体保持ゾーンのから成る試料提示器具は、規定のマルチウェルプレート処理器および実験室液体取り扱いロボットと適合するように好ましくは標準的な96ウェル、384ウェルおよび1536ウェルプレートと類似の方法で構成される。
図面の説明
下記に続く説明は単に例示的であり、他の箇所で説明された本発明の開示の補助であって、本発明の範囲を限定しない。
図1aおよび1bを参照すると、本発明の試料提示器具が図解され、基材の表面が同心配置に組織された三つの隣接するゾーンからさらに成り、中央分析ゾーン2が液体保持ゾーン3に囲まれ、および液体保持ゾーン3が境界ゾーン4に囲まれる、基材1を示す。分析ゾーン2の表面は、好ましくは約40°未満の、より好ましくは約30°未満の、および最も好ましくは約20°未満の接触角を示し、およびさらに好ましくは分析物に関して極小の結合を示す。液体保持ゾーン3の表面は、好ましくは約40°から約95°の範囲の、より好ましくは約60°から約95°の範囲の、最も好ましくは約80°から約95°の範囲の接触角を示し、およびさらに好ましくは分析物に関して極小の結合を示す。境界ゾーン4の表面は、好ましくは約95°より大きく、より好ましくは約105°より大きく、最も好ましくは約115°より大きい接触角を示し、およびさらに好ましくは液体試料に関して極小の湿潤性を示す。
図1aおよび1bをさらに参照すると、本発明の試料提示器具の好ましい実施形態は、分析ゾーン2の接触角が液体保持ゾーン3の接触角よりも好ましくは少なくとも約10°、より好ましくは少なくとも約20°、より好ましくは少なくとも約30°、および最も好ましくは少なくとも約40°少なく、液体保持ゾーン3の接触角は境界ゾーン4の接触角よりも、好ましくは少なくとも約10°、より好ましくは少なくとも約15°、および最も好ましくは少なくとも約20°少なく、液体保持ゾーン3の表面積は分析ゾーン2の表面積よりも、好ましくは少なくとも約4倍大きく、より好ましくは少なくとも約10倍大きく、および最も好ましくは少なくとも約50倍より大きく、および分析ゾーン2の表面積は好ましくは約2mm2未満、より好ましくは約0.2mm2から約1.8mm2の範囲、および最も好ましくは約0.4mmから約1.6mmの範囲にある器具である。
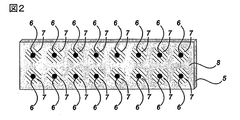
図2に関して、本発明の試料提示器具は、表面が同心の16対の分析ゾーン6および液体保持ゾーン7から成り、これらはすべて共通の境界ゾーン8に囲まれる基材5から成る。この例では、対の標的および液体保持ゾーンは9mmの中心に配列され、これによってこれら器具のうち6個を標準的な96ウェルプレートに対応する規格へと組み合わせることが可能になるであろう。
図2にさらに関して、本発明の試料提示器具の好ましい実施形態は、分析ゾーン6の接触角が液体保持ゾーン7の接触角よりも好ましくは少なくとも約10°、より好ましくは少なくとも約20°、より好ましくは少なくとも約30°、および最も好ましくは少なくとも約40°少なく、液体保持ゾーン7の接触角は境界ゾーン8の接触角よりも、好ましくは少なくとも約10°、より好ましくは少なくとも約15°、および最も好ましくは少なくとも約20°少なく、液体保持ゾーン7の表面積は分析ゾーン6の表面積よりも、好ましくは少なくとも約4倍大きく、より好ましくは少なくとも約10倍大きく、および最も好ましくは少なくとも約50倍より大きく、および分析ゾーン6の表面積は好ましくは約2mm2未満、より好ましくは約0.2mm2から約1.8mm2の範囲、および最も好ましくは約0.4mmから約1.6mmの範囲にある器具である。
図1aに図解するように、分析ゾーンまたは液体保持ゾーンのいずれも円形であってはならないことに留意することが重要である。分析ゾーンおよび液体保持ゾーンの両方とも、試料提示器具の性能を最適化するよう要求されるとおり、特定の用途に関してさまざまな形状を取ることができる。加えて、図1aおよび2に図解するように、分析ゾーンまたは液体保持ゾーンのいずれも互いに同心性であってはならないことに留意することが重要である。分析ゾーンおよび液体保持ゾーンの両方とも、試料提示器具の性能を最適化するよう要求されるとおり、特定の用途に関し位置決めすることができる。
図3に関して、本発明の試料提示器具は、分析ゾーン10の一部および液体保持ゾーン11の一部が互いに隣接しており、および互いに連続していない分析ゾーンおよび液体保持ゾーンのそれら部分が共通の境界ゾーン12に囲まれている、隣接する配置に組織された三つの隣接するゾーンからさらに成る表面を有する基材9から成る。分析ゾーン10の表面は分析物に関して、好ましくは約40°未満の、より好ましくは約30°未満の、および最も好ましくは約20°未満の接触角を示し、およびさらに好ましくは極小の結合を示す。液体保持ゾーン11の表面は分析物に関して、好ましくは約40°から約95°の範囲の、より好ましくは約60°から約95°の範囲の、最も好ましくは約80°から約95°の範囲の接触角を示し、およびさらに好ましくは極小の結合を示す。境界ゾーン12の表面は液体試料に関して、好ましくは約95°より大きく、より好ましくは約105°より大きく、最も好ましくは約115°より大きい接触角を示し、およびさらに好ましくは極小の湿潤性を示す。
図3にさらに関して、本発明の試料提示器具の好ましい実施形態は、分析ゾーン10の接触角が液体保持ゾーン11の接触角よりも好ましくは少なくとも約10°、より好ましくは少なくとも約20°、より好ましくは少なくとも約30°、および最も好ましくは少なくとも約40°少なく、液体保持ゾーン11の接触角は境界ゾーン12の接触角よりも、好ましくは少なくとも約10°、より好ましくは少なくとも約15°、および最も好ましくは少なくとも約20°少なく、液体保持ゾーン11の表面積は分析ゾーン10の表面積よりも、好ましくは少なくとも約4倍大きく、より好ましくは少なくとも約10倍大きく、および最も好ましくは少なくとも約50倍より大きく、および分析ゾーン10の表面積は好ましくは約2mm2未満、より好ましくは約0.2mm2から約1.8mm2の範囲、および最も好ましくは約0.4mmから約1.6mmの範囲にある器具である。
図1a、2および3に図解するように、分析ゾーンまたは液体保持ゾーンのいずれも円形であってはならないことに留意することが重要である。分析ゾーンおよび液体保持ゾーンの両方とも、試料提示器具の性能を最適化するよう要求されるとおり、特定の用途に関してさまざまな形状を取ることができる。
図4aに関して、本発明の試料提示器具は、中央の分析ゾーン14が液体保持ゾーン15に囲まれ、および液体保持ゾーン15が境界ゾーン16に囲まれ、隣接する配置に組織された三つの隣接するゾーンからさらに成る表面を有する基材13から成る。図4bに関して、分析ゾーン14の形状(正方形)は、サイズの点で36領域のラスターに対応するということから質量分析データの自動取り込みを促進してもよい。
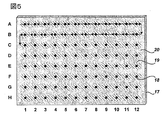
図5に関して本発明の試料提示器具は、表面が分析ゾーン18および液体保持ゾーン19の96対から成り、すべてが共通の境界ゾーン20に囲まれている基材17から成る。この例では、同心の対のゾーンは、標準的な96ウェルプレートに対応する9mmの中心に配列される。液体保持ゾーン19は、液体保持能力を最大化し、および各列における隣接するゾーン間の距離を最小化するように延長される。蛇行パターンが、試料提示器具の最初の二行に重ねられ、自動化画分回収中のクロマトグラフィー溶出液の液流の付着によって描かれる経路を示す。
図5にさらに関して、本発明の試料提示器具の好ましい実施形態は、分析ゾーン18の接触角が液体保持ゾーン19の接触角よりも、好ましくは少なくとも約10°、より好ましくは少なくとも約20°、より好ましくは少なくとも約30°、および最も好ましくは少なくとも約40°少なく、液体保持ゾーン19の接触角は境界ゾーン20の接触角よりも、好ましくは少なくとも約10°、より好ましくは少なくとも約15°、および最も好ましくは少なくとも約20°少なく、液体保持ゾーン11の表面積は分析ゾーン18の表面積よりも、好ましくは少なくとも約4倍大きく、より好ましくは少なくとも約10倍大きく、および最も好ましくは少なくとも約50倍より大きく、および分析ゾーン18の表面積は好ましくは約2mm2未満、より好ましくは約0.2mm2から約1.8mm2の範囲、および最も好ましくは約0.4mm2から約1.6mm2の範囲にある器具である。
試料提示器具の製作
本発明のさらに別の実施形態は、上述の試料提示器具作成または製作する方法を含む。たとえば、表面が、用いられるSAMの差に応じて別個のゾーンを形成する一つ以上の自己組織化単分子膜(SAM)から成る実施形態において、本発明の試料提示器具は、既知の光パターン化技術によって形成されるさまざまなSAMゾーンを含んでもよい。したがって、本発明はさらに、一つの好ましい方法として、光パターン化技術を用いたSAMから成る試料提示器具を作成する方法を含む。
より一般的には、本発明の試料提示器具の基材の表面は、典型的には、当業者に公知である方法によって修飾またはパターン化されている。一例として、基材の表面は、試料提示器具の基材の表面を修飾しおよびその曝露した表面が特定の化学を基材に与えうる自己組織化単分子膜(SAM)を適用することによって修飾またはパターン化されうる。特定の基材のための1°、2°、3°、または4°組成を含む選択されたさまざまなSAMは、基材の表面に独自の表面特性および性質を提供する。特に、複数のSAMの適用は、複数のゾーンを含み各ゾーンが異なる表面特性および性質を有するような、基材のパターン化を結果として生じる。SAMをパターン化する方法は本分野で公知であり、および、紫外光パターン化、フォトリソグラフィーによるパターン化、マイクロスタンピング、電子ビームパターン化、および反応性イオンエッチングを含む。
基材の表面上に形成されるゾーンは、任意の形状であることができ、円形が好ましい。さらに、ゾーンはそれ以外のゾーンに対して連続性または不連続性あってもよい。すなわち、ゾーンはすべて互いに隣接していてもよく、または一つ以上のゾーンは一つ以上の他のゾーンと隣接していなくてもよい。試料提示器具の基材の表面上に形成されるゾーンは、分析すべき試料に関して湿潤性の異なる複数のゾーンを好ましくは有する。
本発明の他の実施形態として、自動データ取り込みを円滑にするよう精密に分析物を位置決めする能力を有する試料提示器具を製造する方法が提供される。
より具体的には、表面パターン化、適当な基材の選択、自己組織化単分子膜の調製へのアプローチ、および表面修飾への他のアプローチが下記に記載される。これら説明は単に例示的であって、および本発明の範囲を限定しない。
本発明の試料提示器具の表面は、好ましくは下記を含むがそれらに限定されないいくつかのアプローチのうち一つによってパターン化される:(1)硬貨鋳造(coinage)金属表面上のアルキルチオールから調製された自己組織化単分子膜(SAM)紫外光パターン化;(2)硬貨鋳造(coinage)金属表面上のアルキルチオールから調製されたSAMのフォトリソグラフィーによるパターン化;(3)硬貨鋳造(coinage)金属表面上のアルキルチオールから調製されたSAMのマイクロスタンピング;および(4)アルキルシランから調製されたSAMのフォトリソグラフィーによるパターン化;(5)電子ビームパターン化、および(6)反応性イオンエッチング。好ましくは、試料提示器具の表面のパターン化は、両方ともが参照により本開示に含まれる、米国特許第5,514,501号に記載された紫外光パターン化工程の適用によって、または米国特許第5,512,131号に記載されたマイクロスタンピング工程によって達成される。代替的に、試料提示器具の表面のパターン化は、文献に記載されおよび当業者に理解されるフォトリソグラフィーによるパターン化工程によって達成されうる。
図6aから6hに関して、金表面上のアルキルチオールから成るSAMの紫外光パターン化に対する段階的な工程を示す。最初は、シリコンウエハ(750μm)といった適当な基材21が、湿式処理およびアルゴンプラズマエッチングの組み合わせによって適切に清浄される。まずクロムまたはチタンおよびタングステン(9:1)のどちらかの接着層(25〜50μm)が、次いで金22の薄膜(100〜1000nm)をウエハの表面に適用される。金属付着は、単位時間当たりの金属付着(厚さ)に関して較正されたスパッタリング(蒸着)工程によって達成される。スパッタリング工程は、無傷のウエハでまたはウエハからさいの目に切られた各片で行ってもよい。
図6bに関して、第一の単分子膜23が0.05ないし5mMアルキルチオールを含むエタノール溶液中での1ないし24時間の期間の基材のインキュベートによって金表面上に集合する。表面修飾した基材を次いでエタノールで洗浄して過剰のアルキルチオールを除去しおよび窒素気流下で乾燥する。第一の単分子膜23は、約100°より大きい接触角を示しおよびさらに液体試料について極小の湿潤性を示す表面を与えるアルキルチオールから調製される。
図6cに関して、表面修飾された基材が酸素の存在下で第一のマスク24を介して紫外光源への曝露によって光パターン化することによって、曝露ゾーンに存在するモノマーを酸化し、これによって金表面に対して低いアフィニティを示すモノマースルホン酸塩を生成する。マスク25における開口は結果として、液体保持ゾーンに対応するサイズおよび形状の特徴の作成をきたす。
図6dから6eに関して、その後の金表面の洗浄によって、モノマースルホン酸塩を除去し、および金26の修飾されない領域を提供する。第二の単分子膜27が、0.05ないし5mMアルキルチオールを含むエタノール溶液中での1ないし24時間の期間の基材のインキュベートによって金表面上に集合する。表面を修飾した基材を次いでエタノールで洗浄して過剰のアルキルチオールを除去しおよび窒素気流下で乾燥する。第二の単分子膜27は、約40°から約95°の範囲の接触角を示しおよびさらに分析物について極小の結合を示す表面を与えるアルキルチオールから調製される。
図6fに関して、パターン化された基材が酸素の存在下で第二のマスク28を介して紫外光源への曝露によってさらに光パターン化することによって、曝露ゾーンに存在するモノマーを酸化し、これによって金表面に対して低いアフィニティを示すモノマースルホン酸塩を生成する。マスク29における開口は結果として、分析ゾーンに対応するサイズおよび形状の特徴の作成をきたす。
図6gから6hに関して、その後の金表面の洗浄によって、モノマースルホン酸塩を除去し、および金30の修飾されない領域を提供する。第三の単分子膜31が、0.05ないし5mMアルキルチオールを含むエタノール溶液中での1ないし24時間の期間の基材のインキュベートによって金表面上に集合する。表面を修飾した基材を次いでエタノールで洗浄して過剰のアルキルチオールを除去しおよび窒素気流下で乾燥する。第三の単分子膜31は、約40°から約95°の範囲の接触角を示しおよびさらに分析物について極小の結合を示す表面を与えるアルキルチオールから調製される。
このようにして、金表面上のアルキルチオールから調製された自己組織化単分子膜の紫外光パターン化に対する段階的な工程が、本発明の試料提示器具を調製するのに利用される。金表面上のアルキルチオールから調製された自己組織化単分子膜の紫外光パターン化の上述の工程は、単に例示的であって、および本発明の範囲を限定しない。
図7aから7hに関して、金表面上のアルキルチオールから成るSAMの紫外光パターン化に対する段階的な工程を示す。シリコンウエハといった適当な基材32が適切に清浄され、および接着層および金33の薄膜(100〜1000nm)をその上にスパッタリングする。
図7bに関して、第一の単分子膜34は0.05ないし5mMアルキルチオールを含むエタノール溶液中での1ないし24時間の期間の基材のインキュベートによって金表面上に集合する。表面を修飾した基材を次いでエタノールで洗浄して過剰のアルキルチオールを除去しおよび窒素気流下で乾燥する。第一の単分子膜34は、40°未満の接触角を示しおよびさらに分析物について極小の結合を示す表面を与えるアルキルチオールから調製される。
図7cに関して、表面修飾された基材はリソグラフィーの前にフォトレジスト35で被覆される。このレジストは、ネガ型またはポジ型のどちらでもよい。ネガ型レジストは結果として、レジストの曝露領域における溶解性を低下させ、したがってマスクに対してネガ型イメージを与える。ポジ型レジストは結果として、レジストの曝露領域における溶解性を上昇させ、したがってマスクに対してポジ型イメージを与える。ポジ型レジストの使用を示す。レジストは、ディップ型の工程を介して適用されてもよいが、しかしスピンコーターを用いて適用されるのが好ましい。レジスト厚さおよび硬化時間に関する製造業者の推奨はガイドラインのとおりに用いられる。
図7dに関して、使用される特定のレジストに関連した使用に求められるように、表面修飾された基材が紫外光源への曝露によって光パターン化される。フォトマスク36は、クロム−水晶、マイラー、酢酸塩、および金属ステンシルを含むがそれらに限定されない多数の一般に用いられる材料から調製してもよい。マスク37における開口部は結果として、分析ゾーンに対応するサイズおよび形状の特徴を作成する。
図7eに関して、最初に、基材は、使用されるレジストに特異的なレジストの曝露領域を溶解する市販の溶液で処理され、一方、紫外光源に曝露されない領域38は、相対的に不溶解性のままである。曝露されたレジストの除去後、酸素プラズマまたは紫外線/オゾン処理を使用して、曝露ゾーン内でアルキルチオールモノマーを酸化し、これによって金表面に関して低いアフィニティを示すスルホン酸モノマーを生成する。その後の金表面の洗浄によってスルホン酸モノマーを除去し、および金39の非修飾領域を与える。
図7fに関して、第二の単分子膜40は、0.05ないし5mMアルキルチオールを含むエタノール溶液中での1ないし24時間の期間の基材のインキュベートによって金表面上に集合する。基材を次いでエタノールで洗浄して過剰のアルキルチオールを除去しおよび窒素気流下で乾燥する。第二の単分子膜40は、約40°から約95°の範囲の接触角を示しおよびさらに分析物について極小の結合を示す表面を与えるアルキルチオールから調製される。
図7gおよび7hについて、残りのフォトレジスト38は、未曝露のレジストを溶解することが知られているいくつかの有機溶媒の一つ(たとえばアセトン、1−メチル−2−ピロリジノン、など)を用いての基材のさらなる洗浄によって除去され、およびここで二つの特徴的なゾーンから成るパターン化された基材は、上記の通りのリソグラフィーの前にフォトレジスト41で被覆される。
図7iおよび7jについて、パターン化された基材が紫外光源への曝露によって上述の第二のフォトマスク42を介して光パターン化される。マスク43における開口部は結果として、液体保持ゾーンに対応するサイズおよび形状の特徴を作成する。最初に、基材は、使用されるレジストに特異的なレジストの曝露領域を溶解する市販の溶液で処理され、一方、紫外光源に曝露されない領域44は、相対的に不溶解性のままである。曝露されたレジストの除去後、酸素プラズマまたは紫外線/オゾン処理を使用して、曝露ゾーン内でアルキルチオールモノマーを酸化し、これによって金表面に関して低いアフィニティを示すスルホン酸モノマーを生成する。その後の金表面の洗浄によってスルホン酸モノマーを除去し、および金45の非修飾領域を与える。
図7kおよび7lについて、第三の単分子膜46が0.05ないし5mMアルキルチオールを含むエタノール溶液中での1ないし24時間の期間の基材のインキュベートによって金表面上に集合する。基材を次いでエタノールで洗浄して過剰のアルキルチオールを除去しおよび窒素気流下で乾燥する。第三の単分子膜46は、100°より大きい接触角を示しおよびさらに液体試料について極小の湿潤性を示す表面を与えるアルキルチオールから調製される。最後に、残りのフォトレジスト44は、未曝露のレジストを溶解することが知られているいくつかの有機溶媒うち一つで基材をさらに洗浄することによって除去し、三つの特徴的なゾーンから成るパターン化された表面を与える。
このようにして、金上のアルキルチオールから成るSAMの光リソグラフィーパターン化に対する段階的な工程が、本発明の試料提示器具を調製するのに利用される。示されたパターン化の順序(分析ゾーン、次いで液体保持ゾーン、次いで境界ゾーン)が任意に選択されたこと、および逆の順序(境界ゾーン、次いで液体保持ゾーン、次いで分析ゾーン)もまた図解された順序と同様適切とわかるであろうことに着目するべきである。金上のアルキルチオールから調製された自己組織化単分子膜の紫外光パターン化の上述の工程は、単に例示的であって、および本発明は記載された工程に限定されない。
多数のアルキルチオールモノマーが、本発明の試料提示器具の調製に適している。アルキルチオールモノマーの合成、それらの単分子膜への集合、および集合した表面の表面張力についてのそれらの分類が記載されている(レイビニス(Laibinis),P.E.;パルマー(Palmer),B.J.;リー(Lee),S.−W.;ジェニングズ(Jennings),G.K.(1998)『有機チオールの合成および金表面上での単分子膜への集合』(”The Synthesis of Organothiols and Their Assembly into Monolayers on Gold”)Thin Films,Vol.24(ウルマン(Ulman),A.編)pp.1−41,アカデミックプレス社(Academic Press)、カリフォルニア州サンディエゴ)、参照により本開示に含まれる。
前述の総説は、アルキルチオールSAMに随伴する末端部分を、集合した表面の表面エネルギーについて分類している。高度に湿潤性である表面を与えおよびしたがって分析ゾーンモノマーの調製に適する部分は:CO2H、B(OH)2、PO3H2、CONH2およびOHを含むがそれらに限定されない。前述の部分のそれぞれは、約40°未満の接触角を示す表面を与えることが報告されている。一般的に言って、高度に湿潤性である表面を与える部分は、水素結合受容体、水素結合供与体、およびその組み合わせから成る。中等度の湿潤性の表面を与えおよびしたがって液体保持ゾーンモノマーの調製に適する末端部分は:CN(60°、10)、O2CCCH3(63°、11)、CO2CH3(67°、10)、NHCOCH3(68°、11)、SCOCH3(70°、11)、OCH3(74°、11)、CONHCH3(76°、11)、NHCOCF3(77°、11)およびCO2CH2CH3(89°、10)を含むがそれらに限定されない。集合した表面に伴う接触角および対応するアルキル鎖長を括弧内に示す。一般的に言って、中等度に湿潤性である表面を与える部分は、双極子−双極子相互反応に関与する官能基から成る傾向がある。極小に湿潤性である表面を与えおよびしたがって境界ゾーンモノマーの調製に適する末端部分は:O(CH2)2CH3(104°、11)、O(CH2)3CH3(113°、16)、NHCO(CF2)7CF3(114.5°、2)、O(CH2)4CH3(115°、16)、O(CH2)5CH3(115°、16)、OCH2CF2CF3(118°、11)、および(CF2)5CF3(118°、2)を含むがそれらに限定されない。集合した表面に伴う接触角および対応するアルキル鎖長を括弧内に示す。一般的に言って、極小に湿潤性である表面を与える部分は、疎水性および疎油性の官能基から成る傾向がある。
好ましくは、本発明の試料提示器具の標的および液体保持ゾーンの両方が、集合した表面上にタンパク質の抵抗性を与えるモノマーから調製される。金表面上のアルキルチオールから調製された多数のSAMは、タンパク質の吸着について特異的に特徴付けられてきた。これまで報告された表面の最もタンパク質抵抗性を示すものは、オリゴ(エチレン酸化物)(OCH2CH2)単位を提示するモノマーに由来する。これら表面の有用性は最初、プライム(Prime)K.L.およびホワイトサイヅ(Whitesides)G.J.Am.Chem.Soc、1993、115、10714−21、参照により本開示に含まれる)によって記載された。タンパク質吸着に抵抗を示す表面の構造特性関係がみられた(オスツニ(Ostuni),E.;チャプマン(Chapman),R.G.;ホルムリン(Holmlin),R.E.;タカヤマ(Takayama),S.;ホワイトサイヅ(Whitesides),G.;ラングムール(Langmuir),2001,17,5605−5620,参照により本開示に含まれる)。近年、多くの両性SAMが、タンパク質の吸着に良好な抵抗性を示してきた(ホルムリン(Holmlin);R.E.;チェン(Chen),X.;チャプマン(Chapman),R.G.;タカヤマ(Takayama),S.;ホワイトサイヅ(Whitesides),G.;ラングムール(Langmuir),2001,17,2841−50,参照により本開示に含まれる)、およびしたがって、高度に湿潤性である表面およびタンパク質吸着への良好な抵抗性の組み合わせを理由に、分析ゾーンとして潜在的に有用である。
好ましい実施形態では、本発明の試料提示器具の分析ゾーンは、一般式I:HS(CH2)11−(OCH2CH2)mOH、mが3から7であるモノマーから調製される。この一般式のモノマーは、約30°から約38°の範囲の接触角を示す表面を与える。これら表面は可能な最小の接触角を示さないが、タンパク質の結合を最小化することについての優れた性能を理由に、好ましくは利用される。さらに、一般式Iの分析ゾーンモノマーは、好ましくは、約60°より大きい接触角を示す表面を与える液体保持ゾーンモノマーと併せて利用される。
同様におよび好ましくは、本発明の試料提示器具の液体保持ゾーンは、一般式II:HS(CH2)11−(OCH2CH2)mR、ここでm=3から7、R基は表面張力および湿潤性に影響を及ぼす末端部分であるモノマーから調製される。好ましくはしかし排他的ではなく、R基は、OCH3、OCH2CN、CO2CH3、CONHCH3、およびCO2CH2CH3部分のうち一つから選択される。上記の末端部分のそれぞれが、約62°から約89°の範囲の接触角を示す表面を与える。
代替的におよび好ましくは、本発明の試料提示器具の液体保持ゾーンは、式HS(CH2)11OCH2C6H5のモノマーから調製されてもよい。末端ベンジル部分(CH2C6H5)は、有機溶媒中で溶解した試料に関して特定の有用性を示し、および約90°の接触角を示す表面を与える。
好ましい実施形態では、本発明の試料提示器具の境界ゾーンは、モノマーから調製される液体試料に関して極小の湿潤性を与え、分析物は水性緩衝液、有機溶媒およびそれらの混合物中で溶解する。末端にペルフルオロ化部分を提供するモノマーは、この点において特定の有用性を示すことが示されてきた(ノード(Naud),C;カラス(Calas),P.;ブランコウ(Blancou),H,;コメイラス(Commeyras),A.J.Fluorine Chem.,2000,104,173−183,参照により本開示に含まれる)。
本発明の好ましい実施形態は、分析ゾーンが式HS(CH2)11−(OCH2CH2)3OHのモノマーから調製され、液体保持ゾーンが式HS(CH2)11(OCH2CH2)3OCH3のモノマーから調製され、および境界ゾーンが式HS(CH2)11OCH2(CF2)5CF3モノマーから調製される。モノマーのこの組み合わせは、分析ゾーン、液体保持ゾーン、および境界ゾーンの接触角がそれぞれ約38°、62°および117°である表面を与える。
本発明の別の好ましい実施形態は、分析ゾーンが式HS(CH2)11−(OCH2CH2)3OHのモノマーから調製され、液体保持ゾーンが式HS(CH2)11OCH2C6H5のモノマーから調製され、および境界ゾーンが式HS(CH2)11OCH2CH2(CF2)5CF3モノマーから調製されるものである。モノマーのこの組み合わせは、分析ゾーン、液体保持ゾーン、および境界ゾーンの接触角がそれぞれ約38°、91°および117°である表面を与える。
二個のアルキルチオールモノマーから調製された混合の(二成分)自己組織化単分子膜が、精密に表面接触角および湿潤性を制御するために用いられてきた。(セマル(Semal),S.;バウチア(Bauthier),C.;ヴー(Voue),M.;バンデンインド(Vanden Eynde),J.J.;グーテンバロン(Gouttebaron),R.;デコニンク(De Coninck),J.J.Phys.Chem.B,2000,104,6225−6232,参照により本開示に含まれる)。高度に湿潤性である表面および中等度に湿潤性である表面を調製するのに用いられたモノマーを混合することによって、40°より大きい角へと接触角が調整されてきた。好ましくは、二成分のSAMが、分析ゾーンまたは液体保持ゾーンのどちらかを調製するのに使用されてきた。代替的に、三成分および四成分の自己組織化単分子膜を使用して分析ゾーンまたは液体保持ゾーンを調製してもよい。三成分および四成分SAMは、置換アルキルチオールおよびヘテロ置換不斉アルキルジスフィルド(すなわち、HS(CH2)11R1およびR2(CH2)11S−S(CH2)11R3)または二個のヘテロ置換不斉アルキルジスフィルド(すなわち、R1(CH2)11S−S(CH2)11S−S(CH2)11R3およびR3(CH2)11S−S(CH2)11R4)のどちらかの二成分混合物から調製される。
図8aから8lに関して、ケイ素表面上のアルキルシランから成るSAMのフォトリソグラフィーによるパターン化に対する段階的な工程を示す。アルキルジメチルクロロシラン、アルキルジメチルアルコキシシラン、アルキルトリハロシラン、またはアルキルトリアルコキシシランのいずれかとの反応によるケイ素およびガラス修飾が、文献に記載され、および当業者に理解される。
図8aに関して、シリコンウエハ、ガラスウエハ、またはその上に二酸化ケイ素を付着した金属基材といった適当な基材47が、表面夾雑物の除去次いで表面の酸化によりシラノール(Si−OH)部分を生成することを含む工程によって、アルキルシランへの共有結合のために適切に活性化される。好ましくは、基材を簡潔に酸素プラズマで処理し、酸化性溶液(ピラニア溶液)で洗浄し、および次いで再び酸素プラズマで処理して、4.9Si−OH/nm2に近い平均シラノール濃縮を提示する活性化された表面48を与える。
図8bに関して、表面活性化の後、第一のアルキルシラン単分子膜49の下記のケイ素表面上に集合する。シラン化は、溶液付着によって、または蒸着によって巧妙に実施してもよい。第一のアルキルシラン単分子膜49は、液体試料に関して好ましくは100°より大きい接触角を示し、およびさらに極小の湿潤性を示す表面を与えるアルキルシランから調製される。
図8cに関して、シラン化された基材は、リソグラフィーの前にフォトレジスト50で被覆される。レジストは、ネガ型またはポジ型のどちらでもよい。ネガ型レジストは結果として、レジストの曝露領域における溶解性を低下させ、したがってマスクに対してネガ型イメージを与える。ポジ型レジストは結果として、レジストの曝露領域における溶解性を上昇させ、したがってマスクに対してポジ型イメージを与える。ポジ型レジストの使用を図6に示す。レジストは、ディップ型の工程を介して適用されてもよいが、しかしスピンコーターを用いて適用されるのが好ましい。レジスト厚さおよび硬化時間に関する製造業者の推奨事項は、ガイドラインのとおりに用いられる。
図8dに関して、使用される特定のレジストに伴う使用に求められるように、基材が紫外光源への曝露によって光パターン化される。フォトマスク51は、クロム−水晶、マイラー、酢酸塩、および金属ステンシルを含むがそれらに限定されない多数の一般に用いられる材料から調製してもよい。マスク52における開口部は結果として、分析ゾーンに対応するサイズおよび形状の特徴を作成する。
図8eおよび8fに関して、最初に、基材は、使用されるレジストに特異的なレジストの曝露領域を溶解する市販の溶液で処理され、一方、紫外光源に曝露されない領域53は、相対的に不溶解性のままである。曝露されたレジストの除去後、酸素プラズマ処理を使用して、さらなるシラン化のための表面を活性化する。第二のアルキルシラン単分子膜55が活性化されたケイ素表面上に集合する。シラン化は、溶液付着によって、または蒸着によって巧妙に実施してもよい。第二のアルキルシラン単分子膜49は、約40°から約95°の範囲にある接触角を示す表面を与え、およびさらに分析物に関して極小の結合を示す表面を与えるアルキルシランから調製される。
図8gおよび8hに関して、残りのフォトレジスト53は、未曝露のレジストを溶解することが知られているいくつかの有機溶媒の一つ(たとえばアセトン、1−メチル−2−ピロリジノン、など)で基材をさらに洗浄することによって除去される。二つの特徴的なゾーンから成るパターン化された基材は、上記の通りのリソグラフィーの前にフォトレジスト56で被覆される。
図8iおよび8jについて、パターン化された基材が紫外光源への曝露によって上述の第二のフォトマスク57を介して光パターン化される。マスク58における開口部は結果として、分析ゾーンに対応するサイズおよび形状の特徴を作成する。次いで基材は、使用されるレジストに特異的なレジストの曝露領域を溶解する市販の溶液で処理され、一方紫外光源に曝露されない領域59は、相対的に不溶解性のままである。曝露されたレジストの除去後、酸素プラズマ処理を使用して、さらなるシラン化のための表面60を活性化する。
図8kおよび8lについて、第三の単分子膜61が活性化されたケイ素表面上に集合する。シラン化は、溶液付着によって、または蒸着によって巧妙に実施してもよい。第三の単分子膜61は、約40°未満の接触角を示す表面を与え、およびさらに分析物に関して極小の結合を示す表面を与えるアルキルシランから調製される。最後に、残りのフォトレジスト59は、未曝露のレジストを溶解することが知られているいくつかの有機溶媒うち一つで基材をさらに洗浄することによって除去し、三つの特徴的なゾーンから成るパターン化された表面を与える。
このようにして、シリコン上のアルキルシランから調製されたSAMの光リソグラフィーパターン化に対する段階的な工程が、本発明の試料提示器具を調製するのに利用される。示されたパターン化の順序(分析ゾーン、次いで液体保持ゾーン、次いで境界ゾーン)が、任意に選択されたことおよび反対の順序(境界ゾーン、次いで液体保持ゾーン、次いで分析ゾーン)もまた図解された順序と同様適切とわかることに着目するべきである。ケイ素上のアルキルシランから調製された自己組織化単分子膜の紫外光パターン化の上述の工程は、単に例示的であって、本発明は記載された工程に限定されない。
多数のアルキルシランが、本発明の試料提示器具の調製における使用に適切である。アルキルシランの大部分は市販されており、およびその合成および表面修飾における使用は理解されている(シュライバー(Shriver)−レイク(Lake),L.C.(1998)『生物医学固定のためのシラン修飾表面、分析における生物分子:実践的なアプローチ(”Silane−modifed sufaces for biomaterial immobilization, Immobilized Biomolecules in Analysis: A Practical Approach”)』,キャス(Cass),T.およびリグラー(Ligler),F.S.編)第一章、オックスフォード大学出版(Oxford University Press)、英国オックスフォード、参照により本開示に含まれる)。
上記に概説したものと若干異なるアプローチを使用して、活性化されたケイ素表面を最初に、求核性部分を有する適切なアルキルシランで誘導体化し、さらに所要の湿潤性を与える官能基化された末端部分を付加してもよい。代替的に、末端部分を備えたアルキルシランが利用可能である場合は、表面は、1回の手順で修飾してもよい。本発明の試料提示器具の調製における使用に適した末端部分は、上述の部分を含むがそれらに限定されない。
好ましい実施形態では、本発明の試料提示器具の分析ゾーンは最初に3−アミノプロピルトリメトキシシランから調製され、および次いでさらに官能基化されて一般式III:(XO)3Si−CH2CH2CH2NHCOCH2(OCH2CH2)nOHの固定化シランを与え、ここでXはケイ素表面または隣接する固定化シランのどちらかへの結合であり、およびnは4ないし8である。一般式IIIのモノマーは、約30°ないし約40°の範囲にある接触角を示す表面を与える。これらの表面は可能な最小の接触角を示さないが、それらは、タンパク質の結合を最小化することについて優れた性能のために好ましくは利用される。さらに、一般式IIIの分析ゾーンモノマーは、好ましくは、約60°より大の接触角を示す表面を与える液体保持ゾーンモノマーと併せて用いられる。
同様におよび好ましくは、本発明の試料提示器具の液体保持ゾーンは、最初に3−アミノプロピルトリメトキシシランから調製され、および次いで、一般式IV:(XO)3SiCH2CH2CH2NHCOCH2(OCH2CH2)nR’、ここでXが基材または隣接するモノマーに対する結合であり、ここでnは4から8までであり、およびここでR基は表面張力および湿潤性に影響する末端部分である。好ましくは、しかし、排他的にでなくR基´は、CH3、CH2CN、CH2CO2CH3、CH2CONHCH3およびCH2CO2CH2CH3部分のうちの一つから選択される。前述の末端部分のそれぞれは、約60°から約90°の範囲の接触角を示す表面を与える。
他の好ましい実施形態では、本発明の試料提示器具の境界ゾーンは、一般式V:(CH3)2(X’)SiCH2CH2−(CF2)7CF3、ここでX’は表面反応性部分である、水性試料に関して最小の湿潤性を与えるアルキルシランから単一の段階で調製される。
さまざまな代替的な表面修飾化学および表面パターン化方法を、本発明の試料提示器具を調製するために利用してもよい。タンパク質抵抗性表面のパターン化に関して、近年、物質のポリマー組成物が注目を集めている。アルキルチオールまたはアルキルシランSAMのいずれかから最初に調製されたパターン化された表面は、表面にポリマー組成物を移植させるかまたは表面から高分子組成物を成長させることによって、さらに官能基化されたてきた(たとえば、フセマン(Husemann),M.;メセレイス(Mecerreyes),D.;ホーカー(Hawker),J.L.;ヘドリック(Hedrick),R.S.;アボット(Abbott),N.L.,Angew.Chem.Int.Ed.1999,35,647−649;シャー(Shah),R.R.;メレセイズ(Merreceyes),D.;フセマン(Husemann),M.;リーズ(Rees),I,アボット(Abbott),N.L.;ホーカー(Hawker),C.J.;ヘドリック(Hedrick),J.L.,Macromolecules2000,33,597−605、およびヒュン(Hyun),J.およびチルコチ(Chilkoti),A.Macromolecules2001,34,5644−5652、これらはすべて参照によって本明細書に組み込まれる)。近年では、ブロック共重合体の吸着による表面パターン化の最初の報告が登場した(デン(Deng),T.;ハ(Ha)Y.H.;チェン(Cheng),J,Y.;ロス(Ross),C.A.;トーマス(Thomas),E.L.Langmuir,2002,75,6719−6722(参照にて本明細書に組み込まれる)。SAMに移植された重合薄膜は、ある程度はトリ(エチレングリコール)基を示すSAMと同等またはそれより良い程度で、タンパク質の吸着に抵抗することを示した(チャプマン(Chapman),R.G.;オスツニ(Ostuni),E.;リアン(Liang),M.N.;メルレニ(Meluleni),G.;キム(Kim),E.;ヤン(Yan),L.;ピエール(Pier),G.;ウオーレン(Warren),H.S.;ホワイトサイズ(Whitesides),G.M.,Langmuir 2001,77,1225−1233(参照にて本明細書に組み込まれる)。
非特異性の態様のみであっても、最も湿潤性の低い表面でさえも、液体試料に由来する所定の部分を保持できることが理解される。事実このような表面は、たとえばその後の分析の標的でない部分の除去によって分析物を濃縮する能力を強化することによって、本発明の試料提示器具の利点に寄与しうる。これは、分析物の分析に干渉しうる非生物学的部分の保持という文脈において特に有用でありうる。しかし、試料提示器具の表面は、この例だけに限定されず、むしろ、分析ゾーン以外の領域中の部分と結合し、分析物含有試料から分離して取り扱いまたは処理されうる表面を含んでもよい。実際、分析生化学方法により分析されうる任意の部分を、本発明の試料提示器具を使用して、保持、保存、輸送、およびその後の分析を行うことができる。したがって本発明は、最高度の湿潤性を有するゾーン以外のゾーン中の部分のある程度の保持が可能であること、および、それら部分のその後の分析が望ましいことを提供する。しかし、目的の分析物の相当な量は、典型的には、最高度の湿潤性を有するゾーン以外のゾーン中では保持されない。したがって、レーザー脱着分光学による分析物の分析の例の文脈において、最も湿潤性の高いゾーン中で保持される標的分析物は、試料提示器具の表面との結合状態からは脱離されない。
試料提示器具の使用および用途
後に続く本発明の試料提示器具のさまざまな使用および用途の説明は、単に例示的であっておよび本発明の範囲を限定しない。
本発明の試料提示器具は、さまざまな分析技術および手順と組み合わせて多くの使用を見出す。このように本発明は、上述した試料提示器具を使用する方法を含む。より具体的には本発明は、本発明の試料提示器具を使用して、試料中の分析物の存在を同定し、および一つの試料提示器具上のまたは複数の試料提示器具上の複数の試料を分析する方法を含む。
液体試料中の分析物の検出、同定または測定を可能にする実質的に任意の分析法が、本発明の試料提示器具と組み合わせて用いることができる。こういった分析法の例は、MALDI−MSまたはエレクトロスプレー・イオン化MSを含むが、それらに限定されない。試料提示器具は、たとえば、試料提示器具の分析ゾーンが高処理量のデータ取り込みを促進するような態様で構成されるMALDI−MS用にといった高処理量の分析測定技術と組み合わせた使用に特に適している。
本発明の試料提示器具は液体試料およびそこに含まれる分析物を操作するために用いてもよい。試料提示器具の表面に備わるように設計されうる異なる湿潤性および捕捉性に基づいて、試料提示器具は、液体試料またはそれに含まれる分析物を操作、濃縮、位置決め、保存、輸送(機械的介入の有無にかかわらず)、復帰(機械的介入の有無にかかわらず)、分析、(試料提示器具上の試薬を修飾する分析物の使用を介して)、修飾または処理、または分画するよう設計されうる。さらに、本発明の試料提示器具は、化学的または物理的な刺激(たとえば、熱、紫外線、圧力、電磁放射)に反応してこれらの機能のいずれかを達成するように設計されうるので、本発明の試料提示器具は可逆的にまたは不可逆的にこれらの機能を達成することができ、および外力に反応してこれらの機能のさまざまな組み合わせをさらに実施することができる。
実質的に任意の液体試料(および分析物)を、本発明の試料提示器具と関連して用いることができる。たとえば、本発明は、液体クロマトグラフィーから回収される分画を分析するために用いることができる。本発明は、2Dゲル電気泳動から切除したタンパク質の点、または、親和性クロマトグラフィー(すなわちICAT)から回収される分画のいずれかから調製される酵素消化物を分析するために用いることができる。本発明は、表面プラスモン共鳴バイオセンサーから回収される試料を分析するのに用いることもできる。本発明は、標準マルチ・ウェル形式ロボットおよび検出法との1:1の試料輸送に使用することができる。実際本発明の試料提示器具は、実質的に任意のソースから得られる、すなわちこれら試料が実験の結果であるか(たとえば、上述のとおり同定される酵素消化物および表面プラスモン共鳴バイオセンサー試料)、環境(たとえば川からの水質試料)から得られるか、または生きている有機体(たとえばヒト尿試料)から直接に得られるかどうかにかかわらず、液体試料を処理および操作するために用いることができる。
本発明は、保存目的での試料の貯蔵のために、または、別の分析のために使うこともできる。言い換えれば、液体試料に含まれる分析物の検出および分析は、液体試料の分析ゾーンへの輸送の直後に発生する必要はない。
したがって本発明のさまざまな実施形態は、試料/分析物の取り扱い、および液体の付着、保持、輸送、位置決めおよび再位置決めおよび保存を含むがそれらに限定されない、さまざまな液体処理機能に役に立つ試料提示器具を提供する。本発明の試料提示器具のこれら使用のいくつかの例が提供されている。
図9aから図9fに関して、試料乾燥のさまざまな段階が例示されている。本発明の試料提示器具の断面図は、中央分析ゾーン63が液体保持ゾーン64に囲まれ、および液体保持ゾーン64が境界ゾーン65にさらに囲まれている、3つの特徴的なゾーンから成る基材62の上付着した表面を示す。
図9bに関して、最初に液体試料滴66を試料提示器具の表面上に付着させた結果、分析ゾーン63および液体保持ゾーン64の表面に、試料滴容量の同時封じ込めが生じる。試料滴の封じ込めは、境界領域65の限られた湿潤性に伴う表面張力を原因とする。付着と同時に、試料滴の接触角は、液体保持ゾーン上にのみ存在する滴の接触角とほぼ等しい。
図9cから9eに関して、試料滴が蒸発によって乾燥するにつれて、滴の半径および接触角の両方が、滴の半径が分析ゾーンの半径に一致するまで、減少する。
図9fに関して、試料滴67の半径と分析ゾーン63の半径とが一致する場合、試料滴の接触角が分析ゾーンに存在する滴のそれにほぼ等しいことがわかる。試料滴が蒸発によって乾燥し続けると、試料滴の半径はさらには減少せず、しかし、分析物が分析ゾーンの表面上の薄膜として付着するため、一定のままである。このような態様で、試料提示器具の表面に付着した最高約100μL量の可変量の水性試料は、分析ゾーンに対応する領域内に封じ込められる分析物の薄膜を乾燥させると即座に提供される。
たとえば、3.0mmの直径(約7.069mm2の表面積)を有する液体保持ゾーンおよび0.5mmの直径(約0.196mm2の表面積)を有する分析ゾーンを有する本発明の試料提示器具は、分析物の付着を、液体保持ゾーンの表面積よりも約36倍小さい分析ゾーンの表面積に封じ込め、平均表面分析物濃度において約36倍同時に増加する。したがって原則的に、上記の試料滴乾燥工程は、潜在的に感度を約36倍増加させるであろう。
図10aから10dに関して、分析ゾーンの非存在時に(液体保持ゾーン68および境界ゾーン69のみが存在する場合)、試料滴70は半径の大幅な減少なしに乾燥し、液体保持ゾーン71の表面の多くの部分の上に分析物の付着が結果として生じる。図10eから10hに関して、液体保持ゾーンの非存在時に(分析ゾーン72および境界ゾーン73のみが存在する場合)、試料滴74の量は、分析ゾーン72の液体保持能力によって制限される。試料滴74は半径の大幅な減少なしに乾燥し、液体保持ゾーン75の表面の多くの部分の上に分析物の付着が結果として生じる。
検出感度の大幅な増大は、図9bから9fに記載されている工程から生じる。この現象は、図9aから9dおよび図10aから10dに関して最も良く理解される。分析ゾーンの非存在時に(図10aを参照)、図10aに表される液体保持ゾーン68中の単位面積あたりの平均分析物表面濃度は、総分析物濃度を表面積で除算したものに等しい。しかし、図9aに表される分析ゾーンの存在時には、分析物の付着は分析ゾーンに限定され、ここでは単位面積あたりの平均分析物表面濃度を分析ゾーンの表面積によって除算したものに等しい。したがってFiG.9aにおいて表される分析ゾーン63の存在によって、分析物の平均表面濃度を増加させ、濃度は図10aに表される液体保持ゾーン68の表面積の図9aに表される分析ゾーン63の表面積に対する比率に等しい。分析ゾーンの表面積が液体保持ゾーンの表面積より大幅に小さいため、分析物付着を分析ゾーンの表面領域に限定すると、結果として、質量分析計に提示された分析物の平均表面濃度を大幅に増加させ、検出感度も付随して増加する。
たとえば、3.0mmの直径(約7.069のmm2の表面積)を有する液体保持ゾーンおよび0.5mmの直径(約0.196のmm2の表面積)を有する分析ゾーンを有する本発明の試料提示器具は、分析物の付着を液体保持ゾーンの表面積よりも約36倍小さい分析ゾーン表面積に限定し、付随して平均表面分析物濃度が約36倍増加する。したがって、原則的に、上記の試料滴乾燥工程は約36倍の感度に増加を潜在的にもたらしうる。
検出感度の上昇をもたらす分析ゾーンの分析物制限特性は、図11aから11hに示されるビデオ接触角の画像において実証される。図11aに関して、本発明の試料提示器具は、約1.6mmのODの値の液体保持ゾーンおよび約0.7mmのODの値の分析ゾーンで、調製した。集束作用の観察を円滑にするために、分析ゾーンは、中心から外して配置した。水滴は、バイオチップの表面に加えられ、急速にそれ自体を液体保持ゾーンおよび分析ゾーンに相当する表面積へと制限することが観察された。最初の左側および右側の接触角が記録され、および両方とも57.1°であり、この値は液体保持ゾーンのモノマーのみから調製される表面によって示される値であった。滴が蒸発のために乾燥するにつれ(図11bから11hを参照)、滴の半径が分析ゾーンの半径に一致するまで、観察された半径および接触角の両方が減少した。さらに、滴が乾燥すると、滴が分析ゾーンの上の中心に来るよう滴の中心が右へ移動したことが観察された。図11hにおいて記録された左側および右側の接触角は両方とも、35.4°であり、この値は分析ゾーンのモノマーだけから調製される表面によって示される値に対応した。図11aから11hに表される画像の取り込みに関連して記録された滴の高さ、幅および接触角のデータは、図12に視覚的にまとめられる。
液体保持ゾーンの傑出した液体保持能力は、図13において実証される。本発明の16部位試料提示器具の実例は、5μLから70μLの範囲の試料滴容量の保持を示す。試料滴容量を大幅に制限するように見える唯一の要因は、隣接する対の分析および液体保持ゾーンの相対的な近さである。
分析ゾーンの分析物制限特性は、図14aおよび14bにさらに示される。第一の図(図14a)は、16部位のうち8ヶ所の表面に付着した5μlから40μLの範囲の試料滴容量を有する本発明の16部位試料提示器具の図である。それぞれの試料滴は、可溶性染料の等量を含んでいた。第二の図(図12b)は、試料滴を乾燥させることができる同じ試料提示器具の図を示す。ここで染料は、分析ゾーンに近接したバイオチップの表面に付着する。分析ゾーンおよび液体保持ゾーンの相対寸法が、比較目的のためにバイオチップに重ねられる。この場合、強く集中した分析物の点を生じない可視材料を提供するために過剰な量の染料が必要となった。
本発明の試料提示器具は、下記から選択されるがそれに限定されない化学的および生物学的分析物の高感度質量分析検出を容易にするために活用してもよい:ペプチド、タンパク質、酵素、酵素基質、酵素基質の類似体、酵素阻害物質、ポリヌクレオチド、オリゴヌクレオチド、核酸、炭水化物、少糖類、多糖類、アビジン、ストレプトアビジン、レクチン、ペプスタチン、プロテアーゼ阻害剤、タンパク質A、凝集素、ヘパリン、タンパク質G、コンカナバリンといった生体高分子;核酸断片、ペプチド断片、およびタンパク質断片といった上記の生体高分子の断片;核酸錯体、タンパク質−DNA錯体、遺伝子転写錯体、遺伝子翻訳錯体、膜、リポソーム、膜受容体、受容体リガンド錯体、シグナリング経路錯体、酵素−基質、酵素阻害物質、ペプチド錯体、タンパク質錯体、炭水化物錯体、および多糖類錯体)といった上記の生体高分子の錯体;およびアミノ酸、ヌクレオチド、ヌクレオシド、糖、ステロイド、脂質、金属イオン、薬剤、ホルモン、アミド、アミン、カルボン酸、ビタミンおよび補酵素、アルコール、アルデヒド、ケトン、脂肪酸、ポルフィリン、カロチノイド、植物成長調整剤、リン酸エステルおよびヌクレオシドジホスホ糖といった生体小分子;および薬学的にまたは治療的に有効な薬剤、モノマー、ペプチド類似体、ステロイド類似体、阻害剤、突然変異原、発癌物質、細胞分裂抑制剤、抗生物質、イオノフォア、代謝拮抗物質、アミノ酸類似体、抗菌薬、輸送阻害剤、表面活性剤(界面活性剤)、アミンを含有する組み合わせライブラリ、染料、毒素、ビオチン、ビオチン化された化合物、DNA、RNA、リジン、アセチルグルコサミン、プロシオンレッド、グルタチオン、アデノシン一リン酸、ミトコンドリアおよび葉緑体機能阻害剤、電子ドナー、キャリアおよびアクセプタ、プロテアーゼの合成基質および類似体、ホスファターゼの合成基質および類似体、エステラーゼおよびリパーゼの合成基質および類似体、およびタンパク質修飾試薬などの合成小分子。さらに、本発明の試料提示器具によって処理できる分析物は、非生物学的であってもよく、およびオリゴマー、ポリアルキレン、ポリアミド、ポリ(メタ)クリレート、ポリスルホン、ポリスチレン、ポリエーテル、ポリビニールエーテル、ポリビニールエステル、ポリカーボネート、ポリビニールのハロゲン化物、ポリシロキサンといった合成ポリマー、および上記の二つまたはそれ以上ならびに殺菌剤といった他のから成る共重合体生物学的分析物を含むが、それらに限定されない。
分析物は、水性緩衝液、有機溶剤またはそれらの混合物に溶解してもよい。緩衝液は、下記を含むがそれらに限定されない揮発成分から調製されるものから選択される:酢酸アンモニウム、重炭酸アンモニウム、炭酸アンモニウム、クエン酸アンモニウム、酢酸トリエチルアンモニウムおよび炭酸トリエチルアンモニウム、ギ酸トリエチルアンモニウム、酢酸トリメチルアンモニウム、炭酸トリメチルアンモニウムおよびギ酸トリメチルアンモニウム。高濃度(>0.1%)の非揮発性界面活性剤を含む水性試料は、界面活性剤は反作用する可能性がありまた分析ゾーンの分析物制限特性があるため、分析の前に脱塩するべきである。有機溶剤は、水性緩衝液中で混合されることおよび生物学的分析物の可溶性を促進することが公知であるものであって、下記を含むがそれらに限定されない:酢酸、アセトン、アセトニトリル、エタノール、N,N−ジメチルホルムアミド(DMF)、N,N−ジメチルスルホキシド(DMSO)、ギ酸、ヘプタフルオロ酪酸、メタノール、N−メチルピロリドン(NMP)、2,2,2−トリフルオロエタノールおよびトリフルオロ酢酸。
試料提示器具は、高沸点有機溶剤の蒸発を促進するために、または、単に試料乾燥に必要な時間を低減するために、(ヒートブロックの表面上、赤外線ランプの下、または熱気流の下のいずれかで)試料乾燥工程の間に加熱してもよい。
本発明の試料提示器具を用いた分析物を測定する好ましい分析法である飛行時間型のレーザー脱着質量分析は、試料提示器具の表面に塗布して、エネルギーを吸収することによって分析物のイオン化を援助する材料(マトリクス)を必要とする。生物学的分析物の検出のためのマトリクスとして高頻度に用いられる試薬は、トランス−3,5−ジメトキシ−4−桂皮酸(シナピン酸、SA)、α−シアノ−4−ヒドロキシ桂皮酸(HCCA)および2,5−ジヒドロキシ安息香酸(DHBA)を含む。上記の水中のマトリクスの限定された可溶性のために、これら試薬の貯蔵液は、多くの場合50%から100%の有機溶剤を含む。本発明の試料提示器具に伴って利用される場合、マトリクスを含有する貯蔵液は、試料を試料提示器具の表面に塗布する前に水性試料に塗布される。あるいは、マトリクスを含有する貯蔵液は、試料付着および乾燥の後、試料提示器具の表面に塗布してもよい。この場合、高いパーセンテージの有機溶剤を含有する貯蔵液が、分析ゾーンの表面に付着する分析物の貯蔵液中での溶解することを最小化するために、好ましくは利用される。
多数の用途が、本発明の試料提示器具を使用するために存在する。本発明において使用しうる試料の種類の例は、分析前にいかなる処理もなしに直接的に分析される試料、ならびにある種の処理が発生した後に試料が分析されるという点において間接的に分析される試料を含むが、それらに限定されない。
分析の前に行われるいかなる処理もなしに直接的に分析される試料のカテゴリに分類される、本発明において使用できる試料の種類の例は、生体液;組織および細胞抽出物および分画;細胞、細菌、ウイルス;培養基;環境流体;環境大気サンプリング;環境メディア抽出物(土壌抽出物、固体廃棄物抽出物、ワイプからの溶出、エアフィルタからの溶出);法医学試料;およびライブラリ、(コンビナトリアル・ケミストリー、オリゴヌクレオチド、ペプチド、糖、脂質、細胞および成分;染色体、および、ウイルスおよびその他大きなタンパク質および核タンパク質集合):を含むが、それらに限定されない。
間接的に、すなわち試料にある種の処理が発生した後に、分析される試料のカテゴリに分類される、本発明において使用できる試料の種類の例は:液体クロマトグラフィー(LC)出力;ガスクロマトグラフィー(GC)出力;ゲルからの溶出物;LC出力またはゲル溶出物からの消化された試料;質量分析出力;表面プラスモン共鳴(SPR)または他のバイオセンサーからの溶出物;脱塩コラム出力;固相抽出物出力;液相分画環境試料;上記のいずれかに関する誘導体化された試料;および、他の化学的または物理的な工程およびそれらの任意の組み合わせ:を含むがそれらに限定されない。
本発明の試料提示器具はさらに、カラム液体クロマトグラフィーまたは電気泳動を利用する分画方式から回収された生物学的分析物の質量分析を円滑にする。とりわけ、有用性は、器具の液体保持能力(クロマトグラフィー分画、電気泳動により精製される試料、試料提示器具から回収される試料、および事前の試料容量の減少なしにバイオセンサーから回収される試料の直接回収を可能にする)および試料の正確な位置決め、および検出感度の増加(それは、自動化されたデータ取り込みを可能にする)の組み合わせの結果生じる。本発明の試料提示器具により提供される液体保持能力は、下記にあるがこれら技術に制限されない技術であるが:親和性クロマトグラフィー、疎水性相互反応クロマトグラフィー、イオン交換クロマトグラフィー、固定された金属イオン親和性クロマトグラフィー、およびサイズ排除クロマトグラフィー、から回収性される分画、ならびに列挙されるクロマトグラフィー方法のうちの二つ以上の連続的な利用を伴う直角分離から回収される分画からの直接的な回収を可能にする。さらに、標準96ウェル、384ウェル、および1536ウェル形式に試料提示器具の利用可能性は、有効性ロボットを扱っているマルチ・ウエルプレート処理器具および研究所の液体取り扱いロボット上のバイオチップに基づく試料回収および処理を可能にする。したがって試料提示器具は、プロテオミクスの出現および化学および生物工学の他の重要な分野を支援するために必要なため、高処理量の質量分析プラットフォームを可能にするために活用することができる。
現代のタンパク質の同定は、しばしば、カラム液体クロマトグラフィーまたは2次元電気泳動ゲルからの切除のいずれかによって精製されたタンパク質の酵素消化物を伴う。一般にタンパク質消化物は、質量分析の前に、逆相液体クロマトグラフィー(RPLC)または固相抽出(SPE)上の脱塩を必要とする。本発明の試料提示器具は、高性能RPLCまたはSPEにより脱塩されたタンパク質消化物の直接的な回収およびその後の分析に適している。
具体的な例として、表面プラスモン共鳴(SPR)バイオセンサーは、固定されたタンパク質を利用して、タンパク質−タンパク質および他の生物学的相互反応を研究する。残念なことに、大量の溶離剤はバイオセンサーから分析物を回収することを必要とし、および、試料中の分析物の濃度は最適な質量分析のためには低すぎる。本発明の試料提示器具は、バイオセンサ・システムから回収される分析物の直接的な回収に適している;試料提示器具は、すでにバイオセンサ・システムに組み込まれた試料回収器具と互換性を持つよう標準96ウェル形式へ構成されてもよく、および質量分析のための自動化された試料回収を可能にするよう利用してもよく、および大量の液体試料を集中できる。
既知の質量分析計試料提示器具に伴う液体保持能力の限界によって、微小量のクロマトグラフィーメディアを充填した小型ピペットチップ(たとえば、ZipTips(登録商標)の使用を伴うさまざまなマイクロカラム液体クロマトグラフィー法の開発を促進した。マイクロカラム法は、試料が直接、試料を保持するために試料を従来の質量分析器具に直接塗布することを可能にするために十分だと報告されている試料容量の同時の減少とともに、タンパク質消化物の脱塩を可能にする。本発明の試料提示器具は、マイクロカラムRPLCにより脱塩されたタンパク質消化物の直接的な回収およびその後の分析に適している。
一般に、本発明の試料提示器具は、上記の試料に関して下記を達成するために用いることができる:濃縮;希釈;位置決め;輸送;保存;分析のために提示;分画;(消化、誘導体化、溶出を含む)洗浄;塗布後処理。このリストが包括的でなく、および本発明の試料提示器具が用いることができるさまざまな適用に関して一般的な意味において例を提供することを理解するべきである。
ひとたび本発明の試料提示器具に試料が塗布され、および試料がその上の液体試料の動きに関して上記に確認された動作のいずれかに供されると、下記の適用を、試料提示器具自体に対して、または、器具から除去した後、実施することができる:MALDI−MS;他の質量分析技術;表面プラスモン共鳴(SPR);蛍光;原子力顕微鏡検査(AFM);生物学および化学発光;X線光電子分光法;偏光解析法;電気化学的検出;リン光;および紫外線、可視光および赤外線分光学。これが、こういった用途の部分的なリストにすぎないことを理解するべきである。上記の分析の任意のものを組み合わせおよび/または連続することが可能であり、および、必要に応じて、これら分析が分析物に対して直接的にまたは間接的に実施してもよいことを理解するべきである。
多くの使用分野が、本発明の試料提示器具に適用可能であると考えられ、これらはゲノミクス、プロテオミクス、薬理ゲノミクス、フィジオミクス、トキシコミクス、メタボノミクス、創薬/薬剤開発/臨床試験モニタリング、毒物学、診断、環境、バイオセンサーおよび生物および化学兵器/バイオテロリズムといった分野を含むが、これら分野に限定されない。次に、試料提示器具の適用の2、3の具体的な例について下記に説明する。続く説明は、単に例示的なものであり、および本発明の範囲を限定しない。
ゲノミクス:遺伝子型および表現型の問題に質量分析法を適用することは、イオン化の前に核酸分析物を脱塩するという必須の前提条件がある。伝統的には、試料がMALDIソースに配置される前に、この脱塩は実行される。一実施形態において、X3形式の試料提示器具は、核酸分析物の濃縮との同時の脱塩を達成することができる。この例は、逆相捕捉ゾーンおよび分析物を結合する抵抗分析ゾーンから成る。別の実施形態は、2つの捕捉ゾーンおよび単一の分析ゾーンが使用されるX4から成ることができる。同心的な配置において、外側の捕捉ゾーンは、補完的なハイブリダイゼーションによって、ポリヌクレオチド被検物質を固定された捕捉プローブと特異的に結合するであろう。内側の捕捉ゾーンは上述の脱塩機能を実施し、および、分析ゾーンは検出のための分析物を提示する。これら実施形態の両方において、脱塩および同一チップ上の分析のための提示を実行することによって、処理量を増加させ、試料損失を最小化して、コストを低減する。
創薬/開発/臨床試験監視:多くの薬剤は、母集団の一部にのみ有効である。この現象の例は、薬剤ハーセプチンであり、乳癌患者の約30%に対してのみ有用である。ハーセプチンの場合、感度の遺伝的およびタンパク質的な基礎は、薬剤の設計とは同一であったが、しかし、ほとんどの場合、高価なおよび長期の臨床試験の前に母集団を可能性の高反応者および非反応者に分けることができない。こういった臨床試験の結果を解釈するという主要な困難の1つは、反応および非反応の生物学的および/または化学的な根拠を理解することである。その知識は、次いで、母集団の標的化のために、および、薬剤自体のさらなる改善のために用いることができる。
この問題への一つのアプローチは、治療の前、中および後に患者からプロフィール(たとえばタンパク質、炭水化物、脂質)を得て、これらのプロフィールを治療結果に関連させることである。本器具のいくつかの実施形態をこのような研究に適用することができる。患者から得られる試料(たとえば血液、尿、組織)は、多次元液体クロマトグラフィーといった上記の節において列挙された前処理方法のうち一つ以上に供することができ、および、その方法によって生成された分画された物質は、質量分析のための濃縮および提示のために本器具に適用される。あるいは、最小の処理に供される試料は、既知の特異性の捕捉ゾーンを有する本器具の一つ以上に適用することができる。次いで、分析物は、分析ゾーンへの輸送の前に補完的な特異性を持つ捕捉ゾーンへ、または、直接的に分析ゾーンへと輸送される。このように、異なる特異性を有する表面を、分画された分析物が質量分析のために同一の分析ゾーンに提示された状態で、直接および並列の両方で自動化された方法で用いることができる。
質量分析は、目的の具体的な分子部分のプロフィール(完全な質量スペクトル)および明確に同定する機会の両方を提供する。次いで質量スペクトルはデータベースに回収することができ、および多因子分析ツールがプロフィールを患者の反応に関連付けるために適用される。このようにして、治療への反応の予測;治療への反応のモニタリング;および治療への反応に影響を及ぼす分子部分の同定を可能にするプロフィールおよび/または特異的な分子部分内にあるパターンを発見することができ、したがってますます高度な薬剤設計が可能になる。
この科学探求の分野は、本明細書中において記載される他と同じように、液体溶液中の分析物を測定する能力にある程度依存している。本発明の試料提示器具および本明細書中に記載される使用は、さらなる研究を行うために用いることができる重要なツールを代表している。
環境:混入物の存在がないかに関して環境試料を分析することは、世界的な取り組みである。こういった研究が直面する特定の問題の中には、混入物が気体、液体、および固体の物質中に存在しうるため、分析物の低い濃度および研究しなければならない試料の多様性がある。一般に、こういった分析は、回収、抽出、誘導体化、分画および検出段階を伴う。
本器具は、環境試料の分析に対する多数の方法において適用することができる。これら実施例は、代表的であり、しかし決して完全でない。捕捉ゾーンを有する器具を、気体または液体のメディアからの分析物の直接的な回収のために用いることができる。たとえば、疎水性表面による水溶液からの疎水性殺菌剤残渣の捕捉は、液体/液体抽出を置換しうるが、時間がかかりおよび有害廃棄物を生成する。次いで回収された材料は、直接分析ゾーンへと輸送するか、分析ゾーンへの輸送の前に補完的な特異性を持つ捕捉ゾーンに直接または並列輸送により分画するか、または、上記の節において列挙された技術のうち一つ以上による分析を可能にするために器具から輸送することができる。一般に、質量分析法は、殺菌剤残渣の同定のために用いられるが、しかし、免疫測定法といった他の技術も適用してもよい。本器具は、前述したように、上記の環境分析の段階のいずれかから生じた材料を提示しおよび/または分画するために用いることもできる。本器具は、分析物を誘導体化して、分析のためのそれらを改変した形態で提示するためのプラットフォームとして用いることができる。たとえば、シリルおよび/またはアセチル部を、装置上に固定された殺菌剤に添加して、分子構造の明確な同定を可能にすることができる。
生物および化学兵器/バイオテロリズム:米国政府は、軍事および非軍事の両方のシナリオにおいて、化学物質および生物物質の検出を容易にするプラットフォームおよび分析技術の必要性に直面している。生物戦検出のための課題は、試料回収および無害な生物と有害な生物との識別を含む。生物物質に関する現在の戦場技術は、生体化合物MSによって容易に検出することができる低分子へ変換する熱分解を利用する。ペプチドバイオマーカーに依存する技術は、現在の方法よりも特異的であるため、大きく期待されている。兵器への曝露の可能性を測定する個人に対する試験は、呼気検査または採血している技術を含むべきである。警報装置としての独立型バイオセンサーに対しても、公的な位置または戦場での使用に対して大きく関心が持たれている。これら方法すべては、試料回収、前処理、およびロボットまたは他の遠隔手段による検査者に対する試料の提示における困難さを示す。試料を保存、操作、濃縮または精製することができる技術、または現在使用されているエアゾールインパクターに連結できる技術は、防御省庁の関心を引きつける可能性がある。本器具は、環境試料のために記載されたものと類似した方法で、生物戦/バイオテロリズム検出に適用することができる。加えて、特別製の捕捉ゾーンを有する装置が、環境または生体液試料に由来する目的の微生物を回収し、キーマーカーを放出するための細胞(またはウイルス)の処理を可能にし、および検出のためにそれらマーカーを提示することができる。
以下の実施例は、本発明の試料提示器具の構成、製造および使用について詳細的な追加的事項を提供するが、しかしこれらは例示的にすぎず、および本発明の範囲を決して制限しない。
実施例I
11−(3,3,4,4,5,5,6,6,7,7,8,8,8−トリデカフルオロオクチルオキシ)ウンデカ−1−エン(1)の調製
褐色バイアル(40mL)に3.0mLの1H,1H,2H,2H−ペルフルオロオクタノール(13.7mmol)を入れ、およびこれに1.4mLの50%水酸化カリウム水溶液(13.7mmol)を加えた。溶液を80℃へ加温し、30分間攪拌し、および3.3mLの11−ブロモウンデカ−1−エン(1.5mmol)を加えた。TLC分析(ヘキサン)が開始物質が消費されたことを示すまで、反応を80℃にて52時間維持した。産物を室温まで冷却し、100mLの酢酸エチルへ加え、および水(2x50mL)および食塩水(1x50mL)で抽出した。酢酸エチル抽出物を硫酸マグネシウム上で乾燥し、ろ過しおよび溶媒を減圧して蒸発し、油状の残渣を与えた。残渣をシリカゲルフラッシュカラム(50x300mm、0%酢酸エチル/ヘキサン、続いて10%酢酸エチル/ヘキサン)で精製した。目的の産物を含む画分を合わせ、および溶媒を蒸発させて、4.52g(64%)の1を無色の油として与えた。
1H NMR(400MHz,CDCl
3):δ5.80(m,1H)、4.95(m,2H)、3.69(t,J=6.8Hz,2H)、3.43(t,J=6.8Hz,2H)、2.39(m,2H)、2.03(m,2H)、1.55(m,2H)、1.36(m,2H)、1.27(broad m,10H)。
実施例II
チオ酢酸S−[11−(3,3,4,4,5,5,6,6,7,7,8,8,8−トリデカフルオロオクチルオキシ)ウンデシル]エステル(2)の調製
乾燥した丸底フラスコ(100mL)に1.0gの1(1.9mmol)をアルゴン下で入れ、および10mLの乾燥メタノールを加えた。結果として生じた溶液に、426μLのチオール酢酸(6.0mmol)、続いて52mgの2,2’−アゾビス(2−メチルプロピオンアミジン)二塩酸塩(0.2mmol)を加えた。反応はホイルテントで覆い、および低圧水銀灯からの光に曝露した。4時間後、TLC分析(5%酢酸エチル/ヘキサン)が、開始物質が消費されてしまったことを示した。溶媒を減圧して蒸発し、油性の残渣を与えた。残渣をシリカゲルフラッシュカラム(40x300mm、0%酢酸エチル/ヘキサン、続いて5%酢酸エチル/ヘキサン)で精製した。目的の産物を含む画分を合わせ、および溶媒を蒸発させて、856mg(76%)の2を無色の油として与えた。
1H NMR(400 MHz,CDCl
3):δ3.69(t,J=6.8Hz,2H)、3.43(t,J=6.8Hz,2H)、2.39(m,2H)、2.31(s,3H)、1.55(m,2H)、1.33(m,2H)、1.25(broad m,10H)。
実施例III
11−(3,3,4,4,5,5,6,6,7,7,8,8,8−トリデカフルオロオクチルオキシ)ウンデカン−l−チオール(3)の調製
褐色バイアル(20mL)にテフロン被覆シリコンセプタムを付け、850mgの2(1.1mmol)および5mLの3Nメタノール酸塩酸(15mmol)を加えた。結果として生じる溶液を40℃に4時間加温した。溶媒を除去して、782mg(98%)の3を無色の油として与えた。
1H NMR(400MHz,CDCl
3):δ3.69(t,J=6.8Hz,2H)、3.43(t,J=6.8Hz,2H)、2.51(dd,J=7.3,7.6Hz,2H)、1.74(m,2H)、1.58(m,2H)、1.34(t,IH)、1.21−1.30(broad m,14H)、1.58(m,4H)、1.32(t,J=8.0Hz,1H)、1.25(broad m,12H)。
実施例IV
11−{2−[2−(2−メトキシエトキシ)エトキシ]エトキシ}ウンデカ−1−エン(4)の調製
丸底フラスコ(200mL)に27.4mLのトリエチレングリコールモノメチルエーテル(171mmol)を入れ、および9.1mLの50%水酸化ナトリウム水溶液(114mmol)を加えた。淡黄色の溶液を80℃へ加温し、30分間攪拌し、および26.6mLの11−ブロモウンデカ−1−エン(114mmol)を滴下して加えた。TLC分析(100%酢酸エチル)が開始物質が消費されるのを示すまで、反応を80℃にて7.5時間維持した。産物を室温まで冷却し、50mLの水で希釈し、およびヘキサン(3x50mL)で抽出した。ヘキサン抽出物を合わせ、硫酸マグネシウム上で乾燥し、ろ過しおよび溶媒を減圧して蒸発し、20g(56%)の4を透明な無色の油として与えた。
1H NMR(400MHz,CDCl
3):δ 5.81(m,1H)、4.96(m,2H)、3.68−3.56(m,12H)、3.44(t,J=6.8Hz,2H)、3.38(s,3H)、2.04(m,2H)、1.57(m,2H)、1.36(m,2H)、1.27(broad s,10H)。
実施例V
チオ酢酸S(11−{2−[2−(2−メトキシエトキシ)エトキシ]エトキシ}ウンデシル)エステル(5)の調製
乾燥した丸底フラスコ(200mL)に5.0gの4(15.8mmol)をアルゴン下で入れ、および10mLの乾燥メタノールを加えた。これに、3.6mLのチオール酢酸(50mmol)、続いて434mgの2,2’−アゾビス(2−メチルプロピオンアミジン)二塩酸塩(1.6mmol)を加えた。反応はホイルテントで覆い、および低圧水銀灯からの光に曝露した。15.5時間後、TLC分析(酢酸エチル/ヘキサン、1:3)が、開始物質が消費されてしまったことを示した。溶媒を減圧して蒸発し、強い硫黄様臭気を有する残渣を与えた。残渣をシリカゲルフラッシュカラム(40x300mm、30%酢酸エチル/ヘキサン、および50%酢酸エチル/ヘキサン)で精製した。目的の産物を含む画分を合わせ、および溶媒を蒸発させて、5.83g(94%)の5を無色の油として与えた。
1H NMR(400MHz,CDCl
3):δ3.67−3.54(m,12H)、3.44(t,J=7.2Hz,2H)、3.38(s,3H)、2.86(t,J=7.2Hz,2H)、2.32(s,3H)、1.57(m,4H)、1.36−1.26(broad m,14H)。
実施例VI
11−{2−[2−(2−メトキシエトケシ)エトケシ]エトケシ}ウンデカン−l−チオール(6)の調製
テフロン被覆シリコンセプタムを付けた褐色バイアル(20mL)に、5.0gの5(12.7mmol)および7mLの3Nメタノール酸塩酸(21mmol)を加えた。溶液を40℃に6時間加温した。溶媒を蒸発させて、4.40g(98%)の6をろう様の無色のゲルとして与えた。溶媒を除去して、782mg(98%)の3を無色の油として与えた。
1H NMR(400MHz,CDCl
3):δ3.67−3.54(m,12H)、3.44(t,J=6.8Hz,2H)、3.37(s,3H)、2.51(dd,J=7.3,8.0Hz,2H)、1.57(m,4H)、1.32(t,J=7.6Hz,1H)、1.26(broad m,14H)。
実施例VII
2−[2−(2−ウンデカ−10−エニルオキシエトキシ)エトキシ]エタノール(7)の調製
丸底フラスコ(250mL)に67.mLのトリエチレングリコールモノメチルエーテル(0.5mmol)を入れ、および8.0mLの50%水酸化ナトリウム水溶液(8mL、0.1mmol)を加えた。溶液を100℃へ加温し、30分間攪拌し、および22.0mLの11−ブロモウンデカ−1−エン(0.1mmol)を滴下して加えて、臭化ナトリウムの付着物を精製する淡黄色の溶液を与えた。TLC分析(メタノール/酢酸エチル/ヘキサン、1:1:8)が開始物質が消費されるのを示すまで、反応を100℃にて2.5時間維持した。反応を室温まで冷却し、300mLの水で希釈し、およびヘキサン(3x100mL)で抽出した。有機抽出物を合わせ、塩水(50mL)で洗い、硫酸マグネシウム上で乾燥し、およびろ過した。溶媒を減圧して蒸発し、油性の残渣を与えた。残渣をシリカゲルフラッシュカラム(50x400mm、メタノール/酢酸エチル/ヘキサン、5:5:90)で精製した。目的の産物を含む画分を合わせ、および溶媒を蒸発させて、20.8g(69%)の7を無色の油として与えた。
1H NMR(400MHz,CDCl
3):δ5.78(m,1H)、4.93(m,2H)、3.72−3.55(m,12H)、3.42(t,J=7.2Hz,2H)、2.64(t,J=5.6Hz,1H)、2.01(m,2H)、1.54(m,2H)、1.34(m,2H)、1.25(broads,10H)。
実施例VIII
チオ酢酸S−(11−{2−[2−(2−ヒドロキシエトキシ)エトキシ]エトキシ}ウンデシル)エステル(8)の調製
乾燥した丸底フラスコ(100mL)に2.0gの7(6.6mmol)をアルゴン下で入れ、および10mLの乾燥メタノールを加えた。これに、2.85mLのチオール酢酸(40mmol)、続いて272mgの2,2’−アゾビス(2−メチルプロピオンアミジン)二塩酸塩(1.0mmol)を加えた。反応はホイルテントで覆い、および低圧水銀灯からの光に曝露した。6時間後、TLC分析(メタノール/酢酸エチル/ヘキサン、1:1:8)が、開始物質が消費されてしまったことを示した。溶媒を減圧して蒸発し、黄色の油を与えた。油をシリカゲルフラッシュカラム(50x300mm、30%メタノール/酢酸エチル/ヘキサン、1:1:8)で精製した。目的の産物を含む画分を合わせ、および溶媒を蒸発させて、2.44g(98%)の8を淡黄色の油として与えた。
1H NMR(400MHz,CDCl
3):δ3.71−3.54(m,12H)、3.42(t,J=6.6Hz,2H)、2.83(t,J=7.2Hz,2H)、2.66(broad s,1H)、2.29(s,3H)、1.52(m,4H)、1.36−1.23(broad m,14H)。
実施例IX
2−{2−[2−(11−メルカプトウンデシルオキシ)エトキシ]エトキシ}エタノール(9)
褐色バイアル(20mL)にテフロン被覆シリコンセプタムを付け、2.40gの8(6.4mmol)および5.0mLの3Nメタノール酸塩酸(15mmol)を加えた。結果として生じる溶液を40℃に4時間加温した。次いで、溶媒を蒸発させて、2.05g(95%)の9をろう様の無色のゲルとして与えた。
1H NMR(400MHz,CDCl
3):δ3.72−3.55(m,12H)、3.43(t,J=6.8Hz,2H)、2.71(broad s,1H)、2.50(dd,J=7.6,7.4Hz,2H)、1.62−1.52(m,4H)、1.31(t,J=7.6Hz,1H)、1.26(broad m,14H)。
実施例X
ウンデカ−10−エニル−オキシメチルベンゼン(10)の調製
乾燥した丸底フラスコ(100mL)に5.0gのウンデカ−10−エン−1−オール(29.4mmol)をアルゴン下で入れ、および25mLの乾燥N,N−ジメチルホルムアミドを加えた。結果として生じた溶液を0℃に冷却し、および2.16gの60%水素化ナトリウムを含む鉱油(45mmol)を一度に加えた。泡立つ混合物をアルゴン下で0℃にて30分間攪拌した。冷却し攪拌した溶液へ、7.7gのブロモメチルベンゼン(45mmol)を含む5mLの乾燥N,N−ジメチルホルムアミドを滴下して加え、および反応を室温まで温める一方、3時間攪拌した。反応を100mLの酢酸エチルの緩やかな添加によって停止し、1N塩酸(2x50mL)および食塩水(1x50ml)で抽出した。有機層を硫酸マグネシウム上で乾燥し、ろ過しおよび溶媒を蒸発し、油状の残渣を与えた(9.5g)。残渣をシリカゲルフラッシュカラム(50x300mm、94:5:1ヘキサン/トルエン/酢酸エチル)で精製し、および目的の産物を含む画分を合わせた。最後に、溶媒を減圧して蒸発し、7.1g(93%)の10を無色の油として与えた。
1H NMR(400MHz,CDCl3):δ7.32(d,4H)、7.28(m,1H)、5.81(m,1H)、4.95(m,2H)、4.49(s,2H)、3.46(t,2H)、2.03(m,2H)、1.61(m,2H)、1.35(broad m,4H)、1.24(broad s,10H)。
実施例XI
チオ酢酸S−(11−ベンジルオキシウンデシル)エステル(11)の調製
ジャケット付き光反応容器(250mL)にまず5.0gの10(19.2mmol)および0.520gの2,2’−アゾビス(2−メチルプロピオンアミジン)二塩酸塩(1.92mmol)を入れた。容器を密封し、脱気し、およびアルゴンで逆流置換した(数サイクル)。アルゴン下での一方、60mLの無水メタノールおよび0.520gのチオ酢酸(92mmol)を反応容器に注入し、および容器の内容を攪拌した。容器を再び脱気し、およびアルゴンで逆流置換した(数サイクル)。紫外灯を点灯し、および混合物をアルゴン下で一定に攪拌して3時間照射した。反応を連続的に冷却し(水ジャケット)および光反応処理中の温度は38℃未満を維持した。反応容器を室温まで冷却させ、および溶媒を蒸発させて淡黄色の油を与えた(10.8g)。油をシリカゲルフラッシュカラム(50x300mm、98:2ヘキサン/酢酸エチル)で精製し、および目的の産物を含む画分を合わせた。最後に、溶媒を減圧して除去し、5.0g(77%)の11を無色の油として与えた。
1H NMR(400MHz,CDCl
3):δ7.32(d,4H)、7.28(m,1H)、4.49(s,2H)、3.46(t,2H)、2.86(t,2H)、2.31(s,3H)、1.50−1.66(m,4H)、1.20−1.40(broad m,14H)。
実施例XII
11−ベンジルオキシウンデカン−1−チオール(12)の調製
褐色バイアル(40mL)にテフロン被覆シリコンセプタムを付け、3.04gの11(9.03mmol)、次いで2mLのジクロロメタン、1mLのヘキサンおよび12mLの4.9Nエタノール酸塩酸を加えた。結果として生じる溶液を40℃に4.5時間加温した。次いで、溶媒を減圧して蒸発し、無色の油状の残渣を与えた(2.8g)。残渣をシリカゲルフラッシュカラム(25x450mm、9:1ヘキサン/クロロフォルム)で精製し、および目的の産物を含む画分を合わせた。溶媒を減圧して蒸発し、2.5g(94%)の12を無色の油として与えた。1H NMR(400MHz,CDCl3):δ7.32(d,4H)、7.28(m,1H)、4.49(s,2H)、3.46(t,2H)、2.51(q,2H)、1.55−1.65(m,4H)、1.20−1.40(broad m,broad t,15H)。
実施例XIII
金被覆されたシリコン基材上での自己組織化単分子膜の調製
シリコンウエハ(200mm、P型、Prime Grade Silicon100)は、個々の基材へと角切りにし、清浄にして、基材あたり10個未満の粒子(0.16μmから3000μm)を有する表面を与えた。金属付着を、5×10−7mmの底面圧で、CPA9900スパッタリングシステム中で実施した。スパッタリングチャンバ内では、アルゴン・プラズマによって基材を清浄にし、およびチタンおよびタングステンの接着剤層(1:9)を5Å/sの速度で厚さ250Åへとスパッタリングした。次いで、金を1000Åの厚さまで5Å/sの速度でスパッタリングした。基材は、アルゴン流下で除去の前に冷却した。
単分子膜の組織化の前に、金で被覆された基材を、300sのための200Wで、アルゴン・プラズマによる処理によって、200Wで300秒間清浄した。基材を、エタノールで洗浄して、および次いで0.1mMの3(11−(3,3,4,4,5,5,6,6,7,7,8,8,8−トリデカフルオロオクチルオキシ)ウンデカン−l−チオール)のエタノール溶液に輸送し、および、1〜24時間の範囲の時間、室温でインキュベートした。最後に、表面修飾基材を集合バスから取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。表面修飾基材に付けられた水滴(0.5μL)の前進接触角は、114°から120°の範囲にあった。表面修飾基材を、透明褐色の紫外線耐性蓋付きの、適合するプラスチック容器に保存した。
実施例XIV
パターン化された試料提示器具の調製
24個の表面修飾基材を上記の通りに調製し、特別製の配列治具に入れ、および液体保持ゾーンとサイズおよび形状が対応する性質を有する、ピンレジスターエッチングしたステンレス鋼シャドーマスク(0.002インチ)で覆った。治具を120W/cm2定格の低圧水銀光源を付けた空冷紫外硬化システムの動くベルトに付け、および1時間の期間にわたって45から75回、光源の下を通した。UV曝露後、基材を治具から取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。曝露された基材を、0.1mMの6(11−{2−[2−(2−メトキシエトキシ)エトキシ]エトキシ}ウンデカン−1−チオール)のエタノール溶液に入れ、および室温にて1ないし24時間の範囲の期間インキュベートした。パターン化された表面修飾基材を集合バスから取り出し、2400rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。液体保持ゾーンに付けられた水滴の前進接触角は60°から65°の範囲にあり、および境界ゾーンに付けられた場合は110°から119°の範囲にあった。
パターン化された表面修飾基材を特別製の配列治具に入れ、および分析ゾーンとサイズおよび形状が対応する性質を有する、第二のピンレジスターエッチングしたステンレス鋼シャドーマスクで覆った。治具を紫外硬化システムの動くベルトに付け、および1時間の期間にわたって45から75回、光源の下を通した。UV曝露後、基材を治具から取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。曝露された基材を、0.1mMの9(2−{2−[2−(11−メルカプトウンデシルオキシ)エトキシ]エトキシ}エタノール)を含むエタノール溶液に入れ、および室温にて1〜24時間インキュベートした。最後に、二回パターン化された表面修飾基材を集合バスから取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。分析ゾーンに付けられた水滴の前進接触角は47°未満であった。二回パターン化された表面修飾基材は、透明褐色の紫外線耐性蓋付きの、適合するプラスチック容器に保存した。
本発明のさまざまな実施形態が上記に説明されている一方、それらは単に例として示されおよび限定ではないことが理解される。特に、分析ゾーン、液体保持ゾーン、および境界ゾーンの物理的配列は上記の例によって限定されない。したがって、本発明の幅および範囲は、上述の典型的な実施形態のいずれによっても限定されない。
実施例XV
試料封じ込めおよび位置決め
検出感度の上昇を与える、分析ゾーンの分析物を閉じ込める特性が、図11aから11hに示される接触角分析像に実証される。図11aに関して、本発明の試料提示器具が、約1.6mmODの値の液体保持ゾーンおよび約0.7mmODの値の分析ゾーンを伴って調製された。集束作用の観察を円滑にするため、分析ゾーンは中心から外れて配置された。水滴がバイオチップの表面に加えられ、および液体保持ゾーンおよび分析ゾーンに相当する表面積へ速やかに閉じ込められるのが観察された。最初の左側および右側接触角を記録し、および両方が57.1°であったことが見出され、液体保持ゾーンモノマーだけから調製された表面によって示されるのと一致する値であった。滴が蒸発のために乾燥する際(図11bから11hを参照)、観察された半径および接触角の両方が、滴の半径が分析ゾーンの半径に一致するまで小さくなった。さらに、滴が乾燥する際、滴が分析ゾーンの中心に来るように、滴の中心が右へ移動するのが観察された。図11hで記録された左側および右側接触角は両方とも35.4°であったことが見出され、分析ゾーンモノマーだけから調製された表面によって示されるのと一致する値であった。図11aから11hに表される画像の取り込みに伴って記録された滴の高さ、幅および接触角データを図12に図式的に要約する。
実施例XVI
パターン化された試料提示器具の液体保持能力
液体保持ゾーンの傑出した液体保持能力が図13に実証される。本発明の16部位試料提示器具の写真は、5μLから70μLの範囲の試料滴容量の保持を示す。試料滴容量を大幅に制限するように見える唯一の要因は、標的および液体保持ゾーンに隣接する対の相対的な近さである。
実施例XVII
分析物誘導および濃縮
分析ゾーンの分析物を閉じ込める特性がさらに図14aおよび14bに実証される。第一の写真(図14a)は、16部位のうち8個の表面に付けた5μLから40μLの範囲にある試料滴容量を伴う本発明の16部位試料提示器具の写真である。試料滴のそれぞれは等量のHCCAを含んだ。図14bは、図14aに表された試料提示器具上の試料乾燥のために濃縮しおよび分析ゾーンへ導かれているHCCAの写真である。分析ゾーンおよび液体保持ゾーンの相対サイズが、比較のためにHCCAの上に重ねられている。
捕捉チップ
本発明の別の実施態様において、試料提示器具は一つ以上の分析物結合領域を含む。結合領域は、試料提示器具上でのさらなる処理および/または測定のための分析物を保持するために適用されてもよい。一用途において、目的の分析物が結合領域により捕捉された後、試料提示器具の表面は望まれない種を除去するために洗浄される。目的の分析物は次いで、結合領域から放出され、そのためさらなる測定および/または処理のための分析ゾーンへと導かれてもよい。あるいは、結合領域は、望まれない種(たとえば塩類、洗剤、タンパク質等)をろ過/分離/除去するために適用されてもよい。一用途において、望まれない種の少なくとも一部は捕捉ゾーンに保持され、一方、試料の残りは、目的の分析物を運搬し、測定および/または処理のために分析ゾーンへと進むことができる。
一変形では、試料提示器具は、「捕捉チップ」または「捕捉/濃縮チップ」と呼び、およびXnと略すことができる、ここで、「n」は試料提示器具の表面上のゾーンの数を示す数表示であり、ここで「n」は、2ないし無限の任意の数でありうる。したがって、たとえば、X2標的チップは二個のゾーンを有し、X3標的チップは三個のゾーンを有するなどである。本発明は、2または3ゾーンよりずっと多数のゾーンを含む試料提示器具を考慮し、および決して特定数のゾーンに限定されない。ゾーンの数が増加するにつれて、全体の効果は勾配に近づく。捕捉チップおよび捕捉/濃縮チップは、分析物を結合するように設計されている一つ以上のゾーンから成る試料提示器具である。典型的に分析物を捕捉することに責任を負う部分は、捕捉ゾーンの特性として設計された特異的な表面修飾を含む。これら表面修飾は、分析物を特異的に(たとえばモノクローナル抗体)または非特異的に(たとえば、それは、静電気引力を基礎として結合する荷電基、など)結合する、生物学的および/または化学的部分、またはこういった引力の任意の組み合わせを含んでもよい。次いでこれらの結合された分析物は、分析の前にさらに表面に加工することができる。これら処理段階、さまざまな洗浄段階による目的の分析物の精製、化学的、生化学的または物理的方法による分析物の修飾、およびその後の使用のための分離を含むが、それらに限定されない。次いで、結合された分析物は、pHの変化、溶媒成分の変化、紫外線、電気または熱といった化学的または物理的な刺激に供した後に放出してもよい。放出後ただちに、次いで分析物を、溶媒の蒸発の直後に分析ゾーンへと濃縮することができる。
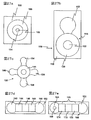
図15に例示される一変形では、捕捉チップ180は、図15の手順(a)で示すように、分析ゾーン182、分析ゾーン182の周辺で同心円を形成する捕捉ゾーン184、および捕捉ゾーン184を囲んでいる境界ゾーン186を有する表面を含む。捕捉ゾーン184内のSAMは、(たとえば、化学的、生物化学的)分析物を捕捉するための結合領域188を含む。図15は、目的分子を液体から抽出し、および次いで目的分子を分析ゾーン182上で濃縮するために捕捉ゾーン184を使用する一例を示す。図15の段階(b)に示すように、目的の分析物192(たとえばタンパク質、ペプチド、など)および望まれない分子194、196、198(たとえば、塩類、洗剤、混入物等)の分析物を含む流体190は、捕捉ゾーン184によって画成される境界内に配置される。図15の段階(c)に示すように、分析物192は、捕捉ゾーン184の表面上の官能基と結合する。図15の段階(c)に示すように、この結合相互反応が発生できるようにする期間が設けられた後、図15の段階(c)および(d)の間に示すように、望まれない分子194、196、198を運搬する液体200を次いで洗い流す。図15の段階(d)に示すように、望まれない分子を含まない液体202の新しい滴は次いで、捕捉ゾーン184および分析ゾーン182上に導かれる。次いで目的の分析物192は、捕捉ゾーン184の表面から放出される。目的分子192のこの放出は、液体202の新しい滴への化学物質の導入、目的分子の放出を円滑にする特定の固有特性を有する液体または溶媒の導入、光子の刺激、pHの変化、温度の変化、または他の化学的および/または物理的変化によって達成してもよい。次いで、液体は、捕捉ゾーン184および分析ゾーン182から蒸発または当業者に周知の他の手段によって除去され、図15の段階(e)に示すように、目的分子192に分析ゾーン182上に濃縮したままとしておく。
さらに、SAMはタンパク質検定に好まれうる。自己組織化分子膜は基材上に直接形成されうる。好ましくは、基材は金のような金属、またはケイ素のような半導体であるが、しかし、たとえば、ガラス、ケイ酸塩、半導体、金属、ポリマー(たとえば、プラスチック)、および他の水酸化材料、たとえば、ケイ素上のSiO2、アルミニウム上のAl2O3、などを含むがそれらに限定されないさまざまな材料を含みうる。しかし、金表面上のアルキルチオール、またはケイ素またはガラス表面上の有機シランの自己組織化単分子膜を形成することが好ましい。特定のゾーンに用いられるSAMを反映する特性を持つ別個のゾーンを生じるような方法で、SAMを本発明の試料提示器具に付加することができる。自己組織化層を形成するために用いられる分子は、基材表面と反応する、末端チオールまたはシラン基といった反応基を有しうる。アルキル部分のような炭化水素鎖もまた、分子の一部を形成しうる。分子はまた、側鎖分枝がほとんどまたは全く無いオリゴマー鎖またはポリマー鎖を有しうる。これらの鎖はまた随意的に、捕捉部分として直接用いることができる(たとえばビオチンまたは抗体)、またはさらに誘導体化されて捕捉表面を生じうる官能基を有しうる。表面修飾がモノクローナル抗体である捕捉ゾーンを含む本発明の試料提示器具は、液体試料から相補的抗原を結合し、および液体試料の残りが器具の表面の別の部分へ物理的移動または湿潤性の差によって移動する間にその抗原を保持しうる。保持された抗原は、その後、試料提示器具の捕捉ゾーンへの他の化合物の添加(たとえば、抗原の一部を切断する酵素の添加)によって修飾されうる。修飾された抗原は次いで、分析ゾーンへ移動、または捕捉表面自体として使用されうる。同様に、表面修飾がビオチンである捕捉ゾーンを含む本発明の試料提示器具は、液体試料からストレプトアビジン結合分析物を結合し、および液体試料の残りが器具の表面の別の部分へ物理的移動または湿潤性の差によって移動する間にその分析物を保持しうる。保持されたストレプトアビジン結合分析物は、その後、試料提示器具の捕捉ゾーンへの他の化合物の添加によって修飾されうる。修飾された分析物は次いで、分析ゾーンへ移動、または捕捉表面自体として使用されうる。
収束法によって作製された捕捉ゾーンを含む本発明の試料提示器具は、末端に反応基を提示している表面によって作製されうる。これらは、アミン末端を有するおよびカルボキシ末端を有するSAMを含みうるがそれらに限定されない。続いて捕捉ゾーン表面を作製するため、アミン反応性またはカルボキシ反応性種を導入できる。このように、アミン末端を有する表面は、無水マレイン酸部分および、一部飽和していてよい短鎖(C4−C11)アルキル基、一部飽和していてよい長鎖(C12−C24)アルキル基、置換されていてもいなくてもよい芳香基、荷電基、求核基、求電子基などを含むがそれらに限定されないさまざまな他の基を含む共重合体で処理されうる。これは、アミン末端と形成されたアミド結合を介して表面と結合した共重合体を生じ、および、捕捉表面としての使用のためのポリマーの機能部分を提示する。
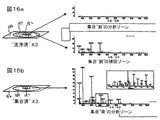
一つの特定の用途では、境界ゾーン186のSAMは11−(3,3,4,4,5,5,6,6,7,7,8,8,8−トリデカフルオロオクチルオキシ)ウンデカン−1−チオールを含み(実施例III)、捕捉ゾーン184のSAMはカルボキシ末端を有するポリエーテルアルキルチオラートを含み(ホワイトサイド(Whitesides)G.M.,ラヒリ(Lahiri)J.,アイザックス(Isaacs)L.,ティエン(Tien)J.Anal.Chem.1999,71(4)、777−790)、および分析ゾーン182のSAMはヒドロキシ末端を有するポリエーテルチオラートを含む(実施例IX)。塩化ナトリウムおよびドデシル硫酸ナトリウムといった望まれない分子を、血清由来のたとえばペプチドおよびタンパク質といった目的分析物と共に含む試料液滴が、この捕捉チップでの処理に提供されうる。質量分析を用いた分析用に目的の分子を抽出するために、図15に示す処理が次いで実施されうる。「試料洗浄」段階によって望まれない分子が除去された後、質量分析を捕捉ゾーン184で実施でき、および図16aに示すスペクトルを生じる。「分析物集中」段階が、分析物を分析ゾーン182へ濃縮するために実施される。質量分析を次いで分析ゾーン182で実施でき、図16bに示すのと同様のスペクトルを生じる。図16bのスペクトルを図16aと比較して、集中段階が目的分子の質量分析測定のシグナル対ノイズ比を顕著に改善しうることがわかる。捕捉チップ構成の上記の例は血清試料との使用に特に有用でありうるが、この捕捉チップはまた、分析物について分析または測定を実施する前の分析物の精製および/または濃縮が望ましい場合の他の用途にも導入されうることを当業者は理解する。
さらに別の変形では、分析ゾーンは分析物を捕捉および/または結合する結合表面より構成され、その一方で、分析ゾーンを囲んでいる液体保持ゾーンおよび他の表面領域は実質的に非結合性特性を有するSAMで覆われている。この設計によって、試料液滴が分析ゾーン上で濃縮することができ、およびさらに分析物が分析ゾーンの表面と結合することができる。次いで、質量分析または他の検出機構は、分析ゾーンの表面上に捕捉された分析物に対して実施してもよい。
別の変形では、分析ゾーンおよび液体保持ゾーンは結合/捕捉表面から構成される。たとえば、液体保持ゾーンは1種類の分子と結合するように構成されてもよく、一方、分析ゾーンは異なる種類の分子と結合するように構成されてもよい。複数の結合ゾーンを有するこれら構成は、分析ゾーンが目的分子を捕捉するために実施され、一方、液体保持ゾーンが一つ以上の望まれない分子を捕捉するために実施さされている用途において適用可能であってもよい。あるいは、一つの領域が1種類の分子を捕捉するために用いられ、一方で、他の領域が分析のために異なる種類の分子を捕捉するために用いられる。分子は、結合領域のちょうど上で分析してもよい。随意的には、捕捉された分子の異なる種類を、結合領域から選択的に放出でき、およびさらなる処理または測定のための分析ゾーンへ輸送してもよい。
本発明の別の実施態様は、表面上の(たとえば、化学的、生化学的、生物学的)分析物をろ過および/または濃縮する方法を含む。好ましくは、本方法は、複数のSAM領域を有する表面に対して実行される。一変形では、方法は、下記の段階を含む:第一に、目的の分析物および望まれない種を含む液体を表面上に送る;次いで、表面の第一の領域上の目的の分析物を捕捉または結合する;望まれない種を洗浄する;目的の分析物を、第一の領域から放出して、表面上の第二の領域へと導かれる;目的の分析物を、第二の領域上に集中および/または濃縮してもよい;次いで分析および/またはさらなる処理を目的の分析物に対して実施してもよい。液体は、表面上の異なる領域における液表面張力のばらつきによって、表面上を流れるよう導いてもよい。好ましくは、第二の領域は、実質的に非結合性である。加えて、本方法は、異なるSAMによって画成された一連の同心リングを含む表面上で実施してもよい。
別の変形では、目的の分析物および望まれない種の両方を含む液体が表面上に導かれる。望まれない種の少なくとも一部が、表面上の第一の領域上で捕捉される。目的の分析物を運搬する液体は、表面上の異なる領域における液表面張力のばらつきによる第二の領域へと導かれる。目的の分析物は、次いで第二の表面領域上に集中および/または濃縮してもよい。次いで分析および/またはさらなる処理を、第二の領域内の目的の分析物に実行してもよい。液体は、表面上の異なる領域における液表面張力のばらつきによって、表面上を流れるよう導いてもよい。好ましくは、第二の領域は、実質的に非結合性である。加えて、本方法は、異なるSAMによって画成された一連の同心リングを含む表面上で実行してもよい。試料提示器具を利用するさまざまな方法も、本明細書中において、記載されている。
実施例XVIII
捕捉チップの一変形の調製
24個の表面修飾基材を実施例XIIIに記載の通りに調製し、配列治具に入れ、および液体保持ゾーンとサイズおよび形状が対応する性質を有する、ピンレジスターエッチングしたステンレス鋼シャドーマスク(0.002インチ)で覆った。治具を120W/cm2定格の低圧水銀光源を付けた空冷紫外硬化システムの動くベルトに付け、および1時間の期間にわたって45から75回、光源の下を通した。UV曝露後、基材を治具から取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。曝露された基材を、0.1mMの11−アミノ−1−ウンデカンチオール(同仁化学(Dojindo Molecular Technologies,Inc.)製品コードA423−10)のエタノール溶液に入れ、および室温にて1ないし24時間の範囲の期間インキュベートした。パターン化された表面修飾基材を集合バスから取り出し、2400rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。液体保持ゾーンに付けられた水滴の前進接触角は48°から55の範囲にあり、および境界ゾーンに付けられた場合は110°から119°の範囲にあった。
上記のパターン化表面修飾基材を配列治具に入れ、および分析ゾーンとサイズおよび形状が対応する性質を有する、第二のピンレジスターエッチングしたステンレス鋼シャドーマスクで覆った。治具を紫外硬化システムの動くベルトに付け、および1時間の期間にわたって45から75回、光源の下を通した。UV曝露後、基材を治具から取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。曝露された基材を、0.1mMの6(11−{2−[2−(2−メトキシエトキシ)エトキシ]エトキシ}ウンデカン−1−チオール)を含むエタノール溶液に入れ、および室温にて1〜24時間インキュベートした。最後に、二回パターン化された表面修飾基材を集合バスから取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。分析ゾーンに付けられた水滴の前進接触角は47°未満であった。
これらの二回パターン化された表面を次いでアミン反応部位を含む長鎖ポリ(アルキル)共重合体の溶液(0.5%v/vピリジンを含む、1mg/mLを含むジクロロメタン)へ室温にて4時間曝露した。基材を続いて温クロロフォルムで洗浄し(2回)、続いてアセトニトリル/エタノール/水(84:13:3)の混合液で洗浄し、およびその後10%アンモニア溶液に30分間入れた。アンモニア溶液を続いて水での3回洗浄によって置換し、および基材をエタノールスピン洗浄に供した(上記参照)。液体保持ゾーンに付けられた水滴の前進接触角は84〜89°であった。
実施例XIX
捕捉チップ上での分析物の精製
MALDI−TOFスペクトル法では、分析物(たとえば;ペプチド、タンパク質、糖、オリゴヌクレオチド、など)のイオン化、およびしたがって検出は、分析すべき試料の純度および組成によって相当に影響される。塩(たとえば;塩化ナトリウム)、界面活性剤(たとえば;ドデシル硫酸ナトリウム、SDS)、緩衝液(たとえばトリス)および尿素といった材料は、特により希薄な試料では、分析物の検出を完全に抑制しうる。これらの材料は、試料に内因性であるかまたは何らかの試料処理段階中に導入される可能性があり、およびMALDI−TOF分析の前に追加の精製段階の必要を生じる。したがって、この処理に利用される現在の技術は、これらの望ましくない混入物を除去するための、逆相液体クロマトグラフィーまたはジップチップ(Ziptips)を含む固相抽出を含む。これらの追加の試料精製段階を用いる場合、容量保持能力がこれらの処理段階に一般的である溶出液量以内であるT3表面を、分析を実施するために使用できる。しかし、長鎖アルキル(LCA)基を液体保持ゾーン(LRZ)に含むX3表面の使用は、これらの混入物を含む試料に由来する分析物の検出を促進しうる。MALDI−TOF分析のために、表面上精製および続いて試料の集中を可能にすることによって、追加の処理段階(および装置および材料)の必要性が除かれうる。
ペプチドを分析するための捕捉チップの使用を説明する例を下記に説明する。酵母エノラーゼ消化物(ウォーターズ社(Waters Corp.)品番186002325、スイスプロットP00924)を、さまざまな混入物を含む20%アセトニトリル(ACN)/80%水の混合溶液に溶解した。水溶液部分はすべて0.1%トリフルオロ酢酸(TFA)および下記のうちの一つを含んだ:1M塩化ナトリウム(NaCl)、1M尿素(尿素)、1Mトリス緩衝液(トリス)、および0.1%ドデシル硫酸ナトリウム(SDS)。このように、エノラーゼ消化物をこれらの4種類の溶液のそれぞれに溶解し、および分析物の終濃度を1fmol/μLに調整した。
分析物を含む溶液を、実施例XVIIIに記載のX3チップの液体保持ゾーン(LRZ)(2x8アレイの16部位)へ10μL部分標本(10fmol総分析物)で加え、および表面上で20分間インキュベートした。並行して、作用を比較するために、同一の溶液をステンレス鋼MALDIプラットフォーム(ブルカー・ダルトニクス社(Bruker Daltonics)品番26755)へ加えた。ステンレス鋼表面の容量限界のために、試料10μLの全量は付けられなかった。
X3チップ上でのインキュベート後、溶液の大部分を除去し、および次いでその部位を0.1%TFA(3回)でピペットを用いて洗浄した。3回目の洗浄後の表面上の残液を乾燥させ、および次いでマトリクスのα−シアノ−4−ヒドロキシ桂皮酸(CHCA、ウォーターズ社(Waters Corp.)品番186002331、0.25mg/mLを含むアセトニトリル/エタノール/0.1%TFA 84:13:3)を含む溶液2μLを各部位に加えた。マトリクス溶液は広がって部位の直径3.0mmを満たした。乾燥に際して、試料およびマトリクスは、随伴するX3部位の分析ゾーン(AZ)へ濃縮された。試料は次いでMALDI−TOF分析用にホルダーへ固定された。同様に、MALDIステンレス鋼プレートについて洗浄を試み、マトリクスを加えおよびプレートをMALDI−TOF分析用に準備した。
MALDI−TOF分析は、陽イオンモードで、アキシマ(Axima)CFR(シマヅ・バイオテク社(Shimadzu Biotech)によるクレイトス・アナリティカル社(Kratos Analytical)、英国マンチェスター)で、パルスN2レーザー(337nm)、遅延引き出し、および加速電圧20kVを用いて実施した。装置はリフレクトロンモードで半自動化手順を用いて操作し、全般的に、25〜50ラスター点/部位、20〜50ショット/ラスター点を生じた。データは全ラスター点の平均として回収および保存し、および次いでMASCOT(http://www.matrixscience.com)を用いたペプチド質量フィンガープリント法(PMF)による分析に供した。MASCOTとは、タンパク質を一次構造から同定するための、質量スペクトル中の観察されたフラグメント(ピーク)を用いる検索エンジンである。
4例すべてで、ステンレス鋼上での直接分析は、実用にならないデータを結果として生じた。各混入物は、スペクトル中で真のピークがノイズと識別できない、ノイズの多いスペクトルの原因となった。きれいな(すなわち、意図的に混入されていない)消化物のステンレス鋼表面への直接使用は、PMFを実施できるスペクトルを確かに生じた。対照的に、X3表面はシグナル対ノイズ(S/N)比が高くおよびピークが多いスペクトルを与えた。図17a〜17dは、記載の混入物の存在下での表面上精製後に生じたスペクトルを図解する。図17aは1M NaClの混入した試料から得られた結果を示し、図17bは1M尿素の混入した試料から得られた結果を示し、図17cは1Mトリスの混入した試料から得られた結果を示し、一方、図17dは0.1%SDSの混入した試料から得られた結果を示す。X3表面からのこれらのスペクトルのMASCOT分析はすべて、正しい消化されたタンパク質を最も高確率の答えとして特定した。これらの結果は、X3表面が目的のペプチドを、一般的な混入物の存在下で、追加の精製段階の必要無しに直接分析する能力を明らかにする。
実施例XX
ゲル内消化されたタンパク質の直接使用および分析
ゲル内でのタンパク質の酵素消化は、プロテオミクスの分野で用いられる一般的な手法である。1−Dまたは2−D電気泳動および染色の完了時に、ゲル片を切り出しおよび消化前に脱色し、およびその後続いて還元および遊離チオールのアルキル化を行う。結果として生じたペプチドをその後、可溶化および酸性溶液中へ放出しうる。試料はこの段階ではしばしば希薄でありおよび混入物(たとえば塩、低分子、など)を含むため、MALDI−TOFによる分析前に精製および濃縮計画が有益でありうる。この精製のための現在の方法は、液相クロマトグラフィーまたは固相抽出カートリッジの使用を含む。液体クロマトグラフィーは機器に依存する処理であり、および市販の固相抽出製品(たとえばジップチップ(ZipTip))は先端間性能の問題を有しうる。この必要は分析を処理量の低い工程にする可能性がある。したがって、これらの干渉する混入物の少なくとも一部を除去する能力を有する試料測定表面が望ましい可能性がある。そのような試料測定表面は、分析物検出および測定のための再現可能なおよび高処理量のプラットフォームを提供しうる。
一つの具体的用途では、ウサギ筋由来ホスホリラーゼb(シグマ社(Sigma)品番P6635、スイスプロットP00489)を18MΩ水に溶解してストック溶液とした。このストックを次いで、1−Dゲル電気泳動用のタンパク質を調製するのに用いた。このように、Laemmli緩衝液(バイオラッド社(Bio−rad)品番161−0737)を取扱説明書に従って調製し、およびタンパク質ストックを使用前に希釈するのに用いた。ゲル電気泳動はトリスHCl緩衝液中プレキャスト4〜15%SDS PAGEゲル(バイオラッド社(Bio−rad)製品番号161−1176)を用いて70V定電圧で実施した。泳動の完了時に、ゲルをゲルコードブルー(Gel Code Blue)(ピアース社(Pierce)製品番号24590)を用いて一夜染色し、および続いて水で洗浄した。材料を次いでトリプシンを用いるゲル内消化のために準備した。市販のゲル内トリプシン消化キット(ピアース社(Pierce)製品番号8987IX)を使用しおよび取扱説明書に従ったが、しかし試料は液体クロマトグラフィー精製に供しなかった。消化された試料ストックの終濃度は約7.5pmol/μLであり、および希釈を実施して作業用溶液濃度7.5fmol/μL含有25%アセトニトリル/0.1%TFAを与えた。消化試料ストックの一部をまた、取扱説明書に従ってジップチップ(ZipTip)μ18(ミリポア社(Millipore)品番ZTC18M)に通した。この試量の濃度を次いで7.5fmol/μL含有25%アセトニトリル/0.1%TFAに調整した。この精製試料をその後、比較のためにT3表面に用いた。
分析物を含む溶液(10μL)を、実施例XVIIIに記載のX3型の液体保持ゾーン(LRZ)へ加え(75fmol総分析物)および表面上で20分間インキュベートした。インキュベート後、溶液の大部分を除去し、および次いでその部位を10μLの0.1%TFA(3回)でピペットを用いて洗浄した。3回目の洗浄後の表面上の残液を乾燥させ、および次いでマトリクスのα−シアノ−4−ヒドロキシ桂皮酸(CHCA、ウォーターズ社(Waters Corp.)品番186002331、0.065mg/mLを含むアセトニトリル/エタノール/0.1%TFA84:13:3)を含む溶液2μLを各部位に加えた。マトリクス溶液は広がって部位の直径3.0mmを満たした。乾燥に際して、試料およびマトリクスは、随伴するX3部位の分析ゾーン(AZ)へ濃縮された。試料表面は次いでMALDI−TOF分析用にホルダーへ固定された。
同様に、精製した消化物試料(10μL)をT3の液体保持ゾーン(LRZ)へ加え(75fmol総分析物)および集中および乾燥させた。その後、マトリクスのα−シアノ−4−ヒドロキシ桂皮酸(CHCA、ウォーターズ社(Waters Corp.)品番186002331、0.065mg/mLを含むアセトニトリル/エタノール/0.1%TFA84:13:3、10mMクエン酸アンモニウム含有)を含む溶液2μLを各部位に加えた。マトリクス溶液は広がって部位の直径3.0mmを満たした。乾燥に際して、試料およびマトリクスは、随伴するT3部位の分析ゾーン(AZ)へ濃縮された。試料表面は次いでMALDI−TOF分析用にホルダーへ固定された。
MALDI−TOF分析は、陽イオンモードで、アキシマ(Axima)CFR(シマヅ・バイオテク社(Shimadzu Biotech)によるクレイトス・アナリティカル社(Kratos Analytical)、英国マンチェスター)で、パルスN2レーザー(337nm)、遅延引き出し、および加速電圧20kVを用いて実施した。装置はリフレクトロンモードで半自動化手順を用いて操作し、全般的に、25〜50ラスター点/部位、20〜50ショット/ラスター点を生じた。データは全ラスター点の平均として回収および保存し、および次いでMASCOT(http://www.matrixscience.com)を用いたペプチド質量フィンガープリント法(PMF)による分析に供した。MASCOTとは、タンパク質を一次構造から同定するための、質量スペクトル中の観察されたフラグメント(ピーク)を用いる検索エンジンである。
試料のステンレス鋼表面への直接使用は、識別可能なスペクトルを生じなかった。10pmol試料の例を図18cに示す。ステンレス鋼上のこれ未満のすべての濃度は、スペクトル中のノイズだけを結果として生じた。X3表面はペプチドを精製しおよび分析ゾーン(AZ)へ集中することができた。図18aに示す通り、スペクトルは特にm/z値1300ダルトンを上回るフラグメントピークに富んだ。ジップチップ(ZipTip)/T3法もまた、ピークに富むスペクトルを結果として生じたが、しかし質量範囲は図18bに示す通り、低分子量(2000ダルトン未満)種側へ歪んでいる。
X3手順またはジップチップ(Ziptip)/T3手順の結果として生じたスペクトルは外見が確かに異なるが、両方の方法がこの種類の分析に適している。ジップチップ(Ziptip)の、脱塩のためのT3表面と組み合わせた使用は、観察されたピークの37%が理論的に決定されるフラグメントと一致する結果を与えた。一致するペプチドは、予想されるトリプシン消化物フラグメントの配列カバー度37%に相当する。ゲル内消化物のX3表面への直接使用は、ピークの44%が、配列カバー度39%に相当する理論的に予想されるフラグメントと一致するスペクトルを生じた。これらの値は、ジップチップ(Ziptip)での精製およびMALDI試料プレートへの移動の、しかし追加の試料調製段階を含まない処理によって得られた値に相当する。
実施例XXI
X3表面の拡大された質量範囲カバー度
X3−アセトニトリル−TFA手順
ウサギホスホリラーゼB(ウォーターズ社(Waters Corp.)品番186002326、スイスプロットP00489)を、50%アセトニトリル(ACN)/50%トリフルオロ酢酸の混合溶液に溶解し、および終濃度を1fmol/μLに調整した。分析物を含む溶液(10μL)を、実施例XVIIIに記載のX3型表面の液体保持ゾーン(LRZ)に加え(10fmol総分析物)、および表面上で20分間インキュベートした。インキュベート後、溶液の大部分を除去し、および次いでその部位を10μLの0.1%TFA(2回)でピペットを用いて洗浄した。3回目の洗浄後の表面上の残液を乾燥させ、および次いでマトリクスの2,5−ジヒドロキシ安息香酸(DHB、ウォーターズ社(Waters Corp.)品番186002333、0.65mg/mLを含む10mMクエン酸アンモニウム含有アセトニトリル/0.1%TFA、4:1)を含む溶液2μLを各部位に加えた。マトリクス溶液は広がって部位の直径3.0mmを満たした。乾燥に際して、試料およびマトリクスは、随伴するX3部位の分析ゾーン(AZ)へ濃縮された。試料表面は次いでMALDI−TOF分析用にホルダーへ固定された。
X3−アセトニトリル−MOPS手順
別に、ウサギホスホリラーゼB(ウォーターズ社(Waters Corp.)品番186002326、スイスプロットP00489)を、50%アセトニトリル(ACN)/50%3−(N−モルホリノ)プロパンスルホン酸(MOPS、200mM、pH6.5)の混合溶液に溶解し、および終濃度を1fmol/μLに調整した。分析物を含む溶液(10μL)を、実施例XVIIIに記載のX3型表面の液体保持ゾーン(LRZ)に加え(10fmol総分析物)、および表面上で20分間インキュベートした。インキュベート後、溶液の大部分を除去し、および次いでその部位を10μLの20mM酢酸アンモニウム(2回)でピペットを用いて洗浄した。3回目の洗浄後の表面上の残液を乾燥させ、および次いでマトリクスの2,5−ジヒドロキシ安息香酸(DHB、ウォーターズ社(Waters Corp.)品番186002333、0.65mg/mLを含む10mMクエン酸アンモニウム含有アセトニトリル/0.1%TFA、4:1)を含む溶液2μLを各部位に加えた。マトリクス溶液は広がって部位の直径3.0mmを満たした。乾燥に際して、試料およびマトリクスは、随伴するX3部位の分析ゾーン(AZ)へ濃縮された。試料表面は次いでMALDI−TOF分析用にホルダーへ固定された。
T3−アセトニトリル−TFA手順
ウサギホスホリラーゼB(ウォーターズ社(Waters Corp.)品番186002326、スイスプロットP00489)を、50%アセトニトリル(ACN)/50%トリフルオロ酢酸の混合溶液に溶解し、および終濃度を1fmol/μLに調整した。分析物を含む溶液(10μL)を、実施例XIIIに記載のT3型表面の液体保持ゾーン(LRZ)に加え(10fmol総分析物)、および表面上で20分間インキュベートした。インキュベート後、溶液の大部分を除去し、および次いでその部位を10μLの0.1%TFA(2回)でピペットを用いて洗浄した。3回目の洗浄後の表面上の残液を乾燥させ、および次いでマトリクスの2,5−ジヒドロキシ安息香酸(DHB、ウォーターズ社(Waters Corp.)品番186002333、0.65mg/mLを含む10mMクエン酸アンモニウム含有アセトニトリル/0.1%TFA、4:1)を含む溶液2μLを各部位に加えた。マトリクス溶液は広がって部位の直径3.0mmを満たした。乾燥に際して、試料およびマトリクスは、随伴するT3部位の分析ゾーン(AZ)へ濃縮された。試料表面は次いでMALDI−TOF分析用にホルダーへ固定された。
MALDI−TOF分析は、陽イオンモードで、アキシマ(Axima)CFR(シマヅ・バイオテク社(Shimadzu Biotech)によるクレイトス・アナリティカル社(Kratos Analytical)、英国マンチェスター)で、パルスN2レーザー(337nm)、遅延引き出し、および加速電圧20kVを用いて実施した。装置はリフレクトロンモードで半自動化手順を用いて操作し、全般的に、25〜50ラスター点/部位、20〜50ショット/ラスター点を生じた。データは全ラスター点の平均として回収および保存し、および次いでMASCOTを用いたペプチド質量フィンガープリント法(PMF)による分析に供した。
X3型表面上で両方の方法が、高いシグナル対ノイズ比を有するピークに富むスペクトルを与えたが、しかし配列の完全な重複は無かった。TFA手順は、図19aに示す通り、配列カバー度44%のスペクトルを与える。MOPS手順は、図19bに示す通り、配列カバー度46%のスペクトルを結果として生じたが、しかし、より重要なことに、試料自体に関する新しい情報を明らかにした。各手順からの同定されたフラグメントを合わせる場合、配列カバー度はホスホリラーゼbのトリプシン消化からの予測されるフラグメントの57%に上昇する。これは、図19cに示す通り、精製された消化物試料を加えた後にT3型表面から得られた結果とよく一致する。この場合、配列カバー度は58%であり、および試料からの容易に検出可能な目的断片の代表でありうる。
捕捉機構として抗体を利用する例
複雑な溶液(たとえば、血清,混合タンパク質分解消化物、血漿など.)に由来する分析物の特異的単離および検出は、さまざまな生物、生化学および化学分析処理に決定的に重要である。抗体は、利用可能な最も選択性が高くおよび高感度な手法の一つであり、およびさまざまな分析物に対して容易に作製できる。抗体は、臨床化学、環境分析、および研究開発に幅広く用いられているイムノアッセイの基礎を成す。抗体を用いて精製された分析物は、典型的には、分析基材(たとえばMALDI基材、など)への使用前に一つ以上のオフライン精製および濃縮段階を必要とし、それは相当な試料損失を結果として生じうる。
単一の基材上で分析物の捕捉および濃縮段階の実施が可能な器具は、試料損失を最小化および検出能力を改善しうる。抗体および分析物を特異的に捕捉する他のリガンドを、試料提示器具上の表面へ固定化して捕捉ゾーンを形成できる。たとえば、X3表面をさまざまな化学によって修飾して、固定化抗体を有する捕捉ゾーンを作製できる。X3チップはその結果、選択的捕捉、濃縮、およびMALDI−MS用の提示を単一の器具上で与えるために利用でき、そのことは追加の処理段階の必要性を解消しうる。
一例では、抗体を固定するための表面を有する試料提示器具の調製用の化学物質を生じるために、下記の群の化学物質が合成された。
2−[2−(2−{2−[2−(2−ウンデカ−10−エニルオキシエトキシ)エトキシ]エトキシ}エトキシ)エトキシ]エタノール(13)。
100mL丸底フラスコにヘキサエチレングリコール(26.9mL、0.1mol)を入れ、およびこれに50%水酸化ナトリウム水溶液(1.72mL、22mmol)を加えた。溶液を100℃へ加温しおよび30分間攪拌した。この時、11−ブロモウンデカ−1−エン(4.7mL、21mmol)を滴下して加え、および反応を100℃にて18時間、TLC分析が開始材料が消費されるのを示すまで継続し、およびその後室温へ冷却した。溶媒を減圧して蒸発し、油性の残渣を与えた。この残渣をカラムクロマトグラフィー(SiO2、40x200mm、20%メタノール/酢酸エチル)に供し、次いで目的の産物を含む画分を合わせ、および溶媒を蒸発させて、2.0g(21%)の13を淡黄色の油として与えた。
1H NMR(400MHz,CDCl3):δ5.78(m,IH)、4.94(m,2H)、3.69−3.54(m,24H)、3.42(t,J=7.0Hz,2H)、2.38(bs,IH)、2.01(m,2H)、1.55(m,2H)3 1.33(m,2H)、1.23(bs,10H)。
{2−[2−(2−{2−[2−(2−ウンデカ−10−エニルオキシエトキシ)エトキシ]エトキシ}エトキシ)エトキシ]エトキシ}−酢酸tert−ブチルエステル(14)。
50mL丸底フラスコに13(2.0g、4.6mmol)を無水条件下で入れた。これを10mLの乾燥ジメチルホルムアミドに溶解し、および0℃へ外から冷却した。この冷溶液へ水素化ナトリウム(60%含有鉱油、267mg、6.9mmol)を一度に加え、および泡立つ混合物をアルゴン下で0℃にて10分間攪拌した。この時、ブロモ酢酸tert−ブチル(1.02mL、6.9mmol)を滴下して加え、および反応を20℃へ8時間加温した。TLC分析は、この時点で反応は進行停止していたことを示した。反応を水10mLの緩やかな添加によって停止し、酢酸エチル50mLで希釈し、および水(2x50mL)で抽出した。有機層を硫酸マグネシウム上で乾燥し、ろ過しおよび溶媒を蒸発し、油状の残渣を与えた。残渣を次いでカラムクロマトグラフィー(SiO
2、40x200mm、100%酢酸エチル)に供し、次いで目的の産物を含む画分を合わせ、および溶媒を減圧して蒸発させて、1.64g(65%)の14を無色の油として与えた。
1H NMR(400MHz,CDCl
3):δ5.79(m,1H)、4.94(m,2H)、4.00(s,2H)、3.71−3.54(m,24H)、3.42(t,J=6.8Hz,2H)、2.01(m,2H)、1.54(m,2H)、1.45(s,9H)、1.34(m,2H)、1.24(bs,10H)。
(2−{2−[2−(2−{2−[2−(11−アセチルスルファニルウンデシルオキシ)エトキシ]エトキシ}エトキシ)エトキシ]−エトキシ}エトキシ)酢酸tert−ブチルエステル(15)。
50mL丸底フラスコに14(1.64g、3.0mmol)を無水条件下で入れ、およびこれを20mLの乾燥メタノールに溶解した。これに2、2’−アゾビス(2−メチルプロピオンアミジン)二塩酸塩(81mg、0.3mmol)を加え、次いでチオール酢酸(715μL、10mmol)を加えた。反応はホイルテントで覆い、および低圧水銀灯からの光に曝露した。4時間後、TLC分析が、開始物質が消費されてしまったことを示した。溶媒を減圧して蒸発し、油状の残渣を与えた。残渣を次いでカラムクロマトグラフィー(SiO
2、40x200mm、100%酢酸エチル)に供し、次いで目的の産物を含む画分を合わせ、および溶媒を蒸発させて、1.48g(79%)の15を無色の油として与えた。
1H NMR(400MHz,CDCl
3):δ4.02(s,2H)、3.73−3.56(m,24H)、3.44(t,J=6.8Hz,2H)、2.86(t,J=7.2Hz,2H)、2.32(s,3H)、1.56(m,4H)、1.48(s,9H)、1.25(bs,14H)。
(2−{2−[2−(2−{2−[2−(11−メルカプトウンデシルオキシ)エトキシ]エトキシ}エトキシ)エトキシ]−エトキシ}エトキシ)酢酸(16)。
テフロン/シリコンセプタムキャップ付き20mL褐色バイアルに15(2.0g、3.2mmol)を入れ、およびこれを3Nメタノール塩酸(5mL、15mmol)に溶解し、および50℃に加温した。溶液を50℃に2時間保った。溶媒を次いで減圧して除去し、および残渣を、残渣の添加前に脱酸素してあった、50%水酸化カリウム水溶液を含むメチルスルホキシド(1:1)5mLに溶解した。混合物を室温にて1時間攪拌し、および次いで溶媒を減圧して蒸発して、1.6g(95%)の16を透明な油として与えた。本発明の化合物はさらにクロマトグラフィー精製を要しなかった。1H NMR(400MHz,CDCl3):δ9.98(bs,1H)、4.14(s,2H)、3.74−3.57(m,24H)、3.44(t,J=6.8Hz,2H)、2.51(q,J=7.2,2H)、1.57(m,4H)、1.32(t,J=7.6Hz,IH)、1.26(bs,14H)。
実施例XXII
パターン化試料提示器具の調製
(X3式、NHS(N−ヒドロキシスクシニミド)例)
抗体を用いた捕捉ゾーンを備えた試料提示器具を製造する工程において、抗体を受容しおよび固定するために修飾された意図された捕捉ゾーンを備えた器具を最初に調製してもよい。次いで、製造された試料提示器具は、意図された用途に応じて特異的な抗体をカスタマイズしてもよい。既成の試料提示装置は大量生産工程に活用して製造コストを最小化してもよい。たとえば、大量の既製の試料提示装置を最初に作製して、次いで製造の選択的なバッチに特異的な種類の抗体をカスタマイズしてもよい。別の用途では、既製の試料提示装置をエンド・ユーザーに提供してもよい。次いでエンド・ユーザーは、試料提示装置の捕捉ゾーン中の特異的な抗体を固定することによって既製の試料提示器具をカスタマイズしてもよい。
既製の試料提示器具を作製する方法の例を下記に記載する。この実施例では、試料提示器具上の捕捉ゾーンは、抗体を固定するために用いてもよいようNHS−エステル基によって誘導される。24個の表面修飾基材を実施例XIIIに記載の通りに調製し、特別製の配列治具に入れ、および液体保持ゾーンとサイズおよび形状が対応する性質を有する、ピンレジスターエッチングしたステンレス鋼シャドーマスク(0.002インチ)で覆った。治具を120W/cm2定格の低圧水銀光源を付けた空冷紫外硬化システムの動くベルトに付け、および1時間の期間にわたって45から75回、光源の下を通した。UV曝露後、基材を治具から取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。曝露された基材を、5%の16−メルカプトヘキサデカン酸および95%の6(0.1mMの全チオール濃度)を含有する混合エタノール溶液中に入れ、室温に冷却し、および室温にて1ないし24時間の範囲の期間インキュベートした。パターン化された表面修飾基材を集合バスから取り出し、2400rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。
パターン化表面修飾基材を特別製の配列治具に入れ、および分析ゾーンとサイズおよび形状が対応する性質を有する、第二のピンレジスターエッチングしたステンレス鋼シャドーマスクで覆った。治具を紫外硬化システムの動くベルトに付け、および1時間の期間にわたって45から75回、光源の下を通した。UV曝露後、基材を治具から取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。曝露された基材を、0.1mMの9を含むエタノール溶液に入れ、および室温にて1〜24時間インキュベートした。最後に、二回パターン化された表面修飾基材を集合バスから取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。
これらの二回パターン化された表面を次いで25mMリン酸緩衝液、pH8.0中で15分間インキュベートした。二回パターン化された表面を次いで緩衝溶液から取り出し、および1−[3−(ジメチルアミノ)プロピル]−3−エチルカルボジイミド塩酸塩(EDC;0.4M)およびN−ヒドロキシスクシニミド(NHS;0.1M)を含む水溶液で60分間室温にて処理した。基材を続いてUHP水で洗浄し、次いでアセトンで洗浄しおよび窒素気流下で風乾した。NHS−エステル基の存在は、図20に示す通り、仰角FTIR(〜1742cm−1)によって確認された。
実施例XXIII
抗体固定化ならびに緩衝液および希釈血清試料からの抗原検出
抗体を固定化して試料提示器具上に捕捉ゾーンを形成し、およびそれらを複雑な検出物からヒトペプチドホルモンを特異的に捕捉および検出するために使用する例を下記に説明する。ヒト副腎皮質刺激ホルモン(ACTH)のC末端(アミノ酸18−39;セロテック社(Serotech)、品番MCA2000)またはN末端(アミノ酸1−24;バイオデザイン社(Biodesign)品番E54057M)部分のどちらかに対するモノクローナル抗体、および非特異的マウス免疫グロブリン(IgG;ケミコン社(Chemicon)、品番PPlOO)調製物を、25mMリン酸ナトリウム、pH8.0および0.1%ツィーン−20を含む緩衝液に溶解して終濃度0.5mg/mLとした。
抗体溶液10μLを、実施例XXIIに記載のX3チップの液体保持ゾーンに加え、および60分間、相対湿度(RH)100%に保たれたチャンバー内でインキュベートした。抗体溶液をチップから、0.05%ツィーン−20(TBS/ツィーン)を含むトリス−緩衝生理食塩水溶液の過剰量で、スプレー瓶を用いて洗い流した。過剰の洗浄溶液をその部位から緩やかな振とうで除去し、次いで10μLの50mMエタノールアミン(シグマ社(Sigma)品番E9508)、pH9.0、0.1%ツィーン−20を含む溶液を部位に加え、および30分間100%RHにてインキュベートした(この操作は残存する活性化NHS基があれば停止させおよびそれらが他の材料と共有結合するのを防ぐ)。インキュベート後、エタノールアミン溶液を、スプレー瓶からのTBS/ツィーンを用いて上記のように洗い流した。各部位を次いで、0.5%ツィーン−20を含むウシ血清アルブミン(BSA;シグマ社(Sigma)品番A3059)1%溶液5μLで処理して、分析物の添加前に非特異的結合部位があればブロックした。BSA溶液をチップ上で30分間100%RHにてインキュベートし、次いで上記の通り洗浄した。
ACTHペプチド(完全長、アミノ酸1−39、バケム社(Bachem)品番H−4998;またはC末端、アミノ酸18−39、バケム社品番H−1215)を含む10%ウサギ血清またはTBS/ツィーンの希釈物の5μL部分試料を、2nMないし100nMの範囲のペプチド濃度で部位に加えた。ペプチドをチップ上で30分間100%RHにてインキュベートし、次いでスプレー瓶からのTBS/ツィーン、その後UHP水で洗浄した。チップを次いで窒素気流下で乾燥した。マトリクスの2、5−ジヒドロキシ安息香酸(DHB;ブルカー・ダルトニクス社(Bruker Daltonics)品番203074)、0.5mg/mLを含む、10mMクエン酸二アンモニウム含有アセトニトリル/エタノール/0.1%TFA(84:13:3)溶液2μLを各部位に加えた。マトリクス溶液は広がって部位の直径3.0mmを満たした。乾燥に際して、試料およびマトリクスは、随伴するX3部位の分析ゾーン(AZ)へ濃縮された。試料は次いでMALDI−TOF分析用にホルダーへ固定された。
MALDI−TOF分析は、陽イオンモードで、アキシマ(Axima)CFR(シマヅ・バイオテク社(Shimadzu Biotech)によるクレイトス・アナリティカル社(Kratos Analytical)、英国マンチェスター)で、パルスN2レーザー(337nm)、遅延引き出し、および加速電圧20kVを用いて実施した。装置はリフレクトロンモードで半自動化手順を用いて操作し、全般的に、25〜50ラスター点/部位、20〜50ショット/ラスター点を生じた。データは全ラスター点の平均として回収および保存した。スペクトルを、予測されたm/Zで明確なピークの存在または非存在がないか評価した。
10%ウサギ血清で終濃度10nMに希釈された両方のACTHペプチドは、ACTHのC末端に対するモノクローナル抗体(mAb)が固定化された部位上で、MALDI−TOF分析によって容易に検出された。非特異的マウスIgGを有する部位からのスペクトルは、どちらのACTHペプチドの捕捉も示さなかった。10%ウサギ血清をステンレス鋼プレートに加えた場合は、追加のACTHペプチドを含んでも含まなくても、有用なMALDI−TOFスペクトルを得ることはできなかった。
TBS/ツィーン緩衝液での各ACTHペプチドの一連の希釈の使用は、これらのX3チップ上での抗原捕捉および検出の特異性および感度をさらに明らかにした。図21は抗体/抗原対合が2nM濃度でのペプチドの検出を可能にすることを示す一方、ミスマッチペアのスペクトルは高濃度(100nM)溶液からペプチドの結合を示さなかった。抗ACTHC末端抗体捕捉ゾーンを用いて、ACTH18−39(C末端)およびACTH1−39(完全長)ペプチドの両方について2nMの低さの抗原濃度は、検出陽性を結果として生じた。抗ACTH N末端抗体捕捉ゾーンを用いて、ACTH18−39(C末端)ペプチド抗原と組み合わせた場合、ペプチド濃度が100nMの高さである場合さえ、予想通り陰性結果が得られる。抗ACTH N末端抗体捕捉ゾーンを用いて、ACTH1−39(完全長)ペプチド抗原と組み合わせた場合、濃度が2nMの低さである場合さえ、予想通り陽性結果が得られた。捕捉ゾーン上に非特異的マウスIgG抗体を使用する対照群を用いて、ACTH18−39(C末端)ペプチドおよびACTH1−39(完全長)ペプチドの両方が、100nMの高さの濃度で、予想通り結果として検出陰性を生じた。これらのデータは、本器具が高感度でありおよび低濃度(たとえば2nM)で抗原検出が可能であることを示唆する。同時に、本器具は抗原濃度が非常に高い(たとえば100nM)場合でさえ検出陰性によって示された通り、偽陽性結果に対する高い耐性を有する。
これらの結果は、このX3表面が抗体を固定化し、およびこれらの抗体を、特異的におよび高感度に生物分子を複雑な混合物から、別の精製または濃縮段階の必要無しに検出するために使用する能力を説明する。
捕捉機構として固定化金属イオンを利用する例
別の変形では、金属イオンを捕捉ゾーンに負荷して、特定の分析物を捕捉するための選択的結合インターフェースを提供できる。適当な金属イオンを捕捉ゾーンに負荷することによって、固定化金属アフィニティクロマトグラフィー(IMAC)表面を捕捉ゾーンに形成できる。
一つの変形では、鉄(すなわち、Fe(III))が捕捉ゾーンに負荷される。別の変形では、ニッケル(すなわち、Ni(II))が捕捉ゾーンに負荷される。捕捉ゾーンに負荷された金属は、選択された分析物を捕捉するためのさまざまな用途に利用されうる。一例では、捕捉ゾーンに負荷されたFe(III)を有する試料提示器具が、リン酸化ペプチドを捕捉するのに用いられる。別の一例では、捕捉ゾーンに負荷されたNi(II)を有する試料提示器具が、Hisタグ化種を捕捉するのに用いられる。本開示を利用する当業者は、さまざまな金属を試料提示器具の捕捉ゾーンに選択的に負荷できること、および次いで対応する生物製剤、生化学物質、および/または化学物質を、分析および/または処理のために捕捉するのに使用できることを理解する。
たとえば、金属負荷された捕捉ゾーンを有する試料提示器具は、プロテオミクス研究に特に有用でありうる。多数のプロテオミクス研究は、疾患経路に関与するタンパク質の翻訳後修飾における差異を特に探索する。一つのそのような修飾は、経路をオンまたはオフに切り替えるスイッチとして作用しうるタンパク質リン酸化である。ホスホペプチドおよびタンパク質を単離するために一般的に用いられる方法は、固定化金属アフィニティクロマトグラフィー(IMAC)である。しかし、典型的なIMAC手順は扱いにくいおよび/または費用を要する可能性があり、および通常は複数の試料液移動段階を必要とする。金属負荷捕捉表面を有する試料提示器具を利用して、使用者は試料移動を最小化および/または標的分子検出能力を増大できる可能性がある。一例では、金属イオンを含むX3表面が、ホスホペプチドまたはタンパク質をキレート化するために用いられ、それが次いで非結合材料を洗い去ることを可能にする。キレート化されたリン酸化試料をその後溶出しおよびMALDI−MS用にマトリクスと共結晶化できる。これは全体の試料取り扱い段階を減少でき、およびしたがって試料損失および混入の危険を最小化する。
別の変形では、試料提示器具は捕捉ゾーン中の別のIMAC表面と構成される。一例では、既製の試料提示器具がNi(II)負荷表面へ変換される。結果として生じる試料提示器具は、Hisタグ材料を試料溶液から捕捉するために利用されうる。Hisタグは、精製を容易にするためにしばしば組み換えタンパク質に組み込まれる。すべての非結合材料をよく洗浄後、結合したタンパク質をさまざまな手段(たとえば、過剰のイミダゾールまたは酸性条件下で、など)によって溶出および単離できる。このように、X3 IMAC表面を、Hisタグを有しないタンパク質を除外して、Hisタグ化タンパク質を捕捉するのに使用できる。
本開示を利用できる当業者は、本明細書中に記載された方法が、さらなる処理または分析のために選択的な種(たとえば、リン酸化チロシン、Hisタグ種、など)を捕捉するさまざまな器具において表面を調製するのに利用できることを理解する。さらに、特異的な分析物を捕捉するための選択的な結合界面を提供するために他の金属(たとえばZn、Cu、など)も捕捉ゾーンへと負荷されてもよいことが意図されている。
一例では、選択的な金属イオンを受容および結合するために構成された捕捉ゾーンを有する既製の試料提示器具の調製用の化学物質を生じるために、下記の群の化学物質が合成された。
1,2,3,4,5−ペンタフルオロ−6−ウンデカ−10−エニルオキシメチル−ベンゼン(17)。
乾燥した200mL丸底フラスコに10−ウンデセニルアルコール(5.11g、30mmol)をアルゴン下で入れ、および30mLの乾燥テトラヒドロフラン(THF)を加えた。結果として生じる溶液を0℃へ冷却し、およびカリウムt−ブトキシド(14.67g、200mmol)を含むTHF60mLの溶液を滴下して加えた。混合物をアルゴン下で0℃にて90分間攪拌した。冷却した攪拌された溶液へ、臭化2,3,4,5,6−ペンタフルオロベンジル(5.07mL、36mmol)を滴下して加え、および反応を90分間0℃にて継続させた。反応を水30mLの緩やかな添加によって停止し、および溶液の総量を30〜40mL以下へ、溶媒のロータリーエバポレーションによって減らした。これを次いで200mLへ酢酸エチルで希釈し、および次いで食塩水(1x200mL)および水(2x200mL)で抽出した。有機層を硫酸マグネシウム上で乾燥し、ろ過しおよび溶媒を蒸発し、17を油として与えた。残渣を「そのまま」次の反応に用いた。
チオ酢酸11−ペンタフルオロフェニルメトキシ−ウンデシルエステル(18)。
乾燥したジャケット付き250mL光反応容器に、17(10.52g、30mmol)およびチオール酢酸(10.72mL、150mmol)を入れた。これらを150mLの乾燥メタノールに溶解し、および次いで2,2’−アゾビス(2−メチルプロピオンアミド)二塩酸塩(814mg、3mmol)を加えた。紫外灯を点灯し、および混合物をアルゴン下で一定に攪拌して4時間照射した。反応を連続的に冷却し(水ジャケット)および光反応処理中の温度は38℃未満を維持した。反応容器を室温まで冷却させ、および溶媒を蒸発させて淡黄色の油を与えた。油をシリカゲルクロマトグラフィー(41x300mm、1%酢酸エチル/ヘキサン、酢酸エチル濃度を2カラム容ごとに1%上昇させる)に供し、および目的の産物を含む画分を回収し、合わせ、および溶媒を減圧して蒸発し、3.74g(29%、2段階)の18を無色の油として与えた。
1H NMR(400MHz,CDCl
3):δ4.46(pt,2H)、3.46(t,2H)、4.16(t,J=6.8Hz,2H)、2.85(t,J=6.0Hz 2H)、2.31(s,3H)、1.72(m,2H)、1.56(m,2H)、1.24−1.36(broad m,14H)。
11−ペンタフルオロフェニルメトキシ−ウンデカン−1−チオール(19)。
40mL褐色バイアルにテフロン被覆シリコンセプタムを付け、および18(1.55g、3.6mmol)を入れた。これを10mLの4.9Nエタノール塩酸に溶解し、および結果として生じる溶液を40℃に2.5時間加温した。溶媒を次いで減圧して蒸発し、無色の油状の残渣を与えた。残渣をシリカゲルクロマトグラフィー(41x450mm、5%酢酸エチル/ヘキサン)に供し、および次いで目的の産物を含む画分を回収しおよび合わせた。溶媒を減圧して蒸発し、144mg(10%)の19を無色の油として与えた。1H NMR(400 MHz,CDCl3):δ4.46(pt,2H)、4.17(t,J=6.4Hz,2H)、2.51(dd,J=7.6,14.6Hz,2H)、1.74(m,2H)、1.58(m,2H)、1.34(t,IH)、1.21−1.30(broad m,14H)。
実施例XXIV
パターン化された試料提示器具(X3、C15−CO2Hの実施例)の調製
24個の表面修飾基材を実施例XIIIに記載の通りに調製し、特別製の配列治具に入れ、および液体保持ゾーンとサイズおよび形状が対応する性質を有する、ピンレジスターエッチングしたステンレス鋼シャドーマスク(0.002インチ)で覆った。治具を120W/cm2定格の低圧水銀光源を付けた空冷紫外硬化システムの動くベルトに付け、および1時間の期間にわたって45から75回、光源の下を通した。UV曝露後、基材を治具から取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。曝露された基材を、5%の16−メルカプトヘキサデカン酸および95%の19(0.1mMの全チオール濃度)を含有する混合エタノール溶液中に入れ、室温に冷却し、および室温にて1ないし24時間の範囲の期間インキュベートした。パターン化された表面修飾基材を集合バスから取り出し、2400rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。
パターン化された表面修飾基材を特別製の配列治具に入れ、および分析ゾーンとサイズおよび形状が対応する性質を有する、第二のピンレジスターエッチングしたステンレス鋼シャドーマスクで覆った。治具を紫外硬化システムの動くベルトに付け、および1時間の期間にわたって45から75回、光源の下を通した。UV曝露後、基材を治具から取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。曝露された基材を、0.1mMの9のエタノール溶液に入れ、および室温にて1〜24時間インキュベートした。最後に、二回パターン化された表面修飾基材を集合バスから取り出し、1000rpmにてエタノールでスピン洗浄し、および窒素気流下で乾燥した。
実施例XXV
NHSチップの調製および続いてNTA(ニトリロトリ酢酸)リガンドへの付加
実施例XXIVに記載の通りの酸性基を有するX3表面を、アンモニア10%溶液で5分間洗浄しおよび次いで水ですすいだ。表面を次いで窒素気流で乾燥した。各ウェルへ、0.1%(v/v)オクチル−β−グルコシド(OBG、ピアース社(Pierce)28310)を含む25mMリン酸ナトリウム(シグマ社(Sigma)S9763)pH8を20μL加え、および10分間静置してインキュベートした。表面を次いで、10μLの0.1%OBG(v/v)でピペットを用いて2回洗浄する。酸性基を次いで、50mM NHS(ピアース社(Pierce)24500)および200mMEDC(ピアース社(Pierce)22981)を含む0.1%OBG溶液10μLを加えおよび20分間静置してインキュベートすることによってNHSと反応させる。表面を次いで、10μLの0.1%OBG(v/v)でピペットを用いて2回洗浄する。次の段階は、表面上に形成されたNHSエステルを、キレート化リガンドと反応させることを含む。20mMAB−NTA(同仁化学(Dojindo)A296)を含む0.1%OBG含有25mMリン酸ナトリウム緩衝液pH8の10μLを表面に加え、および30分間静置してインキュベートする。表面を次いで、10μLの0.1%OBG(v/v)でピペットを用いて2回洗浄する。
実施例XXVI
NTA表面へのFe(III)負荷およびその後の試料添加
次の段階は、金属キレート化が起こる緩衝液中へ導入することである。表面はしたがって100mMAcOH(酢酸)を含む0.1%OBG10μLで2回洗浄される。金属は次いで1mM FeCl3(シグマ社(Sigma)F−1513)の0.1%OBG含有1mM AcOH(pH3以下)溶液10μLを加えおよび10分間静置してインキュベートすることによって負荷される。経時によって酸化する傾向があるため、FeCl3溶液は新しく作製することが重要である。10分間の金属負荷後、表面を100mM AcOHを含む0.1%OBG10μLで2回、および次いで1M尿素(ストラタジーン社(Stratagene)300191)を含む100mM AcOH含有0.1%OBG10μLで1回洗浄する。試料を次いで同じ溶液中で加え、および20分間静置してインキュベートする。表面を続いて試料緩衝液10μLで1回、および次いで100mMAcOH10μLで2回洗浄する。表面を次いで風乾する。試料を次いでX3表面から前溶出し、および1:1ACN(アセトニトリル):0.1%リン酸溶液2μLを各ウェルへ加えることによって中心へ乾燥させる。これはホスホペプチドをFe(III)−NTA表面から溶液中へ放出させ、溶液を次いで中心へ濃縮させる。一旦ウェルが乾燥したら、マトリクス2μLを各ウェルに加える。マトリクス処方は0.5mg/mLDHB含有90:10 ACN:クエン酸アンモニウム(5mM)である。本処方は、ウェル全体にわたり結晶の均一なパッドを生じる。
ゲル内トリプシン消化物からホスホペプチドを取り出すためにFe(III)負荷試料提示器具を利用する使用例を下に記載する。ウシ乳由来β−カゼイン(シグマ社(Sigma)品番C6905、スイスプロットP02666)を18MΩ水に溶解してストック溶液とした。このストックを次いで、1−Dゲル電気泳動用のタンパク質を調製するのに用いた。このように、Laemmli緩衝液(バイオラッド社(Bio−rad)品番161−0737)を取扱説明書に従って調製し、およびタンパク質ストックを使用前に希釈するのに用いた。ゲル電気泳動はトリスHCl緩衝液中プレキャスト4〜15%SDSPAGEゲル(バイオラッド社(Bio−rad)製品番号161−1176)を用いて110V定電圧で実施した。泳動の完了時に、ゲルを水でよく洗浄してSDSの大部分を除去した。ゲルを次いで10%MeOH、7%AcOH溶液に20分間入れて固定した。ゲルを次いでサイプロ・ルビー(Sypro Ruby)(バイオラッド社170−3125番)を用いて一夜染色し、および後で10%MeOH、7%AcOHを用いて脱色した。バンドを暗室内でトランスイルミネーターを用いて目視し、および各切片を除去後にエタノールで清拭した剃刀を用いてゲルから切り出した。ゲル内トリプシン消化は公知の手順(Rapid Comm.in Mass Spec.2001,75,1416−1421)にしたがって実施したが、しかし、ゲル切片はTFA混合物で最後に抽出せず、およびスピードバック(Speedvac)エバポレーターをゲルまたはゲル抽出物を乾燥するのに使用しなかった。このように、ゲル内消化(20μL/切片)からの上清を、さらに精製または濃縮無しで使用した。消化試料ストックの終濃度は約25fmol/μLであり、およびさらに希釈無しで使用した。
Fe(III)−NTA表面は、1M尿素を含む100mM AcOH含有0.1%OBG10μLを用いたインキュベートまでは、前の手順に記載の通りに調製した。ここで、ゲル内消化物上清5μLを各ウェルに加え、ウェル当たり総容量15μLとなった。これを表面上で20分間インキュベートし、および手順の残りは前記の通りである。ゲル混入物が表面に結合していた場合に予想されるような、溶液の集中の問題は無かった。
MALDI−TOF分析は、陽イオンモードで、アキシマ(Axima)CFR(シマヅ・バイオテク社(Shimadzu Biotech)によるクレイトス・アナリティカル社(Kratos Analytical)、英国マンチェスター)で、パルスN2レーザー(337nm)、遅延引き出し、および加速電圧20kVを用いて実施した。装置はリフレクトロンモードで半自動化手順を用いて操作し、全般的に、25〜50ラスター点/部位、20〜50ショット/ラスター点を生じた。データは全ラスター点の平均として回収および保存した。
図22に示す通り、主要ピーク(880m/zのマトリクスクラスター以外)は、β−カゼインの消化から予想される2種類のホスホペプチド(2064m/zおよび3124m/z)である。トリプシン自己消化ピークが存在しないのが判る。
別の使用例では、Fe(III)負荷X3 IMAC表面が、バックグラウンドトリプシン消化物からホスホペプチドを取り出すのに用いられる。100fmolのホスホリラーゼb消化物(ウォーターズ社(Waters Corp.)品番186002326、スイスプロットP00489)および5fmolのβ−カゼイン消化物の混合物を、X3 IMAC表面へ、前記の通りの変更しない手順を用いて加えた。ホスホリラーゼbはリン酸化アミノ酸を含まず、およびここでは試料混入物として作用する。図23に見られる通り、混合タンパク質消化物試料溶液をT3表面上に置いた場合、バックグラウンドノイズは十分高かったため、スペクトル中でホスホペプチドのピークを特定するのは困難である。T3表面は、ホスホペプチドを捕捉および望ましくない種からホスホペプチドを単離する結合表面を有しない。しかし、混合タンパク質消化物試料溶液がX3 IMAC表面上で処理された際、シグナル対ノイズ比は有意に改善した。図24に示す通り、X3 IMAC表面はホスホペプチド(2064m/zおよび3124m/z)の強い結合を示し、それらはT3上に捕捉されたスペクトルには見られない(図23)。
Fe(III)負荷された試料提示器具を、低レベルのホスホチロシンを含む化合物を検出する器具能力を検証するため、次いでさまざまな濃度のリン酸化チロシンペプチドに対して試験した。さまざまな量のリン酸化チロシンペプチド、pp60C−SRCカルボキシ末端リン酸調節ペプチド(バケム社(Bachem)、H−3258)を、Fe(III)負荷されたX3 IMACへ、前に記載された手順に従って負荷した。図25に示す通り、アキシマ(Axima)CFRを用いて良好な感度が達成された。
実施例XXVII
NTA表面へのNi(II)負荷およびその後の試料添加
この例では、金属キレート化は0.1% OBG中で起こった。金属は、0.1%OBG含有10 mM NiSO4・6H2O(シグマ社(Sigma)227676)溶液10μLを加えおよび10分間静置してインキュベートすることによって負荷される。10分間の金属負荷後、表面を0.1%OBG10μLで1回、および次いで、0.1%OBG含有10mM HEPES(4−(2−ヒドロキシエチル)−1−ピペラジンエタンスルホン酸;シグマ社(Sigma)H−4034)pH7.4、150 mM NaCl(カルビオケム社(Calbiochem)567441)10μLで2回洗浄した。試料を次いで同じ溶液中で5μL加え、および20分間静置してインキュベートした。表面を続いて試料緩衝液10μLで3回、および次いで水10μLで2回洗浄した。表面を次いで風乾した。試料を次いでNi(II)−NTA表面から前溶出し、および1:1ACN:0.1%リン酸溶液2μLを各ウェルへ加えることによって中心へ乾燥させる。これらの酸性条件は、Hisタグ化タンパク質をIMAC表面から溶液中へ放出させ、溶液を次いで中心へ濃縮させる。一旦ウェルが乾燥したら、マトリクス2μLを各ウェルに加える。マトリクス処方は0.5mg/mLDHB含有90:10 ACN:5mM クエン酸アンモニウムである。本処方は、ウェル全体にわたり結晶の均一なパッドを生じる。
ウシ赤血球由来ユビキチン(シグマ社(Sigma)U−6253)およびユビキチン、Hisタグ組み換え(カルビオケム社(Calbiochem)662060)を18MΩ水に溶解し、および20fmol/μLへ上記のHEPES緩衝液で希釈した。上記の手順の下で、100fmolのユビキチンおよびHisタグ組み換え変異体をチップに負荷した。ユビキチン(m/z−8500)の結合は無く、およびHisタグ組み換えユビキチン(m/z−9500、図26)について強いシグナルが見えた。
追加的な提示器具構成の実施例
上記の通り、本明細書に記載の発明は、液体を表面の周囲に移動させるさまざまなパターン、形状または構成に適用してもよい。加えて、一つ以上の表面を分析物および/または望まれない種を捕捉するよう構成してもよい。
先に記載された一変形は、中心領域への液体の移動を円滑にし、および結果として分析物を運搬する液体を濃縮する。一設計において図1aに示すように、試料提示器具は境界ゾーンが結合した二個の同心円を含む。
試料提示器具は、分析または処理のために中心領域へと液体を移動する三個またはそれ以上の同心円から構成されてもよい。たとえば図27aに図示するように、試料提示器具は、三個の同心円を含んでもよい。各領域は湿潤性値を有し、および、隣接する領域の湿潤性は異なる。同心リングは、中心円102の表面の接触角(CA1)が内側の同心リング104の表面の接触角(CA2)より小さく、CA1は外側の同心リング106の接触角(CA3)より小さく、およびCA3は境界ゾーン108の接触角(CA4)より小さい(すなわちCAl<CA2<CA3<CA4)。
加えて、表面領域102、104、106の一つ以上は、結合領域として役立つために修飾してもよい。さまざまな結合領域は、目的の分析物、望まれない種またはそれらの組み合わせを捕捉するために構成されてもよい。たとえば、第一の領域は分析物Aを捕捉するよう構成されてもよく、第二の領域は分析物Bを捕捉するよう構成されてもよく、一方、第三の領域は分析ゾーンとして構成されてもよい。別の例では、第一の領域は望まれない種Cを捕捉するために構成され、第二の領域は望まれない種Dを捕捉するために構成され、一方、第三の領域は分析ゾーンとして構成される。さらに別の例では、第一の領域は分析物を捕捉するよう構成され、一方、第二の領域は望まれない種を捕捉するよう構成され、一方、第三の領域は分析ゾーンとして構成される。特定の用途のために、実質的に非結合性の表面を有する分析ゾーンを構成することが望ましいこともありうる。しかし、他の用途で、分析ゾーンは、結合表面で構成してもよい。
一実施例の用途において、第一の領域は第一の抗原を捕捉する第一の抗体表面で構成され、その一方で、第二の領域は第二の抗原を捕捉する第二の抗体表面で構成される。第一および第二の抗原の両方を含む試料液体は、試料提示器具上に導かれる。抗原の抗体表面との結合を可能にするインキュベーション期間の後、試料提示器具を洗浄していかなる残留する試料液体も除去する。次いで第一の抗原は、第一の抗体表面から放出され、および分析ゾーン上に濃縮することができる。次いでさらなる処理および/または測定を、第一の抗原に実施することができる。第一の抗原が分析された後、オペレータは第一の抗原を洗い落とし、および第二の抗原を処理し続けることができる。第二の抗原は、第二の抗体表面から放出され、および分析ゾーン上に濃縮することができる。次いで化学処理および/または測定を第二の抗原に実施することができる。
本明細書中において開示された試料提示器具は、上で述べた同心の表面領域に限定されない。本発明のさまざまな機能を説明するための例として、同心の設計が提供されている。試料提示器具がさまざまな非円形パターン/形状で構成できることも意図されている。
一変形は、図21bに示され、「滴下ゾーン」112は、図1aに示されるものと同様の同心円設計114に加えられている。この構成において、滴下ゾーン112は、試料提示器具116に送られる液体を受容する目的のために提供されている。好ましくは、滴下ゾーン112は、境界線域118の接触角より小さくおよび液体保持ゾーン120の接触角より大きい接触角を有する。滴下ゾーン112に送られる液滴は、液体保持ゾーン120の方に向かって進むことができ、結局分析ゾーン122に濃縮する。液体保持ゾーンは、捕捉ゾーンとして役立つために修飾されてもよい。別の変形では、滴下ゾーンは、複数の液体保持ゾーンおよびそれらに対応する分析ゾーンに試料液体を供給するように構成される。
別の変形では、試料提示器具132は液体の複数の液滴を異なる位置で受けた二つ以上の滴下ゾーン134、136、138、140により構成され、次いで、試料提示器具132の表面上へ放出された後分析ゾーンへと流れるよう導かれる。4つの滴下ゾーン構成を示す例が図27cに示される。試料提示器具上に送られたさまざまな液滴は、同一の化学組成または異なる組成を有してもよい。さらに、試料提示器具上の一つ以上のゾーンは、結合表面で構成してもよい。たとえば、液体保持ゾーン141は、目的の分析物を捕捉するよう修飾してもよい。
図27cに示される器具は、複数の液体を単一の領域に導入するために特に有用でありうる。たとえば、器具は、反応物質または触媒を滴下ゾーンに次々と導入することによって、一連の化学反応を実施するために用いてもよい。高処理量の用途において、各反応物質は、それぞれの分析ゾーンに専用の滴下ゾーンの上に反応物質を送ることによって、同じピペットで導入してもよい。たとえば、試料提示チップは96個の分析ゾーンを有してもよく、各分析ゾーンは液体保持ゾーンに囲まれており、および各液体保持ゾーンは各分析ゾーンに特異的な4個の専用の滴下ゾーンに接続してもよい。96個の異なる鉛化合物を、それ自身の分析ゾーンの96個の鉛化合物それぞれを試料提示器具上の自己の分析ゾーンに配置することによって、このチップ上で同時に試験を行うことができる。4個の異なる反応物質を、一度に一個または二個導入してもよい。4つの反応物質のそれぞれが、各分析領域ごとに専用の滴下ゾーンを介して96個の分析ゾーンに導入してもよいため、送出ピペットによる交差汚染を回避できる。さらに、ひとたび反応が完了されると、最終産物の分析は分析中に直接行うことができる(たとえば、質量分析、など)。
さらに別の変形では、図27cに示す試料提示器具は、試料提示器具の一領域から他のへと液体を輸送する接触角勾配または移行ステップを有する液体輸送領域より構成される。たとえば、表面は、対応する接触角CA21、CA22、CA23、CA24、CA25およびCA26を備える6つの領域(すなわち領域1から6)142、144、146、148、150、152を含んでもよい。領域は、CA21<CA22<CA23<CA24<CA25<CA26となるよう構成してもよい。好ましくは、接触領域のそれぞれは、SAMで構成される。
別の実施例では、図27eの試料提示器具は、滴下ゾーン162、液体輸送領域163、液体保持ゾーン164、および分析ゾーン166から構成される。この特定の例において、液体輸送領域は、湿潤性が異なる3つの領域170、172、174のみを含むが、当業者は、液体輸送領域が4つまたはそれ以上の湿潤性の異なる領域を含んでもよいことを理解する。たとえば液体輸送領域は、液体輸送領域の表面に対する液体接触角の連続的な変化があるよう、一端から他端までの連続的な表面張力勾配で構成されてもよい。これらの連続勾配または多段階で変化する勾配は、さまざまな目的のために、平坦な表面上で液体試薬を移動するのに用いてもよい。たとえば、化学反応が起こりうるよう二つ以上の試薬をチップ上の2つの異なる位置から単一の位置へとしてもよい。別の変形では、さまざまな化学物質または流体を表面張力勾配を用いて分離またはろ過してもよい。たとえば、一つ以上の液体輸送領域は、目的の分析物および/または望まれない種を捕捉するための結合表面で構成してもよい。一変形では、液体輸送領域は、異なる抗原を捕捉するための抗体表面のさまざまな断面で構成される。次いで試料提示器具は、滴下ゾーン162の上に付けた試料液体から望まれない抗原をろ過するのに利用してもよい。別の変形では液体輸送領域163は、一つ以上のクロマトグラフィー表面/ゾーン(たとえばイオン交換面、逆相面、など)で適応されている。
一変形では、試料提示器具は、それぞれが特定の目的(たとえば、試料の負荷、試料の精製/捕捉、液体保持、次いで分析ゾーンへの濃縮およびその後の分析、など)のあるサイズの異なる複数の複数並列を含む。一つの例は図28aに示すように、8×12列の処理部位322、324、326、328、330、332を含む(96個の処理部位のうち一部のみを図28aに示す)。図28bは、図28aの試料提示器具300からの個別の処理部位322を示す。試料負荷ゾーン302は、試料の処理のための機能的な化学的性質を含んでもまたは含まなくてもよい。一つのゾーンから別のゾーンへの液体試料の移動の機序はさまざまでありえる。試料負荷ゾーン302に負荷される試料は、(たとえば、ピペッティングなどによって)機械的に移動しておよび次のゾーンに入れてもよい。上記の試料提示器具において説明されたさまざまなゾーン302、304、306、308は、接続ゾーン342、344、346によって接続されてもよく、およびその湿潤性は一個のゾーンから他のゾーンへの液流を可能にしてもよい。一変形では、異なるゾーン302、304、306、308、310、342、344、346はそれぞれ、一個のゾーンから他のゾーンへの液流を促進するために、異なる表面張力で構成される。たとえば各処理部位332は、負荷ゾーン302から分析ゾーン310への液流を促進するために、表面張力勾配で構成してもよい。別の変形では、接続ゾーン342、344、346のそれぞれの湿潤性が、化学的または物理的な刺激(たとえば、紫外線)に反応して変化してもよく、その結果、試料負荷ゾーンに付けられた試料が次のゾーン304(たとえば、イオン交換ゾーン)へと、二つのゾーン間のゾーン342の紫外線への曝露の結果湿潤性およびその後の液流が変更する場合に、移動する。次いで類似の工程を用いて、イオン交換ゾーン304からの試料を逆相ゾーン306に、および究極的には液体保持ゾーン308に輸送してもよい。この時点で処理される試料は、分析ゾーン310に濃縮することができるであろう。代替的には試料は、溶媒の添加によってゾーンからゾーンまで移動してもよいが、結果として次のゾーンで「オーバフロー」が生じるであろう。この工程は、精製された試料が液体保持ゾーン308に存在するまで繰り返してもよい。この場合も、(異なる湿潤性および/または分析物結合特性を有する)非常に多数の表面およびその構成があるため、(一つ以上の分析物に対して)広大な範囲の精製、濃縮、隔離および修飾能力を有する試料提示器具を作製できる。
イオン交換は、タンパク質、ポリペプチド、核酸、ポリヌクレオチドおよび他の帯電生体分子の分離および精製のために最も頻繁に用いられるクロマトグラフィー技術の一つである(『適切な時間の適切なステップ』(The right step at the right time)Bio/Technology,4,954−958(1986),ボネジェラ(Bonnerjera),J.,オウ(Oh),S.,ホアル(Hoare),M.,ダンヒル(Dunhill),P.)。したがって、さまざまな化学分析および/または合成用途のために、試料提示器具上の機能ゾーンにイオン交換能力を提供することが有利かもしれない。イオン交換工程は、分析ゾーン内での試料液体の分析前に発生する唯一の活性化された化学工程として、試料提示器具上で実施してもよい。別の変形では、イオン交換は、試料提示器具上で発生する一連の二つ以上の化学処理段階内の一つの処理段階として実施してもよい。イオン交換能力は、一つ以上の捕捉ゾーンを有する試料提示器具上でも実施することができる。
イオン交換クロマトグラフィーの分離は、電荷が逆の固定されたイオン交換基への帯電溶質分子の可逆吸着に依存する。これらのイオン交換基は陽イオンまたは陰イオンでもよく、および、「弱い」または「強い」としばしば分類される。したがって、試料提示器具上のイオン交換ゾーンは、強い陽イオン官能基(たとえば、スルホネート基)、弱い陽イオン基(たとえば、カルボン酸塩基)、強い陰イオン基(たとえば、第4級アミン)または弱い陰イオン基(たとえば、第3級アミン)を含むよう構成してもよい。表面の官能基は、これらの官能基を含むさまざまなSAMの集合を介して制御してもよい。表面の湿潤性は、たとえば、集合工程で実施される1°、2°、3°または4°の使用によって制御してもよい。
上記の例に示すように、逆相クロマトグラフィーは、試料提示器具上の機能ゾーン内で実施しうる別の化学的な工程である。タンパク質、ペプチドおよび核酸といったある程度の疎水性を有する分子は、優れた回収性および分解能を備えた逆相クロマトグラフィーによって分離してもよい。加えて、移動相中のイオン対修飾子の使用によって、完全に脱保護されたオリゴヌクレオチドおよび親水性ペプチドといった帯電溶質の逆相クロマトグラフィーを可能にしうる。一変形では、逆相ゾーンはn−アルキル炭化水素または芳香基を含み、これによって疎水性相互反応を介して相互に反応できる。表面官能基は、これら官能基を含むさまざまなSAMの集合を介して制御してもよい。表面の湿潤性は、たとえば集合工程で実施される1°、2°、3°または4°の使用によって制御してもよい。この開示を利用する当業者は、分析ゾーン中の試料液体の分析前に発生する唯一の活性化された化学工程として、または、試料提示器具に発生する一連の工程の一つとして、逆相を試料提示器具上で実施してもよいことを理解する。逆相能力は、一つ以上の捕捉ゾーンを有する試料提示器具上でも実施してもよい。
イオン交換ゾーンおよび逆相ゾーンは、試料提示器具上で実施できる潜在的な官能的な領域/ゾーンの例として、本明細書中において用いられる。この開示を利用する技術の当業者は、機能ゾーン内のSAM表面上の表面化学を修飾することによって、さまざまな他の化学工程を官能基領域中に実施できることを理解する。
加えて、これら試料提示器具は、SBS(Society for Biomolecular Screening)の形式にしたがって調製してもよい。したがって、たとえば、部位は8×12配列で9mmの間隔で配置し、使用のために96個の部位を与えてもよい。図28aに示す図において、間隔を提供するために各部位は分析ゾーンの直角位置に対して45°の角度で作製される。384ヶ所または1536ヶ所の配列と互換性を持つバージョンも、同様に作成できるであろう。この開示を利用する技術の当業者は、試料提示器具が試料処理部位のさまざまな配列構造で構成してもよいことを理解する。
一つ以上の機能ゾーン(たとえば、イオン交換ゾーン、逆相ゾーン、捕捉ゾーン、など)を有する試料提示器具は、さまざまな生物学的、生化学的および/または、化学的試料を処理するのに用いられる。たとえば、その後のタンパク質/ペプチド分析に干渉しうるさまざまな種を含む生物学的粗試料(たとえば血清、プラズマ、など)を、試料提示器具で処理してもよい。特に、試料の「浄化」は、最近粗試料に由来する不必要な、干渉する材料を除去することを目的とした最近の研究の主要領域となった。現在の方法論の多くは、それぞれがクロマトグラフィーを制御する計測器および粗試料を処理するカラムを必要とする一連の表面外クロマトグラフィー段階を伴う。粗試料を加工する一つ以上の機能ゾーンを有する試料提示器具によって、オペレータが表面上でクロマトグラフィー処理を実施することができ、および追加的な計測具およびツールの必要性を回避する。
追加的な提示器具の実施
別の変形では、提示装置は、捕捉ゾーンおよび分析ゾーンを有する表面を含む。捕捉ゾーンおよび分析ゾーンを囲む随意的な境界ゾーンも設けてもよい。捕捉ゾーンは抗原を捕捉するよう活性化されることができるよう構成されている。たとえば、捕捉ゾーンは、化学物質または生化学物質(たとえばヌクレオチド、ペプチド、タンパク質、など)を表面上へ共有結合することによって活性化してもよい。次いで活性化された表面は、試料溶液(たとえば生物流体、など)中の分析物との非共有結合性相互反応によって、分析物を捕捉するために利用してもよい。ひとたび目的の分析物が捕捉ゾーンに結合すると、試料流体中の残りの種を提示装置の表面から除去してもよい(たとえば、試料提示器具の表面の洗浄)。
ひとたび残りの種が除去されると、目的の分析物は捕捉ゾーンから放出されてもよく、および次いで測定のための分析ゾーンへと移動してもよい。一つの方法において、このように、分析物を活性化された表面に結合している非共有結合は、化学的(たとえば化学薬品の導入、など)または物理的(たとえば紫外線照射、など)方法によって、崩壊し、および活性化された表面から分析物の放出を強制する。次いで放出された分析物は、分析ゾーンへ移動するように導かれてもよい。たとえば、放出された分析物は、捕捉ゾーンおよび分析ゾーンとの間で異なる表面張力に起因して、分析ゾーンへと移動してもよい。一設計変形では、分析物が分析ゾーン上へと濃縮するよう、捕捉ゾーンは分析ゾーンより大きい表面積を有する。ひとたび分析物が分析ゾーンに存在すると、次いでさまざまな化学分析技術は分析物を検出/測定するよう実施してもよい。一変形では、分析ゾーンは、実質的に非結合性の表面を含む。別の変形では、分析ゾーンは、分析のための分析物を捕捉するための結合表面を含む。別の設計変形では、捕捉ゾーンからの分析物の放出の前に分析物が捕捉ゾーンにおいて捕捉された後、分析ゾーンの結合特性を活性化してもよい。
別の変形では、分析物は、捕捉ゾーンを含む基内で共有結合を切断することによって、捕捉ゾーンから放出される。次いで表面官能基の切断された端部に付いた放出された分析物は、分析またはさらなる処理のために分析ゾーンに輸送してもよい。
この開示を利用する技術の当業者は、捕捉ゾーンの活性化および捕捉ゾーン内の捕捉は、上記に述べられる共有結合および非共有結合に限定されないことを理解する。試料提示器具の変形は、単独でまたは共有/非共有結合と組み合わせて、イオンおよび他の化学結合特性を利用して、捕捉ゾーン内の捕捉ゾーンおよび捕捉光源を活性化するために実施されうる。
別の用途では、本試料提示器具は、カスタマイズ可能な器具として第三者に送られおよび/または販売される。カスタマイズ可能な器具は、第三者が分析のための特異的な分析物を捕捉するために捕捉ゾーンを選択的に修飾できるよう、修飾可能な捕捉ゾーンで構成される。一変形では、試料提示器具上の捕捉ゾーンは、抗体と共有結合で結合できる表面で適合している。たとえば、捕捉ゾーンは、NHSエステル基を含むSAM面で適合してもよい。第三者は、試料提示器具を修飾するエンド・ユーザーでもよく、および、次いでその後、目的の特定の分析物を分析および/または処理するために、カスタマイズされた試料提示器具を利用してもよい。別の用途では、第三者は、特定の種類の分析物を捕捉するために試料提示器具をカスタマイズし、および次いで、カスタマイズされた試料提示器具をエンド・ユーザーでもありうる他の関係者に提供および/または販売してもよい。別の例では、捕捉ゾーンは、NTAリガンドを含むSAM面で適合される。次いで第三者は、既製のNTA試料提示器具を利用して、異なる生化学物質を捕捉するために異なる金属イオンを有する試料提示器具を生産してもよい。
さらに別の変形では、カスタマイズ可能な試料提示器具が、他の化学物質/溶液とともにキットとして使用者に提供され、これによって使用者は目的の抗原を捕捉するための特定の化学物質/生化学物質で、捕捉ゾーンを活性化することができる。一変形ではキットは、抗体を固定するために活性化することができる捕捉ゾーンおよび抗体を活性化および固定するために利用できる化学溶液を有する試料提示器具を含む。たとえばキットは、(1)チップ;(2)試薬;(3)緩衝液;(4)キャリブラントおよび(5)ツールを含んでもよい。別の変形では、キットは、リンペプチドを捕捉するために活性化できる捕捉ゾーンを有する試料提示器具を含む。たとえばキットは、(1)チップ;(2)試薬;(3)緩衝液;(4)キャリブラント;および(5)ツールを含んでもよい。適当な化学物質/生化学物質(たとえばヌクレオチド、ペプチド、タンパク質、モノクローナル抗体、鉄イオン、など)を捕捉ゾーン上に共役結合、負荷および/または固定することによって活性化させる方法についての指示も、キット内に提供してもよい。別の変形では、捕捉ゾーンに共役結合、負荷、固定および/または他の方法で取り付けられる活性化剤の一つ以上をキットの範囲内に設けてもよい。たとえば、キットは3種類のモノクローナル抗体を備えてもよく、このため、使用者は対応する抗原のうちの一つを捕捉するためにチップをカスタマイズすることができる。
さまざまな検出/測定機構を利用する使用例
上述のとおり、試料提示器具は、さまざまな検出および測定装置で、さまざまな化学、生化学および/または、生物学的試料の検出および測定のために実施することができる。試料提示器具を用いて、さらなる処理のために、および/または追加的な化学反応を起こすために、化学、生化学および/または生物学的粒子をろ過および/または濃縮してもよい。
一変形では試料提示器具402は、反映された光子の検出に基づく測定(たとえば、光学分光学、蛍光検出、など)に基づくシステムとともに利用される。図29に示すようにシステムは、光エミッタ404(たとえば、紫外線、可視光または赤外線光源、など)および光検出器408(たとえば光学センサ、など)で構成してもよい。
別の変形では、提示装置は、試料提示器具402上の分析物をイオン化し、およびイオン化された粒子を検出器416へと導くシステムとともに利用される。たとえばシステムは、図30に示す質量分析計でもよい。ミラー412によって導かれるレーザー410は、試料提示器具402の表面上の分析物を励起するために利用してもよく、および、イオン化された粒子は加速電極414を介して検出器416に向かって加速される。
さらに別の変形では試料提示器具は、光子が試料提示器具自体を通過できるよう構成してもよい。たとえば試料提示装置402の基材は、上部に金の薄層をスパッタリングしたガラス系の層、および金の上に付着したSAM層を含む。金の薄層は、光子の伝送を可能にする。一つの特定の用途において、試料提示器具402は、提示装置402の分析ゾーン420を介して光を透過する光学エミッタ418(たとえば赤外線光源、など)で利用される。図31に示すように、光学式検出器422(たとえば赤外線光線検出器、など)は、提示装置402を通過する光の量および分析ゾーン420における分析物位置(たとえば、赤外線吸収スペクトルの測定)を測定するために、提示装置402の反対側に置かれる。この開示を利用する技術の当業者は、他の検出および/または測定装置も、本明細書中に記載の試料提示器具で実施できることを理解する。
ここまで本発明を記載し、および本発明の具体的な例を描写してきた。本発明は特定の変形および具体的な図において記載してきた一方、当業者は本発明が記載された変形または図に限定されないことを認識する。特に、分析ゾーン、液体保持ゾーンおよび境界ゾーンの物理的配列は、上記の例に限定されない。加えて、上述した方法および段階が所定の順序で発生している所定のイベントを示す場合、当業者は所定の段階の順序は修飾してもよく、および、こういった修飾が本発明の変形に従うと認識している。加えて、所定の段階は、可能な場合並行した工程と同時に実施してもよく、および上記の通り順次実施してもよい。したがって、請求項にみとめられる本発明の開示または等価物の精神の範囲内にある発明の変形の範囲内で本発明の変形が存在するかぎり、本特許がそれら変形も同様に包含することが意図されている。最後に、本明細書中において引用されたすべての刊行物および特許出願はすべて、あたかも個々の刊行物または特許出願が特別におよび個別に示されたかのように、参照によって全文に組み込まれる。