JP4776166B2 - 細胞障害タンパク質及びその利用 - Google Patents
細胞障害タンパク質及びその利用 Download PDFInfo
- Publication number
- JP4776166B2 JP4776166B2 JP2003549386A JP2003549386A JP4776166B2 JP 4776166 B2 JP4776166 B2 JP 4776166B2 JP 2003549386 A JP2003549386 A JP 2003549386A JP 2003549386 A JP2003549386 A JP 2003549386A JP 4776166 B2 JP4776166 B2 JP 4776166B2
- Authority
- JP
- Japan
- Prior art keywords
- protein
- cells
- antibody
- present
- cytotoxic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/205—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Campylobacter (G)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/164—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/12—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from bacteria
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/12—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from bacteria
- C07K16/1203—Gram-negative bacteria
- C07K16/121—Helicobacter (G); Campylobacter (G)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P21/00—Preparation of peptides or proteins
- C12P21/02—Preparation of peptides or proteins having a known sequence of two or more amino acids, e.g. glutathione
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/195—Assays involving biological materials from specific organisms or of a specific nature from bacteria
- G01N2333/205—Assays involving biological materials from specific organisms or of a specific nature from bacteria from Campylobacter (G)
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S435/00—Chemistry: molecular biology and microbiology
- Y10S435/81—Packaged device or kit
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Immunology (AREA)
- Biophysics (AREA)
- Gastroenterology & Hepatology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Epidemiology (AREA)
- Diabetes (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- Communicable Diseases (AREA)
- Emergency Medicine (AREA)
- Endocrinology (AREA)
- Oncology (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
本発明は、ヘリコバクターピロリの産生する新規な細胞障害タンパク質であるM毒素(mucous layer devastating toxin)及びその利用に関する。
背景技術
多くの胃炎、胃潰瘍あるいは胃癌はヘリコバクターピロリによると考えられてきているが、今日まで、それらの疾患の端緒である胃上皮細胞の破壊と不可逆的な細胞死を惹起する、明らかな直接細胞障害因子は特定されてこなかった。胃内のpH環境や免疫反応を変化させる因子や、ヘリコバクターピロリの胃上皮細胞への接着因子、あるいは菌自体の運動性などが疾患成立要件として指摘されてきたが、胃炎、胃潰瘍、胃癌のすべての出発点といえる胃粘膜破壊が、いかなる過程を経るのか、またその直接的な責任因子は何かということは現在まで不明だった。唯一、細胞障害性をもつ空胞化毒素が単離されていたが、これは細胞障害活性が弱く、可逆的な細胞障害活性にとどまり、致死的細胞障害因子としては、in vivoでもin vitroでも病原因子としては認められてこなかった。
ヘリコバクターピロリは、上述のごとく、生体の胃内環境において、胃粘膜細胞に対する直接障害因子を分泌していることは、多くの研究者により推定され、その疾患の重要性をも鑑み、遺伝子の全配列が1996年には確定されたが、血清を使用してもなお困難な培養条件と、分離精製条件および評価系の未確立が、推定毒素の単離同定を阻んできた。
発明が解決しようとする課題
そこで、ヘリコバクターピロリ感染にともなう胃炎、胃潰瘍、胃癌等の原因となる責任タンパク質を見いだし、その毒素タンパク質を大量調製する方法を確立し、もって新規な毒素であるM毒素の同定、診断およびスクリーニング法を確立することが、1つの課題となった。またそれらを用いて、胃粘膜細胞障害の責任毒素の作用を抑制し、胃炎、胃潰瘍、胃癌等の予防・治療剤の開発の道を開き、あわせてその毒素の応用方法にまで緒をつけることが望まれた。
発明の開示
本発明者は、上記の課題を解決するために鋭意研究を重ねた結果、ヘリコバクターピロリを従来と異なる、より胃内環境に近い状態である無血清培養条件下で生育した場合に、不可逆的細胞死をもたらす新規な毒素を同定した。これは、上述の空胞化毒素の単位当たり1000倍から100000倍の毒力を有し、胃上皮細胞のみならず免疫系細胞を含む広範な温血細胞に対して、不可逆的な細胞死を惹起することを見いだした。本発明者は、これらの知見に基づいて、さらに検討を重ねた結果、本発明を完成するに至った。
すなわち、本発明は、(1)配列番号1で表されるアミノ酸配列に対する同一性を少なくとも70%以上有するタンパク質からなることを特徴とする細胞障害タンパク質、(2)配列番号1で表されるアミノ酸配列と等しい細胞障害活性を有することを特徴とする(1)記載のタンパク質の部分ペプチド、(3)ヘリコバクターピロリで産生される(1)1または(2)記載の細胞障害タンパク質、(4)(1)または(2)記載の細胞障害タンパク質をコードする配列番号2のDNAを含有する組換えベクターで形質転換された形質転換体を培養することを特徴とする(1)または(2)記載の細胞障害タンパク質、(5)形質転換体が独立行政法人産業技術総合研究所(IPOD)に寄託番号FERM BP−8218で寄託されている(4)記載の細胞障害タンパク質、(6)(1)1または(2)記載の細胞障害タンパク質を用いる抗腫瘍剤、(7)(1)または(2)記載の細胞障害タンパク質を哺乳類に免疫して得られる細胞障害タンパク質に特異的なモノクローナル抗体、(8)寄託番号FERM BP−8222のハイブリドーマクローンを用いて産生される(7)記載のモノクローナル抗体、(9)寄託番号FERM BP−8223のハイブリドーマクローンを用いて産生される(7)記載のモノクローナル抗体、(10)寄託番号FERM BP−8224のハイブリドーマクローンを用いて産生される(7)記載のモノクローナル抗体、(11)(1)または(2)記載の細胞障害タンパク質を哺乳類に免疫して得られる細胞障害タンパク質に特異的なポリクローナル抗体、(12)(7)から(11)のいずれか1項に記載のモノクローナル抗体またはポリクローナル抗体を用いる(1)または(2)記載の細胞障害タンパク質を検出する方法および診断法、(13)(7)から(11)のいずれか1項に記載のモノクローナル抗体またはポリクローナル抗体を用いる(1)または(2)記載の細胞障害タンパク質により惹き起こされる胃癌、胃炎、胃潰瘍の予防、治療剤、(14)(1)または(2)記載のタンパク質を用いることを特徴とする、(1)または(2)記載のタンパク質の活性を促進または阻害する化合物について、温血動物細胞を用いて陰性または陽性対照群との比較で、細胞増殖阻害活性、細胞障害活性あるいは細胞死により当該化合物をスクリーニングする方法、(15)(1)または(2)記載のタンパク質を含有してなる、(1)または(2)記載のタンパク質の活性を促進または阻害する化合物またはその塩のスクリーニング用キット、(16)(14)記載のスクリーニング方法または(15)記載のスクリーニング用キットを用いて得られる、(1)または(2)記載のタンパク質の活性を促進または阻害する化合物またはその塩、(17)(1)または(2)記載のタンパク質による温血動物細胞の細胞障害活性を阻害する活性を有する化合物またはその塩を含有する医薬、(18)胃炎、胃潰瘍、胃癌および(14)記載のスクリーニング方法または(15)記載のスクリーニング用キットによって、M毒素で惹起されることの示される疾患に対する予防・治療剤である(17)記載の医薬を提供する。
発明を実施するための最良の形態
本発明の配列番号1で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を有するタンパク質は、ヘリコバクターピロリにおける細菌株、例えばNCTC 11637,NCTC 11916,DT 61A,NCTC 11639,R85−13 6P,R85−13−12F,R85−13−11P,T81213−NTB,J99、4、U2−1、85D08、MC903、MC123、Tx30a、26695、UA 1182等に由来するタンパク質であってもよく、合成タンパク質であってもよい。
配列番号1で表わされるアミノ酸配列と実質的に同一のアミノ酸配列としては、配列番号1で表わされるアミノ酸配列と約70%以上、好ましくは約80%以上、より好ましくは約90%以上、さらに好ましくは約95%以上の相同性を有するアミノ酸配列などがあげられる。本発明の配列番号1で表わされるアミノ酸配列と実質的に同一のアミノ酸配列を有するタンパク質としては、例えば、前記の配列番号1で表わされるアミノ酸配列と実質的に同一のアミノ酸配列を有し、配列番号1で表わされるアミノ酸配列を有するタンパク質と実質的に同質の活性を有するタンパク質などが好ましい。実質的に同質の活性としては、例えば、細胞増殖阻害活性、細胞障害活性あるいは細胞死をもたらす活性などがあげられる。実質的に同質とは、それらの活性が性質的に(例、生理化学的に、または薬理学的に)同質であることを示す。従って、細胞障害などの活性が同等(例、約0.1〜100倍、好ましくは約0.5〜10倍、より好ましくは約0.5〜2倍)であることが好ましいが、これらの活性の程度、タンパク質の分子量などの量的要素は異なっていてもよい。細胞増殖阻害活性、細胞障害活性あるいは細胞死をもたらす活性の測定は、自体公知の方法に準じて行なうことができるが、例えば、後述するスクリーニング方法に従って測定することができる。
また、本発明のタンパク質としては、例えば、配列番号1で表わされるアミノ酸配列中の1〜150個(好ましくは、1〜50個)のアミノ酸が欠失したアミノ酸配列;配列番号1で表わされるアミノ酸配列に1〜100個(好ましくは、1〜50個(より好ましくは、1〜30個))のアミノ酸が付加したアミノ酸配列;配列番号1で表わされるアミノ酸配列に1〜50個(好ましくは、1〜30個)のアミノ酸が挿入されたアミノ酸配列;配列番号1で表わされるアミノ酸配列中の1〜50個(好ましくは、1〜30個)のアミノ酸が他のアミノ酸で置換されたアミノ酸配列;またはそれらを組み合わせたアミノ酸配列を含有するタンパク質などのいわゆるムチンも含まれる。前記のようにアミノ酸配列が挿入、欠失または置換されている場合、その挿入、欠失または置換の位置としては、特に限定されない。
本明細書におけるタンパク質は、ペプチド標記の慣例に従って左端がN末端(アミノ末端)、右端がC末端(カルボキシル末端)である。配列番号1で表わされるアミノ酸配列を含有するタンパク質をはじめとする、本発明のタンパク質は、C末端が通常カルボキシル基(−COOH)またはカルボキシレート(−COO−)であるが、C末端がアミド(−CONH2)またはエステル(−COOR)であってもよい。ここでエステルにおけるRとしては、例えば、メチル、エチル、n−プロピル、イソプロピルもしくはn−ブチルなどのC1−6アルキル基、例えば、シクロペンチル、シクロヘキシルなどのC3−8シクロアルキル基、例えば、フェニル、α−ナフチルなどのC6−12アリール基、例えば、ベンジル、フェネチルなどのフェニル−C1−2アルキル基もしくはα−ナフチルメチルなどのα−ナフチル−C1−2アルキル基などのC7−14アラルキル基である。本発明のタンパク質がC末端以外にカルボキシル基(またはカルボキシレート)を有している場合、カルボキシル基がアミド化またはエステル化されているものも本発明のタンパク質に含まれる。この場合のエステルとしては、例えば前記したC末端のエステルなどが用いられる。さらに、本発明のタンパク質には、N末端のアミノ酸残基(例、メチオニン残基)のアミノ基が保護基(例えば、ホルミル基、アセチル基などのC1−6アルカノイルなどのC1−6アシル基など)で保護されているもの、生体内で切断されて生成するN末端のグルタミン残基がピログルタミン酸化したもの、分子内のアミノ酸の側鎖上の置換基(例えば−OH、−SH、アミノ基、イミダゾール基、インドール基、グアニジノ基など)が適当な保護基(例えば、ホルミル基、アセチル基などのC1−6アルカノイル基などのC1−6アシル基など)で保護されているもの、あるいは糖鎖が結合したいわゆる糖タンパク質などの複合タンパク質なども含まれる。
本発明のタンパク質の部分ペプチドとしては、前記した本発明のタンパク質の部分ペプチドであって、好ましくは、前記した本発明のタンパク質と同様の活性(例、細胞増殖阻害または細胞増殖阻害など)を有するものであればいかなるものでもよい。例えば、本発明のタンパク質の構成アミノ酸配列中の少なくとも20%以上、好ましくは50%以上、さらに好ましくは70%以上、より好ましくは90%以上、最も好ましくは95%以上のアミノ酸配列を有し、細胞増殖阻害活性、細胞障害活性あるいは細胞死をもたらす活性を有するペプチドなどが用いられる。また、本発明の部分ペプチドは、そのアミノ酸配列中の1〜5個(好ましくは、1〜3個)のアミノ酸が欠失し、または、そのアミノ酸配列に1〜10個(好ましくは、1〜5個(より好ましくは、1〜3個))のアミノ酸が付加し、または、そのアミノ酸配列に1〜5個(好ましくは、1〜3個)のアミノ酸が挿入され、または、そのアミノ酸配列中の1〜5個(好ましくは、1〜3個)のアミノ酸が他のアミノ酸で置換されていてもよい。
また、本発明の部分ペプチドはC末端が通常カルボキシル基(−COOH)またはカルボキシレート(−COO−)であるが、前記した本発明のタンパク質のごとく、C末端がアミド(−CONH2)またはエステル(−COOR)(Rは前記と同意義を示す)であってもよい。さらに、本発明の部分ペプチドには、前記した本発明のタンパク質と同様に、N末端のアミノ酸残基(例、メチオニン残基)のアミノ基が保護基で保護されているもの、N端側が生体内で切断され生成したグルタミン残基がピログルタミン酸化したもの、分子内のアミノ酸の側鎖上の置換基が適当な保護基で保護されているもの、あるいは糖鎖が結合したいわゆる糖ペプチドなどの複合ペプチドなども含まれる。また、本発明の部分ペプチドは抗体作成のための抗原として用いることができるので、必ずしも細胞増殖阻害活性または細胞障害活性等を有する必要はない。
本発明のタンパク質または部分ペプチドの塩としては、生理学的に許容される酸(例、無機酸、有機酸)や塩基(例、アルカリ金属塩)などとの塩が用いられ、とりわけ生理学的に許容される酸付加塩が好ましい。このような塩としては、例えば、無機酸(例えば、塩酸、リン酸、臭化水素酸、硫酸)との塩、あるいは有機酸(例えば、酢酸、ギ酸、プロピオン酸、フマル酸、マレイン酸、コハク酸、酒石酸、クエン酸、リンゴ酸、蓚酸、安息香酸、メタンスルホン酸、ベンゼンスルホン酸)との塩などが用いられる。本発明のタンパク質またはその塩は、前述したヘリコバクターピロリの種々の菌株の菌体より自体公知のタンパク質の精製方法によって製造することもできるし、後述するタンパク質をコードするDNAを含有する形質転換体を培養することによっても製造することができる。また、後述のペプチド合成法に準じて製造することもできる。ヘリコバクターピロリの種々の菌株の菌体から製造する場合、菌体を超音波破砕などにより菌体内タンパク質を遠心分離した後、硫安沈殿などで抽出を行ない、該抽出液をイオン交換クロマトグラフィー、疎水性クロマトグラフィーなどのクロマトグラフィーを組み合わせることにより精製単離することができる。
本発明のタンパク質、部分ペプチド、もしくはそれらの塩、またはそれらのアミド体の合成には、通常市販のタンパク質合成用樹脂を用いることができる。そのような樹脂としては、例えば、クロロメチル樹脂、ヒドロキシメチル樹脂、ベンズヒドリルアミン樹脂、アミノメチル樹脂、4−ベンジルオキシベンジルアルコール樹脂、4−メチルベンズヒドリルアミン樹脂、PAM樹脂、4−ヒドロキシメチルメチルフェニルアセトアミドメチル樹脂、ポリアクリルアミド樹脂、4−(2’,4’−ジメトキシフェニル−ヒドロキシメチル)フェノキシ樹脂、4−(2’,4’−ジメトキシフェニル−Fmocアミノエチル)フェノキシ樹脂などをあげることができる。このような樹脂を用い、α−アミノ基と側鎖官能基を適当に保護したアミノ酸を、目的とするタンパク質の配列通りに、自体公知の各種縮合方法に従い、樹脂上で縮合させる。反応の最後に樹脂からタンパク質を切り出すと同時に各種保護基を除去し、さらに高希釈溶液中で分子内ジスルフィド結合形成反応を実施し、目的のタンパク質またはそれらのアミド体を取得する。前記した保護アミノ酸の縮合に関しては、タンパク質合成に使用できる各種活性化試薬を用いることができるが、特に、カルボジイミド類がよい。カルボジイミド類としては、DCC、N,N’−ジイソプロピルカルボジイミド、N−エチル−N’−(3−ジメチルアミノプロリル)カルボジイミドなどが用いられる。これらによる活性化にはラセミ化抑制添加剤(例えば、HOBt,HOOBt)とともに保護アミノ酸を直接樹脂に添加するかまたは、対称酸無水物またはHOBtエステルあるいはHOOBtエステルとしてあらかじめ保護アミノ酸の活性化を行なった後に樹脂に添加することができる。
保護アミノ酸の活性化や樹脂との縮合に用いられる溶媒としては、タンパク質縮合反応に使用しうることが知られている溶媒から適宜選択されうる。例えば、N,N−ジメチルホルムアミド,N,N−ジメチルアセトアミド,N−メチルピロリドンなどの酸アミド類、塩化メチレン,クロロホルムなどのハロゲン化炭化水素類、トリフルオロエタノールなどのアルコール類、ジメチルスルホキシドなどのスルホキシド類、ピリジン,ジオキサン,テトラヒドロフランなどのエーテル類、アセトニトリル,プロピオニトリルなどのニトリル類、酢酸メチル,酢酸エチルなどのエステル類あるいはこれらの適宜の混合物などが用いられる。反応温度はタンパク質結合形成反応に使用され得ることが知られている範囲から適宜選択され、通常約−20℃〜50℃の範囲から適宜選択される。活性化されたアミノ酸誘導体は通常1.5〜4倍過剰で用いられる。ニンヒドリン反応を用いたテストの結果、縮合が不十分な場合には保護基の脱離を行なうことなく縮合反応を繰り返すことにより十分な縮合を行なうことができる。反応を繰り返しても十分な縮合が得られないときには、無水酢酸またはアセチルイミダゾールを用いて未反応アミノ酸をアセチル化することによって、後の反応に影響を与えないようにすることができる。
原料のアミノ基の保護基としては、例えば、Z、Boc、t−ペンチルオキシカルボニル、イソボルニルオキシカルボニル、4−メトキシベンジルオキシカルボニル、Cl−Z、Br−Z、アダマンチルオキシカルボニル、トリフルオロアセチル、フタロイル、ホルミル、2−ニトロフェニルスルフェニル、ジフェニルホスフィノチオイル、Fmocなどが用いられる。カルボキシル基は、例えば、アルキルエステル化(例えば、メチル、エチル、プロピル、ブチル、t−ブチル、シクロペンチル、シクロヘキシル、シクロヘプチル、シクロオクチル、2−アダマンチルなどの直鎖状、分枝状もしくは環状アルキルエステル化)、アラルキルエステル化(例えば、ベンジルエステル、4−ニトロベンジルエステル、4−メトキシベンジルエステル、4−クロロベンジルエステル、ベンズヒドリルエステル化)、フェナシルエステル化、ベンジルオキシカルボニルヒドラジド化、t−ブトキシカルボニルヒドラジド化、トリチルヒドラジド化などによって保護することができる。セリンの水酸基は、例えば、エステル化またはエーテル化によって保護することができる。このエステル化に適する基としては、例えば、アセチル基などの低級(C1−6)アルカノイル基、ベンゾイル基などのアロイル基、ベンジルオキシカルボニル基、エトキシカルボニル基などの炭酸から誘導される基などが用いられる。また、エーテル化に適する基としては、例えば、ベンジル基、テトラヒドロピラニル基、t−ブチル基などである。チロシンのフェノール性水酸基の保護基としては、例えば、Bzl、Cl2−Bzl、2−ニトロベンジル、Br−Z、t−ブチルなどが用いられる。ヒスチジンのイミダゾールの保護基としては、例えば、Tos、4−メトキシ−2,3,6−トリメチルベンゼンスルホニル、DNP、ベンジルオキシメチル、Bum、Bos、Trt、Fmocなどが用いられる。
原料のカルボキシル基の活性化されたものとしては、例えば、対応する酸無水物、アジド、活性エステル〔アルコール(例えば、ペンタクロロフェノール、2,4,5−トリクロロフェノール、2,4−ジニトロフェノール、シアノメチルアルコール、パラニトロフェノール、HONB、N−ヒドロキシスクシミド、N−ヒドロキシフタルイミド、HOBt)とのエステル〕などが用いられる。原料のアミノ基の活性化されたものとしては、例えば、対応するリン酸アミドが用いられる。保護基の除去(脱離)方法としては、例えば、Pd−黒あるいはPd−炭素などの触媒の存在下での水素気流中での接触還元や、また、無水フッ化水素、メタンスルホン酸、トリフルオロメタンスルホン酸、トリフルオロ酢酸あるいはこれらの混合液などによる酸処理や、ジイソプロピルエチルアミン、トリエチルアミン、ピペリジン、ピペラジンなどによる塩基処理、また液体アンモニア中ナトリウムによる還元なども用いられる。前記酸処理による脱離反応は、一般に約−20℃〜40℃の温度で行なわれるが、酸処理においては、例えば、アニソール、フェノール、チオアニソール、メタクレゾール、パラクレゾール、ジメチルスルフィド、1,4−ブタンジチオール、1,2−エタンジチオールなどのようなカチオン捕捉剤の添加が有効である。また、ヒスチジンのイミダゾール保護基として用いられる2,4−ジニトロフェニル基はチオフェノール処理により除去され、トリプトファンのインドール保護基として用いられるホルミル基は前記の1,2−エタンジチオール、1,4−ブタンジチオールなどの存在下の酸処理による脱保護以外に、希水酸化ナトリウム溶液、希アンモニアなどによるアルカリ処理によっても除去される。
原料の反応に関与すべきでない官能基の保護ならびに保護基、およびその保護基の脱離、反応に関与する官能基の活性化などは公知の基または公知の手段から適宜選択しうる。タンパク質のアミド体を得る別の方法としては、例えば、まず、カルボキシ末端アミノ酸のα−カルボキシル基をアミド化して保護した後、アミノ基側にペプチド(タンパク質)鎖を所望の鎖長まで延ばした後、該ペプチド鎖のN末端のα−アミノ基の保護基のみを除いたタンパク質とC末端のカルボキシル基の保護基のみを除去したタンパク質とを製造し、この両タンパク質を前記したような混合溶媒中で縮合させる。縮合反応の詳細については前記と同様である。縮合により得られた保護タンパク質を精製した後、前記方法によりすべての保護基を除去し、所望の粗タンパク質を得ることができる。この粗タンパク質は既知の各種精製手段を駆使して精製し、主要画分を凍結乾燥することで所望のタンパク質のアミド体を得ることができる。タンパク質のエステル体を得るには、例えば、カルボキシ末端アミノ酸のα−カルボキシル基を所望のアルコール類と縮合しアミノ酸エステルとした後、タンパク質のアミド体と同様にして、所望のタンパク質のエステル体を得ることができる。
本発明の部分ペプチドまたはその塩は、自体公知のペプチドの合成法に従って、あるいは本発明のタンパク質を適当なペプチダーゼで切断することによって製造することができる。ペプチドの合成法としては、例えば、固相合成法、液相合成法のいずれによっても良い。すなわち、本発明の部分ペプチドを構成し得る部分ペプチドもしくはアミノ酸と残余部分とを縮合させ、生成物が保護基を有する場合は保護基を脱離することにより目的のペプチドを製造することができる。公知の縮合方法や保護基の脱離としては、例えば、以下に記載された方法があげられる。M.BodanszkyおよびM.A.Ondetti、Peptide Synthesis,Interscience Publishers,New York(1966年);SchroederおよびLuebke、The Peptide,Academic Press,New York(1965年);泉屋信夫他、ペプチド合成の基礎と実験、丸善(株)(1975年);矢島治明および榊原俊平、生化学実験講座1、タンパク質の化学IV、205、(1977年);矢島治明監修、続医薬品の開発、第14巻、ペプチド合成、広川書店。また、反応後は通常の精製法、例えば、溶媒抽出・蒸留・カラムクロマトグラフィー・液体クロマトグラフィー・再結晶などを組み合わせて本発明の部分ペプチドを精製単離することができる。前記方法で得られる部分ペプチドが遊離体である場合は、公知の方法あるいはそれに準じる方法によって適当な塩に変換することができ、逆に塩で得られた場合は、公知の方法あるいはそれに準じる方法によって遊離体または他の塩に変換することができる。
本発明のタンパク質をコードするDNAとしては、前述した本発明のタンパク質をコードする塩基配列を含有するものであればいかなるものであってもよい。また、ゲノムDNA、ゲノムDNAライブラリー、前記した細胞・組織由来のcDNA、前記した細胞・組織由来のcDNAライブラリー、合成DNAのいずれでもよい。ライブラリーに使用するベクターは、バクテリオファージ、プラスミド、コスミド、ファージミドなどいずれであってもよい。また、前記した細胞・組織よりtotalRNAまたはmRNA画分を調製したものを用いて直接Reverse Transcriptase Polymerase Chain Reaction(以下、RT−PCR法と略称する)によって増幅することもできる。本発明のタンパク質をコードするDNAとしては、例えば、配列番号2で表わされる塩基配列を含有するDNA、または配列番号2で表わされる塩基配列とハイストリンジェントな条件下でハイブリダイズする塩基配列を有し、本発明のタンパク質と実質的に同質の活性(例、細胞障害活性など)を有するタンパク質をコードするDNAなどであれば何でもよい。
より具体的には、配列番号1で表わされるアミノ酸配列を有するタンパク質をコードするDNAとしては、配列番号2で表わされる塩基配列を有するDNAなどが用いられる。
本発明の部分ペプチドをコードするDNAとしては、前述した本発明の部分ペプチドをコードする塩基配列を含有するものであればいかなるものであってもよい。また、ゲノムDNA、ゲノムDNAライブラリー、前記した細胞・組織由来のcDNA、前記した細胞・組織由来のcDNAライブラリー、合成DNAのいずれでもよい。本発明の部分ペプチドをコードするDNAとしては、例えば、配列番号2で表わされる塩基配列を有するDNAの部分塩基配列を有するDNA、または配列番号2で表わされる塩基配列とハイストリンジェントな条件下でハイブリダイズする塩基配列を有し、本発明のタンパク質と実質的に同質の活性を有するタンパク質をコードするDNAの部分塩基配列を有するDNAなどが用いられる。
本発明のタンパク質または部分ペプチド(以下、これらタンパク質等をコードするDNAのクローニングおよび発現の説明においては、これらタンパク質等を単に本発明のタンパク質と略記する場合がある)を完全にコードするDNAのクローニングの手段としては、本発明のタンパク質の部分塩基配列を有する合成DNAプライマーを用いて自体公知のPCR法によって増幅するか、または適当なベクターに組み込んだDNAを本発明のタンパク質の一部あるいは全領域をコードするDNA断片もしくは合成DNAを用いて標識したものとのハイブリダイゼーションによって選別することができる。ハイブリダイゼーションの方法は、例えば、Molecular Cloning、2nd、J.Sambrook et al.,Cold Spring Harbor Lab.Press,1989に記載の方法などに従って行なうことができる。また、市販のライブラリーを使用する場合、添付の使用説明書に記載の方法に従って行なうことができる。DNAの塩基配列の変換は、公知のキット、例えば、MutanTM−G(宝酒造(株)製)、MutanTM−K(宝酒造(株)製)などを用いて、Gapped duplex法やKunkel法などの自体公知の方法あるいはそれらに準じる方法に従って行なうことができる。クローン化されたタンパク質をコードするDNAは目的によりそのまま、または所望により制限酵素で消化したり、リンカーを付加したりして使用することができる。該DNAはその5’末端側に翻訳開始コドンとしてのATG、GTG、TTGを有し、また3’末端側には翻訳終止コドンとしてのTAA、TGAまたはTAGを有していてもよい。これらの翻訳開始コドンや翻訳終止コドンは、適当な合成DNAアダプターを用いて付加することもできる。本発明のタンパク質の発現ベクターは、例えば、(イ)本発明のタンパク質をコードするDNAから目的とするDNA断片を切り出し、(ロ)該DNA断片を適当な発現ベクター中のプロモーターの下流に連結することにより製造することができる。
ベクターとしては、大腸菌由来のプラスミド(例、pBR322,pBR325,pUC12,pUC13,pET30)、枯草菌由来のプラスミド(例、pUB110,pTP5,pC194)、酵母由来プラスミド(例、pSH19,pSH15)、λファージなどのバクテリオファージ、レトロウイルス,ワクシニアウイルス,バキュロウイルスなどの動物ウイルスなどの他、pA1−11、pXT1、pRc/CMV、pRc/RSV、pcDNAI/Neoなどが用いられる。本発明で用いられるプロモーターとしては、遺伝子の発現に用いる宿主に対応して適切なプロモーターであればいかなるものでもよい。例えば、動物細胞を宿主として用いる場合は、SRαプロモーター、SV40初期プロモーター、HIV・LTRプロモーター、CMVプロモーター、HSV−TKプロモーターなどがあげられる。これらのうち、CMV(サイトメガロウイルス)プロモーター、SRαプロモーターなどを用いるのが好ましい。宿主がエシェリヒア属菌である場合は、trpプロモーター、lacプロモーター、recAプロモーター、λPLプロモーター、lppプロモーター、T7プロモーターなどが、宿主がバチルス属菌である場合は、SPO1プロモーター、SPO2プロモーター、penPプロモーターなど、宿主が酵母である場合は、PHO5プロモーター、PGKプロモーター、GAPプロモーター、ADHプロモーターなどが好ましい。宿主が昆虫細胞である場合は、ポリヘドリンプロモーター、P10プロモーターなどが好ましい。
発現ベクターには、以上の他に、所望によりエンハンサー、選択マーカー、SV40複製オリジン(以下、SV40oriと略称する場合がある)などを含有しているものを用いることができる。選択マーカーとしては、例えば、ジヒドロ葉酸還元酵素(以下、dhfrと略称する場合がある)遺伝子〔メソトレキセート(MTX)耐性〕、アンピシリン耐性遺伝子(以下、Amprと略称する場合がある)、ネオマイシン耐性遺伝子(以下、Neorと略称する場合がある、G418耐性)、カナマイシン耐性遺伝子等があげられる。特に、dhfr遺伝子欠損チャイニーズハムスター細胞を用いてdhfr遺伝子を選択マーカーとして使用する場合、組換え体細胞をチミジンを含まない培地によっても選択できる。また、必要に応じて、宿主に合ったシグナル配列を、本発明のタンパク質のN端末側に付加する。宿主がエシェリヒア属菌である場合は、PhoA・シグナル配列、OmpA・シグナル配列などが、宿主がバチルス属菌である場合は、α−アミラーゼ・シグナル配列、サブチリシン・シグナル配列などが、宿主が酵母である場合は、MFα・シグナル配列、SUC2・シグナル配列など、宿主が動物細胞である場合には、インシュリン・シグナル配列、α−インターフェロン・シグナル配列、抗体分子・シグナル配列などがそれぞれ利用できる。このようにして構築された本発明のタンパク質をコードするDNAを含有するベクターを用いて、形質転換体を製造することができる。
宿主としては、例えば、エシェリヒア属菌、バチルス属菌、酵母、昆虫細胞、昆虫、動物細胞などが用いられる。エシェリヒア属菌の具体例としては、例えば、エシェリヒア・コリ(Escherichia coli)K12・DH1・DH5α(Proc.Natl.Acad.Sci.USA,Vol.60,160(1968))、JM103(Nucleic Acids Research,Vol.9,309(1981))、JA221(Journal of Molecular Biology,Vol.120,517(1978))、HB101(Journal of Molecular Biology,Vol.41,459(1969))、C600(Genetics,Vol.39,440(1954))などが用いられる。バチルス属菌としては、例えば、バチルス・サブチルス(Bacillus subtilis)MI114(Gene,Vol.24,255(1983),207−21(Journal of Biochemistry,Vol.95,87(1984))などが用いられる。酵母としては、例えば、サッカロマイセス セレビシエ(Saccharomyces cerevisiae)AH22,AH22R−,NA87−11A,DKD−5D,20B−12、シゾサッカロマイセス ポンベ(Schizosaccharomyces pombe)NCYC1913,NCYC2036、ピヒア パストリス(Pichia pastoris)KM71などが用いられる。
昆虫細胞としては、例えば、ウイルスがAcNPVの場合は、夜盗蛾の幼虫由来株化細胞(Spodoptera frugiperda cell;Sf細胞)、Trichoplusia niの中腸由来のMG1細胞、Trichoplusia niの卵由来のHigh FiveTM細胞、Mamestra brassicae由来の細胞またはEstigmena acrea由来の細胞などが用いられる。ウイルスがBmNPVの場合は、蚕由来株化細胞(Bombyx mori N細胞;BmN細胞)などが用いられる。該Sf細胞としては、例えば、Sf9細胞(ATCC CRL1711)、Sf21細胞(以上、Vaughn,J.L.ら、In Vivo,13,213−217(1977))などが用いられる。昆虫としては、例えば、カイコの幼虫などが用いられる〔前田ら、Nature,Vol.315,592(1985)〕。動物細胞としては、例えば、サル細胞COS−7,Vero,チャイニーズハムスター細胞CHO(以下、CHO細胞と略記),dhfr遺伝子欠損チャイニーズハムスター細胞CHO(以下、CHO(dhfr−)細胞と略記),マウスL細胞,マウスAtT−20,マウスミエローマ細胞,ラットGH3,ヒトFL細胞などが用いられる。さらに、各種の正常ヒト細胞、例えば肝細胞、脾細胞、神経細胞、グリア細胞、膵臓β細胞、骨髄細胞、メサンギウム細胞、ランゲルハンス細胞、表皮細胞、上皮細胞、内皮細胞、繊維芽細胞、繊維細胞、筋細胞、脂肪細胞、免疫細胞(例、マクロファージ、T細胞、B細胞、ナチュラルキラー細胞、肥満細胞、好中球、好塩基球、好酸球、単球)、巨核球、滑膜細胞、軟骨細胞、骨細胞、骨芽細胞、破骨細胞、乳腺細胞、肝細胞もしくは間質細胞、またはこれら細胞の前駆細胞、幹細胞もしくは癌細胞など)などを用いることも可能である。エシェリヒア属菌を形質転換するには、例えば、Proc.Natl.Acad.Sci.USA,Vol.69,2110(1972)やGene,Vol.17,107(1982)などに記載の方法に従って行なうことができる。
バチルス属菌を形質転換するには、例えば、Molecular & General Genetics,Vol.168,111(1979)などに記載の方法に従って行なうことができる。酵母を形質転換するには、例えば、Methods in Enzymology,Vol.194,182−187(1991)、Proc.Natl.Acad.Sci.USA,Vol.75,1929(1978)などに記載の方法に従って行なうことができる。昆虫細胞または昆虫を形質転換するには、例えば、Bio/Technology,6,47−55(1988)などに記載の方法に従って行なうことができる。
動物細胞を形質転換するには、例えば、細胞工学別冊8 新細胞工学実験プロトコール、263−267(1995)(秀潤社発行)、Virology,Vol.52,456(1973)に記載の方法に従って行なうことができる。このようにして、タンパク質をコードするDNAを含有する発現ベクターで形質転換された形質転換体を得ることができる。宿主がエシェリヒア属菌、バチルス属菌である形質転換体を培養する際、培養に使用される培地としては液体培地が適当であり、その中には該形質転換体の生育に必要な炭素源、窒素源、無機物その他が含有せしめられる。炭素源としては、例えば、グルコース、デキストリン、可溶性澱粉、ショ糖など、窒素源としては、例えば、アンモニウム塩類、硝酸塩類、コーンスチープ・リカー、ペプトン、カゼイン、肉エキス、大豆粕、バレイショ抽出液などの無機または有機物質、無機物としては、例えば、塩化カルシウム、リン酸二水素ナトリウム、塩化マグネシウムなどがあげられる。また、酵母エキス、ビタミン類、生長促進因子などを添加してもよい。培地のpHは約5〜8が望ましい。
エシェリヒア属菌を培養する際の培地としては、例えば、グルコース、カザミノ酸を含むM9培地(Miller,Journal of Experiments in Molecular Genetics,431−433,Cold Spring Harbor Laboratory,New York 1972)が好ましい。ここに必要によりプロモーターを効率よく働かせるために、例えば、3β−インドリルアクリル酸のような薬剤を加えることができる。宿主がエシェリヒア属菌の場合、培養は通常約15〜43℃で約3〜24時間行ない、必要により、通気や撹拌を加えることもできる。宿主がバチルス属菌の場合、培養は通常約30〜40℃で約6〜24時間行ない、必要により通気や撹拌を加えることもできる。
宿主が酵母である形質転換体を培養する際、培地としては、例えば、バークホールダー(Burkholder)最小培地(Bostian,K.L.ら、Proc.Natl.Acad.Sci.USA),Vol.77,4505(1980))や0.5%カザミノ酸を含有するSD培地(Bitter,G.A.ら、Proc.Natl.Acad.Sci.USA,Vol.81,5330(1984))があげられる。培地のpHは約5〜8に調整するのが好ましい。培養は通常約20℃〜35℃で約24〜72時間行ない、必要に応じて通気や撹拌を加える。宿主が昆虫細胞または昆虫である形質転換体を培養する際、培地としては、Grace’s Insect Medium(Grace,T.C.C.,Nature,195,788(1962))に非動化した10%ウシ血清等の添加物を適宜加えたものなどが用いられる。培地のpHは約6.2〜6.4に調整するのが好ましい。培養は通常約27℃で約3〜5日間行ない、必要に応じて通気や撹拌を加える。宿主が動物細胞である形質転換体を培養する際、培地としては、例えば、約5〜20%の胎児牛血清を含むMEM培地(Science,Vol.122,501(1952))、DMEM培地(Virology,Vol.8,396(1959))、RPMI 1640培地(The Jounal of the American Medical Association,Vol.199,519(1967))、199培地(Proceeding of the Society for the Biological Medicine,Vol.73,1(1950))などが用いられる。pHは約6〜8であるのが好ましい。培養は通常約30℃〜40℃で約15〜60時間行ない、必要に応じて通気や撹拌を加える。以上のようにして、形質転換体の細胞外に本発明のタンパク質を生成せしめることができる。
前記培養物から本発明のタンパク質を分離精製するには、例えば、下記の方法により行なうことができる。本発明のタンパク質を培養菌体あるいは細胞から抽出するに際しては、培養後、公知の方法で菌体あるいは細胞を集め、これを適当な緩衝液に懸濁し、超音波、リゾチームおよび/または凍結融解などによって菌体あるいは細胞を破壊したのち、遠心分離やろ過によりタンパク質の粗抽出液を得る方法などが適宜用いられる。緩衝液の中に尿素や塩酸グアニジンなどの蛋白質変性剤や、トリトンX−100TMなどの界面活性剤が含まれていてもよい。培養液中にタンパク質が分泌される場合には、培養終了後、それ自体公知の方法で菌体あるいは細胞と上清とを分離し、上清を集める。このようにして得られた培養上清、あるいは抽出液中に含まれるタンパク質の精製は、自体公知の分離・精製法を適宜組み合わせて行なうことができる。これらの公知の分離、精製法としては、塩析や溶媒沈澱法などの溶解度を利用する方法、透析法、限外ろ過法、ゲルろ過法、およびSDS−ポリアクリルアミドゲル電気泳動法などの主として分子量の差を利用する方法、イオン交換クロマトグラフィーなどの荷電の差を利用する方法、疎水性クロマトグラフィーなどの疎水性の差を利用する方法、アフィニティークロマトグラフィーなどの特異的親和性を利用する方法、逆相高速液体クロマトグラフィーなどの疎水性の差を利用する方法、等電点電気泳動法などの等電点の差を利用する方法などが用いられる。
かくして得られるタンパク質が遊離体で得られた場合には、自体公知の方法あるいはそれに準じる方法によって塩に変換することができ、逆に塩で得られた場合には自体公知の方法あるいはそれに準じる方法により、遊離体または他の塩に変換することができる。なお、組換え体が産生するタンパク質を、精製前または精製後に適当な蛋白修飾酵素を作用させることにより、任意に修飾を加えたり、ポリペプチドを部分的に除去することもできる。蛋白修飾酵素としては、例えば、トリプシン、キモトリプシン、アルギニルエンドペプチダーゼ、プロテインキナーゼ、グリコシダーゼなどが用いられる。かくして生成する本発明のタンパク質またはその塩の存在または活性は、標識したリガンドとの結合実験および特異抗体を用いたエンザイムイムノアッセイなどにより測定することができる。
本発明のタンパク質もしくは部分ペプチドまたはその塩に対する抗体は、本発明のタンパク質もしくは部分ペプチドまたはその塩を認識し得る抗体であれば、ポリクローナル抗体、モノクローナル抗体の何れであってもよい。本発明のタンパク質もしくは部分ペプチドまたはその塩(以下、抗体の説明においては、これらタンパク質等を単に本発明のタンパク質と略記する場合がある)に対する抗体は、本発明のタンパク質を抗原として用い、自体公知の抗体または抗血清の製造法に従って製造することができる。
モノクローナル抗体の作製
(a)モノクロナール抗体産生細胞の作製:本発明のタンパク質は、温血動物に対して投与により抗体産生が可能な部位にそれ自体あるいは担体、希釈剤とともに投与される。投与に際して抗体産生能を高めるため、完全フロイントアジュバントや不完全フロイントアジュバントを投与してもよい。投与は通常2〜6週毎に1回ずつ、計2〜10回程度行われる。用いられる温血動物としては、例えば、サル、ウサギ、イヌ、モルモット、マウス、ラット、ヒツジ、ヤギ、ニワトリがあげられるが、マウスおよびラットが好ましく用いられる。モノクローナル抗体産生細胞の作製に際しては、抗原で免疫された温血動物、例えばマウスから抗体価の認められた個体を選択し最終免疫の2〜5日後に脾臓またはリンパ節を採取し、それらに含まれる抗体産生細胞を同種または異種動物の骨髄腫細胞と融合させることにより、モノクローナル抗体産生ハイブリドーマを調製することができる。抗血清中の抗体価の測定は、例えば、後記の標識化タンパク質と抗血清とを反応させたのち、抗体に結合した標識剤の活性を測定することにより行なうことができる。融合操作は既知の方法、例えば、ケーラーとミルスタインの方法〔ネイチャー(Nature)、256、495(1975)〕に従い実施することができる。融合促進剤としては、例えば、ポリエチレングリコール(PEG)やセンダイウィルスなどがあげられるが、好ましくはPEGが用いられる。
骨髄腫細胞としては、例えば、NS−1、P3U1、SP2/0、AP−1などの温血動物の骨髄腫細胞があげられるが、P3U1が好ましく用いられる。用いられる抗体産生細胞(脾臓細胞)数と骨髄腫細胞数との好ましい比率は1:1〜20:1程度であり、PEG(好ましくはPEG1000〜PEG6000)が10〜80%程度の濃度で添加され、20〜40℃、好ましくは30〜37℃で1〜10分間インキュベートすることにより効率よく細胞融合を実施できる。モノクローナル抗体産生ハイブリドーマのスクリーニングには種々の方法が使用できるが、例えば、タンパク質抗原を直接あるいは担体とともに吸着させた固相(例、マイクロプレート)にハイブリドーマ培養上清を添加し、次に放射性物質や酵素などで標識した抗免疫グロブリン抗体(細胞融合に用いられる細胞がマウスの場合、抗マウス免疫グロブリン抗体が用いられる)またはプロテインAを加え、固相に結合したモノクローナル抗体を検出する方法、抗免疫グロブリン抗体またはプロテインAを吸着させた固相にハイブリドーマ培養上清を添加し、放射性物質や酵素などで標識したタンパク質を加え、固相に結合したモノクローナル抗体を検出する方法などがあげられる。モノクローナル抗体の選別は、自体公知あるいはそれに準じる方法に従って行なうことができる。通常HAT(ヒポキサンチン、アミノプテリン、チミジン)を添加した動物細胞用培地で行なうことができる。選別および育種用培地としては、ハイブリドーマが生育できるものならばどのような培地を用いても良い。例えば、1〜20%、好ましくは10〜20%の牛胎児血清を含むRPMI 1640培地、1〜10%の牛胎児血清を含むGIT培地(和光純薬工業(株))あるいはハイブリドーマ培養用無血清培地(SFM−101、日水製薬(株))などを用いることができる。培養温度は、通常20〜40℃、好ましくは約37℃である。培養時間は、通常5日〜3週間、好ましくは1週間〜2週間である。培養は、通常5%炭酸ガス下で行なうことができる。ハイブリドーマ培養上清の抗体価は、前記の抗血清中の抗体価の測定と同様にして測定できる。
(b)モノクロナール抗体の精製:モノクローナル抗体の分離精製は、自体公知の方法、例えば、免疫グロブリンの分離精製法〔例、塩析法、アルコール沈殿法、等電点沈殿法、電気泳動法、イオン交換体(例、DEAE)による吸脱着法、超遠心法、ゲルろ過法、抗原結合固相あるいはプロテインAあるいはプロテインGなどの活性吸着剤により抗体のみを採取し、結合を解離させて抗体を得る特異的精製法〕に従って行なうことができる。
〔ポリクローナル抗体の作製〕本発明のポリクローナル抗体は、それ自体公知あるいはそれに準じる方法に従って製造することができる。例えば、免疫抗原(タンパク質抗原)自体、あるいはそれとキャリアー蛋白質との複合体をつくり、上記のモノクローナル抗体の製造法と同様に温血動物に免疫を行ない、該免疫動物から本発明のタンパク質に対する抗体含有物を採取して、抗体の分離精製を行なうことにより製造することができる。温血動物を免疫するために用いられる免疫抗原とキャリアー蛋白質との複合体に関し、キャリアー蛋白質の種類およびキャリアーとハプテンとの混合比は、キャリアーに架橋させて免疫したハプテンに対して抗体が効率良くできれば、どの様なものをどの様な比率で架橋させてもよいが、例えば、ウシ血清アルブミンやウシサイログロブリン、ヘモシアニン等を重量比でハプテン1に対し、約0.1〜20、好ましくは約1〜5の割合でカプルさせる方法が用いられる。また、ハプテンとキャリアーのカプリングには、種々の縮合剤を用いることができるが、グルタルアルデヒドやカルボジイミド、マレイミド活性エステル、チオール基、ジチオビリジル基を含有する活性エステル試薬等が用いられる。縮合生成物は、温血動物に対して、抗体産生が可能な部位にそれ自体あるいは担体、希釈剤とともに投与される。投与に際して抗体産生能を高めるため、完全フロイントアジュバントや不完全フロイントアジュバントを投与してもよい。投与は、通常約2〜6週毎に1回ずつ、計約3〜10回程度行なわれる。ポリクローナル抗体は、上記の方法で免疫された温血動物の血液、腹水など、好ましくは血液から採取することができる。抗血清中のポリクローナル抗体価の測定は、上記の抗血清中の抗体価の測定と同様にして測定できる。ポリクローナル抗体の分離精製は、上記のモノクローナル抗体の分離精製と同様の免疫グロブリンの分離精製法に従って行なうことができる。
本発明のタンパク質もしくは部分ペプチド等を含有する治療剤および本発明のタンパク質等は癌細胞障害活性を有しているので、疾患組織摘出(全摘出・部分摘出の双方を含むが、部分摘出が好ましい)とくに固定癌に対する治療医薬として使用することができる。本発明のタンパク質等を上記の治療・予防剤として使用する場合は、少なくとも90%、好ましくは95%以上、より好ましくは98%以上、さらに好ましくは99%以上に精製されたものを使用するのが好ましい。
本発明のタンパク質等の癌細胞増殖阻害活性は、自体公知の方法あるいは、細胞障害活性または細胞死をもたらす活性を、自体公知の方法等それに準じる方法などに従って測定することができ、後述の実施例に記載の方法で行なうことが好ましい。試験化合物としては、例えば、ペプチド、タンパク、非ペプチド性化合物、合成化合物、発酵生産物、細胞抽出液、植物抽出液、動物組織抽出液などがあげられ、これら化合物は新規な化合物であってもよいし、公知の化合物であってもよい。
本発明のスクリーニング方法またはスクリーニング用キットを用いて得られる化合物またはその塩は、上記した試験化合物、例えば、ペプチド、タンパク、非ペプチド性化合物、合成化合物、発酵生産物、細胞抽出液、植物抽出液、動物組織抽出液、血漿などから選ばれた化合物であり、本発明のタンパク質等の細胞障害活性を阻害する活性あるいは癌細胞増殖阻害を阻害する活性を有する化合物である。該化合物の塩としては、上記した本発明のタンパク質の塩と同様のものが用いられる。
本発明のスクリーニング方法またはスクリーニング用キットを用いて得られる化合物を上述の治療剤として使用する場合、常套手段に従って実施することができる。例えば、錠剤、カプセル剤、エリキシル剤、マイクロカプセル剤、無菌性溶液、懸濁液剤などとすることができる。このようにして得られる製剤は安全で低毒性であるので、例えば、ヒトまたは温血動物(例えば、マウス、ラット、ウサギ、ヒツジ、ブタ、ウシ、ウマ、トリ、ネコ、イヌ、サルなど)に対して投与することができる。該化合物またはその塩の投与量は、その作用、対象疾患、投与対象、投与ルートなどにより差異はあるが、一般的に成人(体重60kgとして)においては、一日につき該化合物を約0.1〜100mg、好ましくは約1.0〜50mg、より好ましくは約1.0〜20mg投与する。非経口的に投与する場合は、該化合物の1回投与量は投与対象、対象疾患などによっても異なるが、注射剤の形で通常成人(60kgとして)に投与する場合、一日につき該化合物を約0.01〜30mg程度、好ましくは約0.1〜20mg程度、より好ましくは約0.1〜10mg程度を静脈注射により投与するのが好都合である。他の動物の場合も、60kg当たりに換算した量を投与することができる。
疾病に対する医薬候補化合物のスクリーニング:本発明のタンパク質等は細胞障害活性を有するため、本発明のタンパク質等の機能(例、細胞障害活性など)を促進する化合物またはその塩は、例えば、癌治療剤などの医薬として使用できるが、一方、本発明のタンパク質等の機能を阻害する化合物またはその塩は、例えば、胃炎、胃潰瘍の治療・予防剤などの医薬として使用できる。従って、本発明のタンパク質等は、本発明のタンパク質等の機能を促進または阻害する化合物またはその塩のスクリーニングのための試薬として有用である。すなわち、本発明は、(1)本発明のタンパク質もしくはその部分ペプチドまたはその塩を用いることを特徴とする、本発明のタンパク質もしくはその部分ペプチドまたはその塩の機能(例えば、細胞障害活性など)を促進する化合物もしくはその塩(「(3)疾病に対する医薬候補化合物のスクリーニング」において促進剤と略記する場合がある)、または本発明のタンパク質もしくはその部分ペプチドまたはその塩の機能(例えば、細胞障害活性など)を阻害する化合物(「(3)疾病に対する医薬候補化合物のスクリーニング」において阻害剤と略記する場合がある)のスクリーニング方法;本発明のタンパク質もしくはその部分ペプチドまたはその塩を含有することを特徴とする、促進剤または阻害剤のスクリーニング用キット(「(3)疾病に対する医薬候補化合物のスクリーニング」において本発明のスクリーニング用キットと称することもある)を提供し、より具体的には、例えば、(2)(i)本発明のタンパク質もしくはその部分ペプチドまたはその塩に細胞(例、上記の各種温血動物組織(好ましくはヒトなど)由来の血球細胞を含む正常細胞または上記の癌細胞など)を接触させた場合と(ii)本発明のタンパク質もしくはその部分ペプチドまたはその塩に細胞(例、上記の各種温血動物組織(好ましくはヒトなど)由来の血球細胞を含む正常細胞または上記の癌細胞など)および試験化合物を接触させた場合との比較を行なうことを特徴とする促進剤または阻害剤のスクリーニング方法;本発明のタンパク質もしくはその部分ペプチドまたはその塩および細胞(例、上記の各種温血動物組織(好ましくはヒトなど)由来の血球細胞を含む正常細胞または上記の癌細胞など)を含有することを特徴とする、促進剤または阻害剤のスクリーニング用キットを提供する。具体的には、上記スクリーニング方法においては、例えば、(i)と(ii)の場合における、本発明のタンパク質等の細胞障害活性などを測定して、比較することを特徴とするものである。
本発明のタンパク質等の細胞障害活性、細胞増殖阻害活性あるいは細胞死を導く活性は、自体公知の方法あるいはそれに準じる方法などに従って測定することができる。しかし、さらに具体的には、樹立された細胞株等を用いて、試験化合物を含む基質と、試験化合物を含まない基質である陰性コントロールと、M毒素を含む基質としての陽性コントロールの3者すべて、あるいはこれらのうち2者を用いた方法によって、細胞数は統計的有意を満たしうる条件下で比較して、これらの活性の有無、あるいは増減において、細胞障害活性や細胞増殖活性の阻害活性、あるいは細胞増殖活性や細胞障害活性の阻害活性をもつ特定の試料を検出しうる。用いる細胞としては、例えば、上記の各種温血動物組織(好ましくはヒトなど)由来の血球細胞を含む正常細胞または上記の各種温血動物癌細胞(例、子宮体癌、子宮内膜腫瘍、乳癌、胃癌、肝臓癌、膵臓癌、胆嚢癌、大腸癌、前立腺癌、肺癌、腎臓癌、神経芽腫、膀胱癌、悪性黒色腫、舌癌、歯肉癌、マウス線維芽細胞、ミドリザル腎細胞、ラット肝癌等)などが用いられる。
試験化合物としては、例えば、ペプチド、タンパク、非ペプチド性化合物、合成化合物、発酵生産物、細胞抽出液、植物抽出液、動物組織抽出液などがあげられ、これら化合物は新規な化合物であってもよいし、公知の化合物であってもよい。上記のスクリーニング方法を実施するには、本発明のタンパク質等を、スクリーニングに適したバッファーに懸濁することにより本発明のタンパク質等の標品を調製する。バッファーには、pH約4〜10(望ましくは、pH約6〜8)のリン酸バッファー、トリス−塩酸バッファーなどの、本発明のタンパク質等と試験化合物との反応を阻害しないバッファーであればいずれでもよい。
具体的スクリーニング方法としてはスクリーニング検査後、▲1▼細胞変化を顕微鏡下で直接観察し血球計算盤等をもちいて数える方法、▲2▼細胞死により細胞内より溶液中に溶出するカリウム、ヘモグロビン等の変化をとらえる方法、▲3▼反応後残った生細胞数をテトラゾリウム塩等をもちいて計測する方法、▲4▼放射性標識物質をもちいて残った生細胞数を計測する方法、▲5▼細胞のアポトーシスの誘導により細胞死を確認する方法等が挙げられる。例えば、上記(ii)の場合における細胞障害活性が上記(i)の場合に比べて、約20%以上、好ましくは30%以上、より好ましくは約50%以上上昇させる試験化合物を本発明のタンパク質等の細胞障害活性を促進する化合物として、一方、上記(ii)の場合における細胞障害活性が上記(i)の場合に比べて、約20%以上、好ましくは30%以上、より好ましくは約50%以上阻害する試験化合物を本発明のタンパク質等の細胞障害活性を阻害する化合物として選択することができる。これらは多種大量スクリーニング方法としても行いうる。以下に▲2▼として赤血球の溶血反応によるヘモグロビン測定法と▲3▼としてWST法をそれぞれ用いて、活性炭、CMセルロース、アルギン酸カルシウムが吸着剤として抗M毒素作用を示す化合物として選択された方法を示す。
また、これらの陰性コントロール、陽性コントロールおよび試験化合物を含む溶液を動物モデルで検討比較し、抗M毒素物質の動物レベルでの効果を確認することも可能であり、その場合、ひろく温血動物が使用可能である。とくにマウス、ラット、イヌ、サルが用いられるが、感染モデルとしてスナネズミ、マウス、サルは有用である。
本発明のスクリーニング方法またはスクリーニング用キットを用いて得られる化合物を上述の治療・予防剤として使用する場合、常套手段に従って実施することができる。例えば、上記した本発明のタンパク質等を含有する医薬と同様にして、錠剤、カプセル剤、エリキシル剤、マイクロカプセル剤、無菌性溶液、懸濁液剤などとすることができる。このようにして得られる製剤は安全で低毒性であるので、例えば、ヒトまたは温血動物(例えば、マウス、ラット、ウサギ、ヒツジ、ブタ、ウシ、ウマ、トリ、ネコ、イヌ、サルなど)に対して投与することができる。該化合物またはその塩の投与量は、その作用、対象疾患、投与対象、投与ルートなどにより差異はあるが、例えば、疾患組織摘出後の組織再生剤として、本発明のタンパク質等の機能を促進する化合物を経口投与する場合、一般的に成人(体重60kgとして)においては、一日につき該化合物を約0.1〜100mg、好ましくは約1.0〜50mg、より好ましくは約1.0〜20mg投与する。他の動物の場合も、60kg当たりに換算した量を投与することができる。
本発明のタンパク質もしくはその部分ペプチドまたはその塩の定量:本発明のタンパク質等に対する抗体(以下、本発明の抗体と略記する場合がある)は、本発明のタンパク質等を特異的に認識することができるので、被検液中の本発明のタンパク質等の定量、特にサンドイッチ免疫測定法による定量などに使用することができる。すなわち、本発明は、(i)本発明の抗体と、被検液および標識化された本発明のタンパク質等とを競合的に反応させ、該抗体に結合した標識化された本発明のタンパク質等の割合を測定することを特徴とする被検液中の本発明のタンパク質等の定量法、および(ii)被検液と担体上に不溶化した本発明の抗体および標識化された本発明の別の抗体とを同時あるいは連続的に反応させたのち、不溶化担体上の標識剤の活性を測定することを特徴とする被検液中の本発明のタンパク質等の定量法を提供する。上記(ii)の定量法においては、一方の抗体が本発明のタンパク質等のN端部を認識する抗体で、他方の抗体が本発明のタンパク質等のC端部に反応する抗体であることが望ましい。
また、本発明のタンパク質等に対するモノクローナル抗体(以下、本発明のモノクローナル抗体と称する場合がある)を用いて本発明のタンパク質等の定量を行なえるほか、組織染色等による検出を行なうこともできる。これらの目的には、抗体分子そのものを用いてもよく、また、抗体分子のF(ab’)2、Fab’、あるいはFab画分を用いてもよい。本発明の抗体を用いる本発明のタンパク質等の定量法は、特に制限されるべきものではなく、被測定液中の抗原量(例えば、タンパク質量)に対応した抗体、抗原もしくは抗体−抗原複合体の量を化学的または物理的手段により検出し、これを既知量の抗原を含む標準液を用いて作製した標準曲線より算出する測定法であれば、いずれの測定法を用いてもよい。例えば、ネフロメトリー、競合法、イムノメトリック法およびサンドイッチ法が好適に用いられるが、感度、特異性の点で、後述するサンドイッチ法を用いるのが特に好ましい。標識物質を用いる測定法に用いられる標識剤としては、例えば、放射性同位元素、酵素、蛍光物質、発光物質などが用いられる。放射性同位元素としては、例えば、〔125I〕、〔131I〕、〔3H〕、〔14C〕などが用いられる。上記酵素としては、安定で比活性の大きなものが好ましく、例えば、β−ガラクトシダーゼ、β−グルコシダーゼ、アルカリフォスファターゼ、パーオキシダーゼ、リンゴ酸脱水素酵素などが用いられる。蛍光物質としては、例えば、フルオレスカミン、フルオレッセンイソチオシアネートなどが用いられる。発光物質としては、例えば、ルミノール、ルミノール誘導体、ルシフェリン、ルシゲニンなどが用いられる。さらに、抗体あるいは抗原と標識剤との結合にビオチン−アビジン系を用いることもできる。
抗原あるいは抗体の不溶化に当っては、物理吸着を用いてもよく、また通常タンパク質あるいは酵素等を不溶化、固定化するのに用いられる化学結合を用いる方法でもよい。担体としては、アガロース、デキストラン、セルロースなどの不溶性多糖類、ポリスチレン、ポリアクリルアミド、シリコン等の合成樹脂、あるいはガラス等があげられる。サンドイッチ法においては不溶化した本発明のモノクローナル抗体に被検液を反応させ(1次反応)、さらに標識化した別の本発明のモノクローナル抗体を反応させ(2次反応)たのち、不溶化担体上の標識剤の活性を測定することにより被検液中の本発明のタンパク質量を定量することができる。1次反応と2次反応は逆の順序に行っても、また、同時に行なってもよいし時間をずらして行なってもよい。標識化剤および不溶化の方法は上記のそれらに準じることができる。また、サンドイッチ法による免疫測定法において、固相用抗体あるいは標識用抗体に用いられる抗体は必ずしも1種類である必要はなく、測定感度を向上させる等の目的で2種類以上の抗体の混合物を用いてもよい。本発明のサンドイッチ法による本発明のタンパク質等の測定法においては、1次反応と2次反応に用いられる本発明のモノクローナル抗体は、本発明のタンパク質等の結合する部位が相異なる抗体が好ましく用いられる。すなわち、1次反応および2次反応に用いられる抗体は、例えば、2次反応で用いられる抗体が、本発明のタンパク質等のC端部を認識する場合、1次反応で用いられる抗体は、好ましくはC端部以外、例えばN端部を認識する抗体が用いられる。
本発明のモノクローナル抗体をサンドイッチ法以外の測定システム、例えば、競合法、イムノメトリック法あるいはネフロメトリーなどに用いることができる。競合法では、被検液中の抗原と標識抗原とを抗体に対して競合的に反応させたのち、未反応の標識抗原(F)と、抗体と結合した標識抗原(B)とを分離し(B/F分離)、B,Fいずれかの標識量を測定し、被検液中の抗原量を定量する。本反応法には、抗体として可溶性抗体を用い、B/F分離をポリエチレングリコール、上記抗体に対する第2抗体などを用いる液相法、および、第1抗体として固相化抗体を用いるか、あるいは、第1抗体は可溶性のものを用い第2抗体として固相化抗体を用いる固相化法とが用いられる。イムノメトリック法では、被検液中の抗原と固相化抗原とを一定量の標識化抗体に対して競合反応させた後固相と液相を分離するか、あるいは、被検液中の抗原と過剰量の標識化抗体とを反応させ、次に固相化抗原を加え未反応の標識化抗体を固相に結合させたのち、固相と液相を分離する。次に、いずれかの相の標識量を測定し被検液中の抗原量を定量する。また、ネフロメトリーでは、ゲル内あるいは溶液中で抗原抗体反応の結果生じた不溶性の沈降物の量を測定する。被検液中の抗原量が僅かであり、少量の沈降物しか得られない場合にもレーザーの散乱を利用するレーザーネフロメトリーなどが好適に用いられる。
これら個々の免疫学的測定法を本発明の定量方法に適用するにあたっては、特別の条件、操作等の設定は必要とされない。それぞれの方法における通常の条件、操作法に当業者の通常の技術的配慮を加えて本発明のタンパク質等の測定系を構築すればよい。これらの一般的な技術手段の詳細については、総説、成書などを参照することができる。例えば、入江 寛編「ラジオイムノアッセイ〕(講談社、昭和49年発行)、入江 寛編「続ラジオイムノアッセイ〕(講談社、昭和54年発行)、石川栄治ら編「酵素免疫測定法」(医学書院、昭和53年発行)、石川栄治ら編「酵素免疫測定法」(第2版)(医学書院、昭和57年発行)、石川栄治ら編「酵素免疫測定法」(第3版)(医学書院、昭和62年発行)、「Methods in ENZYMOLOGY」Vol.70(Immunochemical Techniques(Part A))、 同書 Vol.73(Immunochemical Techniques(Part B))、同書 Vol.74(Immunochemical Techniques(Part C))、同書 Vol.84(Immunochemical Techniques(Part D:Selected Immunoassays))、同書 Vol.92(Immunochemical Techniques(Part E:Monoclonal Antibodies and General Immunoassay Methods))、同書 Vol.121(Immunochemical Techniques(Part I:Hybridoma Technology and Monoclonal Antibodies))(以上、アカデミックプレス社発行)などを参照することができる。以上のようにして、本発明の抗体を用いることによって、本発明のタンパク質等を感度良く定量することができる。さらには、本発明の抗体を用いて本発明のタンパク質等の濃度を定量することによって、本発明のタンパク質等の濃度の増加がヘリコバクターピロリ感染者において検出された場合、例えば、胃炎、胃潰瘍、胃癌、心臓弁膜症、糖尿病、各種癌(例、子宮体癌、子宮内膜腫瘍、乳癌、大腸癌、前立腺癌、肺癌、肝臓癌、膵臓癌、胆嚢癌、腎臓癌、神経芽腫、膀胱癌、黒色腫等)などの疾病である、または将来罹患する可能性が高いと診断することができる。また、本発明の抗体は、体液や組織などの被検体中に存在する本発明のタンパク質等を検出するために使用することができる。また、本発明のタンパク質等を精製するために使用する抗体カラムの作製、精製時の各分画中の本発明のタンパク質等の検出、被検細胞内における本発明のタンパク質の挙動の分析などのために使用することができる。
本発明の抗体を含有する医薬本発明のタンパク質等の活性を中和する作用を有する本発明の抗体(中和抗体)は、例えば、胃炎、胃潰瘍、胃癌、心臓弁膜症、糖尿病、各種癌(例、子宮体癌、子宮内膜腫瘍、乳癌、大腸癌、前立腺癌、肺癌、腎臓癌、神経芽腫、膀胱癌、黒色腫等)などの疾病の治療・予防剤などの医薬として使用することができる。本発明のタンパク質等に対する本発明のヒト化抗体は、例えば、胃炎、胃潰瘍、胃癌、心臓弁膜症、糖尿病、各種癌(例、子宮体癌、子宮内膜腫瘍、乳癌、大腸癌、前立腺癌、肺癌、腎臓癌、神経芽腫、膀胱癌、黒色腫等)などの疾病の治療・予防剤などの医薬として使用することができる。該ヒト化抗体は、Nat Biotechnol,14,845−851.(1996)、Nat Genet.15,146−156.(1997)、PNAS,97(2),722−727(2000)等に記載の方法に準じて作製することができる。以下、「(5)本発明の抗体を含有する医薬」において、本発明の中和抗体およびヒト化抗体を本発明の抗体と総称する。本発明の抗体を含有する上記疾患の治療・予防剤は、そのまま液剤として、または適当な剤型の医薬組成物として、ヒトまたは哺乳動物(例、ラット、ウサギ、ヒツジ、ブタ、ウシ、ネコ、イヌ、サルなど)に対して経口的または非経口的に投与することができる。投与量は、投与対象、対象疾患、症状、投与ルートなどによっても異なるが、例えば、成人の子宮内膜腫瘍患者の治療・予防のために使用する場合には、本発明の抗体を1回量として、通常0.01〜20mg/kg体重程度、好ましくは0.1〜10mg/kg体重程度、さらに好ましくは0.11〜5mg/kg体重程度を、1日1〜5回程度、好ましくは1日1〜3回程度、静脈注射により投与するのが好都合である。他の非経口投与および経口投与の場合もこれに準ずる量を投与することができる。症状が特に重い場合には、その症状に応じて増量してもよい。本発明の抗体は、それ自体または適当な医薬組成物として投与することができる。上記投与に用いられる医薬組成物は、上記またはその塩と薬理学的に許容され得る担体、希釈剤もしくは賦形剤とを含むものである。かかる組成物は、経口または非経口投与に適する剤形として提供される。すなわち、例えば、経口投与のための組成物としては、固体または液体の剤形、具体的には錠剤(糖衣錠、フィルムコーティング錠を含む)、丸剤、顆粒剤、散剤、カプセル剤(ソフトカプセル剤を含む)、シロップ剤、乳剤、懸濁剤などがあげられる。かかる組成物は自体公知の方法によって製造され、製剤分野において通常用いられる担体、希釈剤もしくは賦形剤を含有するものである。例えば、錠剤用の担体、賦形剤としては、乳糖、でんぷん、蔗糖、ステアリン酸マグネシウムなどが用いられる。
後述の配列表の配列番号は、以下の配列を示す。
〔配列番号1〕本発明のヘリコバクターピロリ60190由来タンパク質(M毒素)のアミノ酸配列を示す。
〔配列番号2〕配列番号1で表わされるアミノ酸配列を有する本発明のヘリコバクターピロリ60190由来タンパク質(M毒素)をコードするDNAの塩基配列を示す。
〔配列番号3〕実施例3で用いられたプライマー(合成)DNAの塩基配列を示す。
〔配列番号4〕実施例3で用いられたプライマー(合成)DNAの塩基配列を示す。
後述の実施例3で得られた形質転換体エシェリヒア コリ(Escherichia coli)M toxin/pET30EK/LIC/DH5αは、平成14年10月17日から日本国茨城県つくば市東1丁目1番地1中央第6の独立行政法人産業技術総合研究所(IPOD)特許生物寄託センターに寄託番号FERM BP−8218として寄託されている。また、後述の実施例4で得られたハイブリドーマ(hybridoma)クローンNo.4はBALB−c/P3U1/004−1G9として、平成14年10月23日から日本国茨城県つくば市東1丁目1番地1中央第6の独立行政法人産業技術総合研究所(IPOD)特許生物寄託センターに寄託番号FERM BP−8222として寄託されている。またハイブリドーマ(hybridoma)クローンNo.101はBALB−c/P3U1/101−1C10として、平成14年10月23日から日本国茨城県つくば市東1丁目1番地1中央第6の独立行政法人産業技術総合研究所(IPOD)特許生物寄託センターに寄託番号FERM BP−8223として寄託されている。またハイブリドーマ(hybridoma)クローンNo.116はBALB−c/P3U1/116−5D7として、平成14年10月23日から日本国茨城県つくば市東1丁目1番地1中央第6の独立行政法人産業技術総合研究所(IPOD)特許生物寄託センターに寄託番号FERM BP−8224として寄託されている。
実施例
以下に、実施例をあげて本発明をさらに具体的に説明するが、本発明はそれに限定されるものではない。なお、大腸菌を用いての遺伝子操作法は、モレキュラー・クローニング(Molecular Cloning)に記載されている方法に従った。
実施例1 ヘリコバクターピロリから本発明の毒素を精製抽出する方法
ヘリコバクターピロリはすでに確立されている分離株を入手(例えば、American Type Culture Collectionから入手)するか、または臨床検体から分離培養することができる。本実施例ではヘリコバクターピロリ60190の分離株を用いた。この分離株を、まずBrain Heart Infusion寒天培地(Difco社製)に5%牛血清(Sigma社製)を添加した寒天培地を用いて、温度37℃、湿度90%以上の微好気性条件下(CO25−10%)において2−5継体(約1−2週間)培養した。顕微鏡下で死滅またはココイド化していないことを確認し、良好な増殖を確認した後、Brain Heart Infusion寒天培地(Difco社製)に血清を添加せず5%2,6−ジ−O−メチル−β−シクロデキストリンを添加したものに移植した。前記と同じ条件下で培養と生育状態を確認した後、2,6−ジ−O−メチル−β−シクロデキストリン濃度を漸次2%、1%、0.5%としたものに移植していく。
ついで、0.5%2,6−ジ−O−メチル−β−シクロデキストリン添加のBrain Heart Infusion液体培地にて温度37℃、微好気性条件下、100−120rpmにて約16時間振蘯培養後、10000×g、20分間遠心しペレット状の菌体を得た。これを10mM Tris−HCl pH7.7(以下A緩衝液と呼ぶ。pHは目的タンパク質がpI6.08であるので約pH6.1以上であればよい)の緩衝液中で超音波破砕し、−80℃に一昼夜保存後、再度、超音波破砕したものを、100000×g、60分間超遠心し、三層に分離した最上層部分のみを抽出した。
この抽出液に対して70%硫安で粗精製を行った。これにより得た抽出液を比較的粒子口径の大きなビーズをもってなる陰イオン交換樹脂にてイオン交換クロマトグラフィー(Amersham Pharmacia Biotech ABのDEAE Sephacel)を行った。平衡緩衝液にはA緩衝液、溶出液にはA緩衝液に濃度0.3Mの塩NaClを加えたものを用いた。これらにより濃度勾配抽出を行い、各フラクションの適量を用いて、ヒーラ細胞を植えたウェルに滴下して各ウェル中の細胞の生存率を評価した。評価はWST試薬((株)同仁化学研究所Cell Counting Kit)を用い行った。コントロールと比較して、有意に生存率の少ない数値を示した画分と、比較的蛋白量の増加曲線の一致する画分を、電気泳動の結果とも合わせて評価し、次の精製工程に用いるサンプル画分とした。
次に、次回と分離システムの異なるクロマトグラフィーである、疎水性クロマトグラフィー(Amersham Pharmacia Biotech ABのPhenyl Sepharose CL−4B)を選択した。平衡緩衝液には10mMリン酸緩衝液に1M硫酸アンモニウムを加えたものを用い、溶出緩衝液には10mMリン酸緩衝液に40%エチレングリコールを用いた。濃度勾配溶出を行った後、各サンプルの評価は前記と同様に行った。
さらに、前記工程より抽出されたサンプルを、再び粒子口径の比較的小さなビーズをもってなる陰イオン交換クロマトグラフィー(Amersham Pharmacia Biotech ABのRESOURCE Q)で抽出した。平衡緩衝液にはA緩衝液、溶出緩衝液にはA緩衝液に1Mの塩NaClを加えたものを用いた。これらにより最終的に分子量約41000の単一タンパク質のバンドを得た。なお、クロマトグラフィーの種類と順序は、上述とことなることも可能であり、また、さらに追加することも可能である。
得られた単一のバンドをクーマシーブリリアントブルー染色後、ブロッティング装置でニトロセルロース膜または(ポリビニリデンジフルオリド)膜に転写し、アミノ酸シークエンサーで解析した。その結果、先に記述したように、登録データベース(ヘリコバクターピロリ 22695)の遺伝子座HP1037のN末端アミノ酸配列と95%(20塩基中19塩基)の割合で一致した。(図1)
実施例2 遺伝子工学的調整法によるアミノ酸配列およびDNA配列
本実施例ではヘリコバクターピロリ60190の分離株を用いたが、上述のように、菌株の異なるヘリコバクターピロリ22695の全遺伝子解析がすでにおこなわれており、TIGR(The Institute for Genomic Research)のデータベースを検索することにより、相同する遺伝子座を推定しうる。これによりヘリコバクターピロリ22695の遺伝子座HP1037が相同タンパク質をコードしていることが判明した。
これをもとに本発明の毒素のクローニングを行った。すなわち、ヘリコバクターピロリ60190をテンプレートとして、先ず便宜的に遺伝子座HP1037と、その上流の遺伝子座HP1036および下流の遺伝子座HP1038を基にした適当なプライマーを複数組(5‘側と3’側)作製してシークエンスを行った。DNAポリメラーゼは、校正機能のあるプルーフリーディングのものを使用し、各プライマーの組は十分互いのプライマー部分をも包含するように構成し、5‘側からと3’側から複数回シークエンスが行われるようにした。このようにして得られたDNA配列を、配列表の配列番号2に示した。また、このアミノ酸配列を、配列番号1に示した。
実施例3
遺伝子組換えによる毒素タンパク質の発現実験、
遺伝子組換え実験には大腸菌を用いた。ベクターは、pET−30EK/LICベクター(Novagen社)を、発現用大腸菌はBL21(DE3)を用いた。挿入遺伝子は、実施例2でクローニングしたヘリコバクターピロリ60190由来の毒素タンパク質をコードしているものにsense鎖の5’側にGACGACGACAAGが付加された配列番号3をプライマーとして、またantisense鎖の5’側にはGAGGAGAAGCCCGGTTAが付加された配列番号4をプライマーとしてPCR法により作製した。この作製した挿入遺伝子を25mMdATPと100mM DTTの存在下でT4 DNAポリメラーゼによりベクターのLIC siteに合うように削りこみをおこなったのち、25mM EDTA存在下で加温した。作製された組換え体を再度シーケンスし、配列番号1と同一であることを確認した後、発現用大腸菌BL21(DE3)へ形質転換し、30μg/mlカナマイシンを含むLB培地で培養した。
OD600が約0.4ぐらいになるまで37℃、250rpmで振蘯培養し、イソプロピル−ベータ−チオガラクトシドを終濃度1mMとなるように加え、さらに2時間同様に振蘯する。融合タンパク質は封入体を形成していたため、この培養液から大腸菌を遠心回収し、BugBuster試薬およびBenzonase Nuclease(ともにNovagen社)により当該タンパク質の封入体を得た。本タンパク質をドデシル硫酸ナトリウム−ポリアクリルアミドゲル(SDS−PAGE)電気泳動法で分離し、銀染色により、単一な該当するバンドを確認した後、リフォールディングしヒーラ細胞および他の温血動物細胞を用いて、WST試薬((株)同仁化学研究所Cell Counting Kit)によりコントロールとの比較を行った。その結果、生存率に有意な差を認め、発現タンパク質においても精製タンパク質と同等の活性を認めるに至った。さらにヒト子宮頸癌であるヒーラ細胞だけでなく、正常ヒト胃細胞においても同様な活性をもつことを確認した。(図2)またヒトの他の組織のみならず、哺乳類細胞一般に広範な活性を有することも確認された。(図3、図4)
実施例4
モノクローナル抗M毒素抗体の作製:BALB/Cマウス240μgの免疫原リフォールディング済み発現M毒素を数カ所にわけて2回皮下投与を行なった。最終免疫4日後のマウスから脾臓を摘出し、ステンレスメッシュで圧迫ろ過し、イーグルズ・ミニマム・エッセンシャルメデイウム(MEM)に浮遊させ、膵臓細胞浮遊液を得た。細胞融合に用いる細胞として、BALB/Cマウス由来ミエローマ細胞P3−X63.Ag 8.U1(P3U1)を用いた〔カレントトピックスインマイクロバイオロジーアンドイムノロジー、81、1(1978)〕。細胞融合は、原法〔ネイチャー、256、495(1975)〕に準じて行なった。すなわち、脾臓細胞およびP3U1をそれぞれ血清を含有しないMEMで3度洗浄し、脾臓細胞とP3U1数の比率を6.6:1になるよう混合して、750回転で15分間遠心を行なって細胞を沈澱させた。上清を充分に除去した後、沈殿を軽くほぐし、45%ポリエチレン・グリコール(PEG)6000(和光純薬(株))を0.3ml加え、37℃温水槽中で7分間静置して融合を行なった。融合後細胞に徐々にMEMを添加し、合計15mlのMEMを加えた後750回転15分間遠心して上清を除去した。この細胞沈殿物を10%牛胎児血清を含有するGITメデイウム(和光純薬(株))(GIT−10%FCS)にP3U1が1ml当リ2×105個になるように浮遊し、24穴マルチディッシュ(岩城(株)製)に1ウェル1mlずつ168ウェルに播種した。播種後、細胞を37℃で5%炭酸ガスインキュベーター中で培養した。24時間後HAT(ヒポキサンチン1×10−4M、アミノプテリン4×10−7M、チミジン1.6×10−3M)を含んだGIT−10%FCS培地(HAT培地)を1ウェル当リ1mlずつ添加することにより、HAT選択培養を開始した。HAT選択培養は、培養開始4、7日後に旧液を1ml捨てたあと、1mlのHAT培地を添加することにより継続した。ハイブリドーマの増殖は、細胞融合後9日目で認められ、上清を採取した。培養上清中の抗体価は、以下の要領で測定した。すなわち、抗マウスイムノグロブリン抗体結合マイクロプレートの各ウエルに培養上清100μlおよびバッファーCで200倍に希釈したHRP標識化M毒素100μlを加え4℃で一晩反応させた。該プレートをPBSで洗浄したのち、抗マウスイムノグロブリン抗体結合マイクロプレートを作製するため、まずヤギ抗マウスイムノグロブリン抗体(IgG画分、ダコ社製)を100μg/ml含む0.1M炭酸緩衝液、pH9.6溶液を96ウェルマイクロプレートに100μlずつ分注し、4℃で24時間放置した。次に、プレートをリン酸緩衝生理食塩水(PBS、pH7.4)で洗浄したのち、ウェルの余剰の結合部位をふさぐため25%ブロックエース(雪印乳業社製)および0.1%NaN3を含むPBS、pH7.2を300μlずつ分注し、4℃で少なくとも24時間処理した。上記、抗マウスイムノグロブリン抗体結合マイクロプレートの各ウエルにバッファーEC[0.2%BSA、0.4M NaCl、0.4%ブロックエース、0.05%CHAPS〔3−〔(コラミドプロピル)ジメチルアンモニオ〕プロパンスルホン酸〕、2mM EDTAおよび0.1%NaN3を含む0.02Mリン酸緩衝液、pH7.0]で希釈したマウス抗血清100μlを加え4℃で16時間反応させた。次に、該プレートをPBS、pH7.4で洗浄したのち、HRP標識化TGC−839ペプチド(26−34)100μlを加え室温で7時間反応させた。バッファーC[1%BSA、0.4M NaCl、および2mM EDTAを含む0.02Mリン酸緩衝液、PH7.0]で100倍に希釈した上記実施例3で作製したHRP標識化リフォールディング毒素タンパクを調製した。次に、該プレートをPBS、pH7.4で洗浄したのち、固相上の酵素活性をTMBマイクロウェルパーオキシダーゼ基質システム(KIRKEGAARD & PERRY LAB.フナコシ薬品取り扱い)100μlを加え室温で10分間反応させることにより測定した。反応を1Mリン酸100μlを加え停止させたのち、450nmの吸光度(Abs.450)をプレートリーダー(MTP−120、コロナ社製)で測定した。これらの方法に従い固相上の酵素活性を測定した。その結果、123ウェルの中から抗体価の認められた18ウェルを選択し、ハイブリドーマを凍結保存した。さらに6ウェルのハイブリドーマ、No.4、No.53、No.61、No.76、No.101およびNo.116については、希釈法によるクローニングに付した。クローニングに際しては、フィーダー細胞としてBALB/Cマウスの胸腺細胞をウェル当リ5×105個になるように加えた。クローニング後、培養上清中の抗体価を同様の方法に従って測定した。陽性クローンは、No.4、No.101およびNo.116であった。これらを発現M毒素の抗体産生ハイブリドーマとした。
実施例5
モノクローナル抗体のクラス・サブクラスの決定:
実施例4記載の方法に従い、抗ウサギIgG抗体結合マイクロプレートを作製した。すなわち、ヤギ抗ウサギイムノグロブリン抗体(IgG画分、ダコ社製)を100μg/ml含む0.1M炭酸緩衝液、pH9.6溶液を96ウェルマイクロプレートに100μlずつ分注し、4℃で24時間放置した。次に、プレートをリン酸緩衝生理食塩水(PBS、pH7.4)で洗浄したのち、ウェルの余剰の結合部位をふさぐため25%ブロックエース(雪印乳業社製)および0.1%NaN3を含むPBS、pH7.2を300μlずつ分注し、4℃で少なくとも24時間処理した。次に、抗ウサギIgG抗体結合マイクロプレートに、バッファーEC 50μlおよびバイオラッド社製アイソタイプタイピングキットに含まれるサブタイプ特異的抗体100μlを加え、4℃で1日反応させた。プレートをPBS、pH7.4で洗浄後、上記ハイブリドーマ培養上清を加え、4℃で1日反応させた。プレートをPBS pH7.4で洗浄後、バッファーCで100倍に希釈した上記実施例3で作製したHRP標識化リフォールディング毒素タンパク質100μlを加え室温で6時間反応させた。該プレートをPBS、pH7.4で洗浄したのち、実施例4に記載の方法に従い固相上の酵素活性を測定した。その結果、これらのハイブリドーマが産生するモノクローナル抗体のクラス・サブクラスはNo.4(IgG1)、No.101(IgG2b)、No.116(IgG2a)であった。
実施例6
ハイブリドーマのマウス腹水化:ハイブリドーマ、No.4、No.101およびNo.116についてマウス腹水化を実施した。あらかじめミネラルオイル0.5mlを腹腔内投与されたマウス(BALB/C、雌)に1〜3×106セル/匹の上記ハイブリドーマを腹腔内投与したのち、6〜20日後に抗体含有腹水を採取した。モノクローナル抗体は得られた腹水よリプロテイン−Aカラムによリ精製した。即ち、腹水約25mlを等量の結合緩衝液(3.5M NaCl、0.05%NaN3を含む1.5Mグリシン、pH9.0)で希釈したのち、あらかじめ結合緩衝液で平衡化したリコンビナントプロテイン−A−アガロース(Repligen社製)カラムに供し、特異抗体を溶離緩衝液(0.05%NaN3を含む0.1Mクエン酸緩衝液、pH3.0)で溶出した。溶出液はPBS、pH7.4に対して4℃、2日間透析したのち、0.22μmのフィルター(ミリポア社製)により除菌濾過し4℃あるいは−80℃で保存した。
実施例7
ポリクローナル抗M毒素抗体の作製
本発明の細胞障害タンパク質M毒素4.1mgをフロイント完全アジュバントと混合してウサギに皮下免疫し、1週間後さらに同量をフロイント不完全アジュバントと混合して皮下免疫した。免疫後、採血した血液は遠心によって血球成分を除去し、抗血清を得た。
実施例8 M毒素のWestern Blottingによる解析:
実施例3で得た培養上清に、2−メルカプトエタノールを含むSDS−Sample Bufferを加えてPeptide−PAGE(TEFCO)で電気泳動し、これをPVDF膜(Amersham)に電気的に移した。一次抗体として、実施例4、実施例6で得た各抗体(2μg/ml)を用い、二次抗体にはHRP(Horseradish peroxidase)標識抗ウサギおよび抗マウスIgG抗体(2000倍希釈;Dako)を用いた。発色はECL Western Blot Detection System(Amersham)を用いて行なった。その結果、各1次抗体は該発現タンパク質を認識することを確認した。(図5)
実施例9
活性炭(径0.2〜0.1mm)、CMセルロース、アルギン酸カルシウムをそれぞれ0.5ml体積ずつカラムに充填し、トリス緩衝液10mM pH7.7で平衡化後、0.5mlのリフォールディングした活性を有するM毒素400nMをそれぞれのカラムに添加した状態でカラムを閉栓し、25℃、60分間静置。その間、トリス緩衝液のみと、トリス緩衝液に同様のM毒素を含有したものを、同条件で静置した。その後、すべてのカラムを開栓して、100μlづつ滴下したものを分取し、さらにトリス緩衝液を各カラムに0.5mlづつ添加して100μlづつ分取した。赤血球は健常成人の全血を上清が透明になるまで2−3回、800×g、10分間遠心し、沈殿した赤血球10μl体積を10mMトリス緩衝液990μlに添加したものを陽性コントロールとし、同じく10μlを0.9%食塩10mMトリス緩衝液に添加したものを陰性コントロールとし、上記のカラムより分取されたサンプルに赤血球を100分の1体積くわえたものと比較した。比較はマルチプルプレートリーダー(Biorad)で溶出したヘモグロビン相対濃度を吸光度415nmにより計測することによりおこなった。(図6)
実施例10
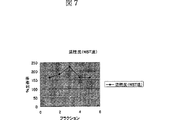
実施例9でえられた各カラムからの分画にヒーラ細胞(ヒト子宮頚癌細胞)が曝され、細胞生存率をテトラゾリウム塩を用いた測定法のひとつであるWST法により測定した。ヒーラ細胞は96穴プレートに24時間、一穴当たり10000個づつ培養する。培養液のみの陰性コントロールと各被検液、および20nMの濃度をふくむ陽性コントロールのそれぞれの各穴に加え、を37℃、12時間培養する。その後、Cell Counting Kit(株式会社同仁研究所)を用いて、WST法により検出される細胞生存率を415nm波長の吸光度で計測した。(図7、図8)
産業上の利用の可能性
本発明のタンパク質またはその部分ペプチドなどは、例えば、癌の治療剤として使用することができる。また本発明の抗体は、被検患者から採取の血液、組織、尿、便中の本発明タンパク質の同定ならびにヘリコバクターピロリによる感染証明に換えることができる。また本発明のタンパク質の定量などに使用することができる。さらに、本発明のタンパク質は、本発明のタンパク質の活性を促進または阻害する化合物をスクリーニングするための試薬として有用である。
【配列表】
【図面の簡単な説明】
図1は、実施例1において得られたサンプルの陰イオンクロマトグラフィーの結果を示す。aは各分画におけるM毒素の活性と、その溶出蛋白質の吸光度である。
bはaのクロマトグラフィー中のフラクション16からフラクション22の銀染色によるSDS−PAGEである。cはエレクトロブロッティングによりPVDF膜に転写した蛋白毒素のバンドである。d、eはコントロールと1nMの抽出された細胞毒液の24時間後のヒーラ細胞の形質変化を示す。スケールは50μmである。
図2は、実施例3において得られた遺伝子組換え体毒素による細胞形態変化を示す。aはヒーラ細胞の陰性コントロールによる6時間後。b、cは組換え体M毒素5nM添加3時間後、6時間後のヒーラ細胞。dは陰性コントロールの6時間後のCRL7407(ATCC)胎児正常胃細胞。e、fは組換え体M毒素5nM添加3時間後、6時間後のCRL7407細胞。
図3は、実施例3における各種癌細胞のM毒素に対する感受性を示す。WST法を用いて計測した。X軸はM毒素の基質中の濃度、Y軸は波長415nm光による吸光度を直接、あるいは陰性コントロールを100%とした場合の相体割合で示す。HLF:ラット肝癌、colon26:マウス大腸癌を示す。
図4は図3と同様に、T24:ヒト膀胱癌、OVK18:ヒト卵巣癌、KLM−1:ヒト膵癌、A−549:ヒト肺癌、Ca9−22:ヒト歯肉癌、CRL1500:ヒト乳癌を示す。
図5は実施例8で行われたモノクローナル抗体のウェスタンブロッティングを示す。全てハイブリドーマ細胞の培養上清の希釈倍率は20倍である。
図6は実施例9において、吸着剤としてアルギン酸カルシウムを用いた場合のM毒素活性を示す。陰性コントロールは基質として10mMトリスpH7.7のみ、陽性コントロールは基質とM毒素10mMを含む。X軸はアルギン酸カルシウムカラムを通過する各フラクションである。各フラクションのM毒素濃度は平均10nMであり、いずれか1つは少なくとも10nMを超える。赤血球の破壊が起こると溶液中のヘモグロビン濃度が上昇し、Y軸においてその415nm吸光度が示される。
図7は実施例10で得られた吸着作用によるM毒素阻害活性を示す活性炭のヒーラ細胞における%生存率を示す。X軸は各フラクションの溶出液を示し、M毒素濃度は平均10nMであり、いずれか1つは少なくとも10nMを超える。Y軸は各フラクションの溶液の毒性をWST法で計測したものを陽性コントロールで除したものの100分率である。
図8は図7と同様に、実施例10で得られた吸着作用によるヒーラ細胞におけるM毒素阻害活性を示すアルギン酸カルシウムおよびCM−セルロースの%生存率を示す。
Claims (12)
- 配列番号1で表されるアミノ酸配列を有するタンパク質からなることを特徴とする細胞障害タンパク質。
- ヘリコバクターピロリで産生される請求項1記載の細胞障害タンパク質。
- 請求項1記載の細胞障害タンパク質をコードする配列番号2のDNAを含有する組換えベクターで形質転換された形質転換体を培養し、この培養体から細胞障害タンパク質を生成させることを特徴とする請求項1記載の細胞障害タンパク質。
- 形質転換体が独立行政法人産業技術総合研究所(IPOD)に寄託番号FERM BP-8218で寄託されている請求項3記載の細胞障害タンパク質。
- 請求項1記載の細胞障害タンパク質をヒトを除く哺乳類に免疫して得られる細胞障害タンパク質に特異的なモノクローナル抗体。
- 寄託番号FERM BP-8222のハイブリドーマクローンを用いて産生される請求項5記載のモノクローナル抗体。
- 寄託番号FERM BP-8223のハイブリドーマクローンを用いて産生される請求項5記載のモノクローナル抗体。
- 寄託番号FERM BP-8224のハイブリドーマクローンを用いて産生される請求項5記載のモノクローナル抗体。
- 請求項1記載の細胞障害タンパク質をヒトを除く哺乳類に免疫して得られる細胞障害タンパク質に特異的なポリクローナル抗体。
- 請求項5から9のいずれか1項に記載のモノクローナル抗体またはポリクローナル抗体を用いる請求項1記載の細胞障害タンパク質を検出する方法。
- 請求項1記載のタンパク質を用いることを特徴とする、請求項1記載のタンパク質の活性を阻害する化合物について、温血動物細胞を用いて陰性または陽性対照群との比較で、細胞増殖阻害活性、細胞障害活性あるいは細胞死により当該化合物をスクリーニングする方法。
- 請求項1記載のタンパク質を含有してなる、請求項1記載の細胞障害タンパク質の活性を阻害する化合物またはその塩のスクリーニング用キット。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003549386A JP4776166B2 (ja) | 2001-12-05 | 2002-12-05 | 細胞障害タンパク質及びその利用 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2001371210 | 2001-12-05 | ||
| JP2001371210 | 2001-12-05 | ||
| JP2003549386A JP4776166B2 (ja) | 2001-12-05 | 2002-12-05 | 細胞障害タンパク質及びその利用 |
| PCT/JP2002/012752 WO2003048199A1 (fr) | 2001-12-05 | 2002-12-05 | Proteine cytotoxique et son utilisation |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2003048199A1 JPWO2003048199A1 (ja) | 2005-04-14 |
| JP4776166B2 true JP4776166B2 (ja) | 2011-09-21 |
Family
ID=19180288
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003549386A Expired - Fee Related JP4776166B2 (ja) | 2001-12-05 | 2002-12-05 | 細胞障害タンパク質及びその利用 |
Country Status (25)
| Country | Link |
|---|---|
| US (3) | US7385035B2 (ja) |
| EP (1) | EP1462457B1 (ja) |
| JP (1) | JP4776166B2 (ja) |
| KR (1) | KR100628917B1 (ja) |
| CN (1) | CN1599750B (ja) |
| AT (1) | ATE393164T1 (ja) |
| AU (1) | AU2002354096B2 (ja) |
| BR (1) | BR0215114A (ja) |
| CA (1) | CA2469154C (ja) |
| CO (1) | CO5590932A2 (ja) |
| DE (1) | DE60226277T2 (ja) |
| ES (1) | ES2305323T3 (ja) |
| HR (1) | HRP20040442A2 (ja) |
| IL (1) | IL162320A0 (ja) |
| IS (1) | IS7270A (ja) |
| MA (1) | MA27504A1 (ja) |
| MX (1) | MXPA04005459A (ja) |
| NO (1) | NO20042130L (ja) |
| NZ (1) | NZ533797A (ja) |
| PL (1) | PL370704A1 (ja) |
| RS (1) | RS49804A (ja) |
| RU (1) | RU2004117155A (ja) |
| TW (1) | TW200303919A (ja) |
| WO (1) | WO2003048199A1 (ja) |
| ZA (1) | ZA200404209B (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004357586A (ja) * | 2003-06-04 | 2004-12-24 | Hiroyuki Ono | 細胞障害タンパク質m毒素の発現方法 |
| WO2007072576A1 (ja) * | 2005-12-21 | 2007-06-28 | Fourier Inc. | ヘリコバクターピロリ由来m毒素大量発現株の製造方法 |
| US8151835B2 (en) * | 2006-08-23 | 2012-04-10 | Fht, Inc. | Automated drug delivery bag filling system |
| CN113567671A (zh) * | 2020-04-29 | 2021-10-29 | 南京农业大学 | 猪血管紧张素转化酶2(ace2)多克隆抗体的制备 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0218158A3 (en) | 1985-09-30 | 1988-12-07 | Asahi Kasei Kogyo Kabushiki Kaisha | Human monoclonal antibody, B-cell line for producing this antibody and method for preparing this B-cell line and antibody. |
| EP0232871A3 (en) | 1986-02-07 | 1989-03-15 | Yoshitomi Pharmaceutical Industries, Ltd. | Human monoclonal antibody, hybridoma producing the same and its use |
| JPH0798000B2 (ja) | 1987-05-23 | 1995-10-25 | 萩原 義秀 | ガン関連抗原特異的ヒト免疫グロブリン |
| US5366865A (en) | 1989-04-06 | 1994-11-22 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Anti-platelet monoclonal antibody |
| US6787153B1 (en) | 1991-06-28 | 2004-09-07 | Mitsubishi Chemical Corporation | Human monoclonal antibody specifically binding to surface antigen of cancer cell membrane |
| US5776427A (en) | 1992-03-05 | 1998-07-07 | Board Of Regents, The University Of Texas System | Methods for targeting the vasculature of solid tumors |
| US6004555A (en) | 1992-03-05 | 1999-12-21 | Board Of Regents, The University Of Texas System | Methods for the specific coagulation of vasculature |
| US5965132A (en) | 1992-03-05 | 1999-10-12 | Board Of Regents, The University Of Texas System | Methods and compositions for targeting the vasculature of solid tumors |
| US6093399A (en) | 1992-03-05 | 2000-07-25 | Board Of Regents, The University Of Texas System | Methods and compositions for the specific coagulation of vasculature |
| US5877289A (en) | 1992-03-05 | 1999-03-02 | The Scripps Research Institute | Tissue factor compositions and ligands for the specific coagulation of vasculature |
| IL125808A0 (en) * | 1996-03-29 | 1999-04-11 | Astra Ab | Nucleic acid and amino acid sequences relating to helicobacter pylori and vaccine compositions thereof |
| US6348581B1 (en) | 1996-10-31 | 2002-02-19 | The Dow Chemical Company | High affinity humanized anti-TAG-72 monoclonalantibodies |
| US6417337B1 (en) | 1996-10-31 | 2002-07-09 | The Dow Chemical Company | High affinity humanized anti-CEA monoclonal antibodies |
| DE69814122T2 (de) * | 1997-10-09 | 2004-03-18 | Dexcel Pharma Technologies Ltd. | Darreichungsform zur verzögerten, vollständigen wirkstoffabgabe im verdauungstrakt |
| JP2000063280A (ja) * | 1998-06-11 | 2000-02-29 | Takeda Chem Ind Ltd | 抗ヘリコバクタ―・ピロリ活性胃腸薬 |
| EP1131106B1 (en) | 1998-11-12 | 2009-06-24 | Novolytics Inc. | Compositions and methods for producing vascular occlusion |
| US20020061569A1 (en) * | 2000-03-21 | 2002-05-23 | Robert Haselbeck | Identification of essential genes in prokaryotes |
-
2002
- 2002-12-04 TW TW091135199A patent/TW200303919A/zh unknown
- 2002-12-05 BR BR0215114-6A patent/BR0215114A/pt not_active IP Right Cessation
- 2002-12-05 JP JP2003549386A patent/JP4776166B2/ja not_active Expired - Fee Related
- 2002-12-05 US US10/496,384 patent/US7385035B2/en not_active Expired - Fee Related
- 2002-12-05 HR HRP20040442 patent/HRP20040442A2/hr not_active Application Discontinuation
- 2002-12-05 RU RU2004117155/13A patent/RU2004117155A/ru not_active Application Discontinuation
- 2002-12-05 CN CN02824401XA patent/CN1599750B/zh not_active Expired - Fee Related
- 2002-12-05 WO PCT/JP2002/012752 patent/WO2003048199A1/ja not_active Ceased
- 2002-12-05 ES ES02786035T patent/ES2305323T3/es not_active Expired - Lifetime
- 2002-12-05 KR KR1020047008649A patent/KR100628917B1/ko not_active Expired - Fee Related
- 2002-12-05 CA CA2469154A patent/CA2469154C/en not_active Expired - Fee Related
- 2002-12-05 EP EP02786035A patent/EP1462457B1/en not_active Expired - Lifetime
- 2002-12-05 DE DE60226277T patent/DE60226277T2/de not_active Expired - Lifetime
- 2002-12-05 PL PL02370704A patent/PL370704A1/xx not_active Application Discontinuation
- 2002-12-05 AT AT02786035T patent/ATE393164T1/de not_active IP Right Cessation
- 2002-12-05 MX MXPA04005459A patent/MXPA04005459A/es active IP Right Grant
- 2002-12-05 AU AU2002354096A patent/AU2002354096B2/en not_active Ceased
- 2002-12-05 RS YU49804A patent/RS49804A/sr unknown
- 2002-12-05 NZ NZ533797A patent/NZ533797A/en unknown
- 2002-12-05 IL IL16232002A patent/IL162320A0/xx unknown
-
2004
- 2004-05-17 IS IS7270A patent/IS7270A/is unknown
- 2004-05-24 NO NO20042130A patent/NO20042130L/no not_active Application Discontinuation
- 2004-05-28 ZA ZA200404209A patent/ZA200404209B/en unknown
- 2004-07-01 CO CO04062951A patent/CO5590932A2/es not_active Application Discontinuation
- 2004-07-05 MA MA27761A patent/MA27504A1/fr unknown
-
2008
- 2008-04-21 US US12/106,775 patent/US20090208972A1/en not_active Abandoned
- 2008-04-21 US US12/106,806 patent/US20080233556A1/en not_active Abandoned
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JPWO2008018472A1 (ja) | 新規モノクローナル抗体およびその用途 | |
| US20090208972A1 (en) | Cytotoxic protein and utlization thereof | |
| KR20070042994A (ko) | 항시노비올린 항체 | |
| JP3472854B2 (ja) | 新規タンパク質およびその用途 | |
| JP4965776B2 (ja) | 新規生理活性ペプチドおよびその用途 | |
| JP4676608B2 (ja) | 新規タヒキニン様ポリペプチドおよびその用途 | |
| JP2001103980A (ja) | 新規タンパク質およびその用途 | |
| JP2002223762A (ja) | 新規タンパク質およびそのdna | |
| WO2000055197A1 (fr) | Nouvelles proteines et leurs utilisations | |
| JP2002233369A (ja) | 新規タンパク質およびそのdna | |
| JPWO2000055197A1 (ja) | 新規タンパク質およびその用途 | |
| JP2002233372A (ja) | 新規タンパク質およびそのdna | |
| JP2005120082A (ja) | 新規タンパク質複合体およびその用途 | |
| JP2002223763A (ja) | 新規タンパク質およびそのdna | |
| JP2002218985A (ja) | 新規タンパク質およびそのdna | |
| JP2002360284A (ja) | 新規タンパク質およびその用途 | |
| JP2002223759A (ja) | 新規タンパク質およびそのdna | |
| JP2002223774A (ja) | 新規タンパク質およびそのdna | |
| JP2003000266A (ja) | 新規タンパク質およびそのdna | |
| JP2002233375A (ja) | 新規タンパク質およびそのdna | |
| JP2002233368A (ja) | 新規タンパク質およびそのdna | |
| JP2002233377A (ja) | 新規タンパク質およびそのdna | |
| JP2002335964A (ja) | 新規タンパク質およびその用途 | |
| JP2002233373A (ja) | 新規タンパク質およびそのdna |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050307 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20070703 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070831 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20070903 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20071106 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080107 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101111 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101215 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110628 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140708 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |