JP4757804B2 - 新規カルボニル還元酵素、その遺伝子、およびその利用法 - Google Patents
新規カルボニル還元酵素、その遺伝子、およびその利用法 Download PDFInfo
- Publication number
- JP4757804B2 JP4757804B2 JP2006543049A JP2006543049A JP4757804B2 JP 4757804 B2 JP4757804 B2 JP 4757804B2 JP 2006543049 A JP2006543049 A JP 2006543049A JP 2006543049 A JP2006543049 A JP 2006543049A JP 4757804 B2 JP4757804 B2 JP 4757804B2
- Authority
- JP
- Japan
- Prior art keywords
- polypeptide
- represented
- dna
- phenylpropanenitrile
- transformant
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 CC(C)(C)OC(CC(C[C@](*)COC(c1ccccc1)=O)=O)=O Chemical compound CC(C)(C)OC(CC(C[C@](*)COC(c1ccccc1)=O)=O)=O 0.000 description 1
- ZAJNMXDBJKCCAT-YFKPBYRVSA-N CCOC(C[C@@H](CCl)O)=O Chemical compound CCOC(C[C@@H](CCl)O)=O ZAJNMXDBJKCCAT-YFKPBYRVSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/0004—Oxidoreductases (1.)
- C12N9/0006—Oxidoreductases (1.) acting on CH-OH groups as donors (1.1)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P13/00—Preparation of nitrogen-containing organic compounds
- C12P13/002—Nitriles (-CN)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P41/00—Processes using enzymes or microorganisms to separate optical isomers from a racemic mixture
- C12P41/002—Processes using enzymes or microorganisms to separate optical isomers from a racemic mixture by oxidation/reduction reactions
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/02—Preparation of oxygen-containing organic compounds containing a hydroxy group
- C12P7/04—Preparation of oxygen-containing organic compounds containing a hydroxy group acyclic
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/62—Carboxylic acid esters
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Analytical Chemistry (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Enzymes And Modification Thereof (AREA)
Description
Bulletin of the Korean Chemical Society, 23, 1693 (2002) Advanced Synthesis & Catalysis, 344, 947 (2002) Organic Letters, 5, 3147 (2003) Tetrahedron:Asymmetry, 3, 677 (1992) Tetrahedron:Asymmetry, 11, 3693 (2000) Organic Letters, 1, 1879 (1999)
本明細書において記述されている、DNAの単離、ベクターの調製、形質転換等の遺伝子操作は、特に明記しない限り、Molecular Cloning 2nd Edition(Cold Spring Harbor Laboratory Press,1989)等の成書に記載されている方法により実施できる。また、本明細書の記述に用いられる%は、特に断りのない限り、%(w/v)を意味する。
本発明のポリペプチドは、3−オキソ−3−フェニルプロパンニトリルを不斉的に還元し、(R)−3−ヒドロキシ−3−フェニルプロパンニトリルを生成する活性を有するポリペプチドである。このようなポリペプチドは、当該活性を有する微生物から単離することができる。本発明のポリペプチドの起源となる微生物は、特に限定されないが、例えばキャンディダ(Candida)属に属する酵母が挙げられ、特に好ましいものとしてはキャンディダ・マグノリエ(Candida magnoliae)NBRC0661株を挙げることができる。当該微生物は、独立行政法人製品評価技術基盤機構バイオテクノロジー本部 生物遺伝資源部門(NBRC:〒292-0818 千葉県木更津市かずさ鎌足2-5-8)より入手することができる。
本発明のポリペプチドの起源となる微生物からの該ポリペプチドの単離は、通常公知の蛋白質精製法を適当に組み合わせて用いることにより実施できる。例えば、以下のように実施できる。まず、当該微生物を適当な培地で培養し、培養液から遠心分離、あるいは、濾過により菌体を集める。得られた菌体を、超音波破砕機、あるいは、グラスビーズ等を用いた物理的手法で破砕した後、遠心分離にて菌体残さを除き、無細胞抽出液を得る。そして、塩析(硫酸アンモニウム沈殿、リン酸ナトリウム沈殿など)、溶媒沈殿(アセトンまたはエタノールなどによる蛋白質分画沈殿法)、透析、ゲル濾過クロマトグラフィー、イオン交換クロマトグラフィー、逆相クロマトグラフィー、限外濾過等の手法を単独で、または組み合わせて用いることにより、該無細胞抽出液から本発明のポリペプチドを単離する。
3−オキソ−3−フェニルプロパンニトリルを還元する活性は、例えば、0.33%(v/v)のジメチルスルホキシドを含む100mMリン酸緩衝液(pH6.5)に、0.5mMの基質3−オキソ−3−フェニルプロパンニトリル、0.25mMの補酵素NADPH、および粗酵素を添加し、30℃で1分間反応させた際の、波長340nmにおける吸光度の減少速度から算出できる。
本発明のDNAは、上述の本発明のポリペプチドをコードするDNAであり、後述する方法に従って導入された宿主細胞内で該ポリペプチドを発現し得るものであればいかなるものでもよく、任意の非翻訳領域を含んでいてもよい。該ポリペプチドが取得できれば、該ポリペプチドの起源となる微生物より、当業者であれば公知の方法で、このようなDNAを取得できる。例えば、以下に示した方法で取得できる。
本発明のポリペプチドの例としては、配列表の配列番号1に示す塩基配列によってコードされる、配列表の配列番号2に示すアミノ酸配列からなるポリペプチドを挙げることができる。
本発明のDNAを宿主微生物内に導入し、導入された宿主微生物内で発現させるために用いられるベクターは、適当な宿主微生物内で当該DNAがコードする遺伝子を発現できるものであれば、特に限定されない。このようなベクターとしては、例えば、プラスミドベクター、ファージベクター、コスミドベクターなどが挙げられ、さらに、他の宿主株との間での遺伝子交換が可能なシャトルベクターも使用できる。
本発明のポリペプチド、カルボニル基を有する化合物、および、NADPH等の補酵素を接触せしめ、反応させることにより、当該カルボニル基を有する化合物を不斉的に還元し、光学活性アルコール類を製造することができる。この時、当該反応の進行に伴い、NADPH等の補酵素は酸化型に変換される。しかし、この酸化型の補酵素を還元型に変換する能力(以後、補酵素再生能と呼ぶ)を有するポリペプチド、および、当該ポリペプチドの基質となる化合物を、本発明のポリペプチドと共存させて当該反応を行うことにより、高価な補酵素の使用量を大幅に削減できる。補酵素再生能を有するポリペプチドとしては、例えば、ヒドロゲナーゼ、ギ酸脱水素酵素、アルコール脱水素酵素、アルデヒド脱水素酵素、グルコース−6−リン酸脱水素酵素およびグルコース脱水素酵素などを使用できる。好適には、グルコース脱水素酵素が使用される。
本発明のポリペプチドのかわりに、該ポリペプチドをコードするDNAを含む形質転換体を使用しても、同様に光学活性アルコール類を製造することができる。また、本発明のポリペプチドをコードするDNA、および、補酵素再生能を有するポリペプチドをコードするDNAの両者を含む形質転換体を使用しても、同様に光学活性アルコール類を製造することができる。とりわけ、本発明のポリペプチドをコードするDNA、および、補酵素再生能を有するポリペプチドをコードするDNAの両者を含む形質転換体を使用した場合には、補酵素を再生するための酵素を別途調製・添加する必要がなく、光学活性アルコール類の製造をより効率良く行うことができる。
本発明のポリペプチド、又は、該ポリペプチドをコードするDNAを含む形質転換体のいずれかを用いた光学活性アルコール類の製造は、適当な溶媒中に、基質となるカルボニル基を有する化合物、NADPH等の補酵素、及び、本発明のポリペプチド又は該ポリペプチドをコードするDNAを含む形質転換体を添加し、pH調整下、攪拌することにより実施できる。
基質となるカルボニル基を有する化合物としては、例えば、下記式(1):
反応で生じた光学活性アルコール類は、常法により精製できる。例えば、反応で生じた光学活性アルコール類を含む反応液を、酢酸エチル、トルエン等の有機溶媒で抽出し、有機溶媒を減圧下で留去した後、蒸留、再結晶、または、クロマトグラフィー等の処理を行うことにより、精製できる。
Molecular Cloning 2nd Edition(Cold Spring Harbor Laboratory Press,1989)、
Current Protocols in Molecular Biology(Greene Publishing Associates and Wiley-Interscience)。
以下の方法に従って、キャンディダ・マグノリエ(Candida magnoliae)NBRC0661株より、3−オキソ−3−フェニルプロパンニトリルを不斉的に還元して(R)−3−ヒドロキシ−3−フェニルプロパンニトリルを生成する活性を有するポリペプチドを分離し、単一に精製した。特に断りのない限り、精製操作は4℃で行った。
30Lジャーファーメンター(丸菱バイオエンジ社製)に、グルコース4%、イーストエキス0.3%、リン酸ニ水素カリウム0.7%、リン酸水素ニアンモニウム1.3%、塩化ナトリウム0.1%、硫酸マグネシウム・七水和物0.08%、硫酸亜鉛・七水和物0.006%、硫酸第一鉄・七水和物0.009%、硫酸銅・五水和物0.0005%、硫酸マンガン・四〜六水和物0.001%、アデカノールLG−109(日本油脂株式会社製)0.01%からなる液体培地18Lを調製し、120℃で20分間蒸気殺菌をおこなった。
この培地に、予め同培地にて前培養しておいたキャンディダ・マグノリエ(Candida magnoliae)NBRC0661株の培養液を180ml接種し、攪拌回転数250rpm、通気量5.0NL/min、30℃で、30%(w/w)水酸化ナトリウム水溶液の滴下により下限pHを5.5に調整しながら培養した。培養開始から18時間後、22時間後、26時間後にそれぞれ55%(w/w)グルコース水溶液655gを添加し、30時間培養を行った。
上記の培養液から遠心分離により菌体を集め、0.8%塩化ナトリウム水溶液を用いて菌体を洗浄した。この菌体を、5mMのβ−メルカプトエタノールおよび0.1mMのフッ化フェニルメタンスルホニルを含む100mMリン酸緩衝液(pH7.0)に懸濁し、ダイノミル( Willy A. Bachofen社製)で破砕した後、破砕物から遠心分離にて菌体残渣を除き、無細胞抽出液1900mlを得た。
上記で得た無細胞抽出液に、5%硫酸プロタミン水溶液を100ml添加し、1夜攪拌後、遠心分離により沈殿を除去した。
上記で得た核酸除去後の粗酵素液のpHを、アンモニア水を用いて7.0に調整した後、同pHを維持しながら、50%飽和となるように硫酸アンモニウムを添加・溶解し、生じた沈殿を遠心分離により除いた。先と同様にpH7.0を維持しながら、この遠心上清に60%飽和となるよう、さらに硫酸アンモニウムを添加・溶解し、生じた沈殿を遠心分離により集めた。この沈殿を10mMリン酸緩衝液(pH7.0)に溶解した後、同一緩衝液で1夜透析し、活性画分を得た。
硫酸アンモニウム分画により得られた活性画分を、10mMリン酸緩衝液(pH7.0)で予め平衡化したDEAE−TOYOPEARL 650M(東ソー株式会社製)カラム(400ml)に供し、活性画分を吸着させた。同一緩衝液でカラムを洗浄した後、NaClのリニアグラジエント(0Mから0.5Mまで)により活性画分を溶出させた。活性画分を集め、10mMリン酸緩衝液(pH7.0)にて1夜透析を行った。
DEAE−TOYOPEARLカラムクロマトグラフィーにより得られた活性画分を、10mMリン酸緩衝液(pH7.0)で予め平衡化したBlue sepharose CL−6B(アマシャムバイオサイエンス株式会社製)カラム(50ml)に供し、活性画分を吸着させた。同一緩衝液でカラムを洗浄した後、NaClのリニアグラジエント(0Mから1Mまで)により活性画分を溶出させた。活性画分を集め、10mMリン酸緩衝液(pH7.0)にて1夜透析を行った。
Blue sepharoseカラムクロマトグラフィーにより得られた活性画分を、10mMリン酸緩衝液(pH7.0)で予め平衡化した2’,5’−ADP sepharose(アマシャムバイオサイエンス株式会社製)カラム(20ml)に供し、活性画分を吸着させた。同一緩衝液でカラムを洗浄した後、NaClのリニアグラジエント(0Mから1Mまで)により活性画分を溶出させた。活性画分を集め、10mMリン酸緩衝液(pH7.0)にて1夜透析を行った。
2’,5’−ADP sepharoseカラムクロマトグラフィーにより得られた活性画分に、終濃度が35%となるよう硫酸アンモニウムを溶解し、35%の硫酸アンモニウムを含む10mMリン酸緩衝液(pH7.0)にて予め平衡化したHiTrap Phenyl HPカラム(アマシャムバイオサイエンス株式会社製)に供し、活性画分を吸着させた。同一緩衝液でカラムを洗浄した後、硫酸アンモニウムのリニアグラジエント(35%から0%まで)により活性画分を溶出させた。活性画分を集め、10mMリン酸緩衝液(pH7.0)にて1夜透析を行い、ポリペプチドの精製標品を得た。
(PCRプライマーの作成)
実施例1で得られた精製ポリペプチドを8M尿素存在下で変性した後、アクロモバクター由来のリシルエンドペプチダーゼ(和光純薬工業株式会社製)で消化し、得られたペプチド断片のアミノ酸配列をABI492型プロテインシーケンサー(パーキンエルマー社製)により決定した。このアミノ酸配列から予想されるDNA配列に基づき、該ポリペプチドをコードする遺伝子の一部をPCRにより増幅するためのプライマー1:5’−cargarcaytaygtntggcc−3’(配列表の配列番号3)、および、プライマー2:5’−atygcrtcnggrtadatcca−3’(配列表の配列番号4)を合成した。
実施例1と同様に培養したキャンディダ・マグノリエ(Candida magnoliae)NBRC0661株の菌体からVisser等の方法(Appl. Microbiol. Biotechnol., 53, 415 (2000))に従って染色体DNAを抽出した。次に、上記で調製したDNAプライマー1および2を用い、得られた染色体DNAを鋳型としてPCRを行ったところ、目的遺伝子の一部と考えられる約0.5kbpのDNA断片が増幅された。PCRは、DNAポリメラ−ゼとしてTaKaRa Ex Taq(タカラバイオ社製)を用いて行い、反応条件はその取り扱い説明書に従った。このDNA断片を、プラスミドpT7Blue T−Vector(Novagen社製)にクローニングし、ABI PRISM Dye Terminator Cycle Sequencing Ready Reaction Kit(Perkin Elmer社製)およびABI 373A DNA Sequencer(Perkin Elmer社製)を用いてその塩基配列を解析した。その結果判明した塩基配列を、配列表の配列番号5に示した。
上記で調製したキャンディダ・マグノリエ(Candida magnoliae)NBRC0661株の染色体DNAを、制限酵素PstIで完全消化し、得られたDNA断片の混合物をT4リガーゼにより分子内環化させた。これを鋳型として用い、i−PCR法(Nucl. Acids Res., 16, 8186 (1988))により、上述の配列番号5に示す塩基配列を含む遺伝子の全塩基配列を決定した。その結果を配列表の配列番号1に示した。i−PCRは、DNAポリメラ−ゼとしてTaKaRa LA Taq(タカラバイオ社製)を用いて行い、反応条件はその取り扱い説明書に従った。また、配列番号1に示した塩基配列がコードするアミノ酸配列を配列番号2に示した。
プライマー3:5’−gtgcatatgtcttctcttcacgctcttg−3’(配列表の配列番号6)と、プライマー4:5’−ggcgaattcttattaaacggtagagccattgtcg−3’(配列表の配列番号7)を用い、実施例2で得たキャンディダ・マグノリエ(Candida magnoliae)NBRC0661株の染色体DNAを鋳型としてPCRを行った。その結果、配列表の配列番号1
に示す塩基配列からなる遺伝子の開始コドン部分にNdeI認識部位が付加され、かつ終始コドンの直後にEcoRI認識部位が付加された二本鎖DNAを得た。PCRは、DNAポリメラ−ゼとしてTaKaRa LA Taq(タカラバイオ社製)を用いて行い、反応条件はその取り扱い説明書に従った。このDNAをNdeI及びEcoRIで消化し、プラスミドpUCNT(国際公開第WO94/03613号公報)のlacプロモーターの下流のNdeI認識部位とEcoRI認識部位の間に挿入し、組換えベクターpNTCMを構築した。
プライマー5:5’−gccgaattctaaggaggttaacaatgtataaa−3’(配列表の配列番号8)と、プライマー6:3’−gcggtcgacttatccgcgtcctgcttgg−5’(配列表の配列番号9)を用い、プラスミドpGDK1(Eur. J. Biochem., 186, 389 (1989))を鋳型としてPCRを行い、バシラス・メガテリウム(Bacillus megaterium)IAM1030株由来のグルコース脱水素酵素(以後、GDHと呼ぶ)遺伝子の開始コドンから5塩基上流に大腸菌のリボゾーム結合配列が、さらにその直前にEcoRI切断点が付加され、かつ、終止コドンの直後にSalI切断点が付加された、二本鎖DNAを取得した。得られたDNA断片をEcoRIおよびSalIで消化し、プラスミドpUCNT(国際公開第WO94/03613号公報)のlacプロモーターの下流のEcoRI認識部位とSalI認識部位の間に挿入し、組換えベクターpNTG1を構築した。
実施例3で構築した組換えベクターpNTCMを用いて、E.coli HB101コンピテントセル(タカラバイオ社製)を形質転換し、E.coli HB101(pNTCM)を得た。この形質転換体は、FERM BP−10418の受託番号にて、2005年9月26日付けで独立行政法人産業技術総合研究所特許生物寄託センター(〒305-8566 茨城県つくば市東1−1−1 中央第6)に寄託されている。(原寄託日2003年10月23日の国内寄託株を、ブダペスト条約に基づく国際寄託に移管)。
実施例5で得た2種の形質転換体、および、ベクタープラスミドpUCNTを含む形質転換体であるE.coli HB101(pUCNT)のそれぞれを、200μg/mlのアンピシリンを含む2×YT培地(トリプトン1.6%、イーストエキス1.0%、NaCl0.5%、pH7.0)50mlに接種し、37℃で24時間振盪培養した。遠心分離により菌体を集め、50mlの100mMリン酸緩衝液(pH6.5)に懸濁した。これを、UH−50型超音波ホモゲナイザー(SMT社製)を用いて破砕した後、遠心分離により菌体残渣を除去し、無細胞抽出液を得た。この無細胞抽出液の3−オキソ−3−フェニルプロパンニトリル還元活性、および、GDH活性を測定し、比活性として表したものを、表1に示した。実施例5で得られた2種の形質転換体のいずれにおいても、3−オキソ−3−フェニルプロパンニトリル還元活性の発現が認められた。また、GDH遺伝子を含むE.coli HB101(pNTCMG1)では、GDH活性の発現も認められた。3−オキソ−3−フェニルプロパンニトリル還元活性は、実施例1に記載の方法で測定した。GDH活性は、1Mトリス塩酸緩衝液(pH8.0)に、グルコース0.1M、補酵素NADP2mM、および粗酵素液を添加して25℃で1分間反応を行い、波長340nmにおける吸光度の増加速度より算出した。この反応条件において、1分間に1μmolのNADPをNADPHに還元する酵素活性を1unitと定義した。また、無細胞抽出液中の蛋白質濃度は、プロテインアッセイキット(BIO−RAD社製)を用いて測定した。
実施例6と同様に調製したE.coli HB101(pNTCM)の無細胞抽出液50mlに、グルコース脱水素酵素(天野エンザイム社製)2000U、グルコース3g、NADP6mg、3−オキソ−3−フェニルプロパンニトリル2gを添加し、5Mの水酸化ナトリウムの滴下によりpH6.5に調整しつつ、30℃で22時間攪拌した。反応終了後、酢酸エチルで抽出し、脱溶剤した後、抽出物を分析した。その結果、収率86.3%で光学純度97.3%e.e.の(R)−3−ヒドロキシ−3−フェニルプロパンニトリルが得られた。
実施例6と同様に調製したE.coli HB101(pNTCMG1)の無細胞抽出液50mlに、グルコース3g、NADP6mg、3−オキソ−3−フェニルプロパンニトリル2gを添加し、5Mの水酸化ナトリウムの滴下によりpH6.5に調整しつつ、30℃で22時間攪拌した。反応終了後、酢酸エチルで抽出し、脱溶剤した後、抽出物を分析した。その結果、収率92.1%で光学純度97.4%e.e.の(R)−3−ヒドロキシ−3−フェニルプロパンニトリルが得られた。
実施例6と同様に培養したE.coli HB101(pNTCMG1)の培養液50mlに、グルコース5g、NADP6mg、2−クロロ−1−(3’−クロロフェニル)エタノン4g、および、トルエン4gを添加し、5Mの水酸化ナトリウムの滴下によりpH6.5に調整しつつ、30℃で24時間攪拌した。反応終了後、反応液をトルエンで抽出し脱溶剤した後、抽出物を分析した。その結果、収率90.5%で光学純度82.0%e.e.の(R)−2−クロロ−1−(3’−クロロフェニル)エタノールが得られた。
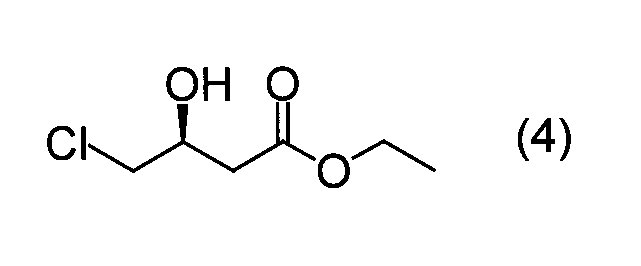
実施例6と同様に培養したE.coli HB101(pNTCMG1)の培養液50mlに、グルコース6g、NADP4mgを添加した。この反応液を30℃で攪拌し、5Mの水酸化ナトリウムの滴下によりpH6.5に調整しつつ、1時間に0.5gの割合で、合計5gの4−クロロ−3−オキソ酪酸エチルを添加した後、さらに5時間攪拌を続けた。反応終了後、反応液を酢酸エチルで抽出し脱溶剤した後、抽出物を分析した。その結果、収率93.1%で、光学純度80.5%e.e.の(S)−4−クロロ−3−ヒドロキシ酪酸エチルが得られた。
実施例6と同様に培養したE.coli HB101(pNTCMG1)の培養液40mlに、グルコース3g、NADP6mg、(S)−6−ベンゾイルオキシ−5−ヒドロキシ−3−オキソヘキサン酸tert−ブチル4g、および、トルエン1.6gを添加し、5Mの水酸化ナトリウムの滴下によりpH6.5に調整しつつ、30℃で24時間攪拌した。反応終了後、反応液をトルエンで抽出し脱溶剤した後、抽出物を分析した。その結果、収率92.3%でジアステレオマー過剰率99.7%d.e.の(3R,5S)−6−ベンゾイルオキシ−3,5−ジヒドロキシヘキサン酸tert−ブチルが得られた。
0.33%(v/v)のジメチルスルフォキシドを含む100mMリン酸緩衝液(pH6.5)に、基質となるカルボニル化合物を終濃度1mM、補酵素NADPHを終濃度0.25mMとなるようそれぞれ溶解した。これに、実施例1で調製した精製ポリペプチドを適当量添加し、30℃で1分間反応を行った。当該反応液の波長340nmにおける吸光度の減少速度から、各カルボニル化合物に対する還元活性を算出し、これを3−オキソ−3−フェニルプロパンニトリルに対する活性を100%とした場合の相対値で表し、表2に示した。表2から明らかなように本発明のポリペプチドは、広範なカルボニル化合物に対して還元活性を示した。
Claims (17)
- 配列表の配列番号2に示すアミノ酸配列からなるポリペプチドをコードするDNA。
- 請求項1記載のDNAにコードされ、かつ、前記式(1)で表される3−オキソ−3−フェニルプロパンニトリルを不斉的に還元して、前記式(2)で表される(R)−3−ヒドロキシ−3−フェニルプロパンニトリルを生成する活性を有するポリペプチド。
- 配列表の配列番号2に示すアミノ酸配列からなるポリペプチド。
- 請求項1又は2記載のDNAを含むベクター。
- 組換えプラスミドが、配列番号1に示す塩基配列からなるDNAを含み、FERM BP−10418の受託番号で寄託されているE.coli HB101(pNTCM)に含まれる、プラスミドpNTCMである請求項5記載のベクター。
- グルコース脱水素酵素活性を有するポリペプチドをコードするDNAをさらに含む、請求項5に記載のベクター。
- 前記グルコース脱水素酵素活性を有するポリペプチドがバシラス・メガテリウム(Bacillus megaterium)由来のグルコース脱水素酵素である、請求項7記載のベクター。
- 請求項5〜8のいずれかに記載のベクターにより宿主細胞を形質転換して得られる形質転換体。
- 前記宿主細胞が大腸菌である請求項9記載の形質転換体。
- E.coli HB101(pNTCM)FERM BP−10418である、請求項10記載の形質転換体。
- 請求項1又は2に記載のDNAおよびグルコース脱水素酵素活性を有するポリペプチドをコードするDNAの両方が導入された形質転換体。
- 請求項3又は4に記載のポリペプチド、又は、請求項9〜11のいずれかに記載の形質転換体または当該形質転換体の培養物を、カルボニル基を有する化合物と反応させることを特徴とする光学活性アルコールの製造方法。
- 前記カルボニル基を有する化合物が、前記式(1)で表される3−オキソ−3−フェニルプロパンニトリルであり、前記光学活性アルコールが、前記式(2)で表される(R)−3−ヒドロキシ−3−フェニルプロパンニトリルである、請求項13記載の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006543049A JP4757804B2 (ja) | 2004-10-27 | 2005-10-20 | 新規カルボニル還元酵素、その遺伝子、およびその利用法 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004312365 | 2004-10-27 | ||
| JP2004312365 | 2004-10-27 | ||
| PCT/JP2005/019269 WO2006046455A1 (ja) | 2004-10-27 | 2005-10-20 | 新規カルボニル還元酵素、その遺伝子、およびその利用法 |
| JP2006543049A JP4757804B2 (ja) | 2004-10-27 | 2005-10-20 | 新規カルボニル還元酵素、その遺伝子、およびその利用法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2006046455A1 JPWO2006046455A1 (ja) | 2008-05-22 |
| JP4757804B2 true JP4757804B2 (ja) | 2011-08-24 |
Family
ID=36227695
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006543049A Expired - Fee Related JP4757804B2 (ja) | 2004-10-27 | 2005-10-20 | 新規カルボニル還元酵素、その遺伝子、およびその利用法 |
Country Status (4)
| Country | Link |
|---|---|
| US (2) | US8008461B2 (ja) |
| EP (1) | EP1811021A4 (ja) |
| JP (1) | JP4757804B2 (ja) |
| WO (1) | WO2006046455A1 (ja) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009041415A1 (ja) * | 2007-09-26 | 2009-04-02 | Kaneka Corporation | 新規グルコース脱水素酵素 |
| TWI601825B (zh) * | 2007-09-27 | 2017-10-11 | Iep有限公司 | 對映異構選擇性酶催化還原中間產物之方法 |
| WO2010004265A1 (en) | 2008-07-07 | 2010-01-14 | Oxford Nanopore Technologies Limited | Enzyme-pore constructs |
| EP2226386A1 (de) | 2009-03-05 | 2010-09-08 | IEP GmbH | Verfahren zur stereoselektiven enzymatischen Reduktion von Ketoverbindungen |
| EP2445890B1 (en) * | 2009-06-22 | 2015-05-06 | SK Biopharmaceuticals Co., Ltd. | Method for preparation of carbamic acid (r)-1-aryl-2-tetrazolyl-ethyl ester |
| CN102482649B (zh) * | 2009-06-23 | 2014-09-03 | 江南大学 | 立体专一性羰基还原酶 |
| US8404461B2 (en) | 2009-10-15 | 2013-03-26 | SK Biopharmaceutical Co. Ltd. | Method for preparation of carbamic acid (R)-1-aryl-2-tetrazolyl-ethyl ester |
| EP2639216B1 (en) | 2010-11-09 | 2018-07-11 | Kaneka Corporation | Halogenated indenones and method for producing optically active indanones or optically active indanols by using same |
| EP2987870B1 (en) | 2011-10-21 | 2020-02-19 | Oxford Nanopore Technologies Limited | Method of characterizing a target polynucleotide using a transmembrane pore and molecular motor |
| CN104136631B (zh) | 2011-12-29 | 2017-03-01 | 牛津纳米孔技术公司 | 使用xpd解旋酶表征多核苷酸的方法 |
| WO2013098562A2 (en) | 2011-12-29 | 2013-07-04 | Oxford Nanopore Technologies Limited | Enzyme method |
| EP2875128B8 (en) | 2012-07-19 | 2020-06-24 | Oxford Nanopore Technologies Limited | Modified helicases |
| US9797009B2 (en) | 2012-07-19 | 2017-10-24 | Oxford Nanopore Technologies Limited | Enzyme construct |
| GB201406151D0 (en) | 2014-04-04 | 2014-05-21 | Oxford Nanopore Tech Ltd | Method |
| CN105899678A (zh) | 2013-10-18 | 2016-08-24 | 牛津纳米孔技术公司 | 经修饰的酶 |
| GB201417712D0 (en) | 2014-10-07 | 2014-11-19 | Oxford Nanopore Tech Ltd | Method |
| CN104388373A (zh) * | 2014-12-10 | 2015-03-04 | 江南大学 | 一种共表达羰基还原酶和葡萄糖脱氢酶的大肠杆菌系统的构建 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001040450A1 (fr) * | 1999-12-03 | 2001-06-07 | Kaneka Corporation | Nouvelle carbonyl reductase, son gene et son procede d'utilisation |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2231772T3 (es) | 1992-08-10 | 2005-05-16 | Kanegafuchi Kagaku Kogyo Kabushiki Kaisha | Adn codante para la descarbamilasa con termoestabilidad mejorada y uso del mismo. |
| IL131241A0 (en) * | 1997-02-07 | 2001-01-28 | Kaneka Corp | Novel carbonyl reductase gene coding same and method for using such reductase and gene |
| WO2003093477A1 (fr) * | 2002-04-30 | 2003-11-13 | Kaneka Corporation | Carbonyl reductase, gene de celle-ci et son utilisation |
-
2005
- 2005-10-20 US US11/665,065 patent/US8008461B2/en not_active Expired - Fee Related
- 2005-10-20 EP EP05795588A patent/EP1811021A4/en not_active Withdrawn
- 2005-10-20 JP JP2006543049A patent/JP4757804B2/ja not_active Expired - Fee Related
- 2005-10-20 WO PCT/JP2005/019269 patent/WO2006046455A1/ja not_active Application Discontinuation
-
2011
- 2011-04-25 US US13/093,610 patent/US20130149769A1/en not_active Abandoned
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001040450A1 (fr) * | 1999-12-03 | 2001-06-07 | Kaneka Corporation | Nouvelle carbonyl reductase, son gene et son procede d'utilisation |
Also Published As
| Publication number | Publication date |
|---|---|
| US20130149769A1 (en) | 2013-06-13 |
| US8008461B2 (en) | 2011-08-30 |
| US20090029430A1 (en) | 2009-01-29 |
| EP1811021A4 (en) | 2008-05-28 |
| EP1811021A1 (en) | 2007-07-25 |
| JPWO2006046455A1 (ja) | 2008-05-22 |
| WO2006046455A1 (ja) | 2006-05-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4757804B2 (ja) | 新規カルボニル還元酵素、その遺伝子、およびその利用法 | |
| JP4746548B2 (ja) | 新規カルボニル還元酵素、その遺伝子、およびその利用法 | |
| JP4510351B2 (ja) | 新規カルボニル還元酵素、その遺伝子、およびその利用法 | |
| Geueke et al. | NADH oxidase from Lactobacillus brevis: a new catalyst for the regeneration of NAD | |
| JP4012257B2 (ja) | 新規カルボニル還元酵素、およびこれをコードする遺伝子、ならびにこれらの利用方法 | |
| JP4651896B2 (ja) | (r)−2−オクタノール脱水素酵素、該酵素の製造方法、該酵素をコードするdnaおよびこれを利用したアルコールの製造方法 | |
| JP5261172B2 (ja) | エリスロ又はスレオ−2−アミノ−3−ヒドロキシプロピオン酸エステルの製造方法、新規カルボニル還元酵素、その遺伝子、ベクター、形質転換体、およびそれらを利用した光学活性アルコールの製造方法 | |
| JP5308163B2 (ja) | 新規アルコール脱水素酵素、その遺伝子、ベクター、形質転換体、およびそれらを利用した光学活性アルコールの製造方法 | |
| JP4414337B2 (ja) | 新規カルボニル還元酵素、その遺伝子、およびその利用法 | |
| JPWO2007094178A1 (ja) | 新規な(s,s)−ブタンジオール脱水素酵素、その遺伝子、及びその利用法 | |
| JP5005672B2 (ja) | 新規カルボニル還元酵素、その遺伝子、およびそれらを利用した光学活性アルコールの製造方法 | |
| JP4426437B2 (ja) | 新規カルボニル還元酵素、その遺伝子、およびその利用法 | |
| JPWO2006013802A1 (ja) | エナンチオマー豊富化化合物の製造方法 | |
| JP4688313B2 (ja) | 新規なエノン還元酵素、その製造方法、およびこれを利用したα,β−不飽和ケトンの炭素−炭素2重結合を選択的に還元する方法 | |
| WO2007099994A1 (ja) | 新規カルボニル還元酵素、その遺伝子、ベクター、形質転換体、およびそれらを利用した光学活性アルコールの製造方法 | |
| JP2005537017A (ja) | Nadh再生のためのリンゴ酸デヒドロゲナーゼの使用 | |
| JP4270918B2 (ja) | 新規カルボニル還元酵素及びこれをコードする遺伝子、ならびにこれらを利用した光学活性アルコールの製造方法 | |
| JPWO2005123921A1 (ja) | 新規グリセロール脱水素酵素、その遺伝子、及びその利用法 | |
| JP5030067B2 (ja) | 新規アルカンポリオール脱水素酵素 | |
| JP4796323B2 (ja) | 新規カルボニル還元酵素、その遺伝子、およびその利用法 | |
| JP2003061668A (ja) | 新規グリセロール脱水素酵素およびその利用法 | |
| JP2010279272A (ja) | 新規カルボニル還元酵素、その遺伝子、ベクター、形質転換体、およびそれらを利用した光学活性アルコールの製造方法 | |
| JP2007274901A (ja) | 光学活性プロパルギルアルコールの製造方法 | |
| JPWO2005044973A1 (ja) | 新規アセトアセチルCoA還元酵素および光学活性アルコールの製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080826 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110315 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110511 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110531 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110601 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140610 Year of fee payment: 3 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140610 Year of fee payment: 3 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| LAPS | Cancellation because of no payment of annual fees |