JP4638418B2 - アスペルギラス・ニガーの酵素−欠失変異体における生物学的物質の生成方法 - Google Patents
アスペルギラス・ニガーの酵素−欠失変異体における生物学的物質の生成方法 Download PDFInfo
- Publication number
- JP4638418B2 JP4638418B2 JP2006509611A JP2006509611A JP4638418B2 JP 4638418 B2 JP4638418 B2 JP 4638418B2 JP 2006509611 A JP2006509611 A JP 2006509611A JP 2006509611 A JP2006509611 A JP 2006509611A JP 4638418 B2 JP4638418 B2 JP 4638418B2
- Authority
- JP
- Japan
- Prior art keywords
- gene
- amylase
- aspergillus niger
- neutral
- strain
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 241000228245 Aspergillus niger Species 0.000 title claims abstract description 200
- 238000000034 method Methods 0.000 title claims abstract description 75
- 239000012620 biological material Substances 0.000 title claims description 71
- 238000012217 deletion Methods 0.000 title description 18
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 127
- 125000003729 nucleotide group Chemical group 0.000 claims abstract description 93
- 239000002773 nucleotide Substances 0.000 claims abstract description 90
- 230000004048 modification Effects 0.000 claims abstract description 63
- 238000012986 modification Methods 0.000 claims abstract description 63
- 101150108358 GLAA gene Proteins 0.000 claims abstract description 55
- 101150115781 prtT gene Proteins 0.000 claims abstract description 50
- 230000007935 neutral effect Effects 0.000 claims abstract description 49
- 108090000637 alpha-Amylases Proteins 0.000 claims abstract description 48
- 101150069712 amyA gene Proteins 0.000 claims abstract description 48
- 101150009288 amyB gene Proteins 0.000 claims abstract description 47
- 102000004190 Enzymes Human genes 0.000 claims abstract description 45
- 108090000790 Enzymes Proteins 0.000 claims abstract description 45
- 108010073178 Glucan 1,4-alpha-Glucosidase Proteins 0.000 claims abstract description 45
- 229940088598 enzyme Drugs 0.000 claims abstract description 45
- 101100277447 Bacillus subtilis (strain 168) degQ gene Proteins 0.000 claims abstract description 43
- 101100162670 Bacillus subtilis (strain 168) amyE gene Proteins 0.000 claims abstract description 42
- 108091005804 Peptidases Proteins 0.000 claims abstract description 38
- 102000004139 alpha-Amylases Human genes 0.000 claims abstract description 38
- 229940024171 alpha-amylase Drugs 0.000 claims abstract description 38
- 238000004519 manufacturing process Methods 0.000 claims abstract description 35
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Natural products OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 claims abstract description 34
- 239000004365 Protease Substances 0.000 claims abstract description 32
- 102100022624 Glucoamylase Human genes 0.000 claims abstract description 31
- 239000002253 acid Substances 0.000 claims abstract description 23
- 108090000604 Hydrolases Proteins 0.000 claims abstract description 21
- 101710081721 Alpha-amylase A Proteins 0.000 claims abstract description 19
- 101710081719 Alpha-amylase B Proteins 0.000 claims abstract description 18
- 102000004157 Hydrolases Human genes 0.000 claims abstract description 17
- 239000000126 substance Substances 0.000 claims abstract description 12
- 235000006408 oxalic acid Nutrition 0.000 claims abstract description 8
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 claims abstract 9
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 48
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 47
- 229920001184 polypeptide Polymers 0.000 claims description 45
- 239000002609 medium Substances 0.000 claims description 36
- 238000006243 chemical reaction Methods 0.000 claims description 32
- 102000035195 Peptidases Human genes 0.000 claims description 29
- 235000019419 proteases Nutrition 0.000 claims description 29
- -1 asa Proteins 0.000 claims description 28
- 238000002703 mutagenesis Methods 0.000 claims description 18
- 231100000350 mutagenesis Toxicity 0.000 claims description 18
- 101000757144 Aspergillus niger Glucoamylase Proteins 0.000 claims description 14
- 108010053835 Catalase Proteins 0.000 claims description 14
- 102000016938 Catalase Human genes 0.000 claims description 12
- 238000012224 gene deletion Methods 0.000 claims description 11
- 108010059892 Cellulase Proteins 0.000 claims description 9
- 102000005367 Carboxypeptidases Human genes 0.000 claims description 8
- 108010006303 Carboxypeptidases Proteins 0.000 claims description 8
- 108010029541 Laccase Proteins 0.000 claims description 7
- 108090001060 Lipase Proteins 0.000 claims description 7
- 102000004882 Lipase Human genes 0.000 claims description 7
- 239000004367 Lipase Substances 0.000 claims description 7
- 102000004316 Oxidoreductases Human genes 0.000 claims description 7
- 108090000854 Oxidoreductases Proteins 0.000 claims description 7
- 102000003992 Peroxidases Human genes 0.000 claims description 7
- 229940106157 cellulase Drugs 0.000 claims description 7
- 235000019421 lipase Nutrition 0.000 claims description 7
- 229940072417 peroxidase Drugs 0.000 claims description 7
- 108040007629 peroxidase activity proteins Proteins 0.000 claims description 7
- 108010011619 6-Phytase Proteins 0.000 claims description 6
- 108010031396 Catechol oxidase Proteins 0.000 claims description 6
- 102000030523 Catechol oxidase Human genes 0.000 claims description 6
- 108010022172 Chitinases Proteins 0.000 claims description 6
- 102000012286 Chitinases Human genes 0.000 claims description 6
- 108010025880 Cyclomaltodextrin glucanotransferase Proteins 0.000 claims description 6
- 108010053770 Deoxyribonucleases Proteins 0.000 claims description 6
- 102000016911 Deoxyribonucleases Human genes 0.000 claims description 6
- 108090000371 Esterases Proteins 0.000 claims description 6
- 108010054377 Mannosidases Proteins 0.000 claims description 6
- 102000001696 Mannosidases Human genes 0.000 claims description 6
- 108010083644 Ribonucleases Proteins 0.000 claims description 6
- 102000006382 Ribonucleases Human genes 0.000 claims description 6
- 102000004357 Transferases Human genes 0.000 claims description 6
- 108090000992 Transferases Proteins 0.000 claims description 6
- 108060008539 Transglutaminase Proteins 0.000 claims description 6
- 108010051210 beta-Fructofuranosidase Proteins 0.000 claims description 6
- 108010005774 beta-Galactosidase Proteins 0.000 claims description 6
- 102000005936 beta-Galactosidase Human genes 0.000 claims description 6
- 238000012258 culturing Methods 0.000 claims description 6
- 108010005400 cutinase Proteins 0.000 claims description 6
- 230000000593 degrading effect Effects 0.000 claims description 6
- 239000001963 growth medium Substances 0.000 claims description 6
- 239000001573 invertase Substances 0.000 claims description 6
- 235000011073 invertase Nutrition 0.000 claims description 6
- 239000001814 pectin Substances 0.000 claims description 6
- 229920001277 pectin Polymers 0.000 claims description 6
- 235000010987 pectin Nutrition 0.000 claims description 6
- 229940085127 phytase Drugs 0.000 claims description 6
- 102000003601 transglutaminase Human genes 0.000 claims description 6
- 101710121765 Endo-1,4-beta-xylanase Proteins 0.000 claims description 5
- 108010015776 Glucose oxidase Proteins 0.000 claims description 5
- 239000004366 Glucose oxidase Substances 0.000 claims description 5
- 102000004195 Isomerases Human genes 0.000 claims description 5
- 108090000769 Isomerases Proteins 0.000 claims description 5
- 102000003960 Ligases Human genes 0.000 claims description 5
- 108090000364 Ligases Proteins 0.000 claims description 5
- 108090000856 Lyases Proteins 0.000 claims description 5
- 102000004317 Lyases Human genes 0.000 claims description 5
- 108010089934 carbohydrase Proteins 0.000 claims description 5
- 229940116332 glucose oxidase Drugs 0.000 claims description 5
- 235000019420 glucose oxidase Nutrition 0.000 claims description 5
- 230000002797 proteolythic effect Effects 0.000 claims description 5
- 108010093031 Galactosidases Proteins 0.000 claims description 4
- 102000002464 Galactosidases Human genes 0.000 claims description 4
- 102000004366 Glucosidases Human genes 0.000 claims description 4
- 108010056771 Glucosidases Proteins 0.000 claims description 4
- 108060008724 Tyrosinase Proteins 0.000 claims description 4
- 102000003425 Tyrosinase Human genes 0.000 claims description 4
- 108010002430 hemicellulase Proteins 0.000 claims description 4
- 229940059442 hemicellulase Drugs 0.000 claims description 4
- 230000035772 mutation Effects 0.000 claims description 2
- 230000008569 process Effects 0.000 claims description 2
- 235000019833 protease Nutrition 0.000 claims 3
- 101000971102 Thauera aromatica 6-oxocyclohex-1-ene-1-carbonyl-CoA hydrolase Proteins 0.000 abstract description 35
- 108091028043 Nucleic acid sequence Proteins 0.000 abstract description 26
- 230000002950 deficient Effects 0.000 abstract description 10
- 108020004414 DNA Proteins 0.000 description 52
- 239000012634 fragment Substances 0.000 description 52
- 239000013598 vector Substances 0.000 description 47
- 230000000694 effects Effects 0.000 description 43
- 239000000523 sample Substances 0.000 description 41
- 108091026890 Coding region Proteins 0.000 description 38
- 230000014509 gene expression Effects 0.000 description 37
- 101150054232 pyrG gene Proteins 0.000 description 35
- DRTQHJPVMGBUCF-XVFCMESISA-N Uridine Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C=C1 DRTQHJPVMGBUCF-XVFCMESISA-N 0.000 description 28
- 239000000499 gel Substances 0.000 description 25
- 239000013612 plasmid Substances 0.000 description 24
- 150000007523 nucleic acids Chemical class 0.000 description 22
- 238000003752 polymerase chain reaction Methods 0.000 description 17
- 238000000855 fermentation Methods 0.000 description 16
- 230000004151 fermentation Effects 0.000 description 16
- 239000003550 marker Substances 0.000 description 16
- 108020004707 nucleic acids Proteins 0.000 description 16
- 102000039446 nucleic acids Human genes 0.000 description 16
- 108010076504 Protein Sorting Signals Proteins 0.000 description 15
- 230000037430 deletion Effects 0.000 description 15
- DRTQHJPVMGBUCF-PSQAKQOGSA-N beta-L-uridine Natural products O[C@H]1[C@@H](O)[C@H](CO)O[C@@H]1N1C(=O)NC(=O)C=C1 DRTQHJPVMGBUCF-PSQAKQOGSA-N 0.000 description 14
- 238000002744 homologous recombination Methods 0.000 description 14
- 230000006801 homologous recombination Effects 0.000 description 14
- DRTQHJPVMGBUCF-UHFFFAOYSA-N uracil arabinoside Natural products OC1C(O)C(CO)OC1N1C(=O)NC(=O)C=C1 DRTQHJPVMGBUCF-UHFFFAOYSA-N 0.000 description 14
- 229940045145 uridine Drugs 0.000 description 14
- 150000001413 amino acids Chemical group 0.000 description 13
- 238000000605 extraction Methods 0.000 description 13
- 230000001105 regulatory effect Effects 0.000 description 13
- 108010065511 Amylases Proteins 0.000 description 12
- 210000004027 cell Anatomy 0.000 description 12
- 238000009396 hybridization Methods 0.000 description 12
- 230000010354 integration Effects 0.000 description 12
- 239000000243 solution Substances 0.000 description 12
- 239000004382 Amylase Substances 0.000 description 11
- 102000013142 Amylases Human genes 0.000 description 11
- 240000006439 Aspergillus oryzae Species 0.000 description 11
- 235000002247 Aspergillus oryzae Nutrition 0.000 description 11
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 11
- 235000019418 amylase Nutrition 0.000 description 11
- 239000008103 glucose Substances 0.000 description 11
- 239000000872 buffer Substances 0.000 description 10
- 238000001962 electrophoresis Methods 0.000 description 10
- 238000003780 insertion Methods 0.000 description 10
- 230000037431 insertion Effects 0.000 description 10
- 239000000047 product Substances 0.000 description 10
- 239000000758 substrate Substances 0.000 description 10
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 9
- 108700007698 Genetic Terminator Regions Proteins 0.000 description 9
- 238000012408 PCR amplification Methods 0.000 description 9
- 238000002105 Southern blotting Methods 0.000 description 9
- 241000499912 Trichoderma reesei Species 0.000 description 9
- 235000001014 amino acid Nutrition 0.000 description 9
- 238000004458 analytical method Methods 0.000 description 9
- 238000010367 cloning Methods 0.000 description 9
- 230000029087 digestion Effects 0.000 description 9
- 229920001282 polysaccharide Polymers 0.000 description 9
- 239000005017 polysaccharide Substances 0.000 description 9
- 210000001938 protoplast Anatomy 0.000 description 9
- 239000000600 sorbitol Substances 0.000 description 9
- SEHFUALWMUWDKS-UHFFFAOYSA-N 5-fluoroorotic acid Chemical compound OC(=O)C=1NC(=O)NC(=O)C=1F SEHFUALWMUWDKS-UHFFFAOYSA-N 0.000 description 8
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 8
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 8
- 238000010276 construction Methods 0.000 description 8
- 239000013604 expression vector Substances 0.000 description 8
- 150000004676 glycans Chemical class 0.000 description 8
- 239000002207 metabolite Substances 0.000 description 8
- 238000013518 transcription Methods 0.000 description 8
- 230000035897 transcription Effects 0.000 description 8
- 241000351920 Aspergillus nidulans Species 0.000 description 7
- 108091081024 Start codon Proteins 0.000 description 7
- 229920001222 biopolymer Polymers 0.000 description 7
- SUYVUBYJARFZHO-RRKCRQDMSA-N dATP Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@H]1C[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O1 SUYVUBYJARFZHO-RRKCRQDMSA-N 0.000 description 7
- SUYVUBYJARFZHO-UHFFFAOYSA-N dATP Natural products C1=NC=2C(N)=NC=NC=2N1C1CC(O)C(COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O1 SUYVUBYJARFZHO-UHFFFAOYSA-N 0.000 description 7
- RGWHQCVHVJXOKC-SHYZEUOFSA-J dCTP(4-) Chemical compound O=C1N=C(N)C=CN1[C@@H]1O[C@H](COP([O-])(=O)OP([O-])(=O)OP([O-])([O-])=O)[C@@H](O)C1 RGWHQCVHVJXOKC-SHYZEUOFSA-J 0.000 description 7
- HAAZLUGHYHWQIW-KVQBGUIXSA-N dGTP Chemical compound C1=NC=2C(=O)NC(N)=NC=2N1[C@H]1C[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O1 HAAZLUGHYHWQIW-KVQBGUIXSA-N 0.000 description 7
- NHVNXKFIZYSCEB-XLPZGREQSA-N dTTP Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)[C@@H](O)C1 NHVNXKFIZYSCEB-XLPZGREQSA-N 0.000 description 7
- 229920002674 hyaluronan Polymers 0.000 description 7
- 102000004169 proteins and genes Human genes 0.000 description 7
- 230000009466 transformation Effects 0.000 description 7
- 108010031797 Candida antarctica lipase B Proteins 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 6
- 229920002472 Starch Polymers 0.000 description 6
- 229930006000 Sucrose Natural products 0.000 description 6
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 6
- 108010006785 Taq Polymerase Proteins 0.000 description 6
- 108010048241 acetamidase Proteins 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- 108010054497 oxaloacetase Proteins 0.000 description 6
- 235000018102 proteins Nutrition 0.000 description 6
- 230000010076 replication Effects 0.000 description 6
- 239000008107 starch Substances 0.000 description 6
- 235000019698 starch Nutrition 0.000 description 6
- 239000005720 sucrose Substances 0.000 description 6
- 239000006228 supernatant Substances 0.000 description 6
- 238000011426 transformation method Methods 0.000 description 6
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 6
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 5
- 101100523058 Aspergillus niger pyrG gene Proteins 0.000 description 5
- 101710098554 Lipase B Proteins 0.000 description 5
- 239000007983 Tris buffer Substances 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 239000005018 casein Substances 0.000 description 5
- 239000003153 chemical reaction reagent Substances 0.000 description 5
- 230000002759 chromosomal effect Effects 0.000 description 5
- 210000000349 chromosome Anatomy 0.000 description 5
- 230000000295 complement effect Effects 0.000 description 5
- 239000002299 complementary DNA Substances 0.000 description 5
- 238000001952 enzyme assay Methods 0.000 description 5
- 229960003160 hyaluronic acid Drugs 0.000 description 5
- 108020004999 messenger RNA Proteins 0.000 description 5
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 5
- 150000003839 salts Chemical class 0.000 description 5
- 229930000044 secondary metabolite Natural products 0.000 description 5
- 230000028327 secretion Effects 0.000 description 5
- 239000011573 trace mineral Substances 0.000 description 5
- 235000013619 trace mineral Nutrition 0.000 description 5
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- 229920001817 Agar Polymers 0.000 description 4
- 108090000915 Aminopeptidases Proteins 0.000 description 4
- 102000004400 Aminopeptidases Human genes 0.000 description 4
- 241000228212 Aspergillus Species 0.000 description 4
- 101150014526 Gla gene Proteins 0.000 description 4
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 4
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 4
- 239000008272 agar Substances 0.000 description 4
- 238000003556 assay Methods 0.000 description 4
- AIYUHDOJVYHVIT-UHFFFAOYSA-M caesium chloride Chemical compound [Cl-].[Cs+] AIYUHDOJVYHVIT-UHFFFAOYSA-M 0.000 description 4
- 239000012876 carrier material Substances 0.000 description 4
- 238000001514 detection method Methods 0.000 description 4
- 230000012010 growth Effects 0.000 description 4
- 229920000669 heparin Polymers 0.000 description 4
- 229960002897 heparin Drugs 0.000 description 4
- 238000011534 incubation Methods 0.000 description 4
- 238000002955 isolation Methods 0.000 description 4
- DVDUMIQZEUTAGK-UHFFFAOYSA-N p-nitrophenyl butyrate Chemical compound CCCC(=O)OC1=CC=C([N+]([O-])=O)C=C1 DVDUMIQZEUTAGK-UHFFFAOYSA-N 0.000 description 4
- 238000003259 recombinant expression Methods 0.000 description 4
- 108091008146 restriction endonucleases Proteins 0.000 description 4
- 238000006467 substitution reaction Methods 0.000 description 4
- 238000013519 translation Methods 0.000 description 4
- 108010037870 Anthranilate Synthase Proteins 0.000 description 3
- 108010017640 Aspartic Acid Proteases Proteins 0.000 description 3
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 3
- 102100024295 Maltase-glucoamylase Human genes 0.000 description 3
- 108020004711 Nucleic Acid Probes Proteins 0.000 description 3
- 241000235403 Rhizomucor miehei Species 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 239000011543 agarose gel Substances 0.000 description 3
- 108010028144 alpha-Glucosidases Proteins 0.000 description 3
- 108010047754 beta-Glucosidase Proteins 0.000 description 3
- 102000006995 beta-Glucosidase Human genes 0.000 description 3
- 230000006696 biosynthetic metabolic pathway Effects 0.000 description 3
- 229940041514 candida albicans extract Drugs 0.000 description 3
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 description 3
- 235000021240 caseins Nutrition 0.000 description 3
- 239000012228 culture supernatant Substances 0.000 description 3
- 238000010348 incorporation Methods 0.000 description 3
- 239000002853 nucleic acid probe Substances 0.000 description 3
- 230000008488 polyadenylation Effects 0.000 description 3
- 229910000160 potassium phosphate Inorganic materials 0.000 description 3
- 235000011009 potassium phosphates Nutrition 0.000 description 3
- 229930010796 primary metabolite Natural products 0.000 description 3
- 238000011084 recovery Methods 0.000 description 3
- 230000002441 reversible effect Effects 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 238000012807 shake-flask culturing Methods 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 239000011550 stock solution Substances 0.000 description 3
- 230000002103 transcriptional effect Effects 0.000 description 3
- 230000017105 transposition Effects 0.000 description 3
- 238000011144 upstream manufacturing Methods 0.000 description 3
- 239000012138 yeast extract Substances 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 2
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 2
- 229920000936 Agarose Polymers 0.000 description 2
- 102000004580 Aspartic Acid Proteases Human genes 0.000 description 2
- 101000690713 Aspergillus niger Alpha-glucosidase Proteins 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 229920002101 Chitin Polymers 0.000 description 2
- 108020004705 Codon Proteins 0.000 description 2
- 102000010911 Enzyme Precursors Human genes 0.000 description 2
- 108010062466 Enzyme Precursors Proteins 0.000 description 2
- PLUBXMRUUVWRLT-UHFFFAOYSA-N Ethyl methanesulfonate Chemical compound CCOS(C)(=O)=O PLUBXMRUUVWRLT-UHFFFAOYSA-N 0.000 description 2
- 241000567178 Fusarium venenatum Species 0.000 description 2
- IAJILQKETJEXLJ-UHFFFAOYSA-N Galacturonsaeure Natural products O=CC(O)C(O)C(O)C(O)C(O)=O IAJILQKETJEXLJ-UHFFFAOYSA-N 0.000 description 2
- 239000004471 Glycine Substances 0.000 description 2
- 229920002683 Glycosaminoglycan Polymers 0.000 description 2
- 102100027612 Kallikrein-11 Human genes 0.000 description 2
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 2
- OVRNDRQMDRJTHS-UHFFFAOYSA-N N-acelyl-D-glucosamine Natural products CC(=O)NC1C(O)OC(CO)C(O)C1O OVRNDRQMDRJTHS-UHFFFAOYSA-N 0.000 description 2
- MBLBDJOUHNCFQT-LXGUWJNJSA-N N-acetylglucosamine Natural products CC(=O)N[C@@H](C=O)[C@@H](O)[C@H](O)[C@H](O)CO MBLBDJOUHNCFQT-LXGUWJNJSA-N 0.000 description 2
- VZUNGTLZRAYYDE-UHFFFAOYSA-N N-methyl-N'-nitro-N-nitrosoguanidine Chemical compound O=NN(C)C(=N)N[N+]([O-])=O VZUNGTLZRAYYDE-UHFFFAOYSA-N 0.000 description 2
- 239000004677 Nylon Substances 0.000 description 2
- 229920001030 Polyethylene Glycol 4000 Polymers 0.000 description 2
- 108020004511 Recombinant DNA Proteins 0.000 description 2
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 2
- 108091023040 Transcription factor Proteins 0.000 description 2
- 102000005924 Triose-Phosphate Isomerase Human genes 0.000 description 2
- 108700015934 Triose-phosphate isomerases Proteins 0.000 description 2
- 101710152431 Trypsin-like protease Proteins 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- IAJILQKETJEXLJ-QTBDOELSSA-N aldehydo-D-glucuronic acid Chemical compound O=C[C@H](O)[C@@H](O)[C@H](O)[C@H](O)C(O)=O IAJILQKETJEXLJ-QTBDOELSSA-N 0.000 description 2
- WQZGKKKJIJFFOK-DVKNGEFBSA-N alpha-D-glucose Chemical group OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-DVKNGEFBSA-N 0.000 description 2
- 108010030291 alpha-Galactosidase Proteins 0.000 description 2
- 102000005840 alpha-Galactosidase Human genes 0.000 description 2
- 239000003242 anti bacterial agent Substances 0.000 description 2
- 230000000692 anti-sense effect Effects 0.000 description 2
- 230000003115 biocidal effect Effects 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 230000001627 detrimental effect Effects 0.000 description 2
- 238000011143 downstream manufacturing Methods 0.000 description 2
- 108010000165 exo-1,3-alpha-glucanase Proteins 0.000 description 2
- 239000013613 expression plasmid Substances 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 229940097043 glucuronic acid Drugs 0.000 description 2
- 229910001385 heavy metal Inorganic materials 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- KIUKXJAPPMFGSW-MNSSHETKSA-N hyaluronan Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)C1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H](C(O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-MNSSHETKSA-N 0.000 description 2
- 229940099552 hyaluronan Drugs 0.000 description 2
- 230000007062 hydrolysis Effects 0.000 description 2
- 238000006460 hydrolysis reaction Methods 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 238000001155 isoelectric focusing Methods 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 230000037353 metabolic pathway Effects 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 229910052756 noble gas Inorganic materials 0.000 description 2
- 229920001778 nylon Polymers 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- 229920001983 poloxamer Polymers 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 230000003248 secreting effect Effects 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 239000010936 titanium Substances 0.000 description 2
- 229910052719 titanium Inorganic materials 0.000 description 2
- 238000000844 transformation Methods 0.000 description 2
- WCDDVEOXEIYWFB-VXORFPGASA-N (2s,3s,4r,5r,6r)-3-[(2s,3r,5s,6r)-3-acetamido-5-hydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-4,5,6-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@@H]1C[C@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](C(O)=O)O[C@@H](O)[C@H](O)[C@H]1O WCDDVEOXEIYWFB-VXORFPGASA-N 0.000 description 1
- ZIIUUSVHCHPIQD-UHFFFAOYSA-N 2,4,6-trimethyl-N-[3-(trifluoromethyl)phenyl]benzenesulfonamide Chemical compound CC1=CC(C)=CC(C)=C1S(=O)(=O)NC1=CC=CC(C(F)(F)F)=C1 ZIIUUSVHCHPIQD-UHFFFAOYSA-N 0.000 description 1
- OSBLTNPMIGYQGY-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;2-[2-[bis(carboxymethyl)amino]ethyl-(carboxymethyl)amino]acetic acid;boric acid Chemical compound OB(O)O.OCC(N)(CO)CO.OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O OSBLTNPMIGYQGY-UHFFFAOYSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- WTLKTXIHIHFSGU-UHFFFAOYSA-N 2-nitrosoguanidine Chemical compound NC(N)=NN=O WTLKTXIHIHFSGU-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- UHPMCKVQTMMPCG-UHFFFAOYSA-N 5,8-dihydroxy-2-methoxy-6-methyl-7-(2-oxopropyl)naphthalene-1,4-dione Chemical compound CC1=C(CC(C)=O)C(O)=C2C(=O)C(OC)=CC(=O)C2=C1O UHPMCKVQTMMPCG-UHFFFAOYSA-N 0.000 description 1
- RNBMPPYRHNWTMA-UAKXSSHOSA-N 5-fluorouridine 5'-monophosphate Chemical compound O1[C@H](COP(O)(O)=O)[C@@H](O)[C@@H](O)[C@@H]1N1C(=O)NC(=O)C(F)=C1 RNBMPPYRHNWTMA-UAKXSSHOSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 108700028369 Alleles Proteins 0.000 description 1
- 108700042778 Antimicrobial Peptides Proteins 0.000 description 1
- 102000044503 Antimicrobial Peptides Human genes 0.000 description 1
- 241000203069 Archaea Species 0.000 description 1
- 101000961203 Aspergillus awamori Glucoamylase Proteins 0.000 description 1
- 101000756530 Aspergillus niger Endo-1,4-beta-xylanase B Proteins 0.000 description 1
- 101900127796 Aspergillus oryzae Glucoamylase Proteins 0.000 description 1
- 101900318521 Aspergillus oryzae Triosephosphate isomerase Proteins 0.000 description 1
- 241000972773 Aulopiformes Species 0.000 description 1
- 108090001008 Avidin Proteins 0.000 description 1
- 108010023063 Bacto-peptone Proteins 0.000 description 1
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 108090000489 Carboxy-Lyases Proteins 0.000 description 1
- 108010084185 Cellulases Proteins 0.000 description 1
- 102000005575 Cellulases Human genes 0.000 description 1
- 108010008885 Cellulose 1,4-beta-Cellobiosidase Proteins 0.000 description 1
- 241000157855 Cinchona Species 0.000 description 1
- 235000001258 Cinchona calisaya Nutrition 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 102000005927 Cysteine Proteases Human genes 0.000 description 1
- 108010005843 Cysteine Proteases Proteins 0.000 description 1
- 230000004544 DNA amplification Effects 0.000 description 1
- 239000003298 DNA probe Substances 0.000 description 1
- 238000001712 DNA sequencing Methods 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 239000003109 Disodium ethylene diamine tetraacetate Substances 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 108010001817 Endo-1,4-beta Xylanases Proteins 0.000 description 1
- 101710132690 Endo-1,4-beta-xylanase A Proteins 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 241000223218 Fusarium Species 0.000 description 1
- 241000223221 Fusarium oxysporum Species 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 101000930822 Giardia intestinalis Dipeptidyl-peptidase 4 Proteins 0.000 description 1
- 229920001503 Glucan Polymers 0.000 description 1
- 108010017544 Glucosylceramidase Proteins 0.000 description 1
- 102000004547 Glucosylceramidase Human genes 0.000 description 1
- 244000068988 Glycine max Species 0.000 description 1
- 235000010469 Glycine max Nutrition 0.000 description 1
- 101100295959 Halobacterium salinarum (strain ATCC 700922 / JCM 11081 / NRC-1) arcB gene Proteins 0.000 description 1
- 241000223198 Humicola Species 0.000 description 1
- 241001480714 Humicola insolens Species 0.000 description 1
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 102000005741 Metalloproteases Human genes 0.000 description 1
- 108010006035 Metalloproteases Proteins 0.000 description 1
- 108090000157 Metallothionein Proteins 0.000 description 1
- GMPKIPWJBDOURN-UHFFFAOYSA-N Methoxyamine Chemical compound CON GMPKIPWJBDOURN-UHFFFAOYSA-N 0.000 description 1
- 102000005431 Molecular Chaperones Human genes 0.000 description 1
- 108010006519 Molecular Chaperones Proteins 0.000 description 1
- OVRNDRQMDRJTHS-RTRLPJTCSA-N N-acetyl-D-glucosamine Chemical compound CC(=O)N[C@H]1C(O)O[C@H](CO)[C@@H](O)[C@@H]1O OVRNDRQMDRJTHS-RTRLPJTCSA-N 0.000 description 1
- OVRNDRQMDRJTHS-FMDGEEDCSA-N N-acetyl-beta-D-glucosamine Chemical group CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O OVRNDRQMDRJTHS-FMDGEEDCSA-N 0.000 description 1
- PWHVEHULNLETOV-UHFFFAOYSA-N Nic-1 Natural products C12OC2C2(O)CC=CC(=O)C2(C)C(CCC2=C3)C1C2=CC=C3C(C)C1OC(O)C2(C)OC2(C)C1 PWHVEHULNLETOV-UHFFFAOYSA-N 0.000 description 1
- 108090000913 Nitrate Reductases Proteins 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- IOVCWXUNBOPUCH-UHFFFAOYSA-N Nitrous acid Chemical compound ON=O IOVCWXUNBOPUCH-UHFFFAOYSA-N 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 108010038807 Oligopeptides Proteins 0.000 description 1
- 102000015636 Oligopeptides Human genes 0.000 description 1
- 108700026244 Open Reading Frames Proteins 0.000 description 1
- 102000007981 Ornithine carbamoyltransferase Human genes 0.000 description 1
- 101710113020 Ornithine transcarbamylase, mitochondrial Proteins 0.000 description 1
- 102100037214 Orotidine 5'-phosphate decarboxylase Human genes 0.000 description 1
- 108010055012 Orotidine-5'-phosphate decarboxylase Proteins 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 241000228143 Penicillium Species 0.000 description 1
- 108010064785 Phospholipases Proteins 0.000 description 1
- 102000015439 Phospholipases Human genes 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 108020004518 RNA Probes Proteins 0.000 description 1
- 239000003391 RNA probe Substances 0.000 description 1
- 101000968489 Rhizomucor miehei Lipase Proteins 0.000 description 1
- 108010022999 Serine Proteases Proteins 0.000 description 1
- 102000012479 Serine Proteases Human genes 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 1
- 101100370749 Streptomyces coelicolor (strain ATCC BAA-471 / A3(2) / M145) trpC1 gene Proteins 0.000 description 1
- 241000187391 Streptomyces hygroscopicus Species 0.000 description 1
- 101710172711 Structural protein Proteins 0.000 description 1
- 208000037065 Subacute sclerosing leukoencephalitis Diseases 0.000 description 1
- 206010042297 Subacute sclerosing panencephalitis Diseases 0.000 description 1
- 239000008051 TBE buffer Substances 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 241000223259 Trichoderma Species 0.000 description 1
- 108010039203 Tripeptidyl-Peptidase 1 Proteins 0.000 description 1
- 102100034197 Tripeptidyl-peptidase 1 Human genes 0.000 description 1
- 108091023045 Untranslated Region Proteins 0.000 description 1
- 102000003990 Urokinase-type plasminogen activator Human genes 0.000 description 1
- 108090000435 Urokinase-type plasminogen activator Proteins 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 238000005273 aeration Methods 0.000 description 1
- 229930013930 alkaloid Natural products 0.000 description 1
- 101150069003 amdS gene Proteins 0.000 description 1
- 238000012870 ammonium sulfate precipitation Methods 0.000 description 1
- 230000001887 anti-feedant effect Effects 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 101150008194 argB gene Proteins 0.000 description 1
- 210000004507 artificial chromosome Anatomy 0.000 description 1
- 238000003149 assay kit Methods 0.000 description 1
- 239000005667 attractant Substances 0.000 description 1
- 235000020054 awamori Nutrition 0.000 description 1
- 101150103518 bar gene Proteins 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- ZYGHJZDHTFUPRJ-UHFFFAOYSA-N benzo-alpha-pyrone Natural products C1=CC=C2OC(=O)C=CC2=C1 ZYGHJZDHTFUPRJ-UHFFFAOYSA-N 0.000 description 1
- 239000003139 biocide Substances 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- 210000002421 cell wall Anatomy 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000002962 chemical mutagen Substances 0.000 description 1
- 230000031902 chemoattractant activity Effects 0.000 description 1
- 238000011098 chromatofocusing Methods 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 235000001671 coumarin Nutrition 0.000 description 1
- 150000004775 coumarins Chemical class 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 230000001066 destructive effect Effects 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 150000002016 disaccharides Chemical group 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- 235000019301 disodium ethylene diamine tetraacetate Nutrition 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 108010091371 endoglucanase 1 Proteins 0.000 description 1
- 108010091384 endoglucanase 2 Proteins 0.000 description 1
- 108010092413 endoglucanase V Proteins 0.000 description 1
- 230000037149 energy metabolism Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 238000001976 enzyme digestion Methods 0.000 description 1
- 125000000219 ethylidene group Chemical group [H]C(=[*])C([H])([H])[H] 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000010195 expression analysis Methods 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 229930003935 flavonoid Natural products 0.000 description 1
- 235000017173 flavonoids Nutrition 0.000 description 1
- 150000002215 flavonoids Chemical class 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 230000037433 frameshift Effects 0.000 description 1
- 230000000855 fungicidal effect Effects 0.000 description 1
- 239000000417 fungicide Substances 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 238000001502 gel electrophoresis Methods 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 238000012239 gene modification Methods 0.000 description 1
- 230000005017 genetic modification Effects 0.000 description 1
- 235000013617 genetically modified food Nutrition 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 125000002791 glucosyl group Chemical group C1([C@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)* 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 229960000789 guanidine hydrochloride Drugs 0.000 description 1
- PJJJBBJSCAKJQF-UHFFFAOYSA-N guanidinium chloride Chemical compound [Cl-].NC(N)=[NH2+] PJJJBBJSCAKJQF-UHFFFAOYSA-N 0.000 description 1
- 125000001475 halogen functional group Chemical group 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 229940014041 hyaluronate Drugs 0.000 description 1
- 108010002685 hygromycin-B kinase Proteins 0.000 description 1
- 239000002955 immunomodulating agent Substances 0.000 description 1
- 230000002584 immunomodulator Effects 0.000 description 1
- 229940121354 immunomodulator Drugs 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 239000002917 insecticide Substances 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 235000019626 lipase activity Nutrition 0.000 description 1
- 101150039489 lysZ gene Proteins 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 238000012269 metabolic engineering Methods 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 239000006151 minimal media Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 229940045641 monobasic sodium phosphate Drugs 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 229910000403 monosodium phosphate Inorganic materials 0.000 description 1
- 235000019799 monosodium phosphate Nutrition 0.000 description 1
- 229950006780 n-acetylglucosamine Drugs 0.000 description 1
- 239000002858 neurotransmitter agent Substances 0.000 description 1
- 101150095344 niaD gene Proteins 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 125000006501 nitrophenyl group Chemical group 0.000 description 1
- 239000002777 nucleoside Substances 0.000 description 1
- 125000003835 nucleoside group Chemical group 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 229920002113 octoxynol Polymers 0.000 description 1
- 108090000021 oryzin Proteins 0.000 description 1
- KHPXUQMNIQBQEV-UHFFFAOYSA-N oxaloacetic acid Chemical compound OC(=O)CC(=O)C(O)=O KHPXUQMNIQBQEV-UHFFFAOYSA-N 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 101150112985 parT gene Proteins 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 108010082527 phosphinothricin N-acetyltransferase Proteins 0.000 description 1
- 238000007747 plating Methods 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920000768 polyamine Polymers 0.000 description 1
- 229930001119 polyketide Natural products 0.000 description 1
- 125000000830 polyketide group Chemical group 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 239000003910 polypeptide antibiotic agent Substances 0.000 description 1
- 229910052573 porcelain Inorganic materials 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000000644 propagated effect Effects 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 230000017854 proteolysis Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 101150108454 pytG gene Proteins 0.000 description 1
- 125000003410 quininyl group Chemical group 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000022532 regulation of transcription, DNA-dependent Effects 0.000 description 1
- 230000003252 repetitive effect Effects 0.000 description 1
- 230000003362 replicative effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 239000003128 rodenticide Substances 0.000 description 1
- 235000019515 salmon Nutrition 0.000 description 1
- 239000012266 salt solution Substances 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 230000024053 secondary metabolic process Effects 0.000 description 1
- 238000012163 sequencing technique Methods 0.000 description 1
- 238000002741 site-directed mutagenesis Methods 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- AJPJDKMHJJGVTQ-UHFFFAOYSA-M sodium dihydrogen phosphate Chemical compound [Na+].OP(O)([O-])=O AJPJDKMHJJGVTQ-UHFFFAOYSA-M 0.000 description 1
- FQENQNTWSFEDLI-UHFFFAOYSA-J sodium diphosphate Chemical compound [Na+].[Na+].[Na+].[Na+].[O-]P([O-])(=O)OP([O-])([O-])=O FQENQNTWSFEDLI-UHFFFAOYSA-J 0.000 description 1
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 1
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 1
- 229940048086 sodium pyrophosphate Drugs 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000001694 spray drying Methods 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-N sulfuric acid Substances OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 150000003505 terpenes Chemical class 0.000 description 1
- 235000007586 terpenes Nutrition 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 235000019818 tetrasodium diphosphate Nutrition 0.000 description 1
- 239000001577 tetrasodium phosphonato phosphate Substances 0.000 description 1
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 229910021654 trace metal Inorganic materials 0.000 description 1
- 108091006106 transcriptional activators Proteins 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 150000003626 triacylglycerols Chemical class 0.000 description 1
- YNJBWRMUSHSURL-UHFFFAOYSA-N trichloroacetic acid Chemical compound OC(=O)C(Cl)(Cl)Cl YNJBWRMUSHSURL-UHFFFAOYSA-N 0.000 description 1
- 108010039189 tripeptidyl-peptidase 2 Proteins 0.000 description 1
- 101150016309 trpC gene Proteins 0.000 description 1
- 229960005356 urokinase Drugs 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/37—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from fungi
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/37—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from fungi
- C07K14/38—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from fungi from Aspergillus
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/37—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from fungi
- C07K14/39—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from fungi from yeasts
- C07K14/40—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from fungi from yeasts from Candida
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/52—Genes encoding for enzymes or proenzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P1/00—Preparation of compounds or compositions, not provided for in groups C12P3/00 - C12P39/00, by using microorganisms or enzymes
- C12P1/02—Preparation of compounds or compositions, not provided for in groups C12P3/00 - C12P39/00, by using microorganisms or enzymes by using fungi
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P21/00—Preparation of peptides or proteins
- C12P21/02—Preparation of peptides or proteins having a known sequence of two or more amino acids, e.g. glutathione
Description
本発明は、酵素−欠失アスペルギラス・ニガー変異体株における異種の生物学的物質の生成方法、酵素−欠失アスペルギラス・ニガー変異体株の入手方法、及び酵素−欠失アスペルギラス・ニガー変異体株に関する。
アスペルギラス・ニガーは、多量のグルコアミラーゼを分泌する。しかしながら、高められたタンパク質発現及び分泌の所望する形質を有するアスペルギラス・ニガー宿主は、好結果をもたらす発酵の最も所望する特徴を必ずしも有する必要はない。発酵は、興味ある生物学的物質の回収及び精製の間、除去を必要とする複数の酵素の分泌のために、最適ではなく、又は酵素は生物学的物質と同時精製することができる。
Pedersen など., 2000, Metabolic Engineering 2: 34-41, 及び WO 00/50576号は、アスペルギラス・ニガーのグルコアミラーゼ−生成株におけるオキサロ酢酸ヒドロラーゼ(EC 3.7.1.1)コードのオキサロ酢酸ヒドロラーゼ(oah)遺伝子の破壊を開示し、ここで得られる株シュウ酸を生成することができなかった。
興味ある生物学的物質の回収及び下流のプロセッシングを複雑化することができる酵素の生成を欠くと共に、商業的量の生物学的物質の発現のための能力を有する。改良されたアスペルギラス・ニガー宿主を提供することが本発明の目的である。
本発明は、異種の生物学的物質の生成方法に関し、ここで前記方法は、
(a)前記異種の生物学的物質の生成のために適切な培地において親アスペルギラス・ニガー株の変異体を培養し、ここで(i)前記変異体株は、前記異種の生物学的物質をコードする第1のヌクレオチド配列、並びにglaA、及びasa, amyA, amyB, prtT及びoahから成る群から選択された少なくとも1つの遺伝子の修飾を含んで成る1又は複数の第2のヌクレオチド配列を含んで成り、そして(ii)前記変異体株は、同一の条件下で培養される場合、親アスペルギラス・ニガーに比較して、グルコアミラーゼ、並びに酸安定性α−アミラーゼ、中性α−アミラーゼA及び中性α−アミラーゼB、プロテアーゼ及びシュウ酸ヒドロラーゼから成る群から選択された少なくとも1つの酵素の生成を欠いており;そして
(b)前記培養培地から前記異種の生物学的物質を回収することを含んで成る。
本発明はまた、酵素−欠失性アスペルギラス・ニガー変異体株、及びその生成方法にも関する。
本発明は、異種の生物学的物質の生成方法に関し、ここで前記方法は、(a)前記異種の生物学的物質の生成のために適切な培地において親アスペルギラス・ニガー株の変異体を培養し、ここで(i)前記変異体株は、前記異種の生物学的物質をコードする第1のヌクレオチド配列、並びにglaA、及びasa, amyA, amyB, prtT及びoahから成る群から選択された少なくとも1つの遺伝子の修飾を含んで成る1又は複数の第2のヌクレオチド配列を含んで成り、そして(ii)前記変異体株は、同一の条件下で培養される場合、親アスペルギラス・ニガーに比較して、グルコアミラーゼ、並びに酸安定性α−アミラーゼ、中性α−アミラーゼA及び中性α−アミラーゼB、プロテアーゼ及びシュウ酸ヒドロラーゼから成る群から選択された少なくとも1つの酵素の生成を欠いており;そして(b)前記培養培地から前記異種の生物学的物質を回収することを含んで成る。
用語“酸安定性α−アミラーゼ活性”とは、酸性pH範囲において最適な活性を有するα−アミラーゼ活性として本明細書において定義される。本発明に関しては、酸安定性α―アミラーゼ活性は、pH4.0でSigma Chemical Co.キット477を用いて、基質として4,6−エチリデン(G7)−p−ニトロフェニル(G1)−α−D−ニトロフェニル(G1)−α−D−マルトヘプタシドを用いて決定される。
もう1つの好ましい観点においては、変異体は、glaA, amyB及びoahの修飾を包含する。もう1つの好ましい観点においては変異体は、glaA, prtT及びoahの修飾を包含する。
もう1つの好ましい観点においては、変異体は、glaA, asa, amyA, amyB, prtT及びoahを包含する。
選択のアスペルギラス・ニガー株においてその対応する遺伝子を修飾するための酵素を生成する他の微生物源からの興味ある酵素の生成に関与する本明細書に記載されるヌクレオチド配列に対して相同か又は相補的なヌクレオチド配列が、使用され得る。
好ましい観点においては、アスペルギラス・ニガー変異体株における酵素の生成に関与する遺伝子の修飾は、選択マーカーにより標識されていない。
本発明のさらなる観点においては、アスペルギラス・ニガー株の変異体は、特定の生物学的物質の生成、回収又は適用に対して有害な物質をコードする他の酵素の修飾、例えば欠失又は破壊を含むことができる。
もう1つの好ましい観点においては、生物ポリマーは、ポリサッカリドである。ポリサッカリドは、いずれかのポリサッカリド、例えばムコポリサッカリド(例えば、ヘパリン及びヒアルロン酸)及び窒素含有ポリサッカリド(例えば、キチン)であり得るが、但しそれらだけには限定されない。より好ましい態様においては、ポリサッカリドはヒアルロン酸である。“ヒアルロン酸”は、β−1,4及びβ−1,3グリコシド結合を変えることによって一緒に結合される、N−アセチルグルコサミン(GlcNAc)及びグルクロン酸(GlcUA)の反復二糖単位から構成される、硫酸化されていないグリコサミノグリカンとして、本明細書においては定義される。ヒアルロン酸はまた、ヒアルロナン、ヒアルロネート又はHAとして知られている。もう1つの好ましい観点においては、ポリサッカリドは、キチンである。もう1つの好ましい観点においては、ポリサッカリドは、ヘパリンである。
二次代謝物は、アルカロイド、クマリン、フラボノイド、ポリケチド、キニン、ステロイド、ペプチド又はテルペンであり得るが、但しそれらだけには限定されない。好ましい態様においては、二次代謝物は、抗生物質、摂食阻害剤、誘引剤、殺菌剤、抗菌剤、ホルモン、殺昆虫剤又は殺鼠薬である。
制御配列はまた、適切なリーダー配列、すなわち、アスペルギラス・ニガー株による翻訳のために重要であるmRNAの非翻訳領域でもあり得る。リーダー配列は、異種生物学的物質をコードするヌクレオチド配列の5’側末端に作用可能に連結される。アスペルギラス・ニガー株において機能的であるいずれかのリーダー配列が、本発明に使用され得る。
制御配列はまた、ポリアデニル化配列、すなわちヌクレオチド配列の3’末端に作用可能に連結され、そして転写される場合、転写されたmRNAにポリアデノシン残基を付加するためにシグナルとしてアスペルギラス・ニガー株により認識される配列であり得る。アスペルギラス・ニガー株において機能するいずれかのポリアデニル化配列が、本発明において使用され得る。
好ましいポリアデニル化配列は、アスペルギラス・オリザエTAKAアミアーゼ、アスペルギラス・ニガーグルコアミラーゼ、アスペルギラス・ニジュランスアントラニル酸シンターゼ及びアスペルギラス・ニガーα−グルコシダーゼをコードする遺伝子から得られる。
上記の種々の核酸及び制御配列は、1又は複数の便利な制限部位で異種生物学的物質をコードするヌクレオチド配列の挿入又は置換を可能にするためにそれらの部位を含むことができる組換え発現ベクターを生成するために一緒に連結され得る。他方では、異種生物学的物質をコードするヌクレオチド配列は、前記配列又は前記配列を含んで成る核酸構造体を、発現のための適切なベクター中に挿入することによって発現され得る。発現ベクターを創造する場合、そのコード配列はベクターに位置し、その結果、コード配列は発現及びたぶん分泌のための適切な制御配列により作用可能に連結される。
“導入”とは、核酸配列を含んで成るベクターをアスペルギラス・ニガー株中に導入することを意味し、その結果、前記ベクターは染色体組み込み体として、又は自己複製染色体ベクターとして維持される。組み込みは一般的に、ヌクレオチド配列が株中に安定して維持される場合、好都合であると思われる。染色体中へのベクターの組み込みは、相同組換え、非相同組換え又はトランスポジションにより起こる。
本発明はさらに、次の例により記載されるが、それらは本発明の範囲を制限するものではない。
DNA配列決定は、ABI 3700 Sequencing (Applied Biosystems,Inc., Foster City, CA)により行われた。
株:
すべての株は、アスペルギラス・ニガーBo−1(DSM 12665)に由来する。アスペルギラス・ニガーBo−1は、α−1,6−トランスグルコシダーゼ活性をもたらさないα−1,6−トランスグルコシダーゼ遺伝子の突然変異を含んで成る。
最少培地は、1L当たり6 g のNaNO3, 0.52 gの KCI, 1.52 g のKH2PO4, 20 g のNoble寒天, 10 gのグルコース, 0.5g のMgSO4・7H2O, 及び 1 mlのCove 微量元素から構成された。
Coveプレートは、1L当たり342. 3 g のスクロース, 20 mlのCove塩(50X), 10 mM のアセトアミド, 15 mM のCsCl, 及び25 g のNoble 寒天から構成された。
50×COVE塩溶液は、1L当たり、26gのKCl、26gのMgSO4・7H2O, 76gのKH2PO4及び50mlのCove微量元素から構成された。
AMG微量元素溶液は、1L当たり、14.3 g のZnS04・7H20, 2.5 g の CuSO4・5H2O, 0.5 g のNiC12・6H20, 13.8 gのFeS04・7H20, 8.5 g のMnSO4 ・H20,及び3 g のクエン酸から成った。
STCは、0.8Mのソルビトール、50mMのトリス(pH8)、25mMのCaCl2から構成された。
SPTCは、40%のPEG4000、0.8Mのソルビトール、50mMのトリス(pH8)、50mMのCaCl2から構成された。
SPCは、1L当たり40%PEG 4000、0.8Mのソルビトール及び50mMのCaCl2(pH4.5)から構成された。
スターチアズールプレートは、1L当たり0.1 gのグルコース, 1 gのKH2PO4, 0.5 g のMgS04, 0.5 g の KCI, 3 gの NaNO3, 0.1 gの酵母抽出物, 1 ml of Cove微量元素, 5 g の スターチアズール, 15 g のNoble寒天, 及び100 mMのグリシンpH 2.9から構成された。
次の例に記載される個々の破壊カセット20μgを、制限酵素により消化し、そして破壊のために使用されるべきフラグメントを切除し、そしてQIAEXII Gel Extraction Kit(QIAGEN, Inc., Chatsworth, CA)を用いて、1%アガロース−50mMのトリス塩基−50mMのボレート−0.1mMの二ナトリウムEDTA緩衝液(TBE)ゲルから精製した。合計体積を、無菌ガラス蒸留された水において20μlにし、そして4種の形質転換の間に流した。
アスペルギラス・ニガー菌糸体を、5%のグルコース(及び適用できる場合、10mMのウリジン)により補充されたYP培地5mlを含む15mmプレートから収穫し、濾過し、そしてサイドアームフラスコ及び磁器を用いて、10mMのトリス(pH7.4)−0.1mMのEDTA(pH8)(TE)によりすすぎ、そして最後に、微小遠心分離管に入れ、高速バキューム下で1時間、乾燥した。
アスペルギラス・ニガーBo−1 DNAをWahleithner など., 1996, Current Genetics. 29: 395-403の方法に従って、グアニジン塩酸塩における溶解により単離し、続いてQiagen Maxiprep 過ラム(QIAGEN, Inc., Chatsworth, CA)上でその製造業者による記載のようにして精製した。アスペルギラス・ニガーBo−1のゲノムライブラリーを、EMBL4(Clonetech, Palo Alto, CA)において、その製造業者の説明書に従って創造した。アスペルギラス・ニガーBo−1ゲノムDNAを、Sau3Aにより部分的に消化した。消化の後、DNAを、分離用低融点アガロースゲル上で電気泳動し、そして8〜23kbのDNAを含む領域をゲルからスライスした。
EMBL4に含まれるアスペルギラス・ニガーBo−1のゲノムライブラリーからの約26,500個のプラークを、ナイロンフィルター上にレプリカプレートし、そしてアスペルギラス・ニジュランスのpyrG遺伝子からの1.4kbのフラグメントによりプローブした。いくつかの陽性クローンを、製造業者により記載の通りにして、精製し、そして増殖した。陽性クローンからのファージDNAを、Qiagen lambda Mini Prep Kit (QIAGEN,Inc., Chatsworth, CA)を用いて単離した。ファージDNAを、いくつかの制限酵素により消化し、続いて、pyrG遺伝子を含むフラグメントを同定するためにサザン分析した。クローン7bと命名された1つのクローンは、3.5kbのXbaIフラグメント上のプロモーター及びターミネーター配列の両者を包含する、アスペルギラス・ニガーpyrG遺伝(配列番号1(DNA配列)及び2(推定されるアミノ酸配列))を含んだ。
プライマー1:5’−GGGACTAGTGGATCGAAGTTCTGATGGTTA−3’(配列番号3)
プライマー2:5’−ATACCGCGGGTTTCAAGGATGGAGATAGGA−3’(配列番号4)
582bpのPCR生成物を、SpeI及びKspIにより消化し、そして下記のようにして直接使用した。
次の例に記載される遺伝子破壊は、選択マーカーとしてアスペルギラス・ニガーpyrG遺伝子を用いた。pyrG遺伝子は、ウリジンを添加しないでウリジン栄養要求株の増殖を可能にするオロトジン−5’−ホスフェートデカルボキシラーゼをコードする。pyrGの反復使用を、例4に記載されるようにマーカーの末端への反復配列の付加により可能にした。pyrGの切除は、5−FOA上での選択に基づいて直線的な反復体間での相同組換えにより生じた(d’Enfert, 1996, Current Genetics 30: 76-82)。
アスペルギラス・ニガーグルコアミラーゼ(gla)遺伝子(配列番号5:DNA配列、及び6:推定されるアミノ酸配列)を、8kbのフラグメントとして、例3に記載されるゲノムλ−ライブラリーから単離し、そしてPUC118(Roche Diagnostics Corporation, Mannheim, Germany)中にサブクローン化し、pJRoy13を生成した。アスペルギラス・ニガーグルコアミラーゼ遺伝子及び1.8kbのフランギングDNAを含むpJRoy13からの4kbのSpeIフラグメントを、pBluescriptSK+ (Stratagene, La Jolla, CA)中に挿入し、pJRoy17(図3)を生成した。
プライマー3:5’− ACTAGTGGCCCTGTACCCAGA−3’(配列番号7)
プライマー4:5’− GCATGCATTGCTGAGGTGTAATGATG−3’(配列番号8)
グルコアミラーゼ遺伝子プロモータープローブを、例2に記載のようにして単離し、そしてラベルした。
アスペルギラス・ニガーグルコアミラーゼ遺伝子ターミネーターを、3’末端でSpeI部位にハイブリダイズするプライマー5、及び5’末端にSphI部位を付加するプライマー6により、800bpのフラグメントとしてpJRoy17から増幅した。
プライマー5:5’− GAGGTCGACGGTATCGATAAG−3’(配列番号9)
プライマー6:5’− GCATGCAGATCTCGAGAATACACCGTTCCTCAG−3’(配列番号10)
グルコアミラーゼ遺伝子ターミネーターを含む800bpのフラグメントを、精製し、そして下記のようにして直接使用した。
プローブを、アスペルギラス・ニガーグルコアミラーゼ及びpyrG遺伝子に対して生成した。上記プライマー3及び5を用いて、pJRoy17からのgla遺伝子(プロモーター及びターミネーターを包含する)をPCR増幅し、そしてプライマー1及び2(例4を参照のこと)を用いて、例4に記載される同じ方法を用いて、pJRoy10からpyrGターミネーター配列を増幅した。プローブを、例2に記載のようにして単離し、そしてラベルした。
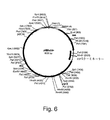
アスペルギラス・ニガー酸安定性α−アミラーゼ遺伝子(asa)の一部を単離し、そしてアメリカ特許第5,252,726号に記載のようにして、pUC19(Roche Diagnostics Corporation, Mannheim, Germany)中にクローン化した。前記酸安定性α−アミラーゼ遺伝子の一部の開始コドンの上流の346bpを、酸安定性アミラーゼ遺伝子の一部を含むpUC19から、HpaIによる消化により切除し、そしてpMBin01(図6)を創造した。pMBin04+の二重消化を、SmaI及びSpeIにより行い、そして4237bpのSmaI/SpeIフラグメントを、1%アガロース−TBEゲル上での電気泳動に続いて、QIAEX11 Gel Extraction Kitを用いて単離した。その4237bpのSmaI/SpeIフラグメントは、酸安定性α−アミラーゼ遺伝子の5’末端、pyrGターミネーター、全pyrG遺伝子(ターミネーターを包含する)、及び酸安定性α−アミラーゼ遺伝子の3’末端から成った。
プライマー7:5’− CTCATTGGCCGAAACTCCGAT−3’(配列番号11)
プライマー8:5’− AGCAGACGATGTCCTGAGCTG−3’(配列番号12)
522bpのプローブを、例2に記載のようにして単離し、そしてラベルした。
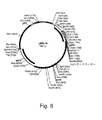
アスペルギラス・ニガーparT遺伝子(配列番号13:DNA配列、及び14:推定されるアミノ酸配列)を、WO00/20596号に記載される2種のオーバーラッピングするクローン、NcE1.4及びCIE1.8を用いて構成した(pMBin09、図7)。NcE, CIE1.8及びpZeRO-2(Invitrogen, Carlsbad, CA)を、PstIにより消化し、それぞれクローンの5’及び3’末端でPstI部位を生成し、そして複数のクローニング部位でpZeRO-2を洗浄化した。両prtTクローンの共有される領域におけるSspI部位を用いて、三元連結を、PstI部位でpZeRO-2中にPstI/SspIクローンフラグメントを連結することにより行い、pMBin09をもたらした。
プライマー9:5’− TGTGATTGAGGTGATTGGCG−3’(配列番号15)
プライマー10:5’− TCAGCCACACCTGCAAAGGC−3’(配列番号16)
プローブを、例2に記載のようにして単離し、そしてラベルし、そしてそのプローブは破壊の下流に232bpのprtTコード配列を含んだ。
アスペルギラス・ニガー中性α−アミラーゼ遺伝子amyA及びamyBを、アメリカ特許第5,252, 726号 (NA1=amyA及びNA2=amyB)に開示されるようにしてクローン化した。
プライマー11:5’−GGCAGCAGGATATGTAAGTCG−3’(配列番号19)
プライマー12:5’−CACTGTAATCGACTGAGCTAC−3’(配列番号20)
アスペルギラス・ニガーamyA遺伝子配列はその3’末端を除いて、amyBと実質的に同一であるので(Korman など, 1990, Current Genetics 17: 203-212)、例10に使用される破壊構造体及びプロトコールが適用された。アスペルギラス・ニガーMBin117を、amyA遺伝子(配列番号21:DNA配列、及び22:推定されるアミノ酸配列)を破壊するために、pMBin03からのEcoRI/AvrIIフラグメントにより、例1に記載されるプロトコールに従って形質転換した。
ゲノムDNAを、4個の形質転換体、及び対照としてのアスペルギラス・ニガーMBin117から単離し、そして例2に記載される方法を用いて、サザン分析にゆだねた。ゲノムDNAを、EcoRI及びBspLU11Iにより消化し、そして例10に記載のようにしてプローブした。amyB遺伝子に対応する2.7kbのバンド、及びamyA遺伝子を表わす、わずかに大きなバンドが野生型アスペルギラス・ニガーBo−1株に存在した。
アスペルギラス・ニガーシュウ酸ヒドロラーゼ(oah)遺伝子(配列番号23:DNA配列、及び24:推定されるアミノ酸配列)を、WO00/50576号に記載される方法に従ってクローン化した。プラスミドpHP1を、WO00/50576号に記載のようにして構成した。
プライマー13:5’−CTACGACATGAAGACCAACGC−3’(配列番号25)
プライマー14:5’−GCACCGTTCTCCACCATGTTG−3’(配列番号26)
グルコアミラーゼ、酸安定性のα−アミラーゼ、中性α−アミラーゼ、及びプロテアーゼを生成する一般宿主アスペルギラス・ニガー株の能力を、振盪フラスコ及び/又は発酵器において株を培養することにより評価した。アスペルギラス・ニガーBo-1を、対照として用いた。
約104/mlの密度でのアスペルギラス・ニガー株の分生子を、5%グルコースにより補充されたYP培地20mlを含む125mlの振盪フラスコ中に接種した。振盪フラスコを、37℃及び200rpmで3〜6日間インキュベートした。振盪フラスコ培養物のサンプルを、3〜6日目に除き、そして遠心分離し、酵素アッセイについての上清液を生成した。
酸安定性及び中性α−アミラーゼ活性を、Sigmaα−アミラーゼ基質(Sigma Kit # 577, Sigma Chemical Co. , St. Louis, MO)を用いて30℃で、それぞれpH4.5及び7.0で測定した。検出は405nmであった。FungamylTMを、標準として使用し、そして活性をFAU/mlで報告した。
アスペルギラス・ニガーMBin114におけるprtT遺伝子の欠失により、合計のプロテアーゼ活性は、アスペルギラス・ニガーBo-1の約20%に低下した。MBin114の6日目の発酵サンプルは、692のプロテアーゼ活性を有し、そしてBo-1は3953蛍光単位/mlであった。
カンジダ・アンタルクチカリパーゼB遺伝子(配列番号27:DNA配列、及び28:推定されるアミノ酸配列)を、アメリカ特許第6,020,180号に記載のようにしてクローン化した。リパーゼB遺伝子を含むプラスミドpMT1335を、Hoegh など., in Can. J. Bot. 73 (Suppl. 1) :S869-S875 (1995)による記載のようにして構成した。アスペルギラス・ニジュランスamdS遺伝子を含むプラスミドpTOC90を、WO91/17243号に記載のようにして構成した。プラスミドpMT1335及びpTOC90を、例1に記載されるプロトコールに従って、アスペルギラス・ニガーMBin114中に同時形質転換し、そして形質転換体をアセトアミド上で選択した。
対照としてのアスペルギラス・ニガーMBin114及びアスペルギラス・ニガーBo-1を、例13に記載のようにして、2Lの発酵器において培養した。
一般的なプロテアーゼ活性を、例9に記載のようにして測定した。
シタリジウム・サーモフィラス(Scytalidium thermophilum)カタラーゼ遺伝子(配列番号29:DNA配列、及び30:推定されるアミノ酸配列)を、アメリカ特許第5,646,025号に記載のようにしてクローン化した。カタラーゼ遺伝子を含むプラスミドpDM153を、アメリカ特許第5,646,025号に記載のようにして構成した。プラスミドpDM153を用いて、例1に記載されるプロトコールに従って、アスペルギラス・ニガー株MBin114, MBin118及びMBin120を形質転換した。
図15は、アスペルギラス・ニガー一般宿主株MBin114, MBin118及びMBin120におけるシタリジウム・サーモフィラムカタラーゼ生成の比較を示す。酵素生成における明白な変化は、試験されるいずれの株にも観察されなかった。
種々の文献が本明細書に引用されており、それらの開示は引用により本明細書に組み込まれている。
Claims (15)
- 異種のポリペプチドの生成方法であって、
(a)前記異種の生物学的物質の生成のために適切な培地において親アスペルギラス・ニガー(Aspergilus niger)株の変異体を培養し、ここで(i)前記変異体株は、前記異種のポリペプチドをコードする第1のヌクレオチド配列、並びにglaA、asa、amyA、amyB、prtT及びoahの修飾を含んで成る第2のヌクレオチド配列を含んで成り、そして(ii)前記変異体株は、同一の条件下で培養される場合、親アスペルギラス・ニガーに比較して、グルコアミラーゼ、酸安定性α−アミラーゼ、中性α−アミラーゼA及び中性α−アミラーゼB、プロテアーゼ及びシュウ酸ヒドロラーゼの生成を欠いており,ここで前記修飾は、(1)遺伝子又は制御要素中の1又は複数のヌクレイチドの導入、置換又は除去、(2)遺伝子破壊、(3)遺伝子転換、(4)遺伝子欠失、或いは(5)ランダム又は特異的変異誘発として定義され;そして
(b)前記培養培地から前記異種の生物学的物質を回収する;
ことを含んで成る方法。 - 前記変異体株が、同一の条件下で培養される場合、親アスペルギラス・ニガーに比較して、グルコアミラーゼ、酸安定性α−アミラーゼ、中性α−アミラーゼA及び中性α−アミラーゼB、プロテアーゼ及びシュウ酸ヒドロラーゼを少なくとも25%少なく生成する、請求項1に記載の方法。
- 前記変異体株が、同一の条件下で培養される場合、親アスペルギラス・ニガーに比較して、グルコアミラーゼ、酸安定性α−アミラーゼ、中性α−アミラーゼA及び中性α−アミラーゼB、プロテアーゼ及びシュウ酸ヒドロラーゼを完全に欠く、請求項1又は2に記載の方法。
- 前記変異体株がさらに、タンパク質分解活性をコードする1又は複数の遺伝子の修飾を含んで成り、ここで前記修飾は、(1)遺伝子又は制御要素中の1又は複数のヌクレイチドの導入、置換又は除去、(2)遺伝子破壊、(3)遺伝子転換、(4)遺伝子欠失、或いは(5)ランダム又は特異的変異誘発として定義される、請求項1〜3のいずれか1項に記載の方法。
- 前記変異体株が、カルボヒドラーゼ、カルボキシペプチダーゼ、カタラーゼ、セルラーゼ、キチナーゼ、クチナーゼ、シクロデキストリングリコシルトランスフェラーゼ、デオキシリボヌクレアーゼ、エステラーゼ、ガラクトシダーゼ、β−ガラクトシダーゼ、グルコースオキシダーゼ、グルコシダーゼ、ハロペルオキシダーゼ、ヘミセルラーゼ、インバーターゼ、イソメラーゼ、ラッカーゼ、リガーゼ、リパーゼ、リアーゼ、マンノシダーゼ、オキシダーゼ、ペクチン分解酵素、ペルオキシダーゼ、フィターゼ、フェノールオキシダーゼ、ポリフェノールオキシダーゼ、リボヌクレアーゼ、トランスフェラーゼ、α−1,6−トランスグルコシダーゼ、トランスグルタミナーゼ及びキシラナーゼから成る群から選択される酵素をコードする1又は複数の遺伝子の修飾をさらに含んで成り、ここで前記修飾は、(1)遺伝子又は制御要素中の1又は複数のヌクレイチドの導入、置換又は除去、(2)遺伝子破壊、(3)遺伝子転換、(4)遺伝子欠失、或いは(5)ランダム又は特異的変異誘発として定義される、請求項1〜4のいずれか1項に記載の方法。
- 異種のポリペプチドをコードする第1のヌクレオチド配列、並びにglaA、asa,amyA,amyB,prtT及びoahの修飾を含んで成る第2のヌクレオチド配列を含んで成る、親アスペルギラス・ニガー株の変異体であって、同一の条件下で培養される場合、親アスペルギラス・ニガーに比較して、グルコアミラーゼ、酸安定性α−アミラーゼ、中性α−アミラーゼA,中性α−アミラーゼB、プロテアーゼ及びシュウ酸ヒドロラーゼを欠いていることを特徴とする変異体株。
- 前記変異体株が、同一の条件下で培養される場合、親アスペルギラス・ニガーに比較して、グルコアミラーゼ、酸安定性α−アミラーゼ、中性α−アミラーゼA、中性α−アミラーゼB、プロテアーゼ及びシュウ酸ヒドロラーゼを少なくとも25%少なく生成する、請求項6に記載の変異体株。
- 前記変異体株が、同一の条件下で培養される場合、親アスペルギラス・ニガーに比較して、グルコアミラーゼ、酸安定性α−アミラーゼ、中性α−アミラーゼA、中性α−アミラーゼB、プロテアーゼ及びシュウ酸ヒドロラーゼを完全に欠く、請求項6又は7に記載の変異体株。
- 前記変異体株がさらに、タンパク質分解活性をコードする1又は複数の遺伝子の修飾を含んで成り、ここで前記修飾は、(1)遺伝子又は制御要素中の1又は複数のヌクレイチドの導入、置換又は除去、(2)遺伝子破壊、(3)遺伝子転換、(4)遺伝子欠失、或いは(5)ランダム又は特異的変異誘発として定義される、請求項6〜8のいずれか1項に記載の変異体株。
- 前記変異体株が、カルボヒドラーゼ、カルボキシペプチダーゼ、カタラーゼ、セルラーゼ、キチナーゼ、クチナーゼ、シクロデキストリングリコシルトランスフェラーゼ、デオキシリボヌクレアーゼ、エステラーゼ、ガラクトシダーゼ、β−ガラクトシダーゼ、グルコースオキシダーゼ、グルコシダーゼ、ハロペルオキシダーゼ、ヘミセルラーゼ、インバーターゼ、イソメラーゼ、ラッカーゼ、リガーゼ、リパーゼ、リアーゼ、マンノシダーゼ、オキシダーゼ、ペクチン分解酵素、ペルオキシダーゼ、フィターゼ、フェノールオキシダーゼ、ポリフェノールオキシダーゼ、リボヌクレアーゼ、トランスフェラーゼ、α−1,6−トランスグルコシダーゼ、トランスグルタミナーゼ及びキシラナーゼから成る群から選択される酵素をコードする1又は複数の遺伝子の修飾をさらに含んで成り、ここで前記修飾は、(1)遺伝子又は制御要素中の1又は複数のヌクレイチドの導入、置換又は除去、(2)遺伝子破壊、(3)遺伝子転換、(4)遺伝子欠失、或いは(5)ランダム又は特異的変異誘発として定義される、請求項6〜9のいずれか1項に記載の変異体株。
- 親アスペルギラス・ニガー株の変異体の入手方法であって、
(a)前記親アスペルギラス・ニガー株中に、異種のポリペプチドをコードする第1のヌクレオチド配列、並びにglaA、asa、amyA、amyB、prtT及びoahの修飾を含んで成る第2のヌクレオチド配列を導入し;そして
(b)同一の条件下で培養される場合、親アスペルギラス・ニガーに比較して、グルコアミラーゼ、酸安定性α−アミラーゼ、中性α−アミラーゼA、中性α−アミラーゼB、プロテアーゼ及びシュウ酸ヒドロラーゼの生成を欠いている、修飾されたヌクレオチド配列を含んで成り、ここで前記修飾は、(1)遺伝子又は制御要素中の1又は複数のヌクレイチドの導入、置換又は除去、(2)遺伝子破壊、(3)遺伝子転換、(4)遺伝子欠失、或いは(5)ランダム又は特異的変異誘発として定義される、段階(a)からの変異体株を同定することを含んで成る方法。 - 前記変異体株が、同一の条件下で培養される場合、親アスペルギラス・ニガーに比較して、グルコアミラーゼ、酸安定性α−アミラーゼ、中性α−アミラーゼA、中性α−アミラーゼB、プロテアーゼ及びシュウ酸ヒドロラーゼを少なくとも25%少なく生成する、請求項11に記載の方法。
- 前記変異体株が、同一の条件下で培養される場合、親アスペルギラス・ニガーに比較して、グルコアミラーゼ、酸安定性α−アミラーゼ、中性α−アミラーゼA、中性α−アミラーゼB、プロテアーゼ及びシュウ酸ヒドロラーゼを完全に欠く、請求項11に記載の方法。
- 前記変異体株がさらに、タンパク質分解活性をコードする1又は複数の遺伝子の修飾を含んで成り、ここで前記修飾は、(1)遺伝子又は制御要素中の1又は複数のヌクレイチドの導入、置換又は除去、(2)遺伝子破壊、(3)遺伝子転換、(4)遺伝子欠失、或いは(5)ランダム又は特異的変異誘発として定義される、請求項11〜13のいずれか1項にに記載の方法。
- 前記変異体株が、カルボヒドラーゼ、カルボキシペプチダーゼ、カタラーゼ、セルラーゼ、キチナーゼ、クチナーゼ、シクロデキストリングリコシルトランスフェラーゼ、デオキシリボヌクレアーゼ、エステラーゼ、ガラクトシダーゼ、β−ガラクトシダーゼ、グルコースオキシダーゼ、グルコシダーゼ、ハロペルオキシダーゼ、ヘミセルラーゼ、インバーターゼ、イソメラーゼ、ラッカーゼ、リガーゼ、リパーゼ、リアーゼ、マンノシダーゼ、オキシダーゼ、ペクチン分解酵素、ペルオキシダーゼ、フィターゼ、フェノールオキシダーゼ、ポリフェノールオキシダーゼ、リボヌクレアーゼ、トランスフェラーゼ、α−1,6−トランスグルコシダーゼ、トランスグルタミナーゼ及びキシラナーゼから成る群から選択される酵素をコードする1又は複数の遺伝子の修飾をさらに含んで成り、ここで前記修飾は、(1)遺伝子又は制御要素中の1又は複数のヌクレイチドの導入、置換又は除去、(2)遺伝子破壊、(3)遺伝子転換、(4)遺伝子欠失、或いは(5)ランダム又は特異的変異誘発として定義される、請求項11〜14のいずれか1項に記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US45990203P | 2003-03-31 | 2003-03-31 | |
| PCT/US2004/010126 WO2004090155A2 (en) | 2003-03-31 | 2004-03-31 | Methods for producing biological substances in enzyme-deficient mutants of aspergillus niger |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2006521826A JP2006521826A (ja) | 2006-09-28 |
| JP2006521826A5 JP2006521826A5 (ja) | 2010-09-09 |
| JP4638418B2 true JP4638418B2 (ja) | 2011-02-23 |
Family
ID=33159708
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006509611A Expired - Lifetime JP4638418B2 (ja) | 2003-03-31 | 2004-03-31 | アスペルギラス・ニガーの酵素−欠失変異体における生物学的物質の生成方法 |
Country Status (8)
| Country | Link |
|---|---|
| US (3) | US7303877B2 (ja) |
| EP (1) | EP1613761B1 (ja) |
| JP (1) | JP4638418B2 (ja) |
| CN (2) | CN101629204A (ja) |
| AT (1) | ATE441664T1 (ja) |
| DE (1) | DE602004022929D1 (ja) |
| DK (1) | DK1613761T3 (ja) |
| WO (1) | WO2004090155A2 (ja) |
Families Citing this family (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7794974B2 (en) * | 2004-10-12 | 2010-09-14 | Dsm Ip Assets B.V. | Fungal transcriptional activators useful in methods for producing a polypeptide |
| ES2543131T3 (es) | 2004-12-22 | 2015-08-14 | Novozymes North America, Inc. | Enzimas para tratamiento de almidón |
| PL2410048T3 (pl) | 2005-01-24 | 2017-02-28 | Dsm Ip Assets B.V. | Sposób otrzymywania związku będącego przedmiotem zainteresowania w komórce grzyba nitkowatego |
| CA2630455A1 (en) | 2005-11-29 | 2007-06-07 | Dsm Ip Assets B.V. | Dna binding site of a transcriptional activator useful in gene expression |
| BRPI0713795B1 (pt) | 2006-06-29 | 2018-03-20 | Dsm Ip Assets B.V. | Método de otimização de uma sequência de nucleotídeos codificadora que codifica uma sequência de aminoácidos predeterminada |
| US8389269B2 (en) | 2006-11-02 | 2013-03-05 | Dsm Ip Assets B.V. | Production of secreted proteins by filamentous fungi |
| WO2008098933A1 (en) | 2007-02-15 | 2008-08-21 | Dsm Ip Assets B.V. | A recombinant host cell for the production of a compound of interest |
| CA2707847A1 (en) | 2007-12-06 | 2009-06-11 | Novozymes A/S | Polypeptides having acetylxylan esterase activity and polynucleotides encoding same |
| US8658409B2 (en) | 2009-03-24 | 2014-02-25 | Novozymes A/S | Polypeptides having acetyl xylan esterase activity and polynucleotides encoding same |
| US20120041171A1 (en) | 2009-04-22 | 2012-02-16 | Dsm Ip Assets B.V. | Process for the production of a recombinant polypeptide of interest |
| CA2758396C (en) | 2009-04-24 | 2018-06-12 | Dsm Ip Assets B.V. | Carbohydrate degrading polypeptide and uses thereof |
| WO2011075677A2 (en) * | 2009-12-18 | 2011-06-23 | Novozymes, Inc. | Methods for producing polypeptides in protease-deficient mutants of trichoderma |
| WO2011098580A1 (en) | 2010-02-11 | 2011-08-18 | Dsm Ip Assets B.V. | Polypeptide having cellobiohydrolase activity and uses thereof |
| CA2789301A1 (en) | 2010-02-11 | 2011-08-18 | Dsm Ip Assets B.V. | Host cell capable of producing enzymes useful for degradation of lignocellulosic material |
| CN101906393B (zh) * | 2010-06-28 | 2012-07-25 | 江南大学 | 一种谷氨酰胺转胺酶编码基因阻断吸水链霉菌及其应用 |
| BR112012033396A2 (pt) | 2010-06-29 | 2015-06-23 | Dsm Ip Assets Bv | Polipetídeo tendo atividade swollenin e seus usos. |
| ES2576062T3 (es) | 2010-06-29 | 2016-07-05 | Dsm Ip Assets B.V. | Polipéptido que tiene actividad beta-glucosidasa y usos del mismo |
| DK3318574T3 (da) | 2010-06-29 | 2021-07-12 | Dsm Ip Assets Bv | Polypeptid med beta-glucosidase-aktivitet og anvendelser deraf |
| PL2588603T3 (pl) | 2010-06-29 | 2017-08-31 | Dsm Ip Assets B.V. | Polipeptyd mający lub wzmacniający aktywność degradacji materiału węglowodanowego i jego zastosowania |
| AU2011273686B2 (en) | 2010-06-29 | 2014-07-10 | Versalis S.P.A. | Polypeptide having acetyl xylan esterase activity and uses thereof |
| EP2588601A1 (en) | 2010-06-29 | 2013-05-08 | DSM IP Assets B.V. | Polypeptide having carbohydrate degrading activity and uses thereof |
| CA2811789A1 (en) | 2010-10-06 | 2012-04-12 | Bp Corporation North America Inc. | Variant cbh i polypeptides with reduced product inhibition |
| US20120276247A1 (en) * | 2011-04-29 | 2012-11-01 | Uwe Bornscheuer | Lipase Variants |
| JP5846476B2 (ja) * | 2011-07-08 | 2016-01-20 | 独立行政法人酒類総合研究所 | 微生物のコウジ酸生産性を向上させる方法 |
| CN102296032B (zh) * | 2011-08-31 | 2013-11-06 | 保龄宝生物股份有限公司 | 转葡糖苷酶及其制备和固定化方法 |
| CN103998612A (zh) * | 2011-11-02 | 2014-08-20 | 马来西亚博特拉大学 | 制造生物聚合物的方法 |
| EP2800809B1 (en) | 2012-01-05 | 2018-03-07 | Glykos Finland Oy | Protease deficient filamentous fungal cells and methods of use thereof |
| EP2852610B1 (en) | 2012-05-23 | 2018-07-11 | Glykos Finland Oy | Production of fucosylated glycoproteins |
| WO2014028833A1 (en) | 2012-08-17 | 2014-02-20 | Novozymes A/S | Methods for co-silencing expression of genes in filamentous fungal strains and uses thereof |
| DK3019602T3 (en) | 2013-07-10 | 2018-11-12 | Glykos Finland Oy | MULTIPLE PROTEASE-DEFECTED FILAMENTARY FUNGAL CELLS AND PROCEDURES FOR USE THEREOF |
| DK3036324T3 (en) * | 2013-08-23 | 2019-04-01 | Novozymes As | Regulated PepC expression |
| CA2954974A1 (en) | 2014-07-21 | 2016-01-28 | Glykos Finland Oy | Production of glycoproteins with mammalian-like n-glycans in filamentous fungi |
| WO2017182442A1 (en) * | 2016-04-19 | 2017-10-26 | Novozymes A/S | Rlma-inactivated filamentous fungal host cell |
| CN108504615B (zh) * | 2018-03-30 | 2020-12-29 | 江南大学 | 一种产酸性蛋白酶的重组菌及其应用 |
| BR112021007367A2 (pt) * | 2018-10-17 | 2021-08-10 | Perfect Day, Inc | componentes e composições recombinantes para uso em produtos alimentares |
| CN114555777A (zh) * | 2019-07-26 | 2022-05-27 | 诺维信公司 | 经修饰的丝状真菌宿主细胞 |
| CN113265417A (zh) * | 2020-02-14 | 2021-08-17 | 中国科学院天津工业生物技术研究所 | 有机酸产量提高的菌株及其构建方法和应用 |
| WO2022079238A1 (en) | 2020-10-15 | 2022-04-21 | Dsm Ip Assets B.V. | Methods of modulating gastrointestinal metabolites |
| WO2023225459A2 (en) | 2022-05-14 | 2023-11-23 | Novozymes A/S | Compositions and methods for preventing, treating, supressing and/or eliminating phytopathogenic infestations and infections |
| CN114736880B (zh) * | 2022-06-09 | 2022-09-27 | 中国农业科学院北京畜牧兽医研究所 | 酸稳定性提高葡萄糖氧化酶GoxM10的突变体D497N及其衍生突变体和应用 |
| WO2023242273A1 (en) * | 2022-06-14 | 2023-12-21 | Newmilkbuzz B.V. | Expression of milk caseins in filamentous fungi |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DK122686D0 (da) | 1986-03-17 | 1986-03-17 | Novo Industri As | Fremstilling af proteiner |
| US5536661A (en) | 1987-03-10 | 1996-07-16 | Novo Nordisk A/S | Process for the production of protein products in aspergillus |
| US5252726A (en) * | 1987-09-04 | 1993-10-12 | Novo Nordisk A/S | Promoters for use in aspergillus |
| WO1991017243A1 (en) | 1990-05-09 | 1991-11-14 | Novo Nordisk A/S | A cellulase preparation comprising an endoglucanase enzyme |
| DK88892D0 (da) | 1992-07-06 | 1992-07-06 | Novo Nordisk As | Forbindelse |
| DK0765394T3 (da) | 1994-06-03 | 2001-12-10 | Novozymes As | Oprensede Myceliopthora-laccaser og nukleinsyrer der koder for disse |
| AU2705895A (en) | 1994-06-30 | 1996-01-25 | Novo Nordisk Biotech, Inc. | Non-toxic, non-toxigenic, non-pathogenic fusarium expression system and promoters and terminators for use therein |
| US5646025A (en) | 1995-05-05 | 1997-07-08 | Novo Nordisk A/S | Scytalidium catalase gene |
| WO1998026051A2 (en) * | 1996-12-12 | 1998-06-18 | Leopold Flohe | Tryparedoxin, expression plasmid, process of production, use, test system and pharmaceutical preparation |
| WO1998046772A2 (en) * | 1997-04-11 | 1998-10-22 | Dsm N.V. | Gene conversion as a tool for the construction of recombinant industrial filamentous fungi |
| JP4563585B2 (ja) | 1998-10-05 | 2010-10-13 | ノボザイムス アクティーゼルスカブ | ポリペプチドの生成方法において有用な菌類転写活性化因子 |
| US6806062B1 (en) * | 1998-10-05 | 2004-10-19 | Novozymes A/S | Fungal transcriptional activator useful in methods for producing polypeptides |
| DE60025467T2 (de) | 1999-02-22 | 2006-09-21 | Novozymes A/S | Oxalacetat-hydrolase defiziente fungale wirtszellen |
| CN100532561C (zh) | 1999-03-22 | 2009-08-26 | 诺沃奇梅兹有限公司 | 新的葡糖淀粉酶及编码它的核酸序列 |
| WO2001068864A1 (en) | 2000-03-14 | 2001-09-20 | Novozymes A/S | Fungal transcriptional activator useful in methods for producing polypeptides |
| US7122330B2 (en) * | 2000-04-13 | 2006-10-17 | Mark Aaron Emalfarb | High-throughput screening of expressed DNA libraries in filamentous fungi |
-
2004
- 2004-03-31 EP EP04758768A patent/EP1613761B1/en not_active Expired - Lifetime
- 2004-03-31 CN CN200910167050A patent/CN101629204A/zh active Pending
- 2004-03-31 DK DK04758768T patent/DK1613761T3/da active
- 2004-03-31 DE DE602004022929T patent/DE602004022929D1/de not_active Expired - Lifetime
- 2004-03-31 WO PCT/US2004/010126 patent/WO2004090155A2/en active Application Filing
- 2004-03-31 JP JP2006509611A patent/JP4638418B2/ja not_active Expired - Lifetime
- 2004-03-31 US US10/815,495 patent/US7303877B2/en active Active
- 2004-03-31 CN CNB2004800151129A patent/CN100547078C/zh not_active Expired - Lifetime
- 2004-03-31 AT AT04758768T patent/ATE441664T1/de not_active IP Right Cessation
-
2007
- 2007-08-10 US US11/837,279 patent/US7771971B2/en not_active Expired - Fee Related
-
2010
- 2010-06-24 US US12/823,046 patent/US8445283B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US7303877B2 (en) | 2007-12-04 |
| WO2004090155A2 (en) | 2004-10-21 |
| WO2004090155A3 (en) | 2005-01-06 |
| CN101629204A (zh) | 2010-01-20 |
| DK1613761T3 (da) | 2009-12-14 |
| US8445283B2 (en) | 2013-05-21 |
| US20080044858A1 (en) | 2008-02-21 |
| US20100323448A1 (en) | 2010-12-23 |
| ATE441664T1 (de) | 2009-09-15 |
| CN1798848A (zh) | 2006-07-05 |
| JP2006521826A (ja) | 2006-09-28 |
| US20040191864A1 (en) | 2004-09-30 |
| EP1613761B1 (en) | 2009-09-02 |
| EP1613761A4 (en) | 2006-08-09 |
| EP1613761A2 (en) | 2006-01-11 |
| US7771971B2 (en) | 2010-08-10 |
| CN100547078C (zh) | 2009-10-07 |
| DE602004022929D1 (de) | 2009-10-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4638418B2 (ja) | アスペルギラス・ニガーの酵素−欠失変異体における生物学的物質の生成方法 | |
| US9790532B2 (en) | Methods for producing polypeptides in enzyme-deficient mutants of Fusarium venentatum | |
| US10100344B2 (en) | AgsE-deficient strain | |
| EP2588616B1 (en) | A method for the production of a compound of interest | |
| US9322045B2 (en) | Host cell for the production of a compound of interest | |
| US9745563B2 (en) | Amylase-deficient strain | |
| JP2021532775A (ja) | タンパク質生産性が強化された表現型を含む突然変異及び遺伝子改変糸状菌株並びにそれらの方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070306 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100119 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100419 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100426 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100720 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20100720 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20101026 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20101125 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131203 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4638418 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |