JP4634367B2 - ピリミジン化合物 - Google Patents
ピリミジン化合物 Download PDFInfo
- Publication number
- JP4634367B2 JP4634367B2 JP2006503537A JP2006503537A JP4634367B2 JP 4634367 B2 JP4634367 B2 JP 4634367B2 JP 2006503537 A JP2006503537 A JP 2006503537A JP 2006503537 A JP2006503537 A JP 2006503537A JP 4634367 B2 JP4634367 B2 JP 4634367B2
- Authority
- JP
- Japan
- Prior art keywords
- amino
- het
- formula
- hydrochloride
- phenyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 0 Cc1nc(*)c(*)c(Cl)n1 Chemical compound Cc1nc(*)c(*)c(Cl)n1 0.000 description 7
- GRJCWULLAJEIIT-UHFFFAOYSA-N CC(C)(C)NC(c1ccccc1Nc1nc(Nc(cc2OC)cc(OC)c2OC)ncc1[N+]([O-])=O)=O Chemical compound CC(C)(C)NC(c1ccccc1Nc1nc(Nc(cc2OC)cc(OC)c2OC)ncc1[N+]([O-])=O)=O GRJCWULLAJEIIT-UHFFFAOYSA-N 0.000 description 1
- DTGURCGTPUDALE-UHFFFAOYSA-N COc(cc(cc1OC)Nc(nc2Nc3cccc(cc4)c3cc4O)ncc2[N+]([O-])=O)c1OC Chemical compound COc(cc(cc1OC)Nc(nc2Nc3cccc(cc4)c3cc4O)ncc2[N+]([O-])=O)c1OC DTGURCGTPUDALE-UHFFFAOYSA-N 0.000 description 1
- ZVAQGTCPHGPJCX-UHFFFAOYSA-N COc(cc(cc1OC)Nc(nc2Nc3cccc4c3OCCO4)ncc2[N+]([O-])=O)c1OC Chemical compound COc(cc(cc1OC)Nc(nc2Nc3cccc4c3OCCO4)ncc2[N+]([O-])=O)c1OC ZVAQGTCPHGPJCX-UHFFFAOYSA-N 0.000 description 1
- MHCRXTLQJHXSHN-UHFFFAOYSA-N NC(c1ccccc1Nc1nc(Cl)ncc1[N+]([O-])=O)=O Chemical compound NC(c1ccccc1Nc1nc(Cl)ncc1[N+]([O-])=O)=O MHCRXTLQJHXSHN-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/32—One oxygen, sulfur or nitrogen atom
- C07D239/42—One nitrogen atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/46—Two or more oxygen, sulphur or nitrogen atoms
- C07D239/48—Two nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Hematology (AREA)
- Oncology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Catalysts (AREA)
- Polysaccharides And Polysaccharide Derivatives (AREA)
Description
R1は、H、ハロ、アルキル、アルケニル、アルキニルからなる群から選択され;
R2は、ハロ、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、-(R7)g-C(O)R6、-(R7)g-CO2R6、-(R7)g-C(O)N(R6)2、-(R7)g-OR6、-O-(R7)g-Ay、-(R7)g-S(O)eR6、-(R7)g-N(R6)2、-(R7)g-N(R6)C(O)R6、-(R7)g-CN、-(R7)g-SCN、-NO2、-N3、Ay、並びにN、O及びSから選択される1又は2個のヘテロ原子を含む5〜9員のヘテロアリールからなる群から選択され;
各R3は、同一又は異なって、そして独立して、H又アルキルであり;
Yは、-C(O)R8、-C(S)R8、-S(O)eR9、-S(O)eN(R9)2、-N(R9)2、-N(R9)-S(O)eR9、-N(R9)-C(O)R9、-N(R9)-CO2R9及び-N(R9)-C(O)N(R9)2からなる群から選択されるか、
又は、Yは、C-2及びC-3と一緒になって、式A:
ここで、R8はアルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay、Het、-OR6、-O-(R7)g-Ay、-O-(R7)g-Het、-N(R6)2、-N(R6)-(R7)g-Ay、-N(R6)-(R7)g-Het、-N(R6)-(R7)g-OR6、-N(R6)-(R7)g-C(O)R6、-N(R6)-(R7)g-CO2R6、-N(R6)-(R7)g-SO2R6及び-N(R6)-(R7)g-N(R6)2からなる群から選択され;
各R9は、同一又は異なって、そして独立して、H、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay及びHetからなる群から選択され;
cは、0又は1であり;
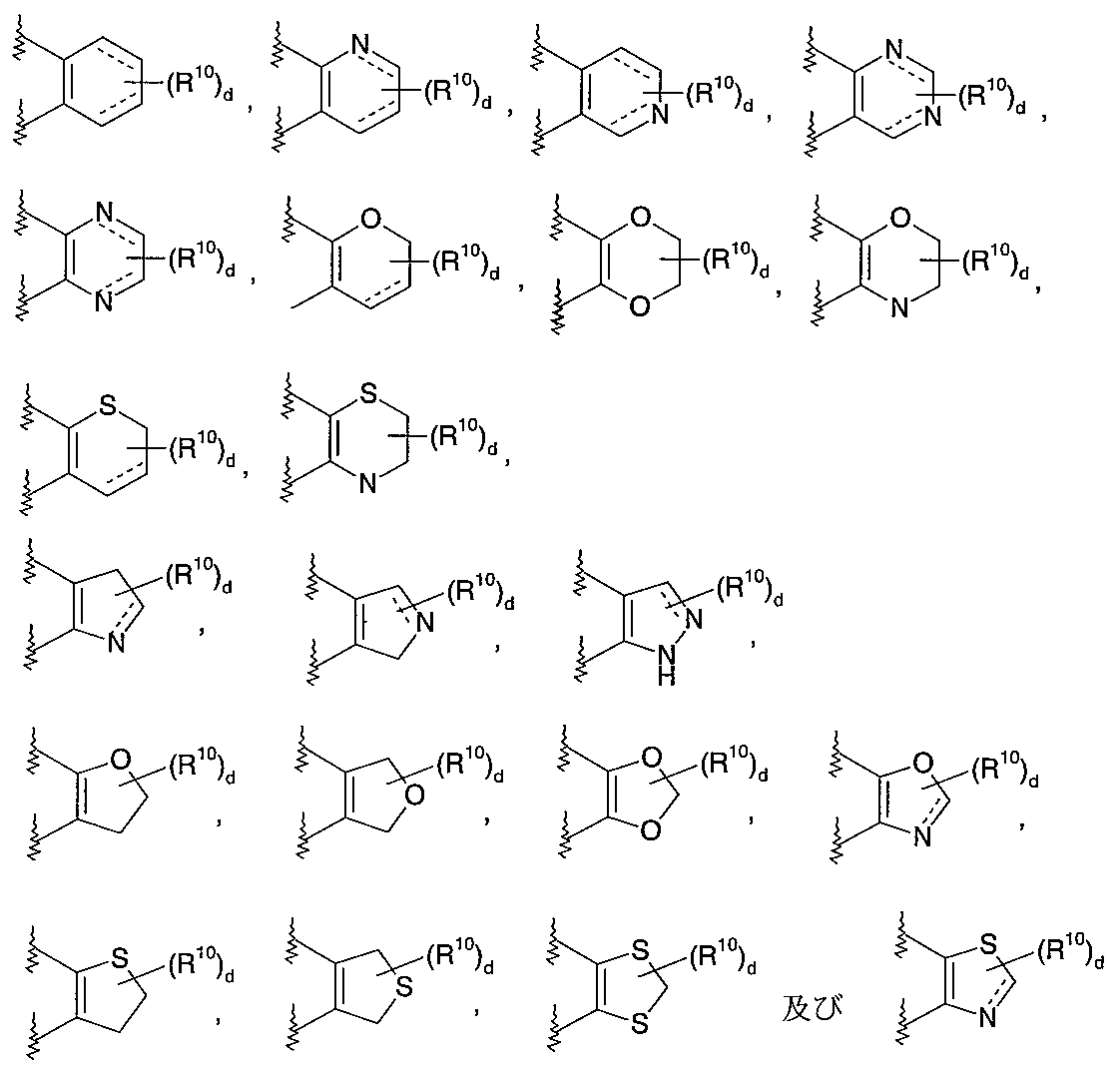
Z1、Z2、Z3及びZ4は、それぞれ独立して、C、O、S及びNからなる群から選択され、ここで、cが0である場合には、Z1、Z2及びZ3の少なくとも1つはCであり、そしてcが1である場合には、Z1、Z2、Z3及びZ4の少なくとも2つはCであり;
各破線は、任意に二重結合を表し;
dは、0、1又は2であり;
各R10は、同一又は異なって、そして独立して、ハロ、アルキル、オキソ、ヒドロキシ、メルカプト及びアミノからなる群から選択され;
aは、0、1、2又は3であり;
各R4は、同一又は異なって、そして独立して、ハロ、アルキル、アルケニル、アルキニル、-(R7)g-シクロアルキル、-(R7)g-シクロアルケニル、-(R7)g-Ay、-(R7)g-Het、-(R7)g-C(O)R6、-(R7)g-C(O)Ay、-(R7)g-C(O)Het、-(R7)g-CO2R6、-(R7)g-CO2Ay、-(R7)g-CO2Het、-(R7)g-C(O)N(R6)2、-(R7)g-OR6、-(R7)g-OAy、-(R7)g-OHet、-(R7)g-OC(O)R6、-(R7)g-OC(O)Ay、-(R7)g-OC(O)Het、-(R7)g-S(O)eR6、-(R7)g-S(O)eAy、-(R7)g-S(O)eHet、-(R7)g-S(O)eN(R6)2、-(R7)g-S(O)eN(R6)Ay、-(R7)g-S(O)eN(R6)Het、-(R7)g-N(R6)2、-(R7)g-N(R6)Ay、-(R7)g-N(R6)Het、-(R7)g-N(R6)C(O)R6、-(R7)g-N(R6)C(O)Ay、-(R7)g-N(R6)C(O)Het、-(R7)g-N(R6)C(O)N(R6)2、-(R7)g-N(R6)S(O)eR6、-(R7)g-N(R6)S(O)eAy、-(R7)g-N(R6)S(O)eHet、-NO2、-CN、-SCN及び-N3からなる群から選択されるか、又は
2個の隣接するR4は、それらが結合している炭素原子と一緒になって、フェニル又はN、O及びSからなる群から選択される1又は2個のヘテロ原子を含む5若しくは6員のヘテロ環若しくはヘテロアリールを形成し;
各eは、同一又は異なって、そして独立して、0、1又は2であり;
bは、0、1、2、3、4又は5であり;
各R5は、同一又は異なって、式(R7)g-R11の基であるか、又は2個の隣接するR5基は、それぞれ同一又は異なって、そして独立して、アルキル、アルケニル、-OR6、-S(O)eR6及び-N(R6)2からなる群から選択され、そしてそれらが結合している炭素原子と一緒になって、C5-6シクロアルキル、C5-6シクロアルケニル又はN、O及びSからなる群から選択される1又は2個のヘテロ原子を含む5若しくは6員のヘテロ環若しくはヘテロアリールを形成し;
各R6は、同一又は異なって、そして独立して、H、アルキル、アルケニル、アルキニル、シクロアルキル及びシクロアルケニルからなる群から選択され;
gは、0又は1であり;
R7はアルキレン又はアルケニレンであり;
Ayは、アリールであり;
Hetは、N、O及びSからなる群から選択される1、2又は3個のヘテロ原子を含む5員又は6員のヘテロ環若しくはヘテロアリールであり;
R11は、ハロ、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay、Het、-C(O)R6、-C(O)Ay、-C(O)Het、-CO2R6、-CO2Ay、-CO2Het、-C(O)-R7-OR6、-C(O)-R7-OAy、-C(O)-R7-OHet、-C(O)N(R6)2、-C(O)N(R6)Ay、-C(O)N(R6)Het、-C(O)N(R6)-(R7)g-N(R6)2、-C(O)N(R6)-(R7)g-CO2R6、-C(O)N(R6)-(R7)g-S(O)eR6、-OR6、-OC(O)R6、-O-(R7)g-Ay、-OC(O)Ay、-O-(R7)g-Het、-OC(O)Het、-O-R7-OR6、-O-R7-N(R6)2、-S(O)eR6、-S(O)e-(R7)g-Ay、-S(O)e-(R7)g-Het、-S(O)e-(R7)g-N(R6)2、-S(O)e-(R7)g-N(R6)Ay、-S(O)e-(R7)g-N(R6)Het、-S(O)eN(R6)-(R7)g-C(O)R6、-S(O)eN(R6)-(R7)g-C(O)Ay、-S(O)eN(R6)-(R7)g-C(O)Het、-N(R6)2、-N(R6)-(R7)g-Ay、-N(R6)-(R7)g-Het、-N(R6)-(R7)g-C(O)R6、-N(R6)-C(O)-(R7)g-Ay、-N(R6)-C(O)-(R7)g-Het、-N(R6)-C(O)-(R7)g-N(R6)2、-N(R6)-C(O)-(R7)g-N(R6)Ay、-N(R6)-C(O)-(R7)g-N(R6)Het、-N(R6)-C(O)-(R7)g-N(R6)-(R7-O)h-N(R6)-CO2R6、-N(R6)-(R7)g-S(O)eR6、-N(R6)-(R7)g-S(O)eAy、-N(R6)-(R7)g-S(O)eHet、-N(R6)-R7-N(R6)2、-N(R6)-R7-OR6、-CN、-SCN、-NO2及び-N3からなる群から選択され;そして
hは、1〜20であり;
ここで、R1が-CH3であり、R2がBr又はNO2であり、両方のR3がHであり、aが0であり、そしてbが0又は1であり、R5が-CO2Hである場合には、Yは-CO2Hではない。]
の化合物又はその薬学的に許容される塩、溶媒和物若しくは生理的機能性誘導体(physiologically functional derivative)が提供される。
本明細書で用いられるように、「本発明の化合物」又は「式(I)の化合物」は、式(I)の化合物又はその薬学的に許容される塩、溶媒和物若しくは生理的機能性誘導体を意味する。同様に、単離可能な中間体、例えば式(IV)の化合物などに関して、「式(番号)の化合物」というフレーズは、その式を有する化合物又はその薬学的に許容される塩、溶媒和物若しくは生理的機能性誘導体を意味する。
R1は、H、ハロ、アルキル、アルケニル、アルキニルからなる群から選択され;
R2は、ハロ、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、-(R7)g-C(O)R6、-(R7)g-CO2R6、-(R7)g-C(O)N(R6)2、-(R7)g-OR6、-O-(R7)g-Ay、-(R7)g-S(O)eR6、-(R7)g-N(R6)2、-(R7)g-N(R6)C(O)R6、-(R7)g-CN、-(R7)g-SCN、-NO2、-N3、Ay、並びにN、O及びSから選択される1又は2個のヘテロ原子を含む5〜9員のヘテロアリールからなる群から選択され;
各R3は、同一又は異なって、そして独立して、H又アルキルであり;
Yは、-C(O)R8、-C(S)R8、-S(O)eR9、-S(O)eN(R9)2、-N(R9)2、-N(R9)-S(O)eR9、-N(R9)-C(O)R9、-N(R9)-CO2R9及び-N(R9)-C(O)N(R9)2からなる群から選択されるか、
又は、Yは、C-2及びC-3と一緒になって、式A:
ここで、R8はアルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay、Het、-OR6、-O-(R7)g-Ay、-O-(R7)g-Het、-N(R6)2、-N(R6)-(R7)g-Ay、-N(R6)-(R7)g-Het、-N(R6)-(R7)g-OR6、-N(R6)-(R7)g-C(O)R6、-N(R6)-(R7)g-CO2R6、-N(R6)-(R7)g-SO2R6及び-N(R6)-(R7)g-N(R6)2からなる群から選択され;
各R9は、同一又は異なって、そして独立して、H、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay及びHetからなる群から選択され;
cは、0又は1であり;
Z1、Z2、Z3及びZ4は、それぞれ独立して、C、O、S及びNからなる群から選択され、ここで、cが0である場合には、Z1、Z2及びZ3の少なくとも1つはCであり、そしてcが1である場合には、Z1、Z2、Z3及びZ4の少なくとも2つはCであり;
各破線は、任意に二重結合を表し;
dは、0、1又は2であり;
各R10は、同一又は異なって、そして独立して、ハロ、アルキル、オキソ、ヒドロキシ、メルカプト及びアミノからなる群から選択され;
aは、0、1、2又は3であり;
各R4は、同一又は異なって、そして独立して、ハロ、アルキル、アルケニル、アルキニル、-(R7)g-シクロアルキル、-(R7)g-シクロアルケニル、-(R7)g-Ay、-(R7)g-Het、-(R7)g-C(O)R6、-(R7)g-C(O)Ay、-(R7)g-C(O)Het、-(R7)g-CO2R6、-(R7)g-CO2Ay、-(R7)g-CO2Het、-(R7)g-C(O)N(R6)2、-(R7)g-OR6、-(R7)g-OAy、-(R7)g-OHet、-(R7)g-OC(O)R6、-(R7)g-OC(O)Ay、-(R7)g-OC(O)Het、-(R7)g-S(O)eR6、-(R7)g-S(O)eAy、-(R7)g-S(O)eHet、-(R7)g-S(O)eN(R6)2、-(R7)g-S(O)eN(R6)Ay、-(R7)g-S(O)eN(R6)Het、-(R7)g-N(R6)2、-(R7)g-N(R6)Ay、-(R7)g-N(R6)Het、-(R7)g-N(R6)C(O)R6、-(R7)g-N(R6)C(O)Ay、-(R7)g-N(R6)C(O)Het、-(R7)g-N(R6)C(O)N(R6)2、-(R7)g-N(R6)S(O)eR6、-(R7)g-N(R6)S(O)eAy、-(R7)g-N(R6)S(O)eHet、-NO2、-CN、-SCN及び-N3からなる群から選択されるか、又は
2個の隣接するR4は、それらが結合している炭素原子と一緒になって、フェニル又はN、O及びSからなる群から選択される1又は2個のヘテロ原子を含む5若しくは6員のヘテロ環若しくはヘテロアリールを形成し;
各eは、同一又は異なって、そして独立して、0、1又は2であり;
bは、0、1、2、3、4又は5であり;
各R5は、同一又は異なって、式(R7)g-R11の基であるか、又は2個の隣接するR5基は、それぞれ同一又は異なって、そして独立して、アルキル、アルケニル、-OR6、-S(O)eR6及び-N(R6)2からなる群から選択され、そしてそれらが結合している炭素原子と一緒になって、C5-6シクロアルキル、C5-6シクロアルケニル又はN、O及びSからなる群から選択される1又は2個のヘテロ原子を含む5若しくは6員のヘテロ環若しくはヘテロアリールを形成し;
各R6は、同一又は異なって、そして独立して、H、アルキル、アルケニル、アルキニル、シクロアルキル及びシクロアルケニルからなる群から選択され;
gは、0又は1であり;
R7はアルキレン又はアルケニレンであり;
Ayは、アリールであり;
Hetは、N、O及びSからなる群から選択される1、2又は3個のヘテロ原子を含む5員又は6員のヘテロ環若しくはヘテロアリールであり;
R11は、ハロ、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay、Het、-C(O)R6、-C(O)Ay、-C(O)Het、-CO2R6、-CO2Ay、-CO2Het、-C(O)-R7-OR6、-C(O)-R7-OAy、-C(O)-R7-OHet、-C(O)N(R6)2、-C(O)N(R6)Ay、-C(O)N(R6)Het、-C(O)N(R6)-(R7)g-N(R6)2、-C(O)N(R6)-(R7)g-CO2R6、-C(O)N(R6)-(R7)g-S(O)eR6、-OR6、-OC(O)R6、-O-(R7)g-Ay、-OC(O)Ay、-O-(R7)g-Het、-OC(O)Het、-O-R7-OR6、-O-R7-N(R6)2、-S(O)eR6、-S(O)e-(R7)g-Ay、-S(O)e-(R7)g-Het、-S(O)e-(R7)g-N(R6)2、-S(O)e-(R7)g-N(R6)Ay、-S(O)e-(R7)g-N(R6)Het、-S(O)eN(R6)-(R7)g-C(O)R6、-S(O)eN(R6)-(R7)g-C(O)Ay、-S(O)eN(R6)-(R7)g-C(O)Het、-N(R6)2、-N(R6)-(R7)g-Ay、-N(R6)-(R7)g-Het、-N(R6)-(R7)g-C(O)R6、-N(R6)-C(O)-(R7)g-Ay、-N(R6)-C(O)-(R7)g-Het、-N(R6)-C(O)-(R7)g-N(R6)2、-N(R6)-C(O)-(R7)g-N(R6)Ay、-N(R6)-C(O)-(R7)g-N(R6)Het、-N(R6)-C(O)-(R7)g-N(R6)-(R7-O)h-N(R6)-CO2R6、-N(R6)-(R7)g-S(O)eR6、-N(R6)-(R7)g-S(O)eAy、-N(R6)-(R7)g-S(O)eHet、-N(R6)-R7-N(R6)2、-N(R6)-R7-OR6、-CN、-SCN、-NO2及び-N3からなる群から選択され;そして
hは、1〜20であり;
ここで、R1が-CH3であり、R2がBr又はNO2であり、両方のR3がHであり、aが0であり、そしてbが0又は1であり、R5が-CO2Hである場合には、Yは-CO2Hではない。]
の化合物又はその薬学的に許容される塩、溶媒和物若しくは生理的機能性誘導体を提供する。
cは0又は1であり;
Z1、Z2、Z3及びZ4は、それぞれ独立して、C、O、S及びNからなる群から選択され、ここで、cが0である場合には、Z1、Z2及びZ3の少なくとも1つはC(炭素)であり、そしてcが1である場合には、Z1、Z2、Z3及びZ4の少なくとも2つはC(炭素)であり;
dは0、1又は2であり;
各R10は同一又は異なって、そして独立して、ハロ、アルキル、オキソ、ヒドロキシ、メルカプト及びアミノからなる群から選択される。
2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)安息香酸塩酸塩;
2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)ベンズアミド塩酸塩;
N-(tert-ブチル)-2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)ベンズアミド塩酸塩;
N-[4-({4-[(2-ベンゾイルフェニル)アミノ]-5-ニトロピリミジン-2-イル}アミノ)フェニル]アセトアミド塩酸塩;
8-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)-3,4-ジヒドロナフタレン-1(2H)-オン塩酸塩;
1-[2-({5-ブロモ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)フェニル]エタノン塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]-N-メチルベンズアミド塩酸塩;
N4-(1H-インドール-4-イル)-5-ニトロ-N2-(3,4,5-トリメトキシフェニル)ピリミジン-2,4-ジアミン塩酸塩;
2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)安息香酸メチル塩酸塩;
N4-(2,3-ジヒドロ-1,4-ベンゾジオキシン-5-イル)-5-ニトロ-N2-(3,4,5-トリメトキシフェニル)ピリミジン-2,4-ジアミン塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]安息香酸シクロヘキシル塩酸塩;
5-ヒドロキシ-2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)安息香酸塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]安息香酸塩酸塩;
N-[4-({4-[(2-アセチルフェニル)アミノ]-5-ブロモピリミジン-2-イル}アミノ)フェニル]アセトアミド塩酸塩;
N-[4-({5-ブロモ-4-[(2-モルホリン-4-イルフェニル)アミノ]ピリミジン-2-イル}アミノ)フェニル]アセトアミド塩酸塩;
5-[(5-ブロモ-4-{[2-(メチルチオ)フェニル]アミノ}ピリミジン-2-イル)アミノ]-1,3-ジヒドロ-2H-ベンズイミダゾール-2-オン塩酸塩;
5-ブロモ-N4-(2-モルホリン-4-イルフェニル)-N2-(3,4,5-トリメトキシフェニル)ピリミジン-2,4-ジアミン塩酸塩;
N-[4-({5-ブロモ-4-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-2-イル}アミノ)フェニル]アセトアミド塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]テレフタル酸ジメチル塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]安息香酸ベンジル塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]-6-メチル安息香酸メチル塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]安息香酸イソブチル塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]-6-メチル安息香酸塩酸塩;
N-シクロヘキシル-2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)ベンズアミド塩酸塩;
1-[2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)フェニル]エタノン塩酸塩;
[5-クロロ-2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)フェニル](2-フルオロフェニル)メタノン塩酸塩;
8-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)-2-ナフトール塩酸塩;
N-(tert-ブチル)-2-({5-メチルケトン-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)ベンズアミド;
4-{[2-(4-メチルベンゾイル)フェニル]アミノ}-2-[(3,4,5-トリメトキシフェニル)アミノ]-ピリミジン-5-カルボニトリル;
並びにその薬学的に許容される塩、溶媒和物及び生理機能性誘導体。
R1は、H、ハロ、アルキル、アルケニル、アルキニルからなる群から選択され;
R2は、ハロ、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、-(R7)g-C(O)R6、-(R7)g-CO2R6、-(R7)g-C(O)N(R6)2、-(R7)g-OR6、-O-(R7)g-Ay、-(R7)g-S(O)eR6、-(R7)g-N(R6)2、-(R7)g-N(R6)C(O)R6、-(R7)g-CN、-(R7)g-SCN、-NO2、-N3、Ay、並びにN、O及びSから選択される1又は2個のヘテロ原子を含む5〜9員のヘテロアリールからなる群から選択され;
各R3は、同一又は異なって、そして独立して、H又アルキルであり;
Yは、-C(O)R8、-C(S)R8、-S(O)eR9、-S(O)eN(R9)2、-N(R9)2、-N(R9)-S(O)eR9、-N(R9)-C(O)R9、-N(R9)-CO2R9及び-N(R9)-C(O)N(R9)2からなる群から選択されるか、
又は、Yは、C-2及びC-3と一緒になって、式A:
ここで、R8はアルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay、Het、-OR6、-O-(R7)g-Ay、-O-(R7)g-Het、-N(R6)2、-N(R6)-(R7)g-Ay、-N(R6)-(R7)g-Het、-N(R6)-(R7)g-OR6、-N(R6)-(R7)g-C(O)R6、-N(R6)-(R7)g-CO2R6、-N(R6)-(R7)g-SO2R6及び-N(R6)-(R7)g-N(R6)2からなる群から選択され;
各R9は、同一又は異なって、そして独立して、H、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay及びHetからなる群から選択され;
cは、0又は1であり;
Z1、Z2、Z3及びZ4は、それぞれ独立して、C、O、S及びNからなる群から選択され、ここで、cが0である場合には、Z1、Z2及びZ3の少なくとも1つはCであり、そしてcが1である場合には、Z1、Z2、Z3及びZ4の少なくとも2つはCであり;
各破線は、任意に二重結合を表し;
dは、0、1又は2であり;
各R10は、同一又は異なって、そして独立して、ハロ、アルキル、オキソ、ヒドロキシ、メルカプト及びアミノからなる群から選択され;
aは、0、1、2又は3であり;
各R4は、同一又は異なって、そして独立して、ハロ、アルキル、アルケニル、アルキニル、-(R7)g-シクロアルキル、-(R7)g-シクロアルケニル、-(R7)g-Ay、-(R7)g-Het、-(R7)g-C(O)R6、-(R7)g-C(O)Ay、-(R7)g-C(O)Het、-(R7)g-CO2R6、-(R7)g-CO2Ay、-(R7)g-CO2Het、-(R7)g-C(O)N(R6)2、-(R7)g-OR6、-(R7)g-OAy、-(R7)g-OHet、-(R7)g-OC(O)R6、-(R7)g-OC(O)Ay、-(R7)g-OC(O)Het、-(R7)g-S(O)eR6、-(R7)g-S(O)eAy、-(R7)g-S(O)eHet、-(R7)g-S(O)eN(R6)2、-(R7)g-S(O)eN(R6)Ay、-(R7)g-S(O)eN(R6)Het、-(R7)g-N(R6)2、-(R7)g-N(R6)Ay、-(R7)g-N(R6)Het、-(R7)g-N(R6)C(O)R6、-(R7)g-N(R6)C(O)Ay、-(R7)g-N(R6)C(O)Het、-(R7)g-N(R6)C(O)N(R6)2、-(R7)g-N(R6)S(O)eR6、-(R7)g-N(R6)S(O)eAy、-(R7)g-N(R6)S(O)eHet、-NO2、-CN、-SCN及び-N3からなる群から選択されるか、又は
2個の隣接するR4は、それらが結合している炭素原子と一緒になって、フェニル又はN、O及びSからなる群から選択される1又は2個のヘテロ原子を含む5若しくは6員のヘテロ環若しくはヘテロアリールを形成し;
各eは、同一又は異なって、そして独立して、0、1又は2であり;
bは、0、1、2、3、4又は5であり;
各R5は、同一又は異なって、式(R7)g-R11の基であるか、又は2個の隣接するR5基は、それぞれ同一又は異なって、そして独立して、アルキル、アルケニル、-OR6、-S(O)eR6及び-N(R6)2からなる群から選択され、そしてそれらが結合している炭素原子と一緒になって、C5-6シクロアルキル、C5-6シクロアルケニル又はN、O及びSからなる群から選択される1又は2個のヘテロ原子を含む5若しくは6員のヘテロ環若しくはヘテロアリールを形成し;
各R6は、同一又は異なって、そして独立して、H、アルキル、アルケニル、アルキニル、シクロアルキル及びシクロアルケニルからなる群から選択され;
gは、0又は1であり;
R7はアルキレン又はアルケニレンであり;
Ayは、アリールであり;
Hetは、N、O及びSからなる群から選択される1、2又は3個のヘテロ原子を含む5員又は6員のヘテロ環若しくはヘテロアリールであり;
R11は、ハロ、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay、Het、-C(O)R6、-C(O)Ay、-C(O)Het、-CO2R6、-CO2Ay、-CO2Het、-C(O)-R7-OR6、-C(O)-R7-OAy、-C(O)-R7-OHet、-C(O)N(R6)2、-C(O)N(R6)Ay、-C(O)N(R6)Het、-C(O)N(R6)-(R7)g-N(R6)2、-C(O)N(R6)-(R7)g-CO2R6、-C(O)N(R6)-(R7)g-S(O)eR6、-OR6、-OC(O)R6、-O-(R7)g-Ay、-OC(O)Ay、-O-(R7)g-Het、-OC(O)Het、-O-R7-OR6、-O-R7-N(R6)2、-S(O)eR6、-S(O)e-(R7)g-Ay、-S(O)e-(R7)g-Het、-S(O)e-(R7)g-N(R6)2、-S(O)e-(R7)g-N(R6)Ay、-S(O)e-(R7)g-N(R6)Het、-S(O)eN(R6)-(R7)g-C(O)R6、-S(O)eN(R6)-(R7)g-C(O)Ay、-S(O)eN(R6)-(R7)g-C(O)Het、-N(R6)2、-N(R6)-(R7)g-Ay、-N(R6)-(R7)g-Het、-N(R6)-(R7)g-C(O)R6、-N(R6)-C(O)-(R7)g-Ay、-N(R6)-C(O)-(R7)g-Het、-N(R6)-C(O)-(R7)g-N(R6)2、-N(R6)-C(O)-(R7)g-N(R6)Ay、-N(R6)-C(O)-(R7)g-N(R6)Het、-N(R6)-C(O)-(R7)g-N(R6)-(R7-O)h-N(R6)-CO2R6、-N(R6)-(R7)g-S(O)eR6、-N(R6)-(R7)g-S(O)eAy、-N(R6)-(R7)g-S(O)eHet、-N(R6)-R7-N(R6)2、-N(R6)-R7-OR6、-CN、-SCN、-NO2及び-N3からなる群から選択され;
hは、1〜20であり;そして
R15は、ハロ及び-S(O)eR6からなる群から選択される。
a)式(II)の化合物を式(III)の化合物と反応させて式(IV)の化合物を製造し;そして
b)式(IV)の化合物を式(V)の化合物と反応させて式(I)の化合物を製造すること
を含む方法により製造することができる。
R16はアルケニル又はアルキニルであり;
R17は、R2からなる群から選択され、すなわち、アルキル、-C(O)R6、-CO2R6、-C(O)N(R6)2、-OR6、-S(O)eR6、-N(R6)2、-N(R6)COR6、-CN、-SCN、Ay、並びにN、O及びSから選択される1若しくは2個のヘテロ原子を含む5〜9員のヘテロアリールからなる群から選択され;
そして他の全ての基は上記で定義したとおりである。
本反応は等モル量の式(I-A)の化合物と式(XIV)のトリブチル錫化合物との反応により行れるが、本反応は過剰量の式(XIV)の化合物の存在下で行うこともできる。パラジウム触媒は式(I-A)の化合物に対して好ましくは5〜20モル%の量で存在する。好適なパラジウム触媒の例は、ジクロロビス(トリフェニルホスフィン)パラジウム(II)、及びトリフェニルホスフィンと一緒の酢酸パラジウム(II)、及びトリス(ジベンジリデンアセトン)ジパラジウム(0)を含むが、これらに限定されるものではない。パラジウム触媒は、典型的にはヨウ化銅と錯体生成したものである。臭化銅はパラジウム触媒に対して好ましくは200モル%の量で存在する。塩基は、式(I-A)の化合物と同様の、又はその200モル%より大きい割合で典型的に存在する。好適な溶剤は、ジオキサン、N,N-ジメチルホルムアミド及びテトラヒドロフランを含むが、これらに限定されるものではない。式(XIV)の化合物は、商業的供給源から入手できるか、又は当業者に公知の方法を用いて慎重に単離した化合物として製造することができる。(Kukla, M. J. Bioorg. Med. Chem. Let. 2001, 11, 2235; Yamada, K. J. Med. Chem. 2001, 44, 3355)。
実施例39: 4-{[2-(4-メチルベンゾイル)フェニル]アミノ}-2-[(3,4,5-トリメトキシフェニル)アミノ]-ピリミジン-5-カルボニトリル
I. PLK1の阻害に関するアッセイ
A. 6x N末端His標識PLKキナーゼドメインの作製
6x N末端His標識PLKキナーゼドメイン(MKKGHHHHHHDが先行するアミノ酸21〜346)は、バキュロウイルスに感染したT. ni細胞から、ポリヘドリンプロモーターで制御して作製した。全ての手順は4℃で行った。細胞を25 mM HEPES、200 mM NaCl、25 mM イミダゾール;pH8.0中で溶解した。このホモジネートを SLA-1500 ローターで14K rpm で40分間遠心分離し、上澄み液を1.2ミクロンフィルターに通して濾過した。上澄み液をニッケルキレート化 Sepharose (Amersham Pharmacia) カラム上に負荷し、25 mM HEPES、500 mM NaCl、25 mM イミダゾール;pH8.0で洗浄した。次いでカラムを16.6%Bの段階(ここで、緩衝液Bは25 mM HEPES、500 mM NaCl、300 mM イミダゾール;pH8.0である)で洗浄した。16.6%B〜100%Bの10倍カラム容量線形勾配を用いてタンパク質を溶離した。PLKを含む分画をSDS-PAGEにより決定した。10 kDa 分子量カットオフ膜を用いてPLKを濃縮し、25 mM HEPES、1 mM DTT、500 mM NaCl;pH8.0中で平衡化したSuperdex 75 ゲル濾過 (Amersham Pharmacia) カラム上に負荷した。PLKを含む分画をSDS-PAGEにより決定した。PLKをプールし、アリコートに分割し、−80℃で保存した。サンプルは質量分析により品質管理した。
化合物をプレートに加えた(100% DMSO 中1μl)。DMSO(最終2%)及びEDTA(最終55.5 mM)をコントロールとして用いた。反応混合物Aは4℃で下記のように調製する:
反応混合物A(基質混合物):
25 mM HEPES、pH7.2
15 mM MgCl2
2μM ATP
0.1μCi/ウェル 33P-γ ATP (10Ci/mMol)
2μM 基質ペプチド(ビオチン-Ahx-SFNDTLDFD)
反応混合物Bは4℃で下記のように調製する:
反応混合物B(酵素混合物):
25 mM HEPES、pH7.2
15 mM MgCl2
0.15 mg/ml BSA
2 mM DTT
2〜10 nM PLK1キナーゼドメイン
反応混合物A(20μl)をウェルごとに加える。反応混合物B(20μl)をウェルごとに加える。室温で1.5時間インキュベートする。酵素反応を175μl のSPA/EDTAビーズ混合物(29 mM EDTA、標準ダルベッコPBS(Mg2+及びCa2+を含まない)中の2.5 mg/ml ストレプトアビジン被覆SPA、60μM ATP)で停止する。プレートを1,000×gで7分間密封遠心分離(室温で1時間インキュベートした後)するか、又は一夜沈降させ、次いでプレートを Packard TopCount において30秒/ウェルでカウントする。
得られたデータを下記表1に報告する。表1において、+ = pIC50 < 5;++ = pIC 50 5〜7;+++ = pIC50 > 7である。
正常非と包皮細胞線維芽細胞(HFF)、並びにヒトの結腸癌(HCT116、RKO)、肺癌(H460)、前立腺癌(PC3)及び乳癌(MCF7)細胞株を、10%ウシ胎仔血清(FBS)を含む高グルコースDMEM (Life Technologies) 中で、加湿した10%CO2、90%空気インキュベーター中37℃で培養した。トリプシン/EDTAを用いて細胞を採取し、血球計算器を用いてカウントし、96ウェル組織培養プレート (Falcon 3075) に入れた100μlの適切な培地に下記の密度で塗布した:HFFは5,000細胞/ウェル、HCT116は3,000細胞/ウェル、RKOは2,500細胞/ウェル、H460は2,000細胞/ウェル、PC3は8,000細胞/ウェル、MCF7は4,000細胞/ウェル。翌日、化合物を、DMSO中の10 mM ストック溶液から、100μg/ml のゲンタマイシンを含むDMEM中で最終必要濃度の2倍に希釈した。100μl/ウェルのこれらの希釈物を、細胞プレート上に現在あるのと同じ培地100μlに加えた。DMEM中で希釈した化合物を全ての細胞株に加えた。全てのウェル中のDMSO最終濃度は0.3%であった。細胞を37℃、10%CO2で3日間インキュベートした。培地を吸引により除去した。細胞をウェル当たり90μl のメチレンブルー (Sigma M9140、50:50のエタノール:水中0.5%) で染色し、室温で30分間インキュベートすることにより細胞バイオマスを評価した。染色液を除去し、プレートを穏やかな水流下ですすぎ、空気乾燥した。細胞から染色を遊離させるために、100μl の可溶化溶液を加え(PBS中1% N-ラウロイルザルコシン、ナトリウム塩、Sigma L5125)、プレートを穏やかに30分間振盪した。620 nM での光学密度をマイクロプレートリーダーで測定した。細胞成長のパーセント阻害をビヒクルで処理したコントロールウェルに対して計算した。細胞成長を50%阻害する化合物の濃度(IC50)を、非線形回帰 (Levenberg-Marquardt) 及び式 y = Vmax *(1−(x/(K+x)))+ Y2を用いて補間した。ここで、式中の「K」はIC50と等しかった。得られたデータを下記表1に報告する。表1において、+ = 10 〜 > 30 uM;++ = 1〜10 uM;+++ = < 1 uM である。
Claims (3)
- 式(I):
R1は、H、ハロ、アルキル、アルケニル、アルキニルからなる群から選択され;
R2は、ハロ、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、-(R7)g-C(O)R6、-(R7)g-CO2R6、-(R7)g-C(O)N(R6)2、-(R7)g-OR6、-O-(R7)g-Ay、-(R7)g-S(O)eR6、-(R7)g-N(R6)2、-(R7)g-N(R6)C(O)R6、-(R7)g-CN、-(R7)g-SCN、-NO2、-N3、Ay、並びにN、O及びSから選択される1又は2個のヘテロ原子を含む5〜9員のヘテロアリールからなる群から選択され;
各R3は、同一又は異なって、そして独立して、H又アルキルであり;
Yは、-C(O)R8、-C(S)R8、-S(O)eR9、-S(O)eN(R9)2、-N(R9)2、-N(R9)-S(O)eR9、-N(R9)-C(O)R9、-N(R9)-CO2R9及び-N(R9)-C(O)N(R9)2からなる群から選択されるか、
又は、Yは、C-2及びC-3と一緒になって、式A:
ここで、R8はアルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay、Het、-OR6、-O-(R7)g-Ay、-O-(R7)g-Het、-N(R6)2、-N(R6)-(R7)g-Ay、-N(R6)-(R7)g-Het、-N(R6)-(R7)g-OR6、-N(R6)-(R7)g-C(O)R6、-N(R6)-(R7)g-CO2R6、-N(R6)-(R7)g-SO2R6及び-N(R6)-(R7)g-N(R6)2からなる群から選択され;
各R9は、同一又は異なって、そして独立して、H、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay及びHetからなる群から選択され;
cは、0又は1であり;
Z1、Z2、Z3及びZ4は、それぞれ独立して、C、O、S及びNからなる群から選択され、ここで、cが0である場合には、Z1、Z2及びZ3の少なくとも1つはCであり、そしてcが1である場合には、Z1、Z2、Z3及びZ4の少なくとも2つはCであり;
各破線は、任意に二重結合を表し;
dは、0、1又は2であり;
各R10は、同一又は異なって、そして独立して、ハロ、アルキル、オキソ、ヒドロキシ、メルカプト及びアミノからなる群から選択され;
aは、0、1、2又は3であり;
各R4は、同一又は異なって、そして独立して、ハロ、アルキル、アルケニル、アルキニル、-(R7)g-シクロアルキル、-(R7)g-シクロアルケニル、-(R7)g-Ay、-(R7)g-Het、-(R7)g-C(O)R6、-(R7)g-C(O)Ay、-(R7)g-C(O)Het、-(R7)g-CO2R6、-(R7)g-CO2Ay、-(R7)g-CO2Het、-(R7)g-C(O)N(R6)2、-(R7)g-OR6、-(R7)g-OAy、-(R7)g-OHet、-(R7)g-OC(O)R6、-(R7)g-OC(O)Ay、-(R7)g-OC(O)Het、-(R7)g-S(O)eR6、-(R7)g-S(O)eAy、-(R7)g-S(O)eHet、-(R7)g-S(O)eN(R6)2、-(R7)g-S(O)eN(R6)Ay、-(R7)g-S(O)eN(R6)Het、-(R7)g-N(R6)2、-(R7)g-N(R6)Ay、-(R7)g-N(R6)Het、-(R7)g-N(R6)C(O)R6、-(R7)g-N(R6)C(O)Ay、-(R7)g-N(R6)C(O)Het、-(R7)g-N(R6)C(O)N(R6)2、-(R7)g-N(R6)S(O)eR6、-(R7)g-N(R6)S(O)eAy、-(R7)g-N(R6)S(O)eHet、-NO2、-CN、-SCN及び-N3からなる群から選択されるか、又は
2個の隣接するR4は、それらが結合している炭素原子と一緒になって、フェニル又はN、O及びSからなる群から選択される1又は2個のヘテロ原子を含む5若しくは6員のヘテロ環若しくはヘテロアリールを形成し;
各eは、同一又は異なって、そして独立して、0、1又は2であり;
bは、0、1、2、3、4又は5であり;
各R5は、同一又は異なって、式(R7)g-R11の基であるか、又は2個の隣接するR5基は、それぞれ同一又は異なって、そして独立して、アルキル、アルケニル、-OR6、-S(O)eR6及び-N(R6)2からなる群から選択され、そしてそれらが結合している炭素原子と一緒になって、C5-6シクロアルキル、C5-6シクロアルケニル又はN、O及びSからなる群から選択される1又は2個のヘテロ原子を含む5若しくは6員のヘテロ環若しくはヘテロアリールを形成し;
各R6は、同一又は異なって、そして独立して、H、アルキル、アルケニル、アルキニル、シクロアルキル及びシクロアルケニルからなる群から選択され;
gは、0又は1であり;
R7はアルキレン又はアルケニレンであり;
Ayは、アリールであり;
Hetは、N、O及びSからなる群から選択される1、2又は3個のヘテロ原子を含む5員又は6員のヘテロ環若しくはヘテロアリールであり;
R11は、ハロ、アルキル、アルケニル、アルキニル、シクロアルキル、シクロアルケニル、Ay、Het、-C(O)R6、-C(O)Ay、-C(O)Het、-CO2R6、-CO2Ay、-CO2Het、-C(O)-R7-OR6、-C(O)-R7-OAy、-C(O)-R7-OHet、-C(O)N(R6)2、-C(O)N(R6)Ay、-C(O)N(R6)Het、-C(O)N(R6)-(R7)g-N(R6)2、-C(O)N(R6)-(R7)g-CO2R6、-C(O)N(R6)-(R7)g-S(O)eR6、-OR6、-OC(O)R6、-O-(R7)g-Ay、-OC(O)Ay、-O-(R7)g-Het、-OC(O)Het、-O-R7-OR6、-O-R7-N(R6)2、-S(O)eR6、-S(O)e-(R7)g-Ay、-S(O)e-(R7)g-Het、-S(O)e-(R7)g-N(R6)2、-S(O)e-(R7)g-N(R6)Ay、-S(O)e-(R7)g-N(R6)Het、-S(O)eN(R6)-(R7)g-C(O)R6、-S(O)eN(R6)-(R7)g-C(O)Ay、-S(O)eN(R6)-(R7)g-C(O)Het、-N(R6)2、-N(R6)-(R7)g-Ay、-N(R6)-(R7)g-Het、-N(R6)-(R7)g-C(O)R6、-N(R6)-C(O)-(R7)g-Ay、-N(R6)-C(O)-(R7)g-Het、-N(R6)-C(O)-(R7)g-N(R6)2、-N(R6)-C(O)-(R7)g-N(R6)Ay、-N(R6)-C(O)-(R7)g-N(R6)Het、-N(R6)-C(O)-(R7)g-N(R6)-(R7-O)h-N(R6)-CO2R6、-N(R6)-(R7)g-S(O)eR6、-N(R6)-(R7)g-S(O)eAy、-N(R6)-(R7)g-S(O)eHet、-N(R6)-R7-N(R6)2、-N(R6)-R7-OR6、-CN、-SCN、-NO2及び-N3からなる群から選択され;そして
hは、1〜20であり;
ここで、R1が-CH3であり、R2がBr又はNO2であり、両方のR3がHであり、aが0であり、そしてbが0又は1であり、R5が-CO2Hである場合には、Yは-CO2Hではない。]
の化合物又はその薬学的に許容される塩若しくは溶媒和物。 - 2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)安息香酸塩酸塩;
2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)ベンズアミド塩酸塩;
N-(tert-ブチル)-2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)ベンズアミド塩酸塩;
N-[4-({4-[(2-ベンゾイルフェニル)アミノ]-5-ニトロピリミジン-2-イル}アミノ)フェニル]アセトアミド塩酸塩;
8-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)-3,4-ジヒドロナフタレン-1(2H)-オン塩酸塩;
1-[2-({5-ブロモ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)フェニル]エタノン塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]-N-メチルベンズアミド塩酸塩;
N4-(1H-インドール-4-イル)-5-ニトロ-N2-(3,4,5-トリメトキシフェニル)ピリミジン-2,4-ジアミン塩酸塩;
2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)安息香酸メチル塩酸塩;
N4-(2,3-ジヒドロ-1,4-ベンゾジオキシン-5-イル)-5-ニトロ-N2-(3,4,5-トリメトキシフェニル)ピリミジン-2,4-ジアミン塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]安息香酸シクロヘキシル塩酸塩;
5-ヒドロキシ-2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)安息香酸塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]安息香酸塩酸塩;
N-[4-({4-[(2-アセチルフェニル)アミノ]-5-ブロモピリミジン-2-イル}アミノ)フェニル]アセトアミド塩酸塩;
N-[4-({5-ブロモ-4-[(2-モルホリン-4-イルフェニル)アミノ]ピリミジン-2-イル}アミノ)フェニル]アセトアミド塩酸塩;
5-[(5-ブロモ-4-{[2-(メチルチオ)フェニル]アミノ}ピリミジン-2-イル)アミノ]-1,3-ジヒドロ-2H-ベンズイミダゾール-2-オン塩酸塩;
5-ブロモ-N4-(2-モルホリン-4-イルフェニル)-N2-(3,4,5-トリメトキシフェニル)ピリミジン-2,4-ジアミン塩酸塩;
N-[4-({5-ブロモ-4-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-2-イル}アミノ)フェニル]アセトアミド塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]テレフタル酸ジメチル塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]安息香酸ベンジル塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]-6-メチル安息香酸メチル塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]安息香酸イソブチル塩酸塩;
2-[(2-{[4-(アセチルアミノ)フェニル]アミノ}-5-ニトロピリミジン-4-イル)アミノ]-6-メチル安息香酸塩酸塩;
N-シクロヘキシル-2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)ベンズアミド塩酸塩;
1-[2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)フェニル]エタノン塩酸塩;
[5-クロロ-2-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)フェニル](2-フルオロフェニル)メタノン塩酸塩;
8-({5-ニトロ-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)-2-ナフトール塩酸塩;
N-(tert-ブチル)-2-({5-メチルケトン-2-[(3,4,5-トリメトキシフェニル)アミノ]ピリミジン-4-イル}アミノ)ベンズアミド;
4-{[2-(4-メチルベンゾイル)フェニル]アミノ}-2-[(3,4,5-トリメトキシフェニル)アミノ]-ピリミジン-5-カルボニトリル;並びに
その薬学的に許容される塩及び溶媒和物
からなる群から選択される化合物。 - 動物における感受性新生物の治療に使用するための、請求項1又は2記載の化合物を含有する医薬組成物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US44879503P | 2003-02-20 | 2003-02-20 | |
| PCT/US2004/004197 WO2004074244A2 (en) | 2003-02-20 | 2004-02-11 | Pyrimidine compounds |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2006518386A JP2006518386A (ja) | 2006-08-10 |
| JP4634367B2 true JP4634367B2 (ja) | 2011-02-16 |
Family
ID=32908652
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006503537A Expired - Lifetime JP4634367B2 (ja) | 2003-02-20 | 2004-02-11 | ピリミジン化合物 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US7514446B2 (ja) |
| EP (1) | EP1597251B1 (ja) |
| JP (1) | JP4634367B2 (ja) |
| AT (1) | ATE433447T1 (ja) |
| DE (1) | DE602004021472D1 (ja) |
| ES (1) | ES2325440T3 (ja) |
| WO (1) | WO2004074244A2 (ja) |
Families Citing this family (107)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI329105B (en) | 2002-02-01 | 2010-08-21 | Rigel Pharmaceuticals Inc | 2,4-pyrimidinediamine compounds and their uses |
| GB0206215D0 (en) | 2002-03-15 | 2002-05-01 | Novartis Ag | Organic compounds |
| HRP20050089B1 (hr) | 2002-07-29 | 2015-06-19 | Rigel Pharmaceuticals | Upotreba 2,4 pirimidindiaminskog spoja za proizvodnju lijeka za lijeäśenje ili sprjeäśavanje autoimunosne bolesti |
| GB0305929D0 (en) | 2003-03-14 | 2003-04-23 | Novartis Ag | Organic compounds |
| WO2005012294A1 (en) | 2003-07-30 | 2005-02-10 | Rigel Pharmaceuticals, Inc. | 2,4-pyrimidinediamine compounds for use in the treatment or prevention of autoimmune diseases |
| ATE506953T1 (de) * | 2003-08-07 | 2011-05-15 | Rigel Pharmaceuticals Inc | 2,4-pyrimidindiamin-verbindungen und verwendungen als antiproliferative mittel |
| PT1660458E (pt) * | 2003-08-15 | 2012-04-27 | Novartis Ag | 2,4-pirimidinodiaminas úteis no tratamento de doenças neoplásicas, desordens inflamatórias e do sistema imunitário |
| GB0321710D0 (en) * | 2003-09-16 | 2003-10-15 | Novartis Ag | Organic compounds |
| US20070105839A1 (en) * | 2003-09-18 | 2007-05-10 | Patricia Imbach | 2, 4-Di (phenylamino) pyrimidines useful in the treatment of proliferative disorders |
| US7521457B2 (en) | 2004-08-20 | 2009-04-21 | Boehringer Ingelheim International Gmbh | Pyrimidines as PLK inhibitors |
| EP2402323A3 (en) | 2004-10-13 | 2012-05-30 | PTC Therapeutics, Inc. | Pyrazole or triazole compounds and their use for the manufacture of a medicament for treating somatic mutation-related diseases |
| SI1814878T1 (sl) | 2004-11-24 | 2012-06-29 | Rigel Pharmaceuticals Inc | Spojine spiro-2,4-pirimidindiamina in njihova uporaba |
| ATE519759T1 (de) | 2004-12-30 | 2011-08-15 | Exelixis Inc | Pyrimidinderivate als kinasemodulatoren und anwendungsverfahren |
| AU2006206458B2 (en) | 2005-01-19 | 2012-10-25 | Rigel Pharmaceuticals, Inc. | Prodrugs of 2,4-pyrimidinediamine compounds and their uses |
| WO2006129100A1 (en) * | 2005-06-03 | 2006-12-07 | Glaxo Group Limited | Novel compounds |
| BRPI0610876B8 (pt) | 2005-06-08 | 2021-05-25 | Rigel Pharmaceuticals Inc | composto, formulação farmacêutica, e métodos de inibir uma atividade de uma jak cinase, e de inibir uma cascata de transdução de sinal em que jak3 cinase desempenha um papel |
| US20070203161A1 (en) | 2006-02-24 | 2007-08-30 | Rigel Pharmaceuticals, Inc. | Compositions and methods for inhibition of the jak pathway |
| TW200736232A (en) * | 2006-01-26 | 2007-10-01 | Astrazeneca Ab | Pyrimidine derivatives |
| TW200804364A (en) | 2006-02-22 | 2008-01-16 | Boehringer Ingelheim Int | New compounds |
| ES2622493T3 (es) | 2006-02-24 | 2017-07-06 | Rigel Pharmaceuticals, Inc. | Composiciones y métodos para la inhibición de la ruta de JAK |
| US7504513B2 (en) | 2006-02-27 | 2009-03-17 | Hoffman-La Roche Inc. | Thiazolyl-benzimidazoles |
| CA2648170A1 (en) * | 2006-04-10 | 2007-10-18 | Boehringer Ingelheim International Gmbh | 2, 4-diaminopyrimidine derivatives and their use for the treatment of cancer |
| PE20120006A1 (es) | 2006-05-15 | 2012-02-02 | Boehringer Ingelheim Int | Compuestos derivados de pirimidina como inhibidores de la quinasa aurora |
| ES2535877T3 (es) * | 2006-06-19 | 2015-05-18 | Asklepios Biopharmaceutical, Inc. | Genes de Factor VIII y Factor IX modificados y vectores para la terapia génica |
| EP2043651A2 (en) * | 2006-07-05 | 2009-04-08 | Exelixis, Inc. | Methods of using igf1r and abl kinase modulators |
| WO2008009458A1 (en) * | 2006-07-21 | 2008-01-24 | Novartis Ag | 2, 4 -di (arylaminio) -pyrimidine-5-carboxamide compounds as jak kinases inhibitors |
| NZ577197A (en) | 2006-12-08 | 2011-02-25 | Irm Llc | Pyrimidine compounds especially 4-phenylamino-2-arylamino-pyrimidine derivatives and compositions as protein kinase inhibitors |
| PE20081636A1 (es) * | 2007-01-26 | 2009-01-10 | Smithkline Beecham Corp | Inhibidores de antranilamida para aurora quinasa |
| TW200840581A (en) * | 2007-02-28 | 2008-10-16 | Astrazeneca Ab | Novel pyrimidine derivatives |
| EP2100894A1 (en) | 2008-03-12 | 2009-09-16 | 4Sc Ag | Pyridopyrimidines used as Plk1 (polo-like kinase) inhibitors |
| WO2009127642A2 (en) * | 2008-04-15 | 2009-10-22 | Cellzome Limited | Use of lrrk2 inhibitors for neurodegenerative diseases |
| US8063058B2 (en) | 2008-04-16 | 2011-11-22 | Portola Pharmaceuticals, Inc. | Inhibitors of syk and JAK protein kinases |
| US8138339B2 (en) | 2008-04-16 | 2012-03-20 | Portola Pharmaceuticals, Inc. | Inhibitors of protein kinases |
| US9273077B2 (en) | 2008-05-21 | 2016-03-01 | Ariad Pharmaceuticals, Inc. | Phosphorus derivatives as kinase inhibitors |
| MX353308B (es) | 2008-05-21 | 2018-01-08 | Ariad Pharma Inc | Derivados fosforosos como inhibidores de cinasa. |
| US11351168B1 (en) | 2008-06-27 | 2022-06-07 | Celgene Car Llc | 2,4-disubstituted pyrimidines useful as kinase inhibitors |
| US8338439B2 (en) | 2008-06-27 | 2012-12-25 | Celgene Avilomics Research, Inc. | 2,4-disubstituted pyrimidines useful as kinase inhibitors |
| NZ603525A (en) * | 2008-06-27 | 2015-02-27 | Celgene Avilomics Res Inc | Pyrimidine based compound and uses thereof |
| WO2010033941A1 (en) | 2008-09-22 | 2010-03-25 | Array Biopharma Inc. | Substituted imidazo[1,2b]pyridazine compounds as trk kinase inhibitors |
| AR074210A1 (es) | 2008-11-24 | 2010-12-29 | Boehringer Ingelheim Int | Derivados de pirimidina como inhibidores de ptk2-quinasa |
| TW201024281A (en) | 2008-11-24 | 2010-07-01 | Boehringer Ingelheim Int | New compounds |
| WO2010121675A2 (en) | 2008-12-18 | 2010-10-28 | F. Hoffmann-La Roche Ag | Thiazolyl-benzimidazoles |
| JP5815411B2 (ja) * | 2008-12-30 | 2015-11-17 | ライジェル ファーマシューティカルズ, インコーポレイテッド | ピリミジンジアミンキナーゼ阻害剤 |
| US9908884B2 (en) | 2009-05-05 | 2018-03-06 | Dana-Farber Cancer Institute, Inc. | EGFR inhibitors and methods of treating disorders |
| TW201100441A (en) | 2009-06-01 | 2011-01-01 | Osi Pharm Inc | Amino pyrimidine anticancer compounds |
| CA2763717A1 (en) * | 2009-06-10 | 2010-12-16 | Cellzome Limited | Pyrimidine derivatives as zap-70 inhibitors |
| AR077468A1 (es) | 2009-07-09 | 2011-08-31 | Array Biopharma Inc | Compuestos de pirazolo (1,5 -a) pirimidina sustituidos como inhibidores de trk- quinasa |
| US8927547B2 (en) | 2010-05-21 | 2015-01-06 | Noviga Research Ab | Pyrimidine derivatives |
| MX336875B (es) | 2010-08-10 | 2016-02-04 | Celgene Avilomics Res Inc | Sal de besilato de un inhibidor de tirosina cinasa de bruton (btk). |
| EP2635284B1 (en) | 2010-11-01 | 2019-12-18 | Celgene CAR LLC | Heterocyclic compounds and uses thereof |
| WO2012061303A1 (en) | 2010-11-01 | 2012-05-10 | Avila Therapeutics, Inc. | Heteroaryl compounds and uses thereof |
| WO2012064706A1 (en) | 2010-11-10 | 2012-05-18 | Avila Therapeutics, Inc. | Mutant-selective egfr inhibitors and uses thereof |
| EP2646448B1 (en) | 2010-11-29 | 2017-08-30 | OSI Pharmaceuticals, LLC | Macrocyclic kinase inhibitors |
| DK2688883T3 (en) | 2011-03-24 | 2016-09-05 | Noviga Res Ab | pyrimidine |
| EP2704572B1 (en) | 2011-05-04 | 2015-12-30 | Ariad Pharmaceuticals, Inc. | Compounds for inhibiting cell proliferation in egfr-driven cancers |
| EP3812387A1 (en) | 2011-07-21 | 2021-04-28 | Sumitomo Dainippon Pharma Oncology, Inc. | Heterocyclic protein kinase inhibitors |
| US9364476B2 (en) | 2011-10-28 | 2016-06-14 | Celgene Avilomics Research, Inc. | Methods of treating a Bruton's Tyrosine Kinase disease or disorder |
| MX363551B (es) | 2011-11-23 | 2019-03-27 | Portola Pharmaceuticals Inc Star | Compuestos derivados de pirazina como inhibidores de cinasa. |
| CA2866852C (en) | 2012-03-15 | 2020-12-29 | Celgene Avilomics Research, Inc. | Solid forms of an epidermal growth factor receptor kinase inhibitor |
| BR112014022790B1 (pt) | 2012-03-15 | 2022-04-19 | Celgene Car Llc | Sais de um inibidor de quinase de receptor de fator do crescimento epidermal, composição farmacêutica e usos do mesmo |
| WO2013169401A1 (en) | 2012-05-05 | 2013-11-14 | Ariad Pharmaceuticals, Inc. | Compounds for inhibiting cell proliferation in egfr-driven cancers |
| US9126950B2 (en) | 2012-12-21 | 2015-09-08 | Celgene Avilomics Research, Inc. | Heteroaryl compounds and uses thereof |
| MX2015009952A (es) | 2013-02-08 | 2015-10-05 | Celgene Avilomics Res Inc | Inhibidores de cinasas reguladas por señales extracelulares (erk) y sus usos. |
| MX394360B (es) * | 2013-03-14 | 2025-03-24 | Sumitomo Pharma Oncology Inc | Inhibidores de jak2 y alk2 y metodos para su uso. |
| US9611283B1 (en) | 2013-04-10 | 2017-04-04 | Ariad Pharmaceuticals, Inc. | Methods for inhibiting cell proliferation in ALK-driven cancers |
| CN104230954A (zh) * | 2013-06-08 | 2014-12-24 | 中国科学院上海药物研究所 | 2,4-二氨基嘧啶类化合物及其医药用途 |
| US9492471B2 (en) | 2013-08-27 | 2016-11-15 | Celgene Avilomics Research, Inc. | Methods of treating a disease or disorder associated with Bruton'S Tyrosine Kinase |
| US9415049B2 (en) | 2013-12-20 | 2016-08-16 | Celgene Avilomics Research, Inc. | Heteroaryl compounds and uses thereof |
| EP3179858B1 (en) | 2014-08-13 | 2019-05-15 | Celgene Car Llc | Forms and compositions of an erk inhibitor |
| US10266549B2 (en) * | 2014-08-25 | 2019-04-23 | Salk Institute For Biological Studies | ULK1 inhibitors and methods using same |
| CN105503827B (zh) * | 2014-10-11 | 2019-09-24 | 上海翰森生物医药科技有限公司 | Egfr抑制剂及其制备方法和用途 |
| BR112018000808A2 (pt) | 2015-07-16 | 2018-09-04 | Array Biopharma Inc | compostos de pirazolo[1,5-a]piridina substituída como inibidores de ret cinase |
| EP3368039A1 (en) | 2015-10-26 | 2018-09-05 | The Regents of The University of Colorado, A Body Corporate | Point mutations in trk inhibitor-resistant cancer and methods relating to the same |
| AU2017246547B2 (en) | 2016-04-04 | 2023-02-23 | Loxo Oncology, Inc. | Methods of treating pediatric cancers |
| FI3439662T3 (fi) | 2016-04-04 | 2024-09-04 | Loxo Oncology Inc | (s)-n-(5-((r)-2-(2,5-difluorifenyyli)pyrrolidin-1-yyli)pyratsolo[1,5-a]pyrimidin-3-yyli)-3-hydroksipyrrolidiini-1-karboksamidin nesteformulaatioita |
| US10045991B2 (en) | 2016-04-04 | 2018-08-14 | Loxo Oncology, Inc. | Methods of treating pediatric cancers |
| EP3458456B1 (en) | 2016-05-18 | 2020-11-25 | Loxo Oncology Inc. | Preparation of (s)-n-(5-((r)-2-(2,5-difluorophenyl)pyrrolidin-1-yl)pyrazolo[1,5-a]pyrimidin-3-yl)-3-hydroxypyrrolidine-1-carboxamide |
| TWI704148B (zh) | 2016-10-10 | 2020-09-11 | 美商亞雷生物製藥股份有限公司 | 作為ret激酶抑制劑之經取代吡唑并[1,5-a]吡啶化合物 |
| TWI752098B (zh) | 2016-10-10 | 2022-01-11 | 美商亞雷生物製藥股份有限公司 | 作為ret激酶抑制劑之經取代吡唑并[1,5-a]吡啶化合物 |
| JOP20190092A1 (ar) | 2016-10-26 | 2019-04-25 | Array Biopharma Inc | عملية لتحضير مركبات بيرازولو[1، 5-a]بيريميدين وأملاح منها |
| WO2018136661A1 (en) | 2017-01-18 | 2018-07-26 | Andrews Steven W | SUBSTITUTED PYRAZOLO[1,5-a]PYRAZINE COMPOUNDS AS RET KINASE INHIBITORS |
| WO2018136663A1 (en) | 2017-01-18 | 2018-07-26 | Array Biopharma, Inc. | Ret inhibitors |
| JOP20190213A1 (ar) | 2017-03-16 | 2019-09-16 | Array Biopharma Inc | مركبات حلقية ضخمة كمثبطات لكيناز ros1 |
| CN107235931B (zh) * | 2017-07-11 | 2019-09-24 | 大连医科大学 | 新型嘧啶类抗肿瘤化合物及其制备方法与用途 |
| TWI876442B (zh) | 2017-10-10 | 2025-03-11 | 美商絡速藥業公司 | 6-(2-羥基-2-甲基丙氧基)-4-(6-(6-((6-甲氧基吡啶-3-基)甲基)-3,6-二氮雜雙環[3.1.1]庚-3-基)吡啶-3-基)吡唑并[1,5-a]吡啶-3-甲腈之調配物 |
| TWI791053B (zh) | 2017-10-10 | 2023-02-01 | 美商亞雷生物製藥股份有限公司 | 6-(2-羥基-2-甲基丙氧基)-4-(6-(6-((6-甲氧基吡啶-3-基)甲基)-3,6-二氮雜雙環[3.1.1]庚-3-基)吡啶-3-基)吡唑并[1,5-a]吡啶-3-甲腈之結晶形式及其醫藥組合物 |
| US11472802B2 (en) | 2018-01-18 | 2022-10-18 | Array Biopharma Inc. | Substituted pyrazolyl[4,3-c]pyridine compounds as RET kinase inhibitors |
| JP7060694B2 (ja) | 2018-01-18 | 2022-04-26 | アレイ バイオファーマ インコーポレイテッド | Retキナーゼ阻害剤としての置換ピロロ[2,3-d]ピリミジン化合物 |
| EP3740490A1 (en) | 2018-01-18 | 2020-11-25 | Array Biopharma, Inc. | Substituted pyrazolo[3,4-d]pyrimidine compounds as ret kinase inhibitors |
| KR20210003780A (ko) | 2018-04-05 | 2021-01-12 | 스미토모 다이니폰 파마 온콜로지, 인크. | Axl 키나제 억제제 및 그의 용도 |
| JP2021521170A (ja) | 2018-04-13 | 2021-08-26 | スミトモ ダイニッポン ファーマ オンコロジー, インコーポレイテッド | 骨髄増殖性新生物およびがんに関連する線維症の処置のためのpimキナーゼ阻害剤 |
| AU2019310590A1 (en) | 2018-07-26 | 2021-01-14 | Sumitomo Pharma Oncology, Inc. | Methods for treating diseases associated with abnormal acvr1 expression and acvr1 inhibitors for use in the same |
| CN117285467A (zh) | 2018-07-31 | 2023-12-26 | 罗索肿瘤学公司 | 喷雾干燥的分散体和制剂 |
| CN112996794A (zh) | 2018-09-10 | 2021-06-18 | 阿雷生物药品公司 | 作为ret激酶抑制剂的稠合杂环化合物 |
| US12351571B2 (en) | 2018-12-19 | 2025-07-08 | Array Biopharma Inc. | Substituted quinoxaline compounds as inhibitors of FGFR tyrosine kinases |
| EP3898626A1 (en) | 2018-12-19 | 2021-10-27 | Array Biopharma, Inc. | Substituted pyrazolo[1,5-a]pyridine compounds as inhibitors of fgfr tyrosine kinases |
| KR20260008165A (ko) | 2019-02-12 | 2026-01-15 | 스미토모 파마 아메리카, 인크. | 헤테로시클릭 단백질 키나제 억제제를 포함하는 제제 |
| EP3994132A1 (en) | 2019-07-03 | 2022-05-11 | Sumitomo Dainippon Pharma Oncology, Inc. | Tyrosine kinase non-receptor 1 (tnk1) inhibitors and uses thereof |
| CN112876420B (zh) * | 2019-11-29 | 2023-01-24 | 沈阳化工研究院有限公司 | 一种硫代苯甲酰衍生物及其应用 |
| IL294214B2 (en) | 2019-12-27 | 2026-04-01 | Schrodinger Inc | Cyclic compounds and methods for using them |
| US12441707B2 (en) | 2019-12-30 | 2025-10-14 | Tyra Biosciences, Inc. | Indazole compounds |
| KR20220153582A (ko) | 2020-02-14 | 2022-11-18 | 솔크 인스티튜트 포 바이올로지칼 스터디즈 | 마크로시클릭 ulk1/2 억제제 |
| CN116490507A (zh) | 2020-09-10 | 2023-07-25 | 薛定谔公司 | 用于治疗癌症的杂环包缩合cdc7激酶抑制剂 |
| EP4284804A1 (en) | 2021-01-26 | 2023-12-06 | Schrödinger, Inc. | Tricyclic compounds useful in the treatment of cancer, autoimmune and inflammatory disorders |
| TW202300150A (zh) | 2021-03-18 | 2023-01-01 | 美商薛定諤公司 | 環狀化合物及其使用方法 |
| CN120302975A (zh) | 2022-10-31 | 2025-07-11 | 住友制药美国公司 | 治疗骨髓增生性肿瘤的pim1抑制剂 |
| WO2025059027A1 (en) | 2023-09-11 | 2025-03-20 | Schrödinger, Inc. | Cyclopenta[e]pyrazolo[1,5-a]pyrimidine derivatives as malt1 inhibitors |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9523675D0 (en) | 1995-11-20 | 1996-01-24 | Celltech Therapeutics Ltd | Chemical compounds |
| GB9622363D0 (en) | 1996-10-28 | 1997-01-08 | Celltech Therapeutics Ltd | Chemical compounds |
| EA002973B1 (ru) | 1998-03-27 | 2002-12-26 | Янссен Фармацевтика Н.В. | Производные пиримидина в качестве ингибиторов репликации вируса иммунодефицита человека |
| ATE342892T1 (de) | 1998-08-29 | 2006-11-15 | Astrazeneca Ab | Pyrimidine verbindungen |
| SK287270B6 (sk) * | 1998-11-10 | 2010-05-07 | Janssen Pharmaceutica N. V. | Derivát pyrimidínu |
| GB9828511D0 (en) * | 1998-12-24 | 1999-02-17 | Zeneca Ltd | Chemical compounds |
| AU3704101A (en) | 2000-02-17 | 2001-08-27 | Amgen Inc | Kinase inhibitors |
| GB0004888D0 (en) | 2000-03-01 | 2000-04-19 | Astrazeneca Uk Ltd | Chemical compounds |
| GB0004886D0 (en) | 2000-03-01 | 2000-04-19 | Astrazeneca Uk Ltd | Chemical compounds |
| GB0004887D0 (en) | 2000-03-01 | 2000-04-19 | Astrazeneca Uk Ltd | Chemical compounds |
| GB0004890D0 (en) | 2000-03-01 | 2000-04-19 | Astrazeneca Uk Ltd | Chemical compounds |
| BR0116452A (pt) | 2000-12-21 | 2003-09-30 | Glaxo Group Ltd | Composto, composição farmacêutica, uso de um composto |
| US20040171630A1 (en) | 2001-06-19 | 2004-09-02 | Yuntae Kim | Tyrosine kinase inhibitors |
| WO2003030909A1 (en) | 2001-09-25 | 2003-04-17 | Bayer Pharmaceuticals Corporation | 2- and 4-aminopyrimidines n-substtituded by a bicyclic ring for use as kinase inhibitors in the treatment of cancer |
| ATE407678T1 (de) * | 2001-10-17 | 2008-09-15 | Boehringer Ingelheim Pharma | Pyrimidinderivate, arzneimittel enthaltend diese verbindungen, deren verwendung und verfahren zu ihrer herstellung |
| TWI329105B (en) * | 2002-02-01 | 2010-08-21 | Rigel Pharmaceuticals Inc | 2,4-pyrimidinediamine compounds and their uses |
| GB0206215D0 (en) * | 2002-03-15 | 2002-05-01 | Novartis Ag | Organic compounds |
| WO2004050068A1 (en) | 2002-11-29 | 2004-06-17 | Janssen Pharmaceutica N.V. | Pharmaceutical compositions comprising a basic respectively acidic drug compound, a surfactant and a physiologically tolerable water-soluble acid respectively base |
| EP1598343A1 (de) | 2004-05-19 | 2005-11-23 | Boehringer Ingelheim International GmbH | 2-Arylaminopyrimidine als PLK Inhibitoren |
-
2004
- 2004-02-11 ES ES04710264T patent/ES2325440T3/es not_active Expired - Lifetime
- 2004-02-11 WO PCT/US2004/004197 patent/WO2004074244A2/en not_active Ceased
- 2004-02-11 EP EP04710264A patent/EP1597251B1/en not_active Expired - Lifetime
- 2004-02-11 US US10/545,352 patent/US7514446B2/en not_active Expired - Lifetime
- 2004-02-11 AT AT04710264T patent/ATE433447T1/de not_active IP Right Cessation
- 2004-02-11 JP JP2006503537A patent/JP4634367B2/ja not_active Expired - Lifetime
- 2004-02-11 DE DE602004021472T patent/DE602004021472D1/de not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| US7514446B2 (en) | 2009-04-07 |
| EP1597251B1 (en) | 2009-06-10 |
| US20070010668A1 (en) | 2007-01-11 |
| ES2325440T3 (es) | 2009-09-04 |
| WO2004074244A2 (en) | 2004-09-02 |
| DE602004021472D1 (en) | 2009-07-23 |
| ATE433447T1 (de) | 2009-06-15 |
| EP1597251A2 (en) | 2005-11-23 |
| JP2006518386A (ja) | 2006-08-10 |
| WO2004074244A3 (en) | 2004-11-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4634367B2 (ja) | ピリミジン化合物 | |
| JP5103403B2 (ja) | 2−ピリミジニルピラゾロピリジンErbBキナーゼ阻害剤 | |
| JP5132319B2 (ja) | 2−ピリミジニルピラゾロピリジンErbBキナーゼ阻害剤 | |
| JP4280442B2 (ja) | イミダゾ[1,2a]ピリジンおよびピラゾロ[2,3a]ピリジン誘導体 | |
| US7189712B2 (en) | 1,3-Oxazole compounds for the treatment of cancer | |
| EP1463730B1 (en) | Pyrazolopyridazine derivatives | |
| MX2013003918A (es) | Derivados de bencimidazol como inhibidores de cinasa pi3. | |
| WO2007030361A2 (en) | Benzimidazole thiophene compounds as plk inhibitors | |
| JP2003502280A (ja) | 置換アザ−オキシインドール誘導体 | |
| EP1608656B1 (en) | Imidazotriazine compounds for the treatment of cancer diseases | |
| JP2007519720A (ja) | チアゾール化合物 | |
| JP2010508301A (ja) | 5−置換及び6−置換ベンゾイミダゾールチオフェン化合物 | |
| US20070142437A1 (en) | Chemical compounds | |
| US7812022B2 (en) | 2-pyrimidinyl pyrazolopyridine ErbB kinase inhibitors | |
| JP2004508372A (ja) | オキシインドール誘導体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20061114 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100309 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100603 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100610 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100909 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20101019 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20101118 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4634367 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131126 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131126 Year of fee payment: 3 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131126 Year of fee payment: 3 |
|
| R371 | Transfer withdrawn |
Free format text: JAPANESE INTERMEDIATE CODE: R371 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R360 | Written notification for declining of transfer of rights |
Free format text: JAPANESE INTERMEDIATE CODE: R360 |
|
| R371 | Transfer withdrawn |
Free format text: JAPANESE INTERMEDIATE CODE: R371 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131126 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |