JP4355794B2 - 非水電解質電池用電極 - Google Patents
非水電解質電池用電極 Download PDFInfo
- Publication number
- JP4355794B2 JP4355794B2 JP50047599A JP50047599A JP4355794B2 JP 4355794 B2 JP4355794 B2 JP 4355794B2 JP 50047599 A JP50047599 A JP 50047599A JP 50047599 A JP50047599 A JP 50047599A JP 4355794 B2 JP4355794 B2 JP 4355794B2
- Authority
- JP
- Japan
- Prior art keywords
- electrode
- active material
- binder
- particle size
- weight
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/13—Electrodes for accumulators with non-aqueous electrolyte, e.g. for lithium-accumulators; Processes of manufacture thereof
- H01M4/131—Electrodes based on mixed oxides or hydroxides, or on mixtures of oxides or hydroxides, e.g. LiCoOx
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/52—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron
- H01M4/525—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron of mixed oxides or hydroxides containing iron, cobalt or nickel for inserting or intercalating light metals, e.g. LiNiO2, LiCoO2 or LiCoOxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
- H01M4/621—Binders
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
- H01M4/621—Binders
- H01M4/622—Binders being polymers
- H01M4/623—Binders being polymers fluorinated polymers
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
- H01M4/624—Electric conductive fillers
- H01M4/626—Metals
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/026—Electrodes composed of, or comprising, active material characterised by the polarity
- H01M2004/028—Positive electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/485—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of mixed oxides or hydroxides for inserting or intercalating light metals, e.g. LiTi2O4 or LiTi2OxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/50—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese
- H01M4/505—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese of mixed oxides or hydroxides containing manganese for inserting or intercalating light metals, e.g. LiMn2O4 or LiMn2OxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
- H01M4/624—Electric conductive fillers
- H01M4/625—Carbon or graphite
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Inorganic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Secondary Cells (AREA)
Description
本発明は、非水電解質電池用電極に関し、より詳しくは、リチウム複合酸化物が活物質として用いられ、柔軟性に優れる非水電解質電池用電極に関する。
背景技術
近年の電子分野の発展はめざましく、ビデオカメラ、液晶カメラ、携帯電話、ラップトップコンピューター、ワープロ等の各種機器が開発されている。それに対応して、これら電子機器の電源に使用される電池においては、小型化、軽量化、高エネルギー密度化への要求が高まっている。
従来、これらの電子機器には鉛電池やニッケルカドミウム電池が使用されていたが、これらの電池は小型化、軽量化、高エネルギー密度化の要求に対して十分に応えることができない。
そこで、非水溶媒にリチウム塩を溶解させた非水電解液を用いる、非水電解液電池が提案されている。この非水電解液電池としては、リチウムやリチウム合金もしくはリチウムイオンをドープ、脱ドープすることが可能な炭素材料を負極材料として用い、リチウムコバルト複合酸化物を正極材料として用いたものがすでに実用化されている。
この種の非水電解液電池は、作動電圧が3〜4Vと高いため、高エネルギー密度化が可能であり、自己放電も少なく、サイクル特性にも優れているという利点を有している。
また、この非水電解液電池では、さらなる小型化、軽量化、高エネルギー密度化を実現するために、活物質等の研究開発が盛んになされている。正極活物質としては、リチウムニッケル複合酸化物やリチウムニッケルコバルト複合酸化物のようなNiを含有するリチウム複合酸化物も提案されている。
例えば、非水電解質電池用電極に関する従来技術として、特公平8−4007号公報には、非水電解質電池用電極における結着剤についての発明が開示されている。すなわち、同号公報には、結着剤として、特定のモル分率の下記モノマーユニットA,B,Cより主として構成されるフッ素系高分子共重合体が記載されている。
A:−CH2−CF2−
B:−CF(CF3)−CF2−
C:−CF2−CF2−
同号公報には、結着剤を溶解する溶剤に関する記述が見られるものの、電極の柔軟性に関する開示は見られない。
特開平4−215252号公報には、正極活物質と導電剤とを含む正極と、負極と、非水電解質とをそれぞれ具備する非水電解質二次電池において、導電剤として鱗片状黒鉛を用いることが開示されている。そして、その効果として、電池内部抵抗の低減が挙げられている。しかし、電極の柔軟性に関する開示は見られない。
特開平6−111823号公報には、非水電解質電池用電極における結着剤についての発明が開示されている。すなわち、同号公報には、結着剤として、
−CF2−CF(CF3)−
で表されるヘキサフルオロプロピレン単位を主鎖に少なくとも1個含有する変性ポリビニリデンフルオライドが記載されている。そして、同号公報には、合剤スラリーの安定性を効果としているものの、電極の柔軟性に関する開示は見られない。
特開平9−274920号公報には、非水電解質電池における結着剤として、数平均分子量Mnが1.0×105以上のポリフッ化ビニリデンが記載されている。そして、同号公報には、効果として、活物質粉体と結着剤とを含有する塗膜と集電体との結着力を向上させることが挙げられているものの、塗膜の柔軟性に関する開示は見られない。
発明の開示
発明の目的
ところが、本発明者らがリチウム複合酸化物の特性を検討したところ、その形状によって柔軟性が変動してしまうということを見出した。この柔軟性が変動してしまうと、リチウム複合酸化物を電池に組み込んだ場合の形状自由度が減少するという問題が生じる。
そこで、本発明の目的は、上記従来技術の問題点を解決し、電池に高容量を付与できると共に電極の柔軟性を向上することができる非水電解質電池用電極を提供することにある。
発明の概要
本発明者らは鋭意研究した結果、粒度分布の平均粒径における半値幅が特定の範囲のリチウムニッケル複合酸化物を、適切な結合剤、あるいは結合剤及び導電剤と組み合わせて用いることによって、柔軟性に優れた電極が得られることを見出し、本発明を完成した。
すなわち、本発明は、活物質としてのリチウム複合酸化物と、導電剤と、結合剤とを少なくとも含有する非水電解質電池用電極であって、前記活物質は、粒度分布の平均粒径における半値幅が2.0〜50μmのLixNiyMzO2(ここで、xは0.8<x<1.5、y+zは0.8<y+z<1.2、zは0≦z<0.35である。Mは、Co、Mg、Ca、Sr、Al、Mn及びFeから選ばれる少なくとも1種の元素を表す。)からなり、かつ結合剤がフッ素ゴムである、非水電解質電池用電極である。
また、本発明は、活物質としてのリチウム複合酸化物と、導電剤と、結合剤とを少なくとも含有する非水電解質電池用電極であって、前記活物質は、粒度分布の平均粒径における半値幅が2.0〜50μmのLixNiyMzO2(ここで、xは0.8<x<1.5、y+zは0.8<y+z<1.2、zは0≦z<0.35である。Mは、Co、Mg、Ca、Sr、Al、Mn及びFeから選ばれる少なくとも1種の元素を表す。)からなり、前記導電剤がグラファイトであり、かつ前記結合剤がポリフッ化ビニリデンである、非水電解質電池用電極である。
本発明の電極によれば、粒度分布の平均粒径における半値幅が特定の範囲のリチウムニッケル複合酸化物を、適切な結合剤、あるいは結合剤及び導電剤と組み合わせて用いるので、柔軟性を保ちつつ活物質の充填が密になされ、電池特性及び柔軟性に優れる。
発明の詳細な説明
本発明に使用されるリチウム複合酸化物は、LixNiyMzO2(ここで、xは0.8<x<1.5、y+zは0.8<y+z<1.2、zは0≦z<0.35である。Mは、Co、Mg、Ca、Sr、Al、Mn及びFeから選ばれる少なくとも1種の元素を表す。)で表されるものである。
このようなリチウム複合酸化物の製造方法としては、例えば、LiMetal3+O2(ここで、MetalはNiを主体として、Co、Mg、Ca、Sr、Al、Mn及びFeから選ばれる少なくとも1種の元素を含む)焼成時に揮散する陰イオンをそれぞれ含むアルカリ性水溶性リチウム化合物と塩基性金属塩とを水媒体中で反応させてスラリーを得て、得られたスラリーを乾燥した後、焼成する方法を例示することができる。
塩基性金属塩は、Metal2+(OH)2-nk(An-)k・mH2Oで表されるものである。ここで、Metal2+には、Niを主体として、場合によってはCo、Mg、Ca、Sr、Al、Mn及びFeから選ばれる少なくとも1種の元素を含む。An-は、硝酸イオン、塩素イオン、臭素イオン、酢酸イオン、炭酸イオン等のn価(n=1〜3)のアニオンを表わす。また、kは、0.03≦k≦0.3、mは、0≦m<2である。
この式で示される塩基性金属塩は、Metal2+の水溶液に、Metal2+に対して、約0.7〜0.95当量、好ましくは約0.8〜0.95当量のアルカリを約80℃以下の反応条件下で加えて反応させた後、40℃〜70℃で0.1〜10時間熟成し、水洗により副生物を取り除くことにより製造することができる。ここで用いるアルカリとしては、水酸化ナトリウム等の水酸化アルカリ金属、水酸化カルシウム等の水酸化アルカリ土類金属、アミン類等が挙げられる。
この式で示される化合物より選択される塩基性金属塩と、水酸化リチウム、炭酸リチウム又はこれらの水和物などの中から選択される1種または複数のリチウム化合物とを水中で、反応液の濃度としては5〜25重量%の範囲で、また反応温度は室温〜100℃の範囲で反応を行いスラリーを得る。そして、組成物の形状の均一性を向上させるために噴霧乾燥を行う。
この乾燥物を空気や酸素あるいはオゾン等を含む酸化力を有したガス雰囲気下で、約700〜1000℃の温度領域で、約0.1〜20時間加熱処理して焼成することにより、リチウム複合酸化物を得ることができる。
本発明に使用されるリチウム複合酸化物の別の製造方法として、水溶性金属化合物から得られる塩基性炭酸金属と水溶性リチウム化合物とを使用する方法を例示することができる。
ここで用いられる水溶性金属化合物は、硝酸塩、硫酸塩、金属塩化物等であり、この水溶性金属化合物は、ニッケル化合物を主体として、Co、Mg、Ca、Sr、Al、Mn及びFeから選ばれる少なくとも1種の元素が配合できるように、さらに所定量の別の水溶性金属化合物を混合したものでよい。
塩基性炭酸金属は、上記水溶性金属化合物の混合物と、炭酸アルカリ、重炭酸アルカリ、炭酸アンモニウム及び重炭酸アンモニウムからなる群から選ばれる化合物とを水中で反応させて得られる沈殿物や、さらにこの反応系に水酸化ナトリウムを存在させて反応させて得られる沈澱物を、濾過、乾燥することによって得られる。この場合に、良好な沈殿を生成させるには、炭酸根が若干過剰となるように使用するのが良く、沈殿の比表面積を制御するために攪拌条件を制御することも重要である。
このようにして得られた塩基性炭酸金属に、炭酸リチウム、水酸化リチウム等の水溶性リチウム化合物の粉末を、前記金属とLiを所望の比率で混合する。この混合物を、粉末のまま先ず不活性ガス又は酸素含有ガスの存在下で、300〜500℃に加熱する。この加熱により、塩基性炭酸金属の分解のみが進行し、結晶構造中の炭酸ガスが離脱する。この加熱を炭酸ガスの発生が実質的に終了するまで続け、塩基性炭酸金属のすべてを多数の微細な孔を有する酸化金属に変換する。
炭酸ガスの発生が実質的に終了した後、さらに昇温すると、溶融した水溶性リチウム化合物が酸化金属の微細孔中に侵入し、両者が極めて密接な接触状態になる。ここで酸素ガス又は酸素富化空気の存在下で700〜900℃の温度で焼成すると、Niは2価から3価になり、Li複合酸化物が生成する。
ここで用いる塩基性炭酸金属は、比表面積が大きな(例えば、100m2/g以上)ものほど、ガス放出と予備焼成後の微細孔生成が効率化されるために好ましい。
本発明に使用されるリチウム複合酸化物は、上記組成LixNiyMzO2(0.8<x<1.5、0.8<y+z<1.2、0≦z<0.35;Mは、Co、Mg、Ca、Sr、Al、Mn及びFeから選ばれる少なくとも1種の元素を表す。)で表され、かつ粒度分布の平均粒径における半値幅が2.0〜50μmのものである。この粒度分布は、レーザー回折・散乱法により測定されたものである。
本発明において、このリチウム複合酸化物の平均粒径は1.0〜30μmが好ましく、2.0〜20μmがより好ましい。粒度分布の平均粒径における半値幅は、2.0〜20μmが好ましい。
このような粒度分布のリチウム複合酸化物は、上記方法によって得られたリチウム複合酸化物を分級処理して得ることができる。
この半値幅が2.0μm未満であると、粒径が均一であるために電極内の活物質間の空隙が多くなって充填が不十分となる。従って、電極容量を上げるために後述のローラープレス機の圧縮力を上げるなどの操作が必要となる。更にこの半値幅のものを作製するのはかなり困難であり、製造上非常に多くの工程が必要となるため実用性が非常に乏しい。
逆にこの半値幅が50μmを越えると、粗大粒子と微小粒子が混在するため活物質の充填が良くなり過ぎる。この場合電極容量的には有利であるものの、電極の物理的柔軟性がなくなって剛直になり、割れや欠けといった弊害が発生してしまう。
一方、本発明の粒度分布を有するリチウム複合酸化物を正極活物質として用いる場合には、電極の柔軟性を保ちつつ活物質の充填を密にすることが可能となり、飛躍的にエネルギー密度を高めることができる。従って、高容量で安価であるというニッケル含有リチウム複合酸化物粒子の長所を持つ非水電解質電池用電極を得ることができる。
本発明に使用される結合剤は、フッ素ゴムもしくはポリフッ化ビニリデン(PVDF)である。フッ素ゴムとしては、フッ化ビニリデン−ヘキサフルオロプロピレン(VDF−HFP)系共重合体、フッ化ビニリデン−ヘキサフルオロプロピレン−テトラフルオロエチレン(VDF−HFP−TFE)系共重合体、フッ化ビニリデン−ペンタフルオロプロピレン(VDF−PFP)系共重合体、フッ化ビニリデン−ペンタフルオロプロピレン−テトラフルオロエチレン(VDF−PFP−TFE)系共重合体、フッ化ビニリデン−パーフルオロメチルビニルエーテル−テトラフルオロエチレン(VDF−PFMVE−TFE)系共重合体、エチレン−テトラフルオロエチレン系共重合体、プロピレン−テトラフルオロエチレン系共重合体等を挙げることができる。また、主鎖の水素をアルキル基で置換した含フッ素ポリマーも用いることができる。
このような結合剤の添加量は、活物質や導電剤の比表面積、粒度分布、目的とする電極の強度等により異なるが、乾燥塗膜中の1〜20重量%が好ましく、特に2〜15重量%が好ましい。
本発明に使用される導電剤について説明する。
本発明において結合剤として、ポリフッ化ビニリデン(PVDF)以外のフッ素ゴム系樹脂を使用する場合には、導電剤は、特に限定されるものではなく、化学変化を起こさない電子伝導材料であれば何でもよい。導電剤としては、通常、天然黒鉛(鱗状黒鉛、鱗片状黒鉛等)、人造黒鉛などのグラファイト類、アセチレンブラック、ケッチェンブラック、チャンネルブラック、ファーネスブラック、サーマルブラック等のカーボンブラック類、炭素繊維、気相成長炭素繊維、金属繊維等の導電性繊維類、銅、ニッケル、アルミニウム、銀等の金属粉末などを挙げることができる。これらの中でも、アセチレンブラック、鱗片状グラファイトが好ましい。上記導電剤は、単独あるいは複数種組み合わせて使用しても差し支えない。
具体的には、中越黒鉛工業所社製のLFシリーズ、昭和電工社製のUFGシリーズ、LONZA社製のKSシリーズ、関西熱化学社製のMICROCARBO−Gシリーズ、エコス技研社製のエコスカーボン等が挙げられる。
本発明において結合剤として、ポリフッ化ビニリデン(PVDF)を使用する場合は、導電剤は上記のうちのグラファイト類に限定される。グラファイト以外のものを使用した場合には、電極の柔軟性が低下し、電池化する際、電極割れが発生する。グラファイトの中でも、鱗片状グラファイトが好ましい。
導電剤の添加量は、乾燥塗膜中の0.1〜15重量%が好ましく、特に1〜10重量%が好ましい。0.1重量%未満では導電性が不十分となり、容量低下を引き起こしやすい。一方、15重量%を越えると実質的に作用する活物質量が減り、やはり容量が低下しやすい。
また、電極活物質合剤塗料用の溶剤としては、特に限定されることなく、一般の有機溶剤を使用することができる。有機溶剤として、具体的には、ヘキサン等の飽和炭化水素類、トルエン、キシレン等の芳香族炭化水素類、メタノール、エタノール、プロパノール、ブタノール等のアルコール類、アセトン、メチルエチルケトン、メチルイソブチルケトン、ジイソブチルケトン等のケトン類、酢酸エチル、酢酸ブチル等のエステル類、テトラヒドロフラン、ジオキサン、ジエチルエーテル等のエーテル類、N,N−ジメチルホルムアミド、N−メチルピロリドン、N,N−ジメチルアセトアミド等のアミド類、エチレンクロライド、クロルベンゼン等のハロゲン化炭化水素等を挙げることができる。これらのなかでも、アミド系の溶剤が含フッ素系ポリマーを溶解可能なため好ましい。これらの溶剤は、単独でも2種以上の混合したものでも使用することができる。
電極活物質合剤塗料の調製は、常法により、活物質、導電剤、結合剤及び有機溶剤を混合・スラリー化して行うことができる。例えば、ロールミル法により、乾燥空気下や不活性ガス下で混合する。
調製された合剤塗料を集電体上に塗布し乾燥する。集電体は特に限定されるものではなく、電池化した際に、化学変化しない電子伝導体であれば何でもよい。例えば、アルミニウム、アルミニウム合金、ニッケル、ステンレス、チタン等が用いられる。これらのほかに、アルミニウムやステンレスの表面がカーボン、ニッケル、チタンで処理されたものも用いられる。特に、アルミニウムあるいはアルミニウム合金が好ましい。集電体の形状としては、箔の他、フィルム、ネット、多孔質体、発泡体等が用いられる。厚みは1〜100μmのものが用いられ、特に1〜50μmが好ましい。
集電体上への電極活物質合剤塗料の塗布は、リバースロール法、ダイレクトロール法、ブレード法、ナイフ法、エクストルージョンノズル法、カーテン法、グラビアロール法、バーコート法、ディップ法、キスコート法、スクイズ法などの一般的によく知られた塗布法によって行うことができる。中でもエクストルージョンノズル法が好ましく、5〜100m/分の速度で塗布されるように、合剤の溶剤組成、乾燥条件を選定することにより、良好な塗布層の表面状態を得ることができる。
乾燥温度は30〜150℃が好ましく、50〜140℃が更に好ましい。30℃未満では溶剤の乾燥が不十分となり、150℃を越えると溶剤の蒸発速度が急激すぎるために電極の表層に結合剤が偏在することとなり、電極特性が劣化することがある。
また塗布層の厚み、長さや巾は、最終的な電池の大きさにより決定される。塗布層の厚みは塗布後に、一般に採用されているカレンダー加工によって調整することが好ましい。その加工圧は、0.2〜10t/cm、加工温度は、10〜150℃が好ましい。
【図面の簡単な説明】
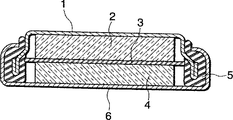
第1図は、実施例で用いられた電池特性測定用のコイン型電池の断面図である。
発明を実施するための形態
以下に実施例を挙げて本発明をさらに具体的に説明するが、本発明はこれら実施例に限定されるものではない。
[実施例1]
正極活物質の作製を以下のように行った。
硝酸ニッケル及び硝酸コバルトを、Ni/Co(モル比)=0.8/0.2となるように水溶液中で混合し、沈殿を形成させ、その後スプレードライヤーで乾燥し、概ね球状の粒子を得た。この粒子と水酸化リチウムをLi/Ni/Co(モル比)=1/0.8/0.2で混合し焼成して、LiNi0.8Co0.2O2を得た。
この活物質の形状を電子顕微鏡写真で観察したところ、概ね球状であった。また、この活物質の粒度分布をマイクロトラック粒度分析計(日機装社製)を使用して測定したところ、平均粒径は10μmでありその平均粒径における半値幅は60μmであった。この活物質の分級処理を行い、平均粒径における半値幅=1.0μm(比較例1−1)、2.0μm(実施例1−1)、5.0μm(実施例1−2)、10μm(実施例1−3)、20μm(実施例1−4)、50μm(実施例1−5)の各サンプルを作成した。また、分級処理を施さない半値幅=60μm(比較例1−2)もサンプルとして用いた。
各サンプルを活物質として用いて、以下の配合組成の活物質合剤塗料をそれぞれ調製した。
(配合組成)
正極活物質:LiNi0.8Co0.2O2 92重量部
導電剤:アセチレンブラック 4重量部
(電気化学工業社製)
結合剤:フッ素ゴム(VDF−HFP共重合体) 4重量部
(昭和電工・デュポン社製VITON A−HV)
混合溶剤:メチルイソブチルケトン(MIBK)
/N−メチル−2−ピロリドン=1/1(重量比) 67重量部
VITON A−HV4重量部を混合溶剤56重量部に溶解し、結合剤溶液60重量部を作製した。活物質92重量部と導電剤4重量部をハイパーミキサーで乾式混合し、この混合物を加圧ニーダーに投入した。この混合物に上記結合剤溶液13重量部を加え、加圧ニーダーのジャケットを水冷しながら、30分間混練した。この混練物を取り出し、結合剤溶液47重量部と混合溶剤11重量部を加えて、ハイパーミキサーにて溶解し、活物質合剤塗料を得た。
調製された合剤塗料を、エクストルージョンノズルにて20μm厚のアルミニウム箔からなる集電体の片面に塗布・乾燥した後、集電体他面に同様にこの合剤を塗布・乾燥した。これをローラープレス機にて同一圧力で圧縮成型し、所定の大きさに切断し、その後、片面の合剤塗膜を剥がして、合剤層厚さ65μmの各電極を得た。
(電極密度)
実施例1−1〜1−5及び比較例1−1〜1−2で得られた各電極についての電極密度を測定した。
(電池特性)
実施例及び比較例で得られた各電極の電池特性を次のように測定した。
得られた各電極について、正極活物質層を残留水分を除去するため乾燥し、直径15.5mmの円形の正極を作製した。別途、負極として、厚さ1.85mmの金属リチウムを直径15.5mmに打ち抜いた。そして、エチレンカーボネートとジメチルカーボネートの1:1(容量比)混合液にLiPF6を1モル/リットルなる濃度で溶解した非水電解液を用意した。
この非水電解液、正極及び負極と、さらにポリプロピレン製の薄膜セパレーター、負極カップ、正極缶、ガスケットとを用いて、第1図に示すような直径20mm×厚さ2.5mmのコイン型電池を作製した。第1図において、このコイン型電池は、正極缶(6)内に収容された正極(4)と負極カップ(1)内に収容された負極(2)とがセパレーター(3)を介して積層され、正極缶(6)と負極カップ(1)とがガスケット(5)を介してかしめられ、密閉されてなるものである。なお、集電体の図示は省略してある。
このようにして作製された電池について、充電電圧4.2V、充電電流1mA、充電時間20時間なる条件で充電を行い、放電電流1mA、終止電圧3.0Vなる条件で放電を行い、充放電容量を求めた。
(曲げ特性)
実施例および比較例で作成した試料電極を、直径1mmの円筒の周面に沿わせて180°曲げた時に割れ等が発生するかどうかを下記基準にて観察した。
○:割れの発生のないもの。
△:軽度の割れはあるものの、実用レベルと判断されるもの。
×:割れが発生し、使用不可能なもの。
以上の結果を表1に示す。
表1より、実施例の電極は、曲げ特性に優れ、電極密度も高く、初期放電容量にも優れる。比較例1−1の電極は、粒度分布の半値幅が2.0μm未満であり、電極密度が低く放電容量が小さい。比較例1−2の電極は、粒度分布の半値幅が50μmを超えており、曲げ特性に劣る。
[実施例2]
正極活物質としてLiNi0.8Co0.2O2(平均粒径=10μm、半値幅=5.0μmのもの)、結合剤として昭和電工・デュポン社製VITON A−HVの代わりに、VITON GF(フッ素ゴムVDF−HFP−TFE共重合体)を使用した以外は、実施例1−2と同様にして電極を作製し、評価した。
その結果を表2に示す。
表2より、実施例2の電極は、曲げ特性に優れ、電極密度も高く、初期放電容量にも優れる。
[実施例3(PVDFサンプル)]
正極活物質としてLiNi0.8Co0.2O2(平均粒径=10μm、半値幅=5.0μmのもの)、結合剤としてポリフッ化ビニリデン(PVDF)を用いて、以下の配合組成の活物質合剤塗料を調製した。
(配合組成)
正極活物質:LiNi0.8Co0.2O2 90重量部
(平均粒径=10μm、半値幅=5.0μm)
導電剤:鱗片状グラファイト 6重量部
(LONZA KS25、平均粒径=11μm)
結合剤:ポリフッ化ビニリデン(PVDF) 4重量部
(エルフアトケムジャパン KYNAR741)
溶剤:N−メチル−2−ピロリドン(NMP) 45重量部
PVDF4重量部をNMP36重量部に溶解し、結合剤溶液40重量部を作製した。活物質90重量部と導電剤6重量部をハイパーミキサーで乾式混合し、この混合物を加圧ニーダーに投入した。この混合物に上記結合剤溶液13重量部を加え、加圧ニーダーのジャケットを水冷しながら、30分間混練した。この混練物を取り出し、結合剤溶液27重量部とNMP9重量部を加えて、ハイパーミキサーにて溶解し、活物質合剤塗料を得た。
調製された合剤塗料を、エクストルージョンノズルにて20μm厚のアルミニウム箔からなる集電体の片面に塗布・乾燥した後、集電体他面に同様にこの合剤を塗布・乾燥した。これをローラープレス機にて圧縮成型し、所定の大きさに切断し、その後、片面の合剤塗膜を剥がして、合剤層厚さ65μmの電極を得た。この電極について、実施例1と同様に評価した。
[比較例2]
導電剤として鱗片状グラファイト6重量部の代わりに、アセチレンブラック6重量部を用いた以外は、実施例3と同様にして活物質合剤塗料を調製した。この合剤塗料を用いて、電極密度が実施例3と同一になるようにローラープレス圧力を調節して電極を作製し、評価した。
以上の結果を表3に示す。
表3より、実施例3の電極は、曲げ特性に優れ、電極密度も高く、初期放電容量にも優れる。比較例2の電極は、曲げ特性に劣る。
本発明は、その精神または主要な特徴から逸脱することなく、他のいろいろな形態で実施することができる。そのため、前述の実施例はあらゆる点で単なる例示にすぎず、限定的に解釈してはならない。さらに、請求の範囲の均等範囲に属する変更は、すべて本発明の範囲内のものである。
産業上の利用可能性
以上のように、本発明の電極によれば、粒度分布の平均粒径における半値幅が特定の範囲のリチウムニッケル複合酸化物を、適切な結合剤、あるいは結合剤及び導電剤と組み合わせて用いるので、柔軟性を保ちつつ活物質の充填が密になされ、電池特性及び柔軟性に優れる。
従って、本発明によれば、高容量で安価であるというニッケル含有リチウム複合酸化物粒子の長所を持つ非水電解質電池用電極が提供される。
Claims (3)
- 活物質としてのリチウム複合酸化物と、導電剤と、結合剤とを少なくとも含有する非水電解質電池用電極であって、
前記活物質は、粒度分布の平均粒径における半値幅が2.0〜50μmのLixNiyMzO2(ここで、xは0.8<x<1.5、y+z
は0.8<y+z<1.2、zは0≦z<0.35である。Mは、Co、
Mg、Ca、Sr、Al、Mn及びFeから選ばれる少なくとも1種の元素を表す。)からなり、かつ結合剤がフッ素ゴムである、非水電解質電池用電極。 - 活物質としてのリチウム複合酸化物と、導電剤と、結合剤とを少なくとも含有する非水電解質電池用電極であって、
前記活物質は、粒度分布の平均粒径における半値幅が2.0〜50μmのLixNiyMzO2(ここで、xは0.8<x<1.5、y+z
は0.8<y+z<1.2、zは0≦z<0.35である。Mは、Co、
Mg、Ca、Sr、Al、Mn及びFeから選ばれる少なくとも1種の元素を表す。)からなり、前記導電剤がグラファイトであり、かつ前記結合剤がポリフッ化ビニリデンである、非水電解質電池用電極。 - 前記活物質Li x Ni y M z O 2 におけるMがCoである、請求項1又は2に記載の非水電解質電池用電極。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP13666697 | 1997-05-27 | ||
| JP13665997 | 1997-05-27 | ||
| JP13666497 | 1997-05-27 | ||
| JP13666797 | 1997-05-27 | ||
| PCT/JP1998/002316 WO1998054776A1 (fr) | 1997-05-27 | 1998-05-27 | Electrode pour cellules electrolytiques non-aqueuses |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP4355794B2 true JP4355794B2 (ja) | 2009-11-04 |
Family
ID=27472013
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP10161504A Withdrawn JPH1145717A (ja) | 1997-05-27 | 1998-05-27 | 非水電解質電池用電極 |
| JP50047599A Expired - Lifetime JP4355794B2 (ja) | 1997-05-27 | 1998-05-27 | 非水電解質電池用電極 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP10161504A Withdrawn JPH1145717A (ja) | 1997-05-27 | 1998-05-27 | 非水電解質電池用電極 |
Country Status (8)
| Country | Link |
|---|---|
| EP (1) | EP0986121B1 (ja) |
| JP (2) | JPH1145717A (ja) |
| KR (1) | KR100512768B1 (ja) |
| CN (1) | CN1118107C (ja) |
| AU (1) | AU7452198A (ja) |
| DE (1) | DE69841309D1 (ja) |
| RU (1) | RU2183369C2 (ja) |
| WO (1) | WO1998054776A1 (ja) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4329434B2 (ja) * | 2003-07-30 | 2009-09-09 | 三菱化学株式会社 | リチウム二次電池用正極及びそれを用いたリチウム二次電池 |
| JP4276063B2 (ja) * | 2003-12-26 | 2009-06-10 | Tdk株式会社 | 電気化学キャパシタ用電極の製造方法及び電気化学キャパシタの製造方法 |
| JP2005191423A (ja) * | 2003-12-26 | 2005-07-14 | Tdk Corp | キャパシタ用電極 |
| CN100421286C (zh) * | 2004-11-30 | 2008-09-24 | 松下电器产业株式会社 | 非水电解质二次电池 |
| RU2465691C1 (ru) * | 2008-10-27 | 2012-10-27 | Ниссан Мотор Ко., Лтд. | Композитный электрод для устройства аккумулирования электроэнергии, способ его получения и устройство аккумулирования электроэнергии |
| EP2398095A4 (en) * | 2009-02-12 | 2013-08-14 | Daikin Ind Ltd | SUSPENSION FOR POSITIVE ELECTRODE MIXTURE OF LITHIUM SECONDARY BATTERY, POSITIVE ELECTRODE, AND LITHIUM SECONDARY BATTERY USING SUSPENSION |
| US8592085B2 (en) * | 2009-10-22 | 2013-11-26 | Toda Kogyo Corporation | Nickel-cobalt-maganese-based compound particles and process for producing the nickel-cobalt-manganese-based compound particles, lithium composite oxide particles and process for producing the lithium composite oxide particles, and non-aqueous electrolyte secondary battery |
| JP5741908B2 (ja) * | 2011-03-09 | 2015-07-01 | 日産自動車株式会社 | リチウムイオン二次電池用正極活物質 |
| JP6092567B2 (ja) * | 2012-05-31 | 2017-03-08 | トヨタ自動車株式会社 | 硫化物系固体電池用正極用スラリー、硫化物系固体電池用正極及びその製造方法、並びに、硫化物系固体電池及びその製造方法 |
| RU2536649C1 (ru) * | 2013-10-28 | 2014-12-27 | Общество с ограниченной ответственностью "АкКо Лаб" | Композиционный наноматериал для химических источников тока и способ его получения |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3071897B2 (ja) * | 1991-09-30 | 2000-07-31 | 旭化成工業株式会社 | 電 池 |
| JPH06243897A (ja) * | 1992-12-24 | 1994-09-02 | Fuji Photo Film Co Ltd | 非水二次電池 |
| JPH07142056A (ja) * | 1993-11-18 | 1995-06-02 | Sanyo Electric Co Ltd | 非水系電池 |
| JPH07263028A (ja) * | 1994-03-25 | 1995-10-13 | Fuji Photo Film Co Ltd | 非水二次電池 |
| JP3687106B2 (ja) * | 1994-04-06 | 2005-08-24 | 住友化学株式会社 | リチウム遷移金属複合酸化物粉末とその製造方法およびリチウム二次電池正極とリチウム二次電池 |
| JPH08213052A (ja) * | 1994-08-04 | 1996-08-20 | Seiko Instr Inc | 非水電解質二次電池 |
| JP3427570B2 (ja) * | 1994-10-26 | 2003-07-22 | ソニー株式会社 | 非水電解質二次電池 |
| JP3539448B2 (ja) * | 1995-04-19 | 2004-07-07 | 日本ゼオン株式会社 | 非水二次電池 |
-
1998
- 1998-05-27 KR KR10-1999-7010902A patent/KR100512768B1/ko not_active IP Right Cessation
- 1998-05-27 JP JP10161504A patent/JPH1145717A/ja not_active Withdrawn
- 1998-05-27 CN CN98805047A patent/CN1118107C/zh not_active Expired - Fee Related
- 1998-05-27 EP EP98921823A patent/EP0986121B1/en not_active Expired - Lifetime
- 1998-05-27 RU RU99128112/09A patent/RU2183369C2/ru active
- 1998-05-27 AU AU74521/98A patent/AU7452198A/en not_active Abandoned
- 1998-05-27 JP JP50047599A patent/JP4355794B2/ja not_active Expired - Lifetime
- 1998-05-27 DE DE69841309T patent/DE69841309D1/de not_active Expired - Lifetime
- 1998-05-27 WO PCT/JP1998/002316 patent/WO1998054776A1/ja active IP Right Grant
Also Published As
| Publication number | Publication date |
|---|---|
| KR100512768B1 (ko) | 2005-09-07 |
| EP0986121A1 (en) | 2000-03-15 |
| CN1118107C (zh) | 2003-08-13 |
| EP0986121B1 (en) | 2009-11-25 |
| EP0986121A4 (en) | 2001-04-11 |
| CN1256015A (zh) | 2000-06-07 |
| AU7452198A (en) | 1998-12-30 |
| DE69841309D1 (de) | 2010-01-07 |
| RU2183369C2 (ru) | 2002-06-10 |
| JPH1145717A (ja) | 1999-02-16 |
| WO1998054776A1 (fr) | 1998-12-03 |
| KR20010012934A (ko) | 2001-02-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5175826B2 (ja) | 活物質粒子およびその利用 | |
| US6497979B1 (en) | Method of producing electrode for non-aqueous electrolytic cells including a narrow-gap dispersing process | |
| WO2012128182A1 (ja) | リチウムイオン二次電池負極用スラリー組成物、リチウムイオン二次電池負極、及びリチウムイオン二次電池 | |
| JP2006244813A (ja) | 二次電池用負極及びそれを用いた二次電池 | |
| JP4355794B2 (ja) | 非水電解質電池用電極 | |
| JP2023015188A (ja) | 非水電解質二次電池用正極活物質の製造方法 | |
| JP4529288B2 (ja) | 非水電解質二次電池用電極 | |
| US8877380B2 (en) | Positive active material, method of preparing the same, and lithium battery including the positive active material | |
| JP5546009B2 (ja) | リチウム電池用正極活物質、その製造方法及びそれを利用したリチウム電池 | |
| JPH1145706A (ja) | 非水電解質電池用電極の製造方法 | |
| JP4203866B2 (ja) | 非水電解質電池用電極の製造方法 | |
| JP4410315B2 (ja) | 非水電解質電池用電極 | |
| JP2005025991A (ja) | 非水電解質二次電池 | |
| JP4029195B2 (ja) | 非水電解質電池用正極電極の製造方法 | |
| JPH1145716A (ja) | 非水電解質電池用電極の製造方法 | |
| JP2002260636A (ja) | 非水電解質二次電池用電極および非水電解質二次電池 | |
| JPH1145707A (ja) | 非水電解質電池用電極の製造方法 | |
| JP2003187787A (ja) | リチウム電池用正極の製造方法 | |
| JP3839590B2 (ja) | 非水電解質二次電池用電極 | |
| CA2462231A1 (en) | Lithium cobalt compound oxide and manufacturing methods thereof, and non-aqueous electrolyte secondary cell | |
| JP2022551705A (ja) | リチウムフリー電池用負極集電体、それを含む電極組立体およびリチウムフリー電池 | |
| JP2015022964A (ja) | リチウムイオン二次電池用負極材料,その製造方法及びリチウムイオン二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A72 | Notification of change in name of applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A721 Effective date: 20040224 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050328 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080909 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20081104 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090115 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20090609 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20090706 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20090706 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120814 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130814 Year of fee payment: 4 |
|
| EXPY | Cancellation because of completion of term |