JP4226552B2 - 3−オキソ−4−アザ−5α−アンドロスタン化合物の選択的製造方法 - Google Patents
3−オキソ−4−アザ−5α−アンドロスタン化合物の選択的製造方法 Download PDFInfo
- Publication number
- JP4226552B2 JP4226552B2 JP2004528926A JP2004528926A JP4226552B2 JP 4226552 B2 JP4226552 B2 JP 4226552B2 JP 2004528926 A JP2004528926 A JP 2004528926A JP 2004528926 A JP2004528926 A JP 2004528926A JP 4226552 B2 JP4226552 B2 JP 4226552B2
- Authority
- JP
- Japan
- Prior art keywords
- compound
- formula
- oxo
- aza
- iii
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000004519 manufacturing process Methods 0.000 title claims description 15
- -1 3-oxo-4-aza-5α-androstane compound Chemical class 0.000 title description 5
- 150000001875 compounds Chemical class 0.000 claims description 37
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 claims description 28
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 claims description 21
- 238000000034 method Methods 0.000 claims description 17
- 239000000203 mixture Substances 0.000 claims description 16
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 claims description 14
- 235000019253 formic acid Nutrition 0.000 claims description 14
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 claims description 8
- 239000011701 zinc Substances 0.000 claims description 8
- 229910052725 zinc Inorganic materials 0.000 claims description 8
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 claims description 6
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 claims description 4
- WERYXYBDKMZEQL-UHFFFAOYSA-N butane-1,4-diol Chemical compound OCCCCO WERYXYBDKMZEQL-UHFFFAOYSA-N 0.000 claims description 4
- 238000010438 heat treatment Methods 0.000 claims description 4
- DNIAPMSPPWPWGF-VKHMYHEASA-N (+)-propylene glycol Chemical compound C[C@H](O)CO DNIAPMSPPWPWGF-VKHMYHEASA-N 0.000 claims description 2
- YPFDHNVEDLHUCE-UHFFFAOYSA-N 1,3-propanediol Substances OCCCO YPFDHNVEDLHUCE-UHFFFAOYSA-N 0.000 claims description 2
- BMRWNKZVCUKKSR-UHFFFAOYSA-N butane-1,2-diol Chemical compound CCC(O)CO BMRWNKZVCUKKSR-UHFFFAOYSA-N 0.000 claims description 2
- 229920000166 polytrimethylene carbonate Polymers 0.000 claims description 2
- OWBTYPJTUOEWEK-UHFFFAOYSA-N butane-2,3-diol Chemical compound CC(O)C(C)O OWBTYPJTUOEWEK-UHFFFAOYSA-N 0.000 claims 1
- ATHHXGZTWNVVOU-UHFFFAOYSA-N N-methylformamide Chemical compound CNC=O ATHHXGZTWNVVOU-UHFFFAOYSA-N 0.000 description 14
- 239000007787 solid Substances 0.000 description 10
- 238000004128 high performance liquid chromatography Methods 0.000 description 7
- MJXIPHMGYJXKLJ-MLGOENBGSA-N (1s,3as,3bs,5ar,9ar,9bs,11as)-9a,11a-dimethyl-7-oxo-1,2,3,3a,3b,4,5,5a,6,8,9,9b,10,11-tetradecahydroindeno[5,4-f]quinoline-1-carboxylic acid Chemical group N1C(=O)CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)C(O)=O)[C@@H]4[C@@H]3CC[C@H]21 MJXIPHMGYJXKLJ-MLGOENBGSA-N 0.000 description 6
- 230000014759 maintenance of location Effects 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 5
- DBEPLOCGEIEOCV-WSBQPABSSA-N finasteride Chemical compound N([C@@H]1CC2)C(=O)C=C[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H](C(=O)NC(C)(C)C)[C@@]2(C)CC1 DBEPLOCGEIEOCV-WSBQPABSSA-N 0.000 description 5
- 229960004039 finasteride Drugs 0.000 description 5
- 239000001257 hydrogen Substances 0.000 description 5
- 229910052739 hydrogen Inorganic materials 0.000 description 5
- 239000002244 precipitate Substances 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- WNUUCDPRBZUXGL-UUBMZHIOSA-N (1s,3as,3bs,9ar,9bs,11as)-9a,11a-dimethyl-7-oxo-1,2,3,3a,3b,4,6,8,9,9b,10,11-dodecahydroindeno[5,4-f]quinoline-1-carboxylic acid Chemical compound N1C(=O)CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)C(O)=O)[C@@H]4[C@@H]3CC=C21 WNUUCDPRBZUXGL-UUBMZHIOSA-N 0.000 description 4
- NVKAWKQGWWIWPM-ABEVXSGRSA-N 17-β-hydroxy-5-α-Androstan-3-one Chemical compound C1C(=O)CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CC[C@H]21 NVKAWKQGWWIWPM-ABEVXSGRSA-N 0.000 description 4
- 238000005160 1H NMR spectroscopy Methods 0.000 description 4
- 201000004384 Alopecia Diseases 0.000 description 4
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 4
- MUMGGOZAMZWBJJ-DYKIIFRCSA-N Testostosterone Chemical compound O=C1CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 MUMGGOZAMZWBJJ-DYKIIFRCSA-N 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 230000000052 comparative effect Effects 0.000 description 4
- 238000006722 reduction reaction Methods 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 206010004446 Benign prostatic hyperplasia Diseases 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- 208000004403 Prostatic Hyperplasia Diseases 0.000 description 3
- 238000001914 filtration Methods 0.000 description 3
- 201000004240 prostatic hypertrophy Diseases 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 238000011282 treatment Methods 0.000 description 3
- 150000003751 zinc Chemical class 0.000 description 3
- YQACAXHKQZCEOI-UDCWSGSHSA-N (8s,9s,10r,13s,14s,17s)-10,13-dimethyl-3-oxo-1,2,6,7,8,9,11,12,14,15,16,17-dodecahydrocyclopenta[a]phenanthrene-17-carboxylic acid Chemical compound O=C1CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)C(O)=O)[C@@H]4[C@@H]3CCC2=C1 YQACAXHKQZCEOI-UDCWSGSHSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 206010068168 androgenetic alopecia Diseases 0.000 description 2
- 201000002996 androgenic alopecia Diseases 0.000 description 2
- 239000006227 byproduct Substances 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 208000024963 hair loss Diseases 0.000 description 2
- 230000003676 hair loss Effects 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 2
- JQWHASGSAFIOCM-UHFFFAOYSA-M sodium periodate Chemical compound [Na+].[O-]I(=O)(=O)=O JQWHASGSAFIOCM-UHFFFAOYSA-M 0.000 description 2
- 229960003604 testosterone Drugs 0.000 description 2
- SPVUYOXSQFMCAO-RIMFYDMWSA-N (3as,3bs,5ar,9ar,9bs,11as)-9a,11a-dimethyl-1,2,3,3a,3b,4,5,5a,6,8,9,9b,10,11-tetradecahydroindeno[5,4-f]quinolin-7-one Chemical class N([C@@H]1CC2)C(=O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CCC[C@@]2(C)CC1 SPVUYOXSQFMCAO-RIMFYDMWSA-N 0.000 description 1
- 108010029908 3-oxo-5-alpha-steroid 4-dehydrogenase Proteins 0.000 description 1
- 102000001779 3-oxo-5-alpha-steroid 4-dehydrogenase Human genes 0.000 description 1
- QZLYKIGBANMMBK-UGCZWRCOSA-N 5α-Androstane Chemical compound C([C@@H]1CC2)CCC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CCC[C@@]2(C)CC1 QZLYKIGBANMMBK-UGCZWRCOSA-N 0.000 description 1
- VCUFZILGIRCDQQ-KRWDZBQOSA-N N-[[(5S)-2-oxo-3-(2-oxo-3H-1,3-benzoxazol-6-yl)-1,3-oxazolidin-5-yl]methyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C1O[C@H](CN1C1=CC2=C(NC(O2)=O)C=C1)CNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F VCUFZILGIRCDQQ-KRWDZBQOSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 102000001307 androgen receptors Human genes 0.000 description 1
- 108010080146 androgen receptors Proteins 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- 239000001273 butane Substances 0.000 description 1
- 150000002009 diols Chemical class 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 238000004880 explosion Methods 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 239000012286 potassium permanganate Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J73/00—Steroids in which the cyclopenta[a]hydrophenanthrene skeleton has been modified by substitution of one or two carbon atoms by hetero atoms
- C07J73/001—Steroids in which the cyclopenta[a]hydrophenanthrene skeleton has been modified by substitution of one or two carbon atoms by hetero atoms by one hetero atom
- C07J73/005—Steroids in which the cyclopenta[a]hydrophenanthrene skeleton has been modified by substitution of one or two carbon atoms by hetero atoms by one hetero atom by nitrogen as hetero atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D221/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00
- C07D221/02—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00 condensed with carbocyclic rings or ring systems
- C07D221/04—Ortho- or peri-condensed ring systems
- C07D221/18—Ring systems of four or more rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Steroid Compounds (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Description
本発明は、穏やかな条件下で3−オキソ−4−アザ−5α−アンドロスタン化合物を選択的に製造するための改善された方法に関する。
アンドロスタン主鎖を有する下記式(II)の化合物、フィナステライド(17β−(N−tert−ブチルカルバモイル)−5α−4−アザ−アンドロスト−1−エン−3−オン)は、陽性前立腺肥大症及び男性型脱毛症の治療に効能がある:
前立腺肥大症及び男性型脱毛症は、テストステロンから得られる5α−ジヒドロテストステロン(DHT)がアンドロゼン受容体と結合することに起因する。テストステロンの5α−ジヒドロテストステロンへの転換は、テストステロン5α−還元酵素(reductase)によって媒介されるが、これはフィナステライドによって抑制される。フィナステライドによる5α−ジヒドロテストステロンの抑制作用は、前立腺を急速に回復させ、毛髪を増加させる。このように、フィナステライドは前立腺肥大症に効果的であり、副作用が軽くて一時的な男性型脱毛に対する優れた治療剤であって、米国のFDAが承認した二つの脱毛治療剤のうち、唯一の経口投与用製品である。
フィナステライドは、通常下記式(I)の3−オキソ−4−アザ−5α−アンドロスタン−17β−カルボン酸の17β位のカルボキシル基をt−ブチルカルバモイル基に転換させた後、1,2−位の脱水素化を行うか、或いは1,2−位の脱水素化を行った後、17β位のカルボキシル基をt−ブチルカルバモイル基に転換することによって製造できる。
例えば、上記式(I)の3−オキソ−4−アザ−5α−アンドロスタン−17β−カルボン酸の製造方法は、米国特許第4,760,071号及び文献[J.Med.Chem.,29,p2298(1986)]に開示されているが、この方法によれば、式(III)の3−オキソ−4−アザ−5−アンドロステン化合物を40psiの水素大気下、PtO2触媒の存在下で水素で還元して、式(I)の化合物を生成する。
上記還元方法は、5α位に配向された5−水素を有する式(I)の化合物のみを選択的に生成し、上記化合物の異性体、即ち5β位に配向された5−水素を有する下記式(IV)の化合物は生成しない。しかし、このような不斉還元方法は、高圧条件下で爆発危険性のある水素及び高価な触媒であるPtO2の使用を要する。
また、文献[J.of Pharmaceutical Sciences. 63, p19(1974)]には、式(III)の化合物と類似する構造を有する他のステロイド化合物を蟻酸とN−メチルホルムアミドを用いて還元して、5α−化合物を得る方法が開示されている。しかし、この方法は、高温及び高圧条件下で行われるため、大量生産に適しない。
本発明の目的は、穏やかな条件下で式(I)の化合物を選択的に製造する改善された方法を提供することである。
本発明は、亜鉛の存在下で下記式(III)の化合物を蟻酸とアルカンジオールとの混合物中で加熱することを含む、下記式(I)の化合物の製造方法を提供する:
本発明によれば、目的とする式(I)の化合物を穏やかな条件下で選択的に高収率で製造できる。
本発明の出発物質である式(III)の化合物は、公知の方法(米国特許第4,760,071号及び文献[J.Med.Chem.,29,p2298(1986)])によって製造できる。
本発明によれば、式(I)の化合物は、式(III)の化合物を蟻酸とアルカンジオールとの混合物に溶解し、これに活性化された亜鉛を添加した後、生成した混合物を加熱することによって製造できる。
本発明の方法において、蟻酸は式(III)の化合物1.0gに対して3〜30ml、好ましくは5〜15mlの量で用いられ得、アルカンジオールは式(III)の化合物1.0gに対して2〜20ml、好ましくは5〜10mlの量で用いられ得る。
本発明で用いられ得るアルカンジオールとしては、エチレングリコール、プロピレングリコール、1,3−プロパンジオール、1,2−ブタンジオール、1,3−ブタンジオール、1,4−ブタンジオール及び2,3−ブタンジオールなどが含まれ、これらの中でエチレングリコールが好ましい。
本発明で用いられる亜鉛は、目的とする5α−化合物に対する選択性及び反応収率を共に向上させ、しかも反応時間を減少させる。亜鉛は、式(III)の化合物1モルに対して4〜10当量、好ましくは6〜8当量で用いられ得、この場合、異性体である5β−副産物を生成することなく目的とする5α−化合物が80%の高収率で生成される。亜鉛を用いない場合、目的とする5α−化合物が約50%の収率で生成されると共に異性体である5β−副産物が10〜20%も生成される。
本発明による還元反応は80〜130℃、好ましくは100〜110℃の温度で4〜8時間行われ得る。
このように、本発明の簡単な方法によれば、目的とする式(I)の化合物が穏やかな条件下で選択的に高収率で製造できる。
以下、本発明を下記実施例によってより詳しく説明する。但し、下記実施例は本発明を例示するためのものであり、これらに限定されない。
[製造例1]:17β−カルボキシ−5−オキソ−A−ノル−3,5−セコアンドロスタン−3−オン酸の製造
3−オキソ−4−アンドロステン−17β−カルボン酸16g(50mmol)をt−ブタノール240mlに溶解して、これに水40mlに溶解した炭酸ナトリウム16g(150mmol)を添加した後、80℃に加熱した。これに、メタ過よう素酸ナトリウム53.5g(250mmol)及び過マンガン酸カリウム4.0g(25mmol)を水300mlに溶解して、60℃に予備加熱した溶液を徐々に滴下した。生成した混合物を3時間還流した後、室温で一晩放置した。無機物をセライトでろ過して、ろ液を水及び10%亜硫酸水素ナトリウム250mlで連続的に洗浄した後、t−ブタノールを減圧下で除去し、残留物を濃塩酸で酸性化させた。次いで、酸性化された残留物を塩化メチレン320mlで抽出し、5%亜硫酸水素ナトリウム320ml及び塩水320mlで連続的に洗浄した後減圧蒸留し、淡黄色の固形物の標題化合物14.5g(収率:86%)を得た。
3−オキソ−4−アンドロステン−17β−カルボン酸16g(50mmol)をt−ブタノール240mlに溶解して、これに水40mlに溶解した炭酸ナトリウム16g(150mmol)を添加した後、80℃に加熱した。これに、メタ過よう素酸ナトリウム53.5g(250mmol)及び過マンガン酸カリウム4.0g(25mmol)を水300mlに溶解して、60℃に予備加熱した溶液を徐々に滴下した。生成した混合物を3時間還流した後、室温で一晩放置した。無機物をセライトでろ過して、ろ液を水及び10%亜硫酸水素ナトリウム250mlで連続的に洗浄した後、t−ブタノールを減圧下で除去し、残留物を濃塩酸で酸性化させた。次いで、酸性化された残留物を塩化メチレン320mlで抽出し、5%亜硫酸水素ナトリウム320ml及び塩水320mlで連続的に洗浄した後減圧蒸留し、淡黄色の固形物の標題化合物14.5g(収率:86%)を得た。
H−NMR(δ,CDCl3):0.82(3H,19−CH3),1.16(3H,18−CH3),1.20〜2.30(15H,鎖型−CH),1.53(2H,1−CH2),2.40(2H,2−CH2),2.50(1H,17−CH),11.85(1H,COOH)
[製造例2]:3−オキソ−4−アザ−5−アンドロステン−17β−カルボン酸(式(III)の化合物)の製造
製造例1で得た17β−カルボキシ−5−オキソ−A−ノル−3,5−セコアンドロスタン−3−オン酸10g(30mmol)をエチレングリコール30mlに溶解し、これに2.0Mのアンモニア・エタノール溶液75ml(150mmol)を加えた後、40〜50℃で1時間攪拌してから12時間還流した。生成した混合物を室温に冷却した後、エタノールを減圧蒸留した。残留物に水150mlを加え、生成した混合物を10%塩酸でpH1.5まで酸性化させた。形成された沈殿物をろ過し、水で洗浄した後、45℃で乾燥して白色の固形物の標題化合物6.6g(収率:70%)を得た。
製造例1で得た17β−カルボキシ−5−オキソ−A−ノル−3,5−セコアンドロスタン−3−オン酸10g(30mmol)をエチレングリコール30mlに溶解し、これに2.0Mのアンモニア・エタノール溶液75ml(150mmol)を加えた後、40〜50℃で1時間攪拌してから12時間還流した。生成した混合物を室温に冷却した後、エタノールを減圧蒸留した。残留物に水150mlを加え、生成した混合物を10%塩酸でpH1.5まで酸性化させた。形成された沈殿物をろ過し、水で洗浄した後、45℃で乾燥して白色の固形物の標題化合物6.6g(収率:70%)を得た。
H−NMR(δ,DMSO−d6):0.57(3H,19−CH3),0.91(3H,18−CH3),0.95〜2.30(18H,鎖型−CH),4.76(1H,6−CH),9.17(1H,NH),11.85(1H,COOH)
[実施例1]:3−オキソ−4−アザ−5α−アンドロスタン−17β−カルボン酸(式(I)の化合物−1)
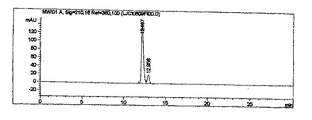
製造例2で得た3−オキソ−4−アザ−5−アンドロステン−17β−カルボン酸3.2g(10mmol)を蟻酸45mlとエチレングリコール15mlとの混合物に溶解し、これに活性化された亜鉛2.6g(80mmol)を加えた。混合物を100〜105℃で8時間反応させ、室温に冷却した。懸濁した固形物をろ過して除去し、ろ液中の溶媒を減圧下で除去した。残留物にN−メチルホルムアミド13mlを加え、生成した混合物を氷浴で30分間攪拌した。次いで、形成された沈殿物をろ過し、45℃で乾燥して白色の固形物の標題化合物2.6g(収率:81%)を得た。
製造例2で得た3−オキソ−4−アザ−5−アンドロステン−17β−カルボン酸3.2g(10mmol)を蟻酸45mlとエチレングリコール15mlとの混合物に溶解し、これに活性化された亜鉛2.6g(80mmol)を加えた。混合物を100〜105℃で8時間反応させ、室温に冷却した。懸濁した固形物をろ過して除去し、ろ液中の溶媒を減圧下で除去した。残留物にN−メチルホルムアミド13mlを加え、生成した混合物を氷浴で30分間攪拌した。次いで、形成された沈殿物をろ過し、45℃で乾燥して白色の固形物の標題化合物2.6g(収率:81%)を得た。
このようにして得られた生成物をHPLCで分析し、その結果を図1に示す。図1から分かるように、目的とする5α−化合物(保有時間:11.996)だけが検出され、異性体である5β−化合物は検出されなかった。
H−NMR(δ,DMSO−d6):0.56(3H,19−CH3),0.72(3H,18−CH3),0.80〜1.30(8H,鎖型−CH),1.40〜1.70(7H,鎖型−CH),1.87(2H,16−CH),2.10(2H,2−CH2),2.30(1H,17−CH),3.0(1H,5−CH),7.15(1H,NH),11.85(1H,COOH)
[実施例2]:3−オキソ−4−アザ−5α−アンドロスタン−17β−カルボン酸(式(I)の化合物−2)
製造例2で得た3−オキソ−4−アザ−5−アンドロステン−17β−カルボン酸3.2g(10mmol)を蟻酸16mlとエチレングリコール32mlとの混合物に溶解し、これに活性化された亜鉛2.6g(80mmol)を加えた。混合物を110〜120℃で8時間反応させ、室温に冷却した。懸濁した固形物をろ過して除去し、蟻酸を減圧下で除去した。残留物をクロロホルム300mlに溶解し、5%炭酸ナトリウム水溶液150mlずつで2回及び水150mlずつで3回連続的に洗浄した。クロロホルム層を分離した後、乾燥させてろ過し、溶媒を減圧下で除去した。残留物にN−メチルホルムアミド13mlを加え、氷浴で30分間攪拌した。次いで、形成された沈殿物をろ過し、45℃で乾燥して、白色の固形物の標題化合物2.7g(収率:83%)を得た。
製造例2で得た3−オキソ−4−アザ−5−アンドロステン−17β−カルボン酸3.2g(10mmol)を蟻酸16mlとエチレングリコール32mlとの混合物に溶解し、これに活性化された亜鉛2.6g(80mmol)を加えた。混合物を110〜120℃で8時間反応させ、室温に冷却した。懸濁した固形物をろ過して除去し、蟻酸を減圧下で除去した。残留物をクロロホルム300mlに溶解し、5%炭酸ナトリウム水溶液150mlずつで2回及び水150mlずつで3回連続的に洗浄した。クロロホルム層を分離した後、乾燥させてろ過し、溶媒を減圧下で除去した。残留物にN−メチルホルムアミド13mlを加え、氷浴で30分間攪拌した。次いで、形成された沈殿物をろ過し、45℃で乾燥して、白色の固形物の標題化合物2.7g(収率:83%)を得た。
このようにして得られた生成物をHPLCで分析し、その結果、目的とする5α−化合物(保有時間:11.996)だけが検出された。H−NMRデータは上記実施例1と同様である。
[比較例1]:亜鉛の不在下で3−オキソ−4−アザ−5α−アンドロスタン−17β−カルボン酸(式(I)の化合物)の製造
製造例2で得た3−オキソ−4−アザ−5−アンドロステン−17β−カルボン酸3.2g(10mmol)を蟻酸45mlとエチレングリコール15mlとの混合物に溶解した後、100〜105℃で8時間反応させた。反応混合物を室温に冷却した後、残留固形物をろ過して除去し、溶媒を減圧蒸留した。生成した残留物にN−メチルホルムアミド13mlを加え、氷浴で30分間攪拌した。次いで、形成した沈殿物をろ過し、45℃で乾燥して、白色の固形物の標題化合物1.7g(収率:53%)を得た。
製造例2で得た3−オキソ−4−アザ−5−アンドロステン−17β−カルボン酸3.2g(10mmol)を蟻酸45mlとエチレングリコール15mlとの混合物に溶解した後、100〜105℃で8時間反応させた。反応混合物を室温に冷却した後、残留固形物をろ過して除去し、溶媒を減圧蒸留した。生成した残留物にN−メチルホルムアミド13mlを加え、氷浴で30分間攪拌した。次いで、形成した沈殿物をろ過し、45℃で乾燥して、白色の固形物の標題化合物1.7g(収率:53%)を得た。
このようにして得られた生成物をHPLCで分析し、その結果を図2に示す。図2では、5β−化合物ピーク(保有時間:12.956)の領域が15%を、5α−化合物ピーク(保有時間:12.187)の領域が85%を占めた。即ち、目的としない5β−化合物が相当量生成した。
[比較例2]:蟻酸とN−メチルホルムアミドとの混合物を用いた、3−オキソ−4−アザ−5α−アンドロスタン−17β−カルボン酸(式(I)の化合物)の製造
製造例2で得た3−オキソ−4−アザ−5−アンドロステン−17β−カルボン酸3.2g(10mmol)を蟻酸45mlとN−メチルホルムアミド15mlとの混合物に溶解した後、100〜105℃で8時間反応させた。反応物を室温に冷却した後、残留固形物をろ過し、蟻酸を減圧下で除去した後、残留溶液を氷浴で30分間攪拌した。次いで、形成された沈殿物をろ過し、45℃で乾燥して、白色の固形物の標題化合物1.9g(収率:59%)を得た。
製造例2で得た3−オキソ−4−アザ−5−アンドロステン−17β−カルボン酸3.2g(10mmol)を蟻酸45mlとN−メチルホルムアミド15mlとの混合物に溶解した後、100〜105℃で8時間反応させた。反応物を室温に冷却した後、残留固形物をろ過し、蟻酸を減圧下で除去した後、残留溶液を氷浴で30分間攪拌した。次いで、形成された沈殿物をろ過し、45℃で乾燥して、白色の固形物の標題化合物1.9g(収率:59%)を得た。
このようにして得られた生成物をHPLCで分析し、その結果を図3に示す。図3では5β−化合物ピーク(保有時間:12.770)の領域が35%を、5α−化合物ピーク(保有時間:12.046)の領域が65%を占めた。即ち、目的としない5β−化合物が相当量生成した。
Claims (6)
- 前記蟻酸が式(III)の化合物1.0gに対して3〜30mlの量で用いられることを特徴とする請求項1記載の方法。
- 前記アルカンジオールがエチレングリコール、プロピレングリコール、1,3−プロパンジオール、1,2−ブタンジオール、1,3−ブタンジオール、1,4−ブタンジオール及び2,3−ブタンジオールからなる群から選択されることを特徴とする請求項1記載の方法。
- 前記アルカンジオールが式(III)の化合物1.0gに対して2〜20mlの量で用いられることを特徴とする請求項1記載の方法。
- 前記亜鉛が式(III)の化合物1モルに対して4〜10当量で用いられることを特徴とする請求項1記載の方法。
- 前記加熱が80〜130℃の温度で4〜8時間行われることを特徴とする請求項1記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR10-2002-0048784A KR100503193B1 (ko) | 2002-08-19 | 2002-08-19 | 3-옥소-4-아자-5α-안드로스탄 화합물의 선택적인 제조방법 |
| PCT/KR2003/001629 WO2004016595A1 (en) | 2002-08-19 | 2003-08-13 | Method for the selective preparation of 3-oxo-4-aza-5a-androstane compound |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2006501221A JP2006501221A (ja) | 2006-01-12 |
| JP4226552B2 true JP4226552B2 (ja) | 2009-02-18 |
Family
ID=31884908
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004528926A Expired - Fee Related JP4226552B2 (ja) | 2002-08-19 | 2003-08-13 | 3−オキソ−4−アザ−5α−アンドロスタン化合物の選択的製造方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US7084274B2 (ja) |
| EP (1) | EP1539703A4 (ja) |
| JP (1) | JP4226552B2 (ja) |
| KR (1) | KR100503193B1 (ja) |
| AU (1) | AU2003256102A1 (ja) |
| WO (1) | WO2004016595A1 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005075497A1 (en) * | 2004-01-07 | 2005-08-18 | Ranbaxy Laboratories Limited | PROCESS FOR THE PREPARATION OF 17ß-SUBSTITUTED-3-OXO-4-AZA-5ALPHA-ANDROSTANE DERIVATIVES |
| KR100698400B1 (ko) | 2004-04-14 | 2007-03-23 | 이은주 | 탈모증 및 전립선비대증 치료를 위한 약제학적 조성물 |
| AU2005232511B2 (en) | 2004-04-14 | 2008-07-03 | Eun-Joo Lee | Pharmaceutical composition for treating hair loss and benign prostatic hyperplasia |
| US7998970B2 (en) | 2004-12-03 | 2011-08-16 | Proteosys Ag | Use of finasteride, dutasteride and related compounds for the prevention or treatment of neurologically-associated disorders |
| EP1846527B1 (en) * | 2004-12-29 | 2008-08-06 | 3M Innovative Properties Company | Multi-photon polymerizable pre-ceramic polymeric compositions |
| CN101775064B (zh) * | 2010-02-05 | 2012-08-22 | 常州佳尔科药业集团有限公司 | 3-羰基-4-氮杂-5α-雄甾化合物的合成方法 |
| HU230730B1 (hu) | 2011-06-30 | 2017-12-28 | Richter Gedeon Nyrt | Eljárás (5alfa,17béta)-N-[2,5-bisz-(trifluormetil)-fenil]-3-oxo-4-aza-5-androszt-1-én-17-karbonsavamid előállítására |
| KR101552813B1 (ko) | 2015-05-18 | 2015-09-11 | 충남대학교산학협력단 | 사군자 추출물을 함유하는 전립선 비대증 예방 또는 치료용 조성물 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4220775A (en) * | 1979-03-15 | 1980-09-02 | Merck & Co., Inc. | Preparation of 4-aza-17-substituted-5α-androstan-3-ones useful as 5α-reductase inhibitors |
| NZ199859A (en) * | 1981-03-02 | 1984-10-19 | Glaxo Group Ltd | 11alpha-amino-3beta-hydroxy-androstanes |
| US4451576A (en) * | 1981-05-11 | 1984-05-29 | The Firestone Tire & Rubber Company | Molecular weight distribution and microstructure modifiers for elastomers |
| US5804576A (en) * | 1983-08-02 | 1998-09-08 | Research Corporation Technologies, Inc. | Derivatives of 5-androsten-17-ones and 5-androstan-17-ones |
| US4760071A (en) * | 1984-02-27 | 1988-07-26 | Merck & Co., Inc. | 17β-N-monosubstituted carbamoyl-4-aza-5α-androst-1-en-3-ones which are active as testosterone 5α-reductase inhibitors |
| GB9002922D0 (en) * | 1990-02-09 | 1990-04-04 | Erba Carlo Spa | 17 beta-substituted-4-aza-5 alpha-androstan-3-one derivatives and process for their preparation |
| JP3164389B2 (ja) * | 1991-12-25 | 2001-05-08 | 三共株式会社 | 4−アザステロイド類 |
| US5237064A (en) * | 1992-05-20 | 1993-08-17 | Merck & Co., Inc. | Process for producing 7β-substituted-aza-5αandrostan-3-ones |
| GB0026876D0 (en) * | 2000-11-03 | 2000-12-20 | Glaxo Group Ltd | Process |
-
2002
- 2002-08-19 KR KR10-2002-0048784A patent/KR100503193B1/ko not_active Expired - Fee Related
-
2003
- 2003-08-13 US US10/524,922 patent/US7084274B2/en not_active Expired - Fee Related
- 2003-08-13 AU AU2003256102A patent/AU2003256102A1/en not_active Abandoned
- 2003-08-13 WO PCT/KR2003/001629 patent/WO2004016595A1/en not_active Ceased
- 2003-08-13 EP EP03788151A patent/EP1539703A4/en not_active Withdrawn
- 2003-08-13 JP JP2004528926A patent/JP4226552B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| US7084274B2 (en) | 2006-08-01 |
| WO2004016595A1 (en) | 2004-02-26 |
| EP1539703A4 (en) | 2007-02-21 |
| AU2003256102A1 (en) | 2004-03-03 |
| KR100503193B1 (ko) | 2005-07-25 |
| EP1539703A1 (en) | 2005-06-15 |
| KR20040016559A (ko) | 2004-02-25 |
| US20060019979A1 (en) | 2006-01-26 |
| JP2006501221A (ja) | 2006-01-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5735465B2 (ja) | 5−(4−[4−(5−シアノ−3−インドリル)ブチル]−1−ピペラジニル)ベンゾフラン−2−カルボキサミドの製造方法 | |
| ES2273328T3 (es) | Metodo de preparacion en oxicodona. | |
| JP4226552B2 (ja) | 3−オキソ−4−アザ−5α−アンドロスタン化合物の選択的製造方法 | |
| CZ283894A3 (en) | 7beta-substituted 4-aza-5alpha-cholestanones, their use for the preparation of pharmaceutical preparations and pharmaceutical compositions containing thereof | |
| JP6815932B2 (ja) | N−カルバメート保護カルボキシ無水物の製造方法 | |
| CN101759762B (zh) | 4ad在制备度他雄胺中的应用 | |
| TW201802103A (zh) | 一種奧貝膽酸及其中間體的製備方法 | |
| US6509466B2 (en) | Process for obtaining 17 β-(N-tert-butylcarbamoyl)-3-one-4-aza-steroids | |
| HU230730B1 (hu) | Eljárás (5alfa,17béta)-N-[2,5-bisz-(trifluormetil)-fenil]-3-oxo-4-aza-5-androszt-1-én-17-karbonsavamid előállítására | |
| JPH04288096A (ja) | 3−オキソ−4−アザ−アンドロスト−1−エン 17β−ケトンの新製造方法 | |
| Sánchez et al. | Using the 9-BBN group as a transient protective group for the functionalization of reactive chains of α-amino acids | |
| SATO et al. | The Chemistry of the Spiroaminoketal Side Chain of Solasodine and Tomatidine. I. 1 Improved Preparation of 3β-Acetoxy-5, 16-pregnadien-20-one and 3β-Acetoxy-5α-pregn-16-en-20-one from Solasodine and Tomatidine. | |
| CN104072495A (zh) | 天然产物生物碱Aaptamine的制备方法 | |
| Luzina et al. | Chemical modification of usnic acid 2. Reactions of (+)-usnic acid with amino acids | |
| CN109232529A (zh) | 一种Rh(III)催化具有氮杂环骨架的化合物的制备方法 | |
| Hasserodt et al. | A class of 4-aza-lithocholic acid-derived haptens for the generation of catalytic antibodies with steroid synthase capabilities | |
| Merlani et al. | Conversion of Epiandrosterone Into 17β-Amino-5α-androstane. | |
| CN110776510B (zh) | 一种1-(2-喹啉基)-β-咔啉天然产物及衍生物的制备方法 | |
| WO2003027132A2 (en) | METHOD OF PREPARING 17β-(N-TERT-BUTYLCARBAMOYL)-3-ONE STEROID DERIVATIVES | |
| CN102807598A (zh) | 非那雄胺的制备方法 | |
| CN106496099A (zh) | 2‑[(2r,6s)‑6‑[(2s)‑2‑羟基‑2‑苯乙基]‑1‑甲基哌啶]‑1‑苯乙酮的合成方法 | |
| 최혜영 et al. | Bioisoster of capsaicin: Synthesis of 1-hydroxy-2-pyridone analogue | |
| WO2009093262A2 (en) | Process for preparing aromatase inhibitor exemestane | |
| JPH0316333B2 (ja) | ||
| CN115626903B (zh) | 一种eed抑制剂中间体的制备方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20081028 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20081126 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111205 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |