JP4219987B2 - ヘモフィルス・パラガリナルム由来新規ポリペプチド及びその製法 - Google Patents
ヘモフィルス・パラガリナルム由来新規ポリペプチド及びその製法 Download PDFInfo
- Publication number
- JP4219987B2 JP4219987B2 JP51449998A JP51449998A JP4219987B2 JP 4219987 B2 JP4219987 B2 JP 4219987B2 JP 51449998 A JP51449998 A JP 51449998A JP 51449998 A JP51449998 A JP 51449998A JP 4219987 B2 JP4219987 B2 JP 4219987B2
- Authority
- JP
- Japan
- Prior art keywords
- dna
- polypeptide
- antibody
- type
- sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/285—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Pasteurellaceae (F), e.g. Haemophilus influenza
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P21/00—Preparation of peptides or proteins
- C12P21/02—Preparation of peptides or proteins having a known sequence of two or more amino acids, e.g. glutathione
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S435/00—Chemistry: molecular biology and microbiology
- Y10S435/8215—Microorganisms
- Y10S435/822—Microorganisms using bacteria or actinomycetales
- Y10S435/851—Haemophilus
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Biochemistry (AREA)
- Medicinal Chemistry (AREA)
- Biomedical Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- General Engineering & Computer Science (AREA)
- Communicable Diseases (AREA)
- General Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Veterinary Medicine (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Analytical Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Gastroenterology & Hepatology (AREA)
- Cell Biology (AREA)
- Oncology (AREA)
- Food Science & Technology (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Plant Pathology (AREA)
- Peptides Or Proteins (AREA)
Description
本発明は鶏伝染性コリーザを阻止するポリペプチドに関する。さらに詳細には、鶏伝染性コリーザを引き起こす因子であるヘモフィルス・パラガリナルム由来のポリペプチド、該ポリペプチドをコードする遺伝子及び該ポリペプチドを認識する抗体蛋白質に関する。本発明はさらに、該ポリペプチドの製造方法並びにワクチン、診断薬及び治療薬への利用に関する。
背景技術
家禽の重要な呼吸器官系疾病として伝染性コリーザがある。この鶏伝染性コリーザは、ヘモフィルス・パラガリナルム(Haemophilus paragallinarum:以下、HPGと称することもある)の感染によって起こる急性呼吸器伝染病であり、鼻汁の漏出、顔面の腫脹あるいは流涙を主な症状とする。鶏伝染性コリーザは、家禽の育成率の低下、産卵開始の遅延、産卵率の低下あるいは産卵停止をもたらすため、その経済的損失は大きい。従来、鶏伝染性コリーザの予防には、ヘモフィルス・パラガリナルムを培養し、回収した菌体をホルマリン、チメロサール等で不活化したワクチンが広く応用されている。しかしながら、これらのワクチンを投与した場合、接種鶏の局所に壊死病巣を形成することが報告される(松本(M.Matsumoto)および山本(R.Yamamoto)、Avian Dis.,15:109−117、1971)など、ワクチンの副作用が問題となっており、安全性の高いワクチンの開発が強く待望されている。
また、近年、養鶏規模の拡大に伴って飼養管理の省力化が進められており、その一環としてワクチン接種に対する省力化の要望が強く、これに応えて、数種のワクチンを混合することにより接種回数を減らすことを狙った混合ワクチンが既に開発され、野外で広く用いられている。
混合ワクチンにおいて、注射量を増やすことなくそれぞれの単味ワクチンと同等の免疫原性を得るためには、混合するそれぞれの抗原量を増やすか、あるいは、良いアジュバントを探し用いることが必要となる。しかしながら、HPGのようなグラム陰性菌は、抗原量を増やした場合には、それに伴って接種局所の腫脹のような注射反応も強まる傾向がある。従って、菌体あるいは培養上清から感染防御抗原すなわち有効な成分(コンポーネント)のみを取り出すか、遺伝子組換え技術により感染防御抗原をコードする遺伝子をクローニングし、該遺伝子を細菌、酵母、動物細胞、植物細胞、昆虫細胞等に発現させ、大量に発現した発現産物を精製し、これを他のワクチンとともに適当なアジュバントと混合する等して、上記の副反応を低減することが望まれる。
一方、ワクチン接種の省力化の方法として、ウイルスや細菌をベクターとして使用することも試みられている。すなわち、一つの弱毒ウイルスあるいは細菌に1ないし複数の病原体の感染防御抗原をコードする遺伝子を組み込むことで多価の生ワクチンを作製するという方法である。これまでに鳥類ではベクターとしてポックスウイルスやマレック病ウイルス等を使用した研究が実施されており、鶏痘ウイルスにニューカッスル病ウイルスのHN及びF蛋白遺伝子を組み込んだウイルスベクターワクチンが実用化されている。
従って、これからの鶏伝染性コリーザに対する安全で有効なワクチンの開発には、コンポーネントワクチン、ベクターワクチンのいずれの場合においても、HPGの感染防御抗原を同定することが重要と考えられる。
HPGの感染防御抗原として赤血球凝集素(HA)、外膜蛋白などが報告されているが、その中でも、鶏にHPGを免疫すると赤血球凝集抑制抗体(以下、HI抗体という)が上昇し、HI抗体が高い鶏ほど感染防御能が高いことなどから、HAが最も重要な感染防御抗原と考えられている(大槻(K.Otsuki)及び入谷(Y.Iritani)、Avian Dis.,18:297−304、1974及び久米(K.Kume)ら、Jpn.J.Vet.Sci.,46:843−850、1984)。
HPGの血清型は凝集反応に基づいて、ページ(Page)(Am.J.Vet.Res.,23:85−95、1962)によりA、B及びC型に、また沢田(Sawata)ら(Jpn.J.Vet.Sci.,40:645−652、1978)により1型及び2型に型別されているが、ページのA型は沢田らの1型に、ページのC型は沢田らの2型に相当すると考えられている(久米ら、Am.J.Vet.Res.,41:757−760、1980及び沢田ら、Am.J.Vet.Res.,41:1901−1904、1980)。
久米らは、A型(1型)菌にはHA−L(易熱性、トリプシン感受性)、HA−HL(易熱性、トリプシン耐性)及びHA−HS(耐熱性、トリプシン耐性)の少なくとも3種類のHAが存在すること及びこれらのうち、HA−Lのみが、通常行われている新鮮鶏赤血球に対するHA活性以外に、グルタルアルデヒド固定鶏赤血球に対してもHA活性を有し、且つ、A型菌の感染防御に関与することを報告している(久米ら、Jpn.J.Vet.Sci.,45:783−792、1983及び沢田ら、Jpn.J.Vet.Sci.,46:21−29、1984)。また、入谷らは、A型菌にはタイプ1HA<易熱性、蛋白分解酵素感受性)及びタイプ2HA(易熱性、蛋白分解酵素耐性)の2種類のHAが存在し、このうち易熱性、蛋白分解酵素感受性で分子量約39kdのポリペプチドをサブユニットとするタイプ1HAが感染防御に関与すると報告している(山口(T.Yamaguchi)及び入谷、Jpn.J.Vet.Sci.,42:709−711、1980及び入谷ら、Am.J.Vet.Res.,41:2114−2118、1980)。久米らのHA−L及びHA−HLは、それぞれ入谷らのタイプ1HA及びタイプ2HAに相当すると考えられている。C型(2型)菌においても、沢田らは、易熱性、トリプシン感受性でグルタルアルデヒド固定鶏赤血球に対してHA活性を示す抗原が存在し、A型菌のHAとは抗原性を異にすると報告している(沢田ら、Am.J.Vet.Res.,43:1311−1314、1982)。しかしながら、入谷らが報告したA型菌の産生するタイプ1HAを除いて、感染防御抗原は物質として明確に同定されていないのが現状である。
上述したように、従来のヘモフィルス・パラガリナルム菌体をチメロサール、ホルマリン等で不活化したワクチンを鶏に大量に使用した場合には、感染防御に関与する抗原以外に、菌体に由来する種々の物質が含まれているために、上記の様な副作用を生じるという問題点があった。
発明の開示
本発明者らは、かかる問題点を解決するために鋭意研究を重ねた結果、ヘモフィルス・パラガリナルムA型菌の培養液から、HI抗体産生を誘導し、ヘモフィルス・パラガリナルムA型菌による鶏伝染性コリーザを防御する該A型菌に由来する分子量約130Kdのポリペプチドを精製することに成功した。さらに、該A型菌よりゲノムDNAライブラリーを作製し、この中から上記の130Kdポリペプチドをコードする遺伝子断片をクローニングし、これを大腸菌にて発現させ、得られた該ポリペプチドがヘモフィルス・パラガリナルムA型菌による鶏伝染性コリーザを阻止することを見い出した。また、上記の130Kdポリペプチドをコードする遺伝子断片をプローブとして用いてC型菌からも該DNA断片とハイブリダイズする遺伝子断片をクローニングし、C型菌由来のポリペプチドを発現する大腸菌をも得た。
本発明は、ヘモフィルス・パラガリナルムを病因菌とする鶏伝染性コリーザに対する、副作用の少ない、より安全で、有効なワクチン及びその製造方法を提供する。
すなわち、本発明の目的は、ヘモフィルス・パラガリナルム由来の新規なポリペプチド及びそのアミノ酸配列の少なくとも一部のアミノ酸配列を有するペプチドを提供することにある。
本発明の他の目的は、ヘモフィルス・パラガリナルム由来の新規なポリペプチド及びそのアミノ酸配列の少なくとも一部のアミノ酸配列を有するペプチドをコードする遺伝子及び該遺伝子を発現させるための組換えベクターを提供することにある。
本発明の更に他の目的は、上記組換えベクターで形質転換された微生物又は細胞形質転換体から、ヘモフィルス・パラガリナルム由来の新規なポリペプチド及びそのアミノ酸配列の少なくとも一部のアミノ酸配列を有するポリペプチドを製造する方法を提供することにある。
本発明の更に他の目的は、かくして得られたヘモフィルス・パラガリナルム由来の新規なペプチド及びそのアミノ酸配列の少なくとも一部のアミノ酸配列を有するポリペプチドを免疫原として作製されるモノクローナル抗体及びポリクローナル抗体を提供することにある。
本発明の更に他の目的は、上記のペプチド、DNA断片、形質転換体、もしくは抗体の組み合わせによるヘモフィルス・パラガリナルム及び該菌体に対する抗体を検出する方法を提供することにある。
本発明の更に他の目的は、ヘモフィルス・パラガリナルム由来の新規なポリペプチドに対する抗体を主成分とする鶏伝染性コリーザの治療剤を提供することにある。
【図面の簡単な説明】
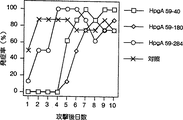
図1は、モノクローナル抗体(クローンHpgA 59−40、HpgA 59−180、HpgA 59−284)を鶏に受身免疫した後、ヘモフィルス・パラガリナルムA型菌221株で攻撃した成績を示した図で、あらかじめHI活性を有するモノクローナル抗体(クローンHpgA 59−40、HpgA 59−180)を投与していた群は発症時期が遅れることを示す。
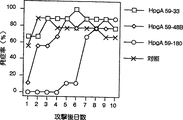
図2は、モノクローナル抗体(クローンHpgA 59−33、HpgA 59−48B、HpgA 59−180)を鶏に受身免疫した後、ヘモフィルス・パラガリナルムA型菌221株で攻撃した成績を示した図で、あらかじめHI活性を有するモノクローナル抗体(クローンHpgA 59−180)を投与していた群は発症時期が遅れることを示す。
図3は、モノクローナル抗体(クローンHpgA 59−48A、HpgA 59−145、HpgA 59−180)を鶏に受身免疫した後、ヘモフィルス・パラガリナルムA型菌221株で攻撃した成績を示した図で、あらかじめHI活性を有するモノクローナル抗体(クローンHpgA 59−145、HpgA 59−180)を投与していた群は発症時期が遅れることを示す。
図4は、モノクローナル抗体(クローンHpgA 59−188、HpgA 59−236、HpgA 59−180)を鶏に受身免疫した後、ヘモフィルス・パラガリナルムA型菌221株で攻撃した成績を示した図で、あらかじめHI活性を有するモノクローナル抗体(クローンHpgA 59−180)を投与していた群は発症時期が遅れることを示す。
図5は、HI活性を有するモノクローナル抗体(クローンHpgA 59−180)をリガンドとするアフィニティークロマトグラフィーにより精製したHPGp130ポリペプチドをSDS−PAGE法により電気泳動した後、CBB染色した結果を示す写真である。
図6は、a)2−メルカプトエタノール処理した精製HPGp130ポリペプチド及びヘモフィルス・パラガリナルムA型菌221株をSDS−PAGE法により電気泳動した後、CBB染色した結果を示す写真;及びb)2−メルカプトエタノール処理した精製HPGp130ポリペプチド及びヘモフィルス・パラガリナルムA型菌221株をSDS−PAGE法により電気泳動した後、薄膜(PVDF)に転写し、精製HPGp130ポリペプチドに対するモルモット抗血清を用いて、これと反応する蛋白質を検出した結果を示す写真である。
図7は、ヘモフィルス・バラガリナルムA型菌221株ゲノムよりクローニングしたHPG1.2k DNA、HPG3.5k DNA、HPG4.1k DNA、HPG6.7k DNA及びHPG2.7k DNA断片の位置を示す模式図である。
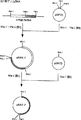
図8は、ヘモフィルス・バラガリナルムA型菌221株ゲノム由来のXhoI−XbaI消化断片(HPG4.1k DNA)をプラスミドpSP72に挿入したプラスミドpSA4.1を構築し、さらに該プラスミドからのXhoI−KpnI消化断片をプラスミドpTrcHisCに挿入したプラスミドpTA4.1を構築する手順を示す模式図である。
図9は、ヘモフィルス・パラガリナルムA型菌221株ゲノム由来のXhoI−PstI消化断片(HPG6.7kDNA)をプラスミドpSP72に挿入したプラスミドpSA6.7を構築し、さらに該プラスミドからのXbaI消化断片をプラスミドpSP72に挿入したプラスミドpSA2.7を構築する手順を示す模式図である。
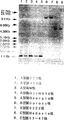
図10は、制限酵素EcoRI消化したヘモフィルス・パラガリナルムA型菌、B型菌及びC型菌由来ゲノムDNA断片をアガロース電気泳動した後、薄膜(ハイボンドN+)に転写し、HPG1.2k DNAをプローブとし、これとハイブリダイズするDNA断片を検出した結果を示す写真である。
図11は、ヘモフルス・バラガリナルムC型菌53−47株ゲノムより、クローニングしたHPG−C1DNA、HPG−C2DNA、HPG−C3DNA及びHPG−C4DNA断片の位置を示す模式図である。
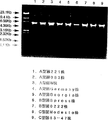
図12は、A型HMTp210ポリペプチドのN末端側およびC末端側アミノ酸残基をコードする塩基配列をもとに作製したプライマーを用いて、ヘモフィルス・パラガリナルムA型菌、B型菌及びC型菌由来ゲノムDNAを鋳型としてPCRを行った後、得られたPCR産物を0.8%アガロースゲル電気泳動で分析した結果を示す写真である。
発明を実施するための最良の形態
以下に、本発明を更に詳しく説明する。
本発明のHI抗体産生を誘導するヘモフィルス・パラガリナルムA型菌由来のポリペプチドは、HI活性を有するモノクローナル抗体をリガンドとするアフィニティークロマトグラフィーを行うことにより該A型菌の培養上清又は菌体の破砕液から調製される。
HI活性を有するモノクローナル抗体(以下、HI−MCAと称することもある)は、常法の細胞融合法により、ヘモフィルス・パラガリナルムA型菌に結合するモノクローナル抗体を産生するハイブリドーマを作製し、ついで、この中からHI試験により、HI活性を有するモノクローナル抗体産生ハイブリドーマを選択することにより取得できる。
上記の抗体を作製する際の免疫原として用いられるヘモフィルス・パラガリナルムA型菌は、通常のヘモフィルス・パラガリナルムの培養に用いられる方法に準じて得られる。例えば221株は、鶏血清加鶏肉汁培地(培地1000ml中、鶏肉水300ml、鶏血清10ml、ポリペプトン5g、ブドウ糖1g、カザミノ酸1g、グルタミン酸ナトリウム5g、塩化ナトリウム5g、ニコチンアミド・アデニン・ジヌクレオチド0.025gを含む)中で37℃、一夜振盪培養し、遠心分離することによって回収できる。
免疫は一般的方法により、例えば、上記のヘモフィルス・パラガリナルムA型菌をチメロサール、ホルマリン等で不活化した後、これを通常のアジュバントを併用してBALB/cマウスに腹腔内投与、皮下投与、皮内投与あるいは静脈内投与することにより行われる。免疫原としては、菌体そのものあるいはロダン化カリウム、超音波、ヒアルロニダーゼ等で処理した菌体もしくはN−ラウロイルサルコシンナトリウム、ノニデート(Nonidet)P−40、トリトン(Triton)X−100等の界面活性剤で処理した加工抗原であってもよい。アジュバントとしてはフロインド完全アジュバント、フロインド不完全アジュバント、水酸化アルミニウムゲル等が使用される。より具体的には以下のように行う。鶏血清加鶏肉汁培地中で培養したヘモフィルス・パラガリナルムA型菌221株をチメロサールで不活化した後、これを超音波処理する。得られた破砕液とフロインド完全アジュバントを混合して得たエマルジョンをBALB/cマウスの背部皮下に投与し、その後2〜4週間おきに同量を不完全アジュバントとともに調製したエマルジョンを背部皮下に投与する。血清抗体をチェックし、抗体価が上がっていることを確認した後、最終免疫として、更に、2〜4週間後に、超音波破砕液を静脈内投与する。
モノクローナル抗体を作製する際の免疫細胞としては、最終投与の2〜4日後に摘出した脾臓細胞を用いるのが好ましい。マウスミエローマ細胞としては、例えば、NSI−Ag4/1(Eur.J.Immunol.,6:511、1976)、P3X63−Ag8.U1(Curr.Topics Microbiol.Immunol.,81:1,1978)、X63−Ag8.653(J.Immunol.,123:1548、1979)等を使用することができる。脾臓細胞とマウスミエローマ細胞との融合反応はミルシュタイン(Milstein)らの方法(Method Enzymol.,73、3−46、1981)に準じて行うことができる。すなわち、融合する際には、マウスミエローマ細胞に対し、1〜10倍程度の脾臓細胞が用いられる。また、融合促進剤としては、分子量1,000〜6,000のポリエチレングリコールが30〜50%(w/v)の濃度で使用される。より具体的には、細胞融合は、約108個の脾臓細胞と約107個のP3X63−Ag8.U1ミエローマ細胞を用いて、予め37℃に加温した45%ポリエチレングリコール4,000を含むリンパ細胞の培養に通常に用いられる培地、例えば、RPMI1640培地中で行うのが好ましい。
ハイブリドーマは、未融合細胞が死滅するのに十分な時間、通常数日〜数週間、HAT培地中で培養することにより得られる。かくして得られるハイブリドーマに対し、その培養上清を用いて、通常の限界希釈法に従い、目的とする抗体産生株の選択及びクローン化が行われる。
ヘモフィルス・パラガリナルムA型菌を認識する抗体を産生する株の検索は、通常使用されるELISA法、RIA法、ウエスタンプロット法等に従って行われる。上記方法に使用される抗原はヘモフィルス・パラガリナルムA型菌体の懸濁液、該菌体をロダン化カリウム、超音波、ヒアルロニダーゼ等で処理した菌体、該菌体の界面活性剤による抽出液のいずれであってもよい。
ついで、HI活性を有する抗体を産生する株が、上記ハイブリドーマの培養上清もしくは該ハイブリドーマを投与したマウスの腹水を用い、通常に行われているHI試験に従って検索される。HA抗原としては、ヘモフィルス・パラガリナルム菌体の懸濁液あるいは該菌体をロダン化カリウム、超音波、ヒアルロニダーゼ等で処理した菌体が使用される。HI試験に用いる赤血球は、0.5%新鮮鶏赤血球、グルタルアルデヒド固定1%鶏赤血球あるいはホルマリン固定1%鶏赤血球のいずれでもよいが、好ましくは、グルタルアルデヒド固定鶏赤血球が用いられる。
より具体的には、5倍量の25%カオリン溶液で処理した腹水の遠心上清をグルタルアルデヒド固定鶏赤血球の沈澱に加え、37℃で60分間振盪感作する。この上清の2倍階段希釈液に4赤血球凝集単位を含む221株の菌懸濁液を等量加えて混和後15分間静置する。次に、グルタルアルデヒド固定1%鶏赤血球懸濁液を加え、室温に60分間静置した後、管底像により判定する。赤血球凝集を阻止する最高希釈倍数をHI抗体価とする。
かくして得られたHI活性を有するモノクローナル抗体を産生するハイブリドーマからの該抗体の採取には、該ハイブリドーマを大量に培養し、その培養上清から又は該ハイブリドーマに適合するマウスにこれを投与して増殖させ、その腹水から得る方法等がとられる。
モノクローナル抗体の精製は、蛋白質化学において通常使用される方法、例えば、塩析法、限外濾過法、等電点沈殿法、電気泳動法、イオン交換クロマトグラフィー法、ゲル濾過クロマトグラフィー法、アフィニティークロマトグラフィー法等を適宜選択して行えばよい。より具体的には、腹水からのモノクローナル抗体の精製は、プロテインA−セファロース(Protein A−Sepharose)CL−4B(ファルマシア製)及びMAPS−IIマウスモノクローナル抗体精製キット(バイオ・ラッド製)を用い、製造業者のプロトコールに従うことによって達成される。
本発明のHI抗体産生を誘導するヘモフィルス・パラガリナルムA型菌由来のポリペプチドの精製に使用されるHI活性を有する抗体をリガンドとするアフィニティーカラムは、一般的な方法、例えば、製造業者のプロトコールに従い、ハイトラップNHS−アクチベーテッド(HiTrap NHS−Activated)カラム(ファルマシア製)に、精製した上記抗体を結合させることにより得られる。
かくして調製されたアフィニティーカラムを用いることにより、該A型菌の培養上清又は菌体の破砕液から、HI抗体産生を誘導するヘモフィルス・パラガリナルムA型菌由来のポリペプチドを得ることができる。具体的には、221株を鶏血清加鶏肉汁培地中で37℃、2日間培養した上清から、高いHI抗体産生能と鶏伝染性コリーザを防御する活性を有する分子量約130Kdのポリペプチドを取得した(HPGp130と称する)。
このようにして得られたポリペプチドのアミノ酸配列は、エドマン分解法など一般的な方法(エドマン(P.Edman,Acta Chem.Scand.,4:283、1950)により決定することができる。該ポリペプチドのN末端側アミノ酸配列を配列表の配列番号:2に示す。
ヘモフィルス・パラガリナルムA型菌由来のポリペプチドをコードする遺伝子又はその断片のクローン化は、サムブルック(Sambrook)らが述べている一般的な方法(モレキュラー・クローニング、ア・ラボラトリー・マニュアル、第2版(Molecular Cloning,A Laboratory Manual,Second Edition)、コールド・スプリング・ハーバー・ラボラトリー・プレス(Cold Spring Harbor Laboratory Press)、ニューヨーク、1989)に従い行うことができる。すなわち、上述した方法によりヘモフィルス・パラガリナルムA型菌221株を培養、回収した後、セパジーンキット(三光純薬社製)を用い、添付のプロトコールに従ってゲノムDNAを抽出・精製し、これを適当な制限酵素(好ましくは、EcoRIが使用される)で切断し、市販のクローニングベクター(例えば、λgt11)に挿入し、DNAライブラリーを調製する。この中から、HI活性を有する適当な抗体と反応する抗原を発現しているクローンを選択する。HI活性を有する抗体としては、上記の方法により得られたモノクローナル抗体を含むハイブリドーマの培養上清又はマウスの腹水等が挙げられるが、好ましくは、HI活性を有するモノクローナル抗体をリガンドとするアフィニティークロマトグラフィーによって得られたヘモフィルス・パラガリナルムA型菌由来のポリペプチドで免疫した抗血清が使用される。このようにして得られた組換えλgt11ファージDNA中の外来DNA断片の塩基配列は、DNAシークエンサー(例えば、アプライド・バイオシステムズ(Applied Biosystems)377型)により決定することができる。また、得られた外来DNA断片の新規性は、その全塩基配列と既存のデータベース(例えば、GeneBank、EMBLなど)とのホモロジー検索を行うことにより確認できる。
例えば実施例3に示すように、DNAライブラリーからは、10個の陽性λgt11ファージが得られ、これらのファージDNAは、アガロース電気泳動法の結果から、いずれも約1.2kbの外来DNA断片(以下、HPG1.2k DNA断片とも称する)を含有する。その外来DNAの塩基配列は配列表の配列番号:1に記載の1988番目から3157番目の塩基配列に相当する。
このHPG1.2k DNA断片には、開始及び終止コドンが見い出されないので、該DNA断片は上記のヘモフィルス・パラガリナルムA型菌由来ポリペプチドの一部をコードしていると考えられる。該ポリペプチドの全長をコードする遺伝子は、HPG1.2k DNA断片をプローブとし、より長鎖のDNA断片を得、該断片の塩基配列を調べ、配列内に開始コドン及び終止コドンを見い出すことにより達成される。
より具体的には、ヘモフィルス・パラガリナルムA型菌221株ゲノムDNAを1.2kb DNA断片の内部で切断しない制限酵素(例えばHindIII)で切断した後、これをアガロース電気泳動法により、各DNA断片を分離する。DIG−DNA標識キット(ベーリンガーマンハイム製)を用いて、ジゴキシゲニン(DIG)で標識した1.2kb DNA断片をプローブとして、サザンハイブリダイゼーションを行い、目的のDNA断片を検出する。その結果、1.2kb DNA断片とハイブリダイズする約3.5kbのHindIII消化DNA断片(以下、HPG3.5k DNA断片とも称する)を得た。このHPG3.5k DNA断片の塩基配列は、配列表の配列番号:1に記載の1番目から3450番目の塩基配列に相当する。なお、前述のHPGp130ポリペプチドのN末端側アミノ酸配列と一致する配列を、配列表の配列番号:1に記載の1番目から13番目のアミノ酸配列(453番目から491番目の塩基配列に相当する)に見い出した。
このHPG3.5k DNA断片には、開始コドンは見い出されたが終止コドンが見い出されないので、さらに、DIGで標識した1.2kb DNA断片および3.5kb DNA断片を用いて、約4.1kbのXhoI−XbaI消化DNA断片(以下、HPG4.1k DNA断片とも称する)を得た。このHPG4.1k DNA断片の塩基配列は、配列表の配列番号:1に記載の2212番目から6275番目の塩基配列に相当する。さらに、DIGで標識した1.2kb DNA断片および3.5kb DNA断片を用いて、約6.7kbのXhoI−PstI消化DNA断片(以下、HPG6.7k DNA断片とも称する;この断片内には上記のHPG4.1k DNA断片が含まれる)を得た。このHPG6.7k DNA断片の塩基配列は、配列表の配列番号:1に記載の2212番目から8930番目の塩基配列に相当する。このHPG6.7k DNA断片に終止コドンが見い出された。
配列表の配列番号:1に記載の塩基配列は、全長8930塩基からなる塩基配列であり、その中に塩基番号243から翻訳され2042個のアミノ酸をコードできるオープンリーディングフレームが存在することが明らかとなった。この2042個のアミノ酸からなるポリペプチドを以下、A型HMTp210とも称する。既存のデータベース(GeneBank及びEMBL)とのホモロジー検索を行ったところ、既知の塩基配列あるいはアミノ酸配列とのホモロジーが認められなかったことから、A型HMTp210ポリペプチドは新規物質と考えられた。
また、配列表の配列番号:1に記載の塩基配列の中に塩基番号8375から翻訳され185個のアミノ酸をコードできるオープンリーディングフレームの存在の可能性が示された。なお、この配列内に終止コドンは見い出されていない。既存のデータベース(GeneBank及びEMBL)とのホモロジー検索を行ったところ、既知の塩基配列あるいはアミノ酸配列とのホモロジーが認められなかったことから、このオープンリーディングフレームがコードするポリペプチドも新規物質と考えられた。
上記のヘモフィルス・パラガリナルムA型菌由来DNA断片は、これをプローブとして、血清型の異なるヘモフィルス・パラガリナルムB型菌及びC型菌由来のDNA断片、更には該DNA断片がコードするポリペプチドを取得するために使用することができる。
より具体的には、C型菌53−47株からゲノムDNAを抽出・精製し、これを適当な制限酵素(好ましくは、HindIIIが使用される)で切断し、市販のクローニングベクター(例えば、λDASHII)に挿入し、DNAライブラリーを調製する。この中から、DIG標識したA型HPG3.5k DNA断片をプローブとして、クローンを選択する。
実施例5に示すように、DNAライブラリーからは、10個の陽性λDASHIIファージが得られ、これらのファージDNAは、アガロース電気泳動法の結果から、いずれも約13.5kbの外来DNA断片(以下、HPG−C1 DNAとも称する)を含有する。
このHPG−C1DNA断片は約13.5kbとかなり大きく、そのままではプラスミドベクターにサブクローニングするのは困難であることから、HPG−C1 DNA断片を適当な制限酵素(好ましくは、XbaIが使用される)で切断し、市販のクローニングベクター(例えば、pUC119)に挿入する。その結果、約5.6kb(以下、HPG−C2 DNAとも称する)、約0.9kb(以下、HPG−C3 DNAとも称する)及び約6.9kb(以下、HPG−C4 DNAとも称する)のDNA断片を得た。HPG−C2 DNA断片の一部とHPG−C4 DNA断片の塩基配列を調べたところ、これらの断片内に開始及び終止コドンが見い出された。
配列表の配列番号:5に記載の塩基配列は、全長7486塩基からなる塩基配列であり、その中に塩基番号848から翻訳され2039個のアミノ酸をコードできるオープンリーディングフレームが存在することが明らかとなった。この2039個のアミノ酸からなるポリペプチドを以下、C型HMTp210とも称する。既存のデータベース(GeneBank及びEMBL)とのホモロジー検索を行ったところ、既知の塩基配列あるいはアミノ酸配列とのホモロジーが認められなかったことから、C型HMTp210ポリペプチドは新規物質と考えられた。
また、C型HMTp210ポリペプチドをコードする塩基配列とA型HMTp210ポリペプチドをコードする塩基配列のホモロジーを調べたところ、約80%のホモロジーがあること、さらに、5’側の約3.4kbの領域と3’側の約1.2kbの領域が非常にホモロジーが高いこと、2つの領域にはさまれた約1.5kbの領域はホモロジーが低いことが明らかとなった。また、これらの遺伝子にコードされるポリペプチドについても、同様のことが認められた。
A型HMTp210ポリペプチドをコードする塩基配列をもとに、PCRによりヘモフィルス・パラガリナルムA型菌のみならず血清型の異なるB型菌及びC型菌由来のDNA断片、更には該DNA断片がコードするポリペプチドを取得することもできる。
より具体的には、A型HMTp210ポリペプチドをコードする塩基配列をもとに、上流側のPCRプライマーとして、配列番号:3に記載の塩基配列を有する合成DNAを、下流側のPCRプライマーとして、配列番号:4に記載の塩基配列を有する合成DNAを作製した。これらのプライマーは、それぞれ5’末端にBamHI認識配列を付加させ、また、A型HMTp210ポリペプチドの翻訳領域の全長を増幅できるようにデザインした。これらのプライマーを用いてヘモフィルス・パラガリナルムA型菌の221株、083株、W株、Germany株及びGeorgia株、B型菌のSpross株及び0222株、C型菌のModesto株及び53−47株の計9株からのゲノムDNAを鋳型としてPCRを行った。得られたPCR産物を0.8%アガロースゲル電気泳動で分析したところ、いずれの株にも約6.1kbのサイズの増幅フラグメントが認められた。
かくして得られたDNA断片あるいはその一部を適当な発現ベクターに組み込み、これを用いて、微生物又は動物細胞を形質転換し、形質転換体を培養することにより、本発明のヘモフィルス・パラガリナルム由来のポリペプチドあるいはそのアミノ酸配列の少なくとも一部のアミノ酸配列を有するペプチドを生産することができる。このような一部のアミノ酸配列を有するペプチドを生産する場合は、ペプチド合成機を利用することもできる。
本発明のポリペプチドをコードするDNAの上流に、分泌のための微生物用又は動物細胞用の適当なシグナル配列を接続すれば、該ポリペプチドを培地中に分泌発現させることも可能である。このように分泌型に改変したDNAは、培地中に分泌した該ポリペプチドの精製を容易にする点で有用である。シグナル配列としては、大腸菌用としてpelBシグナル(レイ(S.P.Lei)ら、J.Bacteriology,169:4379−4383、1987)、酵母用としてα因子のシグナル(ブレイク(A.J.Brake)、Yeast Genetic Engineering,p269、バターワース、1989)、動物細胞用としてイムノグロブリンのシグナルSG−1(前田(H.Maeda)ら、Hum.Antibod.Hybridomas,2:124−134、1991)、C25のシグナル(PCT国際公開番号WO94/20632)などが挙げられる。
発現ベクターとしては、プラスミド、ウイルスベクター等を用いることができる。該発現ベクターに含まれるプロモーターは、宿主として用いる微生物又は動物細胞との組み合わせにより、lac、tac、pho5、adh、SV40初期、SV40後期、βアクチン等、最終的に鶏伝染性コリーザを防御する活性を有するポリペプチドが得られるのであればどのようなものでもよい。また、他の蛋白質やペプチド、例えば、β−ガラクトシダーゼ、グルタチオン−S−トランスフェラーゼ、マルトース結合蛋白、プロテインA、ヒスチジンヘキサマー等との融合蛋白として発現させることもできる。マーカー遺伝子として、微生物細胞用発現ベクターを用いる場合は、宿主として大腸菌を用いる場合、アンピシリン耐性遺伝子、テトラサイクリン耐性遺伝子、宿主として酵母を用いる場合、β−イソプロピルリンゴ酸デヒドロゲナーゼ(Leu2)遺伝子などが利用される。また、動物細胞用発現ベクターを用いる場合は、アミノグリコシド3’ホスホトランスフェラーゼ(neo)遺伝子やジヒドロ葉酸還元酵素(dhfr)遺伝子、グルタミン合成酵素(GS)遺伝子などを利用できる。選択用添加物質としては、G418、ネオマイシン、メソトレキセート等が例示される。
宿主細胞の形質転換は公知の方法、例えば、塩化カルシウム法、リン酸カルシウム共沈澱法、DEAEデキストラン法、リポフェクチン法、プロトプラストポリエチレン融合法、エレクトロポレーション法等が利用でき、用いる宿主細胞により適当な方法を選択すればよい。
本発明のヘモフィルス・パラガリナルム由来の新規ポリペプチドあるいはそのアミノ酸配列の少なくとも一部のアミノ酸配列を有するペプチドは、以下の方法により製造される。例えば、発現ベクターpTrcHisC(インビトロジェン(Invitrogen)社製)にA型菌由来のHPG3.5k DNA断片を組み込み、これを大腸菌JM109株に導入し、形質転換を行う。形質転換細胞の中から、該ポリペプチドに対する抗体との反応性を指標とするドットブロット法により、目的の新規ポリペプチドを生産する形質転換細胞をスクリーニングする。この細胞の超音波破砕液の遠心上清で免疫された鶏は,A型菌221株の攻撃に対し、高い防御能を有する。
新規ポリペプチドの精製は、該ポリペプチドを産生する形質転換細胞を大量培養し、回収したその細胞抽出液又は培養上清から、前述した蛋白質化学において通常使用される方法を適宜選択することにより達成される。
かくして得られるヘモフィルス・パラガリナルム由来の新規なポリペプチドは、鶏伝染性コリーザを防御する活性を有するものである。ヘモフィルス・パラガリナルム由来の該ポリペプチド、該ポリペプチドに対するモノクローナル抗体及びポリクローナル抗体並びに上記の発現ベクターは、鶏伝染性コリーザのワクチン及び治療薬として、単独であるいは薬剤として投与可能な適当な担体、希釈液又は安定剤を添加することにより、注射剤、経口剤等の任意慣用の方法で医薬品に使用される。
上述のヘモフィルス・パラガリナルムの新規ポリペプチド及びそのアミノ酸配列の少なくとも一部のアミノ酸配列を有するポリペプチドは、上述した方法により、ポリクローナル抗体及びモノクローナル抗体を作製するための免疫原として使用される。また、該ポリペプチド及びこれらとの結合能を有する抗体は、ウエスタンブロット法、ELISA法などの抗原及び抗体検出系に利用することができ、診断薬を構築する材料となる。また、上記の抗体を適当な担体に結合させ、これを用いたアフィニティークロマトグラフィーにより、上記のポリペプチドを精製することができる。
本発明によると、鶏伝染性コリーザを予防するためのヘモフィルス・パラガリナルム由来の新規なポリペプチド及び該ポリペプチドをコードする遺伝子断片並びに治療薬として使用可能なHI活性を有する抗体が提供される。
本発明者が見い出したヘモフィルス・パラガリナルム由来のポリペプチドは、分子量が約130Kdで、HI抗体産生を誘導する活性を有し、ヘモフィルス・パラガリナルムによる鶏伝染性コリーザを防御するための重要な新規なポリペプチドである。該ポリペプチドをコードする遺伝子の単離、発現ベクターの構築、発現細胞の作製、上記ポリペプチドの精製法など、該ポリペプチドを実用化するための技術的な問題は本発明により解決され、従来技術に比較してより効果的なワクチンを提供することが可能になった。更に、これらは、迅速かつ簡便な鶏伝染性コリーザ診断薬を提供するための材料としても有用である。
以下に実施例を挙げて本発明をさらに具体的に説明するが、本発明はこれらに限られるものではない。
実施例1:モノクローナル抗体の作製及び性状
1)モノクローナル抗体の作製
ヘモフィルス・パラガリナルムA型菌221株を鶏血清加鶏肉汁培地100mlに接種し、37℃で一夜振盪培養した後、遠心分離(8,000回転、20分間)により菌体を回収した。得られた菌体をPBSで遠心洗浄後、約5×1010個/mlとなるように0.01%チメロサールを含むPBSに懸濁した。この懸濁液をブランソン・ソニファイアー(Branson Sonifier)350を使用して20kHzで、4℃、10分間超音波にかけた(0.5秒間超音波にかけ、0.5秒間の冷却を交互に実施)。このようにして得られた超音波破砕液とフロインドの完全アジュバントとを等量ずつ混合し、油中水滴型(w/o)の状態になるまで充分混和した。このエマルジョン0.1mlずつをBALB/cマウスの背部皮下2箇所に投与し、4週間後に、フロインドの不完全アジュバントで上記と同様に調製したエマルジョン0.1mlずつを背部皮下2箇所に投与した。さらに18日後に超音波破砕液0.1mlを静脈内投与した。
最終投与の3日後に脾臓細胞を採取した。1×108個の該脾臓細胞と1×107個のマウスミエローマ細胞P3X63−Ag8.U1をパディングにより混合し、これに予め37℃に加温した45%ポリエチレングリコール4,000を含むRPMI1640培地を加え、細胞融合を行わせた。この融合反応後の細胞をHAT培地(1×10-4Mヒポキサンチン、4×10-7Mアミノプテリン、1.6×10-5Mチミジンを添加した5%ウシ胎児血清を含むRPMI1640培地)に懸濁し、細胞培養用96ウエルマイクロプレート(コーニング製)に分注後、37℃、5%炭酸ガスの条件下で培養した。
ハイブリドーマの増殖が認められたウエルについて、以下に記載するELISA法を用いて、培養上清中のヘモフィルス・パラガリナルムを認識する抗体の存在の有無を検索した。上記の方法により調製したヘモフィルス・パラガリナルムA型菌221株の超音波破砕液をPBSで300倍希釈し、ELISA用マイクロプレート(イムロンII、ダイナテック製)のウエルに100μlずつ分注し、4℃で一夜放置した後、5%スキムミルクを含むPBS(1ウエル当たり200μl)で室温、2時間マスキングを行った。0.05%トゥイーン20を含むPBS(PBS−T)で洗浄後、5%スキムミルクを含むPBS−Tで10倍希釈したハイブリドーマ培養上清を100μl加え、室温で2時間反応させた。PBS−Tで洗浄後、5%スキムミルクを含むPBS−Tで10,000倍希釈したペルオキシダーゼ標識抗マウスIgG(バイオ・ラッド製)を100μlずつ加え、室温で2時間反応させた。さらに、PBS−Tで洗浄後、11ml当たりオルト−フェニレンジアミン二塩酸塩(OPD、片山化学製)6mg及び過酸化水素水(H2O2 31%含有、三菱瓦斯化学製)4.75μlを含む0.05Mクエン酸−0.1Mリン酸水素二ナトリウムバッファー(pH5.0)を100μlずつ加え、室温で30分間反応させた。3M硫酸を50μlずつ加え、反応停止後、各ウエルの吸光度(490nm)をELISA用オートリーダーで測定した。
培養上清中にヘモフィルス・パラガリナルムA型菌に対する抗体が認められたウエルのハイブリドーマは、さらに限界希釈法でクローニングを行い、単クローンとした。このようにして、ヘモフィルス・パラガリナルムA型菌に対するモノクローナル抗体を産生する株9クローンを得た。
2)モノクローナル抗体のHI活性
これらのハイブリドーマを大量に培養し、免疫抑制剤のプリスタン(2,6,10,14−テトラメチルペンタデカン、アルドリッチ製)で前処理したBALB/cマウスの腹腔内に投与して増殖させ、10〜20日後に産生された腹水を屠殺開腹したマウスより採取し、得られた腹水中のHI活性を調べた。
HI試験に用いるHA抗原としてヘモフィルス・パラガリナルムA型菌221株のチメロサール不活化菌懸濁液を用い、HA価を基に調製した。まず、V型マイクロプレート(三光純薬製)を用い、上記のHA抗原の2倍階段希釈液0.05mlにグルタルアルデヒド固定1%鶏赤血球懸濁液0.05mlを加え、室温に60分間静置した後、管底像により判定した。赤血球を凝集させる最高希釈倍数をHA価とし、このときのHA抗原濃度を1単位とし、HI試験には4単位になるように該HA抗原液を調製した。
次に、マウス腹水0.2mlに5倍量の25%カオリン溶液を加えて37℃で30分間振盪感作し、遠心分離により上清を得た。グルタルアルデヒド固定10%鶏赤血球2mlを遠心して得られた沈澱に、このカオリン処理済の遠心上清を加え、37℃で60分間振盪感作した。感作後、遠心により上清を得、5倍希釈マウス腹水としてHI抗体の測定に使用した。V型マイクロプレートを用い、この上清の2倍階段希釈液0.025mlに上記の4赤血球凝集単位を含む221株のチメロサール不活化菌懸濁液を等量加えて混和後、15分間静置した。充分感作した後、グルタルアルデヒド固定1%鶏赤血球懸濁液0.05mlを加えた。室温に60分間静置した後、管底像により判定した。赤血球凝集を阻止する最高希釈倍数をHI抗体価とした。9クローンの内3クローン(HpgA 59−40、HpgA 59−145、HpgA 59−180)のモノクローナル抗体が高いHI活性を示した(表1)。なお、クローンHpgA 59−180はFERM BP−6084として、1996年9月5日に工業技術院生命工学工業技術研究所(茨城県つくば市東1丁目1番3号)に出願人により寄託されている。
3)モノクローナル抗体の防御活性
これらの抗体を含むマウス腹水0.3mlを一群8〜10羽の4〜6週齢の白色レグホンSPF鶏の腹腔内にそれぞれ注射し、翌日にヘモフィルス・パラガリナルムA型菌221株約108個を鼻腔内に滴下し攻撃した。対照としてマウス腹水非投与群をおき、同様な攻撃を行い、コリーザ症状(鼻汁の漏出、顔面腫脹、流涙)の有無について10日間観察した。あらかじめHI活性を有するモノクローナル抗体(以下、HI−MCAとも称する)を投与していた群は3クローンとも、対照群に較べて発症時期が遅れる傾向が見られた。一方、他のクローンを投与していた群は、いずれも対照群との差は認められなかった(図1〜4)。
実施例2:HI−MCAが認識する抗原の精製及び性状
1)HI−MCAの精製
HI−MCA(HpgA 59−180)をマウス腹水からプロテインA−セファロースCL−4B(ファルマシア製)及びMAPS−IIマウスモノクローナル抗体精製キット(バイオ・ラッド製)を利用して、添付のプロトコールに従い精製した。まず、マウス腹水4mlに等量の抗体精製キットに含まれる結合バッファーを加え、0.45ミクロンのステリベックス・フィルター(ミリポア製)で濾過後、プロテインA−セファロースCL−4Bカラム(ゲルベッドボリューム5ml)にかけ、結合バッファーで280nmの吸光度が0.05以下になるまで充分洗浄した。ついで、キットに含まれる溶出バッファーでカラムに結合した抗体を溶出した。溶出した抗体は、0.5M塩化ナトリウムを含む0.2M炭酸水素ナトリウム溶液(pH8.3)に対して透析し、精製HI−MCA(HpgA 59−180)40mgを得た。HI−MCA(HpgA 59−40)についても同様に精製し12mgを得た。
2)HI−MCAの担体への結合
次に、精製したHI−MCA(HpgA 59−180)をリガンドとして、ハイトラップNHS−アクチベーテッドカラム(ファルマシア製)に、添付のプロトコールに従い結合させた。まず、ハイトラップNHS−アクチベーテッドカラム(ゲルベッドボリューム1ml)を1mM塩酸で洗浄後、これに前記の精製HI−MCA(HpgA 59−180)10mgの0.5M塩化ナトリウムを含む0.2M炭酸水素ナトリウム溶液(10ml)を室温で30分間循環させることによりHI−MCAを結合させた。得られたHI−MCA結合ハイトラップカラムを、0.5M塩化ナトリウムを含む0.5Mエタノールアミン(pH8.3)、0.5M塩化ナトリウムを含む0.1M酢酸ナトリウムバッファー(pH4.0)で交互に3回洗浄後、PBSで平衡化し、HI−MCAが認識する抗原の精製に供試した。
3)HI−MCAが認識する抗原の精製
ヘモフィルス・パラガリナルムA型菌221株の培養液から、HI−MCAをリガンドとしたアフィニティークロマトグラフィーにより、抗原の精製を行った。なお、抗原の検出は、以下に記載するELISA法を利用して行った。
前記の精製したHI−MCA(HpgA 59−40)を0.05M炭酸ナトリウムバッファー(pH9.0)で1.6μg/mlの濃度に希釈し、ELISA用マイクロプレートのウエルに入れ、4℃で一夜放置した後、5%スキムミルクを含むPBSで室温、2時間マスキングを行った。PBS−Tで洗浄後、5%スキムミルクを含むPBS−Tで10倍に希釈したカラム溶出液を室温で2時間反応させた。PBS−Tで洗浄後、5%スキムミルクを含むPBS−Tで10,000倍に希釈したペルオキシダーゼ標識HI−MCA(HpgA 59−180)を室温で2時間反応させた。さらに、PBS−Tで洗浄後、OPD及び過酸化水素水を含む基質液を加え室温で30分間反応させた。ペルオキシダーゼ標識HI−MCA(HpgA 59−180)は吉竹(Yoshitake)らの方法(J.Biochem.,92:1413−1424、1982)に準じて、前記の精製したHI−MCA(HpgA 59−180)に西洋わさびペルオキシダーゼ(東洋紡製)を結合させることにより調製した。
ヘモフィルス・パラガリナルムA型菌221株を鶏血清加鶏肉汁培地100mlに接種し、37℃で2日間振盪培養した。次に8,000回転、20分間の遠心により菌体を除去した培養上清に、直ちにセリンプロテアーゼ阻害剤フェニルメチルスルホニルフルオリドを1mMになるように加え、0.45ミクロンのステリベックス・フィルターにて濾過した。予めPBSで平衡化したHI−MCA結合ハイトラップカラムに、上記の濾液60mlを添加後、PBSで洗浄し、280nmの吸光度が0.05以下になった時点で、HI−MCAと結合する抗原を3Mチオシアン酸ナトリウムで溶出した。HI−MCAが認識する抗原は素通り画分には認められず、ほとんどが3Mチオシアン酸ナトリウム溶出画分に回収された。この溶出液を50mM塩化ナトリウムを含む50mMトリス塩酸バッファー(pH8.0)に対して透析した。
4)HI−MCAが認識する抗原のN末端側アミノ酸分析
アフィニティーカラムからの溶出液について2−メルカプトエタノール処理後、5−20%ポリアクリルアミドゲルを用いてドデシル硫酸ナトリウムポリアクリルアミドゲル電気泳動(SDS−PAGE)をレムリ(Laemmli)の方法(Nature,227:680−685、1970)に準じて行い、50%メタノール−10%酢酸で溶解した0.25%クマジーブリリアントブルーR250(CBB)で染色を行ったところ、分子量約130Kdのバンドが確認できた(図5)。そこで、このポリペプチドをHPGp130と名付け、そのN末端側アミノ酸配列の決定を以下の方法に従って行った。
まず、該精製HPGp130ポリペプチドを2−メルカプトエタノール処理後、5%ポリアクリルアミドゲルを用いてSDS−PAGEを行った。
泳動終了後、ゲルをトランスファーバッファー(10mM N−シクロヘキシル−3−アミノプロパンスルホン酸、10%メタノール、pH11)で洗浄し、あらかじめ100%メタノール及びトランスファーバッファーの順に浸しておいたポリビニリデンジフルオリド(PVDF)膜(ミリポア製)上に重ね、トランス・ブロット・セル(TRANS−BLOT CELL)(バイオ・ラッド製)を用いて20V、一夜転写を行った。転写後のPVDF膜を水洗し、45%メタノール−10%酢酸に溶解した0.1%アミドブラックで30秒間染色後、蒸留水で脱色を行った。
染色された分子量130Kdのバンドを切り出し、この膜をプロテインシークエンサー(アプライド・バイオシステムズ477A型)を用いて分析した。N末端側の13アミノ酸残基を解読した結果、そのアミノ酸配列は配列番号:2で示されるLys−Trp−Leu−Glu−Val−Tyr−Ser−Ser−Ser−Val−Lys−Leu−Serであった。
5)HPGp130ポリペプチドのHI抗体産生の誘導
HPGp130ポリペプチドがHI抗体産生を誘導するかを調べた。該HPGp130ポリペプチド溶液(約40μg/ml)を同量のフロインドの完全アジュバントと混合して調製したエマルジョン1ml(1匹当たりHPGp130ポリペプチド約20μg)をモルモットの背部皮下2箇所に注射し、免疫した。約3週間後に、フロインドの不完全アジュバントで上記と同様に調製したエマルジョン1mlを背部皮下2箇所に注射した。さらに2週間後に、フロインドの不完全アジュバントで調製した同エマルジョンを背部皮下2箇所に追加投与し、その4週間後に採血した。前記と同様の方法で、得られた抗血清中のHI抗体価を調べたところ、高いHI抗体価(5,120倍)を有していた。このように、HPGp130ポリペプチドは、鶏伝染性コリーザの防御に深く関わりがあるといわれているHI抗体の産生を誘導することが明らかとなった。
6)抗HPGp130ポリペプチドモルモット血清が認識するペプチド
次に抗HPGp130ポリペプチドモルモット血清が認識するポリペプチドの解析をウエスタンブロット法で調べた。まず、精製HPGp130ポリペプチド及び前述の鶏血清加鶏肉汁培地中で培養したA型菌221株を2ーメルカプトエタノール処理後にSDS−PAGEを行い、泳動終了後、ゲルをトランスファーバッファー(25mMトリス、192mMグリシン、20%メタノール、pH8.3)に5分間浸し、あらかじめ100%メタノール及びトランスファーバッファーの順に浸しておいたPVDF膜上に重ね、トランス−ブロットSDセル(TRANS−BLOT SD CELL)(バイオ・ラッド製)を用いて7Vで1時間転写を行った。この膜を5%スキムミルクを含むPBSで4℃、一夜マスキングの後、PBS−Tで洗浄し、5%スキムミルクを含むPBS−Tで1,000倍に希釈した抗HPGp130ポリペプチドモルモット血清を室温で2時間反応させた。PBS−Tで洗浄後、5%スキムミルクを含むPBS−Tで2,000倍に希釈したペルオキシダーゼ標識抗モルモットIgG(ザイメット(Zymed)製)を室温で2時間反応させた。さらに、PBS−Tで洗浄後、10ml当たり、3,3’−ジアミノベンジジン四塩酸塩(DAB、同仁化学製)5mg及び過酸化水素水3μlを含む0.1Mトリス塩酸バッファー(pH7.5)に浸し反応させた。その結果、抗HPGp130ポリペプチドモルモット血清はHPGp130ポリペプチド及びその前駆体と考えられる分子量約160Kdのバンドを認識した(図6)。
7)HPGp130ポリペプチドの免疫原性
前記と同様の方法に従い、HPGp130ポリペプチド溶液(約40μg/ml)を同量のフロインドの完全アジュバントで調製したエマルジョン0.5ml(約10μgのHPGp130ポリペプチドを含有する)を10羽の5週齢の白色レグホンSPF鶏脚部皮下に注射し、免疫した。3週間後に、フロインドの不完全アジュバントで上記と同様に調製したエマルジョン0.5mlを脚部皮下に注射した。さらに2週間後に、フロインドの不完全アジュバントで調製した同エマルジョンを脚部皮下に追加投与し、初回免疫後7週目にヘモフィルス・パラガリナルムA型菌221株で攻撃した。他に対照として、水酸化アルミニウムゲル(アルミニウム量換算で0.5mg/ml)を添加した0.25%ホルマリン不活化A型菌221株(不活化前生菌数4×108個/ml)0.5mlを3週間の間隔で2回免疫した群及び非免疫群をおき、同様な攻撃を行った。その結果を表2に示す。HPGp130ポリペプチドあるいはホルマリン不活化菌を免疫した群はいずれも全羽について発症防御が認められた。非免疫群では全羽発症した。
実施例3:ヘモフィルス・パラガリナルムA型菌由来のポリペプチド(A型HMTp210)をコードする遺伝子のクローニング
1)ゲノムライブラリーからのスクリーニング
ヘモフィルス・パラガリナルムA型菌221株を鶏血清加鶏肉汁培地5mlに接種し、37℃で一夜振盪培養した後、遠心分離により菌体を回収した。得られた菌体をPBSで遠心洗浄後、セパジーンキット(三光純薬製)を用い、添付のプロトコールに従って該菌体のDNAを抽出・精製した。これを50μlのTEバッファー(1mM EDTAを含む10mMトリス塩酸バッファー、pH8.0)に溶解してゲノムDNA溶液とした。次に、cDNAラピッド・クローニング・モジュール(rapid cloning module)−λgt11(アマシャム製)を用い、添付のプロトコールに従って、制限酵素EcoRIで消化した該ゲノムDNA0.2μgを、同様に制限酵素EcoRIで処理したλgt11アーム0.5μgに連結させ、さらにλ−DNAイン・ビトロ・パッケージング・モジュール(in vitro packaging module)(アマシャム製)を用い、添付のプロトコールに従って、ラムダファージに導入した。得られたリコンビナントファージ液をゲノムライブラリーとした。
上記ゲノムライブラリー液を、10mM硫酸マグネシウム水溶液に懸濁した大腸菌Y1090株(アマシャム製)約108個に加え、37℃で15分間吸着させた。さらに45℃に加温した重層用LB軟寒天培地(1000ml中、トリプトン10g、酵母エキス5g、塩化ナトリウム10g、アンピシリン50mg、マルトース4g、寒天8gを含む、pH7)を加え、LB寒天培地(1000ml中、トリプトン10g、酵母エキス5g、塩化ナトリウム10g、アンピシリン50mg、寒天15gを含む、pH7)に重層し、42℃で3時間インキュベートした。次に、10mMイソプロピル−β−D−チオガラクトピラノシド(IPTG)水溶液に浸し、風乾したニトロセルロース膜を上記のプレートに重層し、さらに37℃で一夜インキュベートした。ニトロセルロース膜をプレートより剥がし、PBS−Tで洗浄後、5%スキムミルクを含むPBSで室温、2時間マスキングを行った。以後、実施例2の6)と同様の方法に従い、抗HPGp130ポリペプチドモルモット血清、ペルオキシダーゼ標識抗モルモットIgG及び基質を順次反応させた。これらの一連の操作により、ヘモフィルス・パラガリナルムA型菌221株由来の抗HPGp130モルモット血清と特異的に反応する抗原を発現しているプラークを得た。約5,000プラークを上記イムノスクリーニングすることで43個の陽性プラークが得られた。該陽性プラークをSMバッファー(0.1M塩化ナトリウム、10mM硫酸マグネシウム及び0.01%ゼラチンを含む50mMトリス塩酸バッファー、pH7.5)に回収し、クロロホルムを数滴加え、4℃に保存した。回収した陽性プラークのうち10個について、一次スクリーニングと同様な操作で二次、三次スクリーニングを行った。
イムノスクリーニングで陽性となった組換えλgt11ファージを、10mM硫酸マグネシウム水溶液に懸濁した大腸菌Y1090株約108個に加え、37℃で15分間吸着させた。さらに0.4%マルトース、5mM塩化カルシウム及びアンピシリン50μg/mlを含むLB液体培地10mlを加え、37℃で一夜培養した。クロロホルムを数滴加えて溶菌させた後、遠心により未溶菌の大腸菌及びその老廃物等を除去した培養上清5mlに等量の20%ポリエチレングリコール6,000を含む2.5M塩化ナトリウム水溶液を加え、氷中に1時間放置した後、10,000rpmの遠心によりλgt11ファージを沈殿させ、フェノール処理、イソプロパノール沈澱により該ファージDNAを回収した。得られたファージDNA約150μgをEcoRIで消化後、0.8%アガロースゲル電気泳動を行うことにより、ヘモフィルス・パラガリナルムA型菌221株由来のDNA断片を分離し、セファグラス(Sephaglas)TMバンドプレップ・キット(BandPrep Kit)(ファルマシア製)を用い、添付のプロトコールに従って、ゲルから該DNA断片を溶出、回収した。10個の陽性ファージから得られたDNA断片はいずれも約1.2kbであった。そのうちの1個のクローン(クローン2)のファージから得られたDNA断片(以下、HPG1.2k DNAと称する)を以下の試験に用いた。
2)HPG1.2k DNA断片の塩基配列
プラスミドpUC119(宝酒造製)をEcoRIで消化した後、5’末端リン酸をアルカリフォスファターゼ処理により除去し、開裂したpUC119DNAをフェノール・クロロホルム処理、エタノール沈澱により回収した。開裂したpUC119と上記のHPG1.2k DNA断片をDNAライゲーションキットver.2(宝酒造製)を用いて連結し、コンピーテントな大腸菌JM109株(宝酒造製)を形質転換後、50μg/mlのアンピシリンを含むサークルグロウ寒天培地(BIO 101製)で37℃、一夜培養した。寒天培地上に生育したコロニーを50μg/mlのアンピシリンを含むサークルグロウ培地0.5mlに接種し、37℃で5時間培養後、アルカリ法で菌体内のプラスミドを抽出し、EcoRIで消化後、0.8%アガロースゲル電気泳動によってヘモフィルス・パラガリナルムA型菌221株由来の1.2kb DNA断片と同じ長さのDNA断片を含む組換えプラスミドを検出することにより形質転換大腸菌を得た。
得られた形質転換大腸菌を50μg/mlのアンピシリンを含むサークルグロウ培地で培養後、PEG沈澱法によって菌体内の組換えプラスミド(以下、pUA1.2と称する)を回収し、プライマーウォーキング(Primer Walking)法により、HPG1.2k DNA断片の塩基配列をDNAシークエンサー(アプライド・バイオシステムズ377型)を用いて解析した。その結果、1170塩基の配列が決定された。配列番号:1に、後述のA型HMTp210ポリペプチドの塩基配列を示すが、HPG1.2k DNAの塩基配列はこの配列の1988番目から3157番目に相当し、389アミノ酸をコードできること、開始及び終始コドンはこの配列内に存在しないことが明らかになった。対応するアミノ酸配列も示すが、HPGp130ポリペプチドのN末端側アミノ酸配列に相当する配列も認められなかった。従って、HPG1.2k DNAはHPGp130ポリペプチドの一部をコードしていると考えられた。
3)HPG3.5k DNAのクローニング
上記のHPG1.2k DNA断片約0.3μgをDIG−DNA標識キット(ベーリンガーマンハイム製)を用い、添付のプロトコールに従って、ジゴキシゲニン(DIG)で標識した。ヘモフィルス・パラガリナルムA型菌221株ゲノムDNAを数種の制限酵素で切断後、適当量を0.8%アガロースゲル電気泳動にかけ、泳動後にハイボンドN+膜(アマシャム製)にトランスファーした。次に上記のDIG標識HPG1.2k DNAをプローブとして、DIG標識核酸検出キット(ベーリンガーマンハイム製)を用い、添付のプロトコールに従ってサザンハイブリダイゼーションを行い、目的のDNAを検出した。その結果、HindIIIで消化した約3.5kb断片がDIG標識HPG1.2k DNAとハイブリダイズしたことから、この断片を0.8%アガロースゲル電気泳動で各断片から分離し、セファグラスTMバンドプレップ・キットを用い、添付のプロトコールに従って、ゲルからDNA断片を溶出、回収した。
一方、プラスミドpUC119を同じくHindIIIで消化した後、5’末端リン酸をアルカリフォスファターゼ処理により除去し、開裂したpUC119DNAをフェノール・クロロホルム処理、エタノール沈澱により回収した。開裂したpUC119とヘモフィルス・パラガリナルムA型菌221株ゲノム由来の前記HindIII消化物(約3.5kb)をDNAライゲーションキットver.2を用いて連結し、コンピーテントな大腸菌JM109株を形質転換後、50μg/mlのアンピシリンを含むサークルグロウ寒天培地で37℃、一夜培養した。形質転換大腸菌が生育した寒天培地にハイボンドN+膜を載せ、コロニーをリフト後、上記のDIG標識HPG1.2k DNAをプローブとして、常法に従ってコロニーハイブリダイゼーションを行い、DIG標識核酸検出キットを用いて陽性クローンを選別した。
この陽性クローンを50μg/mlのアンピシリンを含むサークルグロウ培地で培養し、PEG沈澱法によって菌体内のプラスミドを回収した。得られた組換えプラスミド(以下、pUA3.5と称する)をHindIIIで消化後、0.8%アガロースゲル電気泳動を行うことにより、ヘモフィルス・パラガリナルムA型菌221株由来の3.5kb DNA断片を分離し、セファグラスTMバンドプレップ・キットを用い、ゲルから該DNA断片(以下、HPG3.5k DNAと称する)を溶出、回収した。なお、組換えプラスミドで形質転換した大腸菌UA3.5JMはFERM BP−6083として、1996年9月5日に工業技術院生命工学工業技術研究所(茨城県つくば市東1丁目1番3号)に出願人により寄託されている。
4)HPG3.5k DNAの発現
発現ベクターpTrcHisC(インビトロジェン製)をHindIIIで消化後、5’末端リン酸をアルカリフォスファターゼ処理により除去し、開裂したpTrcHisCDNAをフェノール・クロロホルム処理、エタノール沈澱により回収した。開裂したpTrcHisCと上記のHPG3.5k DNAをDNAライゲーションキットver.2を用いて連結し、コンピーテントな大腸菌JM109株を形質転換後、50μg/mlのアンピシリンを含むサークルグロウ寒天培地で37℃、一夜培養した。寒天培地上に生育したコロニーを50μg/mlのアンピシリンを含むサークルグロウ培地0.5mlに接種し、37℃で5時間培養後、アルカリ法で菌体内のプラスミドを抽出し、HindIIIで消化後、0.8%アガロースゲル電気泳動によってヘモフィルス・パラガリナルムA型菌221株由来の3.5kb DNA断片と同じ長さのDNA断片を含む組換えプラスミドを検出することにより形質転換大腸菌を得た。
さらに、得られた形質転換大腸菌を50μg/mlのアンピシリンを含むサークルグロウ培地1mlに接種し、37℃で3時間培養した後、IPTG(終濃度1mM)を加え、さらに37℃で3時間培養した。培養液より菌体を遠心で集菌し、PBS50μlに懸濁した。10μlの菌懸濁液と等量の2%SDSを混合し、5分間煮沸後、2μlをニトロセルロース膜にスポットした。ニトロセルロース膜を風乾後、5%スキムミルクを含むPBSで4℃、一夜マスキングを行った。以後、実施例2の6)と同様の方法に従い、抗HPGp130ポリペプチドモルモット血清、ペルオキシダーゼ標識抗モルモットIgG及び基質を順次反応させた。これらの一連の操作により、HPG3.5k DNAが正方向に連結した組換えプラスミドで形質転換された、抗HPGp130モルモット血清と特異的に反応する抗原を発現している大腸菌を得た。
5)HPG3.5k−HISポリペプチドの免疫原性
得られた形質転換大腸菌を50μg/mlのアンピシリンを含むサークルグロウ培地200mlに接種し、37℃で3時間培養した後、IPTG(終濃度1mM)を加え、さらに37℃で3時間培養した。培養液より菌体を遠心で集菌し、PBS10mlに懸濁した。この懸濁液にリゾチームを100μg/mlになるように加え、4℃で1時間反応させた後、超音波処理(ブランソン・ソニファイアー350)を4℃で10分間行い、溶菌させた。遠心により未破砕の菌を除去し、得られた上清を粗HPG3.5k−HISポリペプチドとした。
粗HPG3.5k−HISポリペプチド溶液と同量のフロインドの完全アジュバントを充分混和したエマルジョン0.5mlを10羽の8週齢の白色レグホンSPF鶏脚部皮下に注射し、免疫した。約3週間後に、フロインドの不完全アジュバントで上記と同様に調製したエマルジョン0.5mlを脚部皮下に注射した。さらに2週間後に、フロインドの不完全アジュバントで調製した同エマルジョンを脚部皮下に追加投与し、初回免疫後7週目にヘモフィルス・パラガリナルムA型菌221株で攻撃した。他に対照として、実施例2の7)と同様に、ホルマリン不活化A型菌221株免疫群及び非免疫群をおき、同様な攻撃を行った。その結果を表3に示す。粗HPG3.5k−HISポリペプチド免疫群は10羽中7羽に発症防御が認められた。ホルマリン不活化菌を免疫した群では全羽発症防御し、非免疫群は全羽発症した。
6)HPG3.5k DNA断片の塩基配列
HPG3.5k DNA断片の塩基配列は、前記と同様にDNAシークエンサーにより解析した。その結果、3450塩基の配列が決定された。このHPG3.5k DNA断片の塩基配列は、配列表の配列番号:1に記載の1番目から3450番目の塩基配列に相当する。なお、HPGp130ポリペプチドのN末端側アミノ酸配列と一致するアミノ酸配列をコードする領域を見い出した。HPG3.5k DNAからHPGp130ポリペプチドと同じフレームでオープンリーディングフレームを求めたところ、塩基番号243から翻訳され1069個のアミノ酸をコードすることが明らかとなった。該DNA断片の配列内には終止コドンはなく、HPG3.5k DNAはHPGp130ポリペプチドの一部をコードするDNAと推測された。対応するアミノ酸配列も示す。
7)HPG4.1k DNAのクローニング
上記のHPG3.5k DNA断片を前記と同様にDIGで標識した。次にヘモフィルス・パラガリナルムA型菌221株ゲノムDNAを制限酵素XhoIとXbaIで切断後、実施例3の3)と同様の方法に従い、DIG標識HPG3.5k DNAあるいはDIG標識HPG1.2k DNAをプローブとして、サザンハイブリダイゼーションを行った。その結果、DIG標識HPG3.5k DNAをプローブとした場合、約5.5kb、約4.1kbおよび約1kbのDNAが検出された。また、DIG標識HPG1.2k DNAをプローブとした場合、約4.1kbおよび約1kbのDNAが検出された。図7に示すように、HPG3.5k DNA断片内には、2箇所のXhoI切断部位が存在するため、約5.5kbのDNAは最初のXhoI切断部位より5’側の断片、約4.1kbのDNAは2番目のXhoI切断部位より3’側の断片、そして約1kbのDNAは2箇所のXhoI切断部位にはさまれた断片と考えられた。そこで、約4.1kbの断片を0.8%アガロースゲル電気泳動で各断片から分離、回収した。
次に、図8に示すように、プラスミドpSP72(プロメガ(Promega)製)を同じくXhoIとXbaIで消化し、5’末端を脱リン酸化後、ヘモフィルス・パラガリナルムA型菌221株ゲノム由来の前記XhoI−XbaI消化物(約4.1kb)を連結し、大腸菌JM109株を形質転換した。得られた形質転換大腸菌から、上記のDIG標識HPG3.5k DNAをプローブとして、コロニーハイブリダイゼーションを行い陽性クローンを選別した。
この陽性クローンを50μg/mlのアンピシリンを含むサークルグロウ培地で培養し、PEG沈澱法によって菌体内のプラスミドを回収した。このヘモフィルス・パラガリナルムA型菌221株由来の約4.1kbのXhoI−XbaI消化断片(以下、HPG4.1k DNAと称する)が組み込まれたプラスミド(以下、pSA4.1と称する)をXhoIとKpnIで消化後、0.8%アガロースゲル電気泳動を行うことにより、上記のHPG4.1k DNAにプラスミドpSP72由来のXbaI−KpnI断片が付加された約4.1kbのDNA断片を分離、回収した。
8)HPG4.1k DNAの発現
実施例3の4)と同様の方法に従い、発現ベクターpTrcHisCをXhoIとKpnIで消化し、5’末端を脱リン酸化後、上記の約4.1kbのXhoI−KpnI消化DNA断片を連結し、大腸菌JM109株を形質転換した。得られた形質転換大腸菌の中から、HPG4.1k DNAが正方向に連結した組換えプラスミドで形質転換された、抗HPGp130モルモット血清と特異的に反応する抗原を発現している大腸菌を得た。
9)HPG4.1k−HISポリペプチドの免疫原性
得られた形質転換大腸菌を50μg/mlのアンピシリンを含むサークルグロウ培地200mlに接種し、37℃で3時間培養した後、IPTG(終濃度1mM)を加え、さらに37℃で3時間培養した。培養液より菌体を遠心で集菌し、PBS10mlに懸濁した。この懸濁液にリゾチームを100μg/mlになるように加え、4℃で1時間反応させた後、超音波処理を4℃で10分間行い、溶菌させた。遠心により未破砕の菌を除去し、得られた上清を粗HPG4.1k−HISポリペプチドとした。
粗HPG4.1k−HISポリペプチド溶液と同量のフロインドの完全アジュバントを充分混和したエマルジョン0.5mlを10羽の5週齢の白色レグホンSPF鶏脚部皮下に注射し、免疫した。約3週間後に、フロインドの不完全アジュバントで上記と同様に調製したエマルジョン0.5mlを脚部皮下に注射した。さらに2週間後に、フロインドの不完全アジュバントで調製した同エマルジョンを脚部皮下に追加投与し、初回免疫後7週目にヘモフィルス・パラガリナルムA型菌221株で攻撃した。他に対照として、実施例2の7)と同様に、ホルマリン不活化A型菌221株免疫群及び非免疫群をおき、同様な攻撃を行った。その結果を表4に示す。粗HPG4.1k−HISポリペプチド免疫群は10羽中10羽に発症防御が認められた。ホルマリン不活化菌を免疫した群では全羽発症防御し、非免疫群は全羽発症した。
10)HPG4.1k DNA断片の塩基配列
HPG4.1k DNA断片のHPG3.5k DNA断片とオーバーラップしない部分の塩基配列、すなわち、HindIII切断部位からXbaI切断部位までの塩基配列を、前述と同様に、DNAシークエンサーにより解析した。その結果、2831塩基の配列が決定された。HPG4.1k DNA断片のうち解析した塩基配列は、配列表の配列番号:1に記載の3445番目から6275番目の塩基配列に相当する。なお、該DNA断片の配列内には終止コドンは見い出されなかった。対応するアミノ酸配列も示す。
11)HPG6.7kDNAのクローニング
ヘモフィルス・パラガリナルムA型菌221株ゲノムDNAをXhoIとPstIで切断後、実施例3の3)と同様の方法に従い、前述のDIG標識HPG3.5k DNAあるいはDIG標識HPG1.2k DNAをプローブとして、サザンハイブリダイゼーションを行った。その結果、DIG標識HPG3.5k DNAをプローブとした場合、約9.4kb、約6.7kbおよび約1kbのDNAが検出された。また、DIG標識HPG1.2k DNAをプローブとした場合、約6.7kbおよび約1kbのDNAが検出された。前述のように、HPG3.5k DNA断片内には、2箇所のXhoI切断部位が存在するため、約9.4kbのDNAは最初のXhoI切断部位より5’側の断片、約6.7kbのDNAは2番目のXhoI切断部位より3’側の断片、そして約1kbのDNAは2箇所のXhoI切断部位にはさまれた断片と考えられた。そこで、約6.7kbの断片を0.8%アガロースゲル電気泳動で各断片から分離、回収した。
次に、図9に示すように、プラスミドpSP72を同じくXhoIとPstIで消化し、5’末端を脱リン酸化後、ヘモフィルス・パラガリナルムA型菌221株ゲノム由来の前記XhoI−PstI消化物(約6.7kb)を連結し、大腸菌JM109株を形質転換した。得られた形質転換大腸菌から、上記のDIG標識HPG3.5k DNAをプローブとして、コロニーハイブリダイゼーションを行い、陽性クローンを選別した。
この陽性クローンを50μg/mlのアンピシリンを含むサークルグロウ培地で培養し、PEG沈澱法によって菌体内のプラスミドを回収した。得られた組換えプラスミドを以下、pSA6.7と称する。なお、組換えプラスミドで形質転換した大腸菌SA6.7JMはBP−6081として、1997年8月27日に工業技術院生命工学工業技術研究所(茨城県つくば市東1丁目1番3号)に出願人により寄託されている。
12)HPG2.7kDNAのクローニング
得られた組み換えプラスミド(pSA6.7)に組み込まれた約6.7kbのDNA断片(以下、HPG6.7k DNAと称する)は、前述のHPG4.1k DNA断片を含むことから、HPG6.7k DNAからHPG4.1k DNA断片を除いた約2.7kbの断片(以下、HPG2.7k DNAと称する)のサブクローニングを行った。pSA6.7をXbaIで消化後、0.8%アガロースゲル電気泳動を行うことにより、上記のHPG2.7k DNA断片にプラスミドpSP72由来のPstI−XbaI断片が付加された約2.7kbのDNA断片を分離、回収した。
次に、プラスミドpSP72を同じくXbaIで消化し、5’末端を脱リン酸化後、上記の約2.7kbのXbaI消化DNA断片を連結し、大腸菌JM109株を形質転換した。さらに、得られた形質転換大病菌を50μg/mlのアンピシリンを含むサークルグロウ培地で培養し、PEG沈澱法によって菌体内のプラスミドを回収した。得られた組換えプラスミドを以下、pSA2.7と称する。
13)HPG2.7k DNA断片の塩基配列
HPG2.7k DNA断片の塩基配列は、前記と同様にDNAシークエンサーにより解析した。その結果、2661塩基の配列が決定された。このHPG2.7k DNA断片の塩基配列は、配列表の配列番号:1に記載の6270番目から8930番目の塩基配列に相当する。また、該DNA断片の配列内には終止コドンが見い出された。対応するアミノ酸配列も示す。
配列表の配列番号:1に記載の塩基配列は、全長8930塩基からなる塩基配列であり、その中に塩基番号243から翻訳され2042個のアミノ酸をコードできるオープンリーディングフレームが存在することが明らかとなった。この2042個のアミノ酸からなるポリペプチドを以下A型HMTp210と称する。既存のデータベース(GeneBank及びEMBL)とのホモロジー検索を行ったところ、既知の塩基配列あるいはアミノ酸配列とのホモロジーが認められなかったことから、A型HMTp210ポリペプチドは新規物質と考えられた。
また、配列表の配列番号:1に記載の塩基配列の中に塩基番号8375から翻訳され185個のアミノ酸をコードできるオープンリーディングフレームの存在の可能性が示された。なお、この配列内に終止コドンは見い出されなかった。既存のデータベース(GeneBank及びEMBL)とのホモロジー検索を行ったところ、既知の塩基配列あるいはアミノ酸配列とのホモロジーが認められなかったことから、このオープンリーディングフレームがコードするポリペプチドも新規物質と考えられた。
実施例4:HPG1.2k DNAとハイブリダイズするDNA断片のヘモフィルス・パラガリナルム221株以外からの検索
実施例3の1)と同様の方法に従い、A型菌の221株、083株、W株、Germany株及びGeorgia株、B型菌のSpross株及び0222株、C型菌のModesto株及び53−47株の計9株からゲノムDNAを調製した。調製したゲノムDNAを制限酵素EcoRIで切断後、実施例3の3)と同様の方法に従い、DIG標識HPG1.2k DNAをプローブとして、サザンハイブリダイゼーションを行った。その結果、血清型によってサイズが異なるものの、いずれの株にもHPG1.2k DNAとハイブリダイズする断片が検出された(図10)。
実施例5:ヘモフィルス・パラガリナルムC型菌由来のポリペプチド(C型HMTp210)をコードする遺伝子のクローニング
1)ゲノムライブラリーからのスクリーニング
実施例3の1)と同様の方法に従い、C型菌53−47株のゲノムライブラリーを作製した。すなわち、制限酵素HindIIIで消化したC型菌53−47株のゲノムDNAを、cDNAラピッド・クローニング・モジュール−λgt11を用い、同様に制限酵素HindIIIで処理したλDASHII(ストラタジーン(STRATAGENE)製)アームに連結させ、さらにλ−DNAイン・ビトロ・パッケージング・モジュールを用い、ラムダファージに導入した。得られたリコンビナントファージ液をゲノムライブラリーとした。
上記ゲノムライブラリー液を、10mM硫酸マグネシウム水溶液に懸濁した大腸菌XL1−Blue MRA(P2)株(ストラタジーン製)約108個に加え、37℃で15分間吸着させた。さらに45℃に加温した重層用LB軟アガロース培地(1000ml中、トリプトン10g、酵母エキス5g、塩化ナトリウム10g、アンピシリン50mg、マルトース4g、アガロース8gを含む、pH7)を加え、LB寒天培地に重層し、37℃で一夜培養した。大腸菌が生育した寒天培地にハイボンドN+膜を載せ、ファージプラークをリフト後、前述のDIG標識A型HPG3.5k DNAをプローブとして、常法に従ってプラークハイブリダイゼーションを行い、陽性クローンを選別した。約1,000プラークを上記イムノスクリーニングすることで37個の陽性プラークが得られた。得られた陽性プラークのうち10個について、一次スクリーニングと同様な操作で二次、三次スクリーニングを行った。
プラークハイブリダイゼーションで陽性となった組換えλDASHIIファージを、10mM硫酸マグネシウム水溶液に懸濁した大腸菌XL1−Blue MRA株(ストラタジーン製)約108個に加え、37℃で15分間吸着させた。実施例3の1)と同様の方法に従い、該ファージDNAを回収した。得られたファージDNAをHindIIIで消化後、0.8%アガロースゲル電気泳動を行うことにより、ヘモフィルス・パラガリナルムC型菌53−47株由来のDNA断片を分離、回収した。10個の陽性ファージから得られたDNA断片はいずれも約13.5kbであった。そのうちの1個のクローン(クローン1)のファージから得られたDNA断片(以下、HPG−C1 DNAと称する)を以下の試験に用いた。
2)HPG−C1 DNAの断片化及びサブクローニング
HPG−C1 DNAは約13.5Kbとかなり大きく、そのままではプラスミドベクターにサブクローニングするのは困難であることから、HPG−C1 DNAを数種の制限酵素で切断後、適当量を0.8%アガロースゲル電気泳動にかけたところ、XbaIで消化した場合に、約6.9kb、約5.6kb及び約0.9kbのDNAを検出した。
プラスミドpUC119をHindIIIとXbaIで消化し、5’末端を脱リン酸化後、上記のHPG−C1 DNAのXbaI消化物を連結し、大腸菌JM109株を形質転換した。さらに、約5.6kbあるいは約0.9kb DNA断片を含む組換えプラスミドで形質転換された大腸菌を培養し、PEG沈澱法によって菌体内のプラスミドを回収した。得られた組換えプラスミド(約5.6kbあるいは約0.9kb DNA断片を含む組換えプラスミドをそれぞれ以下、pU−C2、pU−C3と称する)をHindIII−XbaIで消化後、0.8%アガロースゲル電気泳動を行うことにより、約5.6kb及び約0.9kbのDNA断片(以下、HPG−C2 DNA及びHPG−C3 DNAと称する)をそれぞれ分離、回収した。なお、組換えプラスミドpU−C2で形質転換した大腸菌U−C2JMはBP−6082として、1997年8月27日に工業技術院生命工学工業技術研究所(茨城県つくば市東1丁目1番3号)に出願人により寄託されている。
また、プラスミドpUC119をXbaIで消化し5’末端を脱リン酸化後、前述のHPG−C1 DNAのXbaI消化物を連結し、大腸菌JM109株を形質転換した。さらに、約6.9kb DNA断片を含む組換えプラスミドで形質転換された大腸菌を培養し、PEG沈澱法によって菌体内のプラスミドを回収した。得られた組換えプラスミド(以下、pU−C4と称する)をXbaIで消化後、0.8%アガロースゲル電気泳動を行うことにより、約6.9kbのDNA断片(以下、HPG−C4 DNAと称する)を分離、回収した。尚、組換えプラスミドpU−C4で形質転換した大腸菌U−C4JMはBP−6080として、1997年8月27日に工業技術院生命工学工業技術研究所(茨城県つくば市東1丁目1番3号)に出願人により寄託されている。
得られたDNA断片HPG−C2、HPG−C3およびHPG−C4をそれぞれハイボンドN+膜にスポットした。次に前述のDIG標識HPG3.5k DNAあるいは実施例3の3)と同様にDIGで標識したHPG4.1k DNA、HPG2.7k DNAをプローブとして、ドットハイブリダイゼーションを行った。DIG標識HPG3.5k DNAあるいはHPG4.1k DNAをプローブとした場合、HPG−C4 DNAを検出した。また、DIG標識HPG2.7k DNAをプローブとした場合、HPG−C2 DNAを検出した。このことから、図11に示すように、5’側からHPG−C3、HPG−C4、HPG−C2の順番に並んでおり、ポリペプチドをコードしている部分は、主にHPG−C4にあると考えられた。
3)HPG−C4 DNA断片の塩基配列
HPG−C4 DNA断片の塩基配列は、前記と同様にDNAシークエンサーにより解析した。その結果、6871塩基の配列が決定された。このHPG−C4 DNA断片の塩基配列は、配列表の配列番号:5に記載の1番目から6871番目の塩基配列に相当する。なお、A型HMTp210をコードする遺伝子と相同性が高いことが見い出されたことから、HPG−C4 DNAからA型HMTp210をコードする遺伝子と同じフレームでオープンリーディングフレームを求めたところ、塩基番号848から翻訳され2008個のアミノ酸をコードすることが明らかとなった。しかしながら、該DNA断片の配列内には終止コドンは見い出されなかった。対応するアミノ酸配列も示す。
4)HPG−C2 DNA断片の一部の塩基配列
HPG−C4 DNA断片の配列内には終止コドンが見い出されなかったことから、HPG−C4 DNA断片より3’側のHPG−C2 DNA断片の5’側の部分の塩基配列の解析を行った。図11に示すように、HPG−C2 DNA断片に3箇所のAccI切断部位が存在し、クローニング部位であるXbaI切断部位から最初のAccI切断部位までのサイズが約0.6Kbであることがアガロースゲル電気泳動により判明したことから、この約0.6Kbの塩基配列を、前記と同様にDNAシークエンサーにより解析した。その結果、621塩基の配列が決定された。このHPG−C2 DNA断片の一部の塩基配列は、配列表の配列番号:5に記載の6866番目から7486番目の塩基配列に相当する。また、このHPG−C2 DNA断片の一部の配列内に終止コドンが見い出された。対応するアミノ酸配列も示す。
配列表の配列番号:5に記載の塩基配列は、全長7486塩基からなる塩基配列であり、その中に塩基番号848から翻訳され2039個のアミノ酸をコードできるオープンリーディングフレームが存在することが明らかとなった。この2039個のアミノ酸からなるポリペプチドを以下、C型HMTp210と称する。既存のデータベース(GeneBank及びEMBL)とのホモロジー検索を行ったところ、既知の塩基配列あるいはアミノ酸配列とのホモロジーが認められなかったことから、C型HMTp210ポリペプチドは新規物質と考えられた。
また、C型HMTp210ポリペプチドをコードする塩基配列とA型HMTp210ポリペプチドをコードする塩基配列のホモロジーを調べたところ、約80%のホモロジーがあること、さらに、5’側の約3.4kbの領域と3’側の約1.2kbの領域が非常にホモロジーが高いこと、2つの領域にはさまれた約1.5kbの領域はホモロジーが低いことが明らかとなった。また、これらの遺伝子にコードされるポリペプチドについても、同様のことが認められた。
実施例6:A型菌、B型菌及びC型菌由来ゲノムDNAからのHMTp210遺伝子のPCR増幅
実施例3の1)と同様の方法に従い、A型菌の221株、083株、W株、Germany株及びGeorgia株、B型菌のSpross株及び0222株、C型菌のModesto株及び53−47株の計9株からゲノムDNAを調製した。また、A型HMTp210ポリペプチドをコードする塩基配列をもとに、上流側のPCRプライマーとして配列番号:3に記載の塩基配列を有する合成DNAを、下流側のPCRプライマーとして配列番号:4に記載の塩基配列を有する合成DNAを作製した。これらのプライマーは、それぞれ5’末端にBamHI認識配列を付加させ、また、A型HMTp210ポリペプチドの翻訳領域の全長を増幅できるようにデザインした。これらのプライマーを用いて、上記の調製したゲノムDNAを鋳型としてPCRを行った。PCR反応はLA PCRキットver.2(宝酒造製)を用い以下の条件、すなわち、94℃で1分間の反応の後、98℃で40秒間、60℃で10分間の反応を30サイクル行い、72℃で10分間反応させた。得られたPCR産物を0.8%アガロースゲル電気泳動で分析したところ、いずれの株にも約6.1Kbのサイズの増幅フラグメントが認められた(図12)。
実施例7:完全長のA型及びC型HMTp210ポリペプチドの発現
1)A型HMTp210ポリペプチドの発現
ヘモフィルス・パラガリナルムA型菌221株ゲノムDNAを鋳型として、実施例6で得られたPCR産物をBamHIで消化し、0.8%アガロースゲル電気泳動で分離後、約6.1Kbの増幅フラグメントを、セファグラスTMバンドプレップ・キットを用い溶出、回収した。
プラスミドpUC119をBamHIで消化し、5’末端を脱リン酸化後、上記の約6.1kbの増幅フラグメントを連結し、大腸菌JM109株を形質転換した。さらに、約6.1kb DNA断片を含む組換えプラスミドで形質転換された大腸菌を培養し、PEG沈澱法によって菌体内のプラスミドを回収した。得られた組換えプラスミド(以下、pU−AP1と称する)をBamHIで消化後、0.8%アガロースゲル電気泳動を行うことにより、約6.1kb DNA断片(以下、HPG−AP1 DNAと称する)を分離、回収した。
実施例3の4)と同様の方法に従い、発現ベクターpTrcHisA(インビトロジェン製)をBamHIで消化し、5’末端を脱リン酸化後、上記のHPG−AP1 DNAを連結し、大腸菌JM109株を形質転換した。得られた形質転換大腸菌の中から、HPG−AP1 DNAが正方向に連結した組換えプラスミドで形質転換された、抗HPGp130モルモット血清と特異的に反応する抗原を発現している大腸菌を得た。
2)C型HMTp210ポリペプチドの発現
ヘモフィルス・パラガリナルムC型菌53−47株ゲノムDNAを鋳型として、実施例6で得られたPCR産物をBamHIで消化し、0.8%アガロースゲル電気泳動で分離後、約6.1Kbの増幅フラグメントを回収した。
プラスミドpUC119をBamHIで消化し、5’末端を脱リン酸化後、上記の約6.1kbの増幅フラグメントを連結し、大腸菌JM109株を形質転換した。さらに、約6.1kb DNA断片を含む組換えプラスミドで形質転換された大腸菌を培養し、PEG沈澱法によって菌体内のプラスミドを回収した。得られた組換えプラスミド(以下、pU−CP1と称する)をBamHIで消化後、0.8%アガロースゲル電気泳動を行うことにより、約6.1kb DNA断片(以下、HPG−CP1 DNAと称する)を分離、回収した。
実施例3の4)と同様の方法に従い、発現ベクターpTrcHisAをBamHIで消化し、5’末端を脱リン酸化後、上記のHPG−CP1 DNAを連結し、大腸菌JM109株を形質転換した。得られた形質転換大腸菌の中から、HPG−CP1 DNAが正方向に連結した組換えプラスミドで形質転換された、抗HPGp130モルモット血清と特異的に反応する抗原を発現している大腸菌を得た。
配列表
配列番号:1
配列の長さ:8930
配列の型:核酸
鎖の数:2本鎖
トポロジー:直鎖状
配列の種類:genomic DNA
起源:ヘモフィルス・パラガリナルムA型菌221株
配列
配列番号:2
配列の長さ:13
配列の型:アミノ酸
鎖の数:1本鎖
トポロジー:直鎖状
配列の種類:ペプチド
起源:ヘモフィルス・パラガリナルムA型菌221株
配列
配列番号:3
配列の長さ:43
配列の型:核酸
鎖の数:1本鎖
トポロジー:直鎖状
配列の種類:他の核酸(合成DNA)
配列
配列番号:4
配列の長さ:39
配列の型:核酸
鎖の数:1本鎖
トポロジー:直鎖状
配列の種類:他の核酸(合成DNA)
配列
配列番号:5
配列の長さ:7486
配列の型:核酸
鎖の数:2本鎖
トポロジー:直鎖状
配列の種類:genomic DNA
起源:ヘモフィルス・パラガリナルムC型菌53−47株
配列
Claims (23)
- 配列表の配列番号:1で示されるアミノ酸配列からなることを特徴とするポリペプチド。
- 配列表の配列番号:1で示される塩基配列の1番目から3450番目の塩基配列からなるDNAによりコードされることを特徴とするポリペプチド。
- 配列表の配列番号:1で示される塩基配列の2212番目から6275番目の塩基配列からなるDNAによりコードされることを特徴とするポリペプチド。
- 配列表の配列番号:1で示されるアミノ酸配列からなるポリペプチドの一部であって、N末端のアミノ酸配列がアミノ酸配列の1番目から始まり、分子量が130kDaであるポリペプチド。
- ヘモフィルス・パラガリナルムA型菌由来のポリペプチドであって、赤血球凝集抑制抗体を誘導し及び/又は鶏伝染性コリーザを阻止する、請求項1ないし4のいずれかに記載のポリペプチド。
- 請求項5に記載のポリペプチドのアミノ酸配列において1もしくは数個のアミノ酸が欠失、付加、あるいは置換されたアミノ酸配列からなり、赤血球凝集抑制抗体を誘導し及び/又は鶏伝染性コリーザを阻止することを特徴とするポリペプチド。
- 該ポリペプチドが遺伝子組換え技術により得られる組換え型ポリペプチドであることを特徴とする請求項1ないし6のいずれかに記載のポリペプチド。
- 請求項1ないし7のいずれかに記載のポリペプチドをコードする塩基配列からなることを特徴とするDNA。
- 配列表の配列番号:1に記載の塩基配列からなるDNA。
- 配列表の配列番号:1に記載の塩基配列に相補的な塩基配列からなるDNAとストリンジェントな条件下でハイブリダイズするDNAであって、該DNAによってコードされるポリペプチドが赤血球凝集抑制抗体を誘導し及び/又は鶏伝染性コリーザを阻止することを特徴とするDNA。
- 配列表の配列番号:1で示される塩基配列の2212番目から6275番目の塩基配列からなるDNA断片(HPG4.1k DNA断片)又は配列表の配列番号:1で示される塩基配列の1番目から3450番目の塩基配列からなるDNA断片(HPG3.5k DNA断片)である、請求項10に記載のDNA。
- 請求項8ないし11のいずれかに記載のDNAを含むことを特徴とする組換えDNA分子。
- 組換えDNA分子のベクターがプラスミド、ウイルスベクター及びコスミドよりなる群から選ばれる請求項12に記載の組換えDNA分子。
- 請求項8ないし11のいずれかに記載のDNA又は請求項12もしくは13に記載の組換えDNA分子で形質転換した形質転換体。
- 形質転換体が、細菌、酵母、昆虫細胞、動物細胞及び植物細胞よりなる群から選ばれる宿主である請求項14に記載の形質転換体。
- 請求項1ないし7のいずれかに記載のポリペプチドを認識することを特徴とする抗体。
- モノクローナル抗体である請求項16に記載の抗体。
- ポリクローナル抗体である請求項16に記載の抗体。
- 請求項14もしくは15に記載の形質転換体を培養し、該形質転換体に請求項1ないし7のいずれかに記載のポリペプチドを産生させ、ついで該ポリペプチドを精製することを特徴とする、請求項1ないし7のいずれかに記載のポリペプチドの製造方法。
- 請求項1ないし7のいずれかに記載のポリペプチドを主成分とする鶏伝染性コリーザのワクチン。
- 請求項14もしくは15に記載の形質転換体を主成分とする鶏伝染性コリーザのワクチン。
- 請求項1ないし7のいずれかに記載のポリペプチド、請求項8ないし11のいずれかに記載のDNA、請求項12もしくは13に記載の組換えDNA分子、請求項14もしくは15に記載の形質転換体又は請求項16ないし18のいずれかに記載の抗体を用いることを特徴とするヘモフィルス・パラガリナルムの検出方法。
- 請求項1ないし7のいずれかに記載のポリペプチド、請求項14もしくは15に記載の形質転換体又は請求項16ないし18のいずれかに記載の抗体を用いることを特徴とするヘモフィルス・パラガリナルムに対する抗体の検出方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP8-271408 | 1996-09-19 | ||
| JP8271408A JPH1084969A (ja) | 1996-09-19 | 1996-09-19 | ヘモフィルス・パラガリナルム由来新規ポリペプチド及びその製法 |
| PCT/JP1997/003222 WO1998012331A1 (en) | 1996-09-19 | 1997-09-12 | Novel polypeptide originating in hemophilus paragallinarum and process for producing the same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO1998012331A1 JPWO1998012331A1 (ja) | 1999-02-09 |
| JP4219987B2 true JP4219987B2 (ja) | 2009-02-04 |
Family
ID=17499641
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP8271408A Pending JPH1084969A (ja) | 1996-09-19 | 1996-09-19 | ヘモフィルス・パラガリナルム由来新規ポリペプチド及びその製法 |
| JP51449998A Expired - Lifetime JP4219987B2 (ja) | 1996-09-19 | 1997-09-12 | ヘモフィルス・パラガリナルム由来新規ポリペプチド及びその製法 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP8271408A Pending JPH1084969A (ja) | 1996-09-19 | 1996-09-19 | ヘモフィルス・パラガリナルム由来新規ポリペプチド及びその製法 |
Country Status (13)
| Country | Link |
|---|---|
| US (2) | US6544519B1 (ja) |
| EP (1) | EP0870828B1 (ja) |
| JP (2) | JPH1084969A (ja) |
| KR (1) | KR100584904B1 (ja) |
| CN (1) | CN1149288C (ja) |
| AU (1) | AU702080B2 (ja) |
| BR (1) | BR9706813B1 (ja) |
| CA (1) | CA2236165A1 (ja) |
| DE (1) | DE69734761T2 (ja) |
| ES (1) | ES2253784T3 (ja) |
| ID (1) | ID20029A (ja) |
| TR (1) | TR199800898T2 (ja) |
| WO (1) | WO1998012331A1 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101521123B1 (ko) | 2006-05-28 | 2015-05-19 | 시플라 메드프로 리서치 앤드 디벨롭먼트 (피티와이) 엘티디 | 프로바이오틱 스트레인 및 그로부터 유도된 항균 펩티드 |
| CN102007414B (zh) * | 2008-02-08 | 2015-06-17 | 一般财团法人化学及血清疗法研究所 | 副鸡禽杆菌抗体的检测方法和试剂盒 |
| WO2010047347A1 (ja) | 2008-10-21 | 2010-04-29 | 財団法人化学及血清療法研究所 | 封入体形成タンパク質の製造方法 |
| JP5568017B2 (ja) * | 2008-12-25 | 2014-08-06 | 一般財団法人化学及血清療法研究所 | 組換え鶏伝染性コリーザワクチン及びその製造方法 |
| AU2012298125B2 (en) | 2011-08-19 | 2015-09-24 | Immortal Spirit Limited | Antibody and antibody-containing composition |
| CN105198991A (zh) * | 2015-10-16 | 2015-12-30 | 天津瑞普生物技术股份有限公司 | 一种鸡传染性鼻炎单克隆抗体制备方法 |
| CN110540579B (zh) * | 2018-05-29 | 2022-09-06 | 普莱柯生物工程股份有限公司 | 一种副鸡禽杆菌抗原蛋白、含有副鸡禽杆菌抗原的疫苗组合物、及其制备方法和应用 |
| CN115960185B (zh) * | 2023-01-13 | 2026-03-17 | 乾元浩生物股份有限公司 | 一种c型鸡传染性鼻炎亚单位疫苗及其制备方法与应用 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS54113422A (en) * | 1978-02-22 | 1979-09-05 | Shionogi & Co Ltd | Hemagglutinin of haemophilus gallinarum |
| JPS56115724A (en) * | 1979-07-30 | 1981-09-11 | Ajinomoto Co Inc | Prophilaxis and remedy for avian infectious coryza |
| JPS5645416A (en) * | 1979-09-21 | 1981-04-25 | Shionogi & Co Ltd | Inactivated vaccine for respiratory disease of chicken |
| US4746613A (en) * | 1984-03-02 | 1988-05-24 | Wichmann Robert W | Poultry diseases bacterin preparation |
| JPS64467A (en) * | 1987-11-20 | 1989-01-05 | Kitasato Inst:The | Measuring system using hemagglutinin of agglutinin deficient strain to fresh red blood cells of haemophilus paragallinarum |
| JP2779447B2 (ja) * | 1988-03-20 | 1998-07-23 | 財団法人阪大微生物病研究会 | 弱毒マレック病ウイルス・ベクターを用いる組換え遺伝子作成法、及び該ウイルスの組換え体 |
| US5196514A (en) * | 1990-03-06 | 1993-03-23 | The University Of Georgia Research Foundation, Inc. | Method of detecting mycoplasma infection in poultry and compositions therefor |
| IL99097A0 (en) * | 1990-09-05 | 1992-07-15 | Akzo Nv | Haemophilus paragallinarum vaccine |
| JP2913229B2 (ja) * | 1991-10-21 | 1999-06-28 | 塩野義製薬株式会社 | 油性アジュバントワクチン製剤 |
| JPH0827028A (ja) * | 1994-07-21 | 1996-01-30 | Nippon Seibutsu Kagaku Kenkyusho | 油性アジュバント及びアルミニウムゲルアジュバントからなる動物用ワクチン製剤 |
| JP3844501B2 (ja) * | 1995-02-08 | 2006-11-15 | タカラバイオ株式会社 | 癌の制御 |
-
1996
- 1996-09-19 JP JP8271408A patent/JPH1084969A/ja active Pending
-
1997
- 1997-09-12 CA CA002236165A patent/CA2236165A1/en not_active Abandoned
- 1997-09-12 DE DE69734761T patent/DE69734761T2/de not_active Expired - Lifetime
- 1997-09-12 AU AU42200/97A patent/AU702080B2/en not_active Ceased
- 1997-09-12 EP EP97940361A patent/EP0870828B1/en not_active Expired - Lifetime
- 1997-09-12 BR BRPI9706813-6A patent/BR9706813B1/pt not_active IP Right Cessation
- 1997-09-12 TR TR1998/00898T patent/TR199800898T2/xx unknown
- 1997-09-12 ES ES97940361T patent/ES2253784T3/es not_active Expired - Lifetime
- 1997-09-12 KR KR1019980703683A patent/KR100584904B1/ko not_active Expired - Lifetime
- 1997-09-12 JP JP51449998A patent/JP4219987B2/ja not_active Expired - Lifetime
- 1997-09-12 ID IDW980010D patent/ID20029A/id unknown
- 1997-09-12 WO PCT/JP1997/003222 patent/WO1998012331A1/ja not_active Ceased
- 1997-09-12 CN CNB971916985A patent/CN1149288C/zh not_active Expired - Lifetime
- 1997-09-17 US US09/077,098 patent/US6544519B1/en not_active Expired - Fee Related
-
2002
- 2002-07-11 US US10/192,584 patent/US6919080B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| AU702080B2 (en) | 1999-02-11 |
| DE69734761T2 (de) | 2006-09-07 |
| TR199800898T2 (xx) | 1999-10-21 |
| CN1149288C (zh) | 2004-05-12 |
| BR9706813B1 (pt) | 2010-06-29 |
| EP0870828B1 (en) | 2005-11-30 |
| WO1998012331A1 (en) | 1998-03-26 |
| EP0870828A1 (en) | 1998-10-14 |
| JPH1084969A (ja) | 1998-04-07 |
| AU4220097A (en) | 1998-04-14 |
| EP0870828A4 (en) | 2002-08-14 |
| ES2253784T3 (es) | 2006-06-01 |
| US6544519B1 (en) | 2003-04-08 |
| DE69734761D1 (de) | 2006-01-05 |
| KR19990067655A (ko) | 1999-08-25 |
| ID20029A (id) | 1998-09-10 |
| US20030027987A1 (en) | 2003-02-06 |
| US6919080B2 (en) | 2005-07-19 |
| BR9706813A (pt) | 1999-07-20 |
| KR100584904B1 (ko) | 2006-11-30 |
| CA2236165A1 (en) | 1998-03-26 |
| CN1208436A (zh) | 1999-02-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4271231B2 (ja) | 髄膜炎菌(Neisseriameningitidis)のプロテイナーゼK抵抗性表面蛋白質 | |
| EA006232B1 (ru) | Стрептококковые антигены | |
| KR19990022742A (ko) | 스트렙토코커스 속 유래의 hsp70 계열의 쇼크 단백질 | |
| JP4219987B2 (ja) | ヘモフィルス・パラガリナルム由来新規ポリペプチド及びその製法 | |
| JP3072345B1 (ja) | 豚丹毒菌の組換えサブユニットワクチン | |
| JP3236610B2 (ja) | 豚胸膜肺炎用ワクチン | |
| US20090246228A1 (en) | Moraxella catarrhalis Proteins | |
| KR0170752B1 (ko) | 혈호균속 인플루엔자용 백신과 진단검사법 | |
| JPWO1998012331A1 (ja) | ヘモフィルス・パラガリナルム由来新規ポリペプチド及びその製法 | |
| JP3990730B2 (ja) | マラセチア由来の抗原性蛋白質 | |
| EP0694560A2 (en) | Production of antigens of Pasteurella | |
| MXPA98003979A (en) | Novel polypeptide originating in hemophilus paragallinarum | |
| JP2004057078A (ja) | ヘモフィルス・パラガリナルム由来新規ポリペプチドとその遺伝子及び製法 | |
| JPH04502902A (ja) | 魚の出血性敗血症ウィルスの組換え型ポリペプチド | |
| JP2005230015A (ja) | クラミジア・ニューモニエの抗原ポリペプチド | |
| WO1997044464A1 (en) | Helicobacter pylori acid inhibitory factor 1 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20040309 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20060801 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060929 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20070206 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070320 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20081028 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20081113 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111121 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111121 Year of fee payment: 3 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111121 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121121 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121121 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131121 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313532 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |