JP4183288B2 - 微生物を検出するためのセンサー器具、及びそのための方法 - Google Patents
微生物を検出するためのセンサー器具、及びそのための方法 Download PDFInfo
- Publication number
- JP4183288B2 JP4183288B2 JP53172799A JP53172799A JP4183288B2 JP 4183288 B2 JP4183288 B2 JP 4183288B2 JP 53172799 A JP53172799 A JP 53172799A JP 53172799 A JP53172799 A JP 53172799A JP 4183288 B2 JP4183288 B2 JP 4183288B2
- Authority
- JP
- Japan
- Prior art keywords
- layer
- sensor
- sample
- indicator
- microorganisms
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 244000005700 microbiome Species 0.000 title claims description 46
- 238000000034 method Methods 0.000 title description 6
- 238000012360 testing method Methods 0.000 claims description 14
- 230000008859 change Effects 0.000 claims description 13
- 238000001514 detection method Methods 0.000 claims description 12
- 230000003100 immobilizing effect Effects 0.000 claims description 2
- 238000011179 visual inspection Methods 0.000 claims description 2
- 239000010410 layer Substances 0.000 description 122
- 239000011159 matrix material Substances 0.000 description 35
- 230000000813 microbial effect Effects 0.000 description 31
- 239000000499 gel Substances 0.000 description 24
- 239000007789 gas Substances 0.000 description 23
- 229920001296 polysiloxane Polymers 0.000 description 20
- 238000007789 sealing Methods 0.000 description 16
- 239000000243 solution Substances 0.000 description 16
- 239000007788 liquid Substances 0.000 description 15
- 239000000463 material Substances 0.000 description 15
- 239000002609 medium Substances 0.000 description 13
- 229920000642 polymer Polymers 0.000 description 13
- 230000003750 conditioning effect Effects 0.000 description 11
- 239000003349 gelling agent Substances 0.000 description 11
- 239000000049 pigment Substances 0.000 description 11
- 239000012528 membrane Substances 0.000 description 10
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 9
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 9
- 229910002092 carbon dioxide Inorganic materials 0.000 description 9
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 8
- 239000007793 ph indicator Substances 0.000 description 8
- 108090000790 Enzymes Proteins 0.000 description 7
- 102000004190 Enzymes Human genes 0.000 description 7
- 239000012790 adhesive layer Substances 0.000 description 7
- 229940088598 enzyme Drugs 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- CPBJMKMKNCRKQB-UHFFFAOYSA-N 3,3-bis(4-hydroxy-3-methylphenyl)-2-benzofuran-1-one Chemical compound C1=C(O)C(C)=CC(C2(C3=CC=CC=C3C(=O)O2)C=2C=C(C)C(O)=CC=2)=C1 CPBJMKMKNCRKQB-UHFFFAOYSA-N 0.000 description 6
- 239000001913 cellulose Substances 0.000 description 6
- 229920002678 cellulose Polymers 0.000 description 6
- 239000001963 growth medium Substances 0.000 description 6
- 238000011534 incubation Methods 0.000 description 6
- KJFMBFZCATUALV-UHFFFAOYSA-N phenolphthalein Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)C2=CC=CC=C2C(=O)O1 KJFMBFZCATUALV-UHFFFAOYSA-N 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 239000002250 absorbent Substances 0.000 description 5
- 230000002745 absorbent Effects 0.000 description 5
- 210000004369 blood Anatomy 0.000 description 5
- 239000008280 blood Substances 0.000 description 5
- 235000015097 nutrients Nutrition 0.000 description 5
- 239000000843 powder Substances 0.000 description 5
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 4
- 230000002378 acidificating effect Effects 0.000 description 4
- 230000002411 adverse Effects 0.000 description 4
- 239000012298 atmosphere Substances 0.000 description 4
- 230000003115 biocidal effect Effects 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 230000002209 hydrophobic effect Effects 0.000 description 4
- 230000007269 microbial metabolism Effects 0.000 description 4
- PRZSXZWFJHEZBJ-UHFFFAOYSA-N thymol blue Chemical compound C1=C(O)C(C(C)C)=CC(C2(C3=CC=CC=C3S(=O)(=O)O2)C=2C(=CC(O)=C(C(C)C)C=2)C)=C1C PRZSXZWFJHEZBJ-UHFFFAOYSA-N 0.000 description 4
- 239000012463 white pigment Substances 0.000 description 4
- MGUKYHHAGPFJMC-UHFFFAOYSA-N 4-[3-(4-hydroxy-2,5-dimethylphenyl)-1,1-dioxo-2,1$l^{6}-benzoxathiol-3-yl]-2,5-dimethylphenol Chemical compound C1=C(O)C(C)=CC(C2(C3=CC=CC=C3S(=O)(=O)O2)C=2C(=CC(O)=C(C)C=2)C)=C1C MGUKYHHAGPFJMC-UHFFFAOYSA-N 0.000 description 3
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical compound S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 3
- 241000588724 Escherichia coli Species 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 239000004677 Nylon Substances 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 229920004482 WACKER® Polymers 0.000 description 3
- 239000003242 anti bacterial agent Substances 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- 239000001569 carbon dioxide Substances 0.000 description 3
- 238000012258 culturing Methods 0.000 description 3
- 229910000037 hydrogen sulfide Inorganic materials 0.000 description 3
- 230000002101 lytic effect Effects 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- 229920001778 nylon Polymers 0.000 description 3
- 239000001301 oxygen Substances 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 229920005989 resin Polymers 0.000 description 3
- 239000011347 resin Substances 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- GOLORTLGFDVFDW-UHFFFAOYSA-N 3-(1h-benzimidazol-2-yl)-7-(diethylamino)chromen-2-one Chemical compound C1=CC=C2NC(C3=CC4=CC=C(C=C4OC3=O)N(CC)CC)=NC2=C1 GOLORTLGFDVFDW-UHFFFAOYSA-N 0.000 description 2
- ZPLCXHWYPWVJDL-UHFFFAOYSA-N 4-[(4-hydroxyphenyl)methyl]-1,3-oxazolidin-2-one Chemical compound C1=CC(O)=CC=C1CC1NC(=O)OC1 ZPLCXHWYPWVJDL-UHFFFAOYSA-N 0.000 description 2
- 229920001817 Agar Polymers 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-OUBTZVSYSA-N Carbon-13 Chemical compound [13C] OKTJSMMVPCPJKN-OUBTZVSYSA-N 0.000 description 2
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 2
- MJVAVZPDRWSRRC-UHFFFAOYSA-N Menadione Chemical compound C1=CC=C2C(=O)C(C)=CC(=O)C2=C1 MJVAVZPDRWSRRC-UHFFFAOYSA-N 0.000 description 2
- 102000035195 Peptidases Human genes 0.000 description 2
- 108091005804 Peptidases Proteins 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- MZVQCMJNVPIDEA-UHFFFAOYSA-N [CH2]CN(CC)CC Chemical group [CH2]CN(CC)CC MZVQCMJNVPIDEA-UHFFFAOYSA-N 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 239000000853 adhesive Substances 0.000 description 2
- 230000001070 adhesive effect Effects 0.000 description 2
- 239000008272 agar Substances 0.000 description 2
- 229910021529 ammonia Inorganic materials 0.000 description 2
- 229940088710 antibiotic agent Drugs 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- 210000001124 body fluid Anatomy 0.000 description 2
- 239000010839 body fluid Substances 0.000 description 2
- 239000002131 composite material Substances 0.000 description 2
- 230000018044 dehydration Effects 0.000 description 2
- 238000006297 dehydration reaction Methods 0.000 description 2
- 239000008121 dextrose Substances 0.000 description 2
- 238000009792 diffusion process Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 229920001971 elastomer Polymers 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 239000000017 hydrogel Substances 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 150000002431 hydrogen Chemical class 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 239000004816 latex Substances 0.000 description 2
- 229920000126 latex Polymers 0.000 description 2
- 230000002934 lysing effect Effects 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 239000002207 metabolite Substances 0.000 description 2
- 230000003472 neutralizing effect Effects 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 108090000623 proteins and genes Proteins 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- 239000005060 rubber Substances 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 230000001954 sterilising effect Effects 0.000 description 2
- 238000004659 sterilization and disinfection Methods 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- GJCOSYZMQJWQCA-UHFFFAOYSA-N 9H-xanthene Chemical compound C1=CC=C2CC3=CC=CC=C3OC2=C1 GJCOSYZMQJWQCA-UHFFFAOYSA-N 0.000 description 1
- 229920000936 Agarose Polymers 0.000 description 1
- 240000006439 Aspergillus oryzae Species 0.000 description 1
- 235000002247 Aspergillus oryzae Nutrition 0.000 description 1
- 108020004256 Beta-lactamase Proteins 0.000 description 1
- OKTJSMMVPCPJKN-IGMARMGPSA-N Carbon-12 Chemical compound [12C] OKTJSMMVPCPJKN-IGMARMGPSA-N 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- GUBGYTABKSRVRQ-WFVLMXAXSA-N DEAE-cellulose Chemical compound OC1C(O)C(O)C(CO)O[C@H]1O[C@@H]1C(CO)OC(O)C(O)C1O GUBGYTABKSRVRQ-WFVLMXAXSA-N 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- QRLVDLBMBULFAL-UHFFFAOYSA-N Digitonin Natural products CC1CCC2(OC1)OC3C(O)C4C5CCC6CC(OC7OC(CO)C(OC8OC(CO)C(O)C(OC9OCC(O)C(O)C9OC%10OC(CO)C(O)C(OC%11OC(CO)C(O)C(O)C%11O)C%10O)C8O)C(O)C7O)C(O)CC6(C)C5CCC4(C)C3C2C QRLVDLBMBULFAL-UHFFFAOYSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 229920002907 Guar gum Polymers 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- LEVWYRKDKASIDU-IMJSIDKUSA-N L-cystine Chemical compound [O-]C(=O)[C@@H]([NH3+])CSSC[C@H]([NH3+])C([O-])=O LEVWYRKDKASIDU-IMJSIDKUSA-N 0.000 description 1
- 239000004158 L-cystine Substances 0.000 description 1
- 235000019393 L-cystine Nutrition 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 239000007993 MOPS buffer Substances 0.000 description 1
- BPQQTUXANYXVAA-UHFFFAOYSA-N Orthosilicate Chemical compound [O-][Si]([O-])([O-])[O-] BPQQTUXANYXVAA-UHFFFAOYSA-N 0.000 description 1
- BELBBZDIHDAJOR-UHFFFAOYSA-N Phenolsulfonephthalein Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)C2=CC=CC=C2S(=O)(=O)O1 BELBBZDIHDAJOR-UHFFFAOYSA-N 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 239000004809 Teflon Substances 0.000 description 1
- 229920006362 Teflon® Polymers 0.000 description 1
- LDKDGDIWEUUXSH-UHFFFAOYSA-N Thymophthalein Chemical compound C1=C(O)C(C(C)C)=CC(C2(C3=CC=CC=C3C(=O)O2)C=2C(=CC(O)=C(C(C)C)C=2)C)=C1C LDKDGDIWEUUXSH-UHFFFAOYSA-N 0.000 description 1
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 239000000440 bentonite Substances 0.000 description 1
- 229910000278 bentonite Inorganic materials 0.000 description 1
- 229940092782 bentonite Drugs 0.000 description 1
- 235000012216 bentonite Nutrition 0.000 description 1
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 1
- 102000006635 beta-lactamase Human genes 0.000 description 1
- 239000003833 bile salt Substances 0.000 description 1
- 229940093761 bile salts Drugs 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 229940041514 candida albicans extract Drugs 0.000 description 1
- UBAZGMLMVVQSCD-UHFFFAOYSA-N carbon dioxide;molecular oxygen Chemical compound O=O.O=C=O UBAZGMLMVVQSCD-UHFFFAOYSA-N 0.000 description 1
- 239000003575 carbonaceous material Substances 0.000 description 1
- 239000000679 carrageenan Substances 0.000 description 1
- 235000010418 carrageenan Nutrition 0.000 description 1
- 229920001525 carrageenan Polymers 0.000 description 1
- 229940113118 carrageenan Drugs 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 210000004027 cell Anatomy 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 229960005188 collagen Drugs 0.000 description 1
- 230000001143 conditioned effect Effects 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 229960003067 cystine Drugs 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 230000000593 degrading effect Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- UVYVLBIGDKGWPX-KUAJCENISA-N digitonin Chemical compound O([C@@H]1[C@@H]([C@]2(CC[C@@H]3[C@@]4(C)C[C@@H](O)[C@H](O[C@H]5[C@@H]([C@@H](O)[C@@H](O[C@H]6[C@@H]([C@@H](O[C@H]7[C@@H]([C@@H](O)[C@H](O)CO7)O)[C@H](O)[C@@H](CO)O6)O[C@H]6[C@@H]([C@@H](O[C@H]7[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O7)O)[C@@H](O)[C@@H](CO)O6)O)[C@@H](CO)O5)O)C[C@@H]4CC[C@H]3[C@@H]2[C@@H]1O)C)[C@@H]1C)[C@]11CC[C@@H](C)CO1 UVYVLBIGDKGWPX-KUAJCENISA-N 0.000 description 1
- UVYVLBIGDKGWPX-UHFFFAOYSA-N digitonine Natural products CC1C(C2(CCC3C4(C)CC(O)C(OC5C(C(O)C(OC6C(C(OC7C(C(O)C(O)CO7)O)C(O)C(CO)O6)OC6C(C(OC7C(C(O)C(O)C(CO)O7)O)C(O)C(CO)O6)O)C(CO)O5)O)CC4CCC3C2C2O)C)C2OC11CCC(C)CO1 UVYVLBIGDKGWPX-UHFFFAOYSA-N 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 238000002845 discoloration Methods 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 235000012041 food component Nutrition 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 229940014259 gelatin Drugs 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 238000001879 gelation Methods 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 239000003365 glass fiber Substances 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 239000000665 guar gum Substances 0.000 description 1
- 235000010417 guar gum Nutrition 0.000 description 1
- 229960002154 guar gum Drugs 0.000 description 1
- BTIJJDXEELBZFS-QDUVMHSLSA-K hemin Chemical compound CC1=C(CCC(O)=O)C(C=C2C(CCC(O)=O)=C(C)\C(N2[Fe](Cl)N23)=C\4)=N\C1=C/C2=C(C)C(C=C)=C3\C=C/1C(C)=C(C=C)C/4=N\1 BTIJJDXEELBZFS-QDUVMHSLSA-K 0.000 description 1
- 229940025294 hemin Drugs 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 238000013095 identification testing Methods 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 238000002329 infrared spectrum Methods 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- QDLAGTHXVHQKRE-UHFFFAOYSA-N lichenxanthone Natural products COC1=CC(O)=C2C(=O)C3=C(C)C=C(OC)C=C3OC2=C1 QDLAGTHXVHQKRE-UHFFFAOYSA-N 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 239000000395 magnesium oxide Substances 0.000 description 1
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- 230000004066 metabolic change Effects 0.000 description 1
- 230000037353 metabolic pathway Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 239000000693 micelle Substances 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 239000004745 nonwoven fabric Substances 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 238000006053 organic reaction Methods 0.000 description 1
- VDDWRTZCUJCDJM-PNHLSOANSA-N p-Naphtholbenzein Chemical compound C12=CC=CC=C2C(O)=CC=C1\C(=C\1C2=CC=CC=C2C(=O)C=C/1)C1=CC=CC=C1 VDDWRTZCUJCDJM-PNHLSOANSA-N 0.000 description 1
- 229960003531 phenolsulfonphthalein Drugs 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 238000003672 processing method Methods 0.000 description 1
- 229940024999 proteolytic enzymes for treatment of wounds and ulcers Drugs 0.000 description 1
- 108010009004 proteose-peptone Proteins 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 239000001397 quillaja saponaria molina bark Substances 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 229930182490 saponin Natural products 0.000 description 1
- 150000007949 saponins Chemical class 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 229920005573 silicon-containing polymer Polymers 0.000 description 1
- 239000013464 silicone adhesive Substances 0.000 description 1
- 229920002545 silicone oil Polymers 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 239000008247 solid mixture Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 229920001059 synthetic polymer Polymers 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 1
- 239000012137 tryptone Substances 0.000 description 1
- 238000002211 ultraviolet spectrum Methods 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 238000001429 visible spectrum Methods 0.000 description 1
- 235000012711 vitamin K3 Nutrition 0.000 description 1
- 239000011652 vitamin K3 Substances 0.000 description 1
- 229940041603 vitamin k 3 Drugs 0.000 description 1
- 238000004073 vulcanization Methods 0.000 description 1
- 239000002759 woven fabric Substances 0.000 description 1
- 239000000230 xanthan gum Substances 0.000 description 1
- 229920001285 xanthan gum Polymers 0.000 description 1
- 235000010493 xanthan gum Nutrition 0.000 description 1
- 229940082509 xanthan gum Drugs 0.000 description 1
- 239000012138 yeast extract Substances 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
- UHVMMEOXYDMDKI-JKYCWFKZSA-L zinc;1-(5-cyanopyridin-2-yl)-3-[(1s,2s)-2-(6-fluoro-2-hydroxy-3-propanoylphenyl)cyclopropyl]urea;diacetate Chemical compound [Zn+2].CC([O-])=O.CC([O-])=O.CCC(=O)C1=CC=C(F)C([C@H]2[C@H](C2)NC(=O)NC=2N=CC(=CC=2)C#N)=C1O UHVMMEOXYDMDKI-JKYCWFKZSA-L 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M3/00—Tissue, human, animal or plant cell, or virus culture apparatus
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/02—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving viable microorganisms
- C12Q1/04—Determining presence or kind of microorganism; Use of selective media for testing antibiotics or bacteriocides; Compositions containing a chemical indicator therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M23/00—Constructional details, e.g. recesses, hinges
- C12M23/02—Form or structure of the vessel
- C12M23/04—Flat or tray type, drawers
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M23/00—Constructional details, e.g. recesses, hinges
- C12M23/22—Transparent or translucent parts
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M23/00—Constructional details, e.g. recesses, hinges
- C12M23/24—Gas permeable parts
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M25/00—Means for supporting, enclosing or fixing the microorganisms, e.g. immunocoatings
- C12M25/06—Plates; Walls; Drawers; Multilayer plates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M25/00—Means for supporting, enclosing or fixing the microorganisms, e.g. immunocoatings
- C12M25/14—Scaffolds; Matrices
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/02—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving viable microorganisms
- C12Q1/04—Determining presence or kind of microorganism; Use of selective media for testing antibiotics or bacteriocides; Compositions containing a chemical indicator therefor
- C12Q1/045—Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/02—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving viable microorganisms
- C12Q1/24—Methods of sampling, or inoculating or spreading a sample; Methods of physically isolating an intact microorganisms
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Biomedical Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Sustainable Development (AREA)
- Immunology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biophysics (AREA)
- Clinical Laboratory Science (AREA)
- Molecular Biology (AREA)
- Toxicology (AREA)
- Pathology (AREA)
- Cell Biology (AREA)
- Virology (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Materials By The Use Of Chemical Reactions (AREA)
Description
臨床試料中の微生物汚染の存在は、従来では、栄養素源の存在下で試料を培養すること、及び一定期間後の試料中における又は試料上方の大気中における変化を通して微生物活性を検出することによって決定される。例えば、Ahnellらへ付与された米国特許第4,182,656号では、試料が炭素13標識発酵性基質を含む培地が充填された容器に入れられる。容器を密閉して試料を生物学的活性に対して伝導性である条件を受けさせた後、試料上方のガス大気中における炭素13対炭素12の比率が決定され、初期比率と比較される。米国特許第4,152,213号では、容器中のガス圧を監視することを通して試料上方の大気中における酸素量の減少を検出することによって、試料中の酸素消費細菌の存在が密閉容器中で決定される方法が主張されている。米国特許第4,073,691号は、培地を含む密閉容器中で一定期間後における試料上方のガス大気の性質における変化を測定することによって、細菌を含む生物学的に活性な物質の存在を決定するための方法を提供している。
Calandraらへの米国特許第5,094,955号はある非侵襲性検出方法を教示しており、その中では透明な密閉容器中で試料を無菌液体増殖培地と一緒に培養することによって、例えば血液若しくはその他の体液のような臨床試料中及び非臨床試料中の微生物の存在を検出するための器具が開示されている。微生物の存在は、容器の内面又は容器を密閉するために使用される密閉手段に貼付されたセンサーを用いて、試料のpHにおける変化又は試料内の二酸化炭素の産生を検出又は測定することによって決定される。Calandraら法では、非線量計的及び非侵襲性手段を通して、例えば高濃度の赤血球のような妨害材料の存在下で微生物を検出することができる。
Calandraらの検出システムの欠点の1つは、微生物の存在を検出するための所要時間が試料数又は試料内の微生物数に関連している点である。さらに、微生物用の増殖培地が液体であるため、通例インキュベーション中には容器を攪拌しなければならないが、これはインキュベーション装置を作製するときに含まれる追加の出費となり、同時に又機械的故障の可能性を増加させる。さらに、そうしたシステムは微生物の存在を決定することはできるが、計数することはできない。さらにその上、微生物の検出後、その微生物を同定すること及び/又は様々な抗生物質に対するそれらの感受性を決定することが望ましいのがしばしば実状である。Calandra型システムでは、感受性又は同定試験を実施する前には微生物を液体培地から取り出すことが必要になり、そのためには追加の時間が必要とされるが、患者が極めて重篤な場合には、必ずしもそのための時間の余裕がない。
発明の概要
本発明は、臨床試料及び非臨床試料中における微生物の存在を検出するための器具及び方法に関する。本器具(以後は「センサー・プレート」と呼ぶ)は、液体サンプルに含まれる微生物コロニーを培養するための環境と、手動若しくは器具を使用してのどちらかで微生物の検出及び定量を容易にするための手段とを提供する。センサー・プレートは、固体、半固体又は粉末化ゲル固定化マトリックス層とセンサー層とを含む。検出された微生物コロニーは分離され、直ちにそれ以後の試験に利用できる。
より詳細には、センサー・プレートは未知の液体サンプル(微生物が存在するか否かが不明)を受け入れるための領域、液体サンプルをプレートの内面上に固定化するための機構、サンプル中の微生物の増殖を容易にする成分(例、栄養素源)、及びサンプル内の微生物コロニーの検出及び計数を許容するためのセンサーを提供する。センサー・プレートは、固定化マトリックス層中に吸収されるか又は固定化マトリックス層と一緒にゲルを形成するサンプルと一緒に、固定化層(例、ゲル層)及びセンサー層から構成され得る。センサー層は、微生物の存在を指示するためにセンサー・プレートの少なくとも1つの表面上に配置できる。固定化層における実際的な微生物コロニーの増殖を示す小さな面積又はゾーンの変色は、センサー層において発生する。センサー・プレートは、微生物コロニーの存在、位置、及び/又は数を決定するために手動で、又は器具を用いて自動的に検査される。
本発明のその他の様々な特徴及び長所は、添付の図面及び添付のクレームと結合することにより下記の詳細な説明から明白になるであろう。
【図面の簡単な説明】
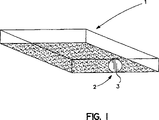
図1は、センサー・プレート器具の図である;
図2は、センサー・プレート器具の断面図である;
図3は、センサー・プレート器具の1つの代替実施形態の断面図である;
図4は、センサー・プレート器具のさらにもう1つの代替実施形態の断面図である;及び
図5は、E.coli(大腸菌)に対して陽性である3枚のセンサー・プレートの底面である。
好ましい実施形態の詳細な説明
図1は、透明若しくは半透明である少なくとも1つの側面(例、底面)を備えているフラットな浅い容器の形であってよいセンサー・プレート1の図である。容器は開放していて(若しくは単純に基質であってさえ)よいが、好ましくは密閉された若しくは密閉可能な容器であり、さらにセンサー・プレート層上方に幾らかのヘッドスペースを備えているのが好ましい。容器にはポート2を備えることができるが、これはストッパー3、スクリューキャップ、セプタム、又はそれらのいずれかの組合せ(若しくは何らかの他の密閉器具)を用いて密閉されてよい。サンプルがいったん容器内に収集されると、微生物の増殖栄養素源に依存して、センサー・プレートはガス透過性又はガス不透過性容器のどちらかとして構成することができる。この構成は、種々のプレート合成材料、積層物(ガス不透過性及び/又は疎水性ガス透過性膜)、及び/又は構成可能な通気口(例、容器壁の開口部に付けられたガス透過性膜)を使用することによって成し遂げられる。
センサー・プレート器具の容器内には、微生物のコロニーを検出する能力を高めるように配置された、微生物のコロニーが増殖できるようにサンプルを固定化/吸収するために役立つ1つ以上の層がある。ある実施形態では、器具内の少なくとも1つの層は微生物の視認に不都合な影響を及ぼすマトリックスを有する。図2から明らかなように、固定化層(固定化マトリックス層)10とセンサー層12とが備えられる。後により十分に説明するこれらの2つの層は、単一層内に一緒に結合することもできるが、2つの層が別個に備えられることが好ましい。同様に図2から明らかなようにプレート底部14があるが、これは、好ましくは微生物増殖に起因するセンサー層における変化を観察/画像描出するために透明である。
センサー層12は、紫外線、可視光線、及び/又は赤外線スペクトルにおいて厳密に局在化された劇的変化を提供することにより微生物増殖の位置を示す目的で備えられる。この局在化された変化は、微生物増殖近位のセンサー表面とは反対側のプレートの底面上で検出できる。センサー層は検出可能な特性が変化する物質(例、指示薬)を含むが、この物質は、好ましくは不透明なマトリックス(支持材料)上及び/又は内に包埋される。
「不透明」という用語は、センサー層が、固定化層と反対側のセンサー層の側からの、固定化層に固定化された試験サンプル及び/又は実際的微生物コロニーの観察又は検出(いずれかの適切な電磁領域において)を十分に妨げることを意味する(例えば、半不透明、実質的に不透明、又は完全に不透明)。試験サンプルも又実質的に透明である(その場合にはセンサー層は微生物コロニーの存在下では透明から不透明へと局在変化をなす)場合には透明若しくは比較的に透明なセンサー層を有していることが可能ではあるが、センサー層が透明ではないことが好ましい。センサー層が不透明であれば、検出を妨害する可能性がある試験サンプル中における微生物を検出する時に改善された結果が得られる。試験サンプル自体が固定化層において微生物の存在又は増殖を直接に観察/検出(例、目又は器具を用いて)することを妨害する場合は、固定化層又はセンサー層の少なくとも1つ(好ましくはセンサー層)が実際的試験サンプル及び/又は実際的微生物の検出/視認を遮断できること、そしてその代わりに固定化層における微生物の存在/増殖に対応するセンサー層における変化を検出することが好ましい。固定化層も又不透明であってよく、さらに本発明を実施した1つの実施形態では、センサー層、固定化層、及びサンプルの全てが不透明である。
センサーは、その上若しくは中に固定化された指示薬培地とともに、固体組成物若しくは膜を含む。センサー層は、外側からセンサー層を視認できるように、好ましくは容器の内側面と同じ高さに、又は容器を密閉するために使用される密閉手段内に配置されるか、又は密閉手段に付着させられる。センサー層は、細胞、タンパク質、その他の固体又はその他の不透明若しくは着色コンポーネントがそれと容器面との間に入るのを防止するために容器に貼付されるのが好ましい。ある実施形態では、センサー層は膜又は他の固体層によってサンプル及びその増殖培地から分離される。
本発明の1つの実施形態は、透明であっても、又は透明部分を有していてもよい、例えば蓋若しくはキャップのような密閉手段を含む。センサーは、透明な蓋若しくは蓋の部分の近位へ配置することができる、又は蓋の一部として作ることができる。容器を密閉するためにその蓋が使用される場合は、指示薬における変化は透明な密閉手段を通して読み取られる。密閉手段はさらに、被包化指示薬ミセルを含む例えばポリマーのような材料から作られてもよい。その材料が微生物の代謝によって惹起される変化に対して透過性であり、指示薬における変化が密閉手段の表面上で視認できる限りは、容器又は密閉手段いずれかにおける透明部分は必要とされない。
全サンプル量につき1種しか微生物を含有していない例えば血液のような体液のサンプル中の微生物は、本発明を使用して検出することができる。そうしたサンプルは、微生物集団が臨界的レベルに到達する前、そして微生物代謝に関わるパラメーターにおける変化を測定できるようになるまでに多数の日数又は多数回のインキュベーションを必要とすることがある。
そこで本センサーは、1)微生物代謝に起因するセンサー層における変化(例、代謝に起因するガス成分の増加若しくは減少)がサンプル上方の大気中におけるよりむしろ固体若しくは半固体固定化層から検出される、2)センサーがプレートの内面又は閉鎖若しくは密閉手段に貼付されている又は閉鎖若しくは密閉手段の外側を通して付着させられているので、プレート又は密閉手段の透明な壁の外側からプレートの完全性を侵害せずに測定を行うことができる、3)目視検査によって、又は拡散反射率、蛍光その他により、若しくは画像捕獲によって測定する器械を用いて外部測定を行うことができる、4)サンプル中の不透明/着色された若しくは蛍光性の成分は、変化を検出する能力又はそれらの変化の測定を妨害しない、及び5)変化を容易に観察又は検出できるようにセンサーの小さな容積内(例、ポリマー乳濁液内又は膜上)に高濃度の指示薬分子を保持できると言う点において有用である。
複合微生物培地を作り上げる栄養成分は、微生物が使用する代謝経路に影響を及ぼす。利用可能な栄養素源に依存して、有機酸、塩基及び様々なガスが比例して産生される。これらの生成物は又、微生物の種毎に相違する。固定化層におけるこれらの生成物の存在は固定化層のpHを変化させることがある。本発明に使用されるセンサー層は、pH変化に反応して測定可能な変化を生じるpH感受性指示薬を含むことができる。又は、指示薬のpHに影響を及ぼす例えばCO2のようなガスの存在を測定できる。微生物増殖はさらに又、O2及び/又は蛍光における変化の測定によっても検出できる。センサー層は、微生物の代謝に起因するO2濃度における減少に反応するようにデザインすることができる。さらに指示薬は、色又はその他のパラメーターよりむしろ蛍光が変化するように選択できる。二酸化炭素はほとんどの微生物が産生する一般的代謝産物であるので、微生物増殖を検出するための好ましい代謝産物である。どのような機構を利用したとしても、好ましい実施形態では、センサー層はほとんどの微生物の存在/増殖に反応して検出可能な変化を生じるであろう。
指示薬は、支持培地へ共有的又は非共有的のどちらかで付着させることができる。或いは又、指示薬は硬化前にポリマーマトリックス内で乳化されるように、ポリマーマトリックス内で被包化することができる。
センサー層は、必要であれば好ましくは適切な接着剤を用いて適切な透明容器の内側又は透明密閉手段に貼付される。それらはさらに密閉手段の統合部分を含んでいても、又はその場所で硬化するポリマーマトリックス内で乳化される指示薬として密閉手段若しくは容器内に貼付されてもよい。それらはさらに又、センサーに影響を及ぼすような微生物に起因する代謝性変化を許容する方法が提供される限り、容器の外側に置くこともできる。
pH、H2、H2S、NH3、O2若しくはCO2センサーにおける活性分子種として、様々な種類の蛍光及び可視pH指示薬を使用できる。一般に、指示薬の選択に関する唯一の制限は、それらが赤外線、蛍光、拡散反射率及び/又はイメージングテクノロジーによって検出可能な容認できるダイナミックレンジ及び波長変化を有していることが必要であるということである。
本発明による培地中のpH変化を検出するためのセンサーは、好ましくは約5.0〜約8.0のpH範囲に渡る蛍光強度又は可視光における変化を示す。
CO2センサーに対する指示薬は、CO2濃度における変化を検出するためには、約pH13〜約5、及び最も好ましくは約pH13〜約9の間で赤外線強度、蛍光強度又は可視光線における変化を示さなければならない。
一定のpH指示薬分子だけが支持培地へ共有的又は非共有的に結合することができ、それらのpH指示特性を保持することができる。キサンテン、フェノールフタレイン及びフェノールスルホンフタレインの群に属する指示薬は有用である。これらの例には、フルオレセイン、クマリン、フェノールフタレイン、チモールフタレイン、ブロモチモールブルー、チモールブルー、キシレノールブルー、オルトクレゾールフタレイン及びα−ナフトールベンゼインが含まれる。
支持培地は、例えばセルロース又は一定のシリコン類のような、有機反応によってそれにpH指示薬を共有的に付着させることのできる物質であってよい。pH指示薬の非共有的付着は、例えばナイロン膜のような正若しくは負のゼータ電位を有するイオン性支持材料を用いて達成できる。使用できるその他のイオン性支持材料は、例えばジエチルアミノエチル(DEAE)樹脂又はDEAEセルロースのような正若しくは負に荷電したイオン性樹脂類である。指示薬膜が微生物増殖培地と直接接触しなければならない場合は、タンパク質による支持材料の前処理が必要になることがある。
pH指示薬センサーは、微生物増殖培地のpH環境に起因するpH変化を直接検出する。しかし、これらのセンサーは微生物代謝に起因するガス(例、二酸化炭素、アンモニア、水素、硫化水素、又は酸素)に選択的に反応するようにさせることができる。選択的に半透過性合成物若しくは膜は、センサー層上に例えばシリコーン、ラテックス、テフロン、又はイオンの通過を防止しながらガスの拡散を選択的に許容する能力を特徴とする様々なプラスチック類を備えることができる。ポリマーマトリックス内に被包化された指示薬を含むセンサーについては、マトリックスを形成するポリマーはガスの通過は許容するがイオンの通過を許容しない半透過性障壁として機能することができる。
ある実施形態では、CO2センサーは複数の成分を含む。第1成分は、6〜10のpH範囲で反応性である可視又は蛍光pH指示薬である。これらの基準を満たす指示薬の例は、ブロモチモールブルー、チモールブルー、キシレノールブルー、フェノールフタレイン、オルトクレゾールフタレイン、クマリン、及びフルオレセインである。必要な場合の第2成分は、選択されたpH指示薬によってCO2を検出するための最適のpH環境を維持する酸、塩基又は緩衝液である。第3成分は、未硬化ポリマー内で乳化される指示薬溶液の溶滴を作り出すことのできるグリセロール若しくは同等の乳化剤であってよい。第4成分は、例えば酸化チタン、酸化亜鉛、酸化マグネシウム、酸化鉄その他のような顔料であってよい。第5成分は、指示薬にとって適正な環境を維持する、例えばシリコーンのような未硬化ポリマーであってよい。ガスには透過性であるがイオンには透過性ではない限り、独自の化学的若しくは物理的特性又は硬化するための必要条件のいずれかから指示薬の化学的活性に過大に影響を及ぼさない、そして滅菌処理を受けたときにこれらの特性が変化しないあらゆるポリマーを使用することができる。さらに同様に申し分のないその他のシリコーン系ポリマーは、高温、触媒活性、又は紫外線加硫によって硬化するポリマーである。乳化剤は様々な成分から調製され、ポリマーは硬化するとpH指示薬の溶滴の周囲に半透過性マトリックスを形成し、これは固定化層からのCO2及びその他のガスの選択的拡散を許容し、センサー層における局在性の測定可能な変化を生じさせる。センサー層は、例えば型に入れて個別に調製し、硬化させ、さらにその後に例えばシリコーン系接着剤のような適切な接着剤を用いてプレートに付着させることができる。或いは又、そして好ましくは、センサーは容器の底面上で形成され、その場所で硬化させられる。硬化後、センサーを備えた容器は、例えばオートクレーブ又はガンマ線照射によって滅菌処理することができる。便宜的には、固定化及び追加のオプション層は滅菌処理の前にセンサー・プレート器具内に導入して、こうして同様にその工程によって滅菌することができる。
他の例では、センサー層は顔料が添加されたシリコーンマトリックス中に乳化させた指示薬溶液を含む。この指示薬溶液は、0.8M水酸化カリウム(10.0ml)及びイソプロピルアルコール(10.0ml)の溶液内に溶かしたチモールブルー指示薬(0.65g)を含む。この指示薬溶液(5.0g)はその後、顔料が添加されたシリコーン成分と混合される。顔料が添加されたシリコーンマトリックスは、Sylgard184シリコーン(成分A(50.0g)及びB(5.0g))及び白色顔料(製品番号61−18000、Ferro Corp.、ニュージャージー州)(1.0g)を含む。その後にセンサー材料が注ぎ入れられ、プレート上に薄層状(およそ0.2〜0.5mm)で広げられる。
別の例では、センサー層は顔料が添加されたシリコーンマトリックスと混合された指示薬溶液とを含む。この指示薬溶液は、イソプロピルアルコール(5.0ml)及び0.9M水酸化カリウム(5.0ml)の溶液内に溶解させたオルト−クレゾールフタレイン指示薬(2.0g)を含む。この指示薬溶液(2.5g)は、その後後顔料を添加したシリコーン成分と混合される。顔料が添加されたシリコーンマトリックスは、Sylgard184シリコーン(成分A(25.0g)及びB(2.5g))及び白色顔料(製品番号61−18000、Ferro Corp.、ニュージャージー州)(0.5g)を含む。その後センサー材料が注ぎ入れられ、プレート上に薄層状(およそ0.2〜0.5mm)で広げられる。この実施例の変形では、上記のオルト−クレゾールフタレインセンサー層は顔料が添加されたシリコーンマトリックスを含むオーバーコート層で被覆される。
さらに別の例では、センサー層は顔料溶液及びシリコーンマトリックスと混合された指示薬溶液を含む。この指示薬溶液は、イソプロピルアルコール(10.0ml)及び0.8M水酸化カリウム(10.0ml)の溶液内に溶解させたオルト−クレゾールフタレイン指示薬(2.0g)を含む。この顔料溶液は、シリコーン油(40.0g)、白色顔料(製品番号61−18000、Ferro Corp.、ニュージャージー州)(4.0g)とを含む。シリコーンマトリックスは、Wacker Elastosil RT 601シリコーン(成分A(200.0g)及びB(20.0g))及びトルエン(40.0g)とを含む。この指示薬溶液(20.0g)はその後顔料溶液(40.0g)及びシリコーンコンポーネントと混合される。センサー材料はその後、プレート上に薄層状(厚さおよそ0.1〜0.3mm)で広げられる。
上記のような酸素、二酸化炭素及びpHにおける変化に反応性の指示薬に追加して、アンモニア、酸化還元電位、水素、硫化水素、又はあらゆるその他の微生物の存在若しくは増殖に起因して変化する物質における変化を検出する指示薬を利用できる。同様に、センサー層(又は複数のセンサー層)において複数の相違する指示薬を使用することもできる。
センサー層は、好ましくはサンプルの特性(例、自然蛍光性、不透過性等)がセンサーの反応に影響を及ぼすこと若しくは遮蔽することを防止できるように不透明である。センサー層は、好ましくは微生物の存在下にある不透明な状態から別の不透明な状態へ変化するが、その変化は画像の捕獲及び処理によって検出可能な変化である。1つの例として、センサー層は白色顔料が添加されたシリコーンのオーバーレイを伴う、白色顔料が添加されたシリコーンマトリックスにおけるオルト−クレゾールフタレイン指示薬の乳化混合物であってよい。又は、センサー層は例えばチモールブルー指示薬、キシレノールブルー指示薬、若しくは「汎用」指示薬のような1種以上の指示薬と一緒に乳化された顔料が添加されたシリコーンマトリックスであってよい。センサー層内のマトリックスは、適切なラテックス、ポリウレタン、ナイロン膜(例、荷電ナイロン膜)又はセルロース粉末であってよい。センサー層マトリックスはさらに又、例えばSylgard 184、Wacker 601、又はWacker 934のようなシリコーンマトリックスであってよい。又は、センサー層は、例えば指示薬層と不透明層のような2つの層から作製されてもよい。
センサー・プレート器具におけるもう1つの主要な層は固定化層10である。固定化層の目的は、マトリックス内若しくはマトリックスの表面上のどちらかでサンプル内の微生物を固定化することである。サンプル自体は、液体、半固体又は半液体(例、ペースト若しくはゲル)のサンプルであってよい。液体サンプルは、混合されると微生物固定化ゲルマトリックスを形成する乾燥粉末ゲル化剤と混合することができる。液体サンプルは、好ましくは既にセンサー・プレート器具内の層として用意されている乾燥粉末ゲル化剤に添加される。しかし、液体サンプルは乾燥粉末ゲル化剤と混合して、その後にゲル化が発生する前に両方を直ちにセンサー・プレート器具内に添加することもできる。同様に、液体サンプルは、ゲルの表面上で微生物を固定化できるように既にゲル化したマトリックス上又は脱水された若しくは部分的に脱水されたゲルマトリックス上に塗布することもできる。ゲル化剤はさらに、物理的支援を加えるために支持マトリックス内に包埋することもできる。例には全体が混合された、若しくはウーブン若しくはノンウーブンファブリックの形のどちらかで混合されたガラス若しくはセルロース合成ポリマー繊維が含まれる。さらに、サンプルを固定化するために、固定化層がゲル化剤である必要はなく、むしろ例えばスポンジ材料、セルロース、ガラス繊維、濾紙、その他のような非ゲル吸収性材料を含むことができる。
センサー・プレート器具には、一緒に混合して若しくは個別層のどちらかで1種以上のゲル化剤を利用することができる。およそ2:1の重量比で結合した例えばグアーゴム及びキサンタンゴムの混合物を使用することができる。その他のゲル化剤は、単独で、又は天然及び合成ヒドロゲル粉末を含む組合せで使用することができる。1種以上のゲル化剤は、ゴム、寒天、アガロース、カラゲナン、ベントナイト、アルギン酸塩、コラーゲン、ゼラチン、溶融ケイ酸塩、水溶性デンプン、ポリアクリレート、セルロース、セルロース誘導体、ポリエチレングリコール、酸化ポリエチレン、ポリビニルアルコール、デキストラン、ポリアクリルアミド、多糖又はその他のゲル化剤若しくは増粘剤類から選択したものと一緒に結合できる。
表面コロニー分離/固定化のためには、1種以上の合成又は天然親水性ポリマーを含む脱水された及び/又は部分的に脱水されたゲルマトリックスが使用できる。2種以上のゲル化剤を使用する場合は、そうしたゲル化剤は一緒に混合されても複数の層で備えられもよい。ある実施形態では、上層は表面上に微生物を捕らえるために備え、下層は上層を通して液体サンプルを引き出すためのウィッキング剤として備えることができる(例、修飾セルロース吸収剤上方の薄層寒天層、又は吸収性パッド、ポリマー若しくはヒドロゲル上方の多孔質親水性膜)。
固定化層はセンサー層に不都合な影響を及ぼしてはならない。センサー層がpH変化に起因して検出可能に変化する場合、極めて酸性のゲル層はセンサー層に不都合な影響を及ぼす可能性がある(同様に一部の製造工程は酸性であり、センサー層に不都合な影響を及ぼす可能性のある酸性残留物を残すことがある)。さらにその上、固定化層が粉末化ゲル層である場合は、微生物が不在である場合にさえセンサー層の変化が引き起こされる可能性があるので、この層を血液サンプルと混合したときに確実に酸性に転換してはならない。
さらに図2から明らかなように、固定化層の上方(又はその中若しくは下方)にオプションのコンディショニング層を用意することができる。図2では固定化層とは別個に図示されているが、コンディショニング層に含まれるコンディショニング材料は、好ましくは固定化層の中に組み込まれる。コンディショニング成分は、固定化層の中に備えられる場合と個別層に備えられる場合のどちらにおいても、微生物を増殖させるための1種以上の培地、溶解剤、溶解酵素、抗生物質中和剤、界面活性剤又はその他の微生物検出能力を向上させるのに有用な材料を含むことができる。コンディショニング成分は、さらに又固定化層の中でも同一センサー・プレート器具内の個別層のどちらにでも備えることができる。
コンディショニングのための溶解剤は、試験サンプル中の血球を溶解させるため、より平滑なゲルを許容するため、及び/又はより良好なゲルの再脱水のために添加することができる。考えられる溶解剤の例には、サポニン、ジギトニン、トゥイーン(Tween)TM、ポリソルビタンモノラウレート及びその他の界面活性剤類が含まれる。典型的には必ずしもタンパク質分解酵素とは限らない溶解酵素類は、血液サンプル中の細胞材料を消化するため、より平滑なゲルを作製するため、及び/又はより良好なゲルの再脱水のために添加されてよい。コンディショニングのための溶解酵素類は、1種以上のプロテアーゼ類、例えばAspergillus oryzae(アスペルギルス・オリザエ)その他に由来する酵素混合物を含むことができる。
抗生物質中和剤は、コンディショニングのため、特に試験サンプル中のより迅速及び/又はより良好な微生物の回収のために添加されてよい。1種以上のそうした中和剤は樹脂、ゴム、及び炭素ベースの材料(例、活性炭又はEcosorb▲R▼)、又は特異的に様々な抗生物質を分解するための種々の酵素類(β−ラクタマーゼ)の1つから選択することができる。
さらにコンディショニングのためには培地を添加することができる(固定化層へ直接又は別個のどちらかで)。培地は、微生物を増殖させるための栄養素源を供給するために添加される。様々なタイプの微生物に対して多数のタイプの培地を使用できるが、微生物が好気性微生物である場合は、ある実施例(各々の量の例は括弧内にg/lで示されている)のように培地は下記のものを含むことができる;トリプトン(17)、ソイトン(3)、プロテオースペプトン(5)、麦芽エキス(2.5)、デキストロース(2.5)及びMOPS(23)。微生物が嫌気性微生物である場合は、培地はさらに好気性微生物のために上記に列挙した培地の他にヘミン(0.005)、L−シスチン(0.2)、Na−m−二硫化物(0.2)及びメナジオン(0.0005)を含むことができる。
大腸菌型に対しては、培地は、1つの例として、ラクトース(5)、胆汁塩類#3(0.8)、K2HPO4(7)、KH2PO4(3)、(NH4)2SO4(0.5)、MgSO4(0.1)、Na−m−二硫化物(0.4)及びSDS(0.1)を含むことができる。酵母、カビ及びその他の耐酸性微生物に対しては、培地はある実施例のように、デキストロース(10)、酵母エキス(10)、(NH4)クエン酸塩(2)及びpH5.5までの酒石酸を含むことができる。
さらに図2から明らかなように、容器の壁にはその下方が疎水性ガス透過性フィルム22でありその上方がガス不透過性(脱着可能)フィルム24である開口部20を備えることができる。又は、容器の壁にはガス不透過性フィルムとそれに固着した疎水性ガス透過性フィルムが一緒に前記開口部を被覆している開口部を備えることができる。微生物が嫌気性である場合、ガス不透過性フィルムはその場所に置かれたままにされるであろう。しかし微生物が好気性である場合は、センサー・プレート器具へ試験サンプルを添加する時点でガス不透過性フィルムが取り除かれるであろう。もちろん、疎水性ガス透過性フィルムが用意される必要は全くないが、容器内に汚染物質が侵入するのを防止するため、そして潜在的に感染性の試験サンプルが器具から漏出するのを防止するためには有益である。
図2における領域Aは、図3及び4においてより詳細に図示されている。図3から明らかなように、センサー・プレート器具の別の実施形態では、単一固定化マトリックス層の代わりに、下記のうちの1つ以上を備えることができる:表面捕獲及び増殖後の回収を許容するために半剛性面のための分離ゲル層30、接着剤層31、吸収性ゲル層32及び追加の接着剤層33。吸収性ゲル層32は1種以上のコンディショニング成分(ゲル中に)、微生物増殖のための培地、溶解酵素類、及び抗生物質中和剤を含むことができる。さらに図3から明らかなように、単一センサー層の代わりに、下記のうちの1つ以上を備えることができる:オーバーコート層34、接着剤層35、指示薬層36、及びプレート底面38と接触している追加の接着剤層37。
図4に図示されているような本発明の追加の実施形態では、下記を含むマトリックス層40が備えられている:ゲル化粉末、及び例えば培地、溶解酵素類及び抗生物質中和剤のような乾燥コンディショニング成分類。図3におけるように、単一センサー層の代わりに、下記のうちの1つ以上を備えることができる。接着剤層41、オーバーコート層42、接着剤層43、指示薬層44、及びプレート底面46と接触している接着剤層45。
センサー・プレート器具のサイズは必要なサンプルサイズに依存して変化させることができる。ある実施例では、センサー・プレート器具は74mm×117mmの寸法の固定化層を有している。固定化層が湿性タイプのゲルを含んでいる場合は、サンプルのサイズを極めて小さく(例、1ml以下)するか、又は血液サンプルを用いる場合のようにサンプルサイズを15mlまでにすることができる。他方、固定化層が乾燥粉末化ゲルを含んでいる場合は、サンプルサイズは粉末化ゲルの量に依存してより大きくできる(例、サンプルは30ml以上)。
使用時に、液体サンプルはセンサー・プレート器具内に導入される。サンプルは、それがセンサー・プレートの底面に広げられるにつれて(必要な場合は)「コンディショニング」される。サンプルはゲル内に吸収されるか、固定化マトリックス層と一緒にゲルを形成する。その後、センサー・プレートは微生物コロニーの増殖を促進するためにインキュベートされる。センサー・プレート器具の底面に向けて配置されたセンサー層は微生物コロニーの存在を指示するように検出可能に変化する。最後に、センサー・プレート器具は、微生物コロニーの存在及び所在位置を決定するために手動で又は自動的に検査される。
センサー・プレート器具が自動的に検査される場合は、3つの主要機能を実行する器械が備えられる:プレートのインキュベーション、画像収集/捕獲、及び画像処理。この器械はプレートをインキュベートするために制御された環境を提供するが、これはインキュベーションが周囲より高温で発生する場合はヒーターを含むことができる(だが全ての状態において高温が必要とされるわけではない)。液体サンプルがセンサー・プレート器具に添加され、その後にセンサー・プレートは器械内に置かれ、引き続いてインキュベーション期間中に画像収集/捕獲装置(例、カメラ又はスキャナー)によってセンシング/観察される。センサー・プレート器具の底面の画像は所定の定期的間隔で捕獲でき、引き続いて1種以上の画像処理法及びアルゴリズムを用いて微生物コロニーがセンサー・プレート上に存在するかどうかを決定するために解析することができる。
種々のタイプのセンサー・プレート器具に関する数多くの実行可能性試験は、良好な検出結果を示している:E. coliは約9時間で、E. facaelisは約10時間で、そしてS. aureus(黄色ブドウ球菌)は約11時間で検出された。図5は、隣接固定化マトリックス層における微生物コロニーの近位にあるセンサー層の領域で検出可能に変化している4枚のセンサー・プレートの下側を示している。試験で検出されたコロニーは引き続いてその後の試験のために直ちに使用可能な微生物希釈液を産生した。
Claims (1)
- 容器;
微生物の存在又は数について試験するサンプルを固定化するための固定化層;及び
固定化層と容器の壁の間に配置されたセンサー層であって、当該センサー層の少なくとも一部分が固定化層の上及び/又は中で固定化された微生物の存在に起因して検出可能に変化することのできるセンサー層;
を含むセンサー器具であって、
センサー層が不透明であること、およびセンサー層が固定化層と反対側のセンサー層の側からの試験サンプルの目による視認又は検出器による検出を妨げることを特徴とする前記センサー器具。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US08/989,560 | 1997-12-12 | ||
| US08/989,560 US5976827A (en) | 1997-12-12 | 1997-12-12 | Sensor device for detecting microorganisms and method therefor |
| PCT/US1998/026376 WO1999029831A1 (en) | 1997-12-12 | 1998-12-10 | Sensor device for detecting microorganisms, and method therefor |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2001511654A JP2001511654A (ja) | 2001-08-14 |
| JP4183288B2 true JP4183288B2 (ja) | 2008-11-19 |
Family
ID=25535225
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP53172799A Expired - Lifetime JP4183288B2 (ja) | 1997-12-12 | 1998-12-10 | 微生物を検出するためのセンサー器具、及びそのための方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (3) | US5976827A (ja) |
| EP (1) | EP1003836A4 (ja) |
| JP (1) | JP4183288B2 (ja) |
| KR (1) | KR20000071045A (ja) |
| AU (1) | AU752954B2 (ja) |
| CA (1) | CA2280697A1 (ja) |
| WO (1) | WO1999029831A1 (ja) |
Families Citing this family (66)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6395506B1 (en) * | 1991-04-18 | 2002-05-28 | Becton, Dickinson And Company | Device for monitoring cells |
| US7122338B2 (en) * | 1995-11-14 | 2006-10-17 | Biocontrol Systems, Inc. | Method for quantification of biological material in a sample |
| US5976827A (en) * | 1997-12-12 | 1999-11-02 | Akzo Nobel, N.V. | Sensor device for detecting microorganisms and method therefor |
| US6596532B1 (en) * | 1997-12-12 | 2003-07-22 | BIOMéRIEUX, INC. | Device for isolation and surface culture of microorganisms from bulk fluids |
| US20040067547A1 (en) * | 1998-03-31 | 2004-04-08 | Stuart Harbron | Rapid method for detecting micro-organisms and evaluating antimicrobial activity |
| GB9818766D0 (en) * | 1998-08-28 | 1998-10-21 | Johnson Matthey Plc | Improvements in sensors |
| US6471788B1 (en) | 1999-12-15 | 2002-10-29 | Lynntech Coatings, Ltd. | Ferrate conversion coatings for metal substrates |
| US6391626B1 (en) * | 1999-08-23 | 2002-05-21 | 3M Innovative Properties Company | Culture medium and device using ballasted pH indicators for detection and enumeration of microorganisms |
| EP1122535A3 (en) * | 2000-01-31 | 2004-09-22 | The Penn State Research Foundation | Interrogation of changes in the contents of a sealed container |
| US20030096315A1 (en) | 2000-05-03 | 2003-05-22 | Sanders Mitchell C. | Device for detecting bacterial contamination and method of use |
| ES2271078T3 (es) * | 2000-05-03 | 2007-04-16 | Expressive Constructs, Inc. | Metodo para detectar listeria monocytogenes. |
| WO2002014539A1 (en) * | 2000-08-14 | 2002-02-21 | University Of Maryland Baltimore County | Bioreactor and bioprocessing technique |
| JP2002085090A (ja) * | 2000-09-13 | 2002-03-26 | Hiroyuki Ogawa | 真菌検査方法および真菌用検査具 |
| WO2002054969A1 (en) * | 2001-01-10 | 2002-07-18 | Blood Cell Storage Inc. | System for growth, analysis, storage, validation and distribution of cells and tissues used for biomedical purposes |
| US6723285B2 (en) * | 2001-04-11 | 2004-04-20 | Natali Chen | Food freshness indicator |
| EP1253203A1 (en) * | 2001-04-25 | 2002-10-30 | Becton Dickinson and Company | Rapid resuscitation, growth, capture and detection of microorganisms |
| US6395537B1 (en) * | 2001-08-04 | 2002-05-28 | Ruth F. Eden | Double container device and method for detecting and enumerating microorganisms in a sample |
| US6780602B2 (en) * | 2001-11-01 | 2004-08-24 | Microbiosystems, Limited Partnership | Taxonomic identification of pathogenic microorganisms and their toxic proteins |
| US7811783B2 (en) | 2001-12-14 | 2010-10-12 | Colifast As | Rapid method of detection and enumeration of sulfide-producing bacteria in food products |
| US6632632B1 (en) * | 2001-12-14 | 2003-10-14 | Colifast As | Rapid method of detection and enumeration of sulfide-producing bacteria in food products |
| AU2003212897B2 (en) * | 2002-01-31 | 2007-08-02 | Expressive Constructs, Inc. | Method for detecting microorganisms |
| US20030190599A1 (en) * | 2002-04-04 | 2003-10-09 | Moats Richard K. | Combinational Biosensor |
| US8697029B2 (en) * | 2002-04-18 | 2014-04-15 | The Regents Of The University Of Michigan | Modulated physical and chemical sensors |
| CA2484195A1 (en) * | 2002-05-03 | 2003-11-13 | Gambro, Inc. | Apparatus and method for detecting bacteria in blood products |
| USD478660S1 (en) | 2002-07-01 | 2003-08-19 | Healthetech, Inc. | Disposable mask with sanitation insert for a respiratory analyzer |
| GB0215878D0 (en) * | 2002-07-09 | 2002-08-14 | Smart Holograms Ltd | Cell detection |
| PL215172B1 (pl) * | 2003-01-31 | 2013-10-31 | Ethicon Inc | Sposób wykrywania Escherichia coli, biosensor do wykrywania Escherichia coli i zestaw do wykrywania Escherichia coli |
| IL156556A (en) * | 2003-06-19 | 2010-02-17 | Eran Schenker | A system detects life signals |
| CA2532414C (en) * | 2003-07-12 | 2017-03-14 | Accelr8 Technology Corporation | Sensitive and rapid biodetection |
| CA2557612C (en) * | 2003-11-03 | 2014-06-17 | Ethicon, Inc. | Methods, peptides and biosensors useful for detecting a broad spectrum of bacteria |
| US20060257929A1 (en) * | 2003-11-12 | 2006-11-16 | Microbiosystems, Limited Partnership | Method for the rapid taxonomic identification of pathogenic microorganisms and their toxic proteins |
| US7425411B2 (en) | 2003-12-09 | 2008-09-16 | Biomerieux, Inc. | Method for recovering microorganisms from a sample |
| CN101036046B (zh) | 2004-08-19 | 2012-02-22 | 血细胞保存公司 | 荧光pH检测器系统和相关方法 |
| US8183052B2 (en) * | 2004-08-19 | 2012-05-22 | Blood Cell Storage, Inc. | Methods and apparatus for sterility testing |
| US8497134B2 (en) | 2004-08-19 | 2013-07-30 | Blood Cell Storage, Inc. | Fluorescent detector systems for the detection of chemical perturbations in sterile storage devices |
| US20060074348A1 (en) * | 2004-09-30 | 2006-04-06 | Gambro, Inc. | Biologic Fluid Sampling Apparatus |
| US8128952B2 (en) * | 2005-01-12 | 2012-03-06 | Clemson University Research Foundation | Ligand-mediated controlled drug delivery |
| JP4628134B2 (ja) * | 2005-02-18 | 2011-02-09 | 独立行政法人国立高等専門学校機構 | 生菌検出方法および生菌検出用具 |
| US7575890B2 (en) * | 2006-01-18 | 2009-08-18 | Oxygen Enterprises, Ltd. | Method for rapid detection and evaluation of cultured cell growth |
| KR100695172B1 (ko) * | 2006-03-09 | 2007-03-14 | 삼성전자주식회사 | 미생물 감지기능이 구비된 로봇청소기 |
| US8852504B2 (en) | 2006-10-11 | 2014-10-07 | The Board Of Trustees Of The University Of Illinois | Apparatus and method for detecting and identifying microorganisms |
| US9068977B2 (en) * | 2007-03-09 | 2015-06-30 | The Regents Of The University Of Michigan | Non-linear rotation rates of remotely driven particles and uses thereof |
| WO2009018544A1 (en) * | 2007-08-01 | 2009-02-05 | Hitachi Chemical Co., Ltd. | Pathogen detection in large-volume particulate samples |
| CN101918531B (zh) | 2007-11-20 | 2013-06-12 | 3M创新有限公司 | 环境取样制品和方法 |
| CN101952457B (zh) | 2007-12-21 | 2013-08-21 | 3M创新有限公司 | 流体样品分析的微生物系统和方法 |
| KR100978616B1 (ko) * | 2008-02-20 | 2010-08-27 | 주식회사바텍 | 대면적 x선 검출장치 |
| US20110059482A1 (en) * | 2008-03-12 | 2011-03-10 | Hector Roldan | Sampling Kit |
| US20100112630A1 (en) * | 2008-11-03 | 2010-05-06 | Scott Martell Boyette | Methods for measuring microbiological content in aqueous media |
| US8481302B2 (en) * | 2008-11-03 | 2013-07-09 | General Electric Company | Total bacteria monitoring system |
| US8753834B2 (en) | 2009-12-30 | 2014-06-17 | 3M Innovative Properties Company | Microbial detection article |
| US8846331B2 (en) | 2010-08-27 | 2014-09-30 | The Regents Of The University Of Michigan | Asynchronous magnetic bead rotation sensing systems and methods |
| WO2012142179A2 (en) | 2011-04-11 | 2012-10-18 | The Regents Of The University Of Michigan | Magnetically induced microspinning for super-detection and super-characterization of biomarkers and live cells |
| WO2012158041A1 (en) | 2011-05-18 | 2012-11-22 | Rna Holding B.V. | Diagnostic methods and kits for determining the presence of a microorganism in a sample |
| US9040307B2 (en) | 2011-05-27 | 2015-05-26 | Blood Cell Storage, Inc. | Fluorescent pH detector system and related methods |
| US9797817B2 (en) | 2012-05-03 | 2017-10-24 | The Regents Of The University Of Michigan | Multi-mode separation for target detection |
| EP2895595B1 (en) * | 2012-09-14 | 2018-11-28 | Charm Sciences, Inc. | Culture medium method and device |
| US9983110B2 (en) | 2013-11-04 | 2018-05-29 | The Regents Of The University Of Michigan | Asynchronous magnetic bead rotation (AMBR) microviscometer for analysis of analytes |
| EP3183332A1 (en) * | 2014-08-20 | 2017-06-28 | 3M Innovative Properties Company | Self-contained anaerobic culture device for sulfate-reducing microorganisms |
| CN106574225B (zh) | 2014-08-20 | 2019-12-17 | 3M创新有限公司 | 用于样品分配和分析的装置和方法 |
| ES2871137T3 (es) * | 2015-12-14 | 2021-10-28 | Quanta Matrix Co Ltd | Método de diferenciación de células particulares a partir de la mezcla de células heterogéneas |
| KR102245743B1 (ko) * | 2017-12-19 | 2021-04-28 | 주식회사 바이오맥스 | 미생물 검출용 미세유체 종이칩, 이의 제조방법 및 이를 이용한 미생물 검출방법 |
| CN109116012B (zh) * | 2018-09-26 | 2021-10-19 | 安徽贝驰生物科技有限公司 | 一种高精度液体检测装置 |
| CN112779176B (zh) * | 2019-11-06 | 2022-07-12 | 珠海恒屹生物科技有限公司 | 分离试剂、其制备方法、应用、分离细菌的方法和凝胶提取管 |
| CN112063505A (zh) * | 2020-06-15 | 2020-12-11 | 天津市儿童医院 | 一种含有β-内酰胺酶的细菌培养瓶及其制备方法 |
| KR102413155B1 (ko) | 2021-10-14 | 2022-06-24 | 주식회사 휴피트 | 패혈증 진단용 이산화탄소 비색 센서 기반의 미생물 생장배지 |
| KR102617827B1 (ko) * | 2021-12-30 | 2023-12-27 | (주)바이오액츠 | 미생물을 검출하기 위한 조성물 |
Family Cites Families (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US35286A (en) * | 1862-05-20 | Improvement in preserve-vessels | ||
| US3856628A (en) * | 1972-05-17 | 1974-12-24 | Crowley R | Method and apparatus for the identification of microorganisms |
| US3962040A (en) * | 1974-03-14 | 1976-06-08 | The United States Of America As Represented By The Department Of Health, Education And Welfare | Method and apparatus for plating and counting aerobic bacteria |
| US4280002A (en) * | 1979-12-03 | 1981-07-21 | Minnesota Mining And Manufacturing Company | Microbiological growth container |
| US4565783A (en) * | 1981-01-27 | 1986-01-21 | Minnesota Mining And Manufacturing Company | Dry culture media |
| US4468456A (en) * | 1982-03-29 | 1984-08-28 | Warner-Lambert Company | Medium for differentiating Streptococcus mutans |
| JPS62272967A (ja) * | 1986-05-22 | 1987-11-27 | Hitachi Electronics Eng Co Ltd | コロニ−自動移植装置 |
| SU1359301A1 (ru) * | 1986-07-16 | 1987-12-15 | Днепропетровский медицинский институт | Индикаторна среда дл определени оксидазной активности AeRococcUS VIRIDaNS |
| US5094955A (en) * | 1988-03-15 | 1992-03-10 | Akzo N.V. | Device and method for detecting microorganisms |
| US5089413A (en) | 1989-05-19 | 1992-02-18 | Minnesota Mining And Manufacturing Company | Method and apparatus for culturing with microbiological dry culture medium |
| CA2022614A1 (en) * | 1989-08-31 | 1991-03-01 | Richard R. Matner | Colony blotting method and device |
| US5232838A (en) * | 1991-12-09 | 1993-08-03 | Minnesota Mining And Manufacturing Company | Culture media device and method of use |
| AU4634593A (en) * | 1992-07-13 | 1994-01-31 | Minnesota Mining And Manufacturing Company | A technique to count objects in a scanned image |
| US5409838A (en) * | 1992-12-23 | 1995-04-25 | Minnesota Mining And Manufacturing Company | Use of acid to stabilize indicator dyes in acrylate adhesives |
| US5364766A (en) * | 1993-05-14 | 1994-11-15 | Minnesota Mining And Manufacturing Company | Culture medium for rapid count of coliform bacteria |
| DE69411268T2 (de) * | 1993-05-14 | 1999-03-04 | Minnesota Mining And Mfg. Co., Saint Paul, Minn. | Verfahren zur schnellen quantifizierung von microorganismenwachstum |
| US5443963A (en) * | 1994-01-31 | 1995-08-22 | Minnesota Mining And Manufacturing Company | Method for detecting staphylococci |
| US5464755A (en) * | 1994-04-29 | 1995-11-07 | Biolog, Inc. | Microbiological medium and method of assay |
| US5573950A (en) * | 1994-05-11 | 1996-11-12 | Minnesota Mining And Manufacturing Company | Cassette for disposable microorganism culturing media and automated scanning system |
| US5462860A (en) * | 1994-06-06 | 1995-10-31 | Minnesota Mining And Manufacturing Company | Conditioned culture medium for rapid growth and detection of microbes |
| US5627045A (en) * | 1995-04-12 | 1997-05-06 | Biolog, Inc. | Multi-test format with gel-forming matrix for characterization of microorganisms |
| US5681712A (en) * | 1995-06-02 | 1997-10-28 | Minnesota Mining And Manufacturing Company | Surface colony counting device and method of use |
| US5976827A (en) * | 1997-12-12 | 1999-11-02 | Akzo Nobel, N.V. | Sensor device for detecting microorganisms and method therefor |
| US5912115A (en) | 1997-12-12 | 1999-06-15 | Akzo Nobel, N.V. | Evacuated sensor device for detecting microorganisms in blood samples, and method thereof |
-
1997
- 1997-12-12 US US08/989,560 patent/US5976827A/en not_active Expired - Lifetime
-
1998
- 1998-12-10 WO PCT/US1998/026376 patent/WO1999029831A1/en not_active Application Discontinuation
- 1998-12-10 KR KR1019997007313A patent/KR20000071045A/ko not_active Application Discontinuation
- 1998-12-10 CA CA002280697A patent/CA2280697A1/en not_active Abandoned
- 1998-12-10 AU AU17241/99A patent/AU752954B2/en not_active Ceased
- 1998-12-10 EP EP98962077A patent/EP1003836A4/en not_active Withdrawn
- 1998-12-10 JP JP53172799A patent/JP4183288B2/ja not_active Expired - Lifetime
-
1999
- 1999-05-27 US US09/320,386 patent/US6197577B1/en not_active Expired - Lifetime
-
2000
- 2000-12-18 US US09/741,402 patent/US6777226B2/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| KR20000071045A (ko) | 2000-11-25 |
| US6777226B2 (en) | 2004-08-17 |
| WO1999029831A1 (en) | 1999-06-17 |
| AU752954B2 (en) | 2002-10-03 |
| CA2280697A1 (en) | 1999-06-17 |
| US6197577B1 (en) | 2001-03-06 |
| EP1003836A4 (en) | 2006-01-04 |
| US5976827A (en) | 1999-11-02 |
| JP2001511654A (ja) | 2001-08-14 |
| AU1724199A (en) | 1999-06-28 |
| US20030100104A1 (en) | 2003-05-29 |
| EP1003836A1 (en) | 2000-05-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4183288B2 (ja) | 微生物を検出するためのセンサー器具、及びそのための方法 | |
| US5912115A (en) | Evacuated sensor device for detecting microorganisms in blood samples, and method thereof | |
| US7183073B2 (en) | Method for detecting microorganisms | |
| US6416969B2 (en) | Susceptibility plates for microbial antibiotic susceptibility testing | |
| EP0333253B1 (en) | Apparatus and device for detecting microorganisms | |
| KR0183402B1 (ko) | 미생물의 검출방법 및 장치 | |
| US5217876A (en) | Method for detecting microorganisms | |
| KR100436473B1 (ko) | 미생물검출장치및방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20051208 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20070529 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20070523 Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20070524 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20070822 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20071001 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20071112 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080108 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20080404 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20080519 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080704 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080819 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20080902 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110912 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110912 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120912 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130912 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |