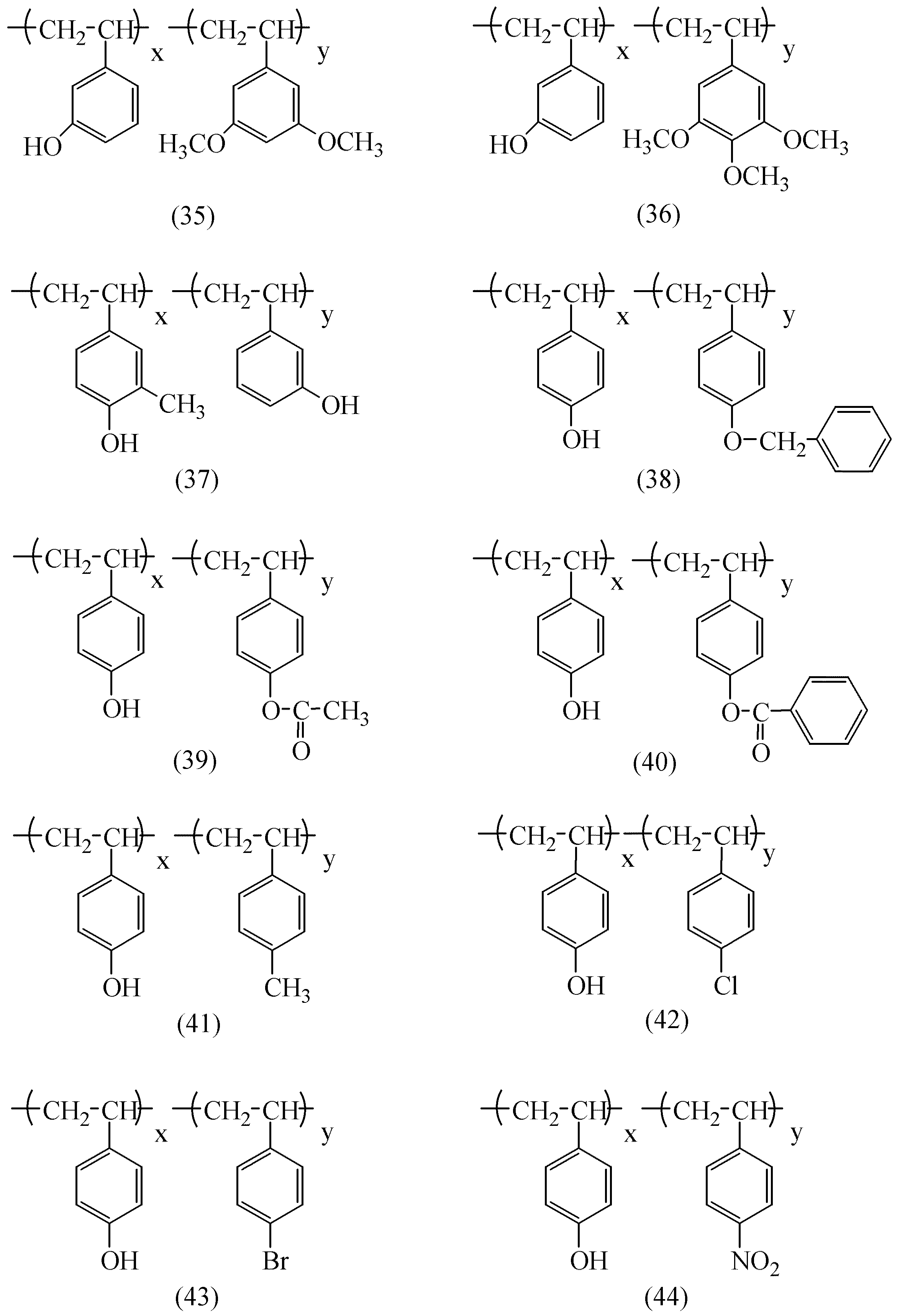JP4149122B2 - 電子線又はx線用ネガ型レジスト組成物 - Google Patents
電子線又はx線用ネガ型レジスト組成物 Download PDFInfo
- Publication number
- JP4149122B2 JP4149122B2 JP2000219253A JP2000219253A JP4149122B2 JP 4149122 B2 JP4149122 B2 JP 4149122B2 JP 2000219253 A JP2000219253 A JP 2000219253A JP 2000219253 A JP2000219253 A JP 2000219253A JP 4149122 B2 JP4149122 B2 JP 4149122B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- substituent
- electron beam
- resin
- hydrogen atom
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 C*c(cc(c(B=I)c1)F)c1F Chemical compound C*c(cc(c(B=I)c1)F)c1F 0.000 description 2
Classifications
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0045—Photosensitive materials with organic non-macromolecular light-sensitive compounds not otherwise provided for, e.g. dissolution inhibitors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C229/00—Compounds containing amino and carboxyl groups bound to the same carbon skeleton
- C07C229/02—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton
- C07C229/04—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being acyclic and saturated
- C07C229/06—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being acyclic and saturated having only one amino and one carboxyl group bound to the carbon skeleton
- C07C229/18—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being acyclic and saturated having only one amino and one carboxyl group bound to the carbon skeleton the nitrogen atom of the amino group being further bound to carbon atoms of six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/62—Oxygen or sulfur atoms
- C07D213/63—One oxygen atom
- C07D213/64—One oxygen atom attached in position 2 or 6
- C07D213/643—2-Phenoxypyridines; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/04—Ortho-condensed systems
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0046—Photosensitive materials with perfluoro compounds, e.g. for dry lithography
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/038—Macromolecular compounds which are rendered insoluble or differentially wettable
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/038—Macromolecular compounds which are rendered insoluble or differentially wettable
- G03F7/0382—Macromolecular compounds which are rendered insoluble or differentially wettable the macromolecular compound being present in a chemically amplified negative photoresist composition
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/039—Macromolecular compounds which are photodegradable, e.g. positive electron resists
- G03F7/0392—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition
- G03F7/0397—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition the macromolecular compound having an alicyclic moiety in a side chain
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- General Physics & Mathematics (AREA)
- Materials For Photolithography (AREA)
- Exposure And Positioning Against Photoresist Photosensitive Materials (AREA)
- Polymerisation Methods In General (AREA)
- Macromonomer-Based Addition Polymer (AREA)
Description
【発明の属する技術分野】
本発明は、超LSIや高容量マイクロチップの製造などの超マイクロリソグラフィプロセスやその他のフォトファブリケーションプロセスに好適に用いられるネガ型レジスト組成物に関するものである。さらに詳しくは、X線、電子線等を使用して高精細化したパターン形成しうるネガ型フォトレジスト組成物に関するものであり、特に電子線等の高エネルギー線を用いる半導体素子の微細加工に好適に用いることのできるネガ型レジスト組成物に関する。
【0002】
【従来の技術】
集積回路はその集積度を益々高めており、超LSIなどの半導体基板の製造に於いてはハーフミクロン以下の線幅から成る超微細パターンの加工が必要とされるようになってきた。その必要性を満たすためにフォトリソグラフィーに用いられる露光装置の使用波長は益々短波化し、今では、遠紫外光やエキシマレーザー光(XeCl、KrF、ArFなど)が検討されるまでになってきている。更に、電子線あるいはX線により更に微細なパターン形成が検討されるに至っている。
【0003】
特に電子線あるいはX線は次世代もしくは次々世代のパターン形成技術として位置付けられ、高感度、高解像かつ矩形なプロファイル形状を達成し得るネガ型レジストの開発が望まれている。
電子線リソグラフィーは、加速された電子線がレジスト材料を構成する原子と衝突散乱を起こす過程で化合物にエネルギーを供給し、レジスト材料の反応を生起し画像を形成させるものである。高加速化した電子線を用いることで直進性が増大し、電子散乱の影響が少なくなり高解像で矩形な形状のパターン形成が可能となるが、一方では電子線の透過性が高くなり、感度が低下してしまう。この様に、電子線リソグラフィーにおいては、感度と解像性・レジスト形状がトレードオフの関係にあり、これを如何に両立し得るかが課題であった。
これらに対するレジスト材料としては、感度を向上させる目的で、主に酸触媒反応を利用した化学増幅型レジストが用いられ、ネガ型レジストに対しては主成分として、アルカリ可溶性樹脂、酸発生剤、及び酸架橋剤から成る化学増幅型組成物が有効に使用されている。
【0004】
従来よりネガ化学増幅型レジストに対し、種々のアルカリ可溶性樹脂が提案されてきた。例えば特許第2505033号、特開平3−170554号、特開平6−118646にはノボラック型フェノール樹脂、特開平7−311463号、特開平8−292559号には分子量分布を狭めたポリビニルフェノール樹脂、特開平3−87746号、特開平8−44061号には水素添加により一部環状アルコール構造に変換したフェノール樹脂、特開平7−295200号、特開平8−152717号にはポリビニルフェノールのOH基の一部をアルキル基で保護した樹脂、特開平8−339086号にはアシル基等の酸に不活性な保護基を有するポリビニルフェノール樹脂、特開平6−67431号、特開平10−10733号にはスチレンと共重合したポリビニルフェノール樹脂、特開平9−166870号には(メタ)アクリレートモノマー類と共重合したポリビニルフェノール樹脂、更に特開平8−240911号にはカルボキシ基を有する樹脂が開示されている。
【0005】
また酸発生剤については、特公平8−3635号には有機ハロゲン化合物、特開平2−52348号にはBr、Clが置換した芳香族化合物、特開平4−367864号、特開平4−367865号にはBr、Clが置換したアルキル基、アルコキシ基を有する芳香族化合物、特開平2−150848号、特開平6−199770号にはヨードニウム、スルホニウム化合物、特開平3−87746号にはハロアルカンスルホネート化合物、特開平4−210960号、特開平4−217249号にはジアゾジスルホン化合物、又はジアゾスルホン化合物、特開平4−336454号にはBr、I置換アルキルトリアジン化合物、特開平4−291258号にはスルホンアミド、スルホンイミド化合物、特開平4−291259号には多価フェノールのスルホン酸化合物、特開平4−291260号、特開平4−291261号、特開平6−202320号にはナフトキノンジアジド−4−スルホネート化合物、特開平5−210239号にはジスルホン化合物、特開平6−236024号にはN−オキシイミドスルホネート化合物、米国特許第5344742号にはベンジルスルホネート化合物等が開示されている。
【0006】
更に酸架橋剤に対しては、特開平3−75652号、特開平5−181277号、特開平7−146556号にはメトキシメチルメラミン化合物、特開平4−281455号、特開平5−232702号、特開平6−83055号にはアルコキシメチルエーテル基を有する化合物、特開平5−281715号にはオキサジン化合物、特開平5−134412号、特開平6−3825号にはアルコキシアルキル基を有する芳香族化合物、特開平6−194838号にはトリオキサン化合物の他、特開平1−293339号記載のアルコキシメチルウリル化合物等が開示されている。
但しこれらの化合物の何れの組み合わせにおいても、高加速電圧条件化での電子線照射下やX線照射下で十分な高感度を得ることは困難であり、且つ感度と解像度、レジスト形状を満足し得るレベルで両立させることは課題となっていた。
【0007】
【発明が解決しようとする課題】
従って、本発明の目的は、電子線又はX線を使用する半導体素子の微細加工における性能向上技術の課題を解決することであり、電子線又はX線の使用に対して感度と解像度、レジスト形状の特性を満足する電子線又はX線用ネガ型化学増幅系レジスト組成物を提供することである。
更に半導体素子の量産性に適合した次世代EB照射装置(スループットの向上を目指した、EBブロック照射機又はEBステッパー(逐次縮小投映照射機))に対応できる、高感度を示す電子線又はX線用ネガ型化学増幅系レジスト組成物を提供することである。
【0008】
【課題を解決するための手段】
本発明者等は、上記諸特性に留意し鋭意検討した結果、本発明の目的が以下の特定の組成物を使用することで見事に達成されることを見出し、本発明に到達した。
即ち、本発明は下記構成である。
【0009】
(1)
(A)電子線又はX線の照射により、ラジカル種を発生する、下記一般式(I)〜(III)で表される化合物、
(B)水不溶でアルカリ水溶液に可溶な樹脂、
(C)ラジカルにより重合可能な不飽和結合を少なくとも1個有する化合物、
を含有することを特徴とする電子線又はX線用ネガ型レジスト組成物。
【化5】
一般式(I)〜一般式(III)中、
R1〜R37は、水素原子、アルキル基、アルコキシ基、ヒドロキシル基、ハロゲン原子、または、−S−R38で示すことができる基である。R38は、アルキル基、又はアリール基である。R1〜R15で示す基、R16〜R27で示す基、R28〜R37で示す基は、各々それらのうちの2つ以上が結合し、環を形成していてもよい。
X-は、アリールスルホン酸アニオンを表す。
(2)
X-のアリールスルホン酸アニオンが、フッ素原子および/またはアルキル基、アルコキシ基、アシル基、アシロキシ基、スルホニル基、スルホニルオキシ基、スルホニルアミノ基、アリール基、アラルキル基、アルコキシカルボニル基、からなる群から選択された少なくとも1種の有機基を有し、該有機基がフッ素原子で置換された有機基である、前記(1)に記載の電子線又はX線用ネガ型レジスト組成物。
【0010】
(3)
(B)成分の樹脂が、一般式(a1)で表される繰り返し単位を含有する樹脂であることを特徴とする前記(1)または(2)に記載の電子線又はX線用ネガ型レジスト組成物。
【0011】
【化4】
【0012】
式中、R1は水素原子、ハロゲン原子、シアノ基、置換基を有していても良い、アルキル基又はハロアルキル基を表す。R2は水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アリール基、アラルキル基、あるいはアシル基を表す。R3、R4は同じでも異なっていても良く、水素原子、ハロゲン原子、シアノ基、又は置換基を有していても良い、アルキル基、シクロアルキル基、アルケニル基、アラルキル基、もしくはアリール基を表す。
Aは単結合、置換基を有しても良い、アルキレン基、アルケニレン基、シクロアルキレン基、もしくはアリーレン基、又は−O−、−SO2−、−O−CO−R5−、−CO−O−R6−、−CO−N(R7)−R8−を表す。
R5、R6、R8は同じでも異なっていても良く、単結合、置換基を有しても良い、アルキレン基、アルケニレン基、シクロアルキレン基、もしくはアリーレン基の単独、又はこれらの基とエーテル構造、エステル構造、アミド構造、ウレタン構造もしくはウレイド構造の群より選択される少なくとも1種が一緒になって形成した2価の基を表す。
R7は同じでも異なっていても良く、水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アラルキル基、又はアリール基を表す。
lは1〜3の整数を表す。また複数のR2、又はR2とR3もしくはR4が結合して環を形成しても良い。
【0013】
(4)
(B)成分の樹脂が、ラジカルにより重合可能な不飽和結合を少なくとも1個有する樹脂であることを特徴とする前記(1)〜(3)のいずれかに記載の電子線又はX線用ネガ型レジスト組成物。
【0014】
(5)
(B)成分の樹脂が、一般式(a2)の繰り返し単位を含有する樹脂であることを特徴とする前記(1)〜(4)のいずれかに記載の電子線又はX線用ネガ型レジスト組成物。
【0015】
【化5】
【0016】
式中、R9は水素原子、ハロゲン原子、シアノ基、置換基を有していても良い、アルキル基又はハロアルキル基を表す。
R10〜R12は水素原子、一般式(b)、(c)、又は(d)の何れかの基、置換基を有していても良い、アルキル基、シクロアルキル基、アリール基、アラルキル基、あるいはアシル基を表す。
R13、R14は同じでも異なっていても良く、水素原子、ヒドロキシル基、ハロゲン原子、シアノ基、又は置換基を有していても良い、アルキル基、シクロアルキル基、アルケニル基、アラルキル基、もしくはアリール基を表す。
【0017】
【化6】
【0018】
式中、R15〜R20、R24、R25は水素原子、ハロゲン原子、シアノ基、置換基を有していても良い、アルキル基又はハロアルキル基を表す。
R21、R22は水素原子、ハロゲン原子、ヒドロキシ基、置換基を有していても良い、アルキル基、アルコキシ基、アシロキシ基を表す。
R23は水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アラルキル基、又はアリール基を表す。
A1は単結合、置換基を有しても良い、2価のアルキレン基、アルケニレン基、シクロアルキレン基、もしくはアリーレン基、又は−O−、−SO2−、−O−CO−R26−、−CO−O−R27−、−CO−N(R28)−R29−を表す。
R26、R27、R29は同じでも異なっていても良く、単結合、又はエーテル構造、エステル構造、アミド構造、ウレタン構造もしくはウレイド構造を有しても良い、また置換基を有しても良い、2価のアルキレン基、アルケニレン基、シクロアルキレン基、アリーレン基を表す。
R28は水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アラルキル基、又はアリール基を表す。
A2は単結合、−O−R27−、−N(R28)−R29−を表す。
A3は単結合、−SO2−もしくはアルキレン構造を有しても良い、また置換基を有しても良い、アリーレン基を表す。
A4は単結合、置換基を有しても良い、2価のアルキレン基、シクロアルキレン基、アリーレン基、−O−、−SO2−、−CO−、−CO−O−R21−を表す。
x、y、zは0又は1を表し、m、nは0又は1以上の整数を表す。
但し、一般式(a2)中、少なくとも一つは一般式(b)、(c)、もしくは(d)の基を有する。またR10〜R12のうちの二つ、又はR10〜R12の一つとR13もしくはR14が結合して環を形成しても良い。
【0019】
(6)
(A)成分の化合物が、スルホニウム、又はヨードニウムのスルホン酸塩化合物から選択されることを特徴とする前記(1)〜(5)のいずれかに記載の電子線又はX線用ネガ型レジスト組成物。
【0020】
(7)
75keV以上の加速電圧条件下で電子線照射することを特徴とする前記(1)〜(6)のいずれかに記載の電子線又はX線用ネガ型レジスト組成物。
(8)
前記(1)〜(7)のいずれかに記載の電子線又はX線用ネガ型レジスト組成物によりレジスト膜を形成し、当該レジスト膜に電子線又はX線を照射し、現像することを特徴とするパターン形成方法。
【0021】
【発明の実施の形態】
以下、本発明に使用する化合物について詳細に説明する。
(1)本発明(B)水不溶でアルカリ水溶液に可溶な樹脂、(以下、アルカリ可溶性樹脂ともいう)
本発明においてアルカリ可溶性樹脂は、これまでネガ化学増幅型レジストで開示されたフェノールノボラック樹脂、ポリビニルフェノール樹脂、ビニルフェノール由来の構造単位を有する共重合体、及びポリビニルフェノール樹脂を一部保護又は修飾することで得られる樹脂等、フェノール骨格を有するポリマーの他、カルボキシル基を有する樹脂等を広く使用することができる。
好ましくは上記一般式(a1)で表される繰り返し構造単位を含有するフェノール樹脂を挙げることができる。
【0022】
一般式(a1)中、 R1は水素原子、ハロゲン原子、シアノ基、置換基を有していても良い、アルキル基又はハロアルキル基を表す。
R2は水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アリール基、アラルキル基、あるいはアシル基を表す。
R3、R4は同じでも異なっていても良く、水素原子、ハロゲン原子、シアノ基、又は置換基を有していても良い、アルキル基、シクロアルキル基、アルケニル基、アラルキル基、もしくはアリール基を表す。
Aは単結合、置換基を有しても良い、2価のアルキレン基、アルケニレン基、シクロアルキレン基、もしくはアリーレン基、又は−O−、−SO2−、−O−CO−R5−、−CO−O−R6−、−CO−N(R7)−R8−を表す。
【0023】
R5、R6、R8は同じでも異なっていても良く、単結合、置換基を有しても良い、アルキレン基、アルケニレン基、シクロアルキレン基、もしくはアリーレン基の単独、又はこれらの基とエーテル構造、エステル構造、アミド構造、ウレタン構造もしくはウレイド構造の群より選択される少なくとも1種が一緒になって形成した2価の基を表す。
R7は同じでも異なっていても良く、水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アラルキル基、又はアリール基を表す。
lは1〜3の整数を表す。また複数のR2、又はR2とR3もしくはR4が結合して環を形成しても良い。
【0024】
(B)アルカリ可溶性樹脂は、好ましくは、ラジカルにより重合可能な不飽和結合を少なくとも1個有する水不溶でアルカリ水溶液に可溶な樹脂であり、フェノールノボラック樹脂、ポリビニルフェノール樹脂、ビニルフェノール由来の構造単位を有する共重合体、ポリビニルフェノール樹脂をラジカルにより重合可能な不飽和結合を有する基で一部保護又は修飾することで得られる樹脂、フェノール骨格を有する(メタ)アクリレートポリマー等のフェノール基の一部又は全部をラジカルにより重合可能な不飽和結合を有する基で置換した樹脂、並びにカルボキシル基を含む構造単位を有する樹脂のカルボキシル基をラジカルにより重合可能な不飽和結合を有する基で一部保護又は修飾することで得られる樹脂等を広く使用することができる。
(B)アルカリ可溶性樹脂としては、更に好ましくは、上記一般式(a2)で表される繰り返し構造単位を含有するフェノール系の樹脂を挙げることができる。
【0025】
一般式(a2)中、R9は水素原子、ハロゲン原子、シアノ基、置換基を有していても良い、アルキル基又はハロアルキル基を表す。
R10〜R12は水素原子、一般式(b)、(c)、又は(d)の何れかの基、置換基を有していても良い、アルキル基、シクロアルキル基、アリール基、アラルキル基、あるいはアシル基を表す。
R13、R14は同じでも異なっていても良く、水素原子、ハロゲン原子、シアノ基、又は置換基を有していても良い、アルキル基、シクロアルキル基、アルケニル基、アラルキル基、もしくはアリール基を表す。
【0026】
R15〜R20、R24、R25は水素原子、ハロゲン原子、シアノ基、置換基を有していても良い、アルキル基又はハロアルキル基を表す。
R21、R22は水素原子、ハロゲン原子、ヒドロキシ基、置換基を有していても良い、アルキル基、アルコキシ基、アシロキシ基を表す。
R23は水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アラルキル基、又はアリール基を表す。
【0027】
A1は単結合、置換基を有しても良い、2価のアルキレン基、アルケニレン基、シクロアルキレン基、もしくはアリーレン基、又は−O−、−SO2−、−O−CO−R26−、−CO−O−R27−、−CO−N(R28)−R29−を表す。
R26、R27、R29は同じでも異なっていても良く、単結合、又はエーテル基、エステル基、アミド基、ウレタン基もしくはウレイド基を有しても良い、また置換基を有しても良い、2価のアルキレン基、アルケニレン基、シクロアルキレン基、アリーレン基を表す。
R22は水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アラルキル基、又はアリール基を表す。
【0028】
A2は単結合、−O−R27−、−N(R28)−R29−を表す。
A3は単結合、置換基を有しても良い、アリーレン基を表す。
A4は単結合、置換基を有しても良い、2価のアルキレン基、シクロアルキレン基、アリーレン基、−O−、−SO2−、−CO−、−CO−O−R27−を表す。
x、y、zは0又は1を表し、m、nは0又は1以上の整数を表す。
但し、一般式(a2)中、少なくとも一つは一般式(b)、(c)、もしくは(d)の基を有する。またR10〜R12のうちの二つ、又はR10〜R12の一つとR13もしくはR14が結合して環を形成しても良い。
【0029】
また上記一般式において、R1〜R4、R7、R9〜R25、R28のアルキル基としては、例えば炭素数1〜8個のアルキル基であって、具体的には、メチル基、エチル基、プロピル基、n−ブチル基、sec−ブチル基、ヘキシル基、2−エチルヘキシル基、オクチル基を好ましく挙げることができる。
R2〜R4、R7、R10〜R14、R23、R28のシクロアルキル基は単環型でも良く、多環型でも良い。
単環型としては炭素数3〜8個の例えば、シクロプロピル基、シクロペンチル基、シクロヘキシル基を好ましく挙げることができる。
多環型としては例えば、アダマンチル基、ノルボルニル基、イソボロニル基、ジシクロペンチル基、a−ピネル基、トリシクロデカニル基等を好ましく挙げることができる。
【0030】
R3、R4、R13、R14のアルケニル基としては、例えば炭素数2〜8個のアルケニル基であって、具体的には、ビニル基、アリル基、ブテニル基、シクロヘキセニル基を好ましく挙げることができる。
R2〜R4、R7、R10〜R14、R23、R28のアリール基としては、例えば炭素数6〜15個のアリール基であって、具体的には、フェニル基、トリル基、ジメチルフェニル基、2,4,6−トリメチルフェニル基、ナフチル基、アントリル基等を好ましく挙げることができる。
【0031】
R2〜R4、R7、R10〜R14、R23、R28のアラルキル基としては、例えば炭素数7〜12個のアラルキル基であって、具体的には、ベンジル基、フェネチル基、ナフチルメチル基等を好ましく挙げることができる。
R1、R9、R15〜R20、R24、R25のハロアルキル基としては、例えば炭素数1〜4個のハロアルキル基であって、具体的にはクロロメチル基、クロロエチル基、クロロプロピル基、クロロブチル基、ブロモメチル基、ブロモエチル基等を好ましく挙げることができる。
【0032】
R2、R10〜R12のアシル基としては、例えば炭素数1〜10個のアシル基であって、ホルミル基、アセチル基、プロパノイル基、ブタノイル基、ピバロイル基、ベンゾイル基等を好ましく挙げることができる。
R21、R22のアルコキシ基としては、例えば炭素数1〜8個のアルコキシ基であって、メトキシ基、エトキシ基、プロポキシ基、ブトキシ基等を好ましく挙げることができる。アシロキシ基としては、例えば炭素数1〜10個のアシロキシ基であって、アセトキシ基、プロパノイルオキシ基、ベンゾイルオキシ基等を好ましく挙げることができる。
【0033】
A、R5、R6、R8、A1、A4、R26、R27、R29のアルキレン基としては、例えば炭素数1〜8個のアルキレン基であって、メチレン基、エチレン基、プロピレン基、ブチレン基、ヘキシレン基、オクチレン基等を好ましく挙げることができる。
A、R5、R6、R8、A1、R26、R27、R29のアルケニレン基としては、例えば炭素数2〜6個のアルケニレン基であって、エテニレン基、プロペニレン基、ブテニレン基等を好ましく挙げることができる。
【0034】
A、R5、R6、R8、A1、A4、R26、R27、R29のシクロアルキレン基としては、例えば炭素数5〜8個のシクロアルキレン基であって、シクロペンチレン基、シクロヘキシレン基等を好ましく挙げることができる。
A、R5、R6、R8、A1、A3、A4、R26、R27、R29のアリーレン基としては、例えば炭素数6〜12個のアリーレン基であって、フェニレン基、トリレン基、キシリレン基、ナフチレン基等を好ましく挙げることができる。
【0035】
更にこれらの基に置換される置換基としては、アミノ基、アミド基、ウレイド基、ウレタン基、ヒドロキシル基、カルボキシル基等の活性水素を有するものや、ハロゲン原子(フッ素原子、塩素原子、臭素原子、沃素原子)、アルコキシ基(メトキシ基、エトキシ基、プロポキシ基、ブトキシ基等)、チオエーテル基、アシル基(アセチル基、プロパノイル基、ベンゾイル基等)、アシロキシ基(アセトキシ基、プロパノイルオキシ基、ベンゾイルオキシ基等)、アルコキシカルボニル基(メトキシカルボニル基、エトキシカルボニル基、プロポキシカルボニル基等)、シアノ基、ニトロ基等が挙げられる。特にアミノ基、ヒドロキシル基、カルボキシル基等の活性水素を有するものが好ましい。
【0036】
また複数のR2、又はR2とR3もしくはR4、R10〜R12のうちの二つ、又はR10〜R12の一つとR13もしくはR14が結合して形成した環としては、ベンゾフラン環、ベンゾジオキソノール環、ベンゾピラン環等の酸素原子を含有する4〜7員環が挙げられる。
【0037】
本発明(B)の樹脂は、一般式(a1)、(a2)の繰り返し構造単位からのみなる樹脂であっても良いが、更に本発明のネガ型レジストの性能を向上させる目的で、他の重合性モノマーを共重合させても良い。
【0038】
使用することができる共重合モノマーとしては、以下に示すものが含まれる。例えば、上記以外のアクリル酸エステル類、アクリルアミド類、メタクリル酸エステル類、メタクリルアミド類、アリル化合物、ビニルエーテル類、ビニルエステル類、スチレン類、クロトン酸エステル類などから選ばれる付加重合性不飽和結合を1個有する化合物である。
【0039】
具体的には、例えばアクリル酸エステル類、例えばアルキル(アルキル基の炭素原子数は1〜10のものが好ましい)アクリレート(例えば、アクリル酸メチル、アクリル酸エチル、アクリル酸プロピル、アクリル酸t−ブチル、アクリル酸アミル、アクリル酸シクロヘキシル、アクリル酸エチルヘキシル、アクリル酸オクチル、アクリル酸−t−オクチル、クロルエチルアクリレート、2−ヒドロキシエチルアクリレート2,2−ジメチルヒドロキシプロピルアクリレート、5−ヒドロキシペンチルアクリレート、トリメチロールプロパンモノアクリレート、ペンタエリスリトールモノアクリレート、グリシジルアクリレート、ベンジルアクリレート、フルフリルアクリレート、テトラヒドロフルフリルアクリレート、など)アリールアクリレート(例えばフェニルアクリレートなど);
【0040】
メタクリル酸エステル類、例えば、アルキル(アルキル基の炭素原子数は1〜10のものが好ましい)メタクリレート(例えば、メチルメタクリレート、エチルメタクリレート、プロピルメタクリレート、イソプロピルメタクリレート、t−ブチルメタクリレート、アミルメタクリレート、ヘキシルメタクリレート、シクロヘキシルメタクリレート、ベンジルメタクリレート、クロルベンジルメタクリレート、オクチルメタクリレート、2−ヒドロキシエチルメタクリレート、4−ヒドロキシブチルメタクリレート、5−ヒドロキシペンチルメタクリレート、2,2−ジメチル−3−ヒドロキシプロピルメタクリレート、トリメチロールプロパンモノメタクリレート、ペンタエリスリトールモノメタクリレート、グリシジルメタクリレート、フルフリルメタクリレート、テトラヒドロフルフリルメタクリレートなど)、アリールメタクリレート(例えば、フェニルメタクリレート、クレジルメタクリレート、ナフチルメタクリレートなど);
【0041】
アクリルアミド類、例えば、アクリルアミド、N−アルキルアクリルアミド、(アルキル基としては、炭素原子数1〜10のもの、例えば、メチル基、エチル基、プロピル基、ブチル基、t−ブチル基、ヘプチル基、オクチル基、シクロヘキシル基、ベンジル基、ヒドロキシエチル基、ベンジル基などがある。)、N−アリールアクリルアミド(アリール基としては、例えばフェニル基、トリル基、ニトロフェニル基、ナフチル基、シアノフェニル基、ヒドロキシフェニル基、カルボキシフェニル基などがある。)、N,N−ジアルキルアクリルアミド(アルキル基としては、炭素原子数1〜10のもの、例えば、メチル基、エチル基、ブチル基、イソブチル基、エチルヘキシル基、シクロヘキシル基などがある。)、N,N−ジアリールアクリルアミド(アリール基としては、例えばフェニル基などがある。)、N−メチル−N−フェニルアクリルアミド、N−ヒドロキシエチル−N−メチルアクリルアミド、N−2−アセトアミドエチル−N−アセチルアクリルアミドなど;
【0042】
メタクリルアミド類、例えば、メタクリルアミド、N−アルキルメタクリルアミド(アルキル基としては、炭素原子数1〜10のもの、例えば、メチル基、エチル基、t−ブチル基、エチルヘキシル基、ヒドロキシエチル基、シクロヘキシル基などがある。)、N−アリールメタクリルアミド(アリール基としては、フェニル基などがある。)、N,N−ジアルキルメタクリルアミド(アルキル基としては、エチル基、プロピル基、ブチル基などがある。)、N,N−ジアリールメタクリルアミド(アリール基としては、フェニル基などがある。)、N−ヒドロキシエチル−N−メチルメタクリルアミド、N−メチル−N−フェニルメタクリルアミド、N−エチル−N−フェニルメタクリルアミドなど;アリル化合物、例えば、アリルエステル類(例えば、酢酸アリル、カプロン酸アリル、カプリル酸アリル、ラウリン酸アリル、パルミチン酸アリル、ステアリン酸アリル、安息香酸アリル、アセト酢酸アリル、乳酸アリルなど)、アリルオキシエタノールなど;
【0043】
ビニルエーテル類、例えば、アルキルビニルエーテル(例えば、ヘキシルビニルエーテル、オクチルビニルエーテル、デシルビニルエーテル、エチルヘキシルビニルエーテル、メトキシエチルビニルエーテル、エトキシエチルビニルエーテル、クロルエチルビニルエーテル、1−メチル−2,2−ジメチルプロピルビニルエーテル、2−エチルブチルビニルエーテル、ヒドロキシエチルビニルエーテル、ジエチレングリコールビニルエーテル、ジメチルアミノエチルビニルエーテル、ジエチルアミノエチルビニルエーテル、ブチルアミノエチルビニルエーテル、ベンジルビニルエーテル、テトラヒドロフルフリルビニルエーテルなど)、ビニルアリールエーテル(例えばビニルフェニルエーテル、ビニルトリルエーテル、ビニルクロルフェニルエーテル、ビニル−2,4−ジクロルフェニルエーテル、ビニルナフチルエーテル、ビニルアントラニルエーテルなど);
【0044】
ビニルエステル類、例えば、ビニルブチレート、ビニルイソブチレート、ビニルトリメチルアセテート、ビニルジエチルアセテート、ビニルバレート、ビニルカプロエート、ビニルクロルアセテート、ビニルジクロルアセテート、ビニルメトキシアセテート、ビニルブトキシアセテート、ビニルフェニルアセテート、ビニルアセトアセテート、ビニルラクテート、ビニル−β−フェニルブチレート、ビニルシクロヘキシルカルボキシレート、安息香酸ビニル、サルチル酸ビニル、クロル安息香酸ビニル、テトラクロル安息香酸ビニル、ナフトエ酸ビニルなど;
【0045】
スチレン類、例えば、スチレン、アルキルスチレン(例えば、メチルスチレン、ジメチルスチレン、トリメチルスチレン、エチルスチレン、ジエチルスチレン、イソプロピルスチレン、ブチルスチレン、ヘキシルスチレン、シクロヘキシルスチレン、デシルスチレン、ベンジルスチレン、クロルメチルスチレン、トリフルオルメチルスチレン、エトキシメチルスチレン、アセトキシメチルスチレンなど)、アルコキシスチレン(例えば、メトキシスチレン、4−メトキシ−3−メチルスチレン、ジメトキシスチレンなど)、ハロゲンスチレン(例えば、クロルスチレン、ジクロルスチレン、トリクロルスチレン、テトラクロルスチレン、ペンタクロルスチレン、ブロムスチレン、ジブロムスチレン、ヨードスチレン、フルオルスチレン、トリフルオルスチレン、2−ブロム−4−トリフルオルメチルスチレン、4−フルオル−3−トリフルオルメチルスチレンなど)、カルボキシスチレン;
【0046】
クロトン酸エステル類、例えば、クロトン酸アルキル(例えば、クロトン酸ブチル、クロトン酸ヘキシル、グリセリンモノクロトネートなど);イタコン酸ジアルキル類(例えば、イタコン酸ジメチル、イタコン酸ジエチル、イタコン酸ジブチルなど);マレイン酸あるいはフマール酸のジアルキルエステル類(例えば、ジメチルマレレート、ジブチルフマレートなど)、無水マレイン酸、マレイミド、アクリロニトリル、メタクリロニトリル、マレイロニトリル等がある。その他、一般的には共重合可能である付加重合性不飽和化合物であればよい。
【0047】
この中で、カルボキシスチレン、N−(カルボキシフェニル)アクリルアミド、N−(カルボキシフェニル)メタクリルアミド等のようなカルボキシル基を有するモノマー、マレイミド等、アルカリ溶解性を向上させるモノマーが共重合成分として好ましい。
本発明における樹脂中の他の重合性モノマーの含有量としては、全繰り返し単位に対して、50モル%以下が好ましく、より好ましくは30モル%以下である。
【0048】
以下に一般式(a1)及び(a2)で表される繰り返し構造単位を有する樹脂の具体例を示すが、本発明がこれに限定されるものではない。
【0049】
【化7】
【0050】
【化8】
【0051】
【化9】
【0052】
【化10】
【0053】
【化11】
【0054】
【化12】
【0055】
【化13】
【0056】
【化14】
【0057】
【化15】
【0058】
【化16】
【0059】
上記具体例中のnは正の整数を表す。x、y、zは樹脂組成のモル比を表し、2成分からなる樹脂では、x=10〜95、y=5〜90、好ましくはx=40〜90、y=10〜60の範囲で使用される。3成分からなる樹脂では、 x=10〜90、y=5〜85、z=5〜85、好ましくはx=40〜80、y=10〜50、z=10〜50の範囲で使用される。
【0060】
【化17】
【0061】
【化18】
【0062】
【化19】
【0063】
【化20】
【0064】
【化21】
【0065】
【化22】
【0066】
【化23】
【0067】
【化24】
【0068】
【化25】
【0069】
【化26】
【0070】
【化27】
【0071】
【化28】
【0072】
m、n、oは樹脂組成のモル比を表し、2成分からなる樹脂では、m=10〜95、n=5〜90、好ましくはm=40〜90、n=10〜60の範囲で使用される。3成分からなる樹脂では、m=10〜90、n=5〜85、o=5〜85、好ましくはm=40〜80、n=10〜50、o=10〜50の範囲で使用される。
【0073】
上記(B)、好ましくは一般式(a1)又は(a2)で表される繰り返し構造単位を有する樹脂の好ましい分子量は重量平均で1,000〜200,000であり、更に好ましくは3,000〜50,000の範囲で使用される。分子量分布は1〜10であり、好ましくは1〜3、更に好ましくは1〜1.5の範囲のものが使用される。分子量分布が小さいものほど、解像度、レジスト形状、及びレジストパターンの側壁がスムーズであり、ラフネス性に優れる。
一般式(a1)又は(a2)で表される繰り返し構造単位の総含有量は、全体の樹脂に対して、5〜100モル%、好ましくは10〜90モル%である。
【0074】
本発明に用いられる一般式(a1)又は(a2)で表わされる構造単位を含有するアルカリ可溶性樹脂は、Macromolecules (1995), 28(11), 3787〜3789, Polym. Bull. (Berlin)(1990), 24(4), 385〜389,特開平8−286375に記載されている方法により合成することができる。即ち、ラジカル重合もしくはリビングアニオン重合法により目的のアルカリ可溶性樹脂を得ることができる。
これらの樹脂は1種で使用しても良いし、複数を混合して用いても良い。
【0075】
ここで、重量平均分子量はゲルパーミエーションクロマトグラフィーのポリスチレン換算値をもって定義される。
アルカリ可溶性樹脂のアルカリ溶解速度は、0.261Nテトラメチルアンモニウムハイドロオキサイド(TMAH)で測定(23℃)して20Å/秒以上のものが好ましい。特に好ましくは200Å/秒以上のものである。
本発明のアルカリ可溶性樹脂は、単独で用いても良いが、他のアルカリ可溶性樹脂を併用することもできる。使用比率は本発明のアルカリ可溶性樹脂100重量部に対して本発明以外の他のアルカリ可溶性樹脂を最大100重量部まで併用することができる。以下に併用できるアルカリ可溶性樹脂を例示する。
【0076】
例えばノボラック樹脂、水素化ノボラツク樹脂、アセトン−ピロガロール樹脂、スチレン−無水マレイン酸共重合体、カルボキシル基含有メタクリル系樹脂及びその誘導体を挙げることができるが、これらに限定されるものではない。
【0077】
樹脂(B)の添加量は組成物の全固形分に対し、30〜95重量%、好ましくは40〜90重量%、更に好ましくは50〜80重量%の範囲で使用される。
【0078】
(2)本発明(A)の電子線又はX線の照射により、ラジカル種を発生する化合物
本発明に使用される(A)成分は、電子線又はX線の照射によりラジカル種を発生する化合物であれば、何れの化合物でも用いることができる。
【0079】
そのような電子線又はX線の照射により、ラジカル種を発生する化合物としては、光ラジカル重合の光開始剤及びそれらの混合物を適宜に選択して使用することができる。
【0080】
また、これらの電子線又はX線の照射により、ラジカル種を発生する基、あるいは化合物をポリマーの主鎖または側鎖に導入した化合物、たとえば、特開昭63−26653号、特開昭55−164824号、特開昭62−69263号、特開昭63−146038号、特開昭63−163452号、特開昭62−153853号、特開昭63−146029号等に記載の化合物を用いることができる。
【0081】
また、公知のヨードニウム塩、スルホニウム塩、セレノニウム塩等のオニウム塩、有機ハロゲン化合物、N−イミノスルホネート化合物、N−イミドスルホネート化合物、ジスルホン化合物等を挙げることができる。
【0082】
好ましくは、スルホニウム、又はヨードニウムのスルホン酸塩化合物、N−ヒドロキシイミドのスルホン酸エステル化合物、又はジスルホン化合物である。
これらの本発明(A)の電子線又はX線の照射により、ラジカル種を発生する化合物中で特に好ましくは、特開平10−7653号、特開平11−2901号等に記載のN−イミドスルホネート化合物、更に下記一般式(I)〜(III)で表されるスルホニウム塩、ヨードニウム塩を挙げることができるが、下記一般式(I)〜(III)で表されるスルホニウム塩、ヨードニウム塩が一番好ましい。
尚、下記一般式(I)〜(III)で表されるスルホニウム塩、ヨードニウム塩は、電子線又はX線の照射により酸を発生する化合物であるが、本発明においては、電子線又はX線の照射によりラジカル種を発生する化合物の一例として用いている。
本発明の(A)電子線又はX線の照射により、ラジカル種を発生する化合物として、ラジカル種と同時に酸を発生する化合物も用いることができる。
【0083】
【化29】
【0084】
一般式(I)〜一般式(III)中のR1〜R37は、水素原子、アルキル基、アルコキシ基、ヒドロキシル基、ハロゲン原子、または、−S−R38で示すことができる基である。
R1〜R37が表すアルキル基は、直鎖状でもよく、分岐状でもよく、環状でもよい。直鎖状又は分岐状アルキル基としては、例えば、メチル基、エチル基、プロピル基、n−ブチル基、sec−ブチル基、t−ブチル基など、例えば炭素数1〜4個のアルキル基を挙げることができる。環状アルキル基としては、例えばシクロプロピル基、シクロペンチル基、シクロヘキシル基など炭素数3〜8個のアルキル基を挙げることができる。
【0085】
R1〜R37が表すアルコキシ基は、直鎖状でもよく、分岐状でもよく、環状アルコキシ基でもよい。直鎖状又は分岐状アルコキシ基としては、例えば炭素数1〜8個のもの例えばメトキシ基、エトキシ基、ヒドロキシエトキシ基、プロポキシ基、n−ブトキシ基、イソブトキシ基、sec−ブトキシ基、t−ブトキシ基、オクチルオキシ基などを挙げることができる。環状アルコキシ基としては、例えば、シクロペンチルオキシ基、シクロヘキシルオキシ基が挙げられる。
【0086】
環状アルコキシ基としては、例えば、シクロペンチルオキシ基、シクロヘキシルオキシ基が挙げられる。
R1〜R37が表すハロゲン原子としては、フッ素原子、塩素原子、臭素原子、沃素原子を挙げることができる。
R1〜R37が表す−S−R38中のR38は、アルキル基、又はアリール基である。R38が表すアルキル基の範囲としては、例えばR1〜R37が表すアルキル基として既に列挙したアルキル基中のいずれをも挙げることができる。
R38が表すアリール基は、フェニル基、トリル基、メトキシフェニル基、ナフチル基など、炭素数6〜14個のアリール基を挙げることができる。
【0087】
R1〜R38が表すアルキル基以下、アリール基までは、いずれも基の一部に更に置換基を結合して炭素数を増やしていてもよく、置換基を有していなくてもよい。更に結合していてもよい置換基としては、好ましくは、炭素数1〜4個のアルコキシ基、炭素数6〜10個のアリール基、炭素数2〜6個のアルケニル基を挙げることができ、シアノ基、ヒドロキシ基、カルボキシ基、アルコキシカルボニル基、ニトロ基等も挙げることができる。その他、ハロゲン原子でもよい。たとえば、フッ素原子、塩素原子、沃素原子を挙げることができる。
【0088】
一般式(I)中のR1〜R15で示す基は、そのうちの2つ以上が結合し、環を 形成していてもよい。環は、R1〜R15で示す基の末端が直接結合して形成して もよい。炭素、酸素、イオウ、及び窒素から選択される1種又は2種以上の元素を介して間接的に結びあい、環を形成していてもよい。R1〜R15のうちの2つ以上が結合して形成する環構造としては、フラン環、ジヒドロフラン環、ピラン環、トリヒドロピラン環、チオフェン環、ピロール環などに見られる環構造と同一の構造を挙げることができる。一般式(II)中のR16〜R27についても同様のことを言うことができる。2つ以上が直接又は間接に結合し、環を形成していてもよい。一般式(III)中のR28〜R37についても同様である。
【0089】
一般式(I)〜(III)はX-を有する。一般式(I)〜(III)が有するX-は、酸のアニオンである。アニオンを形成している酸は、カルボン酸、スルホン酸などのpKa値が7以下の有機酸である。カルボン酸としては、置換基を有していても良い直鎖状、分岐状又は環状のアルキルカルボン酸、アリールカルボン酸(好ましくは安息香酸、ナフタレンカルボン酸、アントラセンカルボン酸)が挙げられる。
スルホン酸としては、置換基を有していても良い直鎖状、分岐状又は環状のアルキルスルホン酸、アリールスルホン酸(好ましくはベンゼンスルホン酸、ナフタレンスルホン酸、アントラセンスルホン酸)が挙げられる。これらの酸には1以上のフッ素原子が置換していることが好ましい。
【0090】
又はその酸は、そのフッ素原子とともにあるいはフッ素原子に代え、アルキル基、アルコキシ基、アシル基、アシロキシ基、スルホニル基、スルホニルオキシ基、スルホニルアミノ基、アリール基、アラルキル基、アルコキシカルボニル基、からなる群から選択された少なくとも1種の有機基を有し、しかも、その有機基は少なくとも1個のフッ素原子を更に置換している。
また、上記のベンゼンスルホン酸、ナフタレンスルホン酸、又はアントラセンスルホン酸は、フッ素以外のハロゲン原子、水酸基、ニトロ基等で置換されていても良い。
【0091】
X-のアニオンを形成する酸に結合するアルキル基は、例えば炭素数1〜12のアルキル基である。アルキル基は、直鎖状でもよく、分岐状でもよく、環状でもよく、少なくとも1個のフッ素原子、好ましくは25個以下のフッ素原子で置換されているものが好ましい。
具体的にはトリフロロメチル基、ペンタフロロエチル基、2,2,2−トリフロロエチル基、ヘプタフロロプロピル基、ヘプタフロロイソプロピル基、パーフロロブチル基、パーフロロオクチル基、パーフロロドデシル基、パーフロロシクロヘキシル基等を挙げることができる。なかでも、全てフッ素で置換された炭素数1〜4のパーフロロアルキル基が好ましい。
【0092】
X-のアニオンを形成する酸に結合するアルコキシ基は、炭素数が1〜12のアルコキシ基である。アルコキシ基は、直鎖状でもよく、分岐状でもよく、環状でもよく、少なくとも1個のフッ素原子、好ましくは25個以下のフッ素原子で置換されているものが好ましい。
具体的にはトリフロロメトキシ基、ペンタフロロエトキシ基、ヘプタフロロイソプロピルオキシ基、パーフロロブトキシ基、パーフロロオクチルオキシ基、パーフロロドデシルオキシ基、パーフロロシクロヘキシルオキシ基等を挙げることができる。なかでも、全てフッ素で置換された炭素数1〜4のパーフロロアルコキシ基が好ましい。
【0093】
X-のアニオンを形成する酸に結合するアシル基は、炭素数2〜12、1〜23個のフッ素原子で置換されているものが好ましい。具体的にはトリフロロアセチル基、フロロアセチル基、ペンタフロロプロピオニル基、ペンタフロロベンゾイル基等を挙げることができる。
【0094】
X-のアニオンを形成する酸に結合するアシロキシ基は、炭素数が2〜12、1〜23個のフッ素原子で置換されているものが好ましい。具体的にはトリフロロアセトキシ基、フロロアセトキシ基、ペンタフロロプロピオニルオキシ基、ペンタフロロベンゾイルオキシ基等を挙げることができる。
X-のアニオンを形成する酸に結合するスルホニル基としては、炭素数が1〜12、1〜25個のフッ素原子で置換されているものが好ましい。具体的にはトリフロロメタンスルホニル基、ペンタフロロエタンスルホニル基、パーフロロブタンスルホニル基、パーフロロオクタンスルホニル基、ペンタフロロベンゼンスルホニル基、4−トリフロロメチルベンゼンスルホニル基等を挙げることができる。
【0095】
X-のアニオンを形成する酸に結合する上記スルホニルオキシ基としては、炭素数が1〜12、1〜25個のフッ素原子で置換されているものが好ましい。具体的にはトリフロロメタンスルホニルオキシ、パーフロロブタンスルホニルオキシ基、4−トリフロロメチルベンゼンスルホニルオキシ基等を挙げることができる。
X-のアニオンを形成する酸に結合する上記スルホニルアミノ基としては、炭素数が1〜12であって、1〜25個のフッ素原子で置換されているものが好ましい。具体的にはトリフロロメタンスルホニルアミノ基、パーフロロブタンスルホニルアミノ基、パーフロロオクタンスルホニルアミノ基、ペンタフロロベンゼンスルホニルアミノ基等を挙げることができる。
【0096】
X-のアニオンを形成する酸に結合する上記アリール基としては、炭素数が6〜14、1〜9個のフッ素原子で置換されているものが好ましい。具体的にはペンタフロロフェニル基、4−トリフロロメチルフェニル基、ヘプタフロロナフチル基、ノナフロロアントラニル基、4−フロロフェニル基、2,4−ジフロロフェニル基等を挙げることができる。
X-のアニオンを形成する酸に結合する上記アラルキル基としては、炭素数が7〜10、1〜15個のフッ素原子で置換されているものが好ましい。具体的にはペンタフロロフェニルメチル基、ペンタフロロフェニルエチル基、パーフロロベンジル基、パーフロロフェネチル基等を挙げることができる。
X-のアニオンを形成する酸に結合する上記アルコキシカルボニル基としては、炭素数が2〜13、1〜25個のフッ素原子で置換されているものが好ましい。具体的にはトリフロロメトキシカルボニル基、ペンタフロロエトキシカルボニル基、ペンタフロロフェノキシカルボニル基、パーフロロブトキシカルボニル基、パーフロロオクチルオキシカルボニル基等を挙げることができる。
【0097】
このようなアニオンの中で、最も好ましいX-はフッ素置換ベンゼンスルホン酸アニオンであり、中でもペンタフルオロベンゼンスルホン酸アニオンが特に好ましい。
また、上記含フッ素置換基を有するベンゼンスルホン酸、ナフタレンスルホン酸、又はアントラセンスルホン酸は、さらに直鎖状、分岐状あるいは環状アルコキシ基、アシル基、アシロキシ基、スルホニル基、スルホニルオキシ基、スルホニルアミノ基、アリール基、アラルキル基、アルコキシカルボニル基(これらの炭素数範囲は前記のものと同様)、ハロゲン(フッ素を除く)、水酸基、ニトロ基等で置換されてもよい。
以下に、これらの一般式(I)〜(III)で表される化合物の具体例を示すが、これに限定されるものではない。
【0098】
【化30】
【0099】
【化31】
【0100】
【化32】
【0101】
【化33】
【0102】
【化34】
【0103】
【化35】
【0104】
【化36】
【0105】
【化37】
【0106】
【化38】
【0107】
【化39】
【0108】
【化40】
【0109】
一般式(I)、一般式(II)の化合物は、次のような方法で合成できる。例えば、アリールマグネシウムブロミドなどのアリールグリニャール試薬とフェニルスルホキシドとを反応させ、得られたトリアリールスルホニウムハライドを対応するスルホン酸と塩交換する。別の方法もある。例えば、フェニルスルホキシドと対応する芳香族化合物をメタンスルホン酸/五酸化二リンあるいは塩化アルミなどの酸触媒を用いて縮合、塩交換する方法がある。また、ジアリールヨードニウム塩とジアリールスルフィドを酢酸銅などの触媒を用いて縮合、塩交換する方法などによって合成できる。上記のいずれの方法でも、フェニルスルホキシドは、置換基をベンゼン環に置換させていてもよく、そのような置換基がなくてもよい。
一般式(III)の化合物は過ヨウ素酸塩を用いて芳香族化合物を反応させることにより合成可能である。
【0110】
本発明で使用する(A)成分の含有量は、全ネガ型レジスト組成物の固形分に対し、0.1〜20重量%が適当であり、好ましくは0.5〜10重量%、更に好ましくは1〜7重量%である。
【0111】
本発明においては、上記一般式(I)〜一般式(III)で表わされる化合物以外に、あるいはこれらと共に、放射線の照射により分解してラジカル種を発生する他の化合物を用いることができる。
一般式(I)〜一般式(III)で表わされる化合物とともに放射線の照射により分解してラジカル種を発生する他の化合物を用いる場合には、上記一般式(I)〜一般式(III)で表わされる化合物と放射線の照射により分解してラジカル種を発生する他の化合物の比率は、モル比で100/0〜20/80、好ましくは90/10〜40/60、更に好ましくは80/20〜50/50である。
【0112】
(3)本発明(C)のラジカルにより重合可能な不飽和結合を有する化合物
本発明(A)の化合物から発生するラジカルにより重合し得る不飽和結合を有する化合物としては、重合性基を有する公知のモノマーが特に制限なく使用することができる。
そのようなモノマーとしては、具体的には、例えば、2−エチルヘキシルアクリレート、2−ヒドロキシエチルアクリレート、2−ヒドロキシプロピルアクリレート等の単官能アクリル酸エステル及びその誘導体あるいはこれらのアクリレートをメタクリレート、イタコネート、クロトネート、マレエート等に代えた化合物;
【0113】
ポリエチレングリコールジアクリレート、ペンタエリスリトールジアクリレート、ビスフェノールAジアクリレート、ヒドロキシピバリン酸ネオペンチルグリコールのε−カプロラクトン付加物のジアクリレート等の2官能アクリル酸エステル及びその誘導体あるいはこれらのアクリレートをメタクリレート、イタコネート、クロトネート、マレエート等に代えた化合物;
【0114】
あるいはトリメチロールプロパントリ(メタ)アクリレート、ジペンタエリスリトールペンタアクリレート、ジペンタエリスリトールヘキサアクリレート、ピロガロールトリアクリレート等の多官能アクリル酸エステル及びその誘導体あるいはこれらのアクリレートをメタクリレート、イタコネート、クロトネート、マレエート等に代えた化合物等を挙げることができる。また、適当な分子量のオリゴマーにアクリル酸又はメタアクリル酸を導入し、光重合性を付与した所謂プレポリマーと呼ばれるものも好適に使用できる。
【0115】
この他に、特開昭58−212994号、同61−6649号、同62−46688号、同62−48589号、同62−173295号、同62−187092号、同63−67189号、特開平1−244891号等に記載の化合物などを挙げることができ、更に「11290の化学商品」化学工業日報社,286〜294頁に記載の化合物、「UV・EB硬化ハンドブック(原料編)」高分子刊行会,11〜65頁に記載の化合物なども好適に用いることができる。
【0116】
なかでも、分子内に2個以上のアクリル基又はメタクリル基を有する化合物が本発明においては好ましく、更に分子量が10,000以下、より好ましくは5,000以下のものが望ましい。本発明においては、重合性化合物は、前記例示したものも含めて重合性基を有するモノマー、プレポリマーのなかから、目的に応じて1種あるいは相溶性、親和性に問題がなければ、2種以上を組合せて用いることができる。
尚、(A)成分がラジカルと同時に酸も発生する化合物の場合、本発明(C)のラジカルにより重合可能な不飽和結合を有する化合物の他に、酸により重合可能な不飽和結合を有する化合物を併用してもよい。
【0117】
不飽和基を有する化合物は、全レジスト組成物固形分中、2〜50重量%、好ましくは5〜40重量%、更に好ましくは10〜30重量%の添加量で用いられる。
【0118】
(4)本発明の組成物に使用されるその他の成分
本発明のネガ型レジスト組成物には必要に応じて、更に別のラジカル発生剤、有機塩基性化合物、染料、界面活性剤などを含有させることができる。
【0119】
(4)−1 染料
好適な染料としては油性染料及び塩基性染料がある。具体的にはオイルイエロー#101、オイルイエロー#103、オイルピンク#312、オイルグリーンBG、オイルブルーBOS,オイルブルー#603、オイルブラックBY、オイルブラックBS、オイルブラックT−505(以上オリエント化学工業株式会社製)、クリスタルバイオレット(CI42555)、メチルバイオレット(CI42535)、ローダミンB(CI45170B)、マラカイトグリーン(CI42000)、メチレンブルー(CI52015)等を挙げることができる。
【0120】
(4)−2 有機塩基性化合物
本発明で用いることのできる好ましい有機塩基性化合物とは、フェノールよりも塩基性の強い化合物である。中でも含窒素塩基性化合物が好ましい。
好ましい化学的環境として、下記式(A)〜(E)の構造を挙げることができる。
【0121】
【化41】
【0122】
ここで、R250 、R251 及びR252 は、同一でも異なってもよく、水素原子、炭素数1〜6個のアルキル基、炭素数1〜6個のアミノアルキル基、炭素数1〜6個のヒドロキシアルキル基又は炭素数6〜20個の置換もしくは非置換のアリール基を表し、ここで、R251とR252は、互いに結合して環を形成してもよい。R253 、R254 、R255 及びR256 は、同一でも異なってもよく、炭素数1〜6個のアルキル基を表す。
更に好ましい化合物は、一分子中に異なる化学的環境の窒素原子を2個以上有する含窒素塩基性化合物であり、特に好ましくは、置換もしくは未置換のアミノ基と窒素原子を含む環構造の両方を含む化合物もしくはアルキルアミノ基を有する化合物である。
【0123】
好ましい具体例としては、置換もしくは未置換のグアニジン、置換もしくは未置換のアミノピリジン、置換もしくは未置換のアミノアルキルピリジン、置換もしくは未置換のアミノピロリジン、置換もしくは未置換のインダゾール、イミダゾール、置換もしくは未置換のピラゾール、置換もしくは未置換のピラジン、置換もしくは未置換のピリミジン、置換もしくは未置換のプリン、置換もしくは未置換のイミダゾリン、置換もしくは未置換のピラゾリン、置換もしくは未置換のピペラジン、置換もしくは未置換のアミノモルフォリン、置換もしくは未置換のアミノアルキルモルフォリン等が挙げられる。好ましい置換基は、アミノ基、アミノアルキル基、アルキルアミノ基、アミノアリール基、アリールアミノ基、アルキル基、アルコキシ基、アシル基、アシロキシ基、アリール基、アリールオキシ基、ニトロ基、水酸基、シアノ基である。
【0124】
特に好ましい化合物として、グアニジン、1,1−ジメチルグアニジン、1,1,3,3,−テトラメチルグアニジン、イミダゾール、2−メチルイミダゾール、4−メチルイミダゾール、N−メチルイミダゾール、2−フェニルイミダゾール、4,5−ジフェニルイミダゾール、2,4,5−トリフェニルイミダゾール、2−アミノピリジン、3−アミノピリジン、4−アミノピリジン、2−ジメチルアミノピリジン、4−ジメチルアミノピリジン、2−ジエチルアミノピリジン、2−(アミノメチル)ピリジン、2−アミノ−3−メチルピリジン、2−アミノ−4−メチルピリジン、2−アミノ−5−メチルピリジン、2−アミノ−6−メチルピリジン、3−アミノエチルピリジン、4−アミノエチルピリジン、
【0125】
3−アミノピロリジン、ピペラジン、N−(2−アミノエチル)ピペラジン、N−(2−アミノエチル)ピペリジン、4−アミノ−2,2,6,6−テトラメチルピペリジン、4−ピペリジノピペリジン、2−イミノピペリジン、1−(2−アミノエチル)ピロリジン、ピラゾール、3−アミノ−5−メチルピラゾール、5−アミノ−3−メチル−1−p−トリルピラゾール、ピラジン、2−(アミノメチル)−5−メチルピラジン、ピリミジン、2,4−ジアミノピリミジン、4,6−ジヒドロキシピリミジン、2−ピラゾリン、3−ピラゾリン、N−アミノモルフォリン、N−(2−アミノエチル)モルフォリンなどが挙げられるがこれに限定されるものではない。
これらの含窒素塩基性化合物は、単独であるいは2種以上一緒に用いられる。
【0126】
ラジカル発生剤と有機塩基性化合物の組成物中の使用割合は、(ラジカル発生剤)/(有機塩基性化合物)(モル比)=2.5〜300であることが好ましい。該モル比が2.5未満では低感度となり、解像力が低下する場合があり、また、300を越えると露光後加熱処理までの経時でレジストパターンの太りが大きくなり、解像力も低下する場合がある。
(ラジカル発生剤)/(有機塩基性化合物)(モル比)は、好ましくは5.0〜200、更に好ましくは7.0〜150である。
【0127】
(4)−3 ラジカル発生剤
本発明のネガ型レジスト組成物には必要に応じ、(C)の重合性化合物の反応を促進させる為、ラジカル発生剤を併用することができる。
このようなラジカル発生剤としては、一般にラジカル重合による高分子合成反応に用いられる公知のラジカル重合開始剤を特に制限なく、使用することができ、2,2’−アゾビスイソブチロニトリル、2,2’−アゾビスプロピオニトリル等のアゾビスニトリル系化合物、過酸化ベンゾイル、過酸化ラウロイル、過酸化アセチル、過安息香酸−t−ブチル、α−クミルヒドロパーオキサイド、ジ−t−ブチルパーオキサイド、ジイソプロピルパーオキシジカーボネート、t−ブチルパーオキシイソプロピルカーボネート、過酸類、アルキルパーオキシカルバメート類、ニトロソアリールアシルアミン類等の有機過酸化物、
【0128】
過硫酸カリウム、過硫酸アンモニウム、過塩素酸カリウム等の無機過酸化物、ジアゾアミノベンゼン、p−ニトロベンゼンジアゾニウム、アゾビス置換アルカン類、ジアゾチオエーテル類、アリールアゾスルホン類等のアゾ又はジアゾ系化合物、ニトロソフェニル尿素、テトラメチルチウラムジスルフィド等のテトラアルキルチウラムジスルフィド類、ジベンゾイルジスルフィド等のジアリールジスルフィド類、ジアルキルキサントゲン酸ジスルフィド類、アリールスルフィン酸類、アリールアルキルスルホン類、1−アルカンスルフィン酸類等を挙げることができる。
【0129】
ラジカル発生剤のラジカル発生のための活性化エネルギーは30Kcal/モル以上であることが好ましく、そのようなものとしてアゾビスニトリル系化合物、有機過酸化物が挙げられる。中でも、常温で安定性に優れ、加熱時の分解速度が速く、分解時に無色となる化合物が好ましく、過酸化ベンゾイル、2,2’−アゾビスイソブチロニトリル等を挙げることができる。
上記ラジカル発生剤は単独で用いても2種以上併用しても良く、ラジカル重合層の全固形分に対し0.5〜30重量%程度、好ましくは2〜10重量%で用いる。
【0130】
(4)−4 溶剤類
本発明の組成物は、上記各成分を溶解する溶媒に溶かして支持体上に塗布する。ここで使用する溶媒としては、エチレンジクロライド、シクロヘキサノン、シクロペンタノン、2−ヘプタノン、γ−ブチロラクトン、メチルエチルケトン、エチレングリコールモノメチルエーテル、エチレングリコールモノエチルエーテル、2−メトキシエチルアセテート、エチレングリコールモノエチルエーテルアセテート、プロピレングリコールモノメチルエーテル、プロピレングリコールモノメチルエーテルアセテート、トルエン、酢酸エチル、乳酸メチル、乳酸エチル、メトキシプロピオン酸メチル、エトキシプロピオン酸エチル、ピルビン酸メチル、ピルビン酸エチル、ピルビン酸プロピル、N,N−ジメチルホルムアミド、ジメチルスルホキシド、N−メチルピロリドン、テトラヒドロフラン等が好ましく、これらの溶媒を単独あるいは混合して使用する。
【0131】
(5)−5 界面活性剤類
上記溶媒に界面活性剤を加えることもできる。具体的には、ポリオキシエチレンラウリルエーテル、ポリオキシエチレンステアリルエーテル、ポリオキシエチレンセチルエーテル、ポリオキシエチレンオレイルエーテル等のポリオキシエチレンアルキルエーテル類、ポリオキシエチレンオクチルフェノールエーテル、ポリオキシエチレンノニルフェノールエーテル等のポリオキシエチレンアルキルアリルエーテル類、ポリオキシエチレン・ポリオキシプロピレンブロックコポリマー類、ソルビタンモノラウレート、ソルビタンモノパルミテート、ソルビタンモノステアレート、ソルビタンモノオレエート、ソルビタントリオレエート、ソルビタントリステアレート等のソルビタン脂肪酸エステル類、ポリオキシエチレンソルビタンモノラウレート、ポリオキシエチレンソルビタンモノパルミテ−ト、
【0132】
ポリオキシエチレンソルビタンモノステアレート、ポリオキシエチレンソルビタントリオレエート、ポリオキシエチレンソルビタントリステアレート等のポリオキシエチレンソルビタン脂肪酸エステル類等のノニオン系界面活性剤、エフトップEF301,EF303,EF352(新秋田化成(株)製)、メガファックF171,F173 (大日本インキ(株)製)、フロラ−ドFC430,FC431(住友スリーエム(株)製)、アサヒガードAG710,サーフロンS−382,SC101,SC102,SC103,SC104,SC105,SC106(旭硝子(株)製)、トロイゾルS−366(トロイケミカル(株)製)等のフッ素系界面活性剤、オルガノシロキサンポリマーKP341(信越化学工業(株)製)やアクリル酸系もしくはメタクリル酸系(共)重合ポリフローNo.75,No.95(共栄社油脂化学工業(株)製)等を挙げることができる。
【0133】
これらの界面活性剤の配合量は、本発明の組成物中の固形分100重量部当たり、通常、2重量部以下、好ましくは1重量部以下である。
これらの界面活性剤は単独で添加してもよいし、また、いくつかの組み合わせで添加することもできる。
【0134】
精密集積回路素子の製造などにおいてレジスト膜上へのパターン形成工程は、基板(例:シリコン/二酸化シリコン皮覆、ガラス基板、ITO基板等の透明基板等)上に、本発明のネガ型フォトレジスト組成物を塗布し、次に電子線(75keV以上の加速電圧条件下)又はX線描画装置を用いて照射を行い、加熱、現像、リンス、乾燥することにより良好なレジストパターンを形成することができる。
【0135】
本発明のネガ型フォトレジスト組成物の現像液としては、水酸化ナトリウム、水酸化カリウム、炭酸ナトリウム、ケイ酸ナトリウム、メタケイ酸ナトリウム、アンモニア水等の無機アルカリ類、エチルアミン、n−プロピルアミン等の第一アミン類、ジエチルアミン、ジ−n−ブチルアミン等の第二アミン類、トリエチルアミン、メチルジエチルアミン等の第三アミン類、ジメチルエタノールアミン、トリエタノーアミン等のアルコ−ルアミン類、テトラメチルアンモニウムヒドロキシド、テトラエチルアンモニウムヒドロキシド、コリン等の第四級アンモニウム塩、ピロール、ピペリジン等の環状アミン類、等のアルカリ類の水溶液を使用することができる。更に、上記アルカリ類の水溶液にイソプロピルアルコール等のアルコール類、ノニオン系等の界面活性剤を適当量添加して使用することもできる。
これらの現像液の中で好ましくは第四アンモニウム塩、更に好ましくは、テトラメチルアンモニウムヒドロオキシド、コリンである。
【0136】
【実施例】
以下、本発明を実施例により更に詳細に説明するが、本発明の内容がこれにより限定されるものではない。
【0137】
1.構成素材の合成例
(1)アルカリ可溶性樹脂
合成例1(樹脂例(29)の合成)
4−アセトキシスチレン3.9g(0.024モル)、4−メトキシスチレン0.8g(0.006モル)を1−メトキシ−2−プロパノール30mlに溶解し、窒素気流及び撹拌下、70℃にて重合開始剤2,2’−アゾビス(2,4−ジメチルバレロニトリル)(和光純薬工業(株)製;商品名V−65)50mg、4−アセトキシスチレン9.1g(0.056モル)、4−メトキシスチレン1.9g(0.014モル)の1−メトキシ−2−プロパノール70ml溶液を2時間かけて滴下した。2時間後開始剤50mgを追加し、更に2時間反応を行った。その後90℃に昇温し撹拌を1時間続けた。反応液を放冷後、イオン交換水1Lに激しく撹拌しながら投入することにより、白色樹脂を析出させた。得られた樹脂を乾燥後、メタノール100mLに溶解し、25%テトラメチルアンモニウムヒドロキシドを加え、樹脂中のアセトキシ基を加水分解した後、塩酸水溶液にて中和して白色樹脂を析出させた。イオン交換水にて水洗、減圧下で乾燥後、本発明の樹脂(29)11.6gを得た。GPCにて分子量を測定したところ、重量平均(Mw:ポリスチレン換算)で9,200、分散度(Mw/Mn)で2.2であった。
【0138】
合成例2(樹脂例(39)の合成)
ポリ(4−ヒドロキシスチレン)12.0g(Mw=10,500、Mw/Mn=1.2)をアセトン100mlに溶解し、ピリジン2.0gを加え、無水酢酸1.3gを添加し、撹拌下50℃にて3時間反応させた。反応液をイオン交換水1Lに激しく撹拌しながら投入することにより、白色樹脂を析出させた。得られた樹脂を減圧下で乾燥後、本発明の樹脂(39)12.2gを得た。 GPCにて分子量を測定したところ、重量平均(Mw:ポリスチレン換算)で11,400、分散度(Mw/Mn)で1.2であった。またNMR測定にて組成比を算出したところ、モル比でx/y(4−ヒドロキシスチレン/4−アセトキシスチレン)=88/12であった。
【0139】
合成例3(樹脂例(91)の合成)
2−[(4’−ヒドロキシフェニル)カルボニルオキシ]エチルメタクリレート3.8g(0.015モル)、2−ヒドロキシエチルアクリレート1.0g(0.009モル)、アクリロニトリル0.3g(0.006モル)を1−メトキシ−2−プロパノール30mlに溶解し、窒素気流及び撹拌下、70℃にて重合開始剤2,2’−アゾビス(2,4−ジメチルバレロニトリル)(和光純薬工業(株)製;商品名V−65)50mg、2−[(4’−ヒドロキシフェニル)カルボニルオキシ]エチルメタクリレート8.8g(0.035モル)、2−ヒドロキシエチルアクリレート2.4g(0.021モル)、アクリロニトリル0.7g(0.014モル)の1−メトキシ−2−プロパノール70ml溶液を2時間かけて滴下した。2時間後開始剤50mgを追加し、更に2時間反応を行った。その後90℃に昇温し撹拌を1時間続けた。反応液を放冷後、イオン交換水1Lに激しく撹拌しながら投入することにより、白色樹脂を析出させた。得られた樹脂を減圧下で乾燥後、本発明の樹脂(91)15.8gを得た。GPCにて分子量を測定したところ、重量平均(Mw:ポリスチレン換算)で15,200、分散度(Mw/Mn)で2.2であった。
【0140】
合成例4(樹脂例(94)の合成)
ポリ(4−ヒドロキシスチレン)(日本曹達株式会社製、商品名VP−15000)12.1g(0.10モル)をTHF100mlに溶解し、メタクリル酸無水物3.7g(0.024モル)を添加した。更にピリジン2.4g(0.030モル)を添加して、攪拌下5時間加熱還流させた。反応液を放冷後、イオン交換水1L中に激しく攪拌しながら投入することにより、白色樹脂を析出させた。イオン交換水で水洗後、得られた樹脂を減圧下で乾燥させ、本発明の樹脂(2)13.1gを得た。NMRで不飽和基の含有率を測定したところ、ポリヒドロキシスチレンのOH基へのメタクリル基の導入量は18モル%であった。またGPCにて分子量を測定したところ、重量平均で16,700(分散度1.2;ポリスチレン標準)であった。
【0141】
合成例5(樹脂例(96)の合成)
ポリ(4−ヒドロキシスチレン)(日本曹達株式会社製、商品名VP−8000)12.1g(0.10モル)をN,N−ジメチルアセトアミド100mlに溶解し、これに2−イソシアナトエチル メタクリレート3.1g(0.020モル)を添加して、攪拌下90℃で7時間加熱した。反応液を放冷後、イオン交換水1L中に激しく攪拌しながら投入することにより、白色樹脂を析出させた。イオン交換水で水洗後、得られた樹脂を減圧下で乾燥させ、本発明の樹脂(4)14.4gを得た。NMRで不飽和基の含有率を測定したところ、ポリヒドロキシスチレンのOH基へのメタクリル基の導入量は16モル%であった。またGPCにて分子量を測定したところ、重量平均で9,100(分散度1.2;ポリスチレン標準)であった。
【0142】
合成例6(樹脂例(99)の合成)
ポリ(4−ヒドロキシスチレン)(日本曹達株式会社製、商品名VP−8000)12.1g(0.10モル)をTHF100mlに溶解し、4−スチレンスルホニルクロリド4.7g(0.023モル)を添加した。更にN,N−ジメチルアミノピリジン0.37g(0.003モル)/トリエチルアミン2.1g(0.020モル)のTHF20ml溶液を氷冷下、攪拌しながら滴下した。更に室温下、5時間攪拌した。反応液を濾過し、濾液をイオン交換水1L中に激しく攪拌しながら投入することにより、白色樹脂を析出させた。イオン交換水で水洗後、得られた樹脂を減圧下で乾燥させ、本発明の樹脂(7)15.0gを得た。NMRで不飽和基の含有率を測定したところ、ポリヒドロキシスチレンのOH基へのスチリル基の導入量は18モル%であった。またGPCにて分子量を測定したところ、重量平均で9,200(分散度1.2;ポリスチレン標準)であった。
【0143】
合成例7(樹脂例(100)の合成)
ポリ(4−ヒドロキシスチレン)(日本曹達株式会社製、商品名VP−8000)12.1g(0.10モル)をN,N−ジメチルアセトアミド100mlに溶解し、これにクロロメチルスチレン3.4g(0.022モル)を添加した。更にトリエチルアミン2.3g(0.022モル)のN,N−ジメチルアセトアミド20ml溶液を室温下、撹拌しながら滴下した。その後反応液を60℃にて5時間撹拌した。反応液を放冷後、イオン交換水1L中に激しく攪拌しながら投入することにより、白色樹脂を析出させた。イオン交換水で水洗後、得られた樹脂を減圧下で乾燥させ、本発明の樹脂(8)13.9gを得た。NMRで不飽和基の含有率を測定したところ、ポリヒドロキシスチレンのOH基へのスチリル基の導入量は17モル%であった。またGPCにて分子量を測定したところ、重量平均で9,300(分散度1.2;ポリスチレン標準)であった。
以下、同様にして本発明(B)の樹脂を合成した。
【0144】
(2)ラジカル発生剤
1)ペンタフロロベンゼンスルホン酸テトラメチルアンモニウム塩の合成
ペンタフロロベンゼンスルホニルクロリド25gを氷冷下メタノール100mlに溶解させ、これに25%テトラメチルアンモニウムヒドロキシド水溶液100gをゆっくり加えた。室温で3時間攪拌するとペンタフロロベンゼンスルホン酸テトラメチルアンモニウム塩の溶液が得られた。この溶液をスルホニウム塩、ヨードニウム塩との塩交換に用いた。
【0145】
2)トリフェニルスルホニウムペンタフロロベンゼンスルホネートの合成
ジフェニルスルホキシド50gをベンゼン800mlに溶解させ、これに塩化アルミニウム200gを加え、24時間還流した。反応液を氷2Lにゆっくりと注ぎ、これに濃塩酸400mlを加えて70℃で10分加熱した。この水溶液を酢酸エチル500mlで洗浄し、ろ過した後にヨウ化アンモニウム200gを水400mlに溶解したものを加えた。析出した粉体をろ取、水洗した後酢酸エチルで洗浄、乾燥するとトリフェニルスルホニウムヨージドが70g得られた。
トリフェニルスルホニウムヨージド30.5gをメタノール1000mlに溶解させ、この溶液に酸化銀19.1gを加え、室温で4時間攪拌した。溶液をろ過し、これに過剰量のペンタフロロベンゼンスルホン酸テトラメチルアンモニウム塩の溶液を加えた。反応液を濃縮し、これをジクロロメタン500mlに溶解し、この溶液を5%テトラメチルアンモニウムヒドロキシド水溶液、および水で洗浄した。有機相を無水硫酸ナトリウムで乾燥後、濃縮するとトリフェニルスルホニウムペンタフロロベンゼンスルホネート(I−1)が得られた。
【0146】
3)ジ(4−t−アミルフェニル)ヨードニウムペンタフロロベンゼンスルホネートの合成
t−アミルベンゼン60g、ヨウ素酸カリウム39.5g、無水酢酸81g、ジクロロメタン170mlを混合し、これに氷冷下濃硫酸66.8gをゆっくり滴下した。氷冷下2時間攪拌した後、室温で10時間攪拌した。反応液に氷冷下、水500mlを加え、これをジクロロメタンで抽出、有機相を炭酸水素ナトリウム、水で洗浄した後濃縮するとジ(4−t−アミルフェニル)ヨードニウム硫酸塩が得られた。この硫酸塩を、過剰量のペンタフロロベンゼンスルホン酸テトラメチルアンモニウム塩の溶液に加えた。この溶液に水500mlを加え、これをジクロロメタンで抽出、有機相を5%テトラメチルアンモニウムヒドロキシド水溶液、および水で洗浄した後濃縮するとジ(4−t−アミルフェニル)ヨードニウムペンタフロロベンゼンスルホネート(III-1)が得られた。
その他の化合物についても上記と同様の方法を用いて合成できる。
【0147】
2.実施例〔実施例、比較例〕
(1)レジストの塗設
上記の合成例から選んだ本発明を構成する化合物と比較用化合物を用いて、下記表1に示す組成のフォトレジスト組成物の溶液を調整した。
各試料溶液を0.1μmのフィルターで濾過したのち、スピンコーターを利用して、シリコンウェハー上に塗布し、110℃、90秒間真空吸着型のホットプレートで乾燥して、膜厚0.3μmのレジスト膜を得た。
【0148】
【表1】
【0149】
表1中、樹脂(62)の組成はx/y/z=80/13/7、樹脂(128)の組成はm/n/o=70/20/10、樹脂(139)の組成はm/n/o=75/15/10、その他の樹脂はx/y、又はm/n=85/15であり、重量平均分子量は何れも8,000〜16,000(分散度1.2〜2.4)の範囲であった。また、実施例(参考例)12でのPAG−1はラジカル発生剤として使用し、比較例1において重合性モノマーは使用せず、架橋剤として下記構造式で表される(CL−1)を0.18g使用した。
【0150】
【化42】
【0151】
【化43】
【0152】
【化44】
【0153】
重合性モノマーとしては、
RM−1:テトラエチレングリコールジアクリレート(日本化薬(株)製)
RM−2:トリメチロールプロパントリアクリレート(日本化薬(株)製)
RM−3:ジペンタエリスリトールヘキサアクリレート(日本化薬(株)製)
を表す。
【0154】
(2)レジストパターンの作成
このレジスト膜に電子線描画装置(加速電圧50KeV)を用いて照射を行った。照射後にそれぞれ110℃の真空吸着型ホットプレートで60秒間加熱を行い、2.38%テトラメチルアンモニウムハイドロオキサイド(TMAH)水溶液で60秒間浸漬し、30秒間水でリンスして乾燥した。得られたパターンの断面形状を走査型電子顕微鏡により観察した。
また、感度は、0.20μmライン(ライン:スペース=1:1)を解像する時の最小照射エネルギーを感度とし、その照射量における限界解像力(ラインとスペースが分離解像)を解像力とした。0.20μmライン(ライン:スペース=1:1)が解像しないものついては限界の解像力を解像力とし、その時の照射エネルギーを感度とした。
性能評価結果を表2に示した。
【0155】
【表2】
【0156】
表2の結果より、本発明のネガ型レジスト組成物は、重合性モノマーのない比較例に比べ、感度、解像度が大きく向上することが判る。
【0157】
上記実施例1、5、8、参考例12と、比較例1の組成を用い、上記と同様にして作成したレジスト膜に対し、100KeVの加速電圧の条件で、電子線描画装置を用いて照射を行った(実施例13〜15、参考例16、比較例3)。照射後に上記実施例と同様に加熱、現像、リンスを行い、得られたパターンを走査型電子線顕微鏡により観察した。上記実施例と同様に評価した結果を表3に示した。
【0158】
【表3】
【0159】
表3の結果より、本発明のネガ型レジスト組成物は、比較例の組成物に対し、高加速電圧での電子線照射においても、良好な感度及び解像度を示すことが判る。
【0160】
【発明の効果】
本発明の電子線及びX線用ネガ型レジスト組成物により、高加速電圧の条件においても、感度、解像度に優れ、矩形なプロファイルを有するネガ型レジスト組成物を提供できる。
Claims (8)
- (A)電子線又はX線の照射により、ラジカル種を発生する、下記一般式(I)〜(III)で表される化合物、
(B)水不溶でアルカリ水溶液に可溶な樹脂、
(C)ラジカルにより重合可能な不飽和結合を少なくとも1個有する化合物、
を含有することを特徴とする電子線又はX線用ネガ型レジスト組成物。
R1〜R37は、水素原子、アルキル基、アルコキシ基、ヒドロキシル基、ハロゲン原子、または、−S−R38で示すことができる基である。R38は、アルキル基、又はアリール基である。R1〜R15で示す基、R16〜R27で示す基、R28〜R37で示す基は、各々それらのうちの2つ以上が結合し、環を形成していてもよい。
X-は、アリールスルホン酸アニオンを表す。 - X-のアリールスルホン酸アニオンが、アルキル基、アルコキシ基、アシル基、アシロキシ基、スルホニル基、スルホニルオキシ基、スルホニルアミノ基、アリール基、アラルキル基、アルコキシカルボニル基、からなる群から選択された少なくとも1種の有機基、および/またはフッ素原子を有するアリールスルホン酸アニオンであり、該有機基がフッ素原子で置換された有機基である、請求項1に記載の電子線又はX線用ネガ型レジスト組成物。
- (B)成分の樹脂が、一般式(a1)で表される繰り返し単位を含有する樹脂であることを特徴とする請求項1または2に記載の電子線又はX線用ネガ型レジスト組成物。
R1は水素原子、ハロゲン原子、シアノ基、置換基を有していても良い、アルキル基又はハロアルキル基を表す。R2は水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アリール基、アラルキル基、あるいはアシル基を表す。
R3、R4は同じでも異なっていても良く、水素原子、ハロゲン原子、シアノ基、又は置換基を有していても良い、アルキル基、シクロアルキル基、アルケニル基、アラルキル基、もしくはアリール基を表す。
Aは単結合、置換基を有しても良い、アルキレン基、アルケニレン基、シクロアルキレン基、もしくはアリーレン基、又は−O−、−SO2−、−O−CO−R5−、−CO−O−R6−、−CO−N(R7)−R8−を表す。
R5、R6、R8は同じでも異なっていても良く、単結合、置換基を有しても良い、アルキレン基、アルケニレン基、シクロアルキレン基、もしくはアリーレン基の単独、又はこれらの基とエーテル構造、エステル構造、アミド構造、ウレタン構造もしくはウレイド構造の群より選択される少なくとも1種が一緒になって形成した2価の基を表す。
R7は同じでも異なっていても良く、水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アラルキル基、又はアリール基を表す。
lは1〜3の整数を表す。また複数のR2、又はR2とR3もしくはR4が結合して環を形成しても良い。 - (B)成分の樹脂が、ラジカルにより重合可能な不飽和結合を少なくとも1個有する樹脂であることを特徴とする請求項1〜3のいずれかに記載の電子線又はX線用ネガ型レジスト組成物。
- (B)成分の樹脂が、一般式(a2)の繰り返し単位を含有する樹脂であることを特徴とする請求項1〜4のいずれかに記載の電子線又はX線用ネガ型レジスト組成物。
R9は水素原子、ハロゲン原子、シアノ基、置換基を有していても良い、アルキル基又はハロアルキル基を表す。
R10〜R12は水素原子、一般式(b)、(c)、又は(d)の何れかの基、置換基を有していても良い、アルキル基、シクロアルキル基、アリール基、アラルキル基、あるいはアシル基を表す。
R13、R14は同じでも異なっていても良く、水素原子、ヒドロキシル基、ハロゲン原子、シアノ基、又は置換基を有していても良い、アルキル基、シクロアルキル基、アルケニル基、アラルキル基、もしくはアリール基を表す。
R21、R22は水素原子、ハロゲン原子、ヒドロキシ基、置換基を有していても良い、アルキル基、アルコキシ基、アシロキシ基を表す。
R23は水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アラルキル基、又はアリール基を表す。
A1は単結合、置換基を有しても良い、2価のアルキレン基、アルケニレン基、シクロアルキレン基、もしくはアリーレン基、又は−O−、−SO2−、−O−CO−R26−、−CO−O−R27−、−CO−N(R28)−R29−を表す。
R26、R27、R29は同じでも異なっていても良く、単結合、又はエーテル構造、エステル構造、アミド構造、ウレタン構造もしくはウレイド構造を有しても良い、また置換基を有しても良い、2価のアルキレン基、アルケニレン基、シクロアルキレン基、アリーレン基を表す。
R28は水素原子、置換基を有していても良い、アルキル基、シクロアルキル基、アラルキル基、又はアリール基を表す。
A2は単結合、−O−R27−、−N(R28)−R29−を表す。
A3は単結合、−SO2−もしくはアルキレン構造を有しても良い、また置換基を有しても良い、アリーレン基を表す。
A4は単結合、置換基を有しても良い、2価のアルキレン基、シクロアルキレン基、アリーレン基、−O−、−SO2−、−CO−、−CO−O−R21−を表す。
x、y、zは0又は1を表し、m、nは0又は1以上の整数を表す。
但し、一般式(a2)中、少なくとも一つは一般式(b)、(c)、もしくは(d)の基を有する。またR10〜R12のうちの二つ、又はR10〜R12の一つとR13もしくはR14が結合して環を形成しても良い。 - (A)成分の化合物が、スルホニウム、又はヨードニウムのスルホン酸塩化合物から選択されることを特徴とする請求項1〜5のいずれかに記載の電子線又はX線用ネガ型レジスト組成物。
- 75keV以上の加速電圧条件下で電子線照射することを特徴とする請求項1〜6のいずれかに記載の電子線又はX線用ネガ型レジスト組成物。
- 請求項1〜7のいずれかに記載の電子線又はX線用ネガ型レジスト組成物によりレジスト膜を形成し、当該レジスト膜に電子線又はX線を照射し、現像することを特徴とするパターン形成方法。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2000219253A JP4149122B2 (ja) | 2000-07-19 | 2000-07-19 | 電子線又はx線用ネガ型レジスト組成物 |
| TW090116739A TW567402B (en) | 2000-07-19 | 2001-07-09 | Negative resist composition for electron ray or X-ray |
| KR1020010043328A KR100775453B1 (ko) | 2000-07-19 | 2001-07-19 | 전자선 또는 엑스선용 네가티브 레지스트 조성물 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2000219253A JP4149122B2 (ja) | 2000-07-19 | 2000-07-19 | 電子線又はx線用ネガ型レジスト組成物 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2002040656A JP2002040656A (ja) | 2002-02-06 |
| JP2002040656A5 JP2002040656A5 (ja) | 2006-01-12 |
| JP4149122B2 true JP4149122B2 (ja) | 2008-09-10 |
Family
ID=18714064
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000219253A Expired - Fee Related JP4149122B2 (ja) | 2000-07-19 | 2000-07-19 | 電子線又はx線用ネガ型レジスト組成物 |
Country Status (3)
| Country | Link |
|---|---|
| JP (1) | JP4149122B2 (ja) |
| KR (1) | KR100775453B1 (ja) |
| TW (1) | TW567402B (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NO20031736D0 (no) * | 2003-04-15 | 2003-04-15 | Amersham Health As | Forbindelser |
| US9469941B2 (en) | 2011-07-01 | 2016-10-18 | Empire Technology Development Llc | Paraben derivatives for preserving cellulosic materials |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08240911A (ja) * | 1995-03-02 | 1996-09-17 | Japan Synthetic Rubber Co Ltd | 感放射線性樹脂組成物 |
| JPH08272099A (ja) * | 1995-03-31 | 1996-10-18 | Oki Electric Ind Co Ltd | 放射線感応性樹脂組成物およびこれを用いたパターン形成方法 |
| JP3633179B2 (ja) * | 1997-01-27 | 2005-03-30 | Jsr株式会社 | ポジ型フォトレジスト組成物 |
| JPH1149847A (ja) * | 1997-05-15 | 1999-02-23 | Hitachi Ltd | 感光性樹脂組成物とそれを用いた絶縁フィルム及び多層配線板 |
| JPH1115154A (ja) * | 1997-06-20 | 1999-01-22 | Chisso Corp | 感光性樹脂組成物及びこれを用いた表示素子 |
| TWI250379B (en) * | 1998-08-07 | 2006-03-01 | Az Electronic Materials Japan | Chemical amplified radiation-sensitive composition which contains onium salt and generator |
| JP2000147752A (ja) * | 1998-11-05 | 2000-05-26 | Fuji Photo Film Co Ltd | ネガ型レジスト組成物 |
| JP2000159828A (ja) * | 1998-11-30 | 2000-06-13 | Nippon Shokubai Co Ltd | 感光性樹脂組成物、電子線硬化性樹脂組成物、及びそれらの硬化物 |
-
2000
- 2000-07-19 JP JP2000219253A patent/JP4149122B2/ja not_active Expired - Fee Related
-
2001
- 2001-07-09 TW TW090116739A patent/TW567402B/zh not_active IP Right Cessation
- 2001-07-19 KR KR1020010043328A patent/KR100775453B1/ko not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| KR100775453B1 (ko) | 2007-11-12 |
| JP2002040656A (ja) | 2002-02-06 |
| KR20020008077A (ko) | 2002-01-29 |
| TW567402B (en) | 2003-12-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4857138B2 (ja) | レジスト組成物及びそれを用いたパターン形成方法 | |
| JP2002006491A (ja) | 電子線又はx線用ネガ型レジスト組成物 | |
| JP3790960B2 (ja) | ネガ型レジスト組成物 | |
| US6824948B1 (en) | Electron beam or X-ray negative-working resist composition | |
| JP3821570B2 (ja) | ネガ型レジスト組成物 | |
| JP4092083B2 (ja) | 電子線又はx線用ネガ型レジスト組成物 | |
| JP2002372783A (ja) | ネガ型レジスト組成物 | |
| JP2004062044A (ja) | 電子線、x線又はeuv用ネガ型レジスト組成物 | |
| JP4276773B2 (ja) | 電子線又はx線用ネガ型レジスト組成物 | |
| JP4208418B2 (ja) | 電子線又はx線用ネガ型レジスト組成物 | |
| JPH10312060A (ja) | ポジ型レジスト組成物 | |
| JP3755690B2 (ja) | ポジ型感光性組成物 | |
| JP4149122B2 (ja) | 電子線又はx線用ネガ型レジスト組成物 | |
| JP2006215271A (ja) | レジスト組成物及びそれを用いたパターン形成方法 | |
| JP2002049150A (ja) | 電子線又はx線用ネガ型レジスト組成物 | |
| JP2000089461A (ja) | ポジ型レジスト組成物 | |
| JPH11258802A (ja) | ネガ型レジスト組成物 | |
| JP2002014470A (ja) | 電子線又はx線用ネガ型レジスト組成物 | |
| JP2003057827A (ja) | ポジ型レジスト組成物 | |
| JP2004198724A (ja) | ネガ型レジスト組成物 | |
| JP2002049149A (ja) | 電子線又はx線用ネガ型レジスト組成物 | |
| JP2002333714A (ja) | レジスト組成物 | |
| JP2003207898A (ja) | ポジ型レジスト組成物 | |
| JP3841378B2 (ja) | ポジ型レジスト組成物 | |
| JP3731776B2 (ja) | ポジ型感光性組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20051117 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20051117 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20060324 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A712 Effective date: 20061124 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20071108 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20071115 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20071122 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20071226 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080116 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080307 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080402 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080512 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080604 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20080625 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110704 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4149122 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110704 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120704 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120704 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130704 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |