JP4100707B2 - 軸索再生を促進する単核貪食細胞の組成物及び使用方法 - Google Patents
軸索再生を促進する単核貪食細胞の組成物及び使用方法 Download PDFInfo
- Publication number
- JP4100707B2 JP4100707B2 JP51207797A JP51207797A JP4100707B2 JP 4100707 B2 JP4100707 B2 JP 4100707B2 JP 51207797 A JP51207797 A JP 51207797A JP 51207797 A JP51207797 A JP 51207797A JP 4100707 B2 JP4100707 B2 JP 4100707B2
- Authority
- JP
- Japan
- Prior art keywords
- cells
- nerve
- injury
- optic nerve
- monocytes
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 230000008929 regeneration Effects 0.000 title claims abstract description 58
- 238000011069 regeneration method Methods 0.000 title claims abstract description 58
- 210000002864 mononuclear phagocyte Anatomy 0.000 title claims abstract description 51
- 230000003376 axonal effect Effects 0.000 title claims abstract description 50
- 238000000034 method Methods 0.000 title claims abstract description 39
- 239000000203 mixture Substances 0.000 title abstract description 13
- 210000001616 monocyte Anatomy 0.000 claims abstract description 98
- 210000004027 cell Anatomy 0.000 claims abstract description 67
- 208000014674 injury Diseases 0.000 claims abstract description 59
- 230000006378 damage Effects 0.000 claims abstract description 52
- 208000027418 Wounds and injury Diseases 0.000 claims abstract description 46
- 210000003169 central nervous system Anatomy 0.000 claims abstract description 43
- 201000010099 disease Diseases 0.000 claims abstract description 23
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 23
- 241000124008 Mammalia Species 0.000 claims abstract description 8
- 210000001328 optic nerve Anatomy 0.000 claims description 67
- 210000003497 sciatic nerve Anatomy 0.000 claims description 56
- 239000002609 medium Substances 0.000 claims description 52
- 210000001539 phagocyte Anatomy 0.000 claims description 43
- 210000002540 macrophage Anatomy 0.000 claims description 26
- 230000001143 conditioned effect Effects 0.000 claims description 17
- 238000012258 culturing Methods 0.000 claims description 16
- 210000004443 dendritic cell Anatomy 0.000 claims description 13
- 239000008194 pharmaceutical composition Substances 0.000 claims description 12
- 230000008733 trauma Effects 0.000 claims description 11
- 238000000338 in vitro Methods 0.000 claims description 10
- 210000000578 peripheral nerve Anatomy 0.000 claims description 10
- 210000001185 bone marrow Anatomy 0.000 claims description 9
- 210000004556 brain Anatomy 0.000 claims description 9
- 239000003636 conditioned culture medium Substances 0.000 claims description 9
- 210000004369 blood Anatomy 0.000 claims description 8
- 239000008280 blood Substances 0.000 claims description 8
- 210000005259 peripheral blood Anatomy 0.000 claims description 8
- 239000011886 peripheral blood Substances 0.000 claims description 8
- 239000002243 precursor Substances 0.000 claims description 7
- 230000001737 promoting effect Effects 0.000 claims description 6
- 208000028389 Nerve injury Diseases 0.000 claims description 5
- 230000008764 nerve damage Effects 0.000 claims description 5
- 239000003937 drug carrier Substances 0.000 claims description 4
- 230000002708 enhancing effect Effects 0.000 claims description 4
- 210000004185 liver Anatomy 0.000 claims description 4
- 210000001165 lymph node Anatomy 0.000 claims description 4
- 208000010412 Glaucoma Diseases 0.000 claims description 3
- 208000016988 Hemorrhagic Stroke Diseases 0.000 claims description 3
- 208000032382 Ischaemic stroke Diseases 0.000 claims description 3
- 206010061323 Optic neuropathy Diseases 0.000 claims description 3
- 208000006011 Stroke Diseases 0.000 claims description 3
- 210000001132 alveolar macrophage Anatomy 0.000 claims description 3
- 208000020658 intracerebral hemorrhage Diseases 0.000 claims description 3
- 208000020911 optic nerve disease Diseases 0.000 claims description 3
- 210000003491 skin Anatomy 0.000 claims description 3
- 210000000278 spinal cord Anatomy 0.000 claims description 3
- 208000020431 spinal cord injury Diseases 0.000 claims description 3
- 210000000952 spleen Anatomy 0.000 claims description 3
- 208000030768 Optic nerve injury Diseases 0.000 claims description 2
- 230000007844 axonal damage Effects 0.000 claims description 2
- 210000002751 lymph Anatomy 0.000 claims description 2
- 210000004880 lymph fluid Anatomy 0.000 claims description 2
- 230000002093 peripheral effect Effects 0.000 claims 4
- 230000000472 traumatic effect Effects 0.000 claims 2
- 230000008736 traumatic injury Effects 0.000 claims 2
- 206010057249 Phagocytosis Diseases 0.000 claims 1
- 210000000601 blood cell Anatomy 0.000 claims 1
- 210000002798 bone marrow cell Anatomy 0.000 claims 1
- 230000008782 phagocytosis Effects 0.000 claims 1
- 210000004927 skin cell Anatomy 0.000 claims 1
- 230000004936 stimulating effect Effects 0.000 abstract description 32
- 210000005036 nerve Anatomy 0.000 abstract description 23
- 230000000735 allogeneic effect Effects 0.000 abstract description 19
- 210000004207 dermis Anatomy 0.000 abstract description 3
- 241000700159 Rattus Species 0.000 description 72
- 230000000242 pagocytic effect Effects 0.000 description 36
- 210000001519 tissue Anatomy 0.000 description 34
- 210000003994 retinal ganglion cell Anatomy 0.000 description 18
- 238000011282 treatment Methods 0.000 description 16
- 230000015572 biosynthetic process Effects 0.000 description 13
- 239000000835 fiber Substances 0.000 description 12
- 238000003556 assay Methods 0.000 description 11
- 210000003050 axon Anatomy 0.000 description 8
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical group P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 8
- 210000002569 neuron Anatomy 0.000 description 8
- 239000002953 phosphate buffered saline Substances 0.000 description 8
- 238000002360 preparation method Methods 0.000 description 8
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 7
- 241000699666 Mus <mouse, genus> Species 0.000 description 7
- 108010025020 Nerve Growth Factor Proteins 0.000 description 7
- 239000011324 bead Substances 0.000 description 7
- 238000001816 cooling Methods 0.000 description 7
- 238000000684 flow cytometry Methods 0.000 description 7
- 210000002592 gangliocyte Anatomy 0.000 description 7
- 238000002372 labelling Methods 0.000 description 7
- 230000003902 lesion Effects 0.000 description 7
- 102000004169 proteins and genes Human genes 0.000 description 7
- 108090000623 proteins and genes Proteins 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 239000012867 bioactive agent Substances 0.000 description 6
- 230000000975 bioactive effect Effects 0.000 description 6
- 239000002245 particle Substances 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 239000004809 Teflon Substances 0.000 description 5
- 229920006362 Teflon® Polymers 0.000 description 5
- 210000001428 peripheral nervous system Anatomy 0.000 description 5
- 230000004044 response Effects 0.000 description 5
- 102000004127 Cytokines Human genes 0.000 description 4
- 108090000695 Cytokines Proteins 0.000 description 4
- 102000015336 Nerve Growth Factor Human genes 0.000 description 4
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 4
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 4
- 239000000654 additive Substances 0.000 description 4
- 230000033228 biological regulation Effects 0.000 description 4
- 238000005138 cryopreservation Methods 0.000 description 4
- 239000000975 dye Substances 0.000 description 4
- 229940053128 nerve growth factor Drugs 0.000 description 4
- 238000005057 refrigeration Methods 0.000 description 4
- 210000001525 retina Anatomy 0.000 description 4
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 4
- 102000004219 Brain-derived neurotrophic factor Human genes 0.000 description 3
- 108090000715 Brain-derived neurotrophic factor Proteins 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 108010046938 Macrophage Colony-Stimulating Factor Proteins 0.000 description 3
- 102100028123 Macrophage colony-stimulating factor 1 Human genes 0.000 description 3
- 102000007072 Nerve Growth Factors Human genes 0.000 description 3
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 3
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- 229940077737 brain-derived neurotrophic factor Drugs 0.000 description 3
- 210000005252 bulbus oculi Anatomy 0.000 description 3
- 239000002577 cryoprotective agent Substances 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 230000007383 nerve stimulation Effects 0.000 description 3
- 239000003900 neurotrophic factor Substances 0.000 description 3
- 229910052757 nitrogen Inorganic materials 0.000 description 3
- 102000004196 processed proteins & peptides Human genes 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 238000011084 recovery Methods 0.000 description 3
- 238000012453 sprague-dawley rat model Methods 0.000 description 3
- 238000003860 storage Methods 0.000 description 3
- 238000010257 thawing Methods 0.000 description 3
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 2
- KMZHZAAOEWVPSE-UHFFFAOYSA-N 2,3-dihydroxypropyl acetate Chemical compound CC(=O)OCC(O)CO KMZHZAAOEWVPSE-UHFFFAOYSA-N 0.000 description 2
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- 229920002307 Dextran Polymers 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- 102100029268 Neurotrophin-3 Human genes 0.000 description 2
- 229930040373 Paraformaldehyde Natural products 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 2
- 230000002776 aggregation Effects 0.000 description 2
- 238000004220 aggregation Methods 0.000 description 2
- VREFGVBLTWBCJP-UHFFFAOYSA-N alprazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1 VREFGVBLTWBCJP-UHFFFAOYSA-N 0.000 description 2
- 210000001130 astrocyte Anatomy 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 208000015114 central nervous system disease Diseases 0.000 description 2
- 210000001951 dura mater Anatomy 0.000 description 2
- 210000003743 erythrocyte Anatomy 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 238000007710 freezing Methods 0.000 description 2
- 230000008014 freezing Effects 0.000 description 2
- 210000000020 growth cone Anatomy 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 239000002085 irritant Substances 0.000 description 2
- 231100000021 irritant Toxicity 0.000 description 2
- FZWBNHMXJMCXLU-BLAUPYHCSA-N isomaltotriose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O)O1 FZWBNHMXJMCXLU-BLAUPYHCSA-N 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 210000000274 microglia Anatomy 0.000 description 2
- 210000004248 oligodendroglia Anatomy 0.000 description 2
- 229920002866 paraformaldehyde Polymers 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 230000002285 radioactive effect Effects 0.000 description 2
- 230000001172 regenerating effect Effects 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 238000012216 screening Methods 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 210000005222 synovial tissue Anatomy 0.000 description 2
- 210000002435 tendon Anatomy 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- ZNQVEEAIQZEUHB-UHFFFAOYSA-N 2-ethoxyethanol Chemical compound CCOCCO ZNQVEEAIQZEUHB-UHFFFAOYSA-N 0.000 description 1
- 239000001763 2-hydroxyethyl(trimethyl)azanium Substances 0.000 description 1
- IJRKANNOPXMZSG-SSPAHAAFSA-N 2-hydroxypropane-1,2,3-tricarboxylic acid;(2r,3s,4r,5r)-2,3,4,5,6-pentahydroxyhexanal Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O.OC(=O)CC(O)(C(O)=O)CC(O)=O IJRKANNOPXMZSG-SSPAHAAFSA-N 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- GUBGYTABKSRVRQ-DCSYEGIMSA-N Beta-Lactose Chemical compound OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-DCSYEGIMSA-N 0.000 description 1
- 241000212384 Bifora Species 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 235000019743 Choline chloride Nutrition 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 102000016911 Deoxyribonucleases Human genes 0.000 description 1
- 108010053770 Deoxyribonucleases Proteins 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 206010018341 Gliosis Diseases 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 102000008100 Human Serum Albumin Human genes 0.000 description 1
- 108091006905 Human Serum Albumin Proteins 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 229920001612 Hydroxyethyl starch Polymers 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- NNJVILVZKWQKPM-UHFFFAOYSA-N Lidocaine Chemical compound CCN(CC)CC(=O)NC1=C(C)C=CC=C1C NNJVILVZKWQKPM-UHFFFAOYSA-N 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 108010083674 Myelin Proteins Proteins 0.000 description 1
- 102000006386 Myelin Proteins Human genes 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- 108090000189 Neuropeptides Proteins 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- SXEHKFHPFVVDIR-UHFFFAOYSA-N [4-(4-hydrazinylphenyl)phenyl]hydrazine Chemical compound C1=CC(NN)=CC=C1C1=CC=C(NN)C=C1 SXEHKFHPFVVDIR-UHFFFAOYSA-N 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 210000001715 carotid artery Anatomy 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- SGMZJAMFUVOLNK-UHFFFAOYSA-M choline chloride Chemical compound [Cl-].C[N+](C)(C)CCO SGMZJAMFUVOLNK-UHFFFAOYSA-M 0.000 description 1
- 229960003178 choline chloride Drugs 0.000 description 1
- 229910017052 cobalt Inorganic materials 0.000 description 1
- 239000010941 cobalt Substances 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 230000002338 cryopreservative effect Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 description 1
- 239000000834 fixative Substances 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- 238000002073 fluorescence micrograph Methods 0.000 description 1
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 238000005194 fractionation Methods 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 1
- 230000036571 hydration Effects 0.000 description 1
- 238000006703 hydration reaction Methods 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 229940050526 hydroxyethylstarch Drugs 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- CDAISMWEOUEBRE-GPIVLXJGSA-N inositol Chemical compound O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-GPIVLXJGSA-N 0.000 description 1
- 238000009413 insulation Methods 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 210000001865 kupffer cell Anatomy 0.000 description 1
- 210000001821 langerhans cell Anatomy 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229960004194 lidocaine Drugs 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 210000002418 meninge Anatomy 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 1
- 239000004005 microsphere Substances 0.000 description 1
- 239000003068 molecular probe Substances 0.000 description 1
- 210000005012 myelin Anatomy 0.000 description 1
- PPAYPDQCRKDOKR-UHFFFAOYSA-M n,n-didecyl-4-[2-(1-methylpyridin-1-ium-4-yl)ethenyl]aniline;iodide Chemical compound [I-].C1=CC(N(CCCCCCCCCC)CCCCCCCCCC)=CC=C1\C=C\C1=CC=[N+](C)C=C1 PPAYPDQCRKDOKR-UHFFFAOYSA-M 0.000 description 1
- 210000004126 nerve fiber Anatomy 0.000 description 1
- 210000004498 neuroglial cell Anatomy 0.000 description 1
- 230000002887 neurotoxic effect Effects 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 208000027232 peripheral nervous system disease Diseases 0.000 description 1
- 210000003024 peritoneal macrophage Anatomy 0.000 description 1
- 210000004303 peritoneum Anatomy 0.000 description 1
- 235000020030 perry Nutrition 0.000 description 1
- 210000003281 pleural cavity Anatomy 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 238000007388 punch biopsy Methods 0.000 description 1
- 238000011555 rabbit model Methods 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000002787 reinforcement Effects 0.000 description 1
- 230000008458 response to injury Effects 0.000 description 1
- 230000002207 retinal effect Effects 0.000 description 1
- 230000007441 retrograde transport Effects 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 210000004116 schwann cell Anatomy 0.000 description 1
- CDAISMWEOUEBRE-UHFFFAOYSA-N scyllo-inosotol Natural products OC1C(O)C(O)C(O)C(O)C1O CDAISMWEOUEBRE-UHFFFAOYSA-N 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 210000003594 spinal ganglia Anatomy 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
- 230000003313 weakening effect Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0645—Macrophages, e.g. Kuepfer cells in the liver; Monocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/10—Cellular immunotherapy characterised by the cell type used
- A61K40/17—Monocytes; Macrophages
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/20—Cellular immunotherapy characterised by the effect or the function of the cells
- A61K40/24—Antigen-presenting cells [APC]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/40—Cellular immunotherapy characterised by antigens that are targeted or presented by cells of the immune system
- A61K40/41—Vertebrate antigens
- A61K40/414—Nervous system antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/06—Antiglaucoma agents or miotics
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0618—Cells of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K40/00
- A61K2239/38—Indexing codes associated with cellular immunotherapy of group A61K40/00 characterised by the dose, timing or administration schedule
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/08—Coculture with; Conditioned medium produced by cells of the nervous system
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biomedical Technology (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Epidemiology (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Microbiology (AREA)
- Immunology (AREA)
- General Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Ophthalmology & Optometry (AREA)
- Hematology (AREA)
- Gastroenterology & Hepatology (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- External Artificial Organs (AREA)
- Thermotherapy And Cooling Therapy Devices (AREA)
- Secondary Cells (AREA)
Description
1. 発明の分野
本発明は、中枢神経系の損傷あるいは疾患を有する哺乳動物において軸索再生を促進するための単核貪食細胞を含む組成物、及び単核貪食細胞の使用方法、並びに軸索再生を促進する単核貪食細胞の治療的能力を増強する組成物及び方法に関する。本発明は特に、(a)刺激された、あるいは刺激されていない同種単核貪食細胞を含む医薬組成物、あるいは前記同種単核貪食細胞を損傷あるいは疾患を有する哺乳動物の中枢神経系の部位あるいはその近傍に投与して軸索再生を促進する方法、(b)単核貪食細胞を刺激してその軸索再生を促進する能力を増強するための組成物及び方法、及び(c)組織、細胞、タンパク質、ペプチド及びその他の生物活性物質を、軸索を再生するために単核貪食細胞を刺激する能力についてスクリーニングする方法に関する。
2. 発明の背景
軸索に損傷を受けると哺乳動物の中枢神経系(CNS)のニューロンの軸索を再生する能力は貧弱なものとなる。これに対し、哺乳動物末梢神経系(PNS)のニューロンは実質的により大きい軸索再生能力を有する。Schwartzら、1989, FASEB J. 3:2371-2378参照。
CNSとPNSとの間の軸索再生の相違はニューロンそのものではなく、ニューロンの細胞環境によるものであるとされている。ニューロンが損傷すると、PNSニューロンを取り囲むシュワン細胞が調節され、軸索再生を許容し、あるいはそれを促進するようになる。これに対し、CNSニューロンを取り囲む神経膠星状細胞、乏突起神経膠細胞、及びミクログリアはそのような調節を示さず、軸索再生を促進しないままであるか、それを阻害する。Schwartzら、1987, CRC Crit. Rev. Biochem. 22:89-110参照。
この調節の不存在は損傷後の炎症反応の違いと相関するものとされている。Perry及びBrown, 1992, Bioessays 14:401-406; Lotan及びSchwartz, 1994, FASEB J. 8:1026-1033参照。特に、CNSの損傷に応答する単核貪食細胞の蓄積はPNSにおける損傷に対する応答と比較して遅れ、限定されたものとなる。この限定されたCNS単核貪食細胞応答により、(1)報告されたところによれば軸索再生を阻害するミエリン断片の除去が非効率的なものとなり、そして(2)神経膠星状細胞及び乏突起神経膠細胞の調節を促進して軸索再生を支持するマクロファージ由来サイトカインの放出が最適なものに達しなくなる。
上記の観察により、マクロファージ応答を適切に調節すればCNS損傷の後の軸索再生を促進し得るという理論が想起された。Davidらはin vitro系において、正常ラット視神経のクリオスタット切片をラットCNSの病巣から得た単核貪食細胞と共培養すると、その視神経切片の胎児ニワトリ後根神経節細胞に対する接着性が増強されることを示した。Davidら、1990, Neuron 5:463-469。活性化された腹膜マクロファージからのコンディショニングされた培地も、このin vitroアッセイにおいて視神経切片の接着性を促進するのに有効であった。
しかし、CNS損傷のin vivoモデルから得られた結果によれば、CNS損傷に対してマクロファージ反応を増強する処置は再生を増強しないことが示されている。例えば、腫瘍壊死因子α(TNF-α)あるいはコロニー刺激因子-1(CSF-1)を局所投与すると実験的な視神経損傷に対するマクロファージの応答は増強される。しかし、TNF-αのみがin vitroでアッセイした場合の神経接着に対する損傷視神経の許容性を増加させ、CSF-1は増加させなかった。Lotanら、1984, Exp. Neurol. 126:284-290。一つの可能性のある説明として、「適切に刺激されたマクロファージのみが神経再生に影響し得る」ということが示唆されている。Schwartzら、1994, Progress Brain Res. 103:331-341, 338。
実際、本発明の教示とは相反して、単核貪食細胞はCNS損傷の後の損傷を悪化させ、回復を制限し得ると報告している他の研究者もいる。脳マクロファージは、サイトカインにより刺激された場合、神経毒活性を示す。Chamakら、1994, J. Neurosci. Res. 38:221-233。単核貪食細胞機能を薬剤により阻害すると、脊髄損傷のウサギモデルにおける回復が促進されることが報告されている。Giulian及びRobertson, 1990, Annals Neurol. 27:33-42。マクロファージ由来サイトカインがグリア細胞瘢痕の形成を促進し、これにより軸索再生が阻害されるという報告もある。Khan及びWigley, 1994, NeuroReport 5:1381-1385; Vickら、1992, J. Neurotrauma 9:S93-S103。
本発明者らの知る限りでは、CNSにおける軸索再生を促進するためにCNS中に単核貪食細胞を投与することは本発明以前に示唆されたことはない。
本出願の第2節(あるいはその他の節)における参考文献の引用や特定は、そのような文献はいずれも本発明の先行技術として利用できたものであることを認めるものと解されるべきものではない。
3. 発明の概要
本発明は、同種単核貪食細胞を使用して哺乳動物の中枢神経系における軸索の再生を促進するための方法及び組成物に関する。同種単核貪食細胞は損傷あるいは疾患部位またはその近傍においてCNSに投与される。
本発明の方法と組成物に有用な同種単核貪食細胞としては、限定するものではないが、同種の単球、マクロファージ、及び樹状細胞、及び自己由来の単球、マクロファージ、及び樹状細胞が挙げられる。
本発明はさらに、同種単核貪食細胞の軸索再生を促進する能力を増強するためにそれらを刺激するための方法及び組成物、及び刺激された同種単核貪食細胞を使用して哺乳動物の中枢神経系における軸索再生を促進するための方法及び組成物を提供する。単核貪食細胞は、適切な組織あるいは適切な細胞とともに培養するか、あるいは適切な組織あるいは適切な細胞でコンディショニングした培地中で単核貪食細胞を培養することにより刺激する。この目的に適した組織としては、限定するものではなが、神経セグメント、特に末梢神経のセグメント、真皮、滑膜組織、腱鞘、肝臓、及びその他の再生組織が挙げられる。あるいは、単核貪食細胞は、少なくとも一種の適切な生物活性物質を添加した培地中で培養することにより刺激する。この目的に適した生物活性物質としては、限定するものではないが、神経ペプチド、サイトカイン、例えばトランスフォーミング増殖因子-β(TGF-β)、及び神経栄養因子、例えば神経栄養因子3(NT-3)、神経成長因子(NGF)、及び脳由来神経栄養因子(BDNF)が挙げられる。生物学的に活性なタンパク質あるいはペプチドはその天然の形態あるいは組換体の形態で使用し得る。
さらに本発明は、単核貪食細胞を刺激してその軸索再生を促進する能力を増強させるのに適したその他の組織、細胞、及び生物活性物質を同定するためのアッセイを提供する。このアッセイによれば、まず単核貪食細胞を試験すべき組織あるいは細胞と共に培養するか、試験すべき組織あるいは細胞でコンディショニングした培地あるいは試験すべき生物活性物質を添加した培地中で単核貪食細胞を培養する。その後培養した単核貪食細胞の貪食細胞活性を測定する。増加した貪食細胞活性を有する単核貪食細胞が、増強された軸索再生を促進する能力を有するものである。
【図面の簡単な説明】
以下の発明の詳細な説明、本発明の特定の態様の実施例、及び添付の図面を参照することにより本発明をより完全に理解し得るであろう。添付の図面は以下の通りである。
図1は、蛍光染料の網膜神経節細胞(RGC)への逆行性輸送により検出された、ラットの横断面形成視神経における軸索再生を示す。実験の詳細についてはテキストの第6節を参照。横断面を形成したすぐ後に、細胞を含まない(MED);2.5 x 103〜1 x 105の非刺激(刺激されていない、NS)単球を含む;2.5 x 103〜1 x 105の視神経刺激(視神経で刺激された、OS)単球を含む;あるいは2.5 x 103〜1 x 105の坐骨神経刺激(坐骨神経で刺激された、SS)単球を含むDCCM-1培地の2μlを損傷の部位に適用した。白丸は個々の実験動物を示す。黒丸は標識されたRGCを示さなかった動物を示す(MED、NS及びOS処理群のそれぞれの番号7、7及び6)。水平な線は各処理群の中央値を示す。
図2には、横断面形成直後の損傷部位に適用した単球の数及び種類の関数として、横断面形成されたラットの視神経における軸索再生を示す。実験の詳細についてはテキストの第6節を参照。横断面形成の際に、視神経刺激単球(OS)あるいは坐骨神経刺激単球(SS)を2.5 x 103細胞;5 x 103細胞;104細胞;あるいは105細胞の合計用量で含むDCCM-1培地の2μlを損傷の部位に適用した。
図3(A, B)は、視神経横断面形成と、その後の(A)5 x 103坐骨神経刺激単球あるいは(B)対照培地の投与を受けたラットにおける網膜神経節細胞の逆行性標識化を示す代表的な顕微鏡写真である。実験の詳細についてはテキストの第6節を参照。
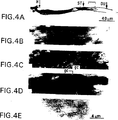
図4(A〜E)は、視神経横断面形成と、その後の坐骨神経刺激単球(A〜D)あるいは対照培地(E)の投与を受けたラットにおける視神経繊維の順行性標識化を表す代表的な顕微鏡写真を示す。実験の詳細についてはテキストの第6節を参照。図4Aは、HRPを適用した位置(H)、横断面形成(ST)の部位、及び周囲の硬膜(DU)を示す低倍率視野である。横断面形成部位に対して遠位の括弧を付した領域を図4B、4C及び4Dにおいてより高倍率で示す。これらにおいては、繊維の先端に成長円錐状構造(gc)が見られる。
図5は、坐骨神経と2〜17時間培養した単球を損傷の部位に適用した後のラットの横断面形成した視神経における軸索再生を示す。実験の詳細についてはテキストの第6節を参照。横断面形成の際に、5 x 103の非刺激単球(NS)あるいは坐骨神経と2時間(2h)、12時間(12h)もしくは17時間(17h)培養した5 x 103の単球を含むDCCM-1培地の2μlを損傷の部位に適用した。
図6は、マウス坐骨神経あるいはラット坐骨神経により刺激されたラット単球の損傷の部位における投与の後の横断面形成された視神経での軸索再生を示す。実験の詳細についてはテキストの第6節を参照。横断面形成の際に、マウス坐骨神経(マウス)あるいはラット坐骨神経(ラット)のいずれかと24時間培養した5 x 103の単球を含むDCCM-1培地の2μlを損傷の部位に適用した。
図7は、ラット坐骨神経と2時間培養したラット単球の貪食細胞活性を示す。実験の詳細についてはテキストの第6節を参照。2.5 x 105のラット単球を、1mlのDCCM-1培地のみ(対照)、あるいはラット坐骨神経の2セグメント(2SS)、もしくはラット坐骨神経の4セグメント(4SS)を含む1mlのDCCM-1培地中で培養した。2時間後に単球を蛍光ビーズと接触させ、フローサイトメトリーにより細胞に結合した蛍光を測定した。
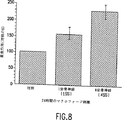
図8は、ラット坐骨神経と24時間培養されたラット単球の貪食細胞活性を示す。実験の詳細についてはテキストの第6節を参照。2.5 x 105のラット単球を、1mlのDCCM-1培地のみ(対照)、あるいはラット坐骨神経の1セグメント(1SS)、もしくはラット坐骨神経の4セグメント(4SS)を含む1mlのDCCM-1培地中で培養した。16〜24時間後に単球を蛍光ビーズと接触させ、フローサイトメトリーにより細胞に結合した蛍光を測定した。
図9は、ラット視神経と2時間培養したラット単球の貪食細胞活性を示す。実験の詳細についてはテキストの第6節を参照。2.5 x 105のラット単球を、1mlのDCCM-1培地のみ(対照)、あるいはラット視神経の4セグメント(4OS)を含む1mlのDCCM-1培地中で培養した。2時間後に単球を蛍光ビーズと接触させ、フローサイトメトリーにより細胞に結合した蛍光を測定した。
図10は、ラット視神経と24時間培養したラット単球の貪食細胞活性を示す。実験の詳細についてはテキストの第6節を参照。2.5 x 105のラット単球を、1mlのDCCM-1培地のみ(対照)、あるいはラット視神経の4セグメント(4OS)を含む1mlのDCCM-1培地中で培養した。24時間後に単球を蛍光ビーズと接触させ、フローサイトメトリーにより細胞に結合した蛍光を測定した。
図11は、ラット視神経によりコンディショニングされた培地の存在下でラット坐骨神経と一晩培養したラット単球の貪食細胞活性を示す。5 x 105のラット単球を、ラット坐骨神経の6セグメントを含み、さらに添加物を含まない(0)、あるいは視神経によりコンディショニングされた培地を0.1μg/ml(0.1)、1.0μg/ml(1)、あるいは10μg/ml(10)の総タンパク質濃度で添加した1mlのDCCM-1培地中で培養した。24時間後に単球を蛍光ビーズと接触させ、フローサイトメトリーにより細胞に結合した蛍光を測定した。
5. 発明の詳細な説明
5.1 単核貪食細胞
本発明は、同種単核貪食細胞を使用して中枢神経系(CNS)の損傷あるいは疾患の後の軸索の再生を促進するための方法及び組成物を提供する。同種単核貪食細胞はCNS損傷あるいは疾患の部位またはその近傍に導入される。
本明細書で使用する「単核貪食細胞」の用語は、限定するものではないが、中枢または末梢血から得られた単球、任意の組織あるいは体腔を含む任意の部位から得られたマクロファージ、骨髄あるいは血液から得られたマクロファージ前駆体を培養することによって得られたマクロファージ、脾臓、リンパ節、皮膚、及びリンパ液を含む任意の部位から得られた樹状細胞、骨髄あるいは血液から得られた樹状細胞前駆体を培養することによって得られた樹状細胞を包含することを意図するものである。
同種単核貪食細胞は、循環、あるいはそれらが存在する任意の組織から得ることができる。末梢血は容易に入手できる手近な同種単球の源であり、本発明の好ましい態様において源として使用する。特に好ましいのは、治療用調製物を投与することを意図した患者の末梢血から精製された自己由来の単球を使用することである。
その他の源からの同種単核貪食細胞は当分野において周知であり、限定するものではないが、腹膜あるいは胸膜腔等の漿膜腔から得られたマクロファージ、肺胞マクロファージ、クッパー細胞(肝臓内)、ミクログリア細胞(CNS内)等の種々の用語で知られているその他の組織に関連するマクロファージ等が挙げられる。同種単核貪食細胞はさらに樹状細胞を包含し、これもランゲルハンス細胞(皮膚内)、ベール細胞(リンパ液内)、相互鉗合細胞(リンパ節内)等の種々の用語により知られている。さらに単核貪食細胞は、骨髄あるいは血液から得られる、同種脳由来混合神経膠細胞あるいは同種前駆体細胞を培養しても得られる。
好ましい態様においては、投与すべき細胞集団から単核貪食細胞以外の細胞を取り除く。濃縮技術は当業者に周知であり、限定するものではないが、水ひ法、Percoll勾配のような適切な密度の物質を介した遠心分離(Colottaら、1983, J. Immunol. 132:936-944)、適切な表面への選択的接着とその後の低温あるいは低い二価カチオン濃度における除去(Rosen及びGordon, 1987, J. Exp. Med. 166:1685-1701)、機械的除去、あるいはリドカインの存在下における除去、及び血液(O'Dohertyら、1993, J. Exp. Med. 178:1067-1078)、骨髄(Inabaら,1992, J. Exp. Med. 176:1693-1702)及びリンパ様組織(Macatoniaら、J. Exp. Med. 169:1255-1264)から樹状細胞を単離するための方法等が挙げられる。特に好ましいのは、単核貪食細胞の実質的に精製された調製物である。
単核貪食細胞が得られたら、患者の必要に従い、任意の所望される時点で治療に使用することができる。単核貪食細胞は、所望の場合には投与の前に任意の適切な培養培地中で培養することができる。好ましくは、単核貪食細胞を、該細胞が限られた接着を示すか全く接着しない滅菌材料で形成された容器中で培養する。好ましい態様においては、単核貪食細胞は投与の前に滅菌テフロンバッグ中で培養する。
本明細書で使用する、「刺激された」単核貪食細胞は、軸索再生の促進の能力が増強された単核貪食細胞である。好ましくは、単核貪食細胞の軸索再生を促進する能力は非刺激単核貪食細胞と比較して少なくとも3倍に増強されているものであり、より好ましくは、単核貪食細胞の軸索再生を促進する能力は非刺激単核貪食細胞と比較して少なくとも15倍に増強されているものである。「刺激性の」組織、細胞及び生物活性物質は、単核貪食細胞と共に培養すると、単核貪食細胞の軸索再生を促進する能力を増強する組織、細胞及び生物活性物質である。
好ましい態様においては、刺激性の組織、細胞または少なくとも一種の刺激性の生物活性物質を培養に添加して単核貪食細胞の軸索再生を促進する能力を増強する。好ましくは神経、最も好ましくは坐骨神経のような末梢神経の一以上のセグメントを培養に加える。異種神経がこの目的に適しており、あるいはより好ましくは同種あるいは自己由来の神経である。所望により、ヒト神経は利用可能な任意のヒト組織、例えばヒト死体、あるいは外科標本(例えば切断肢)等から得ることができる。あるいは別の刺激性の組織あるいは細胞を培養に加えてもよい。真皮がこの目的に適しており、生体ドナーあるいは死体からパンチバイオプシー、手術的切除、あるいはその他の任意の適切な技術により得ることができる。滑膜組織、腱鞘及び肝臓もこの目的に適しており、その他の再生組織も同様である。その他の刺激性の組織及び細胞は以下に記載するアッセイにより同定することができる。所望であれば、刺激性の組織あるいは細胞は培養に添加する前に均質化してもよい。当業者には明らかであるが、刺激性の組織あるいは細胞のホモジネートは使用の前に凍結保存等により保存することができる。
別の態様においては、少なくとも一種の刺激性の生物活性物質を培養に添加して単核貪食細胞の軸索再生を促進する能力を増強する。神経栄養因子3(NT-3)、神経成長因子(NGF)、脳由来神経栄養因子、及びトランスフォーミング増殖因子-β(TGF-β)がこの目的に適しており、単独でも組み合わせてもよく、天然の形態あるいは組換体の形態とすることができる。別の刺激性の生物活性物質(別の刺激性のタンパク質及びペプチドを含む)は、後記するアッセイにより同定することができる。
好ましくは、単核貪食細胞を刺激性の組織、刺激性の細胞、刺激性の組織もしくは刺激性の細胞のホモジネート、あるいは少なくとも一種の刺激性の生物活性物質と共に24時間培養する。より短い培養時間、例えば約2時間でも有効であるが、より長い培養期間、例えば一週間以上も有効である。別の態様においては、刺激性の組織または細胞、好ましくは神経の一以上のセグメント、最も好ましくは坐骨神経のような末梢神経の一以上のセグメントを、単核貪食細胞の培養に適した任意の培地でインキュベートすることにより刺激性のコンディショニングされた培地を調製する。組織または細胞を除去した後、単核貪食細胞を前記刺激性のコンディショニングされた培地で培養してその軸索再生を促進する能力を増強する。組織または細胞を除去した後に、刺激性のコンディショニングされた培地を貯蔵し、後に単核貪食細胞を刺激するために所望されるように使用することができる。このような刺激性のコンディショニングされた培地は市販用のキットの形態とすることができる。好ましくは、刺激性のコンディショニングされた培地は、貯蔵の間、例えば液体あるいは凍結培地の形態で冷蔵により保存する。あるいは、刺激性のコンディショニングされた培地を凍結乾燥する。
当業者には明らかであるように、単核貪食細胞は、培養の前あるいは後に、例えば凍結保存により保存することができる。
使用できる凍結保存剤としては、限定するものではないが、ジメチルスルホキシド(DMSO)(Lovelock及びBishop, 1959, Nature 183:1394-1395; Ashwood-Smith, 1961, Nature 190:1204-1205)、グリセロール、ポリビニルピロリドン(Rinfret, 1960, Ann. N.Y. Acad. Sci. 85:576)、ポリエチレングリコール(Sloviter及びRavdin, 1962, Nature 196:548)、アルブミン、デキストラン、シュクロース、エチレングリコール、i-エリスリトール、D-リビト−ル、D-マンニトール(Roweら、1962, Fed. Proc. 21:157)、D-ソルビト−ル、i-イノシトール、D-ラクトース、塩化コリン(Benderら、1960, J. Appl. Physiol. 15:520)、アミノ酸(Phan The Tran及びBender、1960, Exp. Cell Res. 20:651)、メタノール、アセトアミド、グリセロールモノアセテート(Lovelock, 1954, Biochem. J. 56:265)、無機塩(Phan The Tran及びBender、1960, Proc. Soc. Exp. Biol. Med. 104:388: Phan The Tran及びBender、1961, Radiobiology, Proceedings of the Third Australian Conference on Radiobiology, Ilbery, P.L.T., ed., Butterworth, London, p.59)、及びヒドロキシエテルスターチ及びヒト血清アルブミンと組み合わせたDMSO(Zaroulis及びLeiderman, 1980, Cryobiology 17:311-317)等が挙げられる。
冷却速度を制御するのが重要である。凍結保護剤(Raspatzら、1968, Cryobiology 5(1):18-25)及び細胞種によって最適な冷却速度が異なる。骨髄幹細胞の生存及びその移植能に対する冷却速度の影響については例えば、Rowe及びRinfret, 1962, Blood 20:636; Rowe, 1966, Cryobiology 3(1):12-18; Lewisら、1967, Transfusion 7(1):17-32; 及びMazur, 1970, Science 168:939-949を参照。水が氷に変わる溶融相における熱は最小限にしなければならない。冷却操作は、例えばプログラム可能な冷凍装置、あるいはメタノール浴法等を使用して行うことができる。
プログラム可能な冷凍装置により最適な冷却速度を決定することができ、標準的で再現可能な冷却を容易に行える。CryomedあるいはPlanarのようなプログラム可能な速度制御冷凍機により、冷凍工程を所望の冷却速度曲線に合わせることができる。
完全に凍結した後、細胞を迅速に長期低温保存容器に移すことができる。一つの態様においては、例えば約-80℃あるいは約-20℃の温度を維持する冷凍機のような機械的冷凍機にサンプルを低温貯蔵することができる。好ましい態様においては、サンプルを液体窒素(-196℃)あるいはその蒸気中に低温貯蔵することができる。このような貯蔵は、高効率液体窒素冷凍機を利用できることにより非常に容易に行うことができ、これは非常に低度の減圧と内部に高度な絶縁体を有する大きなThermos容器のようなものであり、熱の漏洩と窒素の損失が絶対最小となるように維持されるものである。
造血幹細胞、特に骨髄あるいは末梢血からのものの取り扱い、低温保存及び長期貯蔵についての注意事項及び方法は概ね本発明の単核貪食細胞に適用できる。これらについての記載は例えば、以下の文献、Gorin, 1986, Clinics in Haematology 15(1):19-48; Bone-Marrow Conservation, Culture and Transplantation, Proceedings of a Panel, Moscow, July 22-26, 1968, International Atomic Energy Agency, Vienna, pp. 107-186に見られ、これらは引用により本明細書の一部とする。
生存能のある細胞の低温保存法のその他の方法、及びその改変法が利用及び想起され、使用することができる。そのようなものとして例えば冷却金属鏡法がある。Livesey及びLinner, 1987, Nature 327:255; Linnerら、1986, J. Histochem. Cytochem. 34(9):1123-1135参照。Senkenらによる米国特許第4,199,022号、Schwartzによる米国特許第3,753,357号、Fahyによる米国特許第4,559,298号も参照。
凍結細胞は好ましくは迅速に解凍し(例えば37〜41℃に維持した水浴中で)、解凍したら直ちに冷却する。解凍時の細胞の凝集を防ぐために細胞を処理することが望ましい場合がある。凝集を防ぐためには種々の方法を使用することができ、限定するものではないが、DNアーゼ(Spitzerら、1980, Cancer 45:3075-3085)、低分子量デキストラン及びクエン酸塩、ヒドロキシエチルスターチ(Stiffら、1983, Cryobiology 20:17-24)、あるいは酸クエン酸デキストロース(Zaroulis及びLeiderman, 1980, Cryobiology17:311-317)等を凍結の前及び/または後に添加する方法が挙げられる。
凍結保護剤がヒトに有害である場合は、解凍した単核貪食細胞を治療に使用する前にそれを除去しなければならない。凍結保護剤を除去する一つの方法は、ごく薄い(insignificant)濃度まで希釈することによるものである。
凍結された単核貪食細胞は、解凍し、回収した後、凍結していない単核貪食細胞について本明細書に記載したように軸索再生を促進するのに使用する。
5.2 使用方法
本発明によれば、単核貪食細胞を滅菌された医薬上許容される担体に懸濁し、ヒト患者等の哺乳動物のCNSに、損傷あるいは疾患の部位あるいはその近傍で投与する。
好ましい態様においては、医薬上許容される担体はPBSあるいは培養培地であるが、代替できる医薬上許容される担体は当業者に容易に理解されるであろう。
好ましい態様においては、単核貪食細胞をCNS損傷の直後に投与し、例えばガラスマイクロピペットによりCNSの損傷部位に導入する。但し本発明は、CNS損傷あるいは疾患の後の任意の時点における単核貪食細胞の投与を包含し、CNS損傷あるいは疾患の部位あるいはその近傍において任意の神経外科的な適当な方法により単核貪食細胞を導入することを包含する。
本発明の組成物及び方法は、軸索損傷を生じるかあるいはそれを伴うあらゆるCNSの損傷あるいは疾患を治療するのに有用である。上記損傷あるいは疾患は、脳、脊髄、あるいは視神経を含む任意の位置のCNSに存在し得る。そのような損傷あるいは疾患の一つの例は外傷であり、受傷直下損傷、反受傷直下損傷、貫通外傷、及び神経外科手術あるいはその他の処置の間に生じる外傷を含む。そのような損傷あるいは疾患の別の例は卒中であり、出血性卒中及び虚血性卒中が含まれる。前記のような損傷あるいは疾患のさらに別の例は視神経ニューロパシーあるいは緑内障を伴う視神経損傷である。CNS損傷あるいは疾患のさらに別の例は本明細書の記載から当業者に明らかであり、本発明に包含される。本発明の組成物及び方法は、患者がその他の中枢あるいは末梢神経系の疾患、例えば遺伝性、代謝性、毒性、栄養性、感染性あるいは自己免疫由来の神経疾患にも罹患しているかどうかにかかわらず、軸索損傷を生じるCNS損傷あるいは疾患を治療するのに有用である。
単核貪食細胞の適当な投与量は、治療する部位におけるCNS損傷あるいは疾患に罹患する神経繊維の数に比例する。好ましい態様においては、例えばラット視神経の完全な横断面のような約105の神経繊維が罹患する病巣を治療するための投与量は約2.5 x 103〜約105の単核貪食細胞の範囲であり、例えばヒト視神経の完全な横断面のような約106の神経繊維が罹患する病巣を治療するための投与量は約2.5 x 104から約106の単核貪食細胞の範囲である。より好ましくは、約105の神経繊維が罹患する病巣を治療するための投与量は約2.5 x 103〜約5 x 104の単核貪食細胞の範囲であり、約106の神経繊維が罹患する病巣を治療するための投与量は約2.5 x 104の単核貪食細胞から約5 x 105の単核貪食細胞の範囲である。特に好ましくは、約105の神経繊維が罹患する病巣を治療するための投与量は約5 x 103の単核貪食細胞であり、約106の神経繊維が罹患する病巣を治療するための投与量は約5 x 104の単核貪食細胞である。
5.3 刺激性の組織、細胞及び生物活性物質のアッセイ
本発明は、刺激性の組織及び細胞及び刺激性の生物活性物質を同定するためのアッセイを提供する。単核貪食細胞は、試験される組織あるいは細胞と共に、試験される組織あるいは細胞でコンディショニングされた培地で、あるいは試験される一種以上の生物活性物質を種々の濃度で添加した培地中で培養する。その後単核貪食細胞の貪食活性を測定する。上昇した貪食活性を有する単核貪食細胞が、軸索再生を促進する能力が増強されているものである。好ましくは、単核貪食細胞の貪食活性が少なくとも10%、より好ましくは少なくとも25%、さらに好ましくは少なくとも50%増加するものである。
一つの態様においては、単核貪食細胞を標識された粒子と接触させ、その後細胞に結合した標識の量を測定することにより貪食活性を測定する。この目的には広範な種類の粒子を使用することができ、限定するものではないが、ラテックスあるいはポリスチレンビーズ及び天然の細胞、例えば赤血球細胞、酵母、及び細菌等が挙げられる。任意に、例えば免疫グロブリンあるいは補体により粒子をオプソニン化することができる。粒子は任意の適当なマーカーで標識することができ、マーカーとしては、限定するものではないが、蛍光マーカー(例えばフルオレセインやローダミン)、放射性マーカー(例えばヨウ素、炭素あるいは水素の放射性同位体)、及び酵素等が挙げられる。あるいは、非標識粒子(例えば赤血球細胞あるいは酵母)を使用してアッセイを行うことができ、非標識粒子は任意の適当な方法、例えば染色してあるいは染色せずに、顕微鏡により検出する。好ましい態様においては、単核貪食細胞を最初に蛍光性ポリスチレンビーズに接触させ、その後細胞に結合した蛍光をフローサイトメトリーにより測定する。
本発明のアッセイは、単核貪食細胞を刺激するのに必要な培養期間を決定する手段ともなる。刺激性の組織あるいは細胞と共に、刺激性の組織あるいは細胞でコンディショニングされた培地中で、あるいは刺激性の一種以上の生物活性物質を添加した培地中で単核貪食細胞を培養する。その後単核貪食細胞の貪食活性を測定する。単核貪食細胞の貪食活性を少なくとも10%、より好ましくは少なくとも25%、さらに好ましくは少なくとも50%増加させるのに十分な培養期間が、単核貪食細胞の軸索再生を増強する能力を刺激するのに十分なものである。
以下の実施例は例示のためにのみ示すものであり、いかなる意味においても本発明の範囲を限定することを意図するものではない。
6. 実施例: 軸索再生を促進するための単球の使用
6.1 材料及び方法
6.1.1 単球の単離及び培養
末梢血は成体Sprague-Dawley(SPD)ラットから集めた。これまでに記載されたようにして(F. Colottaら、1984, J. Immunol. 132:936-944)、一段階Percoll勾配上での分画化により単球を単離した。単球濃縮フラクションをPercoll界面から回収し、PBSで一回洗浄して残存するPercollを除去し、DCCM-1培地(Beit Ha'emek Ltd., Kibbutz Beit Ha'emek, Israel)中に1 x 106細胞/mlで再懸濁した。細胞を以前に記載されたように(Andreesenら、1983, J. Immunolog. Meth. 56:295-304)、37℃でテフロンバッグ中で培養した。通常は1 x 107の細胞を含む10mlを各バッグに入れた。
6.1.2 単球の刺激
単離した単球を上記したようにテフロンバッグ中で2〜24時間培養することにより非刺激単球(NS)を調製した。単球をテフロンバッグ中でラット坐骨神経の少なくとも一つのセグメントと共に2〜24時間培養することにより坐骨神経刺激単球(SS)を調製した。単球をテフロンバッグ中でラット視神経の少なくとも一つのセグメントと共に2〜24時間培養することにより視神経刺激単球(OS)を調製した。実験6.2.1及び6.2.2において各神経セグメントは1.0〜1.5cmの長さとし、実験6.2.3から6.2.7においては0.5〜1.0cmの長さとした。特に記載した場合を除いて1神経セグメント対5 x 106培養単球の一定の比を使用した。
2〜24時間の培養の後、単球を1000 x gで3分間遠心分離し、リン酸緩衝食塩水(PBS)で一回洗浄し、1.25 x 106〜5 x 106細胞/mlでDCCM-1培地中に再懸濁した。単球は形態学的に、及びモノクローナル抗体ED1(Serotec, Oxford, England)を使用して記載されたようにして(Hirschbergら、1994, J, Neuroimmunol. 50:9-16)、免疫細胞化学的に調べたところ純度95%であった。
6.1.3 視神経横断面形成
麻酔を施した8〜9週齢の成体SPDラットに、記載されたようにして(Eitanら、1994, Science 264:1764-1768)、視神経の横断面形成を施術した。髄膜の小さな開孔を通して左の視神経を露出した。200μmの先端と平滑な鈍端を有する曲線ガラス解剖刃を、末梢血管を損傷しないように注意しながら神経を横切るように動かして眼球に対して2〜3mm遠位に完全な横断面を形成した。本明細書で使用する「遠位」の用語は、眼球から離れ、脳に近づくことを意味する。横断面形成のすぐ後に、培養した単球を含む培地の2μl、または培地のみの2μlを、25μm内孔を有する曲線ガラスマイクロピペットにより損傷の部位に導入した。横断面形成部位から約200μmに髄膜開孔を形成し、適用部位からの細胞の漏洩を防止した。
6.1.4 軸索再生のアッセイ
6.1.4.1 軸索の逆行的標識化
横断面形成の7〜8週後、親油性神経トレーサー染料、4-(4-(ジデシルアミノ)スチリル)-N-メチルピリジニウムイオダイド(4Di-10ASP)(Molecular Probes, Eugene, Oregon, USA)を、損傷の部位に対して2mm遠位で損傷を受けた視神経に適用した。前記染料の適用の1週間後に網膜を切除し、4%パラホルムアルデヒド溶液中の平坦化全組織標本とし、蛍光顕微鏡で観察して網膜全体の標識網膜神経節細胞(RGC)を検出し、その数をカウントした。損傷の部位を過ぎて染料を適用した部位まで再成長した軸索のみが染料を取り込み、それを網膜神経節細胞に逆行的に輸送した。
前以って横断面形成しなかったラット視神経に適用した場合、この方法により網膜あたり平均21,623RGCが標識される。横断面形成した視神経についての結果はこの標準、4Di-10ASP標識法の効率の対照に対するパーセンテージで表す。
6.1.4.2 軸索の順行性標識化
横断面形成の7〜8週間後、先に横断面形成した視神経の横断面形成部位に対して1mm近位に新たな切開を形成した。本明細書で使用する「近位」は眼球に向かい、脳から離れることを意味する。ホースラディッシュペルオキシダーゼ(HRP)(VI-A型、Sigma, Tel Aviv, Israel)を、PBS中のHRPの50%(W/V)溶液に浸した滅菌スワブにより切開部を通して導入した。HRPの適用の8〜12時間後、頸動脈からラットにPBSを灌流させ、その後固定剤としてPBS中の4%パラホルムアルデヒドを灌流させた。視神経を切り出し、長さ方向の50μmの凍結切片を取り、これまでに記載された(Lavieら、1992, Brain Res. 575:1-5)、ジアミノベンジジン及びコバルト強化を使用してHRP活性の可視化用に加工した。
6.1.5 貪食活性のアッセイ
ラットの単球をDCCM-1培地に懸濁し(1ml中2.5 x 105細胞)、さらになにも添加しないか、あるいは表示数(indicated number)のラット坐骨神経あるいは視神経セグメントとともに培養した。貪食活性をアッセイするために、蛍光非カルボキシル化マイクロスフィア(“FLUORESBRITE”TM, Polysciences, Warrington, Pennsylvania, USA,カタログ番号17152)の作業用溶液を、ストック溶液の一滴を10mlのDCCM-1培地に希釈することにより調製し、この作業用溶液をさらに1:100の希釈率で単球懸濁液に加えた。37℃で3時間おいた後、細胞をDCCM-1培地またはリン酸緩衝食塩水で一回洗浄し、フローサイトメトリー(FACS)により細胞に結合した蛍光を測定した。
6.2 結果
6.2.1 刺激単球及び非刺激単球による軸索再生の促進
ラットにおいて視神経横断面形成を行い、損傷時に、対照培地、あるいは2.5 x 103〜1 x 105非刺激(NS)単球、2.5 x 103〜1 x 105坐骨神経刺激(SS)単球、もしくは2.5 x 103〜1 x 105視神経刺激(OS)単球で処理した。
各処理群からのラットの標識された網膜神経節細胞(RGC)の数を、正常視神経における標識RGCのパーセンテージとして図1に示す。細胞の投与を受けていないラットはRGCの標識化を殆ど示さなかった。NS単球を投与されたラットはRGCの中程度の数の標識化を示したが、OS単球による処理はより多数のRGCの標識化を生じた。SS単球を投与されたラットにおいては、標識RGCの中央値はOS単球で処理されたラットにおけるものよりも5倍以上高く、NS単球で処理されたラットにおけるものよりも約15倍高かった。
6.2.2 種々の投与量の坐骨神経刺激単球あるいは視神経刺激単球による処理の後の軸索再生
投与した単球の投与量の関数としての再生を調べるために、ラットに視神経横断面形成を行い、損傷時に2.5 x 103、5 x 103、1 x 104あるいは1 x 105細胞の合計投与量で、OS単球またはSS単球で処理した。
各処理群の標識網膜RGCの平均値を、正常視神経における標識されたRGCのパーセンテージとして図2に示す。RGC標識化は5 x 103のSS単球での処理の後に最も高かった。SS単球のより多い投与量あるいはより少ない投与量でも軸索再生が促進されたが、有効性はより低かった。OS単球による処理でも同様に軸索再生が促進されたが、有効性はより低かった。OS及びSS単球のいずれによっても、ピーク効果は5 x 103単球投与時において見られ、より多い投与量あるいはより少ない投与量での軸索再生に対する有益な効果はより低いものであった。
SS単球あるいは対照培地による処理の後の網膜における標識RGCの代表的な蛍光顕微鏡像を図3に示す。対照培地による処理の後に標識RGCが見られないことは、横断面が完全であり、標識RGCは、横断面の部位を横切り、単に実験的な損傷から逃れた繊維ではない再生軸索を表すものであることを示している。
図4の顕微鏡写真は再成長が起こったことをさらに証明するものである。対照培地で処理された神経(E)においては、HRP適用の部位から遠位に標識繊維はみられなかった。SS単球で処理された神経(A〜D)においては、神経の近位部分から現れ、横断面の部位(ST)を越えて遠位に伸びている標識繊維が見られた。成長円錐(gc)に似た構造がこれらの標識繊維の先端に観察された。
6.2.3 ラット坐骨神経セグメントで種々の時間刺激した単球による処理の後の軸索再生
坐骨神経セグメントにより種々の時間刺激された後に軸索再生を刺激する単球の能力を調べるために、ラットに視神経損傷を与え、ラット坐骨神経セグメントと共に2時間(2h)、12時間(12h)または17時間(17h)培養した5 x 103の単球により損傷時に処理した。各処理群からの個々のラットにおける標識RGCの数を正常視神経における標識されたRGCのパーセンテージとして図5に示す。単球は、試験した各時間の間の坐骨神経セグメントとの培養の後に軸索再生を促進する能力を増加させた。
6.2.4 ラットまたはマウス坐骨神経セグメントにより刺激された単球での処理の後の軸索再生
ラット及びマウスから得た坐骨神経セグメントの、軸索再生を促進する単球の能力を刺激する能力を比較するため、ラットにおいて視神経横断面形成を行い、ラット坐骨神経の1〜8のセグメント(ラット)またはマウス坐骨神経の2〜16セグメント(マウス)のいずれかとともに24時間培養した5 x 103のラット単球で損傷時に処理した。各処理群からの個々のラットにおける標識RGCの数を正常視神経における標識されたRGCのパーセンテージとして図6に示す。ラット及びマウス坐骨神経はいずれも軸索再生を促進する単球の能力を刺激した。
6.2.5 ラット坐骨神経のセグメントとの培養の後の単球の貪食活性
2.5 x 105細胞のラット単球を1mlのDCCM-1培地中に懸濁し、さらに添加物を加えず(対照)、あるいはラット坐骨神経の1セグメント(1SS)、ラット坐骨神経の2セグメント(2SS)、もしくはラット坐骨神経の4セグメント(4SS)と共に2〜24時間培養した。
2時間の培養後の2SS及び4SS調製物の貪食活性を対照単球の貪食活性と比較して図7に示す。坐骨神経の2つのセグメントとの2時間の培養の後、単球の貪食活性は増加し、坐骨神経の4つのセグメントとの2時間の培養の後には、単球の貪食活性はさらに増加した。
24時間の培養後の1SS及び4SS調製物の貪食活性を対照単球の貪食活性と比較して図8に示す。坐骨神経の1つのセグメントとの24時間の培養の後、単球の貪食活性は増加し、坐骨神経の4つのセグメントとの24時間の培養の後には、貪食活性の増加はさらに大きくなった。4SS調製物では、2時間後よりも24時間後の方が貪食活性の増加はより大きかった。
6.2.6 ラット視神経のセグメントとの培養の後の単球の貪食活性
ラット単球の2.5 x 105細胞を1mlのDCCM-1培地中に懸濁し、さらに添加物を加えず(対照)、またはラット視神経の4セグメント(4OS)と共に2〜24時間培養した。2時間の培養後の4OS調製物の貪食活性を対照単球の貪食活性と比較して図9に示す。視神経の4つのセグメントとの2時間の培養の後、単球の貪食活性は減少した。
24時間の培養後の4OS調製物の貪食活性を対照単球の貪食活性と比較して図10に示す。視神経の4つのセグメントとの24時間の培養の後、単球の貪食活性は2時間後において見られたのと同様に減少した。
6.2.7 視神経によりコンディショニングされた培地の存在下で坐骨神経と培養した後の単球の貪食活性
1mlのDCCM-1培地中でラット視神経の10セグメントを2時間培養することにより視神経によりコンディショニングされた培地を調製した。新鮮なDCCM-1培地はタンパク質を含まないが、視神経によりコンディショニングされた培地はタンパク質を含んでいた。ラット単球の2.5 x 105細胞を1mlのDCCM-1培地に懸濁し、ラット坐骨神経の1〜6セグメントと共に、さらに添加物を含ませず(0)、あるいは10μg/ml(10)、1μg/ml(1)、もしくは0.1μg/ml(0.1)の総タンパク質濃度の視神経によりコンディショニングされた培地と共に24時間培養した。
図11は、視神経でコンディショニングした培地の存在下に坐骨神経と共に培養した単球の貪食活性を、視神経でコンディショニングした培地の不存在下に坐骨神経と共に培養した単球の貪食活性と比較して示す。視神経でコンディショニングした培地の添加により、坐骨神経との培養により生じる貪食活性の増強が弱められた。この弱化は0.1μg/mlの視神経でコンディショニングした培地を添加した調製物において最も顕著であった。
6.3 考察
これらの実施例は、CNS損傷の部位に投与された単球が軸索再生を促進したことを示している。試験した全ての単球は軸索再生の促進に有効であった。但し単球は、ラットあるいはマウスからの神経セグメント、特に坐骨神経のような末梢神経のセグメントと共に培養することにより刺激された(即ち、軸索再生を促進する能力の増強を示した)。この刺激は、試験した培養の全ての時間、即ち2〜24時間の後において明確であった。約105の神経繊維を含むラット視神経の全横断面の処理については、約5 x 103の単球を投与することにより最適な結果が得られた。但し、試験した全ての投与量において軸索再生について有益な結果が示された。
これらの実施例は、単球が坐骨神経の一つ以上のセグメントと共に培養した後に貪食活性を増加させることも示している。従って、貪食活性の測定により、軸索再生を促進するように単球を刺激する能力について組織及び細胞をスクリーニングする迅速で効率的な方法が得られる。
例示した態様は本発明の一つの形態を説明することを意図したものであり、本発明の範囲はこれに限定されることはない。実際、本明細書に示し、記載したものに加えて本発明の種々の改変はこれまでの記載と添付の図面から当業者に明らかであろう。そのような改変は添付の請求の範囲の範囲内にあることを意図するものである。
本明細書中で引用した全ての刊行物は引用によりその全体を本明細書の一部とする。
Claims (18)
- 軸索損傷を生じるかまたはそれを伴う中枢神経系(CNS)の損傷または疾患を患う哺乳動物のCNSにおける軸索再生を促進するための医薬組成物であって、
(a) 坐骨神経および視神経のセグメントを含む少なくとも一種の末梢神経のセグメント、または、坐骨神経および視神経のセグメントを含む少なくとも一種の末梢神経セグメントでコンディショニングされた培地と共に培養された哺乳動物の単核貪食細胞、および
(b) 医薬上許容される担体
を含む上記医薬組成物。 - 哺乳動物の単核貪食細胞が、ヒト末梢坐骨神経のセグメントと共に培養されたものである、請求項1に記載の医薬組成物。
- 哺乳動物の単核貪食細胞が、ヒト末梢視神経のセグメントと共に培養されたものである、請求項1に記載の医薬組成物。
- 哺乳動物の単核貪食細胞が、ヒト末梢坐骨神経のセグメントでコンディショニングされた培地と共に培養されたものである、請求項1に記載の医薬組成物。
- 哺乳動物の単核貪食細胞が、ヒト末梢視神経のセグメントでコンディショニングされた培地と共に培養されたものである、請求項1に記載の医薬組成物。
- 哺乳動物の単核貪食細胞が、自己由来のヒト単球、マクロファージまたは樹状細胞である、請求項1〜5のいずれかに記載の医薬組成物。
- 自己由来のヒト単球が、中枢または末梢血から得られたものである、請求項6に記載の医薬組成物。
- 自己由来のヒトマクロファージが、漿膜腔から得られたマクロファージ、肺胞マクロファージ、肝臓から得られたマクロファージ、または骨髄もしくは血液から得られたマクロファージ前駆体を培養することによって得られたマクロファージであり、樹状細胞が、脾臓、リンパ節、皮膚もしくはリンパ液から得られた樹状細胞、または骨髄もしくは血液から得られた樹状細胞前駆体を培養することによって得られた樹状細胞である、請求項6に記載の医薬組成物。
- CNSの損傷または疾患が、脳、脊髄もしくは視神経の損傷または疾患である、請求項1に記載の医薬組成物。
- CNSの損傷または疾患が、受傷直下損傷もしくは反受傷直下損傷、貫通外傷、および神経外科手術の間に生じる外傷などの外傷、出血性卒中および虚血性卒中などの卒中、脊髄損傷、または視神経ニューロパシーもしくは緑内障を伴う視神経損傷である、請求項9に記載の医薬組成物。
- 哺乳動物の単核貪食細胞のCNSにおける軸索再生を促進する能力をin vitroで増強するための方法であって、該哺乳動物の単核貪食細胞を、坐骨神経および視神経のセグメントを含む少なくとも一種の末梢神経のセグメント、または、坐骨神経および視神経のセグメントを含む少なくとも一種の末梢神経のセグメントでコンディショニングされた培地と共に培養することを含む、上記in vitro方法。
- 哺乳動物の単核貪食細胞が、坐骨神経および視神経のセグメントを含む少なくとも一種の末梢神経のセグメントと共に培養されたものである、請求項11に記載のin vitro方法。
- 哺乳動物の単核貪食細胞が、坐骨神経および視神経のセグメントを含む少なくとも一種の末梢神経のセグメントでコンディショニングされた培地と共に培養されたものである、請求項11に記載のin vitro方法。
- 哺乳動物の単核貪食細胞が、自己由来のヒト単球、マクロファージまたは樹状細胞である、請求項11〜13のいずれかに記載のin vitro方法。
- 自己由来のヒト単球が、中枢または末梢血から得られたものである、請求項14に記載のin vitro方法。
- 自己由来のマクロファージが、漿膜腔から得られたマクロファージ、肺胞マクロファージ、肝臓から得られたマクロファージ、または骨髄もしくは血液から得られたマクロファージ前駆体を培養することによって得られたマクロファージであり、樹状細胞が、脾臓、リンパ節、皮膚もしくはリンパ液から得られた樹状細胞、または骨髄もしくは血液から得られた樹状細胞前駆体を培養することによって得られた樹状細胞である、請求項15に記載のin vitro方法。
- 哺乳動物の単核貪食細胞が、軸索損傷を伴う脳、脊髄もしくは視神経の損傷または疾患においてCNSにおける軸索再生を促進する能力が増強される、請求項11〜16のいずれかに記載のin vitro方法。
- CNSの損傷または疾患が、受傷直下損傷もしくは反受傷直下損傷、貫通外傷、および神経外科手術の間に生じる外傷などの外傷、出血性卒中および虚血性卒中などの卒中、脊髄損傷、または視神経ニューロパシーもしくは緑内障を伴う視神経損傷である、請求項17に記載のin vitro方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US52884595A | 1995-09-15 | 1995-09-15 | |
| US08/695,351 US5800812A (en) | 1995-09-15 | 1996-08-09 | Methods of use of mononuclear phagocytes to promote axonal regeneration |
| US08/528,845 | 1996-08-09 | ||
| US08/695,351 | 1996-08-09 | ||
| PCT/US1996/014578 WO1997009885A1 (en) | 1995-09-15 | 1996-09-12 | Compositions and methods of use of mononuclear phagocytes to promote axonal regeneration |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JPH11513370A JPH11513370A (ja) | 1999-11-16 |
| JPH11513370A5 JPH11513370A5 (ja) | 2004-09-16 |
| JP4100707B2 true JP4100707B2 (ja) | 2008-06-11 |
Family
ID=27062850
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP51207797A Expired - Fee Related JP4100707B2 (ja) | 1995-09-15 | 1996-09-12 | 軸索再生を促進する単核貪食細胞の組成物及び使用方法 |
Country Status (13)
| Country | Link |
|---|---|
| US (2) | US5800812A (ja) |
| EP (1) | EP0952772B1 (ja) |
| JP (1) | JP4100707B2 (ja) |
| AT (1) | ATE290789T1 (ja) |
| AU (1) | AU714205B2 (ja) |
| CA (1) | CA2232262A1 (ja) |
| DE (1) | DE69634499T2 (ja) |
| DK (1) | DK0952772T3 (ja) |
| ES (1) | ES2241002T3 (ja) |
| IL (1) | IL123642A (ja) |
| NZ (1) | NZ319365A (ja) |
| PT (1) | PT952772E (ja) |
| WO (1) | WO1997009885A1 (ja) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6267955B1 (en) * | 1995-09-15 | 2001-07-31 | Yeda Research And Development Co. Ltd. | Mononuclear phagocytes and their use to promote axonal regeneration |
| US7795202B2 (en) * | 1997-08-04 | 2010-09-14 | Neurorepair, Inc. | Methods for treating a neurological disorder by peripheral administration of a transforming growth factor alpha (TGF-a) |
| US20010007657A1 (en) * | 1997-08-04 | 2001-07-12 | Reid James Steven | Compositions and methods for manipulating glial progenitor cells and treating neurological deficits |
| CA2298506A1 (en) * | 1997-08-04 | 1999-02-11 | The Regents Of The University Of California | Methods for treating neurological deficits |
| CA2328612A1 (en) * | 1998-05-19 | 1999-11-25 | Yeda Research And Development Co., Ltd. | Activated t cells, nervous system-specific antigens and their uses |
| SE9802264D0 (sv) | 1998-06-25 | 1998-06-25 | Neuronova Ab | A method of isolating cells |
| US6541247B1 (en) | 1998-06-25 | 2003-04-01 | Neuronova Ab | Method of isolating ependymal neural stem cells |
| IL125983A0 (en) * | 1998-08-30 | 1999-04-11 | Yeda Res & Dev | Pharmaceutical composition comprising factor xiiia |
| ATE422901T1 (de) * | 2001-03-12 | 2009-03-15 | Inst Of Gene And Brain Science | Granulocyte-macrophage colony-stimulating factor (gm-csf) als heilmittel für nervenschäden |
| AU2002353465B2 (en) * | 2001-11-21 | 2008-10-16 | Yeda Research And Development Co. Ltd. | Process for the manufacture of human mononuclear phagocytic leukocytes |
| WO2003105750A2 (en) * | 2002-06-14 | 2003-12-24 | Yeda Research And Development Co. Ltd | Antigen-presenting cells for neuroprotection and nerve regeneration |
| US20090010873A1 (en) * | 2004-11-29 | 2009-01-08 | Yeda Research And Development Co. Ltd. | Methods of Cell Therapy, Neurogenesis and Oligodendrogenesis |
| BRPI0919020B8 (pt) * | 2008-09-12 | 2021-05-25 | Cryopraxis Criobiologia Ltda | uso de células de linhagem monocitária enriquecidas para tratar isquemia e para tratar angina pectoris |
| EP2790712B1 (en) | 2011-12-14 | 2016-08-31 | Yeda Research and Development Co. Ltd. | Human monocyte sub-population for treatment of central nervous system injury |
| CN105377273A (zh) | 2013-05-22 | 2016-03-02 | 耶达研究与发展公司 | 用于治疗眼睛疾病或病症的人类单核细胞亚群 |
| EP3615568A4 (en) * | 2017-04-25 | 2021-01-20 | Purdue Research Foundation | TISSUE RESTORATION THREE-DIMENSIONAL (3D) ARTIFICIAL MUSCLE |
| EP4096635A4 (en) | 2020-01-27 | 2024-02-21 | GeniPhys, Inc. | BIOLOGICAL FILLER FOR TISSUE RESTORATION AND REGENERATION |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5157024A (en) * | 1977-10-16 | 1992-10-20 | Strategic Medical Research Corporation | Method of enhancing the activity of phagocytes including macrophages, modulating the cellular or humoral immune response, and reducing the adverse effects of stress in warm blooded animals |
| IL71440A0 (en) * | 1984-04-04 | 1984-07-31 | Univ Ramot | Composition for nerve regeneration |
| US5078996A (en) * | 1985-08-16 | 1992-01-07 | Immunex Corporation | Activation of macrophage tumoricidal activity by granulocyte-macrophage colony stimulating factor |
| US5082670A (en) * | 1988-12-15 | 1992-01-21 | The Regents Of The University Of California | Method of grafting genetically modified cells to treat defects, disease or damage or the central nervous system |
| IL97365A0 (en) * | 1991-02-27 | 1992-05-25 | Yeda Res & Dev | Pharmaceutical compositions comprising a lymphokine |
| IL91459A0 (en) * | 1989-08-28 | 1990-04-29 | Yeda Res & Dev | Oligodendrocyte inhibitory factor |
-
1996
- 1996-08-09 US US08/695,351 patent/US5800812A/en not_active Expired - Lifetime
- 1996-09-12 WO PCT/US1996/014578 patent/WO1997009885A1/en not_active Ceased
- 1996-09-12 AT AT96932991T patent/ATE290789T1/de not_active IP Right Cessation
- 1996-09-12 CA CA002232262A patent/CA2232262A1/en not_active Abandoned
- 1996-09-12 ES ES96932991T patent/ES2241002T3/es not_active Expired - Lifetime
- 1996-09-12 AU AU71572/96A patent/AU714205B2/en not_active Ceased
- 1996-09-12 PT PT96932991T patent/PT952772E/pt unknown
- 1996-09-12 DK DK96932991T patent/DK0952772T3/da active
- 1996-09-12 EP EP96932991A patent/EP0952772B1/en not_active Expired - Lifetime
- 1996-09-12 JP JP51207797A patent/JP4100707B2/ja not_active Expired - Fee Related
- 1996-09-12 IL IL12364296A patent/IL123642A/xx not_active IP Right Cessation
- 1996-09-12 NZ NZ319365A patent/NZ319365A/xx not_active IP Right Cessation
- 1996-09-12 DE DE69634499T patent/DE69634499T2/de not_active Expired - Lifetime
-
1997
- 1997-03-14 US US08/818,818 patent/US6117424A/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| AU714205B2 (en) | 1999-12-23 |
| ES2241002T3 (es) | 2005-10-16 |
| WO1997009885A1 (en) | 1997-03-20 |
| NZ319365A (en) | 1999-08-30 |
| DE69634499T2 (de) | 2006-01-05 |
| CA2232262A1 (en) | 1997-03-20 |
| EP0952772A4 (en) | 2002-01-02 |
| JPH11513370A (ja) | 1999-11-16 |
| ATE290789T1 (de) | 2005-04-15 |
| PT952772E (pt) | 2005-07-29 |
| EP0952772B1 (en) | 2005-03-16 |
| IL123642A (en) | 2005-08-31 |
| EP0952772A1 (en) | 1999-11-03 |
| DE69634499D1 (de) | 2005-04-21 |
| AU7157296A (en) | 1997-04-01 |
| US5800812A (en) | 1998-09-01 |
| DK0952772T3 (da) | 2005-07-18 |
| IL123642A0 (en) | 1998-10-30 |
| US6117424A (en) | 2000-09-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4100707B2 (ja) | 軸索再生を促進する単核貪食細胞の組成物及び使用方法 | |
| US7514261B2 (en) | Platelet-derived growth factor protection of cardiac myocardium | |
| DE69729455T2 (de) | Methode und zusammensetzungen zum erlangen reifer dendritischer zellen | |
| US6267955B1 (en) | Mononuclear phagocytes and their use to promote axonal regeneration | |
| Rochester et al. | Dendritic Cells from Rat Lung Are Potent Accessory Cells1-3 | |
| US20060159666A1 (en) | Method of potentiating inflammatory and immune modulation for cell and drug therapy | |
| JPH089967A (ja) | 癌細胞障害性tリンパ球の誘導培養方法 | |
| US20230210898A1 (en) | Microparticle-Assisted Treg Therapy for Treatment of Tissue Injury and Fibrosis | |
| WO2014089397A1 (en) | Compositions and methods of treating and preventing pulmonary fibrosis | |
| US7022321B2 (en) | Use of marrow-derived glial progenitor cells as gene delivery vehicles into the central nervous system | |
| MX2007010451A (es) | Metodo y composicion para la reparacion del tejido cardiaco. | |
| KR100569609B1 (ko) | 세포면역치료제의 제조를 위한 림프구 장기 보관 방법 | |
| EP4364747A1 (en) | Pharmaceutical composition containing irradiated hematopoietic stem cells | |
| CN121127252A (zh) | 从悬浮细胞的线粒体分离 | |
| WO1997045534A1 (de) | Verfahren zur kultivierung von zellen | |
| HK40077476A (en) | Optimally activated dendritic cells that induce an improved or increased anti-tumor immune response | |
| WO2025017354A1 (en) | Isolated autological double-derived cell population enriched with mesenchymal stem cells (mscs) and methods for obtaining and using the same | |
| AU2002332486A1 (en) | Platelet-derived growth factor protection of cardiac myocardium |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20070828 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20071120 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080122 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20080221 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20080318 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110328 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20080331 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130328 Year of fee payment: 5 |
|
| LAPS | Cancellation because of no payment of annual fees |