JP4030397B2 - 非水電解質二次電池 - Google Patents
非水電解質二次電池 Download PDFInfo
- Publication number
- JP4030397B2 JP4030397B2 JP2002275555A JP2002275555A JP4030397B2 JP 4030397 B2 JP4030397 B2 JP 4030397B2 JP 2002275555 A JP2002275555 A JP 2002275555A JP 2002275555 A JP2002275555 A JP 2002275555A JP 4030397 B2 JP4030397 B2 JP 4030397B2
- Authority
- JP
- Japan
- Prior art keywords
- secondary battery
- positive electrode
- electrolyte secondary
- nonaqueous electrolyte
- lithium
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 239000011255 nonaqueous electrolyte Substances 0.000 title claims description 26
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 claims description 20
- 229910001416 lithium ion Inorganic materials 0.000 claims description 20
- 239000010416 ion conductor Substances 0.000 claims description 17
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Inorganic materials [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 claims description 17
- 229910052744 lithium Inorganic materials 0.000 claims description 11
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 claims description 8
- 239000011149 active material Substances 0.000 claims description 8
- 229910052731 fluorine Inorganic materials 0.000 claims description 7
- 239000002033 PVDF binder Substances 0.000 claims description 6
- 229910003002 lithium salt Inorganic materials 0.000 claims description 6
- 159000000002 lithium salts Chemical class 0.000 claims description 6
- 229920002981 polyvinylidene fluoride Polymers 0.000 claims description 6
- 239000011737 fluorine Substances 0.000 claims description 5
- -1 fluorine may Chemical class 0.000 claims description 5
- 239000000463 material Substances 0.000 claims description 5
- 229920000642 polymer Polymers 0.000 claims description 5
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 claims description 4
- ZDQNWDNMNKSMHI-UHFFFAOYSA-N 1-[2-(2-prop-2-enoyloxypropoxy)propoxy]propan-2-yl prop-2-enoate Chemical compound C=CC(=O)OC(C)COC(C)COCC(C)OC(=O)C=C ZDQNWDNMNKSMHI-UHFFFAOYSA-N 0.000 claims description 3
- 229910013870 LiPF 6 Inorganic materials 0.000 claims description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 2
- 229910015015 LiAsF 6 Inorganic materials 0.000 claims description 2
- 229910013063 LiBF 4 Inorganic materials 0.000 claims description 2
- 229910012513 LiSbF 6 Inorganic materials 0.000 claims description 2
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 claims description 2
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 claims description 2
- 229910052732 germanium Inorganic materials 0.000 claims description 2
- GNPVGFCGXDBREM-UHFFFAOYSA-N germanium atom Chemical compound [Ge] GNPVGFCGXDBREM-UHFFFAOYSA-N 0.000 claims description 2
- 239000007773 negative electrode material Substances 0.000 claims description 2
- 229910052710 silicon Inorganic materials 0.000 claims description 2
- 239000010703 silicon Substances 0.000 claims description 2
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims 2
- 229910052799 carbon Inorganic materials 0.000 claims 1
- 229920003229 poly(methyl methacrylate) Polymers 0.000 claims 1
- 239000004926 polymethyl methacrylate Substances 0.000 claims 1
- 150000003839 salts Chemical group 0.000 claims 1
- 239000010949 copper Substances 0.000 description 22
- 229910016509 CuF 2 Inorganic materials 0.000 description 12
- 238000006243 chemical reaction Methods 0.000 description 9
- 238000007599 discharging Methods 0.000 description 6
- 238000004090 dissolution Methods 0.000 description 6
- 239000007774 positive electrode material Substances 0.000 description 6
- 239000000243 solution Substances 0.000 description 5
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 4
- 239000008151 electrolyte solution Substances 0.000 description 4
- GKZFQPGIDVGTLZ-UHFFFAOYSA-N 4-(trifluoromethyl)-1,3-dioxolan-2-one Chemical compound FC(F)(F)C1COC(=O)O1 GKZFQPGIDVGTLZ-UHFFFAOYSA-N 0.000 description 3
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 3
- 239000011248 coating agent Substances 0.000 description 3
- 238000000576 coating method Methods 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 150000005676 cyclic carbonates Chemical class 0.000 description 3
- 239000012046 mixed solvent Substances 0.000 description 3
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 2
- 229910021589 Copper(I) bromide Inorganic materials 0.000 description 2
- 229910021591 Copper(I) chloride Inorganic materials 0.000 description 2
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 2
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 2
- 150000005678 chain carbonates Chemical class 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- OXBLHERUFWYNTN-UHFFFAOYSA-M copper(I) chloride Chemical compound [Cu]Cl OXBLHERUFWYNTN-UHFFFAOYSA-M 0.000 description 2
- 239000003792 electrolyte Substances 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 229920000193 polymethacrylate Polymers 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 238000007086 side reaction Methods 0.000 description 2
- ZZXUZKXVROWEIF-UHFFFAOYSA-N 1,2-butylene carbonate Chemical compound CCC1COC(=O)O1 ZZXUZKXVROWEIF-UHFFFAOYSA-N 0.000 description 1
- LZDKZFUFMNSQCJ-UHFFFAOYSA-N 1,2-diethoxyethane Chemical compound CCOCCOCC LZDKZFUFMNSQCJ-UHFFFAOYSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000006230 acetylene black Substances 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 239000003575 carbonaceous material Substances 0.000 description 1
- 239000006258 conductive agent Substances 0.000 description 1
- 239000004020 conductor Substances 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 239000004210 ether based solvent Substances 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 238000005755 formation reaction Methods 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 229920002239 polyacrylonitrile Polymers 0.000 description 1
- 229920000570 polyether Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 238000005096 rolling process Methods 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 229910052718 tin Inorganic materials 0.000 description 1
- 238000001291 vacuum drying Methods 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Battery Electrode And Active Subsutance (AREA)
- Secondary Cells (AREA)
Description
【発明の属する技術分野】
本発明は、非水電解質二次電池に関するものである。
【0002】
【従来の技術】
CuF2は、高い容量密度が期待されるので、正極活物質としてリチウム二次電池の研究初期に検討された(非特許文献1〜4)。しかしながら、電解液への溶解性が高いこと、並びに充放電効率が悪いことから、CuF2を用いたリチウム二次電池は実用化されていない。
【0003】
【非特許文献1】
K.M.Abraham,J.Power.Sourcs,7(1981/82)
【非特許文献2】
D.P.Boden,H.R,Buhner and V.J.Spera,Final Rep.Contract DA28-043-AMC-c1394(E) September,1966;Rep.AD639709,Nat.Tech.Info.Ser.,Va.,U.S.A. 1976
【非特許文献3】
碇真一著,新しい電池(第2版3刷),東京電機大学出版局(1982)P.118
【非特許文献4】
吉沢四郎著,電池ハンドブック(第1版2刷),電気書院(1975)P.3-167〜3-168
【0004】
【発明が解決しようとする課題】
CuF2の充放電機構において、放電時には以下の反応が生じ、CuとLiFが生成する。
【0005】
CuF2+2Li++2e-→Cu+2LiF
また、充電時には、以下の反応が生じ、CuF2に戻る。
Cu+2LiF→CuF2+2Li++2e-
しかしながら、実際には、充電時に、CuF2の生成反応と同時に副反応としてCuの溶解反応(Cu→Cu2++2e-)が生じる。この副反応は、充放電効率を低下させる原因となっている。従って、Cuの溶解反応を抑制することができれば充放電効率を向上させることができる。
【0006】
本発明の目的は、正極からのCuの溶解反応を抑制することができ、充放電効率を向上させることができる非水電解質二次電池を提供することにある。
【0007】
【課題を解決するための手段】
本発明は、Cuを活物質として含む正極と、非水電解質と、リチウムを吸蔵・放出する材料を含む負極とを備え、LiFが、正極、非水電解質、及び負極の少なくともいずれかに含まれている非水電解質二次電池であり、正極または正極の活物質の表面がリチウムイオン伝導体で被覆されていることを特徴としている。
【0008】
正極の表面または正極の活物質の表面を、リチウムイオン伝導体で被覆することにより、充電の際に銅の溶解によって生成するCuイオンは、リチウムイオン伝導膜を通過できず、正極表面に残る。このため、電極表面のCuイオン濃度が増加し、Cuの溶解反応を抑制することができる。従って、本発明によれば、充放電効率を向上させることができる。
【0009】
本発明において、LiFは、正極、非水電解質、及び負極の少なくともいずれかに含まれる。非水電解質中に溶解したLiFが、充放電反応に関与するので、非水電解質中にLiFが含まれていることが好ましい。しかしながら、非水電解質には多量のLiFを溶解させることができないので、LiFは正極及び/または負極に含ませることができる。一般には、正極にLiFを含ませることが好ましい。
【0010】
LiFは、放電生成物の形態であり、充電によりLiFをLiとFに分け、Liを放出するとともに、Fを貯蔵する必要がある。放電の際には、LiとFからLiFを生成させる必要がある。
【0011】
本発明において正極活物質として含まれるCu及びCu化合物は、充電の際に生じたFを貯蔵するものである。Cuを活物質として用いた場合には、CuF2の形態でFを貯蔵する。
【0012】
また、Cu化合物を活物質として用いてFを貯蔵することができる。Cu化合物としては、Cu2O、CuS、Cu2S、CuCl、CuCl2、CuBr、CuBr2、及びCuIから選ばれる少なくとも1種が挙げられる。
【0013】
また、本発明に従う他の局面においては、CuF2を正極活物質として含んでもよい。
すなわち、本発明の他の局面に従う非水電解質二次電池は、CuF2を活物質として含む正極と、非水電解質と、リチウムを吸蔵・放出する材料を含む負極とを備え、正極または正極活物質の表面がリチウムイオン伝導体で被覆されていることを特徴としている。
【0014】
本発明におけるリチウムイオン伝導体としては、リチウムイオンを通過させることができ、それ自体が電解液に溶解しないものであれば特に限定されない。このようなものとして、ポリフッ化ビニリデン、ポリメタクリレート、トリプロピレングリコールジアクリレートの重合体、ポリエチレンなどのポリオレフィン系誘導体重合物、ポリアクリロニトリルなどのビニル系重合体、ポリエチレンオキシドのようなポリエーテルなどが挙げられる。これらの中でも特に、ポリフッ化ビニリデン、ポリメタクリレート、及びトリプロピレングリコールジアクリレートの重合体が好ましく用いられる。
【0015】
正極の表面をリチウムイオン伝導体で被覆する場合、リチウムイオン伝導体の被膜の厚みは特に限定されるものではないが、1μm以上の厚みであることが好ましく、さらに好ましくは1μm〜100μmである。
【0016】
正極活物質の表面をリチウムイオン伝導体で被覆する場合には、正極活物質100重量部に対し、1重量部以上のリチウムイオン伝導体を被覆することが好ましく、さらに好ましくは1〜100重量部のリチウムイオン伝導体で被覆する。
【0017】
本発明において用いる非水電解質の溶媒としては、非水電解質二次電池に一般に用いられている溶媒を用いることができる。例えば、エチレンカーボネート、プロピレンカーボネート、ブチレンカーボネートなどの環状カーボネートと、ジメチルカーボネート、メチルエチルカーボネート、ジエチルカーボネートなどの鎖状カーボネートとの混合溶媒が例示される。また、上記環状カーボネートと1,2−ジメトキシエタン、1,2−ジエトキシエタンなどのエーテル系溶媒との混合溶媒も例示される。
【0018】
また、本発明者らは、トリフルオロプロピレンカーボネート(TFPC)のようなフッ素化炭酸エステル及びCF3CH2O−CO−OCH2CF3のようなフッ素化炭酸エステル等のフッ素化された有機溶媒が、CuF2を溶解しにくいことを見出している。従って、これらの有機溶媒を用いてもよい。
【0019】
TFPCは、環状炭酸エステルであるプロピレンカーボネート(PC)をフッ素化したものであるが、同じ炭酸エステルであるエチレンカーボネート(EC)をフッ素化したものや、鎖状の炭酸エステルをフッ素化したもの、さらにはγ−ブチロラクトン(γBL)などのエステルやTHFなどのエーテルをフッ素化したものも、CuF2を溶解しない溶媒として使用できる可能性がある。
【0020】
本発明において、非水電解質には、フッ素を含むリチウム塩が溶質として含有されていることが好ましい。フッ素を含むリチウム塩としては、LiPF6、LiBF4、LiAsF6、LiSbF6、LiF・(C6F5)3B、及びLiCl・(C6F5)3Bなどのルイス酸塩を挙げることができる。これらのフッ素を含むリチウム塩が電解質中に含有されていると、これらが媒介となって、CuとLiFとの反応が進行するものと思われる。
【0021】
本発明における負極材料は、リチウムを吸蔵・放出し得る材料であれば特に限定されるものではないが、炭素材料や、ケイ素、ゲルマニウム及び錫などのリチウムと合金化し得る材料が好ましく用いられる。
【0022】
【発明の実施の形態】
以下、実施例により本発明を説明するが、本発明は以下の実施例に限定されるものではなく、本発明を逸脱しない範囲において適宜変更して実施することが可能なものである。
【0023】
〔正極の作製〕
Cu粉末が20重量%、LiF粉末が20重量%、導電剤としてのアセチレンブラックが40重量%、結着剤としてのポリフッ化ビニリデンが20重量%となるように混合し、この混合物をN−メチル−2−ピロリドン(NMP)に添加してスラリーを調製し、これをアルミニウム箔上に塗布した。その後、110℃で真空乾燥し、圧延した後、2cm×2cmのサイズに切り出した。なお、塗布量は、2mg/cm2となるようにした。
【0024】
次に、ポリフッ化ビニリデンを10重量%溶解したNMP溶液を、正極活物質層の上に塗布した後、110℃で真空乾燥した。塗布量は、乾燥後の厚みが10μmとなるように塗布した。これにより、リチウムイオン伝導体で被覆した正極を得た。
比較として、リチウムイオン伝導体で被覆しない正極を作製した。
【0025】
〔試験セルの作製〕
得られた正極を用いて、図2に示すような構造の試験セルを作製した。図2に示すように、容器5内には電解液が入れられており、この電解液中に正極1、負極2、及び参照極3が挿入されている。正極1と負極2の間にはセパレータ4が設けられている。負極2及び参照極3としてはリチウム金属を用いた。セパレータ4としては、ポリプロピレンを用いた。電解液としては、エチレンカーボネートとジエチルカーボネートの体積比1:1の混合溶媒に、1モル/リットルの濃度のLiPF6と、500mg/リットルの濃度のLiFを溶解させたものを用いた。
【0026】
〔充放電試験〕
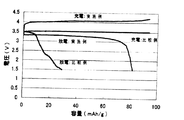
上記の実施例及び比較例の試験セルについて、充放電試験を行った。充電は、一定電流0.1mAで3時間行い、放電は一定電流0.1mAで1.5V(vs.Li/Li+)まで行った。試験結果を図1に示す。図1は、充放電特性を示しており、横軸は充放電容量であり、縦軸は電圧である。
【0027】
図1に示すように、リチウムイオン伝導体で被覆していない比較例の電極では、3時間充電を行った後、放電を行うと、3.4V(vs.Li/Li+)付近でプラトーが認められた。その後、電圧は急激に減少し、充放電効率は30%であった。これに対し、リチウムイオン伝導体で被覆した実施例の電極においては、3.3V(vs.Li/Li+)において放電のプラトーが認められ、充放電効率は87%であった。以上の結果から、本発明に従い正極の表面をリチウムイオン伝導体で被覆することにより、充放電効率が向上することがわかる。
【0028】
上記の実施例では、リチウムイオン伝導体の被膜を形成するための溶液として、ポリフッ化ビニリデンのNMP溶液を用いているが、この溶液中にさらにリチウム塩を溶解させたものを用いて、リチウムイオン伝導体の被膜を形成してもよい。
【0029】
【発明の効果】
本発明によれば、正極からのCuの溶解反応を抑制することができ、充放電効率を向上させることができる。
【図面の簡単な説明】
【図1】本発明の実施例における充放電特性を示す図。
【図2】本発明の実施例において作製した試験セルを示す模式図。
【符号の説明】
1…正極
2…負極
3…参照極
4…セパレータ
5…容器
Claims (6)
- Cuを活物質として含む正極と、非水電解質と、リチウムを吸蔵・放出する材料を含む負極とを備え、LiFが、前記正極、前記非水電解質、及び前記負極の少なくともいずれかに含まれている非水電解質二次電池であって、
前記正極または前記正極の活物質の表面がリチウムイオン伝導体で被覆されていることを特徴とする非水電解質二次電池。 - LiFが、前記正極に含まれていることを特徴とする請求項1に記載の非水電解質二次電池。
- 前記リチウムイオン伝導体が、ポリフッ化ビニリデン、ポリメタクリレート、及びトリプロピレングリコールジアクリレートの重合体から選ばれる少なくとも1種であることを特徴とする請求項1または2に記載の非水電解質二次電池。
- 前記非水電解質が、フッ素を含むリチウム塩を溶質として含有していることを特徴とする請求項1〜3のいずれか1項に記載の非水電解質二次電池。
- 前記フッ素を含むリチウム塩が、LiPF6、LiBF4、LiF・(C6F5)3B、LiCl・(C6F5)3B、LiAsF6、及びLiSbF6から選ばれる少なくとも1種のリチウム塩であることを特徴とする請求項4に記載の非水電解質二次電池。
- 前記負極の材料が、炭素、ケイ素、ゲルマニウム、及び錫から選ばれる少なくとも1種からなることを特徴とする請求項1〜5のいずれか1項に記載の非水電解質二次電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002275555A JP4030397B2 (ja) | 2002-05-23 | 2002-09-20 | 非水電解質二次電池 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002148581 | 2002-05-23 | ||
| JP2002275555A JP4030397B2 (ja) | 2002-05-23 | 2002-09-20 | 非水電解質二次電池 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2004047405A JP2004047405A (ja) | 2004-02-12 |
| JP4030397B2 true JP4030397B2 (ja) | 2008-01-09 |
Family
ID=31719660
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002275555A Expired - Fee Related JP4030397B2 (ja) | 2002-05-23 | 2002-09-20 | 非水電解質二次電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4030397B2 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4593488B2 (ja) * | 2005-02-10 | 2010-12-08 | 昭和電工株式会社 | 二次電池用集電体、二次電池用正極、二次電池用負極、二次電池及びそれらの製造方法 |
| JP5249258B2 (ja) * | 2005-02-10 | 2013-07-31 | 昭和電工株式会社 | 二次電池用集電体、二次電池用正極、二次電池用負極、二次電池及びそれらの製造方法 |
| JP2007194104A (ja) * | 2006-01-20 | 2007-08-02 | Sony Corp | ゲル状電解質電池 |
| KR102468500B1 (ko) | 2018-07-02 | 2022-11-17 | 주식회사 엘지에너지솔루션 | 황-탄소 복합체, 이를 포함하는 리튬-황 전지용 양극 및 리튬-황 전지 |
-
2002
- 2002-09-20 JP JP2002275555A patent/JP4030397B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2004047405A (ja) | 2004-02-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4725728B2 (ja) | 二次電池 | |
| JP4449907B2 (ja) | 二次電池用電解液およびそれを用いた二次電池 | |
| JP2021044254A5 (ja) | ||
| JP5376771B2 (ja) | 有機電解液及びこれを採用したリチウム電池 | |
| JP5306749B2 (ja) | 電気化学デバイス | |
| JP4433163B2 (ja) | リチウム二次電池用電解液およびそれを用いたリチウム二次電池 | |
| TW200948795A (en) | Non-aqueous electrolyte and non-aqueous electrolyte secondary battery using the same | |
| JP4465968B2 (ja) | 二次電池用電解液およびそれを用いた二次電池 | |
| JP4352719B2 (ja) | リチウムイオン二次電池用電解液およびそれを用いたリチウムイオン二次電池 | |
| JP2009105069A (ja) | リチウム二次電池用電解液及びこれを含むリチウム二次電池 | |
| KR101972034B1 (ko) | 아미노 기능화 환원 그래핀 옥사이드 박막을 포함하는 이차전지 음극 보호용 고체-전해질 중간상, 이의 제조방법 및 이를 포함하는 리튬금속 이차전지 | |
| JP4345641B2 (ja) | 二次電池 | |
| JP2003203674A (ja) | 非水電解質二次電池 | |
| JP3199426B2 (ja) | 非水電解液二次電池 | |
| JP4328915B2 (ja) | 二次電池用非水電解液及びそれを用いた二次電池 | |
| JP4345643B2 (ja) | 二次電池 | |
| JP2004047416A (ja) | 非水電解質電池 | |
| JP2006156315A (ja) | 二次電池 | |
| JP4701601B2 (ja) | リチウム二次電池用電解液およびそれを用いたリチウム二次電池 | |
| JP5421220B2 (ja) | 二次電池用電解液および二次電池 | |
| CN114865073B (zh) | 一种金属锂电池 | |
| JP4030397B2 (ja) | 非水電解質二次電池 | |
| JP4265169B2 (ja) | 二次電池用電解液およびそれを用いた二次電池 | |
| JP2006351332A (ja) | 非水電解液二次電池の充放電方法 | |
| JP2007173014A (ja) | 非水電解質二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050107 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20070420 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20070529 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070726 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20070918 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20071016 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20101026 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20101026 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111026 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111026 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121026 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121026 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131026 Year of fee payment: 6 |
|
| LAPS | Cancellation because of no payment of annual fees |