JP3916632B2 - 形態形成及び成長促進活性を有する新規化学物質 - Google Patents
形態形成及び成長促進活性を有する新規化学物質 Download PDFInfo
- Publication number
- JP3916632B2 JP3916632B2 JP2004521191A JP2004521191A JP3916632B2 JP 3916632 B2 JP3916632 B2 JP 3916632B2 JP 2004521191 A JP2004521191 A JP 2004521191A JP 2004521191 A JP2004521191 A JP 2004521191A JP 3916632 B2 JP3916632 B2 JP 3916632B2
- Authority
- JP
- Japan
- Prior art keywords
- chemical substance
- culture
- strain
- new chemical
- substance
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07G—COMPOUNDS OF UNKNOWN CONSTITUTION
- C07G13/00—Vitamins of unknown constitution
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01G—HORTICULTURE; CULTIVATION OF VEGETABLES, FLOWERS, RICE, FRUIT, VINES, HOPS OR SEAWEED; FORESTRY; WATERING
- A01G33/00—Cultivation of seaweed or algae
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/80—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having two double bonds between ring members or between ring members and non-ring members
- C07D211/84—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having two double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms, with at the most one bond to halogen directly attached to ring carbon atoms
- C07D211/90—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/78—Carbon atoms having three bonds to hetero atoms, with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/84—Nitriles
- C07D213/85—Nitriles in position 3
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/12—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains three hetero rings
- C07D491/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/12—Unicellular algae; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P1/00—Preparation of compounds or compositions, not provided for in groups C12P3/00 - C12P39/00, by using microorganisms or enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P11/00—Preparation of sulfur-containing organic compounds
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P17/00—Preparation of heterocyclic carbon compounds with only O, N, S, Se or Te as ring hetero atoms
- C12P17/02—Oxygen as only ring hetero atoms
- C12P17/06—Oxygen as only ring hetero atoms containing a six-membered hetero ring, e.g. fluorescein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P17/00—Preparation of heterocyclic carbon compounds with only O, N, S, Se or Te as ring hetero atoms
- C12P17/10—Nitrogen as only ring hetero atom
- C12P17/12—Nitrogen as only ring hetero atom containing a six-membered hetero ring
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P17/00—Preparation of heterocyclic carbon compounds with only O, N, S, Se or Te as ring hetero atoms
- C12P17/18—Preparation of heterocyclic carbon compounds with only O, N, S, Se or Te as ring hetero atoms containing at least two hetero rings condensed among themselves or condensed with a common carbocyclic ring system, e.g. rifamycin
- C12P17/188—Heterocyclic compound containing in the condensed system at least one hetero ring having nitrogen atoms and oxygen atoms as the only ring heteroatoms
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A40/00—Adaptation technologies in agriculture, forestry, livestock or agroalimentary production
- Y02A40/80—Adaptation technologies in agriculture, forestry, livestock or agroalimentary production in fisheries management
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Health & Medical Sciences (AREA)
- Biotechnology (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Genetics & Genomics (AREA)
- General Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Marine Sciences & Fisheries (AREA)
- Environmental Sciences (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Mycology (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Botany (AREA)
- Cell Biology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Virology (AREA)
- Biomedical Technology (AREA)
- Epidemiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Breeding Of Plants And Reproduction By Means Of Culturing (AREA)
- Pyrane Compounds (AREA)
Description
本発明はこのような新規ビタミン様作用物質を提供することを目的とする。
本発明者は、かかる事情を鑑み、新規な有効成分の探索を行い、その結果YM−2−23株(受託番号FERM BP−8417で、2001年8月20日付(原寄託)で独立行政法人 産業技術総合研究所 特許生物寄託センター(日本国茨城県つくば市東1丁目1番地1 中央第6)に寄託されている(2003年6月25日付で原寄託よりブダペスト条約に基づく寄託への移管請求受領))、テナシバキュラム・スピーシーズ(Tenacibaculum sp.)YM−1−69(受託番号FERM BP−8418で、2001年8月20日付(原寄託)で独立行政法人 産業技術総合研究所 特許生物寄託センター(日本国茨城県つくば市東1丁目1番地1 中央第6)に寄託されている(2003年6月25日付で原寄託よりブダペスト条約に基づく寄託への移管請求受領))、及びそれらの類似菌株の培養液から極めて強い活性を有する活性物質を単離し、またその化合物が新規物質であることを見出し、本発明を完成した。これまでYM−2−23株及び/又はYM−1−69株に類似するフラボバクテリウム(Flavobacterium)属、ゾベリア(Zobellia)属又はテナシバキュラム(Tenacibaculum)属の産生する物質としてはリコペン、ゼアキサンチン等のカロテノイド類縁体が報告されているが、大型藻類の成長を促進する、あるいは形態をコントロールするような化合物の単離例はなく、世界で初めての報告となる。
すなわち、本発明は、以下の発明を包含する。
(1)下記の理化学的性質:
1.物質の色:無色
2.分子量:457
3.分子式:C24H31N3O4S
質量分析:FABMS:m/z 456[M−H]−(図1)
高分解能質量分析:実測値 456.1960[M−H]−
計算値 456.1930(C24H30N3O4S)
4.核磁気共鳴シグナル:
1)1H−NMR(D2O−20mM Na2HPO4(pH9)、750MHz):(図2)
δppm0.818(3H,s),0.837(3H,s),0.882(3H,s),0.960(1H,m),1.058(1H,m),1.167(1H,m),1.326(3H,s),1.37(1H,m),1.38(1H,m),1.40(1H,m),1.58(1H,m),1.61(2H,m),1.52(1H,br d,J=13Hz),1.76(1H,br d,J=14Hz),2.024(1H,m),2.181(1H,dd,J=4,14Hz),2.291(1H,dd,J=14,16.5Hz),7.698(1H,d,J=7.5Hz),7.845(1H,d,J=7.5Hz)
2)13C−NMR(D2O−20mM Na2HPO4(pH9)、125MHz):(図3)
δppm15.236(q),19.037(t),20.287(t),20.955(q),21.835(q),25.987(t),33.381(s),33.636(q),37.308(s),39.590(t),41.199(t),42.346(t),52.769(d),56.381(d),79.096(s),114.965(s),124.399(d),139.004(s),141.232(d),150.282(s),152.656(s),172.081(s),173.538(s),174.661(s)
を有する新規化学物質1。
(2)下記の理化学的性質:
1.物質の色:無色
2.核磁気共鳴シグナル:
1H−NMR(D2O−20mM Na2HPO4(pH9)、500MHz):(図4)
δppm0.815(3H,s),0.834(3H,s),0.877(3H,s),0.949(1H,m),1.048(1H,m),1.163(1H,m),1.297(3H,s),1.35−1.40(3H,m),1.52−1.63(4H,m),1.753(1H,br d,J=14Hz),2.012(1H,m),2.158(1H,m),2.299(1H,m),7.646(1H,d,J=8.0Hz),7.769(1H,d,J=8.0Hz)
を有する新規化学物質2。
(3)前記(1)に記載の新規化学物質1又は前記(2)に記載の新規化学物質2を生産する能力を有する微生物を培地に培養し、培養物中に新規化学物質1又は2を生成蓄積させ、該生成蓄積した新規化学物質1又は2を採取することを特徴とする新規化学物質1又は2の製造法。
(4)微生物がYM−2−23株(FERM BP−8417)、テナシバキュラム・スピーシーズ(Tenacibaculum sp.)YM−1−69(FERM BP−8418)又はそれらの類似菌株である前記(3)に記載の製造法。
(5)前記(1)に記載の新規化学物質1又は前記(2)に記載の新規化学物質2を有効成分として含有する藻類培養用培地。
(6)前記(1)に記載の新規化学物質1をトリメチルシリルジアゾメタンで処理することにより得られる該新規化学物質1のモノメチル化体、ジメチル化体又はトリメチル化体。
(7)前記(6)に記載のトリメチル化体を水素化ホウ素ナトリウムで処理することにより得られる化合物又はその誘導体。
以下、本発明を詳細に説明する。
本発明の新規化学物質1及び2は、微生物を用いて生産することが可能である。本発明の化学物質の製造に用いる微生物としては、該化学物質の生産能を有する微生物であれば特に限定されず、例えば、フラボバクテリウム属、ゾベリア属、テナシバキュラム属等のCytophaga−Flavobacterium−Bacteriodes complexに属する菌株や、これらの菌株に由来する変異株を挙げることができる。具体的には、YM−2−23株(FERM BP−8417)、テナシバキュラム・スピーシーズ(Tenacibaculum sp.)YM−1−69(FERM BP−8418)や、これらの菌株に由来する変異株を挙げることができる。YM−1−69株やYM−2−23株の代わりに、これらの菌株の類似菌株を使用してもよい。「YM−1−69株の類似菌株」には、例えば、海洋性大型緑藻類に対し葉状体形成活性又は生長促進活性を示す菌株であって、配列番号1記載の塩基配列と85%以上、好ましくは95%以上相同な塩基配列で表される16S rRNA V3領域遺伝子を持つ菌株や配列番号3記載の塩基配列と72%以上、好ましくは95%以上相同な塩基配列で表されるgyrB遺伝子を持つ菌株が含まれる。「YM−2−23株の類似菌株」には、例えば、海洋性大型緑藻類に対し葉状体形成活性又は生長促進活性を示す菌株であって、配列番号2記載の塩基配列と85%以上、好ましくは95%以上相同な塩基配列で表される16S rRNA V3領域遺伝子を持つ菌株や配列番号4記載の塩基配列と72%以上、好ましくは80%以上、更に好ましくは95%以上相同な塩基配列で表されるgyrB遺伝子を持つ菌株が含まれる。
「YM−1−69株の類似菌株」及び「YM−2−23株の類似菌株」としては、例えばYM2−10(MBIC 04671)、YM2−11(MBIC 04672)、YM2−12(MBIC 04673)、YM2−13(MBIC 04674)、YM1−66(MBIC 04663)、YM2−24(MBIC 04684)、YM1−51(MBIC 04662)、Zobellia uliginosa(ATCC 14397)、YM1−11(MBIC 04693)、T−588(MBIC 05930)、YM2−22(MBIC 04682)、YM2−27(MBIC 04687)、YM2−6(MBIC 04669)、YM1−68(MBIC 04664)、YM1−38(MBIC 04661)、YM2−4(MBIC 04667)、YM2−5(MBIC 04668)、YM2−7(MBIC 04670)、YM2−21(MBIC 04681)、YM2−1(MBIC 04666)、T−565(MBIC 05877)、T−424(MBIC 05876)、[Cytophaga]sp.UP7(MBIC 01484)、T−551(MBIC 05929)、Pedobacter heparinus(IFO 12017)、T−561(MBIC 05879)、Cyclobacterium marinum(LMG 13164)、Cytophaga sp.(MBIC 01539)、Cytophaga sp.(MBIC 01599)、Chitinophaga pinensis(DSM 2588)が挙げられる。
前記の菌株のうち、「MBIC」が付された菌株は、海洋バイオテクノロジー研究所カルチャーコレクション(Marine Biotechnology Institute Culture collection;MBIC)(日本国岩手県釜石市平田3−75−1)(http://seasquirt.mbio.co.jp/mbic/index.php?page=top)から、「IFO」が付された菌株は、財団法人発酵研究所(Institute for Fermentation,Osaka;IFO)(日本国大阪府大阪市淀川区十三本町2丁目17番85号)から、「ATCC」が付された菌株は、アメリカン タイプ カルチャー コレクション(American Type Culture Collection;ATCC)(12301 Parklawn Drive,Rockville,Maryland 20852,U.S.A.)から、「DSM」が付された菌株は、Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH(DSMZ)(Mascheroder Weg 1b,38124 Braunschweig,Germany)から、「LMG」が付された菌株は、BCCMTM/LMG Bateria Collection(Belgian Co−ordinated Collections of Micro−organisms,Laboratorium voor Microbiologie,Universiteit Gent(RUG),K.L.Ledegancksfaat 35,B−9000 Gent,Brussels,Belgium)から、それぞれ入手可能である。
16S rRNA V3領域遺伝子及び/又はgyrB遺伝子の塩基配列がYM−1−69株やYM−2−23株のそれと同一である菌株は、これらの類似菌株の中でも特に好ましい菌株である。
前記の微生物の培養に際しては、通常の海洋細菌の培養方法が一般に用いられる。培地としては資化可能な炭素源、窒素源、無機物などを程よく含有する培地であれば合成培地、天然培地のいずれでも使用可能である。
炭素源としては、グルコース、澱粉、デキストリン、マンノース、フルクトース、シュクロース、ラクトース、キシロース、アラビノース、マンニトール、糖蜜などが単独又は組合せて用いられる。更に、菌の資化能によっては炭化水素、アルコール類、有機酸なども用いられる。
窒素源としては、塩化アンモニウム、硝酸アンモニウム、硫酸アンモニウム、硝酸ナトリウム、尿素、ペプトン、肉エキス、酵母エキス、乾燥酵母、コーン・スチープ・リカー、大豆粉、カザミノ酸などが単独又は組合せて用いられる。
そのほか、必要に応じて塩化ナトリウム、塩化カリウム、硫酸マグネシウム、炭酸カルシウム、リン酸二水素カリウム、リン酸マグネシウム・8水塩、硫酸第一鉄、塩化カルシウム、硫酸マンガン、硫酸亜鉛、硫酸銅などの無機塩類を加える。
更に、使用菌の生育や本発明の化学物質の生産を促進する微量成分(例えば糖類、アミノ酸、無機塩類など)を適当に添加することができる。
培養法としては、液体培養が最も効率よく、培養温度は30℃程度が適当であり、培地のpHは、通常7〜9、好ましくは7.5〜8である。培地のpH調整には水酸化ナトリウム水溶液や塩酸などが用いられる。
液体培養で1〜4日間培養を行うと、新規化学物質1又は2が培養液中及び菌体中に生成蓄積される。培養物中の生成量が最大に達したときに培養を停止することが好ましい。特に、培養3日後がもっとも好ましい。
培養物から新規化学物質1又は2を単離精製するに際しては、微生物代謝産物をその培養物から単離精製するために常用される方法に従って行われる。例えば、培養物を濾過や遠心分離により培養濾液と菌体に分け、菌体を含水メタノール、含水アセトニトリルなどで抽出する。次いで、抽出液から有機溶媒をロータリーエバポレーター等で減圧除去し、この抽出液と培養濾液とをあわせてポリスチレン系吸着剤(例えばスチレンジビニルベンゼンポリマー)などに吸着させる。吸着した活性物質を水洗して脱塩し、含水メタノール、含水アセトニトリルなどで活性物質を溶出する。溶出液を凍結乾燥などで減圧濃縮し、スチレンジビニルベンゼン系ポリマー、陰イオン交換樹脂によるイオン交換クロマトグラフィー、ゲル濾過クロマトグラフィー、高速液体クロマトグラフィーなどにより、新規化学物質1又は2を得る。新規化学物質2は極めて不安定な化合物であるが、新規化学物質2を水酸化ナトリウム水溶液やアンモニア水などの強アルカリ水溶液中におくことにより、徐々に新規化学物質1に変化する。新規化学物質1は極めて安定な化合物である。
新規化学物質1を適当なメチル化剤(例えば、トリメチルシリルジアゾメタン)で処理することにより、新規化学物質1のモノメチル化体、ジメチル化体又はトリメチル化体を得ることができる。トリメチルシリルジアゾメタンの新規化学物質1に対するモル比を調節したり、反応条件の選択(例えば、反応温度やpHの設定、ジメチルアミノスルファートリフルオリド(DAST)の存在下で反応)により、モノメチル化体、ジメチル化体又はトリメチル化体を選択的に得ることができる。
更に、前記トリメチル化体を水素化ホウ素ナトリウムで処理することにより、後述する理化学的性質を有するMe1H3を得ることができる。また、反応溶媒の極性、反応温度を変えることによりMe1H3よりも更に還元された化合物Me1H1を得ることができる。また、Me1H1を強アルカリ条件下、式:RI(ここで、Rは炭素数1〜6のアルキル基を表す。)で示されるヨウ化アルキル(例えば、ヨウ化メチル)を作用させることによりメチル化体Me1H1Me等のアルキル化体を得ることができる。これらの反応と、得られる生成物の情報は新規化学物質1及び2を特定する場合等に有益である。
本発明の新規化学物質1及び2は、藻類培養用培地の有効成分として有用である。新規化学物質1及び2は、単独で用いても、また両者を併用してもよい。
前記藻類培養用培地の適用対象となる藻類としては、好ましくは海洋性大型緑藻類が挙げられる。海洋性大型緑藻類としては、アオサ(ULVALES)目の海藻で、例えば、ヒトエグサ科(Monostromataceae)、アオサ科(Ulvaceae)などの緑藻を挙げることができる。具体的にはヒトエグサ科に属する海藻としてヒトエグサ属ヒトエグサ(Monostroma nitidum)、同属マキヒトエ(Monostroma oxyspermum)、同属エゾヒトエグサ(Monostroma angicava)、アオサ科に属する海藻としてアオノリ属ヒラアオノリ(Enteromorpha compressa)、同属ボウアオノリ(Enteromorpha intestinalis)、同属ウスバアオノリ(Enteromorpha linza)、アオサ属ボタンアオサ(Ulva conglobata)、同属アナアオサ(Ulva pertusa)などを例示することができる。
海洋性大型緑藻類の培養に使用する培地は、有効成分である新規化学物質1及び/又は2を含むこと以外は、従来の培養方法(海洋性大型緑藻類が単細胞化してしまう培養方法)で使用されていたものと同様でよく、例えば、ASP7培地、PES培地、PESI培地など、又は単に滅菌済みの海水を使用することができる。培地中における新規化学物質1及び/又は2の有効濃度は、葉状体形成誘導を発揮できる範囲内であれば特に限定されないが、10−12〜10−3μg/mlとするのが好ましい。
培養時の温度は、海洋性大型緑藻類が生存できる範囲内であれば特に制限はないが、15〜25℃程度が適当である。
図2は、新規化学物質1の1H−NMRスペクトルを示す。
図3は、新規化学物質1の13C−NMRスペクトルを示す。
図4は、新規化学物質2の1H−NMRスペクトルを示す。
図5は、実施例1のマキヒトエ培養実験におけるサンプルを添加しない場合の培養5日後のマキヒトエ培養細胞の写真である。
図6は、実施例1のマキヒトエ培養実験におけるサンプルを添加した場合の培養5日後のマキヒトエ培養細胞の写真である。
図7は、Me1の1H−NMRスペクトルを示す。
図8は、Me1の13C−NMRスペクトルを示す。
図9は、Me1Bの1H−NMRスペクトルを示す。
図10は、Me1H3の1H−NMRスペクトルを示す。
図11は、Me1H1の1H−NMRスペクトルを示す。
図12は、Me1H1Meの1H−NMRスペクトルを示す。
図13は、実施例5の培養10日後の7段階希釈の写真である。
図14は、実施例5の培養10日後の6段階希釈の写真である。
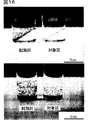
図15は、実施例7におけるアナアオサでの実験結果を示す写真である。
図16は、実施例7におけるボウアオノリでの実験結果を示す写真である。
図17は、YM−1−69株、YM−2−23株及びこれらの類似菌株のgyrB DNA系統樹を示す。
図18は、YM−1−69株、YM−2−23株及びこれら類似菌株の16S rDNA系統樹、並びにこれらの菌株の大型緑藻に対する形態形成誘導の比活性を示す。
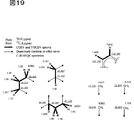
図19は、新規化学物質1の部分構造を示す。
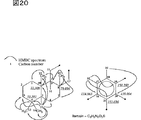
図20は、新規化学物質1のHMBCスペクトルを解析した結果を示す。
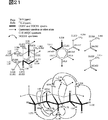
図21は、Me1の部分構造及び相対立体配置を示す。
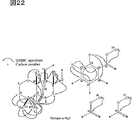
図22は、Me1のHMBCスペクトルを解析した結果を示す。
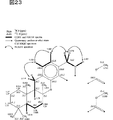
図23は、Me1H3のスペクトルを解析した結果を示す。
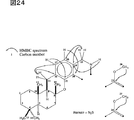
図24は、Me1H3のHMBCスペクトルを解析した結果を示す。
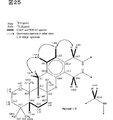
図25は、Me1H1のスペクトルを解析した結果を示す。
図26は、Me1H1のHMBCスペクトルを解析した結果を示す。
図27は、Me1H1Meのスペクトルを解析した結果を示す。
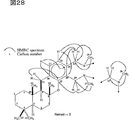
図28は、Me1H1MeのHMBCスペクトルを解析した結果を示す。
本明細書は、本願の優先権の基礎である特願2002−203608の明細書及び/又は図面に記載される内容を包含する。
〔参考例1〕微生物の単離
本発明に使用する菌株は以下のように単離した。採集した新鮮藻体約1グラムに滅菌済みの海水10ミリリットルを添加し、1分程度激しくボルテックスした。上清を滅菌済み海水で更に10倍、100倍希釈し、そのうち100マイクロリットルを1/10マリンアガープレートに分注し、滅菌済みのコンラージ棒でプレート全体に塗り広げた。室温で2〜3日後に成長した黄〜赤色のコロニーをそれぞれ別のマリンアガープレートに植菌し、単菌化されるまで植菌を続けた。24穴あるいは48穴のマイクロプレートに2ないし1ミリリットルのASP7培地を分注し、それぞれのウェルに単細胞化したマキヒトエを20細胞程度添加した。これに単菌化した各分離株のコロニーを滅菌済みの白金耳などを使って2穴ずつ直接接種した。このプレートを19〜22℃、明期14時間/暗期10時間で5日間培養し、マキヒトエの葉状体形成を倒立顕微鏡下で確認した。葉状体の形成がみられた菌株については前記と同じ方法で追試を行って確認をした。以上のようなスクリーニングの結果、葉状体形成活性を示す菌株として、YM−1−69株とYM−2−23株が単離された。YM−1−69株はサボテングサ(Halimeda opuntia)(緑藻ミル目)から単離された菌株であり、YM−2−23株はヒトエグサ(Monostroma nitidum)(緑藻アオサ目)から単離された菌株である。
〔参考例2〕微生物の同定
参考例1で得られた微生物の16S rRNA V3領域及びgyrB遺伝子のDNA塩基配列を決定した。YM−1−69株の16S rRNA V3領域及びgyrB遺伝子のDNA塩基配列をそれぞれ配列番号1及び配列番号3に示す。また、YM−2−23株の16S rRNA V3領域及びgyrB遺伝子のDNA塩基配列をそれぞれ配列番号2及び配列番号4に示す。得られた配列についてデータベース検索(DDBJ−fasta)を行った結果、各配列は表1に示す微生物の配列と高い相同性を示した。
また、YM−1−69株及びYM−2−23株の生理生化学的性質について調査した結果を表2に示す。
表1及び表2の結果から、YM−1−69株はテナシバキュラム・スピーシーズ(Tenacibaculum sp.)と同定され、YM−2−23株はCytophaga−Flavobacterium−Bacteriodes complexに属する菌株と同定された。
[実施例1]マキヒトエ培養実験
抗生物質等で無菌化処理したマキヒトエ(Monostroma oxyspermum)はASP7培地などの合成培地中では天然に見られるような葉状形態を失い、ほぼ単細胞状態となる。
48孔浮遊培養用マイクロプレート(IWAKI社製、以下48−MTPと略す)の一列目に改変ASP7培地を1ml、二列目以降に0.9mlを添加し、一列目に試験対象となる活性物質分画フラクションを11μlずつ添加し、ピペッティングによりよく撹拌しながら次の列に100μlを添加した。この操作を各フラクションに対して8〜18回繰りかえすことにより、10倍ずつの希釈系列を8〜18段階作成することができる。最後の列に余る100μlは破棄した。ここに、最終的に細胞濃度が1mlあたり10〜20細胞となるように希釈したマキヒトエ培養液を48−MTPのすべての孔に100μlずつ添加して総量を1mlとした。この48−MTPを明期のみの条件で22℃、3〜5日間培養し、倒立顕微鏡下で葉状体形成の判定を行った。葉状体形成が見られた最も低いサンプル濃度を最少有効濃度(MEC)と定義し、MECの最も低いサンプルに活性物質が集中していると考え、分離の指標とした。
サンプルを添加しない場合の培養5日後のマキヒトエ培養細胞の写真を図5に示す。また、サンプルを添加した場合の培養5日後のマキヒトエ培養細胞の写真を図6に示す。活性物質が存在した場合は図6のように葉状体の形成が見られた。
なお、ASP7培地の組成は以下の通りである。
[実施例2]新規化学物質1の分離・精製
種菌としてYM−2−23株(FERM BP−8417)を用いた。本培養培地は、マリンブロス(ディフコ社製、37.4g/l、又は表示成分に従って各試薬を混合して調製)を用いた。該菌株を100ml三角フラスコ中で50mlのマリンブロスを用いて30℃で24時間振盪(毎分100回転)培養し、これを更に培地450mlのバッフル付1リットル容三角フラスコに全量を植菌し、同様の条件で24時間培養した。本培養は、培地が800ml入ったバッフル付1リットル容三角フラスコ16本で振盪培養(毎分130回転)及び培地が450ml入った1リットル容三角フラスコ10本で振盪培養(毎分100回転)で行い、培養温度30℃、培養時間は3日間とした。このようにして得られた培養液約18リットルを遠心分離した。菌体は抽出するまで−20℃に、培養濾液は4℃で保管した。前記本培養4回分(約72リットル分)の菌体を50%アセトニトリル水溶液1200mlで二回抽出し、濃縮した。濃縮液を培養濾液約72リットルとあわせ、スチレンジビニルベンゼンポリマーであるダイヤイオンHP−20(三菱化学株式会社)2500mlに吸着させた。樹脂を10%アセトニトリル水溶液6000mlで洗浄して脱塩し、50%アセトニトリル水溶液6000mlで溶出して葉状体形成誘因画分を得た。活性画分をTOYOPEARL DEAE−650(M)(東ソー株式会社)に吸着させ、180mM NaCl−20%アセトニトリルで洗浄した後、450mM NaCl−20%アセトニトリル水溶液で活性画分を溶出した。溶出画分を減圧濃縮してアセトニトリルを除いた後、ダイヤイオンHP−20(三菱化学株式会社)500mlに吸着させ、10%アセトニトリル水溶液1000mlで洗浄して脱塩し、50%アセトニトリル水溶液1000mlで活性画分を得た。減圧濃縮した後、凍結乾燥を行い葉状体形成誘因画分を得た。前記培養と粗画分の調製二回分(培養液約140リットル分)をあわせて、移動相として100mM NaCl−20mM Na2HPO4−20%アセトニトリル水溶液(pH9)を用いたゲル濾過クロマトグラフィー(アマシャムバイオサイエンス株式会社製Sephacryl S−100 HR内径25mm×長さ1200mm)で精製し、葉状体誘因活性を示す画分を得た。この活性画分を濃縮、脱塩後、凍結乾燥し、移動相として14〜22%アセトニトリル−5g(NH4)2CO3/l水溶液を用いた高速液体クロマトグラフィー(アマシャムバイオサイエンス株式会社製RESOURCE RPC 3 ML、内径6.4mm×長さ100mm×2本直列)で分離し、活性画分を凍結乾燥後、更に移動相として5〜25%アセトニトリル−1% NH3水溶液を用いた高速液体クロマトグラフィー(アマシャムバイオサイエンス株式会社製RESOURCE RPC 3 ML、内径6.4mm×長さ100mm×2本直列)にて精製したところ、前記の理化学的性質を有する本発明の新規化学物質1を約140μg得た。
[実施例3]新規化学物質2の分離・精製
実施例2に従って分離される新規化学物質1は最終精製における5〜25%アセトニトリル−1% NH3水溶液という強アルカリ条件で新規化学物質2が変化したものであることが明らかになっている。また、新規化学物質1は精製前の培養液上清に新規化学物質2とともに存在する。新規化学物質2は中性−弱酸性で極めて不安定であるがアルカリ条件で誘導される新規化学物質1は比較的安定である。実施例2における最終精製の段階で、移動相として17%アセトニトリル−5g(NH4)2CO3+5ml NH3/l水溶液を用いた高速液体クロマトグラフィー(アマシャムバイオサイエンス株式会社製RESOURCE RPC 3 ML、内径6.4mm×長さ100mm×2本直列)により分離を行うと図4のような1H−NMRスペクトルを示す化学物質2を得ることができる。
[実施例4]新規化学物質1のメチル化体及びその誘導体の調製と理化学的性質
新規化学物質1約140μgをメタノール40μlに溶かし、ベンゼン160μl、トリメチルシリルジアゾメタン(10%、n−ヘキサン溶液、東京化成工業株式会社製)100μlを添加してよく撹拌し室温で2時間反応させた。ジアゾメタンの黄色が消えるまで少量ずつ酢酸を添加し、エバポレーターで溶媒を留去した後、移動相として50〜100%アセトニトリル−水を用いた高速液体クロマトグラフィー(東ソー株式会社製TSKgel ODS−80Ts、内径4.6mm×長さ150mm)にて分離したところほぼ定量的(収量約152μg、収率99%)に新規化学物質1のトリメチル体(以下Me1と略す)を得た。また、このトリメチル体はNMR測定溶媒である重メタノール中でメトキシ基(−OCH3)の一つが徐々に重メトキシ基(−OCD3)と置換しMe1Bを与える。Me1約152μgをメタノール200μlに溶かし氷冷下水素化ホウ素ナトリウム1mgを添加し1時間還元させた。反応液を、移動相として50〜100%アセトニトリル−水を用いた高速液体クロマトグラフィー(東ソー株式会社製TSKgel ODS−80Ts、内径4.6mm×長さ150mm)にて分離したところ高収量で(収量約140μg、収率98%)Me1の還元体(以下Me1H3と略す)を得た。ここで得たMe1H3の全量を乾燥ジエチルエーテル400μlに溶かし、室温で20mg/ml水素化ホウ素ナトリウムエタノール溶液100μlを添加し室温で150分間反応させた。飽和塩化ナトリウム水溶液100μlを添加して10分間撹拌した後、エバポレーターで溶媒を留去した。移動相として50〜100%アセトニトリル−水を用いた高速液体クロマトグラフィー(東ソー株式会社製TSKgel ODS−80Ts、内径4.6mm×長さ150mm)にて分離したところほぼ定量的(収量約123μg、収率99%)にMe1の高還元体(以下Me1H1と略す)を得た。更に、ここで得たMe1H1の全量を乾燥ジメチルスルホキシド400μlに溶かし、細かく砕いた水酸化ナトリウム1mgを添加した後、ヨウ化メチル40μlを加えて室温で30分反応させた。氷冷下、蒸留水500μlを加えて反応を止めた後、移動相として50〜100%アセトニトリル−水を用いた高速液体クロマトグラフィー(東ソー株式会社製TSKgel ODS−80Ts、内径4.6mm×長さ150mm)にて反応液をそのまま分離したところほぼ定量的(収量約135μg、収率99%)にMe1H1のメチル化体(以下Me1H1Meと略す)を得た。
ここで得た化合物は、以下に示した理化学的性質を示した。
[Me1の理化学的性質]
1.物質の色:無色
2.分子量:499
3.分子式:C27H37N3O4S
質量分析:FABMS:m/z 500[M+H]+
高分解能質量分析:実測値 500.2569[M+H]+
計算値 500.2583(C27H38N3O4S)
4.核磁気共鳴シグナル:
1)1H−NMR(重メタノール、500MHz):(図7)
δppm0.916(3H,s),0.941(3H,s),0.973(3H,s),1.086(1H,ddd,J=3.5,12.5,13.0Hz),1.136(1H,dd,J=2.0,12.0Hz),1.271(1H,ddd,J=4.0,13.0,14.0Hz),1.380(3H,s),1.47(2H,m),1.50(1H,m),1.65(1H,m),1.69(2H,m),1.73(1H,m),1.84(1H,m),2.130(1H,ddd,J=3.5,7.0,12.5Hz),2.34(2H,m),3.488(3H,s),3.914(3H,s),4.034(3H,s),7.911(1H,d,J=8.0Hz),8.258(1H,d,J=8.0Hz)
2)13C−NMR(重メタノール、125MHz):(図8)
δppm15.413(q),19.559(t),20.797(t),20.961(q),21.981(q),28.416(t),33.855(q),34.164(s),37.928(s),40.356(t),41.722(t),42.996(t),52.266(q),53.255(q),52.255(q),53.328(d),57.432(d),79.291(s),120.0(s),127.392(d),140.407(d),141.6(s),146.659(s),149.8(s),164.761(s),166.027(s),167.402(s)
5.溶解性:水及びDMSOに難溶、50〜100%メタノール水溶液、50〜100%アセトニトリル水溶液などの含水溶媒に可溶、ヘキサン、クロロホルム等の低極性有機溶媒に難溶。
[Me1Bの理化学的性質]
1.物質の色:無色
2.分子量:502
3.分子式:C27H34D3N3O4S
質量分析:FABMS:m/z 503[M+H]+
高分解能質量分析:実測値 503.2777[M+H]+
計算値 503.2772(C27H35D3N3O4S)
4.核磁気共鳴シグナル:
1H−NMR(重メタノール、500MHz):(図9)
δppm0.916(3H,s),0.941(3H,s),0.973(3H,s),1.086(1H,ddd,J=3.5,12.5,13.0Hz),1.136(1H,dd,J=2.0,12.0Hz),1.271(1H,ddd,J=4.0,13.0,14.0Hz),1.380(3H,s),1.47(2H,m),1.50(1H,m),1.65(1H,m),1.69(2H,m),1.73(1H,m),1.84(1H,m),2.130(1H,ddd,J=3.5,7.0,12.5Hz),2.34(2H,m),3.488(3H,s),3.914(3H,s),7.911(1H,d,J=8.0Hz),8.258(1H,d,J=8.0Hz)
5.溶解性:水及びDMSOに難溶、50〜100%メタノール水溶液、50〜100%アセトニトリル水溶液などの含水溶媒に可溶、ヘキサン、クロロホルム等の低極性有機溶媒に難溶。
[Me1H3の理化学的性質]
1.物質の色:無色
2.分子量:471
3.分子式:C26H37N3O3S
質量分析:FABMS:m/z 472[M+H]+
高分解能質量分析:実測値 472.2630[M+H]+
計算値 472.2634(C26H38N3O3S)
4.核磁気共鳴シグナル:
1H−NMR(DMSO−d6、500MHz):(図10)
δppm0.802(3H,s),0.810(3H,s),0.885(3H,s),0.951(1H,m),1.018(1H,m),1.150(1H,m),1.254(3H,s),1.35(1H,m),1.36(1H,m)1.37(1H,m),1.50(1H,m),1.54(1H,m),1.57(1H,m),1.58(1H,m),1.688(1H,m),1.984(1H,m),2.174(2H,br d,J=8.5Hz),3.399(3H,s),3.741(3H,s),4.570(2H,br d,J=5.5Hz),5.495(1H,br t,J=5.5Hz),7.587(1H,d,J=8.0Hz),7.722(1H,d,J=8.0Hz)
2)13C−NMR(重メタノール、HMBC(Heteronuclear Multiple Bond Coherence)及びHSQC(Heteronuclear Single Quantum Coherence)スペクトルをもとにケミカルシフトを算定):
δppm14.2(q),17.7(t),19.0(t),20.0(q),21.1(q),26.7(t),33.0(q),33.3(s),36.1(s),38.3(t),40.1(t),41.1(t),51.2(q),51.2(d),52.0(q),55.2(d),63.7(t),76.8(s),119.2(s),121.8(d),134.1(s),138.3(d),146.2(s),159.8(s),162.8(s),166.2(s)
5.溶解性:水及び100%メタノールに難溶、50%メタノール水溶液、50%アセトニトリル水溶液などの含水溶媒に可溶、DMSOに可溶、ヘキサン、クロロホルム等の低極性有機溶媒に難溶。
[Me1H1の理化学的性質]
1.物質の色:無色
2.分子量:415
3.分子式:C24H37N3OS
質量分析:FABMS:m/z 416[M+H]+
高分解能質量分析:実測値 416.2747[M+H]+
計算値 416.2735(C24H38N3OS)
4.核磁気共鳴シグナル:
1)1H−NMR(重クロロホルム、500MHz):(図11)
δppm0.842(6H,s),0.918(3H,s),0.97(1H,m),1.04(1H,m),1.18(1H,m),1.327(3H,s),1.36(1H,m),1.42(1H,m),1.45(1H,m),1.55(1H,m),1.58(1H,m),1.64(1H,m),1.667(1H,dd,J=5.5,12Hz),1.78(1H,m),2.02(2H,m),2.05(1H,m),3.650(2H,d,J=12Hz),4.647(2H,d,J=14Hz),4.801(2H,br s),7.226(1H,d,J=8.0Hz),7.474(1H,d,J=8.0Hz)
2)13C−NMR(重クロロホルム、HMBC(Heteronuclear Multiple Bond Coherence)及びHSQC(Heteronuclear Single Quantum Coherence)スペクトルをもとにケミカルシフトを算定)
δppm15.1(q),18.4(t),19.8(t),20.9(q),21.5(q),25.1(t),33.2(s),33.3(q),36.8(s),39.2(t),40.7(t),41.7(t),52.5(d),56.0(d),60.61(t),62.33(t),64.73(t),77.0(s),106.0(s),119.8(d),133.2(s),139.7(d),148.0(s),156.2(s)
5.溶解性:水に難溶、10〜100%メタノール水溶液、10〜100%アセトニトリル水溶液などの含水溶媒に可溶、ヘキサン、クロロホルム等の低極性有機溶媒に可溶。
[Me1H1Meの理化学的性質]
1.物質の色:無色
2.分子量:457
3.分子式:C27H43N3OS
質量分析:FABMS:m/z 458[M+H]+
高分解能質量分析:実測値 458.3201[M+H]+
計算値 458.3205(C27H44N3OS)
4.核磁気共鳴シグナル:
1)1H−NMR(重クロロホルム、500MHz):(図12)
δppm0.847(6H,s),0.921(3H,s),0.96(1H,m),1.05(1H,m),1.18(1H,m),1.331(3H,s),1.36(1H,m),1.41(1H,m),1.43(1H,m),1.57(1H,m),1.59(1H,m),1.67(1H,m),1.68(1H,m),1.77(1H,br d,J=13Hz),2.00(1H,m),2.09(1H,m),2.16(1H,m),3.19(3H,br s),3.45(3H,br s),3.509(3H,s),3.564(2H,d,J=12Hz),4.419(2H,dd,J=8.5,10.5Hz),4.644(2H,br s),7.356(1H,d,J=7.0Hz),7.488(1H,d,J=7.0Hz)
2)13C−NMR(重クロロホルム、HMBC(Heteronuclear Multiple Bond Coherence)及びHSQC(Heteronuclear Single Quantum Coherence)スペクトルをもとにケミカルシフトを算定)
δppm15.0(q),18.7(t),20.0(t),20.6(q),21.7(q),26.2(t),33.2(s),33.5(q),36.9(s),39.4(t),41.0(t),42.0(t),52.8(d),56.2(d),58.4(q),59.0(q),59.1(q),70.2(s),74.0(s),75.6(s),76.9(s),109.9(s),120.5(d),135.1(s),139.2(d),145.7(s),155.1(s)
5.溶解性:水に難溶、30〜100%メタノール水溶液、30〜100%アセトニトリル水溶液などの含水溶媒に可溶、ヘキサン、クロロホルム等の低極性有機溶媒に可溶。
[実施例5]新規化学物質1の最少有効濃度(MEC)の検討
実施例1の場合と同様に48−MTPに単離精製した新規化学物質1を終濃度1μg/mlからはじめ、16段階希釈を行った。このとき、マキヒトエの細胞は培地1mlあたり約20細胞とした。希釈の際は一段階希釈するごとにピペットチップを交換した。このシリーズを3列用意し、実施例1と同様に3日間培養した。その結果、12段階希釈の列までマキヒトエの葉状体形成が見られた。このことから新規化学物質1のMECは、
1μg/ml×10−12=1ag/ml(atto−gram per milliliter)
となる。長期の培養に伴い、新規化学物質1は増殖したマキヒトエに消費され、葉状体が崩壊し始める。培養10日後の7段階希釈(新規化学物質1終濃度1×10−7μg/ml)の写真を図13に示す。葉状体の原型がやや残っているが葉状体崩壊が観察される。培養10日後の6段階希釈(新規化学物質1終濃度1×10−6μg/ml)の写真を図14に示す。葉状体が崩壊せずに維持されており、培養10日後のMECは、
1×10−6μg/ml=1pg/ml(pico−gram per milliliter)
となる。マキヒトエの細胞は実施例1の条件では一日に約2回細胞分裂を行うことから初期細胞数が20の場合、3日後には計算上、
20×(2×2)3=1,280細胞
であるが、10日間の培養では計算上、
20×(2×2)10=20,971,520細胞
となり、3日後と比べると10日後には細胞数が10,000倍以上に増殖しており、MECが細胞数と培養日数によって大きく変化することが説明できる。つまり、新規化学物質1は培養日数と細胞の増殖に応じて適宜添加する必要がある。
[実施例6]新規化学物質1及び誘導体の活性
実施例5と同様に新規化学物質1及びその誘導体についての最少有効濃度を測定したところ以下のような結果となった。
新規化学物質1をメチル化すると活性が1/108に減少した。このことから活性には実施例4に示したようにトリメチルシリルジアゾメタン等のメチル化剤でメチル化される官能基が重要であると考えられる。
[実施例7]アナアオサ、ボウアオノリの培養実験
静岡県清水市三保で採集したアナアオサ(Ulva pertusa)、ボウアオノリ(Enteromorpha intestinalis)から得られた遊走細胞を抗生物質混液添加ASP7培地で走光性を利用して洗浄後、滅菌したカバーガラスを敷き詰めた角形シャーレに添加して5日間の無菌化処理を行った。カバーガラスに遊走細胞が着底し発生が始まったところで各カバーガラスを6−MTPの各孔に入れ、抗生物質の入っていないASP7培地10mlを添加した。試験区には新規化学物質1を1ng/mlとなるように添加し、対象区には何も添加せずに実施例1と同じ条件で7日間培養した。10日後、試験区、対象区のカバーガラスを更に同じ条件の培地が添加してある培養試験管に植え継いで更に7日間培養した。アナアオサでの実験結果を図15に、ボウアオノリの実験結果を図16に示す。試験区、対象区を比較すると明らかなように、対象区の場合は仮根だけが異常に発達し、正常な葉状体の形成が見られないが、新規化学物質1を添加した場合は、着底後の正常な発生と葉状体の形成が見られた。
また、抗生物質混液添加ASP7培地は、ASP7培地に以下の組成を持つ抗生物質混液を2%添加したものである。
[実施例8]大型緑藻に対する形態形成誘導の比活性
実施例5と同様にして、YM−1−69株及びYM−2−23株、並びに図17に示した類似菌株についての最少有効濃度を測定したところ図18に示す結果が得られた。ここで、横軸は類似菌株の培養上清1μlで活性化されるマキヒトエ培養液のml数を表す。例えば、図18においてYM−2−23株は培養上清液1μlでマキヒトエ培養液約8000ml活性化させることが可能である。
[実施例9]新規化学物質1及びその誘導体の部分構造の決定
新規化学物質1の各種NMRスペクトル及びマススペクトルから図19に示した部分構造が導かれた。これらの部分構造を、HMBCスペクトルを解析することにより図20に示したdrimanタイプのテルペノイド構造と4置換ベンゼン環につなげることができた。図21に示したように、新規化学物質1のトリメチル化体Me1のNMRスペクトルからは更に4置換ベンゼン環の一置換基の部分構造とNOESYスペクトルを解析することにより相対立体配置を決定した。また、図22に示したようにHMBCスペクトルからこれまでの推定構造を確認した。図23及び図24に示したようにMe1H3においては、driman部分とベンゼン環の間でNOESY及びHMBCスペクトルの相関ピークが観察され、これら二つの構造を炭素番号11−16、及び8−0−21でつなぎ、部分構造を推定した。新規化学物質1の還元体Me1H1においては24位のメチレン基とベンゼン環上の21位の間に相関ピークが観測され、図25及び図26に示したように4置換ベンゼン環の最後の置換基が決定した。Me1H1のメチル化体Me1H1Meの各種NMRスペクトルから図27及び図28に示したようにベンゼン環、N−メチル基、24位のメチレン基の相関が観測され、これまでの推定部分構造を確認した。
実施例4に示したように、Me1H1Meは新規化学物質1をメチル化、還元反応、再メチル化した化合物であるので、新規化学物質1は式1:
に示したような構造となる。また、実施例3に示したように、新規化学物質1は新規化学物質2のアルカリ処理による誘導体であるため、新規化学物質2は、前記式1の化合物のケトン体である式2、式3あるいは式4のいずれかで示される化合物、あるいはこれらの混合物である。
式2:
式3:
式4:
更に、Me1の構造を式5に、実施例4に示したMe1の重メトキシ置換基体Me1Bの構造を式6に、Me1の部分還元体Me1H3の構造を式7に、Me1の還元体Me1H1の構造を式8に、Me1H1の再メチル化体Me1H1Meの構造を式9に示した。
式5:
式6:
式7:
式8:
式9:
本明細書中で引用した全ての刊行物、特許及び特許出願をそのまま参考として本明細書中にとり入れるものとする。
Claims (10)
- 下記の理化学的性質:
(i)物質の色:無色
(ii)分子量:457
(iii)質量分析:FABMS:m/z 456[M−H]−(図1)
(iv)核磁気共鳴シグナル:
1)1H−NMR(D2O−20mM Na2HPO4(pH9)、750MHz):(図2)
δppm0.818(3H,s),0.837(3H,s),0.882(3H,s),0.960(1H,m),1.058(1H,m),1.167(1H,m),1.326(3H,s),1.37(1H,m),1.38(1H,m),1.40(1H,m),1.58(1H,m),1.61(2H,m),1.52(1H,br d,J=13Hz),1.76(1H,br d,J=14Hz),2.024(1H,m),2.181(1H,dd,J=4,14Hz),2.291(1H,dd,J=14,16.5Hz),7.698(1H,d,J=7.5Hz),7.845(1H,d,J=7.5Hz)
2)13C−NMR(D2O−20mM Na2HPO4(pH9)、125MHz):(図3)
δppm15.236(q),19.037(t),20.287(t),20.955(q),21.835(q),25.987(t),33.381(s),33.636(q),37.308(s),39.590(t),41.199(t),42.346(t),52.769(d),56.381(d),79.096(s),114.965(s),124.399(d),139.004(s),141.232(d),150.282(s),152.656(s),172.081(s),173.538(s),174.661(s)
を有する新規化学物質1。 - 下記の理化学的性質:
(i)物質の色:無色
(ii)核磁気共鳴シグナル:
1H−NMR(D2O−20mM Na2HPO4(pH9)、500MHz):(図4)
δppm0.815(3H,s),0.834(3H,s),0.877(3H,s),0.949(1H,m),1.048(1H,m),1.163(1H,m),1.297(3H,s),1.35−1.40(3H,m),1.52−1.63(4H,m),1.753(1H,br d,J=14Hz),2.012(1H,m),2.158(1H,m),2.299(1H,m),7.646(1H,d,J=8.0Hz),7.769(1H,d,J=8.0Hz)
を有する新規化学物質2であって、
YM−2−23株(FERM BP−8417)を培養する工程、
培養物を濾過又は遠心分離により培養濾液と菌体に分ける工程、
菌体を含水メタノール又は含水アセトニトリルで抽出し、次いで抽出液から有機溶媒を減圧除去する工程、
抽出液と培養濾液とをあわせる工程、
得られた混合物をポリスチレン系吸着剤に吸着させる工程、
吸着した活性物質を水洗して脱塩する工程、
含水メタノール又は含水アセトニトリルにより活性物質を溶出する工程、
溶出液を減圧濃縮する工程、並びに
濃縮物を、スチレンジビニルベンゼン系ポリマー、陰イオン交換樹脂によるイオン交換クロマトグラフィー、ゲル濾過クロマトグラフィー、又は高速液体クロマトグラフィーを用い、移動相として17%アセトニトリル−5g(NH 4 ) 2 CO 3 +5ml NH 3 /l水溶液を用いたクロマトグラフィーにより精製する工程、を含む方法によりYM−2−23株(FERM BP−8417)から単離精製されたものである新規化学物質2。 - 請求の範囲第1項記載の新規化学物質1を生産する能力を有する、ゾベリア属又はテナシバキュラム属に属する微生物を培地に培養し、培養物中に新規化学物質1を生成蓄積させ、該生成蓄積した新規化学物質1を採取することを特徴とする新規化学物質1の製造法。
- 請求の範囲第2項記載の新規化学物質2を生産する能力を有する、ゾベリア属又はテナシバキュラム属に属する微生物を培地に培養し、培養物中に新規化学物質2を生成蓄積させ、該生成蓄積した新規化学物質2を採取することを特徴とする新規化学物質2の製造法。
- 微生物がYM−2−23株(FERM BP−8417)、テナシバキュラム・スピーシーズ(Tenacibaculum sp.)YM−1−69(FERM BP−8418)又はそれらの類似菌株である請求の範囲第3項記載の製造法。
- 微生物がYM−2−23株(FERM BP−8417)、テナシバキュラム・スピーシーズ(Tenacibaculum sp.)YM−1−69(FERM BP−8418)又はそれらの類似菌株である請求の範囲第4項記載の製造法。
- 請求の範囲第1項記載の新規化学物質1を有効成分として含有する藻類培養用培地。
- 請求の範囲第2項記載の新規化学物質2を有効成分として含有する藻類培養用培地。
- 請求の範囲第1項記載の新規化学物質1をトリメチルシリルジアゾメタンで処理することにより得られる該新規化学物質1のモノメチル化体、ジメチル化体又はトリメチル化体。
- 請求の範囲第9項記載のトリメチル化体を水素化ホウ素ナトリウムで処理することにより得られる化合物又はその誘導体。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002203608 | 2002-07-12 | ||
| JP2002203608 | 2002-07-12 | ||
| PCT/JP2003/008840 WO2004007510A1 (ja) | 2002-07-12 | 2003-07-11 | 形態形成及び成長促進活性を有する新規化学物質 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2004007510A1 JPWO2004007510A1 (ja) | 2005-11-10 |
| JP3916632B2 true JP3916632B2 (ja) | 2007-05-16 |
Family
ID=30112680
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004521191A Expired - Lifetime JP3916632B2 (ja) | 2002-07-12 | 2003-07-11 | 形態形成及び成長促進活性を有する新規化学物質 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US7279314B2 (ja) |
| JP (1) | JP3916632B2 (ja) |
| KR (1) | KR20050028018A (ja) |
| CN (2) | CN101580523A (ja) |
| AU (1) | AU2003280974A1 (ja) |
| WO (1) | WO2004007510A1 (ja) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101580523A (zh) | 2002-07-12 | 2009-11-18 | 三得利控股株式会社 | 具有形态形成活性和促进生长活性的新化学物质 |
| AU2003259781A1 (en) * | 2002-08-13 | 2004-02-25 | Vanu, Inc. | Convolutional decoding |
| US20040209580A1 (en) * | 2002-11-15 | 2004-10-21 | Vanu Bose | Communications system |
| EP1730649A2 (en) * | 2004-03-05 | 2006-12-13 | Vanu, Inc. | Controlling jitter effects |
| EP1757033A4 (en) * | 2004-06-09 | 2009-04-22 | Vanu Inc | Reducing backhaul bandwidth |
| WO2007044501A2 (en) * | 2005-10-07 | 2007-04-19 | Vanu, Inc. | Decoding of walsh codes |
| US8940520B2 (en) | 2010-05-20 | 2015-01-27 | Pond Biofuels Inc. | Process for growing biomass by modulating inputs to reaction zone based on changes to exhaust supply |
| US8889400B2 (en) | 2010-05-20 | 2014-11-18 | Pond Biofuels Inc. | Diluting exhaust gas being supplied to bioreactor |
| US11512278B2 (en) | 2010-05-20 | 2022-11-29 | Pond Technologies Inc. | Biomass production |
| US20120156669A1 (en) | 2010-05-20 | 2012-06-21 | Pond Biofuels Inc. | Biomass Production |
| US8969067B2 (en) | 2010-05-20 | 2015-03-03 | Pond Biofuels Inc. | Process for growing biomass by modulating supply of gas to reaction zone |
| US20120276633A1 (en) | 2011-04-27 | 2012-11-01 | Pond Biofuels Inc. | Supplying treated exhaust gases for effecting growth of phototrophic biomass |
| US9534261B2 (en) | 2012-10-24 | 2017-01-03 | Pond Biofuels Inc. | Recovering off-gas from photobioreactor |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003189845A (ja) * | 2001-12-27 | 2003-07-08 | Marine Biotechnol Inst Co Ltd | 海洋性葉状緑藻の培養方法 |
| CN101580523A (zh) | 2002-07-12 | 2009-11-18 | 三得利控股株式会社 | 具有形态形成活性和促进生长活性的新化学物质 |
-
2003
- 2003-07-11 CN CNA2009101288903A patent/CN101580523A/zh active Pending
- 2003-07-11 WO PCT/JP2003/008840 patent/WO2004007510A1/ja not_active Ceased
- 2003-07-11 CN CNB038214989A patent/CN100519573C/zh not_active Expired - Fee Related
- 2003-07-11 AU AU2003280974A patent/AU2003280974A1/en not_active Abandoned
- 2003-07-11 JP JP2004521191A patent/JP3916632B2/ja not_active Expired - Lifetime
- 2003-07-11 KR KR1020057000575A patent/KR20050028018A/ko not_active Ceased
-
2004
- 2004-01-30 US US10/767,260 patent/US7279314B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2004007510A1 (ja) | 2005-11-10 |
| CN100519573C (zh) | 2009-07-29 |
| US7279314B2 (en) | 2007-10-09 |
| CN1681830A (zh) | 2005-10-12 |
| AU2003280974A1 (en) | 2004-02-02 |
| CN101580523A (zh) | 2009-11-18 |
| US20040228854A1 (en) | 2004-11-18 |
| WO2004007510A1 (ja) | 2004-01-22 |
| KR20050028018A (ko) | 2005-03-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP3916632B2 (ja) | 形態形成及び成長促進活性を有する新規化学物質 | |
| JP2018524000A (ja) | 抗菌剤製造のためのミクロバクテリウム株の使用 | |
| PETERSEN et al. | Production of cladospirone bisepoxide, a new fungal metabolite | |
| EP2211625A1 (en) | Fungal strains and a process for production of insecticide thereof | |
| IE44992B1 (en) | 3-hydroxyalkyl (or acetylalkyl)-6,6a,7,8,10,10a-hexahydro -9h-dibenzo(b,d)pyran derivatites | |
| CN104250621A (zh) | 一种海洋烬灰红链霉菌及其应用于制备橙酮化合物的方法 | |
| US5334613A (en) | Antibacterial substance BE-24566B | |
| EP1561820A1 (en) | Novel substance fki-1033 and process for producing the same | |
| JPH10245383A (ja) | アスペルパラリン、その製造方法及びそれを有効成分とする殺虫剤 | |
| CN102260271B (zh) | 细胞松弛素类化合物及其制备方法和用途 | |
| CA2004304A1 (en) | Angucyclinones from streptomycetes, a process for the preparation thereof and the use thereof | |
| NZ245333A (en) | Herbicide and streptomyces strain producing it | |
| KR950005548B1 (ko) | 항생물질 gtx-01 및 그 제조방법 | |
| KR100386197B1 (ko) | 올레아미드를 생산하는 스트렙토미세스 속 신균주 및 그균주로부터 올레아미드를 생산하는 방법 | |
| JP2663096B2 (ja) | 新規ホスホン酸およびその製造法ならびにその用途 | |
| Sujarit et al. | Actinomycete, Streptomyces palmae CMU-AB204T | |
| JP2005218320A (ja) | 新規抗真菌物質fa424a(n)、fa424a(o)、fa424b、及びfa424d | |
| JPS63154695A (ja) | 新規抗生物質sf2446物質及びその製造法 | |
| CN121294572A (zh) | 一种利用海洋真菌ghq-208制备啶喃平的方法 | |
| KR830001245B1 (ko) | 항생물질 마이코플라네신의 제조방법 | |
| JPS6371190A (ja) | フエノキサジノン化合物およびその製法 | |
| JPH0515385A (ja) | 新規な抗生物質アリサマイシンおよびその製法 | |
| JPH04120087A (ja) | 新規抗腫瘍性抗生物質sf2587c物質およびその製造法 | |
| JPH08109182A (ja) | 化合物rp−1551類 | |
| CN109575040A (zh) | 一种具有抗菌活性的化合物及其制备方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20060919 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20061120 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20070116 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20070206 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 3916632 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100216 Year of fee payment: 3 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100216 Year of fee payment: 3 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100216 Year of fee payment: 3 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100216 Year of fee payment: 3 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313115 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100216 Year of fee payment: 3 |
|
| R360 | Written notification for declining of transfer of rights |
Free format text: JAPANESE INTERMEDIATE CODE: R360 |
|
| R360 | Written notification for declining of transfer of rights |
Free format text: JAPANESE INTERMEDIATE CODE: R360 |
|
| R371 | Transfer withdrawn |
Free format text: JAPANESE INTERMEDIATE CODE: R371 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100216 Year of fee payment: 3 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313115 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100216 Year of fee payment: 3 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100216 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110216 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120216 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120216 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130216 Year of fee payment: 6 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140216 Year of fee payment: 7 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |