JP2023123712A - ポリアルキル汚染が少ないモノアルキルスズ化合物、それらの組成物及び方法 - Google Patents
ポリアルキル汚染が少ないモノアルキルスズ化合物、それらの組成物及び方法 Download PDFInfo
- Publication number
- JP2023123712A JP2023123712A JP2023105608A JP2023105608A JP2023123712A JP 2023123712 A JP2023123712 A JP 2023123712A JP 2023105608 A JP2023105608 A JP 2023105608A JP 2023105608 A JP2023105608 A JP 2023105608A JP 2023123712 A JP2023123712 A JP 2023123712A
- Authority
- JP
- Japan
- Prior art keywords
- group
- carbon atoms
- tin
- monoalkyltin
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000000034 method Methods 0.000 title claims abstract description 85
- 150000003606 tin compounds Chemical class 0.000 title claims abstract description 8
- 239000000203 mixture Substances 0.000 title claims description 103
- 238000011109 contamination Methods 0.000 title claims description 7
- 150000001875 compounds Chemical class 0.000 claims abstract description 60
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 claims abstract description 58
- -1 alkoxide compound Chemical class 0.000 claims abstract description 31
- 239000003960 organic solvent Substances 0.000 claims abstract description 28
- 150000001408 amides Chemical class 0.000 claims abstract description 10
- 239000003513 alkali Substances 0.000 claims abstract description 9
- 229910052783 alkali metal Inorganic materials 0.000 claims abstract description 4
- 150000001340 alkali metals Chemical group 0.000 claims abstract description 4
- 125000004432 carbon atom Chemical group C* 0.000 claims description 62
- 238000006243 chemical reaction Methods 0.000 claims description 52
- 239000000047 product Substances 0.000 claims description 49
- 239000000356 contaminant Substances 0.000 claims description 43
- 125000000217 alkyl group Chemical group 0.000 claims description 42
- 125000001183 hydrocarbyl group Chemical group 0.000 claims description 42
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 33
- 239000002168 alkylating agent Substances 0.000 claims description 27
- 229940100198 alkylating agent Drugs 0.000 claims description 27
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 24
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 23
- 239000003153 chemical reaction reagent Substances 0.000 claims description 21
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 20
- 230000008569 process Effects 0.000 claims description 20
- 239000003446 ligand Substances 0.000 claims description 18
- 239000002904 solvent Substances 0.000 claims description 18
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 17
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 14
- 239000000376 reactant Substances 0.000 claims description 13
- 150000004703 alkoxides Chemical class 0.000 claims description 12
- 239000000126 substance Substances 0.000 claims description 12
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 claims description 11
- 150000001335 aliphatic alkanes Chemical class 0.000 claims description 10
- 150000004945 aromatic hydrocarbons Chemical class 0.000 claims description 10
- 229910052739 hydrogen Inorganic materials 0.000 claims description 10
- MBYLVOKEDDQJDY-UHFFFAOYSA-N tris(2-aminoethyl)amine Chemical compound NCCN(CCN)CCN MBYLVOKEDDQJDY-UHFFFAOYSA-N 0.000 claims description 10
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 9
- 239000002585 base Substances 0.000 claims description 9
- 239000008139 complexing agent Substances 0.000 claims description 9
- 239000001257 hydrogen Substances 0.000 claims description 9
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 9
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 9
- 229910052799 carbon Inorganic materials 0.000 claims description 8
- UOCJDOLVGGIYIQ-PBFPGSCMSA-N cefatrizine Chemical group S([C@@H]1[C@@H](C(N1C=1C(O)=O)=O)NC(=O)[C@H](N)C=2C=CC(O)=CC=2)CC=1CSC=1C=NNN=1 UOCJDOLVGGIYIQ-PBFPGSCMSA-N 0.000 claims description 8
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 claims description 8
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 claims description 8
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 claims description 8
- 125000004429 atom Chemical group 0.000 claims description 7
- 229910052736 halogen Inorganic materials 0.000 claims description 6
- 125000005843 halogen group Chemical group 0.000 claims description 5
- 230000007935 neutral effect Effects 0.000 claims description 5
- 239000012265 solid product Substances 0.000 claims description 5
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 4
- 239000002738 chelating agent Substances 0.000 claims description 4
- 150000002170 ethers Chemical class 0.000 claims description 4
- 239000012298 atmosphere Substances 0.000 claims description 3
- 230000005855 radiation Effects 0.000 abstract description 5
- 229910020813 Sn-C Inorganic materials 0.000 abstract description 2
- 229910018732 Sn—C Inorganic materials 0.000 abstract description 2
- 125000006657 (C1-C10) hydrocarbyl group Chemical group 0.000 abstract 1
- 229910052718 tin Inorganic materials 0.000 description 53
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 34
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 30
- 238000005481 NMR spectroscopy Methods 0.000 description 26
- 239000000243 solution Substances 0.000 description 26
- 230000015572 biosynthetic process Effects 0.000 description 25
- 238000003786 synthesis reaction Methods 0.000 description 22
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 21
- 229910052786 argon Inorganic materials 0.000 description 17
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 15
- 238000000059 patterning Methods 0.000 description 15
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 15
- 238000001942 tin-119 nuclear magnetic resonance spectrum Methods 0.000 description 15
- 238000003756 stirring Methods 0.000 description 13
- 239000013078 crystal Substances 0.000 description 11
- 238000004821 distillation Methods 0.000 description 11
- 239000002243 precursor Substances 0.000 description 11
- 238000010966 qNMR Methods 0.000 description 11
- 239000006227 byproduct Substances 0.000 description 10
- 125000000753 cycloalkyl group Chemical group 0.000 description 10
- 150000004795 grignard reagents Chemical class 0.000 description 10
- 238000000746 purification Methods 0.000 description 10
- 239000000523 sample Substances 0.000 description 10
- 238000005292 vacuum distillation Methods 0.000 description 10
- 239000007818 Grignard reagent Substances 0.000 description 9
- 238000004508 fractional distillation Methods 0.000 description 9
- 238000010926 purge Methods 0.000 description 9
- 238000001228 spectrum Methods 0.000 description 9
- 239000011701 zinc Substances 0.000 description 9
- LKUDPHPHKOZXCD-UHFFFAOYSA-N 1,3,5-trimethoxybenzene Chemical compound COC1=CC(OC)=CC(OC)=C1 LKUDPHPHKOZXCD-UHFFFAOYSA-N 0.000 description 8
- CBUZTNDEGHJMSI-UHFFFAOYSA-K N-[bis[acetyl(methyl)amino]-tert-butylstannyl]-N-methylacetamide Chemical compound C(C)(C)(C)[Sn](N(C(C)=O)C)(N(C(C)=O)C)N(C(C)=O)C CBUZTNDEGHJMSI-UHFFFAOYSA-K 0.000 description 8
- UHOVQNZJYSORNB-MZWXYZOWSA-N benzene-d6 Chemical compound [2H]C1=C([2H])C([2H])=C([2H])C([2H])=C1[2H] UHOVQNZJYSORNB-MZWXYZOWSA-N 0.000 description 8
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 8
- MSXVEPNJUHWQHW-UHFFFAOYSA-N 2-methylbutan-2-ol Chemical compound CCC(C)(C)O MSXVEPNJUHWQHW-UHFFFAOYSA-N 0.000 description 7
- 239000004698 Polyethylene Substances 0.000 description 7
- 239000000463 material Substances 0.000 description 7
- 229910052757 nitrogen Inorganic materials 0.000 description 7
- 239000003921 oil Substances 0.000 description 7
- 235000019198 oils Nutrition 0.000 description 7
- 229920000573 polyethylene Polymers 0.000 description 7
- 239000012230 colorless oil Substances 0.000 description 6
- 125000005842 heteroatom Chemical group 0.000 description 6
- 238000006460 hydrolysis reaction Methods 0.000 description 6
- 239000004615 ingredient Substances 0.000 description 6
- 239000007787 solid Substances 0.000 description 6
- OHLUUHNLEMFGTQ-UHFFFAOYSA-N N-methylacetamide Chemical compound CNC(C)=O OHLUUHNLEMFGTQ-UHFFFAOYSA-N 0.000 description 5
- 238000005194 fractionation Methods 0.000 description 5
- 125000000524 functional group Chemical group 0.000 description 5
- 230000007062 hydrolysis Effects 0.000 description 5
- 239000012535 impurity Substances 0.000 description 5
- CQRPUKWAZPZXTO-UHFFFAOYSA-M magnesium;2-methylpropane;chloride Chemical compound [Mg+2].[Cl-].C[C-](C)C CQRPUKWAZPZXTO-UHFFFAOYSA-M 0.000 description 5
- 229910052760 oxygen Inorganic materials 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 238000012545 processing Methods 0.000 description 5
- 238000000926 separation method Methods 0.000 description 5
- 238000000902 119Sn nuclear magnetic resonance spectroscopy Methods 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- 239000012043 crude product Substances 0.000 description 4
- 239000011521 glass Substances 0.000 description 4
- 229910052744 lithium Inorganic materials 0.000 description 4
- 229910052751 metal Inorganic materials 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- YNPFMWCWRVTGKJ-UHFFFAOYSA-N mianserin hydrochloride Chemical compound [H+].[Cl-].C1C2=CC=CC=C2N2CCN(C)CC2C2=CC=CC=C21 YNPFMWCWRVTGKJ-UHFFFAOYSA-N 0.000 description 4
- 210000003739 neck Anatomy 0.000 description 4
- 229920002120 photoresistant polymer Polymers 0.000 description 4
- 229910052710 silicon Inorganic materials 0.000 description 4
- 238000005160 1H NMR spectroscopy Methods 0.000 description 3
- OISVCGZHLKNMSJ-UHFFFAOYSA-N 2,6-dimethylpyridine Chemical compound CC1=CC=CC(C)=N1 OISVCGZHLKNMSJ-UHFFFAOYSA-N 0.000 description 3
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical group NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 3
- 238000012565 NMR experiment Methods 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 3
- 125000003368 amide group Chemical group 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- 239000007795 chemical reaction product Substances 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 3
- 239000000706 filtrate Substances 0.000 description 3
- 239000011888 foil Substances 0.000 description 3
- 150000004820 halides Chemical class 0.000 description 3
- 150000002367 halogens Chemical class 0.000 description 3
- 238000010438 heat treatment Methods 0.000 description 3
- 238000011065 in-situ storage Methods 0.000 description 3
- 239000011261 inert gas Substances 0.000 description 3
- 125000002524 organometallic group Chemical group 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 238000011084 recovery Methods 0.000 description 3
- 239000002002 slurry Substances 0.000 description 3
- 230000003595 spectral effect Effects 0.000 description 3
- 238000010189 synthetic method Methods 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- VILCJCGEZXAXTO-UHFFFAOYSA-N 2,2,2-tetramine Chemical compound NCCNCCNCCN VILCJCGEZXAXTO-UHFFFAOYSA-N 0.000 description 2
- JYYNAJVZFGKDEQ-UHFFFAOYSA-N 2,4-Dimethylpyridine Chemical compound CC1=CC=NC(C)=C1 JYYNAJVZFGKDEQ-UHFFFAOYSA-N 0.000 description 2
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 2
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 238000002441 X-ray diffraction Methods 0.000 description 2
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical group [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- 125000000304 alkynyl group Chemical group 0.000 description 2
- 239000012300 argon atmosphere Substances 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- 238000009833 condensation Methods 0.000 description 2
- 230000005494 condensation Effects 0.000 description 2
- 239000000470 constituent Substances 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 230000020169 heat generation Effects 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 238000011002 quantification Methods 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 239000004065 semiconductor Substances 0.000 description 2
- 238000000526 short-path distillation Methods 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 229960001124 trientine Drugs 0.000 description 2
- YWWDBCBWQNCYNR-UHFFFAOYSA-N trimethylphosphine Chemical compound CP(C)C YWWDBCBWQNCYNR-UHFFFAOYSA-N 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- 239000003039 volatile agent Substances 0.000 description 2
- 229910052725 zinc Inorganic materials 0.000 description 2
- WLNBMPZUVDTASE-HXIISURNSA-N (2r,3r,4s,5r)-2-amino-3,4,5,6-tetrahydroxyhexanal;sulfuric acid Chemical compound [O-]S([O-])(=O)=O.O=C[C@H]([NH3+])[C@@H](O)[C@H](O)[C@H](O)CO.O=C[C@H]([NH3+])[C@@H](O)[C@H](O)[C@H](O)CO WLNBMPZUVDTASE-HXIISURNSA-N 0.000 description 1
- VDFVNEFVBPFDSB-UHFFFAOYSA-N 1,3-dioxane Chemical compound C1COCOC1 VDFVNEFVBPFDSB-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- XWKFPIODWVPXLX-UHFFFAOYSA-N 2-methyl-5-methylpyridine Natural products CC1=CC=C(C)N=C1 XWKFPIODWVPXLX-UHFFFAOYSA-N 0.000 description 1
- MEFMCVBJTJFJIH-UHFFFAOYSA-N C1(CCCCCC1)[Zn]C1CCCCCC1 Chemical compound C1(CCCCCC1)[Zn]C1CCCCCC1 MEFMCVBJTJFJIH-UHFFFAOYSA-N 0.000 description 1
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 1
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 1
- 229930194542 Keto Chemical group 0.000 description 1
- 235000019502 Orange oil Nutrition 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 239000004809 Teflon Substances 0.000 description 1
- 229920006362 Teflon® Polymers 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 125000003670 adamantan-2-yl group Chemical group [H]C1([H])C(C2([H])[H])([H])C([H])([H])C3([H])C([*])([H])C1([H])C([H])([H])C2([H])C3([H])[H] 0.000 description 1
- ORILYTVJVMAKLC-UHFFFAOYSA-N adamantane Chemical group C1C(C2)CC3CC1CC2C3 ORILYTVJVMAKLC-UHFFFAOYSA-N 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000002152 alkylating effect Effects 0.000 description 1
- 150000001412 amines Chemical group 0.000 description 1
- 239000012491 analyte Substances 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 235000011089 carbon dioxide Nutrition 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 230000000536 complexating effect Effects 0.000 description 1
- 238000006482 condensation reaction Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 125000004093 cyano group Chemical group *C#N 0.000 description 1
- DIOQZVSQGTUSAI-NJFSPNSNSA-N decane Chemical compound CCCCCCCCC[14CH3] DIOQZVSQGTUSAI-NJFSPNSNSA-N 0.000 description 1
- 238000001212 derivatisation Methods 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000000609 electron-beam lithography Methods 0.000 description 1
- 150000002148 esters Chemical group 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000003517 fume Substances 0.000 description 1
- 239000005337 ground glass Substances 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- 239000000543 intermediate Substances 0.000 description 1
- 238000002075 inversion recovery Methods 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 125000000468 ketone group Chemical group 0.000 description 1
- 238000012417 linear regression Methods 0.000 description 1
- AFRJJFRNGGLMDW-UHFFFAOYSA-N lithium amide Chemical class [Li+].[NH2-] AFRJJFRNGGLMDW-UHFFFAOYSA-N 0.000 description 1
- 238000001459 lithography Methods 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- PSHKMPUSSFXUIA-UHFFFAOYSA-N n,n-dimethylpyridin-2-amine Chemical compound CN(C)C1=CC=CC=N1 PSHKMPUSSFXUIA-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- DIOQZVSQGTUSAI-UHFFFAOYSA-N n-butylhexane Natural products CCCCCCCCCC DIOQZVSQGTUSAI-UHFFFAOYSA-N 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 238000010943 off-gassing Methods 0.000 description 1
- 239000010502 orange oil Substances 0.000 description 1
- 150000002902 organometallic compounds Chemical class 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 238000012856 packing Methods 0.000 description 1
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 238000004064 recycling Methods 0.000 description 1
- 239000012925 reference material Substances 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 229920002545 silicone oil Polymers 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- 238000000427 thin-film deposition Methods 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- TUQOTMZNTHZOKS-UHFFFAOYSA-N tributylphosphine Chemical compound CCCCP(CCCC)CCCC TUQOTMZNTHZOKS-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/22—Tin compounds
- C07F7/2284—Compounds with one or more Sn-N linkages
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0042—Photosensitive materials with inorganic or organometallic light-sensitive compounds not otherwise provided for, e.g. inorganic resists
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/22—Tin compounds
- C07F7/2224—Compounds having one or more tin-oxygen linkages
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/22—Tin compounds
- C07F7/2296—Purification, stabilisation, isolation
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/16—Coating processes; Apparatus therefor
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Paints Or Removers (AREA)
Abstract
【課題】リソグラフィで構造物をパターニングするために使用され得る放射線感受性Sn-C結合を有する化合物を高純度で調製する方法を提供する。【解決手段】RSn(NR’2)3によって表されるモノアルキルスズトリアミド化合物をアミド(R’’CONHR’’’)と有機溶媒中で反応させ、RSn-(NR’COR’’)3によって表されるモノアルキルトリアミドスズ化合物を合成し、結晶性生成物を集めた後、これをQOR’のアルカリアルコキシド化合物と有機溶媒中で反応させてRSn(OR’)3によって表されるモノアルキルスズトリアルコキシド化合物を調製する。(Rは、C1~C31ヒドロカルビル基;R’及びR’’が独立に、C1~C10のヒドロカルビル基;Qがアルカリ金属)【選択図】なし
Description
関連出願の相互参照
本出願は、Edson et al.,“Monoalkyl Tin Compounds With Low Polyalkyl Contamination,Their Compositions and Methods”に対する2018年4月11日に出願された係属中の米国特許出願第15/950,292号の一部継続出願及びEdson et al.,“Monoalkyl Tin Compounds With Low Polyalkyl Contamination,Their Compositions and Methods”に対する2018年4月11日に出願された係属中の米国特許出願第15/950,286号の一部継続出願(両方とも、参照によって本願に組み入れられる)である。
本出願は、Edson et al.,“Monoalkyl Tin Compounds With Low Polyalkyl Contamination,Their Compositions and Methods”に対する2018年4月11日に出願された係属中の米国特許出願第15/950,292号の一部継続出願及びEdson et al.,“Monoalkyl Tin Compounds With Low Polyalkyl Contamination,Their Compositions and Methods”に対する2018年4月11日に出願された係属中の米国特許出願第15/950,286号の一部継続出願(両方とも、参照によって本願に組み入れられる)である。
本発明は、モノアルキルスズトリアミド、モノアルキルスズトリアルコキシド、又はモノアルキルトリアミドスズの高純度組成物及びそれらを製造する方法に関する。
有機金属化合物は、溶液加工可能な形態で金属イオンを提供するために関心を集めている。アルキルスズ化合物は、リソグラフィで構造物をパターニングするために使用され得る放射線感受性Sn-C結合を提供する。絶えず小さくなっている寸法を有する半導体材料の加工は、所望のパターニング分解能を達成するためのいっそう用途が広い材料の需要をもたらし、アルキルスズ化合物は、パターニングの利点を提供する有望な先端材料である。
第1の態様において、本発明は、化学式RSn(OR’)3によって表されるモノアルキルスズトリアルコキシド化合物又は化学式RSn(NR’2)3によって表されるモノアルキルスズトリアミド化合物と、全スズ量に対して4モル%以下のジアルキルスズ化合物とを含む組成物に関し、式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、及びR’が、1~10個の炭素原子を有するヒドロカルビル基である。モノアルキルスズトリアミドを式HOR’’によって表されるアルコールと有機溶媒中で反応させてRSnOR’’3(式中、R’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である)を形成して、スズの全量に対して4モル%以下のジアルキルスズ化合物を有する生成物組成物を形成することができる。
更なる態様において、本発明は、化学式RSn-(NR’COR’’)3(式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’及びR’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である)によって表されるモノアルキルトリアミドスズ化合物を含む組成物に関する。
別の態様において、本発明は、モノアルキルスズトリアミド化合物を形成するための方法に関し、方法は、RMgX、R2Zn、RZnNR’2、又はそれらの組合せからなる群から選択されるアルキル化剤を有機溶媒を含む溶液中でSn(NR’2)4と反応させる工程を含み、式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、Xがハロゲンであり、及びR’が、1~10個の炭素原子を有するヒドロカルビル基である。
他の態様において、本発明は、RSn(NR’2)3を式HOR’’によって表されるアルコールと有機溶媒中で反応させてRSnOR’’3を形成する工程であって、RSn(NR’2)3反応体が約4モル%以下のジアルキルスズ汚染物質を有し、請求項17に記載の方法の生成物であり、式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’及びR’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である、工程を含む、ジアルキルスズの汚染が少ないモノアルキルスズトリアルコキシド化合物を選択的に形成するための方法に関する。
さらに別の態様において、本発明は、モノアルキルトリアミドスズを形成するための方法に関し、方法は、化学式RSn(NR’2)3によって表されるモノアルキルスズトリアミド化合物をアミド(R’’CONHR’’’)と有機溶媒中で反応させる工程であって、式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’、R’’及びR’’’が独立に、1~8個の炭素原子を有するヒドロカルビルである工程と、式RSn(NR’’’COR’’)3によって表される固体生成物を集める工程とを含む。
さらに、本発明は、モノアルキルスズトリアルコキシドを形成するための方法に関し、方法は、モノアルキルトリアミドスズ化合物(RSn(NR’’’COR’’)3)をアルカリアルコキシド化合物(QOR’、式中、Qがアルカリ金属原子である)と有機溶媒中で反応させて、化学式RSn(OR’)3によって表される生成物化合物を形成する工程であって、式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’、R’’及びR’’’が独立に、1~10個の炭素を有するヒドロカルビル基である工程を含む。
さらに、本発明は、モノアルキルスズトリアルコキシド(monoalkyl tine trialkoxide)と四座非平面錯生成剤とのブレンドを蒸留する工程を含む、モノアルキルスズトリアルコキシドを精製するための方法に関する。
ポリアルキルスズ副生成物が少ない、モノアルキルスズ組成物、特にモノアルキルスズトリアミド、モノアルキルスズトリアルコキシド、及びモノアルキルトリミドスズを得る方法が見出されている。特に、合成されただけで使用されるか又はさらに精製され得るポリアルキルスズ副生成物が比較的少ないモノアルキルスズトリアミドの合成のための3つの方法が開発されている。その場合には、選択的に合成されたモノアルキルスズトリアミドを使用して、ポリアルキルスズ副生成物が相応して少ないモノアルキルスズトリアルコキシドを合成することができる。さらに、高純度であるか否かに関わらず、モノアルキルスズトリアミドを溶液中で反応させて、結晶中のポリアルキル副生成物を取り除く固体モノアルキルトリアミドスズを形成することができ、この方法は、ポリアルキル副生成物が少ないモノアルキルトリアミドスズを形成するために有効であることが見出された。合成されたモノアルキルスズアミド及びモノアルキルスズアルコキシドを分留によってさらに精製して、ポリアルキル汚染物質を、直接合成からすでに比較的少ない場合があるレベルよりも有効に低減することができる。解析技法を使用して、汚染物質のレベルを求めることができる。いくつかの実施形態において、定量的NMR(qNMR)は、副生成物が1モルパーセント未満の濃度に低減され得ることを示す。生成物スズ組成物は、望ましいパターニング材料の合成のための前駆体として有用であり得る。パターニング材料の前駆体としての用途のために、ポリアルキルスズ副生成物の低減は、EUV及びUVフォトレジスト又は電子ビームパターニングレジストとして使用するためにモノアルキルスズ生成物組成物の性質に対して有用であり得る。
モノアルキルスズトリアミドは、有機スズフォトレジストの調製において有用な中間生成物であり得る。モノアルキルスズトリアミドの調製方法は、スズテトラアミドを所望のトリアミドに変換するためにリチウム試薬をかねてより使用している。例えば、t-ブチルトリス(ジエチルアミド)スズ、(t-BuSn(NEt2)3)は、Haenssgen,D.;Puff,H.;Beckerman,N.J.Organomet.Chem.1985,293,191(参照によって本願明細書に組み込まれる)の方法に従ってリチウム試薬を使用して合成され得る。しかしながら、リチウム試薬を使用するこれらの方法は、モノアルキルとジアルキルスズ生成物との混合物を製造することができる。また、リチウム汚染物質は、半導体用途のために望ましくないことがあり得る。第二級アルキル基を含有するモノアルキルスズトリアミドを調製するための報告された方法は、モノ-、ジ-、及びトリアキル(triakyl)スズ生成物が豊富な混合物を製造する。以下に説明するように、一切のポリアルキル副生成物、例えば、ジアルキルスズ汚染物質を低減するのが望ましい場合がある。モノアルキル種及びジアルキル種がいくつかの化合物について互いに分離され得るが、この分離又は精製プロセスは一般的に、製造コストを増し、伴出したジアルキル不純物は、下流のフォトレジスト生成物の性能を損なう場合がある。このように、より高い純度を有するモノアルキルスズ化合物を合成することが望ましいことがあり得、必要ならば、例えば分留などを使用して、任意の後続の精製により、ジアルキル又はポリアルキル汚染がさらに低くなるようにする。合成されたままの組成物が十分に高純度である場合、分留による更なる精製を避けることができる。
ポリマー安定剤として高純度モノアルキルスズ化合物、特にメルカプト化合物の使用は、“High Purity Monoalkyltin Compounds and Uses Thereof”と題されたDeelmanらに対する米国特許第8,198,352号明細書及び“Stabilizers Containing High Purity Mono-Alkyltin Compounds”と題されたFrenkelらに対する米国特許第9,745,450号明細書(両方とも、参照によって本願に組み入れられる)に記載されている。これらの特許は、安定剤化合物の合成のための前駆体として高純度モノアルキルハロゲン化物の形成を記載している。ここで記載されるプロセスは、精製のための分留と共に使用され得る、異なった且つ有効な合成方法を使用する高純度モノアルキルスズトリアミド、モノアルキルスズトリアルコキシド、又はモノアルキルトリアミドスズ化合物の合成に焦点を合わせている。
高性能の放射線ベースのパターニング組成物におけるアルキル金属配位化合物の使用は、例えば、参照によって本願明細書に組み込まれる“Organometallic Solution Based High Resolution Patterning Compositions”と題されたMeyersらに対する米国特許第9,310,684号明細書に記載されている。パターニングのためのこれらの有機金属組成物の改良は、“Organometallic Solution Based High Resolution Patterning Compositions and Corresponding Methods”と題されたMeyersらに対する米国特許出願公開第2016/0116839A1号明細書及び“Organotin Oxide Hydroxide Patterning Compositions,Precursors,and Patterning”と題されたMeyersらに対する米国特許出願公開第2017/0102612A1号明細書(以下に出願公開第’612号)(両方とも、参照によって本願に組み入れられる)に記載されている。
アルキルスズ組成物を使用して行われる放射線パターニングは一般的に、アルキルスズオキソ-ヒドロキソ部分を使用して行われる。ここで合成される組成物は、高分解能パターニングのために有効であるアルキルスズオキソ-ヒドロキソ組成物を形成するための有効な前駆体であり得る。アルキルスズ前駆体組成物は、適切な条件下で水又は他の適した試薬で加水分解されて式RSnO(1.5-(x/2))(OH)x(式中、0<x≦3)によって表され得るアルキルスズオキソ-ヒドロキソパターニング組成物を形成することができる基を含む。加水分解基(X)で組成物を変化させることができる加水分解及び縮合反応は、以下の反応において示される:
RSnX3+3H2O→RSn(OH)3+3HX、
RSn(OH)3→RSnO(1.5-(x/2))OHx+(x/2)H2O。
RSnX3+3H2O→RSn(OH)3+3HX、
RSn(OH)3→RSnO(1.5-(x/2))OHx+(x/2)H2O。
加水分解生成物HXが十分に揮発性である場合、in situ加水分解は、支持体コーティングプロセスの間に水蒸気を使用して行われ得るが、加水分解反応はまた、溶液中で行われてアルキルスズオキソ-ヒドロキソ組成物を形成することができる。これらの加工オプションは、出願公開第’612号にさらに記載されている。
ポリアルキルスズ不純物組成物は縮合に影響を与え得、リソグラフィ加工の間にフォトレジストのガス放出をもたらし、それは、薄膜堆積及びパターニングのために使用される装置のスズ汚染の可能性を増加させる。これらの問題に基づいて、ジアルキル又は他のポリアルキル成分を低減するか又は除くことが非常に望まれている。最終レジスト組成物中のポリアルキルスズ汚染物質を低減するために3種類の組成物、具体的には、モノアルキルスズトリアミド、モノアルキルスズトリアルコキシド、及びモノアルキルトリアミドスズが本明細書に記載される加工のために適切である。以下にさらに説明されるように、モノアルキルスズトリアミド組成物はまた、モノアルキルスズトリアルコキシド及びモノアルキルトリアミドスズ組成物のための前駆体として役立ち得る。モノアルキルトリアミドスズ組成物はまた、モノアルキルスズトリアルコキシド組成物を形成するための便利な前駆体であり得る。モノアルキルスズトリアルコキシド組成物は、in situ加水分解及び縮合を受けやすく、in situ加水分解に見合った除去のために一般的に適切に揮発性であるアルコール副生成物と共にモノアルキルスズオキソ-ヒドロキソ組成物を形成するので、前駆体パターニング組成物溶液中の望ましい構成成分であり得る。
本明細書に記載される3つの方法のいずれか1つを使用してポリアルキル汚染物質が比較的少ないモノアルキルスズトリアミド組成物を直接に合成することができる。Zn試薬を使用する方法は、第二級アルキル基を含有する高純度モノアルキルスズトリアミドの合成のために特に開発された。さらに、モノアルキルスズトリアミド組成物の少なくともいくつかは、分留を使用してさらに精製され得る。モノアルキルスズトリアミド組成物からのモノアルキルトリアミドスズ組成物の合成は、ポリアルキル汚染物質を低減する更なる方法を提供する。これらの方法を組み合わせて、ポリアルキル汚染物質の更なる低減をもたらすことができる。
モノアルキルスズトリアミド組成物は一般的に、式RSn(NR’)3によって表され得、式中、R及びR’は独立に、1~31個の炭素原子を有するアルキル又はシクロアルキルであり、一個以上の炭素原子がO、N、Si、及び/又はハロゲン原子を含有する複数のヘテロ原子官能基のうちの1つで任意選択により置換されているか又はアルキル若しくはシクロアルキルがフェニル若しくはシアノ基でさらに官能化されている。いくつかの実施形態において、R’は≦10個の炭素原子を含むことができ、例えば、メチル、エチル、プロピル、イソプロピル、ブチル、t-ブチル、イソブチル、又はt-アミルであり得る。R基は直鎖、分岐、(すなわち、金属に結合した炭素原子で第二級又は第三級)、又は環状ヒドロカルビル基であり得る。各々のR基は、個々に及び一般的に1~31個の炭素原子を有し、二級の結合炭素原子を有する基については3~31個の炭素原子及び三級の結合炭素原子を有する基については4~31個の炭素原子を有する。特に、分岐アルキル配位子は、いくつかのパターニング組成物のために望ましいことがあり得、そこで化合物は、R1R2R3CSn(NR’)3(式中、R1及びR2が独立に1~10個の炭素原子を有するアルキル基であり、R3が水素又は1~10個の炭素原子を有するアルキル基である)として表され得る。下記の通り、アルキル配位子Rのこの表現は、R1R2R3CSn(X)3(Xがトリアルコキシド又はトリアミド部分に相当する)を一般的に有する他の実施形態に同様に適用可能である。いくつかの実施形態においてR1及びR2は、環状アルキル部分を形成することができ、R3はまた、環状部分の他の基に接合し得る。適した分岐アルキル配位子は、例えば、イソプロピル(R1及びR2はメチルであり、R3は水素である)、tert-ブチル(R1、R2及びR3はメチルである)、t-アミル(R1及びR2はメチルであり、R3は、-CH2CH3である)、sec-ブチル(R1はメチルであり、R2は-CH2CH3であり、R3は水素である)、ネオペンチル(R1及びR2は水素であり、R3は-C(CH3)3である)、シクロヘキシル、シクロペンチル、シクロブチル、及びシクロプロピルであり得る。適した環状基の例には、例えば、1-アダマンチル(第三級炭素において金属に結合した-C(CH2)3(CH)3(CH2)3又はトリシクロ(3.3.1.13,7)デカン)及び2-アダマンチル(第二級炭素において金属に結合した-CH(CH)2(CH2)4(CH)2(CH2)又はトリシクロ(3.3.1.13,7)デカン)が含まれる。他の実施形態においてヒドロカルビル基には、アリール又はアルケニル基、例えば、ベンジル又はアリル、又はアルキニル基が含まれ得る。他の実施形態においてヒドロカルビル配位子Rには、C及びHだけからなり且つ1~31個の炭素原子を含有する任意の基が含まれ得る。例えば:直鎖又は分岐アルキル(i-Pr((CH3)2CH-)、t-Bu((CH3)3C-)、Me(CH3-)、n-Bu(CH3CH2CH2CH2-))、シクロ-アルキル(シクロ-プロピル、シクロ-ブチル、シクロ-ペンチル)、オレフィン(アルケニル、アリール、アリル)、若しくはアルキニル基、又はそれらの組合せ。更なる実施形態において適したR基には、シアノ、チオ、シリル、エーテル、ケト、エステル、若しくはハロゲン化基又はそれらの組合せなどのヘテロ原子官能基で置換されたヒドロカルビル基が含まれ得る。
アルキルスズトリアルコキシド組成物は式RSn(OR0)3によって表され得、アルキルトリアミドスズ組成物は式RSn(NR’’COR’’’)3によって表され得る。アルキルスズトリアルコキシド及びアルキルトリアミドスズ組成物の式中のR基は、アルキルスズトリアミド組成物の上に記載されたのと同じR基であり得、上記のこれらのR基の相当する考察をそのまま全部この段落に写し取るかのようにしている。アルキルアミド(-NR’’COR’’’)又はアルコキシド配位子-OR0については、R’’、R’’’及びR0基は独立に、1~10個の炭素原子を有する炭化水素基、例えばメチル基、エチル基等であり得る。また、R’’及びR’’’は独立に、水素であり得る。
いくつかの実施形態において、本明細書における組成物(モノアルキルスズトリアミド、モノアルキルスズトリアルコキシド又はモノアルキルトリアミドスズ)は、スズに対して約4モルパーセント以下の、更なる実施形態において約3モルパーセント以下の、いくつかの実施形態において約2モルパーセント以下の、さらに別の実施形態において約1モルパーセント以下のジアルキルスズ汚染物質、他の実施形態において約0.5モルパーセント以下のジアルキルスズ汚染物質、及び別の実施形態において約0.1モルパーセント以下の量のジアルキルスズ汚染物質を有し得る。上記の明示範囲内のジアルキルスズ汚染物質のさらに別の範囲が考えられ、本開示の範囲内であることを当業者は認識するであろう。ジアルキルスズ汚染物質のレベルは一般的に、任意の適正な解析技法を使用して求めることができる。いくつかの実施形態において、ジアルキルスズジアミド又はジアルキルスズジアルコキシドの量は、定量的NMRによって0.1モルパーセント付近又は未満であると示され得る。未同定汚染物質があり得る結果として、モノアルキルスズ組成物の定量化は数パーセント内で測定され得るが、以下の実施例に記載されるような定量的NMRを使用して、ジアルキルスズ汚染物質の比較的少量のエラーレベルが信頼性を提供する。
モノアルキルSn前駆体は1H及び119Sn NMR分光分析法によって誘導体化せずに解析された。内部標準に対してモノアルキルSn前駆体のNMRスペクトルピークからの積分値を使用して純度を定量した。値がモノアルキルSn前駆体の純度を正確に反映することを確実にするようにした。較正された90度パルスを使用して、1HNMR及び逆ゲート付き119Sn{1H}NMR実験のために試料を照射した。さらに、1H及び119Sn{1H}NMR実験の両方のために、反転回復実験を使用して標準及び分析物のT1リラクセーション値を測定した。測定されたT1値を用いて、試料の最も長いT1時間の5倍に等しいリサイクル遅延時間を設定したが、それは核(Z=1-e-(経過時間/T1))から平衡(Z=1-e-5=0.99326)へのほぼ完全なリラクセーションを可能にする。最後に、スペクトルウインドウの中心に位置していないスペクトルピークの減少した強度を119Sn{1H}NMR実験により説明するために、分析物と標準との間のスペクトルを中央に置くことによってNMR分光計のB1プロファイルを測定及び説明した。スペクトルの信号雑音比を高める逆ゲート付き119Sn{1H}NMR分光分析法のために設定されるパラメーターを用いて微量Sn不純物の検出及び定量化を実施した:スペクトルの中心及び掃引幅を較正値に設定し、30度パルスを用いて、リサイクル遅延時間が1秒にされた試料を照射した。線形回帰分析を用いて、定量値を検出された低レベルSn不純物に割り当てた。この方法は、モノアルキルスズ化合物に対してジアルキル、テトラキスアミド、及びテトラキスアルコキシドスズ不純物について0.1%の定量下限を提供する。定量的NMRは、Weber et al.,“Method development in quantitative NMR towards metrologically traceable organic certified reference materials used as 31P qNMR standards”,Anal.Bioanal.Chem.,407:3115-3123(2015);及びPauli et al.,“Importance of Purity Evaluation and the Potential of Quantitative 1H NMR as a Purity Assay”,J.Medicinal Chemistry,57,9220-9231(2014)(両方とも、参照によって本願に組み入れられる)にさらに説明されている。
一般的には、モノアルキルスズトリアミドを調製するための本明細書における改良されたプロセスは、アルキル化剤としても記載される、アルキル供与基を有する化合物をスズテトラアミドと反応させる工程を含む。望ましい結果が達成されており、そこでアルキル化剤はグリニャール試薬、ジオルガノ亜鉛試薬、又はモノオルガノ亜鉛アミドであり得る。これらの合成は、レジストを形成するために使用することができるか又はさらに精製して汚染物質レベルをさらにいっそう低減することができるポリアルキル汚染物質が少ないモノアルキルスズトリアミドを直接に製造することができる。合成方法において、アルキル化剤は、スズテトラアミドのアミド基をアルキル基で選択的に置換する。いくつかの実施形態において、反応は、ポリアルキルスズ汚染物質が少ない、特にジアルキルスズ汚染物質が少ないモノアルキルスズトリアミドを選択的に製造する。記載された合成方法は、ジアルキルスズ副生成物の形成を抑えることによってモノアルキルスズトリアミドの選択率及び収率を改良する。方法は、分岐アルキル系のために特に有用である。次に、ポリアルキル汚染物質が少ないモノアルキルスズトリアミドを使用して、ポリアルキル汚染物質が少ないモノアルキルスズトリアルコキシドを形成することができる。以下にさらに考察されるように、結晶性モノアルキルトリアミドスズ組成物の形成は、結晶からポリアルキル汚染物質を取り除くことによってそれらを避ける代替方法を提供する。
反応がモノアルキルスズトリアミド化合物を形成するために、スズテトラアミド化合物は、商業的に得られるか又は公知の技術を使用して合成され得る。例えば、テトラキス(ジメチルアミド)スズ、Sn(NMe2)4は、Sigma-Aldrichから入手可能である。モノアルキルスズ組成物の合成のために、溶液中のスズテトラアミド反応体は一般的に、約0.025M~約5Mの間、更なる実施形態において約0.05M~約4Mの間、又はさらに別の実施形態において約0.1M~2Mの間の濃度を有することができる。上記の明示範囲内の反応体濃度のさらに別の範囲が考えられ、本開示の範囲内であることを当業者は認識するであろう。一般的には、アルキル配位子をSnに導入する関連反応は、不活性ガスパージ下で且つ暗所の反応器内の溶液中のスズテトラアミドを使用して開始され得る。代替実施形態において、スズテトラアミド反応体の一部又は全てが段階的に添加され、その場合、段階的に添加される溶液中の濃度がより高めであるのが適切であり得、反応器内の濃度が一時的であり得るので、上記の濃度は直接関連していないことがあり得る。
アルキル化剤は一般的に、化学量論量に比較的近い量で添加される。言い換えれば、アルキル化剤を添加して、1個のスズ原子に対して1つのアルキル基のモル当量を提供する。アルキル化剤が、亜鉛原子1個当たり2つのアルキル基を供与することができるジオルガノ亜鉛化合物など、複数のアルキル基を提供することができる場合、アルキル化剤の化学量論量をそれに応じて調節して、各Snに対して約1つのアルキル基を提供する。そのため、Sn2モル当たりZn1モルのオーダーのジオルガノ亜鉛化合物が必要とされる。アルキル化剤の量は、試薬の化学量論量に対して約±25%、約±20%、若しくは約±15%であり得るか、又は言い換えれば試薬の化学量論量+又は-所望のプロセス性能を達成するための選択された量であり得る。上記の明示範囲内のアルキル化剤の相対量のさらに別の範囲が考えられ、本開示の範囲内であることを当業者は認識するであろう。
実施例2及び3はアルキル化剤のほぼ化学量論量を使用し、実施例1及び実施例4は約110%(すなわち100%+10%)のアルキル化剤を使用する。有機溶媒中に溶解されるアルキル化剤を、反応を制御するための適した速度で反応器に段階的に、例えば滴状に又は流して添加することができる。添加の速度を、例えば約1分~約2時間及び更なる実施形態において約10分~約90分間の時間にわたって調節して反応プロセスを制御することができる。添加溶液中のアルキル化剤の濃度は、添加の速度を考慮して適度な値内に調節され得る。基本的には、アルキル化試薬は、スズテトラアミドの段階的な添加によって反応器内で開始することができる。上記の明示範囲内のさらに別の範囲のアルキル化剤及び添加時間が考えられ、本開示の範囲内であることを当業者は認識するであろう。
アルキル配位子をスズ原子に導入するための反応は、低酸素、実質的に酸素を含有しない、又は無酸素環境において行われ得、アクティブな不活性ガスパージは、例えば無水窒素パージ又はアルゴンパージなどの適切な雰囲気を提供することができる。以下の添加剤が、スズへの第二アルキル基の付加を低減することが観察された:ピリジン、2,6-ルチジン、2,4-ルチジン、4-ジメチルアミノピリジン、2-ジメチルアミノピリジン、トリフェニルホスフィン、トリブチルホスフィン、トリメチルホスフィン、1,2-ジメトキシエタン、1,4-ジオキサン、及び1,3-ジオキサン。他の中性配位塩基が同様に機能し得る。反応は任意選択により、スズ1モル当たり約0.25~約4モルの中性配位塩基をさらに含むことができる。反応は、反応中に光から遮蔽され得る。反応は、有機溶媒、例えば、アルカン(例えばペンタン又はヘキサン)、芳香族炭化水素(例えばトルエン)、エーテル(例えばジエチルエーテル、C2H5OC2H5)、又はそれらの混合物中で行われ得る。溶媒は、水との反応を避けるために無水であり得る。反応は一般的に、約15分~約24時間、更なる実施形態において約30分~約18時間及びさらに別の実施形態において約45分~約15時間の間行われる。反応中の温度は、約-100℃~約100℃の間、更なる実施形態において約-75℃~約75℃の間、さらに別の実施形態において約-60℃~約60℃の間であり得る。冷却又は加熱を使用して反応温度を所望の範囲内に制御することができ、また、反応体の添加速度の制御を使用して、反応の過程で温度発展に影響を与えることができる。生成物モノアルキルスズトリアミドは一般的に、真空蒸留を使用して精製され得る油である。典型的な収率は、約50~85パーセントであると観察されている。上記の明示範囲内のさらに別の範囲の濃度及び作業条件が考えられ、本開示の範囲内であることを当業者は認識するであろう。
アルキル化剤は、グリニャール試薬、ジオルガノ亜鉛試薬、又はモノオルガノ亜鉛アミドであり得る。グリニャール試薬は有機マグネシウムハロゲン化物であり得る。具体的には、記載された反応中のグリニャール試薬は、RMgX(式中、Xがハロゲン化物、一般的にCl、Br、又はIである)であり得る。Rはアルキル又はシクロアルキルであり得、1~31個の炭素原子を有し得、一般的にRは、この考察のためにその全部が組み込まれるかのように、生成物組成物のR部分に対して上記のようにより完全に説明され得る。例えば、アルキル又はシクロアルキルは分岐であってもよく、芳香族基を含み得、及び/又はO、N、Si、及び/又はハロゲンなどの原子を含有する1つ以上のヘテロ原子官能基を有してもよい。グリニャール試薬は商業的に入手可能であるか又は公知の方法を使用して合成され得る。商用供給源には、American Elements Company、Sigma-Aldrich、及び多くの他の供給元が含まれる。
いくつかの実施形態において、アルキル化剤はジオルガノ亜鉛試薬である。ジオルガノ亜鉛試薬は2つのアルキル基をスズに供与することができ、そのためジオルガノ亜鉛試薬の量は、モル当量の違いについて調節される。具体的には、ジオルガノ亜鉛試薬はR2Znであってもよい。Rは、1~31個の炭素原子を有するアルキル又はシクロアルキルであってもよい。R基は、生成物組成物のR部分に対して上記のようにより完全に規定され得、生成物モノアルキルスズ化合物に関連するR基についての上記の考察は、ここで再現されるかのように本考察の一部であると考えられる。例えば、アルキル又はシクロアルキルは分岐であり得、O、N、Si、及び/又はハロゲンなどの原子を含有する1つ以上のヘテロ原子官能基を有し得る。ジシクロヘプチル亜鉛((C7H13)2Zn)反応体は以下に例示される。ジオルガノ亜鉛化合物は商業的に入手可能であるか又は公知の技術を使用して合成され得る。商用供給源には、例えば、Alfa Aesar、Sigma-Aldrich、Rieke Metals(Nebraska,USA)及びTriveni Chemicals(インド)が含まれる。実施例の反応体は合成された。
更なる実施形態においてアルキル化剤はモノオルガノ亜鉛アミド(RZnNR’2)である。Rは、1~30個の炭素原子を一般的に有するアルキル又はシクロアルキルであり得る。R基は、生成物組成物のR部分に対して上記のようにより完全に規定され得、生成物モノアルキルスズ化合物に関連するR基についての上記の考察は、ここで再現されるかのように本考察の一部であると考えられる。例えば、アルキル又はシクロアルキルは分岐であり得、O、N、Si、及び/又はハロゲンなどの原子を含有する1つ以上のヘテロ原子官能基で置換された1つ以上の炭素原子を有し得る。いくつかの実施形態において、R’は、アルキル又はシクロアルキル基であり、それはヘテロ原子で置換され得る。いくつかの実施形態において、R’は1~8個の炭素原子、いくつかの実施形態において1~5個の炭素原子、さらに別の実施形態において1~3個の炭素原子を有し得る。R’はメチル、エチル、プロピル、イソプロピル、ブチル、イソ-ブチル、t-ブチル、又はt-アミル基であってもよい。モノオルガノ亜鉛アミドは、例えば、アルキル亜鉛ハロゲン化物(RZnX、X=I、Br、Cl)及びリチウムアミド(LiNR’2)から合成され得、それらはSigma-Aldrichからの市販の試薬である。
上述の方法又は本明細書に明示されていない他の方法を使用して製造されるモノアルキルスズトリアミドは、分留を使用してさらに精製され得る。蒸留プロセスの温度を低減するために、圧力は、例えば、約0.01トールから約10トール、更なる実施形態において約0.05トールから約5トール、更なる実施形態において約0.1トールから約2トールの圧力に低減され得る。プロセスのために適した体積を有する、適した分留カラムを使用でき、これらは市販されている。精製される材料を保持する容器内で且つカラムに沿って温度を制御して、所望の分離を達成することができる。一実施形態のための熱的条件は、以下の実施例8に示され、これらの条件は、本明細書における教示に基づいて他の組成物のために容易に一般化され得る。ジアルキルスズトリアミド汚染物質は、モノアルキルスズトリアミドよりも高い沸点を有する場合、モノアルキルスズトリアミドは、蒸留プロセスの間に分離除去され得る。分留の諸段階の間に除去される大量の液体と共に画分を取ることができるが、実施例8は、検出可能な汚染物質を含有しない適度の収率で良い分離を示す。ジアルキルスズトリアミド汚染物質がモノアルキルスズトリアミドよりも低い沸点を有する場合、ジアルキルスズトリアミドは、蒸留プロセスの間に初期画分を集めて廃棄することによって分離除去され得る。
モノアルキルスズトリアルコキシドは、相当するモノアルキルスズトリアミドを非水溶媒中のアルコール及び塩基と反応させることによって製造され得る。本明細書に記載された加工を用いてモノアルキルスズトリアミド中の少ないポリアルキルスズ汚染物質を生成物モノアルキルスズトリアルコキシドへ送りやることができ、その結果、生成物モノアルキルスズトリアルコキシドは本質的に上述のモルパーセンテージの、少ないジアルキルスズ汚染物質を有する。適した有機溶媒には、例えば、アルカン(例えばペンタン又はヘキサン)、芳香族炭化水素(例えばトルエン)、エーテル(例えばジエチルエーテル、C2H5OC2H5)、又はそれらの混合物が含まれる。アルコールは所望のアルコキシド基を提供するように選択され、アルコールROHが、スズに結合した配位子として-OR基を導入するようにする。適したR基の候補が上に提供され、相応してアルコールを示す。t-アミルアルコールを使用する実施例が以下に与えられるが、他のアルコールを同様に使用して、所望の-ORアルコキシド配位子を提供することができる。アルコールはほぼ化学量論量において提供され得る。アルコールを用いて3つのアミド基を置換するので、アルコールの3モル当量が化学量論量である。一般的には、アルコールの量は、少なくとも約-5%化学量論的当量及び更なる実施形態において少なくともおよそ化学量論的当量であり得、大過剰なアルコールを使用することができる。実施例5はアルコールを化学量論的当量よりも+3.33%超で使用して行われ、すなわち、モノ-アルキルスズトリアミド1モル当たり3.1モルのアルコールを用いて行われる。
生成物アルキルスズトリアルコキシドの精製を促進するために、四座キレート剤を添加して、未反応スズテトラアミド種を配位させて、蒸留中に気化しない錯体を形成することができる。例えば、TREN、トリエチレンテトラアミン(trien)、又は他の四座(tertadentate)非平面配位配位子を用いて、未反応種と錯体を形成して精製を促進することができる。配位配位子は、反応の開始から蒸留を行なう前の任意の時間まで選択された時間において、スズのモル量に対して約0.5モル%~約15モル%及び更なる実施形態において約1.0モル%~約10モル%の量において加えられ得る。TRENなどの四座非平面配位配位子はまた、スズテトラアルコキシド化合物と錯体を形成してそれらの蒸留を抑えるために有効であり得ることも見出されている。一般的には、それぞれのスズテトラアミドを蒸留させないために四座キレート剤の少なくともほぼ化学量論量を有することが望ましいであろう。このように、テトラアミドの与えられた量に対して四価の錯生成剤の量は、約1:1モル比、又はいくつかの実施形態においてスズテトラアミド1モル当たり少なくとも約95モルパーセント、更なる実施形態において約98モルパーセント~約200モルパーセント及びさらに別の実施形態において約99モルパーセント~約120モルパーセントの四価の錯生成剤であり得る。このように、四座非平面配位配位子は、テトラアミド又はテトラアルコキシドスズ化合物のどちらかからのモノアルキルスズトリアルキド(monalkyl tin trialkides)の精製を改良するのに有効であり得る。上記の明示範囲内の反応体の量のさらに別の範囲が考えられ、本開示の範囲内であることを当業者は認識するであろう。必要ならば、ポリアルキル汚染物質からモノアルキルスズトリアルコキシドをさらに精製するために分留を行なうことができる。
ポリアルキル汚染物質が少ないモノアルキルスズトリアミドを有効に使用して、相応してポリアルキル汚染物質が少ない誘導体を形成することができるが、モノアルキルスズトリアミドからのモノ-アルキルトリアミドスズの合成を用いて、モノアルキルスズトリアミドの、汚染物質レベルが低くないとしても、汚染物質が少ない生成物を形成することができ、これはポリアルキル汚染物質を明白に取り除くことができるモノアルキルトリアミドスズの結晶形成に拠る。このように、モノアルキルトリアミドスズの合成は、ジアルキルスズ汚染物質が少ない組成物を形成する補助的な又は代替経路を提供する。このため、いくつかの実施形態において、ジアルキルスズ汚染物質が少ない生成物組成物を依然として得ながら、汚染物質レベルが高めである商用供給源又は反応経路などからの、所望の汚染物質が高めであるモノアルキルスズトリアミドを用いることができる。モノアルキルトリアミドスズ化合物を用いて、ジアルキルスズ汚染物質が少ないモノアルキルスズトリアルコキシド組成物を形成することができる。
反応は、N-メチルアセトアミド(CH3CONHCH3)などのN-アルキルアミドの、モノアルキルスズトリアミドへの添加を必要とする。一般的には、N-アルキルアミド反応体は、RaCONHRb(式中、Ra及びRbは独立に、メチル基、エチル基、プロピル基、イソプロピル基等の、1~10個の炭素原子を有する炭化水素基である)として記載することができる。生成物化合物の結晶構造は確認されており、構造は、以下の実施例において示される。要約すると、生成物中のアミド基が窒素原子においてスズに結合しており、相当する配位子構造を形成する。
反応の熱発生及び進行を制御するために、N-アルキルアミド反応体を段階的に、例えば少なくとも約2分間にわたって添加することができる。モノアルキルスズトリアミドを約0.1M~約8M及び更なる実施形態において約0.2M~約6Mの濃度で有機溶媒中に溶解することができる。適した有機溶媒には、例えば、アルカン(例えばペンタン又はヘキサン)、芳香族炭化水素(例えばトルエン)、エーテル(例えばジエチルエーテル、C2H5OC2H5)、又はそれらの混合物が含まれる。反応は発熱性であり、熱は一般的に加えられる必要はない。反応生成物は、結晶を形成することができ、反応は一般的に約20分~24時間継続され得る。反応の終了後に、溶媒を除去して生成物の結晶を集めることができる。結晶を洗浄して乾燥させることができる。ジアルキルスズ化合物が生成物結晶から取り除かれるのが観察される。上記の明示範囲内の反応体濃度、添加時間、及び反応時間のさらに別の範囲が考えられ、本開示の範囲内であることを当業者は認識するであろう。
放射線感受性レジスト組成物の加工のために、モノアルキルトリアミドスズを反応させてモノアルキルスズトリアルコキシド化合物を形成するのが望ましい場合がある。アルカリアルコキシドを用いて、有機スラリー中の反応によってトリアミド配位子をアルコキシド配位子で置換することができる。モノアルキルスズトリアルコキシド化合物が形成されるとき、それは約0.01M~2M及び更なる実施形態において約0.04M~約1Mの濃度において有機溶媒中に溶解する。アルカリアルコキシド化合物は、ZOR’(式中、ZはK、Na、又はLiなどのアルカリ原子であり、-OR’は、RSn(OR’)3生成物組成物のために相当するR’基を提供するアルコキシド基である)として記載することができる。いくつかのアルカリアルコキシドは、例えば、Sigma-Aldrichから商業的に入手可能であり、これらの化合物は高吸湿性であり、そのためそれらは空気から単離され得る。適した有機溶媒には、例えば、アルカン(例えばペンタン又はヘキサン)、芳香族炭化水素(例えばトルエン)、エーテル(例えばジエチルエーテル、C2H5OC2H5)、又はそれらの混合物が含まれる。アルカリアルコキシドは、スズ原子1個当たり3つのアルコキシド基に相当する、少なくとも化学量論量において提供され得る。反応は、約15分~約48時間の間実施され得る。生成物液体を蒸留して、生成物を精製することができる。上記の明示範囲内の濃度及び時間のさらに別の範囲が考えられ、本開示の範囲内であることを当業者は理解するであろう。
実施例1:t-BuSn(NMe
2
)
3
の合成
この実施例は、N-メチルアミド基を置換するスズに結合したt-ブチル基を有するスズ化合物の合成を目的としている。
この実施例は、N-メチルアミド基を置換するスズに結合したt-ブチル基を有するスズ化合物の合成を目的としている。
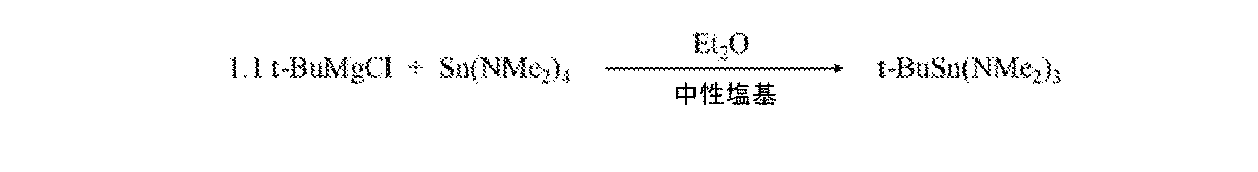
アルゴン充填グローブボックス内で5Lの3首丸底フラスコに、Sn(NMe2)4(827.5g、2805mmol、Sigma)を入れた。無水エーテル(2000mL)をフラスコに添加した。多量のt-BuMgCl(1500mL、2.06M(滴定したばかり)、3090mmol)を別個の2Lの2首丸底フラスコに添加した。フラスコに栓をし、シュレンクラインに取り付けた。Sn(NMe2)4溶液を5Lのジャケット付き反応器に移し、240RPMで撹拌した。自動シリンジポンプを使用して、t-BuMgCl溶液を5Lのジャケット付き反応器に50ml min-1の速度で供給した。ジャケット付き反応器内の混合物の温度を20℃に維持した。t-BuMgCl溶液を完全に添加した後、反応物を一晩撹拌した。得られた混合物を、10Lフィルター反応器を通して撹拌バーを備えた5Lの3首丸底フラスコ内に移した。5Lジャケット付き反応器及びフィルター反応器内の固形分をペンタンで洗浄した(2×1L)。撹拌バーを備えた5Lの3首丸底フラスコ内に洗浄物を集め、真空下で揮発物を取り除いた。揮発物を取り除いた後、粗生成物に相当する淡黄色油性懸濁液が観察された。フラスコをグローブボックス内に入れ、粗生成物を粗多孔性フリット漏斗を通して濾過した。濾液を撹拌バーを備えた2Lの2首丸底フラスコ内に移し、それに栓をし、シュレンクラインに移した。粗生成物をショートパス真空蒸留によって1L受けフラスコ(500ミリトール、65℃~75℃)内で精製して、t-BuSn(NMe2)3として同定された無色の油323~604g、37~70%を生じた。プロトンNMR(図1)及び119Sn NMR(図2)を実施して、以下のピークが観察される生成物の特性を決定する:1H NMR(C6D6,MHz):2.84(s,18H,-NCH3),1.24(s,9H,H3CC-);119Sn NMR(C6D6,186.4MHz:-85.69.定量的プロトンNMR及びスズNMRを実施して、生成物の純度を測定した塩基dona標準。qNMR:1H、標準1,3,5-トリメトキシベンゼン、純度94.5(3)モル%(94.5±0.3モル%)モノアルキルスズ;119Sn、標準MeSnPh3、純度93.5(2)モル%モノアルキルスズ。
実施例2:CySn(NMe
2
)
3
(Cy=シクロヘキシル)の合成
この実施例は、Sn(NMe2)4のN-メチルアミド基を置換するZn試薬からのシクロヘキシル基を有するスズ化合物の合成を目的としている。
この実施例は、Sn(NMe2)4のN-メチルアミド基を置換するZn試薬からのシクロヘキシル基を有するスズ化合物の合成を目的としている。
アルゴン充填グローブボックス内で250mLの3首丸底フラスコ(RBF)にSn(NMe2)4(5.61g、19.0mmol、Sigma)を入れた。無水エーテル(150mL)をフラスコに添加した。別個に、100mLのRBFにw/LiNMe2(0.97g、19.0mmol、Sigma)及び無水エーテル(20mL)を入れた。CyZnBr(Cy=シクロヘキシル、48.5mL、0.392M、19.0mmol、Sigma])をこのフラスコにゆっくりと添加して、CyZnNMe2を製造した。反応は発熱性であるので、CyZnBrをゆっくりと添加して反応温度を制御した。滴下漏斗及び還流冷却器をシュレンクライン上の250mLの3首RBFに活性アルゴンパージ下で取り付けた。250mLのRBFをアルミニウム箔で覆って光を入れないようにしながらCyZnNMe2溶液を滴下漏斗に添加し、撹拌しながら滴状に分与した。完全に添加した後、反応物を一晩撹拌し、溶媒を真空中で除去して沈殿物と共に薄い橙色油を生じた。油を真空蒸留(58~62℃、150ミリトール)によって精製した。得られた生成物は、CySn(NMe2)3として同定された無色の油4.38g(69%の収率)であった。プロトンNMR(図3)及び119Sn NMR(図4)は、以下のピークが観察される生成物の特性を決定する:1H NMR(C6D6,500MHz):2.85(s,18H,-NCH3),1.86(m,3H,-CyH),1.69(m,2H,-CyH),1.53(m,3H,-CyH),1.24(m,3H,-CyH);119Sn NMR(C6D6,186.4MHz):-73.77.
実施例3.(CyHp)Sn(NMe
2
)
3
(CyHp=シクロヘプチル)の合成
この実施例は、以下の式に示されるようにシクロヘプチル基を有するスズトリアミドの合成を目的としている。この合成において、亜鉛試薬(CyHp)2Znからのシクロヘプチル基は、Sn(NMe2)4のN-メチルアミド基を置換する。
この実施例は、以下の式に示されるようにシクロヘプチル基を有するスズトリアミドの合成を目的としている。この合成において、亜鉛試薬(CyHp)2Znからのシクロヘプチル基は、Sn(NMe2)4のN-メチルアミド基を置換する。
アルゴン充填グローブボックス内で250mLの3首丸底フラスコ(RBF)にSn(NMe2)4(6.49g、22.0mmol、Sigma)を入れた。無水エーテル(150mL)を添加した。滴下漏斗及び還流冷却器をシュレンクライン上の250mLの3首RBFに活性アルゴンパージ下で取り付けた。別個に調製される(CyHp)2Zn(0.351M、31.3mL、11.0mmol)を以下のように合成した:2CyHpMgBr+Zn(OCH3)2。250mLのRBFをアルミニウム箔で覆って光を入れないようにしながら(CyHp)2Zn溶液を活性アルゴンパージ下で滴下漏斗に添加し、次いで撹拌しながら滴状に分与した。完全に添加した後、反応物を一晩撹拌した。次に、溶媒を真空中で除去した。反応フラスコをグローブボックス内に入れ、ヘキサンを添加した。溶液をセライト(登録商標)上で濾過し、溶媒を真空中で除去して沈殿物と共に無色の油を生じた。油を真空蒸留によって精製した(82~86℃、180ミリトール)。得られた生成物は、(CyHp)Sn(NMe2)3として同定された無色の油4.01g(52%の収率)であった。プロトンNMR(図5)及び119Sn NMR(図6)は、以下のピークが観察される生成物の特性を決定する:1H NMR(C6D6,500MHz):2.84(s,18H,-NCH3),2.01(m,2H,-CyHpH),1.82(m,1H,-CyHpH),1.69-1.23(m,10H,-CyHpH);119Sn NMR(C6D6,186.4MHz):-66.93.
アルゴン充填グローブボックス内で5Lの3首RBFにSn(NMe2)4(539.0g、1.827mol、Sigma)を入れた。約3Lの無水ジエチルエーテル及びピリジン(289.1g、3.66mol)をフラスコに添加した。フラスコに首部の2つにガラス栓で栓をし、真空アダプターを第3の首部に取り付けた。別個に、2Lの2首RBFに、メスフラスコ(2.01M(滴定された)、2.01mol、Sigma)で測定された1Lのt-BuMgCl(グリニャール試薬)を入れた。アルゴン充填シュレンクライン上で、5Lのジャケット付きケミグラス(Chemglass)(商標)反応器が高真空及び熱反応のために用意された。反応器にアルゴンを戻し、次に、反応器容器の周りのジャケットを-30℃に冷却した。
5Lの3首RBFの内容物をアルゴン正圧下でポリエチレン(PE)管を通してケミグラス(Chemglass)(商標)反応器に移した。オーバーヘッド攪拌機を用いて撹拌を開始し、反応の温度を-15℃に冷却させた。シュレンクライン上で、内部反応温度を5℃未満に維持しながらアルゴン正圧を用いて20~30分間かけてグリニャール試薬をポリエチレン(PE)管を通して添加した。濃い橙色及び沈殿物が生じた。完全に添加した後、アルミニウム箔を用いて反応物を光から遮蔽したままで反応物を一晩撹拌し、室温に達するようにさせた。
一晩の反応後、反応色は淡黄色であった。30~35℃の加熱ジャケットの補助で溶媒を真空中で除去した。溶媒の除去後、無水ペンタン(約2.5L)をアルゴン正圧下で反応器にポリエチレン管によって添加し、オーバーヘッド攪拌機を用いて固形分を十分に混合した。ペンタン中に分散された反応生成物をアルゴン正圧を用いてポリエチレン管によって10Lフィルター反応器に移した。反応生成物を濾過し、次にポリエチレン管を通って3LのRBF中に移した。ペンタン溶媒を、得られた淡黄色濾液から真空中で除去して、黄色の油を残した。油を1Lのシュレンクフラスコに移し、ショートパス蒸留ヘッド(50~52℃、300ミリトール)を使用して真空蒸留し、無色の油349.9g(62%)を生じた。図7(1HNMR)及び図8(119Sn NMR)は図1及び図2に似ており、生成物がSn(NMe2)4と平衡しているモノアルキル種からなることを示す。選択された標準を用いて定量的プロトンNMR及びスズNMRを実施して、生成物の純度を測定した。qNMR:1H、標準1,3,5-トリメトキシベンゼン、純度89.9(7)モル%モノアルキルスズ;119Sn、標準MeSnPh3、純度93.6(4)モル%モノアルキルスズ。
実施例5.t-BuSn(NMe
2
)
3
からの高純度モノアルキルアルコキシドt-BuSn(OtAm)3の調製
この実施例は、以下の反応による相当するモノアルキルスズトリアミドからのモノアルキルスズトリアルコキシドの合成を示す。
この実施例は、以下の反応による相当するモノアルキルスズトリアミドからのモノアルキルスズトリアルコキシドの合成を示す。
グローブボックス内で、2Lの2首RBFに、実施例4からの約500mLのペンタン及びt-BuSn(NMe2)3(329.4g、1.07モル)を入れた。フラスコを天秤上で風袋を差し引き、トリス(2-アミノエチル)アミン(3.91g、26.7mmol)をシリンジによって反応混合物中に直接に添加した。反応及び精製の間にアミンが錯体を形成し、スズテトラキスアミドを除去する。スズテトラキスアミドを系から除去することが必要でない場合、実施例1の生成物を使用して、付加的なモノアルキルスズ生成物を合成することができる。実施例1に従って合成される材料を使用して反応順序を継続することができる。磁気撹拌バーを加え、次に反応を封止し、シュレンクラインにもたらした。フラスコをドライアイス/イソプロパノール槽内で冷却した。別個に、1Lシュレンクフラスコにtert-アミルアルコール(2-メチル-2-ブタノール)(292.2g、3.315mol)及び少量のペンタンを入れ、次にシュレンクラインに取り付けた。シュレンクフラスコ中のアルコール/ペンタン溶液は、脱ガスしたNMe2Hのための酸トラップ溶液にインライン接続される鉱油バブラーへの出口パージがある反応フラスコにカニューレによって移される。アルコールを完全に添加した後、反応を室温に達するようにさせ、1時間の間撹拌した。1時間の反応後に、溶媒を真空中で除去し、生成物を真空蒸留して(95~97℃、500ミリトール)435g(93%)の無色の油をもたらした。図9(1HNMR)及び図10(119Sn NMR)は、以下のピークが観察される最終生成物t-BuSn(Ot-Am)3のNMRスペクトルを示す:1H NMR(C6D6,500MHz):1.61(m,6H,-OC(CH3)2CH2),1.37(m,18H,-OC(CH3)2),1.28(s,9H,-C(CH3)3),1.01(m,9H,-OC(CH3)2CH2CH3);119Sn NMR(C6D6,186.4MHz):-240.70.定量的プロトンNMRを実施して、生成物の純度レベルを測定した。qNMR:1H、標準1,3,5-トリメトキシベンゼン、純度97.7(3)%;119Sn、標準MeSnPh3、99(1)モル%モノアルキルスズ。
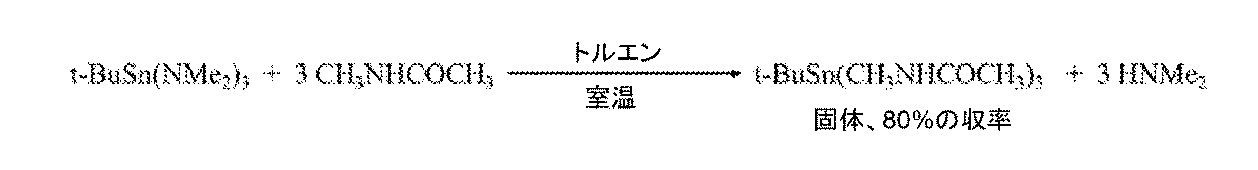
グローブボックス内で、250mLシュレンク丸底フラスコに、1%のt-Bu2Sn(NMe2)2を含有するt-BuSn(NMe2)3(40.13g、130mmol)を入れた。t-BuSn(NMe2)3は、実施例1又は実施例4によって合成された。50ミリリットルのトルエンを丸底フラスコに添加し、それにその後に、N-メチルアセトアミド(28.6g、391mmol、Sigma)をゆっくりと添加して熱発生を制御した。付加的な30mLのトルエンを使用して、反応フラスコ内で全てのN-メチルアセトアミドを洗浄した。フラスコをすりガラス栓で封止し、シュレンクラインに移した。数時間にわたって、大きな結晶が溶液から沈殿した。トルエンを活性アルゴンパージ下でカニューレによって除去した。白色結晶を取り出し、カニューレを付加して100mLのペンタンで2回洗浄し、引き続いて除去した。それらは真空中で乾燥され、40.6g(80%)のt-ブチルトリス(N-メチルアセトアミド)スズ(IV)を生じた。図11は、X線回折によって確認された固体の結晶構造を示す。図12に示されるように、プロトンNMRスペクトルは以下のピークを生じる:1H NMR(C6D6,500MHz):2.52(s,9H,-NCH3),2.01(m,2H,-CyHpH),1.74(s,9H,-(H3C)3CSn),1.69(s,9H,-CH3CO).図13に示されるように、スズNMRスペクトルは以下のピークをもたらす:119Sn NMR(C6D6、186.4MHz):-346.5.
実施例7.t-BuSn(Ot-Am)
3
の合成
この実施例は、実施例6のt-ブチルトリス(N-メチルアセトアミド)スズ(IV)生成物からのt-BuSn(Ot-Am)3の合成を示す。
この実施例は、実施例6のt-ブチルトリス(N-メチルアセトアミド)スズ(IV)生成物からのt-BuSn(Ot-Am)3の合成を示す。
アルゴン雰囲気を有するグローブボックス内で、3L丸底フラスコに実施例6からのt-ブチルトリス(N-メチルアセトアミド)スズ(IV)(100g、255mmol)を入れ、その後に、NaOtAm(98g、890mmol、Sigma)を添加した。電磁攪拌機及び長さ2.5インチの卵形撹拌バーを使用して混合物を1.5Lのペンタン中でスラリーにした。スラリーは濃縮し、30~60分後に乳白色になった。撹拌を約16時間の間続けた。次に、スラリーをグローブボックス内の中多孔性フリット漏斗を通して濾過し、回収された固形分を100mLのペンタンで2回洗浄した。保有された固形分は、濾過の間に非常に微細なケークを形成し、そのため撹拌を時折用いて回収を促進した。
濾液を撹拌バーを備えた2首2Lフラスコに移し、次に、フラスコをすり合せ栓及びシュレンクインレットアダプターで封止した。フラスコをグローブボックスから取り出し、過剰な溶媒を真空下で取り除くヒュームフード内の真空ラインに接続する。次に粗生成物を真空蒸留によって精製し、100mLシュレンク貯蔵フラスコ内に集めた。真空蒸留のために、油槽を150℃に設定した。生成物を300ミリトール及び98~102℃の温度で蒸留して、74g(66%)の生成物を生じた。図14に示されるように、プロトンNMRスペクトルは以下のシフトを示した:1H NMRシフト[400MHz,C6D6]:1.64(q,6H,-CH2),1.39(s,18H,-C(CH3)2),1.29(s,9H,(CH3)3CSn),1.03(t,9H,-CCH3).図15に示されるように、119Sn NMRスペクトルは以下のピークを示した:119Sn NMRシフト[149.18MHz,C6D6]:-241.9.定量的NMRを実施して、標準の評価に続いて純度を求めた。1HqNMR、標準1,3,5-トリメトキシベンゼン、純度97.3(1)モル%モノアルキル。
実施例8.分留精製
この実施例は、t-Bu2Sn(NMe2)2とt-BuSn(NMe2)3との混合物からのその分離によってt-BuSn(NMe2)3を精製する分留の有効性を実証する。
この実施例は、t-Bu2Sn(NMe2)2とt-BuSn(NMe2)3との混合物からのその分離によってt-BuSn(NMe2)3を精製する分留の有効性を実証する。
グローブボックス内で、3000mLの3首丸底フラスコ(RBF)に約3.27%のt-Bu2Sn(NMe2)2を含有するt-BuSn(NMe2)3(合計1420g、4.6mol)を入れた;試料は、実施例1に記載された方法によって改質t-BuMgCl:Sn(NMe2)4比を用いて調製された。ガラス栓をRBFの2つの首部に置き、第3の首部をシュレンクラインに取り付けた。別個に、5Lのケミグラス(Chemglass)ジャケット付き反応器は、オーバーヘッド攪拌機、温度プローブ、及び上下に重ねて配置された2つの18インチ蒸留塔を取り付けられた。蒸留塔は、Pro-Pak(商標)(ThermoScientific、0.24in2)高効率蒸留塔充填物で充填された。温度プローブを有するショートパス蒸留ヘッドが蒸留塔の頂部に取り付けられた。次に、ショートパスヘッドの頂部を3つの500mLシュレンク型フラスコ(Schlenk bombs)を保持する3アーム・カウ・ジョイントに接続した。反応器を脱気し、アルゴンで3回充填し戻した。t-Bu2豊富混合物をアルゴン下で大きなカニューレによって反応器に添加した。ジャケット付き反応器を減圧(500ミリトール)において110~120℃の間で加熱して蒸留を開始した。蒸留塔の底の温度を測定すると95~100℃であったが、他方、カラムの頂部の温度は58~60℃の間に維持された。3つの画分が集められ、それぞれ119Sn NMR分光分析法によって分析された。図16~19は、プールされた試料(図16)、3つの画分のそれぞれ(順に図17~19)の119Sn NMRスペクトルのプロットである。全ての3つの画分は、t-Bu2Sn(NMe2)2のNMR信号を示さなかった。全ての画分を組み合わせる合計収率は850g(60%)であった。119Sn NMR(C6D6、186.4MHz):-85.45
実施例9.真空蒸留精製
この実施例は、Sn(OtAm)4とt-BuSn(OtAm)3との混合物からのその分離によって実証されるように、t-BuSn(OtAm)3を精製してアミドを含有しない組成物を製造するための真空蒸留の有効性を示す。トリス(2-アミノエチル)アミン(TREN)が精製助剤として使用された。
この実施例は、Sn(OtAm)4とt-BuSn(OtAm)3との混合物からのその分離によって実証されるように、t-BuSn(OtAm)3を精製してアミドを含有しない組成物を製造するための真空蒸留の有効性を示す。トリス(2-アミノエチル)アミン(TREN)が精製助剤として使用された。
アルゴン雰囲気を有するグローブボックス内で、100mL丸底シュレンクフラスコに、約1.3%のSn(OtAm)4で汚染されたt-BuSn(OtAm)3[25g、55.825mmol]を入れ、その後に、10mLの無水ペンタンを入れた。ガラスホールピペットを使用してTREN[0.112g、0.7686mmol]を添加する前に、電磁攪拌機を使用して混合物を撹拌した。24/40STジョイントのためのガラス栓及びサイドアームポートのためのテフロン(登録商標)弁を使用してフラスコを封止した。フラスコをシュレンクラインに接続し、不活性ガス(窒素)下に置き、シリコーン油槽内に置いた。Pt/1000温度プローブを有するHeidolph HEI-TEC撹拌プレートを使用して撹拌及び加熱制御を達成し、油槽のためのフィードバック温度制御を可能にした。真空下で過剰な溶媒を取り除く前に槽を45℃に保持した。ミリトール真空計を使用して溶媒除去を検証するとき、50mLシュレンク型フラスコを受容容器として使用してショートパス真空蒸留装置を設定した。真空蒸留は300ミリトールの絶対圧、150℃の槽温、及び94~98℃の範囲の蒸気温度で実施された。
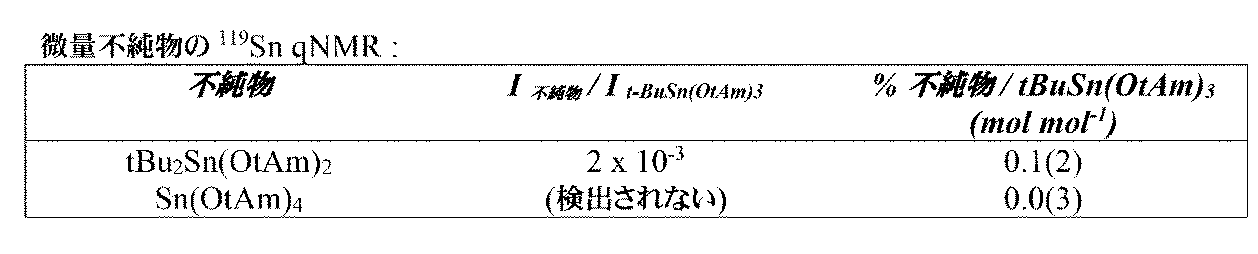
Sn(OtAm)4の100%除去を仮定する理論的回収は24.66gであり、回収された留出物は21.70gであり、88%の回収をもたらした。119Sn NMRスペクトルは、図20(ベースライン)及び図21(精製された)に示されている。119Sn NMRシフト[149.18MHz,C6D6]:tBu2Sn(OtAm)2:-113ppm;tBuSn(OtAm)3:-241ppm;Sn(OtAm)4:-370ppm.
上記の実施形態は例示のためのものであり限定的でないことを意図している。更なる実施形態が請求の範囲内である。さらに、本発明は特定の実施形態を参照して説明されたが、本発明の趣旨及び範囲から逸脱せずに形態及び詳細に変更を加えることができることを当業者は認識するであろう。本明細書の明示的な開示に反する主題が組み込まれないように上記の文献の参照による任意の組み込みは制限される。特定の構造、組成物及び/又はプロセスが構成要素、要素、成分又は他の区分に関して本明細書において説明される限りにおいて、本明細書における開示は、特に記載のない限り、考察において示唆されるように、主題の基本的な性質を変えない付加的な特徴を含むことができる特定の実施形態、特定の構成要素、要素、成分、他の区分又はそれらの組合せを含む実施形態並びにこのような特定の構成要素、成分又は他の区分又はそれらの組合せから本質的になる実施形態におよぶことが理解されるはずである。
上記の実施形態は例示のためのものであり限定的でないことを意図している。更なる実施形態が請求の範囲内である。さらに、本発明は特定の実施形態を参照して説明されたが、本発明の趣旨及び範囲から逸脱せずに形態及び詳細に変更を加えることができることを当業者は認識するであろう。本明細書の明示的な開示に反する主題が組み込まれないように上記の文献の参照による任意の組み込みは制限される。特定の構造、組成物及び/又はプロセスが構成要素、要素、成分又は他の区分に関して本明細書において説明される限りにおいて、本明細書における開示は、特に記載のない限り、考察において示唆されるように、主題の基本的な性質を変えない付加的な特徴を含むことができる特定の実施形態、特定の構成要素、要素、成分、他の区分又はそれらの組合せを含む実施形態並びにこのような特定の構成要素、成分又は他の区分又はそれらの組合せから本質的になる実施形態におよぶことが理解されるはずである。
なお、上述した本発明は、次の態様を包含していることを確認的に述べておく。
第1態様:化学式RSn(OR’) 3 によって表されるモノアルキルスズトリアルコキシド化合物又は化学式RSn(NR’ 2 ) 3 によって表されるモノアルキルスズトリアミド化合物と、
全スズ量に対して4モル%以下のジアルキルスズ化合物とを含む組成物であって、式中、
Rが、1~31個の炭素原子を有するヒドロカルビル基であり、及び
R’が、1~10個の炭素原子を有するヒドロカルビル基である、組成物。
第2態様:Rが、R 1 R 2 R 3 C-(式中、R 1 及びR 2 が独立に1~10個の炭素原子を有するアルキル基であり、R 3 が水素又は1~10個の炭素原子を有するアルキル基である)によって表される分岐アルキル配位子である、上記第1態様に記載の組成物。
第3態様:Rがメチル(CH 3 -)、エチル(CH 3 CH 2 -)、イソプロピル(CH 3 CH 3 HC-)、tert-ブチル((CH 3 ) 3 C-)、tert-アミル(CH 3 CH 2 (CH 3 ) 2 C-)、sec-ブチル(CH 3 (CH 3 CH 2 )CH-)、ネオペンチル(CH 3 ) 3 CCH 2 -)、シクロヘキシル、シクロペンチル、シクロブチル、又はシクロプロピルを含む、上記第1態様に記載の組成物。
第4態様:R’がメチル基、エチル基、イソプロピル基、又はt-ブチル基を含む、上記第1態様~上記第3態様のいずれかに記載の組成物。
第5態様:R’がt-アミル基を含む、上記第1態様~上記第3態様のいずれかに記載の組成物。
第6態様:約1モル%以下のジアルキルスズ化合物を含む、上記第1態様~上記第5態様のいずれかに記載の組成物。
第7態様:モノアルキルスズトリアミドを含む、上記第1態様~上記第6態様のいずれかに記載の組成物。
第8態様:上記第1態様又は上記第4態様~上記第7態様のいずれかに記載の組成物と、有機溶媒とを含む溶液。
第9態様:約0.005M~約0.5Mの濃度を有する上記第8態様に記載の溶液であって、前記溶媒がアルコールを含む、溶液。
第10態様:Rがメチル(CH 3 -)、エチル(CH 3 CH 2 -)、イソプロピル(CH 3 CH 3 HC-)、tert-ブチル((CH 3 ) 3 C-)、tert-アミル(CH 3 CH 3 (CH 3 ) 2 C-)、sec-ブチル(CH 3 (CH 3 CH 2 )CH-)、ネオペンチル(CH 3 ) 3 CCH 2 -)、シクロヘキシル、シクロペンチル、シクロブチル、又はシクロプロピルを含み、R’がメチル基、エチル基、イソプロピル基、t-ブチル基、又はt-アミル基を含む、上記第8態様又は上記第9態様に記載の溶液。
第11態様:ジアルキルスズの汚染が少ないモノアルキルスズトリアルコキシド化合物を選択的に形成するための方法であって、
上記第7態様に記載の組成物を式HOR’’によって表されるアルコールと有機溶媒中で反応させてRSnOR’’ 3 (式中、R’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である)を形成して、スズの全量に対して4モル%以下のジアルキルスズ化合物を有する生成物組成物を形成する工程を含む方法。
第12態様:化学式RSn-(NR’COR’’) 3 (式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、及び
R’及びR’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である)によって表されるモノアルキルトリアミドスズ化合物を含む組成物。
第13態様:R’がメチル基である、上記第12態様に記載の組成物。
第14態様:R’’がメチル基である、上記第12態様又は上記第13態様に記載の組成物。
第15態様:Rがメチル(CH 3 -)、エチル(CH 3 CH 2 -)、イソプロピル(CH 3 CH 3 HC-)、tert-ブチル((CH 3 ) 3 C-)、t-アミル(CH 3 CH 3 (CH 3 CH 2 )C-)、sec-ブチル(CH 3 (CH 3 CH 2 )HC-)、ネオペンチル(CH 3 ) 3 CCH 2 -)、シクロヘキシル、シクロペンチル、シクロブチル、又はシクロプロピルを含む、上記第12態様に記載の組成物。
第16態様:結晶性であり、約1モルパーセント以下のジアルキルスズ汚染物質を含む、上記第12態様~上記第15態様のいずれかに記載の組成物。
第17態様:RMgX、R 2 Zn、RZnNR’ 2 、又はそれらの組合せからなる群から選択されるアルキル化剤を有機溶媒を含む溶液中でSn(NR’ 2 ) 4 と反応させる工程であって、
式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、
Xがハロゲンであり、及び
R’が、1~10個の炭素原子を有するヒドロカルビル基である工程を含む、モノアルキルスズトリアミド化合物を形成するための方法。
第18態様:前記溶液が、約0.01M~約5Mの間のスズの濃度を有する、上記第17態様に記載の方法。
第19態様:前記有機溶媒がアルカン、芳香族炭化水素、エーテル、又はそれらの混合物を含む、上記第17態様又は上記第18態様に記載の方法。
第20態様:前記溶液が、スズ試薬及び前記アルキル化剤の化学量論的反応に対して約±25%のアルキル化剤の濃度を有する、上記第17態様~上記第19態様のいずれかに記載の方法。
第21態様:前記反応が、周辺光から遮蔽して前記アルキル化剤の段階的な添加によって不活性雰囲気下で行われる、上記第17態様~上記第20態様のいずれかに記載の方法。
第22態様:前記アルキル化剤が10分~90分間にわたって段階的に添加される、上記第17態様~上記第21態様のいずれかに記載の方法。
第23態様:前記反応が15分~24時間にわたって-100℃~100℃の温度で行われる、上記第17態様~上記第21態様のいずれかに記載の方法。
第24態様:前記溶液がスズに対して0.25~4モル当量の中性配位塩基をさらに含む、上記第17態様~上記第23態様のいずれかに記載の方法。
第25態様:RSn(NR’ 2 ) 3 を式HOR’’によって表されるアルコールと有機溶媒中で反応させてRSnOR’’ 3 を形成する工程であって、RSn(NR’ 2 ) 3 反応体が約4モル%以下のジアルキルスズ汚染物質を有し、上記第1態様に記載の方法の生成物であり、式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’及びR’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である、工程を含む、ジアルキルスズの汚染が少ないモノアルキルスズトリアルコキシド化合物を選択的に形成するための方法。
第26態様:前記反応が、前記スズのモル量に対して約0.5モル%~約15モル%の量の四座キレート剤を使用して行われる、上記第25態様に記載の方法。
第27態様:化学式RSn(NR’ 2 ) 3 によって表されるモノアルキルスズトリアミド化合物をアミド(R’’CONHR’’’)と有機溶媒中で反応させる工程であって、式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’、R’’及びR’’’が独立に、1~8個の炭素原子を有するヒドロカルビルである工程と、
式RSn(NR’’’COR’’) 3 によって表される固体生成物を集める工程とを含む、モノアルキルトリアミドスズを形成するための方法。
第28態様:前記モノアルキルスズトリアミドが約0.1M~約8Mの初期濃度であり、前記溶媒がアルカン、芳香族炭化水素、又はエーテルである、上記第27態様に記載の方法。
第29態様:前記アミドが、少なくとも約2分間にわたって段階的に添加される、上記第27態様又は上記第28態様に記載の方法。
第30態様:前記固体生成物が結晶性であり、スズに対してジアルキルスズ化合物の汚染物質約1モルパーセント以下を有する、上記第27態様~上記第29態様のいずれかに記載の方法。
第31態様:モノアルキルトリアミドスズ化合物(RSn(NR’’’COR’’) 3 )をアルカリアルコキシド化合物(QOR’、式中、Qがアルカリ金属原子である)と有機溶媒中で反応させて、化学式RSn(OR’) 3 (式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’、R’’及びR’’’が独立に、1~10個の炭素を有するヒドロカルビル基である)によって表される生成物化合物を形成する工程を含む、モノアルキルスズトリアルコキシドを形成するための方法。
第32態様:アルコキシド供与化合物が、少なくとも化学量論量において提供される、上記第31態様に記載の方法。
第33態様:前記溶媒がアルカン、芳香族炭化水素、又はエーテルである、上記第31態様又は上記第32態様に記載の方法。
第34態様:モノアルキルスズ(monoalkyl tine)トリアルコキシドと四座非平面錯生成剤とのブレンドを蒸留する工程を含む、モノアルキルスズトリアルコキシドを精製するための方法。
第35態様:前記四座非平面錯生成剤がTRENを含む、上記第34態様に記載の方法。
第36態様:前記四座非平面錯生成剤が、スズのモル量に対して約0.5モル%~約15モル%の量で存在している、上記第34態様又は上記第35態様に記載の方法。
第37態様:前記アルキル基が、R 1 R 2 R 3 C-(式中、R 1 及びR 2 が独立に1~10個の炭素原子を有するアルキル基であり、R 3 が水素又は1~10個の炭素原子を有するアルキル基である)によって表される、上記第34態様~上記第36態様のいずれかに記載の方法。
第38態様:前記アルキル基が、イソプロピル、tert-ブチル、tert-アミル、sec-ブチル又はネオペンチルを含む、上記第34態様~上記第36態様のいずれかに記載の方法。
なお、上述した本発明は、次の態様を包含していることを確認的に述べておく。
第1態様:化学式RSn(OR’) 3 によって表されるモノアルキルスズトリアルコキシド化合物又は化学式RSn(NR’ 2 ) 3 によって表されるモノアルキルスズトリアミド化合物と、
全スズ量に対して4モル%以下のジアルキルスズ化合物とを含む組成物であって、式中、
Rが、1~31個の炭素原子を有するヒドロカルビル基であり、及び
R’が、1~10個の炭素原子を有するヒドロカルビル基である、組成物。
第2態様:Rが、R 1 R 2 R 3 C-(式中、R 1 及びR 2 が独立に1~10個の炭素原子を有するアルキル基であり、R 3 が水素又は1~10個の炭素原子を有するアルキル基である)によって表される分岐アルキル配位子である、上記第1態様に記載の組成物。
第3態様:Rがメチル(CH 3 -)、エチル(CH 3 CH 2 -)、イソプロピル(CH 3 CH 3 HC-)、tert-ブチル((CH 3 ) 3 C-)、tert-アミル(CH 3 CH 2 (CH 3 ) 2 C-)、sec-ブチル(CH 3 (CH 3 CH 2 )CH-)、ネオペンチル(CH 3 ) 3 CCH 2 -)、シクロヘキシル、シクロペンチル、シクロブチル、又はシクロプロピルを含む、上記第1態様に記載の組成物。
第4態様:R’がメチル基、エチル基、イソプロピル基、又はt-ブチル基を含む、上記第1態様~上記第3態様のいずれかに記載の組成物。
第5態様:R’がt-アミル基を含む、上記第1態様~上記第3態様のいずれかに記載の組成物。
第6態様:約1モル%以下のジアルキルスズ化合物を含む、上記第1態様~上記第5態様のいずれかに記載の組成物。
第7態様:モノアルキルスズトリアミドを含む、上記第1態様~上記第6態様のいずれかに記載の組成物。
第8態様:上記第1態様又は上記第4態様~上記第7態様のいずれかに記載の組成物と、有機溶媒とを含む溶液。
第9態様:約0.005M~約0.5Mの濃度を有する上記第8態様に記載の溶液であって、前記溶媒がアルコールを含む、溶液。
第10態様:Rがメチル(CH 3 -)、エチル(CH 3 CH 2 -)、イソプロピル(CH 3 CH 3 HC-)、tert-ブチル((CH 3 ) 3 C-)、tert-アミル(CH 3 CH 3 (CH 3 ) 2 C-)、sec-ブチル(CH 3 (CH 3 CH 2 )CH-)、ネオペンチル(CH 3 ) 3 CCH 2 -)、シクロヘキシル、シクロペンチル、シクロブチル、又はシクロプロピルを含み、R’がメチル基、エチル基、イソプロピル基、t-ブチル基、又はt-アミル基を含む、上記第8態様又は上記第9態様に記載の溶液。
第11態様:ジアルキルスズの汚染が少ないモノアルキルスズトリアルコキシド化合物を選択的に形成するための方法であって、
上記第7態様に記載の組成物を式HOR’’によって表されるアルコールと有機溶媒中で反応させてRSnOR’’ 3 (式中、R’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である)を形成して、スズの全量に対して4モル%以下のジアルキルスズ化合物を有する生成物組成物を形成する工程を含む方法。
第12態様:化学式RSn-(NR’COR’’) 3 (式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、及び
R’及びR’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である)によって表されるモノアルキルトリアミドスズ化合物を含む組成物。
第13態様:R’がメチル基である、上記第12態様に記載の組成物。
第14態様:R’’がメチル基である、上記第12態様又は上記第13態様に記載の組成物。
第15態様:Rがメチル(CH 3 -)、エチル(CH 3 CH 2 -)、イソプロピル(CH 3 CH 3 HC-)、tert-ブチル((CH 3 ) 3 C-)、t-アミル(CH 3 CH 3 (CH 3 CH 2 )C-)、sec-ブチル(CH 3 (CH 3 CH 2 )HC-)、ネオペンチル(CH 3 ) 3 CCH 2 -)、シクロヘキシル、シクロペンチル、シクロブチル、又はシクロプロピルを含む、上記第12態様に記載の組成物。
第16態様:結晶性であり、約1モルパーセント以下のジアルキルスズ汚染物質を含む、上記第12態様~上記第15態様のいずれかに記載の組成物。
第17態様:RMgX、R 2 Zn、RZnNR’ 2 、又はそれらの組合せからなる群から選択されるアルキル化剤を有機溶媒を含む溶液中でSn(NR’ 2 ) 4 と反応させる工程であって、
式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、
Xがハロゲンであり、及び
R’が、1~10個の炭素原子を有するヒドロカルビル基である工程を含む、モノアルキルスズトリアミド化合物を形成するための方法。
第18態様:前記溶液が、約0.01M~約5Mの間のスズの濃度を有する、上記第17態様に記載の方法。
第19態様:前記有機溶媒がアルカン、芳香族炭化水素、エーテル、又はそれらの混合物を含む、上記第17態様又は上記第18態様に記載の方法。
第20態様:前記溶液が、スズ試薬及び前記アルキル化剤の化学量論的反応に対して約±25%のアルキル化剤の濃度を有する、上記第17態様~上記第19態様のいずれかに記載の方法。
第21態様:前記反応が、周辺光から遮蔽して前記アルキル化剤の段階的な添加によって不活性雰囲気下で行われる、上記第17態様~上記第20態様のいずれかに記載の方法。
第22態様:前記アルキル化剤が10分~90分間にわたって段階的に添加される、上記第17態様~上記第21態様のいずれかに記載の方法。
第23態様:前記反応が15分~24時間にわたって-100℃~100℃の温度で行われる、上記第17態様~上記第21態様のいずれかに記載の方法。
第24態様:前記溶液がスズに対して0.25~4モル当量の中性配位塩基をさらに含む、上記第17態様~上記第23態様のいずれかに記載の方法。
第25態様:RSn(NR’ 2 ) 3 を式HOR’’によって表されるアルコールと有機溶媒中で反応させてRSnOR’’ 3 を形成する工程であって、RSn(NR’ 2 ) 3 反応体が約4モル%以下のジアルキルスズ汚染物質を有し、上記第1態様に記載の方法の生成物であり、式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’及びR’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である、工程を含む、ジアルキルスズの汚染が少ないモノアルキルスズトリアルコキシド化合物を選択的に形成するための方法。
第26態様:前記反応が、前記スズのモル量に対して約0.5モル%~約15モル%の量の四座キレート剤を使用して行われる、上記第25態様に記載の方法。
第27態様:化学式RSn(NR’ 2 ) 3 によって表されるモノアルキルスズトリアミド化合物をアミド(R’’CONHR’’’)と有機溶媒中で反応させる工程であって、式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’、R’’及びR’’’が独立に、1~8個の炭素原子を有するヒドロカルビルである工程と、
式RSn(NR’’’COR’’) 3 によって表される固体生成物を集める工程とを含む、モノアルキルトリアミドスズを形成するための方法。
第28態様:前記モノアルキルスズトリアミドが約0.1M~約8Mの初期濃度であり、前記溶媒がアルカン、芳香族炭化水素、又はエーテルである、上記第27態様に記載の方法。
第29態様:前記アミドが、少なくとも約2分間にわたって段階的に添加される、上記第27態様又は上記第28態様に記載の方法。
第30態様:前記固体生成物が結晶性であり、スズに対してジアルキルスズ化合物の汚染物質約1モルパーセント以下を有する、上記第27態様~上記第29態様のいずれかに記載の方法。
第31態様:モノアルキルトリアミドスズ化合物(RSn(NR’’’COR’’) 3 )をアルカリアルコキシド化合物(QOR’、式中、Qがアルカリ金属原子である)と有機溶媒中で反応させて、化学式RSn(OR’) 3 (式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’、R’’及びR’’’が独立に、1~10個の炭素を有するヒドロカルビル基である)によって表される生成物化合物を形成する工程を含む、モノアルキルスズトリアルコキシドを形成するための方法。
第32態様:アルコキシド供与化合物が、少なくとも化学量論量において提供される、上記第31態様に記載の方法。
第33態様:前記溶媒がアルカン、芳香族炭化水素、又はエーテルである、上記第31態様又は上記第32態様に記載の方法。
第34態様:モノアルキルスズ(monoalkyl tine)トリアルコキシドと四座非平面錯生成剤とのブレンドを蒸留する工程を含む、モノアルキルスズトリアルコキシドを精製するための方法。
第35態様:前記四座非平面錯生成剤がTRENを含む、上記第34態様に記載の方法。
第36態様:前記四座非平面錯生成剤が、スズのモル量に対して約0.5モル%~約15モル%の量で存在している、上記第34態様又は上記第35態様に記載の方法。
第37態様:前記アルキル基が、R 1 R 2 R 3 C-(式中、R 1 及びR 2 が独立に1~10個の炭素原子を有するアルキル基であり、R 3 が水素又は1~10個の炭素原子を有するアルキル基である)によって表される、上記第34態様~上記第36態様のいずれかに記載の方法。
第38態様:前記アルキル基が、イソプロピル、tert-ブチル、tert-アミル、sec-ブチル又はネオペンチルを含む、上記第34態様~上記第36態様のいずれかに記載の方法。
Claims (38)
- 化学式RSn(OR’)3によって表されるモノアルキルスズトリアルコキシド化合物又は化学式RSn(NR’2)3によって表されるモノアルキルスズトリアミド化合物と、
全スズ量に対して4モル%以下のジアルキルスズ化合物とを含む組成物であって、式中、
Rが、1~31個の炭素原子を有するヒドロカルビル基であり、及び
R’が、1~10個の炭素原子を有するヒドロカルビル基である、組成物。 - Rが、R1R2R3C-(式中、R1及びR2が独立に1~10個の炭素原子を有するアルキル基であり、R3が水素又は1~10個の炭素原子を有するアルキル基である)によって表される分岐アルキル配位子である、請求項1に記載の組成物。
- Rがメチル(CH3-)、エチル(CH3CH2-)、イソプロピル(CH3CH3HC-)、tert-ブチル((CH3)3C-)、tert-アミル(CH3CH2(CH3)2C-)、sec-ブチル(CH3(CH3CH2)CH-)、ネオペンチル(CH3)3CCH2-)、シクロヘキシル、シクロペンチル、シクロブチル、又はシクロプロピルを含む、請求項1に記載の組成物。
- R’がメチル基、エチル基、イソプロピル基、又はt-ブチル基を含む、請求項1~3のいずれか一項に記載の組成物。
- R’がt-アミル基を含む、請求項1~3のいずれか一項に記載の組成物。
- 約1モル%以下のジアルキルスズ化合物を含む、請求項1~5のいずれか一項に記載の組成物。
- モノアルキルスズトリアミドを含む、請求項1~6のいずれか一項に記載の組成物。
- 請求項1又は請求項4~7のいずれか一項に記載の組成物と、有機溶媒とを含む溶液。
- 約0.005M~約0.5Mの濃度を有する請求項8に記載の溶液であって、前記溶媒がアルコールを含む、溶液。
- Rがメチル(CH3-)、エチル(CH3CH2-)、イソプロピル(CH3CH3HC-)、tert-ブチル((CH3)3C-)、tert-アミル(CH3CH3(CH3)2C-)、sec-ブチル(CH3(CH3CH2)CH-)、ネオペンチル(CH3)3CCH2-)、シクロヘキシル、シクロペンチル、シクロブチル、又はシクロプロピルを含み、R’がメチル基、エチル基、イソプロピル基、t-ブチル基、又はt-アミル基を含む、請求項8又は請求項9に記載の溶液。
- ジアルキルスズの汚染が少ないモノアルキルスズトリアルコキシド化合物を選択的に形成するための方法であって、
請求項7に記載の組成物を式HOR’’によって表されるアルコールと有機溶媒中で反応させてRSnOR’’3(式中、R’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である)を形成して、スズの全量に対して4モル%以下のジアルキルスズ化合物を有する生成物組成物を形成する工程を含む方法。 - 化学式RSn-(NR’COR’’)3(式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、及び
R’及びR’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である)によって表されるモノアルキルトリアミドスズ化合物を含む組成物。 - R’がメチル基である、請求項12に記載の組成物。
- R’’がメチル基である、請求項12又は請求項13に記載の組成物。
- Rがメチル(CH3-)、エチル(CH3CH2-)、イソプロピル(CH3CH3HC-)、tert-ブチル((CH3)3C-)、t-アミル(CH3CH3(CH3CH2)C-)、sec-ブチル(CH3(CH3CH2)HC-)、ネオペンチル(CH3)3CCH2-)、シクロヘキシル、シクロペンチル、シクロブチル、又はシクロプロピルを含む、請求項12に記載の組成物。
- 結晶性であり、約1モルパーセント以下のジアルキルスズ汚染物質を含む、請求項12~15のいずれか一項に記載の組成物。
- RMgX、R2Zn、RZnNR’2、又はそれらの組合せからなる群から選択されるアルキル化剤を有機溶媒を含む溶液中でSn(NR’2)4と反応させる工程であって、
式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、
Xがハロゲンであり、及び
R’が、1~10個の炭素原子を有するヒドロカルビル基である工程を含む、モノアルキルスズトリアミド化合物を形成するための方法。 - 前記溶液が、約0.01M~約5Mの間のスズの濃度を有する、請求項17に記載の方法。
- 前記有機溶媒がアルカン、芳香族炭化水素、エーテル、又はそれらの混合物を含む、請求項17又は請求項18に記載の方法。
- 前記溶液が、スズ試薬及び前記アルキル化剤の化学量論的反応に対して約±25%のアルキル化剤の濃度を有する、請求項17~19のいずれか一項に記載の方法。
- 前記反応が、周辺光から遮蔽して前記アルキル化剤の段階的な添加によって不活性雰囲気下で行われる、請求項17~20のいずれか一項に記載の方法。
- 前記アルキル化剤が10分~90分間にわたって段階的に添加される、請求項17~21のいずれか一項に記載の方法。
- 前記反応が15分~24時間にわたって-100℃~100℃の温度で行われる、請求項17~21のいずれか一項に記載の方法。
- 前記溶液がスズに対して0.25~4モル当量の中性配位塩基をさらに含む、請求項17~23のいずれか一項に記載の方法。
- RSn(NR’2)3を式HOR’’によって表されるアルコールと有機溶媒中で反応させてRSnOR’’3を形成する工程であって、RSn(NR’2)3反応体が約4モル%以下のジアルキルスズ汚染物質を有し、請求項1に記載の方法の生成物であり、式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’及びR’’が独立に、1~10個の炭素原子を有するヒドロカルビル基である、工程を含む、ジアルキルスズの汚染が少ないモノアルキルスズトリアルコキシド化合物を選択的に形成するための方法。
- 前記反応が、前記スズのモル量に対して約0.5モル%~約15モル%の量の四座キレート剤を使用して行われる、請求項25に記載の方法。
- 化学式RSn(NR’2)3によって表されるモノアルキルスズトリアミド化合物をアミド(R’’CONHR’’’)と有機溶媒中で反応させる工程であって、式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’、R’’及びR’’’が独立に、1~8個の炭素原子を有するヒドロカルビルである工程と、
式RSn(NR’’’COR’’)3によって表される固体生成物を集める工程とを含む、モノアルキルトリアミドスズを形成するための方法。 - 前記モノアルキルスズトリアミドが約0.1M~約8Mの初期濃度であり、前記溶媒がアルカン、芳香族炭化水素、又はエーテルである、請求項27に記載の方法。
- 前記アミドが、少なくとも約2分間にわたって段階的に添加される、請求項27又は請求項28に記載の方法。
- 前記固体生成物が結晶性であり、スズに対してジアルキルスズ化合物の汚染物質約1モルパーセント以下を有する、請求項27~29のいずれか一項に記載の方法。
- モノアルキルトリアミドスズ化合物(RSn(NR’’’COR’’)3)をアルカリアルコキシド化合物(QOR’、式中、Qがアルカリ金属原子である)と有機溶媒中で反応させて、化学式RSn(OR’)3(式中、Rが、1~31個の炭素原子を有するヒドロカルビル基であり、並びにR’、R’’及びR’’’が独立に、1~10個の炭素を有するヒドロカルビル基である)によって表される生成物化合物を形成する工程を含む、モノアルキルスズトリアルコキシドを形成するための方法。
- アルコキシド供与化合物が、少なくとも化学量論量において提供される、請求項31に記載の方法。
- 前記溶媒がアルカン、芳香族炭化水素、又はエーテルである、請求項31又は請求項32に記載の方法。
- モノアルキルスズ(monoalkyl tine)トリアルコキシドと四座非平面錯生成剤とのブレンドを蒸留する工程を含む、モノアルキルスズトリアルコキシドを精製するための方法。
- 前記四座非平面錯生成剤がTRENを含む、請求項34に記載の方法。
- 前記四座非平面錯生成剤が、スズのモル量に対して約0.5モル%~約15モル%の量で存在している、請求項34又は請求項35に記載の方法。
- 前記アルキル基が、R1R2R3C-(式中、R1及びR2が独立に1~10個の炭素原子を有するアルキル基であり、R3が水素又は1~10個の炭素原子を有するアルキル基である)によって表される、請求項34~36のいずれか一項に記載の方法。
- 前記アルキル基が、イソプロピル、tert-ブチル、tert-アミル、sec-ブチル又はネオペンチルを含む、請求項34~36のいずれか一項に記載の方法。
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US15/950,286 US11673903B2 (en) | 2018-04-11 | 2018-04-11 | Monoalkyl tin compounds with low polyalkyl contamination, their compositions and methods |
| US15/950,286 | 2018-04-11 | ||
| US15/950,292 | 2018-04-11 | ||
| US15/950,292 US10787466B2 (en) | 2018-04-11 | 2018-04-11 | Monoalkyl tin compounds with low polyalkyl contamination, their compositions and methods |
| PCT/US2019/024470 WO2019199467A1 (en) | 2018-04-11 | 2019-03-28 | Monoalkyl tin compounds with low polyalkyl contamination, their compositions and methods |
| JP2020554212A JP7305671B2 (ja) | 2018-04-11 | 2019-03-28 | ポリアルキル汚染が少ないモノアルキルスズ化合物、それらの組成物及び方法 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020554212A Division JP7305671B2 (ja) | 2018-04-11 | 2019-03-28 | ポリアルキル汚染が少ないモノアルキルスズ化合物、それらの組成物及び方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2023123712A true JP2023123712A (ja) | 2023-09-05 |
Family
ID=68164483
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020554212A Active JP7305671B2 (ja) | 2018-04-11 | 2019-03-28 | ポリアルキル汚染が少ないモノアルキルスズ化合物、それらの組成物及び方法 |
| JP2023105608A Pending JP2023123712A (ja) | 2018-04-11 | 2023-06-28 | ポリアルキル汚染が少ないモノアルキルスズ化合物、それらの組成物及び方法 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020554212A Active JP7305671B2 (ja) | 2018-04-11 | 2019-03-28 | ポリアルキル汚染が少ないモノアルキルスズ化合物、それらの組成物及び方法 |
Country Status (6)
| Country | Link |
|---|---|
| JP (2) | JP7305671B2 (ja) |
| KR (5) | KR20230107905A (ja) |
| CN (1) | CN112088335A (ja) |
| CA (2) | CA3219374A1 (ja) |
| TW (3) | TWI752308B (ja) |
| WO (1) | WO2019199467A1 (ja) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TW202404985A (zh) * | 2018-06-21 | 2024-02-01 | 美商英培雅股份有限公司 | 包含溶劑與單烷基錫三烷氧化物之混合物的溶液 |
| US11092890B2 (en) | 2018-07-31 | 2021-08-17 | Samsung Sdi Co., Ltd. | Semiconductor resist composition, and method of forming patterns using the composition |
| US11092889B2 (en) | 2018-07-31 | 2021-08-17 | Samsung Sdi Co., Ltd. | Semiconductor resist composition, and method of forming patterns using the composition |
| KR102538092B1 (ko) * | 2020-04-17 | 2023-05-26 | 삼성에스디아이 주식회사 | 반도체 포토레지스트용 조성물 및 이를 이용한 패턴 형성 방법 |
| KR102577300B1 (ko) * | 2020-04-17 | 2023-09-08 | 삼성에스디아이 주식회사 | 반도체 포토레지스트용 조성물 및 이를 이용한 패턴 형성 방법 |
| TWI765767B (zh) * | 2020-07-03 | 2022-05-21 | 美商恩特葛瑞斯股份有限公司 | 製備有機錫化合物的方法 |
| KR102586112B1 (ko) * | 2020-09-14 | 2023-10-05 | 삼성에스디아이 주식회사 | 반도체 포토레지스트용 조성물 및 이를 이용한 패턴 형성 방법 |
| US11697660B2 (en) * | 2021-01-29 | 2023-07-11 | Entegris, Inc. | Process for preparing organotin compounds |
| KR102382858B1 (ko) | 2021-08-06 | 2022-04-08 | 주식회사 레이크머티리얼즈 | 트리할로 주석 화합물의 제조방법 및 이를 포함하는 트리아미드 주석 화합물의 제조방법 |
| KR20240049398A (ko) | 2021-09-13 | 2024-04-16 | 젤리스트 인코퍼레이티드 | 옥소스탄네이트가 풍부한 필름을 제조하기 위한 방법 및 전구체 |
| WO2023043682A1 (en) * | 2021-09-14 | 2023-03-23 | Entegris, Inc. | Synthesis of fluoroalkyl tin precursors |
| US20230391803A1 (en) * | 2022-06-03 | 2023-12-07 | Entegris, Inc. | Compositions and related methods of alkyltintrihalides |
| WO2023245047A1 (en) * | 2022-06-17 | 2023-12-21 | Lam Research Corporation | Tin precursors for deposition of euv dry resist |
| WO2024076481A1 (en) * | 2022-10-04 | 2024-04-11 | Gelest, Inc. | Cyclic azastannane and cyclic oxostannane compounds and methods for preparation thereof |
| CN116410222B (zh) * | 2023-06-09 | 2023-08-08 | 研峰科技(北京)有限公司 | 一种叔丁基三(二甲氨基)锡烷的合成方法 |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2822409A (en) * | 1954-04-29 | 1958-02-04 | Gulf Research Development Co | Distilling alcohols in presence of amines |
| GB1051391A (ja) * | 1959-12-24 | |||
| US3240795A (en) * | 1962-07-02 | 1966-03-15 | Exxon Research Engineering Co | Organometallic compounds |
| DE3109309A1 (de) * | 1981-03-11 | 1982-09-30 | Siemens AG, 1000 Berlin und 8000 München | "verfahren zur herstellung einer fluessigkristallanzeige" |
| US5008417A (en) * | 1990-05-21 | 1991-04-16 | Ethyl Corporation | Haloalkylation process |
| FR2775914B1 (fr) * | 1998-03-13 | 2000-04-21 | Saint Gobain Vitrage | Procede de depot de couches a base d'oxyde(s) metallique(s) |
| JP4320564B2 (ja) * | 2002-06-28 | 2009-08-26 | 日亜化学工業株式会社 | 透明導電膜形成用組成物、透明導電膜形成用溶液および透明導電膜の形成方法 |
| JP2005298433A (ja) | 2004-04-15 | 2005-10-27 | Asahi Kasei Chemicals Corp | ジアルキルスズアルコキシド |
| EP1743898A1 (en) * | 2005-07-12 | 2007-01-17 | Arkema Vlissingen B.V. | Process for the preparation of monoalkyl tin trihalides and dialkyl tin dihalides |
| EP2123659A1 (en) * | 2008-05-15 | 2009-11-25 | Arkema France | High purity monoalkyltin compounds and uses thereof |
| MX344578B (es) * | 2010-07-01 | 2016-12-20 | Pmc Organometallix Inc | Proceso para preparar trihaluros de monoalquilestaño y dihaluros de dialquilestaño. |
| US9281207B2 (en) * | 2011-02-28 | 2016-03-08 | Inpria Corporation | Solution processible hardmasks for high resolution lithography |
| JP6784670B2 (ja) * | 2014-10-23 | 2020-11-11 | インプリア・コーポレイションInpria Corporation | 有機金属溶液に基づいた高解像度パターニング組成物および対応する方法 |
| TR201808874T4 (tr) * | 2015-06-05 | 2018-07-23 | Galata Chemicals Llc | Yüksek saflıkta mono-oktilkalay ve di-metilkalay bileşikleri içeren stabilizatörler. |
| EP3391148B1 (en) * | 2015-10-13 | 2021-09-15 | Inpria Corporation | Organotin oxide hydroxide patterning compositions, precursors, and patterning |
| US10011737B2 (en) * | 2016-03-23 | 2018-07-03 | Eastman Chemical Company | Curable polyester polyols and their use in thermosetting soft feel coating formulations |
-
2019
- 2019-03-28 WO PCT/US2019/024470 patent/WO2019199467A1/en active Application Filing
- 2019-03-28 KR KR1020237023086A patent/KR20230107905A/ko not_active Application Discontinuation
- 2019-03-28 JP JP2020554212A patent/JP7305671B2/ja active Active
- 2019-03-28 KR KR1020207013930A patent/KR20200058572A/ko active Application Filing
- 2019-03-28 KR KR1020237023292A patent/KR102560231B1/ko active IP Right Grant
- 2019-03-28 CA CA3219374A patent/CA3219374A1/en active Pending
- 2019-03-28 CA CA3080934A patent/CA3080934C/en active Active
- 2019-03-28 CN CN201980020757.8A patent/CN112088335A/zh active Pending
- 2019-03-28 KR KR1020217016553A patent/KR102556775B1/ko active IP Right Grant
- 2019-03-28 KR KR1020217016552A patent/KR102645923B1/ko active IP Right Grant
- 2019-04-11 TW TW108112721A patent/TWI752308B/zh active
- 2019-04-11 TW TW112100607A patent/TWI827433B/zh active
- 2019-04-11 TW TW111100052A patent/TWI790882B/zh active
-
2023
- 2023-06-28 JP JP2023105608A patent/JP2023123712A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| KR20200058572A (ko) | 2020-05-27 |
| KR20230109781A (ko) | 2023-07-20 |
| TWI790882B (zh) | 2023-01-21 |
| KR102556775B1 (ko) | 2023-07-17 |
| CA3219374A1 (en) | 2019-10-17 |
| KR20210068152A (ko) | 2021-06-08 |
| TWI827433B (zh) | 2023-12-21 |
| WO2019199467A9 (en) | 2020-11-19 |
| KR20230107905A (ko) | 2023-07-18 |
| JP2021519340A (ja) | 2021-08-10 |
| CA3080934A1 (en) | 2019-10-17 |
| TW202214665A (zh) | 2022-04-16 |
| TW201943725A (zh) | 2019-11-16 |
| CA3080934C (en) | 2024-01-02 |
| KR102560231B1 (ko) | 2023-07-26 |
| JP7305671B2 (ja) | 2023-07-10 |
| WO2019199467A1 (en) | 2019-10-17 |
| TW202317593A (zh) | 2023-05-01 |
| KR102645923B1 (ko) | 2024-03-08 |
| TWI752308B (zh) | 2022-01-11 |
| CN112088335A (zh) | 2020-12-15 |
| KR20210068153A (ko) | 2021-06-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7305671B2 (ja) | ポリアルキル汚染が少ないモノアルキルスズ化合物、それらの組成物及び方法 | |
| US10975109B2 (en) | Monoalkyl tin compounds with low polyalkyl contamination, their compositions and methods | |
| US20210024552A1 (en) | Monoalkyl tin compounds with low polyalkyl contamination, their compositions and methods | |
| JP2804089B2 (ja) | ジオルガノジアルコキシシランの選択的製造方法 | |
| Horstmann et al. | Fluoride complexation by bidentate silicon Lewis acids | |
| WO2022165381A1 (en) | Process for preparing organotin compounds | |
| JP2009263316A (ja) | 不完全縮合オリゴシルセスキオキサンの製造方法 | |
| Higashiya et al. | Synthesis of fluorinated α-sila-β-diketones and their copper (II) complexes | |
| TW202413384A (zh) | 高純度液體組合物及其應用 | |
| KR100371312B1 (ko) | 알킬(아미노)디알콕시실란의 제조 방법 | |
| JP6665437B2 (ja) | 第3級アルキルシラン及び第3級アルキルアルコキシシランの製造方法 | |
| JP2020527584A5 (ja) | ||
| WO2024076481A1 (en) | Cyclic azastannane and cyclic oxostannane compounds and methods for preparation thereof | |
| JP5926797B2 (ja) | ビス(パーフルオロアルキル)ホスフィン酸無水物の調製方法 | |
| JP2020002077A (ja) | 第三級アルキルシランの製造方法及び第三級アルキルアルコキシシランの製造方法 | |
| WO2024035914A1 (en) | High purity tin compounds containing unsaturated substituent and method for preparation thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230706 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230706 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20240513 |