JP2021528096A - エキソソーム細胞外小胞及びその使用方法 - Google Patents
エキソソーム細胞外小胞及びその使用方法 Download PDFInfo
- Publication number
- JP2021528096A JP2021528096A JP2020573481A JP2020573481A JP2021528096A JP 2021528096 A JP2021528096 A JP 2021528096A JP 2020573481 A JP2020573481 A JP 2020573481A JP 2020573481 A JP2020573481 A JP 2020573481A JP 2021528096 A JP2021528096 A JP 2021528096A
- Authority
- JP
- Japan
- Prior art keywords
- lnp
- exosome
- cells
- lipid
- modified rna
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 210000001808 exosome Anatomy 0.000 title claims abstract description 283
- 210000004027 cell Anatomy 0.000 claims abstract description 365
- 238000000034 method Methods 0.000 claims abstract description 79
- 101000987586 Homo sapiens Eosinophil peroxidase Proteins 0.000 claims description 369
- 102000044890 human EPO Human genes 0.000 claims description 369
- 150000002632 lipids Chemical class 0.000 claims description 293
- 238000012384 transportation and delivery Methods 0.000 claims description 104
- 238000011282 treatment Methods 0.000 claims description 76
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 70
- 239000008194 pharmaceutical composition Substances 0.000 claims description 60
- 239000002773 nucleotide Substances 0.000 claims description 58
- 125000003729 nucleotide group Chemical group 0.000 claims description 58
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 claims description 56
- 150000003904 phospholipids Chemical class 0.000 claims description 53
- 208000035475 disorder Diseases 0.000 claims description 50
- NRLNQCOGCKAESA-KWXKLSQISA-N [(6z,9z,28z,31z)-heptatriaconta-6,9,28,31-tetraen-19-yl] 4-(dimethylamino)butanoate Chemical compound CCCCC\C=C/C\C=C/CCCCCCCCC(OC(=O)CCCN(C)C)CCCCCCCC\C=C/C\C=C/CCCCC NRLNQCOGCKAESA-KWXKLSQISA-N 0.000 claims description 43
- NRJAVPSFFCBXDT-HUESYALOSA-N 1,2-distearoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCCCCCCCCCCC NRJAVPSFFCBXDT-HUESYALOSA-N 0.000 claims description 33
- 235000012000 cholesterol Nutrition 0.000 claims description 28
- 210000000130 stem cell Anatomy 0.000 claims description 25
- 102000004127 Cytokines Human genes 0.000 claims description 24
- 108090000695 Cytokines Proteins 0.000 claims description 24
- 239000002105 nanoparticle Substances 0.000 claims description 24
- 230000028993 immune response Effects 0.000 claims description 21
- 201000010099 disease Diseases 0.000 claims description 20
- 102000003951 Erythropoietin Human genes 0.000 claims description 17
- 108090000394 Erythropoietin Proteins 0.000 claims description 17
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 17
- 210000003719 b-lymphocyte Anatomy 0.000 claims description 17
- 230000028709 inflammatory response Effects 0.000 claims description 17
- 210000001616 monocyte Anatomy 0.000 claims description 17
- 210000002966 serum Anatomy 0.000 claims description 17
- 101000920686 Homo sapiens Erythropoietin Proteins 0.000 claims description 16
- 210000002865 immune cell Anatomy 0.000 claims description 16
- 210000002919 epithelial cell Anatomy 0.000 claims description 15
- 239000006143 cell culture medium Substances 0.000 claims description 12
- 238000012606 in vitro cell culture Methods 0.000 claims description 12
- 239000003937 drug carrier Substances 0.000 claims description 11
- 102100021943 C-C motif chemokine 2 Human genes 0.000 claims description 10
- 101710155857 C-C motif chemokine 2 Proteins 0.000 claims description 10
- 108010055166 Chemokine CCL5 Proteins 0.000 claims description 9
- 206010058314 Dysplasia Diseases 0.000 claims description 9
- 108090001005 Interleukin-6 Proteins 0.000 claims description 9
- 102000004889 Interleukin-6 Human genes 0.000 claims description 9
- 208000007502 anemia Diseases 0.000 claims description 9
- 208000026278 immune system disease Diseases 0.000 claims description 9
- 208000027866 inflammatory disease Diseases 0.000 claims description 9
- 230000002829 reductive effect Effects 0.000 claims description 9
- 210000000278 spinal cord Anatomy 0.000 claims description 9
- 102100032367 C-C motif chemokine 5 Human genes 0.000 claims description 8
- 102100025248 C-X-C motif chemokine 10 Human genes 0.000 claims description 8
- 101710098275 C-X-C motif chemokine 10 Proteins 0.000 claims description 8
- 208000024556 Mendelian disease Diseases 0.000 claims description 7
- 230000001413 cellular effect Effects 0.000 claims description 7
- 238000000338 in vitro Methods 0.000 claims description 5
- 230000008569 process Effects 0.000 claims description 5
- 230000002265 prevention Effects 0.000 claims description 4
- 239000000203 mixture Substances 0.000 abstract description 31
- 208000027418 Wounds and injury Diseases 0.000 abstract 1
- 230000006378 damage Effects 0.000 abstract 1
- 238000010586 diagram Methods 0.000 abstract 1
- 208000014674 injury Diseases 0.000 abstract 1
- 108020004999 messenger RNA Proteins 0.000 description 328
- 229920002477 rna polymer Polymers 0.000 description 186
- 241000699666 Mus <mouse, genus> Species 0.000 description 102
- 241000699670 Mus sp. Species 0.000 description 66
- 108090000623 proteins and genes Proteins 0.000 description 55
- 102000004169 proteins and genes Human genes 0.000 description 53
- 210000000056 organ Anatomy 0.000 description 48
- 229920001223 polyethylene glycol Polymers 0.000 description 40
- 238000011529 RT qPCR Methods 0.000 description 35
- 238000002347 injection Methods 0.000 description 34
- 239000007924 injection Substances 0.000 description 34
- 238000002965 ELISA Methods 0.000 description 27
- 238000011002 quantification Methods 0.000 description 27
- 238000012360 testing method Methods 0.000 description 26
- 230000000694 effects Effects 0.000 description 24
- 239000002245 particle Substances 0.000 description 24
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 23
- 238000000692 Student's t-test Methods 0.000 description 23
- 238000001543 one-way ANOVA Methods 0.000 description 23
- 238000003762 quantitative reverse transcription PCR Methods 0.000 description 21
- 238000012353 t test Methods 0.000 description 21
- 210000001519 tissue Anatomy 0.000 description 20
- 238000002474 experimental method Methods 0.000 description 19
- 239000000523 sample Substances 0.000 description 19
- 210000001163 endosome Anatomy 0.000 description 18
- 239000006228 supernatant Substances 0.000 description 18
- 238000001514 detection method Methods 0.000 description 17
- 230000001225 therapeutic effect Effects 0.000 description 17
- 210000000952 spleen Anatomy 0.000 description 16
- 102100025222 CD63 antigen Human genes 0.000 description 15
- 101000934368 Homo sapiens CD63 antigen Proteins 0.000 description 15
- 238000004458 analytical method Methods 0.000 description 14
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 14
- 210000000805 cytoplasm Anatomy 0.000 description 13
- 239000003981 vehicle Substances 0.000 description 12
- 210000002216 heart Anatomy 0.000 description 11
- 210000004185 liver Anatomy 0.000 description 11
- 241001465754 Metazoa Species 0.000 description 10
- 238000003556 assay Methods 0.000 description 10
- 230000001404 mediated effect Effects 0.000 description 10
- 239000000243 solution Substances 0.000 description 10
- 210000004369 blood Anatomy 0.000 description 9
- 239000008280 blood Substances 0.000 description 9
- 238000009472 formulation Methods 0.000 description 9
- 230000003834 intracellular effect Effects 0.000 description 9
- 210000004072 lung Anatomy 0.000 description 9
- 239000013642 negative control Substances 0.000 description 9
- 238000002360 preparation method Methods 0.000 description 9
- 238000012546 transfer Methods 0.000 description 9
- 230000014616 translation Effects 0.000 description 9
- 230000012202 endocytosis Effects 0.000 description 8
- 210000003734 kidney Anatomy 0.000 description 8
- 239000012528 membrane Substances 0.000 description 8
- 210000000496 pancreas Anatomy 0.000 description 8
- 239000002096 quantum dot Substances 0.000 description 8
- 239000000126 substance Substances 0.000 description 8
- 230000032258 transport Effects 0.000 description 8
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 7
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 7
- 102000006382 Ribonucleases Human genes 0.000 description 7
- 108010083644 Ribonucleases Proteins 0.000 description 7
- 229920004890 Triton X-100 Polymers 0.000 description 7
- 210000004556 brain Anatomy 0.000 description 7
- 239000000872 buffer Substances 0.000 description 7
- 239000003153 chemical reaction reagent Substances 0.000 description 7
- -1 cholesterol) Chemical class 0.000 description 7
- 239000002299 complementary DNA Substances 0.000 description 7
- 239000012228 culture supernatant Substances 0.000 description 7
- 239000003814 drug Substances 0.000 description 7
- 238000001727 in vivo Methods 0.000 description 7
- 238000011534 incubation Methods 0.000 description 7
- 238000002156 mixing Methods 0.000 description 7
- 210000001541 thymus gland Anatomy 0.000 description 7
- 239000013504 Triton X-100 Substances 0.000 description 6
- 238000010162 Tukey test Methods 0.000 description 6
- 239000011324 bead Substances 0.000 description 6
- 230000008859 change Effects 0.000 description 6
- 239000002552 dosage form Substances 0.000 description 6
- 238000005516 engineering process Methods 0.000 description 6
- 239000000546 pharmaceutical excipient Substances 0.000 description 6
- 208000024891 symptom Diseases 0.000 description 6
- 238000005199 ultracentrifugation Methods 0.000 description 6
- 108091054442 EV proteins Proteins 0.000 description 5
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 5
- 108020002230 Pancreatic Ribonuclease Proteins 0.000 description 5
- 102000005891 Pancreatic ribonuclease Human genes 0.000 description 5
- 239000004480 active ingredient Substances 0.000 description 5
- 230000004663 cell proliferation Effects 0.000 description 5
- 239000003636 conditioned culture medium Substances 0.000 description 5
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 5
- 230000003248 secreting effect Effects 0.000 description 5
- ANRHNWWPFJCPAZ-UHFFFAOYSA-M thionine Chemical compound [Cl-].C1=CC(N)=CC2=[S+]C3=CC(N)=CC=C3N=C21 ANRHNWWPFJCPAZ-UHFFFAOYSA-M 0.000 description 5
- 238000001946 ultra-performance liquid chromatography-mass spectrometry Methods 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 description 4
- 238000008157 ELISA kit Methods 0.000 description 4
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 description 4
- 101000946889 Homo sapiens Monocyte differentiation antigen CD14 Proteins 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- 102100035877 Monocyte differentiation antigen CD14 Human genes 0.000 description 4
- 206010028980 Neoplasm Diseases 0.000 description 4
- 239000012980 RPMI-1640 medium Substances 0.000 description 4
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 4
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 4
- 230000002146 bilateral effect Effects 0.000 description 4
- 201000011510 cancer Diseases 0.000 description 4
- 125000002091 cationic group Chemical group 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 238000005538 encapsulation Methods 0.000 description 4
- 230000028023 exocytosis Effects 0.000 description 4
- 230000002163 immunogen Effects 0.000 description 4
- 238000001990 intravenous administration Methods 0.000 description 4
- 239000010410 layer Substances 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 239000002609 medium Substances 0.000 description 4
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 4
- 231100000252 nontoxic Toxicity 0.000 description 4
- 230000003000 nontoxic effect Effects 0.000 description 4
- 230000005298 paramagnetic effect Effects 0.000 description 4
- 230000037361 pathway Effects 0.000 description 4
- 229920001184 polypeptide Polymers 0.000 description 4
- 102000004196 processed proteins & peptides Human genes 0.000 description 4
- 108090000765 processed proteins & peptides Proteins 0.000 description 4
- 230000000770 proinflammatory effect Effects 0.000 description 4
- DAEPDZWVDSPTHF-UHFFFAOYSA-M sodium pyruvate Chemical compound [Na+].CC(=O)C([O-])=O DAEPDZWVDSPTHF-UHFFFAOYSA-M 0.000 description 4
- 238000002560 therapeutic procedure Methods 0.000 description 4
- 231100000419 toxicity Toxicity 0.000 description 4
- 230000001988 toxicity Effects 0.000 description 4
- KILNVBDSWZSGLL-KXQOOQHDSA-N 1,2-dihexadecanoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCCCCCCCCC KILNVBDSWZSGLL-KXQOOQHDSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 108010074328 Interferon-gamma Proteins 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- 239000000232 Lipid Bilayer Substances 0.000 description 3
- 108091028043 Nucleic acid sequence Proteins 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 3
- 238000002123 RNA extraction Methods 0.000 description 3
- 229930182558 Sterol Natural products 0.000 description 3
- 230000004900 autophagic degradation Effects 0.000 description 3
- 238000009739 binding Methods 0.000 description 3
- 230000004071 biological effect Effects 0.000 description 3
- 230000015556 catabolic process Effects 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 108091092328 cellular RNA Proteins 0.000 description 3
- 238000012512 characterization method Methods 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 238000006731 degradation reaction Methods 0.000 description 3
- 238000012217 deletion Methods 0.000 description 3
- 230000037430 deletion Effects 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 229940105423 erythropoietin Drugs 0.000 description 3
- 230000004927 fusion Effects 0.000 description 3
- 239000001963 growth medium Substances 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- 239000006166 lysate Substances 0.000 description 3
- 230000005291 magnetic effect Effects 0.000 description 3
- 239000004005 microsphere Substances 0.000 description 3
- 208000010125 myocardial infarction Diseases 0.000 description 3
- 230000004770 neurodegeneration Effects 0.000 description 3
- 230000007935 neutral effect Effects 0.000 description 3
- 102000039446 nucleic acids Human genes 0.000 description 3
- 108020004707 nucleic acids Proteins 0.000 description 3
- 150000007523 nucleic acids Chemical class 0.000 description 3
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 3
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 description 3
- 150000003432 sterols Chemical class 0.000 description 3
- 235000003702 sterols Nutrition 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 229940124597 therapeutic agent Drugs 0.000 description 3
- 231100000331 toxic Toxicity 0.000 description 3
- 230000002588 toxic effect Effects 0.000 description 3
- DJJCXFVJDGTHFX-XVFCMESISA-N uridine 5'-monophosphate Chemical compound O[C@@H]1[C@H](O)[C@@H](COP(O)(O)=O)O[C@H]1N1C(=O)NC(=O)C=C1 DJJCXFVJDGTHFX-XVFCMESISA-N 0.000 description 3
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 206010057248 Cell death Diseases 0.000 description 2
- 102000019034 Chemokines Human genes 0.000 description 2
- 108010012236 Chemokines Proteins 0.000 description 2
- GZDFHIJNHHMENY-UHFFFAOYSA-N Dimethyl dicarbonate Chemical compound COC(=O)OC(=O)OC GZDFHIJNHHMENY-UHFFFAOYSA-N 0.000 description 2
- 241000196324 Embryophyta Species 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 2
- 102100037850 Interferon gamma Human genes 0.000 description 2
- 108010065805 Interleukin-12 Proteins 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- 229930182816 L-glutamine Natural products 0.000 description 2
- 206010057249 Phagocytosis Diseases 0.000 description 2
- 108020004459 Small interfering RNA Proteins 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- DJJCXFVJDGTHFX-UHFFFAOYSA-N Uridinemonophosphate Natural products OC1C(O)C(COP(O)(O)=O)OC1N1C(=O)NC(=O)C=C1 DJJCXFVJDGTHFX-UHFFFAOYSA-N 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 238000010171 animal model Methods 0.000 description 2
- 238000003149 assay kit Methods 0.000 description 2
- 230000004888 barrier function Effects 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 239000007979 citrate buffer Substances 0.000 description 2
- 210000004748 cultured cell Anatomy 0.000 description 2
- 238000012258 culturing Methods 0.000 description 2
- 230000009089 cytolysis Effects 0.000 description 2
- 238000000502 dialysis Methods 0.000 description 2
- 238000010828 elution Methods 0.000 description 2
- 210000000981 epithelium Anatomy 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 235000019253 formic acid Nutrition 0.000 description 2
- 230000009368 gene silencing by RNA Effects 0.000 description 2
- 229960004956 glycerylphosphorylcholine Drugs 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 230000009851 immunogenic response Effects 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 230000007794 irritation Effects 0.000 description 2
- 230000002045 lasting effect Effects 0.000 description 2
- 231100001231 less toxic Toxicity 0.000 description 2
- 239000013554 lipid monolayer Substances 0.000 description 2
- 239000002502 liposome Substances 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 210000002864 mononuclear phagocyte Anatomy 0.000 description 2
- 208000015122 neurodegenerative disease Diseases 0.000 description 2
- 108091027963 non-coding RNA Proteins 0.000 description 2
- 102000042567 non-coding RNA Human genes 0.000 description 2
- 239000002777 nucleoside Substances 0.000 description 2
- 230000008782 phagocytosis Effects 0.000 description 2
- 239000008363 phosphate buffer Substances 0.000 description 2
- 230000036470 plasma concentration Effects 0.000 description 2
- 239000013641 positive control Substances 0.000 description 2
- 238000004094 preconcentration Methods 0.000 description 2
- 210000004990 primary immune cell Anatomy 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 229940054269 sodium pyruvate Drugs 0.000 description 2
- 230000006641 stabilisation Effects 0.000 description 2
- 238000011105 stabilization Methods 0.000 description 2
- 238000007619 statistical method Methods 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 239000003643 water by type Substances 0.000 description 2
- XLKQWAMTMYIQMG-SVUPRYTISA-N (2-{[(2r)-2,3-bis[(4z,7z,10z,13z,16z,19z)-docosa-4,7,10,13,16,19-hexaenoyloxy]propyl phosphonato]oxy}ethyl)trimethylazanium Chemical compound CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CC XLKQWAMTMYIQMG-SVUPRYTISA-N 0.000 description 1
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 1
- LGJMUZUPVCAVPU-ANOYILKDSA-N (3s,8r,9s,10s,13r,14s,17r)-17-[(2r,5s)-5-ethyl-6-methylheptan-2-yl]-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-3-ol Chemical class C1CC2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CC[C@H](CC)C(C)C)[C@@]1(C)CC2 LGJMUZUPVCAVPU-ANOYILKDSA-N 0.000 description 1
- DSNRWDQKZIEDDB-SQYFZQSCSA-N 1,2-dioleoyl-sn-glycero-3-phospho-(1'-sn-glycerol) Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OC[C@H](COP(O)(=O)OC[C@@H](O)CO)OC(=O)CCCCCCC\C=C/CCCCCCCC DSNRWDQKZIEDDB-SQYFZQSCSA-N 0.000 description 1
- SNKAWJBJQDLSFF-NVKMUCNASA-N 1,2-dioleoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCC\C=C/CCCCCCCC SNKAWJBJQDLSFF-NVKMUCNASA-N 0.000 description 1
- WTJKGGKOPKCXLL-VYOBOKEXSA-N 1-hexadecanoyl-2-(9Z-octadecenoyl)-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCC\C=C/CCCCCCCC WTJKGGKOPKCXLL-VYOBOKEXSA-N 0.000 description 1
- LRFJOIPOPUJUMI-KWXKLSQISA-N 2-[2,2-bis[(9z,12z)-octadeca-9,12-dienyl]-1,3-dioxolan-4-yl]-n,n-dimethylethanamine Chemical compound CCCCC\C=C/C\C=C/CCCCCCCCC1(CCCCCCCC\C=C/C\C=C/CCCCC)OCC(CCN(C)C)O1 LRFJOIPOPUJUMI-KWXKLSQISA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 206010002091 Anaesthesia Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 102100036170 C-X-C motif chemokine 9 Human genes 0.000 description 1
- 101710085500 C-X-C motif chemokine 9 Proteins 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 108010008978 Chemokine CXCL10 Proteins 0.000 description 1
- 102000006579 Chemokine CXCL10 Human genes 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 108010092408 Eosinophil Peroxidase Proteins 0.000 description 1
- DNVPQKQSNYMLRS-NXVQYWJNSA-N Ergosterol Natural products CC(C)[C@@H](C)C=C[C@H](C)[C@H]1CC[C@H]2C3=CC=C4C[C@@H](O)CC[C@]4(C)[C@@H]3CC[C@]12C DNVPQKQSNYMLRS-NXVQYWJNSA-N 0.000 description 1
- 102100031939 Erythropoietin Human genes 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 102100031181 Glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 description 1
- JZNWSCPGTDBMEW-UHFFFAOYSA-N Glycerophosphorylethanolamin Natural products NCCOP(O)(=O)OCC(O)CO JZNWSCPGTDBMEW-UHFFFAOYSA-N 0.000 description 1
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 1
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 description 1
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 1
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 101100021481 Homo sapiens LNPK gene Proteins 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 208000026350 Inborn Genetic disease Diseases 0.000 description 1
- 108010002352 Interleukin-1 Proteins 0.000 description 1
- 108010002350 Interleukin-2 Proteins 0.000 description 1
- 108010002386 Interleukin-3 Proteins 0.000 description 1
- 108090000978 Interleukin-4 Proteins 0.000 description 1
- 108010002616 Interleukin-5 Proteins 0.000 description 1
- 108090001007 Interleukin-8 Proteins 0.000 description 1
- 108010002335 Interleukin-9 Proteins 0.000 description 1
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 1
- 102100032352 Leukemia inhibitory factor Human genes 0.000 description 1
- 108090000581 Leukemia inhibitory factor Proteins 0.000 description 1
- 108700011259 MicroRNAs Proteins 0.000 description 1
- 101710151805 Mitochondrial intermediate peptidase 1 Proteins 0.000 description 1
- 101710151803 Mitochondrial intermediate peptidase 2 Proteins 0.000 description 1
- 108700026244 Open Reading Frames Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 240000007594 Oryza sativa Species 0.000 description 1
- 235000007164 Oryza sativa Nutrition 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 238000012228 RNA interference-mediated gene silencing Methods 0.000 description 1
- 230000006819 RNA synthesis Effects 0.000 description 1
- 108091030071 RNAI Proteins 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 108091058545 Secretory proteins Proteins 0.000 description 1
- 102000040739 Secretory proteins Human genes 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 229920002472 Starch Chemical class 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- XYNPYHXGMWJBLV-VXPJTDKGSA-N Tomatidine Chemical compound O([C@@H]1[C@@H]([C@]2(CC[C@@H]3[C@@]4(C)CC[C@H](O)C[C@@H]4CC[C@H]3[C@@H]2C1)C)[C@@H]1C)[C@@]11CC[C@H](C)CN1 XYNPYHXGMWJBLV-VXPJTDKGSA-N 0.000 description 1
- QMGSCYSTMWRURP-UHFFFAOYSA-N Tomatine Natural products CC1CCC2(NC1)OC3CC4C5CCC6CC(CCC6(C)C5CCC4(C)C3C2C)OC7OC(CO)C(OC8OC(CO)C(O)C(OC9OCC(O)C(O)C9OC%10OC(CO)C(O)C(O)C%10O)C8O)C(O)C7O QMGSCYSTMWRURP-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- NJFCSWSRXWCWHV-USYZEHPZSA-N [(2R)-2,3-bis(octadec-1-enoxy)propyl] 2-(trimethylazaniumyl)ethyl phosphate Chemical compound CCCCCCCCCCCCCCCCC=COC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC=CCCCCCCCCCCCCCCCC NJFCSWSRXWCWHV-USYZEHPZSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 150000001413 amino acids Chemical group 0.000 description 1
- 229940067621 aminobutyrate Drugs 0.000 description 1
- 230000037005 anaesthesia Effects 0.000 description 1
- 238000000540 analysis of variance Methods 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000012131 assay buffer Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 238000004166 bioassay Methods 0.000 description 1
- 239000003124 biologic agent Substances 0.000 description 1
- 239000013060 biological fluid Substances 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 239000000090 biomarker Substances 0.000 description 1
- 238000001815 biotherapy Methods 0.000 description 1
- 230000008499 blood brain barrier function Effects 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 210000001218 blood-brain barrier Anatomy 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 235000004420 brassicasterol Nutrition 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- NKWPZUCBCARRDP-UHFFFAOYSA-L calcium bicarbonate Chemical compound [Ca+2].OC([O-])=O.OC([O-])=O NKWPZUCBCARRDP-UHFFFAOYSA-L 0.000 description 1
- 229910000020 calcium bicarbonate Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 235000000431 campesterol Nutrition 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 230000004637 cellular stress Effects 0.000 description 1
- 230000004700 cellular uptake Effects 0.000 description 1
- 239000001913 cellulose Chemical class 0.000 description 1
- 229920002678 cellulose Chemical class 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 150000001783 ceramides Chemical class 0.000 description 1
- 235000013339 cereals Nutrition 0.000 description 1
- 238000007385 chemical modification Methods 0.000 description 1
- 230000001143 conditioned effect Effects 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 239000013068 control sample Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 230000009260 cross reactivity Effects 0.000 description 1
- 230000001461 cytolytic effect Effects 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000000432 density-gradient centrifugation Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 150000001982 diacylglycerols Chemical class 0.000 description 1
- 125000005265 dialkylamine group Chemical class 0.000 description 1
- 150000001985 dialkylglycerols Chemical class 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 230000009429 distress Effects 0.000 description 1
- 238000002296 dynamic light scattering Methods 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 230000002828 effect on organs or tissue Effects 0.000 description 1
- 230000004651 endocytosis pathway Effects 0.000 description 1
- 210000003038 endothelium Anatomy 0.000 description 1
- 210000003989 endothelium vascular Anatomy 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 150000002137 ergosterols Chemical class 0.000 description 1
- 239000003797 essential amino acid Substances 0.000 description 1
- 235000020776 essential amino acid Nutrition 0.000 description 1
- 239000005038 ethylene vinyl acetate Substances 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 150000002197 fecosterols Chemical class 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 230000002538 fungal effect Effects 0.000 description 1
- BTCSSZJGUNDROE-UHFFFAOYSA-N gamma-aminobutyric acid Chemical compound NCCCC(O)=O BTCSSZJGUNDROE-UHFFFAOYSA-N 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 208000016361 genetic disease Diseases 0.000 description 1
- 108020004445 glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 1
- PEDCQBHIVMGVHV-UHFFFAOYSA-N glycerol Substances OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 1
- 125000003827 glycol group Chemical group 0.000 description 1
- 238000003306 harvesting Methods 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 102000052441 human LNPK Human genes 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- 238000005462 in vivo assay Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 229940025708 injectable product Drugs 0.000 description 1
- 229940102213 injectable suspension Drugs 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 229960002725 isoflurane Drugs 0.000 description 1
- 239000007951 isotonicity adjuster Substances 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 230000002934 lysing effect Effects 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- VLBPIWYTPAXCFJ-XMMPIXPASA-N lysophosphatidylcholine O-16:0/0:0 Chemical compound CCCCCCCCCCCCCCCCOC[C@@H](O)COP([O-])(=O)OCC[N+](C)(C)C VLBPIWYTPAXCFJ-XMMPIXPASA-N 0.000 description 1
- 230000006674 lysosomal degradation Effects 0.000 description 1
- 230000002132 lysosomal effect Effects 0.000 description 1
- 210000003712 lysosome Anatomy 0.000 description 1
- 230000001868 lysosomic effect Effects 0.000 description 1
- 206010025482 malaise Diseases 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 239000002679 microRNA Substances 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- NFQBIAXADRDUGK-KWXKLSQISA-N n,n-dimethyl-2,3-bis[(9z,12z)-octadeca-9,12-dienoxy]propan-1-amine Chemical compound CCCCC\C=C/C\C=C/CCCCCCCCOCC(CN(C)C)OCCCCCCCC\C=C/C\C=C/CCCCC NFQBIAXADRDUGK-KWXKLSQISA-N 0.000 description 1
- 239000002086 nanomaterial Substances 0.000 description 1
- 150000002790 naphthalenes Chemical class 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 150000003833 nucleoside derivatives Chemical class 0.000 description 1
- 125000003835 nucleoside group Chemical group 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 1
- 150000008103 phosphatidic acids Chemical class 0.000 description 1
- 150000008104 phosphatidylethanolamines Chemical class 0.000 description 1
- 125000004437 phosphorous atom Chemical group 0.000 description 1
- 230000004962 physiological condition Effects 0.000 description 1
- 230000003169 placental effect Effects 0.000 description 1
- 235000002378 plant sterols Nutrition 0.000 description 1
- 229920001200 poly(ethylene-vinyl acetate) Polymers 0.000 description 1
- 229920001515 polyalkylene glycol Polymers 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 229940068977 polysorbate 20 Drugs 0.000 description 1
- 230000001376 precipitating effect Effects 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 238000002331 protein detection Methods 0.000 description 1
- 238000000751 protein extraction Methods 0.000 description 1
- 239000012460 protein solution Substances 0.000 description 1
- 238000003908 quality control method Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 235000009566 rice Nutrition 0.000 description 1
- 238000005464 sample preparation method Methods 0.000 description 1
- 210000003752 saphenous vein Anatomy 0.000 description 1
- 125000005471 saturated fatty acid group Chemical group 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- PWRIIDWSQYQFQD-UHFFFAOYSA-N sisunine Natural products CC1CCC2(NC1)OC3CC4C5CCC6CC(CCC6(C)C5CCC4(C)C3C2C)OC7OC(CO)C(OC8OC(CO)C(O)C(OC9OC(CO)C(O)C(O)C9OC%10OC(CO)C(O)C(O)C%10O)C8O)C(O)C7O PWRIIDWSQYQFQD-UHFFFAOYSA-N 0.000 description 1
- 235000015500 sitosterol Nutrition 0.000 description 1
- 229940083492 sitosterols Drugs 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- JJGWLCLUQNFDIS-GTSONSFRSA-M sodium;1-[6-[5-[(3as,4s,6ar)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]hexanoyloxy]-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCCCCNC(=O)CCCC[C@H]1[C@H]2NC(=O)N[C@H]2CS1 JJGWLCLUQNFDIS-GTSONSFRSA-M 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 239000012086 standard solution Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 235000016831 stigmasterol Nutrition 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 230000035882 stress Effects 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 230000000153 supplemental effect Effects 0.000 description 1
- 238000012385 systemic delivery Methods 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 231100001274 therapeutic index Toxicity 0.000 description 1
- 230000004797 therapeutic response Effects 0.000 description 1
- XYNPYHXGMWJBLV-OFMODGJOSA-N tomatidine Natural products O[C@@H]1C[C@H]2[C@@](C)([C@@H]3[C@H]([C@H]4[C@@](C)([C@H]5[C@@H](C)[C@]6(O[C@H]5C4)NC[C@@H](C)CC6)CC3)CC2)CC1 XYNPYHXGMWJBLV-OFMODGJOSA-N 0.000 description 1
- REJLGAUYTKNVJM-SGXCCWNXSA-N tomatine Chemical compound O([C@H]1[C@H](O)[C@@H](CO)O[C@H]([C@@H]1O[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)O[C@H]1[C@@H](CO)O[C@H]([C@@H]([C@H]1O)O)O[C@@H]1C[C@@H]2CC[C@H]3[C@@H]4C[C@H]5[C@@H]([C@]4(CC[C@@H]3[C@@]2(C)CC1)C)[C@@H]([C@@]1(NC[C@@H](C)CC1)O5)C)[C@@H]1OC[C@@H](O)[C@H](O)[C@H]1O REJLGAUYTKNVJM-SGXCCWNXSA-N 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- GPRLSGONYQIRFK-MNYXATJNSA-N triton Chemical compound [3H+] GPRLSGONYQIRFK-MNYXATJNSA-N 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 230000029663 wound healing Effects 0.000 description 1
- 235000004835 α-tocopherol Nutrition 0.000 description 1
- 150000003772 α-tocopherols Chemical class 0.000 description 1
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/127—Liposomes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/127—Liposomes
- A61K9/1271—Non-conventional liposomes, e.g. PEGylated liposomes, liposomes coated with polymers
- A61K9/1272—Non-conventional liposomes, e.g. PEGylated liposomes, liposomes coated with polymers with substantial amounts of non-phosphatidyl, i.e. non-acylglycerophosphate, surfactants as bilayer-forming substances, e.g. cationic lipids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/7115—Nucleic acids or oligonucleotides having modified bases, i.e. other than adenine, guanine, cytosine, uracil or thymine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/127—Liposomes
- A61K9/1271—Non-conventional liposomes, e.g. PEGylated liposomes, liposomes coated with polymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/53—DNA (RNA) vaccination
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55555—Liposomes; Vesicles, e.g. nanoparticles; Spheres, e.g. nanospheres; Polymers
Abstract
【選択図】なし
Description
様々な実施形態において、本開示は、少なくとも1つのエキソソーム(例えば、本明細書に記載のエキソソームのいずれか)を含む医薬組成物を提供する。一部の実施形態では、医薬組成物は、複数のエキソソームを含む。本明細書で使用される場合、用語「医薬組成物」は、被験者への投与に好適な他の成分、例えば、薬学的に許容可能な担体及び/又は賦形剤に加えて、少なくとも1つのエキソソームの調製物を指す。本明細書に提供される医薬組成物は、投与を可能にし、その後、有効成分の意図される生物活性を提供し、且つ/又は治療効果を達成するような形態である。本明細書に提供される医薬組成物は、好ましくは、製剤が投与される被験者に対して許容できない毒性の追加成分を一切含有しない。
様々な実施形態では、本開示は、有効量のエキソソーム又は少なくとも1つのエキソソームを含む医薬組成物(例えば、本明細書に記載のエキソソーム又は医薬組成物のいずれか)と細胞を接触させ、これにより修飾RNAを細胞に送達することによって、修飾RNAを細胞に送達する方法を提供する。
脂質ナノ粒子(LNP)の製剤化及び特性決定
2つの異なるタイプのLNP、すなわち、修飾hEPO mRNA(858ヌクレオチド)(5meC、Ψ)(Trilink)を含有するDLin−MC3−DMA(MC3−LNP)及びDLin−DMA LNP(DD−LNP)は、以前記載されている(Yanez Arteta et al.(2018)PNAS 115(15):E3351−60)通りに、4つの異なる脂質成分と一緒にmRNAを沈殿させることによって調製した。4つの成分は、以下:低pHでイオン化可能な(カチオン性)イオン化脂質(DLin−MC3−DMA又はDLin−DMA);2つのヘルパー脂質(DSPC及びコレステロール);並びにPEG化脂質(PEG2000−DMPE)を含んだ。MilliQ−waterに溶解させたmRNA、100mMクエン酸バッファー(pH3)、及びMilliQ−waterを混合して、50mMクエン酸塩の溶液を取得することにより、hEPO mRNA水溶液を調製した。4つの脂質成分(イオン化脂質:DSPC:コレステロール:PEG2000−DMPE=50:10:38.5:1.5モルパーセント)及び総脂質含量12.5mMの組成物を用いて、エタノール中の脂質溶液(99.5%)を調製した。容積調合比がAq:EtOH=3:1で、定全流量が12mL/分のNanoAssemblr(Precision Nanosystems)マイクロ流体混合システムで、mRNA及び脂質溶液を混合した。混合時に、イオン化脂質上の窒素原子とmRNA鎖上のリン原子の比は、3.1であった。「空」のLNP(すなわち、mRNAを含まないLNP)が調製された場合には、エタノール相を50mMクエン酸バッファー(pH3)のみと混合した。調製されたLNP溶液の初期0.35mLと最終0.05mLを廃棄し、容積の残りをサンプル画分として収集した。
ヒト上皮HTB−177(NCI−H460)細胞株をAmerican Type Culture Collection(ATCC)から購入し、ATCCガイドラインに記載される通りに培養した。ピルビン酸ナトリウム及びHEPESを含まず、重炭酸ナトリウムを含有するRPMI−1640増殖培地(Sigma Aldrich)に、5%CO2の存在下、37℃で、エキソソーム欠失ウシ胎仔血清(FBS)(Sigma Aldrich)、1%のL−グルタミン(2mM)(Thermo Fisher Scientific)及び1%ペニシリン−ストレプトマイシン(10,000U/mL)(Thermo Fisher Scientific)を添加した。熱不活性化FBSは、70Tiロータ(Beckman Coulter)を備えるOptima L−100 XP超遠心分離機において120,000×g、4℃で2時間の超遠心分離によりエキソソームを欠失させ、エキソソーム欠失上清を0.2μmフィルタで濾過した。
ヒト上皮(HTB−177)細胞を、30mLの増殖培地に175Tフラスコ当たり3×106細胞の密度で接種し、24時間インキュベートした。24時間のインキュベーション後、1%ヒト血清(Sigma Aldrich)の存在下、フラスコ当たり100μgのhEPO mRNAを含有する1mLのDD−LNP又はMC3−LNPで細胞を処理した。1mLのLNP溶液中100μgのhEPO mRNAは、以下:(1)日目:200μLのLNP(20μgのmRNA);(2)日目:400μLのLNP(40μgのmRNA);(3)日目:400μLのLNP(40μgのmRNA)のように3つの異なる用量で投与し、96時間後に採取した。同量(200μL、400μL、400μL)の対応する空のDD−LNP又は空のMC3−LNP(すなわち、mRNAを含まないLNP)で処理した細胞、並びに非処理の細胞を陰性対照として使用した。
以前記載されている(El−Andaloussi et al.(2012)Nat Protoc.7(12):2112−26)通りに、LNP処置細胞の馴化培地及び陰性対照からEVを単離した。手短には、細胞残屑を除去するために、4K15遠心分離機(Sigma)により、4℃、3000×gで15分間遠心分離した。得られた上清を収集し、4℃、60,000×gで35分間の超遠心分離後、0.2μmフィルタによる濾過を実施して、直径が200nm未満のEVを取得した。続いて、濾過した上清を4℃、120,000×gで70分間超遠心分離して、EVをペレット化した。EVペレットを適切な量(50〜80μL)のPBS(Sigma Aldrich)中に再懸濁させた。全ての超遠心分離工程は、70Tiロータ(Beckman Coulter)を用いたOptima L−100 XP超遠心分離機で実施した。
miRCURY(商標)RNA単離キット−細胞及び植物(Exiqon)を用いて、製造者の指示に従い、EV及びLNP処理細胞から全RNAを単離した。全RNAは、Qubit 2.0フルオロメータ(Thermo Fisher Scientific)を用いて定量した。NanoDrop 1000(Thermo Fisher Scientific)を用いて、RNA品質(230/260比)を評価した。
Hamamatsu C11440−50B/A11893−02カメラを備えたNanoSight LM10計器(Malvern Panalytical)を用いて、HTB−177 MC3−EV及び非処理EVを粒径(nm)及び濃度(粒子/mL)について評価した。解析の前に、粒子を0.1μM濾過PBS(Sigma)中で500倍希釈して、視野内の粒子数をフレーム当たり180粒子未満に減少させた。3回の独立した測定(生物学的反復)をスキャッターモードで実施した。各EVサンプルについての測定読取りは、個別のサンプル及び手動での温度モニタリングに応じて、調節したカメラレベル(10〜16)及び検出閾値(5〜15)、各々25フレーム毎秒(fps)で、60秒間5キャプチャーにて取得した。ブラー・マックスジャンプ距離(Blur and Max Jump Distance)は自動に設定した。NanoSight Fluorescent NTA LM10ソフトウェア バージョン3.3(Malvern Panalytical)を用いて、読取り、収集、及びデータ解析を実施した。
EV、LNP投与後のそれらの親細胞の溶解物、及び対応する陰性対照におけるhEPO mRNAを、定量的リアルタイムPCR(RT−qPCR)を用いて定量した。RNA収率に基づき、0.25〜1μgの全EV RNA及び細胞の全RNAを、大容量cDNAキット(Thermo Fisher Scientific)を用いてcDNAに変換した。製造者の指示に従い、ViiA(商標)7 instrument(Thermo Fisher Scientific)でのTaqManプローブアッセイを用いて、hEPO mRNAの定量に100ngの全cDNAを使用した。2μgの純粋なhEPO mRNA(TrilinkからのRNA)を逆転写し、得られたcDNAを段階希釈(10倍)して、7つの標準(最高点:100ng)を調製し、これらを3回技術反復することにより、標準曲線を作成した。続いて、EV cDNA及び細胞cDNAをhEPO mRNA解析のために使用し;最小R2>0.975の標準曲線に対して、絶対定量を補間した。GAPDHを内標準として使用した。hEPO mRNAのモル量を計算するために、以下のように推定した:1モルhEPO mRNA=858hEPO mRNAヌクレオチド。
HTB−177細胞を、前述したように、100μgのCy5−mRNA(Trilink)を含有するMC3−LNPで処理した。非処理細胞を対照として含んだ。96時間後、分画超遠心分離(前濃縮)により、LNP処理細胞(MC3−EV)及び非処理細胞(EV)の培地から全EVを単離し、PBSに再懸濁させた後、定量した。前濃縮後、親和性に基づく方法を用いて、CD63/CD9陽性EVを単離し、FACSにより、Cy5−mRNAの存在について評価した。細胞培地についてのエキソソーム−ヒトCD63単離/検出試薬(Thermo Fisher Scientific)を使用して、製造者の指示に従い、CD63陽性EVを常磁性Dynabeadsに固定化した。結合反応の際に、20μLの常磁性Dynabeadsを25μg又は50μgの全MC3−EVと一緒にインキュベートした。陰性対照として、20μLの常磁性Dynabeadsを等量のPBS(EVなし)と一緒にインキュベートした。CD63陽性EVの固定化後、EVをマウス抗ヒトPE−CD9抗体(BD Pharmingen、Cat.No.555372)で、製造者の指示に従い染色した。BD FACSLyric system(BD Biosciences)によりEVを取得した後、CD9及びCy5−mRNAを検出した。FlowJoソフトウェア(TreeStar Inc.)を用いて、データを解析した。実験は、生物学的二重反復で実施した。
LNPとEVを直接混合した後、様々な割合(量)のLNP及びEVを用いて、37℃でインキュベート(細胞の非存在下)した。いずれの事前の処理も受けていない2つの異なる割合(量)のEVを300μLのDD−LNP又はMC3−LNP(39μgのhEPO mRNA)と一緒に、37℃の30mLのPBS中で2時間インキュベートした。第1のセットアップにおいて、EVとLNPとの割合は、200μgのEV+300μLのLNP(1×)であったが、第2のセットアップでは、この割合は、50μgのEV+300μLのLNP(4×)であった。2時間のインキュベーション後、超遠心分離によりEVを再度単離し、EVから全RNAを単離し、hEPO mRNAをqPCRにより定量して、LNPからEVへのhEPO mRNAの直接移入を評価した。陰性対照として、等量のDD−LNP又はMC3−LNPを、EVを含まないPBS中でインキュベートした後、超遠心分離した。陽性対照として、hEPO mRNAを含有するDD−LNP又はMC3−LNPを細胞に投与した後、EVを単離した(それぞれ、DD−EV又はMC3−EV)。RNAを単離し、hEPO mRNAをqPCRにより定量した。実験は生物学的三重反復で実施した。データは、LNPにより細胞に送達されたhEPO mRNAの投与量又はEVと直接混合したhEPO mRNAの量に対して、EV中に検出されたhEPO mRNAのパーセンテージとして表示する。反復の標準偏差(SD)と共に平均値を示す。
前述したように、100μgのhEPO mRNAを含有するMC3−LNPで、HTB−177細胞を処理した。非処理細胞を対照として含んだ。96時間後、EVを単離し、定量した。初めに、RNase A活性(Thermo Fisher Scientific)の効率を評価するために、280ngの純粋なhEPO mRNA(Trilink)をRNase A(0.5μg/μL)又は等量のPBSと一緒に37℃で20分間インキュベートした。次に、同じ条件を用いて、200μgのMC3−EVをRNase Aで処理した。陰性対照として、200μgのMC3−EV及び150μgの非処理EVを、RNase Aの代わりにPBSを用いた以外は同じ条件下でインキュベートした。インキュベーション後、miRCURYTM RNA Isolationキット−Cell and Plant(Exiqon)を用いて、EVからの全RNAを単離した。EVの外部に存在する場合に、hEPO mRNA含量に対するRNase Aの作用を評価するために、hEPO mRNAをqPCRにより定量した。実験は、生物学的三重反復で実施した。
EVの画分を使用して、EV中のLNP由来イオン化脂質の存在を検定した。5〜10μLの各EVサンプル(MC3−LNP及びDD−LNP処理細胞から取得)をPBSで50倍希釈した後、トリス/EDTAバッファー中2w/v%のTriton(登録商標)X−100の混合物でさらに1+1希釈した。サンプルを37℃で30分間インキュベートした後、Single Quad Detector(SQD)(Waters)に接続したAcquity Ultra Performance LCに注入した。分析カラムは、60℃に維持したWaters Acquity UPLC(登録商標)CSH C18、1.7μm、2.1×100mmであった。流量は、水中の0.1%ギ酸(A)と、アセトニトリル及びイソプロピルアルコールの等量混合物中の0.1%ギ酸(B)との移動相を用いて、0.50mL/分であった。0.0minで10%Bを、1.0から5.0minまで85%Bに上昇させた後、7.5minまで85%Bに維持する勾配ランを適用した。勾配ランには、7.6minから9.5minまで99%Bの洗浄ステップを加えた。次に、10%Bをコンディショニングのために9.6minから12.0minまで適用した。これらの条件下で、DLin−DMAの溶離時間は6.3minであり、DLin−MC3−DMAの溶離時間は6.5minであった。エタノール99.5%に溶解させたDLin−DMA及びDLin−MC3−DMAの外部標準溶液を用いて、定量を決定した。エレクトロスプレー、ポジティブモードを用いて、SQDを実行し、DLin−MC3−DMAの溶液による自動調整を用いて調整した。カチオン性脂質の記録は、各カチオン性脂質についてM+1のSingle Ion Recording(SIR)を用いて実施した。
LNP処理の後、細胞馴化上清を収集し、hEPOタンパク質検出のために直接使用したのに対し、1%ハルト(halt)プロテアーゼ阻害剤カクテル(Thermo Fisher Scientific)の存在下、500μLのM−PER Mammalian Protein Extraction Reagent(Thermo Fisher Scientific)を用いて、細胞溶解物から全細胞タンパク質を抽出した。手短には、細胞を3次元Bio−rockerにより4℃で10分間穏やかに攪拌し、14,000×gで10分間遠心分離することにより、細胞残屑をペレット化した。得られた上清(タンパク質含有)を新しいチューブに移した。同時に、培養した上清を4K15遠心分離機(Sigma)により4℃、3000×gで15分間遠心分離して、細胞残屑を除去した。得られた上清を新しいチューブに移した。また、hEPOタンパク質は、エリスロポエチンELISAキット(STEMCELL Technologies)を用いて、製造者の指示に従い、EV溶解物中でも分析した。2μLのEV懸濁液を2μLのM−PER Mammalian Protein Extraction Reagent(Thermo Fisher Scientific)と一緒にインキュベートし、Ultrasonic cleaner(VWR)により54℃で5分間超音波処理して、EV抽出物を生成した。培養上清からの全細胞タンパク質及び全タンパク質、並びに全EVタンパク質を、Qubit 2.0フルオロメータ(Thermo Fisher Scientific)を用いて、製造者のプロトコルに従い、定量した。hEPOタンパク質を検出するために、エリスロポエチンELISAキット(STEMCELL Technologies)を製造者の指示に従って使用した。50μLの全タンパク質溶液(細胞及び培養上清の両方について)を使用し、相対標準曲線に従って、hEPOタンパク質レベルをmU/mLとして算出した。換算法(119mU=1ng)を用いて、濃度をfg/mLに変換し、細胞の総数に対して正規化した。
細胞挙動に対するLNPの作用を決定すると共に、LNP処理(DD−LNP又はMC3−LNP)に対する細胞耐容性を評価するために、DD−LNP又はMC3−LNPによる96時間の処理後に、細胞世代時間(細胞増殖)、細胞全RNA、細胞内タンパク質の総含量、及び分泌されたタンパク質の総含量を計算した。LNPによる処理後の全EV RNA及びタンパク質含量を定量することにより、EVに対するLNPの作用も検定した。
G=t/n
t=LNP投与間隔(h)
ヒト上皮(HTB−177)細胞をT175フラスコ当たり5×106細胞の密度で接種し、RPMI−1640完全培地中で培養した。MC3−LNP処理細胞から単離した600μgのMC3−EV(700ngのhEPO mRNA)、及びDD−LNP処理細胞から単離した600μgのDD−EV(1100ngのhEPO mRNA)をRPMI−1640培地中に溶解させ、以下の通り2日にわたり、独立したアッセイでレシピエント細胞に移入した:(1)日目:300μgのMC3−EV、及び(2)日目:300μgのMC3−EVを、150μgの2回の個別用量で各々8時間後。同様に、300μgのDD−EV(1日目)及び300μg(2日目)を独立したアッセイでレシピエント細胞に移入した。空のEV(hEPO mRNAを含まない)及び非処理細胞からのEVを、対照としてレシピエント細胞に送達した。48時間後、細胞及び培養上清を収集し、全RNAを単離した。hEPO mRNA及びhEPOタンパク質を、それぞれRT−qPCR及びELISAにより、前述のプロトコルに従って評価した。実験は、2回の独立した生物学的反復で実施した。
1mLのLNPが、フラスコ当たり76μgの蛍光Cy5−EGFP−mRNAを含有する(これに対し、hEPO mRNAは、100μg/mLであった)以外は前述のプロトコルに従って、蛍光シアニン5(Cy5)−EGFP−mRNAを含有する1mLのDD−LNPを様々な用量(200μL、400μL、400μL)でHTB−177細胞に送達した。LNPの投与から96時間後、馴化培地(上清)並びに親細胞を採取し、hEPO mRNA及びhEPOタンパク質について分析したか、又はさらなる試験のために保存した。空のDD−LNP(mRNAを含まない)及び非処理細胞を対照として使用した。HTB−177細胞並びに、末梢血単核細胞(PBMC、前述した通り、バフィーコートから単離される)から精製したB細胞、T細胞、及び単球などの免疫細胞をウェル当たり2×105細胞の密度で接種し、96ウェルの丸底プレート内の200μLの培地に培養し、37℃、5%CO2で一晩インキュベートした。培養細胞の24時間の刺激後、25μLのPBS溶液中のCy5−EGFP−mRNA(Trilink)を含有する78μgのDD−EVをレシピエント細胞に送達した。対照アッセイのために、空のDD−EV(EGFP−mRNAを含まない)及びネイティブEV(非処理細胞からのEV)を細胞に送達するか、又は細胞を未処理のまま残した。5時間、24時間、及び48時間のEV処理後、細胞を採取し、CD19(B細胞)、CD3(T細胞)、及びCD14(単球)(Becton−Dickinson Biosciences)に対し、モノクローナル抗体(mAb)により表面マーカについて染色した。細胞は、FACSVerse(BD Biosciences)で取得した。Cy5−EGFP−mRNAは、各細胞型における蛍光に基づいて検出し、FlowJoソフトウェア(TreeStar Inc.)を用いて、データを解析した。
0.011mg/mLの濃度でhEPO mRNAを含有するMC3−LNPを、静止条件下、37℃で、150mM NaCl(pH7.4、6.6、若しくは5.8)と一緒に、10mMクエン酸−Na2HPO4バッファー溶液中でインキュベートした。RiboGreenアッセイにおいて0.125mM TritonX−100(VWR Proteomics Grade)及び0.125mMドデシル硫酸ナトリウム(Sigma)を用い、ゼロ時点でmRNAの総量を測定した。様々なpH(pH7.4、6.6、又は5.8)のLNPから放出されたmRNAの画分を評価するために、Perkin Elmer LS55 Luminescence Spectrometer(例えば、480nm、em:525nm)を用い、Quant−iT RiboGreen RNA Reagent Assayキット(Thermo Fisher ScientificによるInvitrogen)で遊離量のmRNAを分析した。
実験手順は、ゴーテンバーグの地域実験動物倫理委員会(Regional Laboratory Animal Ethics Committee of Gothenburg,Sweden)により承認された(倫理審査申請書番号83−2015)。手順は全て、スウェーデン動物保護法(Swedish Animal Welfare Act)及び規定SJVFS 2012:26に準拠する。C57BL6/N Crl雌マウス(n=36)、9〜10週齢をCharles River Laboratory(Germany)から購入し、AstraZeneca,Molndal,Swedenにある動物施設に収容した。マウスは、標準の条件(21℃ RT、12:12h光周期、45〜55%湿度)下でケージ当たり4匹のマウスの群で飼育し、通常の固形飼料(R70、Lactamin AB)及び水を自由に摂取させた。環境エンリッチメントを提供した(カートン、木製舌圧子、及び綿ネスティングパッド)。等量の1.5μg hEPO mRNAを含有する100μLのMC3−LNP由来EV又はMC3−LNPをマウスに静脈内注射した(群当たりn=4)。100μLのPBSを対照マウスに注射した。EV及びLNPの注射から2、5、24、及び48時間後に伏在静脈(Vena Saphena)マイクロサンプリングにより、血液サンプルをマウスの群(n=4)から収集した。35μL EDTA−プレップキャピラリーチューブに収集した血液サンプルを、血漿を収集するため1700×gで遠心分離し、分析の時間まで−86℃で冷凍保存した。注射から5、24、及び96時間後、臓器を収集するために、マウス群を死なせた。イソフルラン麻酔によりマウスを鎮静させ、眼窩静脈叢から採血した後、心臓を切除した。続いて、全臓器(肝臓、腎臓、脾臓、膵臓、心臓、胸腺、肺、及び脳)を収集し、液体窒素でスナップ冷凍し、分析の時間まで−86℃で保存した。
MC3−LNP及びMC3−EVによるhEPO mRNA送達後のマウス血漿中のhEPOタンパク質を分析するために、Gyrosプラットフォーム上でhEPOアッセイを自社開発した。EZ−Link Sulfo−NHS−LC−Biotinキット(Thermo Fisher Scientific、#21327)を用いて、キット添付文書に従って、補足抗体(3F6、MAIIA Diagnostics)をビオチン化した。モノクローナル抗体標識キット(Thermo Fisher Scientific、#A20186)を用いて、検出抗体(7D3、MAIIA Diagnostics)をAlexa 647標識した。hEPOタンパク質(自社製)を用いて、12.2pg/mL〜50ng/mLの範囲で、Rexxip Aバッファー(Gyros Protein Technologies)中の標準曲線を作成した。分析前に、マウス血漿サンプルをRexxip A−maxバッファー(Gyros Protein Technologies)で1:1(v:v)希釈した。Gyrolab計器(Gyrolab xP workstation、Gyros Protein Technologies)を備えるGyrolab Bioaffy 1000 CD(Gyros Protein Technologies)でサンプルを分析した。標準曲線のために5パラメータ曲線当てはめを使用した。全ての標準及びサンプルは、10%未満のCVを有した。
1%ハルト(halt)プロテアーゼ阻害剤カクテル(Thermo Fisher Scientific)の存在下、M−PER Mammalian Protein Extraction Reagent(Thermo Fisher Scientific)を用いて、製造者の指示に従い、臓器からの全タンパク質を抽出した。手短には、Tissue Lyser II(Qiagen)中のプロテアーゼ阻害剤(Thermo Fisher Scientific)を添加した200〜350μLの溶解バッファー(組織重量に応じて)において、最大速(30Hz)で3〜5分間20〜70mgの組織を溶解させた後、4℃、10,000×gで15分間遠心分離することにより、組織残屑を全て除去した。得られた上清は、Qubit 2.0フルオロメータ(Thermo Fisher Scientific)を用いるタンパク質定量のために使用した。エリスロポエチンELISAキット(STEMCELL Technologies)を用いて、製造者の指示に従い、hEPOタンパク質検出について50μLの全タンパク質を分析した。各臓器中のhEPOタンパク質(ng)の量を相対臓器重量(g)に対して正規化した。
MC3−LNP及びMC3−EVの静脈内投与後、IL−6、KC、MCP−1、RANTES、TNFα、IFN−γ、IL−1β、及びIP−10の同時定量のために、EMD Millipore’s MILLIPLEX(登録商標)MAP Mouse Cytokine磁気ビーズキット(Merck KGaA、#MCYTOMAG−70K)により、マウスサイトカインの血漿中濃度を測定した。まず、サンプルをアッセイバッファーで1:2希釈し、次に、標準及び品質対照と一緒に96ウェルプレート内に配置した。ビーズを含有する溶液を添加し;ビーズは、特定の抗体でコーティングした磁気ミクロスフィアである。混合物を4℃で一晩インキュベートした後、各ミクロスフィアの表面上での反応を完了させるために、ストレプトアビジン−PEコンジュゲートと一緒にインキュベートした。プレートを分析装置Bio Rad Luminex 200(登録商標)上で読み取った。個別のミクロスフィアを各々同定し、そのバイオアッセイの結果を、蛍光リポータシグナルに基づいて定量化した。5パラメータロジスティック曲線当てはめ法を使用し、蛍光強度中央値(MFI)のデータを用いて、濃度を測定した。
RNeasyキット(Qiagen)を用いて、製造者の推奨に従い、マウス臓器から全RNAを単離した。Tissue Lyser II(Qiagen)中のRLTバッファー(600μL)において10〜50mgの組織を最大速(30Hz)で3〜4分間溶解させた後、20℃、10,000×gで3分間遠心分離することにより、組織残屑を全て除去した。続いて、上清をカラムに移し、さらに処理した。RNAを定量し、Qubit 2.0フルオロメータ(Thermo Fisher Scientific)を用いて、RNAを定量し、NanoDrop 1000(Thermo Fisher Scientific)を用いて、RNA品質を評価した。RNA収率に基づき、0.5〜1μgの全RNAをcDNAにレトロ転写し、100ngを用い、RT−qPCRにより、前述したプロトコルに従って、hEPO mRNAを検出した。各臓器中のhEPO mRNAの量(μg)を相対臓器重量(g)に対して正規化した。
全ての実験について、GraphPad Prism v.7(GraphPad)を用いて、統計解析を実施した。インビトロデータは、独立2群両側スチューデントt検定を用いて解析したが、例外的に、HTB−177増殖、RNA含量、及びタンパク質含量に対するLNP投与の効果については、1元配置分散分析(one−way ANOVA)、続いてテューキー(Tukey)の多重比較検定を用いて解析した(有意なP値<0.05)。マウス血漿及び臓器中のhEPO含量は、独立2群両側スチューデントt検定を用いて解析したのに対し、マウス血漿中のサイトカインのレベルは、1元配置分散分析、続いてシダックの多重比較検定を用いて解析した。P値の有意性のレベルは、以下のように表示した:*p<0.05、**p<0.01、***p<0.001、及び****p<0.0001。
実施例1:脂質ナノ粒子(LNP)の特性決定
本明細書に記載の実験で使用されるLNPは、5つの主要成分、すなわち、イオン化脂質(DLin−MC3−DMA又はDLin−DMA)、DSPC(1,2−ジステアロイル−sn−グリセロ−3−ホスホコリン)、コレステロール、PEG化脂質(PEG2000−DMPE)、及びmRNA(hEPO mRNA)を含んだ。DLin−MC3−DMAイオン化脂質を含有するLNPは、MC3−LNPと呼ばれ;DLin−DMAイオン化脂質を含有するLNPは、DD−LNPと呼ばれる。両方のLNP製剤を、ローディング効率、平均粒径、多分散指数(PDI)、及び個々のLNP成分間のモルパーセント比を含め、複数の生物物理的パラメータに関して、特性決定した(表2)。データは、表2に平均値±平均値の標準誤差(SEM)として表示する(MC3−LNP、n=4;DD−LNP、n=9)。
LNPの2つの異なる製剤による、細胞へのヒトエリスロポエチン(hEPOタンパク質)をコードするmRNAの送達を調べた。DLin−DMA−LNP(DD−LNPと称する)及びDLin−MC3−LNP(MC3−LNPと称する)を介したmRNA送達の有効性を、細胞内hEPO mRNAの量、並びに細胞内及び細胞外環境の両方で産生されたhEPOの量を決定することによって検定した。
研究から、大部分のLNPで送達されたRNAは、リソソーム分解及び/又はエンドサイトーシス再循環経路を経るのに対し、エンドソームから脱出するのは、僅かな量のみであり;例えば、LNP送達siRNAの正味脱出は、2%未満であり得ると推定されている(Semple et al.(2010)Nat Biotechnol.28(2):172−6;Sahay et al.(2013)Nat Biotechnol.31(7):653−8;Sahay et al.(2010)J Control Release 145(3):82−95)。
前述した実験は、LNPのエンドサイトーシスの後、外性hEPO mRNAをエンド−EVに組み込むことができることを示唆している(図1F及び図9)。次に、(a)EVが、その後、送達ビヒクルとして働くことにより、外性hEPO mRNAをレシピエント細胞に輸送することができるか否か;並びに(b)EVを介して細胞に送達されたhEPO mRNAが、機能性である、すなわち、mRNAを翻訳して、hEPOタンパク質を産生することができるか否かを調べた。
エンド−EVが、インビトロでhEPO mRNAを送達することができると判定した後、これらのEVが、外性mRNA(すなわち、hEPO mRNA)をインビボで送達することもできるか否かを調べた。hEPO mRNAをインビボで投与する前に、非処理の健康なC57BL6/NCrlマウスから血液を採取し、ヒトエリスロポエチンELISAによりhEPOタンパク質を検定して、レシピエントマウスにヒト型のEPOタンパク質(hEPO)が欠失しており、且つこれを発現しないことを確認した。予想通り、非処理のマウスの血漿は、hEPOタンパク質について陰性であった(図12)。
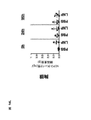
MC3−LNPに比べて、EVが、hEPO mRNAをいかに効率的に送達するかを決定するために、インビボでのLNP及びEVによるhEPO mRNAの送達後に、hEPOタンパク質の産生を比較した。臓器において、LNPによるhEPO mRNA送達からのhEPOタンパク質の量は、脾臓を除いて概ねEVと同等であり、脾臓は、タンパク質産生に有意な差を示し、それに心臓が続いた(有意差はより小さい)(図5)。血液中のhEPOタンパク質の量は、EVと比較して、LNP送達の方が高かった(図5)。さらに、組織に対するMC3−LNP及びMC3−EVの作用を検定した。MC3−LNP及びMC3−EVは、レシピエントマウスの臓器重量に有意な作用を示さなかった(図15A〜H)。
EVが、レシピエントマウスに対しLNPと比べて低免疫原性であるか否かを調べるために、単回用量のMC3−LNP(マウス1匹当たり1.5μgのhEPO mRNA)及びMC3−EV(マウス1匹当たり1.5μgのhEPO mRNA)をC57BL6/NCrlマウスに静脈内注射した。2つの時間間隔(5時間及び24時間)で、一般に免疫及び炎症反応に関与する8つの異なるサイトカインの濃度をマウス血漿中で測定した。注射から5時間後に検出された複数の炎症誘発性サイトカイン(特に、IL−6、IP−10、RANTES、MCP−1、及びKC)の分泌レベルは、EV送達後よりLNP送達後で有意に高かった(図6A〜E)。
LNP−mRNAが、EVにより担持されていることを確認するために、HTB−177細胞を、100μgのCy5−mRNAを含有するMC3−LNPで処理するか、又はそれなしで処理した。96時間後、LNP処理細胞(MC3−EV)及び非処理細胞(EV)の培地から全EVを分画超遠心分離により単離し、PBS中に再懸濁させた後、定量した。25μg若しくは50μgの全MC3−EV又は全非処理EVを、抗CD63抗体と共役した20μLの常磁性Dynabeadsと一緒にインキュベートした後、Exosome−Human CD63 Isolation/Detectionキット(Thermo Fisher Scientific)を用いて、CD63陽性EVを特異的に単離した。次に、CD63陽性EVを、マウス抗ヒトPE−CD9抗体(BD Pharmingen、Cat.No.555372)で染色してから、Cy5−mRNA検出についてFACSにより分析した。FACS分析から、非処理細胞からの免疫沈降EV(50μgアッセイ)の約96%は、CD63及びCD9について陽性であったが、mRNAについては陰性であったことが明らかにされた。対照的に、LNP−mRNA処理細胞からの免疫沈降EV(50μgアッセイ)の約88%は、CD63及びCD9について陽性であったが、26%が、Cy5−mRNAを含有するLNPのエンドサイトーシス後に分泌されたmRNA(Cy5−mRNA)を含有する(図17A)。陰性対照(ビーズのみ、並びに非処理細胞から得られるCD63/CD9陽性EV)では、Cy5−mRNAシグナルは一切検出されず、これは、mRNAがEV(CD63/CD9陽性EV)により担持されていることを示している。
mRNAが、EV膜と結合しているのではなく、EV内部に位置し、且つ保護されていることを確認するために、hEPO mRNAを含有するMC3−EVをRNase処理に曝露した。RNase処理の後、全RNAをEVから単離し、qPCRにより、hEPO mRNAを定量した。RNaseの効率的なエンドヌクレオチド結合分解活性(EVフリーRNAに示される)にもかかわらず、RNaseで処理しなかったMC3−EVと比較して、RNase処理MC3−EVでは、hEPO mRNA含量に2Ct倍率変化の減少しか認められなかった。3回の生物学的反復(n=3)で実験を実施し、hEPO mRNA qPCRデータを散布ドットプロット及び平均標準偏差(SD)として表す(図17B)。RNase処理なしの非処理細胞から得られたEVは、陰性対照として使用した。送達mRNAの僅かな部分がEVの外膜層に結合している可能性はあるが、ほとんどのhEPO mRNAは、エンドヌクレオチド結合分解活性から保護されて、EV内に存在することが判明した。
Claims (92)
- 以下:
(a)修飾RNAを含む1つ以上の脂質ナノ粒子(LNP)を提供するステップ;
(b)細胞によるLNP取込みを可能にする条件下で、1つ以上の前記細胞をLNPと接触させるステップ;及び
(c)前記1つ以上の細胞により産生されるエキソソームを単離するステップを含むプロセスにより調製される修飾RNAを含む単離エキソソームであって、ここで、前記少なくとも1つの単離エキソソームは、前記修飾RNAを含む、単離エキソソーム。 - 前記LNPが、少なくとも1つのイオン化脂質、リン脂質、構造脂質、及び/又はPEG脂質を含む、請求項1に記載のエキソソーム。
- 前記少なくとも1つのイオン化脂質が、DLin−MC3−DMA及び/又はDLin−DMAである、請求項2に記載のエキソソーム。
- 前記少なくとも1つのイオン化脂質が、DLin−MC3−DMAである、請求項2又は3のいずれか1項に記載のエキソソーム。
- 前記少なくとも1つのイオン化脂質が、DLin−DMAである、請求項2又は3のいずれか1項に記載のエキソソーム。
- 前記少なくとも1つのリン脂質が、DSPCである、請求項2〜5のいずれか1項に記載のエキソソーム。
- 前記少なくとも1つの構造脂質が、コレステロールである、請求項2〜6のいずれか1項に記載のエキソソーム。
- 前記少なくとも1つのPEG脂質が、PEG−DMPE又はPEG2000−DMPEである、請求項2〜7のいずれか1項に記載のエキソソーム。
- 前記LNPが、DLin−MC3−DMA若しくはDLin−DMAであるイオン化脂質、DSPCであるリン脂質、コレステロールである構造脂質、及び/又はPEG−DMPE若しくはPEG2000−DMPEであるPEG脂質を含有する、請求項1〜8のいずれか1項に記載のエキソソーム。
- 前記LNPが、DLin−MC3−DMAであるイオン化脂質、DSPCであるリン脂質、コレステロールである構造脂質、及びPEG−DMPE若しくはPEG2000−DMPEであるPEG脂質を含有する、請求項9に記載のエキソソーム。
- 前記LNPが、DLin−DMAであるイオン化脂質、DSPCであるリン脂質、コレステロールである構造脂質、及びPEG−DMPE若しくはPEG2000−DMPEであるPEG脂質を含有する、請求項9に記載のエキソソーム。
- 前記LNPが、約2:1〜約4:1、又は約4:1、約3:1、又は約2:1のイオン化脂質:修飾RNAヌクレオチドモル比を有する、請求項1〜11のいずれか1項に記載のエキソソーム。
- 前記LNPが、約3:1のイオン化脂質:修飾RNAヌクレオチドモル比を有する、請求項1〜12のいずれか1項に記載のエキソソーム。
- 前記エキソソームが、少なくとも1つのイオン化脂質、リン脂質、構造脂質、及び/又はPEG脂質を含む、請求項1〜13のいずれか1項に記載のエキソソーム。
- 前記少なくとも1つのイオン化脂質、リン脂質、構造脂質、及び/又はPEG脂質が、LNPに由来する、請求項14に記載のエキソソーム。
- 前記少なくとも1つのイオン化脂質が、DLin−MC3−DMA及び/又はDLin−DMAである、請求項14又は15に記載のエキソソーム。
- 前記少なくとも1つのイオン化脂質が、DLin−MC3−DMAである、請求項14〜16のいずれか1項に記載のエキソソーム。
- 前記少なくとも1つのイオン化脂質が、DLin−DMAである、請求項14〜16のいずれか1項に記載のエキソソーム。
- 前記少なくとも1つのリン脂質が、DSPCである、請求項14〜18のいずれか1項に記載のエキソソーム。
- 前記少なくとも1つの構造脂質が、コレステロールである、請求項14〜19のいずれか1項に記載のエキソソーム。
- 前記エキソソームが、DLin−MC3−DMA若しくはDLin−DMAであるイオン化脂質、DSPCであるリン脂質、及び/又はコレステロールである構造脂質を含有する、請求項1〜20のいずれか1項に記載のエキソソーム。
- 前記エキソソームが、DLin−MC3−DMAであるイオン化脂質、DSPCであるリン脂質、及びコレステロールである構造脂質を含有する、請求項21に記載のエキソソーム。
- 前記エキソソームが、DLin−DMAであるイオン化脂質、DSPCであるリン脂質、及びコレステロールである構造脂質を含有する、請求項21に記載のエキソソーム。
- 前記エキソソームが、約1:1〜約3:1、又は約3:1、約2:1、約1:1、又は約1:1未満のイオン化脂質:修飾RNAヌクレオチドモル比を含む、請求項1〜23のいずれか1項に記載のエキソソーム。
- 前記エキソソームが、約1:1又は約1:1未満のイオン化脂質:修飾RNAヌクレオチドモル比を含む、請求項1〜24のいずれか1項に記載のエキソソーム。
- 前記エキソソームは、前記LNPが含むイオン化脂質:修飾RNAヌクレオチドモル比より低いイオン化脂質:修飾RNAヌクレオチドモル比を含む、請求項1〜25のいずれか1項に記載のエキソソーム。
- 前記エキソソームは、約1:1又は約1:1未満のイオン化脂質:修飾RNAヌクレオチドモル比を含み、前記LNPが、約3:1のイオン化脂質:修飾RNAヌクレオチドモル比を含む、請求項1〜26のいずれか1項に記載のエキソソーム。
- 前記エキソソームが、約30nm〜約300nmの直径を有する、請求項1〜27のいずれか1項に記載のエキソソーム。
- 前記エキソソームが、約40nm〜約150nmの直径を有する、請求項1〜28のいずれか1項に記載のエキソソーム。
- 前記細胞が、被験者から取得される、請求項1〜29のいずれか1項に記載のエキソソーム。
- 前記細胞が、上皮細胞、免疫細胞、前駆細胞、又は幹細胞である、請求項1〜30のいずれか1項に記載のエキソソーム。
- 前記細胞が、Bリンパ球、Tリンパ球、又は単球である、請求項1〜31のいずれか1項に記載のエキソソーム。
- 前記修飾RNAが、エリスロポエチンポリペプチドをコードする、請求項1〜32のいずれか1項に記載のエキソソーム。
- 前記修飾RNAが、ヒトエリスロポエチンポリペプチドをコードする、請求項1〜33のいずれか1項に記載のエキソソーム。
- 前記修飾RNAが、配列番号1のエリスロポエチンポリペプチドをコードする、請求項1〜34のいずれか1項に記載のエキソソーム。
- 前記プロセスが、インビトロで実施される、請求項1〜35のいずれか1項に記載のエキソソーム。
- 1つ以上の細胞を前記LNPと接触させるステップが、ヒト血清の存在下で実施される、請求項1〜36のいずれか1項に記載のエキソソーム。
- 前記ヒト血清が、約0.5体積%、約1体積%、又は約1.5体積%で存在する、請求項37に記載のエキソソーム。
- 前記ヒト血清が、約1体積%で存在する、請求項37又は38に記載のエキソソーム。
- 1つ以上の細胞を前記LNPと接触させるステップが、前記1つ以上の細胞を、少なくとも2つ、少なくとも3つ、又は少なくとも4つの異なる用量の前記LNPと接触させることを含む、請求項1〜39のいずれか1項に記載のエキソソーム。
- 1つ以上の細胞を前記LNPと接触させるステップが、前記1つ以上の細胞を、少なくとも3つの異なる用量の前記LNPと接触させることを含む、請求項1〜40のいずれか1項に記載のエキソソーム。
- エキソソームを単離するステップが、インビトロ細胞培地のサンプルからエキソソームを単離するステップを含む、請求項1〜41のいずれか1項に記載のエキソソーム。
- 請求項1〜42のいずれか1項に記載の少なくとも1つのエキソソームと、薬学的に許容可能な担体とを含む医薬組成物。
- 修飾RNAを細胞に送達する方法であって、有効量の請求項1〜42のいずれか1項に記載のエキソソーム又は請求項43に記載の医薬組成物と前記細胞を接触させ、これにより、前記修飾RNAを前記細胞に送達するステップを含む方法。
- 前記細胞を接触させるステップが、前記エキソソーム若しくは医薬組成物をインビトロ細胞培養物に添加するか、又は前記エキソソーム若しくは医薬組成物を被験者に投与するステップを含む、請求項44に記載の方法。
- 前記細胞が、インビトロ細胞培地中に存在する、請求項44又は45に記載の方法。
- 前記細胞が、被験者から取得される、請求項44〜46のいずれか1項に記載の方法。
- 前記細胞が、被験者に存在する、請求項44又は45に記載の方法。
- 前記細胞が、上皮細胞、免疫細胞、前駆細胞、又は幹細胞である、請求項44〜48のいずれか1項に記載の方法。
- 前記細胞が、Bリンパ球、Tリンパ球、又は単球である、請求項44〜49のいずれか1項に記載の方法。
- 前記細胞への修飾RNAの送達が、細胞世代時間を改変しない、請求項44〜50のいずれか1項に記載の方法。
- 前記細胞への修飾RNAの送達が、重量単位での総細胞タンパク質含量を改変しない、請求項44〜51のいずれか1項に記載の方法。
- 細胞への修飾RNAの送達における、有効量の請求項1〜42のいずれか1項に記載のエキソソーム又は請求項43に記載の医薬組成物の使用。
- 前記細胞が、インビトロ細胞培地中に存在する、請求項53に記載の使用。
- 前記細胞が、被験者から取得される、請求項53又は54に記載の使用。
- 前記細胞が、被験者に存在する、請求項53に記載の使用。
- 前記細胞が、上皮細胞、免疫細胞、前駆細胞、又は幹細胞である、請求項53〜56のいずれか1項に記載の使用。
- 前記細胞が、Bリンパ球、Tリンパ球、又は単球である、請求項53〜57のいずれか1項に記載の使用。
- 前記細胞への前記修飾RNAの送達が、細胞世代時間を改変しない、請求項53〜58のいずれか1項に記載の使用。
- 前記細胞への前記修飾RNAの送達が、重量単位での総細胞タンパク質含量を改変しない、請求項53〜59のいずれか1項に記載の使用。
- 被験者の障害を処置又は予防する方法であって、有効量の請求項1〜42のいずれか1項に記載のエキソソーム又は請求項43に記載の医薬組成物を前記被験者に投与するステップを含み、ここで、前記エキソソームが、前記障害を処置する上で有効な修飾RNAを含む方法。
- 前記障害が、貧血、脊髄形成異常、免疫若しくは炎症性疾患、単一遺伝子病、及び複合病から選択される、請求項61に記載の方法。
- 前記障害が、貧血である、請求項61又は62に記載の方法。
- 前記障害が、脊髄形成異常である、請求項61又は62に記載の方法。
- 前記障害が、免疫若しくは炎症性疾患である、請求項61又は62に記載の方法。
- 前記修飾RNAが、エリスロポエチンポリペプチドをコードする、請求項61〜65のいずれか1項に記載の方法。
- 前記修飾RNAが、ヒトエリスロポエチンポリペプチドをコードする、請求項61〜66のいずれか1項に記載の方法。
- 前記修飾RNAが、配列番号1のエリスロポエチンポリペプチドをコードする、請求項61〜67のいずれか1項に記載の方法。
- 前記被験者が、エキソソームの非存在下での処置に比べ、エキソソームの存在下での処置に対して低下した免疫及び/又は炎症反応を有する、請求項61〜68のいずれか1項に記載の方法。
- 前記免疫及び/又は炎症反応の低下が、少なくとも1つのサイトカインのレベルの増加又は減少を含む、請求項69に記載の方法。
- 前記免疫及び/又は炎症反応の低下が、少なくとも1つのサイトカインのレベルの減少を含み、ここで、前記サイトカインは、IL−6、IP−10、RANTES、MCP−1、及びKCから選択される、請求項69又は70に記載の方法。
- 前記エキソソームが、前記被験者から取得された細胞から単離される、請求項61〜71のいずれか1項に記載の方法。
- 被験者の障害の処置又は予防における、有効量の請求項1〜42のいずれか1項に記載のエキソソーム又は請求項43に記載の医薬組成物の使用であって、前記エキソソームが、前記障害を処置する上で有効な修飾RNAを含む使用。
- 被験者の障害を処置又は予防する方法であって、以下:
(a)前記被験者から取得された1つ以上の細胞を提供するステップ;
(b)前記細胞によるLNP取込みを可能にする条件下で、修飾RNAを含む1つ以上の脂質ナノ粒子(LNP)と前記1つ以上の細胞を接触させるステップ;
(c)前記1つ以上の細胞により産生されるエキソソームを単離するステップであって、少なくとも1つの単離エキソソームが、前記修飾RNAを含むステップ;並びに
(d)有効量の前記単離エキソソームを前記被験者に投与するステップ
を含み、ここで、前記修飾RNAは、前記障害を処置する上で有効である方法。 - 前記細胞が、上皮細胞、免疫細胞、前駆細胞、又は幹細胞である、請求項74に記載の使用。
- 前記細胞が、Bリンパ球、Tリンパ球、又は単球である、請求項74又は75に記載の使用。
- 前記障害が、貧血、脊髄形成異常、免疫若しくは炎症性疾患、単一遺伝子病、及び複合病から選択される、請求項74〜76のいずれか1項に記載の方法。
- 前記障害が、貧血である、請求項74〜77のいずれか1項に記載の方法。
- 前記障害が、脊髄形成異常である、請求項74〜77のいずれか1項に記載の方法。
- 前記障害が、免疫又は炎症性疾患である、請求項74〜77のいずれか1項に記載の方法。
- 前記修飾RNAが、エリスロポエチンポリペプチドをコードする、請求項74〜80のいずれか1項に記載の方法。
- 前記修飾RNAが、ヒトエリスロポエチンポリペプチドをコードする、請求項74〜81のいずれか1項に記載の方法。
- 前記修飾RNAが、配列番号1のエリスロポエチンポリペプチドをコードする、請求項74〜82のいずれか1項に記載の方法。
- 前記被験者が、エキソソームの非存在下の処置に比べ、エキソソームの存在下での処置に対して低下した免疫及び/又は炎症反応を有する、請求項74〜83のいずれか1項に記載の方法。
- 前記免疫及び/又は炎症反応の低下が、少なくとも1つのサイトカインのレベルの増加又は減少を含む、請求項84に記載の方法。
- 前記免疫及び/又は炎症反応の低下が、少なくとも1つのサイトカインのレベルの減少を含み、ここで、前記サイトカインは、IL−6、IP−10、RANTES、MCP−1、及びKCから選択される、請求項84又は85に記載の方法。
- 1つ以上の細胞を前記LNPと接触させるステップが、ヒト血清の存在下で実施される、請求項74〜86のいずれか1項に記載の方法。
- 前記ヒト血清が、約0.5体積%、約1体積%、又は約1.5体積%で存在する、請求項87に記載の方法。
- 前記ヒト血清が、約1体積%で存在する、請求項87又は88に記載の方法。
- 1つ以上の細胞を前記LNPと接触させるステップが、前記1つ以上の細胞を、少なくとも2つ、少なくとも3つ、又は少なくとも4つの異なる用量の前記LNPと接触させることを含む、請求項74〜89のいずれか1項に記載の方法。
- 1つ以上の細胞を前記LNPと接触させるステップが、前記1つ以上の細胞を、少なくとも3つの異なる用量の前記LNPと接触させることを含む、請求項74〜90のいずれか1項に記載の方法。
- エキソソームを単離するステップが、インビトロ細胞培地のサンプルからエキソソームを単離することを含む、請求項74〜91のいずれか1項に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862691348P | 2018-06-28 | 2018-06-28 | |
| US62/691,348 | 2018-06-28 | ||
| PCT/EP2019/067232 WO2020002540A1 (en) | 2018-06-28 | 2019-06-27 | Exosome extracellular vesicles and methods of use |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021528096A true JP2021528096A (ja) | 2021-10-21 |
| JPWO2020002540A5 JPWO2020002540A5 (ja) | 2022-07-04 |
Family
ID=67139730
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020573481A Pending JP2021528096A (ja) | 2018-06-28 | 2019-06-27 | エキソソーム細胞外小胞及びその使用方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20210315819A1 (ja) |
| EP (1) | EP3813798A1 (ja) |
| JP (1) | JP2021528096A (ja) |
| CN (1) | CN112543629A (ja) |
| WO (1) | WO2020002540A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11786607B2 (en) | 2017-06-15 | 2023-10-17 | Modernatx, Inc. | RNA formulations |
| WO2019046809A1 (en) | 2017-08-31 | 2019-03-07 | Modernatx, Inc. | METHODS OF MANUFACTURING LIPID NANOPARTICLES |
| CA3190790A1 (en) * | 2020-08-06 | 2022-02-10 | Modernatx, Inc. | Methods of preparing lipid nanoparticles |
| WO2023178500A1 (en) * | 2022-03-22 | 2023-09-28 | Beijing Theraxyte Bioscience Co. Ltd. | Therapeutic vesicles and methods of processing the same |
| CN114848608B (zh) * | 2022-05-17 | 2024-01-30 | 东南大学 | 一种蛋白或多肽递送载体及其制备方法与应用 |
| CN115887758B (zh) * | 2022-11-15 | 2024-01-26 | 西南交通大学 | 负载外泌体促进糖尿病创面修复的共聚水凝胶 |
| CN117679354A (zh) * | 2024-02-04 | 2024-03-12 | 知想(山东)医疗科技有限公司 | 含有γ-氨基丁酸的外泌体制剂及其制备方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010285426A (ja) * | 2009-05-11 | 2010-12-24 | National Cancer Center | 核酸導入方法 |
| JP2012524052A (ja) * | 2009-04-17 | 2012-10-11 | アイシス イノヴェイション リミテッド | 遺伝物質の送達用の組成物 |
| JP2015501844A (ja) * | 2011-12-16 | 2015-01-19 | モデルナ セラピューティクス インコーポレイテッドModerna Therapeutics,Inc. | 修飾ヌクレオシド、ヌクレオチドおよび核酸組成物 |
| JP2017502997A (ja) * | 2014-01-21 | 2017-01-26 | アンヤリウム バイオサイエンシーズ アーゲー | ハイブリドソーム、それを含む組成物、それらの製造方法、およびその使用 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SI3431076T1 (sl) | 2009-06-10 | 2022-04-29 | Arbutus Biopharma Corporation | Izboljšana lipidna formulacija |
| CN103068980B (zh) | 2010-08-02 | 2017-04-05 | 瑟纳治疗公司 | 使用短干扰核酸(siNA)的RNA干扰介导的联蛋白(钙粘蛋白关联蛋白质),β1(CTNNB1)基因表达的抑制 |
| US8691750B2 (en) | 2011-05-17 | 2014-04-08 | Axolabs Gmbh | Lipids and compositions for intracellular delivery of biologically active compounds |
| US9738593B2 (en) | 2014-06-25 | 2017-08-22 | Acuitas Therapeutics Inc. | Lipids and lipid nanoparticle formulations for delivery of nucleic acids |
| AU2016209295B2 (en) * | 2015-01-21 | 2021-08-12 | Genevant Sciences Gmbh | Methods, compositions, and systems for delivering therapeutic and diagnostic agents into cells |
| EP3500244A4 (en) * | 2016-08-22 | 2020-05-13 | Codiak BioSciences, Inc. | METHOD FOR SUPPRESSING THE DELIVERY OF EXOSOMES TO LIVER AND SPLEEN |
| EP3292861A1 (en) * | 2016-09-13 | 2018-03-14 | Centre National De La Recherche Scientifique (Cnrs) | An in vitro method for obtaining a biohybrid vector |
-
2019
- 2019-06-27 CN CN201980042830.1A patent/CN112543629A/zh active Pending
- 2019-06-27 WO PCT/EP2019/067232 patent/WO2020002540A1/en active Application Filing
- 2019-06-27 JP JP2020573481A patent/JP2021528096A/ja active Pending
- 2019-06-27 US US16/972,190 patent/US20210315819A1/en active Pending
- 2019-06-27 EP EP19735277.6A patent/EP3813798A1/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012524052A (ja) * | 2009-04-17 | 2012-10-11 | アイシス イノヴェイション リミテッド | 遺伝物質の送達用の組成物 |
| JP2010285426A (ja) * | 2009-05-11 | 2010-12-24 | National Cancer Center | 核酸導入方法 |
| JP2015501844A (ja) * | 2011-12-16 | 2015-01-19 | モデルナ セラピューティクス インコーポレイテッドModerna Therapeutics,Inc. | 修飾ヌクレオシド、ヌクレオチドおよび核酸組成物 |
| JP2017502997A (ja) * | 2014-01-21 | 2017-01-26 | アンヤリウム バイオサイエンシーズ アーゲー | ハイブリドソーム、それを含む組成物、それらの製造方法、およびその使用 |
Non-Patent Citations (3)
| Title |
|---|
| NATURE COMMUNICATIONS, vol. 8: 1145, JPN6023023378, 2017, pages 1 - 15, ISSN: 0005190731 * |
| THE NEW ENGLAND JOURNAL OF MEDICINE, vol. 334, no. 17, JPN6023004527, 1996, pages 1135 - 1138, ISSN: 0005190732 * |
| 膜(MEMBRANE), vol. 40(5), JPN6023045832, 2015, pages 235 - 241, ISSN: 0005190733 * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3813798A1 (en) | 2021-05-05 |
| US20210315819A1 (en) | 2021-10-14 |
| CN112543629A (zh) | 2021-03-23 |
| WO2020002540A1 (en) | 2020-01-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2021528096A (ja) | エキソソーム細胞外小胞及びその使用方法 | |
| Maugeri et al. | Linkage between endosomal escape of LNP-mRNA and loading into EVs for transport to other cells | |
| Qu et al. | Dopamine-loaded blood exosomes targeted to brain for better treatment of Parkinson's disease | |
| ES2922462T3 (es) | Nanopartículas lipídicas para suministrar ARN modificado que codifica un polipéptido de VEGF-A | |
| Merkel et al. | Nonviral siRNA delivery to the lung: Investigation of PEG− PEI polyplexes and their in vivo performance | |
| US20220273566A1 (en) | Nanomaterials containing constrained lipids and uses thereof | |
| JP7066632B2 (ja) | 親油性抗炎症剤を含む脂質ナノ粒子およびその使用方法 | |
| JP2022501367A (ja) | 脂質ナノ粒子の調製及びその投与方法 | |
| US11471515B2 (en) | Restoration of tumor suppression using MRNA-based delivery system | |
| KR20170046145A (ko) | 리포솜 캡슐화 친화 약제 | |
| US20220226498A1 (en) | Substrate delivery of embedded liposomes | |
| Mocanu et al. | P-selectin targeted RAGE-shRNA lipoplexes alleviate atherosclerosis-associated inflammation | |
| KR20230002300A (ko) | 지질 나노입자 | |
| Scalzo et al. | Ionizable lipid nanoparticle-mediated delivery of plasmid DNA in cardiomyocytes | |
| Rahman et al. | Liposome-based nanomedicine therapeutics for rheumatoid arthritis | |
| KR20230050313A (ko) | 지질 나노입자 | |
| WO2020262150A1 (ja) | 脂質ナノ粒子 | |
| JP2018070555A (ja) | 皮膚線維症処置剤 | |
| Lewis et al. | Optimization of ionizable lipids for aerosolizable mRNA lipid nanoparticles | |
| JP2023513302A (ja) | 治療的に活性な作用物質を内皮へと送達するための脂質組成物およびその使用 | |
| Tang et al. | Nanovector assembled from natural egg yolk lipids for tumor-targeted delivery of therapeutics | |
| CN117582510A (zh) | 金属-多酚复合物在核酸递送系统中的应用 | |
| KR102537540B1 (ko) | 만노스를 포함하는 지질 나노입자 또는 이의 용도 | |
| Mao et al. | Theranostic Lipid Nanoparticles for Renal Cell Carcinoma | |
| Liu et al. | A nano-bioconjugate modified with anti-SIRPα antibodies and antisense oligonucleotides of mTOR for anti-atherosclerosis therapy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220624 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220624 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20230530 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230606 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230905 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20231107 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240306 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20240423 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20240502 |