JP2020007342A - 頭痛治療用の鼻腔内dhe - Google Patents
頭痛治療用の鼻腔内dhe Download PDFInfo
- Publication number
- JP2020007342A JP2020007342A JP2019162995A JP2019162995A JP2020007342A JP 2020007342 A JP2020007342 A JP 2020007342A JP 2019162995 A JP2019162995 A JP 2019162995A JP 2019162995 A JP2019162995 A JP 2019162995A JP 2020007342 A JP2020007342 A JP 2020007342A
- Authority
- JP
- Japan
- Prior art keywords
- dhe
- powder formulation
- administered
- auc
- average
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4985—Pyrazines or piperazines ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/48—Ergoline derivatives, e.g. lysergic acid, ergotamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
- A61K31/52—Purines, e.g. adenine
- A61K31/522—Purines, e.g. adenine having oxo groups directly attached to the heterocyclic ring, e.g. hypoxanthine, guanine, acyclovir
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/22—Heterocyclic compounds, e.g. ascorbic acid, tocopherol or pyrrolidones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0043—Nose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/146—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/06—Antimigraine agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Inorganic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Otolaryngology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Pain & Pain Management (AREA)
- Biomedical Technology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Description
本出願は、2013年9月24日に出願された米国仮特許出願第61/881,947号の優先権を主張するものであり、該出願は全体が参照により本明細書に組み入れられる。
片頭痛は、非常にありふれた、しばしば身体を衰弱させる、頭痛の形態である。一般的に、この頭痛は片側性(頭の半分に影響を及ぼす)および拍動性の性質がある。頭部痛に加えて、関連する症状として、吐き気、嘔吐、羞明(光に対する感受性の増加)、および音恐怖(音に対する感受性の増加)を挙げることができる。片頭痛はまた、一過性の視覚、感覚、言語、または運動の障害である「前兆」に関連付けることができ、多くの場合、頭部痛発症の直前に生じる着色光または点滅光の閃光として現れる。
この発明の概要に提示される本発明の態様は、単なる例示であって、本明細書に開示される選択的な態様の要約を提供するものである。発明の概要は、例示的および選択的であり、特許請求の範囲を限定するものでなく、本明細書に開示または企図された本発明の態様の全体範囲を提供するものでなく、かつ本開示の範囲もしくはクレームされた本発明の態様を制限または制約するものとして解釈されるべきでない。
[本発明1001]
ヒトに粉末製剤を鼻腔内投与することを含む方法であって、該粉末製剤が、
a)ジヒドロエルゴタミン(DHE)またはその薬学的に許容される塩、ここで、投与されるDHEの総用量は0.1〜10.0mgである;b)該製剤の総重量の少なくとも15%を構成する微結晶性セルロース成分を含む、方法。
[本発明1002]
以下の少なくとも1つをさらに含む、本発明1001の方法:
a) 粉末製剤の投与後のDHEの平均Tmaxが、約1〜約120分である;
b) 粉末製剤の投与後のDHEの(AUC0 - 30 min/AUC0 - inf) x 100%が、2.5%超である;
c) 粉末製剤の投与後のDHEの(AUC0 - 30 min/AUC0 - inf) x 100%が、2.5%超〜25%である;
d) 粉末製剤の投与後のDHEの(AUC0 - 60 min/AUC0 - inf) x 100%が、10%超である;
e) 粉末製剤の投与後のDHEの(AUC0 - 60 min/AUC0 - inf) x 100%が、10%超〜45%である;
f) 粉末製剤の投与後のDHEの(AUC0 - 120 min/AUC0 - inf) x 100%が、25%超である;
g) 粉末製剤の投与後のDHEの(AUC0 - 120 min/AUC0 - inf) x 100%が、25%超〜75%である;
h) 粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されたとき、(AUC0 - 30 min/AUC0 - inf) x 100%が、10%超である;
i) 粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されたとき、(AUC0 - 60 min/AUC0 - inf) x 100%が、20%超である;
j) 粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されたとき、(AUC0 - 120 min/AUC0 - inf) x 100%が、40%超である。
[本発明1003]
微結晶性セルロース成分が約100μm以下の平均粒子径を有する、本発明1001〜1002のいずれかの方法。
[本発明1004]
微結晶性セルロース成分が、約30μm以下の平均粒子径を有する第1の微結晶性セルロース部分と、約30〜約100μmの平均粒子径を有する第2の微結晶性セルロース部分とを含む、本発明1003の方法。
[本発明1005]
第1の微結晶性セルロース部分が約15〜約30μmの平均粒子径を有し、かつ第2の微結晶性セルロース部分が約45〜約65μmの平均粒子径を有する、本発明1004の方法。
[本発明1006]
微結晶性セルロース成分が約31〜約44μmの平均粒子径を有する粒子を実質的に含まない、本発明1005の方法。
[本発明1007]
第1の微結晶性セルロース部分が約20μmの平均粒子径を有し、かつ第2の微結晶性セルロース部分が約50〜約55μmの平均粒子径を有する、本発明1006の方法。
[本発明1008]
前記粉末製剤が53°以下の安息角を有する、本発明1007の方法。
[本発明1009]
第1の微結晶性セルロース部分が前記粉末製剤の総重量の約5%〜約90%であり、かつ第2の微結晶性セルロース部分が前記粉末製剤の総重量の約10%である、本発明1004〜1008のいずれかの方法。
[本発明1010]
微結晶性セルロース成分が前記粉末製剤の総重量の約15%〜約99%を構成する、本発明1009の方法。
[本発明1011]
第1の微結晶性セルロース成分が前記粉末製剤の総重量の約70%〜約90%を構成する、本発明1010の方法。
[本発明1012]
前記粉末製剤が流動化剤をさらに含む、本発明1001〜1011のいずれかの方法。
[本発明1013]
流動化剤が第三リン酸カルシウムである、本発明1012の方法。
[本発明1014]
第三リン酸カルシウムが前記粉末製剤の総重量の約0.5%〜約1.5%である、本発明1013の方法。
[本発明1015]
第三リン酸カルシウムが前記粉末製剤の総重量の約0.8%である、本発明1014の方法。
[本発明1016]
前記粉末製剤が以下の少なくとも1つをさらに含む、本発明1001〜1015のいずれかの方法:
アデノシン受容体拮抗薬、ホスホジエステラーゼ阻害剤、アセチルコリンエステラーゼ阻害剤、血管拡張剤、キサンチン、カフェイン、パラキサンチン、テオブロミン、テオフィリン。
[本発明1017]
前記粉末製剤がカフェインを含む、本発明1016の方法。
[本発明1018]
前記粉末製剤が約1%〜60%のカフェインを含む、本発明1017の方法。
[本発明1019]
前記粉末製剤が約5%〜10%のカフェインを含む、本発明1018の方法。
[本発明1020]
カフェインが無水カフェインである、本発明1017〜1019のいずれかの方法。
[本発明1021]
投与される前記粉末製剤の総用量が約0.1〜約25mgである、本発明1001〜1020のいずれかの方法。
[本発明1022]
投与される前記粉末製剤の総用量が約25mgである、本発明1021の方法。
[本発明1023]
前記粉末製剤が約0.1〜約4.0mgの投与されるDHEの総用量を含む、本発明1001〜1022のいずれかの方法。
[本発明1024]
前記粉末製剤が約0.5mgの投与されるDHEの総用量を含む、本発明1023の方法。
[本発明1025]
前記粉末製剤がジヒドロエルゴタミン(DHE)メシル酸塩を含む、本発明1001〜1024のいずれかの方法。
[本発明1026]
頭痛を治療するために使用される、本発明1001〜1025のいずれかの方法。
[本発明1027]
片頭痛を治療するために使用される、本発明1026の方法。
[本発明1028]
片頭痛を治療する方法が、前兆を伴うまたは前兆を伴わない片頭痛の急性期治療のための方法である、本発明1027の方法。
[本発明1029]
前記粉末製剤の少なくとも一部がヒトの単一の鼻孔に投与される、本発明1001〜1028のいずれかの方法。
[本発明1030]
前記粉末製剤の少なくとも一部がヒトの各鼻孔に投与される、本発明1001〜1028のいずれかの方法。
[本発明1031]
DHE Cmaxの対象間変動度が30%未満であるように前記粉末製剤が投与される、本発明1001〜1030のいずれかの方法。
[本発明1032]
DHEの平均Tmaxが約10〜約30分であり、前記粉末製剤の投与後のDHEの平均Cmaxが約0.5〜約6ng/mLであり、前記粉末製剤の投与後のDHEの平均AUC0-infが約1〜約15ng・h/mLであり、かつ前記粉末製剤の投与後のDHEの平均T1/2が約100〜約300分である、本発明1001〜1031のいずれかの方法。
[本発明1033]
DHEの平均Tmaxが約10〜約50分であり、前記粉末製剤の投与後のDHEの平均Cmaxが約1〜約15ng/mLであり、前記粉末製剤の投与後のDHEの平均AUC0-infが約10〜約50ng・h/mLであり、かつ前記粉末製剤の投与後のDHEの平均T1/2が約100〜約300分である、本発明1001〜1031のいずれかの方法。
[本発明1034]
DHEの平均Tmaxが約10〜約50分であり、前記粉末製剤の投与後のDHEの平均Cmaxが約2〜約20ng/mLであり、前記粉末製剤の投与後のDHEの平均AUC0-infが約15〜約110ng・h/mLであり、かつ前記粉末製剤の投与後のDHEの平均T1/2が約100〜約300分である、本発明1001〜1031のいずれかの方法。
[本発明1035]
DHEの平均Tmaxが約10〜約50分であり、前記粉末製剤の投与後のDHEの平均Cmaxが約2〜約50ng/mLであり、前記粉末製剤の投与後のDHEの平均AUC0-infが約15〜約200ng・h/mLであり、かつ前記粉末製剤の投与後のDHEの平均T1/2が約100〜約300分である、本発明1001〜1031のいずれかの方法。
[本発明1036]
前記粉末製剤の投与後のDHEの平均Tmaxが約2〜約50分である、本発明1001〜1035のいずれかの方法。
[本発明1037]
前記粉末製剤の投与後のDHEの平均Cmaxが約0.1〜約150ng/mLである、本発明1001〜1036のいずれかの方法。
[本発明1038]
前記製剤の投与後のDHEの平均AUC0-infが約1〜約700ng・h/mLである、本発明1001〜1037のいずれかの方法。
[本発明1039]
前記製剤の投与後のDHEの平均AUC0-tが約1〜約700ng・h/mLである、本発明1001〜1038のいずれかの方法。
[本発明1040]
前記製剤の投与後のDHEの平均T1/2が約10〜約300分である、本発明1001〜1039のいずれかの方法。
[本発明1041]
前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均Tmaxが約0.5〜約70分である、本発明1001〜1040のいずれかの方法。
[本発明1042]
前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均Tmaxが約1〜約60分である、本発明1041の方法。
[本発明1043]
前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均Cmaxが約0.1〜約150ng/mLである、本発明1001〜1042のいずれかの方法。
[本発明1044]
前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均AUC0-infが約1〜約700ng・h/mLである、本発明1041〜1043のいずれかの方法。
[本発明1045]
前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均T1/2が約10〜約300分である、本発明1041〜1044のいずれかの方法。
[本発明1046]
ヒトに粉末製剤を鼻腔内投与することを含む方法であって、該粉末製剤が、
a)ジヒドロエルゴタミン(DHE)またはその薬学的に許容される塩、ここで、投与されるDHEの総用量は0.1〜10.0mgである;b)該製剤の総重量の少なくとも15%を構成する微結晶性セルロース成分を含む、方法。
[本発明1047]
前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均Tmaxが約2〜約50分である、本発明1046の方法。
[本発明1048]
前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均Cmaxが約0.1〜約150ng/mLである、本発明1046〜1047のいずれかの方法。
[本発明1049]
前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均AUC0-infが約1〜約700ng・h/mLである、本発明1046〜1048のいずれかの方法。
[本発明1050]
前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均T1/2が約10〜約300分である、本発明1046〜1049のいずれかの方法。
[本発明1051]
ジヒドロエルゴタミン(DHE)またはその薬学的に許容される塩を含有する粉末製剤組成物。
[本発明1052]
前記投与することが鼻腔内投与することである、前記本発明のいずれかの方法。
特に定義のない限り、本明細書で使用される全ての技術用語および科学用語は、本発明が属する技術分野の当業者によって一般的に理解されるのと同じ意味を有する。本明細書に記載のものと類似または同等の方法および材料はどれも、本明細書に記載の該製剤もしくは単位用量の実施またはテストにおいて使用することができるが、いくつかの方法および材料が以下に記載される。特に言及しない限り、本明細書で使用または検討される技術は標準的な方法である。材料、方法および実施例は例示にすぎず、限定するものではない。
本明細書には、ジヒドロエルゴタミンまたはその薬学的に許容される塩を含む特定の製剤を、頭痛、例えば片頭痛を有する対象に、例えばヒトに、鼻腔内投与することを含んでなる、対象における、例えばヒトにおける、頭痛の治療方法、例えば、片頭痛の治療方法が提示される。例えば、本明細書には、本明細書に提示される製剤を鼻腔内投与することを含んでなる、片頭痛を含む頭痛の即効的治療のための、例えば前兆を伴うまたは前兆を伴わない片頭痛の急性期治療のための、方法が提示される。
6.1 実施例1:DHE粉末製剤の調製
6.1.1 0.1mg DHE粉末製剤の調製
0.1mgのDHEを含む粉末製剤は、本明細書に記載するように調製した。
0.5mgのDHEを含む粉末製剤は、本明細書に記載するように調製した。
1.0mgのDHEを含む粉末製剤は、本明細書に記載するように調製した。
以下の表2には、本明細書に提示される片頭痛を含む頭痛の治療方法において利用することができる代表的なDHE粉末製剤が提示される。このような製剤は、例えば、前述の実施例に記載したような手順に従って、製造することができる。こうした製剤の総量は単一の鼻孔に鼻腔内投与してもよいし、あるいは、一部を各鼻孔に投与してもよい;例えば、総量の約半分を各鼻孔に投与することができる。
単位: mg
DHE-ジヒドロエルゴタミンメシル酸塩
MCC(Ceolus PH-F20JP)-微結晶性セルロース公称粒子径20μm; メッシュサイズ400を通してふるいにかけたとき1%未満の保持。
MCC(Ceolus PH 301)-微結晶性セルロース公称粒子径50μm; メッシュサイズ60を通してふるいにかけたとき1%未満の保持およびメッシュサイズ200を通してふるいにかけたとき30%未満の保持。
以下の表3には、本明細書に提示される片頭痛を含む頭痛の治療方法において利用することができる、カフェインを含有する代表的なDHE粉末製剤が提示される。このようなカフェイン含有製剤は、例えば、前述の実施例に記載したものに類似する手順に従って、製造することができる。こうした製剤の総量は単一の鼻孔に鼻腔内投与してもよいし、あるいは、一部を各鼻孔に投与してもよい;例えば、総量の約半分を各鼻孔に投与することができる。
単位:mg
DHE-ジヒドロエルゴタミンメシル酸塩
MCC(Ceolus PH-F20JP)-微結晶性セルロース公称粒子径20μm; メッシュサイズ400を通してふるいにかけたとき1%未満の保持。
MCC(Ceolus PH 301)-微結晶性セルロース公称粒子径50μm; メッシュサイズ60を通してふるいにかけたとき1%未満の保持およびメッシュサイズ200を通してふるいにかけたとき30%未満の保持。
本明細書に記載するこの試験は、本明細書に記載のDHE粉末製剤を用いて鼻腔内投与した後の血漿中のジヒドロエルゴタミン(DHE)および8'-ヒドロキシDHEのレベルの薬物動態を評価するために、また、このような製剤の鼻腔内投与により達成された薬物動態プロファイルを、種々の投与経路により投与された比較DHE製剤のそれと比較するために、設計されたものである。
動物 4〜6歳齢の雄カニクイザル(macaca fascicularis、試験用に特別に繁殖させたもの)6匹を公認の動物福祉基準に従って使用する。
表4は、0.5mg DHEメシル酸塩点鼻スプレー、すなわちMigranal(液体製剤)、および実施例1に記載のDHE粉末製剤のカニクイザルの鼻腔内投与からのCmax、Tmax、およびAUCの結果を示す。0.5mgのMigranalと0.1、0.5および1.0mgの鼻腔内DHE粉末の鼻腔内投与後のサル血漿中のDHEの対応するPK曲線を図1および2に示す。表4ならびに図1および2のデータは、鼻腔内粉末製剤がテストした全ての用量にわたって短いTmax (17.5〜30分)を維持していることを示す。この実施例では、粉末製剤またはMigranalの投与後480分にAUC0-t(すなわち、AUC0-480 minutes)をテストしている。さらに、IN粉末DHEの薬物動態プロファイルは、承認されたMigranal治療よりも改善されている。具体的には、IN粉末から得られたTmax値は、Migranal投与から得られたものよりも短くなっている。さらに、0.5mgの同じDHE用量で、IN粉末はMigranalと比べてDHE Cmaxの30%増加をもたらす。この改善されたPKは図3にも反映されており、図3は、Migranalに対してIN粉末を投与したとき、投与後最初の30分間のDHE AUCがサルではより高いことを示している。
この実施例の結果は、本明細書に記載のジヒドロエルゴタミンの粉末製剤の鼻腔内投与が、霊長類血漿中のDHEへの即効的で良好な暴露をもたらすことを実証している。FDA承認のMigranal点鼻DHE製剤と比較したとき、本明細書に提示されるIN DHE粉末製剤はより高いCmax値およびより短いTmax値をもたらす。さらに、投与後の最初の30分間の暴露は、IN DHE粉末製剤を用いて改善される。これらのPKパラメータの改善は片頭痛の治療において特に重要である。DHEは一般的に、すでに発生している片頭痛を緩和するために投与されるので、短時間でのこの薬物へのより早発性でより多くの暴露は、最適な薬物動態プロファイルである。最後に、この薬物への血漿暴露は、IN DHE粉末製剤にカフェインを添加することによって、かつ/または2鼻孔間で該用量を分割することによって、さらに改善される。このようなPKの改善は、治療上有効な血漿レベルを達成するために、DHEのより低い用量の投与を可能にする。
本明細書に記載のこの試験は、若い健康な対象においてDHE鼻腔内粉末1mg、1.5mg、2mgおよび3mgの薬物動態プロファイル、用量比例性、安全性および忍容性を測定し、かつそのバイオアベイラビリティを溶液として皮下投与したDHE 1mgと比較するために設計されたものである。DHEとその代謝産物(8'-β-ヒドロキシジヒドロエルゴタミン;8'-β-OH-DHE)の薬物動態は、本試験において特性解析される。
・若い健康な男性または女性であって、登録時に18歳から45歳まで(18歳と45歳とを含む)であり、署名入りのインフォームドコンセントを提供し、該当する場合にはHIPAA承認を提供した者。
・担当医師によって健康と判断され、12誘導心電図を含む医療または検査室評価で臨床的に有意な異常が確認されない。この年齢層のための基準範囲を外れる臨床異常または検査値を有する対象は、検査結果が追加の危険因子を導入することがなく、かつ試験手順を妨げることがないと治験責任医師が考える場合にのみ、含めることができる。
・体格指数(BMI)≧18および≦32kg/m2を有する対象。
・女性対象は、彼女らが閉経後または不妊である場合に含められる;あるいは、彼女らが妊娠の可能性がある場合、彼女らは母乳を与えない、負の妊娠検査を有する、本試験の過程で妊娠するつもりがなく、本試験の過程で適切な避妊薬またはデバイスを使用している。対象および/または彼女のパートナーが使用することのできる医学的に許容可能な避妊方法は、以下のとおりである:経口避妊薬、プロゲスチン注射もしくはインプラント、殺精子剤が入っているコンドーム、殺精子剤を含むペッサリー、IUD、別のバリア式避妊法(コンドーム、ペッサリー)と組み合わせた膣殺精子坐剤、ホルモンパッチおよび膣リング、パートナーの避妊手術または禁欲。経口避妊を使用する女性は、スクリーニングの少なくとも4週間前にその薬を用いて開始していなければならない。パートナーの避妊手術は、スクリーニングの少なくとも6週間前に行っている必要がある。
・非喫煙者(治験薬投与前の6ヶ月間、無煙タバコ、ニコチンパッチなどを含めて、あらゆるタバコの使用をやめる)。
・無傷の鼻粘膜を有する対象(紅斑なし、炎症なし、潰瘍なし、腫脹なし、出血なし、萎縮(重度の局所乾燥および/または痂皮形成)なし、鼻中隔穿孔なし、およびIN投与を妨害しうる他の鼻の症状なし)。
・治験薬の初回投与の24時間前から最後の治療期間後の血液採取期間の終了までアルコールを進んで控える対象。
・プロトコルの要件を進んで順守しかつ順守することができ、かつクリニックのスタッフからの指示に従う対象。
・治験薬投与前の24時間以内から試験の終了までグレープフルーツ、ポメロ(pomelo)およびダイダイ(Seville orange)の製品およびジュースの消費を進んで避ける対象。
・治験責任医師の意見では、この治験への参加者として対象を容認できないリスクにさらすか、または薬物の吸収、分布、代謝もしくは排泄を妨げる可能性がある、臨床的に有意な中枢神経系(例えば、発作)、心臓、肺、代謝、腎臓、肝臓もしくは胃腸の疾患、またはこうした疾患の病歴。
・本試験の目的を妨げる、スクリーニング検査またはベースラインで臨床的に重要である身体所見の異常。
・いずれかの薬物に対する深刻な副作用もしくは過敏症の病歴、または治験製品もしくは治験製品の任意の成分のいずれかにアレルギーがあることが知られている者、または治験薬概要書に記載されているような治験製剤のいずれかに対する過敏症もしくはアレルギー反応の病歴。
・スクリーニング評価で臨床的に有意な異常検査値(治験責任医師により測定)。
・スクリーニングで得られた12誘導ECG:PR>240msec、QRS>110msecおよびQTc 430msec、スクリーニングECG上の徐脈(<50bpm)もしくは臨床的に重要なマイナーST波の変化、またはQT間隔の測定を妨害するスクリーニングECG上のその他の変化。
・スクリーニング時に存在する起立性低血圧または起立性高血圧の病歴。
・治験責任医師によって臨床的に有意であると判断された、本試験での初回投与の14日以内に急性医学的状態(例えば、下痢、発熱、上気道ウイルス感染)の存在。
・急性または慢性の治療を必要とするアレルギー(季節性アレルギー性鼻炎を除く)の存在または病歴。
・薬物投与に先立つ4週間における重大な身体的または精神的疾患の症状。
・昨年の片頭痛発作の病歴または存在。
・本試験の6ヶ月以内に外科的介入。
・陽性の試験前B型肝炎表面抗原;陽性のC型肝炎(HCV)抗体もしくは検出可能なHCVリボ核酸(RNA);または陽性のHIV抗体結果を有する。
・5-HT1B/D受容体作動薬に対するまたは(臨床試験ユニットが静脈内カニューレの開通性を維持するためにヘパリンを使用している場合)ヘパリンに対する感受性の病歴。
・任意の処方薬(例えば、エルゴタミン含有薬または麦角系薬(例えば、ジヒドロエルゴタミン)、または別の5-HT1B/D受容体作動薬)、または非処方薬、例えばビタミン、天然のハーブ系サプリメントもしくは栄養補助食品の、治験薬の初回投与に先立つ7日以内または半減期の5倍(どちらか長い方)以内での使用、あるいはセントジョーンズワート(St. John's Wort)の治験薬の初回投与に先立つ28日以内での使用。しかし、治験責任医師と試験チームは、その使用が対象の安全性を損なうか、または試験手順もしくはデータ解釈を妨害するかを判断するために、ケースバイケースで薬の使用を検討することができる。例外として、ボランティアは、治験薬の初回投与に先立つ48時間まで、パラセタモールまたはアセトアミノフェン(≦2g/日)またはイブプロフェン(1600mg/日)を服用してもよい。
・他の全身的処方薬、またはCYP1A2(例えばフルボキサミン)、CYP2D6(例えばパロキセチン、キニジンおよびフルオキセチン)、もしくはCYP3A(例えばクラリスロマイシン、イトラコナゾール、ケトコナゾール、インジナビルおよびエリスロマイシン)を阻害することが知られているか、CYP1A2(例えばリファンピン)もしくはCYP3A(例えばリファンピンおよびカルバマゼピン)を誘導することが知られている任意の薬物(またはハーブ系製剤)を、投薬に先立つ28日以内に使用するか、使用している対象。
・本試験の12ヶ月以内の薬物乱用または依存性の病歴。
・スクリーニング訪問の6ヶ月以内に、平均して>14ドリンク/週(1ドリンク(12gのアルコール)=5オンス(150ml)のワインまたは12オンス(360ml)のビールまたは1.5オンス(45ml)の80プルーフの蒸留酒)の習慣的アルコール消費歴を有する。
・本試験前の3ヶ月間に500ml以上の血液の損失、例えば血液ドナー。
・対象が陽性の治験前アルコールまたは尿薬物スクリーニングを有する。スクリーニングされる薬物の最小リストには、アンフェタミン、バルビツール酸、コカイン、アヘン、カンナビノイドおよびベンゾジアゼピンが含まれる。(疑わしい偽陽性の結果は、治験責任医師の裁量で繰り返すことができる。)
・別の薬物の調査試験への、または登録の60日以内の同時参加。
・治験責任医師が本試験には適さない候補であると考える者。
薬物動態: 薬物動態サンプルの収集:合計20の血液サンプル(各6mL)を以下の時間に収集する:0(投薬前)、投薬後5、10、15、20、25、30、35、40、45分、および1、1.5、2、3、4、6、8、12、18、24時間。
1. 身体検査
2. バイタルサインおよび体重
3. 12誘導ECG
4. 血液学および生化学分析のための血液検査
5. 尿検査
6. 有害事象(AE)
7. 受けた非治験薬の検討
8. 鼻への刺激の主観的評価:鼻に関連するさまざまな症状の存在についての、対象が回答するアンケート
9. 簡易匂い識別検査(B-SIT(商標))、標準化された嗅覚機能検査
10.鼻への刺激の客観的評価:鼻腔および粘膜の完全性の構造検査
11.臨床的に有意な異常が上記3つの評価のいずれかに観察された場合は、鼻の内視鏡検査
12.コロンビア自殺重大度評価尺度(C-SSRS)による自殺評価
薬物動態 以下の薬物動態パラメータは、標準ノンコンパートメント解析を用いて、DHEとその主要代謝産物である8'-β-ヒドロキシジヒドロエルゴタミンの両方について計算する:
1. 濃度-時間曲線下面積(AUC0-∞、およびAUC0-t)
2. 観察された最大血漿中濃度(Cmax)
3. Cmaxに達するまでの時間(Tmax)
4. 終末相半減期(t1/2)
5. 終末相速度定数(kel)
6. AUC0-tとAUC0-∞の比(AUC0-t/0-∞)
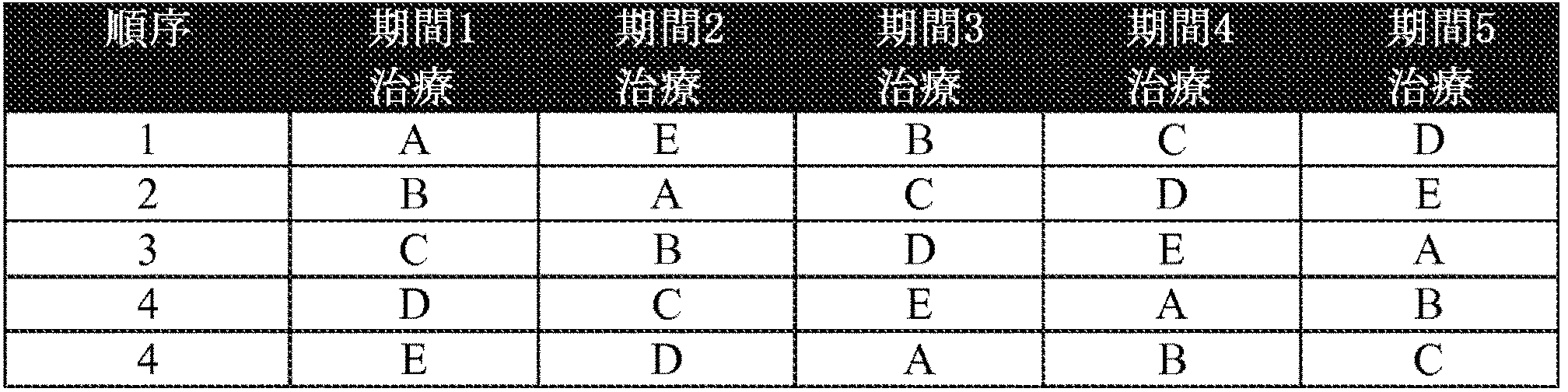
1. DHE 1mg、1.5mg、2mgおよび3mg鼻腔内粉末の薬物動態ならびに用量比例性。用量比例性は、血漿中DHEおよび8'-β-OH-DHE濃度プロファイルから推定されるAUC0-∞、AUC0-tおよびCmaxを比較することによって決定される(治療A〜D)。
2. 皮下投与したDHE 1mg溶液の薬物動態(治療E)。
3. DHE 1mg鼻腔内粉末の相対的バイオアベイラビリティは、該鼻腔内粉末(治療A)のAUC0-t、AUC0-∞およびCmaxを、DHE 1mg皮下溶液(治療E)のそれらと比較することによって、決定される。
4. 鼻腔内粉末の投与後の健康な成人におけるDHEの安全性および忍容性(治療A〜D)。
5. 本試験の全治療についての全ての安全性評価尺度(すなわち、有害事象、バイタルサイン、およびラボパラメータ)の検査および報告。
本明細書に記載のこの試験は、若い健康な対象においてDHE鼻腔内粉末0.5mgおよび1mgのDHEとその8'-ヒドロキシ-DHE代謝産物の薬物動態プロファイル、安全性および忍容性を測定し、かつそのバイオアベイラビリティを静脈内に、筋肉内に、または鼻腔内溶液として投与したDHE 0.5mgと比較するために設計されたものである。
・若い健康な男性または女性であって、登録時に18歳から45歳まで(18歳と45歳とを含む)であり、署名入りのインフォームドコンセントを提供し、該当する場合にはHIPAA承認を提供した者。
・担当医師によって健康と判断され、12誘導心電図を含む医療または検査室評価で臨床的に有意な異常が確認されない。この年齢層のための基準範囲を外れる臨床異常または検査値を有する対象は、検査結果が追加の危険因子を導入することがなく、かつ試験手順を妨げることがないと治験責任医師が考える場合にのみ、含めることができる。
・体格指数(BMI)≧18および≦32kg/m2を有する対象。
・女性対象は、彼女らが閉経後または不妊である場合に含められる;あるいは、彼女らが妊娠の可能性がある場合、彼女らは母乳を与えない、負の妊娠検査を有する、本試験の過程で妊娠するつもりがなく、本試験の過程で適切な避妊薬またはデバイスを使用している。対象および/または彼女のパートナーが使用することのできる医学的に許容可能な避妊方法は、以下のとおりである:経口避妊薬、プロゲスチン注射もしくはインプラント、殺精子剤が入っているコンドーム、殺精子剤を含むペッサリー、IUD、別のバリア式避妊法(コンドーム、ペッサリー)と組み合わせた膣殺精子坐剤、ホルモンパッチおよび膣リング、パートナーの避妊手術または禁欲。経口避妊を使用する女性は、スクリーニングの少なくとも4週間前にその薬を用いて開始していなければならない。パートナーの避妊手術は、スクリーニングの少なくとも6週間前に行っている必要がある。
・非喫煙者(治験薬投与前の6ヶ月間、無煙タバコ、ニコチンパッチなどを含めて、あらゆるタバコの使用をやめる)。
・無傷の鼻粘膜を有する対象(紅斑なし、炎症なし、潰瘍なし、腫脹なし、出血なし、萎縮(重度の局所乾燥および/または痂皮形成)なし、鼻中隔穿孔なし、およびIN投与を妨害しうる他の鼻の症状なし)。
・治験薬の初回投与の24時間前から最後の治療期間後の血液採取期間の終了までアルコールを進んで控える対象。
・プロトコルの要件を進んで順守しかつ順守することができ、かつクリニックのスタッフからの指示に従う対象。
・治験薬投与前の24時間以内から試験の終了までグレープフルーツ、ザボンおよびダイダイの製品およびジュースの消費を進んで避ける対象。
・治験責任医師の意見では、この治験への参加者として対象を容認できないリスクにさらすか、または薬物の吸収、分布、代謝もしくは排泄を妨げる可能性がある、臨床的に有意な中枢神経系(例えば、発作)、心臓、肺、代謝、腎臓、肝臓もしくは胃腸の疾患、またはこうした疾患の病歴。
・本試験の目的を妨げる、スクリーニング検査またはベースラインで臨床的に重要である身体所見の異常。
・いずれかの薬物に対する深刻な副作用もしくは過敏症の病歴、または治験製品もしくは治験製品の任意の成分のいずれかにアレルギーがあることが知られている者、または治験薬概要書に記載されているような治験製剤のいずれかに対する過敏症もしくはアレルギー反応の病歴。
・スクリーニング評価で臨床的に有意な異常検査値(治験責任医師により測定)。
・スクリーニングで得られた12誘導ECG:PR>240msec、QRS>110msecおよびQTc 430msec、スクリーニングECG上の徐脈(<50bpm)もしくは臨床的に重要なマイナーST波の変化、またはQT間隔の測定を妨害するスクリーニングECG上のその他の変化。
・スクリーニング時に存在する起立性低血圧または起立性高血圧の病歴。
・治験責任医師によって臨床的に有意であると判断された、本試験での初回投与の14日以内に急性医学的状態(例えば、下痢、発熱、上気道ウイルス感染)の存在。
・急性または慢性の治療を必要とするアレルギー(季節性アレルギー性鼻炎を除く)の存在または病歴。
・薬物投与に先立つ4週間における重大な身体的または精神的疾患の症状。
・昨年の片頭痛発作の病歴または存在。
・本試験の6ヶ月以内に外科的介入。
・陽性の試験前B型肝炎表面抗原;陽性のC型肝炎(HCV)抗体もしくは検出可能なHCVリボ核酸(RNA);または陽性のHIV抗体結果を有する。
・5-HT1B/D受容体作動薬に対するまたは(臨床試験ユニットが静脈内カニューレの開通性を維持するためにヘパリンを使用している場合)ヘパリンに対する感受性の病歴。
・任意の処方薬(例えば、エルゴタミン含有薬または麦角系薬(例えば、ジヒドロエルゴタミン)、または別の5-HT1B/D受容体作動薬)、または非処方薬、例えばビタミン、天然のハーブ系サプリメントもしくは栄養補助食品の、治験薬の初回投与に先立つ7日以内または半減期の5倍(どちらか長い方)以内での使用、あるいはセントジョーンズワート(St. John's Wort)の治験薬の初回投与に先立つ28日以内での使用。しかし、治験責任医師と試験チームは、その使用が対象の安全性を損なうか、または試験手順もしくはデータ解釈を妨害するかを判断するために、ケースバイケースで薬の使用を検討することができる。例外として、ボランティアは、治験薬の初回投与に先立つ48時間まで、パラセタモールまたはアセトアミノフェン(≦2g/日)またはイブプロフェン(1600mg/日)を服用してもよい。
・他の全身的処方薬、またはCYP1A2(例えばフルボキサミン)、CYP2D6(例えばパロキセチン、キニジンおよびフルオキセチン)、もしくはCYP3A(例えばクラリスロマイシン、イトラコナゾール、ケトコナゾール、インジナビルおよびエリスロマイシン)を阻害することが知られているか、CYP1A2(例えばリファンピン)もしくはCYP3A(例えばリファンピンおよびカルバマゼピン)を誘導することが知られている任意の薬物(またはハーブ系製剤)を、投薬に先立つ28日以内に使用するか、使用している対象。
・本試験の12ヶ月以内の薬物乱用または依存性の病歴。
・スクリーニング訪問の6ヶ月以内に、平均して>14ドリンク/週(1ドリンク(12gのアルコール)=5オンス(150ml)のワインまたは12オンス(360ml)のビールまたは1.5オンス(45ml)の80プルーフの蒸留酒)の習慣的アルコール消費歴を有する。
・本試験前の3ヶ月間に500ml以上の血液の損失、例えば血液ドナー。
・対象が陽性の治験前アルコールまたは尿薬物スクリーニングを有する。スクリーニングされる薬物の最小リストには、アンフェタミン、バルビツール酸、コカイン、アヘン、カンナビノイドおよびベンゾジアゼピンが含まれる。(疑わしい偽陽性の結果は、治験責任医師の裁量で繰り返すことができる。)
・別の薬物の調査試験への、または登録の60日以内の同時参加。
・治験責任医師が本試験には適さない候補であると考える者。
薬物動態: 薬物動態サンプルの収集:合計20の血液サンプル(各6mL)を以下の時間に収集する:0(投薬前およびIV腕での投薬直後)、投薬後5、10、15、20、25、30、35、40、45分、および1、1.5、2、3、4、6、8、12、18、24時間。
・身体検査
・バイタルサインおよび体重
・12誘導ECG
・血液学および生化学分析のための血液検査
・尿検査
・有害事象(AE)
・受けた非治験薬の検討
・鼻への刺激の主観的評価:鼻に関連するさまざまな症状の存在についての、対象が回答するアンケート
・簡易匂い識別検査(B-SIT(商標))、標準化された嗅覚機能検査
・鼻への刺激の客観的評価:鼻腔および粘膜の完全性の構造検査
・臨床的に有意な異常が上記3つの評価のいずれかに観察された場合は、鼻の内視鏡検査
・コロンビア自殺重大度評価尺度(C-SSRS)による自殺評価
薬物動態 以下の薬物動態パラメータは、標準ノンコンパートメント解析を用いて、DHEとその主要代謝産物である8'-β-ヒドロキシジヒドロエルゴタミンの両方について計算する:
1. 濃度-時間曲線下面積(AUC0-∞、およびAUC0-t)
2. 観察された最大血漿中濃度(Cmax)
3. Cmaxに達するまでの時間(Tmax)
4. 終末相半減期(t1/2)
5. 終末相速度定数(kel)
6. AUC0-tとAUC0-∞の比(AUC0-t/0-∞)
1. DHE 0.5および1mg鼻腔内粉末の薬物動態ならびに用量比例性。用量比例性は、血漿中のDHEおよび8'-β-OH-DHEの濃度プロファイルから推定されるAUC0-∞、AUC0-tおよびCmaxを比較することによって決定される(治療AおよびB)。
2. 静脈内、筋肉内および鼻腔内に投与したDHE 0.5mg溶液の薬物動態(治療C、DおよびE)。
3. DHE 0.5mg鼻腔内粉末の絶対的および相対的バイオアベイラビリティは、該鼻腔内粉末(治療A)のAUC0-t、AUC0-∞およびCmaxを、DHE 0.5mg静脈内、筋肉内および鼻腔内溶液(治療C、DおよびE)のそれらと比較することによって、決定される。
4. 鼻腔内粉末の投与後の健康な成人におけるDHEの安全性および忍容性(治療AおよびB)。
5. 本試験の全治療についての全ての安全性評価尺度(すなわち、有害事象、バイタルサイン、およびラボパラメータ)の検査および報告。
DHE経鼻粉末製剤は、前兆を伴うまたは前兆を伴わない急性片頭痛の即効的治療に用いられる。患者が活発な片頭痛を有する場合、その患者は該製品を使用するように指示される。具体的には、使用に先立って、鼻孔が開くのを助けるために、穏やかに自分の鼻をかむように患者に指示する。全用量を単一の鼻孔に送達しようとする場合には、空気の流れのよい方の鼻孔を選択するように患者に指示する。医師によっては、自分の診療室または医療現場でのDHE経鼻粉末の使用を検討することができる。単回投与におけるDHEの総量は、約0.1〜10mgの範囲である。典型的には、患者は約1.0〜2.0mgの用量を受ける。カフェインを含むまたは含まないDHE経鼻粉末を患者に投与することができる。
特許、特許出願および刊行物などのさまざまな参考文献が本明細書に引用されており、それらの開示はその全体が参照により本明細書に組み入れられるものとする。本明細書中の用語と参照により組み入れられた用語との間に矛盾が生じた場合には、本明細書中の用語が優先する。
Claims (52)
- ヒトに粉末製剤を鼻腔内投与することを含む方法であって、該粉末製剤が、
a)ジヒドロエルゴタミン(DHE)またはその薬学的に許容される塩、ここで、投与されるDHEの総用量は0.1〜10.0mgである;b)該製剤の総重量の少なくとも15%を構成する微結晶性セルロース成分を含む、方法。 - 以下の少なくとも1つをさらに含む、請求項1記載の方法:
a) 粉末製剤の投与後のDHEの平均Tmaxが、約1〜約120分である;
b) 粉末製剤の投与後のDHEの(AUC0 - 30 min/AUC0 - inf) x 100%が、2.5%超である;
c) 粉末製剤の投与後のDHEの(AUC0 - 30 min/AUC0 - inf) x 100%が、2.5%超〜25%である;
d) 粉末製剤の投与後のDHEの(AUC0 - 60 min/AUC0 - inf) x 100%が、10%超である;
e) 粉末製剤の投与後のDHEの(AUC0 - 60 min/AUC0 - inf) x 100%が、10%超〜45%である;
f) 粉末製剤の投与後のDHEの(AUC0 - 120 min/AUC0 - inf) x 100%が、25%超である;
g) 粉末製剤の投与後のDHEの(AUC0 - 120 min/AUC0 - inf) x 100%が、25%超〜75%である;
h) 粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されたとき、(AUC0 - 30 min/AUC0 - inf) x 100%が、10%超である;
i) 粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されたとき、(AUC0 - 60 min/AUC0 - inf) x 100%が、20%超である;
j) 粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されたとき、(AUC0 - 120 min/AUC0 - inf) x 100%が、40%超である。 - 微結晶性セルロース成分が約100μm以下の平均粒子径を有する、請求項1〜2のいずれかに記載の方法。
- 微結晶性セルロース成分が、約30μm以下の平均粒子径を有する第1の微結晶性セルロース部分と、約30〜約100μmの平均粒子径を有する第2の微結晶性セルロース部分とを含む、請求項3記載の方法。
- 第1の微結晶性セルロース部分が約15〜約30μmの平均粒子径を有し、かつ第2の微結晶性セルロース部分が約45〜約65μmの平均粒子径を有する、請求項4記載の方法。
- 微結晶性セルロース成分が約31〜約44μmの平均粒子径を有する粒子を実質的に含まない、請求項5記載の方法。
- 第1の微結晶性セルロース部分が約20μmの平均粒子径を有し、かつ第2の微結晶性セルロース部分が約50〜約55μmの平均粒子径を有する、請求項6記載の方法。
- 前記粉末製剤が53°以下の安息角を有する、請求項7記載の方法。
- 第1の微結晶性セルロース部分が前記粉末製剤の総重量の約5%〜約90%であり、かつ第2の微結晶性セルロース部分が前記粉末製剤の総重量の約10%である、請求項4〜8のいずれか一項記載の方法。
- 微結晶性セルロース成分が前記粉末製剤の総重量の約15%〜約99%を構成する、請求項9記載の方法。
- 第1の微結晶性セルロース成分が前記粉末製剤の総重量の約70%〜約90%を構成する、請求項10記載の方法。
- 前記粉末製剤が流動化剤をさらに含む、請求項1〜11のいずれか一項記載の方法。
- 流動化剤が第三リン酸カルシウムである、請求項12記載の方法。
- 第三リン酸カルシウムが前記粉末製剤の総重量の約0.5%〜約1.5%である、請求項13記載の方法。
- 第三リン酸カルシウムが前記粉末製剤の総重量の約0.8%である、請求項14記載の方法。
- 前記粉末製剤が以下の少なくとも1つをさらに含む、請求項1〜15のいずれか一項記載の方法:
アデノシン受容体拮抗薬、ホスホジエステラーゼ阻害剤、アセチルコリンエステラーゼ阻害剤、血管拡張剤、キサンチン、カフェイン、パラキサンチン、テオブロミン、テオフィリン。 - 前記粉末製剤がカフェインを含む、請求項16記載の方法。
- 前記粉末製剤が約1%〜60%のカフェインを含む、請求項17記載の方法。
- 前記粉末製剤が約5%〜10%のカフェインを含む、請求項18記載の方法。
- カフェインが無水カフェインである、請求項17〜19のいずれか一項記載の方法。
- 投与される前記粉末製剤の総用量が約0.1〜約25mgである、請求項1〜20のいずれか一項記載の方法。
- 投与される前記粉末製剤の総用量が約25mgである、請求項21記載の方法。
- 前記粉末製剤が約0.1〜約4.0mgの投与されるDHEの総用量を含む、請求項1〜22のいずれか一項記載の方法。
- 前記粉末製剤が約0.5mgの投与されるDHEの総用量を含む、請求項23記載の方法。
- 前記粉末製剤がジヒドロエルゴタミン(DHE)メシル酸塩を含む、請求項1〜24のいずれか一項記載の方法。
- 頭痛を治療するために使用される、請求項1〜25のいずれか一項記載の方法。
- 片頭痛を治療するために使用される、請求項26記載の方法。
- 片頭痛を治療する方法が、前兆を伴うまたは前兆を伴わない片頭痛の急性期治療のための方法である、請求項27記載の方法。
- 前記粉末製剤の少なくとも一部がヒトの単一の鼻孔に投与される、請求項1〜28のいずれか一項記載の方法。
- 前記粉末製剤の少なくとも一部がヒトの各鼻孔に投与される、請求項1〜28のいずれか一項記載の方法。
- DHE Cmaxの対象間変動度が30%未満であるように前記粉末製剤が投与される、請求項1〜30のいずれか一項記載の方法。
- DHEの平均Tmaxが約10〜約30分であり、前記粉末製剤の投与後のDHEの平均Cmaxが約0.5〜約6ng/mLであり、前記粉末製剤の投与後のDHEの平均AUC0-infが約1〜約15ng・h/mLであり、かつ前記粉末製剤の投与後のDHEの平均T1/2が約100〜約300分である、請求項1〜31のいずれか一項記載の方法。
- DHEの平均Tmaxが約10〜約50分であり、前記粉末製剤の投与後のDHEの平均Cmaxが約1〜約15ng/mLであり、前記粉末製剤の投与後のDHEの平均AUC0-infが約10〜約50ng・h/mLであり、かつ前記粉末製剤の投与後のDHEの平均T1/2が約100〜約300分である、請求項1〜31のいずれか一項記載の方法。
- DHEの平均Tmaxが約10〜約50分であり、前記粉末製剤の投与後のDHEの平均Cmaxが約2〜約20ng/mLであり、前記粉末製剤の投与後のDHEの平均AUC0-infが約15〜約110ng・h/mLであり、かつ前記粉末製剤の投与後のDHEの平均T1/2が約100〜約300分である、請求項1〜31のいずれか一項記載の方法。
- DHEの平均Tmaxが約10〜約50分であり、前記粉末製剤の投与後のDHEの平均Cmaxが約2〜約50ng/mLであり、前記粉末製剤の投与後のDHEの平均AUC0-infが約15〜約200ng・h/mLであり、かつ前記粉末製剤の投与後のDHEの平均T1/2が約100〜約300分である、請求項1〜31のいずれか一項記載の方法。
- 前記粉末製剤の投与後のDHEの平均Tmaxが約2〜約50分である、請求項1〜35のいずれか一項記載の方法。
- 前記粉末製剤の投与後のDHEの平均Cmaxが約0.1〜約150ng/mLである、請求項1〜36のいずれか一項記載の方法。
- 前記製剤の投与後のDHEの平均AUC0-infが約1〜約700ng・h/mLである、請求項1〜37のいずれか一項記載の方法。
- 前記製剤の投与後のDHEの平均AUC0-tが約1〜約700ng・h/mLである、請求項1〜38のいずれか一項記載の方法。
- 前記製剤の投与後のDHEの平均T1/2が約10〜約300分である、請求項1〜39のいずれか一項記載の方法。
- 前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均Tmaxが約0.5〜約70分である、請求項1〜40のいずれか一項記載の方法。
- 前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均Tmaxが約1〜約60分である、請求項41記載の方法。
- 前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均Cmaxが約0.1〜約150ng/mLである、請求項1〜42のいずれか一項記載の方法。
- 前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均AUC0-infが約1〜約700ng・h/mLである、請求項41〜43のいずれか一項記載の方法。
- 前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均T1/2が約10〜約300分である、請求項41〜44のいずれか一項記載の方法。
- ヒトに粉末製剤を鼻腔内投与することを含む方法であって、該粉末製剤が、
a)ジヒドロエルゴタミン(DHE)またはその薬学的に許容される塩、ここで、投与されるDHEの総用量は0.1〜10.0mgである;b)該製剤の総重量の少なくとも15%を構成する微結晶性セルロース成分を含む、方法。 - 前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均Tmaxが約2〜約50分である、請求項46記載の方法。
- 前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均Cmaxが約0.1〜約150ng/mLである、請求項46〜47のいずれかに記載の方法。
- 前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均AUC0-infが約1〜約700ng・h/mLである、請求項46〜48のいずれか一項記載の方法。
- 前記粉末製剤が霊長類、好ましくはサル、好ましくはカニクイザルに投与されるとき、DHEの平均T1/2が約10〜約300分である、請求項46〜49のいずれか一項記載の方法。
- ジヒドロエルゴタミン(DHE)またはその薬学的に許容される塩を含有する粉末製剤組成物。
- 前記投与することが鼻腔内投与することである、前記請求項のいずれかに記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361881947P | 2013-09-24 | 2013-09-24 | |
| US61/881,947 | 2013-09-24 | ||
| JP2016516520A JP2016531850A (ja) | 2013-09-24 | 2014-09-24 | 頭痛治療用の鼻腔内dhe |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016516520A Division JP2016531850A (ja) | 2013-09-24 | 2014-09-24 | 頭痛治療用の鼻腔内dhe |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2020007342A true JP2020007342A (ja) | 2020-01-16 |
| JP6902583B2 JP6902583B2 (ja) | 2021-07-14 |
Family
ID=52424045
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016516520A Pending JP2016531850A (ja) | 2013-09-24 | 2014-09-24 | 頭痛治療用の鼻腔内dhe |
| JP2019162995A Active JP6902583B2 (ja) | 2013-09-24 | 2019-09-06 | 頭痛治療用の鼻腔内dhe |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016516520A Pending JP2016531850A (ja) | 2013-09-24 | 2014-09-24 | 頭痛治療用の鼻腔内dhe |
Country Status (6)
| Country | Link |
|---|---|
| US (5) | US20160228433A1 (ja) |
| EP (2) | EP3049059B1 (ja) |
| JP (2) | JP2016531850A (ja) |
| DK (1) | DK3049059T3 (ja) |
| ES (1) | ES2904570T3 (ja) |
| WO (1) | WO2015044782A2 (ja) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101980738A (zh) | 2008-02-07 | 2011-02-23 | 华盛顿大学 | 圆周气雾设备 |
| BR122021002471B8 (pt) | 2011-03-03 | 2022-10-25 | Impel Neuropharma Inc | Dispositivo de distribuição de droga nasal |
| RU2741249C2 (ru) | 2011-05-09 | 2021-01-22 | Импел Ньюрофарма Инк. | Наконечники для назальной доставки лекарственных средств |
| CA2909954C (en) | 2013-04-28 | 2021-03-23 | Impel Neuropharma, Inc. | Medical unit dose container |
| CA2998182A1 (en) | 2015-09-10 | 2017-03-16 | Impel Neuropharma, Inc. | In-line nasal delivery device |
| BR112019002371A2 (pt) | 2016-08-05 | 2019-06-04 | Shin Nippon Biomedical Laboratories Ltd | composições farmacêuticas |
| BR112019027508A2 (pt) * | 2017-07-02 | 2020-07-07 | Dr. Reddys Laboratories Limited | formas de dosagem nasal de di-hidroergotamina |
| JP2021503988A (ja) | 2017-11-21 | 2021-02-15 | インペル ニューロファーマ インコーポレイテッド | インレットインターフェースを用いた鼻腔内装置 |
| EP3713628A4 (en) | 2017-11-21 | 2021-08-18 | Impel Neuropharma Inc. | INTRA-NASAL DEVICE WITH DIVER TUBE |
| KR20200118034A (ko) | 2018-01-05 | 2020-10-14 | 임펠 뉴로파마 인코포레이티드 | 정밀 후각기관 장치에 의한 올란자핀의 비강내 전달 |
| CA3088942C (en) * | 2018-01-05 | 2023-01-03 | Impel Neuropharma, Inc. | Intranasal delivery of dihydroergotamine by precision olfactory device |
| JP2021532098A (ja) | 2018-07-19 | 2021-11-25 | インペル ニューロファーマ インコーポレイテッド | パーキンソン病の治療のためのレボドパおよびドーパデカルボキシラーゼ阻害剤の呼吸管路送達 |
| CN113423400A (zh) | 2018-12-11 | 2021-09-21 | 小蜜橘制药公司 | 用于治疗或预防头痛的组合物、装置和方法 |
| GB2581431A (en) * | 2018-12-11 | 2020-08-19 | Satsuma Pharmaceuticals Inc | Compositions, devices, and methods for treating or preventing headaches |
| CN113473967B (zh) | 2019-01-03 | 2022-09-09 | 英倍尔制药公司 | 经鼻药物递送装置 |
| BR112021023049A8 (pt) | 2019-05-17 | 2022-10-18 | Impel Neuropharma Inc | Dispositivo de dispensação nasal de uso único |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH1059841A (ja) * | 1996-02-27 | 1998-03-03 | Teijin Ltd | 吸収性が改善された粉末状経鼻投与組成物 |
| JP2003206227A (ja) * | 2002-01-09 | 2003-07-22 | Translational Research株式会社 | 薬物の経鼻投与用組成物 |
| WO2006016530A1 (ja) * | 2004-08-10 | 2006-02-16 | Translational Research, Ltd. | 速効性でかつ高い吸収性を可能とする経鼻投与用組成物 |
| JP2006519219A (ja) * | 2003-02-28 | 2006-08-24 | ブリタニア ファーマシューティカルズ リミテッド | 鼻腔送達用医薬品組成物 |
| JP4721212B2 (ja) * | 2001-07-05 | 2011-07-13 | 株式会社新日本科学 | インスリンの経鼻投与用組成物 |
| US20110171141A1 (en) * | 2009-06-26 | 2011-07-14 | Kellerman Donald J | Administration of dihydroergotamine mesylate particles using a metered dose inhaler |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5169849A (en) * | 1982-02-01 | 1992-12-08 | Sandoz Ltd. | Nasal pharmaceutical compositions |
| JPS59163313A (ja) * | 1983-03-09 | 1984-09-14 | Teijin Ltd | 経鼻投与用ペプチドホルモン類組成物 |
| ES2194867T3 (es) * | 1993-03-26 | 2003-12-01 | Franciscus Wilhelmus He Merkus | Composiciones farmaceuticas para la administracion intranasal de apomorfina. |
| JP4691298B2 (ja) * | 1999-10-12 | 2011-06-01 | 科研製薬株式会社 | 粉末吸入用製剤及びその製造方法 |
| JP2004531333A (ja) * | 2001-06-20 | 2004-10-14 | ネクター セラピューティクス | 粉末エアロゾル化装置及び方法 |
| FR2834212B1 (fr) * | 2001-12-27 | 2004-07-09 | Besins Int Belgique | Utilisation d'une poudre a liberation immediate dans des compositions pharmaceutiques et nutraceutiques |
| GB0228826D0 (en) * | 2002-12-11 | 2003-01-15 | Okpala Joseph | Hair technology in creating particles with improved delivery capabilities |
| US7638138B2 (en) * | 2003-02-21 | 2009-12-29 | Translational Research, Ltd. | Compositions for nasal administration of pharmaceuticals |
| AU2006278571B2 (en) * | 2005-08-05 | 2011-11-24 | 3M Innovative Properties Company | Compositions exhibiting improved flowability |
| EP1958619B1 (en) * | 2005-12-06 | 2015-04-15 | Asahi Kasei Chemicals Corporation | Process for producing tablet by high-speed direct compression |
| JP5415769B2 (ja) * | 2006-12-26 | 2014-02-12 | 株式会社新日本科学 | 経鼻投与用製剤 |
| JP2009076785A (ja) * | 2007-09-21 | 2009-04-09 | Panasonic Corp | 半導体装置の製造方法 |
| EP2429495A4 (en) * | 2009-05-15 | 2014-01-22 | Shin Nippon Biomedical Lab Ltd | INTRANASAL PHARMACEUTICAL COMPOSITIONS WITH ENHANCED PHARMACOKINETICS |
| WO2011013003A2 (en) | 2009-07-31 | 2011-02-03 | Shin Nippon Biomedical Laboratories, Ltd. | Intranasal granisetron and nasal applicator |
| KR102136036B1 (ko) * | 2010-04-15 | 2020-07-20 | 신 니뽄 바이오메디칼 라보라토리즈, 엘티디. | 비강내 전달을 위한 방법 및 조성물 |
| US20110318277A1 (en) * | 2010-06-25 | 2011-12-29 | APT Pharmaceuticals, Inc. University of Maryland, Baltimore | Tacrolimus compositions for aerosol administration |
| AU2012212866B2 (en) | 2011-01-31 | 2016-09-15 | Shin Nippon Biomedical Laboratories, Ltd. | Intranasal delivery devices |
| SG10201604653TA (en) * | 2011-12-11 | 2016-07-28 | Recro Pharma Inc | Intranasal dexmedetomidine compositions and methods of use thereof |
-
2014
- 2014-09-24 ES ES14830861T patent/ES2904570T3/es active Active
- 2014-09-24 US US15/023,206 patent/US20160228433A1/en not_active Abandoned
- 2014-09-24 JP JP2016516520A patent/JP2016531850A/ja active Pending
- 2014-09-24 EP EP14830861.2A patent/EP3049059B1/en active Active
- 2014-09-24 EP EP21205407.6A patent/EP4008307A1/en active Pending
- 2014-09-24 WO PCT/IB2014/002706 patent/WO2015044782A2/en active Application Filing
- 2014-09-24 DK DK14830861.2T patent/DK3049059T3/da active
-
2019
- 2019-05-16 US US16/414,350 patent/US20190275036A1/en not_active Abandoned
- 2019-09-06 JP JP2019162995A patent/JP6902583B2/ja active Active
-
2020
- 2020-02-14 US US16/791,431 patent/US20200179379A1/en not_active Abandoned
-
2022
- 2022-06-07 US US17/834,583 patent/US20230000860A1/en active Pending
-
2023
- 2023-10-02 US US18/479,335 patent/US20240108619A1/en active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH1059841A (ja) * | 1996-02-27 | 1998-03-03 | Teijin Ltd | 吸収性が改善された粉末状経鼻投与組成物 |
| JP4721212B2 (ja) * | 2001-07-05 | 2011-07-13 | 株式会社新日本科学 | インスリンの経鼻投与用組成物 |
| JP2003206227A (ja) * | 2002-01-09 | 2003-07-22 | Translational Research株式会社 | 薬物の経鼻投与用組成物 |
| JP2006519219A (ja) * | 2003-02-28 | 2006-08-24 | ブリタニア ファーマシューティカルズ リミテッド | 鼻腔送達用医薬品組成物 |
| WO2006016530A1 (ja) * | 2004-08-10 | 2006-02-16 | Translational Research, Ltd. | 速効性でかつ高い吸収性を可能とする経鼻投与用組成物 |
| US20110171141A1 (en) * | 2009-06-26 | 2011-07-14 | Kellerman Donald J | Administration of dihydroergotamine mesylate particles using a metered dose inhaler |
Also Published As
| Publication number | Publication date |
|---|---|
| DK3049059T3 (da) | 2022-01-31 |
| ES2904570T3 (es) | 2022-04-05 |
| EP3049059A2 (en) | 2016-08-03 |
| JP2016531850A (ja) | 2016-10-13 |
| US20200179379A1 (en) | 2020-06-11 |
| US20190275036A1 (en) | 2019-09-12 |
| WO2015044782A3 (en) | 2015-06-11 |
| US20160228433A1 (en) | 2016-08-11 |
| EP3049059B1 (en) | 2021-11-03 |
| WO2015044782A2 (en) | 2015-04-02 |
| EP4008307A1 (en) | 2022-06-08 |
| JP6902583B2 (ja) | 2021-07-14 |
| US20230000860A1 (en) | 2023-01-05 |
| US20240108619A1 (en) | 2024-04-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6902583B2 (ja) | 頭痛治療用の鼻腔内dhe | |
| TWI777515B (zh) | 治療嗜伊紅性食道炎之方法 | |
| RU2769397C2 (ru) | Композиции и способы лечения передозировки опиоидами | |
| JP5886632B2 (ja) | オキシコドンおよびナロキソンを含む即時放出医薬組成物 | |
| US11890272B2 (en) | Non-sedating dexmedetomidine treatment regimens | |
| US20220226288A1 (en) | Dexmedetomidine treatment regimens | |
| JP2019520361A (ja) | アルコール使用障害の処置のための組成物、装置、及び、方法 | |
| AU2011253775B2 (en) | Compositions and Methods for Increasing Blood Platelet Levels in Humans | |
| US20200345730A1 (en) | Compositions, Devices, and Methods for Treating or Preventing Headaches | |
| JP2022514340A (ja) | 過剰摂取および報酬に基づく障害を処置するための、組成物、装置、および方法 | |
| US20240173299A1 (en) | Non-sedating dexmedetomidine treatment regimens | |
| US20230301903A1 (en) | Intranasal olanzapine formulations and methods of their use | |
| CN116801863A (zh) | 右美托咪定治疗方案 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20191003 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20191004 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20191004 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200930 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20201221 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20210115 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210526 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210621 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6902583 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |