JP2017526371A - 化合物および方法 - Google Patents
化合物および方法 Download PDFInfo
- Publication number
- JP2017526371A JP2017526371A JP2017511702A JP2017511702A JP2017526371A JP 2017526371 A JP2017526371 A JP 2017526371A JP 2017511702 A JP2017511702 A JP 2017511702A JP 2017511702 A JP2017511702 A JP 2017511702A JP 2017526371 A JP2017526371 A JP 2017526371A
- Authority
- JP
- Japan
- Prior art keywords
- cell
- antigen
- cells
- cytokine
- antigen molecule
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000000034 method Methods 0.000 title claims abstract description 167
- 150000001875 compounds Chemical class 0.000 title claims description 14
- 210000004027 cell Anatomy 0.000 claims abstract description 267
- 102000036639 antigens Human genes 0.000 claims abstract description 209
- 108091007433 antigens Proteins 0.000 claims abstract description 209
- 239000000427 antigen Substances 0.000 claims abstract description 207
- 102000004127 Cytokines Human genes 0.000 claims abstract description 109
- 108090000695 Cytokines Proteins 0.000 claims abstract description 109
- 230000028993 immune response Effects 0.000 claims abstract description 64
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 claims abstract description 59
- 230000002265 prevention Effects 0.000 claims abstract description 11
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 5
- 239000003504 photosensitizing agent Substances 0.000 claims description 128
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 60
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 claims description 57
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 54
- 238000002255 vaccination Methods 0.000 claims description 40
- 239000003814 drug Substances 0.000 claims description 38
- 229940079593 drug Drugs 0.000 claims description 35
- 208000015181 infectious disease Diseases 0.000 claims description 32
- 201000010099 disease Diseases 0.000 claims description 30
- 239000000203 mixture Substances 0.000 claims description 25
- 208000035475 disorder Diseases 0.000 claims description 24
- 210000000172 cytosol Anatomy 0.000 claims description 23
- 210000004443 dendritic cell Anatomy 0.000 claims description 23
- 206010028980 Neoplasm Diseases 0.000 claims description 22
- 238000011282 treatment Methods 0.000 claims description 22
- 229960005486 vaccine Drugs 0.000 claims description 22
- 201000011510 cancer Diseases 0.000 claims description 20
- 238000000338 in vitro Methods 0.000 claims description 19
- 210000000612 antigen-presenting cell Anatomy 0.000 claims description 16
- 108010002350 Interleukin-2 Proteins 0.000 claims description 15
- 102000000588 Interleukin-2 Human genes 0.000 claims description 15
- 108010002586 Interleukin-7 Proteins 0.000 claims description 15
- 230000030741 antigen processing and presentation Effects 0.000 claims description 15
- 230000000890 antigenic effect Effects 0.000 claims description 12
- 239000003795 chemical substances by application Substances 0.000 claims description 12
- 239000003446 ligand Substances 0.000 claims description 12
- 230000004936 stimulating effect Effects 0.000 claims description 12
- 102000003812 Interleukin-15 Human genes 0.000 claims description 11
- 108090000172 Interleukin-15 Proteins 0.000 claims description 11
- 241000699666 Mus <mouse, genus> Species 0.000 claims description 11
- 102000014150 Interferons Human genes 0.000 claims description 10
- 108010050904 Interferons Proteins 0.000 claims description 10
- 238000004519 manufacturing process Methods 0.000 claims description 10
- 230000000638 stimulation Effects 0.000 claims description 10
- 108010047761 Interferon-alpha Proteins 0.000 claims description 8
- 102000006992 Interferon-alpha Human genes 0.000 claims description 8
- 229940079322 interferon Drugs 0.000 claims description 8
- 108010074108 interleukin-21 Proteins 0.000 claims description 8
- 229920001661 Chitosan Polymers 0.000 claims description 6
- 230000001678 irradiating effect Effects 0.000 claims description 6
- OHDXDNUPVVYWOV-UHFFFAOYSA-N n-methyl-1-(2-naphthalen-1-ylsulfanylphenyl)methanamine Chemical compound CNCC1=CC=CC=C1SC1=CC=CC2=CC=CC=C12 OHDXDNUPVVYWOV-UHFFFAOYSA-N 0.000 claims description 6
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 6
- 238000002360 preparation method Methods 0.000 claims description 6
- 102000010789 Interleukin-2 Receptors Human genes 0.000 claims description 5
- 108010038453 Interleukin-2 Receptors Proteins 0.000 claims description 5
- 241000124008 Mammalia Species 0.000 claims description 5
- 239000000969 carrier Substances 0.000 claims description 5
- PBHVCRIXMXQXPD-UHFFFAOYSA-N chembl2369102 Chemical compound C1=CC(S(=O)(=O)O)=CC=C1C(C1=CC=C(N1)C(C=1C=CC(=CC=1)S(O)(=O)=O)=C1C=CC(=N1)C(C=1C=CC(=CC=1)S(O)(=O)=O)=C1C=CC(N1)=C1C=2C=CC(=CC=2)S(O)(=O)=O)=C2N=C1C=C2 PBHVCRIXMXQXPD-UHFFFAOYSA-N 0.000 claims description 5
- 239000003085 diluting agent Substances 0.000 claims description 5
- 229910052760 oxygen Inorganic materials 0.000 claims description 5
- 229940124856 vaccine component Drugs 0.000 claims description 5
- 102000016355 Granulocyte-Macrophage Colony-Stimulating Factor Receptors Human genes 0.000 claims description 4
- 108010092372 Granulocyte-Macrophage Colony-Stimulating Factor Receptors Proteins 0.000 claims description 4
- 229910005965 SO 2 Inorganic materials 0.000 claims description 4
- 229910052717 sulfur Inorganic materials 0.000 claims description 4
- AVWQQPYHYQKEIZ-UHFFFAOYSA-K trisodium;2-dodecylbenzenesulfonate;3-dodecylbenzenesulfonate;4-dodecylbenzenesulfonate Chemical compound [Na+].[Na+].[Na+].CCCCCCCCCCCCC1=CC=C(S([O-])(=O)=O)C=C1.CCCCCCCCCCCCC1=CC=CC(S([O-])(=O)=O)=C1.CCCCCCCCCCCCC1=CC=CC=C1S([O-])(=O)=O AVWQQPYHYQKEIZ-UHFFFAOYSA-K 0.000 claims description 4
- 102000042287 type II cytokine receptor family Human genes 0.000 claims description 4
- 108091052254 type II cytokine receptor family Proteins 0.000 claims description 4
- 241000251468 Actinopterygii Species 0.000 claims description 3
- 241000283690 Bos taurus Species 0.000 claims description 3
- 241000283707 Capra Species 0.000 claims description 3
- 241000283074 Equus asinus Species 0.000 claims description 3
- 241000282326 Felis catus Species 0.000 claims description 3
- 102100030703 Interleukin-22 Human genes 0.000 claims description 3
- 241000283973 Oryctolagus cuniculus Species 0.000 claims description 3
- 241001494479 Pecora Species 0.000 claims description 3
- 241000700159 Rattus Species 0.000 claims description 3
- 238000012360 testing method Methods 0.000 claims description 3
- 102000042286 type I cytokine receptor family Human genes 0.000 claims description 3
- 108091052247 type I cytokine receptor family Proteins 0.000 claims description 3
- 241000700199 Cavia porcellus Species 0.000 claims description 2
- 241000283073 Equus caballus Species 0.000 claims description 2
- 241000282898 Sus scrofa Species 0.000 claims description 2
- 102000000704 Interleukin-7 Human genes 0.000 claims 1
- 241000009328 Perro Species 0.000 claims 1
- 238000004581 coalescence Methods 0.000 claims 1
- 230000001225 therapeutic effect Effects 0.000 abstract description 8
- 230000000069 prophylactic effect Effects 0.000 abstract description 5
- 102000004457 Granulocyte-Macrophage Colony-Stimulating Factor Human genes 0.000 abstract description 3
- 238000002560 therapeutic procedure Methods 0.000 abstract description 3
- 241000699670 Mus sp. Species 0.000 description 55
- 108010058846 Ovalbumin Proteins 0.000 description 51
- 229940092253 ovalbumin Drugs 0.000 description 51
- 210000001744 T-lymphocyte Anatomy 0.000 description 43
- 102000004196 processed proteins & peptides Human genes 0.000 description 29
- 238000002649 immunization Methods 0.000 description 28
- 230000003053 immunization Effects 0.000 description 28
- 238000001727 in vivo Methods 0.000 description 28
- 150000001413 amino acids Chemical class 0.000 description 27
- 238000000684 flow cytometry Methods 0.000 description 24
- 235000001014 amino acid Nutrition 0.000 description 22
- 230000003834 intracellular effect Effects 0.000 description 22
- 102000005962 receptors Human genes 0.000 description 21
- 108020003175 receptors Proteins 0.000 description 21
- 229940024606 amino acid Drugs 0.000 description 20
- JVJGCCBAOOWGEO-RUTPOYCXSA-N (2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-4-amino-2-[[(2s,3s)-2-[[(2s,3s)-2-[[(2s)-2-azaniumyl-3-hydroxypropanoyl]amino]-3-methylpentanoyl]amino]-3-methylpentanoyl]amino]-4-oxobutanoyl]amino]-3-phenylpropanoyl]amino]-4-carboxylatobutanoyl]amino]-6-azaniumy Chemical compound OC[C@H](N)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@H](C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(O)=O)CC1=CC=CC=C1 JVJGCCBAOOWGEO-RUTPOYCXSA-N 0.000 description 19
- 230000000694 effects Effects 0.000 description 19
- 210000004369 blood Anatomy 0.000 description 16
- 239000008280 blood Substances 0.000 description 16
- 102100032912 CD44 antigen Human genes 0.000 description 14
- 101000868273 Homo sapiens CD44 antigen Proteins 0.000 description 14
- 102100021592 Interleukin-7 Human genes 0.000 description 14
- 239000007924 injection Substances 0.000 description 14
- 238000002347 injection Methods 0.000 description 14
- 108090000623 proteins and genes Proteins 0.000 description 14
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 13
- 210000004379 membrane Anatomy 0.000 description 13
- 239000012528 membrane Substances 0.000 description 13
- 241001465754 Metazoa Species 0.000 description 12
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 12
- 201000001441 melanoma Diseases 0.000 description 12
- 210000001519 tissue Anatomy 0.000 description 12
- 238000004458 analytical method Methods 0.000 description 11
- 239000000460 chlorine Substances 0.000 description 11
- 102000004169 proteins and genes Human genes 0.000 description 11
- 239000000872 buffer Substances 0.000 description 10
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 10
- 238000011081 inoculation Methods 0.000 description 10
- 239000000463 material Substances 0.000 description 10
- 235000018102 proteins Nutrition 0.000 description 10
- 108010074328 Interferon-gamma Proteins 0.000 description 9
- 108091054437 MHC class I family Proteins 0.000 description 9
- 210000003719 b-lymphocyte Anatomy 0.000 description 9
- 230000027455 binding Effects 0.000 description 9
- 210000001163 endosome Anatomy 0.000 description 9
- 210000000987 immune system Anatomy 0.000 description 9
- 229920001184 polypeptide Polymers 0.000 description 9
- 238000010186 staining Methods 0.000 description 9
- 102100037850 Interferon gamma Human genes 0.000 description 8
- 230000006870 function Effects 0.000 description 8
- 244000052769 pathogen Species 0.000 description 8
- 210000004989 spleen cell Anatomy 0.000 description 8
- 102000043129 MHC class I family Human genes 0.000 description 7
- 230000004913 activation Effects 0.000 description 7
- 230000030833 cell death Effects 0.000 description 7
- 230000001472 cytotoxic effect Effects 0.000 description 7
- 210000003743 erythrocyte Anatomy 0.000 description 7
- 238000002474 experimental method Methods 0.000 description 7
- 239000012634 fragment Substances 0.000 description 7
- 230000001965 increasing effect Effects 0.000 description 7
- 210000003712 lysosome Anatomy 0.000 description 7
- 230000001868 lysosomic effect Effects 0.000 description 7
- 239000002609 medium Substances 0.000 description 7
- 210000001616 monocyte Anatomy 0.000 description 7
- 230000004044 response Effects 0.000 description 7
- 210000000952 spleen Anatomy 0.000 description 7
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 6
- 231100000433 cytotoxic Toxicity 0.000 description 6
- 230000012202 endocytosis Effects 0.000 description 6
- 210000002865 immune cell Anatomy 0.000 description 6
- -1 photofurins Substances 0.000 description 6
- 150000004032 porphyrins Chemical class 0.000 description 6
- 230000008569 process Effects 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 230000035755 proliferation Effects 0.000 description 6
- 238000010992 reflux Methods 0.000 description 6
- 241000894007 species Species 0.000 description 6
- 238000005406 washing Methods 0.000 description 6
- 241000282412 Homo Species 0.000 description 5
- 102100040019 Interferon alpha-1/13 Human genes 0.000 description 5
- 108091008874 T cell receptors Proteins 0.000 description 5
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 5
- 239000002671 adjuvant Substances 0.000 description 5
- 230000037396 body weight Effects 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- 210000004698 lymphocyte Anatomy 0.000 description 5
- 210000002540 macrophage Anatomy 0.000 description 5
- 229940023041 peptide vaccine Drugs 0.000 description 5
- 230000002165 photosensitisation Effects 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- 210000000130 stem cell Anatomy 0.000 description 5
- MVBCOYVJSZKRIV-UHFFFAOYSA-N 4-[10,15-diphenyl-20-(4-sulfophenyl)-2,3,22,24-tetrahydroporphyrin-5-yl]benzenesulfonic acid Chemical compound C1=CC(S(=O)(=O)O)=CC=C1C(C1=CC=C(N1)C(C=1C=CC=CC=1)=C1C=CC(=N1)C(C=1C=CC=CC=1)=C1C=CC(N1)=C1C=2C=CC(=CC=2)S(O)(=O)=O)=C2N=C1CC2 MVBCOYVJSZKRIV-UHFFFAOYSA-N 0.000 description 4
- 101000959820 Homo sapiens Interferon alpha-1/13 Proteins 0.000 description 4
- 102000015696 Interleukins Human genes 0.000 description 4
- 108010063738 Interleukins Proteins 0.000 description 4
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 4
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 4
- 210000001015 abdomen Anatomy 0.000 description 4
- HUVXQFBFIFIDDU-UHFFFAOYSA-N aluminum phthalocyanine Chemical class [Al+3].C12=CC=CC=C2C(N=C2[N-]C(C3=CC=CC=C32)=N2)=NC1=NC([C]1C=CC=CC1=1)=NC=1N=C1[C]3C=CC=CC3=C2[N-]1 HUVXQFBFIFIDDU-UHFFFAOYSA-N 0.000 description 4
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 4
- 239000002552 dosage form Substances 0.000 description 4
- 210000002443 helper t lymphocyte Anatomy 0.000 description 4
- 239000004615 ingredient Substances 0.000 description 4
- 230000007246 mechanism Effects 0.000 description 4
- 230000001404 mediated effect Effects 0.000 description 4
- 210000000822 natural killer cell Anatomy 0.000 description 4
- 210000004988 splenocyte Anatomy 0.000 description 4
- 238000006467 substitution reaction Methods 0.000 description 4
- 230000002195 synergetic effect Effects 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- YNHJECZULSZAQK-UHFFFAOYSA-N tetraphenylporphyrin Chemical class C1=CC(C(=C2C=CC(N2)=C(C=2C=CC=CC=2)C=2C=CC(N=2)=C(C=2C=CC=CC=2)C2=CC=C3N2)C=2C=CC=CC=2)=NC1=C3C1=CC=CC=C1 YNHJECZULSZAQK-UHFFFAOYSA-N 0.000 description 4
- 231100000331 toxic Toxicity 0.000 description 4
- 230000002588 toxic effect Effects 0.000 description 4
- 102000003390 tumor necrosis factor Human genes 0.000 description 4
- PVOAHINGSUIXLS-UHFFFAOYSA-N 1-Methylpiperazine Chemical compound CN1CCNCC1 PVOAHINGSUIXLS-UHFFFAOYSA-N 0.000 description 3
- JOMNTHCQHJPVAZ-UHFFFAOYSA-N 2-methylpiperazine Chemical compound CC1CNCCN1 JOMNTHCQHJPVAZ-UHFFFAOYSA-N 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- 102000008949 Histocompatibility Antigens Class I Human genes 0.000 description 3
- 101000767631 Human papillomavirus type 16 Protein E7 Proteins 0.000 description 3
- 102000018682 Interleukin Receptor Common gamma Subunit Human genes 0.000 description 3
- 108010066719 Interleukin Receptor Common gamma Subunit Proteins 0.000 description 3
- 102000004388 Interleukin-4 Human genes 0.000 description 3
- 108090000978 Interleukin-4 Proteins 0.000 description 3
- 102000010782 Interleukin-7 Receptors Human genes 0.000 description 3
- 108010038498 Interleukin-7 Receptors Proteins 0.000 description 3
- 102000002689 Toll-like receptor Human genes 0.000 description 3
- 108020000411 Toll-like receptor Proteins 0.000 description 3
- 208000036142 Viral infection Diseases 0.000 description 3
- 230000002159 abnormal effect Effects 0.000 description 3
- 230000003213 activating effect Effects 0.000 description 3
- 238000007792 addition Methods 0.000 description 3
- 230000008033 biological extinction Effects 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 210000001185 bone marrow Anatomy 0.000 description 3
- 230000010261 cell growth Effects 0.000 description 3
- 210000000170 cell membrane Anatomy 0.000 description 3
- 230000036755 cellular response Effects 0.000 description 3
- SURLGNKAQXKNSP-DBLYXWCISA-N chlorin Chemical compound C\1=C/2\N/C(=C\C3=N/C(=C\C=4NC(/C=C\5/C=CC/1=N/5)=CC=4)/C=C3)/CC\2 SURLGNKAQXKNSP-DBLYXWCISA-N 0.000 description 3
- 150000004035 chlorins Chemical class 0.000 description 3
- 238000003776 cleavage reaction Methods 0.000 description 3
- 230000003013 cytotoxicity Effects 0.000 description 3
- 231100000135 cytotoxicity Toxicity 0.000 description 3
- 230000004069 differentiation Effects 0.000 description 3
- 238000000295 emission spectrum Methods 0.000 description 3
- 230000002708 enhancing effect Effects 0.000 description 3
- 230000012010 growth Effects 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 230000001900 immune effect Effects 0.000 description 3
- 230000001976 improved effect Effects 0.000 description 3
- 229940028885 interleukin-4 Drugs 0.000 description 3
- 230000002601 intratumoral effect Effects 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- 210000000265 leukocyte Anatomy 0.000 description 3
- 244000144972 livestock Species 0.000 description 3
- 210000001165 lymph node Anatomy 0.000 description 3
- 201000006417 multiple sclerosis Diseases 0.000 description 3
- 150000007523 nucleic acids Chemical class 0.000 description 3
- 239000000816 peptidomimetic Substances 0.000 description 3
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 3
- 208000017983 photosensitivity disease Diseases 0.000 description 3
- 231100000434 photosensitization Toxicity 0.000 description 3
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 3
- 230000007017 scission Effects 0.000 description 3
- 230000019491 signal transduction Effects 0.000 description 3
- 230000011664 signaling Effects 0.000 description 3
- 238000010561 standard procedure Methods 0.000 description 3
- 238000011200 topical administration Methods 0.000 description 3
- 230000001960 triggered effect Effects 0.000 description 3
- 230000009385 viral infection Effects 0.000 description 3
- LSTRKXWIZZZYAS-UHFFFAOYSA-N 2-bromoacetyl bromide Chemical compound BrCC(Br)=O LSTRKXWIZZZYAS-UHFFFAOYSA-N 0.000 description 2
- VRGCYEIGVVTZCC-UHFFFAOYSA-N 3,4,5,6-tetrachlorocyclohexa-3,5-diene-1,2-dione Chemical compound ClC1=C(Cl)C(=O)C(=O)C(Cl)=C1Cl VRGCYEIGVVTZCC-UHFFFAOYSA-N 0.000 description 2
- ICGLPKIVTVWCFT-UHFFFAOYSA-N 4-methylbenzenesulfonohydrazide Chemical compound CC1=CC=C(S(=O)(=O)NN)C=C1 ICGLPKIVTVWCFT-UHFFFAOYSA-N 0.000 description 2
- UJKPHYRXOLRVJJ-MLSVHJFASA-N CC(O)C1=C(C)/C2=C/C3=N/C(=C\C4=C(CCC(O)=O)C(C)=C(N4)/C=C4\N=C(\C=C\1/N\2)C(C)=C4C(C)O)/C(CCC(O)=O)=C3C Chemical class CC(O)C1=C(C)/C2=C/C3=N/C(=C\C4=C(CCC(O)=O)C(C)=C(N4)/C=C4\N=C(\C=C\1/N\2)C(C)=C4C(C)O)/C(CCC(O)=O)=C3C UJKPHYRXOLRVJJ-MLSVHJFASA-N 0.000 description 2
- 241000282472 Canis lupus familiaris Species 0.000 description 2
- 108010078791 Carrier Proteins Proteins 0.000 description 2
- 102000000844 Cell Surface Receptors Human genes 0.000 description 2
- 108010001857 Cell Surface Receptors Proteins 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 102000003886 Glycoproteins Human genes 0.000 description 2
- 108090000288 Glycoproteins Proteins 0.000 description 2
- 206010018910 Haemolysis Diseases 0.000 description 2
- 102000003745 Hepatocyte Growth Factor Human genes 0.000 description 2
- 108090000100 Hepatocyte Growth Factor Proteins 0.000 description 2
- 241000238631 Hexapoda Species 0.000 description 2
- 101000852870 Homo sapiens Interferon alpha/beta receptor 1 Proteins 0.000 description 2
- 101001001420 Homo sapiens Interferon gamma receptor 1 Proteins 0.000 description 2
- 101000917826 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor II-a Proteins 0.000 description 2
- 101000917824 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor II-b Proteins 0.000 description 2
- 102100036714 Interferon alpha/beta receptor 1 Human genes 0.000 description 2
- 102100035678 Interferon gamma receptor 1 Human genes 0.000 description 2
- 108010017411 Interleukin-21 Receptors Proteins 0.000 description 2
- 102000004527 Interleukin-21 Receptors Human genes 0.000 description 2
- 102000000646 Interleukin-3 Human genes 0.000 description 2
- 108010002386 Interleukin-3 Proteins 0.000 description 2
- YQEZLKZALYSWHR-UHFFFAOYSA-N Ketamine Chemical compound C=1C=CC=C(Cl)C=1C1(NC)CCCCC1=O YQEZLKZALYSWHR-UHFFFAOYSA-N 0.000 description 2
- 102100029204 Low affinity immunoglobulin gamma Fc region receptor II-a Human genes 0.000 description 2
- 102000043131 MHC class II family Human genes 0.000 description 2
- 108091054438 MHC class II family Proteins 0.000 description 2
- 108010075205 OVA-8 Proteins 0.000 description 2
- 229930040373 Paraformaldehyde Natural products 0.000 description 2
- 108010043958 Peptoids Proteins 0.000 description 2
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 2
- 230000006044 T cell activation Effects 0.000 description 2
- 230000024932 T cell mediated immunity Effects 0.000 description 2
- 230000005867 T cell response Effects 0.000 description 2
- 206010043376 Tetanus Diseases 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 210000000628 antibody-producing cell Anatomy 0.000 description 2
- 230000002238 attenuated effect Effects 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- BHPNXACHQYJJJS-UHFFFAOYSA-N bacteriochlorin Chemical compound N1C(C=C2N=C(C=C3NC(=C4)C=C3)CC2)=CC=C1C=C1CCC4=N1 BHPNXACHQYJJJS-UHFFFAOYSA-N 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 238000009566 cancer vaccine Methods 0.000 description 2
- 229940022399 cancer vaccine Drugs 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 230000020411 cell activation Effects 0.000 description 2
- 239000006143 cell culture medium Substances 0.000 description 2
- 230000005779 cell damage Effects 0.000 description 2
- 230000024245 cell differentiation Effects 0.000 description 2
- 208000037887 cell injury Diseases 0.000 description 2
- 239000006285 cell suspension Substances 0.000 description 2
- 230000003833 cell viability Effects 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- 208000030499 combat disease Diseases 0.000 description 2
- 229940125898 compound 5 Drugs 0.000 description 2
- 230000009089 cytolysis Effects 0.000 description 2
- 230000001086 cytosolic effect Effects 0.000 description 2
- 230000007123 defense Effects 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 238000012217 deletion Methods 0.000 description 2
- 230000037430 deletion Effects 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 210000002472 endoplasmic reticulum Anatomy 0.000 description 2
- 230000002538 fungal effect Effects 0.000 description 2
- 239000003102 growth factor Substances 0.000 description 2
- 230000003394 haemopoietic effect Effects 0.000 description 2
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 2
- 230000008588 hemolysis Effects 0.000 description 2
- 230000036039 immunity Effects 0.000 description 2
- 230000016784 immunoglobulin production Effects 0.000 description 2
- 238000011065 in-situ storage Methods 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 238000001802 infusion Methods 0.000 description 2
- 229940047124 interferons Drugs 0.000 description 2
- 230000004073 interleukin-2 production Effects 0.000 description 2
- 229940047122 interleukins Drugs 0.000 description 2
- 238000010212 intracellular staining Methods 0.000 description 2
- 239000007928 intraperitoneal injection Substances 0.000 description 2
- 229960003299 ketamine Drugs 0.000 description 2
- 239000012139 lysis buffer Substances 0.000 description 2
- 210000004962 mammalian cell Anatomy 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 description 2
- 102000039446 nucleic acids Human genes 0.000 description 2
- 108020004707 nucleic acids Proteins 0.000 description 2
- 210000003463 organelle Anatomy 0.000 description 2
- 229920002866 paraformaldehyde Polymers 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 235000019260 propionic acid Nutrition 0.000 description 2
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 238000007910 systemic administration Methods 0.000 description 2
- 239000003053 toxin Substances 0.000 description 2
- 231100000765 toxin Toxicity 0.000 description 2
- 108700012359 toxins Proteins 0.000 description 2
- 230000009261 transgenic effect Effects 0.000 description 2
- 230000032258 transport Effects 0.000 description 2
- 210000003462 vein Anatomy 0.000 description 2
- 230000003612 virological effect Effects 0.000 description 2
- BPICBUSOMSTKRF-UHFFFAOYSA-N xylazine Chemical compound CC1=CC=CC(C)=C1NC1=NCCCS1 BPICBUSOMSTKRF-UHFFFAOYSA-N 0.000 description 2
- 229960001600 xylazine Drugs 0.000 description 2
- UAOUIVVJBYDFKD-XKCDOFEDSA-N (1R,9R,10S,11R,12R,15S,18S,21R)-10,11,21-trihydroxy-8,8-dimethyl-14-methylidene-4-(prop-2-enylamino)-20-oxa-5-thia-3-azahexacyclo[9.7.2.112,15.01,9.02,6.012,18]henicosa-2(6),3-dien-13-one Chemical compound C([C@@H]1[C@@H](O)[C@@]23C(C1=C)=O)C[C@H]2[C@]12C(N=C(NCC=C)S4)=C4CC(C)(C)[C@H]1[C@H](O)[C@]3(O)OC2 UAOUIVVJBYDFKD-XKCDOFEDSA-N 0.000 description 1
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 1
- HMSMOZAIMDNRBW-UHFFFAOYSA-N 100572-96-1 Chemical compound C1=CC2=NC1=CC=C(N1)C=CC1=C(N1)C=CC1=CC=C1C=CC2=N1 HMSMOZAIMDNRBW-UHFFFAOYSA-N 0.000 description 1
- YEDUAINPPJYDJZ-UHFFFAOYSA-N 2-hydroxybenzothiazole Chemical compound C1=CC=C2SC(O)=NC2=C1 YEDUAINPPJYDJZ-UHFFFAOYSA-N 0.000 description 1
- RSEBUVRVKCANEP-UHFFFAOYSA-N 2-pyrroline Chemical compound C1CC=CN1 RSEBUVRVKCANEP-UHFFFAOYSA-N 0.000 description 1
- MHIITNFQDPFSES-UHFFFAOYSA-N 25,26,27,28-tetrazahexacyclo[16.6.1.13,6.18,11.113,16.019,24]octacosa-1(25),2,4,6,8(27),9,11,13,15,17,19,21,23-tridecaene Chemical class N1C(C=C2C3=CC=CC=C3C(C=C3NC(=C4)C=C3)=N2)=CC=C1C=C1C=CC4=N1 MHIITNFQDPFSES-UHFFFAOYSA-N 0.000 description 1
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 1
- ZGXJTSGNIOSYLO-UHFFFAOYSA-N 88755TAZ87 Chemical compound NCC(=O)CCC(O)=O ZGXJTSGNIOSYLO-UHFFFAOYSA-N 0.000 description 1
- 208000030507 AIDS Diseases 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- 241000714266 Bovine leukemia virus Species 0.000 description 1
- 241000208199 Buxus sempervirens Species 0.000 description 1
- ZJVHUBRPWHTDAZ-UHFFFAOYSA-N C1=CC=CC=C1Cl(C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 Chemical compound C1=CC=CC=C1Cl(C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 ZJVHUBRPWHTDAZ-UHFFFAOYSA-N 0.000 description 1
- 0 CC(C(C)(C)N1CC*CC1)C(C)=O Chemical compound CC(C(C)(C)N1CC*CC1)C(C)=O 0.000 description 1
- 101150013553 CD40 gene Proteins 0.000 description 1
- SIVLAIGVJZOYPH-FOJLVQLTSA-N CNc(cc1)ccc1/C(/C(C=C1)=N/C1=C(\c1ccc(/C(/c2ccccc2)=C2\N=C3CC2)[nH]1)/c1ccccc1)=C(\C=C1)/N/C1=C3/c1ccccc1 Chemical compound CNc(cc1)ccc1/C(/C(C=C1)=N/C1=C(\c1ccc(/C(/c2ccccc2)=C2\N=C3CC2)[nH]1)/c1ccccc1)=C(\C=C1)/N/C1=C3/c1ccccc1 SIVLAIGVJZOYPH-FOJLVQLTSA-N 0.000 description 1
- 241000701931 Canine parvovirus Species 0.000 description 1
- 108090000565 Capsid Proteins Proteins 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 102000014914 Carrier Proteins Human genes 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 102000019034 Chemokines Human genes 0.000 description 1
- 108010012236 Chemokines Proteins 0.000 description 1
- VGCXGMAHQTYDJK-UHFFFAOYSA-N Chloroacetyl chloride Chemical compound ClCC(Cl)=O VGCXGMAHQTYDJK-UHFFFAOYSA-N 0.000 description 1
- 108010071942 Colony-Stimulating Factors Proteins 0.000 description 1
- 101100193633 Danio rerio rag2 gene Proteins 0.000 description 1
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 208000031886 HIV Infections Diseases 0.000 description 1
- 208000037357 HIV infectious disease Diseases 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 108010088652 Histocompatibility Antigens Class I Proteins 0.000 description 1
- 101001034829 Homo sapiens Interferon alpha-10 Proteins 0.000 description 1
- 101001034828 Homo sapiens Interferon alpha-14 Proteins 0.000 description 1
- 101001034835 Homo sapiens Interferon alpha-16 Proteins 0.000 description 1
- 101001034834 Homo sapiens Interferon alpha-17 Proteins 0.000 description 1
- 101000959794 Homo sapiens Interferon alpha-2 Proteins 0.000 description 1
- 101001034833 Homo sapiens Interferon alpha-21 Proteins 0.000 description 1
- 101000959708 Homo sapiens Interferon alpha-4 Proteins 0.000 description 1
- 101000959704 Homo sapiens Interferon alpha-5 Proteins 0.000 description 1
- 101000959714 Homo sapiens Interferon alpha-6 Proteins 0.000 description 1
- 101000961126 Homo sapiens Interferon alpha-7 Proteins 0.000 description 1
- 101000999391 Homo sapiens Interferon alpha-8 Proteins 0.000 description 1
- 101000852865 Homo sapiens Interferon alpha/beta receptor 2 Proteins 0.000 description 1
- 101000599613 Homo sapiens Interferon lambda receptor 1 Proteins 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 102000002227 Interferon Type I Human genes 0.000 description 1
- 108010014726 Interferon Type I Proteins 0.000 description 1
- 101710192051 Interferon alpha-1/13 Proteins 0.000 description 1
- 102100039734 Interferon alpha-10 Human genes 0.000 description 1
- 102100039733 Interferon alpha-14 Human genes 0.000 description 1
- 102100039728 Interferon alpha-16 Human genes 0.000 description 1
- 102100039730 Interferon alpha-17 Human genes 0.000 description 1
- 102100040018 Interferon alpha-2 Human genes 0.000 description 1
- 102100039729 Interferon alpha-21 Human genes 0.000 description 1
- 102100039949 Interferon alpha-4 Human genes 0.000 description 1
- 102100039948 Interferon alpha-5 Human genes 0.000 description 1
- 102100040007 Interferon alpha-6 Human genes 0.000 description 1
- 102100039350 Interferon alpha-7 Human genes 0.000 description 1
- 102100036532 Interferon alpha-8 Human genes 0.000 description 1
- 102100036718 Interferon alpha/beta receptor 2 Human genes 0.000 description 1
- 102100026720 Interferon beta Human genes 0.000 description 1
- 102100036157 Interferon gamma receptor 2 Human genes 0.000 description 1
- 102100037971 Interferon lambda receptor 1 Human genes 0.000 description 1
- 108090000467 Interferon-beta Proteins 0.000 description 1
- 102000008070 Interferon-gamma Human genes 0.000 description 1
- 102000004556 Interleukin-15 Receptors Human genes 0.000 description 1
- 108010017535 Interleukin-15 Receptors Proteins 0.000 description 1
- 102000010790 Interleukin-3 Receptors Human genes 0.000 description 1
- 108010038452 Interleukin-3 Receptors Proteins 0.000 description 1
- 102000010787 Interleukin-4 Receptors Human genes 0.000 description 1
- 108010038486 Interleukin-4 Receptors Proteins 0.000 description 1
- 102100039897 Interleukin-5 Human genes 0.000 description 1
- 108010002616 Interleukin-5 Proteins 0.000 description 1
- 102000010786 Interleukin-5 Receptors Human genes 0.000 description 1
- 108010038484 Interleukin-5 Receptors Proteins 0.000 description 1
- 102000010682 Interleukin-9 Receptors Human genes 0.000 description 1
- 108010038414 Interleukin-9 Receptors Proteins 0.000 description 1
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical group [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 1
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 1
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 102000008072 Lymphokines Human genes 0.000 description 1
- 108010074338 Lymphokines Proteins 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 102000007651 Macrophage Colony-Stimulating Factor Human genes 0.000 description 1
- 108010046938 Macrophage Colony-Stimulating Factor Proteins 0.000 description 1
- 201000005505 Measles Diseases 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 206010027480 Metastatic malignant melanoma Diseases 0.000 description 1
- 101100193635 Mus musculus Rag2 gene Proteins 0.000 description 1
- 108010049175 N-substituted Glycines Proteins 0.000 description 1
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- 108010038807 Oligopeptides Proteins 0.000 description 1
- 102000015636 Oligopeptides Human genes 0.000 description 1
- 108700020796 Oncogene Proteins 0.000 description 1
- 208000000474 Poliomyelitis Diseases 0.000 description 1
- 102000004245 Proteasome Endopeptidase Complex Human genes 0.000 description 1
- 108090000708 Proteasome Endopeptidase Complex Proteins 0.000 description 1
- 108010076504 Protein Sorting Signals Proteins 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 230000020385 T cell costimulation Effects 0.000 description 1
- 230000006052 T cell proliferation Effects 0.000 description 1
- 108030001722 Tentoxilysin Proteins 0.000 description 1
- 239000004098 Tetracycline Substances 0.000 description 1
- 210000000068 Th17 cell Anatomy 0.000 description 1
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 1
- 239000004473 Threonine Substances 0.000 description 1
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 1
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 description 1
- 102100040245 Tumor necrosis factor receptor superfamily member 5 Human genes 0.000 description 1
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 1
- 241000700647 Variola virus Species 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- 238000000862 absorption spectrum Methods 0.000 description 1
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 description 1
- 239000012346 acetyl chloride Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000033289 adaptive immune response Effects 0.000 description 1
- 210000005006 adaptive immune system Anatomy 0.000 description 1
- 230000004721 adaptive immunity Effects 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 229960002749 aminolevulinic acid Drugs 0.000 description 1
- 230000003042 antagnostic effect Effects 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 229960001230 asparagine Drugs 0.000 description 1
- 235000009582 asparagine Nutrition 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- 150000004036 bacteriochlorins Chemical class 0.000 description 1
- 210000003651 basophil Anatomy 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 230000036760 body temperature Effects 0.000 description 1
- KQNZDYYTLMIZCT-KQPMLPITSA-N brefeldin A Chemical compound O[C@@H]1\C=C\C(=O)O[C@@H](C)CCC\C=C\[C@@H]2C[C@H](O)C[C@H]21 KQNZDYYTLMIZCT-KQPMLPITSA-N 0.000 description 1
- JUMGSHROWPPKFX-UHFFFAOYSA-N brefeldin-A Natural products CC1CCCC=CC2(C)CC(O)CC2(C)C(O)C=CC(=O)O1 JUMGSHROWPPKFX-UHFFFAOYSA-N 0.000 description 1
- 210000004899 c-terminal region Anatomy 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 230000008568 cell cell communication Effects 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000003915 cell function Effects 0.000 description 1
- 230000011748 cell maturation Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 229940030156 cell vaccine Drugs 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 210000003850 cellular structure Anatomy 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000007385 chemical modification Methods 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 229940126086 compound 21 Drugs 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 102000003675 cytokine receptors Human genes 0.000 description 1
- 108010057085 cytokine receptors Proteins 0.000 description 1
- 238000004163 cytometry Methods 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 239000012636 effector Substances 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 210000002257 embryonic structure Anatomy 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 210000003979 eosinophil Anatomy 0.000 description 1
- 230000008029 eradication Effects 0.000 description 1
- 210000003527 eukaryotic cell Anatomy 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 210000003918 fraction a Anatomy 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 210000002175 goblet cell Anatomy 0.000 description 1
- 210000002288 golgi apparatus Anatomy 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 239000003324 growth hormone secretagogue Substances 0.000 description 1
- 150000003278 haem Chemical class 0.000 description 1
- 229960003569 hematoporphyrin Drugs 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 239000000833 heterodimer Substances 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 230000013632 homeostatic process Effects 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 208000033519 human immunodeficiency virus infectious disease Diseases 0.000 description 1
- 230000004727 humoral immunity Effects 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 1
- 230000002163 immunogen Effects 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 239000000367 immunologic factor Substances 0.000 description 1
- 239000002955 immunomodulating agent Substances 0.000 description 1
- 229940121354 immunomodulator Drugs 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 206010022000 influenza Diseases 0.000 description 1
- 230000015788 innate immune response Effects 0.000 description 1
- 210000005007 innate immune system Anatomy 0.000 description 1
- 229960003130 interferon gamma Drugs 0.000 description 1
- 108010085650 interferon gamma receptor Proteins 0.000 description 1
- 108010018844 interferon type III Proteins 0.000 description 1
- 210000002490 intestinal epithelial cell Anatomy 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 210000004020 intracellular membrane Anatomy 0.000 description 1
- 230000031146 intracellular signal transduction Effects 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 229960000310 isoleucine Drugs 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 210000004324 lymphatic system Anatomy 0.000 description 1
- 230000002132 lysosomal effect Effects 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 208000021039 metastatic melanoma Diseases 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- CXKWCBBOMKCUKX-UHFFFAOYSA-M methylene blue Chemical compound [Cl-].C1=CC(N(C)C)=CC2=[S+]C3=CC(N(C)C)=CC=C3N=C21 CXKWCBBOMKCUKX-UHFFFAOYSA-M 0.000 description 1
- 229960000907 methylthioninium chloride Drugs 0.000 description 1
- 238000000386 microscopy Methods 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 210000003643 myeloid progenitor cell Anatomy 0.000 description 1
- SHXOKQKTZJXHHR-UHFFFAOYSA-N n,n-diethyl-5-iminobenzo[a]phenoxazin-9-amine;hydrochloride Chemical compound [Cl-].C1=CC=C2C3=NC4=CC=C(N(CC)CC)C=C4OC3=CC(=[NH2+])C2=C1 SHXOKQKTZJXHHR-UHFFFAOYSA-N 0.000 description 1
- OLAPPGSPBNVTRF-UHFFFAOYSA-N naphthalene-1,4,5,8-tetracarboxylic acid Chemical compound C1=CC(C(O)=O)=C2C(C(=O)O)=CC=C(C(O)=O)C2=C1C(O)=O OLAPPGSPBNVTRF-UHFFFAOYSA-N 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 244000045947 parasite Species 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 229940125667 peptide vaccine candidate Drugs 0.000 description 1
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 1
- 230000000886 photobiology Effects 0.000 description 1
- 238000007747 plating Methods 0.000 description 1
- 229920002704 polyhistidine Polymers 0.000 description 1
- 229940115272 polyinosinic:polycytidylic acid Drugs 0.000 description 1
- 230000008092 positive effect Effects 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 230000004952 protein activity Effects 0.000 description 1
- 230000012846 protein folding Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 150000003233 pyrroles Chemical class 0.000 description 1
- ZVJHJDDKYZXRJI-UHFFFAOYSA-N pyrroline Natural products C1CC=NC1 ZVJHJDDKYZXRJI-UHFFFAOYSA-N 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 239000003642 reactive oxygen metabolite Substances 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 238000012770 revaccination Methods 0.000 description 1
- 239000011435 rock Substances 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 210000002955 secretory cell Anatomy 0.000 description 1
- 239000012679 serum free medium Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 229940031626 subunit vaccine Drugs 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- CWXPZXBSDSIRCS-UHFFFAOYSA-N tert-butyl piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCNCC1 CWXPZXBSDSIRCS-UHFFFAOYSA-N 0.000 description 1
- BCNZYOJHNLTNEZ-UHFFFAOYSA-N tert-butyldimethylsilyl chloride Chemical compound CC(C)(C)[Si](C)(C)Cl BCNZYOJHNLTNEZ-UHFFFAOYSA-N 0.000 description 1
- FPGGTKZVZWFYPV-UHFFFAOYSA-M tetrabutylammonium fluoride Chemical compound [F-].CCCC[N+](CCCC)(CCCC)CCCC FPGGTKZVZWFYPV-UHFFFAOYSA-M 0.000 description 1
- UGNWTBMOAKPKBL-UHFFFAOYSA-N tetrachloro-1,4-benzoquinone Chemical compound ClC1=C(Cl)C(=O)C(Cl)=C(Cl)C1=O UGNWTBMOAKPKBL-UHFFFAOYSA-N 0.000 description 1
- 235000019364 tetracycline Nutrition 0.000 description 1
- 150000003522 tetracyclines Chemical class 0.000 description 1
- 229940040944 tetracyclines Drugs 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- AYEKOFBPNLCAJY-UHFFFAOYSA-O thiamine pyrophosphate Chemical compound CC1=C(CCOP(O)(=O)OP(O)(O)=O)SC=[N+]1CC1=CN=C(C)N=C1N AYEKOFBPNLCAJY-UHFFFAOYSA-O 0.000 description 1
- 210000001541 thymus gland Anatomy 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 210000003956 transport vesicle Anatomy 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 102000003298 tumor necrosis factor receptor Human genes 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- DAFUFNRZWDWXJP-UHFFFAOYSA-N uroporphyrin i Chemical compound N1C(C=C2C(=C(CC(O)=O)C(C=C3C(=C(CC(O)=O)C(=C4)N3)CCC(O)=O)=N2)CCC(O)=O)=C(CC(O)=O)C(CCC(O)=O)=C1C=C1C(CC(O)=O)=C(CCC(=O)O)C4=N1 DAFUFNRZWDWXJP-UHFFFAOYSA-N 0.000 description 1
- 239000004474 valine Substances 0.000 description 1
- 231100000513 vascular toxicity Toxicity 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 238000001429 visible spectrum Methods 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K41/00—Medicinal preparations obtained by treating materials with wave energy or particle radiation ; Therapies using these preparations
- A61K41/0042—Photocleavage of drugs in vivo, e.g. cleavage of photolabile linkers in vivo by UV radiation for releasing the pharmacologically-active agent from the administered agent; photothrombosis or photoocclusion
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K41/00—Medicinal preparations obtained by treating materials with wave energy or particle radiation ; Therapies using these preparations
- A61K41/0057—Photodynamic therapy with a photosensitizer, i.e. agent able to produce reactive oxygen species upon exposure to light or radiation, e.g. UV or visible light; photocleavage of nucleic acids with an agent
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/549—Sugars, nucleosides, nucleotides or nucleic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/515—Animal cells
- A61K2039/5154—Antigen presenting cells [APCs], e.g. dendritic cells or macrophages
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Polysaccharides And Polysaccharide Derivatives (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicinal Preparation (AREA)
- Peptides Or Proteins (AREA)
Abstract
Description
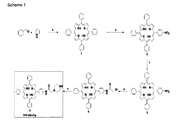
Rは該化合物においてn回現れ、
前記総Rn基の0.1%〜99.9%(好ましくは0.5%〜99.5%)において、各Rは、
と
と、から選択されるA基であり、
各R基は同一であっても異なっていてもよく、
前記総Rn基の0.1%〜99.9%(好ましくは0.5%〜99.5%)において、各Rは
R2は
と、から選択される基であり、
R3は
と、から選択される基であり、
R4は、同一であっても異なっていてもよいが、H、−OH、−OCH3、−CH3、−COCH3、C(CH3)4、−NH2、−NHCH3、−N(CH3)2、および−NCOCH3から選択される基(o位、m位、またはp位が置換されている)であり、好ましくはHである。]
と、から選択されるB基であり、
各R基は同一であっても異なっていてもよい。
17: B:25%、A:75%
19: B:25%、A:75%
33: B:10%、A:90%
37: B:10%、A:90%
実施例1:インビボでのOVAの接種に対するサイトカインの効果
材料および方法
マウス
C57BL/6マウスを、ハーラン社(Harlan)(ホルスト、オランダ)から購入する。オボアルブミン(OVA)のMHCクラスI制限エピトープOVA257-264を認識するT細胞受容体についてトランスジェニックであるOT−Iマウスを、チューリッヒ大学の施設内で飼育する(もともとは、タコニック・ヨーロッパ(Taconic Europe)(リュー、デンマーク)から購入)。全てのマウスは、特定病原体を除去した(SPF)条件下で飼育し、行った手順は、スイス家畜当局によって承認されている。OT−1マウスにおいて、T細胞受容体の遺伝子は、これらのマウスのCD8+ T細胞(OT−1細胞と呼ぶ)のほぼ全てが、オボアルブミン(OVA)抗原の特定のペプチドエピトープ(SIINFEKL)を特異的に認識するように設計される。
0日目に、雌のC57BL/6マウスの尾静脈に、Rag2/OT−1マウスの脾細胞1.5×106個を静脈注射する。このように、接種されたマウスは、OVAのSIINFEKLエピトープが、抗原提示細胞のMHCクラスIで適切に提示された場合に限り、OVAのSIINFEKLエピトープに応答することができるCD8 T細胞の「バックグラウンド」を有する。したがって、OT−1細胞を移植することによって、接種されたマウスにおける検出システムが「増強」され、抗原特異的CD8+ T細胞並びにIFN−γおよびIL−2の産生を測定することによって、インビボでの接種の効果を容易に分析することが可能になる。
4時間後に、動物の腹腔に皮内接種を行う(以下に明示される成分を含む溶液を2×50 μl)。4匹ずつの14群に対し、以下の全用量を与える。
1群:250μg TPCS2a(アンフィネックス(Amphinex))+10μg オボアルブミン(OVA、グレードV、シグマ・アルドリッチ社(Sigma-Aldrich))
2群:250μg TPCS2a+10μg オボアルブミン+10μg GM−CSF
3群:250μg TPCS2a+10μg オボアルブミン+500000IU IL−2
4群:250μg TPCS2a+10μg オボアルブミン+10μg IL−7
5群:250μg TPCS2a+10μg オボアルブミン+10μg IL−15
6群:250μg TPCS2a+10μg オボアルブミン+10μg IL−21
7群:250μg TPCS2a+10μg オボアルブミン+3,000,000IU IFNα
8群:10μg オボアルブミン
9群:10μg オボアルブミン+25μg GM−CSF
10群:10μg オボアルブミン+500,000IU IL−2
11群:10μg オボアルブミン+10μg IL−7
12群:10μg オボアルブミン+10μg IL−15
13群:10μg オボアルブミン+10μg IL−21
14群:10μg オボアルブミン+3,000,000IU IFNα
1日目に、1〜7群の動物に麻酔をかけ、ルミソース(LumiSource)ランプ(PCIバイオテクAS社(PCI Biotech AS))を用いて、青色光を6分間照射する。抗原溶液を注射してから約18時間後に動物に照射を行う。照射のフルエンス率は、約13mW/cm2である。7日目に、マウスの尾静脈から採血し、フローサイトメトリー解析(下記プロトコール参照)のために、血液細胞をSIINFEKLペンタマー(プロイミューン社(ProImmune))、CD8抗体、およびCD44抗体で染色する。14日目に、マウスを安楽死させ、脾臓を採取する。脾細胞の一定分量をSIINFEKLペプチド(EMCマイクロコレクション社(EMC microcollections)、テュービンゲン、ドイツ)で再刺激し、細胞内IFN−γの発現を見るために染色し、フローサイトメトリー解析によって解析する(以下参照)。脾細胞の別の一定分量を細胞培養液に再懸濁し、再刺激を行わずにこの培地中で一晩(単に、実施上の理由のため)おき、上述のようにSIINFEKLペンタマーで染色して、フローサイトメトリーによって解析する(下記プロトコール参照)。
細胞培地に再懸濁し、再刺激を行わずにこの培地中で一晩(単に、実施上の理由のため)おいた細胞に対して、脾臓細胞に対するSIINFEKLペンタマー染色およびフローサイトメトリーを行う。
尾から、全血を5〜10滴採取し、赤血球溶解溶液(シグマ社(Sigma))を0.5ml加える。5〜6分後、細胞を遠沈させ、0.5mlのPBSで2回洗浄する。細胞ペレットをFACSバッファー(0.01% アジ化ナトリウムを含む2% FCS/PBS)に再懸濁し、U型の96穴プレートに移し、氷上で10分間、FcR阻止抗体(1.0μl 抗CD16/CD32、ファーミンジェン社(Pharmingen))とインキュベートする(1μl+49μl FACSバッファー)。洗浄せずに、SIINFEKLペンタマー−PE(プロイミューン社(ProImmune);1試料あたり5μl)を加え、混合し、37℃で15分間インキュベートする。洗浄せずに、蛍光ラベルしたCD8またはCD44を終濃度が1:100となるように加え、氷上で25〜45分間インキュベートする。細胞を100μlのFACSバッファーで洗浄し、100μlのFACSバッファーに懸濁する。細胞を、FACSカント(FACSCanto)を用いて解析する。
溶解バッファー(シグマ社(Sigma))中で1〜2分攪拌後、2% FCS/PBSで洗浄することによって、脾臓を破砕し、2% FCS/PBS中で細胞を分離することで、細胞内染色のために脾細胞を単離、調製する。完全培地の細胞懸濁液を24穴プレート1ウェルあたり1ml(500,000細胞/ml)加え、各ウェルに5μg/mlのSIINFEKL を加え、37℃で一晩インキュベートする。ブレフェルディンA(Brefeldin A)(1〜2μg/ml)を各ウェルに加え、37℃で4時間インキュベートする。細胞をU型の96穴プレートに移し、2% FCS/PBSで洗浄し、FcR阻止抗体(1.0μl 抗CD16/CD32、ファーミンジェン社(Pharmingen))を加えたFACSバッファー50μlに再懸濁し、氷上で10分間インキュベートする。洗浄せずに、細胞を、表面抗体CD8またはCD44と氷上(暗所)で20〜45分間インキュベートし、FACSバッファーで洗浄し、氷上で10〜20分間、100μlのパラホルムアルデヒド(PFA)(PBS中1%)に再懸濁することで固定する。細胞をFACSバッファーで洗浄し、100μlのNP40(PBS中0.1%)に再懸濁し、氷上で3分間インキュベートする。FACSバッファーで洗浄した後、蛍光ラベルしたインターフェロンγ抗体を加え、氷上、暗所で35分間インキュベートする。FACSバッファーで洗浄し、再懸濁した後、FlowJo8.5.2ソフトウェア(ツリー・スター社(Tree Star, Inc.)、アシュランド、OR)を用いたFACSカント(FACSCanto)によって、細胞を解析する。
フローサイトメトリー(FACSカント(FACSCanto)、BDバイオサイエンス社(BD Biosciences)、サンノゼ、USA)によって、OVA特異的T細胞の度数を求める。フローサイトメトリーを行う前に、各抗体で別々に染色したビーズを用いて補正を行う。抗体染色の前に、赤血球溶解溶液(シグマ社(Sigma))を用いて、赤血球を溶解する。各試料につき10000のCD8+のイベントを記録し、SIINFEKLペンタマー陽性細胞の割合を、ツリー・スター社(Tree Star, Inc.)(アシュランド、OR;http://www.flowjo.com/)のFlowJo8.5.2ソフトウェアを用いて算出する。
当該分子用のレディ・セット・ゴー!(Ready-set Go!)キット(eバイオサイエンス社(eBioscience))を用い、製造元の説明書にしたがってELISAを行う。
上述した免疫化のプロトコールによって、マウスにインビボで接種を行う。7日後に血液を、14日後に脾臓を単離する。血液に関しては、抗原特異的CD8+ T細胞についての解析を行い、脾臓細胞に関しては、抗原特異的CD8+ T細胞についての直接的な解析か、インビトロで再刺激した後のIFN−γまたはIL−2の産生についての解析のいずれかを行う。
抗原特異的T細胞レベルを、抗原特異的T細胞に特異的に結合する蛍光ラベルした抗原特異的「ペンタマー」を用いて、フローサイトメトリーによって測定する。動物における全CD8+ T細胞に対する抗原特異的CD8+T細胞数の%を求める(免疫化のプロトコールで述べた染色およびフローサイトメトリー解析、並びにSIINFEKL染色の詳細を参照)。
T細胞に対する一般的な刺激効果は、抗原特異的な細胞の%を増加させない内因性T細胞にも影響を及ぼすので、内因性T細胞は、この効果の抗原特異性に対する内部標準として役立つ。典型的には、OT−1細胞の%を、接種前、および接種後の(複数の)時点において測定する。抗原のみの効果(「従来の接種」)を、抗原+PCIの効果と比較する。
接種から14日後に採取した脾臓を、脾細胞単離に供し、SIINFEKL抗原ペプチドによる再刺激、および上記プロトコールで述べたフローサイトメトリーによるCD8+ T細胞の解析のためのIFN−γ産生の細胞内染色を行う。
接種から14日後に採取した脾臓を、脾細胞単離に供し、SIINFEKL抗原ペプチドによる再刺激、および上記プロトコールで述べたELISAによるIFN−γおよびIL−2産生の解析を行う。
材料および方法
動物
C57BL/6マウスを、ハーラン社(Harlan)(ホルスト、オランダ)から購入した。CD8 T細胞受容体トランスジェニックOT−Iマウス(B6.129S6−Rag2tm1Fwa Tg(TcraTcrb)1100Mjb)を、タコニック・ヨーロッパ(Taconic Europe)(リュー、デンマーク)またはジャクソン・ラボラトリー(Jackson Laboratories)(バー・ハーバー、メイン州)から購入した。OT−I CD8 T細胞は、オボアルブミンのH−2Kb制限エピトープSIINFEKL(OVA、aa257〜264)を認識する。マウスは全てSPF条件下で飼育され、行った手順は、スイスおよびノルウェーの家畜当局によって承認された。
ニワトリOVAをシグマ・アルドリッチ社(Sigma-Aldrich)(ブフス、スイス)から、SIINFEKLペプチドをEMCマイクロコレクション社(EMC microcollections)(テュービンゲン、ドイツ)から、GM−CSFをプレプロテック社(Preprotech)(ウィーン)から購入した。光増感剤であるジスルホン酸テトラフェニルクロリン(TPCS2a)を、PCIバイオテク社(PCI Biotech)(ライサカー、ノルウェー)から入手した。OVA、TPCS2a、および、目的に適合する場合は、GM−CSFをPBS中で混合し、遮光した状態を維持し、調製してから60分以内にマウスに投与した。ルミソース(LumiSource)(商標)(PCIバイオテク社(PCI Biotech))を用いた照射によって、TPCS2aを活性化した。
免疫化の1日前に、雌のOT−1マウスから脾臓およびリンパ節を単離し、溶血(赤血球溶解バッファー ハイブリ・マックス(Hybri-Max)、シグマ・アルドリッチ社(Sigma-Aldrich))によって、均質化した細胞懸濁液から赤血球を除去した。残った細胞をPBSで洗浄し、70ミクロンのナイロン濾過器を通して濾過し、2×106個のOT−1細胞を、静脈注射によって、受容者である雌のC57BL/6マウスに投与した。SIINFEKL特異的CD8 T細胞の養子免疫伝達によって、フローサイトメトリーによる免疫応答の測定が容易となる。1日後または8時間後、マウスの尾から採血を行い、OVA特異的CD8 T細胞の基準度数解析のために、ヘパリンが入った試験管に血液を集めた。
次に、マウスの腹部領域の毛を剃り、OVAからなる、あるいはOVA、TPCS2a、およびGM−CSF(10μg)の異なる混合物からなるワクチンを、29G注射針を付けたシリンジを用いて皮内注射した。ワクチンは、遮光した状態を維持し、調製してから60分以内に用いられた。ワクチンは、腹部の正中線の左側および右側に、50μlずつ2回注射して与えられた。OVAは、10μgまたは100μgの用量で用いられ、TPCS2aの用量は150μgであった。ワクチンを注射してから18時間後、ケタミン(25mg/kg体重)およびキシラジン(4mg/kg)の混合物を腹腔内注射することによって、マウスに麻酔をかけ、ルミソース(LumiSource)光源上に置いた(照射および光増感剤TPCS2aの活性化のため)。照射時間は、6分であった。
その後7日目に、マウスの尾から採血を行い、赤血球を溶血によって除去してから、フローサイトメトリーによって、抗原特異的CD8 T細胞を解析した。実験の最後に、マウスを安楽死させた。
抗CD8抗体およびH−2Kb/SIINFEKLプロ5ペンタマー(プロイミューン社(Proimmune)、オックスフォード、UK)を用いてフローサイトメトリー解析用に細胞を染色することで、血液中のOVA特異的CD8 T細胞の度数を測定した。フローサイトメトリーによってCD44の発現を調べることで、細胞の活性化の状況をさらに解析した。細胞の解析は、FACSカント(FACSCanto)(BDバイオサイエンス社(BD Biosciences)、サンノゼ、USA)を用いて行い、またFlowJo8.5.2ソフトウェア(ツリー・スター社(Tree Star, Inc.)、アシュランド、OR)を用いた。
材料および方法で述べたように実験を行い、接種から7日後のマウス血液試料を、上述したように、フローサイトメトリーによって解析した。マウスは全て、上述したようにOT−1細胞を投与された。
以下の実験群が含まれる。
1.未処理:マウスは、OT−1細胞を投与されているが、接種または照射は行わなかった。
2.OVA:10μgのOVAをマウスに接種した。照射は行わなかった。
3.OVA+GM−CSF:10μg OVA+10μg GM−CSFの混合物をマウスに接種した。照射は行わなかった。
4.OVA PCI:10μg OVA+150μg TPCS2aの混合物をマウスに接種した。上述のように照射を行った。
5.OVA+gm−CSF PCI:10μg OVA+10μg gm−CSF+150μg TPCS2aの混合物をマウスに接種した。上述のように照射を行った。
図2Aは、フローサイトメトリー解析の代表的なドットプロットを示す。したがって、楕円内の集団は、CD8+、ペンタマー+、CD44+である細胞を表し、これは、抗原特異的(ペンタマー結合性)かつ活性化された(CD44の発現)CD8+細胞である。OVA+GM−CSF群およびOVA PCI群において、この集団中の細胞数が増加しており(OVA群との比較)、OVA+GM−CSF PCI群において、この効果がさらに顕著に増強されていることがわかる。
図2Bは、実験群の平均値(全CD8+細胞に対する抗原特異的CD44+細胞の%)を示し、その他すべての群よりもOVA+GM−CSF PCI群において実質的に増加していることが、あらためて示されている。
材料および方法
動物
C57BL/6マウスを、ハーラン社(Harlan)(ホルスト、オランダ)から購入した。マウスは全てSPF条件下で飼育され、行った手順は、ノルウェーの家畜当局によって承認された。
HPV 16 E7ペプチド抗原(配列はQAEPDRAHYNIVTFCCKCDSTLRLCVQSTHVDIR、CD8エピトープを下線で示す)を、ユナイテッド・ペプチド社(United Peptides)(ハーンドン、VA)から入手した。高分子量ポリ(IC)をインビボジェン社(InvivoGen)(サンディエゴ、USA)から入手した。GM−CSF(ネズミ組み換え体)をペプロテック社(PeproTech Inc.)(ロッキーヒル、USA)から購入した(カタログ番号:315−03)。光増感剤であるジスルホン酸テトラフェニルクロリン(TPCS2a)をPCIバイオテク社(PCI Biotech)(ライサカー、ノルウェー)から、HPVペンタマーをプロイミューン社(Proimmune)(オックスフォード、UK)から入手した(プロイミューンのペプチドコード:502H)。
マウスの腹部領域の毛を剃り、50μg HPV長鎖ペプチド抗原、100μg TPCS2a、および10μg GM−CSF、および/またはポリ(IC)からなるワクチン(以下に明示する通り)を、29G注射針を付けたシリンジを用いて皮内注射した。ワクチンは、遮光した状態を維持し、調製してから60分以内に用いられた。ワクチンは、腹部の正中線の左側および右側に、50μlずつ2回注射して与えられた。免疫化してから18時間後、ケタミン(25mg/kg体重)およびキシラジン(4mg/kg)の混合物を腹腔内注射することによって、マウスに麻酔をかけ、以下に述べるように照射を行った。
免疫化後7日目に、マウスの尾から採血を行い、赤血球を溶血によって除去してから、フローサイトメトリーによって、抗原特異的CD8 T細胞を解析した。
ルミソース(LumiSource)(商標)(PCIバイオテク社(PCI Biotech))を用いた照射によってTPCS2aを活性化した。ルミソースによる照射は、免疫化してから18時間後に6分間行った。
抗CD8抗体、抗CD44抗体、および用いられたHPV抗原に応じたペンタマーを用いて細胞を染色した後、血液中の抗原特異的CD8 T細胞の度数を、フローサイトメトリーによって測定した。フローサイトメトリーによってCD44の発現を調べることで、細胞の活性化の状況を解析した。細胞の解析は、FACSカント(FACSCanto)(BDバイオサイエンス社(BD Biosciences)、サンノゼ、USA)を用いて行い、またFlowJo8.5.2ソフトウェア(ツリー・スター社(Tree Star, Inc.)、アシュランド、OR)を用いた。
材料および方法で述べたように実験を行った。0日目および14日目に、以下に明示されるワクチン混合物を用いて動物を免疫化した。免疫化してから18時間後に、ルミソース(LumiSource)照明装置を用いて6分間の照射を行った。各免疫化後6日目の血液試料を、HPVペンタマー、CD8抗体、およびCD44抗体で染色し、上述したように、フローサイトメトリーによって解析した。以下の実験群が含まれる。
2×HPV:50μg HPV長鎖ペプチドを用いて、マウスを2回免疫化した。マウスに対して照射は行わなかった。
2×HPV+GM−CSF:50μg HPV長鎖ペプチドおよび10μg GM−CSFを用いて、マウスを2回免疫化した。マウスに対して照射は行わなかった。
2×HPV+GM−CSF+PCI:50μg HPV長鎖ペプチド、100μg TPCS2a、および10μg GM−CSFを用いて、マウスを2回免疫化した。いずれの免疫化後も、マウスに対して照射を行った。
図3からわかるように、抗原+GM−CSFを用いて免疫化を2回行っても、免疫学的なCD8細胞応答は、抗原のみの場合に観察される応答より上昇することはなかった。しかしながら、GM−CSFをPCIと組み合わせると、CD8細胞応答は実質的に上昇した。
材料および方法で述べたように実験を行った。0日目および14日目に、以下に明示されるワクチン混合物を用いて動物を免疫化した。免疫化してから18時間後に、ルミソース(LumiSource)照明装置を用いて6分間の照射を行った。各免疫化後6日目の血液試料を、HPVペンタマー、CD8抗体、およびCD44抗体で染色し、上述したように、フローサイトメトリーによって解析した。以下の実験群が含まれる。
2×HPV:50μg HPV長鎖ペプチドを用いて、マウスを2回免疫化した。マウスに対して照射は行わなかった。
2×HPV+ポリ(IC):50μg HPV長鎖ペプチドおよび10μg ポリ(IC)を用いて、マウスを2回免疫化した。マウスに対して照射は行わなかった。
1回目:HPV+p(IC)+PCI;2回目:HPV+PCI:50μg HPV長鎖ペプチド、10μg ポリ(IC)、および100μg TPCS2aの混合物(1回目の免疫化)、並びに50μg HPV長鎖ペプチドおよび100μg TPCS2a(2回目の免疫化)を用いて、マウスを免疫化した。いずれの免疫化後も、マウスに対して照射を行った。
1回目:HPV+p(IC)+GM−CSF+PCI;2回目:HPV+GM−CSF+PCI:50μg HPV長鎖ペプチド、10μg ポリ(IC)、10μg GM−CSF、および100μg TPCS2aの混合物(1回目の免疫化)、並びに50μg HPV長鎖ペプチド、10μg GM−CSF、および100μg TPCS2a(2回目の免疫化)を用いて、マウスを免疫化した。いずれの免疫化後も、マウスに対して照射を行った。
本実験では、1回目の免疫化を、HPV抗原のみ、抗原+ポリ(IC)の組み合わせ、あるいは抗原+ポリ(IC)+PCI、または抗原+ポリ(IC)+GM−CSF+PCIの組み合わせ、を用いて行った。2回目の免疫化は、同じ組み合わせを用いて行ったが、PCI処理を行う試料についてはポリ(IC)を用いなかった。図4から、PCI+ポリ(IC)を用いた処理方法のみが免疫応答に好影響を与えたが、同じ処理方法にGM−CSFを加えることで、その応答が実質的に高まったことがわかる。抗原+GM−CSF+PCIを用いて免疫化を行うと、免疫学的なCD8細胞応答は、抗原のみの場合(図3)に観察される応答よりも顕著に上昇したが、その応答の規模は、GM−CSF、ポリ(IC)、およびPCIの組み合わせ(図4)の場合に観察される応答よりも実質的に小さかった。ポリ(IC)を用いても、PCIを行わなければ、抗原のみを用いた場合に達成される免疫応答よりも免疫応答が上昇することはないという観察結果と合わせると、本実験は、GM−CSFおよびポリ(IC)を用いてPCIを行う場合、PCIが相乗効果的に作用してペプチド抗原に対するCD8の応答を増強するということを示している。
Claims (34)
- 細胞の表面に抗原分子または抗原分子の一部を発現させる方法であって、
細胞を抗原分子、光感作性薬剤、およびサイトカインと接触させること、並びに、光感作性薬剤を活性化するのに有効な波長の光を細胞に照射すること、を含み、
前記抗原分子は、前記細胞のサイトゾルに放出され、その後、前記抗原分子または前記抗原分子の一部が、細胞の表面に提示される、方法。 - 前記サイトカインは、I型サイトカイン受容体またはII型サイトカイン受容体のリガンドである、請求項1に記載の方法。
- 前記サイトカインは、IL−2受容体ファミリーメンバーのリガンド、またはGM−CSF受容体ファミリーメンバーのリガンドである、請求項1または2に記載の方法。
- 前記サイトカインは、インターフェロンであり、好ましくはI型IFNである、請求項1または2に記載の方法。
- 前記サイトカインは、GM−CSF、IL−7、IFN−α、IL−2、IL−15、およびIL−21、あるいはこれらの相同体または誘導体から選択され、前記サイトカインは、好ましくはGM−CSFである、請求項1から4のいずれか1項に記載の方法。
- 前記抗原分子は、免疫応答を刺激することができる分子であり、好ましくはワクチン抗原またはワクチン成分である、請求項1から5のいずれか1項に記載の方法。
- 前記抗原提示によって免疫応答が刺激される、請求項6に記載の方法。
- 前記方法は、インビトロまたはエキソビボで行われる、請求項1から7のいずれか1項に記載の方法。
- 前記光感作性薬剤は、TPCS2a、AlPcS2a、TPPS4、およびTPBS2aから選択され、好ましくはTPCS2aであるか、または光増感剤と式(I)で定義されるキトサンとの抱合体である、請求項1から8のいずれか1項に記載の方法。
Rは前記化合物においてn回現れ、
前記総Rn基の0.1%〜99.9%(好ましくは0.5%〜99.5%)において、各Rは、
と
と、から選択されるA基であり、
各R基は同一であっても異なっていてもよく、
前記総Rn基の0.1%〜99.9%(好ましくは0.5%〜99.5%)において、各Rは、
R2は
と、から選択される基であり、
R3は
と、から選択される基であり、
R4は、同一であっても異なっていてもよいが、H、−OH、−OCH3、−CH3、−COCH3、C(CH3)4、−NH2、−NHCH3、−N(CH3)2、および−NCOCH3から選択される基(o位、m位、またはp位が置換されている)であり、好ましくはHである。]
と、から選択されるB基であり、
各R基は同一であっても異なっていてもよい。 - 前記抗原分子は、ペプチドである、請求項1から9のいずれか1項に記載の方法。
- 前記細胞は、抗原提示細胞であり、好ましくは樹状細胞である、請求項1から10のいずれか1項に記載の方法。
- 前記細胞を、前記抗原分子、前記光感作性薬剤、および前記サイトカインと、同時に、別々に、または順次に接触させる、請求項1から11のいずれか1項に記載の方法。
- 被験体の免疫応答を引き起こす方法であって、
前記被験体に、請求項1、6または10に記載の抗原分子、請求項1または9に記載の光感作性薬剤、および請求項1から5のいずれか1項に記載のサイトカインを投与すること、並びに、前記被験体に、前記光感作性薬剤を活性化するのに有効な波長の光を照射すること、を含み、免疫応答が引き起こされる、方法。 - 前記方法は、予防接種の方法である、請求項13に記載の方法。
- 疾患、障害、または感染を治療または予防するための、好ましくは癌を治療または予防するための、請求項13または14に記載の方法。
- 前記被験体は、非哺乳動物であり、好ましくは魚類であるか、または哺乳類であり、好ましくはネコ、イヌ、ウマ、ロバ、ヒツジ、ブタ、ヤギ、ウシ、マウス、ラット、ウサギ、またはモルモットであり、最も好ましくは被験体はヒトである、請求項13から15のいずれか1項に記載の方法。
- 前記抗原分子、前記光感作性薬剤、および前記サイトカインを、前記被験体へ、同時に、別々に、または順次に投与する、請求項13から16のいずれか1項に記載の方法。
- 請求項1、6または10のいずれか1項に記載の抗原分子、請求項1または9に記載の光感作性薬剤、および請求項1から5のいずれか1項に記載のサイトカイン、並びに1つ以上の薬学的に許容される希釈剤、担体、または賦形剤を含む、医薬組成物。
- 細胞表面に抗原分子または抗原分子の一部を発現する細胞またはその集団であって、細胞は、請求項1から12のいずれか1項に記載の方法によって得ることができ、前記細胞は、好ましくは樹状細胞である、細胞。
- 請求項19に記載の細胞または細胞の集団、および1つ以上の薬学的に許容される希釈剤、担体、または賦形剤を含む、医薬組成物。
- 予防または治療に用いられる、請求項19に記載の細胞または細胞集団、あるいは請求項18または20に記載の組成物。
- 被験体の免疫応答を刺激するのに用いられる、好ましくは被験体の疾患、障害、または感染を治療または予防するための、好ましくは予防接種および/または癌の治療または予防のための、請求項19に記載の細胞または細胞集団、あるいは請求項18または20に記載の組成物。
- 被験体の免疫応答を刺激する薬物の調製のための、好ましくは被験体の疾患、障害、または感染を治療または予防するための、好ましくは予防接種および/または癌の治療または予防のための、請求項19に記載の細胞集団の使用、あるいは請求項18または20に記載の組成物の使用。
- 前記刺激、前記治療、または前記予防は、前記被験体に前記薬物を投与することを含む、請求項23に記載の使用。
- 予防または治療に用いる、請求項1、6または10のいずれか1項に記載の抗原分子、請求項1または9に記載の光感作性薬剤、および請求項1から5のいずれか1項に記載のサイトカイン。
- 被験体の免疫応答を刺激するのに用いられる、好ましくは被験体の疾患、障害、または感染を治療または予防するための、好ましくは予防接種および/または癌の治療または予防のための、請求項25に記載の使用のための抗原分子、光感作性薬剤、およびサイトカインであって、好ましくは、前記使用は、請求項1から17のいずれか1項に記載の方法を含む、抗原分子、光感作性薬剤、およびサイトカイン。
- 請求項25または26に記載の使用のための、請求項1から5のいずれか1項に記載の抗原分子、光感作性薬剤、およびサイトカインであって、前記使用は、細胞集団を調製するために請求項1から12のいずれか1項に記載の方法を含み、好ましくは前記細胞は樹状細胞である、抗原分子、光感作性薬剤、およびサイトカイン。
- 前記細胞集団は、前記被験体に投与されるものである、請求項27に記載の使用のための抗原分子、光感作性薬剤、および薬剤。
- 被験体の免疫応答を刺激するための、好ましくは被験体の疾患、障害、または感染を治療または予防するための、好ましくは予防接種および/または癌の治療または予防のための薬物の製造における、請求項1、6、または10のいずれか1項に記載の抗原分子、および/または請求項1または9に記載の光感作性薬剤、および/または請求項1から5のいずれか1項に記載のサイトカインの使用であって、好ましくは前記免疫応答は請求項13から17に記載の方法で刺激される、使用。
- 前記薬物は、抗原分子または抗原分子の一部を細胞表面に発現する細胞集団であって、請求項1から12のいずれか1項に記載の方法によって得ることができる細胞集団を含む、前記被験体に投与するための、請求項29に記載の使用。
- 請求項1から12のいずれか1項に記載の方法において、前記抗原分子、および/または前記光感作性薬剤、および/または前記サイトカインを用いて、前記薬物の製造のための前記細胞集団を得る、請求項30に記載の使用。
- 被験体の免疫応答を刺激するのに同時に、別々に、または順次に用いられる、好ましくは被験体の疾患、障害、または感染を治療するまたは予防するための、好ましくは予防接種および/または癌の治療または予防のための、あるいは請求項1から17のいずれか1項に記載の方法において、細胞表面に抗原分子または抗原分子の一部を発現させるための、組み合わせ製剤として、請求項1、6、または10のいずれか1項に記載の抗原分子、請求項1または9に記載の光感作性薬剤、および請求項1から5のいずれか1項に記載のサイトカインを含む、製品。
- 被験体の免疫応答を刺激するのに用いられる、好ましくは被験体の疾患、障害、または感染を治療するまたは予防するための、好ましくは予防接種および/または癌の治療または予防のための、あるいは請求項1から17のいずれか1項に記載の方法において、細胞表面に抗原分子または抗原分子の一部を発現させる、キットであって、
請求項1または9に記載の光感作性薬剤を含む第1の容器と、
請求項1、6または10のいずれか1項に記載の抗原分子を含む第2の容器と、
請求項1から5のいずれか1項に記載のサイトカインを含む第3の容器と、を含む、キット。 - 被験体の免疫応答を引き起こす、好ましくは被験体の疾患、障害、または感染を治療するまたは予防する、好ましくは予防接種および/または癌の治療または予防のための方法であって、
請求項1から12のいずれか1項に記載の方法にしたがって細胞集団を調製すること、および、その後に細胞を被験体に投与すること、を含む、方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB1415247.4 | 2014-08-28 | ||
| GB201415247A GB201415247D0 (en) | 2014-08-28 | 2014-08-28 | Compound and method |
| GB1420773.2 | 2014-11-21 | ||
| GB201420773A GB201420773D0 (en) | 2014-11-21 | 2014-11-21 | Compound and method |
| PCT/EP2015/069794 WO2016030529A1 (en) | 2014-08-28 | 2015-08-28 | Compound and method |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020123157A Division JP7079819B2 (ja) | 2014-08-28 | 2020-07-17 | 化合物および方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2017526371A true JP2017526371A (ja) | 2017-09-14 |
Family
ID=54065872
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017511702A Pending JP2017526371A (ja) | 2014-08-28 | 2015-08-28 | 化合物および方法 |
| JP2020123157A Active JP7079819B2 (ja) | 2014-08-28 | 2020-07-17 | 化合物および方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020123157A Active JP7079819B2 (ja) | 2014-08-28 | 2020-07-17 | 化合物および方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US10537639B2 (ja) |
| EP (1) | EP3185901B1 (ja) |
| JP (2) | JP2017526371A (ja) |
| KR (1) | KR20170047336A (ja) |
| CN (1) | CN108136016A (ja) |
| AU (1) | AU2015308345B9 (ja) |
| BR (1) | BR112017003486A2 (ja) |
| CA (1) | CA2959207A1 (ja) |
| NZ (1) | NZ729408A (ja) |
| WO (1) | WO2016030529A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020170330A1 (ja) | 2019-02-19 | 2020-08-27 | 大塚電子株式会社 | 光線力学的療法条件パラメータの決定方法および光線力学的療法装置 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN109912607B (zh) * | 2018-12-11 | 2021-01-22 | 南华大学 | 一类卟啉-白杨素复合物及其抗肿瘤活性 |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NO180167C (no) | 1994-09-08 | 1997-02-26 | Photocure As | Fotokjemisk fremgangsmåte til å innföre molekyler i cellers cytosol |
| GB9905911D0 (en) | 1999-03-15 | 1999-05-05 | Photocure As | Method |
| CZ301427B6 (cs) | 2000-11-29 | 2010-02-24 | Pci Biotech As | Zpusob zavedení molekuly do cytosolu bunky |
| EP1351969A4 (en) | 2000-12-13 | 2006-04-05 | Immunex Corp | PROCESS RELATING TO THE PRODUCTION OF IMMORTAL DENDRITIC CELL LINES |
| GB0121023D0 (en) | 2001-08-30 | 2001-10-24 | Norwegian Radium Hospital Res | Compound |
| EP1687322B1 (en) | 2003-11-12 | 2017-02-08 | The Government of the United States of America, represented by the Secretary, Department of Health and Human Services | Custom vectors for treating and preventing pancreatic cancer |
| WO2005097976A1 (ja) | 2004-04-06 | 2005-10-20 | Ehime University | 抗原パルスして得られた樹状細胞 |
| WO2005100547A1 (ja) * | 2004-04-06 | 2005-10-27 | Techno Network Shikoku Co., Ltd. | 抗原パルスして得られた樹状細胞 |
| CA2728423A1 (en) * | 2008-06-06 | 2009-12-10 | Baylor Research Institute | Respiratory syncytial virus renders dendritic cells tolerogenic |
| US20120269765A1 (en) | 2009-07-24 | 2012-10-25 | Garcia K Christopher | Cytokine compositions and methods of use thereof |
| GB201208548D0 (en) * | 2012-05-15 | 2012-06-27 | Pci Biotech As | Compound and method |
| CA2906279A1 (en) | 2013-03-15 | 2014-09-18 | Pci Biotech As | A method of generating antigen presenting cells using photochemical internalisation |
| WO2015028575A1 (en) | 2013-08-28 | 2015-03-05 | Pci Biotech As | Immunisation method by photochemical internalisation |
| ES2959398T3 (es) | 2013-08-28 | 2024-02-26 | Pci Biotech As | Compuesto y método para vacunación e inmunización |
| EP3129045B1 (en) | 2014-04-11 | 2022-03-02 | PCI Biotech AS | Method of treating melanoma |
-
2015
- 2015-08-28 WO PCT/EP2015/069794 patent/WO2016030529A1/en active Application Filing
- 2015-08-28 AU AU2015308345A patent/AU2015308345B9/en active Active
- 2015-08-28 US US15/506,453 patent/US10537639B2/en active Active
- 2015-08-28 EP EP15760426.5A patent/EP3185901B1/en active Active
- 2015-08-28 BR BR112017003486A patent/BR112017003486A2/pt active Search and Examination
- 2015-08-28 CA CA2959207A patent/CA2959207A1/en active Pending
- 2015-08-28 CN CN201580055883.9A patent/CN108136016A/zh active Pending
- 2015-08-28 NZ NZ729408A patent/NZ729408A/en unknown
- 2015-08-28 JP JP2017511702A patent/JP2017526371A/ja active Pending
- 2015-08-28 KR KR1020177008280A patent/KR20170047336A/ko active IP Right Grant
-
2020
- 2020-07-17 JP JP2020123157A patent/JP7079819B2/ja active Active
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020170330A1 (ja) | 2019-02-19 | 2020-08-27 | 大塚電子株式会社 | 光線力学的療法条件パラメータの決定方法および光線力学的療法装置 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3185901A1 (en) | 2017-07-05 |
| JP2020182486A (ja) | 2020-11-12 |
| US10537639B2 (en) | 2020-01-21 |
| CA2959207A1 (en) | 2016-03-03 |
| AU2015308345B9 (en) | 2020-12-24 |
| WO2016030529A1 (en) | 2016-03-03 |
| EP3185901B1 (en) | 2023-10-04 |
| EP3185901C0 (en) | 2023-10-04 |
| AU2015308345B2 (en) | 2020-12-10 |
| BR112017003486A2 (pt) | 2018-01-16 |
| JP7079819B2 (ja) | 2022-06-02 |
| US20170252441A1 (en) | 2017-09-07 |
| NZ729408A (en) | 2021-12-24 |
| KR20170047336A (ko) | 2017-05-04 |
| CN108136016A (zh) | 2018-06-08 |
| AU2015308345A1 (en) | 2017-03-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9339535B2 (en) | Vaccines and immunopotentiating compositions and methods for making and using them | |
| JP2007501602A5 (ja) | ||
| US8834899B2 (en) | Photodynamic therapy-generated mesothelioma vaccine | |
| JP7079819B2 (ja) | 化合物および方法 | |
| Haug et al. | Photochemical internalization of peptide antigens provides a novel strategy to realize therapeutic cancer vaccination | |
| CA2570218C (en) | Adjuvancy and immune potentiating properties of natural products of onchocerca volvulus | |
| EP2989121B1 (en) | Methods of preparation and composition of peptide constructs useful for treatment of rheumatoid arthritis | |
| US20160040128A1 (en) | Method | |
| JP2021514661A (ja) | サイトカインに連結させたecm親和性ペプチドを用いてがんを処置するための方法および組成物 | |
| WO2015028575A1 (en) | Immunisation method by photochemical internalisation | |
| US10973896B2 (en) | Treatment or prevention of melanoma using photochemical internalization of a melanoma antigen | |
| WO2016030528A1 (en) | Compound and method | |
| US20220054631A1 (en) | MHC Class I Associated Hepatitis B Peptides | |
| KR101857705B1 (ko) | 백신용 분자 아쥬반트로서 뇌하수체 아데닐산 고리화효소 활성화 펩타이드의 용도 | |
| Qin et al. | Generation of an immune microenvironment as a novel mechanism for myotoxins to potentiate genetic vaccines | |
| Shen et al. | Grain-sized moxibustion enhances anti-tumor immunity of tumor cell lysate vaccine | |
| TWI228993B (en) | Fusion antigen specific for a target cell | |
| CN1127982C (zh) | 细胞-蛋白抗肿瘤制剂 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20180807 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190709 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20190924 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20191125 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200109 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20200319 |