JP2017191012A - 可溶性インターロイキン2受容体の免疫学的測定法 - Google Patents
可溶性インターロイキン2受容体の免疫学的測定法 Download PDFInfo
- Publication number
- JP2017191012A JP2017191012A JP2016080659A JP2016080659A JP2017191012A JP 2017191012 A JP2017191012 A JP 2017191012A JP 2016080659 A JP2016080659 A JP 2016080659A JP 2016080659 A JP2016080659 A JP 2016080659A JP 2017191012 A JP2017191012 A JP 2017191012A
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- added
- receptor
- plasma
- serum
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Landscapes
- Investigating Or Analysing Biological Materials (AREA)
Abstract
Description
IL−2の受容体(以下、IL−2Rと略することがある)はα鎖、β鎖、γ鎖からなるが、α鎖の一部が細胞上から遊離した可溶性インターロイキン−2受容体(以下、sIL−2Rと略することがある)が血中に存在することが知られている。sIL−2Rは活性化T細胞、B細胞によって産生される。生体の免疫防御機構の活性化、T細胞系及びB細胞系などの活性化に伴い血中のsIL−2Rが上昇することが報告されている。血清中のsIL−2R濃度は、慢性関節リウマチ、全身性エリテマトーデス(SLE)などの自己免疫疾患や、ウイルス性肝炎、後天性免疫不全症候群(AIDS)などのウイルス感染症の患者で高値を示し、体内の活性化リンパ球の指標の1つとなることが報告されている。また腫瘍細胞がsIL−2Rを産生し、成人T細胞白血病(ATL)や非ホジキンリンパ腫の進行と血清中のsIL−2R濃度の変動が良く相関することが知られている。このように様々な免疫系の疾患や病態との関連が報告され、造血疾患のなかで有望な血液中のマーカーとなってきている。血清中のsIL−2R濃度は成人T細胞白血病においては病態モニタリングの指標など、非ホジキンリンパ腫においては治療効果の判定、寛解後のフォロー、再発の早期発見の指標などとして臨床的に有効活用されている。
また、血清又は血漿中のsIL−2R定量用試薬としては、「デミタナーCL IL−2R」、「セルフリーIL−2Rメデックス」(協和メデックス社製)、「シーメンス・イムライズIL−2R II」(シーメンス社製)等があり、臨床の現場で使用されている。
また、IL−2Rはマトリックスメタロプロテアーゼ9によりT細胞表面上のαサブユニット(CD25)が血中に放出される。細胞表面抗原の切断及び血中への分泌に採血管中のEDTAが関与することも知られている(非特許文献1)。sIL−2R測定としては、血清を使用することが多く、例えば、「デミタナーCL IL−2R」「セルフリーIL−2Rメデックス」(協和メデックス社製)の場合には、血清のみが対象とされ、「シーメンス・イムライズIL−2R II」(シーメンス社製)の場合には、血清とヘパリン加血漿のみが対象とされている。このように、被検試料として、汎用的に簡便且つ高精度にsIL−2Rの免疫学的測定を行うことができなかった。
本発明は、生体試料中のsIL−2Rを検出する場合に、異なる血液凝固阻害剤の使用による血清、ヘパリン加血漿、EDTA加血漿といった被検試料の種類に関わらず、被検試料中の干渉物質の影響を受けることなく、汎用的に簡便且つ高精度な測定値を得ることができる測定方法及びキットを提供することを目的とする。
[1]生体試料中の可溶性インターロイキン2受容体を免疫学的に測定する方法において、該可溶性インターロイキン2受容体とそれに特異的に結合する抗体との免疫複合体の形成を硫酸化多糖類及びキレート剤の存在下で行うことを特徴とする、該可溶性インターロイキン2受容体を測定する方法、
[2]生体試料中の可溶性インターロイキン2受容体の免疫学的測定において、抗凝固剤としてヘパリンを添加した血液試料を用いた場合の測定値と、EDTAを添加した血液試料を用いた場合の測定値と、血清を用いた場合の測定値との間の乖離を減少させる方法であって、可溶性インターロイキン2受容体とそれに特異的に結合する抗体との免疫複合体の形成を硫酸化多糖類及びキレート剤の存在下で行うことを特徴とする、前記方法、
[3]前記キレート剤を検体希釈液及び/又は抗体溶液に含有する、[1]又は[2]の方法、
[4]前記硫酸化多糖類を検体希釈液及び/又は抗体溶液に含有する、[1]〜[3]のいずれかの方法、
[5]可溶性インターロイキン2受容体に特異的に結合する第1抗体と第2抗体を接触させ、抗原抗体反応により形成された免疫複合体を測定する、[1]〜[4]のいずれかの方法、
[6][1]〜[5]のいずれかの方法のための、可溶性インターロイキン2受容体に特異的に結合する抗体、硫酸化多糖類を含有する緩衝液、及び、キレート剤を含有する緩衝液を含む、該可溶性インターロイキン2受容体測定キット
に関する。
例えば、デキストラン硫酸(分子量20,000)は0.000004%以上0.04%以下、デキストラン硫酸(分子量4,000)は0.0004%以上0.04%以下、βシクロデキストリン硫酸塩は0.02%以上0.4%以下等が挙げられる。
例えば、ニトリロトリ酢酸は0.08mmol/L以上0.38mmol/L以下、エチレンジアミン四酢酸は0.08mmol/L以上3.85mmol/L以下、トリエチレンテトラミン六酢酸は0.02mmol/L以上1.92mmol/L以下等が挙げられる。
参考例1−1:可溶性インターロイキン2受容体測定用試薬の作製と被検試料の調製
可溶性インターロイキン2受容体の測定用試薬として、可溶性インターロイキン2受容体(sIL−2R)測定用の試薬を作製した。
全自動臨床検査システム(STACIA:LSIメディエンス社製)による測定
STACIA専用ボトルに、調製した検体希釈液、第1抗体溶液(磁性ラテックス試薬)、第2抗体溶液(酵素標識抗体試薬)をそれぞれ充填し、装置にセットした。以下、前記装置の運転方法に従い、測定した。
具体的には、検体5μLに検体希釈液50μLを加え、37℃で3.5分間加温した後、第1抗体溶液(磁性ラテックス試薬)25μLを加え、37℃で4.2分間加温した。検体中のsIL−2Rは第1抗体(磁性ラテックス)と反応し、磁性ラテックス−sIL−2R複合体を形成した。次いで、第2抗体溶液(酵素標識抗体試薬)50μLを加え、37℃で4.4分間加温した。第2抗体溶液(ALP標識抗体)を加えると、ALP標識抗体は磁性ラテックス−sIL−2R複合体と反応し、磁性ラテックス−sIL−2R−ALP標識抗体複合体を形成した。B/F洗浄液により洗浄した後、発光基質溶液(CDP−Star)100μLを加え、37℃で2.7分間反応後に発光量を測定した。CDP−Starを加えると、CDP−Starは複合体中のALPにより加水分解され発光する。検出は、光電子増倍管(PMT)により検出される化学発光基質の発光カウントを測定し、前記標準品を使用し、公知の方法に従って、発光カウントから各濃度(U/mL)を算出した。
βシクロデキストリン硫酸塩を、反応液中に0.04%になるように検体希釈液に添加したこと、及び、各キレート剤を、反応液中に下記の濃度になるように検体希釈液に添加したこと以外は、参考例1に従って行った。
・ニトリロトリ酢酸を、反応液中に各濃度(0、0.04、0.08、0.38mmol/L)になるように検体希釈液に添加した。
・エチレンジアミン四酢酸(EDTA)を、反応液中に各濃度(0、0.02、0.04、0.08、0.15、0.77、1.92、3.85mmol/L)になるように検体希釈液に添加した。
・トリエチレンテトラミン六酢酸を、反応液中に各濃度(0、0.004、0.02、0.04、0.38、1.92mmol/L)になるように検体希釈液に添加した。
それ以外は、参考例1に従って行った。
その結果、従来使用されているキレート剤添加の無い検体希釈液だと、血清およびヘパリン加血漿とEDTA加血漿では、可溶性インターロイキン2受容体の反応性が異なることがわかった。さらに、ニトリロトリ酢酸は0.08mmol/L以上0.38mmol/L以下、エチレンジアミン四酢酸は0.08mmol/L以上3.85mmol/L以下、トリエチレンテトラミン六酢酸は0.02mmol/L以上1.92mmol/L以下添加されることにより、血清およびヘパリン加血漿はEDTA加血漿の可溶性インターロイキン2受容体の反応性が一致することが確認された。血清とヘパリン加血漿及びEDTA加血漿の反応性を一致させるには、硫酸基を持つ多糖類及びキレート剤の添加が必要であることが示された。
エチレンジアミン四酢酸を、反応液中に0.15mmol/Lになるように添加したこと及び、各硫酸化多糖類を、反応液中に下記の濃度になるように検体希釈液に添加したこと以外は、参考例1に従って行った。
・デキストラン硫酸(分子量20,000)を、反応液中に各濃度(0.0000004、0.000004、0.00004、0.0004、0.004、0.04%)になるように検体希釈液に添加した。
・デキストラン硫酸(分子量4,000)を、反応液中に各濃度(0.000004、0.00004、0.0004、0.004、0.04%)になるように検体希釈液に添加した。
・βシクロデキストリン硫酸塩を、反応液中に各濃度(0.004、0.01、0.02、0.04、0.08、0.2、0.4%)になるように検体希釈液に添加した。
それ以外は、参考例1に従って行った。
その結果、硫酸化多糖の添加が無い検体希釈液だと、血清およびヘパリン加血漿とEDTA加血漿では、可溶性インターロイキン2受容体の反応性が異なることがわかった。さらに、デキストラン硫酸(分子量20,000)は0.000004%以上0.04%以下、デキストラン硫酸(分子量4,000)は0.0004%以上0.04%βシクロデキストリン硫酸塩は0.02%以上0.4%以下添加されることにより、血清およびヘパリン加血漿はEDTA加血漿の可溶性インターロイキン2受容体の反応性が一致することが確認された。血清とヘパリン加血漿及びEDTA加血漿の反応性を一致させるには、硫酸基を持つ多糖類及びキレート剤の添加が必要であることが示された。
硫酸化多糖類又は硫酸基を持たない多糖類又は多糖類を持たず硫酸基を含む化合物を、反応液中に下記の濃度になるように検体希釈液に添加したこと以外は、参考例1に従って行った。
・硫酸化多糖類:デキストラン硫酸塩(分子量4000)を、0.04%になるように検体希釈液に添加した。βシクロデキストリン硫酸塩を、0.04%になるように検体希釈液に添加した。
・硫酸基を持たない多糖類:デキストランを、0.04%になるように検体希釈液に添加した。
・多糖類を持たず硫酸基を含む化合物:CHAPSOを、0.04%になるように検体希釈液に添加した。オクタン酸ナトリウムを、0.04%になるように検体希釈液に添加した。それ以外は、参考例1に従って行った。
硫酸化多糖類と同様な反応性となるか、硫酸基を持たない多糖類及び多糖類を持たず硫酸基を含む化合物を、同時に反応液中に添加して検討した。硫酸基を持たない多糖類及び多糖類を持たず硫酸基を含む化合物を、下記の濃度になるように検体希釈液に添加したこと以外は、参考例1に従って行った。
・多糖類を持たず硫酸基を含む化合物:NDSB−195、NDSB−201、NDSB−256を、それぞれ0.385mmol/L、3.85mmol/Lになるように検体希釈液に添加した。
・多糖類を持たず硫酸基を含む化合物及び硫酸基を持たない多糖類の混合:NDSB−195を3.85mmol/L、及び、デキストラン(分子量2000)を0.19%になるように検体希釈液に添加した。
各キレート剤を反応液中に下記の濃度になるように検体希釈液に添加したこと以外は、参考例1に従って行った。
・EDTAを、0、0.004、0.01、0.02、0.04、0.08、0.15、0.38、0.77、1.92、3.85mmol/Lになるように検体希釈液に添加した。
・CyDTAを、0、0.04、0.01、0.19mmol/Lになるように検体希釈液に添加した。
・TTHAを、0、0.04、0.10、0.19mmol/Lになるように検体希釈液に添加した。
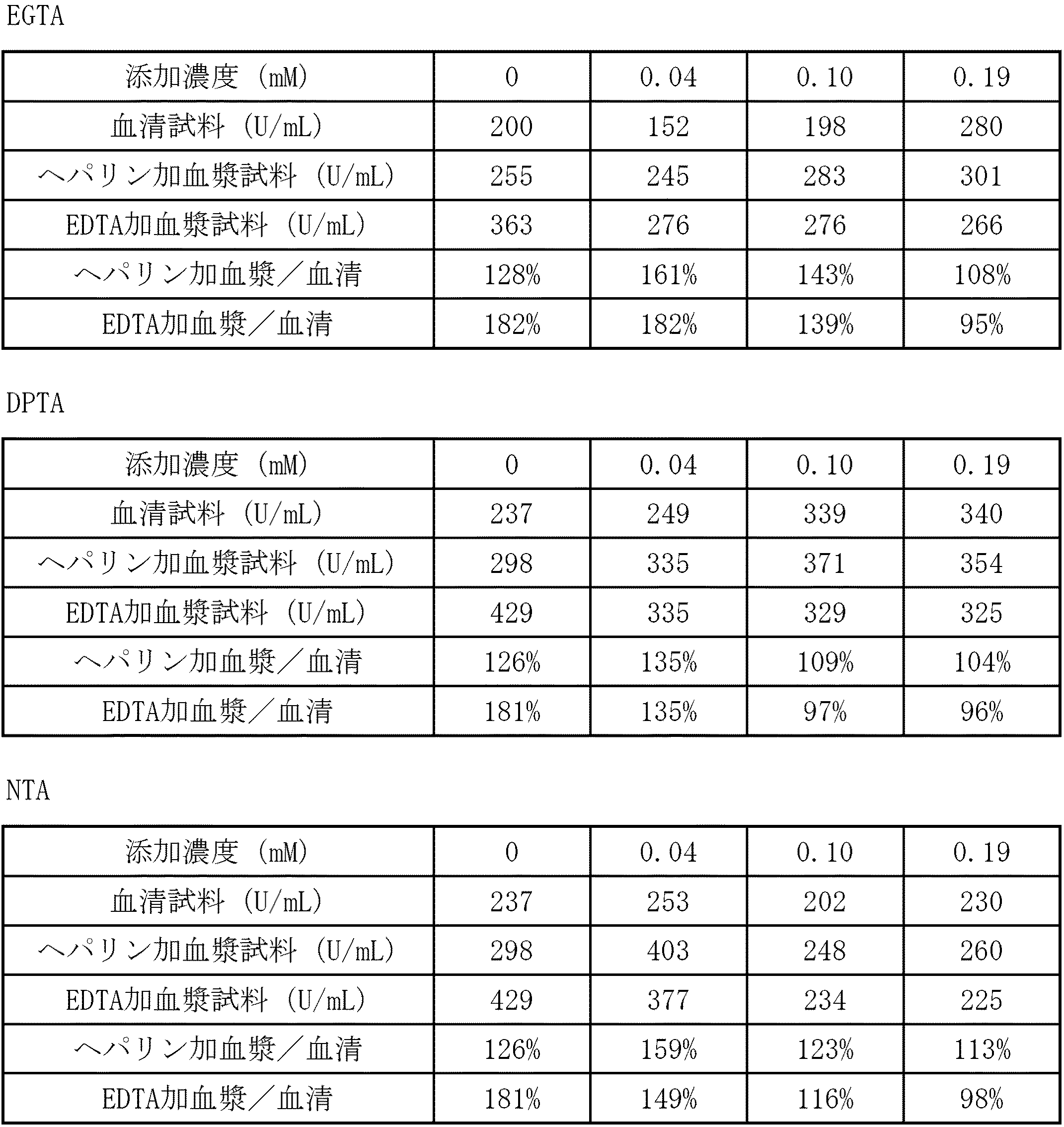
・EGTAを、0、0.04、0.10、0.19mmol/Lになるように検体希釈液に添加した。
・DPTAを、0、0.04、0.10、0.19mmol/Lになるように検体希釈液に添加した。
・NTAを、0、0.04、0.10、0.19mmol/Lになるように検体希釈液に添加した。それ以外は、参考例1に従って行った。
さらに、EDTAでは、0.15mmol/L、3.85mmol/L、CyDTAでは、0.19mmol/L、TTHAでは、0.10mmol/L、EGTAでは、0.19mmol/L、DPTAでは、0.10〜0.19mmol/Lで、血清・ヘパリン加血漿・EDTA加血漿の全てで反応性が一致することがわかった。また、EDTAでは、0.08〜0.15mmol/L、1.92〜3.85mmol/L、CyDTAでは、0.10〜0.19mmol/L、TTHAでは、0.04〜0.19mmol/L、EGTAでは、0.19mmol/L、DPTAでは、0.10〜0.19mmol/L、NTAでは、0.19mmol/Lで、血清とEDTA加血漿で反応性が一致することがわかった。
以上より、キレート剤のみで、血清・ヘパリン加血漿・EDTA加血漿の全ての可溶性インターロイキン2受容体の反応性を一致させるためには、限られた条件のみしかなく、安定して試薬として臨床の現場に供給することが難しいが、キレート剤によって、その一部(特に血清とEDTA加血漿)の反応性を一致させることができ、全て(血清・ヘパリン加血漿・EDTA加血漿)の反応性を一致させるための条件の一つになる可能性が示された。
Claims (6)
- 生体試料中の可溶性インターロイキン2受容体を免疫学的に測定する方法において、該可溶性インターロイキン2受容体とそれに特異的に結合する抗体との免疫複合体の形成を硫酸化多糖類及びキレート剤の存在下で行うことを特徴とする、該可溶性インターロイキン2受容体を測定する方法。
- 生体試料中の可溶性インターロイキン2受容体の免疫学的測定において、抗凝固剤としてヘパリンを添加した血液試料を用いた場合の測定値と、EDTAを添加した血液試料を用いた場合の測定値と、血清を用いた場合の測定値との間の乖離を減少させる方法であって、可溶性インターロイキン2受容体とそれに特異的に結合する抗体との免疫複合体の形成を硫酸化多糖類及びキレート剤の存在下で行うことを特徴とする、前記方法。
- 前記キレート剤を検体希釈液及び/又は抗体溶液に含有する、請求項1又は2に記載の方法。
- 前記硫酸化多糖類を検体希釈液及び/又は抗体溶液に含有する、請求項1〜3のいずれか一項に記載の方法。
- 可溶性インターロイキン2受容体に特異的に結合する第1抗体と第2抗体を接触させ、抗原抗体反応により形成された免疫複合体を測定する、請求項1〜4のいずれか一項に記載の方法。
- 請求項1〜5のいずれか一項に記載の方法のための、可溶性インターロイキン2受容体に特異的に結合する抗体、硫酸化多糖類を含有する緩衝液、及び、キレート剤を含有する緩衝液を含む、該可溶性インターロイキン2受容体測定キット。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016080659A JP6697314B2 (ja) | 2016-04-13 | 2016-04-13 | 可溶性インターロイキン2受容体の免疫学的測定法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016080659A JP6697314B2 (ja) | 2016-04-13 | 2016-04-13 | 可溶性インターロイキン2受容体の免疫学的測定法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2017191012A true JP2017191012A (ja) | 2017-10-19 |
| JP2017191012A5 JP2017191012A5 (ja) | 2018-11-22 |
| JP6697314B2 JP6697314B2 (ja) | 2020-05-20 |
Family
ID=60084863
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016080659A Active JP6697314B2 (ja) | 2016-04-13 | 2016-04-13 | 可溶性インターロイキン2受容体の免疫学的測定法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6697314B2 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113588943A (zh) * | 2020-11-04 | 2021-11-02 | 北京北方生物技术研究所有限公司 | 一种天然聚合多糖用于制备样本处理液及其在免疫层析检测试剂盒的应用 |
| CN115478096A (zh) * | 2022-10-20 | 2022-12-16 | 北京安图生物工程有限公司 | 一种肌酸激酶检测试剂盒 |
| CN120870546A (zh) * | 2025-09-25 | 2025-10-31 | 广州悦洋生物技术有限公司 | 一种样本稀释液及其用途、试剂盒 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050069953A1 (en) * | 2003-09-30 | 2005-03-31 | Ye Fang | Assay solution compositions and methods for GPCR arrays |
| WO2005121795A1 (ja) * | 2004-06-14 | 2005-12-22 | Kyowa Medex Co., Ltd. | 非特異反応が抑制された免疫測定方法および試薬 |
| US20100323376A1 (en) * | 2009-06-17 | 2010-12-23 | Maine Standards Company, Llc | Method for Measuring Lipoprotein-Specific Apolipoproteins |
| JP2011007782A (ja) * | 2009-05-22 | 2011-01-13 | Kyowa Medex Co Ltd | 可溶性インターロイキン−2受容体の測定方法及び測定用試薬 |
| WO2014157723A1 (ja) * | 2013-03-29 | 2014-10-02 | 積水メディカル株式会社 | インスリン測定方法 |
| JP2014221745A (ja) * | 2013-05-14 | 2014-11-27 | 富士レビオ株式会社 | タンパク質標識抗体およびそれを含む組成物、ならびにそれらの製造方法 |
-
2016
- 2016-04-13 JP JP2016080659A patent/JP6697314B2/ja active Active
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050069953A1 (en) * | 2003-09-30 | 2005-03-31 | Ye Fang | Assay solution compositions and methods for GPCR arrays |
| WO2005121795A1 (ja) * | 2004-06-14 | 2005-12-22 | Kyowa Medex Co., Ltd. | 非特異反応が抑制された免疫測定方法および試薬 |
| KR20070026576A (ko) * | 2004-06-14 | 2007-03-08 | 교와 메덱스 가부시키가이샤 | 비특이 반응이 억제된 면역 측정 방법 및 시약 |
| EP1767942A1 (en) * | 2004-06-14 | 2007-03-28 | Kyowa Medex Co., Ltd. | Immunoassay in which non-specific reaction is suppressed and reagent therefore |
| JP2011007782A (ja) * | 2009-05-22 | 2011-01-13 | Kyowa Medex Co Ltd | 可溶性インターロイキン−2受容体の測定方法及び測定用試薬 |
| US20100323376A1 (en) * | 2009-06-17 | 2010-12-23 | Maine Standards Company, Llc | Method for Measuring Lipoprotein-Specific Apolipoproteins |
| JP2012530900A (ja) * | 2009-06-17 | 2012-12-06 | メイン スタンダーズ カンパニー リミテッド ライアビリティ カンパニー | リポタンパク質特異的アポリポタンパク質を測定する方法 |
| WO2014157723A1 (ja) * | 2013-03-29 | 2014-10-02 | 積水メディカル株式会社 | インスリン測定方法 |
| JP2014221745A (ja) * | 2013-05-14 | 2014-11-27 | 富士レビオ株式会社 | タンパク質標識抗体およびそれを含む組成物、ならびにそれらの製造方法 |
Non-Patent Citations (2)
| Title |
|---|
| JONGH, R.D. ET AL.: "The effects of anticoagulation and processing on assays of IL-6, sIL-6R, sIL-2R and soluble transfer", CYTOKINE, vol. 9, no. 9, JPN6019028706, September 1997 (1997-09-01), pages 696 - 701, ISSN: 0004164282 * |
| 坂田秀人: "大腸癌における可溶性Interleukin-2 receptor (IL-2R)値の変動", 埼玉医科大学雑誌, vol. 31, no. 3, JPN6019028707, July 2003 (2003-07-01), pages 27 - 33, ISSN: 0004164283 * |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113588943A (zh) * | 2020-11-04 | 2021-11-02 | 北京北方生物技术研究所有限公司 | 一种天然聚合多糖用于制备样本处理液及其在免疫层析检测试剂盒的应用 |
| CN115478096A (zh) * | 2022-10-20 | 2022-12-16 | 北京安图生物工程有限公司 | 一种肌酸激酶检测试剂盒 |
| CN120870546A (zh) * | 2025-09-25 | 2025-10-31 | 广州悦洋生物技术有限公司 | 一种样本稀释液及其用途、试剂盒 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP6697314B2 (ja) | 2020-05-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN103380377B (zh) | 心肌肌钙蛋白的测定方法 | |
| JP2009085753A (ja) | サンドイッチイムノアッセイ法 | |
| TWI224674B (en) | Immunoassay using insoluble magnetic support particles | |
| JP4167491B2 (ja) | 全血測定法 | |
| KR102390761B1 (ko) | HBsAg의 정량적 검출을 위한 키트 및 방법 | |
| JPWO2017138497A1 (ja) | 被検物質の検出方法および被検物質の検出用試薬キット | |
| KR102228440B1 (ko) | 황산화 다당류를 이용한 면역학적 측정법 | |
| JP2010107363A (ja) | トロポニンiの測定方法及び測定用試薬キット | |
| JP2015132631A (ja) | 可溶性インターロイキン−2受容体の測定方法及び測定用試薬 | |
| JP6697314B2 (ja) | 可溶性インターロイキン2受容体の免疫学的測定法 | |
| JP2013125005A (ja) | Ck−mb測定用ラテックス凝集免疫試薬及び測定方法 | |
| JPWO2009084369A1 (ja) | Hiv−1抗原の検出用試薬及び検出方法 | |
| JP2016194437A (ja) | 前立腺特異抗原の測定方法及び測定キット | |
| JP4273311B2 (ja) | 試料中の測定対象物質の測定方法及び測定試薬 | |
| HK1262656B (zh) | 使用硫酸化多糖类的免疫学测定法 | |
| JP2021099243A (ja) | 免疫学的測定法 | |
| HK1262656A1 (en) | Immunoassay employing sulfated polysaccharide | |
| WO2023163176A1 (ja) | セリンプロテアーゼの検出用または測定用試薬 | |
| CN113474655A (zh) | 目标物质的检测方法、用于目标物质的检测的试剂、及用于目标物质的检测的试剂盒 | |
| EP2960654A1 (en) | A method for detecting EP3 antibodies | |
| HK40082358A (en) | Reagent and method for assaying thrombin-antithrombin complex |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181009 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20181009 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20190717 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190730 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190930 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20191203 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200123 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20200407 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20200424 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6697314 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313111 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |