(i) 序文
癌胎児性抗原(CEA;CEACAM5;CD66e)は、免疫グロブリン遺伝子スーパーファミリーのCEA関連細胞接着分子(CEACAM)ファミリーに属するグリコシル化ヒト腫瘍胎児抗原である。CEACAM5は、CEACAM1、CEACAM3、CEACAM4、CEACAM6、CEACAM7、およびCEACAM8と密接に関連する。CEAは、細胞と細胞の接着を媒介し、腸の細菌定着を促進し、感染性細菌を結合および捕捉することによって微生物感染から結腸を保護することが示唆されている。本明細書に使用されるように、CEAとは、CEACAM5、特に、ヒトCEACAM5を指す。
CEAは、偏光様式での上皮性起源(Hammarstrom,1999)の正常組織中に低いレベルで発現され、そのような発現は、細胞の内腔部分でのみ観察される。対照的に、CEAの発現は、癌腫(結腸、膵臓、胃、食道、肺、胸部、子宮、卵巣、および子宮内膜を含む)および黒色腫のサブセット(Hammarstrom,1999、Sanders et al,1994)中で高い。癌細胞は、CEAの偏光(内腔)発現を欠失するだけでなく、CEAの高血中濃度をもたらす、ホスホリパーゼの作用によってそれらの表面からCEAを能動的に切断する(Hammarstrom,1999)。
CEAの血中濃度は、胃腸癌を患っている患者における、有用な予後指標としての役割を果たし(Duffy,2001,Locker et al,2006、Rother,2007)、上昇した濃度は、不良な予後を示し、低下した全生存と相関する。さらに、CEAを発現する癌を治療するために開発されている療法がある。診断ツールおよび推定治療薬の開発にもかかわらず、CEAについての多くが依然として不明である。
本明細書に記載の実験前に、タンパク質が細胞表面に結合していることそしてタンパク質が血清および他の流体中に観察されるにもかかわらず、ある癌細胞に発現し、血清、および他の体液に流れるCEAは、単一タンパク質であることが仮定された。換言すると、CEA発現を検出した試薬が、細胞表面上に発現し、ある流体中に見出される単一タンパク質の発現を検出し、そして治療効果を提供するためにCEAを標的とした化合物が、このタンパク質に結合すると仮定された。しかしながら、本明細書に詳述されるように、CEAは、一般に、CEAと称される約702アミノ酸タンパク質(成熟タンパク質には存在しない約34アミノ酸N末端シグナルペプチドプロ配列および約17アミノ酸C末端プロ配列の除去前)に対応する完全長型、ならびに本明細書で短型CEAと称されるスプライス変異体の少なくとも2つの型で存在すると思われる。2つの型のCEAの存在は、細胞内のまたは流体中のCEAの検出に基づく診断試験の特異性および関連性について質問を提起する。例えば、診断試験が、完全長および短型CEAの両方を認識することができる試薬に無意識のうちに依存する場合、試験が、生物学的関連性の一貫した結果を提供するかどうか明らかではない。このようなことを踏まえて、短型CEAの特定、およびヒトCEAが、完全長および短型の両方(これらの両方は、細胞表面上または流体中に検出することができる)に存在するという正しい認識は、改善された診断試薬および治療試薬の作製および試験を可能にするという重要な情報を提供することになる。
さらに、本明細書に詳述されるように、短型CEAの特定は、健常な患者からの試料において、ならびにCEAを発現する癌および生物学的流体においての短型CEAの発現の分析を可能にする。さらになお、短型CEAの特定は、例えば、完全長CEA対短型CEAの発現の一致/不一致、短型CEA発現の予後値、短型CEAに対する完全長CEAの比率の予後値、ならびに完全長あるいは短型CEAのいずれかを標的化するが、両方を標的としない特定の診断試薬の生成、および/または最適化の分析を可能にする。さらに、2つの型のCEAの存在の評価、ならびにこのような型の1つのみに特異的な診断試薬および治療試薬を生成する潜在的価値の評価は、適合した試薬の使用を可能にする。つまり、ヘルスケアプロバイダーは、診断目的のために、患者の治療計画の一部として、CEAを標的とする治療試薬によって認識されるものと同一または実質的に同一のCEAのエピトープを認識する試薬を選択することができる。この適合型は、診断および治療試薬が、CEA型に対して同一の特異性を有することを保証する。理論によって拘束されることなく、そのような適合は、治療効果と診断データとの間の相関を改善する可能性がある。
ある態様および実施形態において、本開示の方法は、治療試薬(例えば、癌治療薬)として同一または実質的に同一のエピトープに結合する診断試薬を利用する。これに関連して、2つの試薬は、それらが互いに競合することができる場合、関連濃度で、そのエピトープに結合するために、実質的に同一のエピトープに結合する。例えば、重複するエピトープに結合する試薬は、実質的に同一のエピトープに結合する試薬と称する。そのような抗体は、競合的阻害剤であると言われる場合がある。
(ii) 専門用語
さらなる詳しく本開示の説明を続ける前に、本開示が、特定の組成物またはプロセスステップに限定されないことを理解すべきである。そのようなものは変わり得るものであるからである。本明細書および添付の特許請求の範囲中に使用する場合、単数形の「1つの(a)」、「1つの(an)」、および「その(the)」は、文脈が明らかにそうではないと示していない限り、複数の指示対象を包含していることに留意しなければならない。
アミノ酸は、その一般に公知の3文字記号か、またはIUPAC−IUB生化学命名法委員会(Biochemical Nomenclature Commission)によって推奨される1文字記号のいずれかにより、本明細書中で言及され得る。ヌクレオチドも同様に、一般に受け入れられた1文字コードにより言及され得る。
抗体の、可変領域中のアミノ酸の付番、相補性決定領域(CDR)およびフレームワーク領域(FR)は、別途指示されない限り、Kabat et al.Sequences of Proteins of Immunological Interest, 5th Ed.Public Health Service, National Institutes of Health, Bethesda, MD.(1991)に記述されるような、Kabatの定義に従う。この付番系を用いて、実際の直線状アミノ酸配列は、可変ドメインのFRまたはCDRの短縮、またはそれらへの挿入に対応する、少数のまたはさらなるアミノ酸を含み得る。例えば、重鎖可変ドメインは、H2の残基52の後ろの単一のアミノ酸挿入物(Kabatによれば、残基52)および重鎖FR残基82の後ろに挿入された残基(例えば、Kabatによれば、残基82a、82b、および82cなど)を含み得る。残基のKabat付番は、この抗体の配列の、「標準」Kabat付番配列との相同性の領域でのアラインメントによって、所定の抗体について決定され得る。フレームワーク残基の最大アラインメントは、しばしば、Fv領域に使用されるべき、付番系の「スペーサー」残基の挿入を必要とする。加えて、任意の所定のKabat部位番号でのある特定の個々の残基の同一性は、種間または対立遺伝子の相違のため、抗体鎖間で変化してもよい。
免疫グロブリンとしても知られている、本明細書に使用される「抗体および抗体群」は、モノクローナル抗体(完全長モノクローナル抗体を含む)、ポリクローナル抗体、少なくとも2つの異なるエピトープ結合フラグメントから形成された多特異的抗体(例えば、二重特異性抗体)、ヒト抗体、ヒト化抗体、ラクダ化抗体、キメラ抗体、一本鎖Fv(scFv)、一本鎖抗体、単一ドメイン抗体、ドメイン抗体、Fabフラグメント、F(ab′)2フラグメント、所望の生物学的活性を示す抗体フラグメント(例えば、抗原結合部分)、ジスルフィド結合Fv(dsFv)、および抗イディオタイプ(抗Id)抗体(例えば、本開示の抗体に対する抗Id抗体を含む)、イントラボディー、ならびに上記のいずれかのエピトープ結合フラグメントを包含する。特に、抗体は、免疫グロブリン分子および免疫グロブリン分子の免疫学的に活性なフラグメント、すなわち、少なくとも1つの抗原結合部位を含有する分子を含む。免疫グロブリン分子は、任意のアイソタイプ(例えば、IgG、IgE、IgM、IgD、IgA、およびIgY)、サブアイソタイプ(例えば、IgG1、IgG2、IgG3、IgG4、IgA1、およびIgA2)、またはアロタイプ(例えば、Gm、例えば、G1m(f、z、a、もしくはx)、G2m(n)、G3m(g、b、もしくはc)、Am、Em、およびKm(1、2、もしくは3))からのものであり得る。抗体は、ヒト、サル、ブタ、ウマ、ウサギ、イヌ、ネコ、マウス等、またはトリ(例えば、ニワトリ)等の他の動物を含むが、これらに限定されない、いずれの哺乳動物に由来してもよい。
本明細書に使用される「免疫グロブリン様分子」という用語は、抗体模倣体または抗体様スカフォールドを指す。ある実施形態において、免疫グロブリン様分子は、一本鎖抗体、ダイアボディ、ミニボディ等の非免疫グロブリン抗原結合スカフォールドを含む任意のポリペプチドであり得る。免疫グロブリン様分子は、免疫グロブリン様フォールドを含むことができる。ある態様において、免疫グロブリン様分子は、変異アミノ酸配列を有することによって比較タンパク質から由来され得る。ある実施形態において、免疫グロブリン様分子は、抗体サブ構造、ミニボディ、アドネクチン、アンチカリン、アフィボディ、ノッティン(knottin)、グルボディ(glubody)、C型レクチン様ドメインタンパク質、テトラアクチン、クニツ(kunitz)ドメインタンパク質、チオレドキシン、シトクロムb562、亜鉛フィンガースカフォールド、ブドウ球菌ヌクレアーゼスカフォールド、フィブロネクチンもしくはフィブロネクチンダイマー、テネイシン、N−カドヘリン、E−カドヘリン、ICAM、タイチン、GCSF受容体、サイトカイン受容体、グリコシダーゼ阻害剤、抗生物質色素タンパク質、ミエリン膜接着分子P0、CD8、CD4、CD2、クラスI MHC、T細胞抗原受容体、CD1、C2およびVCAM−1のIセットドメイン、ミオシン結合タンパク質CのIセット免疫グロブリンドメイン、ミオシン結合タンパク質HのIセット免疫グロブリンドメイン、テロキンのIセット免疫グロブリンドメイン、NCAM、トゥイッチン、ニューログリアン、成長ホルモン受容体、エリスロポエチン受容体、プロラクチン受容体、インターフェロンガンマ受容体、β−ガラクトシダーゼ/グルクロニダーゼ、β−グルクロニダーゼ、トランスグルタミナーゼ、T細胞抗原受容体、スーパーオキシドジスムターゼ、組織因子ドメイン、シトクロムF、緑色蛍光タンパク質、GroEL、またはタウマチン由来であり得る。
本明細書に使用される「完全長CEA」という用語は、10エキソンによってコードされる完全長CEACAM5タンパク質またはそのようなタンパク質をコードするヌクレオチド配列を指す。完全長CEAタンパク質は、約702アミノ酸である(NおよびC末端プロ配列の除去前;N末端プロ配列は、約34アミノ酸シグナル配列であり、C末端プロ配列は、約17アミノ酸配列である)。プロ配列を含む完全長CEAタンパク質のアミノ酸配列は、図1に記述され、また、NCBI RefSeq NP_004354.2でGenBankに見出され得る。成熟完全長CEAタンパク質は、配列番号2に記述される。配列番号2に記述される配列は、特定の多型(太字および下線で示される)を参照することに留意されたい。他のCEA多型は、当技術分野で特定されている。しかしながら、表示された多型は、短型CEAに特有のスプライス部位で生じ、故に、本開示に潜在的関連性を有する。例えば、このスプライス部位での多型は、特定の抗体の結合特異性に影響を及ぼし得る可能性がある。ある実施形態において、完全長CEAとは、成熟完全長型のCEA(プロ配列のない)を指す。完全長(または短型)CEAに免疫特異的に結合する診断または治療試薬に対する特異性は、成熟CEAに対する免疫特異性(プロ配列の存在または不在に関係なく)を指すことが意図される。しかしながら、例えば、成熟完全長CEAタンパク質に対して免疫特異的な抗体はまた、プロ配列の存在下で、完全長CEAに免疫特異的に結合することができることも容易に理解されよう。試薬は、成熟標的CEAタンパク質に免疫特異的に結合する(そして、非標的CEAタンパク質に免疫特異的に結合しない)限り、標的CEAタンパク質に対して免疫特異的であると見なされる。しかしながら、その成熟標的CEAに対応するプロタンパク質は、別の型または非標的型のCEAであると見なされない。同様に、可溶性および膜に固定された成熟標的CEAは、非標的型のCEAへの結合であると見なされない、あるいは、免疫特異性の欠如の証拠としても見なされない。さらに、ある試薬が、特定のCEA多型に対して免疫特異性があり得ると理解されるが、1つを超える多型の標的CEAに対する試薬の免疫特性が、非標的型のCEAへの結合であると見なされない、あるいは、免疫特異性の欠如の証拠としても見なされない。
本明細書に使用される「短型CEA」という用語は、約420アミノ酸のCEACAM5のスプライス変異体またはそのようなタンパク質をコードするヌクレオチド配列を指す。短型CEAタンパク質は、エキソン3および4を欠失する完全長CEAのスプライス変異体である。つまり、短型CEAには、完全長CEAの残基116〜396(N末端プロ配列を含むように付番されるとき)のインフレーム短縮型が含まれる。プロ配列を含む短型CEAタンパク質のアミノ酸配列は、配列番号1と記述されている。配列番号1と記述される配列は、特定の多型(太字および下線で示される)を参照することに留意されたい。他のCEA多型は、当技術分野で特定されている。しかしながら、表示された多型は、短型CEAに特有のスプライス部位で生じ、故に、本開示に潜在的関連性を有する。ある実施形態において、短型CEAとは、成熟タンパク質中に存在しないプロ配列のない、成熟短型のCEAを指す。短型CEAに免疫特異的に結合する診断または治療試薬に対する特異性は、成熟CEAに対する免疫特異性(プロ配列の存在または不在に関係なく)を指すことが意図される。しかしながら、例えば、成熟短型CEAタンパク質に対して免疫特異的な抗体はまた、プロ配列の存在下で、短型CEAに免疫特異的にも結合することができることは容易に理解されよう。試薬は、成熟標的CEAタンパク質に免疫特異的に結合する(そして、非標的CEAタンパク質に免疫特異的に結合しない)限り、標的CEAタンパク質に対して免疫特異的であると見なされる。しかしながら、その成熟標的CEAに対応するプロタンパク質は、別の型または非標的型のCEAであると見なされない。同様に、可溶性および膜に固定された成熟標的CEAは、非標的型のCEAへの結合であると見なされない、あるいは、免疫特異性の欠如の証拠としても見なされない。さらに、ある試薬が、特定のCEA多型に対して免疫特異性があり得ると理解されるが、1つを超える多型の標的CEAに対する試薬の免疫特性が、非標的型のCEAへの結合であると見なされない、あるいは、免疫特異性の欠如の証拠としても見なされない。
本明細書に使用される「免疫特異的に結合する」という用語は、抗体等の特異的結合対の1つのメンバーが、診断的もしくは治療的関連濃度で、当技術分野における技術によって測定されるような、例えば、競合ELISAによって、またはBIACOREもしくはKINEXAアッセイを用いたKDの測定によって、その特異的結合パートナー(複数可)以外の分子に有意に結合しない(すなわち、約25%、20%、15%、10%、もしくは5%未満の交差反応)状態を指す。この用語はまた、例えば、本開示の抗体の抗原結合ドメインが、多くの抗原によって担持される特定のエピトープに対して特異的である場合に適用可能であり、そのような場合、抗原結合ドメインを担持する特異的抗体は、エピトープを担持する様々な抗原に特異的に結合することが可能である。ある実施形態において、CEAに免疫特異的に結合する抗体は、癌胎児性抗原関連の細胞接着タンパク質に結合しない。ある実施形態において、CEAに免疫特異的に結合する抗体は、CEACAM1、CEACAM3、CEACAM4、CEACAM6、CEACAM7、およびCEACAM8に結合しない。ある実施形態において、CEAに免疫特異的に結合する抗体は、 CEACAM1、CEACAM3、CEACAM4、CEACAM6、CEACAM7、およびCEACAM8から選択されるタンパク質のうちの少なくとも1つにも結合しない。可溶性および膜結合型の標的CEAの両方に結合する診断または治療試薬の能力は、免疫特異性の欠如の証拠ではないことに留意されたい。実際には、免疫特異的試薬は、しばしば、可溶性および膜結合型の標的CEAの両方に免疫特異的に結合することが好ましい。さらに、成熟標的CEAおよびその成熟標的CEAに対応するプロタンパク質の両方に結合する診断または治療試薬の能力は、免疫特異性の欠如であると見られない。
本明細書に使用される「A5B7」という用語は、CEAに対して免疫特異的なマウスモノクローナル抗体を指し、例えば、WO第07/071426号、Int J Cancer(1988)3:34−37、British J Cancer(1994)69:307−314、Clin Cancer Res(2008)14:2639−2646、British J Cancer(1986)54:75−82、Cancer Res(1992)52:2329−2339に記載されている。
本明細書に使用される「MEDI−565」という用語は、抗CEA結合部分および抗CD3結合部分を含むBiTEクラスの二重特異性一本鎖抗体を指す。抗CEA結合部分は、マウスモノクローナル抗体A5B7由来のヒト化scFvである。MEDI−565は、WO第07/071426号、Lutterbuese et al.,2009,Journal of Immunother 32:341−352、およびOsada et al.、2010,British Journal of Cancer,102:124−33に記載され、開示されている。抗体または抗体様分子のクラスに言及されるとき、「BiTE」という用語は、二重特異性T細胞結びつけ(bi−specific T−cell engager)を指す。そのような分子は、疾患状態と関連する抗原(例えば、癌性細胞上に発現した抗原)に対して免疫特異的である一部分およびそのような罹患した細胞をT細胞に連結する一部分を有する。WO第07/071426号は、BiTE型分子のさらなる例示的な説明を提供する。
(iii) 診断および予後に用いる方法
本明細書に開示される抗体、抗原結合フラグメント、または免疫グロブリン様分子は、疾患および障害、特に、CEA発現に関連する癌の診断および予後評価に有用である。疾患のそれぞれの段階で、抗体は、診断の正確さを向上し、治療判断を促進するために使用され得る。臓器またはリンパ節の大きさまたは構造の変化に依存する、コンピュータ断層撮影(CT)スキャン等の腫瘍および癌のための標準的な診断方法とは異なって、標識抗体は、CEA等の腫瘍抗原の発現または体液へのそのような抗原の脱落から、初期段階で異常細胞を検出することができる。癌が診断された時点で、正確な病期診断が、最も適切な療法を決定する際に、重要である。後で、外科手術後のフォローアップ中または他の治療中もしくはその後、血清および糞便等の体液中の腫瘍抗原のレベルの上昇は、従来の方法によって検出され得る前に、再発を示す場合がある。これらの方法は、特定の標的型のCEAに免疫特異的に結合するが、他の型のCEAには免疫特異的に結合しない抗体等の本明細書に記載の抗体、抗原結合フラグメント、または免疫グロブリン様分子のいずれかとともに使用することができる。
ある態様において、本開示は、CEAを発現する癌の再発を検出する方法を提供する。CEAを発現する癌であると以前診断され、治療を受けたことがある患者は、完全長CEAタンパク質の濃度を検出することによって、癌の再発のための試験が行われ得る。本方法は、その患者の前の結果に見出される完全長CEAタンパク質の濃度を比較することを、長期にわたって繰り返すことができる。これらの方法は、完全長CEAに免疫特異的に結合するが、短型CEAには免疫特異的に結合しない本明細書に記載の抗体、抗原結合フラグメント、または免疫グロブリン様分子(例えば、診断試薬)のいずれかとともに使用することができる。診断ステップが、複数回行われる際、検出ステップは、同一の診断試薬を用いて、または同一もしくは実質的に同一のエピトープに結合する診断試薬を用いて行うことができることが企図される。同様に、CEA濃度が、単一型の生物学的試料(例えば、血清または糞便)中に検出することができる、あるいは、CEA濃度が、1つを超える型の生物学的試料中で測定することができることが企図される。
ある態様において、本開示は、抗CEA癌療法に対する感受性を判定する方法を提供する。CEAを発現する癌であると以前診断されたことがある患者は、完全長CEAタンパク質の濃度を検出することによって、抗CEA癌療法に対する感受性について試験を行うことができる。ある実施形態において、本方法は、完全長CEAタンパク質の濃度を、健常な対象からの試料中の完全長CEAタンパク質の標準濃度を反映する標準と比較することをさらに提供する。これらの方法は、特定の標的型のCEAに免疫特異的に結合するが、他の型のCEAには免疫特異的に結合しない抗体等の本明細書に記載の抗体、抗原結合フラグメント、または免疫グロブリン様分子(例えば、診断試薬)のいずれかとともに使用することができる。診断ステップが、複数回行われる際、検出ステップは、同一の診断試薬を用いて、または同一もしくは実質的に同一のエピトープに結合する診断試薬を用いて行うことができることが企図される。同様に、CEA濃度が、単一型の生物学的試料(例えば、血清または糞便)中に検出することができる、あるいは、CEA濃度が、1つを超える型の生物学的試料中で測定することができることが企図される。
ある態様において、本開示は、抗CEA癌療法をモニタリングする方法を提供する。CEAを発現する癌であると以前診断され、治療を受けたことがある患者は、完全長CEAタンパク質の濃度を検出することによって、モニタリングすることができる。ある実施形態において、本方法は、治療前あるいは治療の早期時点のいずれかで、同一の患者に対して判定された過去の濃度と、完全長CEAタンパク質の濃度を比較することをさらに提供する。これらの方法は、特定の標的型のCEAに免疫特異的に結合するが、他の型のCEAには免疫特異的に結合しない抗体等の本明細書に記載の抗体、抗原結合フラグメント、または免疫グロブリン様分子のいずれかとともに使用することができる。診断ステップが、複数回行われる際、検出ステップは、同一の診断試薬を用いて、または同一もしくは実質的に同一のエピトープに結合する診断試薬を用いて行うことができることが企図される。同様に、CEA濃度が、単一型の生物学的試料(例えば、血清または糞便)中に検出することができる、あるいは、CEA濃度が、1つを超える型の生物学的試料中で測定することができることが企図される。
ある態様において、本開示は、抗CEA治療をモニタリングする方法、またはその患者に使用されるもしくは考えられている癌治療薬と同一もしくは実質的に同一のCEAのエピトープに免疫特異的に結合する抗体を用いて、抗CEA治療に対する感受性を判定する方法を提供する。ある実施形態において、抗CEA治療薬は、標的型のCEAに免疫特異的に結合するが、他の型のCEAには免疫特異的に結合しない。
ある態様において、本開示は、対象からの試料中の、完全長CEAタンパク質の濃度および短型CEAタンパク質の濃度を検出することによって、完全長CEAタンパク質濃度と短型CEAタンパク質濃度との比率を判定するための方法を提供する。ある実施形態において、本方法は、この比率を、健常な対象からの試料中の完全長CEAタンパク質濃度と短型CEAタンパク質濃度との標準比率を反映する標準と比較することをさらに提供する。ある実施形態において、標準比率とは著しく異なる比率は、CEAを発現する癌の存在を示す。ある実施形態において、標準比率とは著しく異なる比率は、抗CEA治療薬に対する感受性を示す。ある実施形態において、治療後の比率の変化は、療法の有効性を示す。ある実施形態において、抗CEA治療薬は、標的型のCEAに免疫特異的に結合するが、他の型のCEAには免疫特異的に結合しない。ある実施形態において、完全長CEAタンパク質の濃度の検出は、完全長CEAタンパク質に免疫特異的に結合するが、短型CEAタンパク質には免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子と、試料を接触させることによって行われる。ある実施形態において、短型CEAタンパク質の濃度の検出は、短型CEAタンパク質に免疫特異的に結合するが、完全長CEAタンパク質には免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子と、試料を接触させることによって行われる。
ある態様において、本開示は、対象からの試料中の、完全長CEAタンパク質をコードするRNAの濃度および短型CEAタンパク質をコードするRNAの濃度を検出することによって、完全長CEAタンパク質濃度をコードするRNAと短型CEAタンパク質濃度をコードするRNAの比を判定するための方法を提供する。ある実施形態において、本方法は、この比率を、健常な対象からの試料中の、完全長CEAタンパク質濃度をコードするRNAと短型CEAタンパク質濃度をコードするRNAの標準比率を示す標準と比較することをさらに提供する。ある実施形態において、標準比率とは著しく異なる比率は、CEAを発現する癌の存在を示す。ある実施形態において、標準比率とは著しく異なる比率は、抗CEA治療薬に対して感受性があることを示す。ある実施形態において、治療後の比率の変化は、療法の有効性を示す。ある実施形態において、抗CEA治療薬は、標的型のCEAに免疫特異的に結合するが、他の型のCEAには免疫特異的に結合しない。ある実施形態において、完全長CEAタンパク質の濃度の検出は、完全長および短型CEAタンパク質をコードするRNAに対して特異的なプライマーおよびまたはプローブを用いて行われる。
診断方法は、患者からの生物学的試料(例えば、血液試料、リンパ節生検、または組織)を用いてインビトロ(エクスビボ)で行うことができるか、あるいはインビボイメージングによって行うことができる。ある実施形態において、生物学的試料(「試料」としても称される)は、全血、血清、血漿、唾液、尿、糞便、精漿、汗、羊水、痰、母乳、胆液、組織ホモジネート、および腹水から選択される。ある実施形態において、生物学的試料は、腫瘍試料である。ある実施形態において、生物学的試料は、患者が患っている、または患っている疑いがある特定のCEAを発現する癌に基づいて選択される。例えば、痰試料は、ある実施形態において、患者が肺癌を患っている場合、選択することができる。さらなる例として、糞便試料は、ある実施形態において、患者が結腸または直腸癌を患っている場合、選択することができる。しかしながら、他の実施形態において、全血、血清、または血漿試料は、癌の型に関わらず、検査される。
特定の実施形態において、本出願は、本開示の抗体、または他の免疫特異的診断試薬が、診断造影剤に共役させる、抗体複合体を提供する。本出願の免疫特異的診断試薬を含む組成物は、例えば、ラジオイムノアッセイ、ELISA、フローサイトメトリー分析(FACSを含むが、これに限定されない)、免疫細胞化学、免疫組織化学等によって、標的CEAを検出するために使用することができる。1つ以上の検出可能な標識は、診断試薬抗体、または一次診断試薬を検出するために使用される二次抗体に結合され得る。例示的な標識部分は、特に、放射線または磁気共鳴画像技術における、放射線不透過性色素、放射線造影剤、蛍光分子、スピン標識分子、酵素、または診断価値のある他の標識部分を含む。ある実施形態において、標的部分は、蛍光分子である。
本開示に従って、放射性標識抗体は、インビトロ診断試験に使用することができる。抗体、その結合部分、プローブ、またはリガンドの比活性は、放射性標識の半減期、同位体純度、およびこの標識がこの生物学的薬剤にいかに組み込まれているかに依存する。免疫学的検定では、一般に、比活性が高いほど、感受性が良好である。例えば、診断で用いる標識として有用な放射性同位体は、ヨウ素(131Iもしくは125I)、インジウム(111In)、テクネチウム(99Tc)、リン(32P)、炭素(14C)、およびトリチウム(3H)、または上に列挙した治療同位体のうちの1つを含む。
放射性標識抗体は、患者に投与することができ、抗体が反応する抗原を担持する癌細胞に局在化し、例えば、ガンマ検出器および放射トモグラフィーを用いた放射性核走査法等の既知の技術を用いてインビボで検出または「画像」される。例えば、Bradwell et al.,“Developments in Antibody Imaging”,Monoclonal Antibodies for Cancer Detection and Therapy,Baldwin et al.,(eds.),pp.65−85(Academic Press 1985)、Wu and Olafsen(2008)Cancer J 14:191−197を参照し、これらは、参照することにより本明細書に組み込まれる。あるいは、放射標識が陽電子(例えば、11C、18F、15O、および13N)を放射するときは、Brookhaven National LaboratoryにあるPet VIと称するもの等の、陽電子放射横断軸断層撮影スキャナーを用いることができる。陽電子走査技術におけるさらなる例示的な情報は、例えば、Gambhir(2002)Nature Reviews 2:683−693に見出され得る。
フルオロフォアおよび発色団標識した生物学的薬剤は、当技術分野で公知の標準的部分から調製することができる。抗体および他のタンパク質が、最高約310nmまでの波長を有する光を吸収するため、蛍光部分は、310nmを超える、例えば、約400nmを超えるような波長で、実質的な吸収を有するように選択することができる。様々な適した蛍光体および発色団は、Stryer,Science,162:526(1968)およびBrand et al.,Annual Review of Biochemistry,41:843−868(1972)によって記載され、これらは、参照することによって本明細書に組み込まれる。抗体は、米国特許第3,940,475号、第4,289,747号、および第4,376,110号(これらは、参照することによって本明細書に組み込まれる)に開示されるもののような従来の手順によって、蛍光性発色団基を用いて標識化することができる。
診断および/または治療試薬に共役され、本方法および本明細書に記載の組成物に使用される、標識は、280nmを上回る波長で、最高の吸収を示し、抗体に共有結合する際にそのスペクトル特性を保持する任意の化学部分、有機物、または無機物である。標識としては、発色団、フルオロフォア、蛍光タンパク質、リン光性色素、タンデム色素、粒子、ハプテン、酵素、および放射性同位体が含まれるが、これらに限定されない。
ある実施形態において、抗標的CEA抗体(診断試薬および/または治療試薬)は、フルオロフォアに共役される。したがって、本開示の標識抗体に使用されるフルオロフォアとしては、ピレン(米国特許第5,132,432号に開示される対応する誘導体化合物のいずれかを含む)、アントラセン、ナフタレン、アクリジン、スチルベン、インドールもしくはベンズインドール、オキサゾールもしくはベンズオキサゾール、チアゾールもしくはベンゾチアゾール、4−アミノ−7−ニトロベンズ−2−オキサ−1,3−ジアゾール(NBD)、シアニン(米国特許第6,977,305号および第6,974,873号に記載のあらゆる対応する化合物を含む)、カルボシアニン(米国特許第09/557,275号、米国特許第4,981,977号、第5,268,486号、第5,569,587号、第5,569,766号、第5,486,616号、第5,627,027号、第5,808,044号、第5,877,310号、第6,002,003号、第6,004,536号、第6,008,373号、第6,043,025号、第6,127,134号、第6,130,094号、第6,133,445号、国際公開WO第02/26891号、WO第97/40104号、WO第99/51702号、WO第01/21624号、欧州特許EP第1 065 250 A1号に記載の、あらゆる対応する化合物を含む)、カルボスチリル、ポルフィリン、サリチレート、アントラニレート、アズレン、ペリレン、ピリジン、キノリン、ボラポリアザインダセン(米国特許第 4,774,339号、第5,187,288号、第5,248,782号、第5,274,113号、および第5,433,896号に記載のあらゆる対応する化合物を含む)、キサンテン(米国特許第6,162,931号、第6,130,101号、第6,229,055号、第6,339,392号、第5,451,343号、第5,227,487号、第5,442,045号、第5,798,276号、第5,846,737号、第4,945,171号、米国出願第09/129,015号および第09/922,333号に開示されるあらゆる対応する化合物を含む)、オキサジン(米国特許第4,714,763号に開示されるあらゆる対応する化合物を含む)もしくはベンゾオキサジン、カルバジン(米国特許第4,810,636号に開示されるあらゆる対応する化合物を含む)、フェナレノン、クマリン(米国特許第5,696,157号、第5,459,276号、第5,501,980号、および第5,830,912号に開示される対応する化合物を含む)、ベンゾフラン(米国特許第4,603,209号および4,849,362号に開示される対応する化合物を含む)、ベンズフェナレノン(米国特許第4,812,409号に開示されるあらゆる対応する化合物を含む)、ならびにそれらの誘導体がふくまれるが、これらに限定されない。本明細書に使用される、オキサジンには、レゾルフィン(第5,242,805号に開示されるあらゆる対応する化合物を含む)、アミノオキサジノン、ジアミノオキサジン、およびそれらのベンゾ置換類似体が含まれる。
特定の実施形態において、本明細書に記載の診断または治療試薬に共役されるフルオロフォアには、キサンテン(ロードール、ローダミン、フルオレセイン、およびそれらの誘導体)、クマリン、シアニン、ピレン、オキサジン、およびボラポリアザインダセンが含まれる。他の実施形態において、そのようなフルオロフォアは、スルホン酸化キサンテン、フッ素化キサンテン、スルホン酸化クマリン、フッ素化クマリン、およびスルホン酸化シアニンである。また、Alexa Fluor、DyLight、Cy Dyes、BODIPY、Oregon Green、Pacific Blue、IRDyes、FAM、FITC、およびROXの商品名で販売され、一般に知られている色素も含まれる。
抗標的CEA診断および/または治療試薬に結合させるフルオロフォアの選択は、共役試薬の吸収および蛍光発光特性を判定するだろう。抗体および抗体結合リガンドに使用することができるフルオロフォア標識の物理的特性としては、スペクトル特性(吸収、発光、ストークスシフト)、蛍光強度、寿命、偏光および光退色速度、またはこれらの組み合わせが含まれるが、これらに限定されない。これらの物理的特性のすべてが、1種のフルオロフォアを別のフルオロフォアと区別するために使用することができ、これによって多様な分析が可能になる。ある実施形態において、フルオロフォアは、480nmを超える波長に吸収極大を有する。他の実施形態において、フルオロフォアは、488nmまたは488nm付近〜514nm(アルゴンイオンレーザー励起源の出力による励起に特に適する)または546nm付近(水銀アークランプによる励起に特に適する)で吸収する。他の実施形態において、フルオロフォアは、組織または生物全体への適用においてNIR(近赤外領域)で発光することができる。蛍光標識の他の所望の特性には、例えば、標識化が、細胞または生物(例えば、生きている動物)において行われる場合、透過性および低毒性を含むことができる。
ある実施形態において、酵素は、標識であり、抗標的CEA診断および/または治療試薬に共役される。検出可能なシグナルの増幅を得ることができ、その結果、増加したアッセイ感度をもたらすため、酵素は、望ましい標識である。酵素自体は、検出可能な応答を生成しないが、適切な基質が酵素に接触した際に基質を分解する機能を果たすため、その変換された基質は、蛍光性、比色性、または発光性のシグナルを生成する。標識試薬上の1つの酵素が、検出可能なシグナルへと変換される複数の基質をもたらすことができるため、酵素は、検出可能なシグナルを増幅する。酵素基質は、好ましい測定可能な生成物、例えば、比色性、蛍光性、または化学発光性の生成物をもたらすように選択される。そのような基質は、当技術分野で広範に使用され、当業者によって周知である。
一実施形態において、発色または蛍光発生基質および酵素の組み合わせは、西洋ワサビペルオキシダーゼ等のオキシドレダクターゼ、および3,3′−ジアミノベンジジン(DAB)および3−アミノ−9−エチルカルバゾール(AEC)等の基質を使用し、これらは、特徴的な色(それぞれ、茶色および赤色)を呈する。検出可能な生成物を呈する他の発色オキシドレダクターゼ基質としては、2,2−アジノ−ビス(3−エチルベンゾチアゾリン−6−スルホン酸)(ABTS)、o−フェニレンジアミン(OPD)、3,3′,5,5′−テトラメチルベンジジン(TMB)、o−ジアニシジン、5−アミノサリチル酸、4−クロロ−1−ナフトールが含まれるが、これらに限定されない。蛍光発生基質としては、ホモバニリン酸または4−ヒドロキシ−3−メトキシフェニル酢酸、Amplex(登録商標)Red試薬およびその変形(米国特許第4,384,042号)を含む還元体フェノキサジンおよび還元体ベンゾチアジン、ジヒドロフルオレセイン(米国特許第6,162,931号)を含む還元体ジヒドロキサンテン、ならびにジヒドロローダミン123を含むジヒドロローダミンが含まれるが、これらに限定されない。チラミド(米国特許第5,196,306号、第5,583,001号、および第5,731,158号)であるペルオキシダーゼ基質は、酵素の作用の前に本質的に検出可能であるが、チラミドシグナル増幅法(TSA)として記載されるプロセスにおいてペルオキシダーゼの作用により「適所に固定される」という点で、独特のクラスのペルオキシダーゼ基質を表す。これらの基質は、顕微鏡検査、フローサイトメトリー、光学式走査、および蛍光光度法による、その後の検出のために、細胞、組織、またはアレイである試料中の標的を標識するのに広く利用されている。
別の実施形態において、発色(および、場合によっては、蛍光発生)基質および酵素の組み合わせは、5−ブロモ−6−クロロ−3−インドリルホスフェート(BCIP)、6−クロロ−3−インドリルホスフェート、5−ブロモ−6−クロロ−3−インドリルホスフェート、p−ニトロフェニルホスフェート、もしくはo−ニトロフェニルホスフェート等の発色基質と組み合わせて、または4−メチルアンベリフェリルホスフェート、6,8−ジフルオロ−7−ヒドロキシ−4−メチルクマリニリルホスフェート(DiFMUP、米国特許第5,830,912号)、フルオレセインジホスフェート、3−O−メチルフルオレセインホスフェート、レソルフィンホスフェート、9H−(1,3−ジクロロ−9,9−ジメチルアクリジン−2−オン−7−イル)ホスフェート(DDAOホスフェート)もしくはELF97、ELF39、または関連するホスフェート(米国特許第5,316,906号および第5,443,986号)等の蛍光発生基質と組み合わせて、酸性ホスファターゼ、アルカリ性ホスファターゼ等のホスファターゼ酵素、またはかかるホスファターゼの組換え型バージョンを使用する。
グリコシダーゼ、特に、β−ガラクトシダーゼ、β−グルクロニダーゼ、およびβ−グルコシダーゼは、さらなる適した酵素である。適切な発色基質としては、5−ブロモ−4−クロロ−3−インドリルβ−D−ガラクトピラノシド(X−gal)および同様のインドリルガラクトシド、グルコシド、ならびにグルクロニド、o−ニトロフェニルβ−D−ガラクトピラノシド(ONPG)およびp−ニトロフェニルβ−D−ガラクトピラノシドが含まれるが、これらに限定されない。一実施形態において、蛍光発生基質には、レソルフィンβ−D−ガラクトピラノシド、フルオレセインジガラクトシド(FDG)、フルオレセインジグルクロニド、およびそれらの構造変異体(米国特許第5,208,148号、第5,242,805号、第5,362,628号、第5,576,424号、および第5,773,236号)、4−メチルアンベリフェリルβ−D−ガラクトピラノシド、カルボキシアンベリフェリルβ−D−ガラクトピラノシド、およびフッ素化クマリンβ−D−ガラクトピラノシド(米国特許第5,830,912号)が含まれる。
さらなる酵素としては、ヒドロラーゼ(例えば、コリンエステラーゼおよびペプチダーゼ)、オキシダーゼ(例えば、グルコースオキシダーゼおよびシトクロムオキシダーゼ)、ならびに適切な基質が公知であるレダクターゼが含まれるが、これらに限定されない。
化学発光を生成する酵素およびその適切な基質は、いくつかのアッセイにおいて好ましい。これらとしては、天然型および組換え型のルシフェラーゼおよびエクオリンが含まれるが、これらに限定されない。さらに、安定なジオキセタン、ルミノール、イソルミノール、およびアクリジニウムエステルを含有するもの等のホスファターゼ、グリコシダーゼ、およびオキシダーゼに対して化学発光を生成する基質が、有用である。
別の実施形態において、ビオチン等のハプテンも、標識として利用される。ビオチンは、酵素系において検出可能なシグナルをさらに増幅する機能を果たすことができ、単離目的のためのアフィニティークロマトグラフィーで使用できるタグとして機能を果たすことができるので、有用である。検出目的では、アビジン−HRP等の、ビオチンに親和性を有する酵素共役体が、使用される。その後、ペルオキシダーゼ基質を加えて検出可能なシグナルを生成することが付加される。
また、ハプテンには、ホルモン、天然および合成薬物、汚染物質、アレルゲン、エフェクター分子、成長因子、ケモカイン、サイトカイン、リンフォカイン、アミノ酸、ペプチド、化学中間体、ヌクレオチド等が含まれる。
ある実施形態において、蛍光タンパク質は、標識として抗体に共役することができる。蛍光タンパク質の例には、緑色蛍光タンパク質(GFP)およびフィコビリタンパク質、ならびにそれらの誘導体が含まれる。蛍光タンパク質、特に、フィコビリタンパク質は、タンデム色素標識した標識試薬を作製する際に特に有用である。これらのタンデム色素は、より大きなストークスシフトを得るために蛍光タンパク質およびフルオロフォアを含み、その発光スペクトルは、蛍光タンパク質の吸収スペクトルの波長からさらにシフトしている。これは、発光した蛍光が最大限に最適化されている試料(つまり、その発光がほとんどまたは少しも、蛍光タンパク質により再吸収されない試料)中の少量の標的を検出する際に特に有利である。このために作用して、その蛍光タンパク質およびフルオロフォアは、エネルギー転移対として機能し、その蛍光タンパク質は、フルオロフォアが吸収する波長で発光し、その後、その蛍光タンパク質のみを用いて得られ得るよりも蛍光タンパク質から遠く離れた波長で、フルオロフォアが発光する。特に有用な組み合わせは、米国特許第4,520,110号、第4,859,582号、第5,055,556号に開示されるフィコビリタンパク質、ならびに米国特許第5,798,276号に開示されるスルホローダミンフルオロフォア、または米国特許第6,977,305号および第6,974,873号に開示されるスルホン化シアニンフルオロフォア、または米国特許第6,130,101号に開示されるスルホン化キサンテン誘導体、ならびに米国特許第4,542,104号に開示されるこれらの組み合わせである。あるいは、フルオロフォアは、エネルギードナーとして機能し、蛍光タンパク質は、エネルギーアクセプターである。
本出願は、そのような検出を必要とする対象における該癌細胞中のCEAのmRNAまたはタンパク質の差次的発現を検出することを含む、癌を検出する方法を提供する。1つの例示的な実施形態において、癌を検出する方法は、a)患者から試料を単離することと、b)本出願の免疫特異的診断試薬と該試料を接触させることと、c)本出願の免疫特異的診断試薬と、該試料細胞の同じ型の非癌性細胞を接触させることと、d)非癌性細胞と、該試料細胞中の発現を検出し、その差異を比較することと、を含む。
ある実施形態において、本出願で用いる診断用の抗体複合体は、インビトロでの使用のために意図され、この抗体は、発色基質との接触の際、着色した生成物を生成する二次結合リガンドまたは酵素(酵素タグ)に連結される。好適な酵素の例には、ウレアーゼ、アルカリ性ホスファターゼ、(西洋ワサビ)水素ペルオキシダーゼおよびグルコースオキシダーゼが挙げられる。ある実施形態において、二次結合リガンドは、ビオチンおよびアビジンまたはストレプトアビジン化合物である。さらに、フルオロフォア、放射性部分等のいずれかが、同様に、インビトロ診断アッセイとの関連で使用することができることを容易に理解されよう。
ある実施形態において、本出願の診断方法は、他の癌診断試験と組み合わせて使用することができる。
本出願はまた、抗CEA免疫特異性診断試薬を含む診断キットも提供する。そのような診断キットは、診断アッセイを行うための使用説明書とともに、既定量の試薬のパッケージ化された組み合わせをさらに含むことができる。免疫特異的診断試薬が、酵素で標識化される場合、キットは、酵素によって要求される基質および補酵素を含む。加えて、他の添加剤は、安定剤、緩衝液等を含むことができる。相対量の様々な試薬は、アッセイの感受性を実質的に最適化する試薬の溶液中の濃度を提供するために広範に変化させることができる。特に、試薬は、分解において、適切な濃度を有する試薬溶液を提供する賦形剤を含む、通常、凍結乾燥された乾燥粉末として提供することができる。
別の態様において、本開示は、CEAタンパク質成分を結合、精製し、定量化、そうでなければ、一般に検出するための免疫学的検定に関する。以下に詳述されるように、それらの最も単純かつ直接的な意味では、免疫学的検定は、結合アッセイである。ある実施形態において、免疫学的検定は、当技術分野で公知の様々な型の酵素結合免疫吸着アッセイ(ELISA)および放射免疫測定(RIA)である。組織切片を用いる免疫組織化学的検出もまた、特に、有用である。しかしながら、検出が、そのような技法に限定されず、ウエスタンブロッティング、ドットアンドスロットブロッティング、フローサイトメトリー分析等もまた使用することが容易に理解されよう。
様々な有用な免疫学的検定のステップは、例えば、Nakamura et al.,in Enzyme Immunoassays:Heterogeneous and Homogeneous Systems,Chapter 27(1987)等の科学文献に記載されており、参照することにより本明細書に組み込まれる。
一般に、免疫結合法は、タンパク質またはペプチド(この場合、CEA)を含有する疑いがある試料を得ること、および免疫複合体の形成を可能にするのに有効な条件下でCEAとの免疫反応性のある第1の抗体と試料を接触させることを含む。
免疫結合方法は、CEAタンパク質を精製するための方法を含み、患者の試料からのタンパク質の精製において、または組み換えにより発現したタンパク質を精製するために採用することができる。それらはまた、組織試料または他の生物学的試料中のCEAの量を検出または定量化するための方法も含み、結合過程で形成された任意の免疫複合体の検出または定量化を必要とする。
分析した生物学的試料は、CEAを含むと考えられる任意の試料、例えば、均質化した新生物組織試料であってよい。選択された生物学的試料を、免疫特異的診断試薬(一次免疫複合体の形成を可能にするのに有効な条件下で、十分な時間)と接触させることは、一般に、免疫特異的診断試薬を試料に添加すること、および存在する任意の標的CEAを用いて免疫複合体を形成する、すなわち、結合するために、免疫特異的診断試薬に対して十分な期間にわたる混合物のインキュベーションの問題である。この試料−抗体組成物を徹底的に洗浄して、いかなる非特異的に結合した種を除去し、一次免疫複合体内の特異的に結合される免疫特異的診断試薬のみを検出させる。
一般的に、免疫複合体形成の検出は、当技術分野で公知であり、多数のアプローチの適用を通して達成され得る。これらの方法は、放射性、蛍光、生物学的、または酵素的タグの検出に基づいている。もちろん、当技術分野で公知であるように、二次抗体等の二次結合リガンドまたはビオチン/アビジンリガンド結合配置の使用を通してさらなる有利性を見出し得る。
検出に使用される抗CEA免疫特異的診断試薬は、それ自体、検出可能な標識に共役されることができ、単にこの標識を検出する。それによって、組成物中の一次免疫複合体の量が決定される。
あるいは、一次免疫複合体内で結合することになる第1の免疫特異的診断試薬が、その抗体に対して結合親和性を有する第2の結合リガンドを用いて検出され得る。これらの場合、第2の結合リガンドは、検出可能な標識に連結され得る。第2の結合リガンドは、それ自体、抗体であることが多く、したがって、「二次」抗体と称される場合がある。一次免疫複合体を、二次免疫複合体の形成を可能にするのに効果的な条件下および十分な時間、標識された二次結合リガンドまたは抗体と接触させる。二次免疫複合体は、任意の非特異的に結合した標識二次抗体またはリガンドを除去するために広範囲に洗浄され、二次免疫複合体における残りの標識が検出される。
特に、完全長および短型の両方の検出が望ましい実施形態(例えば、完全長と短型との比率を評価する場合)では、例えば、完全長CEAタンパク質および短型CEAタンパク質の濃度を検出するために異なる検出可能な標識を用いることによって、同一のアッセイにおいて、両方のタンパク質の濃度を測定することが企図される。しかしながら、2つの型のCEAタンパク質が、別個に、例えば、同一の患者試料の2つのアリコートで、評価することができることも企図される。
酵素結合免疫吸着アッセイ(ELISA)は、結合アッセイの一種である。1つの型のELISAでは、本出願の診断方法に使用される抗CEA免疫特異的診断試薬は、ポリスチレンマイクロタイタープレート内のウェル等のタンパク質親和性を示す選択された表面上に固定化される。次いで、疑わしい新生物組織試料をウェルに添加する。結合および非特異的に結合した免疫複合体を除去するために除去した後、結合した標的CEAを検出することができる。検出は、一般的に、検出可能な標識に連結されている、標的CEAに対してのみ免疫特異的である必要のないもう1つの抗CEA抗体の添加により達成される。この型のELISAは、単純な「サンドイッチELISA」である。検出はまた、第2の抗CEA抗体の添加、続いて、二次抗体に対する結合親和性を有する第3の抗体の添加によって達成されることができ、第3の抗体は、検出可能な標識に連結されている。
別の型のELISAでは、新生物組織試料は、ウェル表面上に固定化され、本出願において使用される抗CEA免疫特異的診断試薬と接触させる。結合および非特異的に結合した免疫複合体を除去するために洗浄した後、結合した抗CEA免疫特異的診断試薬が検出される。最初の抗CEA免疫特異的診断試薬が、検出可能な標識に連結されている場合、免疫複合体は、直接検出され得る。あるいは、免疫複合体は、第1の抗CEA免疫特異的診断試薬に対する結合親和性を有する二次抗体を用いて検出されることができ、二次抗体は、検出可能な標識に連結されている。
採用した形式に関わらず、ELISAは、ある共通の機能、例えば、コーティング、インキュベーション、または結合、非特異的に結合した種を除去するための洗浄、結合した免疫複合体の検出を有する。
放射免疫測定(RIA)は、抗体分子上の抗原結合部位に対する抗原の競合(親和性)に依存する分析技法である。標準曲線は、同一の既知濃度の標識抗原、および様々であるが、既知濃度の非標識抗原をそれぞれ含有する一連の試料から収集したデータから構築される。抗原は、放射性同位体トレーサーで標識される。その混合物を、免疫特異的診断試薬と接触させてインキュベートする。次いで、遊離抗原は、免疫特異的診断試薬から分離し、それと結合させる。次いで、ガンマまたはベータ放射線検出器等の適切な検出器を用いて、結合または遊離した標識抗原のいずれか、または両方の割合を決定する。この手順を、非標識抗原の様々な既知濃度を含有するいくつかの試料に対して反復し、結果を標準グラフとしてプロットする。結合トレーサー抗原率は、抗原濃度の関数としてプロットされる。典型的には、総抗原濃度は、増加するにつれ、抗体に結合したトレーサー抗原の相対量は、減少する。標準グラフを準備した後、分析を行っている試料中の抗原の濃度を決定するために標準グラフを使用する。
分析において、抗原の濃度を決定すべき試料を、既知量のトレーサー抗原と混合する。トレーサー抗原は、試料中にあることが既知である同一の抗原であるが、適切な放射性同位体で標識されている抗原である。次いで、トレーサーを有する試料を、抗体と接触させてインキュベートする。次いで、試料中の残りの遊離抗原を、計測に適した検出器において計測することができる。抗体または免疫吸着剤と結合した抗原も、同様に計測され得る。次いで、標準曲線から元の試料中の抗原濃度を決定する。
前述のものは、生物学的試料中の標的CEAの濃度を検出するために使用することができる特定の診断技法の単なる例示である。本開示の免疫特異的診断試薬は、標的CEAに免疫特異的に結合するが、非標的型のCEAには免疫特異的に結合しない。
(iv)役立つ治療方法
ある実施形態において、本開示の抗CEA治療薬およびその組成物は、癌の予防および/または治療のために投与することができる。本開示は、CEA媒介型疾患または障害を予防、治療、維持、改善、または阻害するための方法を包含し、これらの方法は、抗CEA治療薬を投与することを含む。ある実施形態において、抗CEA治療薬は、標的型のCEAに免疫特異的に結合するが、他の型のCEAには免疫特異的に結合しない。ある実施形態において、治療薬は、抗体である。ある実施形態において、抗CEA抗体は、標的型のCEAに免疫特異的に結合するが、他の型のCEAには免疫特異的に結合しない。
本明細書に使用される、上皮または他の腫瘍との関連で、本開示の薬学的組成物の「有効量」または「治療有効量」とは、一次、局所的、または転移性腫瘍組織を破壊、修正、制御、または除去するのに十分な治療薬剤の量を指す。治療有効量は、上皮腫瘍の広がりを遅延させるまたは最小化するのに十分な治療薬剤の量を指すことができる。治療有効量はまた、上皮腫瘍の治療または管理において、治療的有用性を提供する治療薬剤または薬学的薬剤の量を指すこともできる。さらに、本開示の治療薬剤または薬学的薬剤に関する治療有効量は、上皮腫瘍の治療または管理において、治療的有用性を提供する、治療薬剤または薬学的薬剤のみの量、または他の両方と組み合わせた量を意味する。本開示の抗体の量に関連して使用される、この用語は、全体の療法を改善し、望ましくない効果を軽減もしくは回避し、別の治療薬剤の治療有効性を増進する、または別の治療薬剤との相乗作用(本明細書に定義されるような)を与える、量を包含することができる。ある実施形態において、治療有効量の治療薬は、全体の療法を改善し、望ましくない効果を軽減もしくは回避するか、または、上皮腫瘍の治療での別の治療薬剤の治療有効性を増進するか、あるいは別の治療薬剤との相乗作用を与える。例えば、抗CEA抗体は、単剤療法として患者に投与される場合、上皮腫瘍の直径の20%の縮小を引き起こすことができる。対照的に、二次治療薬、例えば、以下に定義される抗癌剤は、10%の腫瘍の縮小を引き起こすことができる。しかしながら、抗CEA抗体および該二次治療薬の両方が、併用療法の形態で組み合わせて投与される場合、50%の腫瘍の縮小が観察され得る。そのような効果は、本明細書に使用される相乗効果として理解される。本明細書に言及される場合、「療法」という用語は、上皮腫瘍の予防、治療、または改善に使用することができる任意の投与スキーム、方法、および/または薬剤を指す。「上皮腫瘍の予防、治療、または改善」という用語は、以下にさらに詳述される。「療法」という用語は、生物学的療法、支持療法、化学的療法、放射線療法、および/または上皮腫瘍、もしくは1つ以上のその症状の治療、予防、または改善に有用な他の療法を指すことができる。
本明細書に使用される、患者への1つまたは複数の療法を投与するという状況で、「治療する(treat)」、「治療(treatment)」、および「治療すること(treating)」という用語は、上皮腫瘍の進行、重症度、および/または持続時間の軽減または改善を指す。該上皮腫瘍(複数可)は、異常な発現、例えば、CEAの過剰発現もしくは活性、および/または1つ以上の療法における薬剤投与(1つ以上の薬学的または治療薬剤の投与を含む)に起因する1つ以上のその症状の改善との関連があり得る。
治療は、経口投与、局所性投与、注射によって、鼻腔内、直腸に、経皮的、眼球内挿入、カテーテル、ワイヤー、もしくはインプラント等の含浸もしくは被覆装置、または他の投与の経路の中でイオン泳動による治療薬剤の投与を含むことができる。
文脈は、治療がまた、治療レジメンまたは療法とも交換可能に使用されることを示すことを留意されたい。つまり、治療という用語は、患者の治療レジメンのすべてまたは一部を指すことができる。ある実施形態において、そのような治療レジメンは、標的CEAに免疫特異的に結合する抗CEA癌治療薬の投与を含む。そのような治療はまた、単独でまたは抗CEA癌治療薬に加えて、1つ以上のさらなる治療法を含むこともできる。そのような1つ以上のさらなる治療法としては、外科手術、化学療法、放射線療法、鍼療法、栄養療法、薬草療法等が含まれるが、これらに限定されない。ある実施形態において、治療には、標的CEAに免疫特異的に結合する抗CEA癌治療薬の投与を含み、患者は、抗CEA癌治療薬と同一または実質的に同一のエピトープに免疫特異的に結合する診断試薬を用いる診断に従う。ある実施形態において、診断試薬および抗CEA癌治療薬は、同一の抗体であるか、または少なくとも1つの抗原結合ドメインを共有する。ある実施形態において、診断試薬は、MEDI−565および/またはその変異体ではないが、治療試薬は、MEDI−565および/またはその変異体である。
注射による投与では、抗CEA治療薬は、眼球内、眼周囲、筋肉内、動脈内、皮下、または静脈内に注射することができる。ポンピング機構は、事前選択された期間にわたって、抗CEA治療薬を投与するために採用することができる。本開示のいくつかの実施形態では、薬物を局所に送達することが望ましく、したがって、注射は、眼周囲、眼球内、硝子体内、結膜下、眼球後方、強膜、または前眼房になされ得る。本開示のいくつかの実施形態では、全身送達が好ましい。ある実施形態において、投与は、所定の時間/期間にわたる静脈内投与である。
全身投与では、抗CEA治療薬は、経口用に配合され、投与することができる。治療薬剤の局所あるいは全身への送達のいずれかをもたらし得る投与では、本開示の組成物は、鼻腔内、経皮的、吸入によって、または経口投与のいくつかの形態によって、例えば、胃腸管から吸収不良である本開示の化合物を組み込むうがい薬またはトローチ剤を用いて、投与することができる。本開示の組成物の局所または局所的送達をもたらし得る投与では、イオン導入または局所性投与を使用することができる。
抗CEA療法が単独で投与され得る一方、ある実施形態において、投与は、薬学的に許容される担体を介してなされる。好適な薬学的担体は、当技術分野で公知であり、リン酸緩衝生理食塩水、水、リポソーム、様々な種類の湿潤剤、滅菌溶液等が含まれる。そのような担体を含む組成物は、公知の従来の方法によって製剤化することができる。これらの薬学的組成物は、好適な用量で、対象に投与することができる。用量レジメンは、担当の医師および臨床的因子によって決定される。医療業界で周知であるとおり、いずれか一人の患者のための投薬量は、患者の大きさ、体表面積、年齢、投与されるべき特定の化合物、性別、投与の時間および経路、全般的健康度、および併用して投与される予定の他の薬物を含む多くの因子による。非経口投与のための製剤としては、滅菌水性または非水性溶液、および懸濁液が含まれる。非水性溶媒の例は、プロピレングリコール、ポリエチレングリコール、およびオレイン酸エチル等の注射可能な有機エステルである。水性担体には、生理食塩水および緩衝媒体を含む、水、水性溶液、または懸濁液が含まれる。非経口ビヒクルとしては、塩化ナトリウム溶液、リンガーのデキストロース、デキストロースおよび塩化ナトリウム、乳酸化リンガー液、または固定油が含まれる。静脈内ビヒクルには、流動体および栄養補給剤、電解質補給剤(リンガーのデキストロースに基づいたもののような)等が含まれる。例えば、抗微生物剤、抗酸化剤、キレート剤、および不活性ガス等の保存剤および他の添加剤も、存在し得る。加えて、組成物は、ヒト起源のある実施形態において、例えば、血清アルブミンまたは免疫グロブリン等のタンパク質担体を含んでもよい。併用療法は、抗CEA療法に加えて、薬学的組成物の使用目的によって、さらなる生物学的に活性な薬剤を含むことができることが想定される。そのような薬剤は、胃腸管系に作用する薬剤、細胞増殖抑制剤(cytostatica)として作用する薬剤、高尿酸血症を予防する薬剤、免疫反応を阻害する薬剤(例えば、コルチコステロイド、FK506)、循環系に作用する薬剤、および/またはT細胞共刺激分子もしくはサイトカイン等の当技術分野で公知の薬剤であってよい。ある実施形態において、抗CEA療法は、緩衝液、安定剤、および界面活性剤中に製剤化される。緩衝液は、リン酸、クエン酸、コハク酸、または酢酸緩衝液であってもよい。安定剤は、アミノ酸(複数可)および/または糖類であってもよい。界面活性剤は、洗浄剤、PEG等であってもよい。ある実施形態において、抗CEA療法は、クエン酸塩、リシン、トレハロース、およびTween80中に製剤化される。該薬学的組成物のための希釈剤としては、等張塩類溶液およびTween80が好ましい。
本明細書に使用される「寛解(amelioration)」という用語は、疾患、すなわち、上皮腫瘍の重症度における改善または緩和を指す。例えば、そのような寛解は、本開示の薬学的組成物の投与に起因する、安定な疾患の達成、またはさらにより好ましくは、上皮腫瘍の縮小、すなわち、微小、部分的応答または完全寛解であり得る。「安定な疾患」とは、臨床的および/もしくは組織学的診断方法によって、腫瘍進行/増殖が全くまたはほとんど観察されないまたは検出されない疾患状態を指す。例えば、指標病変の断面積の合計が50%より多くの縮小である、腫瘍の縮小は、「部分的応答」と考えられ得る。「完全寛解」は、治療後に病変がこれ以上全く検出することができない状態を意味する。安定な疾患と部分的応答との間の腫瘍縮小を伴う応答は、微小応答と考えられ得る。例えば、指標病変の断面積の合計の20%、25%、または30%縮小は、微小応答と称され得る。本明細書に使用される「寛解」はまた、上皮腫瘍の数の減少も包含する。それは、さらに、腫瘍進行の阻止/減速を意味する。さらに、治療しなかった患者と比較して、治療した腫瘍患者の全体的な生存の改善は、本明細書に使用される「寛解」として考えられ得る。これは、必要な変更を加えて、治療しなかった腫瘍患者と比較して、治療した腫瘍患者の進行のない生存または再発のない生存の改善にも当てはまる。加えて、「寛解」という用語は、上皮腫瘍の症状の強度の減少も指し、その結果得られる、例えば、治療した腫瘍患者の生活の質の改善も指すことができる。
本明細書に使用される「上皮腫瘍の予防」という用語は、次のように理解される。ヒト患者からの原発上皮腫瘍の外科切除後、および/または原発上皮腫瘍の化学療法または放射線治療後に、腫瘍細胞のすべてが身体から排除されない場合もあり得る。しかしながら、これらの残存腫瘍細胞は、患者において再発性癌、すなわち、局所再発および/または転移を引き起こす可能性がある。転移は、よく見られる癌の合併症であるが、癌細胞が原発腫瘍から播種されて遠位のコロニーを形成する過程はあまり分かっていない。転移性癌は、ほぼ例外なく難治性で新しい治療方法の必要性が生じる。本開示の薬学的組成物を使用して、これらの播種された腫瘍細胞を死滅させて二次性腫瘍(一次療法後に身体に残存する腫瘍細胞から生じる)の形成を予防することができる。このようにして、薬学的組成物は、腫瘍患者において、局所再発および/または転移の形成を予防するために役立つ。
抗腫瘍療法の成功は、それぞれの疾病について、例えば、コンピュータ断層撮影、X線、核磁気共鳴断層撮影(例えば、米国国立癌研究所の判定基準に基づく応答評価[Cheson(1999),J.Clin.Oncol.;17(4):1244])、陽電子放射断層撮影走査、内視鏡検査、蛍光活性化細胞分類、骨髄の吸引、胸水または腹水、組織/組織学、および様々な上皮腫瘍特異的臨床化学パラメータ(例えば、血清中の可溶性CEA濃度)により確立された標準的な方法でモニターすることができ、さらに、他の確立された標準的な方法を用いてよい。加えて、T細胞の活性化を判定するアッセイを用いてもよい;例えば、WO第99/054440号を参照のこと。治療しなかった腫瘍患者と比較して、治療した腫瘍患者の全体的な生存、進行のない生存または再発のない生存の決定のために統計学を用いることができる。
ある実施形態において、該上皮腫瘍は、胃腸腺癌、乳腺腺癌、または肺腺癌である。ある実施形態において、該胃腸腺癌は、結腸直腸腺癌、膵臓腺癌、食道腺癌、または胃腺癌である。
他の実施形態において、本開示の該薬学的組成物は、腫瘍患者の血清/血漿中の高レベルの可溶性CEA抗原を特徴とする、進行性腫瘍、後期腫瘍、腫瘍負荷量/腫瘍組織量が高い腫瘍患者、転移性腫瘍、またはCEA血清中濃度が100ng/mLより高い腫瘍患者(例えば、ELISAにより測定)の治療のためのものである。
本開示の使用または方法の別の実施形態において、上記に定義されるような該薬学的組成物は、追加薬物と組み合わせて、すなわち、併用療法の一部として、投与されるのに適している。
ある実施形態において、抗CEA抗体または治療薬学的組成物は、1つ以上の他の治療薬と組み合わせて投与される。ある実施形態において、抗CEA抗体または治療薬学的組成物は、1つ以上の他の治療薬と同時に患者に投与される。ある実施形態において、そのような治療薬は、上皮腫瘍の治療に有用である。「同時に」という用語は、厳密に同一時点での薬学的組成物または治療薬剤の投与に限定されるものではなく、抗CEA抗体または治療薬学的組成物が他の薬剤と共に作用して、それらがそれ以外の様態で投与された場合よりも増加した利益をもたらし得るように、ある配列および時間間隔内で、抗CEA抗体または治療薬学的組成物が対象に投与されることを意味する。例えば、それぞれの治療薬剤は、同時に、または異なる時点においていずれかの順序で連続的に投与され得るが、それらは、同時に投与されない場合には、所望の治療効果が得られるように、時間的に十分に接近して投与されるべきである。それぞれの治療薬剤は、任意の適当な形態および任意の適当な経路で、別々に対象に投与することができる。他の実施形態において、抗CEA抗体または治療薬学的組成物は、外科手術前に、同時に、またはその後に投与される。ある実施形態において、外科手術は、局所性上皮腫瘍を完全に切除し、サイズの大きい上皮腫瘍を縮小させる。外科手術はまた、予防手段として、または痛みを鎮めるために行うこともできる。本明細書に提供される投与の投薬量および頻度は、上で定義されるように、「治療効果のある」という用語によって包含される。投薬量および頻度は、さらに、一般的に、それぞれの患者に対して特異的な要因に従って異なり、これは、投与される特定の治療または予防薬剤、上皮腫瘍の重症度および型、投与経路、ならびに年齢、体重、反応、および患者の過去の病歴によって異なる。好適なレジメンは、そのような因子を考慮することによって、および例えば、文献に報告され、Physicians’ Desk Reference(59th ed.,2005)で推奨されている投薬量に従うことにより、当業者によって選択することができる。
いくつかの実施形態において、抗CEA抗体または治療薬学的組成物の投与による療法は、1つ以上の療法、例えば、化学療法、放射線療法、ホルモン療法、および/または生物学的療法/免疫療法の投与と組み合わせる。治療薬剤には、ペプチド、ポリペプチド、タンパク質(翻訳後修飾されたタンパク質、抗体等を含む)、または小分子(1000ダルトン未満)、無機もしくは有機化合物、または核酸分子(2本鎖もしくは1本鎖DNA、または2本鎖もしくは1本鎖RNA、ならびに三重らせん核酸分子を含む)が含まれるが、これらに限定されない、タンパク質性分子が含まれるが、これらに限定されない。治療薬剤は、任意の既知生物(動物、植物、細菌、真菌、および原生生物、またはウイルスが含まれるが、これらに限定されない)に由来するか、または合成分子ライブラリーに由来してよい。
特定の実施形態において、本開示の方法および使用は、キナーゼ、例えば、当技術分野に記載されるゲフィチニブ(イレッサ)、エルロチニブ(タルセバ)、抗EGFR抗体(例えば、セツキシマブ、エルビタックス)、または抗Her2/neu抗体(例えば、トラスツズマブ、ハーセプチン)の阻害剤である1つ以上の治療薬剤の投与と組み合わせた、抗CEA抗体または治療薬学的組成物の投与を包含し、例えば、Hardie and Hanks(1995)The Protein Kinase Facts Book,I and II,Academic Press,San Diego,Californiaを参照のこと。
別の特定の実施形態において、本開示の方法および使用は、例えば、当技術分野に記載される、抗VEGF抗体(例えば、ベバシズマブ;アバスチン)、小分子化合物(例えば、バタラニブもしくはソラフェニブ)、またはCOX阻害剤である、1つ以上の治療薬剤の投与と組み合わせた、抗CEA抗体または治療薬学的組成物の投与を包含する。
別の特定の実施形態において、本開示の方法および使用は、例えば、当技術分野に記載される、5−フルオロウラシル、ロイコボリン、カペシタビン、オキサリプラチン、イリノテカン、ゲムシタビン、ドキソルビシン、エピルビシン、エトポシド、シスプラチン、カルボプラチン、タキサン類(例えば、ドセタキセル、パクリタキセル)である、1つ以上の治療薬剤の投与と組み合わせた、抗CEA抗体または治療薬学的組成物の投与を包含する。
ある実施形態において、さらなる治療薬剤と組み合わせた抗CEA抗体または治療薬学的組成物を用いて、上皮腫瘍を患っている患者の併用療法は、相乗効果をもたらす。本明細書に使用される「相乗な」という用語は、任意の2つ以上の単一療法(例えば、1つ以上の治療薬剤)の相加効果よりも効果的な療法の組み合わせ(例えば、上に説明される、抗CEA抗体または治療薬およびさらなる治療薬剤の組み合わせ)を指す。例えば、抗CEA抗体または治療薬は、単剤療法として患者に投与される場合、上皮腫瘍の直径の20%の縮小を引き起こすことができる。対照的に、二次治療薬、例えば、以下に定義される抗癌剤は、10%の腫瘍の縮小を引き起こすことができる。しかしながら、抗CEA抗体または治療薬および該二次治療薬の両方が、併用療法の形態で組み合わせて投与される場合、50%の腫瘍の縮小が観察され得る。
療法の組み合わせ(例えば、上に説明される、抗CEA抗体または治療薬およびさらなる治療薬剤(複数可))の相乗効果により、低投薬量の1つ以上の療法(例えば、1つ以上の治療薬剤)および/または疾患、例えば、上皮腫瘍のある患者へ該療法の低頻度の投与が可能となる。低投薬量の療法(例えば、治療薬剤)を用いることができ、かつ/または該療法を低頻度で投与することができると、疾患、例えば、上皮腫瘍の予防または治療において該療法の効果を低下させることなく、該療法の対象への投与に関連する毒性が低減される。加えて、相乗効果は、上皮腫瘍(CEAの異常な発現(例えば、過剰発現)または活性を伴う可能性がある)の予防、制御、治療、および/または寛解において、療法(例えば、治療薬剤)の改善された有効性をもたらし得る。最後に、療法(例えば、治療薬剤)の組み合わせの相乗効果は、任意の単一療法の使用に関連する、有害なまたは望ましくない副作用を回避または減少させることができる。
該併用療法において、活性薬剤は、任意に、抗CEA抗体または治療薬と同一の薬学的組成物中に含まれ得るか、または別個の薬学的組成物中に含まれ得る。この後者の場合、該別個の薬学的組成物は、抗CEA抗体または治療薬を含む該薬学的組成物の投与よりも前に、同時に、または後に、投与されるのに適している。さらなる薬物または薬学的組成物は、非タンパク質性化合物またはタンパク質性化合物であり得る。さらなる薬物が、タンパク質性化合物である場合、該タンパク質性化合物は、免疫エフェクター細胞の活性化シグナルを提供できることが有利である。
ある実施形態において、該タンパク質化合物または非タンパク質化合物は、抗CEA抗体または治療薬と同時に、または非同時に投与することができる。ある実施形態において、治療されるべき該対象は、ヒトである。
癌療法およびそれらの用量、投与経路および推奨される使用は、当技術分野で既知であり、Physician’s Desk Reference(56th ed.,2002)等の文献に記載されている。
ある実施形態において、治療レジメンは、抗CEA部分および抗CD3部分の両方を含む二重特異性抗体(二重特異性一本鎖抗体を含む)による治療を含む。ある実施形態において、本開示の方法で使用されるべき治療薬は、MEDI−565である。MEDI−565を含むそのような二重特異性抗体により治療するための特定の方法は、PCT公開WO第2007/071426号に見出され、これは、参照することによりその全体が本明細書に組み込まれる。Lutterbuese et al.,2009,Journal of Immunotherapy 32:341−352、Osada et al.2010,British Journal of Cancer,102:124−33、およびMedical News Today(http://www.medicalnewstoday.com/articles/145690.php)も参照されたく、これらのそれぞれは、MEDI−565を説明し、参照することによりそれらの全体が本明細書に組み込まれる。ある実施形態において、使用されるべき治療薬には、少なくとも、MEDI−565と同一または実質的に同一のエピトープに結合するCEA結合部分が含まれる。
ある実施形態において、使用されるべき治療薬は、少なくとも、配列番号28〜44および46〜51のいずれかで表されるアミノ酸配列を含むCEA部分を含む。ある実施形態において、使用されるべき治療薬は、配列番号28〜44および47のいずれかで表されるアミノ酸配列を含む二重特異性抗体である。ある実施形態において、使用されるべき治療薬は、配列番号34、36、41、42、43、および47のいずれかで表されるアミノ酸配列を含む二重特異性抗体である。ある実施形態において、使用されるべき治療薬は、配列番号37〜40のいずれかで表されるアミノ酸配列を含む二重特異性抗体である。ある実施形態において、使用されるべき治療薬は、配列番号48で表されるアミノ酸配列を含む二重特異性抗体である。ある実施形態において、使用されるべき治療薬は、配列番号49で表されるアミノ酸配列を含む二重特異性抗体である。ある実施形態において、使用されるべき治療薬は、配列番号48および49で表されるアミノ酸配列を含む二重特異性抗体である。ある実施形態において、使用されるべき治療薬は、配列番号46で表されるアミノ酸配列を含む二重特異性抗体である。
ある実施形態において、使用されるべき治療薬は、二重特異性一本鎖抗体等の二重特異性抗体である。第1および第2の結合ドメイン、例えば、二重特異性抗体または二重特異性一本鎖抗体内の配列の順序は、関連がある。結合ドメインの配列は、VHCEA−VLCEA−VHCD3−VLCD3、VLCEA−VHCEA−VHCD3−VLCD3、VHCD3−VLCD3−VHCEA−VLCEA、またはVHCD3−VLCD3−VLCEA−VHCEAであり得ることが想定される。いくつかの例において、ヒトCD3に特異的に結合する第1の結合ドメインは、VH−VL配向に配列される。例えば、本明細書に定義される二重特異性一本鎖抗体の結合ドメインは、VHCEA−VLCEA−VHCD3−VLCD3またはVLCEA−VHCEA−VHCD3−VLCD3の順序に配列され得る。この文脈に使用される、「N末端に」または「C末端に」およびその文法的な変形は、分子の絶対的なNまたはC末端での配置よりもむしろ、一次アミノ酸配列内の相対的位置を示す。したがって、非限定例として、「第2の結合ドメインにC末端に位置する」第1の結合ドメインは、単に、第1の結合ドメインが、二重特異性抗体内の第2の結合ドメインのカルボキシル側に位置し、さらなる配列、例えば、上で説明されるタグ、または放射性同位体等の別のタンパク質もしくは非タンパク質化合物が、二重特異性抗体の最終C末端で位置する可能性を除外しないことを意味する。
ある実施形態において、治療薬は、結合ドメインが、VHCEA−VLCEA−VHCD3−VLCD3またはVLCEA−VHCEA−VHCD3−VLCD3の順序で配列される、二重特異性抗体または二重特異性一本鎖抗体である。ある実施形態において、配列は、VLCEA−VHCEA−VHCD3−VLCD3である。ある実施形態において、治療薬は、配列番号46に定義される、二重特異性一本鎖抗体構築物A240 VL−B9 VHx配列番号50 VHVLである。
いくつかの例において、二重特異性抗体または二重特異性一本鎖抗体のヒトCEAに免疫特異的に結合する結合ドメインは、少なくとも1つのCDR、例えば、CDR−H3、例えば、アミノ酸配列「FYFDY」(配列番号28)が、それぞれ、マウスモノクローナル抗体A5B7のCDR−H3のKabat位置100、100a、100b、101、および102に対応する、マウスモノクローナル抗体A5B7のCDR−H3の一部を含む。いくつかの例において、CDH−H3は、アミノ酸配列「DX1X2X3X4FYFDY」(配列番号29)を有し、「X1」、「X2」、「X3」、または「X4」は、あらゆるアミノ酸残基を表し、アミノ酸残基「D」は、マウスモノクローナル抗体A5B7のCDR−H3のKabat位置95に対応し、アミノ酸残基「FYFDY」は、それぞれ、マウスモノクローナル抗体A5B7のCDR−H3の、Kabat位置100、100a、100b、101、および102に対応する。この点で、「X1」、「X2」、「X3」、および「X4」は、それぞれ、マウスモノクローナル抗体A5B7のCDR−H3の、Kabat位置96(「X1」)、97(「X2」)、98(「X3」)、および99(「X4」)に対応する。「X1」、「X2」、「X3」、または「X4」は、アミノ酸残基「R」(アルギニン)、「G」(グリシン)、「L」(ロイシン)、「Y」(チロシン)、「A」(アラニン)、「D」(アスパラギン酸)、「S」(セリン)、「W」(トリプトファン)、「F」(フェニルアラニン)、または「T」(トレオニン)を表すことが想定される。ある実施形態において、「X1」、「X2」、「X3」、および「X4」は、同一のアミノ酸、例えば、「X1」、「X2」、「X3」、および「X4」はすべて、「F」(フェニルアラニン)であることを表すことは、本開示の範囲から除外される。ある実施形態において、「X1」は、「R」(アルギニン)、「F」(フェニルアラニン)、「M」(メチオニン)、「E」(グルタミン酸)、または「T」(トレオニン)を表し、「X2」は、「G」(グリシン)、「Y」(チロシン)、「A」(アラニン)、「D」(アスパラギン酸)または、「S」(セリン)を表し、「X3」は、「L」(ロイシン)、「F」(フェニルアラニン)、「M」(メチオニン)、「E」(グルタミン酸)または、「T」(トレオニン)を表し、「X4」は、「R」(アルギニン)、「Y」(チロシン)、「A」(アラニン)、「D」(アスパラギン酸)または、「S」(セリン)を表す。
いくつかの例において、ヒトCEAに対して特異的な第2の結合ドメインは、モノクローナル抗体A5B7のCDR−H3の、少なくとも、アミノ酸配列「RFYFDY」(配列番号30)、「LRFYFDY」(配列番号31)、「GLRFYFDY」(配列番号32)、または「RGLRFYFDY」(配列番号33)を含む。いくつかの例において、第2の結合ドメインは、アミノ酸配列「DRGLRFYFDY」(配列番号34)が、それぞれ、Kabat位置95(「D」、アスパラギン酸)、96(「R」、アルギニン)、97(「G」、グリシン)、98(「L」、ロイシン)、99(「R」、アルギニン)、100(「F」、フェニルアラニン)、100a(「Y」、チロシン)、100b(「F」、フェニルアラニン)、101(「D」、アスパラギン酸)、および102(「Y」、チロシン)に対応する、A5B7の完全CDR−H3を含む。Kabatによる付番系は、例えば、Kabat,E.A.,T.T.Wu,H.M.Perry,K.S.Gottesman,and C.Foeller.1991.Sequences of Proteins of Immunological Interest,5th ed.Bethesda,Md.:National Center for Biotechnology Information,National Library of Medicineに記載されている。
ある実施形態において、例えば、(上皮腫瘍細胞上の)CEA標的抗原に対する親和性を改善する、および/または本明細書に定義される二重特異性一本鎖抗体の「微細特異性」を最適化するために、このA5B7由来の「DRGLRFYFDY」(配列番号34)のCDR−H3アミノ酸配列をさらに修飾することが望ましい場合がある。そのために、アミノ酸配列「DX1X2X3X4FYFDY」(配列番号29)において、様々なアミノ酸残基は、向上した親和性および/または微細特異性を有する修飾されたCDR−H3を特定するために、位置「X1」、「X2」、「X3」、および/または「X4」(マウスモノクローナル抗体A5B7のCDR−H3の、それぞれ、Kabat位置96(「X1」)、97(「X2」)、98(「X3」)、および99(「X4」)に対応する)で、試験することができる。例えば、「X1」、「X2」、「X3」、または「X4」は、アミノ酸残基「R」(アルギニン)、「G」(グリシン)、「L」(ロイシン)、「Y」(チロシン)、「A」(アラニン)、「D」(アスパラギン酸)、「S」(セリン)、「W」(トリプトファン)、「F」(フェニルアラニン)または、「T」(トレオニン)を表すことができる。本明細書では、1つ、2つ、3つ、またはすべて4つの表示された「X」位置は、CDR−H3「DRGLRFYFDY」(配列番号34)アミノ酸配列において、Kabat位置96〜99で元の「RGLR」アミノ酸配列と比較して、交換することができる。ある実施形態において、「X1」、「X2」、「X3」、および「X4」は、同一のアミノ酸、例えば、「X1」、「X2」、「X3」、および「X4」はすべて、「F」(フェニルアラニン)であることを表すことは、除外される。A5B7由来の「DRGLRFYFDY」CDR−H3アミノ酸配列の上記の修飾は、当技術分野で既知の方法、例えば、無作為プライマーを用いて、PCR法によって達成することができ、それは、CEA結合ドメインのそのような修飾されたCDR−H3領域を有する二重特異性一本鎖抗体の生成を可能にする。これらの修飾された二重特異性一本鎖抗体の親和性または微細特異性は、当技術分野で記載の方法、例えば、ELISA、Biacore、またはFACS分析によって、試験することができる。
いくつかの実施形態において、二重特異性一本鎖抗体等の治療薬剤のヒトCEAに対して特異的な結合ドメインは、アミノ酸配列「SYWMH」(配列番号36)を有するCDR−H1および/またはアミノ酸配列「FIRNKANGGTTEYMSVKG」(配列番号37)または「FILNKANGGTTEYMSVKG」(配列番号38)を有するCDR−H2を含む。
いくつかの実施形態において、二重特異性一本鎖抗体等の治療薬剤のヒトCEAに対して特異的な結合ドメインは、アミノ酸配列「SYWMH」(配列番号36)を有するCDR−H1および/またはアミノ酸配列「FIRNKANGGTTEYMSVKG」(配列番号37)または「FIRNKANGGTTEYAASVKG」(配列番号47)を有するCDR−H2を含む。
あるいは、本明細書に定義される二重特異性一本鎖抗体のヒトCEAに対して特異的な該第2の結合ドメインは、アミノ酸配列「TYAMH」(配列番号39)を有するCDR−H1および/またはアミノ酸配列「LISNDGSNKYYADSVKG」(配列番号40)を有するCDR−H2を含む。
ある実施形態において、二重特異性抗体または二重特異性一本鎖抗体等のヒトCEAに対して特異的な結合ドメインのVH領域のアミノ酸配列は、マウスモノクローナル抗体A5B7のCDR−H3のKabat位置95〜102に対応する「DRGLRFYFDY」(配列番号34)、アミノ酸配列「SYWMH」(配列番号36)を有するCDR−H1、およびアミノ酸配列「FIRNKANGGTTEYMSVKG」(配列番号37)を有するCDR−H2を含む。
ある実施形態において、二重特異性形式または二重特異性一本鎖形式等において、ヒトCEAに対して特異的な結合ドメインのVH領域のアミノ酸配列は、マウスモノクローナル抗体A5B7のCDR−H3のKabat位置95〜102に対応する「DRGLRFYFDY」(配列番号34)、アミノ酸配列「SYWMH」(配列番号36)を有するCDR−H1、およびアミノ酸配列「FILNKANGGTTEYAASVKG」(配列番号44)を有するCDR−H2を含む配列番号146である。
ある実施形態において、二重特異性形式または二重特異性一本鎖形式等において、ヒトCEAに対して特異的な結合ドメインのVH領域のアミノ酸配列は、マウスモノクローナル抗体A5B7のCDR−H3のKabat位置95〜102に対応する「DRGLRFYFDY」(配列番号34)、アミノ酸配列「SYWMH」(配列番号36)を有するCDR−H1、およびアミノ酸配列「FIRNKANGGTTEYAASVKG」(配列番号47)を有するCDR−H2を含む。
ある実施形態において、二重特異性一本鎖形式等において、ヒトCEAに対して特異的な結合ドメインのVH領域のアミノ酸配列は、マウスモノクローナル抗体A5B7のCDR−H3のKabat位置95〜102に対応する「DRGLRFYFDY」(配列番号34)、アミノ酸配列「TYAMH」(配列番号39)を有するCDR−H1、およびアミノ酸配列「LISNDGSNKYYADSVKG」(配列番号40)を有するCDR−H2を含む。
ある実施形態において、ヒトCEAに対して特異的な結合ドメインのVH領域のアミノ酸配列は、配列番号59の配列を有するアミノ酸配列を含む。
したがって、例えば、二重特異性一本鎖抗体のヒトCEAに対して特異的な該結合ドメインは、上に定義される1つ、2つ、または3つのCDR−H領域を含むことができる。
ある実施形態において、ヒトCEAに対して特異的な結合ドメインのVL領域のアミノ酸配列は、例えば、二重特異性形式または二重特異性一本鎖形式で、アミノ酸配列「TLRRGINVGAYSIY」(配列番号41)を有するCDR−L1、アミノ酸配列「YKSDSDKQQGS」(配列番号42)を有するCDR−L2、およびアミノ酸配列「MIWHSGASAV」(配列番号43)を有するCDR−L3を含む。
ある実施形態において、ヒトCEAに対して特異的な結合ドメインのVH領域のアミノ酸配列は、配列番号48の配列を有するアミノ酸配列を含む。
上記のように、CEAに特異的に結合する第2の結合ドメインの可変領域の順序または配列は、VH−VLまたはVL−VHであり得る。
ある実施形態において、治療用二重特異性抗体または二重特異性一本鎖抗体等の治療薬剤のCEA結合部分のV領域は、
(a)配列番号49に示されるアミノ酸配列からなるVH領域および配列番号48に示されるアミノ酸配列からなるVL領域、
(b)配列番号51に示されるアミノ酸配列からなるVH領域および配列番号48に示されるアミノ酸配列からなるVL領域、から選択される。
ある実施形態において、治療薬は、
(a)配列番号28〜51のいずれかに示されるアミノ酸配列、
(b)配列番号28〜51のいずれかをコードするアミノ酸配列、
(c)(b)の相補的核酸配列に対するストリンジェント条件下でハイブリダイズする核酸配列によってコードされるアミノ酸配列、
(d)(b)の核酸配列への遺伝子コードの結果として、変性される核酸配列によってコードされるアミノ酸配列、および
(e)(a)または(b)のアミノ酸配列に対して少なくとも85%同一、少なくとも90%同一、または少なくとも95%同一のアミノ酸配列、から選択されるアミノ酸配列を含む二重特異性一本鎖抗体である。
ある実施形態において、治療薬は、配列番号46のアミノ酸配列を含む二重特異性一本鎖抗体である。
(v)薬学的製剤
抗体ベースの治療薬剤に特に有用な製剤はまた、米国特許出願公開第20030202972号、第20040091490号、および第20050158316号にも記載されている。ある実施形態において、本出願の液体製剤は、実質的には、界面活性剤および/または無機塩がない。別の特定の実施形態において、液体製剤は、約5.0〜約7.0の範囲のpHを有する。なお別の特定の実施形態において、液体製剤は、約1mM〜約100mMの範囲の濃度で、ヒスチジンを含む。さらに別の特定の実施形態において、液体製剤は、1mM〜100mMの範囲の濃度で、ヒスチジンを含む。液体製剤は、サッカリド、アミノ酸(例えば、アルギニン、リジン、およびメチオニン)、ならびにポリオール等の1つ以上の賦形剤をさらに含むことができることも企図される。液体製剤を調製し、分析するさらなる説明および方法は、例えば、PCT公開WO第03/106644号、WO第04/066957号、およびWO第04/091658号に見出され得る。
ラウリル硫酸ナトリウムおよびステアリン酸マグネシウム等の湿潤剤、乳化剤、および潤滑剤、ならびに着色剤、放出剤、被覆剤、甘味料、香味剤および香料、保存料および酸化防止剤もまた、本出願の薬学的組成物中に存在することができる。
ある実施形態において、対象抗体の製剤は、実質的に内毒素および/または関連する発熱物質がない、発熱物質非含有製剤である。内毒素は、微生物内に限定されていて、微生物が、破壊されるかまたは死んだ場合に放出される毒素が含まれる。また、発熱物質には、細菌および他の微生物の外膜由来の発熱誘発性熱安定性物質(糖タンパク質)が含まれる。これらの物質は共に、ヒトに投与された場合に、発熱、低血圧、およびショックを引き起こし得る。潜在的な有害な作用のため、低量の内毒素であっても、それを静脈内に投与される医薬品溶液から除去したほうが好都合である。Food&Drug Administration(「FDA」)は、静脈内薬物投与の1回の1時間の期間中、5内毒素単位(EU)/用量/キログラム体重の上限を定めている(The United States Pharmacopeial Convention,Pharmacopeial Forum 26(1):223(2000))。治療タンパク質が、数百または数千ミリグラム/キログラム体重の量で投与される場合、モノクローナル抗体を用いる場合であり得るように、微量の内毒素であってもそれを除去するのが好都合である。
対象治療試薬の製剤には、経口、食事、局所、非経口(例えば、静脈内、動脈内、筋肉内、皮下注射)、眼科用(例えば、局所もしくは眼球内)、吸入(例えば、気管支内、経鼻投与もしくは経口吸入、鼻内滴剤)、直腸、ならびに/または膣内投与に適したものが含まれる。他の好適な投与方法はまた、再充電可能なまたは生物分解可能なデバイスおよび制御放出ポリマーデバイスも含むことができる。特に、ステントは、本出願の薬剤と混合した制御放出ポリマーで被覆され得る。本開示の薬学的組成物はまた、他の薬剤を用いた組み合わせ療法の一部として(同一の製剤中あるいは別個の製剤中のいずれか)、投与することもできる。診断試薬用の製剤は、当技術分野の技術レベル内であり、インビトロ(エクスビボ)またはインビボ使用のために好適な賦形剤を含む。
治療的に有効である製剤の量は、標準臨床技法によって決定することができる。加えて、インビトロアッセイを、任意に採用して、最適な投薬量範囲を特定するのに役立てることができる。製剤で採用される正確な用量も、投薬経路、および疾患または障害の重篤度に依存し、医師の判断、およびそれぞれの患者の状況に従って決定されなければならない。有効用量は、インビトロまたは動物モデル試験系より得た用量応答曲線から外挿され得る。投与される組成物の投薬量は、標準用量応答試験と併せて必要以上の実験を行わずに、当業者が決定することができる。これらの決定を行う際に検討される関連状況は、治療される1つ以上の状態、投与される組成物の選択、個々の患者の年齢、体重、および応答、ならびに患者の症状の重症度を含む。例えば、患者の実際の体重を使用して、投与される製剤の用量がミリリットル(mL)で計算され得る。「理想」体重への下方調整は行われ得ない。そのような状況で、適切な用量は、以下の式:
用量(mL)=[患者体重(kg)×用量レベル(mg/kg)/薬物濃度(mg/mL)]によって計算され得る。
体液パラメーターの所望の減少を達成するために、そのような抗CEA抗体は、様々な単位剤形で投与され得る。用量は、特定の抗体に従って異なる。例えば、異なる抗体は、異なる質量および/または親和性を有し得、そしてしたがって、異なる投薬量レベルを必要とし得る。Fab′フラグメントとして調製される抗体または一本鎖抗体はまた、それらは天然免疫グロブリンよりかなり小さい質量であり、そしてしたがって、患者の血液中で同一のモルレベルに達するためにより低い投薬量を必要とするので、等価な天然免疫グロブリンとは異なる投薬量を必要とする。
本開示の他の治療薬はまた、様々な単位剤形で投与され得、それらの投薬量はまた、投与される特定の治療薬の大きさ、有効性、およびインビボ半減期によって異なる。
疾患の治療の目的には、本化合物(例えば、抗体)の適切な投薬量は、疾患の重症度および経過、患者の病歴および応答、抗体の毒性、ならびに医師の判断によって異なる。初期の候補投薬量が、患者に投与され得る。適切な投薬量および治療レジメンは、当業者に公知である従来の技術を用いて療法の経過をモニターすることにより確立することができる。
本出願の製剤は、包装材料、ならびに投与様式に適切であるように、例えば、抗体および薬学的に許容される担体を含む薬学的薬剤を含む製品として流通され得る。包装材料は、製剤が癌の治療で用いることを示すラベルを含む。
本開示の診断試薬についての有効な投薬量および投薬レジメンは、治療されるべき疾患または状態によって異なり、当業者によって決定することができる。
(vi)製品およびキット
本開示は、本開示の液体製剤または凍結乾燥製剤で充填された1つ以上の容器を含む薬学的パックまたはキットを提供する。特定の実施形態において、本開示の製剤は、異種タンパク質、異種ポリペプチド、異種ペプチド、大分子、小分子、マーカー配列、診断もしくは検出可能な薬剤、治療的部分、薬物部分、放射性金属イオン、二次抗体、および固体支持体が含まれるが、これらに限定されない、別の部分に組み換え技術によって融合されるまたは化学的に共役される抗CEA診断または治療試薬を含む。特定の実施形態において、本開示の製剤は、無菌液体として単回用量バイアル中に製剤化される。本開示の製剤は、3ccのUSP I型ホウケイ酸褐色バイアル(West Pharmaceutical Services−部品番号6800−0675)中に標的容積の1.2mLで供給される。任意に、かかる容器(複数可)は、医薬品または生物学的製品の製造、使用、または販売を管理している行政機関によって規定された形態の注意書きを伴い、そのような注意書きは、ヒト診断および/または投与のための製造、使用、または販売に関する機関による承認を反映するものである。
ある実施形態において、様々な目的、例えば、細胞からCEAの精製または免疫沈降、標的CEAの検出用等を含む研究および診断のために有用である抗CEA診断試薬を含むキットも提供される。CEAの単離および精製のために、キットは、ビーズ(例えば、セファロースビーズ)に結合された抗CEA診断試薬を含有することができる。例えば、ELISAまたはウエスタンブロット法において、インビトロで標的CEAの検出および定量のための抗体を含有するキットが、提供され得る。製品と同様に、キットは、容器と、容器上あるいは容器に付属したラベルまたは添付文書とを含む。容器は、本開示の少なくとも1つの抗CEA診断試薬を含む組成物を保持する。例えば、希釈剤および緩衝液、対照診断試薬を含有するさらなる容器が、含まれ得る。ラベルまたは添付文書は、組成物の説明、ならびに意図したインビトロでまたは診断的使用のための指示を提供することができる。
ある実施形態において、本開示は、抗CEA治療試薬および好適な診断試薬の両方を含むキット(いわゆる、二重試薬キット)を提供する。そのようなキットは、前述の実施形態のいずれか、例えば、好適な緩衝液等を使用するための取扱説明書等を含むことができる。ある実施形態において、二重試薬キットは、一致するため、治療試薬および診断試薬が、同一または実質的に同一のエピトープに結合する。例えば、治療試薬および診断試薬は、標的CEA(完全長または短型)に免疫特異的に結合し、診断および治療試薬は、同一または実質的に同一のエピトープに免疫特異的に結合する。ある実施形態において、診断試薬および治療試薬は、同一物である。ある実施形態において、2つの試薬は、少なくとも1つの抗原結合部分を共有する。
(vii)RNA検出方法
本出願は、生物学的試料中の完全長および/または短型癌胎児性抗原(CEA)のRNAの発現を検出する方法を提供する。(i)完全長CEAヌクレオチドに存在する配列(例えば、短型からスプライスされた領域)、または短型CEAヌクレオチド配列に特異的にハイブリダイズするが、完全長CEAヌクレオチド配列(例えば、完全長が不在の短型CEAヌクレオチドにおけるスプライス部位)には特異的にハイブリダイズしないこと、(ii)短型CEAの発現と完全長CEAの発現を区別する様式で、短型CEAヌクレオチド配列および完全長CEAヌクレオチド配列の両方に特異的にハイブリダイズすることによって、完全長および/または短型CEAの発現を特異的に特定するCEAヌクレオチド配列にハイブリダイズする核酸プローブまたは核酸プライマーのうちの1つまたは両方が、提供される。生物学的試料からのRNAが、さらに提供される。最終的に、生物学的試料中の短型CEAのRNAの発現は、核酸プローブおよび/または核酸プライマーを用いることによって検出される。
生物学的試料中の対象となる核酸の検出は、任意に、オリゴヌクレオチドプローブを用いるハイブリダイズベースのアッセイによって達成され得る(本開示によるプローブの非限定例が、前述された)。
従来のハイブリダイゼーションアッセイには、PCR、RT−PCR、リアルタイムPCR、RNase保護、原位置ハイブリダイゼーション、プライマー伸長、サザンブロット(DNA検出)、ドットまたはスロットブロット(DNA、RNA)、およびノーザンブロット(RNA検出)が含まれる。より最近になって、PNAが(Nielsen et al.1999,Current Opin.Biotechnol.10:71−75)記載されている。他の検出方法は、ディップスティック構成等のプローブを具備するキットを含む。
生物学的試料中の対象となる標的(すなわち、DNAまたはRNA)の検出を可能にするハイブリダイゼーションベースのアッセイは、例えば、10、15、20、もしくは30〜100ヌクレオチド長、10〜50、または40〜50ヌクレオチド長であり得るオリゴヌクレオチドの使用に依拠する。
ある実施形態において、本開示の単離されたポリヌクレオチド(オリゴヌクレオチド)は、穏和ないしストリンジェントなハイブリダイゼーション条件下で、本明細書に記載された核酸配列のいずれかとハイブリダイズ可能である。
生物学的試料中の対象となる核酸の検出はまた、任意に、NATベースのアッセイによって達成され得、これには、例えば、PCR(またはその変形、例えば、リアルタイムPCR等)等の核酸増幅技術を含む。
異なる技法を用いたRNA発現を検出する例は、本出願の実施例のセクションに提供される。そのような例には、従来のPCR反応によってRNAを増幅するためのプライマーの使用、ならびにTaqManと称されるアプローチに採用されるプローブおよびプライマーの組み合わせの使用が含まれる。RNAを検出する方法のさらなる例には、定量的RT−PCR、SAGE、MPSS、アレイベースの方法、および直接配列決定が含まれる。
本明細書に使用される「プライマー」は、標的配列にアニーリングを起こさせる(ハイブリダイズする)ことが可能であり、それによって、適切な条件下でDNA合成のための開始点として機能し得る二本鎖の領域を生成する、オリゴヌクレオチドを定義する。
選択または標的核酸配列の増幅を、いくつかの適切な方法で実行することができる。一般に、Kwoh et al.,1990,Am.Biotechnol.Lab.8:14を参照のこと。数多くの増幅技法が記載されており、それらは当業者の特定の要求を満たすことに容易に適応することができる。増幅技法の非限定例には、ポリメラーゼ鎖反応(PCR)、リガーゼ鎖反応(LCR)、鎖置換増幅(SDA)、転写に基づく増幅、q3レプリカーゼ系、およびNASBAが含まれる(Kwoh et al.,1989,Proc.Natl.Acad.Sci.USA 86,1173−1177、Lizardi et al.,1988,BioTechnology 6:1197−1202、Malek et al.,1994,Methods Mol.Biol.,28:253−260、およびSambrook et al.,1989、上記参照)。
「増幅対」(または「プライマー対」)という専門用語は、本明細書では、本開示のオリゴヌクレオチド(オリゴ)の一対を指し、いくつかの種類の増幅プロセスの1つ、例えば、ポリメラーゼ鎖反応等によって、選択された核酸配列を増幅する際に一緒に用いられるように選択される。他の種類の増幅プロセスには、以下にさらに詳細に説明されるように、リガーゼ鎖反応、鎖置換増幅、または核酸配列に基づいた増幅が含まれる。当技術分野で一般に公知のように、オリゴは、選択された条件下で相補的配列に結合するように設計される。
特定の一実施形態において、患者からの核酸試料の増幅は、最も豊富に異なった形で発現した核酸の増幅に好都合の条件下で、増幅される。好ましい一実施形態において、RT−PCRは、最も豊富なmRNAの増幅に好都合の条件下で、患者からのmRNA試料に対して実行される。別の好ましい実施形態において、異なった形で発現した核酸の増幅は、同時に実行される。そのような方法が、異なった形で発現した核酸配列の代わりに、異なった形で発現したタンパク質の検出に適することもあり得ることを当業者によって理解されよう。
本開示のオリゴヌクレオチドプライマーは、特定のアッセイ形式、特定のニーズ、および採用した標的ゲノムに応じて、任意の適当な長さのものであってもよい。任意に、オリゴヌクレオチドプライマーは、少なくとも12ヌクレオチド長、ある実施形態において、15〜24分子であり、選択された核酸増幅系に特に適するように、適合され得る。当技術分野で一般に公知のように、オリゴヌクレオチドプライマーは、その標的配列とのハイブリダイゼーションの融点を考慮に入れることで設計することができる(Sambrook et al.,1989,Molecular Cloning−−A Laboratory Manual,2nd Edition,CSH Laboratories、Ausubel et al.,1989,in Current Protocols in Molecular Biology,John Wiley & Sons Inc.,N.Y.)。
代替的な実施形態において、発現は、cDNAの直接配列決定によって検出することができる。そのような直接配列決定は、RNAを検出し、定量化するためのさらなる方法を提供する。
(viii)RNAの検出を用いた診断方法
別の態様において、本開示は、腫瘍が、完全長CEAのRNAおよび/または短型CEAのRNAのうちの1つまたは両方を発現するかどうかを評価するために腫瘍試料を評価することによって、標的癌胎児性抗原(CEA)タンパク質に免疫特異的に結合する癌治療薬に対して感受性があり得る患者を特定する方法を提供する。ある実施形態において、本方法は、患者から腫瘍試料を得ることと、標的CEAのRNAの腫瘍試料中の発現を検出することと、を伴う。例えば、この試料は、完全長CEAのRNA発現と短型CEAのRNA発現を区別するプローブおよび/またはプライマーと接触させることができる。ある実施形態において、プローブおよび/またはプライマー(または複数のプローブおよびプライマーの組み合わせ)との試料の接触は、完全長および短型CEAのRNAの両方の特定を可能にする。他の実施形態において、プローブおよび/またはプライマーとの試料の接触は、完全長あるいは短型CEAのRNAのいずれかを一意的に特定する。アッセイが行われる特定の方法に関わらず、腫瘍試料が、完全長CEAのRNAおよび/または短型CEAのRNAを発現するかどうかに関わらず情報を提供する。この情報は、患者が、特定の標的CEAタンパク質(長型あるいは短型のいずれか)に免疫特異的に結合する癌治療薬による治療に対して感受性があるかどうかを判定する際、有用であり得る。
理論によって拘束されることなく、特定の標的型CEAのRNAを発現しない、または低濃度のそのRNAを発現する腫瘍が、そのRNAによってコードされるCEAタンパク質に免疫特異的に結合する治療薬剤を投与することに基づいて治療レジメンに応答する可能性は低い。したがって、例えば、患者からの腫瘍試料が、完全長CEAのRNAを発現しない、または低濃度のそのRNAを発現する場合、この患者は、完全長CEAタンパク質に免疫特異的に結合する治療薬による治療のふさわしい候補者ではない。同様に、患者からの腫瘍試料が、短型CEAのRNAを発現しない、または低濃度のそのRNAを発現する場合、この患者も、短型CEAタンパク質に免疫特異的に結合する治療薬による治療のふさわしい候補者ではない。
しかしながら、患者からの腫瘍試料が、完全長および/または短型CEAのうちの1つまたは両方を発現する場合、この患者は、標的型のCEAタンパク質に免疫特異的に結合する治療薬による治療に対して感受性があり得る。したがって、腫瘍試料が、完全長CEAのRNAを発現する場合、この患者は、完全長CEAに免疫特異的に結合する治療薬による治療に対して感受性があり得る。腫瘍試料が、短型CEAのRNAを発現するが、完全長CEAのRNAを発現しない場合、この患者は、短型CEAに免疫特異的に結合する治療薬による治療に対して感受性があり得る。したがって、ある実施形態において、患者から採取された腫瘍試料中のRNA発現の分析後、この患者は、抗CEA治療薬等の適切な治療薬により治療することができる。さらに、腫瘍試料が、CEAのRNAを発現しない場合、この患者の治療レジメンは、抗CEA療法に対して不必要な曝露をすることなく、他のラインに沿って作成することができる。
ある実施形態において、腫瘍試料が、特定の標的CEAのRNA発現の検査で陽性と出る場合、1つ以上のさらなる生物学的試料(例えば、血液、血清、痰、糞便、尿等)を患者から得て、特定の標的CEAのタンパク質発現を評価することができる。例えば、これらの1つ以上のさらなる生物学的試料を得て、完全長CEAまたは短型CEAに免疫特異的に結合する抗体と接触させて、腫瘍が、RNA発現の検査で陽性と出た患者からの試料が、タンパク質発現の検査でも陽性と出るかどうかを評価することができる。ある実施形態において、1つ以上の生物学的試料中のタンパク質発現の試験の結果に応じて、この対象は、標的CEAタンパク質に免疫特異的に結合する癌治療薬により治療することができる(例えば、患者が、完全長CEAタンパク質および/または短型CEAタンパク質に対して陽性である場合、完全長CEAタンパク質に免疫特異的に結合し、患者が、短型CEAタンパク質のみに陽性である場合、短型CEAタンパク質に免疫特異的に結合する)。
腫瘍試料等の試料中のRNAを検出するための診断方法は、当技術分野で公知である。非限定例として、RNA発現は、RT−PCR分析、SAGE、MPSS、マイクロアレイ、直接配列決定、またはTaqMan定量分析を用いて検出することができる。1つ以上の生物学的試料中のタンパク質発現を評価するための方法は、本明細書の他の箇所で提供される通りである。さらに、患者が、例えば、完全長CEAに免疫特異的に結合する薬剤による治療に適していると特定される場合、例示的な癌治療薬が本明細書に提供される。
(ix)タンパク質を産生する方法
本開示は、配列番号1(プロ配列の存在または不在下)で表されるアミノ酸配列を含む精製されたポリペプチド、または連続するアミノ酸残基:NIIQNELSVD(配列番号11)を含む、そのフラグメントを提供する。本開示は、配列番号1で表されるアミノ酸配列を含む精製されたポリペプチド、または連続するアミノ酸残基:QNIIQNELSVDH(配列番号13)を含む、そのフラグメントを提供する。本開示は、配列番号1で表されるアミノ酸配列を含む精製されたポリペプチド、または連続するアミノ酸残基:IQNIIQNELSVDHS(配列番号14)を含む、そのフラグメントを提供する。ある実施形態において、このフラグメントは、約10個、15個、20個、25個もしくは30個、35個、40個、45個、50個、55個、60個、65個、70個、75個、80個、85個、90個、95個、100個、150個、200個、250個、300個、350個、もしくは400個のアミノ酸を含む。
本開示は、配列番号1(プロ配列の存在または不在下)で表されるアミノ酸配列を含む精製されたポリペプチド、または連続するアミノ酸残基:NIIQNKLSVD(配列番号12)を含む、そのフラグメントを提供する。本開示は、配列番号1で表されるアミノ酸配列を含む精製されたポリペプチド、または連続するアミノ酸残基:QNIIQNKLSVDH(配列番号15)を含む、そのフラグメントを提供する。本開示は、配列番号1で表されるアミノ酸配列を含む精製されたポリペプチド、または連続するアミノ酸残基:IQNIIQNKLSVDHS(配列番号16)を含む、そのフラグメントを提供する。ある実施形態において、このフラグメントは、約10個、15個、20個、25個もしくは30個、35個、40個、45個、50個、55個、60個、65個、70個、75個、80個、85個、90個、95個、100個、150個、200個、250個、300個、350個、もしくは400個のアミノ酸を含む。
標的CEAタンパク質またはフラグメントは、多くの方法のうちのいずれで産生することができる。例として、そのようなタンパク質およびフラグメントは、合成的に産生することができる。さらなる例として、そのようなタンパク質およびフラグメントは、組み換えによって産生することができる。
標的CEAタンパク質の組み換え発現は、所望の標的CEAタンパク質のすべてまたは一部をコードするポリヌクレオチドを含む発現ベクターを構築することによって行うことができる。そのような標的CEAタンパク質をコードするポリヌクレオチドが、得られると、エピトープ結合分子の産生のためのベクターは、当技術分野で公知の技法を用いて、組み換えDNA技術によって産生することができる。例えば、米国特許第6,331,415号を参照されたく、これは、参照することによってその全体が本明細書に組み込まれる。このようにして、ヌクレオチド配列をコードする抗体を含有するポリヌクレオチドを発現することによってタンパク質を調製するための方法が本明細書に記載される。標的CEAタンパク質は、多くの異なる発現系において産生することができる。一実施形態において、標的CEAタンパク質が、産生され、哺乳動物細胞によって分泌される。別の実施形態において、標的CEAタンパク質が、産生され、ヒト細胞中に分泌される。特定の実施形態において、本開示の標的CEAタンパク質は、293F、CHO、またはNS0細胞株の細胞中に産生される。他の実施形態において、標的CEAタンパク質は、酵母または細菌性細胞中に産生される。別の実施形態において、標的CEAタンパク質は、例えば、SF9細胞中のバキュロウイルス媒介発現を用いて産生される。
当業者に周知である方法を用いて、タンパク質コード配列ならびに適切な転写および翻訳調節シグナルを含有する発現ベクターを構築することができる。これらの方法には、例えば、インビトロ組み換えDNA技術、合成技術、およびインビボ遺伝子組み換えが含まれる。このようにして、本開示は、プロモーターに操作可能に結合されるCEAタンパク質分子をコードするヌクレオチド配列を含む複製可能なベクターを提供する。
一旦、発現ベクターが従来の技法によって宿主細胞に移送されると、トランスフェクトされた細胞は、従来の技法によって培養されて、CEAタンパク質を産生する。したがって、本開示は、異種プロモーターに操作可能に連結される標的CEAタンパク質をコードする宿主細胞を含む。
多種多様の宿主発現ベクター系を利用して、米国特許第5,807,715号に記載されるCEAタンパク質またはその一部を発現させることができる。例えば、チャイニーズハムスター卵巣細胞(CHO)等の哺乳動物細胞は、ヒトサイトメガロウイルス由来の主な中間型初期遺伝子プロモーターエレメント等のベクターと併せて、CEAタンパク質のための有効な発現系である(Foecking et al.,Gene,45:101(1986)およびCockett et al.,Bio/Technology,8:2(1990))。加えて、所望される具体的な様式で、挿入された配列の発現を調節する、または遺伝子産物を修飾および処理する宿主細胞株が選択されてもよい。タンパク質産物のかかる修飾(例えば、グリコシル化)およびプロセシング(例えば、切断)は、タンパク質の機能に重要であり得る。異なる宿主細胞は、タンパク質および遺伝子産物の翻訳後プロセシングならびに修飾のための、特徴的および特異的機構を有する。適切な細胞株または宿主系を選択して、本開示のタンパク質の正しい修飾およびプロセシングを確保することができる。この目的のために、遺伝子産物の適切な一次転写、グリコシル化、およびリン酸化のプロセシングのための細胞機構を有する真核性宿主細胞が使用することが可能である。かかる哺乳動物宿主細胞としては、CHO、VERY、BHK、Hela、COS、MDCK、293、3T3、W138、BT483、Hs578T、HTB2、BT2OおよびT47D、NS0、CRL7O3O、およびHsS78Bst細胞が挙げられるが、これらに限定されない。
細菌系において、いくつかの発現ベクターは、発現させられているタンパク質分子のために意図される使用に応じて、有利に選択されてもよい。例えば、CEAタンパク質を含む薬学的または診断的組成物の生成のために、大量のそのようなCEAタンパク質が産生されるべきである場合、容易に精製される高レベルの融合タンパク質産物の発現を誘導するベクターが望ましい可能性がある。かかるベクターとしては、融合タンパク質が産生されるように、コード配列を個々にlacZコード領域とインフレームで該ベクターに連結され得るE.coli発現ベクターpUR278(Ruther et al.,EMBO,12:1791(1983))pINベクター(Inouye & Inouye,1985,Nucleic Acids Res.13:3101−3109(1985)、Van Heeke & Schuster,1989,J.Biol.Chem.,24:5503−5509(1989))等が含まれるが、これらに限定されない。また、pGEXベクターを使用して、グルタチオン−S−トランスフェラーゼ(GST)との融合タンパク質として外来ポリペプチドを発現させてもよい。概して、かかる融合タンパク質は、可溶性であり、グルタチオン−アガロース親和性マトリックスへの吸着および結合、続いて遊離グルタチオンの存在下での溶出によって、溶解した細胞から容易に精製することができる。pGEXベクターは、トロンビンおよび/または因子Xaプロテアーゼ切断部位を発現させたポリペプチドに導入し、その結果、クローン化された標的遺伝子産物がGST部分から放出され得るように設計される。
昆虫系においては、外来遺伝子を発現させるためのベクターとして、オートグラファ・カリフォルニカ核多角体病ウイルス(AcNPV)が使用される。該ウイルスは、スポドプテラ・フルギペルダ細胞中で成長する。タンパク質コード配列は、ウイルスの非必須領域(例えば、ポリヘドリン遺伝子)へと個々にクローン化され、AcNPVプロモーター(例えば、ポリヘドリンプロモーター)の調節下に配置されてもよい。
哺乳動物宿主細胞では、複数のウイルスベースの発現系が利用されてもよい。アデノウイルスが発現ベクターとして使用される場合、対象となるコード配列は、アデノウイルス転写/翻訳調節複合体、例えば、後期プロモーターおよびトリパータイトリーダー配列に連結されてもよい。次いでこのキメラ遺伝子は、インビトロまたはインビボ組み換えによって、アデノウイルスゲノムに挿入されてもよい。ウイルスゲノムの非必須領域(例えば、領域E1またはE3)への挿入は、感染宿主中で生存可能で、かつ抗体分子を発現することができる組み換えウイルスをもたらすであろう(例えば、Logan&Shenk,Proc.Natl.Acad.Sci USA,81:355−359(1984)を参照されたい)。また、効果的な翻訳のために、具体的な開始シグナルが必要とされ得る。これらのシグナルには、ATG開始コドンおよび隣接配列が含まれる。さらに、挿入物全体の翻訳を確保するために、開始コドンは、所望のコード配列のリーディングフレームと同相であるべきである。これらの外因性翻訳調節シグナルおよび開始コドンは、天然および合成の両方で、多種多様の起源由来であってもよい。発現の効率は、適切な転写エンハンサー要素、転写ターミネーター等の組み込みによって強化されてもよい(例えば、Bittner et al.,Methods in Enzymol.,153:51−544(1987)を参照されたい)。
(x)抗体を作製する方法
本開示はまた、モノクローナル抗CEA抗体も提供する。モノクローナル抗体は、実質的に均一な抗体の集団から得られ得る、すなわち、集団を含む個々の抗体が、少量で存在し得る潜在的な自然発生突然変異を除いて同一である。モノクローナル抗体は、高特異的であり、単一の抗原部位に対して向けられる。さらに、異なる決定基(エピトープ)に対して向けられる異なる抗体を典型的に含む従来の(ポリクローナル)抗体調製物と対照的に、各モノクローナル抗体は、抗原上の単一の決定基に対して向けられる。それらの特異性に加えて、モノクローナル抗体は、他の免疫グロブリンによって汚染されていないハイブリドーマ培養によりしばしば合成される点で有利である。モノクローナル抗体はまた、CHO細胞およびNS0細胞等のトランスフェクト細胞中に産生されてもよい。「モノクローナル」という修飾語は、実質的に均一な抗体の集団から得られるという抗体の特徴を示し、任意の特定の方法による抗体の産生を必要としない。例えば、本開示に従って使用されるべきモノクローナル抗体は、Kohler et al.,Nature 1975;256:495によって初めに記載されるハイブリドーマ法によって作製され得るか、または組み換えDNA法(例えば、米国特許第4,816,567号および第6,331,415号を参照されたい)によって作製され得る。「モノクローナル抗体」はまた、例えば、Clackson et al.,Nature 1991;352:624−628およびMarks et al.,J.Mol.Biol.1991;222:581−597に記載される技法を用いて、ファージ抗体ライブラリーから単離してもよい。
動物の免疫化のため(CEAを用いた場合)、抗体を産生する細胞の単離、モノクローナル抗体を分泌するハイブリドーマを生成するための不死化細胞(例えば、骨髄腫細胞)とのそのような細胞の融合、所望の抗原による分泌モノクローナル抗体の反応性のためのハイブリドーマ上清のスクリーニング(免疫原または免疫原を含有する分子の場合)、ハイブリドーマ上清または腹水中のそのような抗体の量の調製、ならびにそのようなモノクローナル抗体の精製および保存のための一般的方法は、多くの刊行物に見出され得る。これらには、Coligan et al.,eds.Current Protocols In Immunology,John Wiley & Sons,New York,1992、Harlow and Lane,Antibodies,A Laboratory Manual,Cold Spring Harbor Laboratory,New York,1988、Liddell and Cryer,A Practical Guide To Monoclonal Antibodies,John Wiley & Sons,Chichester,West Sussex,England,1991、Montz et al.,Cellular Immunol.127:337−351,1990、Wurzner et al.,Complement Inflamm.8:328−340,1991、およびMollnes et al.,Scand.J.Immunol.28:307−312,1988が含まれる。
特に企図される他の抗体は、オリゴクローナル抗体である。本明細書に使用される「オリゴクローナル抗体」という語句は、別々のモノクローナル抗体の予め決定された混合物を指す。例えば、PCT公開WO第95/20401号、米国特許第5,789,208号および第6,335,163号を参照されたい。一実施形態において、1つ以上のエピトープに対する抗体の予め決定された混合物からなるオリゴクローナル抗体は、単一細胞中で生成される。他の実施形態において、オリゴクローナル抗体は、通常の軽鎖と対を成して複数の特異性を有する抗体を生成することができる複数の重鎖を含む(例えば、PCT公開WO第04/009618号)。オリゴクローナル抗体は、単一の標的分子上の複数のエピトープを標的にすることが望ましい場合に、特に有用である。本明細書に開示されるアッセイおよびエピトープを考慮して、当業者は、意図された目的および所望の必要性に適用可能な抗体または抗体の混合物を生成するか、または選択することができる。
あるいは、上記の方法がポリクローナル抗体を産生するために使用される場合、免疫化後、血流に分泌されるポリクローナル抗体は、既知の技法を用いて回収することができる。当然ながら、精製型のこれらの抗体は、例えば、プロテインA、抗免疫グロブリン、または抗原それ自体を用いた親和性クロマトグラフィー等の標準精製技法によって容易に調製することができる。どんな場合でも、免疫化の成功をモニターするために、血清中の抗原に対する抗体レベルは、ELISA、RIA等の標準技法を用いてモニターされる。
さらに、抗CEA抗体はまた、それらのゲノム中のCEAマウスをコードする遺伝子を欠失するトランスジェニックマウス(CEAノックアウトマウス)のCEA免疫化によって産生することもできる。
二重特異性抗体を作製するための方法は、当業者の範囲内である。伝統的に、二重特異性抗体の組み換え産生は、2つの免疫グロブリン重鎖/軽鎖対の同時発現に基づき、ここで、2つの重鎖は、異なる特異性を持っている(Milstein and Cuello,Nature,305:537−539(1983))。所望の結合特異性を有する抗体可変ドメイン(抗体−抗原結合部位)は、免疫グロブリン定常ドメイン配列に融合させることができる。ある実施形態において、融合は、ヒンジ、CH2、およびCH3領域の少なくとも一部を含む、免疫グロブリン重鎖との融合である。免疫グロブリン重鎖の融合、および必要に応じて、免疫グロブリン軽鎖をコードするDNAを、別個の発現ベクターに挿入し、好適な宿主生物に同時形質移入する。二重特異性抗体を生成するための例証される現在公知の方法のさらなる詳細に関しては、例えば、Suresh et al.,Methods in Enzymology,121:210(1986)、WO第96/27011号、Brennan et al.,Science 229:81(1985)、Shalaby et al.,J.Exp.Med.175:217−225(1992)、Kostelny et al.,J.Immunol.148(5):1547−1553(1992)、Hollinger et al.,Proc.Natl.Acad.Sci.USA 90:6444−6448(1993)、Gruber et al.,J.Immunol.152:5368(1994)、およびTutt et al.,J.Immunol.147:60(1991)を参照されたい。また、二重特性抗体には、架橋抗体またはヘテロ抱合抗体が含まれる。ヘテロ抱合抗体は、任意の便利な架橋方法を用いて作製することができる。好適な架橋薬剤は、当技術分野で公知であり、それらは複数の架橋技法と共に、米国特許第4,676,980号に開示されている。
組み換え細胞培養から直接的に二重特異性抗体フラグメントを作製し、単離する様々な技法もまた記載されている。例えば、二重特異性抗体は、ロイシンジッパーを使用して産生された。Kostelny et al.,J.Immunol.,148(5):1547−1553(1992)。FosおよびJunタンパク質からのロイシンジッパーペプチドは、遺伝子融合により2つの異なった抗体のFab′部分に連結することができる。抗体ホモダイマーは、ヒンジ領域で還元されてモノマーを形成し、次いで、再酸化させて抗体ヘテロダイマーを形成する。この方法はまた、抗体ホモダイマーの産生に対して使用することもできる。一本鎖Fv(scFv)ダイマーの使用による二重特異性抗体フラグメントを作製するための戦略もまた、報告されている。Gruber et al.,J.Immunol.,152:5368(1994)を参照されたい。あるいは、抗体は、Zapata et al.Protein Eng.8(10):1057−1062(1995)に記載される「直線状抗体」であり得る。簡潔に言えば、これらの抗体は、一対の抗原結合領域を形成するタンデムFdセグメント(VH−CH1−VH−CH1)を含む。直線状抗体は、二重特異性または単一特異性であり得る。
キメラ抗体を産生するために、2つの異なる種(例えば、ヒト定常領域およびマウス可変もしくは結合領域)に由来する部分は、従来の技法によって化学的に連結することができる、または遺伝子操作技法を用いて、単一の隣接タンパク質として調製することができる。キメラ抗体の軽鎖および重鎖部分の両方のタンパク質をコードするDNA分子は、隣接タンパク質として発現することができる。キメラ抗体を作製する方法は、米国特許第5,677,427号、米国特許第6,120,767号、および米国特許第6,329,508号に開示され、これらのそれぞれは、参照することによりその全体が本明細書に組み込まれる。
CEAに対する完全ヒト抗体は、様々な技法によって産生することができる。一例が、トリオーマ方法論である。基本アプローチ、およびこのアプローチにおいて使用するための例示的な細胞融合パートナー、SPAZ−4は、Oestberg et al.,Hybridoma 2:361−367(1983)、Oestbergの米国特許第4,634,664号、およびEnglemanらの米国特許第4,634,666号(これらのそれぞれは、参照することによりその全体が組み込まれる)によって記載されている。
CEAに対するヒト抗体はまた、ヒト免疫グロブリン遺伝子座の少なくとも1つのセグメントをコードするトランス遺伝子を有する非ヒトトランスジェニック動物から産生することもできる。これらの特性を有する動物の産生および特性は、例えば、LonbergらのWO第93/12227号、米国特許第5,545,806号、およびKucherlapatiらのWO第91/10741号、米国特許第6,150,584号を参照することによって、詳細に記載され、これらは、参照することによってその全体が本明細書に組み込まれる。
また、様々な組み換え抗体ライブラリー技術を利用して、完全ヒト抗体を産生することもできる。例えば、1つのアプローチは、Huse et al.,Science 246:1275−1281(1989)によって概説される一般的なプロトコルに従ってヒトB細胞からDNAライブラリーをスクリーニングすることである。抗体を結合するCEAまたはそのフラグメントが、選択される。次いで、かかる抗体(または結合フラグメント)をコードする配列は、クローン化され、増幅される。Huseによって記載されるプロトコルは、ファージディスプレイ技術と組み合わせて、さらに効率的に表示される。例えば、DowerらのWO第91/17271号、McCaffertyらのWO第92/01047号、米国特許第5,969,108号を参照されたい(参照することによってその全体が組み込まれる)。これらの方法では、メンバーが、それらの外面上に異なる抗体を提示するファージのライブラリーを産生する。抗体は、通常、FvまたはFabフラグメントとして提示される。所望の特異性を有するファージディスプレイ抗体が、CEAまたはそのフラグメントへの親和性濃縮によって選択される。さらなるアプローチが、本出願と共に使用することができる(米国特許出願第20040072164号および第20040175736号、これらのそれぞれは、参照することによってその全体が組み込まれる)。
真核細胞リボソームはまた、Coia G,et al.,J.Immunol.Methods 1:254(1−2):191−7(2001)、Hanes J.et al.,Nat.Biotechnol.18(12):1287−92(2000)、Proc.Natl.Acad.Sci.U.S.A.95(24):14130−5(1998)、Proc.Natl.Acad.Sci.U.S.A.94(10):4937−42(1997)(これらのそれぞれは、参照することによってその全体が組み込まれる)によって記載されるように、抗体のライブラリーを提示し、CEA等の標的抗原に対してスクリーニングすることによって、結合ヒト抗体を単離する手段として使用することもできる。
酵母系はまた、抗体等の哺乳動物細胞表面または分泌タンパク質をスクリーニングするのにも適している。抗体ライブラリーは、標的抗原に対するヒト抗体を得る目的のために、酵母細胞の表面上に提示され得る。このアプローチは、Yeung,et al.,Biotechnol.Prog.18(2):212−20(2002)、Boeder,E.T.,et al.,Nat.Biotechnol.15(6):553−7(1997)によって記載されており、これらのそれぞれは、参照することによりその全体が本明細書に組み込まれる。あるいは、ヒト抗体ライブラリーを細胞内で発現させ、酵母2ハイブリッド系によってスクリーニングすることができる(WO第0200729A2号、これは参照することによりその全体が組み込まれる)。
組み換えDNA技法を使用して、細菌、酵母、昆虫細胞、植物細胞、哺乳動物細胞(例えば、NS0細胞)等の原核生物および真核生物発現系の両方を含む任意の発現系において、組み換え抗CEA抗体、ならびにキメラもしくはヒト化抗CEA抗体、または任意の他の抗CEAを遺伝子操作された抗体およびそのフラグメントもしくは共役体を産生することができる。
一旦産生されると、本出願の全抗体、それらの二量体、個々の軽鎖および重鎖、または他の免疫グロブリン型は、硫酸アンモニウム沈殿、親和性カラム、カラムクロマトグラフィー、ゲル電気泳動等を含む、当技術分野の標準的な手法に従って精製することができる(概して、Scopes,R.,Protein Purification(Springer−Verlag,N.Y.,1982)を参照のこと)。ある実施形態において、例えば、少なくとも約90〜95%均一性、ある実施形態において、98〜99%またはそれ以上の均一性の実質的に純粋な免疫グロブリンが、薬学的目的のために使用することができる。所望により部分的に、または均一になるまで一旦精製されると、ポリペプチドは、(体外を含めて)治療で、あるいはアッセイ手法、免疫蛍光染色法等を開発し、実行する際に、使用することができる(概して、Immunological Methods,Vols.I and II(Lefkovits and Pernis,eds.,Academic Press,NY,1979 and 1981を参照のこと)。
例示的な実施形態
1. 癌胎児性抗原(CEA)を発現する癌の再発を検出する方法であって、
癌胎児性抗原(CEA)を発現する癌であると以前に診断され、治療された患者から試料を取得することと、
完全長CEAタンパク質に免疫特異的に結合するが、短型CEAタンパク質には免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いて、該試料中の完全長CEAタンパク質の濃度を検出し、それによって、該試料中の短型CEAタンパク質の濃度を検出することなく、完全長CEAタンパク質の濃度を検出することと、
を含み、
治療後に観察された濃度を超える、該試料中の完全長CEAタンパク質の濃度の検出は、該CEAを発現する癌の再発を示す、方法。
2. 癌胎児性抗原(CEA)を発現する癌の再発を検出する方法であって、
癌胎児性抗原(CEA)を発現する癌を患っている対象から、治療前に得られる第1の試料を得ることと、
完全長CEAタンパク質に免疫特異的に結合するが、短型CEAタンパク質には免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いて、該第1の試料中の完全長CEAタンパク質の治療前の濃度を検出し、それによって、該第1の試料中の短型CEAタンパク質の濃度を検出することなく、完全長CEAタンパク質の濃度を検出することと、
該対象から第2の試料を得て、該抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いて、該第2の試料中の完全長CEAタンパク質の濃度を検出し、それによって、該第2の試料中の短型CEAタンパク質の濃度を検出することなく、完全長CEAタンパク質の濃度を検出することと、
該第2の試料を得るためのものより後の時点で、該対象から1つ以上のさらなる試料を得ていることと、該抗体、抗原結合フラグメント、または免疫グロブリン様分子(例えば、該診断試薬)を用いて、該1つ以上のさらなる試料中の完全長CEAタンパク質の濃度を検出し、それによって、該1つ以上のさらなる試料中の短型CEAタンパク質の濃度を検出することなく、完全長CEAタンパク質の濃度を検出することと、
を含み、
該第2の試料で観察された完全長CEAタンパク質の濃度を超える、該1つ以上のさらなる試料中の完全長CEAタンパク質の濃度の検出は、該CEAを発現する癌の再発を示す、方法。
3. 抗癌胎児性抗原(CEA)癌治療薬に対する感受性を判定する方法であって、
完全長CEAタンパク質に免疫特異的に結合するが、短型CEAタンパク質には免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いて、試料中の完全長CEAタンパク質の濃度を検出し、それによって、該試料中の該短型CEAタンパク質の濃度を検出することなく、該完全長CEAタンパク質の濃度を検出することと、
該完全長CEAタンパク質の濃度を、健常な対象からの試料中の標準範囲を示す完全長CEAタンパク質濃度と比較することと、
を含み、
該標準範囲を超える完全長CEAタンパク質の濃度の検出は、抗CEA癌治療に対する感受性を示す、方法。
4. 抗癌胎児性抗原(CEA)癌療法をモニタリングする方法であって、
完全長CEAタンパク質に免疫特異的に結合するが、短型CEAタンパク質には免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いて、CEAを発現する癌の治療を受けている対象からの試料中の完全長CEAタンパク質の濃度を検出し、それによって、該試料中の該短型CEAタンパク質の濃度を検出することなく、該完全長CEAタンパク質の濃度を検出することと、
該完全長CEAタンパク質の濃度を、該治療前または該治療中の早期の時点で得られた該同一の対象からの試料中の完全長CEAタンパク質の濃度と比較することと、
を含み、
治療前または該治療中の早期の時点で得られた濃度に対する、治療中の後半の時点で得られた試料中の完全長CEA濃度の低下は、該治療の有効性を示し、それによって、該抗CEA癌療法をモニタリングする、方法。
5. 癌胎児性抗原(CEA)を発現する癌を患っている対象を治療する方法であって、
癌胎児性抗原(CEA)を発現する癌に対する治療前に、対象から試料を得ることと、
完全長CEAタンパク質に免疫特異的に結合するが、短型CEAタンパク質には免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いて、該試料中の完全長CEAタンパク質の濃度を検出し、それによって、該試料中の前記短型CEAタンパク質の濃度を検出することなく、該完全長CEAタンパク質の濃度を検出することと、
該完全長CEAタンパク質の濃度を、健常な対象からの試料中の完全長CEAタンパク質濃度を反映する標準範囲と比較することであって、
前記標準範囲を超える該完全長CEAタンパク質の濃度の検出は、抗CEA癌治療に対する感受性を示す、比較することと、
該対象が、抗CEA癌療法に対して感受性があると判定される場合、抗CEA癌治療薬を用いて該対象を治療することと、
任意に、完全長CEAタンパク質に免疫特異的に結合するが、短型CEAタンパク質には免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いて、該対象からの治療後の試料中の完全長CEAタンパク質の濃度を検出し、それによって、該治療後の試料中の該短型CEAタンパク質の濃度を検出することなく、該完全長CEAタンパク質の濃度を検出することと、
該治療後の試料中の該完全長CEAタンパク質の濃度を、治療前に得られた試料中の該濃度と比較することと、
を含み、
該治療前の試料と比較して、該治療後の試料中の完全長CEAタンパク質濃度の低下が、該対象を治療する該方法での該抗CEA癌治療薬の有効性を示す、方法。
6. 癌胎児性抗原(CEA)タンパク質に免疫特異的に結合する癌治療薬に対する感受性を判定する方法であって、
CEAを発現する癌を患っている対象の治療に使用される癌治療薬を選択することであって、この癌治療薬は、CEAタンパク質の1つの型に免疫特異的に結合するが、CEAタンパク質の第2の型には免疫特異的に結合せず、CEAタンパク質の1つの型は、標的CEAタンパク質と称される、選択することと、
該癌治療薬が免疫特異的に結合するエピトープと同じまたは実質的に同じである前記標的CEAタンパク質上のエピトープに免疫特異的に結合する抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いて、該対象からの試料中の該標的CEAタンパク質の濃度を検出し、それによって、該試料中の該非標的型のCEAタンパク質の濃度を検出することなく、該標的CEAタンパク質の濃度を検出することと、
該標的CEAタンパク質の該濃度を、健常な対象からの試料中の標的CEAタンパク質濃度を反映する標準範囲と比較することと、
を含み、
該標準範囲を超える該試料中の該標的CEAタンパク質の濃度の検出は、前記癌治療薬に対する感受性を示す、方法。
7. 治療をモニタリングする方法であって、
CEAを発現する癌を患っている対象の治療に使用される癌治療薬を選択することであって、この癌治療薬は、CEAタンパク質の1つの型に免疫特異的に結合するが、CEAタンパク質の第2の型には免疫特異的に結合せず、CEAタンパク質の1つの型は、標的CEAタンパク質と称される、選択することと、
該癌治療薬が免疫特異的に結合するエピトープと同一または実質的に同一である該標的CEAタンパク質上のエピトープに免疫特異的に結合する抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いて、CEAを発現する癌の治療を受けている該対象からの試料中の該標的CEAタンパク質の濃度を検出し、それによって、該試料中の他の非標的型のCEAタンパク質の濃度を検出することなく、該標的CEAタンパク質の濃度を検出することと、
該標的CEAタンパク質の濃度を、該癌治療薬による治療前または該癌治療薬による治療中の早期の時点で得られる該同一の対象からの早期試料中の標的CEAタンパク質の濃度と比較することと、
を含み、
該癌治療薬による治療前または治療中の早期の時点で得られた濃度に対する、該癌治療薬による治療中の後期の時点で得られた試料中の標的CEA濃度の低下は、該癌治療薬の有効性を示し、それによって、該治療をモニタリングする、方法。
8. 癌胎児性抗原(CEA)を発現する癌を患っている対象を治療する方法であって、
CEAを発現する癌を患っている対象の治療に使用される癌治療薬を選択することであって、この癌治療薬は、CEAタンパク質の1つの型に免疫特異的に結合するが、CEAタンパク質の第2の型には免疫特異的に結合せず、CEAタンパク質の1つの型は、標的CEAタンパク質と称される、選択することと、
該治療薬が免疫特異的に結合するエピトープと同一または実質的に同一である該標的CEAタンパク質上のエピトープに免疫特異的に結合する抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いて、該対象からの試料中の該標的CEAタンパク質の濃度を検出し、それによって、該試料中の他の非標的型のCEAタンパク質の濃度を検出することなく、該標的CEAタンパク質の濃度を検出することと、
該標的CEAタンパク質の該濃度を、健常な対象からの試料中の標的CEAタンパク質濃度を反映する標準範囲と比較することであって、
該標準範囲を超える該標的CEAタンパク質の濃度の検出は、標的CEAタンパク質に免疫特異的に結合する癌治療薬に対する感受性を示す、比較することと、
該対象が該癌治療薬に対して感受性があると判定される場合、標的CEAタンパク質に免疫特異的に結合する該癌治療薬により該対象を治療することと、
任意に、該癌治療薬が免疫特異的に結合するエピトープと同一または実質的に同一である標的CEA上のエピトープに免疫特異的に結合する抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いて、該癌治療薬による治療を受けている該対象からの治療後の試料中の標的CEAタンパク質の濃度を検出し、それによって、該試料中の他の非標的型のCEAタンパク質の濃度を検出することなく、該標的CEAタンパク質の濃度を検出することと、
該標的CEAタンパク質の濃度を、該同一の対象からの、該癌治療薬による治療前、または前記治療中の早期の時点で得られた試料中の標的CEAタンパク質の濃度と比較することと、
を含み、
該治療前または該治療中の早期の時点で得られた濃度に対する、該癌治療薬による治療中の後期の時点で得られた試料中の標的CEA濃度の低下は、該対象の該治療の有効性を示す、方法。
9. 対象からの試料中の完全長CEAタンパク質の濃度および短型CEAタンパク質の濃度を検出することと、
完全長CEAタンパク質濃度と短型CEAタンパク質濃度との比率を判定することと、
を含む、方法。
10. 該比率を、健常な対象からの試料中の、完全長CEAタンパク質濃度と短型CEAタンパク質濃度との標準比率を反映する標準と比較することをさらに含み、
該標準比率よりも高いまたは低い比率は、CEAを発現する癌の存在を示す、実施形態9に記載の方法。
11. 完全長CEAタンパク質の濃度の検出は、完全長CEAタンパク質に免疫特異的に結合するが、短型CEAタンパク質には免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子と試料を接触させることを含む、実施形態9または10に記載の方法。
12. 完全長CEAタンパク質の濃度の検出は、完全長CEAタンパク質に免疫特異的に結合するが、短型CEAタンパク質に免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子と、試料を接触させることを含み、短型CEAタンパク質の濃度の検出は、短型CEAタンパク質に免疫特異的に結合するが、完全長CEAタンパク質に免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子と、試料を接触させることを含む、実施形態9〜11のいずれか1項に記載の方法。
13. 抗CEA癌治療薬によって該対象を治療することをさらに含む、実施形態1〜4または6〜7のいずれか1項に記載の方法。
14. 該癌治療薬は、該検出ステップに使用される該抗体、抗原結合フラグメント、または免疫グロブリン様分子によって免疫特異的に結合されるものと同一または実質的に同一であるCEAタンパク質上のエピトープに免疫特異的に結合する、実施形態5、8、または13のいずれか1項に記載の方法。
15. 該対象は、ヒトである、実施形態1〜14のいずれか1項に記載の方法。
16. 該癌治療薬は、タンパク質治療薬を含む、実施形態3〜8のいずれか1項に記載の方法。
17. 該タンパク質治療薬は、抗体または抗原結合フラグメントである、実施形態16に記載の方法。
18. 該タンパク質治療薬は、モノクローナル抗体である、実施形態17に記載の方法。
19. 該モノクローナル抗体は、キメラ抗体、ヒト化抗体、または完全ヒト抗体である、実施形態18に記載の方法。
20. 該タンパク質治療薬は、配列番号2のアミノ酸配列を含むタンパク質に免疫特異的に結合する、実施形態17〜19のいずれか1項に記載の方法。
21. 該タンパク質治療薬は、配列番号2のアミノ酸配列を含むタンパク質に免疫特異的に結合するが、配列番号1のアミノ酸配列を含むタンパク質には免疫特異的に結合しない、実施形態20に記載の方法。
22. 該タンパク質治療薬は、抗体A5B7の抗原結合ドメインを含む、実施形態17に記載の方法。
23. 該タンパク質治療薬は、二重特異性抗体である、実施形態17に記載の方法。
24. 該二重特異性抗体は、CEA結合部分およびCD3結合部分を含む、実施形態23に記載の方法。
25. 該試料は、全血、血清、血漿、唾液、尿、糞便、精漿、汗、羊水、痰、母乳、胆液、組織ホモジネート、および腹水から選択される、実施形態1〜24のいずれか1項に記載の方法。
26. 該試料は、腫瘍組織試料である、実施形態1〜24のいずれか1項に記載の方法。
27. 該CEAを発現する癌は、結腸癌、直腸癌、膵臓癌、食道癌、胃食道癌、胃癌、肺癌、および乳癌から選択される、実施形態1〜26のいずれか1項に記載の方法。
28. 該検出するステップは、
該抗体、抗原結合フラグメント、または免疫グロブリン様分子と、該試料を接触させることと、
免疫組織化学によって完全長CEAタンパク質の濃度を検出することと、
を含む、実施形態1〜8のいずれか1項に記載の方法。
29. 該試料は、モノクローナル抗体である該抗体と接触させる、実施形態28に記載の方法。
30. 該モノクローナル抗体は、キメラ抗体、ヒト化抗体、または完全ヒト抗体である、実施形態29に記載の方法。
31. 該検出ステップは、
配列番号2のアミノ酸配列を含むタンパク質に結合する該抗体、抗原結合フラグメント、または免疫グロブリン様分子と、該試料を接触させることと、
免疫組織化学によって完全長CEAタンパク質の濃度を検出することと、
を含む、実施形態1〜8のいずれか1項に記載の方法。
32. 該検出ステップは、
抗体A5B7の抗原結合ドメインを含む抗体または抗原結合フラグメントと該試料を接触させることを含むが、但し、該抗体は、A5B7ではない、実施形態1〜8または28〜31のいずれか1項に記載の方法。
33. 該検出ステップは、
A5B7と同一または実質的に同一のエピトープに結合する抗原結合ドメインを含む抗体または抗原結合フラグメントと該試料を接触させることを含むが、但し、該抗体が、A5B7ではない、実施形態1〜8または28〜31のいずれか1項に記載方法。
34. 該検出ステップは、
A5B7と同一または実質的に同一のエピトープに結合する抗原結合ドメインを含む抗体または抗原結合フラグメントと該試料を接触させることを含むが、但し、該抗体が、A5B7または二重特異性抗体ではない、実施形態1〜8または28〜31のいずれか1項に記載方法。
35. 生物学的試料中の短型癌胎児性抗原(CEA)のRNAの発現を検出する方法は、
CEAヌクレオチド配列にハイブリダイズする核酸プローブまたは核酸プライマーのうちの1つまたは両方であって、(i)短型CEAヌクレオチド配列に特異的にハイブリダイズするが、完全長CEAヌクレオチド配列に特異的にハイブリダイズしないこと、または(ii)短型CEAの発現と完全長CEAの発現を区別する様式で、短型CEAヌクレオチド配列および完全長CEAヌクレオチド配列の両方に特異的にハイブリダイズすることによって、短型CEAの発現を特異的に特定する、核酸プローブまたは核酸プライマーを提供することと、
生物学的試料からRNAを提供することと、
該核酸プローブまたは核酸プライマーを用いて、該生物学的試料中の短型CEAのRNAの発現を検出することと、
を含む、方法。
36. 生物学的試料中の短型癌胎児性抗原(CEA)タンパク質の発現を検出する方法は、
短型CEAタンパク質に免疫特異的に結合するが、完全長CEAタンパク質に免疫特異的に結合しない抗体、抗原結合フラグメント、または免疫グロブリン様分子を提供することと、
生物学的試料を提供することと、
該抗体を用いて、該生物学的試料中の短型CEAタンパク質の発現を検出することと、
を含む、方法。
37. 該生物学的試料は、腫瘍組織試料である、実施形態35または36に記載の方法。
38. 該生物学的試料は、全血、血清、血漿、唾液、尿、糞便、精漿、汗、羊水、組織ホモジネート、痰、母乳、胆液、および腹水から選択される、実施形態36に記載の方法。
39. 抗体を提供することを含み、該抗体は、モノクローナル抗体である、実施形態36に記載の方法。
40. 該モノクローナル抗体は、キメラ抗体、ヒト化抗体、または完全ヒト抗体である、実施形態39に記載の方法。
41. 該抗体は、配列番号1のアミノ酸配列を含むタンパク質に結合する、実施形態36に記載の方法。
42. 完全長癌胎児性抗原(CEA)タンパク質に対して免疫特異的な抗体を生成する方法であって、
短型CEAタンパク質に存在しない完全長CEAタンパク質の一部を提供することと、
該抗体を生成するための抗原として、該完全長CEAタンパク質の一部を使用することと、
を含む、方法。
43. 該抗体は、モノクローナル抗体である、実施形態42に記載の方法。
44. 配列番号1で表されるアミノ酸配列を含む精製されたポリペプチド、または連続するアミノ酸残基:NIIQNELSVD(配列番号11)またはNIIQNKLSVD(配列番号12)を含む、そのフラグメント。
45. 標的癌胎児性抗原(CEA)タンパク質に免疫特異的に結合する癌治療薬に対する感受性がある可能性がある患者を特定する方法であって、
患者から試料を得ることと、
完全長CEAのRNA発現と短型CEAのRNA発現を区別するために、該試料中の、標的CEAのRNAの発現を検出することと、
を含み、
該患者からの腫瘍試料が、該標的CEAのRNAを発現する場合、該患者は、その標的CEAタンパク質に免疫特異的に結合する癌治療薬による治療に対する感受性がある可能性があり、該患者からの腫瘍試料が、該標的CEAのRNAを発現しない場合、該患者は、その標的CEAタンパク質に免疫特異的に結合する癌治療薬による治療に対する感受性がないであろう、方法。
46. 標的CEAのRNA発現の検出は、プローブおよび/またはプライマーと該試料を接触させて、完全長CEAのRNAの発現を評価することを含む、実施形態45に記載の方法。
47. 標的CEAのRNA発現の検出は、プローブおよび/またはプライマーと該試料を接触させて、短型CEAのRNAの発現を評価することを含む、実施形態45に記載の方法。
48. 標的CEAのRNA発現の検出は、プローブおよび/またはプライマーと該試料を接触させて、完全長CEAのRNAおよび短型CEAのRNAの両方の発現を評価することを含む、実施形態45に記載の方法。
49. 該方法は、該患者から1つ以上のさらなる生物学的試料を採取することと、該標的CEAタンパク質の発現について該1つ以上の生物学的試料をアッセイすることと、をさらに含む、実施形態45〜48のいずれか1項に記載の方法。
50. 該方法は、癌治療薬によって該対象を治療することをさらに含む、実施形態45〜49のいずれか1項に記載の方法。
51. 該抗体、抗原結合フラグメント、または免疫グロブリン様分子は、配列番号28〜44および46〜51のアミノ酸配列から選択されるアミノ酸配列を含む、実施形態1〜8、11〜34、および36〜41のいずれか1項に記載の方法。
52. 該抗CEA治療薬は、配列番号28〜44および46〜51のアミノ酸配列から選択されるアミノ酸配列を含む、実施形態3、5〜8、13〜34、および45〜50のいずれか1項に記載の方法。
53. 該抗体、抗原結合フラグメント、または免疫グロブリン様分子は、配列番号48のアミノ酸配列を含む、実施形態51に記載の方法。
54. 該抗体、抗原結合フラグメント、または免疫グロブリン様分子は、配列番号49のアミノ酸配列を含む、実施形態51に記載の方法。
55. 該抗体、抗原結合フラグメント、または免疫グロブリン様分子は、配列番号46のアミノ酸配列を含む、実施形態51に記載の方法。
56. 該抗体、抗原結合フラグメント、または免疫グロブリン様分子は、配列番号51のアミノ酸配列を含む、実施形態51に記載の方法。
57. 該抗CEA治療薬は、配列番号48のアミノ酸配列を含む、実施形態52に記載の方法。
58. 該抗CEA治療薬は、配列番号49のアミノ酸配列を含む、実施形態52に記載の方法。
59. 該抗CEA治療薬は、配列番号46のアミノ酸配列を含む、実施形態52に記載の方法。
59. 該抗CEA治療薬は、配列番号51のアミノ酸配列を含む、実施形態60に記載の方法。
60. 癌胎児性抗原(CEA)を発現する癌の再発を検出する方法であって、
癌胎児性抗原(CEA)を発現する癌であると以前に診断され、治療された患者から試料を得ることと、
該試料中の、完全長CEAタンパク質をコードするRNAの濃度を検出することと、を含み、
治療後に観察された濃度を超える、該試料中の完全長CEAのRNAの濃度の検出は、該CEAを発現する癌の再発を示す、方法。
61. 癌胎児性抗原(CEA)を発現する癌の再発を検出する方法であって、
癌胎児性抗原(CEA)を発現する癌を患っている対象から、治療前に得られる第1の試料を得ることと、
該第1の試料中の、完全長CEAをコードするRNAの治療前の濃度を検出することと、
該対象から第2の試料を得て、該第2の試料中の、完全長CEAタンパク質をコードするRNAの濃度を検出することと、
該第2の試料を得たものよりも後の時点で、該対象から1つ以上のさらなる試料を得て、該1つ以上のさらなる試料中の、完全長CEAタンパク質をコードするRNAの濃度を検出することと、
を含み、
該第2の試料中で観察された完全長CEAタンパク質をコードするRNAの濃度を超える該1つ以上のさらなる試料中の完全長CEAタンパク質をコードするRNAの濃度の検出は、該CEAを発現する癌の再発を示す、方法。
62. 抗癌胎児性抗原(CEA)癌治療薬に対する感受性を判定する方法であって、
対象からの試料中の完全長CEAタンパク質をコードするRNAの濃度を検出することと、
該完全長CEAタンパク質をコードするRNAの濃度を、健常な対象からの試料中の完全長CEAタンパク質をコードするRNAの濃度を反映する標準範囲と比較することと、
を含み、
該標準範囲を超える完全長CEAタンパク質をコードするRNAの濃度の検出は、抗CEA癌療法に対する感受性を示す、方法。
63. 抗癌胎児性抗原(CEA)癌療法をモニタリングする方法であって、
CEA発現の治療を受けている対象からの試料中の完全長CEAタンパク質をコードするRNAの濃度を検出することと、
該完全長CEAタンパク質をコードするRNAの濃度を、該治療前または前記治療中の早期の時点で得られた該同一の対象からの試料中の完全長CEAタンパク質の濃度と比較することと、
を含み、
治療前または該治療中の早期の時点で得られた濃度に対する、治療中の後半の時点で得られた試料中の完全長CEA濃度をコードするRNAの低下は、該治療の有効性を示し、それによって、該抗CEA癌療法をモニタリングする、方法。
64. 癌胎児性抗原(CEA)を発現する癌を患っている対象を治療する方法であって、
癌胎児性抗原(CEA)を発現する癌に対する治療前に、対象から試料を得ることと、
該試料中の、完全長CEAをコードするRNAの濃度を検出することと、
完全長CEAタンパク質をコードする該RNAの濃度を、健常な対象からの試料中の完全長CEAタンパク質をコードするRNAの濃度を反映する標準範囲と比較することであって、
該標準範囲を超える完全長CEAタンパク質をコードするRNAの濃度の検出は、抗CEA癌療法に対する感受性を示す、比較することと、
該対象が、抗CEA癌療法に対して感受性があると判定される場合、抗CEA癌治療薬を用いて該対象を治療することと、
任意に、該対象からの治療後の試料中の完全長CEAタンパク質をコードするRNAの濃度を検出することと、
該治療後の試料中の完全長CEAタンパク質をコードする該RNAの濃度を、治療前に得られた試料中の該濃度と比較することと、
を含み、
該治療前の試料と比較して、該治療後の試料中の完全長CEAタンパク質濃度をコードするRNAの低下が、該対象を治療する該方法での該抗CEA癌治療薬の有効性を示す、方法。
65. 癌胎児性抗原(CEA)タンパク質に免疫特異的に結合する癌治療薬に対する感受性を判定する方法であって、
CEAを発現する癌を患っている対象の治療に使用される癌治療薬を選択することであって、この癌治療薬は、CEAタンパク質の1つの型に免疫特異的に結合するが、CEAタンパク質の第2の型には免疫特異的に結合せず、CEAタンパク質の1つの型は、標的CEAタンパク質と称される、選択することと、
非標的型のCEAタンパク質をコードするRNAの濃度を検出することなく、該対象からの試料中の該標的CEAタンパク質をコードするRNAの濃度を検出することと、
該標的CEAタンパク質をコードする該RNAの該濃度を、健常な対象からの試料中の該標的CEAタンパク質をコードするRNAの濃度を反映する標準範囲を比較することと、
を含み、
該標準範囲を超える該試料中の該標的CEAタンパク質をコードする該RNAの濃度の検出は、該癌治療薬に対する感受性を示す、方法。
66. 治療をモニタリングする方法であって、
CEAを発現する癌を患っている対象の治療に使用される癌治療薬を選択することであって、この癌治療薬は、CEAタンパク質の1つの型に免疫特異的に結合するが、CEAタンパク質の第2の型には免疫特異的に結合せず、CEAタンパク質の1つの型は、標的CEAタンパク質と称される、選択することと、
CEAを発現する癌の治療を受けている該対象からの試料中の該標的CEAタンパク質をコードするRNAの濃度を、該試料中の非標的型のCEAタンパク質の濃度を検出することなく、検出することと、
該標的CEAタンパク質をコードする該RNAの濃度を、該癌治療薬による治療前または該癌治療薬による治療中の早期の時点で得られた該同一の対象からの早期の試料中の該標的CEAタンパク質をコードするRNAの濃度と比較することと、を含み、
該癌治療薬による治療前または治療中の早期の時点で得られた濃度に対する、該癌治療薬による治療中の後期の時点で得られた試料中の該標的CEA濃度をコードするRNAの低下は、該癌治療薬の有効性を示し、それによって、該治療をモニタリングする、方法。
67. 癌胎児性抗原(CEA)を発現する癌を患っている対象を治療する方法であって、
CEAを発現する癌を患っている対象の治療に使用される癌治療薬を選択することであって、この癌治療薬は、CEAタンパク質の1つの型に免疫特異的に結合するが、CEAタンパク質の第2の型には免疫特異的に結合せず、CEAタンパク質の1つの型は、標的CEAタンパク質と称される、選択することと、
プライマーおよび/またはプローブを用いて、該対象からの試料中の該標的CEAタンパク質をコードするRNAの濃度を検出し、該治療薬が免疫特異的に結合するエピトープと同一または実質的に同一である該標的CEAタンパク質上のエピトープをコードするRNAを検出し、それによって、該試料中の非標的型のCEAタンパク質をコードするRNAの濃度を検出することなく、該RNA標的CEAタンパク質をコードするRNAの濃度を検出することと、
該標的CEAタンパク質をコードする該RNAの濃度を、健常な対象からの試料中の標的CEAタンパク質濃度を反映する標準範囲と比較することであって、
該標準範囲を超える該標的CEAタンパク質の濃度の検出は、標的CEAタンパク質に免疫特異的に結合する癌治療薬に対する感受性を示す、比較することと、
該対象が該癌治療薬に対して感受性があると判定される場合、標的CEAタンパク質に免疫特異的に結合する該癌治療薬により該対象を治療することと、
任意に、該癌治療薬による治療を受けている該対象からの治療後の試料中の、標的CEAタンパク質をコードするRNAの濃度を検出し、それによって、該試料中の非標的型のCEAタンパク質をコードするRNAの濃度を検出することなく、該標的CEAタンパク質の濃度を検出することと、
該標的CEAタンパク質をコードする該RNAの濃度を、該癌治療薬による治療前または該治療中の早期の時点で得られた該同一の対象からの試料中の該標的CEAタンパク質をコードするRNAの濃度と比較することと、
を含み、
該癌治療薬による治療前または該治療中の早期の時点で得られた試料中の該標的CEA濃度に対する、該癌治療薬による治療中の後期の時点で得られた試料中の該標的CEA濃度をコードするRNAの低下は、該対象の該治療の有効性を示す、方法。
68. 対象からの試料中の完全長CEAタンパク質をコードするRNAの濃度および短型CEAタンパク質をコードするRNAの濃度を検出することと、
完全長CEAタンパク質をコードするRNAの濃度と短型CEAタンパク質濃度をコードするRNAの濃度との比率を判定することと、を含む、方法。
69. 該比率を、健常な対象からの試料中の、完全長CEAタンパク質をコードするRNAの濃度と短型CEAタンパク質をコードするRNAの濃度との標準比率を反映する標準と比較することをさらに含み、
該標準比率よりも高いまたは低い比率は、CEAを発現する癌の存在を示す、実施形態68に記載の方法。
11. 完全長CEAタンパク質をコードするRNAの濃度の検出は、完全長CEAタンパク質をコードするRNAにハイブリダイズするが、短型CEAタンパク質にはハイブリダイズしないプライマーおよびまたはプローブと、試料を接触させることを含む、実施形態68または69に記載の方法。
71. 完全長CEAタンパク質をコードするRNAの濃度の検出は、完全長CEAタンパク質をコードするRNAにハイブリダイズするが、短型CEAタンパク質にはハイブリダイズしないプライマーおよびまたはプローブと、試料を接触させることと、短型CEAタンパク質をコードするRNAにハイブリダイズするが、完全長CEAタンパク質にはハイブリダイズしないプライマーおよびまたはプローブと、試料を接触させることと、を含む、実施形態68〜70のいずれか1項に記載の方法。
72. 抗CEA癌治療薬によって該対象を治療することをさらに含む、実施形態60〜63または65〜66のいずれか1項に記載の方法。
73. 該癌治療薬は、該検出ステップに使用される該抗体、抗原結合フラグメント、または免疫グロブリン様分子によって免疫特異的に結合されるものと同一または実質的に同一であるCEAタンパク質上のエピトープに免疫特異的に結合する、実施形態64、67、または72のいずれか1項に記載の方法。
74. 該対象は、ヒトである、実施形態60〜73のいずれか1項に記載の方法。
75. 該癌治療薬は、タンパク質治療薬を含む、実施形態63〜67のいずれか1項に記載の方法。
76. 該タンパク質治療薬は、抗体または抗原結合フラグメントである、実施形態75に記載の方法。
77. 該タンパク質治療薬は、モノクローナル抗体である、実施形態76に記載の方法。
78. 該モノクローナル抗体は、キメラ抗体、ヒト化抗体、または完全ヒト抗体である、実施形態77に記載の方法。
79. 該タンパク質治療薬は、配列番号2のアミノ酸配列を含むタンパク質に免疫特異的に結合する、実施形態76〜78のいずれか1項に記載の方法。
80. 該タンパク質治療薬は、配列番号2のアミノ酸配列を含むタンパク質に免疫特異的に結合するが、配列番号1のアミノ酸配列を含むタンパク質には免疫特異的に結合しない、実施形態79に記載の方法。
81. 該タンパク質治療薬は、抗体A5B7の抗原結合ドメインを含む、実施形態76に記載の方法。
82. 該タンパク質治療薬は、二重特異性抗体である、実施形態76に記載の方法。
83. 該二重特異性抗体は、CEA結合部分およびCD3結合部分を含む、実施形態82に記載の方法。
84. 該試料は、全血、血清、血漿、唾液、尿、糞便、精漿、汗、羊水、痰、母乳、胆液、組織ホモジネート、および腹水から選択される、実施形態60〜83のいずれか1項に記載の方法。
85. 該試料は、腫瘍組織試料である、実施形態60〜83のいずれか1項に記載の方法。
86. 該CEAを発現する癌は、結腸癌、直腸癌、膵臓癌、食道癌、胃食道癌、胃癌、肺癌、および乳癌から選択される、実施形態60〜85のいずれか1項に記載の方法。
87. 該検出ステップは、実施形態35または45に記載の方法を含む、実施形態60〜67のいずれか1項に記載の方法。
88. 該試料は、実施形態46に記載のプローブ/およびまたはプライマーと接触させる、実施形態87に記載の方法。
89. 該試料は、実施形態47に記載のプローブ/およびまたはプライマーと、任意に、実施形態46に記載のプローブおよび/またはプライマーと接触させる、実施形態87に記載の方法。
90. 該検出ステップは、
配列番号2のアミノ酸配列を含むタンパク質をコードするRNAにハイブリダイズするプライマーおよび/またはプローブと、該試料を接触させる、実施形態60〜67のいずれか1項に記載の方法。
91. 該検出ステップは、
抗体A5B7の抗原結合ドメインによって結合されるエピトープを含むタンパク質をコードするRNAにハイブリダイズするプライマーおよび/またはプローブと、該試料を接触させることを含む、実施形態60〜67または87〜90のいずれか1項に記載の方法。
92. 該検出ステップは、
A5B7によって結合される同一または実質的に同一のエピトープを含むタンパク質をコードするRNAにハイブリダイズするプライマーおよび/またはプローブと、該試料を接触させることを含む、実施形態60〜67または87〜90のいずれか1項に記載の方法。
93. 該検出ステップは、
A5B7によって結合される同一または実質的に同一のエピトープを含まないタンパク質をコードするRNAにハイブリダイズするプライマーおよび/またはプローブと、該試料を接触させることを含む、実施形態60〜67または87〜90のいずれか1項に記載の方法。
94. 生物学的試料中の短型癌胎児性抗原(CEA)タンパク質の発現を検出する方法は、
短型CEAタンパク質をコードするRNAにハイブリダイズするが、完全長CEAタンパク質をコードするRNAにはハイブリダイズしないプライマーおよびまたはプローブを提供することと、
生物学的試料を提供することと、
該プライマーおよびまたはプローブを用いて、該生物学的試料中の短型CEAタンパク質をコードするRNAの発現を検出することと、
を含む、方法。
95. 該生物学的試料は、腫瘍組織試料である、実施形態94に記載の方法。
96. 該生物学的試料は、全血、血清、血漿、唾液、尿、糞便、精漿、汗、羊水、組織ホモジネート、痰、母乳、胆液、および腹水から選択される、実施形態94に記載の方法。
97. プライマーを提供することを含む、実施形態94に記載の方法。
98. プライマーおよびプローブを提供することを含む、実施形態94に記載の方法。
99. 該プライマーおよび/またはプローブは、配列番号1のアミノ酸配列を含むタンパク質をコードするRNAに結合する、実施形態94に記載の方法。
100. 該抗体、抗原結合フラグメント、または免疫グロブリン様分子は、配列番号28〜44および46〜51のアミノ酸配列から選択されるアミノ酸配列を含む、実施形態60〜67、70〜93、および94〜99のいずれか1項に記載の方法。
101. 抗CEA治療薬は、配列番号28〜44および46〜51のアミノ酸配列から選択されるアミノ酸配列を含む、実施形態62、64〜67、および72〜93のいずれか1項に記載の方法。
102. 該抗体、抗原結合フラグメント、または免疫グロブリン様分子は、配列番号48のアミノ酸配列を含む、実施形態100に記載の方法。
103. 該抗体、抗原結合フラグメント、または免疫グロブリン様分子は、配列番号49のアミノ酸配列を含む、実施形態100に記載の方法。
104. 該抗体、抗原結合フラグメント、または免疫グロブリン様分子は、配列番号46のアミノ酸配列を含む、実施形態100に記載の方法。
105. 該抗体、抗原結合フラグメント、または免疫グロブリン様分子は、配列番号51のアミノ酸配列を含む、実施形態100に記載の方法。
106. 該抗CEA治療薬は、配列番号48のアミノ酸配列を含む、実施形態101に記載の方法。
107. 該抗CEA治療薬は、配列番号49のアミノ酸配列を含む、実施形態101に記載の方法。
108. 該抗CEA治療薬は、配列番号46のアミノ酸配列を含む、実施形態101に記載の方法。
109. 該抗CEA治療薬は、配列番号51のアミノ酸配列を含む、実施形態101に記載の方法。
110. 該標的は、完全長CEAタンパク質である、実施形態6、7、8、13〜34、45〜48、65〜67、および72〜93のいずれか1項に記載の方法。
111. 該標的は、短型CEAタンパク質である、実施形態6、7、8、13〜34、45〜48、65〜67、および72〜93のいずれか1項に記載の方法。
112. 実施形態61〜111のいずれか1項に記載のCEAタンパク質をコードするRNAを検出することをさらに含む、実施形態1〜34、36〜41、および51〜60のいずれか1項に記載のCEAタンパク質を検出する方法。
配列表 例示
本開示をここで一般的に記載したが、本開示は、以下の実施例を参照することによりさらに容易に理解され、これらの実施例は、本開示のある態様および実施形態の説明のためにのみ含まれ、本開示を限定することを意図しない。例えば、本明細書に開示される特定の構築物および実験設計は、適切な機能を検証するための例示的なツールおよび方法を表す。したがって、開示された特定の構築物および実験計画のいずれかは、本開示に範囲内で置き換えることができることは、容易に明らかであろう。
実施例1:短型CEAの特定
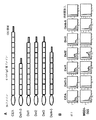
CEA(NCBI RefSeq NM_002483;CEACAM5;CD66e)の完全長転写物は、10エキソンを含有し、それは、702アミノ酸(aa)(NCBI RefSeq NP_004354.2;図1および2)のタンパク質前駆体に翻訳する。N末端34アミノ酸シグナルペプチドおよびCEAのC末端の17アミノ酸ポリペプチドは、タンパク質成熟中に除去される(Bachman,1987)。結腸癌組織からのより短いCEAスプライス変異体(NCBI RefSeq CR749337;短型CEA)のcDNA配列は、Genbank遺伝子配列データベースに特定された。この転写物は、エキソン2の代替的なスプライシングドナー部位を使用し、エキソン3および4をスキップし、したがって、転写物は、完全長CEAのアミノ酸116から396(N末端プロ配列を含む場合、計数される)のインフレーム短縮を伴い、420アミノ酸タンパク質をもたらす(図2)。この短縮は、V−setドメインの一部分および3つのIgC2様ドメインを欠損する(図3)。
実施例2:完全長CEAおよび短型CEAの定量分析
TissueScan(商標)Disease Tissue定量的ポリメラーゼ連鎖反応(qPCR)アレイを採用して、様々な病期および悪性度の正常および癌組織中完全長および短型CEA転写物の発現を判定した。アレイは、TissueScan(商標)Colon Cancer Tissue qPCR Array I、TissueScan(商標)Pancreatic Cancer Tissue qPCR Array I、TissueScan(商標)Gastroesophageal Cancer Tissue qPCR Array I、TissueScan(商標)Lung Cancer Tissue qPCR Array I、およびTissueScan(商標)Breast Cancer Tissue qPCR Array Iを含んだ。それぞれの組織cDNAアレイのために、凍結乾燥したcDNAを、2.5μLのリボヌクレアーゼ(RNase)free水中に再懸濁した。プレートは、密閉し、ボルテックスし、遠心分離して、完全DNA試料の再懸濁を確保した。エキソン2および5のスプライス部位(短型CEA用)ならびにエキソン3および4のスプライス部位(完全長CEA用)を特異的に標的化したプライマーおよびプローブを分析に使用した(表1)。
次いで、TaqManアッセイのプールが、前増幅、続いて、特異的標的転写物の増幅のために製造業者によって供給されたプロトコルに従って作製された。具体的には、短型CEA、完全長CEA、またはリボソームサブユニット18S cDNAに対して特異的な10μLの20X Custom TaqMan遺伝子発現アッセイミックスを、990μLの水と混合して、アッセイの最終濃度を0.2Xにした。前増幅反応は、2.5μLのプールしたアッセイミックスおよび5μLのTaqMan PreAmp Master Mixを再懸濁したcDNAに添加することによって、供給された96ウェルプレート中に調製された。前増幅反応は、表2中に示される条件下で、Tetrad Thermalcycler上で実施された。前増幅後、試料は、pH8.0で、90μLのDNA再懸濁緩衝液を添加することによって、100μLまで希釈した。定量PCRは、標的遺伝子のそれぞれのために、前増幅したcDNA試料およびTaqManアッセイ構成要素を用いて調製された(表3)。
必要な反応構成要素を添加した後、それぞれのプレートは、MicroAmp Optical Adhesive Filmで密閉し、ボルテックスし、短時間遠心分離し、次いで、表4中に示されるサイクル条件を用いて、ABI 7900HT Fast Real Time PCR Instrument中で、高速モードでqPCRのために処理した。
qPCRの完了後、SDS2.2ソフトウェアを使用し、閾値サイクル(Ct)値を生成した。典型的な反応では、PCR生成物は、指数関数的に生成される。生成物が検出可能になるまでにはいくつかのサイクルが必要であるため、蛍光対サイクル数のプロットは、S字状の外観を示す。後の方のサイクルでは、反応基質が枯渇し、PCR生成物はもう2倍にはならず、曲線が平らになり始める。通常、ベースラインをわずかな標準偏差だけ超える、蛍光の量が指数関数的に増加し始める曲線上の点が、Ct値と称される。すべてのCt値が出力された後に、相対定量の算出が行われた。遺伝子発現に対してそれより低ければ試料が陽性であると見なされ、それより高ければ試料が陰性であると見なされる、30のCtカットオフ値が任意に選択された。
陽性対照として、完全長(CHO/huCEA)あるいは短型CEA(CHO/短型CEAクローン72−4)のいずれかを発現するチャイニーズハムスター卵巣(CHO)細胞からのcDNAが使用された。相補的DNAは、RNeasy Mini Kitを用いたRNAの単離、続いて、Superscript(登録商標)ワンサイクルcDNAキットを用いるcDNA合成によって、調製された。得られたcDNAは、RNAクリーンビーズによって洗浄し、25μLのRNase−free水中に再懸濁した。完全長あるいは短型CEAのいずれも発現しないジヒドロ葉酸還元酵素(dhfr−CHO)の発現を欠損する親CHO細胞からの陰性対照cDNAは、同一の様式で調製された。陽性および陰性対照cDNA(5μL)は、RNase−free水中で50倍に希釈され、上記のqPCR増幅プロトコルにおいて、前増幅アレイcDNAとして使用された。陽性対照cDNAは、それらの関連遺伝子特異的プライマーおよびプローブセットで、Ct値が30を下回り、非関連セットで、Ct値が30を上回ることを示した。予想通りに、30を上回るCt値が、完全長および短型CEAの両方のプライマーおよびプローブセットで陰性対照cDNAに対して観察された。所定の試料中の完全長および短型CEAの相対発現レベルの算出のためのCt値の正規化のために、リボソーム18S RNA cDNAのCt値が、使用された。
この方法を用いて、TissueScan Disease Tissue qPCRアレイを使用して、正常および癌性の結腸、膵臓、胃食道、肺、および乳房組織における完全長および短型CEA転写物の発現を判定した(表5)。
完全長CEA転写物は、一般に、様々な悪性度および病期の、膵臓腺癌(5つのうち4つ)、結腸(42のうち41)、胃食道(42のうち38)、肺(40のうち39)、および乳房癌(41のうち38)において、検出された(Ct<30)。完全長CEA転写物は、まれに、膵臓癌の神経内分泌(9つのうち1つ)、島細胞(4つのうち1つ)、および腺房細胞(1つのうち0)において検出された。正常な結腸、肺、および胃食道組織において、完全長CEA転写物は、相対的に高い数字(Ct<25)で発現した。対照的に、正常な乳房組織において、完全長CEA転写物は、低い数字(25<Ct<30)で発現した。完全長CEA転写物の低い発現(Ct<30)は、TissueScan Arrayからの正常な膵臓組織において見出された。
短型CEA転写物の発現(Ct<30)は、一般に、結腸(42のうち41)および胃食道癌の半分(42のうち21)において、見出された。発現はまた、様々な悪性度および病期の、肺癌(40のうち12)と乳房癌(41のうち5つ)の比率にも見られた。短型CEAの発現は、まれに、膵臓腺癌(5つのうち1つ)に見出され、膵臓の神経内分泌癌(9つのうち0)、島細胞癌(4つのうち0)、または腺房細胞癌(1つのうち0)において見出されなかった。短型CEA転写物の発現は、常に、完全長CEA転写物の発現と一致した。これらの結果は、短型CEAスプライス転写物の発現は、異なる癌で異なるが、常に、完全長CEA転写物と同時発現することを示す。
実施例3:チャイニーズハムスター卵巣細胞における短型CEAのクローニングおよび発現
短型CEAの配列を含むcDNAクローンDKFZp781M2392Qのプラスミドは、B Bridge Internationalと合併したImaGenes GmbHから購入した。プラスミドDNAは、QIAprepスピンミニ調製キットを用いて、プラスミドDNA精製による細胞培養物から調製された。続いて、精製したDNAは、PCR反応においてテンプレートとして、使用し(表6および7)、Herculase II Fusion DNAポリメラーゼキットおよび遺伝子特異的プライマー376および377を用いて、短型CEAを増幅した(表8)。
反応生成物は、1% TAE(トリスアセテートエチレンジアミン四酢酸)ゲル電気泳動後、1.2キロベースのDNAバンドとして検出され、QIAquick PCR精製キットを用いてゲルから精製した。生成物は、TOPO(登録商標)TAクローニング(登録商標)によってpCR2.1ベクターにクローン化され、続いて、CEA遺伝子特異的プライマー376および377を用いて、青色/白色選択および診断PCRによってスクリーニングされたTOP10細菌に形質転換された。陽性コロニーからのDNAは、Prism Big Dye Terminatorによって配列を決定し、正確な短型CEA配列を確認した。照合された短型CEAは、Quick Ligation Kit(商標)を用いて、NheI/EcoRI消化したウイルスにNheI/EcoRI消化したCEAスプライス変異体を連結反応させることによって、pCDH1−HCS1−EF1−Puroベクターにサブクローン化された。そのようなサブクローニングは、遺伝子の構成的発現を誘導するサイトメガロウイルスプロモーターの短型CEA下流に位置付けられた。短型CEAを担持するレンチウイルスベクターは、TOP10細菌に形質転換され、細菌コロニーは、レンチウイルスおよび短型CEA配列に対して特異的なプライマーを用いて、PCRによってスクリーニングされた。正確な配向に短型CEAを含有する陽性コロニーを使用して、Rapid Plasmid Maxiprep Systemを用いて、レンチウイルスDNAを調製した。精製したレンチウイルスDNAは、Lipofectamine(商標)2000トランスフェクション試薬によって、凝縮プラスミドと一緒に293T細胞にトランスフェクトされて、感染性レンチウイルスを産生した。レンチウイルスを含有する細胞培養培地は、dhfr−CHO細胞の感染のために使用された。続いて、細胞は、短型CEAを発現するレンチウイルス感染CHO細胞の選択のために、72時間あるいは2週間のいずれかで、完全成長培地中の5μg/mLのピューロマイシンで処理された。ピューロマイシンによって選択された細胞のプールしたクローンは、限界希釈法によって単一細胞としてクローン化された。様々なレベルの短型CEAタンパク質を発現する単一細胞由来のクローンは、実施例4に定義されるように、抗体結合アッセイによって特定された。
実施例4:抗体結合
IgG B9(IgG B9は、(a)マウスA5B7のヒト化CDRおよび(b)マウスIgG1 Fcドメインを有するキメラ抗体である)、抗CEA抗体(抗CEACAM 5モノクローナル抗体、FITC共役抗ヒトCD66a、c、d、e、[CEACAM1、3、5、6]、および抗CEACAM1、3、4、5、6)の結合のために、抗体を、蛍光活性化細胞分類(FACS)緩衝液(リン酸緩衝生理食塩水[PBS]+2% ウシ胎仔血清[FBS])中に希釈された10μg/mLの濃度の細胞とともに、4℃で20分間インキュベートした。結合IgG B9および非標識抗CEAモノクローナル抗体の検出のために、細胞を、FACS緩衝液で2回洗浄し、FACS緩衝液中の10μg/mLのヤギ抗マウスAlexaFluor(登録商標)488二次抗体とともに、暗室中で、4℃で15分間インキュベートした。蛍光強度を判定する前に、細胞を、FACS緩衝液で1回洗浄した。T細胞への抗体の結合は、製造業者によって推奨された濃度で、CD4、CD8、およびCD25に対して抗体を用いて、FACS緩衝液中で行われた。結合アッセイのために、細胞を、FACS緩衝液中に再懸濁し、抗体および10μg/mLのヨウ化プロピジウム(PI)とともに、暗室中で、4℃で20分間インキュベートした。結合二次または直接共役抗体の蛍光強度は、LSRIIフローサイトメーターを用いたフローサイトメトリーによって判定され、データは、FlowJoソフトウェアを用いて分析された。生存細胞は、補正マトリックスを構築するために、単一染色した対照細胞による蛍光補正後の抗体結合について検査された。Fluorescence−minus−one対照が、陰性および陽性染色事象のゲートのために含まれた。
短型CEAを発現するCHO細胞の生成は、実施例3に記載される。単一細胞クローンは、IgG B9またはCEACAM5特異的MAbの結合によって、短型CEAタンパク質の細胞表面発現についてスクリーニングされた(図4)。抗CEACAM5 MAbが、様々なレベルで数多くのクローンに結合された。対照的に、IgG B9は、いかなるクローンにも実質的には結合しなかった。IgG B9によって認識されたエピトープを欠失し、また、2つの他の抗CEAモノクローナル抗体への結合を欠失する2つのクローン株、72−4および72−14は、さらなる研究のために選択された(図5)。これらのクローンはまた、高レベルの抗CEACAM5特異的モノクローナル抗体結合も示した(図4)。
実施例5:細胞傷害性
CHO/huCEA細胞のエフェクターT細胞媒介殺作用が、色素標識標的細胞の生存能力を測定するフローサイトメトリーベースのアッセイを用いて判定された。エフェクターCD3+T細胞は、RosetteSep(登録商標)ヒトT細胞濃縮カクテルおよびRosetteSep T細胞密度培地によって、健常なドナーのヘパリン化された全血から単離された。簡潔に言えば、20mLのヒト全血を、1mLのヒトT細胞濃縮カクテルに添加し、混合し、25℃で20分間インキュベートした。次いで、血液を、FACS緩衝液を用いて1:1に希釈し、RosetteSep T細胞密度培地で遠心分離した。濃縮ヒトT細胞は、血清/密度培地界面で除去され、FACS緩衝液を用いて2回洗浄した。最終的に、CD3+濃縮T細胞は、2.8×106細胞/mLの密度で、10% FBSおよび4.5g/Lのグルコースを含有するRoswell Park Memorial Institute(RPMI)−1640細胞培養培地中に再懸濁した。
CHO/huCEA細胞(完全長CEAタンパク質を発現する)またはCHO/短型CEAクローン72−4および72−14(これらのそれぞれは、短型CEAタンパク質を発現する)は、標的細胞として使用された。細胞を、採取し、洗浄し、最終的に、1×106細胞/mLの密度で、FACS緩衝液中に再懸濁した。細胞を、1mLあたり5μLの3,3′−ジオクタデシルオキサカルボシアニン(DiO)細胞標識溶液に迅速に添加し、37℃で1分間インキュベートした。細胞を、洗浄し、2.8×105細胞/mLの密度で、RPMI−1640細胞培養培地中に再懸濁した。
連続希釈のBiTE抗体(20μL)を、10対1のエフェクター対標的比で、96ウェル非組織培養で処理されたプレート中に、90μLの標的およびエフェクター細胞のそれぞれに添加した。MEC14 BiTEは、MEDI−565の対照BiTEとして使用した。MEC14 BiTEは、MEDI−565を構築するために使用された同一の抗CD3一本鎖抗体に連結したマウス抗Mecoprop(除草剤)一本鎖抗体からなる。
BiTE媒介細胞傷害性反応は、5% CO2を有する雰囲気下で、72時間、37℃で行われた。
細胞膜完全性として定義される細胞毒性は、PIの細胞取り込みによってモニタリングされた。生存細胞は、PIを除外する一方で、PIは、非生存細胞中の核酸を染色する。非生存ヨウ化プロピジウム陽性、DiO標識標的細胞の割合は、LSRIIフローサイトメーターを用いたフローサイトメトリーによって判定され、データは、FlowJoソフトウェアを用いて分析された。
MEDI−565は、CHO/huCEA細胞(完全長CEAタンパク質を発現する細胞)の用量依存性殺作用を媒介した。対照的に、MEDI−565は、CHO/短型CEA細胞クローン72−4および72−14(短型CEAタンパク質を発現する細胞)の殺作用を媒介しなかった(図6)。予想されたように、MEDI−565は、CEAの発現を欠失している親dhfr−CHO細胞の殺作用を媒介しなかった。
MEDI−565は、CHO/huCEA細胞によって共培養した後、用量依存性様式で、ヒトCD4+およびCD8+T細胞上の表面抗原CD25の発現を誘発した(図7)。CD4+およびCD8+T細胞へのこの効果は、CHO/短型CEA細胞クローン72−4および72−14の存在下で見られなかった。加えて、MEDI−565は、CEAの発現を欠失している親dhfr−CHO細胞で培養されたヒトCD4+および/またはCD8+T細胞を活性化しなかった。これらの結果は、MEDI−565が短型CEAタンパク質のみを発現する細胞に結合する、またはこのT細胞殺作用を媒介することができないことと一致した。
以下の結論は、実施例1〜5からもたらされ得る。完全長CEA転写物は、結腸、膵臓、胃食道、肺、および乳房癌において、広範に発現した。短型CEA転写物は、結腸癌において広範に、胃食道、肺、および乳房癌にわずかに、膵臓癌にまれに発現した。しかしながら、発現レベルおよび頻度は、異なるが、すべての組織試料中の短型CEA転写物の発現は、完全長CEA転写物の発現と一致した。
短型CEAを伴うCEAの発現を欠失している親dhfr−CHO細胞株の転写物により、短型CEAタンパク質を発現し、CEACAM5に対して特異的なMAbに結合した単一細胞クローンを得た。しかしながら、短型CEAタンパク質は、MEDI−565を有する同一のCEA結合部分を共有するIgG B9、マウスモノクローナル抗体によって、または2つの別個のモノクローナル汎CEA抗体(CD66a、c、d、e/CEACAM1、3、5、6およびCEACAM1,3,4,5,6)によって結合されなかった。この結果は、短型CEAタンパク質が、完全長CEAタンパク質に存在し、IgG B9によって認識される特異的エピトープを保持しないことを示す。予想されるように、MEDI−565は、CHO/短型CEA細胞(短型CEAタンパク質のみを発現するCHO細胞)のT細胞媒介殺作用を媒介せず、T細胞は、これらの細胞毒性アッセイにおいて活性化されなかった。これは、CHO/huCEA細胞のMEDI−565媒介殺作用と対照的に、同時T細胞活性化を支持する。
集合的に、本明細書に示される結果は、短型CEAの発現が、細胞表面上の完全長CEAへのMEDI−565の結合に干渉しないことを示唆している。さらに、短型CEAの存在は、CEAを発現する癌細胞のMEDI−565を媒介したT細胞殺作用を妨げない。
実施例6:欠失変異体を介したエピトープマッピング
702アミノ酸(aa)でコードされる完全長ヒトCEA前駆タンパク質は、34アミノ酸N末端シグナルペプチド(成熟タンパク質において除去される)、1つのIgV様Nドメイン、6つのIgC様ドメイン、および17アミノ酸C末端ペプチド(成熟タンパク質において除去される)からなる。完全長ヒトCEAの成熟タンパク質のアミノ酸配列は、配列番号2である。MEDI−565によって認識されるCEAのドメインを特定するために、CEA欠失変異体は、短縮型IgC様ドメインによって、改変された。IgC様ドメイン1−3(Del1−3、配列番号3)の欠失、IgC様ドメイン1(Del1、配列番号4)の欠失、IgC様ドメイン2(Del2、配列番号5)の欠失、IgC様ドメイン3(Del3、配列番号6)の欠失、およびIgC様ドメイン4−5(Del4−5、配列番号7)の欠失の、5つの欠失変異体が、図8に示されるように構築された。
欠失変異体は、テンプレートとして、組織内の完全長CEAクローンを用いて、重複伸長PCRを介して、増幅され、組み立てられた。完全長および欠失変異体はともに、ヒトサイトメガロウイルス主要前初期(hCMVie)エンハンサー、プロモーター、および5′非翻訳領域を有する哺乳動物発現ベクターにクローン化された。
欠失変異体は、293フェクチンを用いてHEK293F細胞への一過性トランスフェクションによって、膜結合型GPIアンカータンパク質として発現された。形質移入体は、MEDI−565、続いて、Alexa Fluor 488で標識された抗ペンタ−His抗体とともにインキュベートされ、次いで、LSRIIフローサイトメーターを用いた結合のためにスクリーニングされた。すべての構築物のタンパク質発現は、抗CEAポリクローナル抗体でモニタリングされた。
ドメイン欠失変異体を用いて、MEDI−565のエピトープを、CEAのIgC3ドメインにマッピングした。IgC3またはIgC1−3ドメインの欠失は、CEAへのMEDI−565の結合を妨害した(図8)。他の欠失変異体は、MEDI−565結合を保持した(例えば、MEDI−565結合は、IgC1、2、または4−5ドメインが欠失した場合、妨害されなかった)。さらに、IgC3ドメインをコードする短縮型CEAタンパク質(IgC3_GPI)、フランキングNドメインおよびGPI領域は、完全長CEAタンパク質に等しいMEDI−565結合を保持した(図9)。
実施例7:スワップ変異体を用いたエピトープマッピング
スワップ変異体は、CEAの第3のIgC様ドメイン(IgC3)の短セグメントを第5のIgC様ドメイン(IgC5)と交換して構築され、そのようなスワップ変異体が、MEDI−565結合に対して評価された。IgC5は、MEDI−565結合には関与しないが、IgC3との高度な相同性を共有するため、IgC3のそれぞれのセグメントをノックアウトする際に使用するために選択された(図9)。2つの短縮型CEAタンパク質は、スワップ変異体、IgC3_GPI(配列番号8)およびIgC5_GPI(配列番号9、図9)のテンプレートとして構築された。それぞれの構築物は、Nドメイン、IgC3またはIgC5ドメイン、GPI領域からなるが、これらの構築物は、他の5つのIgC様ドメインをコードしない(図9)。
IgC3およびIgC5ドメインは、約30アミノ酸からなる3つのセグメントに分割され、それぞれのセグメントは、セグメントA、B、およびCとして示された(図9)。「ノックアウト」変異体(KO)のために、IgC3_GPIは、IgC3のセグメントを、KO_A、KO_B、およびKO_Cを操作するIgC5の対応するセグメントで置き換えるテンプレートとして使用された(図9)。「ノックイン」変異体(KI)のために、IgC5_GPIは、IgC3セグメントを、KI_A、KI_B、KI_C、およびKI_A+Cを構築する、IgC5の対照物の代わりに接合した構造的テンプレートとして使用された(図9)。
スワップ変異体は、重複伸長PCRを用いて組み立てられ、一過性哺乳動物発現のヒトサイトメガロウイルス主要前初期(hCMVie)エンハンサー、プロモーター、および5′非翻訳領域をコードする哺乳動物発現ベクターにクローン化された。
スワップ変異体は、HEK293F細胞への一過性トランスフェクションによって膜結合型GPIアンカータンパク質として発現された。形質移入体は、MEDI−565、続いて、Alexa Fluor488で標識された抗ペンタ−Hisモノクローナル抗体とともにインキュベートされ、次いで、LSRIIフローサイトメーターを用いた結合のためにスクリーニングされた。すべての構築物のタンパク質発現は、抗CEAポリクローナル抗体でモニタリングされた。
IgC3ドメインの2つのセグメントは、MEDI−565結合にとって重要であることが見出された。IgC3_GPIのセグメントA(292−315)またはC(354−376)の対応するIgC5セグメントとの置換は、MEDI−565の結合を破壊した(セグメントの付番は、成熟完全長CEAタンパク質についてのものである)。常に、IgC5_GPIへのIgC3のセグメントAおよびCの両方の接合は、MEDI−565結合をもたらした。セグメントBは、結合に対する影響を及ぼさなかった。したがって、スワップ変異体を用いた試験は、MEDI−565が、セグメントA(残基292〜315)および残基C(354〜376)からなるCEAのIgC3ドメインにおいて、非直線状エピトープに結合することを示した。短型CEAの上記の分析からの明白であるように、このエピトープは、短型CEAタンパク質中に存在しない。
実施例8:部位特異的突然変異誘発法および計算ホモロジーモデリングを介したエピトープマッピング
部位特異的突然変異誘発法および計算ホモロジーモデリングを実行して、MEDI−565結合にとって重要であるCEAの残基を特定した。以下の残基が、セグメントAおよびセグメントCのIgC3エピトープ含有領域に限局されるため、およびこれらの残基が、IgC3とIgC5との間で異なるため、それらは、対応するIgC5アミノ酸:F292T294N299、N299E304、E304L309I315、V354G355P356E358、E364L365V367D368H369、およびI374N376(成熟タンパク質の付番)をコードするクラスターとして突然変異した。
CEAのIgC3ドメインのモデル構造は、SWISS−MODELワークスペースを用いたテンプレートとして、マウスCEACAM1A(33.7%の配列相同性)の結晶構造を用いて構築された(図10)。部位特異的突然変異誘発法およびモデル構造からの結果に基づいて、IgC3のN299のIgC5の対応する残基との置き換え(KO_N)、IgC3のV354G355P356E358およびI374N376のIgC5の対照物との置換(KO_VGPE+IN)、およびIgC3のF292T294N299、V354G355P356E358、およびI374N376のIgC5への接合(KI_FTN+VGPE+IN)である、3つのさらなる変異体が構築された。
すべての変異体は、テンプレートとして、短縮型CEAタンパク質のIgC3_GPIまたはIgC5_GPIを用いて、重複伸長PCRを用いて組み立てられた。様々な変異構築物は、一過性哺乳動物発現のヒトサイトメガロウイルス主要前初期(hCMVie)エンハンサー、プロモーター、および5′非翻訳領域をコードする哺乳動物発現ベクターにクローン化された。
変異体構築物は、HEK293F細胞への一過性トランスフェクションによってGPIアンカータンパク質として発現された。形質移入体は、MEDI−565、続いて、Alexa Fluor 488で標識された抗ペンタ−His Mabとともにインキュベートされ、次いで、LSRIIフローサイトメーターを用いて結合のためにスクリーニングされた。すべての構築物のタンパク質発現は、抗CEAポリクローナル抗体でモニタリングされた。
IgC3セグメントA中の残基F292T294N299が、IgC5の対応する残基で置き換えられた時、MEDI−565の結合は、妨害された(図10)(成熟タンパク質の付番)。特に、残基N299は、IgC3中の単一アミノ酸のノックアウトが、MEDI−565結合を破壊するため、臨界ホットスポット残基として特定された。
IgC3のセグメントC中の残基V354、G355、P356、E358、I374、およびN376はまた、MEDI−565結合にも関与する。IgC3のモデル構造は、セグメントAの必須残基N299に空間的に近いセグメントC中の残基の2つのクラスター(V354G355P356E358およびI374N376)を示す(図10)(成熟タンパク質の付番)。このモデルは、セグメントC中のこれらの残基が、MEDI−565結合に寄与し得ることを示唆した。実際に、これらの残基のノックアウトはともに、MEDI−565結合に大きな影響を及ぼした(が、完全に破壊しなかった)。最終的に、IgC5にセグメントCのアミノ酸V354G355P356E358およびI374N376を組み合わせた、セグメントAのアミノ酸F292T294N299の接合は、MEDI−565結合をもたらし、この結合のレベルは、セグメントAおよびCの両方を一緒にしたノックイン変異体のレベルに匹敵した(60アミノ酸残基をノックインした合計)(図10)。
以下の結論が、実施例6〜8からもたらされ得る。欠失およびスワップ変異体分析、部位特異的突然変異誘発法、および計算ホモロジーモデリングの組み合わせとともに、CEAの第3の免疫グロブリンC様ドメインにおいて、MEDI−565の非直線状、立体構造エピトープがマップされ、これらは、N299のホットスポット必須残基を有する、残基292〜315および354〜376の2つの領域からなる(成熟タンパク質の付番)。残基F292、T294、V354、G355、P356、E358、I374、およびN376はまた、MEDI−565の結合にとっても重要である(成熟タンパク質の付番)。このエピトープは、完全長CEAタンパク質に存在するが、短型CEAタンパク質(本明細書に記載のCEAスプライス変異体)には存在しない。CEAの残基の付番は、成熟タンパク質について示されることを留意されたい(例えば、残基の計数は、N末端プロ配列を含まない)。しかしながら、これらの残基はまた、例えば、実施例8に示される残基付番に34を加えることによって、プロタンパク質(例えば、残基の計数は、N末端プロ配列を含む)に関して特定することもできる。
実施例9:CEA多型の検討
他の起こり得るCEA変異体を特定するために、アミノ酸多型が、NCBI単一ヌクレオチド多型(SNP)データベース(http://www.ncbi.nlm.nih.gov/projects/SNP/)を用いて調査された。10個の個々の非同義コード多型が、下表に示されるように、完全長CEAタンパク質において特定された。
2つの非同義コードSNP(rs10407503、rs7249230)が、MEDI−565結合エピトープ領域において、特定された。rs10407503における、CからAへの単一ヌクレオチドの変化は、成熟完全長CEAのアミノ酸位置306で、アラニン(AlaまたはA)からアスパラギン酸(AspまたはD)へのアミノ酸変化をもたらした。rs7249230における、AからGへの単一ヌクレオチドの変化は、成熟完全長CEAのアミノ酸位置364で、リシン(LysまたはK)からグルタミン酸(GluまたはE)へのアミノ酸変化をもたらした。
SNPデータベースによれば、集団の平均ヘテロ接合性は、rs10407503およびrs7249230に対して、それぞれ、0.141および0.168である。しかしながら、rs10407503に対するマイナーアレルホモ接合体の比率は、ヨーロッパ人およびアジア人ともほぼ0であり、サハラ以南のアフリカ人集団では、0.08である。rs7249230に対するマイナーアレルホモ接合体の比率は、異なる集団において、0から0.03であった。両方のSNPのホモ接合体の比率が、非常に低く、それらがMEDI−565結合に関与する必須残基に影響を及ぼさないため、CEAへのMEDI−565の結合において、これらのSNPの影響がほとんどないと見込んでいる。
実施例10:抗CEA癌療法に対する感受性の判定
CEAを発現する癌を患っている患者は、抗CEA癌治療に対する感受性の試験を受ける資格がある。癌治療薬は、試験に対して選択される。癌治療薬は、完全長型のCEAタンパク質(細胞表面および分泌された完全長CEAタンパク質)、標的CEAに免疫特異的に結合するが、短型のCEAタンパク質(本実施例では、非標的CEA)には免疫特異的に結合しない。試料、例えば、血液試料が、患者から採取され、標的CEAタンパク質に特異的なELISAアッセイで分析されて、他の非標的型のCEAタンパク質の濃度を検出することなく、標的CEAタンパク質の濃度を判定する。標的CEAタンパク質の濃度を、健常な対象からの試料中の標的CEAタンパク質濃度を反映する標準範囲と比較する。標的CEAタンパク質濃度が、標準範囲を超える場合、この患者は、標的CEAタンパク質に免疫特異的に結合する癌治療薬に対して感受性がある。任意に、他のパラメーターもまた、評価されて、癌治療プロトコルが、患者に対して有益であるかどうかを判定する。
あるいは、または加えて、試料、例えば、血液試料が、患者から採取され、完全長および/または短型CEAタンパク質をコードするRNAを検出するための方法で分析される。標的CEAのRNAの濃度を、健常な対象からの試料中の標的CEAのRNA濃度を反映する標準範囲と比較する。標的CEAのRNA濃度が、標準範囲を超える場合、この患者は、標的CEAタンパク質に免疫特異的に結合する癌治療薬に対して感受性がある。任意に、他のパラメーターもまた、評価されて、癌治療プロトコルが、患者に対して有益であるかどうかを判定する。
癌を患っている対象は、本出願に記載される特異型のCEAに対して標的にされたある種の療法に対して感受性があることが予想される。
標的CEAタンパク質に免疫特異的に結合する癌治療薬に対して感受性があると判定された患者の診断用モニタリングは、治療後の様々な期間で(特定の治療後あるいは全レジメンの締結後のいずれか)、標的CEA濃度および/またはCEAのRNA濃度の検出に基づいた診断方法を用いるものである。例えば、診断用モニタリングは、標的CEAに免疫特異的に結合する抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いるものである。ある実施形態において、診断用抗体、抗原結合フラグメント、または免疫グロブリン様分子は、癌治療薬として、標的CEA上の同一または実質的に同一のエピトープに免疫特異的に結合する。
特定型のCEAを発現する癌に応じて、標的CEA濃度は、他の流体の試料を採取することによってモニタリングすることができる。例えば、特に、結腸癌および直腸癌については、治療前、治療中、および/または治療後に、血液または糞便試料を採取し、使用して、CEA濃度をモニタリングすることができる。さらなる例として、肺癌については、痰試料を、同様に使用することができる。
実施例11:完全長CEAに対する特異性
MEDI−565結合にとって重要な完全長CEAのアミノ酸は、大部分は、セグメントCのアミノ酸I408およびN410を除いて、CEAスプライス変異体に存在しないことが見出される(図2、シグナル配列を含むタンパク質に対して示される、これらの残基は、成熟タンパク質に対してのみ計数される場合、I374およびN376に対応することを留意されたい)。実際には、ノックアウト(KO_A)およびノックイン(KI_C)変異体は、エピトープマッピングに対して構築され、これは、セグメントC(アミノ酸I408およびN410を含有する)を有するが、Aの欠失(残基N333を含有する)(完全長CEAタンパク質の付番)は、MEDI−565によって認識されなかった(図9)。この観察は、CEAスプライス変異体へのMEDI−565の結合が、生じる可能性が低いことを示唆した。この仮説を試験するために、CHO細胞は、完全長CEA(CHO FL CEA)もしくはCEAスプライス変異体(CHO SV CEA)、または順次に両方(CHO FL+SV CEA)の発現を誘導するレンチウイルス構築物で感染され、CEAタンパク質発現は、ウエスタンブロット法によって検証された(データは示されず)。予想されたように、MEDI−565は、完全長CEAを発現する細胞に結合するが、CEAスプライス変異体を発現する細胞には結合しない(図11A)。Zhouらは、IgV様ドメインおよびIgC5は、併置する細胞表面上で同種親和性CEA相互作用を媒介し、両方のドメインは、CEAスプライス変異体内に存在することを示した。したがって、CEAスプライス変異体(短型)および完全長CEAタンパク質の同時発現が、同種親和性相互作用を通して、完全長型においてマスクされるMEDI−565結合エピトープをもたらし、続いて、完全長CEAへのMEDI−565結合を妨げる可能性があるという仮説を試験することを望んだ。同一の細胞上のCEAスプライス変異体(短型)と完全長CEAの同時発現は、完全長CEAに対するMEDI−565の結合親和性に有意に影響を及ぼさなかった(CHO FL CEA、KD=5.0±0.15nM、CHO FL+SV CEA、KD=5.6±3.0nM;p=0.86)。同種親和性相互作用は、MEDI−565結合を阻止するようには見なされない。
MEDI−565結合データと一致して、CHO SV CEAは、健常なドナーからのT細胞の活性化を媒介せず、また、MEDI−565で培養された時、CHO SV CEA細胞を溶解するように誘発されるヒトT細胞を刺激しなかった(図11)。対照的に、MEDI−565は、T細胞で活性化し、同様の活性レベル(EC50値)で、CHO FL CEAまたはCHO FL+SV CEA細胞の殺作用を誘発した;CHO FL CEA、EC50=75±35ng/mL;CHO FL+SV CEA、EC50=59±43ng/mL;p=0.79。MEDI−565は、CEAスプライス変異体に結合しないため、CEAスプライス変異体および完全長CEAの同時発現は、完全長CEAへのMEDI−565結合に干渉せず、また、完全長CEAを発現する癌細胞のMEDI−565を媒介したT細胞殺作用を阻害しないことが予想される。しかしながら、完全長CEAとCEAスプライス変異体の区別は、MEDI−565療法を受けている患者における、血清CEAレベルの変化によってCEA陽性腫瘍細胞の状態をモニタリングする際に、重要であり得る。
実施例12:CEAを発現する癌の治療
CEAを発現する癌を患っている患者は、治療を受ける資格がある。任意に、患者は、実施例10に示されるように、標的CEAタンパク質に免疫特異的に結合する癌治療薬に対して感受性があることを示している。試料、例えば、血液試料が、患者から採取され、標的CEAタンパク質、完全長CEAに対して特異的なELISAアッセイを用いて分析されて、他の非標的型のCEAタンパク質の濃度を検出することなく、標的CEAタンパク質の濃度を判定する。あるいは、試料、例えば、血液試料が、患者から採取され、完全長および/または短型CEAをコードするRNAの濃度を分析する。
患者は、標的CEAタンパク質に免疫特異的に結合する癌治療薬、MEDI−565で治療される。任意に、CEA発現に対して特異的ではない、外科手術、化学療法、および放射線療法等の治療法を含む、治療法の組み合わせが、治療において使用される。治療後の血液試料は、患者から採取され、他の非標的型のCEAタンパク質の濃度を検出することなく、標的CEAタンパク質の濃度について試験される。標的CEAタンパク質の濃度は、同一の患者からの治療前の標的CEAタンパク質濃度と比較される。
標的CEAタンパク質濃度の変化は、療法の有効性を示すことが期待される。
標的CEAタンパク質に免疫特異的に結合する癌治療薬に対して感受性があると判定された患者の診断用モニタリングは、治療後の様々な期間で(特定の治療後あるいは全レジメンの締結後のいずれか)、標的CEA濃度の検出に基づいた診断方法を用いるものである。例えば、診断用モニタリングは、標的CEAに免疫特異的に結合する抗体、抗原結合フラグメント、または免疫グロブリン様分子を用いるものである。ある実施形態において、診断用抗体、抗原結合フラグメント、または免疫グロブリン様分子は、癌治療薬として、標的CEA上の同一または実質的に同一のエピトープに免疫特異的に結合する。
特定型のCEAを発現する癌に応じて、標的CEA濃度は、他の流体の試料を採取することによってモニタリングすることができる。例えば、特に、結腸癌および直腸癌については、治療前、治療中、および/または治療後に、血液 糞便試料を採取し、使用して、CEA濃度をモニタリングすることができる。さらなる例として、肺癌については、痰試料を、同様に使用することができる。
配列
配列番号1−短型ヒトCEA(プロ配列を含む)
太字および下線を引いた位置が、多型を示すため、その位置での残基は、EあるいはKのいずれか(両方ではない)であり得ることに留意されたい。
太字および下線を引いた位置が、多型を示すため、その位置での残基は、EあるいはKのいずれか(両方ではない)であり得ることに留意されたい。
太字および下線を引いた位置が、多型を示すため、その位置での残基は、EあるいはKのいずれか(両方ではない)であり得ることに留意されたい。
参照による引用
本明細書で言及されるすべての刊行物および特許は、あたかも個々の刊行物または特許出願書が具体的かつ個別に示され、参照することにより組み込まれているかのように、参照することによりその全体が本明細書に組み込まれる。
対象開示の特定の実施形態が論じられているが、上の明細書は、例示的なものであり、限定されるものではない。本開示の多くの変形は、本明細書および以下の特許請求の範囲の概説の際、当業者には明らかであろう。本開示の全範囲は、特許請求の範囲をそれらの同等物の全範囲と共に、および本明細書をそのような変形と共に参照することにより決定されるべきである。