JP2011524908A - 溶液処理可能な有機半導体 - Google Patents
溶液処理可能な有機半導体 Download PDFInfo
- Publication number
- JP2011524908A JP2011524908A JP2011514647A JP2011514647A JP2011524908A JP 2011524908 A JP2011524908 A JP 2011524908A JP 2011514647 A JP2011514647 A JP 2011514647A JP 2011514647 A JP2011514647 A JP 2011514647A JP 2011524908 A JP2011524908 A JP 2011524908A
- Authority
- JP
- Japan
- Prior art keywords
- semiconductor
- layer
- alkyl
- formula
- alkenyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic System
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/40—Organosilicon compounds, e.g. TIPS pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K10/00—Organic devices specially adapted for rectifying, amplifying, oscillating or switching; Organic capacitors or resistors having a potential-jump barrier or a surface barrier
- H10K10/40—Organic transistors
- H10K10/46—Field-effect transistors, e.g. organic thin-film transistors [OTFT]
- H10K10/462—Insulated gate field-effect transistors [IGFETs]
- H10K10/464—Lateral top-gate IGFETs comprising only a single gate
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K10/00—Organic devices specially adapted for rectifying, amplifying, oscillating or switching; Organic capacitors or resistors having a potential-jump barrier or a surface barrier
- H10K10/40—Organic transistors
- H10K10/46—Field-effect transistors, e.g. organic thin-film transistors [OTFT]
- H10K10/462—Insulated gate field-effect transistors [IGFETs]
- H10K10/466—Lateral bottom-gate IGFETs comprising only a single gate
Abstract
Description
トリイソプロピルシリルアセチレン(12.32g、67.5mmol)及び乾燥ヘキサン(140mL)を、オーブンで乾燥させた丸底フラスコ(1L)に乾燥窒素雰囲気下で添加した。ブチルリチウム(ヘキサン中2.7M、14.5mL、39.2mmol)を、乾燥窒素下で、シリンジを通して混合物に滴加した。混合物を室温で2時間攪拌した。この無色の溶液に、乾燥THF(300mL)及び2,6−ジブロモアントラキノン(5.49g、15.0mmol)を乾燥窒素下で添加した。溶液は即座に赤色になり、数分で2,6−ジブロモアントラキノン(dibromoanthraquininone)が溶解した。混合物を室温で一晩攪拌すると、溶液は暗赤色になった。脱イオン(DI)水(6.0mL)を添加すると、色が薄赤色に変化し、白色沈殿が生じた。次いで、塩化スズ(II)(8.088g、42.6mmol)のHCl(18mL、10%)水溶液を添加した。混合物を60℃に2時間加熱し、次に室温まで冷却した。溶媒を回転蒸発により除去した。DI水(100mL)を混合物に添加し、次いでヘキサン(100mL×3)で抽出した。中性になるまで、ヘキサン溶液をDI水で洗浄した。カラムクロマトグラフィー(シリカゲル/ヘキサン)を通して濃縮及び精製した。生成物として鮮黄色の固体(8.55g、収率:82%)を得た。
予備例1の、2,6−ジブロモ−9,10−ビス−[(トリイソプロピルシリル)エチニル]アントラセン(5.225g、7.5mmol)、ビス(ピナコラト)ジボロン(4.763g、18.8mmol)、KOAc(2.940g、30.0mmol)、及びCHCl3(100mL)を、乾燥窒素下で250mLのフラスコに充填した。KOAcを懸濁した黄色溶液を得た。懸濁液を脱気し、微量の酸素を除去した。次いで[1,1’−ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(0.205g)を乾燥窒素下で添加した。溶液は橙色になった。混合物を70℃で3日間攪拌した後、室温まで冷却した。DI水(100mL×3)で洗浄し、MgSO4上で乾燥させた。溶媒を回転蒸発により除去した。固体残渣をカラムクロマトグラフィー(シリカゲル、CHCl3)により精製し、酢酸エチルから再結晶化した。生成物として橙色の針状結晶を得た(3.20g、収率55%)。
250mLのシュレンクフラスコに、2,6−ビス−(4,4,5,5−テトラメチル−1,3,2−ジオキサボロラン−2−イル)−9,10−ビス−[(トリイソプロピルシリル)エチニル]アントラセン(1.266g、1.60mmol)、4−ブロモアニソール(0.748g、4.00mmol)、炭酸ナトリウム(0.848g、8.00mmol)、ALIQUAT 336(0.072g、[CH3(CH2)9]3NCH3 +Cl−及び[CH3(CH2)7]3NCH3 +Cl−の混合物、相間移動触媒として使用する)、蒸留水(25mL)、及びトルエン(100mL)を充填した。混合物をシュレンクラインを用いて窒素下で脱気して、酸素を除去した。次いで、テトラキス(トリフェニルホスフィン)パラジウム(0)(0.024g、0.02mmol)を、窒素流下で添加した。脱気後もう一度、混合物を90℃にて窒素下で撹拌した。上方有機層は緑色がかった橙色に変化し、下方水層は無色であった。90℃で20時間撹拌した後、混合物を室温まで冷却した。少量の不溶性黒色固体をろ去した。暗緑色のトルエン溶液を、回転蒸発により約15mLまで濃縮し、次いでMeOH(100mL)でクエンチした。橙色固体(1.13g)をろ過により回収した。それを領域昇華により精製した。真空は1.1×10−6Torrであり、供給源領域温度は260℃であり、中心領域温度は200℃であった。綺麗な赤色/橙色結晶(1.0)を生成物として得た。
250mLのシュレンクフラスコに、2,6−ビス−(4,4,5,5−テトラメチル−1,3,2−ジオキサボロラン−2−イル)−9,10−ビス−[(トリイソプロピルシリル)エチニル]アントラセン(1.266g、1.60mmol)、2−ブロモ−6−メトキシアントラセン(0.949g、4.00mmol)、炭酸ナトリウム(0.848g、8.00mmol)、ALIQUAT 336(0.072g、[CH3(CH2)9]3NCH3 +Cl−及び[CH3(CH2)7]3NCH3 +Cl−の混合物、相間移動触媒として使用する)、蒸留水(25mL)、及びトルエン(100mL)を充填する。混合物をシュレンクラインを用いて窒素下で3回脱気して、酸素を除去した。次いで、テトラキス(トリフェニルホスフィン)パラジウム(0)(0.024g、0.02mmol)を、窒素流下で添加した。脱気後もう一度、混合物を90℃にて窒素下で撹拌した。赤色上方有機層は約1時間で暗緑色に変化し、下方水層は無色であった。90℃で20時間撹拌した後、混合物を室温まで冷却した。少量の不溶性黒色固体をろ去した。暗緑色のトルエン溶液を、回転蒸発により約15mLまで濃縮し、次いでMeOH(100mL)でクエンチした。橙色固体(1.15g)をろ過により回収した。それを領域昇華により更に精製した。真空は3〜5×10−6Torrであり、供給源領域温度は300℃であり、中心領域温度は220℃であった。橙色固体(0.4g)を中心領域にて回収した。
実施例1にて合成されたB4MP−TIPS−Anの溶解度を、室温にて種々の溶媒中で測定した。この低分子半導体は、n−ブチルベンゼンに対して中程度の溶解度(約1.0重量%)を、並びにジクロロベンゼン(6.0重量%以上)及びキシレン(約3.5重量%)に対しては良好な溶解度を有していた。重量%は、溶液の総重量を基準にしている。
高濃度ドープされたSiウエハ(Si100、Silicon Valley Microelectronics,Inc.,Santa Clara,CA)を、1000rpmで30秒間のスピンコーティングにより1,1,1,3,3,3−ヘキサメチルジシラザン(HMDS)で前処理した。B4MP−TIPS−An及びポリスチレン(Mw=97400、Sigma Aldrich)を室温にてキシレンに溶解させ、それらの濃度を、組成物の総重量に基づいてぞれぞれ3.0重量%及び1.0重量%にした。次いで溶液をHMDS−処理された基材の一片にナイフコーティングした。風乾後、サンプルを空気中120℃にて30分間アニールした。金ソース/ドレイン電極(60nm厚さ)を2×10−6Torrの減圧下、熱蒸発法を用いてポリマーシャドーマスクを通してパターン付けした。Hewlett Packard半導体パラメータ分析機(モデル4145A、Hewlett Packard Corporation,Palo Alto,CAから入手可能)を使用して、ドレイン電圧(Vds)を−40Vに維持する一方、ゲート電圧(Vg)を+10V〜−40Vまで掃引することにより、薄膜トランジスタを周囲条件下で特性決定した。Id 1/2−Vgトレースへの線形フィットは、飽和移動度及び閾値電圧(Vt)の抽出を可能にした。Id−Vgトレースへの線形フィットは、電流オン/オフ比を算出できるようにした。ホール移動度μは、0.21cm2/Vsと算出され、閾値電圧は−8Vであり、オン/オフ比は6×104であった。
B4MP−TIPS−AnのTFTデバイスを実施例4に記載の手順にしたがって作製した。この実験にて使用される半導体溶液の組成は、総溶液重量に基づいて3.0重量%のB4MP−TIPS−An、2.0重量%のポリスチレン、及び95.0重量%のキシレンであった。16個のTFTデバイスをランダムに選択し、サンプルを作製直後にTFT特性を試験した。120℃に設定したエアオーブンにサンプルを入れた。これら16個のデバイスのTFT特性を3日間及び7日間経年させた後に再び測定した。これらの経年期間後、試験された16個のデバイスすべてが非常に良好に機能した。表1からわかるように、デバイスの移動度は3日間の経年後に元の値より約75%までわずかに低下し、空気中120℃にて7日間の経年後には約50%を維持した。驚くべきことに、オン/オフ比及びサブ閾値の傾きは、経年後に大きく改善した。平均して、移動度は0.079cm2/Vsから0.059cm2/Vsまで(3日間)及び0.039cm2/Vsまで(7日間)低下し、オン/オフ比は1.0×104から1.7×104まで(3日間)及び8.7×104まで(7日間)増大し、サブ閾値の傾きは、3.2V/decadeから1.4V/decadeまで(3日間)及び1.5V/decadeまで(7日間)低下し、これは経年後にデバイスがより速くオンになることを示す。
Claims (24)
- R3がアルコキシである、請求項2又は3に記載の化合物。
- それぞれのR2がアルキル又はアルケニルである、請求項1〜3のいずれか一項に記載の化合物。
- 前記組成物が、前記組成物の総重量に基づいて少なくとも0.1重量%の溶解した式(I)の低分子半導体を含む、請求項6に記載の組成物。
- 更に絶縁ポリマーを含む、請求項6〜8のいずれか一項に記載の組成物。
- 前記絶縁ポリマーが、ポリスチレン、ポリ(α−メチルスチレン)、ポリ(メチルメタクリレート)、ポリ(ビニルフェノール)、ポリ(ビニルアルコール)、ポリ(ビニルアセテート)、ポリ(塩化ビニル)、ポリ(ビニリデンフルオライド)、シアノエチルプルラン、又はポリ(ジビニルテトラメチルジシロキサン−ビス(ベンゾシクロブテン))を含む、請求項9に記載の組成物。
- 前記有機溶媒が、(a)非置換であるか又は少なくとも1つのアルキル基で置換されているベンゼン、(b)少なくとも1つのハロ基で置換されているアルカン、(c)少なくとも1つのハロ基で置換されているベンゼン、(d)ケトン、(e)エーテル、(f)アミド、(g)アルカン、又は(h)これらの混合物を含む、請求項6〜10のいずれか一項に記載の組成物。
- 前記半導体層が更に絶縁ポリマーを含む、請求項12に記載の半導体デバイス。
- 導電層、誘電体層、又はこれらの組み合わせを、前記半導体層に隣接させて更に含む、請求項12又は13に記載の半導体デバイス。
- 前記半導体層の1つの表面に隣接した導電層及び前記半導体層の反対側の表面に隣接した誘電体層を更に含む、請求項12〜14のいずれか一項に記載の半導体デバイス。
- 互いに分離されかつ両方が前記半導体層と接触しているソース電極及びドレイン電極を含んでなる電極層を更に含む、請求項12〜15のいずれか一項に記載の半導体デバイス。
- 前記半導体デバイスが、有機薄膜トランジスタを含む、請求項12〜16のいずれか一項に記載の半導体デバイス。
- 半導体デバイスを製造する方法であって、前記方法が、式(I)の低分子半導体を含む半導体層を提供することであって、
R1はフェニル又はナフチルであり、前記フェニル又はナフチルは、非置換であるか、又はハロゲン、ヒドロキシル、アミノ、アルキル、アルケニル、アルコキシ、アシルオキシ、ヘテロアリール、ヘテロアルキル又はヘテロアラルキルから選択される1つ以上の置換基で置換され、
それぞれのR2は独立して、アルキル、アルケニル、アルコキシ、アリール、ヘテロアリール、アラルキル、ヘテロアルキル、ヘテロアラルキル、又はヒドロキシアルキルである、半導体層を提供すること、を含む、半導体デバイスを製造する方法。 - 前記半導体層が更に絶縁ポリマーを含む、請求項18に記載の方法。
- 前記半導体層に隣接する第1の層を提供することを更に含み、前記第1の層が導電層又は誘電体層を含む、請求項18又は19に記載の方法。
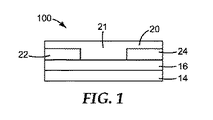
- 前記半導体デバイスが、
ゲート電極、
ゲート誘電体層、
前記半導体層、並びに
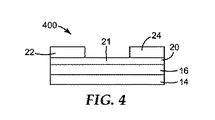
ソース電極及びドレイン電極を含む電極層であって、前記ソース電極及び前記ドレイン電極が互いに分離されており、かつ前記半導体層が前記ドレイン電極及び前記ソース電極の両方と接触している電極層、の順番で配置された多層を含む有機薄膜トランジスタを含む、請求項18〜20のいずれか一項に記載の方法。 - 前記半導体デバイスが、
ゲート電極、
ゲート誘電体層、
ソース電極及びドレイン電極を含む電極層であって、前記ソース電極及び前記ドレイン電極が互いに分離された電極層、並びに
前記ソース電極及び前記ドレイン電極の両方と接触している前記半導体層、の順番で配置された多層を含む有機薄膜トランジスタを含む、請求項18〜20のいずれか一項に記載の方法。 - 前記半導体層を提供することが、組成物を前記半導体デバイスの別の層の表面に適用することを含み、前記組成物が、式(I)の低分子半導体及び前記低分子半導体の少なくとも一部を溶解する有機溶媒を含む、請求項18〜22のいずれか一項に記載の方法。
- 前記方法が、前記組成物の適用後に、前記有機溶媒の少なくとも一部を除去することを更に含む、請求項23に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US7400208P | 2008-06-19 | 2008-06-19 | |
| US61/074,002 | 2008-06-19 | ||
| PCT/US2009/041904 WO2009154877A1 (en) | 2008-06-19 | 2009-04-28 | Solution processable organic semiconductors |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2011524908A true JP2011524908A (ja) | 2011-09-08 |
| JP2011524908A5 JP2011524908A5 (ja) | 2012-06-14 |
Family
ID=40756318
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011514647A Pending JP2011524908A (ja) | 2008-06-19 | 2009-04-28 | 溶液処理可能な有機半導体 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20110079775A1 (ja) |
| EP (1) | EP2318420A1 (ja) |
| JP (1) | JP2011524908A (ja) |
| CN (1) | CN102119164A (ja) |
| WO (1) | WO2009154877A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009079150A1 (en) * | 2007-12-17 | 2009-06-25 | 3M Innovative Properties Company | Solution processable organic semiconductors based on anthracene |
| CN102106012B (zh) * | 2008-06-11 | 2013-05-29 | 3M创新有限公司 | 用于沉积有机半导体的混合溶剂体系 |
| KR20100075100A (ko) * | 2008-12-24 | 2010-07-02 | 서울대학교산학협력단 | 잉크젯 프린팅 방법을 이용한 유기 전계효과 트랜지스터의 활성 채널층 형성방법 및 이를 이용한 유기 전계효과 트랜지스터 |
| CN103380503B (zh) * | 2011-02-19 | 2017-07-28 | 阿联酋大学 | 半导体聚合物 |
| WO2012123058A1 (en) * | 2011-03-11 | 2012-09-20 | Merck Patent Gmbh | Dinaphtho[2,3-a:2',3'-h]phenazines and their use as organic semiconductors |
| CN102637825B (zh) * | 2012-04-24 | 2015-03-04 | 中国科学院苏州纳米技术与纳米仿生研究所 | 一种有机薄膜晶体管的制备方法 |
| CN107628924A (zh) * | 2017-09-25 | 2018-01-26 | 中国科学院化学研究所 | 一种蒽类衍生物及其制备方法与应用 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006050496A1 (en) * | 2004-11-02 | 2006-05-11 | E.I. Dupont De Nemours And Company | Substituted anthracenes and electronic devices containing the substituted anthracenes |
| JP2007088115A (ja) * | 2005-09-21 | 2007-04-05 | Konica Minolta Holdings Inc | 有機半導体材料,有機半導体膜,有機半導体デバイス及び有機薄膜トランジスタ |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6433359B1 (en) * | 2001-09-06 | 2002-08-13 | 3M Innovative Properties Company | Surface modifying layers for organic thin film transistors |
| US6998068B2 (en) * | 2003-08-15 | 2006-02-14 | 3M Innovative Properties Company | Acene-thiophene semiconductors |
| US6617609B2 (en) * | 2001-11-05 | 2003-09-09 | 3M Innovative Properties Company | Organic thin film transistor with siloxane polymer interface |
| US6946676B2 (en) * | 2001-11-05 | 2005-09-20 | 3M Innovative Properties Company | Organic thin film transistor with polymeric interface |
| US20030227014A1 (en) * | 2002-06-11 | 2003-12-11 | Xerox Corporation. | Process for forming semiconductor layer of micro-and nano-electronic devices |
| ES2387304T3 (es) * | 2003-10-28 | 2012-09-20 | Basf Se | Nuevos polímeros de dicetopirrolopirrol |
| EP1808866A1 (en) * | 2003-11-28 | 2007-07-18 | Merck Patent GmbH | Organic semiconducting layer formulations comprising polyacenes and organic binder polymers |
| JP4984891B2 (ja) * | 2004-07-02 | 2012-07-25 | Jnc株式会社 | 発光材料およびこれを用いた有機電界発光素子 |
| CN102174296A (zh) * | 2005-07-05 | 2011-09-07 | 日立化成工业株式会社 | 粘接剂组合物、薄膜、薄片、半导体晶圆、半导体装置 |
| KR101215758B1 (ko) * | 2006-01-17 | 2012-12-26 | 삼성전자주식회사 | Npn-타입의 저분자 방향족 고리 화합물, 이를 이용한유기 반도체 및 전자 소자 |
| US7667230B2 (en) * | 2006-03-31 | 2010-02-23 | 3M Innovative Properties Company | Electronic devices containing acene-thiophene copolymers |
| US7495251B2 (en) * | 2006-04-21 | 2009-02-24 | 3M Innovative Properties Company | Electronic devices containing acene-thiophene copolymers with silylethynyl groups |
| JP4781434B2 (ja) * | 2006-08-03 | 2011-09-28 | 旭化成イーマテリアルズ株式会社 | 感光性樹脂組成物及び積層体 |
| EP2132213B1 (en) * | 2007-03-07 | 2013-05-15 | University of Kentucky Research Foundation | Silylethynylated heteroacenes and electronic devices made therewith |
| WO2008120839A1 (en) * | 2007-03-30 | 2008-10-09 | Gyeongsang National University Industrial And Academic Collaboration Foundation | Novel organic semiconductor compound, and organic thin film transistor using the same |
| JP5524043B2 (ja) * | 2007-04-19 | 2014-06-18 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 置換されたペンタセン類の調製方法 |
| JP5603233B2 (ja) * | 2007-05-17 | 2014-10-08 | エルジー・ケム・リミテッド | 新規なアントラセン誘導体およびそれを用いた有機電子素子 |
| CN101918512B (zh) * | 2007-06-01 | 2014-09-24 | E.I.内穆尔杜邦公司 | 绿色发光材料 |
| WO2009079150A1 (en) * | 2007-12-17 | 2009-06-25 | 3M Innovative Properties Company | Solution processable organic semiconductors based on anthracene |
-
2009
- 2009-04-28 EP EP09767189A patent/EP2318420A1/en not_active Withdrawn
- 2009-04-28 CN CN2009801310799A patent/CN102119164A/zh active Pending
- 2009-04-28 WO PCT/US2009/041904 patent/WO2009154877A1/en active Application Filing
- 2009-04-28 JP JP2011514647A patent/JP2011524908A/ja active Pending
- 2009-04-28 US US12/994,898 patent/US20110079775A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006050496A1 (en) * | 2004-11-02 | 2006-05-11 | E.I. Dupont De Nemours And Company | Substituted anthracenes and electronic devices containing the substituted anthracenes |
| JP2007088115A (ja) * | 2005-09-21 | 2007-04-05 | Konica Minolta Holdings Inc | 有機半導体材料,有機半導体膜,有機半導体デバイス及び有機薄膜トランジスタ |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102119164A (zh) | 2011-07-06 |
| US20110079775A1 (en) | 2011-04-07 |
| WO2009154877A1 (en) | 2009-12-23 |
| EP2318420A1 (en) | 2011-05-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8178873B2 (en) | Solution processable organic semiconductors | |
| JP5454139B2 (ja) | カーボンナノチューブ複合体、有機半導体コンポジットならびに電界効果型トランジスタ | |
| US7319153B2 (en) | 6,13-Bis(thienyl)pentacene compounds | |
| DK2715818T3 (en) | Organic semiconductor compositions | |
| JP2011524908A (ja) | 溶液処理可能な有機半導体 | |
| TWI549327B (zh) | 有機場效電晶體及有機半導體材料 | |
| JP5123289B2 (ja) | シリルエチニル基を有するアセン−チオフェンコポリマー | |
| KR20150135792A (ko) | 방향족 복소환 화합물, 그 제조방법, 유기 반도체 재료 및 유기 반도체 디바이스 | |
| KR20070100174A (ko) | 폴리(알키닐티오펜) 및 이로부터 제조된 전자 디바이스 | |
| JP2015199716A (ja) | 多環縮環化合物、有機半導体材料、有機半導体デバイス及び有機トランジスタ | |
| US8546796B2 (en) | Semiconductor device, method of manufacturing the same, and method of forming multilayer semiconductor thin film | |
| CN110326122B (zh) | 有机晶体管 | |
| KR20130087424A (ko) | 이소티오인디고계 폴리머 | |
| JP4380261B2 (ja) | 高分子の製造方法 | |
| TWI688135B (zh) | 有機半導體元件、化合物、有機半導體組成物以及有機半導體膜及其製造方法 | |
| KR102114805B1 (ko) | 유기 트랜지스터용 유기 반도체 재료 및 유기 트랜지스터 소자 | |
| KR101831858B1 (ko) | 반도체 조성물 | |
| KR100865703B1 (ko) | 아릴아세틸렌 구조의 유기반도체 화합물 및 이를 이용한유기박막트랜지스터 | |
| CN111808270A (zh) | 半导体组合物及其应用 | |
| KR20130087423A (ko) | 디티오이소인디고계 폴리머 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120425 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120425 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130826 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130903 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140408 |