JP2010080229A - 電極及び電池 - Google Patents
電極及び電池 Download PDFInfo
- Publication number
- JP2010080229A JP2010080229A JP2008246493A JP2008246493A JP2010080229A JP 2010080229 A JP2010080229 A JP 2010080229A JP 2008246493 A JP2008246493 A JP 2008246493A JP 2008246493 A JP2008246493 A JP 2008246493A JP 2010080229 A JP2010080229 A JP 2010080229A
- Authority
- JP
- Japan
- Prior art keywords
- group
- positive electrode
- negative electrode
- active material
- electrode active
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/60—Selection of substances as active materials, active masses, active liquids of organic compounds
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Materials Engineering (AREA)
- Secondary Cells (AREA)
- Battery Electrode And Active Subsutance (AREA)
Abstract
【解決手段】正極活物質の表面、又は該正極活物質層の少なくとも表面に、式(1)の塩を有する正極(Rは不飽和結合を有しても良い炭化水素基、あるいはこの炭化水素基をハロゲン化又はヒドロキシル化した基、又は水素基であり、該環にN又はOをさらに含んでも良い基、又は水素基であり、Aa−はR、R1、R2、及び前記環の少なくとも何れかに結合し得る酸アニオンであり、Mx+はAa−と塩を形成する金属イオン)、および負極集電体に設けられた負極活物質層を有する負極と共に電解液を備えた電池とする。
【選択図】なし
Description
1) 正極集電体に設けられた正極活物質層に含まれる活物質の表面、又は該正極活物質層の少なくとも表面に、式(1)の塩を有する正極。
2)正極および負極集電体に設けられた負極活物質層を有する負極と共に電解液を備えた電池であって、前記正極は、1)の正極である電池。
Rについて説明する。
Rは不飽和結合を有しても良い炭化水素基、あるいはこの炭化水素基をハロゲン化又はヒドロキシル化した基、又は水素基である。炭化水素基としては、炭素数1〜20の分岐、直鎖、又は環状の、アルキル基、アルケニル基、またはアルキニル基、炭素数6〜28のアリール基、アラルキル基が挙げられる。
上記各々のRは、ハロゲン化又はヒドロキシル化されて良く、両者が修飾されていてもよい。該ハロゲン原子としては、塩素、フッ素が好ましい。
R1、R2について説明する。
R1とR2は各々独立に不飽和結合、N又はOを有しても良い炭化水素基であって、お互いに結合して環を形成しても良く、該環にN又はOをさらに含んでも良い基、又は水素基である。炭化水素基としては、上記Rと同様のものが挙げられる。この炭化水素基は、Nを含む場合は、アミノ基を有するものが好ましく、Oを含む場合は、ヒドロキシル基を有するものが好ましい。
形成される環としては、3〜8員環が好ましく、飽和環が好ましい。該環の化合物としては、例えば、ピペリジン、ピペラジン、モルホリン、エチレンイミン、トリメチレンイミン、ヘキサメチレンイミン、オクトゲン、ピロール、イミダゾール、ピラゾール、オキサゾール、イソオキサゾール、ピリジン、ピラジン、チオモルホリン等が挙げられる。
Aa−とMx+について説明する。
Aa−はR、R1、R2、及び前記環の少なくとも何れかに結合し得る酸アニオンである。酸アニオンとしては、スルホン酸、カルボン酸、スルフィン酸、ホスホン酸、ホスフィン酸等の各アニオンが挙げられる。Mx+はAa−と塩を形成する金属イオンである。a、b、x、yは1以上の整数である。Aa−の上記置換基への結合位置は、特に限定されないが、鎖状部の末端、又は環上が好ましい。
bは、1〜6が好ましく、1〜4が更に好ましい。Mは、周期表の1族もしくは2族の金属であることが好ましい。従って、xは1または2が好ましい。
本発明の式(1)の塩は、例えば二次電池などの電気化学デバイスに用いられるものであり、アミノ基を含む金属塩である(以下、式(1)の塩を「金属塩」ともいう)。この金属塩が電気化学デバイスに用いられる場合には、例えば、正極や正極活物質などの固体の表面に被膜として形成されてもよいし、正極中に分散されていても良い。
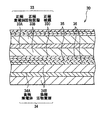
図1および図2は第1の二次電池の断面構成を表しており、図2では図1に示した巻回電極体20の一部を拡大して示している。
そして、正極活物質は金属塩の皮膜が設けられている。この被膜が正極活物質上に設けられているのは、正極の化学的安定性が向上し、それに伴って正極に隣接する電解液の化学的安定性も向上するからである。これにより、正極においてリチウムが効率よく吸蔵および放出されると共に、電解液の分解反応が抑制されるため、サイクル特性が向上する。
また、未処理の活物質を用い、圧縮形成して正極活物質層21Bを形成した後に、式(1)の塩の水溶液に浸漬または水溶液を塗布し、乾燥させ電極上に正極皮膜21Cを形成させることができる。
図3は第2の二次電池の分解斜視構成を表しており、図4は図3に示した巻回電極体30のVIII−VIII線に沿った断面を拡大して示している。
平均粒子径13μm(レーザー散乱法により測定)のリチウムコバルト複合酸化物(LiCo0.98Al0.01Mg0.01O2)100質量部に対して下記化aに示す化合物(式(1)の塩)を1質量部になるよう秤量し、100mlの純水中で5分攪拌した。攪拌後、エバポレーターにより水分を除去した後オーブンで120℃−12h乾燥しコバルト酸リチウムに化aに示す化合物を被覆処理した正極活物質を得た。
以上で得られた正極活物質を用い、以下に記すようにラミネート電池を作製し、サイクル特性および高温保存時のセル厚みを評価した。
リチウムコバルト複合酸化物91質量部と、導電剤としてグラファイト6質量部と、結着剤としてポリフッ化ビニリデン(PVdF)3質量部とを混合して正極合剤としたのち、N−メチル−2−ピロリドンに分散させてペースト状の正極合剤スラリーとした。続いて、バーコータによって帯状のアルミニウム箔(厚さ=12μm)からなる正極集電体33Aの両面に正極合剤スラリーを均一に塗布して乾燥させたのち、ロールプレス機によって圧縮成形して正極活物質層33Bを形成した。
負極は、次のようにして作製した。黒鉛粉末90質量%と、PVdF10質量%とを混合して負極合剤を調製した。この負極合剤をN−メチル−2−ピロリドンに分散させて負極合剤スラリーを作製した後、負極合剤スラリーを帯状銅箔よりなる負極集電体の両面に均一に塗布し、さらに、これを加熱プレス成型することにより、負極活物質層を形成した。
セパレーターは、次のようにして作製した。まず、ポリフッ化ビリデン樹脂(平均分子量150000)にN−メチル−2−ピロリドンを、質量比10:90で加え十分に溶解させ、PVdFのN−メチル−2−ピロリドン10質量%溶液を作製した。
次に、作製したスラリーを卓上コーターにて、基材層としての厚さ7μmのポリエチレン(PE)とポリプロピレン(PP)の混合体である微多孔膜上に塗布し、ついで水浴で相分離させた後、熱風にて乾燥し、厚さ4μmのPVdF微多孔層を有する微多孔膜を得た。
次に、セパレーターと正極と負極とを、負極、セパレーター、正極、セパレーターの順に積層し、多数回巻回し、発電素子を作製した。この発電素子と電解液を厚さ180μmの防湿性アルミラミネートフィルム外装中に入れた後、真空封止、熱圧着を行い、寸法およそ34mm×50mm×3.8mmである平板型ラミネート電池を作製した。
電解液はエチレンカーボネート(EC)とジエチルカーボネート(DEC)との体積混合比が1:1である混合溶液に1mol/dm3の濃度になるようにLiPF6を溶解して非水電解液を調製した。
実施例1−1において、該実施例の電解液に対して、表1の0.5%(質量基準)の電解液添加剤(ただし、FECは溶媒)を添加した以外は、同様にして非水電解液2次電池を作製した。
(実施例1−8〜実施例1−10)
実施例1−1において、式(1)の塩を下記化b、化c、または化dに変更した以外は、同様にして非水電解液2次電池を作製した。
(比較例1−1)
実施例1−1において、式(1)の塩を用いなかった以外は、同様にして非水電解液2次電池を作製した。
1)放電容量維持率
23℃の雰囲気中において2サイクル充放電させて放電容量を測定し、引き続き同雰囲気中においてサイクル数の合計が100サイクルとなるまで充放電させて放電容量を測定したのち、放電容量維持率(%)=(100サイクル目の放電容量/2サイクル目の放電容量)×100を算出した。この際、1サイクルの充放電条件としては、800mAの定電流密度で電池電圧が4.2Vに達するまで充電し、さらに4.2Vの定電圧で40mAに達するまで充電したのち、800mAの定電流密度で電池電圧が3Vに達するまで放電した。
2)12時間後の膨れ量
環境温度45℃、充電電圧4.20V、充電電流800mA、充電時間2.5時間の条件で充電を行った後、放電電流400mA、終止電圧3.0Vで放電を行った。セルを充電電圧4.2V、充電電流800mA、充電時間2.5時間の条件で充電を行った後、85℃で12時間保存を行い、保存前後でのセル厚みの増加量を測定し、12時間後の膨れ量とした。
以下の手順により、図3〜図5に示したラミネートフィルム型の二次電池を作製した。この際、負極34の容量がリチウムの吸蔵および放出に基づいて表されるリチウムイオン二次電池となるようにした。
実施例2−1において、該実施例の電解液に対して、表2の0.5%(質量基準)の電解液添加剤を添加した以外は、同様にして非水電解液2次電池を作製した。
(実施例2−6〜実施例2−8)
実施例2−1において、金属塩を上記化b、化c、または化dの金属塩に変更した以外は、同様にして非水電解液2次電池を作製した。
(比較例2−1)
実施例2−1において、金属塩を用いなかった以外は、同様にして非水電解液2次電池を作製した。
(比較例2−2)
比較例2−1において、該比較例の電解液に対して1%(質量基準)のテトラブチルアミンを添加した以外は、同様にして非水電解液2次電池を作製した。
1)放電容量維持率
23℃の雰囲気中において2サイクル充放電させて放電容量を測定し、引き続き同雰囲気中においてサイクル数の合計が100サイクルとなるまで充放電させて放電容量を測定したのち、放電容量維持率(%)=(100サイクル目の放電容量/2サイクル目の放電容量)×100を算出した。この際、1サイクルの充放電条件としては、1mA/cm2の定電流密度で電池電圧が4.2Vに達するまで充電し、さらに4.2Vの定電圧で電流密度が0.02mA/cm2に達するまで充電したのち、1mA/cm2の定電流密度で電池電圧が2.5Vに達するまで放電した。
2)4時間後の膨れ量
23℃の雰囲気中において2サイクル充放電させてから再び充電して厚さを測定し、引き続き充電状態のままで90℃の恒温槽中に4時間保存してから厚さを測定したのち、膨れ(mm)=(保存後の厚さ−保存前の厚さ)を算出した。この際、1サイクルの充放電条件としては、0.2Cの定電流で電池電圧が4.2Vに達するまで充電したのち、0.2Cの定電流で電池電圧が2.5Vに達するまで放電した。「0.2C」とは、理論容量を5時間で放電しきる電流値である。
負極活物質としてケイ素に代えて後述のSnCoC含有材料を用い、塗布法により負極活物質層52Bを形成すると共に、電解液における溶媒の組成を後述のように変更したことを除き、実施例2−1〜2−8、比較例2−1〜2−2と同様の手順を経て非水電解液2次電池を作製し、同様に評価した。詳細は以下の通りである。
得られた非水電解液2次電池の評価結果を表3に示した。なお、比較例3−2は、比較例3−1の電解液に対して1%(質量基準)のテトラブチルアミンを添加した以外は、同様にして非水電解液2次電池を作製した。
正極活物質として(LiCo0.98Al0.01Mg0.01O2)に代えてLiNi0.8Co0.2O2を用いたことを除き、実施例1−1、実施例1−8と同様の手順を経て非水電解液2次電池を作製し、同様に評価した(負極は実施例1−1等と同じである。)。
(実施例4−3〜4−6、比較例4−1〜4−2)
実施例4−1と同じ正極活物質を用い、粒子状の正極活物質の表面に金属塩の皮膜を形成する代わりに正極活物質層上に正極被膜33Cを形成したことを除き、実施例2−1、実施例2−6〜実施例2−8、比較例2−1〜2−2と同様の手順を経て非水電解液2次電池を作製し、同様に評価した(負極は実施例2−1等と同じである。また、膨れ量は、12時間保存に変更した)。実施例4−3は、実施例2−1に対応、実施例4−4〜実施例4−6は、実施例2−6〜実施例2−8に対応、比較例4−1〜4−2は、比較例2−1〜2−2に対応する。正極被膜33Cを形成する場合には、化a、化b、化c、または化dの3%水溶液を準備し、正極活物質層33Bが形成された正極集電体を水溶液中に数秒間浸漬させてから引き上げたのち、150℃の減圧環境中において乾燥させた。
評価結果を表4に示した。
Claims (14)
- 式(1)の塩は、三級アミンである請求項1の正極。
- Aa−は、SO3 −もしくはCO2 −である請求項1の正極。
- 式(1)のMは、周期表の1族もしくは2族の金属塩である請求項1の正極。
- 正極および負極集電体に設けられた負極活物質層を有する負極と共に電解液を備えた電池であって、前記正極は、請求項1の正極である電池。
- 負極活物質層は、ケイ素の単体、合金および化合物、ならびにスズの単体、合金および化合物のうちの少なくとも1種を含有する負極活物質を含む請求項5の電池。
- 請求項7の化2のハロゲンを有する鎖状炭酸エステルは、炭酸フルオロメチルメチル、炭酸ジフルオロメチルメチルおよび炭酸ビス(フルオロメチル)のうちの少なくとも1種であり、請求項7の化3のハロゲンを有する環状炭酸エステルは、4−フルオロ−1,3−ジオキソラン−2−オンおよび4,5−ジフルオロ−1,3−ジオキソラン−2−オンのうちの少なくとも1種である請求項5の電池。
- 電解液は、スルトンを含有する溶媒を含む請求項5の電池。
- 電解液は、酸無水物を含有する溶媒を含む請求項5の電池。
- 電解液は、六フッ化リン酸リチウム(LiPF6)、四フッ化ホウ酸リチウム(LiBF4)、過塩素酸リチウム(LiClO4)および六フッ化ヒ酸リチウム(LiAsF6)のうちの少なくとも1種を含有する電解質塩を含む請求項5の電池。
- 電解液は、化4〜化6の化合物のうちの少なくとも1種を含有する電解質塩を含む請求項5の電池。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008246493A JP4952693B2 (ja) | 2008-09-25 | 2008-09-25 | リチウムイオン二次電池用正極及びリチウムイオン二次電池 |
| KR1020090088120A KR20100035109A (ko) | 2008-09-25 | 2009-09-17 | 전지 및 전극 |
| US12/565,330 US20100075233A1 (en) | 2008-09-25 | 2009-09-23 | Battery and electrode |
| CN2009101761831A CN101685857B (zh) | 2008-09-25 | 2009-09-24 | 电池以及电极 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008246493A JP4952693B2 (ja) | 2008-09-25 | 2008-09-25 | リチウムイオン二次電池用正極及びリチウムイオン二次電池 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010080229A true JP2010080229A (ja) | 2010-04-08 |
| JP4952693B2 JP4952693B2 (ja) | 2012-06-13 |
Family
ID=42038006
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008246493A Expired - Fee Related JP4952693B2 (ja) | 2008-09-25 | 2008-09-25 | リチウムイオン二次電池用正極及びリチウムイオン二次電池 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US20100075233A1 (ja) |
| JP (1) | JP4952693B2 (ja) |
| KR (1) | KR20100035109A (ja) |
| CN (1) | CN101685857B (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9515350B2 (en) | 2013-02-15 | 2016-12-06 | Sony Corporation | Electrolytic solution, non-aqueous secondary battery, battery pack, electric vehicle, electric power storage system, electric power tool, and electronic apparatus |
| CN115706262A (zh) * | 2021-08-05 | 2023-02-17 | 株式会社村田制作所 | 一种电解液添加剂、包含其的电解液和锂离子二次电池以及其用途 |
| JP2024524799A (ja) * | 2022-05-20 | 2024-07-09 | 寧徳時代新能源科技股▲分▼有限公司 | 非水電解液及びそれを含む二次電池、電池モジュール、電池パック並びに電気装置 |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5446612B2 (ja) * | 2009-08-28 | 2014-03-19 | Tdk株式会社 | リチウムイオン二次電池 |
| WO2012102259A1 (ja) | 2011-01-25 | 2012-08-02 | 株式会社 村田製作所 | 非水電解液二次電池 |
| JP6287830B2 (ja) * | 2012-04-03 | 2018-03-07 | 株式会社Gsユアサ | 電池用正極及び電池 |
| CN104205444A (zh) * | 2012-04-03 | 2014-12-10 | 株式会社杰士汤浅国际 | 电池用正极糊剂 |
| US11177505B2 (en) * | 2017-01-03 | 2021-11-16 | Basf Se | Pyridine sulfur trioxide complexes as electrolyte component for high voltage batteries |
| CA3192359A1 (en) | 2020-08-18 | 2022-02-24 | Enviro Metals, LLC | Metal refinement |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08268998A (ja) * | 1995-03-06 | 1996-10-15 | Minnesota Mining & Mfg Co <3M> | フッ素化合物系電解質塩及びこれを含む電解質組成物並びにこれらを含んで成るバッテリー |
| JP2003192661A (ja) * | 2001-12-17 | 2003-07-09 | Three M Innovative Properties Co | 非水溶媒中におけるフルオロアルキルスルホニル基含有アルカリ金属塩の製造方法及びその使用方法 |
| JP2004071159A (ja) * | 2002-08-01 | 2004-03-04 | Central Glass Co Ltd | 非水電解質二次電池 |
| JP2004103433A (ja) * | 2002-09-10 | 2004-04-02 | Mitsubishi Chemicals Corp | 非水系電解液二次電池およびそれに用いる電解液 |
| JP2007005293A (ja) * | 2005-05-26 | 2007-01-11 | Sony Corp | 電解質および電池 |
| JP2008027837A (ja) * | 2006-07-25 | 2008-02-07 | Sony Corp | 電解質および電池 |
| JP2009110845A (ja) * | 2007-10-31 | 2009-05-21 | Sony Corp | 負極および電池 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2687671B1 (fr) * | 1992-02-21 | 1994-05-20 | Centre Nal Recherc Scientifique | Monomeres derives de sultones perhalogenees et polymeres obtenus a partir de ces monomeres. |
| JP3419119B2 (ja) * | 1994-11-15 | 2003-06-23 | 日本電池株式会社 | 非水電解質二次電池 |
| US5652072A (en) * | 1995-09-21 | 1997-07-29 | Minnesota Mining And Manufacturing Company | Battery containing bis(perfluoroalkylsulfonyl)imide and cyclic perfluoroalkylene disulfonylimide salts |
| DE69736970T2 (de) * | 1996-09-03 | 2007-09-13 | Ube Industries, Ltd., Ube | Nichtwässrige Lithium-Ion Sekundärbatterie |
| US6350545B2 (en) * | 1998-08-25 | 2002-02-26 | 3M Innovative Properties Company | Sulfonylimide compounds |
| JP4895335B2 (ja) * | 2001-03-23 | 2012-03-14 | 日立マクセルエナジー株式会社 | 非水電池 |
| WO2002076924A1 (en) * | 2001-03-26 | 2002-10-03 | Nisshinbo Industries, Inc., | Ionic liquid, electrolyte salt for storage device, electrolytic solution for storage device, electric double layer capacitor, and secondary battery |
| CN1215595C (zh) * | 2001-07-10 | 2005-08-17 | 三菱化学株式会社 | 非水系电解液和使用该电解液的蓄电池 |
| AU2003235119A1 (en) * | 2002-04-24 | 2003-11-10 | Nisshinbo Industries, Inc. | Ionic liquid, method of dehydration, electric double layer capacitor, and secondary battery |
| JP5229527B2 (ja) * | 2006-08-25 | 2013-07-03 | ソニー株式会社 | 二次電池用電解液および二次電池 |
-
2008
- 2008-09-25 JP JP2008246493A patent/JP4952693B2/ja not_active Expired - Fee Related
-
2009
- 2009-09-17 KR KR1020090088120A patent/KR20100035109A/ko not_active Withdrawn
- 2009-09-23 US US12/565,330 patent/US20100075233A1/en not_active Abandoned
- 2009-09-24 CN CN2009101761831A patent/CN101685857B/zh not_active Expired - Fee Related
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08268998A (ja) * | 1995-03-06 | 1996-10-15 | Minnesota Mining & Mfg Co <3M> | フッ素化合物系電解質塩及びこれを含む電解質組成物並びにこれらを含んで成るバッテリー |
| JP2003192661A (ja) * | 2001-12-17 | 2003-07-09 | Three M Innovative Properties Co | 非水溶媒中におけるフルオロアルキルスルホニル基含有アルカリ金属塩の製造方法及びその使用方法 |
| JP2004071159A (ja) * | 2002-08-01 | 2004-03-04 | Central Glass Co Ltd | 非水電解質二次電池 |
| JP2004103433A (ja) * | 2002-09-10 | 2004-04-02 | Mitsubishi Chemicals Corp | 非水系電解液二次電池およびそれに用いる電解液 |
| JP2007005293A (ja) * | 2005-05-26 | 2007-01-11 | Sony Corp | 電解質および電池 |
| JP2008027837A (ja) * | 2006-07-25 | 2008-02-07 | Sony Corp | 電解質および電池 |
| JP2009110845A (ja) * | 2007-10-31 | 2009-05-21 | Sony Corp | 負極および電池 |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9515350B2 (en) | 2013-02-15 | 2016-12-06 | Sony Corporation | Electrolytic solution, non-aqueous secondary battery, battery pack, electric vehicle, electric power storage system, electric power tool, and electronic apparatus |
| CN115706262A (zh) * | 2021-08-05 | 2023-02-17 | 株式会社村田制作所 | 一种电解液添加剂、包含其的电解液和锂离子二次电池以及其用途 |
| JP2024527152A (ja) * | 2021-08-05 | 2024-07-19 | 株式会社村田製作所 | 電解液添加剤、それを含む電解液とリチウムイオン二次電池及びその使用 |
| JP7708303B2 (ja) | 2021-08-05 | 2025-07-15 | 株式会社村田製作所 | 電解液 |
| JP2024524799A (ja) * | 2022-05-20 | 2024-07-09 | 寧徳時代新能源科技股▲分▼有限公司 | 非水電解液及びそれを含む二次電池、電池モジュール、電池パック並びに電気装置 |
| JP7689582B2 (ja) | 2022-05-20 | 2025-06-06 | 香港時代新能源科技有限公司 | 非水電解液及びそれを含む二次電池、電池モジュール、電池パック並びに電気装置 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20100035109A (ko) | 2010-04-02 |
| CN101685857B (zh) | 2013-03-27 |
| JP4952693B2 (ja) | 2012-06-13 |
| CN101685857A (zh) | 2010-03-31 |
| US20100075233A1 (en) | 2010-03-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5407273B2 (ja) | 負極集電体、負極および二次電池 | |
| JP4952680B2 (ja) | リチウムイオン二次電池およびリチウムイオン二次電池用負極 | |
| JP5234247B2 (ja) | 負極、二次電池、スルホン化合物および電子機器 | |
| US20090169985A1 (en) | Electrolytic solution, secondary battery and method of manufacturing same, and sulfone compound | |
| JP5239473B2 (ja) | 二次電池用電解液、二次電池および電子機器 | |
| JP5181754B2 (ja) | 二次電池用電解液、二次電池および電子機器 | |
| JP5278657B2 (ja) | 二次電池および電子機器 | |
| JP4952693B2 (ja) | リチウムイオン二次電池用正極及びリチウムイオン二次電池 | |
| JP2009129893A (ja) | 負極、電池およびそれらの製造方法 | |
| JP2010198922A (ja) | 二次電池 | |
| JP2010177026A (ja) | 電池 | |
| JP2010044958A (ja) | 二次電池およびその製造方法、ならびに負極、正極および電解質 | |
| JP5532559B2 (ja) | リチウムイオン二次電池、リチウムイオン二次電池用負極、リチウムイオン二次電池用正極およびリチウムイオン二次電池用電解液 | |
| JP2010192327A (ja) | 非水電解液および非水電解液二次電池 | |
| JP5463632B2 (ja) | リチウムイオン二次電池用負極、リチウムイオン二次電池用正極、リチウムイオン二次電池および電子機器 | |
| JP2009193696A (ja) | 負極、二次電池およびそれらの製造方法 | |
| JP5217536B2 (ja) | 二次電池および電子機器 | |
| JP2009170146A (ja) | 電解液および二次電池 | |
| JP2009032491A (ja) | 電解液および電池 | |
| JP5256798B2 (ja) | 二次電池用電解液、二次電池および電子機器 | |
| JP5181740B2 (ja) | 二次電池用電解液、二次電池および電子機器 | |
| JP2009163999A (ja) | 電解液および電池 | |
| JP2009245926A (ja) | 二次電池、電解質およびチオ化合物 | |
| JP2010010080A (ja) | 負極、二次電池およびそれらの製造方法 | |
| JP2010103005A (ja) | 負極の形成方法および二次電池の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20110126 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110215 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110418 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120214 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120227 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150323 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |