JP2010047750A - アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク - Google Patents
アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク Download PDFInfo
- Publication number
- JP2010047750A JP2010047750A JP2009169542A JP2009169542A JP2010047750A JP 2010047750 A JP2010047750 A JP 2010047750A JP 2009169542 A JP2009169542 A JP 2009169542A JP 2009169542 A JP2009169542 A JP 2009169542A JP 2010047750 A JP2010047750 A JP 2010047750A
- Authority
- JP
- Japan
- Prior art keywords
- group
- general formula
- aliphatic
- substituent
- pigment
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 C[*@@](*)*=C(c1ccccc1C=C1N=O)C1=O Chemical compound C[*@@](*)*=C(c1ccccc1C=C1N=O)C1=O 0.000 description 2
- AZQSPRDGBPINTM-UHFFFAOYSA-N COC(c(ccc(C(OC)=O)c1)c1N)O Chemical compound COC(c(ccc(C(OC)=O)c1)c1N)O AZQSPRDGBPINTM-UHFFFAOYSA-N 0.000 description 1
- DSSKDXUDARIMTR-UHFFFAOYSA-N COC(c1ccc(C(OC)=O)c(N)c1)=O Chemical compound COC(c1ccc(C(OC)=O)c(N)c1)=O DSSKDXUDARIMTR-UHFFFAOYSA-N 0.000 description 1
- OUYJTAOERRBAMD-UHFFFAOYSA-N Nc(c1ccccc1cc1C(Nc2ccccc2)=O)c1O Chemical compound Nc(c1ccccc1cc1C(Nc2ccccc2)=O)c1O OUYJTAOERRBAMD-UHFFFAOYSA-N 0.000 description 1
- JFGQHAHJWJBOPD-UHFFFAOYSA-N Oc1cc2ccccc2cc1C(Nc1ccccc1)=O Chemical compound Oc1cc2ccccc2cc1C(Nc1ccccc1)=O JFGQHAHJWJBOPD-UHFFFAOYSA-N 0.000 description 1
Images
Landscapes
- Inks, Pencil-Leads, Or Crayons (AREA)
- Plural Heterocyclic Compounds (AREA)
- Heterocyclic Compounds Containing Sulfur Atoms (AREA)
- Thiazole And Isothizaole Compounds (AREA)
- Nitrogen- Or Sulfur-Containing Heterocyclic Ring Compounds With Rings Of Six Or More Members (AREA)
- Pyridine Compounds (AREA)
Abstract
【解決手段】下記一般式(1)で表されるアゾ顔料、その互変異性体、それらの塩又は水和物。
一般式(1)中、Gは水素原子、脂肪族基、アリール基、ヘテロ環基、アシル基、脂肪族オキシカルボニル基、カルバモイル基、又はスルホニル基を表し、R1は、アミノ基又は脂肪族オキシ基を表し、R2は置換基を表し、Aは1〜3個の環員窒素原子を有する複素5員環を含む基を表す。mは0〜5の整数を表し、nは1〜4の整数を表す。n=2の場合は、R1、R2、A又はGを介した2量体を表す。n=3の場合はR1、R2、A又はGを介した3量体を表す。n=4の場合はR1、R2、A又はGを介した4量体を表す。
【選択図】なし
Description
また、顔料を使用するにあたっては、他にも、所望の透明性を発現させるために必要な粒子径及び粒子形を有すること、使用される環境条件下における堅牢性、例えば耐光性、耐熱性、オゾンなどの酸化性ガスに対する耐性、その他有機溶剤や亜硫酸ガスなどへの耐薬品堅牢性が良好であること、使用される媒体中において微小粒子まで分散し、かつ、その分散状態が安定であること、等の性質も必要となる。特に、良好な色相を有し、光、湿熱及び環境中の活性ガス、中でも着色力が高く、光に対して堅牢な顔料が強く望まれている。
従来から知られている含窒素5員環をアゾ成分とするアゾ染料は、特許文献5にも開示されている。また、特許文献6〜8にはベンゼン環とナフタレン環をアゾ基を介して結合させたナフトール系アゾ顔料、色素が開示されている。
さらに、本発明の顔料分散物及びインクジェット用記録用インクは、本発明のアゾ顔料を種々の媒体に分散させてなり、色彩的特性、耐久性、インク液安定性及び分散安定性に優れる。
下記一般式(1)で表されるアゾ顔料、その互変異性体、それらの塩又は水和物。
〔2〕
前記一般式(1)で表されるアゾ顔料が、下記一般式(2)で表わされることを特徴とする〔1に記載のアゾ顔料、その互変異性体、それらの塩又は水和物。
〔3〕
〔1〕又は〔2〕に記載のアゾ顔料、その互変異性体、それらの塩又は水和物を少なくとも一種含有することを特徴とする顔料分散物。
〔4〕
〔1〕又は〔2〕に記載のアゾ顔料、その互変異性体、それらの塩又は水和物を少なくとも一種含有することを特徴とする着色組成物。
〔5〕
〔3〕に記載の顔料分散物を用いたことを特徴とするインクジェット記録用インク。
〔6〕
一般式(1)で表わされることを特徴とするアゾ化合物。
〔7〕
前記一般式(1)で表されるアゾ化合物が、下記一般式(2)で表わされることを特徴とする〔6〕記載のアゾ化合物。
本発明における脂肪族基において、その脂肪族部位は直鎖、分岐鎖及び環状のいずれであってもよい。また、飽和であっても不飽和であってもよい。具体的には例えば、アルキル基、アルケニル基、シクロアルキル基、シクロアルケニル基等を挙げることができる。さらに脂肪族基は無置換であっても置換基を有していてもよい。
アシル基は、脂肪族カルボニル基であっても、アリールカルボニル基であっても、ヘテロ環カルボニル基であってもよく、置換基を有していてもよく、置換してもよい基としては、下記置換基の項で述べた基で、置換可能な基であれば何でもよい。例えばアセチル、プロパノイル、ベンゾイル、3−ピリジンカルボニル等が挙げられる。
ハメット則はベンゼン誘導体の反応又は平衡に及ぼす置換基の影響を定量的に論ずるために1935年L.P.Hammettにより提唱された経験則であるが、これは今日広く妥当性が認められている。ハメット則に求められた置換基定数にはσp値とσm値があり、これらの値は多くの一般的な成書に見出すことができるが、例えば、J.A.Dean編、「Lange’s Handbook of Chemistry」第12版、1979年(Mc Graw−Hill)や「化学の領域」増刊、122号、96〜103頁、1979年(南光堂)に詳しい。なお、本発明において各置換基をハメットの置換基定数σpにより限定したり説明したりするが、これは上記の成書で見出せる、文献既知の値がある置換基にのみ限定されるという意味ではなく、その値が文献未知であってもハメット則に基づいて測定した場合にその範囲内に含まれるであろう置換基をも含むことはいうまでもない。本発明の一般式(1)又は(2)、で表される化合物はベンゼン誘導体ではないが、置換基の電子効果を示す尺度として、置換位置に関係なくσp値を使用する。本発明においては今後、σp値をこのような意味で使用する。
顔料は、色素分子間の強力な相互作用による凝集エネルギーによって、分子同士がお互いに強固に結合しあっている状態のことである。この状態を作るには、分子間のファンデルワールス力、分子間水素結合が必要であることが、例えば、日本画像学会誌、43巻、10頁(2004年)等に記載されている。
分子間のファンデルワールス力を強めるには、分子への芳香族基、極性基及び/又はヘテロ原子の導入等が考えられる。また、分子間水素結合を形成させるには、分子へのヘテロ原子に結合した水素原子を含有する置換基の導入及び/又は電子供与性の置環基の導入等が考えられる。更に分子全体の極性が高い方が好ましいと考えられる。そのためには、例えば、アルキル基等鎖状の基は短い方が好ましく、分子量/アゾ基の値は小さい方が好ましいと考えられる。
これらの観点から、顔料分子は、アミド結合、スルホンアミド結合、エーテル結合、スルホン基、オキシカルボニル基、イミド基、カルバモイルアミノ基、ヘテロ環、ベンゼン環等を含有することが好ましい。
一般式(1)で表される化合物は、その特異的な構造により色素分子の分子間相互作用を形成しやすく、水又は有機溶媒等に対する溶解性が低く、アゾ顔料とすることができる。
顔料は、水や有機溶媒等に分子分散状態で溶解させて使用する染料とは異なり、溶媒中に分子集合体等の固体粒子として微細に分散させて用いるものである。
また、下記一般式(1)で表される特定の構造を有することにより、着色力、色相等の色彩的特性において優れた特性を示し、かつ耐光性、耐オゾン性等の耐久性にも優れた特性を示すことができる。
次に一般式(1)で表される顔料について説明する。
Gで表されるアリールスルホニル基としては、置換基を有していてもよい。置換してもよい基としては、前述の置換基の項で述べた基で、置換可能な基であれば何でもよく、好ましい置換基としては、ヒドロキシ基、脂肪族基、脂肪族オキシ基、カルバモイル基、脂肪族オキシカルボニル基、脂肪族チオ基、アミノ基、脂肪族アミノ基、アシルアミノ基、カルバモイルアミノ基である。Gで表されるアリールスルホニル基として、好ましくは総炭素原子数6〜10のアリールスルホニル基であり、例えばベンゼンスルホニル等が挙げられる。
これらの置換基は、更に置換基を有していてもよく、その置換基としては、脂肪族基、ヒドロキシ基、アミド結合、エーテル結合、オキシカルボニル結合、チオエーテル結合等を有する置換基が好ましく、ヘテロ原子と水素原子の結合を有する置換基が、分子間水素結合等の分子間相互作用をし易くする観点でより好ましい。
R1で表される置換基を有してもよいアミノ基として、好ましくは無置換のアミノ基、総炭素原子数1〜10のアルキルアミノ基、総炭素原子数2〜10のジアルキルアミノ基、総炭素原子数6〜13のアリールアミノ基、総炭素原子数2〜12の飽和であっても、不飽和であってもよいヘテロ環アミノ基であり、より好ましくは、無置換のアミノ基、総炭素原子数1〜8のアルキルアミノ基、総炭素原子数6〜13のアリールアミノ基、総炭素原子数2〜12の飽和であっても、不飽和であってもよいヘテロ環アミノ基であり、例えばメチルアミノ、N,N−ジメチルアミノ、N−フェニルアミノ、N−(2−ピリミジル)アミノ等が挙げられる。
更に好ましくは、置換基を有していても良い総炭素原子数6〜13のアリールアミノ基及び置換基を有していても良い総炭素原子数2〜12の飽和であっても、不飽和であってもよいヘテロ環アミノ基である。
アリール基上の置換基が、アミノ基との結合位置からパラ位に置換した場合、置換基が分子の末端にあるために、分子間水素結合等の分子間相互作用をし易く、そのために色相がシャープになる。該アリール基上の置換基が更に置換基を有する場合は、脂肪族基、ヒドロキシ基、アミド結合、エーテル結合、オキシカルボニル結合、チオエーテル結合等を有する置換基が好ましく、ヘテロ原子と水素原子の結合を有する置換基が、分子間水素結合等の分子間相互作用をし易くする観点でより好ましい。
R1がへテロ環アミノ基の場合、その置換基としては、前述の置換基の項で述べた基で置換可能な基であればなんでも良く、好ましくは、前記アリールアミノ基の場合と同じ置換基が好ましい。該ヘテロ環基上の置換基が更に置換基を有する場合は、脂肪族基、ヒドロキシ基、アミド結合、エーテル結合、オキシカルボニル結合、チオエーテル結合等を有する置換基が好ましく、ヘテロ原子と水素原子の結合を有する置換基が、分子間水素結合等の分子間相互作用をし易くする観点でより好ましい。
これらの置換基が更に置換基を有する場合は、脂肪族基、ヒドロキシ基、アミド結合、エーテル結合、オキシカルボニル結合、チオエーテル結合等を有する置換基が好ましく、ヘテロ原子と水素原子の結合を有する置換基が、分子間水素結合等の分子間相互作用をし易くする観点でより好ましい。
ミノ、4−ピリジンカルバモイルアミノ等が挙げられる。
本発明の効果の点で、R2は、脂肪族オキシ基、脂肪族オキシカルボニル基、置換基を有していてもよいカルバモイル基である場合が好ましく、脂肪族オキシ基である場合はより好ましい。
Aで表される一般式(A−1)〜(A−6)は、置換含窒素5員へテロ環であり、アゾ基に結合する炭素原子(アゾ基との結合部位)の隣接原子が窒素原子であり、その窒素原子に置換基R55を有する。
本発明の効果の点でY1〜Y11は水素原子、脂肪族基、アリール基、ヘテロ環基、脂肪族オキシカルボニル基、置換基を有していてもよいカルバモイル基、アシルアミノ基、スルホンアミド基、脂肪族オキシ基、脂肪族チオ基、シアノ基等である場合が好ましく、水素原子、脂肪族基、脂肪族オキシカルボニル基、置換基を有していてもよいカルバモイル基、脂肪族オキシ基、シアノ基である場合はより好ましい。
本発明の効果の点でAは、色相長波長化の点からヘテロ原子を2個以上含有する5員へテロ環である場合は更に好ましく、(A−4)である場合は更に好ましい。
R2で表される置換基として好ましくは、一般式(1)で表されるR2で説明したものと同じである。
Zは一般式(1)のR58に相当する基であって、ハメットのσp値が0.2以上の電子求引性基を表し、好ましくはアシル基、置換基を有していても良いカルバモイル基、アルキルオキシカルボニル基、シアノ基、又はアルキルスルホニル基を表す。
本発明の効果の点で、Zとしては、総炭素原子数1〜7の置換基を有していても良いカルバモイル基(例えば、カルバモイル、N−メチルカルバモイル、N,N−ジメチルカルバモイル)、総炭素原子数2〜7の置換基を有していても良いアルコキシカルボニル基(例えばメトキシカルボニル、エトキシカルボニル、アリルオキシカルボニル)、シアノ基、総炭素原子数1〜6の置換基を有していても良いアルキルスルホニル基(例えばメタンスルホニル、エタンスルホニル、プロパンスルホニル)であることがより好ましく、カルバモイル基、アルコキシカルボニル基又はシアノ基がさらに好ましく、アルキルオキシカルボニル基、シアノ基である場合が特に好ましく、シアノ基である場合が最も好ましい。
Zがシアノ基である場合色相長波長化、高光堅牢性であり好ましい。
一般式(1)、及び一般式(2)は、化学構造上取りうる数種の互変異性体の中から極限構造式の形で示しているが、記載された構造以外の互変異性体であってもよく、複数の互変異性体を含有した混合物として用いてもよい。
例えば、一般式(1)で表される顔料には、下記一般式(1’)で表されるアゾ−ヒドラゾンの互変異性体が考えられる。
本発明は、一般式(1)で表されるアゾ顔料の互変異性体である以下の一般式(1’)で表される化合物もその範囲に含むものである。
また、本発明において、一般式(1)で表されるアゾ顔料は、分子内水素結合又は分子内交叉水素結合を形成する置換基を有することが好ましい。少なくとも1個以上の分子内水素結合を形成する置換基を有することがより好ましく、少なくとも1個以上の分子内交叉水素結合を形成する置換基を有することが特に好ましい。
また、一般式(3−2)及び(3−4)で示すように、一般式(1)のR1がアミノ基である場合には更に分子内水素結合を形成しやすい構造であり、好ましい。
その結果、分子の平面性が上がり、更に分子内・分子間相互作用が向上し、一般式(3−1)〜一般式(3−4)で表されるアゾ顔料の結晶性が高くなり(高次構造を形成し易くなり)、顔料としての要求性能である、光堅牢性、熱安定性、湿熱安定性、耐水性、耐ガス性及び又は耐溶剤性が大幅に向上するため、更に好ましい例となる。
この観点からも、一般式(1)及び(2)で表される顔料は、(3−1)〜(3−4)で表される顔料であることが好ましく、(3−2)及び(3−4)で表される顔料がより好ましい。
本発明は前記一般式(1)で表されるアゾ化合物、その互変異性体、それらの塩又は水和物にも関する。
本発明の新規なアゾ化合物は、アゾ顔料として有用である。
アゾ顔料における結晶多形の混合比は、単結晶X線結晶構造解析、粉末X線回折(XRD)、結晶の顕微鏡写真(TEM)、IR(KBr法)等の固体の物理化学的測定値から確認できる。
以下に反応スキームを示す。
一般式(1)及び一般式(2)のnが2以上の場合の合成方法は、一般式(4)又は一般式(5)のR1〜R2、R55、R56、R58等において、置換可能な2価、3価あるいは4価の置換基を導入した原料を合成し、前記スキームと同様に合成することができる。 このようにして反応させたものは、結晶が析出しているものもあるが、一般的には反応液に水、あるいはアルコール系溶媒を添加し、結晶を析出させ、結晶を濾取することができる。また、反応液にアルコール系溶媒、水等を添加して結晶を析出させて、析出した結晶を濾取することができる。濾取した結晶を必要に応じて洗浄・乾燥して、一般式(1)で表されるアゾ顔料を得ることができる。
溶媒加熱処理に使用される溶媒としては、例えば、水、トルエン、キシレン等の芳香族炭化水素系溶媒、クロロベンゼン、o−ジクロロベンゼン等のハロゲン化炭化水素系溶媒、イソプロパノール、イソブタノール等のアルコール系溶媒、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド、N−メチル−2−ピロリドン等の極性非プロトン性有機溶媒、氷酢酸、ピリジン、又はこれらの混合物等が挙げられる。上記で挙げた溶媒に、さらに無機又は有機の酸又は塩基を加えてもよい。溶媒加熱処理の温度は所望する顔料の一次粒子径の大きさによって異なるが、40〜150℃が好ましく、60〜100℃が更に好ましい。また、処理時間は、30分〜24時間が好ましい。
ソルベントソルトミリングとしては、例えば、粗アゾ顔料と、無機塩と、それを溶解しない有機溶剤とを混練機に仕込み、その中で混練磨砕を行うことが挙げられる。上記無機塩としては、水溶性無機塩が好適に使用でき、例えば塩化ナトリウム、塩化カリウム、硫酸ナトリウム等の無機塩を用いることが好ましい。また、平均粒子径0.5〜50μmの無機塩を用いることがより好ましい。当該無機塩の使用量は、粗アゾ顔料に対して3〜20質量倍とするのが好ましく、5〜15質量倍とするのがより好ましい。有機溶剤としては、水溶性有機溶剤が好適に使用でき、混練時の温度上昇により溶剤が蒸発し易い状態になるため、安全性の点から高沸点溶剤が好ましい。このような有機溶剤としては、例えばジエチレングリコール、グリセリン、エチレングリコール、プロピレングリコール、液体ポリエチレングルコール、液体ポリプロピレングリコール、2−(メトキシメトキシ)エタノール、2−ブトキシエタノール、2ー(イソペンチルオキシ)エタノール、2−(ヘキシルオキシ)エタノール、ジエチレングリコールモノメチルエーテル、ジエチレングルコールモノエチルエーテル、ジエチレングリコールモノブチルエーテル、トリエチレングリコール、トリエチレングリコールモノメチルエーテル、1−メトキシ−2−プロパノール、1−エトキシ−2−プロパノール、ジプロピレングリコール、ジプロピレングリコールモノメチルエーテル、ジプロピレングリコールモノメチルエーテル、ジプロピレングリコール又はこれらの混合物が挙げられる。当該水溶性有機溶剤の使用量は、粗アゾ顔料に対して0.1〜5質量倍が好ましい。混練温度は、20〜130℃が好ましく、40〜110℃が特に好ましい。混練機としては、例えばニーダーやミックスマーラー等が使用できる。
本発明の顔料分散物は、一般式(1)及び一般式(2)で表されるアゾ顔料、互変異性体、その塩又は水和物を少なくとも1種を含むことを特徴とする。これにより、色彩的特性、耐久性及び分散安定性に優れた顔料分散物とすることができる。
ヒクルとして、光硬化性樹脂を用いてもよい。
本発明の着色組成物は、少なくとも一種の本発明のアゾ顔料を含有する着色組成物を意味する。本発明の着色組成物は、媒体を含有させることができるが、媒体として溶媒を用いた場合は特にインクジェット記録用インクとして好適である。本発明の着色組成物は、媒体として、親油性媒体や水性媒体を用いて、それらの中に、本発明のアゾ顔料を分散させることによって作製することができる。好ましくは、水性媒体を用いる場合である。本発明の着色組成物には、媒体を除いたインク用組成物も含まれる。本発明の着色組成物は、必要に応じてその他の添加剤を、本発明の効果を害しない範囲内において含有しうる。その他の添加剤としては、例えば、乾燥防止剤(湿潤剤)、褪色防止剤、乳化安定剤、浸透促進剤、紫外線吸収剤、防腐剤、防黴剤、pH調整剤、表面張力調整剤、消泡剤、粘度調整剤、分散剤、分散安定剤、防錆剤、キレート剤等の公知の添加剤(特開2003−306623号公報に記載)が挙げられる。これらの各種添加剤は、水溶性インクの場合にはインク液に直接添加する。油溶性インクの場合には、アゾ顔料分散物の調製後分散物に添加するのが一般的であるが、調製時に油相又は水相に添加してもよい。
次に、本発明のインクジェット記録用インクについて説明する。
本発明のインクジェット記録用インク(以下、「インク」という場合がある)は、上記で説明した顔料分散物を用いる。好ましくは、水溶性溶媒、水等を混合して調製される。ただし、特に問題がない場合は、前記本発明の顔料分散物をそのまま用いてもよい。
具体例としては、多価アルコール類では、エチレングリコール、ジエチレングリコール、プロピレングリコール、ブチレングリコール、トリエチレングリコール、1、5−ペンタンジオール、1,2,6−ヘキサントリオール、グリセリン等が挙げられる。
インクの表面張力は、20mN/m以上60mN/m以下であることが好ましい。より好ましくは、20mN以上45mN/m以下であり、更に好ましくは、25mN/m以上35mN/m以下である。表面張力が20mN/m未満となると記録ヘッドのノズル面に液体が溢れ出し、正常に印字できない場合がある。一方、60mN/mを超えると、印字後の記録媒体への浸透性が遅くなり、乾燥時間が遅くなる場合がある。
なお、上記表面張力は、前記同様ウイルヘルミー型表面張力計を用いて、23℃、55%RHの環境下で測定した。
なお、上記粘度(後述するものを含む)の測定は、回転粘度計レオマット115(Contraves社製)を用い、23℃でせん断速度を1400s−1として行った。
その他必要に応じ、pH緩衝剤、酸化防止剤、防カビ剤、粘度調整剤、導電剤、紫外線吸収剤、等も添加することができる。
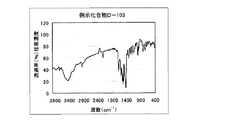
具体的化合物例D−1の合成
具体的化合物例D−1の合成は、以下のルートで合成した。
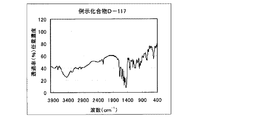
1.0gの化合物(1)を10mlのリン酸(和光純薬株式会社;試薬特級純度85%、以下同様)に加えて溶かした。この溶液を氷冷して−5〜0℃に保ち、亜硝酸ナトリウム0.38gを加えて1時間攪拌し、ジアゾニウム塩溶液を得た。別に化合物(0)1.30gにアセトニトリル25mlを添加し攪拌下に、前述のジアゾニウム塩溶液を8℃以下で加えた。添加終了と同時に氷浴をはずし、更に3時間攪拌した。反応液にアセトニトリル50mlを添加し、30分間攪拌し、析出している結晶を濾別し、アセトニトリル30mlでかけ洗いをした。結晶を乾燥せずに水100mlに加え、炭酸水素ナトリウム0.5gを水30mlに溶かした溶液を添加し、20〜25℃で30分間攪拌した。析出している結晶を濾別し、更に水で充分にかけ洗いした。得られた結晶を乾燥させずにジメチルアセトアミド50mlに加え、100℃で加熱攪拌を30分間行なった。室温で30分間攪拌し、析出している結晶を濾過し、ジメチルアセトアミド30mlでかけ洗いをした。得られた結晶を乾燥させずにジメチルアセトアミド50mlに加え、水25mlを徐々に滴下し、80℃で1時間攪拌し、更に室温下で30分間攪拌した。析出している結晶を濾過し、ジメチルアセトアミド/水=2/1の20ml及びメタノール20mlでかけ洗いした。得られた結晶を乾燥し、本発明の化合物D−1を1.2g得た。収率52%。
図1に赤外吸収チャートを示す。
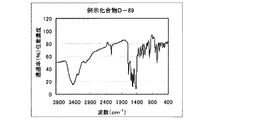
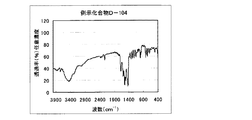
具体的化合物例D−33の合成
具体的化合物例D−33の合成は、以下のルートで合成した。
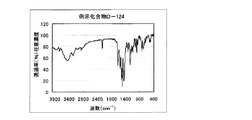
1.0gの化合物(2)を10mlのリン酸に加えて30℃に加温し溶かした。この溶液を氷冷して0〜5℃に保ち、亜硝酸ナトリウム0.38gを加えて1.5時間攪拌し、ジアゾニウム塩溶液を得た。このジアゾニウム塩溶液を、化合物(0)1.4gをジメチルアセトアミド5mlに溶かした溶液に5〜10℃に保ちながら滴下し、その後5〜10℃に保ちながら1時間攪拌した。その後、氷浴をはずし、更に0.5時間攪拌した。反応液に酢酸エチル50mlを加え、80℃で加熱完溶した。その反応液にヘキサン50mlを加え、さらに80℃で20分間、室温で40分間攪拌した。析出した結晶を濾別し、ヘキサン50mlでかけ洗いをした。結晶を乾燥せずに水200ml、飽和炭酸水素ナトリウムを0.1ml加えて中和した。結晶にアセトニトリル100mlを加え、80℃で3時間、室温で1時間攪拌し、析出している結晶を濾過し、アセトニトリル50mlでかけ洗いした。得られた結晶を乾燥し、本発明の化合物D−33を0.51g得た。収率21%。 λmax:504nm、ε:1.59×104(CHCl3)
図2に赤外吸収チャートを示す。
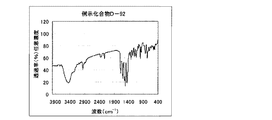
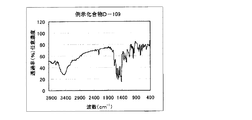
具体的化合物例D−20の合成
具体的化合物例D−20の合成は、以下のルートで合成した。
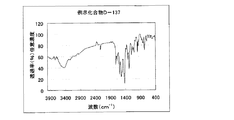
1.0gの化合物(3)を10mlのリン酸に加えて30℃に加温し溶かした。この溶液を氷冷して0〜5℃に保ち、亜硝酸ナトリウム0.35gを加えて2時間攪拌し、ジアゾニウム塩溶液を得た。このジアゾニウム塩溶液を、化合物(0)1.3gをジメチルアセトアミド5mlに溶かした溶液に5〜10℃に保ちながら滴下し、その後5〜10℃に保ちながら20分間、その後、氷浴をはずし、更に20分間攪拌した。反応液にジメチルアセトアミド100mlを加え、40℃で20分間攪拌した。その反応液にアセトニトリル100mlを加え、室温で10分間攪拌した。析出した結晶を濾別し、アセトニトリル50mlでかけ洗いをした。結晶を乾燥せずに水200ml、飽和炭酸水素ナトリウムを0.1ml加えて中和し、ジメチルアセトアミド/水=1/1、30mlを添加し、内温80℃で45分間攪拌した。その後空冷下で1時間拡販し、析出した結晶をろ過し、ジメチルアセトアミド/水=1/1、10mlでかけ洗いした後、水、20mlでかけ洗いをした。得られた結晶を乾燥し、本発明の化合物D−20を0.49g得た。収率21%。 λmax:493nm、ε:1.93×104(CHCl3)
図3に赤外吸収チャートを示す。
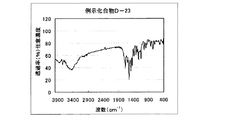
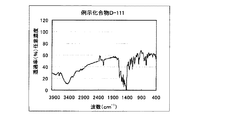
具体的化合物例D−22の合成
具体的化合物例D−22の合成は、以下のルートで合成した。
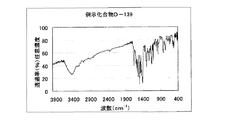
4.5gの化合物(4)を45mlのリン酸に加えて30℃に加温し溶かした。この溶液を氷冷して0〜5℃に保ち、亜硝酸ナトリウム1.47gを加えて1時間攪拌し、ジアゾニウム塩溶液を得た。このジアゾニウム塩溶液を、化合物(0)4.5gをジメチルアセトアミド70mlに溶かした溶液に5〜10℃に保ちながら滴下し、その後5〜10℃に保ちながら30分間、その後、氷浴をはずし、更に1時間攪拌した。反応液に水200mlを加えて、析出した結晶を濾別し、水200mlでかけ洗いをした。結晶にアセトニトリル200mlを加え、80℃で2時間攪拌した。その後、室温で2時間攪拌したのちに析出した結晶を濾別した。結晶は飽和炭酸水素ナトリウムを0.1ml加えて中和し、ジメチルアセトアミド/水=1/1、30mlを添加し、内温80℃で45分間攪拌した。その後空冷下で1時間拡販し、析出した結晶をろ過し、ジメチルアセトアミド/水=1/1、10mlでかけ洗いした後、水、20mlでかけ洗いをした。得られた結晶を乾燥し、本発明の化合物D−22を6.9g得た。収率82%。 λmax:494nm、ε:1.91×104(CHCl3)
図4に赤外吸収チャートを示す。
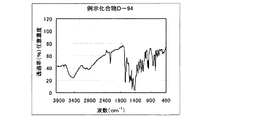
具体的化合物例3と同様にして他の化合物を合成した。合成した化合物の赤外吸収チャートを図5〜53に示す。
比較化合物4の合成
比較化合物4の合成は、以下のルートで合成した。
比較化合物5の合成
比較化合物5の合成は、以下のルートで合成した。
特許第3894726号に記載の化合物
具体的化合物例D−1の顔料2.5部、オレイン酸ナトリウム0.5部、グリセリン5部、水42部を混合し、直径0.1mmのジルコニアビーズ100部とともに遊星型ボールミルを用いて毎分300回転、6時間分散を行った。分散終了後、ジルコニアビーズを分離し、顔料分散物1を得た。
〔実施例2〕
実施例1で合成した顔料(D−1)5部、高分子分散剤として、国際公開番号WO2006/064193号パンフレットの22ページに記載されているDispersant Solution 10で表されるメタクリル酸−メタクリル酸エステル共重合体水溶液25.5部、水19.5部を混合し、直径0.1mmのジルコニアビーズ100部とともに遊星型ボールミルを用いて毎分300回転で6時間分散を行った。分散終了後、ジルコニアビーズを分離し、顔料分散物2を得た。
実施例1の顔料に変えてC.I.ピグメント・レッド254(チバスペシャリティ社製B−CF)を用いた以外は実施例1と同様にして赤色の比較顔料分散物1を得た。
実施例1で用いた顔料(D−1)に変えてC.I.ピグメント・イエロー74(チバスペシャリティ社製Iralite YELLOW GO)を用いた以外は実施例1と同様にして黄色の比較顔料分散物2を得た。
実施例1で用いた顔料(D−1)に変えてC.I.ピグメント・イエロー155(クラリアント社製INKJET YELLOW 4G VP2532)を用いた以外は実施例1と同様にして黄色の比較顔料分散物3を得た。
[比較例4]
実施例1で用いた顔料(D−1)に変えて比較化合物4を用いた以外は実施例1と同様にして赤色の比較顔料分散物4を得た。
[比較例5]
実施例1で用いた顔料(D−1)に変えて比較化合物5を用いた以外は実施例1と同様にして赤色の比較顔料分散物5を得た。
[比較例4]
実施例1で用いた顔料(D−1)に変えて比較化合物6を用いた以外は実施例1と同様にして赤色の比較顔料分散物6を得た。
<分散安定性>
上記で得られた各顔料分散物を動的光散乱粒径測定装置(日機装(株)マイクロトラックUPA150)を用いて、常法により体積平均粒子径を測定した。顔料分散物を作製して2時間後に測定した体積平均粒子径、及び70℃で2日間保存後の体積平均粒子径が、共に230nm以下のものを○(良好)、いずれかが230nm以上のものを×(不良)とした。結果を表1に示す。
<着色力評価>
上記で得られた各顔料分散物をNo.3のバーコーターを用いてセイコーエプソン(株)社製フォトマット紙<顔料専用>に塗布した。得られた塗布物の画像濃度を反射濃度計(X−Rite社製X−Rite938)を用いて測定し、「着色力(OD:OpticalDensity)」として結果を表1に示す。
<耐光性評価>
着色力評価に用いた画像濃度1.0の塗布物を、フェードメーターを用いてキセノン光(170000lux.;325nm以下カットフィルター存在下)を14日間照射し、キセノン照射前後の画像濃度を、反射濃度計を用いて測定し、色素残存率[(照射後濃度/照射前濃度)×100%]として評価した。結果を表1に示す。
実施例1の具体的化合物例D−1を表1のように変更した以外は、同様にして顔料分散物3〜19を作成し、同様な評価を行なった。
国際公開番号WO06/064193号パンフレットの22ページに記載されているDispersant 10で表される高分子分散剤を水酸化カリウム水溶液で中和した。得られた分散剤水溶液75質量部(固形分濃度20%)の中に、前記合成のアゾ顔料(D−1)30質量部及びイオン交換水95質量部を加えて、ディスパー攪拌翼にて混合・粗分散する。混合・粗分散した液にジルコニア・ビーズを600質量部を入れて、これを分散機(サンドグラインダミル)で4時間分散した後、ビーズと分散液に分離した。得られた混合物を攪拌しながら、25℃でポリエチレングリコールジグリシジルエ−テル2質量部をゆっくり加え、50℃で6時間攪拌した。更に、分画分子数300Kの限外濾過膜を使って不純物を除去し、これをポアサイズ5μmのフィルター(アセチルセルロース膜、外径:25mm、富士フイルム(株)社製)を取り付けた容量20mlのシリンジで濾過し、粗大粒子を除去することにより固形分濃度10%の顔料分散物101(粒径80nm:日機装(株)社製Nanotrac150(UPA−EX150)を用いて測定)を得た。
実施例101において用いたアゾ顔料(D−1)の代わりに、レッド顔料(C.I.ピグメント・レッド254(チバスペシャリティ社製B−CF)を用いた以外は実施例101と同様にして比較顔料分散物101を得た。
実施例101で得られた顔料分散物101の代わりに、比較例101で得られた比較顔料分散物101を用いた以外は実施例102と同様にして比較顔料インク液5を得た。
1)吐出安定性については、カートリッジをプリンターにセットし全ノズルからのインクの突出を確認した後、A4 20枚出力し、以下の基準で評価した。
A:印刷開始から終了まで印字の乱れ無し
B:印字の乱れのある出力が発生する
C:印刷開始から終了まで印字の乱れあり
[1]光堅牢性は印画直後の画像濃度CiをX−rite310にて測定した後、アトラス社製ウェザーメーターを用い画像にキセノン光(10万ルックス)を14日照射した後、再び画像濃度Cfを測定し画像残存率Cf/Ci×100を求め評価を行った。
画像残像率について反射濃度が1、1.5、2の3点にて評価し、いずれの濃度でも画像残存率が80%以上の場合をA、2点が80%未満の場合をB、全ての濃度で80%未満の場合をCとした。
何れの濃度でも画像残存率が80%以上の場合をA、1又は2点が80%未満をB、全ての濃度で70%未満の場合をCとして、三段階で評価した。
金属光沢の見えないものを「○」、金属光沢の見えるものを「×」として評価した。
表2の結果から明らかなように、本発明のインク液を使用した系ではすべての性能に優れていることがわかる。特に比較例に対して、光堅牢性及びインク液安定性が優れている。
実施例102で作製した顔料インク液を、エプソン(株)社製のPX−V630にて画像を富士フイルム(株)社製インクジェットペーパーフォト光沢紙「画彩」にプリントし、実施例102と同様な評価を行ったところ、同様な結果が得られた。
表1、表2の結果から明らかなように、本発明の顔料を用いた顔料分散物1〜19及び顔料インク液5は色調に優れ、高い着色力及び耐光性を示す。
従って、本発明の顔料を用いた顔料分散物は、例えば、インクジェットなどの印刷用のインク等に好適に使用することができる。
Claims (7)
- 下記一般式(1)で表されるアゾ顔料、その互変異性体、それらの塩又は水和物。
- 請求項1又は請求項2に記載のアゾ顔料、その互変異性体、それらの塩又は水和物を少なくとも一種含有することを特徴とする顔料分散物。
- 請求項1又は請求項2に記載のアゾ顔料、その互変異性体、それらの塩又は水和物を少なくとも一種含有することを特徴とする着色組成物。
- 請求項3に記載の顔料分散物を用いたことを特徴とするインクジェット記録用インク。
- 一般式(1)で表わされることを特徴とするアゾ化合物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009169542A JP5559998B2 (ja) | 2008-07-17 | 2009-07-17 | アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008186507 | 2008-07-17 | ||
| JP2008186507 | 2008-07-17 | ||
| JP2009169542A JP5559998B2 (ja) | 2008-07-17 | 2009-07-17 | アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010047750A true JP2010047750A (ja) | 2010-03-04 |
| JP5559998B2 JP5559998B2 (ja) | 2014-07-23 |
Family
ID=42014878
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009169543A Abandoned JP2010043255A (ja) | 2008-07-17 | 2009-07-17 | アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク |
| JP2009169542A Active JP5559998B2 (ja) | 2008-07-17 | 2009-07-17 | アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009169543A Abandoned JP2010043255A (ja) | 2008-07-17 | 2009-07-17 | アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク |
Country Status (1)
| Country | Link |
|---|---|
| JP (2) | JP2010043255A (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010084135A (ja) * | 2008-09-02 | 2010-04-15 | Fujifilm Corp | アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク |
| JP2011144298A (ja) * | 2010-01-15 | 2011-07-28 | Fujifilm Corp | アゾ顔料の製造方法、顔料分散物、着色組成物、インクジェット記録用インクの調製方法、カラーフィルター用着色組成物及びカラーフィルター |
| EP2390283A1 (en) | 2010-05-31 | 2011-11-30 | FUJIFILM Corporation | Azo pigment or tautomer thereof, process for producing same, pigment dispersion, coloring composition, inkjet recording ink, coloring composition for color filter, and color filter |
| JP2011252065A (ja) * | 2010-06-01 | 2011-12-15 | Fujifilm Corp | 顔料分散組成物、着色硬化性組成物、固体撮像素子用カラーフィルタ及びその製造方法、並びに固体撮像素子 |
| JP2012012498A (ja) * | 2010-06-30 | 2012-01-19 | Fujifilm Corp | 顔料組成物、インクジェット記録用インク、カラーフィルター用着色組成物及びカラーフィルター |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5622379B2 (ja) * | 2009-11-06 | 2014-11-12 | 富士フイルム株式会社 | アゾ化合物、顔料組成物、顔料組成物の製造方法、インクジェット記録用インク、カラーフィルター用着色組成物及びカラーフィルター |
| JP5740089B2 (ja) * | 2010-01-15 | 2015-06-24 | 富士フイルム株式会社 | アゾ顔料の製造方法、インクジェット記録用インクの製造方法、カラーフィルター用着色組成物の製造方法、及びカラーフィルターの製造方法。 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63148267A (ja) * | 1986-12-12 | 1988-06-21 | Canon Inc | 電子写真感光体 |
| JPS63158561A (ja) * | 1986-12-23 | 1988-07-01 | Canon Inc | 電子写真感光体 |
| JPH0427959A (ja) * | 1990-05-24 | 1992-01-30 | Canon Inc | 電子写真感光体、該電子写真感光体を備えた電子写真装置並びにファクシミリ |
| JPH0488349A (ja) * | 1990-08-01 | 1992-03-23 | Canon Inc | 電子写真感光体、該電子写真感光体を備えた電子写真装置並びにファクシミリ |
| JP2003237240A (ja) * | 2002-02-21 | 2003-08-27 | Ricoh Co Ltd | 光記録媒体 |
| JP2003246148A (ja) * | 2002-02-26 | 2003-09-02 | Ricoh Co Ltd | 光記録媒体及びそれを用いた光記録方法 |
-
2009
- 2009-07-17 JP JP2009169543A patent/JP2010043255A/ja not_active Abandoned
- 2009-07-17 JP JP2009169542A patent/JP5559998B2/ja active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63148267A (ja) * | 1986-12-12 | 1988-06-21 | Canon Inc | 電子写真感光体 |
| JPS63158561A (ja) * | 1986-12-23 | 1988-07-01 | Canon Inc | 電子写真感光体 |
| JPH0427959A (ja) * | 1990-05-24 | 1992-01-30 | Canon Inc | 電子写真感光体、該電子写真感光体を備えた電子写真装置並びにファクシミリ |
| JPH0488349A (ja) * | 1990-08-01 | 1992-03-23 | Canon Inc | 電子写真感光体、該電子写真感光体を備えた電子写真装置並びにファクシミリ |
| JP2003237240A (ja) * | 2002-02-21 | 2003-08-27 | Ricoh Co Ltd | 光記録媒体 |
| JP2003246148A (ja) * | 2002-02-26 | 2003-09-02 | Ricoh Co Ltd | 光記録媒体及びそれを用いた光記録方法 |
Non-Patent Citations (4)
| Title |
|---|
| JPN6009051180; 小松紀陸他: 'アミノイミダゾールからのアゾ染料' 工業化学雑誌 Vol.73, No.7, 1970, p.1694-1697 * |
| JPN6009051182; ANDREEVA,M.A. et al.: 'Syntheses based on dimethylpyrazoles. I. Synthesis of nitro- and amino-substituted 1,3- and 1,5-di' Zhurnal Obshchei Khimii Vol.50, No.9, 1980, p.2106-2109 * |
| JPN6009051188; SEBE,I. et al.: 'Triazo heterocyclic disperse dyes' Revue Roumaine de Chimie Vol.41, No.11-12, 1996, p.971-977 * |
| JPN6009051190; POSKOCIL,J. et al.: 'Some new triazole dyes' Chemicky Prumysl Vol.32, No.6, 1982, p.300-307 * |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010084135A (ja) * | 2008-09-02 | 2010-04-15 | Fujifilm Corp | アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク |
| JP2011144298A (ja) * | 2010-01-15 | 2011-07-28 | Fujifilm Corp | アゾ顔料の製造方法、顔料分散物、着色組成物、インクジェット記録用インクの調製方法、カラーフィルター用着色組成物及びカラーフィルター |
| EP2390283A1 (en) | 2010-05-31 | 2011-11-30 | FUJIFILM Corporation | Azo pigment or tautomer thereof, process for producing same, pigment dispersion, coloring composition, inkjet recording ink, coloring composition for color filter, and color filter |
| US8298299B2 (en) | 2010-05-31 | 2012-10-30 | Fujifilm Corporation | Azo pigment or tautomer thereof, process for producing same, pigment dispersion, coloring composition, inkjet recording ink, coloring composition for color filter, and color filter |
| JP2011252065A (ja) * | 2010-06-01 | 2011-12-15 | Fujifilm Corp | 顔料分散組成物、着色硬化性組成物、固体撮像素子用カラーフィルタ及びその製造方法、並びに固体撮像素子 |
| JP2012012498A (ja) * | 2010-06-30 | 2012-01-19 | Fujifilm Corp | 顔料組成物、インクジェット記録用インク、カラーフィルター用着色組成物及びカラーフィルター |
| TWI577743B (zh) * | 2010-06-30 | 2017-04-11 | 富士軟片股份有限公司 | 顏料組成物、噴墨記錄墨水、用於彩色濾光片的著色組成物及彩色濾光片 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5559998B2 (ja) | 2014-07-23 |
| JP2010043255A (ja) | 2010-02-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5433173B2 (ja) | アゾ顔料および該アゾ顔料の製造方法、該顔料を含む顔料分散物、着色組成物及びインクジェット記録用インク | |
| JP5667815B2 (ja) | アゾ顔料の製造方法、アゾ顔料、及び、着色組成物 | |
| WO2010008081A1 (ja) | アゾ化合物、アゾ顔料、顔料分散物、着色組成物、インクジェット記録用インク、カラーフィルター用着色組成物、カラーフィルター及びカラーフィルター用着色組成物の調製方法 | |
| JP5559998B2 (ja) | アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク | |
| JP5380098B2 (ja) | アゾ化合物、アゾ顔料および該アゾ化合物又は該アゾ顔料を含む分散物、着色組成物、インクジェット記録用インク、インクジェット記録用インクタンク、インクジェット記録方法、及び記録物 | |
| JP5380068B2 (ja) | アゾ化合物、アゾ顔料および該アゾ化合物又は該アゾ顔料を含む分散物、着色組成物、インクジェット記録用インク、インクジェット記録用インクタンク、インクジェット記録方法、及び記録物 | |
| JP5860926B2 (ja) | アゾ顔料、該アゾ顔料を含む顔料分散物及び着色組成物 | |
| WO2009110554A1 (ja) | アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク | |
| JP5433180B2 (ja) | アゾ顔料、該顔料を含む顔料分散物、着色組成物及びインクジェット記録用インク | |
| JP5205102B2 (ja) | アゾ顔料および該アゾ顔料の製造方法、該顔料を含む顔料分散物、着色組成物及びインクジェット記録用インク | |
| JP2009275112A (ja) | アゾ顔料、顔料分散物、着色組成物、インクジェット記録用インク及びアゾ化合物 | |
| JP5271568B2 (ja) | アゾ顔料、該アゾ顔料を含む顔料分散物、着色組成物およびインクジェット記録用インク | |
| JP2010138245A (ja) | アゾ顔料、アゾ顔料分散物、着色組成物およびインクジェット記録用インク | |
| JP5205103B2 (ja) | アゾ顔料、該アゾ顔料を含む顔料分散物、着色組成物及びインクジェット記録用インク | |
| JP2010132778A (ja) | アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク | |
| JP2010059282A (ja) | アゾ化合物、アゾ顔料、顔料分散物、着色組成物、及びインクジェット記録用インク | |
| JP2009215382A (ja) | アゾ顔料、顔料分散物、着色組成物、インクジェット記録用インク及びアゾ化合物 | |
| JP2010229177A (ja) | アゾ化合物、アゾ顔料、分散物、着色組成物、及びインクジェット記録用インク | |
| JP2009079201A (ja) | アゾ顔料、該顔料を含む顔料分散物、着色組成物、及びインクジェット記録用インク |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20111216 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120201 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20120914 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20121004 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131105 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131219 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140513 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140609 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5559998 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |