JP2010032360A - 磁性粒子を用いた測定対象物質の濃度測定法 - Google Patents
磁性粒子を用いた測定対象物質の濃度測定法 Download PDFInfo
- Publication number
- JP2010032360A JP2010032360A JP2008194754A JP2008194754A JP2010032360A JP 2010032360 A JP2010032360 A JP 2010032360A JP 2008194754 A JP2008194754 A JP 2008194754A JP 2008194754 A JP2008194754 A JP 2008194754A JP 2010032360 A JP2010032360 A JP 2010032360A
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- magnetic particles
- substance
- measured
- target substance
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Landscapes
- Peptides Or Proteins (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Abstract
【解決手段】検体と、標識物質で標識された第1抗体とを混合して混合液を調製する工程、互いに親和性を有する2種類の結合材の一方が結合した第2抗体と、該2種類の結合材の他方が結合した磁性粒子を、前記混合液に添加する工程、前記磁性粒子を回収する工程、及び前記標識を検出する工程を含み、前記第1抗体と前記第2抗体は測定対象物質に対する結合能を有し、その結合に際して互いに競合しないことを特徴とする、検体中の測定対象物質の濃度を測定する方法により、測定対象物質を安価に、高精度且つ高感度に測定する。
【選択図】なし
Description
ロBNPもしくはγ−BNP誘導体に反応するがα−BNPには反応しない第2の抗体とを用いることを特徴とする哺乳類のγ−BNP誘導体に特異的な免疫測定方法が開示されている。
(1)検体と、標識物質で標識された第1抗体とを混合して混合液を調製する工程、
互いに親和性を有する2種類の結合材の一方が結合した第2抗体と、該2種類の結合材の他方が結合した磁性粒子を、前記混合液に添加する工程、
前記磁性粒子を回収する工程、及び
前記標識を検出する工程
を含み、
前記第1抗体と前記第2抗体は測定対象物質に対する結合能を有し、その結合に際して互いに競合しないことを特徴とする、
検体中の測定対象物質の濃度を測定する方法。
(2)前記第2抗体と前記磁性粒子とを、前記混合液に同時に添加することを特徴とする、(1)に記載の方法。
(3)前記第2抗体を前記混合液に添加した後に、前記磁性粒子を添加することを特徴とする、(1)に記載の方法。
(4)前記磁性粒子を前記混合液に添加した後に、前記第2抗体を添加することを特徴とする、(1)に記載の方法。
(5)前記磁性粒子が、1〜1000nmの平均粒径であることを特徴とする、(1)〜(4)のいずれかに記載の方法。
(6)前記磁性粒子が、50〜200nmの平均粒径であることを特徴とする、(5)に記載の測定方法。
(7)前記第1抗体及び前記第2抗体の少なくとも一方がモノクローナル抗体である、(1)〜(6)のいずれかに記載の方法。
(8)前記測定対象物質がペプチドである、(1)〜(7)のいずれかに記載の方法。
(9)前記ペプチドが脳性ナトリウム利尿ペプチドである、(8)に記載の方法。
本発明により測定できる臨床検体中の測定対象物質としては、微生物、細菌、ウィルス、タンパク質、ポリペプチド、ペプチド、糖タンパク質、脂質、糖脂質、核酸、毒素等またはこれらの複合体等が挙げられ、低分子物質がこれらと結合したものも含まれる。測定対象物質としては、例えば、癌胎児性抗原(CEA)、α−フェトプロテイン(AFP)、前立腺性酸性ホスファターゼ(PAP)、CA19−9、CA125、CA15−3、前立腺特異抗原(PSA)、遊離PSA等の腫瘍マーカー、HBs抗原、HBs抗体、HBe抗原、HBe抗体、HBc抗体、HCV抗体、p24抗原等の感染症マーカー、FDP、Dダイマー、PIC、ATIII、FM等の凝固線溶マーカー、CK−MB、ミオグロビン、トロポニン、CRP、BNP等の心不全マーカー、TSH、HCG等のホルモン類、インスリン等が例示できるが、これらに限定されるものではなく、サンドイッチ免疫測定法で測定できるものは全て本発明の方法の測定対象物質に含まれる。
本発明により測定できる食品検体中の測定対象物質としては、微生物、細菌、ウィルス、タンパク質、ポリペプチド、ペプチド、糖タンパク質、脂質、糖脂質、核酸、毒素、アレルゲン等またはこれらの複合体等が挙げられ、低分子物質がこれらと結合したものも含まれるが、これらに限定されるものではなく、サンドイッチ免疫測定法又はこれに準じる方法で測定できるものは全て本発明の方法の測定対象物質に含まれる。
本発明により測定できる環境サンプリング検体中の測定対象物質としては、微生物、細菌、ウィルス、タンパク質、ポリペプチド、ペプチド、糖タンパク質、脂質、糖脂質、核
酸、毒素等またはこれらの複合体等が挙げられ、低分子物質がこれらと結合したものも含まれるが、これらに限定されるものではなく、サンドイッチ免疫測定法又はこれに準じる方法で測定できるものは全て本発明の方法の測定対象物質に含まれる。
4−メトキシ−4−(3''−ホスホリルオキシ)フェニル−1,2−ジオキセタン・2ナトリウム塩)、9−(4−クロロフェニルチオホスホリルオキシメチリデン)−10−メチルアクリダン二ナトリウム塩等の発光基質を使用することができる。また、FITC(fluorescein isothiocyanate)、ローダミン等の蛍光色素等を使用することができる。
また、温度変化だけでなく、凝集剤を用いることで、凝集塊を生成させることもできる。凝集剤としては、例えば、硫酸リチウム、硫酸カリウム、硫酸ナトリウム等の硫酸金属塩等や、酢酸ナトリウムやクエン酸ナトリウム等のカルボン酸金属塩等が利用できる。凝集剤を使用して生成した凝集塊は、加熱または冷却により生成した凝集塊と同様に短時間で磁集が可能になる。
標識物質で標識された第1抗体として、アルカリフォスファターゼ標識抗BNP抗体(以下「R2抗体」と略すことがある)、互いに親和性を有する2種類の結合材の一方が結合した第2抗体としてビオチン標識抗BNP抗体(以下「R1抗体」と略すことがある)、及び互いに親和性を有する2種類の結合材の他方が結合した磁性粒子としてアビジンを固定した磁性粒子を用い、サンドイッチ免疫測定法によりBNPを定量した。
0秒反応後、Magna−Stand6((商品名)、マグナビート株式会社、商品コードTMM001)にセットし、30℃で1分間、磁気分離し、その後、上清を除去した。洗浄液(塩野義製薬株式会社製、MI02シオノギBNP(商品名)、ブロック液)100μLにて沈殿物を再分散し、凝集剤30μLを加えピペッティングにて攪拌し、30℃で30秒反応後、30℃で1分間、磁気分離し、洗浄を行なった。洗浄は同様の手順で2回繰り返した。最後に洗浄液100μLにて沈殿物を再分散し、全量をマイクロプレートに移し、APS−5(Lumigen社製、商品コードAP5−101)100μLを混合し、5秒間攪拌した後、10秒反応させ、マルチラベルプレートリーダー(ベルトールドジャパン株式会社製、Mithras LB940(商品名))にて0.1秒間発光強度を測定した。測定結果を表1に示した。ここでは、凝集剤として、1M Na2SO4水溶液を用いた。
最小検出濃度は以下の方法で算出した。
(最小濃度×2SD/最小濃度時の平均値−濃度0時の平均値)
比較例として、検体に磁性粒子とR1抗体及び、R2抗体の混合物を添加して、従来のサンドイッチ法によりBNPを定量した例を示す。
測定方法は、以下の通りである。検体として標準BNP試薬(塩野義製薬株式会社製、MI02シオノギBNP(商品名)、標準BNP試薬)をマイクロチューブに65μL分
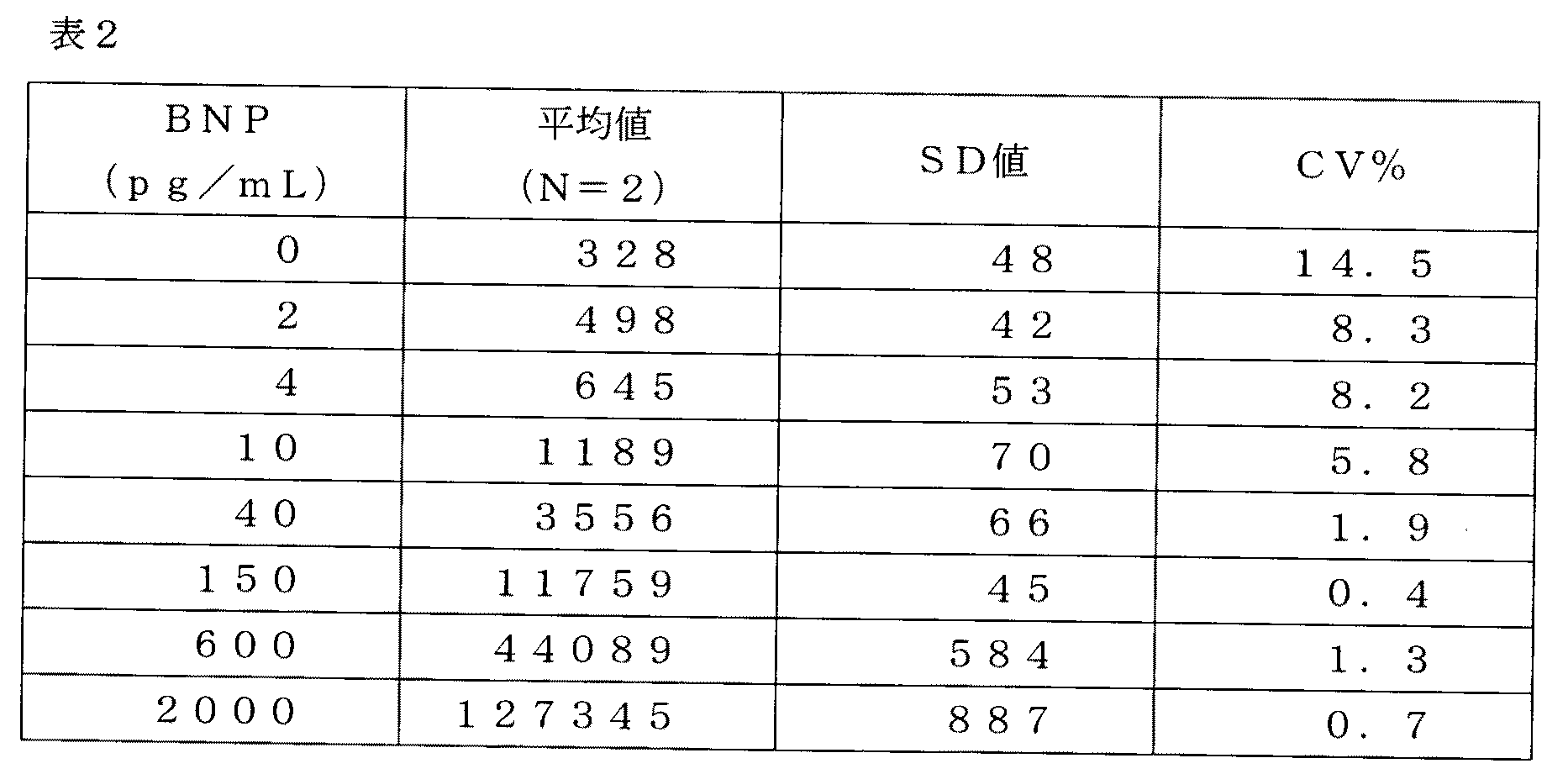
注した。ここに、R1抗体(塩野義製薬株式会社製、MI02シオノギBNP(商品名)、BNP第一抗体試薬)2μL、R2抗体(塩野義製薬株式会社製、MI02シオノギBNP(商品名)、BNP第二抗体試薬)0.5μLと標準試薬O(塩野義製薬株式会社製、MI02シオノギBNP(商品名)、標準BNP試薬)12.5μLと磁性粒子(マグナビート株式会社製、Therma−Max(登録商標) LA Avidin、商品コードTML001、濃度4mg/mL、平均粒径110nm)20μLの混合液を35μL加えてピペッティングにて攪拌し、30℃で5分間反応させた。反応終了後、反応混合物に凝集剤30μLを加えてピペッティングにて攪拌し、30℃で30秒反応後、Magna−Stand6((商品名)、マグナビート株式会社製、商品コードTMM001)にセットし、30℃で1分間磁気分離し、その後、上清を除去した。洗浄液(塩野義製薬株式会社製、MI02シオノギBNP(商品名)、ブロック液)100μLにて沈殿物を再分散し、凝集剤30μLを加えピペッティングにて攪拌し、30℃で30秒反応後、30℃で1分間磁気分離し、洗浄を行なった。洗浄は同様の手順で2回繰り返した。最後に洗浄液100μLにて沈殿物を再分散し、全量をマイクロプレートに移し、APS−5(Lumigen社製、商品コードAP5−101)100μLを混合し、5秒間攪拌した後、10秒反応させ、マルチラベルプレートリーダー(ベルトールドジャパン株式会社製、Mithras LB940(商品名))にて0.1秒間発光強度を測定した。測定結果を表2に示した。ここでは、凝集剤として、1M Na2SO4水溶液を用いた。
に適した測定方法であり、例えばBNPの検査に利用することができる。
Claims (9)
- 検体と、標識物質で標識された第1抗体とを混合して混合液を調製する工程、
互いに親和性を有する2種類の結合材の一方が結合した第2抗体と、該2種類の結合材の他方が結合した磁性粒子を、前記混合液に添加する工程、
前記磁性粒子を回収する工程、及び
前記標識を検出する工程
を含み、
前記第1抗体と前記第2抗体は測定対象物質に対する結合能を有し、その結合に際して互いに競合しないことを特徴とする、
検体中の測定対象物質の濃度を測定する方法。 - 前記第2抗体と前記磁性粒子とを、前記混合液に同時に添加することを特徴とする、請求項1に記載の方法。
- 前記第2抗体を前記混合液に添加した後に、前記磁性粒子を添加することを特徴とする、請求項1に記載の方法。
- 前記磁性粒子を前記混合液に添加した後に、前記第2抗体を添加することを特徴とする、請求項1に記載の方法。
- 前記磁性粒子が、1〜1000nmの平均粒径であることを特徴とする、請求項1〜4のいずれか一項に記載の方法。
- 前記磁性粒子が、50〜200nmの平均粒径であることを特徴とする、請求項5に記載の測定方法。
- 前記第1抗体及び前記第2抗体の少なくとも一方がモノクローナル抗体である、請求項1〜6のいずれか一項に記載の方法。
- 前記測定対象物質がペプチドである、請求項1〜7のいずれか一項に記載の方法。
- 前記ペプチドが脳性ナトリウム利尿ペプチドである、請求項8に記載の方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008194754A JP5104622B2 (ja) | 2008-07-29 | 2008-07-29 | 磁性粒子を用いた測定対象物質の濃度測定法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008194754A JP5104622B2 (ja) | 2008-07-29 | 2008-07-29 | 磁性粒子を用いた測定対象物質の濃度測定法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010032360A true JP2010032360A (ja) | 2010-02-12 |
| JP5104622B2 JP5104622B2 (ja) | 2012-12-19 |
Family
ID=41737010
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008194754A Active JP5104622B2 (ja) | 2008-07-29 | 2008-07-29 | 磁性粒子を用いた測定対象物質の濃度測定法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5104622B2 (ja) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8426214B2 (en) | 2009-06-12 | 2013-04-23 | University Of Washington | System and method for magnetically concentrating and detecting biomarkers |
| US8507283B2 (en) | 2007-03-08 | 2013-08-13 | University Of Washington | Stimuli-responsive magnetic nanoparticles and related methods |
| US9080933B2 (en) | 2009-11-09 | 2015-07-14 | University Of Washington Through Its Center For Commercialization | Stimuli-responsive polymer diagnostic assay comprising magnetic nanoparticles and capture conjugates |
| EP2797081A4 (en) * | 2011-12-21 | 2016-04-06 | Jnc Corp | METHOD FOR REMOVING CÉSIUM IONS IN AQUEOUS SOLUTION THROUGH MAGNETIC PARTICLES |
| JP2016121940A (ja) * | 2014-12-25 | 2016-07-07 | Jnc株式会社 | アプタマーを用いた検査診断方法 |
| WO2020031436A1 (ja) | 2018-08-06 | 2020-02-13 | コニカミノルタ株式会社 | 脳性ナトリウム利尿ペプチドの測定方法および脳性ナトリウム利尿ペプチドの測定キット |
| WO2020171158A1 (ja) * | 2019-02-20 | 2020-08-27 | 株式会社パートナーファーム | 固相反応チップ及びこれを用いた測定方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH05180836A (ja) * | 1991-12-26 | 1993-07-23 | Fujirebio Inc | 免疫測定用試薬の安定保存方法 |
| JPH10111293A (ja) * | 1996-10-04 | 1998-04-28 | Hitachi Ltd | 免疫測定装置 |
| JP2005505757A (ja) * | 2001-09-18 | 2005-02-24 | ファイブローゲン、インコーポレーテッド | 結合組織増殖因子の分析方法 |
| JP2005200422A (ja) * | 1994-02-07 | 2005-07-28 | Yeda Research & Development Co Ltd | インターフェロンα/β結合タンパク質およびその製造法 |
| JP2006162467A (ja) * | 2004-12-08 | 2006-06-22 | Kyowa Medex Co Ltd | 光透過性磁性粒子を用いた免疫測定方法 |
-
2008
- 2008-07-29 JP JP2008194754A patent/JP5104622B2/ja active Active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH05180836A (ja) * | 1991-12-26 | 1993-07-23 | Fujirebio Inc | 免疫測定用試薬の安定保存方法 |
| JP2005200422A (ja) * | 1994-02-07 | 2005-07-28 | Yeda Research & Development Co Ltd | インターフェロンα/β結合タンパク質およびその製造法 |
| JPH10111293A (ja) * | 1996-10-04 | 1998-04-28 | Hitachi Ltd | 免疫測定装置 |
| JP2005505757A (ja) * | 2001-09-18 | 2005-02-24 | ファイブローゲン、インコーポレーテッド | 結合組織増殖因子の分析方法 |
| JP2006162467A (ja) * | 2004-12-08 | 2006-06-22 | Kyowa Medex Co Ltd | 光透過性磁性粒子を用いた免疫測定方法 |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8507283B2 (en) | 2007-03-08 | 2013-08-13 | University Of Washington | Stimuli-responsive magnetic nanoparticles and related methods |
| US8426214B2 (en) | 2009-06-12 | 2013-04-23 | University Of Washington | System and method for magnetically concentrating and detecting biomarkers |
| US9080933B2 (en) | 2009-11-09 | 2015-07-14 | University Of Washington Through Its Center For Commercialization | Stimuli-responsive polymer diagnostic assay comprising magnetic nanoparticles and capture conjugates |
| US9429570B2 (en) | 2009-11-09 | 2016-08-30 | University Of Washington Through Its Center For Commercialization | Stimuli-responsive polymer diagnostic assay comprising magnetic nanoparticles and capture conjugates |
| EP2797081A4 (en) * | 2011-12-21 | 2016-04-06 | Jnc Corp | METHOD FOR REMOVING CÉSIUM IONS IN AQUEOUS SOLUTION THROUGH MAGNETIC PARTICLES |
| JP2016121940A (ja) * | 2014-12-25 | 2016-07-07 | Jnc株式会社 | アプタマーを用いた検査診断方法 |
| WO2020031436A1 (ja) | 2018-08-06 | 2020-02-13 | コニカミノルタ株式会社 | 脳性ナトリウム利尿ペプチドの測定方法および脳性ナトリウム利尿ペプチドの測定キット |
| WO2020171158A1 (ja) * | 2019-02-20 | 2020-08-27 | 株式会社パートナーファーム | 固相反応チップ及びこれを用いた測定方法 |
| JPWO2020171158A1 (ja) * | 2019-02-20 | 2021-12-23 | 株式会社パートナーファーム | 固相反応チップ及びこれを用いた測定方法 |
| JP7205940B2 (ja) | 2019-02-20 | 2023-01-17 | 株式会社パートナーファーム | 固相反応チップ及びこれを用いた測定方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5104622B2 (ja) | 2012-12-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN105548565B (zh) | 一种用于检测克氏锥虫抗体的试剂盒及其制备和应用 | |
| RU2608656C2 (ru) | Связанные со стрептавидином магнитные частицы и способ их изготовления | |
| Ha et al. | Recent developments in innovative magnetic nanoparticles-based immunoassays: from improvement of conventional immunoassays to diagnosis of COVID-19 | |
| JP5104622B2 (ja) | 磁性粒子を用いた測定対象物質の濃度測定法 | |
| CN104698184B (zh) | 检测糖类抗原的试剂盒 | |
| Yang et al. | Automated support-resolution strategy for a one-way chemiluminescent multiplex immunoassay | |
| CN107543932A (zh) | 一种降钙素的磁微粒化学发光检测试剂盒及制备方法 | |
| CN101566626A (zh) | 一种抗原检测方法及其应用 | |
| CN102323417B (zh) | 胃蛋白酶原i(pgi)定量测定试剂盒及其检测方法 | |
| WO2019088142A1 (ja) | バイオアッセイのための検出剤及びそれを用いたシグナルの増幅方法 | |
| CN108020666A (zh) | 一种可同时定量检测血液中cea和ca19-9的磁性免疫层析试纸条及制备方法 | |
| EP3929584A1 (en) | Method for measuring thyroglobulin | |
| CN106645756A (zh) | 一种检测nmp22的试剂盒及其制备方法 | |
| CN1773281A (zh) | 免疫胶体金粒子荧光淬灭的测量方法 | |
| CN108872594A (zh) | 一种甲胎蛋白检测试剂盒及其制备方法 | |
| CN109142753A (zh) | 鳞状上皮细胞癌抗原化学发光免疫检测试剂盒及其制备方法 | |
| CN106415271A (zh) | 用于执行多重分析方法的对照 | |
| CN115718134B (zh) | 一种基于镧系纳米探针同时检测多种乳腺癌生物标志物的分析方法 | |
| Huang et al. | Development of up-converting phosphor technology-based lateral flow assay for quantitative detection of serum PIVKA-II: Inception of a near-patient PIVKA-II detection tool | |
| CN112166323A (zh) | 自身抗体的直接免疫测定测量 | |
| CN102004146B (zh) | 一种混合标记物质和标记方法及其应用 | |
| CN114563578A (zh) | 人膜性肾病诊断试剂盒 | |
| JP2010101703A (ja) | 免疫学的測定方法および測定用試薬キット | |
| CN104777317B (zh) | 一种金纳米粒子探针的制备及其在快速免疫检测中的应用 | |
| JPH02124462A (ja) | 改良免疫測定法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110204 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20110331 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120131 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20120131 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120306 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120904 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120917 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5104622 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20151012 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |