JP2010030937A - 新規なジカルバゾリルフェニル誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 - Google Patents
新規なジカルバゾリルフェニル誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 Download PDFInfo
- Publication number
- JP2010030937A JP2010030937A JP2008193206A JP2008193206A JP2010030937A JP 2010030937 A JP2010030937 A JP 2010030937A JP 2008193206 A JP2008193206 A JP 2008193206A JP 2008193206 A JP2008193206 A JP 2008193206A JP 2010030937 A JP2010030937 A JP 2010030937A
- Authority
- JP
- Japan
- Prior art keywords
- group
- layer
- dicarbazolylphenyl
- derivative
- transport layer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- YXFVVABEGXRONW-UHFFFAOYSA-N Cc1ccccc1 Chemical compound Cc1ccccc1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 55
- 0 *C*c1c(CC**)c(C*)c(**)c2c1-c1c(*C=**)c(O*)c(*)c(*N)c1*2C1C=C(*2c3c(*(*)*)c(O)c(*)c(*)c3-c3c(*)c(*)c(*)c(*)c23)C=C*1 Chemical compound *C*c1c(CC**)c(C*)c(**)c2c1-c1c(*C=**)c(O*)c(*)c(*N)c1*2C1C=C(*2c3c(*(*)*)c(O)c(*)c(*)c3-c3c(*)c(*)c(*)c(*)c23)C=C*1 0.000 description 6
- ABMKWMASVFVTMD-UHFFFAOYSA-N Cc1ccccc1-c1c(C)cccc1 Chemical compound Cc1ccccc1-c1c(C)cccc1 ABMKWMASVFVTMD-UHFFFAOYSA-N 0.000 description 4
- UJOBWOGCFQCDNV-UHFFFAOYSA-N c1ccc2[nH]c(cccc3)c3c2c1 Chemical compound c1ccc2[nH]c(cccc3)c3c2c1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N c1ccncc1 Chemical compound c1ccncc1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- WCFAPJDPAPDDAQ-UHFFFAOYSA-N C1N=CC=CN1 Chemical compound C1N=CC=CN1 WCFAPJDPAPDDAQ-UHFFFAOYSA-N 0.000 description 1
- ZEFGUWRQFNTGGX-UHFFFAOYSA-N C1NN=CC=C1 Chemical compound C1NN=CC=C1 ZEFGUWRQFNTGGX-UHFFFAOYSA-N 0.000 description 1
- UKDLIQSUEPAXPJ-NODMUBTPSA-N CC(C)/C(/[n]1c2ccccc2c2c1cccc2)=C\C(\[n]1c2ccccc2c2c1cccc2)=C/c1cncnc1 Chemical compound CC(C)/C(/[n]1c2ccccc2c2c1cccc2)=C\C(\[n]1c2ccccc2c2c1cccc2)=C/c1cncnc1 UKDLIQSUEPAXPJ-NODMUBTPSA-N 0.000 description 1
- IGEYQCUSAYMNAC-UHFFFAOYSA-N CC(C1)C([n]2c3ccccc3c3c2cccc3)=CC=C1C1(C)C(C2C(c(cc3)ccc3-[n]3c(cccc4)c4c4c3cccc4)=CC=CC2)=CC=CC1 Chemical compound CC(C1)C([n]2c3ccccc3c3c2cccc3)=CC=C1C1(C)C(C2C(c(cc3)ccc3-[n]3c(cccc4)c4c4c3cccc4)=CC=CC2)=CC=CC1 IGEYQCUSAYMNAC-UHFFFAOYSA-N 0.000 description 1
- RVUIKWBRUBEOMW-BYNWCGPESA-N CC(C1)C=Cc(c2ccccc22)c1[n]2/C1=C/C(C)(C)C(C2)=CC=CN2C(C)(C)/C(/[n]2c(cccc3)c3c3c2cccc3)=C1 Chemical compound CC(C1)C=Cc(c2ccccc22)c1[n]2/C1=C/C(C)(C)C(C2)=CC=CN2C(C)(C)/C(/[n]2c(cccc3)c3c3c2cccc3)=C1 RVUIKWBRUBEOMW-BYNWCGPESA-N 0.000 description 1
- QMFJIJFIHIDENY-UHFFFAOYSA-N CC1=CC=CCC1 Chemical compound CC1=CC=CCC1 QMFJIJFIHIDENY-UHFFFAOYSA-N 0.000 description 1
- IORRUKOUOGHOLX-UHFFFAOYSA-N CC1C=CC(c2c(C)cccc2)=C(C)C1 Chemical compound CC1C=CC(c2c(C)cccc2)=C(C)C1 IORRUKOUOGHOLX-UHFFFAOYSA-N 0.000 description 1
- ZNKKYYNWFKHNHZ-UHFFFAOYSA-N CC1C=CC=CC1 Chemical compound CC1C=CC=CC1 ZNKKYYNWFKHNHZ-UHFFFAOYSA-N 0.000 description 1
- BEZLOGBEFSQIBW-UHFFFAOYSA-N CN1N=CC=CC1 Chemical compound CN1N=CC=CC1 BEZLOGBEFSQIBW-UHFFFAOYSA-N 0.000 description 1
- MXNCVMWPUAIYLH-YWEYNIOJSA-N Cc1c(/C=C\C=C)[nH]c2c1cccc2 Chemical compound Cc1c(/C=C\C=C)[nH]c2c1cccc2 MXNCVMWPUAIYLH-YWEYNIOJSA-N 0.000 description 1
- YHXLUVHGBYHQDQ-UHFFFAOYSA-N Cc1cccc(-[n]2c3ccccc3c3c2CCC=C3)c1 Chemical compound Cc1cccc(-[n]2c3ccccc3c3c2CCC=C3)c1 YHXLUVHGBYHQDQ-UHFFFAOYSA-N 0.000 description 1
- QVUJWELWWCBLAS-UHFFFAOYSA-N Cc1ccccc1C1=C(C)C=CCC1 Chemical compound Cc1ccccc1C1=C(C)C=CCC1 QVUJWELWWCBLAS-UHFFFAOYSA-N 0.000 description 1
- UCJDCGANFAKTKA-UHFFFAOYSA-N Cc1nc(C)ncn1 Chemical compound Cc1nc(C)ncn1 UCJDCGANFAKTKA-UHFFFAOYSA-N 0.000 description 1
- CAWHJQAVHZEVTJ-UHFFFAOYSA-N Cc1nccnc1 Chemical compound Cc1nccnc1 CAWHJQAVHZEVTJ-UHFFFAOYSA-N 0.000 description 1
- YIUOAAUFVBZQPM-UHFFFAOYSA-N Cc1ncncn1 Chemical compound Cc1ncncn1 YIUOAAUFVBZQPM-UHFFFAOYSA-N 0.000 description 1
- VFUDMQLBKNMONU-UHFFFAOYSA-N c(cc1)cc(c2c3cccc2)c1[n]3-c(cc1)ccc1-c(cc1)ccc1-[n]1c(cccc2)c2c2ccccc12 Chemical compound c(cc1)cc(c2c3cccc2)c1[n]3-c(cc1)ccc1-c(cc1)ccc1-[n]1c(cccc2)c2c2ccccc12 VFUDMQLBKNMONU-UHFFFAOYSA-N 0.000 description 1
- MZYDBGLUVPLRKR-UHFFFAOYSA-N c(cc1c2ccccc22)ccc1[n]2-c1cccc(-[n]2c(cccc3)c3c3c2cccc3)c1 Chemical compound c(cc1c2ccccc22)ccc1[n]2-c1cccc(-[n]2c(cccc3)c3c3c2cccc3)c1 MZYDBGLUVPLRKR-UHFFFAOYSA-N 0.000 description 1
- PBMFSQRYOILNGV-UHFFFAOYSA-N c1cnncc1 Chemical compound c1cnncc1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 1
Images
Landscapes
- Electroluminescent Light Sources (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
そこでこの問題を解決する目的で、近年リン光材料による有機EL素子の検討がなされている(非特許文献1)。
リン光材料は、従来の蛍光材料と異なり、三重項励起状態を使用することができるため量子効率が非常に高く、エネルギー失活がほとんどなく内部発光量子収率でほぼ100%に達する材料である。
しかしこのリン光材料は、濃度消光を起こしやすいため蛍光材料と同様にホスト材料との併用が必要になってくる。
高効率発光を得るためには、輸送材料やホスト材料の最適化を図らないといけないが、リン光材料は蛍光材料と異なり三重項エネルギーを完全に閉じ込めないと満足な効果が得られない。特に青色の材料に関してはエネルギーレベルが非常に高い。そのためにこれまで使用されていた4,4′−ジ(N−カルバゾール)−1,1′−ビフェニル(CBP)では十分なエネルギーの閉じ込めができない。これまでこの青色リン光エネルギーを満足に閉じ込めることのできるワイドギャップ化されたホスト材料はほとんどなく、青色リン光材料の開発を妨げる一つの要因になっていた。
で示されることを特徴とするジカルバゾリルフェニル誘導体に関する。
本発明の第2は、下記一般式(2)
で示されることを特徴とするジカルバゾリルフェニル誘導体に関する。
本発明の第3は、請求項1または2記載のジカルバゾリルフェニル誘導体よりなるホスト材料に関する。
本発明の第4は、請求項1または2記載のジカルバゾリルフェニル誘導体を用いた有機エレクトロルミネッセンス素子に関する。
またR4〜R19の炭素数6〜20のアリール基としては、フェニル基、ナフチル基、アントラニル基などを例示することができる。これらのアリール基には前記で例示したような炭素数1〜6の直鎖または分岐のアルキル基が付加していても構わない。
R20〜R35における炭素数1〜4の直鎖または分岐のアルキル基としては、メチル、エチル、n−プロピル、iso−プロピル、n−ブチル、iso−ブチル、sec−ブチル、tert−ブチルなどを挙げることができる。
溶媒に対する原料の溶解性が反応進行の鍵になるため、好ましくはトルエンとアルコール系の混合溶媒、より好ましくはトルエンとエタノールの混合溶媒である。
反応で使用する塩基類に関しては、アルカリ金属を含むものであれば特に限定されるものではない。例示すれば、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化セシウムのような水酸化物、炭酸リチウム、炭酸ナトリウム、炭酸カリウム、炭酸セシウムなような炭酸塩、炭酸水素リチウム、炭酸水素ナトリウム、炭酸水素カリウム、炭酸水素セシウムのような重炭酸塩あるいはリチウム、ナトリウム、カリウムあるいはセシウムなどのアルカリ金属のアルコラート、酢酸塩などの有機塩基である。好ましくは、炭酸塩もしくはアルコラートである。より好ましくは上記で述べた溶媒類に可溶な炭酸塩(化9ではNa2CO3を例示)であり、反応時間を考慮した場合炭酸ナトリウムである。
反応で使用するパラジウムについては、第一反応はハロゲン化合物とホウ酸化合物とのカップリング反応であるため、Pd(0)のものが使用できる。好ましくは、テトラキス(トリフェニルホスフィン)パラジウムあるいはトリス(ジベンジリデンアセトン)ジパラジウムであり、より好ましくはパラジウム化合物の反応性よりテトラキス(トリフェニルホスフィン)パラジウム〔Pd(pph3)4〕である。
またパラジウムを活性化するために添加するリン触媒については、第3アルキルホスフィンを使用することができる。例えば、トリメチルホスフィン、トリエチルホスフィン、トリ〔n−(iso−)プロピル〕ホスフィン、トリ〔n−(iso−、tert−)ブチル〕ホスフィンを挙げることができる。好ましくは、トリ〔n−(iso−、tert−)ブチル〕ホスフィン、より好ましくは、トリ(tert−ブチル)ホスフィンを挙げることができる。
ここで使用する溶媒としては、トルエン、キシレン、エチルベンゼン、テトラリン、デカリンなどの芳香族炭化水素系の溶媒で、原料のカルバゾールと反応するハロゲンを含有しないものであれば特に限定されるものではない。好ましくは、トルエン、キシレンおよびエチルベンゼンであり、より好ましくはキシレンである。キシレンに関しては、o−,m−,p−の3種類の異性体が存在するが、これらが必ずしも分離されている必要はなく単一のものでも2種類以上の異性体が混合していても構わない。
本発明の有機EL素子の発光を効率よく取り出すために、陽極または陰極の少なくとも一方の電極は透明もしくは半透明であることが好ましい。
ホール注入材料としては、下記化学式に示されるPEDOT−PSS(ポリマー混合物)やDNTPDを挙げることができる。
電子注入材料としては、下記化学式に示されるフッ化リチウム(LiF)や8−ヒドロキシキノリノラトリチウム錯体(Liq)などを挙げることができるが、本出願人の特願2006−292032号にかかげるフェナントロリン誘導体のリチウム錯体(LiPB)や特願2007−29695号に掲げるフェノキシピリジンのリチウム錯体(LiPP)を用いることもできる。
よって本発明の化合物は、素子を高効率化させるために必要なものであり、工業的に極めて重要なものである。
3−〔3,5−ジ(カルバゾール−9−イル)フェニル〕ピリジン(略称DCzPyB)の合成
1)3−(3,5−ジブロモフェニル)ピリジン(略称DBrPyB)の合成
精製はカラムクロマトグラフィー法(展開溶媒:クロロホルム/酢酸エチル=1/2,クロロホルム/酢酸エチル/メタノール=10/20/1)を行った。3−(3,5−ジブロモフェニル)ピリジン〔3−(3,5−Dibromo−phenyl)pyridine〕(DBrPyB) 収量:9.33g,収率:49.7%、
構造の確認は1H−NMRで行い、その結果を図1に示す。
2)3−〔3,5−ジ(カルバゾール−9−イル)フェニル〕ピリジン(略称DCzPyB)の合成
精製はカラムクロマトグラフィー法(展開溶媒:クロロホルム)を行い、白色の固体を得た。収率:73.4%。
構造の確認は1H−NMR、13C−NMRと質量分析(MS)で行った。1H−NMRのチャートを図2に、13C−NMRのチャートを図3に示す。またMSの結果、得られたクロマトグラフを図4に、スペクトルを図5に示す。
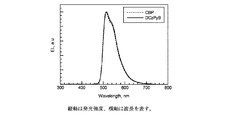
得られた3−〔3,5−ジ(カルバゾール−9−イル)フェニル〕ピリジン(略称DCzPyB)の蒸着膜(厚み500nm)の紫外線吸収スペクトル(Abs)と蛍光スペクトル(PL)を図6に示す。
また電気化学特性を表1に示す。
Ea:エネルギーアフィニティ(電子親和力)(Ip−Eg)に相当する
Eg:エネルギーギャップ:UVの吸収端より求めた。
エネルギーギャップ(Eg)については、蒸着機で作成した薄膜を紫外−可視吸光度計で薄膜の吸収曲線を測定する。その薄膜の短波長側の立ち上がりのところに接線を引き、求まった交点の波長W(nm)を次の式に代入し目的の値を求める。それによって得た値がEgになる。
Eg=1240÷W
例えば接線を引いて求めた値W(nm)が470nmだったとしたらこの時のEgの値は
Eg=1240÷470=2.63(eV)
と言うことになる。
IP(イオン化ポテンシャル)はイオン化ポテンシャル測定装置(例えば理研計器AC−3)を使用して測定し、測定するサンプルがイオン化を開始したところの電圧(eV)の値を読む。
Ea(電子親和力)は、IpからEgを引いた値である。
3−〔3,5−ジ(カルバゾール−9−イル)フェニル〕ピリジン(略称DCzPyB)の熱特性を表2に示す。
Tm :融点
Td5:目的物を加熱していき、熱分解により重量減少が5%発生した時点の
温度を指す。
実施例1で合成した3−〔3,5−ジ(カルバゾール−9−イル)フェニル〕ピリジン(略称DCzPyB)の蒸着膜(厚み500nm)を作成し、リン光スペクトルを測定した。またDCzPyBにFIrpicを3wt%ドープした膜(厚み500nm)を作成し、それぞれのリン光減衰曲線を測定した。
DCzPyBのリン光減衰曲線を図7に、DCzPyBの蒸着膜にFIrpicを3wt%ドープして得られた膜のリン光減衰曲線を図8に示す。これによりドーパントの励起子が閉じこめられ、リン光だけが出ているかどうかを調べている。
図8において、0μsからまっすぐ立上って、そのまま減衰して行く直線は、リン光が減衰して行くときの理想である。リン光ドーパントからのリン光の衰退については、他の因子がない場合、この直線にのるような感じで減衰する。一方、ギザギザ状のラインは実測したラインである。大局的にみて、実測ラインがほぼ理想の直線状であると解釈できることから、このケースではドーパントからの発光だけがおこっているものと解される。
ホスト材料の三重項レベルとFIrpicへの三重項エネルギー閉じこめ効果の相関関係を表3に示す。
IPL:PL強度
t :減衰時間
ET :各材料の三重項レベルの状態を示すもの
onest:各材料の三重項エネルギーの立ち上り部を示すもの
peak :各材料の三重項エネルギーのピークを示すもの
τ :組成物の寿命
μs:マイクロ秒
A*:励起状態における組成物の発光量
−:測定不能
表3は、図7と関係している。DCzPyBのリン光の立ち上りは438nm(2.83eV)のところからはじまり、449nm(2.76eV)で極大に達している。一方、FIrpicのリン光の立ち上りは452nm(2.74eV)からはじまり、469nm(2.64eV)で極大に達するものであるから、図7で得られた結果から、DCzPyBのリン光の方が早く立ち上りはじめて、FIrpicのリン光の立ち上りの手前で極大になり、この極大のエネルギーよりFIrpicが立ち上るという関係が成り立っている。このようにホストはドーパントより早く立ち上り、早く極大をむかえなければ、ドーパントをよりよく発光させることはできない。
実施例1で合成した3−〔3,5−ジ(カルバゾール−9−イル)フェニル〕ピリジン(略称DCzPyB)をホスト材料に使用した青色リン光素子を作成した。また比較のためにホスト材料にCBPを用いた素子もあわせて作成し、両者の比較を行った。
素子構造:
実施例3●:ITO/TPDPES(20nm)(ホール注入層)/3DTAPBP(30nm)(ホール輸送層)/DCzPyB:FIrpic(13wt%)(10nm)(発光層)/tetra−mPyPhBP(40nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm);
比較例1○:ITO/TPDPES(20nm)(ホール注入層)/3DTAPBP(30nm)(ホール輸送層)/CBP:FIrpic(13wt%)(10nm)(発光層)/tetra−mPyPhBP(40nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm).
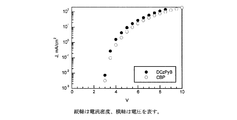
電流密度−電圧特性は図9に、
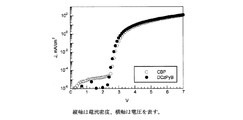
輝度−電圧特性は図10に、
視感効率−電圧特性は図11に、
電流効率−電圧特性は図12に、
視感効率−輝度特性は図13に、
外部量子効率−輝度特性は図14に
エレクトロルミネッセンス(EL)スペクトルは図15に、
拡大図は図16に、
それぞれ示す。
100cd/m2時の電圧、電流密度、視感効率および外部量子効率を表4に示す。
実施例1で合成した3−〔3,5−ジ(カルバゾール−9−イル)フェニル〕ピリジン(略称DCzPyB)をホスト材料に使用した青色リン光素子を作成した。また比較のためにホスト材料にCBPを用いた素子もあわせて作成し両者の比較を行った。
素子構造:
比較例2○:ITO/TPDPES(20nm)(ホール注入層)/TAPC(30nm)/CBP:Ir(PPy)3(8wt%)(10nm)(発光層)/TpPyPhB(50nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm);
実施例4●:ITO/TPDPES(20nm)/TAPC(30nm)/DCzPyB:Ir(PPy)3(8wt%)(10nm)(発光層)/TpPyPhB(50nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm).
電流密度−電圧特性は図17に、
輝度−電圧特性は図18に、
視感効率−電圧特性は図19に、
電流効率−電圧特性は図20に、
視感効率−輝度特性は図21に、
外部量子効率−輝度特性は図22に、
エレクトロルミネッセンス(EL)スペクトルは図23に、
それぞれ示す。
100cd/m2時の電圧、電流密度、視感効率および外部量子効率を表6に示す。
実施例1で合成した3−〔3,5−ジ(カルバゾール−9−イル)フェニル〕ピリジン(略称DCzPyB)のホールと電子の移動特性を調べるために、以下に示すような素子を作成した。
素子構造:
実施例5○:ITO/α−NPD(50nm)(ホール輸送層)/DCzPyB(10nm)(発光層)/Alq3(50nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm)
この素子の
電流密度−電圧特性は図24に、
輝度−電圧特性は図25に、
エレクトロルミネッセンス(EL)スペクトルは図26に、
それぞれ示す。
電子輸送層側(Alq3)およびホール輸送層側(α−NPD)由来の発光比率(@0.625mA/cm2)の結果を表8に示す。@は、単位電流密度を示す。
fAlq3は、Alq3での励起子の発光確率
この表から、電子輸送能がホール輸送性に比べて約5倍(0.84÷0.16)高いことが判る。
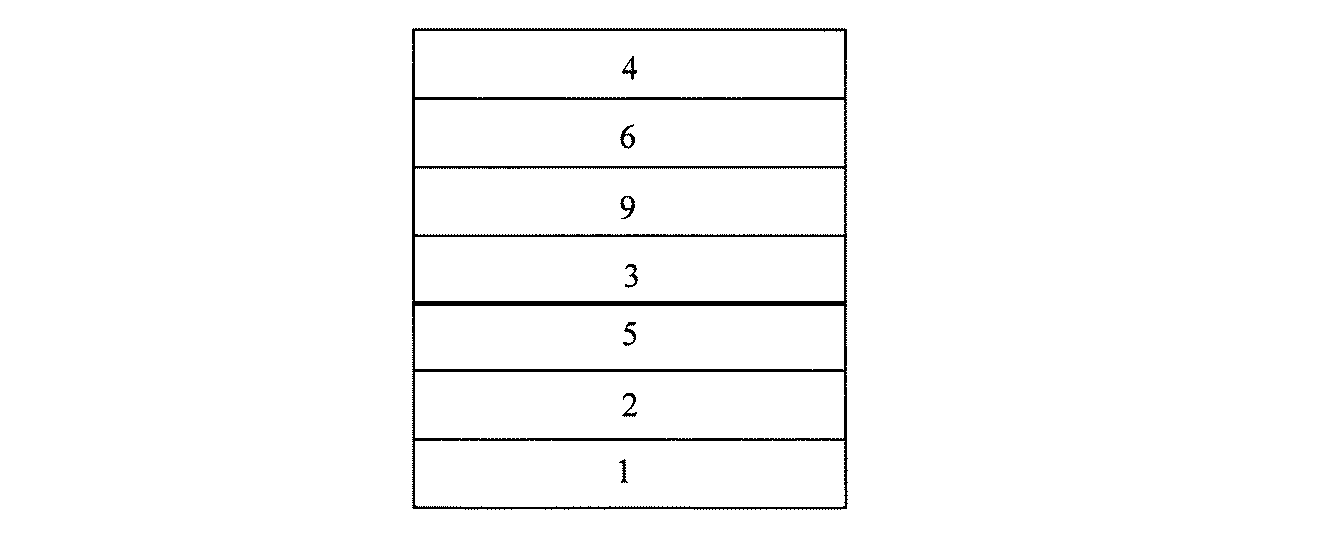
2 陽極(ITO)
3 発光層
4 陰極
5 正孔(ホール)輸送層
6 電子輸送層
7 正孔(ホール)注入層
8 電子注入層
9 正孔(ホール)ブロック層
Claims (4)
- 下記一般式(1)
で示されることを特徴とするジカルバゾリルフェニル誘導体。 - 下記一般式(2)
で示されることを特徴とするジカルバゾリルフェニル誘導体。 - 請求項1または2記載のジカルバゾリルフェニル誘導体よりなるホスト材料。
- 請求項1または2記載のジカルバゾリルフェニル誘導体を用いた有機エレクトロルミネッセンス素子。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008193206A JP5371312B2 (ja) | 2008-07-28 | 2008-07-28 | 新規なジカルバゾリルフェニル誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008193206A JP5371312B2 (ja) | 2008-07-28 | 2008-07-28 | 新規なジカルバゾリルフェニル誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010030937A true JP2010030937A (ja) | 2010-02-12 |
| JP5371312B2 JP5371312B2 (ja) | 2013-12-18 |
Family
ID=41735887
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008193206A Active JP5371312B2 (ja) | 2008-07-28 | 2008-07-28 | 新規なジカルバゾリルフェニル誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5371312B2 (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111171010A (zh) * | 2020-01-13 | 2020-05-19 | 北京大学深圳研究生院 | 一种阴极电刺激响应材料及其制备方法 |
| WO2020111673A1 (ko) * | 2018-11-27 | 2020-06-04 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기 발광 소자 |
| US11746117B2 (en) | 2018-11-27 | 2023-09-05 | Lg Chem, Ltd. | Heterocyclic compound and organic light emitting device comprising same |
| US12022730B2 (en) | 2018-11-27 | 2024-06-25 | Lg Chem, Ltd. | Compound and organic light emitting device comprising the same |
| US12037337B2 (en) | 2018-11-27 | 2024-07-16 | Lg Chem, Ltd. | Compound and organic light emitting device comprising the same |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003080760A1 (en) * | 2002-03-22 | 2003-10-02 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescent devices and organic electroluminescent devices made by using the same |
| WO2005076669A1 (ja) * | 2004-02-09 | 2005-08-18 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子 |
| JP2006188493A (ja) * | 2004-12-10 | 2006-07-20 | Pioneer Electronic Corp | 有機化合物、電荷輸送材料および有機電界発光素子 |
| JP2006199679A (ja) * | 2004-12-24 | 2006-08-03 | Pioneer Electronic Corp | 有機化合物、電荷輸送材料および有機電界発光素子 |
| JP2006232813A (ja) * | 2005-01-25 | 2006-09-07 | Pioneer Electronic Corp | 有機化合物、電荷輸送材料及び有機電界発光素子 |
| WO2009031855A1 (en) * | 2007-09-05 | 2009-03-12 | Cheil Industries Inc. | Material for organic photoelectric device, and organic photoelectric device including the same |
-
2008
- 2008-07-28 JP JP2008193206A patent/JP5371312B2/ja active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003080760A1 (en) * | 2002-03-22 | 2003-10-02 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescent devices and organic electroluminescent devices made by using the same |
| WO2005076669A1 (ja) * | 2004-02-09 | 2005-08-18 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子 |
| JP2006188493A (ja) * | 2004-12-10 | 2006-07-20 | Pioneer Electronic Corp | 有機化合物、電荷輸送材料および有機電界発光素子 |
| JP2006199679A (ja) * | 2004-12-24 | 2006-08-03 | Pioneer Electronic Corp | 有機化合物、電荷輸送材料および有機電界発光素子 |
| JP2006232813A (ja) * | 2005-01-25 | 2006-09-07 | Pioneer Electronic Corp | 有機化合物、電荷輸送材料及び有機電界発光素子 |
| WO2009031855A1 (en) * | 2007-09-05 | 2009-03-12 | Cheil Industries Inc. | Material for organic photoelectric device, and organic photoelectric device including the same |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020111673A1 (ko) * | 2018-11-27 | 2020-06-04 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기 발광 소자 |
| US11746117B2 (en) | 2018-11-27 | 2023-09-05 | Lg Chem, Ltd. | Heterocyclic compound and organic light emitting device comprising same |
| US12022730B2 (en) | 2018-11-27 | 2024-06-25 | Lg Chem, Ltd. | Compound and organic light emitting device comprising the same |
| US12037337B2 (en) | 2018-11-27 | 2024-07-16 | Lg Chem, Ltd. | Compound and organic light emitting device comprising the same |
| US12098156B2 (en) | 2018-11-27 | 2024-09-24 | Lg Chem, Ltd. | Compound and organic light emitting device comprising the same |
| US12275736B2 (en) | 2018-11-27 | 2025-04-15 | Lg Chem, Ltd. | Compound and organic light emitting device comprising the same |
| CN111171010A (zh) * | 2020-01-13 | 2020-05-19 | 北京大学深圳研究生院 | 一种阴极电刺激响应材料及其制备方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5371312B2 (ja) | 2013-12-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5325402B2 (ja) | 新規なビカルバゾール誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 | |
| JP5063992B2 (ja) | 新規なジ(ピリジルフェニル)誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5207760B2 (ja) | 新規なピリミジン系またはトリアジン系誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5495578B2 (ja) | 新規なトリアリールホスフィンオキシド誘導体、それよりなるホスト材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP2008195623A (ja) | 新規な複素環含有ヒドロキシフェニル金属誘導体およびそれを用いた電子注入材料、電子輸送材料および有機エレクトロルミネッセンス素子 | |
| JP2008120696A (ja) | 新規なトリピリジルフェニル誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5783749B2 (ja) | エキシマー特性を有する1,8−アリール置換ナフタレン誘導体及びこれを用いた有機el素子 | |
| JP5201956B2 (ja) | 新規なジ(ピリジルフェニル)誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5727237B2 (ja) | 新規なビカルバゾリル誘導体、それよりなるホスト材料およびそれを用いた有機エレクトロルミネッセンス素子 | |
| JP5481076B2 (ja) | 新規な9,10−ジフェニルアントラセン誘導体、それよりなるホール輸送材料、発光材料およびそれを用いた有機エレクトロルミネッセンス素子 | |
| JP2008106015A (ja) | 新規なフェナントロリン誘導体、そのリチウム錯体、それを用いた電子輸送材料、電子注入材料および有機el素子 | |
| JP5220429B2 (ja) | 新規なジピレン誘導体、それよりなる電子輸送材料、発光材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5371312B2 (ja) | 新規なジカルバゾリルフェニル誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 | |
| JP5476034B2 (ja) | 新規なトリアリールアミン化合物、それよりなるホール輸送材料およびそれを用いた有機エレクトロルミネッセンス素子 | |
| JP5349889B2 (ja) | 新規なターフェニル誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5963467B2 (ja) | 単分子でエキシプレックス発光を示す化合物を用いた有機エレクトロルミネッセンス素子 | |
| JP2010013421A (ja) | 新規なビス(ジカルバゾリルフェニル)誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 | |
| JP2010090084A (ja) | 新規なビス(カルバゾリルフェニル)誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 | |
| JP6081210B2 (ja) | 単分子でエキシプレックス発光を示す化合物 | |
| JP5086608B2 (ja) | 新規なジ(フェナントロリン)誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP2010248112A (ja) | 芳香族炭化水素化合物、それよりなるホスト材料、それを用いた有機エレクトロルミネッセンス素子 | |
| JP5674266B2 (ja) | 新規なカルバゾール系誘導体、それよりなるホスト材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5798754B2 (ja) | 新規な置換ジフェニルカルバゾール誘導体、該誘導体よりなるホスト材料及び該誘導体を含む有機エレクトロルミネッセンス素子 | |
| JP5001914B2 (ja) | ビスホスフィンジオキサイド誘導体よりなるホスト材料およびビスホスフィンジオキサイド誘導体を含有する有機エレクトロルミネッセンス素子 | |
| JP5279377B2 (ja) | 新規なポリアルコキシキンクフェニル誘導体、それよりなるホスト材料およびそれを用いた有機エレクトロルミネッセンス素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100517 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110609 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130326 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130527 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130611 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130805 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130827 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130917 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5371312 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |