JP2010019767A - 検出方法、検出装置、検出用試料セルおよび検出用キット - Google Patents
検出方法、検出装置、検出用試料セルおよび検出用キット Download PDFInfo
- Publication number
- JP2010019767A JP2010019767A JP2008182227A JP2008182227A JP2010019767A JP 2010019767 A JP2010019767 A JP 2010019767A JP 2008182227 A JP2008182227 A JP 2008182227A JP 2008182227 A JP2008182227 A JP 2008182227A JP 2010019767 A JP2010019767 A JP 2010019767A
- Authority
- JP
- Japan
- Prior art keywords
- substance
- fluorescent
- detected
- liquid sample
- fluorescent label
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/648—Specially adapted constructive features of fluorimeters using evanescent coupling or surface plasmon coupling for the excitation of fluorescence
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54366—Apparatus specially adapted for solid-phase testing
- G01N33/54373—Apparatus specially adapted for solid-phase testing involving physiochemical end-point determination, e.g. wave-guides, FETS, gratings
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/01—Arrangements or apparatus for facilitating the optical investigation
- G01N21/03—Cuvette constructions
- G01N2021/0346—Capillary cells; Microcells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/01—Arrangements or apparatus for facilitating the optical investigation
- G01N21/03—Cuvette constructions
- G01N21/05—Flow-through cuvettes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/75—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated
- G01N21/77—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated by observing the effect on a chemical indicator
- G01N21/78—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated by observing the effect on a chemical indicator producing a change of colour
- G01N21/80—Indicating pH value
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S436/00—Chemistry: analytical and immunological testing
- Y10S436/805—Optical property
Landscapes
- Health & Medical Sciences (AREA)
- Immunology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Analytical Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Hematology (AREA)
- Molecular Biology (AREA)
- Urology & Nephrology (AREA)
- Biomedical Technology (AREA)
- Cell Biology (AREA)
- Medicinal Chemistry (AREA)
- Food Science & Technology (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Optics & Photonics (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Investigating Or Analysing Materials By The Use Of Chemical Reactions (AREA)
- Optical Measuring Cells (AREA)
- Automatic Analysis And Handling Materials Therefor (AREA)
Abstract
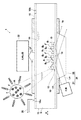
【解決手段】センサ14部上に、液体試料中の被検出物質Aの量に応じた量の蛍光標識結合物質BFを結合させ、この蛍光標識結合物質BFの蛍光標識Fの励起に起因して生じる光の量に基づいて、被検出物質の量を検出する検出方法において、蛍光標識Fとして、複数の蛍光色素分子を、該蛍光色素分子からの蛍光を透過する材料により包含してなる、液体試料中において該液体試料のpHに応じて荷電状態が変化する蛍光物質を用い、センサ部14に蛍光標識結合物質BFを結合させた状態で、液体試料のpHを調整して、蛍光物質Fの荷電状態を中性化することにより、蛍光物質Fをセンサ部14表面に引き寄せ、該蛍光物質Fを引き寄せた状態で被検出物質Aの量を検出する。
【選択図】図1
Description
前記センサ部に液体試料を接触させることにより、該センサ部上に、該液体試料中の被検出物質の量に応じた量の蛍光標識結合物質を結合させ、
前記センサ部に励起光を照射することにより、該センサ部上に増強した光電場を生じさせ、該増強した光電場内において前記蛍光標識結合物質の蛍光標識を励起し、該蛍光標識の励起に起因して生じる光の量に基づいて、前記被検出物質の量を検出する検出方法において、
前記蛍光標識として、複数の蛍光色素分子を、該蛍光色素分子からの蛍光を透過する材料により包含してなる、前記液体試料中において該液体試料のpHに応じて荷電状態が変化する蛍光物質を用い、
前記センサ部に前記蛍光標識結合物質を結合させた状態で、前記液体試料のpHを調整して、前記蛍光物質の荷電状態を中性化することにより、該蛍光物質を前記センサ部表面に引き寄せ、
該蛍光物質を引き寄せた状態で、前記被検出物質の量を検出することを特徴とする。
本明細書において、蛍光物質の粒径は、略球状の粒子の場合にはその直径であり、球状でない粒子の場合にはその最大幅と最小幅との平均の長さで定義するものとする。
また、「増強した光電場を生じさせる」とは、光電場を増強させることによって、増強した光電場を形成することを意味するものであり、光電場を増強させる方法は、プラズモン共鳴によるものであってもよいし、光導波モードの励起によるものであってもよい。
(1)前記励起光の照射により前記金属層にプラズモンを励起し、該プラズモンにより前記増強した光電場を生じさせ、前記蛍光標識の励起に起因して生じる前記光として、該励起によって該蛍光標識から生じる蛍光を検出することにより前記被検出物質の量を検出する。
前記センサチップを収容する収容部と、
前記センサ部に前記励起光を照射する励起光照射光学系と、
該励起光の照射により該センサ部上に生じた前記増強した光電場における、前記蛍光標識の励起に起因して生じる光を検出する光検出手段と、
前記センサチップに、pH調整液を注入して前記液体試料のpHを調整するpH調整手段とを備えたことを特徴とするものである。
液体試料が流下される流路を有する基台と、
前記流路の上流側に設けられた該流路に前記液体試料を注入するための注入口と、
前記流路の下流側に設けられた、前記注入口から注入された前記液体試料を該下流側に流すための空気孔と、
前記流路の、前記注入口と前記空気孔との間に設けられたセンサチップ部であって、前記流路の内壁面の少なくとも一部として設けられた誘電体プレートと、該プレートの試料接触面に設けられた少なくとも金属層を含むセンサ部とからなるセンサチップ部とを備えてなることを特徴とするものである。
液体試料が流下される流路を有する基台と、前記流路の上流側に設けられた該流路に前記液体試料を注入するための注入口と、前記流路の下流側に設けられた、前記注入口から注入された前記液体試料を該下流側に流すための空気孔と、前記流路の、前記注入口と前記空気孔との間に設けられたセンサチップ部であって、前記流路の内壁面の少なくとも一部として設けられた誘電体プレートと、該プレートの試料接触面に設けられた少なくとも金属層を含むセンサ部とからなるセンサチップ部と、該センサ部上に固定された、前記蛍光標識結合物質と結合する固定層とを備えた試料セル、および
前記液体試料と同時もしくは前記液体試料の流下後に、前記流路内に流下される、複数の蛍光色素分子を、該蛍光色素分子からの蛍光を透過する材料により包含してなる、前記液体試料中において該液体試料のpHに応じて荷電状態が変化する蛍光物質を、前記蛍光標識として含む前記蛍光標識結合物質を含んだ標識用溶液を備えてなることを特徴とするものである。
「検出方法および装置」
本発明の検出方法は、例えば図1に示すように、誘電体プレート11と、該プレート11の一面に設けられた少なくとも金属層12を含むセンサ部14とからなるセンサチップ10を用い、センサ部14に試料を接触させることにより、該センサ部14上に、該試料に含有される被検出物質Aの量に応じた量の蛍光標識結合物質BFを結合させ、センサ部14に励起光L0を照射することにより、センサ部14上に増強した光電場Dを生じさせ、該増強した光電場D内において、蛍光標識結合物質BFの蛍光標識Fの励起し、該蛍光標識の励起に起因して生じる光の量に基づいて、被検出物質Aの量を検出する検出方法であって、蛍光標識として、複数の蛍光色素分子fを、該蛍光色素分子fからの蛍光を透過する材料により包含してなる、液体試料中において該液体試料のpHに応じて荷電状態が変化する蛍光物質Fを用い、センサ部14に蛍光標識結合物質BFを結合させた状態で、液体試料のpHを調整して、蛍光物質の荷電状態を中性化することにより、該蛍光物質をセンサ部表面に引き寄せ、該蛍光物質Fを引き寄せた状態で被検出物質Aの量を検出することを特徴とする。
従来金属消光を防止する方法としては、金属層12上に自己組織化膜(SAM)を形成し、さらにカルボキシメチルデキストラン(CMD)膜を作製して金属膜と蛍光色素分子との距離を離す方法が知られている。しかしながら、金属膜上にこれらの金属消光を防止するための膜を設けるのは、センサチップ作製工程を複雑なものとし、非常に手間がかかる。一方、蛍光物質Fを用いれば、上述のような金属消光防止のための膜を設けることなく、非常に簡便な方法で効果的に金属消光を防止することができる。
まず、ポリスチレン粒子(Estapor社、φ500nm、10%solid、カルボキシル基、製品番号K1―050)を調液して0.1%solid in phosphate(ポリスチレン溶液:pH7.0)を作製する。
次に、蛍光色素(林原生物化学研究所 NK−2014(励起 〜780nm))0.3mgの酢酸エチル溶液(1mL)を作製する。
上記ポリスチレン溶液と蛍光色素溶液を混合し、エバポレートしながら含浸を行った後、遠心分離(15000rpm、4℃、20分を2回)を行い、上清を除去する。以上の工程により、ポリスチレンにより蛍光色素を内包してなる蛍光物質Fを得ることができる。このような手順で、ポリスチレン粒子に蛍光色素を含浸させて作製された蛍光物質Fの粒径はポリスチレン粒子の粒径と同一(上記例ではφ500nm)となる。なお、上記において用いるポリスチレン粒子は表面にpHに応じて荷電状態が変化する官能基であるカルボキシル基が修飾されており、蛍光物質Fは表面にカルボキシル基が修飾された、蛍光pHに応じて荷電状態が変化する蛍光物質である。
第1実施形態の検出方法および装置について図1を参照して説明する。図1は第1の実施形態の検出装置の概略構成を示す全体図である。本実施形態の検出方法および装置は、表面プラズモン共鳴により光電場を増強させ、増強された光電場において励起された蛍光を検出する蛍光検出方法および装置である。
金属膜12は、所定領域に開口を有するマスクをプレート11の一表面に形成し、既知の蒸着法で成膜形成することができる。金属膜12の厚みは、金属膜12の材料と、励起光の波長により表面プラズモンが強く励起されるように適宜定めることが望ましい。例えば、励起光として780nmに中心波長を有するレーザ光を用い、金属膜として金(Au)膜を用いる場合、金属膜の厚みは50nm±20nmが好適である。さらに好ましくは、47nm±10nmである。なお、金属膜は、Au、Ag、Cu、Al、Pt、Ni、Ti、およびこれらの合金からなる群より選択される少なくとも1種の金属を主成分とするものが好ましい。
ここでは、一例として、試料Sに含まれる被測定物質として抗原Aを検出する場合について説明する。
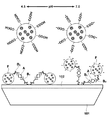
まず、試料保持部13中に検査対象である液体試料Sを流し、センサチップ10の金属膜12上に試料Sを接触させる。次いで同様に抗原Aと特異的に結合する第2の結合物質である2次抗体B2と蛍光標識Fとからなる蛍光標識結合物質(標識2次抗体)BFを含む溶液を流す。この場合、金属膜12に表面修飾される1次抗体B1と蛍光標識結合物質BFの2次抗体B2として、被検出物質である抗原Aに対して互いに別の部位に結合するものを用いる。なお、ここでは、蛍光標識として、蛍光色素分子fを内包する、カルボキシル基(−COOH)が表面に修飾されてなる蛍光物質Fを用いている。カルボキシル基は生理食塩水等のpH7.4近傍の液体試料中においてCOO−にイオン化し、pHを下げるとプロトン化してCOOHとなり電気的に中性化する。
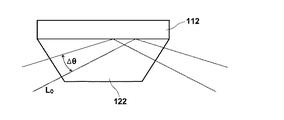
上述の各実施形態においては励起光Loとして、界面に所定の角度θで入射する平行光を入射するものとしたが、励起光としては、図3に模式的に示すような、角度θを中心に角度幅Δθを持つファンビーム(集束光)を用いてもよい。ファンビームの場合、プリズム122とプリズム上の金属膜112との界面に対して、角度θ―Δθ/2〜θ+Δθ/2の範囲の入射角度で入射することになり、この角度範囲内に共鳴角があれば、金属膜112に表面プラズモンを励起することができる。金属膜上への試料供給の前後において、金属膜上の媒質の屈折率が変化し、そのために表面プラズモンが生じる共鳴角が変化する。上述の実施形態のように平行光を励起光として用いる場合、共鳴角が変化するたびに平行光の入射角度を調整する必要がある。しかし、図3に示すような、界面に入射する入射角度に幅を持たせたファンビームを用いることにより、入射角度の調整をすることなく、共鳴角の変化に対応することができる。なお、ファンビームは入射角度による強度変化が少ないフラットな分布を持つものであることがより好ましい。
第2の実施形態である検出方法および装置について図4を参照して説明する。図4は第2の実施形態の検出装置の概略構成を示す全体図である。本実施形態の検出方法および装置は、局在プラズモン共鳴により光電場を増強させ、増強された光電場において励起された蛍光を検出する蛍光検出方法および装置である。なお、以下においては、第1実施形態と同じ構成要素には同じ参照符号を付してある。
図5Aに示すセンサチップ10Aは、誘電体プレート11と、該プレート11の所定領域上にアレイ状に固着された複数の金属粒子73aからなる金属微細構造体73で構成されている。金属粒子73aの配列パターンは適宜設計できるが、略規則的であることが好ましい。かかる構成では、金属粒子73aの平均的な径及びピッチが励起光Loの波長よりも小さく設計される。
図5Cに示す例では、マッシュルーム状の金属75aの頭部が粒子状であり、サンプルプレート表面から見れば、金属微粒子が配列されたような構造になっている。かかる構成では、マッシュルーム状の金属75aの頭部が凸部であり、その平均的な径およびピッチが測定光Lの波長よりも小さく設計される。
センサチップを用意し、抗原―抗体反応をさせ、蛍光物質をセンサ部上に引き寄せる工程は、第1の実施形態と同様であるため、説明を省略する。以下の実施形態において同様とする。
蛍光物質Fをセンサ部14に引き寄せた状態で、センサチップ10の誘電体プレート11の所定領域に向けて励起光照射光学系20’により励起光Loを照射する。光源21から出射された励起光Loはハーフミラー23により反射されてセンサチップ10’の試料接触面上に入射される。この励起光Loの照射により、金属層12’の表面で局在プラズモンが励起される。励起光の入射により金属層上に生じている光電場(近接場光に起因する電場)が、この局在プラズモンにより増強され、金属層上に光電場増強領域Dが形成される。光電場増強領域の金属膜表面には、蛍光物質Fが引き寄せられており、蛍光物質Fが励起されて(実質的にはその蛍光物質中の蛍光色素分子fが励起されて)蛍光Lfが発生する。局在プラズモンによる光電場増強の効果により蛍光は増強されたものとなる。この蛍光Lfを光検出器30により検出することにより、蛍光標識結合物質と結合した被検出物質の有無および/または量を検出することができる。
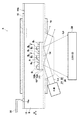
第3の実施形態の検出方法および装置について図6を参照して説明する。図6は第3の実施形態の検出装置の概略構成を示す全体図である。本実施形態の検出方法および装置は、表面プラズモン共鳴により電場を増強させ、増強された電場において励起された蛍光が金属層に新たにプラズモンを誘起することにより、誘電体プレートの金属層形成面と反対の面側から放射される、新たに誘起されたプラズモンからの放射光を検出する放射光検出方法および装置である。
蛍光物質Fをセンサ部14に引き寄せた状態で、第1の実施形態と同様に、励起光照射光学系20により励起光Loを照射する。励起光照射光学系20により励起光Loが誘電体プレート11と金属膜12との界面に対して全反射角以上の特定の入射角度で入射されることにより、金属膜上12の試料S中にエバネッセント波が滲み出し、このエバネッセント波によって金属膜12中に表面プラズモンが励起される。励起光の入射により金属層上に生じている光電場(エバネッセント波に起因する電場)が、この表面プラズモンにより増強され、金属層上に光電場増強領域Dが形成される。光電場増強領域の金属膜表面には、蛍光物質Fが引き寄せられており、蛍光物質Fが励起されて(実質的にはその蛍光物質中の蛍光色素分子fが励起されて)蛍光Lfが発生する。このとき、表面プラズモンによる光電場増強の効果により蛍光は増強されたものとなる。金属膜12上で生じたこの蛍光Lfが、金属膜12に表面プラズモンを新たに誘起し、この表面プラズモンによりセンサチップ10の金属膜形成面と反対側から特定の角度で放射光Lpが射出される。光検出器30によって、この放射光Lpを検出することにより、蛍光標識結合物質と結合した被検出物質の有無および/または量を検出することができる。
第4の実施形態の検出方法および装置について図7を参照して説明する。図7は第4の実施形態の検出装置の概略構成を示す全体図である。本実施形態の検出方法および装置は、金属層上に光導波層を備えたセンサチップを用い、励起光の照射により光導波層に光導波モードを励起し、光導波モードにより光電場を増強させ、増強された光電場において励起された蛍光を検出する蛍光検出方法および装置である。
第5の実施形態の検出方法および装置について図8を参照して説明する。図8は第5の実施形態の検出装置の概略構成示す全体図である。本実施形態の検出方法および装置は、金属層上に光導波層を備えたセンサチップを用い、励起光の照射により光導波層に光導波モードを励起し、光導波モードにより光電場を増強させ、増強された光電場において励起された蛍光が金属層に新たにプラズモンを誘起することにより、誘電体プレートの金属層形成面と反対の面側から放射される、新たに誘起されたプラズモンからの放射光を検出する放射光検出方法および装置である。
まず、前述手順により蛍光物質を作製し、その表面にポリエチレンイミン(PEI)(エポミン、日本触媒社)を修飾する。
次に、粒子表面のPEIに粒径15nmのPdナノ粒子(平均粒径19nm、徳力本社)を吸着させる。
Pdナノ粒子が吸着したポリスチレン粒子を無電解金メッキ液(HAuCl4、小島化学薬品社)に浸漬させることで、Pdナノ粒子を触媒とする無電界メッキを利用して、ポリスチレン粒子表面に金膜を作製する。
本発明の検出方法のセンサチップとして使用される検出用試料セルについて説明する。
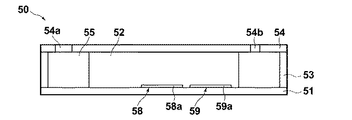
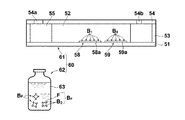
図10Aは、第1の実施形態の試料セル50の構成を示す平面図、図10Bは試料セル50の側断面図である。
検出用試料セル50は、誘電体プレートからなる基台51と、該基台51上に液体試料Sを保持し、液体試料Sの流路52を形成するスペーサ53と、試料Sを注入する注入口54aおよび流路52を流下した試料を排出する排出口となる空気孔54bを備えたガラス板からなる上板54とから構成され、流路52の注入口54aと空気孔54bとの間の試料接触面となる基台51の所定領域上に設けられた金属層58a、59aからなるセンサ部58、59が備えられている。また、注入口54aから流路52に至る箇所にはメンブレンフィルター55が備えられ、流路52下流の空気孔54bに接続する部分には廃液だめ56が形成されている。
さらに、流路内の、センサ部より上流側に、被検出物質と特異的に結合する第2の結合物質および被検出物質と競合して第1の結合物質と特異的に結合する第3の結合物質のうちのいずれか一方の結合物質とその結合物質および、液体試料中で極性を示す官能基が表面に修飾された蛍光物質とからなる蛍光標識結合物質を適宜固定して使用することができる。
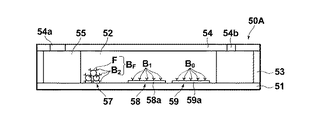
図11は、サンドイッチ法によるアッセイに適した第2の実施形態の試料セルの側断面を示すものである。本実施形態の試料セル50Aにおいては、基台51上に流路52上流側から、被検出物質である抗原と特異的に結合する2次抗体(第2の結合物質)B2と該2次抗体B2および液体試料のpHにより荷電状態が変化する官能基(例えば、−COOHや−NH2等、図示せず。)が表面修飾された蛍光物質Fとからなる蛍光標識結合物質BF(以下、「標識2次抗体BF」という。)が物理吸着させてある標識2次抗体吸着エリア57、被検出物質である抗原と特異的に結合する1次抗体(第1の結合物質)B1が固定された第1の測定エリア58、被検出物質である抗原Aとは結合せず標識2次抗体BFと特異的に結合する1次抗体B0が固定された第2の測定エリア59が順に設けられている。この第1および第2の測定エリア58,59がセンサ部に相当する。本例では、センサ部に2つの測定エリアを設けた例を挙げているが、測定エリアは1つのみであってもよい。
step2:全血Soはメンブレンフィルター55により濾過され、赤血球、白血球などの大きな分子が残渣となる。
step3:メンブレンフィルター55で血球分離された血液(血漿)Sが毛細管現象で流路52に染み出す。または反応を早め、検出時間を短縮するために、空気孔54bにポンプを接続し、メンブレンフィルター55で血球分離された血液をポンプの吸引、押し出し操作によって流下させてもよい。図12中において血漿Sは斜線領域で示している。
step4:流路52に染み出した血漿Sと標識2次抗体BFとが混ぜ合わされ、血漿中の抗原Aが標識2次抗体BFの2次抗体B2と結合する。
step5:血漿Sは流路52に沿って空気孔54b側へと徐々に流れ、2次抗体B2と結合した抗原Aが、第1の測定エリア58上に固定されている1次抗体B1と結合し、抗原Aが1次抗体B1と2次抗体B2(標識2次抗体BF)で挟み込まれたいわゆるサンドイッチが形成される。
step6:抗原Aと結合しなかった標識2次抗体BFの一部は第2の測定エリア59上に固定されている1次抗体B0と結合する。さらに抗原Aまたは1次抗体B0と結合しなかった標識2次抗体BFが測定エリア上に残っている場合があっても、後続の血漿が洗浄の役割を担い、プレート上に浮遊および非特異吸着していた標識2次抗体を洗い流す。
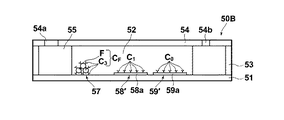
図13は、競合法によるアッセイに適した第3の実施形態の試料セルの側断面を示すものである。本実施形態の試料セル50Bにおいては、基台51上には流路52上流側から、被検出物質である抗原Aとは結合せず、後述の1次抗体と特異的に結合する2次抗体C3(第3の結合物質)と該2次抗体C3および液体試料のpHにより荷電状態が変化する官能基(例えば、−COOHや−NH2等、図示せず。)が表面修飾された蛍光物質Fとからなる蛍光標識結合物質CF(以下、「標識2次抗体CF」という。)を物理吸着させてある標識2次抗体吸着エリア57’、被検出物質である抗原Aおよび2次抗体C3と特異的に結合する1次抗体C1(第1の結合物質)が固定された第1の測定エリア58’、被検出物質である抗原Aとは結合せず標識2次抗体CFの2次抗体C3と特異的に結合する1次抗体C0が固定された第2の測定エリア59’が順に設けられている。
step2:全血Soはメンブレンフィルター55により濾過され、赤血球、白血球などの大きな分子が残渣となる。
step3:メンブレンフィルター55で血球分離された血液(血漿)Sが毛細管現象で流路52に染み出す。または反応を早め、検出時間を短縮するために、空気孔54bにポンプを接続し、メンブレンフィルター55で血球分離された血液をポンプの吸引、押し出し操作によって流下させてもよい。図14中において血漿Sは斜線領域で示している。
step4:流路52に染み出した血漿Sと標識2次抗体CFとが混ぜ合わされる。
step5:血漿Sは流路52に沿って空気孔54b側へと徐々に流れ、抗原Aと標識2次抗体CFの2次抗体C3とが競合して、第1の測定エリア58’上に固定されている1次抗体C1と結合する。
step6:第1の測定エリア58’上の1次抗体C1と結合しなかった標識2次抗体CFの一部は、第2の測定エリア59’上に固定されている1次抗体C0と結合する。さらに1次抗体C1またはC0と結合していない標識2次抗体CFが測定エリア上に残っている場合があっても、後続の血漿が洗浄の役割を担い、プレート上に浮遊および非特異吸着していた標識2次抗体CFを洗い流す。
図15は、第4の実施形態の試料セル70の構成を示す平面図である。
検出用試料セル70は、誘電体プレートからなる図示しない基台と、該基台上に液体試料Sを保持し、液体試料Sの流路72および該流路から分岐した枝路80を形成するスペーサと、試料Sを注入する注入口74a、流路72を流下した試料を排出する排出口となる空気孔74b、および枝路80にpH調整液を注入するためのpH調整液注入口79を備えたガラス板からなる上板とから構成され、流路72の注入口74aと空気孔74bとの間の試料接触面となる基台の所定領域上に設けられた金属層からなるセンサ部78が備えられている。また、注入口74aから流路72に至る箇所にはメンブレンフィルターが備えられ、流路72下流の空気孔74bに接続する部分には廃液だめ76が形成されている。また、流路72と枝路80の分岐部分には切り替えバルブ81が設けられており、試料とpH調整液とのセンサ部78に送液する順序を制御可能となっている。また、センサ部下流側にもバルブ82が設けられており、センサ部に蛍光標識結合物質を結合させる(抗原―抗体反応をさせる)際に一旦試料液をセンサ部に溜めるためにバルブを閉じ、センサ部への蛍光標識結合物質の結合反応の後、未反応の蛍光標識結合物質を洗い流す際、及びpH調整液によりセンサ部上に溶液のpHを調整する際などには、バルブを開き、試料液を廃液だめ76へと流下可能に構成されている。
さらに、流路内の、センサ部より上流側に、具体的には、本試料セル70は流路81の、注入口74aからセンサ部78に至る箇所に、標識2次抗体吸着エリア75を備え、被検出物質と特異的に結合する第2の結合物質および被検出物質と競合して第1の結合物質と特異的に結合する第3の結合物質のうちのいずれか一方の結合物質とその結合物質および、液体試料中で極性を示す官能基が表面に修飾された蛍光物質とからなる蛍光標識結合物質を適宜固定して使用することができる。
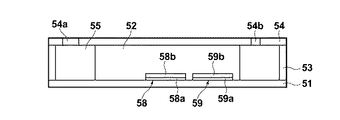
光導波モードによる光電場増強を利用する検出方法および装置に用いる試料セルの断面図を図16に示す。図10Aおよび図10Bに示した第1の実施形態の試料セルの構成と略同一であるが、センサ部の金属層58a、59a上にさらに光導波層58b、59bを備えている。
本発明の検出方法に使用される検出用キットについて説明する。
step2:全血Soはメンブレンフィルター55により濾過され、赤血球、白血球などの大きな分子が残渣となる。引き続き、メンブレンフィルター55で血球分離された血液(血漿)Sが毛細管現象で流路52に染み出す。または反応を早め、検出時間を短縮するために、空気孔にポンプを接続し、メンブレンフィルター55で血球分離された血液をポンプの吸引、押し出し操作によって流下させてもよい。図17中において血漿Sは斜線領域で示している。
step3:血漿Sは流路52に沿って空気孔54b側へと徐々に流れ、血漿S中の抗原Aが、第1の測定エリア58上に固定されている1次抗体B1と結合する。
step4:標識2次抗体BFを含む標識用溶液63を供給口54aから注入する。
step5:標識2次抗体BFが毛細管現象により流路52に染み出す。または反応を早め、検出時間を短縮するために、空気孔にポンプを接続し、メンブレンフィルター55で血球分離された血液をポンプの吸引、押し出し操作によって流下させてもよい。
step6:標識2次抗体BFは徐々に下流側に流れ、該標識2次抗体BFの2次抗体B2が抗原Aと結合し、抗原Aが1次抗体B1と2次抗体B2で挟み込まれたいわゆるサンドイッチが形成される。抗原Aと結合しなかった2次抗体B2の一部は第2の測定エリア59上に固定されている1次抗体B0と結合する。さらに抗原Aまたは1次抗体B0と結合しなかった標識2次抗体BFが測定エリア上に残っている場合があっても、後続の血漿が洗浄の役割を担い、プレート上に浮遊および非特異吸着していた標識2次抗体BFを洗い流す。
前述の手順で作製した蛍光物質溶液(蛍光物質の直径500nm、励起波長780nm)に50mM MESバッファーおよび、5.0mg/mLの抗hCGモノクローナル抗体(Anti−hCG 5008 SP−5、Medix Biochemica社)溶液を加えて撹拌する。これにより蛍光物質への抗体の修飾がなされる。
さらに、2mol/L Glycine水溶液を添加し撹拌した後、遠心分離にて、粒子を沈降させる。
最後に、上清を取り除き、PBS(pH7.4)を加え、超音波洗浄機により、表面修飾された蛍光物質を再分散させる。さらに遠心分離を行い、上清を除いた後、1%BSAのPBS(pH7.4)溶液500μL加え、表面修飾された蛍光物質を再分散させて標識用溶液とする。
光導波モードによる光電場増強を利用する検出方法および装置に用いる試料セルとしては、図15に示す、センサ部の金属層58a、59a上にさらに光導波層58b、59bを備え試料セルの光導波層58b、59b上に、それぞれ1次抗体B1、1次抗体B1とは異なる1次抗体B0を固定したものを用いればよい。
10、10’、10” センサチップ
11 誘電体プレート
12 金属層(金属膜)
12’ 金属層(金属微細構造体)
14 センサ部
16 材料
19 金属被膜
20、20’ 励起光照射光学系
21 光源
22 プリズム
30 光検出器
35 pH調整手段
50、50A、50B、61、70 試料セル
51 誘電体プレート
52 流路
53 スペーサ
54 上板
57 標識2次抗体吸着エリア
58、59 検出エリア
60 検出用キット
63 検出用標識溶液
A 抗原(被検出物質)
B1、C1 1次抗体(第1の結合物質)
B2 2次抗体(第2の結合物質)
BF、CF 標識2次抗体(蛍光標識結合物質)
C3 2次抗体(第3の結合物質)
F 蛍光物質
f 蛍光色素分子
Lo 励起光
Lf 蛍光
Lp 放射光
Claims (14)
- 誘電体プレートと、該プレートの一面に設けられた少なくとも金属層からなるセンサ部とからなるセンサチップを用意し、
前記センサ部に液体試料を接触させることにより、該センサ部上に、該液体試料中の被検出物質の量に応じた量の蛍光標識結合物質を結合させ、
前記センサ部に励起光を照射することにより、該センサ部上に増強した光電場を生じさせ、該増強した光電場内において前記蛍光標識結合物質の蛍光標識を励起し、該蛍光標識の励起に起因して生じる光の量に基づいて、前記被検出物質の量を検出する検出方法において、
前記蛍光標識として、複数の蛍光色素分子を、該蛍光色素分子からの蛍光を透過する材料により包含してなる、前記液体試料中において該液体試料のpHに応じて荷電状態が変化する蛍光物質を用い、
前記センサ部に前記蛍光標識結合物質を結合させた状態で、前記液体試料のpHを調整して、前記蛍光物質の荷電状態を中性化することにより、該蛍光物質を前記センサ部表面に引き寄せ、
該蛍光物質を引き寄せた状態で、前記被検出物質の量を検出することを特徴とする検出方法。 - 前記蛍光物質の粒径が30nm以上であることを特徴とする請求項1記載の検出方法。
- 前記蛍光物質として、前記液体試料のpHに応じて荷電状態が変化する官能基が表面修飾された蛍光物質を用い、
前記該センサ部に、前記蛍光標識結合物質を結合させる際、前記液体試料を前記官能基がイオン化するpHとし、
前記蛍光標識結合物質を結合させた後、前記液体試料を前記官能基が中性化するpHに調整することにより、前記蛍光物質を前記センサ部表面に引き寄せることを特徴とする請求項1または2記載の検出方法。 - 前記励起光の照射により前記金属層にプラズモンを励起し、該プラズモンにより前記増強した光電場を生じさせ、
前記蛍光標識の励起に起因して生じる前記光として、該励起によって該蛍光標識から生じる蛍光を検出することにより前記被検出物質の量を検出することを特徴とする請求項1から3いずれか1項記載の検出方法。 - 前記励起光の照射により前記金属層にプラズモンを励起し、該プラズモンにより前記増強した光電場を生じさせ、
前記蛍光標識の励起に起因して生じる前記光として、該励起によって該蛍光標識から生じる蛍光が前記金属層に新たにプラズモンを誘起することにより、前記誘電体プレートの前記他面から放射される放射光を検出することにより前記被検出物質の量を検出することを特徴とする請求項1から3いずれか1項記載の検出方法。 - 前記センサチップとして、前記金属層上に光導波層を備えたものを用い、
前記励起光の照射により前記光導波層に光導波モードを励起し、該光導波モードにより前記増強した光電場を生じさせ、
前記蛍光標識の励起に起因して生じる前記光として、該励起によって該蛍光標識から生じる蛍光を検出することにより前記被検出物質の量を検出することを特徴とする請求項1から3いずれか1項記載の検出方法。 - 前記センサチップとして、前記金属層上に光導波層を備えたものを用い、
前記励起光の照射により前記光導波層に光導波モードを励起し、該光導波モードにより前記増強した光電場を生じさせ、
前記蛍光標識の励起に起因して生じる前記光として、該励起によって該蛍光標識から生じる蛍光が前記金属層に新たにプラズモンを誘起することにより、前記誘電体プレートの前記他面から放射される放射光を検出することにより前記被検出物質の量を検出することを特徴とする請求項1から3いずれか1項記載の検出方法。 - 請求項1から7いずれか1項に記載の検出方法に用いられる検出装置であって、
前記センサチップを収容する収容部と、
前記センサ部に前記励起光を照射する励起光照射光学系と、
該励起光の照射により該センサ部上に生じた前記増強した光電場における、前記蛍光標識の励起に起因して生じる光を検出する光検出手段と、
前記センサチップに、pH調整液を注入して前記液体試料のpHを調整するpH調整手段とを備えたことを特徴とする検出装置。 - 請求項1から7いずれか1項に記載の検出方法において使用される検出用試料セルであって、
液体試料が流下される流路を有する基台と、
前記流路の上流側に設けられた該流路に前記液体試料を注入するための注入口と、
前記流路の下流側に設けられた、前記注入口から注入された前記液体試料を該下流側に流すための空気孔と、
前記流路の、前記注入口と前記空気孔との間に設けられたセンサチップ部であって、前記流路の内壁面の少なくとも一部に設けられた誘電体プレートと、該プレートの試料接触面に設けられた少なくとも金属層を含むセンサ部とからなるセンサチップ部とを備えてなることを特徴とする検出用試料セル。 - 前記センサ部に、前記蛍光標識結合物質と結合する固定層を備えていることを特徴とする請求項9記載の検出用試料セル。
- 複数の蛍光色素分子を、該蛍光色素分子からの蛍光を透過する材料により包含してなる、前記液体試料中において該液体試料のpHに応じて荷電状態が変化する蛍光物質を、前記蛍光標識として含む前記蛍光標識結合物質が、前記流路内の、前記センサ部より上流側に固定されていることを特徴とする請求10記載の検出用試料セル。
- 前記センサ部において、前記金属層上に光導波層が備えられていることを特徴とする請求項9から11いずれか1項記載の検出用試料セル。
- 請求項1から7のいずれか1項に記載の検出方法に使用される検出用キットであって、
液体試料が流下される流路を有する基台と、前記流路の上流側に設けられた該流路に前記液体試料を注入するための注入口と、前記流路の下流側に設けられた、前記注入口から注入された前記液体試料を該下流側に流すための空気孔と、前記流路の、前記注入口と前記空気孔との間に設けられたセンサチップ部であって、前記流路の内壁面の少なくとも一部に設けられた誘電体プレートと、該プレートの試料接触面に設けられた少なくとも金属層を含むセンサ部とからなるセンサチップ部と、該センサ部上に固定された、前記蛍光標識結合物質と結合する固定層とを備えた試料セル、および
前記液体試料と同時もしくは前記液体試料の流下後に、前記流路内に流下される、複数の蛍光色素分子を、該蛍光色素分子からの蛍光を透過する材料により包含してなる、前記液体試料中において該液体試料のpHに応じて荷電状態が変化する蛍光物質を、前記蛍光標識として含む前記蛍光標識結合物質を含んだ標識用溶液を備えてなることを特徴とする検出用キット。 - 前記センサ部において、前記金属層上に光導波層が備えられていることを特徴とする請求項12記載の検出用キット。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008182227A JP5190945B2 (ja) | 2008-07-14 | 2008-07-14 | 検出方法、検出装置、検出用試料セルおよび検出用キット |
| US12/501,923 US8039267B2 (en) | 2008-07-14 | 2009-07-13 | Detection method, detection apparatus, and sample cell and kit for detection |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008182227A JP5190945B2 (ja) | 2008-07-14 | 2008-07-14 | 検出方法、検出装置、検出用試料セルおよび検出用キット |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010019767A true JP2010019767A (ja) | 2010-01-28 |
| JP5190945B2 JP5190945B2 (ja) | 2013-04-24 |
Family
ID=41505498
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008182227A Expired - Fee Related JP5190945B2 (ja) | 2008-07-14 | 2008-07-14 | 検出方法、検出装置、検出用試料セルおよび検出用キット |
Country Status (2)
| Country | Link |
|---|---|
| US (1) | US8039267B2 (ja) |
| JP (1) | JP5190945B2 (ja) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010048756A (ja) * | 2008-08-25 | 2010-03-04 | Fujifilm Corp | 検出方法、検出装置、検出用試料セルおよび検出用キット |
| JP2012042233A (ja) * | 2010-08-13 | 2012-03-01 | Konica Minolta Holdings Inc | Spfs(表面プラズモン励起増強蛍光分光法)により測定される蛍光シグナルの補正方法およびこれを用いたアッセイ方法、並びにこれらの方法に用いられる構造体および表面プラズモン共鳴センサー |
| WO2012120874A1 (ja) * | 2011-03-10 | 2012-09-13 | 富士フイルム株式会社 | 検出方法および検出装置 |
| WO2013080505A1 (ja) * | 2011-11-28 | 2013-06-06 | 富士フイルム株式会社 | センシング装置およびこれを用いたセンシング方法 |
| JP2014509745A (ja) * | 2011-03-22 | 2014-04-21 | サイヴェク・インコーポレイテッド | マイクロ流体装置並びに製造及び使用の方法 |
| JP2015025820A (ja) * | 2014-11-04 | 2015-02-05 | 株式会社東芝 | 光導波路型測定システムおよび糖化ヘモグロビンの測定方法 |
| JPWO2016208421A1 (ja) * | 2015-06-24 | 2018-04-12 | コニカミノルタ株式会社 | 測定方法、並びにこれに用いる測定チップ、及び測定用キット |
| CN110869769A (zh) * | 2017-06-14 | 2020-03-06 | 株式会社日立高新技术 | 试验套件、试验方法、分注装置 |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11639932B2 (en) * | 2011-03-11 | 2023-05-02 | Orono Spectral Solutions, Inc. | Apparatus for preconcentrating and transferring analytes from surfaces and measurement thereof using spectroscopy |
| US20180299439A1 (en) * | 2011-03-11 | 2018-10-18 | Orono Spectral Solutions, Inc. | Apparatus for preconcentrating and transferring analytes from surfaces and measurement thereof using spectroscopy |
| US9551662B2 (en) * | 2011-05-19 | 2017-01-24 | Konica Minolta, Inc | Surface plasmon-field enhanced fluorescence measurement device and fluorescence detection method using the same |
| GB2550561A (en) * | 2016-05-17 | 2017-11-29 | Sumitomo Chemical Co | Apparatus for optically exciting and detecting fluorescence |
| GB2550560A (en) * | 2016-05-17 | 2017-11-29 | Sumitomo Chemical Co | Device for optically exciting fluorescence |
| EP3381547A1 (en) * | 2017-03-30 | 2018-10-03 | Canon Medical Systems Corporation | Specimen test apparatus |
| FR3069927B1 (fr) | 2017-08-04 | 2021-06-04 | Ecole Polytech | Procede de detection ultra-sensible a l'aide de particules photoluminescentes |
| KR20200034563A (ko) * | 2018-09-20 | 2020-03-31 | 주식회사 제우스 | 유동매체 모니터링장치 |
| CN109884064B (zh) * | 2019-04-24 | 2021-09-07 | 山东协和学院 | 一种液体传感器的数据采集装置 |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07174693A (ja) * | 1991-06-08 | 1995-07-14 | Hewlett Packard Co <Hp> | 生体分子検出方法および装置 |
| JP2004069397A (ja) * | 2002-08-02 | 2004-03-04 | Nec Corp | 分析チップおよび分析装置 |
| JP2005189085A (ja) * | 2003-12-25 | 2005-07-14 | Canon Chemicals Inc | 光学プローブ及びその製造方法 |
| JP2006010515A (ja) * | 2004-06-25 | 2006-01-12 | Aisin Seiki Co Ltd | 蛍光強度検出装置 |
| JP2006214741A (ja) * | 2005-02-01 | 2006-08-17 | Toyota Central Res & Dev Lab Inc | 微小物体の光固定化方法 |
| WO2007034877A1 (ja) * | 2005-09-22 | 2007-03-29 | National Institute Of Advanced Industrial Science And Technology | 半導体ナノ粒子分散ガラス微粒子及びその作製方法 |
| JP2007139540A (ja) * | 2005-11-17 | 2007-06-07 | Kyoto Univ | 蛍光増強素子、蛍光素子、及び蛍光増強方法 |
| JP2008145309A (ja) * | 2006-12-12 | 2008-06-26 | Fujifilm Corp | 表面プラズモン増強蛍光センサ |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5512492A (en) * | 1993-05-18 | 1996-04-30 | University Of Utah Research Foundation | Waveguide immunosensor with coating chemistry providing enhanced sensitivity |
| JPH09257702A (ja) | 1996-03-21 | 1997-10-03 | Toto Ltd | 表面プラズモン共鳴センサ装置 |
| DE19715483A1 (de) * | 1997-04-14 | 1998-10-15 | Boehringer Mannheim Gmbh | Methode zur gleichzeitigen Bestimmung von biomolekularen Wechselwirkungen mittels Plasmonenresonanz undFluoreszenzdetektion |
| US20050053974A1 (en) | 2003-05-20 | 2005-03-10 | University Of Maryland | Apparatus and methods for surface plasmon-coupled directional emission |
| JP4381752B2 (ja) | 2003-09-02 | 2009-12-09 | シスメックス株式会社 | 光学的定量方法及び光学的定量装置 |
| US7623231B2 (en) | 2005-02-14 | 2009-11-24 | Fujifilm Corporation | Device for Raman spectroscopy and Raman spectroscopic apparatus |
| EP1715085B1 (en) | 2005-04-18 | 2013-04-03 | FUJIFILM Corporation | Method for producing anodized structure |
| EP1896832A4 (en) * | 2005-06-17 | 2011-12-14 | Univ Maryland Biotech Inst | METAL-REINFORCED MEASURING METHODS AT FLUORESCENT BASIS |
| JP2007085770A (ja) | 2005-09-20 | 2007-04-05 | Fujifilm Corp | 可動式導電体を備えたバイオセンサー |
| JP2007139612A (ja) | 2005-11-18 | 2007-06-07 | Fujifilm Corp | 微細構造体、微細構造体の作製方法、ラマン分光法、及び装置 |
| JP2007171003A (ja) | 2005-12-22 | 2007-07-05 | Fujifilm Corp | 質量分析用基板並びに分析方法および装置 |
-
2008
- 2008-07-14 JP JP2008182227A patent/JP5190945B2/ja not_active Expired - Fee Related
-
2009
- 2009-07-13 US US12/501,923 patent/US8039267B2/en active Active
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07174693A (ja) * | 1991-06-08 | 1995-07-14 | Hewlett Packard Co <Hp> | 生体分子検出方法および装置 |
| JP2004069397A (ja) * | 2002-08-02 | 2004-03-04 | Nec Corp | 分析チップおよび分析装置 |
| JP2005189085A (ja) * | 2003-12-25 | 2005-07-14 | Canon Chemicals Inc | 光学プローブ及びその製造方法 |
| JP2006010515A (ja) * | 2004-06-25 | 2006-01-12 | Aisin Seiki Co Ltd | 蛍光強度検出装置 |
| JP2006214741A (ja) * | 2005-02-01 | 2006-08-17 | Toyota Central Res & Dev Lab Inc | 微小物体の光固定化方法 |
| WO2007034877A1 (ja) * | 2005-09-22 | 2007-03-29 | National Institute Of Advanced Industrial Science And Technology | 半導体ナノ粒子分散ガラス微粒子及びその作製方法 |
| JP2007139540A (ja) * | 2005-11-17 | 2007-06-07 | Kyoto Univ | 蛍光増強素子、蛍光素子、及び蛍光増強方法 |
| JP2008145309A (ja) * | 2006-12-12 | 2008-06-26 | Fujifilm Corp | 表面プラズモン増強蛍光センサ |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010048756A (ja) * | 2008-08-25 | 2010-03-04 | Fujifilm Corp | 検出方法、検出装置、検出用試料セルおよび検出用キット |
| JP2012042233A (ja) * | 2010-08-13 | 2012-03-01 | Konica Minolta Holdings Inc | Spfs(表面プラズモン励起増強蛍光分光法)により測定される蛍光シグナルの補正方法およびこれを用いたアッセイ方法、並びにこれらの方法に用いられる構造体および表面プラズモン共鳴センサー |
| WO2012120874A1 (ja) * | 2011-03-10 | 2012-09-13 | 富士フイルム株式会社 | 検出方法および検出装置 |
| JP2012189429A (ja) * | 2011-03-10 | 2012-10-04 | Fujifilm Corp | 検出方法および検出装置 |
| JP2014509745A (ja) * | 2011-03-22 | 2014-04-21 | サイヴェク・インコーポレイテッド | マイクロ流体装置並びに製造及び使用の方法 |
| WO2013080505A1 (ja) * | 2011-11-28 | 2013-06-06 | 富士フイルム株式会社 | センシング装置およびこれを用いたセンシング方法 |
| JP2015025820A (ja) * | 2014-11-04 | 2015-02-05 | 株式会社東芝 | 光導波路型測定システムおよび糖化ヘモグロビンの測定方法 |
| JPWO2016208421A1 (ja) * | 2015-06-24 | 2018-04-12 | コニカミノルタ株式会社 | 測定方法、並びにこれに用いる測定チップ、及び測定用キット |
| US10895535B2 (en) | 2015-06-24 | 2021-01-19 | Konica Minolta, Inc. | Measurement method, and measuring chip and measuring kit used for the same |
| CN110869769A (zh) * | 2017-06-14 | 2020-03-06 | 株式会社日立高新技术 | 试验套件、试验方法、分注装置 |
| CN110869769B (zh) * | 2017-06-14 | 2023-11-03 | 株式会社日立高新技术 | 试验套件、试验方法、分注装置 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5190945B2 (ja) | 2013-04-24 |
| US20100009458A1 (en) | 2010-01-14 |
| US8039267B2 (en) | 2011-10-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5190945B2 (ja) | 検出方法、検出装置、検出用試料セルおよび検出用キット | |
| JP5301894B2 (ja) | 検出方法 | |
| JP5160985B2 (ja) | 検出方法、検出装置、検出用試料セルおよび検出用キット | |
| JP5152917B2 (ja) | 検出方法、検出用試料セルおよび検出用キット | |
| JP5143668B2 (ja) | 検出方法、検出用試料セルおよび検出用キット | |
| JP5180703B2 (ja) | 検出方法、検出用試料セルおよび検出用キット | |
| JP2010190880A (ja) | 光信号検出方法、光信号検出装置、光信号検出用試料セルおよび光信号検出用キット | |
| US8106368B2 (en) | Fluorescence detecting method | |
| JP5450993B2 (ja) | 検出方法、検出用試料セルおよび検出用キット | |
| US20160123968A1 (en) | Device and method for detecting an analyte | |
| JP2010043934A (ja) | 検出方法、検出用試料セル、検出用キット及び検出装置 | |
| CN111295580A (zh) | 使用光致发光颗粒的超灵敏检测方法 | |
| JP5315381B2 (ja) | 蛍光検出装置、蛍光検出用の試料セルおよび蛍光検出方法 | |
| JP2009258034A (ja) | 表面プラズモン放射光検出方法および装置、表面プラズモン放射光検出用試料セルおよびキット | |
| JP5563789B2 (ja) | 検出方法 | |
| EP2063256A1 (en) | Fluorescence detecting method | |
| US20110195516A1 (en) | Wire grid substrate structure and method for manufacturing such a substrate | |
| EP1321761A1 (en) | Method of detecting an analyte | |
| JP2007279027A (ja) | バイオセンサー表面の検査方法 | |
| JP5754309B2 (ja) | 表面プラズモン励起増強蛍光分光法を利用して蛍光量を測定する定量分析方法ならびにそれに用いられる定量分析用キットおよびアナライト解離抑制剤 | |
| JP5655125B2 (ja) | 蛍光検出方法 | |
| JP2010223802A (ja) | 光信号検出方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110126 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20120829 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120904 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121105 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130108 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130124 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5190945 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20160208 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |