JP2009517015A - 組換えポリペプチドならびにtshレセプターに対する自己抗体を検出及び/又は定量化する方法 - Google Patents
組換えポリペプチドならびにtshレセプターに対する自己抗体を検出及び/又は定量化する方法 Download PDFInfo
- Publication number
- JP2009517015A JP2009517015A JP2008541846A JP2008541846A JP2009517015A JP 2009517015 A JP2009517015 A JP 2009517015A JP 2008541846 A JP2008541846 A JP 2008541846A JP 2008541846 A JP2008541846 A JP 2008541846A JP 2009517015 A JP2009517015 A JP 2009517015A
- Authority
- JP
- Japan
- Prior art keywords
- tsh receptor
- amino acid
- acid sequence
- isolated
- purified recombinant
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/72—Receptors; Cell surface antigens; Cell surface determinants for hormones
- C07K14/723—G protein coupled receptor, e.g. TSHR-thyrotropin-receptor, LH/hCG receptor, FSH receptor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/564—Immunoassay; Biospecific binding assay; Materials therefor for pre-existing immune complex or autoimmune disease, i.e. systemic lupus erythematosus, rheumatoid arthritis, multiple sclerosis, rheumatoid factors or complement components C1-C9
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/20—Fusion polypeptide containing a tag with affinity for a non-protein ligand
- C07K2319/23—Fusion polypeptide containing a tag with affinity for a non-protein ligand containing a GST-tag
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/20—Fusion polypeptide containing a tag with affinity for a non-protein ligand
- C07K2319/24—Fusion polypeptide containing a tag with affinity for a non-protein ligand containing a MBP (maltose binding protein)-tag
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/60—Fusion polypeptide containing spectroscopic/fluorescent detection, e.g. green fluorescent protein [GFP]
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/72—Assays involving receptors, cell surface antigens or cell surface determinants for hormones
Abstract
本発明は、TSHレセプター(TSHR)に対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質を有するグリコシド化されていない単離かつ精製した組換えポリペプチドに関する。更に、開示されているものは前記の単離かつ精製した組換えポリペプチドを用いてこのような自己抗体を検出及び/又は定量化する方法ならびに各々のキットに関する。
Description
本発明は、TSHレセプター(TSHR)に対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質を有する、グリコシド化されていない単離かつ精製した組換えポリペプチドに関する。更に、本発明は、前記単離かつ精製した組換えポリペプチドを用いて、このような自己抗体を検出及び/又は定量化する方法ならびに、各々のキットに関する。
発明の背景
甲状腺疾患は、ヒトにおいて最も一般的な自己免疫疾患であり、かつグレーヴス病(GD)、グレーヴス眼症(GO)、橋本甲状腺炎ならびに特発性粘液水腫からの幅広いスペクトルを有する。この中でもグレーヴス病は、甲状腺機能の増大、かつ臨床的甲状腺機能亢進症を導く。この器官特異的な自己免疫疾患は、年に10000人中約4人の発生率がある。一般的に容認されているグレーヴス病のメカニズムは、免疫系が甲状腺刺激ホルモン(TSH)レセプターに対して直接に自己抗体を産生し、かつこれらの種類の自己抗体が、自然に産生される甲状腺刺激ホルモン(TSH)の機能を真似できることである。
甲状腺疾患は、ヒトにおいて最も一般的な自己免疫疾患であり、かつグレーヴス病(GD)、グレーヴス眼症(GO)、橋本甲状腺炎ならびに特発性粘液水腫からの幅広いスペクトルを有する。この中でもグレーヴス病は、甲状腺機能の増大、かつ臨床的甲状腺機能亢進症を導く。この器官特異的な自己免疫疾患は、年に10000人中約4人の発生率がある。一般的に容認されているグレーヴス病のメカニズムは、免疫系が甲状腺刺激ホルモン(TSH)レセプターに対して直接に自己抗体を産生し、かつこれらの種類の自己抗体が、自然に産生される甲状腺刺激ホルモン(TSH)の機能を真似できることである。
TSHレセプター自己抗体(TRAbs)を検出する確立した方法には、機能作用(TSHRシグナル経路でのTRAbsの刺激又は阻害)を測定する生物アッセイ、及び単離又は組換えTSHレセプターに結合するTSHの阻害を検出するインビトロアッセイが含まれる。
細胞株:
チャイニーズハムスターの卵巣細胞株をTSHレセプターでトランスフェクトし、これを細胞膜で発現させる。患者血清を細胞株に加えた後に、細胞膜中のTSHレセプターに関連するエピトープへのTSHR自己抗体の結合を、患者血清の処理の際に、新たに合成されたサイクリックAMPの刺激又は阻害により検出する。
チャイニーズハムスターの卵巣細胞株をTSHレセプターでトランスフェクトし、これを細胞膜で発現させる。患者血清を細胞株に加えた後に、細胞膜中のTSHレセプターに関連するエピトープへのTSHR自己抗体の結合を、患者血清の処理の際に、新たに合成されたサイクリックAMPの刺激又は阻害により検出する。
コーティングチューブ法:
コーティングチューブ法は、BRAHMS AG社により開発されたものである。チューブ上にコートしたTSHRへの患者血清中のTRAbsの結合を、放射線標識したウシTSHの相互作用の阻害、いわゆるTSH阻害性免疫グロブリン(TBII)により間接的に測定する。TBIIアッセイは、甲状腺刺激抗体(TSAbs)と甲状腺ブロッキング抗体(TBAbs)を識別しない。
コーティングチューブ法は、BRAHMS AG社により開発されたものである。チューブ上にコートしたTSHRへの患者血清中のTRAbsの結合を、放射線標識したウシTSHの相互作用の阻害、いわゆるTSH阻害性免疫グロブリン(TBII)により間接的に測定する。TBIIアッセイは、甲状腺刺激抗体(TSAbs)と甲状腺ブロッキング抗体(TBAbs)を識別しない。
放射性−免疫アッセイ(RIA):
ヒト又は動物からアフィニティー精製したTSHRは、放射線により標識される。患者血清を添加した後に、TSHRに結合した患者血清中の自己抗体は、抗原−抗体複合体を形成する。この複合体は、免疫沈降法により分離され、かつ放射線活性を測定して、患者血清中の自己抗体の量を評価する。
ヒト又は動物からアフィニティー精製したTSHRは、放射線により標識される。患者血清を添加した後に、TSHRに結合した患者血清中の自己抗体は、抗原−抗体複合体を形成する。この複合体は、免疫沈降法により分離され、かつ放射線活性を測定して、患者血清中の自己抗体の量を評価する。
しかしTRAbsの異種の特性により、様々なアプローチの中で矛盾がある。最近ではモノクロナール甲状腺刺激抗体がホルモン刺激を阻害することが分かった(Chae, C. B.等、2001, J Clin Endocrinol Metab 86(7): 3311-3318)。しかし、その利用は極めて制限されている。一方で、モノクロナール抗体の特異性と親和性は不明であり、かつ2つのモノクロナール細胞株だけが利用されてきた。現在の方法において、自己抗体の低い感度と特異性の識別力の無さは、結果として臨床試験の矛盾を生じている(DeGroot, L. J., 1990, J. Ckin Endocronol Metab 83 (11): 3777-3785)。
TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を検出するための、ヒト甲状腺ホルモンレセプターの種々の断片の使用は、EP-A1078986に記載されている。バキュロウイルスの1本鎖配列を用いて種々の断片を、昆虫細胞中で発現させている。しかし、グリコシド化されていないヒトタンパク質の産生に昆虫細胞を使用することは不都合である。昆虫細胞により合成されるタンパク質は、おそらくそれらの平均の炭水化物の組成ならびにグリコシドル化パターンにおいて、天然に生じるグルコシド化されたヒトタンパク質とは異なっている。従って、バキュロウイルスの1本鎖配列を用いるTSHレセプター断片の調製と、昆虫細胞中でのそれらの発現は、それらの炭水化物の組成ならびにパターンが、ヒト細胞による生理学的状況で発現させたものとは異なるTSHレセプター断片を生じるであろう。
抗−TSHレセプター自己抗体を検出するためのヒト甲状腺ホルモンレセプターの種々の断片の使用は、WO 03/018632にも記載されていて、その際、断片をCHO細胞中で発現させている。しかし、CHO細胞により合成されたタンパク質は、おそらくそれらの平均の炭水化物の組成において、天然に生じるグルコシド化されたヒトタンパク質とは異なっている。従って、CHO細胞中で発現させたTSHレセプタータンパク質は、おそらくそれらのグリコシド化パターンにおいて、天然に生じるヒトTSHレセプターとは異なっていて、従って抗−TSHレセプター自己抗体を検出するアッセイにおいて、天然に生じるヒトTSHレセプターとは異なる結合特性を有するであろう。低い発現率、遅い増殖速度及び哺乳類成長因子を補足した複合培地の必要性ゆえに、CHO細胞中でのTSHレセプターの産生は時間を浪費し、かつ高価である。
アミノ酸20-414含有のヒトTSHRの細胞外ドメインのTSHレセプター断片は、Huang等により、1995, Endocrinology 136(2): 588-593に記載されているように、大腸菌中でグリコシド化されていない形で、GST融合タンパク質として発現させていた。しかし、精製した組換えレセプターの調製物はグレーヴス病の患者からの自己抗体に対して結合を示さないので、TSHレセプター断片の正しいフォールディングが、自己抗体の結合に重要であるかもしれないことを示している。この発見は、Bobovnikova等により、1997, J. Mol. Endocrinology 8(2): 137-144に強調されている。彼らは、可溶性の生物学的に活性なアミノ酸21-415含有のヒトTSHレセプター断片を、大腸菌のチオレドキシン還元酵素突然変異株中でGST融合タンパク質を発現させることにより得ていて、これがその細胞質内でジスルフィド結合の正しい形成を可能にする。しかし、標識したTSHに対するチオレドキシン還元酵素突然変異株中で産生されたTSHレセプター断片の結合親和性は極めて低かったので、得られたTSHレセプター断片の特性が、天然に生じるヒトTSHレセプターのものとは著しく異なることを示している。
本発明の対象は、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を検出するための新規TSHレセプター断片を提供することであり、これは、高い感度と低い交差反応性を有し、かつこのような自己抗体を定量的かつ定性的に検出する方法で使用できる。
本発明のまとめ
前記の対象は、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質を有するグリコシド化されていない単離かつ精製した新規組換えポリペプチド、グリコシド化されていないTSHレセプターの部分配列、かつグリコシド化されていないTSHレセプターの部分配列の新規エピトープ、ならびにグリコシド化されていない単離かつ精製した新規組換えポリペプチド、グリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列の新規エピトープを用いて、このような自己抗体を検出及び/又は定量化する新規方法により達成された。
前記の対象は、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質を有するグリコシド化されていない単離かつ精製した新規組換えポリペプチド、グリコシド化されていないTSHレセプターの部分配列、かつグリコシド化されていないTSHレセプターの部分配列の新規エピトープ、ならびにグリコシド化されていない単離かつ精製した新規組換えポリペプチド、グリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列の新規エピトープを用いて、このような自己抗体を検出及び/又は定量化する新規方法により達成された。
意外にも、1つ以上のTSHレセプターの部分配列が、原核宿主細胞の細胞質内でジスルフィド結合の形成を可能にする突然変異を有さない原核宿主内で発現されるポリペプチドに融合している融合タンパク質を有するグリコシド化されていない単離かつ精製した組換えポリペプチドが、ヒトTSHRに対する自己抗体に高い結合活性と、高い結合特異性を有し、かつ低い交差反応性を示すことが見出された。これらの発見は、以前に検討された分野に関して予想に反する。従って、本発明のグリコシド化されていない単離かつ精製した新規組換えポリペプチドは、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される新規自己抗体の検出、単離及び同定を容易にする。
以下の説明から明らかになると思われる上記の対象及び他の対象は、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される新規自己抗体に結合できる融合タンパク質を有する、グリコシド化されていない単離かつ精製した新規組換えポリペプチドを提供することにより達成された。また、次のものが提供される:グリコシド化されていないTSHレセプターの部分配列;グリコシド化されていない単離かつ精製した組換えポリペプチドと、グリコシド化されていないTSHレセプターの部分配列の新規エピトープから成る融合タンパク質をコードする単離かつ精製した核酸配列;前記の単離かつ精製した核酸配列の少なくとも1つのコピーを有するベクター、及び前記の単離かつ精製した核酸配列及び/又は前記ベクターで形質転換した原核宿主細胞;被験者の生体液中で、グリコシド化されていない単離かつ精製した新規組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列の新規エピトープを用いて、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を検出及び/又は定量化する方法;TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される新規自己抗体;TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を検出及び/又は定量化する各々のキット;TSHレセプターに対する免疫反応と関連する自己免疫疾患を診断するキットの使用;医薬組成物;TSHレセプターに対する免疫反応と関連する自己免疫疾患を治療又は予防する医薬品を調製するための前記グリコシド化されていない単離かつ精製した組換えポリペプチドの使用及び/又は前記グリコシド化されていないTSHレセプターの部分配列及の使用及び/又はグリコシド化されていないTSHレセプターの部分配列の新規エピトープの使用及び/又は前記医薬組成物の使用、ならびに被験者において、TSHレセプターに対する免疫反応と関連する自己免疫疾患を治療する方法;更に、TSHレセプターの結合相手を同定する方法及び前記方法により得られたTSHレセプターの結合相手が提供される。
他の対象と利点は、詳細な説明の概要から当業者には明らかになるであろう。以下の実証となる図面及び付随する請求項を参照して進めることにする。
図の簡単な説明
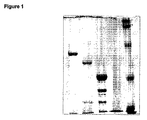
図1は、SDS−PAGEとクーマシー菌株によるGST−TSHR融合タンパク質の分析を示している。左から右に向かって:TSHR−ED、TSHR−210、TSHR−310、空、タンパク質標準物。
図1は、SDS−PAGEとクーマシー菌株によるGST−TSHR融合タンパク質の分析を示している。左から右に向かって:TSHR−ED、TSHR−210、TSHR−310、空、タンパク質標準物。
図2は、ウェスタンブロッティングによるGST−TSHR融合タンパク質の分析を示している。左から右に向かって:TSHR−ED、TSHR−210、TSHR−310。
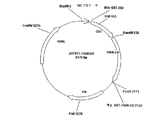
図3は、tacプロモーターにより制御したGST−TSHR融合タンパク質(TSHR−ED,GST)を含有するプラスミドpGEX2T−TSHR−EDを示している。
図4は、TSHに対するGST−TSHR融合タンパク質の特異的結合を示している。
図5は、マイクロタイタープレート中の、マウス抗−TSHR抗体に対するGST−TSHR融合タンパク質の結合活性を示している。GSTは、負のコントロールとしてはたらく。
図6は、市販のプール血清L1とL2中での抗−TSHR自己抗体の検出を示している。
図7は、マイクロタイタープレートのプラスチックウェル上にGST−TSHR融合タンパク質を固定することによる、患者血清と市販のプール血清L1とL2中での抗−TSHR自己抗体の検出を示している。
図8は、GST、TSHR−ED及びTSHR−310をコートしたプレート上での、90/672(国際基準)、L1(市販の抗−TSHRR陽性血清)及びH07(患者血清)のシグナル応答の比較を示している。
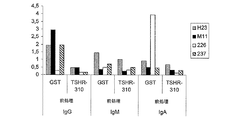
図9は、患者血清中の抗−TSHR自己抗体アイソフォームの検出を示している。
図10は、市販の血清L2中での抗−TSHR自己抗体に対するGST−TSHR−融合タンパク質(TSHR−EDとTSHR−310)の混合物の用量依存性反応を示している。
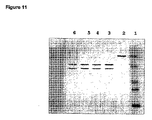
図11は、トロンビンによるGST−TSHR−融合タンパク質TSHR−EDの切断を示している。TSHR−EDとその断片は、抗−TSHRmAb2C11と二次的試薬で視覚化した。右から左に向かって:予備染色したマーカー:200、119、66、43、20、14.3 kD;GST−TSHR−ED、トロンビン無し;GST−TSHR−ED、0.1U トロンビン;GST−TSHR−ED、0.5Uトロンビン;GST−TSHR−ED、1Uトロンビン;GST−TSHR−ED、2Uトロンビン。
図12AとBは、患者血清L2、L1、M4及びM21中でのIgA(A.)とIgM(B.)抗−TSHR自己抗体に対する、直接にコーティング(白棒)した、又はグルタチオンによりコートした(黒棒)GSTタグ−TSHR−EDタンパク質の結合活性を示している。
図13AとBは、患者血清L2、L1、M4及びM21中でのIgA(A.)とIgM(B.)抗−TSHR自己抗体に対する、変性GST−TSHR−EDと非変性GST−TSHR−EDの結合活性を示している。
図14は、ヒトTSHRの種々のペプチドに対する個々の血清サンプル(血清M23)の反応性を示している。
図15は、ペップスキャン(Pepscan)法を用いた38個の患者血清の分析を示している。X軸は個々のペプチドを示し、Y軸は反応血清の頻度を示している。
図16は、同定したホットスポット(1−8)を用いたヒトTSHRの細胞外ドメインの概略グラフを示している。ホットスポット数の下には、同定したアミノ酸ドメイン(AA)の位置ならびに反応血清の数(カッコ内)が記載されている。
図17は、詳細な説明と、同定したホットスポットのペプチド配列が示されている。
図18は、TSHR特異的ペプチドに対する血清M460の反応性が示されている。一番右側には、正のコントロールである組換えTSHR−ED(ED)に対する反応性が示されている。
図19は、血清23及び血清460と組換えタンパク質(GST−TSHR−EDならびに負のコントロールGST)の結合活性の比較を示している。
図20は、自己反応性ホットスポットのコアエピトープを示し、角カッコ内の配列は、最小のエピトープ配列を示している。
本発明の詳細な説明
本明細書で使用されているような以下の定義は本発明を理解しやすくするために提供するものである。
本明細書で使用されているような以下の定義は本発明を理解しやすくするために提供するものである。
本明細書で使用されているように、"ポリペプチド"、"ペプチド"、"タンパク質"、"ポリペプチドの"及び"ペプチドの"という用語は区別なく使用され、α−アミノ酸と隣接する配列のカルボキシ基の間でのペプチド結合により、別のものに結合する一連のアミノ酸配列を示す。
本明細書で使用されているように、"融合タンパク質"という用語は、複合タンパク質を意味する。すなわち、通常は1本のアミノ酸配列中では融合しない2つ(以上)の別個の異種ポリペプチドから成る一本の連続したアミノ酸の配列を意味する。従って、融合タンパク質には、2つ(以上)の別個のアミノ酸配列を有する1本のアミノ酸配列も含まれるが、但し、これらの配列が一緒になっても天然にある1本のアミノ酸配列中で同じ配置では通常は見られない。
"グリコシド化されていないTSHレセプターの部分配列"、"グリコシド化されていない融合タンパク質"及び"グリコシド化されていない単離かつ精製した組換えポリペプチド"とは、グリコシル基と結合を形成しないポリペプチド配列を意味する。
"アミノ酸配列の断片"又は"その断片"とは、部分的には全く同じであるが、しかし、これらが誘導されるポリペプチドの各々の配列のアミノ酸配列の全てが同じわけではないアノ酸配列を意味する。通常、これらの配列は、これらが誘導されるポリペプチドの各々の配列と、少なくとも20%のアミノ酸長さを共有する。有利には、これらの配列は、これらが誘導されるポリペプチドの各々の配列と、少なくとも50%、有利には80%以上、特に90%以上のアミノ酸、特に95%以上のアミノ酸長さを共有する。これらの配列は、同じ特性、すなわち、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる生物学的機能と活性を示す限り、これらが誘導されるポリペプチドの各々の配列として使用できる。
"アミノ酸配列の変異体"又は"その変異体"とは、リファレンスの天然配列ポリペプチドとは或る程度異なるアミノ酸配列を有するポリペプチドを意味する。アミノ酸配列の変異体は、天然配列ポリペプチドと少なくとも80%の相同性を有する。有利には、これらの変異体は、このような天然配列ポリペプチドと、少なくとも約90%、特に少なくとも約95%の相同性を有する。アミノ酸配列の変異体は、天然のアミノ酸配列の一定の部位のアミノ酸配列内で、置換、欠失及び/又は挿入を有する。通常、これらのアミノ酸配列は、アミノ酸置換、有利には保存的アミノ酸置換によって天然の配列とは変化し、これにより、1つ以上のアミノ酸は、同じ特性を有する他のものにより置換される。本明細書中では、保存的アミノ酸置換は、例えば以下の5個の基のうち1つの中での置換として定義される。
I. 小さな脂肪族、非極性又は僅かに極性の配列:Ala、Ser、Thr、Pro、Gly
II. 極性の、プラスに帯電した配列:His、Arg、Lys
III. 極性の、負に帯電した配列:及びそれらのアミド:Asp、Asn、Glu、Gln
IV. 長い芳香族配列:Phe、Tyr、Trp
V. 長い脂肪族、非極性配列:Met、Leu、IlE、Val、Cys
"アミノ酸配列の変異体"又は"変異体"は、同じ特性、すなわち、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる生物学的機能と活性を示す限り、これらが誘導されるポリペプチドの各々の配列として使用できる。"ホモロジー"は、配列を並べ、かつギャップを挿入した後に同一であるアミノ酸配列変異体中の配列のパーセンテージとして定義される。必要な場合には、最大のパーセントのホモロジーを達成する。アライメントの方法とコンピュータープログラムは、当業者には周知である。
I. 小さな脂肪族、非極性又は僅かに極性の配列:Ala、Ser、Thr、Pro、Gly
II. 極性の、プラスに帯電した配列:His、Arg、Lys
III. 極性の、負に帯電した配列:及びそれらのアミド:Asp、Asn、Glu、Gln
IV. 長い芳香族配列:Phe、Tyr、Trp
V. 長い脂肪族、非極性配列:Met、Leu、IlE、Val、Cys
"アミノ酸配列の変異体"又は"変異体"は、同じ特性、すなわち、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる生物学的機能と活性を示す限り、これらが誘導されるポリペプチドの各々の配列として使用できる。"ホモロジー"は、配列を並べ、かつギャップを挿入した後に同一であるアミノ酸配列変異体中の配列のパーセンテージとして定義される。必要な場合には、最大のパーセントのホモロジーを達成する。アライメントの方法とコンピュータープログラムは、当業者には周知である。
"ベクター"、"宿主中で発現可能なベクター"又は"発現ベクター"とは、宿主細胞内で特殊な核酸配列の転写を可能にする特異的なポリ核酸成分の系列を用いて組換え又は合成により生じるポリ核酸構造物である。一般に、このベクターには、プロモーターに作動的に連結した転写すべき特殊な核酸配列を有する転写ユニットが含まれる。宿主細胞内で発現可能なベクターは、例えば自律的、又は自己複製プラスミド、コスミド又はファージである。
"宿主"、"宿主細胞"及び"組換え宿主細胞"は、本明細中では区別なく使用され、1つ以上のベクター又は本発明の単離かつ精製した核酸配列が組込まれた原核細胞を示す。このような用語は、特殊な被験者細胞だけを意味するのではなく、このような細胞の後代又は潜在的な後代も意味すると解釈される。突然変異又は環境の影響により後続の世代で特定の変性が起こるかもしれないので、事実上このような後代は、親細胞と同じであるが、本明細書で使用されているような用語の範囲に含まれる。
"単離かつ精製した核酸配列"という用語は、本発明に従った核酸配列になる状態を意味する。核酸配列は、それらの天然環境で、又は組換え技術によってこのような調製がインビトロ又はインビボで行われる場合には、それが調製(例えば、細胞培養)される環境で見られる他の核酸のような自然に関連する材料を含有しないか、又は殆ど含有しないであろう。
"細胞感染"又は"細胞形質転換"又は"感染/形質転換細胞"という用語は、細胞外核酸配列を挿入して細胞外核酸配列を宿らせた細胞を意味する。該核酸配列は、核酸が染色体の構成要素として、又は余分な染色体の成分として複製可能であるように細胞内に挿入される。
"抗体"とは、抗原により刺激された後に免疫系のB−細胞により産生されるプラズマタンパク質のクラスを意味する。哺乳類(すなわち、ヒト)の抗体は、IgG、IgM、IgA、IgE、IgDアイソタイプの免疫グロブリンである。本発明の目的のために使用される"抗体"という用語には、ポリクロナール抗体、モノクロナール抗体、抗イディオタイプ抗体及び自己免疫疾患で存在する自己抗体ならびにキメラ抗体が含まれるが、これに限定されるわけではない。抗体という用語は、全ての抗体とそれらの結合断片を意味して使用される。結合断片には、1本鎖断片、Fv断片とFab断片が含まれる。Fab断片という用語は、この分野では時折、無傷の抗体のパパイン切断から生じる結合断片を意味して使用される。Fab’とF(ab’)2という用語は、この分野では時折、ペプシン切断から生じる結合断片を意味して使用される。本発明の範囲内では、Fabは、遺伝学的に、抗原特異的結合に十分な、少なくとも殆ど完全なL鎖とH鎖の可変ドメインと、L鎖とH鎖の関係を維持するために十分な該L鎖とH鎖の定常領域の部分を有する無傷な抗体の二本鎖結合断片を意味する。更に含まれるものは、キメラ抗体であり、これは例えば、種々の種に属する免疫グロブリンの遺伝子セグメント(例えば、可変領域をコードするセグメントと定常領域をコードするセグメント)から、そのL鎖とH鎖の遺伝子が遺伝子工学により構築された抗体である。
"TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体"、"TSHRに対する自己抗体"又は"抗−TSHR抗体"とは、TSHレセプターに結合できるTSHレセプターに対する抗体を意味する。これらの自己抗体のタイプにより、甲状腺ホルモンT3及びT4の形成又は放出の阻害が生じ得るか、又は他方では、抗−TSHレセプター自己抗体が、TSHの作用を真似て甲状腺ホルモンの合成と放出を刺激するので、これらの甲状腺ホルモンが制御されずに放出されてしまう。更に、TSHレセプターに結合するが、甲状腺ホルモンの産生を刺激しない自己抗体は、ブロッキング活性を有するものとして記載される。
ここで、"被験者"とは通常はヒト又は動物、有利にはヒトを意味する。より好ましく"被験者"とは、TSHレセプターに対する免疫反応と関連する自己免疫疾患を患っている疑いのある、該疾患にかかりやすい、該疾患を保持又は回復しているヒト又は動物を意味する。
本明細書では、"エピトープ"とは抗体を誘発し、かつ結合する能力又はポテンシャルのあるポリペプチドのような抗原上の一部又は一カ所を意味する。ポリペプチドは、しばしば1つ以上のエピトープを含む。本開示の目的で、ポリペプチドのエピトープは、通常少なくとも3つのアミノ酸、有利には5〜50個のアミノ酸、より有利には約5〜20個のアミノ酸、最も有利には約8〜15個のアミノ酸を含み、本明細書中では、ペプチド中の"コアエピトープ"と称される。ペプチドの長さには決定的な上限がなく、ポリペプチド配列の全長を殆ど有することができる。エピトープは、線状又は構造的エピトープであることができる。線状エピトープは、ポリペプチド鎖の一次配列の1本のセグメントから成る。線状エピトープは、連続的又は重複していてよい。構造的エピトープは、ポリペプチドのフォールディングにより一緒になって三次構造を形成したアミノ酸から成り、かつ前記アミノ酸は、必ずしも線状配列中で互いに隣り合っているわけではない。
もう1つの態様では、本発明は、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質を有する、グリコシド化されていない単離かつ精製した組換えポリペプチドを提供する。該ポリペプチドは、次の
a)原核宿主細胞の細胞質内でジスルフィド結合の形成を可能にする突然変異を有さない原核宿主を、前記融合タンパク質をコードする単離かつ精製した核酸配列を有するベクターで形質転換させ、その際、1つ以上のTSHレセプターの部分配列はポリペプチドに融合し、かつ前記TSHレセプターの部分配列は、主にTSHレセプターの細胞外ドメイン、その断片又はその変異体から成っている;
b)前記原核宿主細胞を培養し、それにより前記融合タンパク質を発現させ、前記原核宿主細胞内に蓄積させ;
c)前記原核宿主細胞を単離し;
d)界面活性剤の存在で前記原核宿主細胞を溶解し;
e)溶解産物の可溶性成分を不溶性成分から分離し;かつ
f)前記溶解産物の可溶性成分からの融合タンパク質を精製する
方法により得られる。
a)原核宿主細胞の細胞質内でジスルフィド結合の形成を可能にする突然変異を有さない原核宿主を、前記融合タンパク質をコードする単離かつ精製した核酸配列を有するベクターで形質転換させ、その際、1つ以上のTSHレセプターの部分配列はポリペプチドに融合し、かつ前記TSHレセプターの部分配列は、主にTSHレセプターの細胞外ドメイン、その断片又はその変異体から成っている;
b)前記原核宿主細胞を培養し、それにより前記融合タンパク質を発現させ、前記原核宿主細胞内に蓄積させ;
c)前記原核宿主細胞を単離し;
d)界面活性剤の存在で前記原核宿主細胞を溶解し;
e)溶解産物の可溶性成分を不溶性成分から分離し;かつ
f)前記溶解産物の可溶性成分からの融合タンパク質を精製する
方法により得られる。
本発明のもう1つの態様では、原核宿主細胞の細胞質内でジスルフィド結合の形成を可能にする突然変異を有さない原核宿主内で発現される、グリコシド化されていない単離かつ精製した組換えポリペプチドを提供し、前記グリコシド化されていない単離かつ精製した組換えポリペプチドは、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質を有し、その際、1つ以上のTSHレセプターの部分配列は、主にグルタチオンSトランスフェラーゼ(GST)から成るポリペプチド、その断片又はその変異体に融合し、かつ前記TSHレセプターの部分配列は、主にTSHレセプターの細胞外ドメイン、その断片又はその変異体から成っている。
TSHレセプターの部分配列は、ヒト、ブタ、ウシ、サル又はマウス由来であることができる。有利には、本発明のTSHレセプターの部分配列は、ヒト由来である。ヒトTSHレセプターのアミノ酸配列は、例えば、Frazier等、Mol. Endocrinol. 4(8), 1264-1276(1990)に記載されている。
融合させるべきポリペプチドは、当業者に公知のポリペプチド又はそれらの断片又は変異体であることができる。真核生物又は原核生物由来のポリペプチドを使用できる。数ある中で、融合構造を製造するために通常市販されているポリペプチド、例えば、グルタチオンSトランスフェラーゼ(GST)、β−グルクロニダーゼ(GUS)、緑色蛍光タンパク質(GFP)又はマルトース結合タンパク質(MBP)もしくはセルロース結合ドメイン(CBD)のような原核結合タンパク質を使用できる。同様に、オープンリーディングフレーム(orf)配列、又は例えば、様々な組換え技法において望ましい又は利用してもよい他の有利な配列を使用できる。これには相同組み換え(例えば、遺伝子ターゲッティング)で使用する配列が含まれる。同様に、ポリヒスチジンリンカー、T7−タグ、myc−タグ、Flag−タグ又はV5−タグのようなポリアミノ酸配列を融合すべきポリペプチドとして使用できる。
通常、1つのTSHレセプターの部分配列は、1つのペプチドに融合する。本発明のTSHレセプターの部分配列は、ポリペプチドのN末端又はC末端でポリペプチドに融合し、有利にはこれはポリペプチドのC末端に融合する。TSHレセプターの部分配列は、ポリペプチド配列のN末端又はC末端でポリペプチドに直接融合できる。すなわち、各々の配列の最後のアミノ酸に、他の各々の配列の最初のアミノ酸が続く。また、有利には、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質の生物学的機能と活性が維持される限り、付加的なアミノ酸が両方の配列の間に位置する。融合タンパク質が、ポリペプチドの最後のアミノ酸と、TSHレセプターの部分配列の最初のアミノ酸との間に付加的なアミノ酸を含有する場合には、これらの付加的なアミノ酸の数は通常は最大で4つのアミノ酸、有利には、最大で2つのアミノ酸、より有利には丁度2個のアミノ酸に限定され、特に有利には、ポリペプチドのC末端から次の順番で存在する2個のアミノ酸に限定される:グリシンに続いてセリン。
本発明のTSHレセプターの部分配列に融合すべき有利なポリペプチドは、主にグルタチオンSトランスフェラーゼ(GST)、β−グルクロニダーゼ(GUS)、緑色蛍光タンパク質(GFP)又はマルトース結合タンパク質(MBP)もしくはセルロース結合ドメイン(CBD)のような原核結合タンパク質、その断片又はその変異体から成る。より有利には、本発明のTSHレセプターの部分配列と融合すべきポリペプチドは、主にグルタチオンSトランスフェラーゼ(GST)、その断片又はその変異体から成る。通常、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質の生物学的機能と活性が維持される限り、融合タンパク質はTSHレセプターの部分配列のC末端で、0〜10個、有利には4〜8個の付加的なアミノ酸を有する。より有利には、融合タンパク質は、TSHレセプターの部分配列で丁度6個の付加的なアミノ酸を有する。6個のアミノ酸をTSHレセプターの部分配列のC末端から次の順番で有する融合タンパク質が最も有利である:グルタミン酸、続いてフェニルアラニン、続いてイソロイシン、続いてバリン、続いてトレオニン及び続いてアスパラギン酸。
"TSHレセプターの部分配列"とは、TSHレセプターの細胞外ドメイン、その断片又はその変異体と全く同じアミノ酸配列を意味する。通常は、TSHレセプターの細胞外ドメイン、その断片又はその変異体は、主にTSHのN末端から20〜418番目のアミノ酸配列から成る。有利には、TSHレセプターの部分配列は、主に次のアミノ酸配列のうち1つ、その断片又はその変異体:
TSHレセプターのN−末端から22〜415番目のアミノ酸配列;
TSHレセプターのN−末端から210〜415番目のアミノ酸配列;
TSHレセプターのN−末端から310〜415番目のアミノ酸配列から成る。
TSHレセプターのN−末端から22〜415番目のアミノ酸配列;
TSHレセプターのN−末端から210〜415番目のアミノ酸配列;
TSHレセプターのN−末端から310〜415番目のアミノ酸配列から成る。
TSHレセプターの部分配列が主に以下のアミノ酸配列のうちの1つ:配列番号1、配列番号2及び配列番号3、特に主に配列番号3、その断片又はその変異体から成るグリコシド化されていない単離かつ精製したポリペプチドがより有利である。
TSHレセプターの部分配列が次のもの:
a)配列番号1に示したTSHレセプターのN末端から22〜415番目のアミノ酸配列を有するアミノ酸配列;
b)a)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
c)配列番号2に示したTSHレセプターのN末端から210〜415番目のアミノ酸配列を有するアミノ酸配列;
d)c)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
e)配列番号3に示したTSHレセプターのN末端から310〜415番目のアミノ酸配列を有するアミノ酸配列;
f)e)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
から成るグループから選択される、グリコシド化されていない単離かつ精製した組換えポリペプチドも更に有利であり、特に、TSHレセプターの部分配列がe)とf)で定義したアミノ酸から成るグループから選択される、グリコシド化されていない単離かつ精製した組換えポリペプチドが有利である。
a)配列番号1に示したTSHレセプターのN末端から22〜415番目のアミノ酸配列を有するアミノ酸配列;
b)a)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
c)配列番号2に示したTSHレセプターのN末端から210〜415番目のアミノ酸配列を有するアミノ酸配列;
d)c)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
e)配列番号3に示したTSHレセプターのN末端から310〜415番目のアミノ酸配列を有するアミノ酸配列;
f)e)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
から成るグループから選択される、グリコシド化されていない単離かつ精製した組換えポリペプチドも更に有利であり、特に、TSHレセプターの部分配列がe)とf)で定義したアミノ酸から成るグループから選択される、グリコシド化されていない単離かつ精製した組換えポリペプチドが有利である。
b)、d)及びf)で定義したアミノ酸配列は、有利にはa)、c)及びe)で定義したリファレンスのアミノ酸配列に少なくとも85%、より有利には少なくとも90%、最も有利には少なくとも95%、特に少なくとも97%、とりわけ有利には99%相同であるアミノ酸配列を有し、かつアミノ酸の保存的置換により、リファレンスの配列とは異なっているのが有利である。
主に以下のアミノ酸配列:配列番号4、配列番号5及び配列番号6のうち1つ、特に主に配列番号6、その断片又はその変異体から成るグリコシド化されていない単離かつ精製した組換えポリペプチドが最も有利である。
次のもの:
a)配列番号4に示したアミノ酸配列を有するアミノ酸配列;
b)a)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
c)配列番号5に示したアミノ酸配列を有するアミノ酸配列;
d)c)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
e)配列番号6に示したアミノ酸配列を有するアミノ酸配列;
f)e)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
から成るグループから選択される、グリコシド化されていない単離かつ精製した組換えポリペプチドが特に有利であり、更に有利であるのは、e)とf)で定義したアミノ酸配列から成るグループから選択されるグリコシド化されていない単離かつ精製した組換えポリペプチドである。b)、d)及びf)で定義したアミノ酸配列は、有利にはa)、c)及びe)で定義したリファレンスのアミノ酸配列に少なくとも85%、より有利には少なくとも90%、最も有利には少なくとも95%、特に少なくとも97%、とりわけ有利には99%相同であるアミノ酸配列を有し、かつアミノ酸の保存的置換により、リファレンスの配列とは異なっているのが有利である。
a)配列番号4に示したアミノ酸配列を有するアミノ酸配列;
b)a)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
c)配列番号5に示したアミノ酸配列を有するアミノ酸配列;
d)c)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
e)配列番号6に示したアミノ酸配列を有するアミノ酸配列;
f)e)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
から成るグループから選択される、グリコシド化されていない単離かつ精製した組換えポリペプチドが特に有利であり、更に有利であるのは、e)とf)で定義したアミノ酸配列から成るグループから選択されるグリコシド化されていない単離かつ精製した組換えポリペプチドである。b)、d)及びf)で定義したアミノ酸配列は、有利にはa)、c)及びe)で定義したリファレンスのアミノ酸配列に少なくとも85%、より有利には少なくとも90%、最も有利には少なくとも95%、特に少なくとも97%、とりわけ有利には99%相同であるアミノ酸配列を有し、かつアミノ酸の保存的置換により、リファレンスの配列とは異なっているのが有利である。
なお特に有利であるのは、主に次のアミノ酸配列のうち1つ:配列番号4、配列番号5及び配列番号6、特に配列番号6から成るグリコシド化されていない単離かつ精製した組換えポリペプチドである。最も特に有利であるのは、次のアミノ酸配列のうち1つ:配列番号4、配列番号5及び配列番号6、特に配列番号6から成るグリコシド化されていない単離かつ精製した組換えポリペプチドである。
意外にも、本発明のグリコシド化されていない単離かつ精製した組換えポリペプチドが、それらの生理学的リガンドであるTSH(甲状腺刺激ホルモン)ならびに2C11及び4C1のようなモノクロナール抗−TSHR抗体(両方ともSerotec GmbH社から市販されている)ならびに甲状腺刺激抗体の国際基準血清90/672(一人の患者から調製される)に含まれている、国立生物製剤基準管理研究所(NIBSC)から入手可能なTSHR自己抗体に結合できることが見出された。
本発明のグリコシド化されていない単離かつ精製した組換えポリペプチドは、融合ポリペプチドのない各々のTSHレセプターの部分配列を得るために、消化又は切断されることになる。
従って、本発明の更なる実施態様は、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる、グリコシド化されていないTSHレセプターの部分配列であり、前記グリコシド化されていないTSHレセプターの部分配列は、主にTSHレセプターの細胞外ドメイン、その断片又はその変異体から成り、次のもの
a)原核宿主細胞の細胞質内でジスルフィド結合の形成を可能にする突然変異を有さない原核宿主を、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質をコードする単離かつ精製した核酸配列を有するベクターで形質転換し、その際、1つ以上のTSHレセプターの部分配列は、ポリペプチドに融合し、かつその際前記TSHレセプターの部分配列は、主にTSHレセプターの細胞外ドメイン、その断片及びその変異体から成っている、
b)前記原核宿主細胞を培養し、それにより前記融合タンパク質を発現させ、前記原核宿主細胞内に蓄積させ;
c)前記原核宿主細胞を単離し;
d)界面活性剤の存在で前記原核宿主細胞を溶解し;
e)溶解産物の可溶性成分を不溶性成分から分離し;かつ
f)前記溶解産物の可溶性成分から融合タンパク質を精製し;
g)前記TSHレセプターの部分配列に融合したポリペプチドを消化又は切断し;かつ
h)前記TSHレセプターの部分配列、その断片又はその変異体を回収する
から成る方法により得られる。
a)原核宿主細胞の細胞質内でジスルフィド結合の形成を可能にする突然変異を有さない原核宿主を、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質をコードする単離かつ精製した核酸配列を有するベクターで形質転換し、その際、1つ以上のTSHレセプターの部分配列は、ポリペプチドに融合し、かつその際前記TSHレセプターの部分配列は、主にTSHレセプターの細胞外ドメイン、その断片及びその変異体から成っている、
b)前記原核宿主細胞を培養し、それにより前記融合タンパク質を発現させ、前記原核宿主細胞内に蓄積させ;
c)前記原核宿主細胞を単離し;
d)界面活性剤の存在で前記原核宿主細胞を溶解し;
e)溶解産物の可溶性成分を不溶性成分から分離し;かつ
f)前記溶解産物の可溶性成分から融合タンパク質を精製し;
g)前記TSHレセプターの部分配列に融合したポリペプチドを消化又は切断し;かつ
h)前記TSHレセプターの部分配列、その断片又はその変異体を回収する
から成る方法により得られる。
有利なグリコシド化されていないTSHレセプターの部分配列として、ポリペプチドに融合したTSHレセプターの部分配列は、主に次のアミノ酸配列のうち1つ、その断片又はその変異体:
TSHレセプターのN−末端から22〜415番目のアミノ酸配列;
TSHレセプターのN−末端から210〜415番目のアミノ酸配列;
TSHレセプターのN−末端から310〜415番目のアミノ酸配列;
から成る。
TSHレセプターのN−末端から22〜415番目のアミノ酸配列;
TSHレセプターのN−末端から210〜415番目のアミノ酸配列;
TSHレセプターのN−末端から310〜415番目のアミノ酸配列;
から成る。
より有利であるのは、次のもの
a)配列番号1に示したTSHレセプターのN末端から22〜415番目のアミノ酸配列を有するアミノ酸配列;
b)a)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
c)配列番号2に示したTSHレセプターのN末端から210〜415番目のアミノ酸配列を有するアミノ酸配列;
d)c)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
e)配列番号3に示したTSHレセプターのN末端から310〜415番目のアミノ酸配列を有するアミノ酸配列;
f)e)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
から成るグループから選択されるグリコシド化されていないTSHレセプターの部分配列である。
a)配列番号1に示したTSHレセプターのN末端から22〜415番目のアミノ酸配列を有するアミノ酸配列;
b)a)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
c)配列番号2に示したTSHレセプターのN末端から210〜415番目のアミノ酸配列を有するアミノ酸配列;
d)c)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
e)配列番号3に示したTSHレセプターのN末端から310〜415番目のアミノ酸配列を有するアミノ酸配列;
f)e)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
から成るグループから選択されるグリコシド化されていないTSHレセプターの部分配列である。
特に、TSHレセプターの部分配列が、e)とf)で定義したアミノ酸配列から成るグループから選択されるグリコシド化されていない単離かつ精製した組換えポリペプチドが有利である。
b)、d)及びf)で定義したアミノ酸配列は、有利にはa)、c)及びe)で定義したリファレンスのアミノ酸配列に少なくとも85%、より有利には少なくとも90%、最も有利には少なくとも95%、特に少なくとも97%、とりわけ有利には少なくとも99%相同であるアミノ酸配列を有し、かつアミノ酸の保存的置換により、リファレンスの配列とは異なっているのが有利である。最も有利には、ポリペプチドに融合したTSHレセプターの部分配列は、主に以下のアミノ酸配列のうちの1つ:配列番号1、配列番号2及び配列番号3、その断片又はその変異体から成り、特に、これは主に配列番号3から成る。
グリコシド化されていない単離かつ精製した組換えポリペプチドと各々のグリコシド化されていないTSHレセプターの部分配列が得られる方法ならびに、本発明の原核宿主細胞の細胞質内でジスルフィド結合の形成を可能にする突然変異を有さない原核宿主内で発現したグリコシド化されていない単離かつ精製した組換えポリペプチドを得るために利用できる方法は、まず所望のポリペプチドをコードする核酸に融合できるTSHレセプターの部分配列をコードする単離かつ精製した核酸配列を生成することにより実施できる。得られた構造物は、通常は適切な規則的配列を宿らせるベクター内にライゲーションでき、かつベクターをこの分野で周知の標準的方法に従って使用して、各々の原核宿主を形質転換できる。細胞培養系として、バッチ培養又はフェドバッチ培養のような連続又は不連続培養を、培養管、振盪フラスコ又は細菌発酵槽で利用できる。宿主細胞は、この分野で公知の"栄養酵母エキス培地"又はLurin Berthani(LB)培地のような複合培地のような通常の培地で培養される。ポリペプチドの発現を実施するために有利な培地は、Lurin Berthani(LB)培地である。
培地は、例えば、緩衝液、塩、ビタミン又はアミノ酸のような更なる成分を添加して適切に変性される。同様に、種々の培地又は培地の組合せを細胞の培養の際に使用できる。適切なpH範囲は、例えば、6〜8、有利には7〜7.5であり、適切な培養温度は、10〜40℃の間、有利には20〜37℃の間である。宿主細胞は、通常は発現生成物が蓄積されるまで、有利には1時間から5日の間培養される。細胞の単離は、この分野で公知の方法、例えば、遠心分離により実施でき、これが好ましい。界面活性剤の存在での単離細胞の溶解は、通常細胞を界面活性剤中に再懸濁させるか、又は有利には細胞を初めにTRIS緩衝生理食塩水(TBS)又はリン酸緩衝生理食塩水(PBS)のような緩衝液中に再懸濁させ、次に、更に界面活性剤中に再懸濁させて行われる。界面活性剤として、通常はSDS(ドデシル硫酸ナトリウム)のような1つ以上のイオン界面活性剤、又はTriton X-100、Nonidet P40、N−オクチルグルコシドのような1つ以上の非イオン界面活性剤を使用できる。有利には、1つ以上の非イン界面活性剤が使用され、より有利には1つの非イオン界面活性剤、最も有利にはTritonX-100が使用される。本発明の界面活性剤は、尿素を含まない。界面活性剤は、一般にTRIS緩衝生理食塩水(TBS)又はリン酸緩衝生理食塩水(PBS)のような緩衝液中に含有されていて、これらには更にジチオトレイトール(DTT)又はメルカプトエタノールのような還元化合物が含まれていてもよい。界面活性剤は、一般に0.1〜2%の間、有利には0.5〜1.5%の間の濃度で利用される。単離細胞は、例えば、超音波処理、リゾチームの添加、細胞ホモジナイザー中で金属ビーズを用いる機械的崩壊のようなこの分野で公知の方法、有利には、超音波処理により溶解できる。
細菌の溶解産物をインキュベートするのが有利である。有利には、低温で、例えば、氷の上で、1〜60分間の間、有利には20〜40分間の間インキュベートし、タンパク質の最大の溶解化を得る。
不溶性成分からの溶解産物の可溶性成分の分離は、この分野で公知の方法により実施できる。一般に、融合タンパク質の構成に影響を与えない方法として、例えば遠心分離が使用され、これが好ましい。次に、この分野では公知のタンパク質精製法により、溶解産物の可溶性成分から融合タンパク質が精製される。前記精製法には、示差沈殿(differential precipitation)、分子篩クロマトグラフィー、イオン交換クロマトグラフィー、等電集束法、ゲル電気泳動、アフィニティー・クロマトグラフィー及びイムノアフィニティー・クロマトグラフィーが含まれる。これらの周知かつ日常的に行われている方法は、例えば、Ausubel等、1994、Current protocols in molecular biology, John Wiley and Sons, and Wu等(著者), Academic Press Inc., N. Y.; Immunochemical Methods In Cell And Molecular Biologyに記載されている。一般に、融合タンパク質の構成に影響を与えない方法として、例えば分子篩いクロマトグラフィー、イオン交換クロマトグラフィー、等電集束法、ゲル電気泳動、アフィニティー・クロマトグラフィー及びイムノアフィニティー・クロマトグラフィーが使用され、アフィニティー・クロマトグラフィーが好ましい。GSTが融合ポリペプチドとして使用される場合には、溶解産物の可溶性成分から融合タンパク質を精製するために、グルタチオンセファロースクロマトグラフィーのようなグルタチオン・アフィニティー・クロマトグラフィーを用いるのが有利である。ポリヒスチジンリンカーを付加的なアミノ酸として使用する場合には、Ni−アガロースのような固定化金属アフィニティー・クロマトグラフィーを使用して精製を実施することができる。精製した融合タンパク質は、通常公知のTBSのような緩衝液に透析でき、かつこのような緩衝液中に溶解して本発明の自己抗体を検出及び/又は定量化する方法に使用できる。
精製した融合タンパク質を更に消化又は切断して、各々のTSHレセプターの部分配列を得る場合には、当業者に公知の方法に従って、例えば融合ポリペプチドの化学的消化により、又は例えばトロンビンのような特異的なプロテアーゼによって、融合ポリペプチドと、各々のTSHレセプターの部分配列の間での酵素切断により行うことができる。
各々のTSHレセプターの部分配列は、ゲル電気泳動又はアフィニティー・クロマトグラフィーのような公知の方法により消化又は切断した後に、回収できる。例11から分かるように、本発明の融合タンパク質のTSHレセプターの部分配列は、トロンビンにより、見かけ分子量約45kDaと約35kDaの2つの断片に切断され、本発明のグリコシド化されていない単離かつ精製した組換えポリペプチドが、TSHレセプターの部分配列の中に少なくとも1つのトロンビン切断領域を有することを示している。
トロンビンにより、見かけ分子量約45kDaと約35kDaの2つの断片に切断された本発明の有利な融合タンパク質は、TSHレセプターの部分配列の中に少なくとも1つのトロンビン切断領域を有する本発明のグリコシド化されていない単離かつ精製した組換えポリペプチドが、
a)配列番号4に示されているようなアミノ酸配列を有するアミノ酸配列;
b)a)で定義したアミノ酸配列に少なくとも80%の相同であるアミノ酸配列
から成るグループから選択グリコシド化されていない単離かつ精製した組換えポリペプチドであることを示している。
a)配列番号4に示されているようなアミノ酸配列を有するアミノ酸配列;
b)a)で定義したアミノ酸配列に少なくとも80%の相同であるアミノ酸配列
から成るグループから選択グリコシド化されていない単離かつ精製した組換えポリペプチドであることを示している。
更に、本発明により提供されるものは、
a)配列番号10〜27から選択されるアミノ酸配列の少なくとも5個の連続したアミノ酸を有するエピトープ;
b)配列番号10〜27から選択されるアミノ酸配列を有するエピトープ:
c)a)又はb)で定義したアミノ酸配列に少なくとも60%相同であるエピトープ;
から成るグループから選択されるグリコシド化されていないTSHレセプターの部分配列のエピトープである。
a)配列番号10〜27から選択されるアミノ酸配列の少なくとも5個の連続したアミノ酸を有するエピトープ;
b)配列番号10〜27から選択されるアミノ酸配列を有するエピトープ:
c)a)又はb)で定義したアミノ酸配列に少なくとも60%相同であるエピトープ;
から成るグループから選択されるグリコシド化されていないTSHレセプターの部分配列のエピトープである。
a)のエピトープは、有利には配列番号10〜27から選択されるアミノ酸配列の少なくとも8個の連続したアミノ酸を有する。
図15に示されているように、a)〜c)から成るグループから選択される有利なエピトープは、抗−TSHR自己抗体含有の患者血清少なくとも15個、有利には20〜38個と反応性を示す。
本発明のより有利なエピトープは、
a)配列番号12、13、16、17、20、21、26及び27から選択されるアミノ酸配列の少なくとも5個の連続したアミノ酸を有するエピトープ;
b)配列番号12、13、16、17、20、21、26及び27から選択されるアミノ酸配列を有するエピトープ:
c)a)又はb)で定義したアミノ酸配列に少なくとも60%相同であるエピトープ;
から成るグループから選択されるグリコシド化されていないTSHレセプターの部分配列のエピトープである。
a)配列番号12、13、16、17、20、21、26及び27から選択されるアミノ酸配列の少なくとも5個の連続したアミノ酸を有するエピトープ;
b)配列番号12、13、16、17、20、21、26及び27から選択されるアミノ酸配列を有するエピトープ:
c)a)又はb)で定義したアミノ酸配列に少なくとも60%相同であるエピトープ;
から成るグループから選択されるグリコシド化されていないTSHレセプターの部分配列のエピトープである。
c)で定義されたエピトープは、(a)又は(b)で定義したアミノ酸配列に、有利には少なくとも70%、より有利には少なくとも80%、最も有利には少なくとも90%、特に少なくとも95%相同である。
更に提供されるものは、本発明のグリコシド化されていない単離かつ精製した組換えポリペプチドから成る融合タンパク質をコードする単離かつ精製した核酸配列である。本発明により包含される単離かつ精製した核酸配列は、DNA又はcDNA、RNA、又はDNA/RNAハイブリッドである。一般に、これはDNA又はcDNAである。
有利には、グリコシド化されていない単離かつ精製した組換えポリペプチドから成る融合タンパク質をコードする単離かつ精製した核酸配列は、主に、配列番号7、配列番号8又は配列番号 9から、より有利には配列番号9から成る。
前記精製かつ単離した核酸配列は、通常は更にこの分野で公知であるような1つ以上の調節領域、例えば、プロモーター及び/又はエンハンサー、ポリアデニル化部位及びスプライス接合部を有する。これらは、通常はタンパク質を発現するために、又は場合により選択可能なマーカーをコード化するために使用される。有利には、前記の精製かつ単離した核酸配列は、有利な配列又は遺伝子に作動的に結合しているプロモーターを有する。本発明の核酸配列は、標準的なPCRプロトコールにより、かつこの分野で周知の方法により単離できる。また、本発明には、遺伝子コードの変性により、かつ保存的核酸の置換により1個以上の核酸が同じ特性を有する他のものにより置換されて、リファレンス配列とは変化した核酸配列が含まれる。
本発明の単離かつ精製した核酸配列は、通常はベクター上に存在する。従って、同じく本発明に包含されるものは、本発明の単離かつ精製した核酸の少なくとも1つのコピーを有するベクターである。
本発明によるベクターは、有利には自律的又は自己複製プラスミド、コスミド又はファージである。本発明の核酸配列の発現において、様々な宿主/ベクターの組合せを使用してもよい。有用なベクターは、例えば、染色体、非染色体及び/又は合成核酸配列から成っていてよい。適切なベクターには、例えば大腸菌に特異的なベクターのような特異的宿主範囲を有するベクターならびにグラム陰性細菌に有用なベクターのような幅広い宿主範囲を有するベクターが含まれる。"低コピー数"、"中コピー数"ならびに"高コピー数"プラスミドを使用できる。例えば、大腸菌で発現させるのに有用なベクターは次のものである:pQE70、pQE60及びpQE-9(QIAGEN, Inc.社);pブルースクリプトベクター、ファージスクリプトベクター、pNH8A、pNH16a、pNH18A、pNH46A(Stratagene Cloning Systems, Inc.社);ptrc99a、pKK223-3、pKK233-3、pDR540、pRIT5(Pharmacia Bio-tech, Inc.社)、pGEX-2T(Amersham Biosciences社)、pET14b(Novagen社)のようなpETベクター又はその誘導体である。更に有用なプラスミドは、当業者に周知であり、かつ例えば、"Cloning Vectors"(出版社Pouwels P. H. 等、Elsevier, Amsterdam-New York-Oxford, 1985)に記載されている。
本発明によるベクターは、有利には自律的又は自己複製プラスミド、コスミド又はファージである。本発明の核酸配列の発現において、様々な宿主/ベクターの組合せを使用してもよい。有用なベクターは、例えば、染色体、非染色体及び/又は合成核酸配列から成っていてよい。適切なベクターには、例えば大腸菌に特異的なベクターのような特異的宿主範囲を有するベクターならびにグラム陰性細菌に有用なベクターのような幅広い宿主範囲を有するベクターが含まれる。"低コピー数"、"中コピー数"ならびに"高コピー数"プラスミドを使用できる。例えば、大腸菌で発現させるのに有用なベクターは次のものである:pQE70、pQE60及びpQE-9(QIAGEN, Inc.社);pブルースクリプトベクター、ファージスクリプトベクター、pNH8A、pNH16a、pNH18A、pNH46A(Stratagene Cloning Systems, Inc.社);ptrc99a、pKK223-3、pKK233-3、pDR540、pRIT5(Pharmacia Bio-tech, Inc.社)、pGEX-2T(Amersham Biosciences社)、pET14b(Novagen社)のようなpETベクター又はその誘導体である。更に有用なプラスミドは、当業者に周知であり、かつ例えば、"Cloning Vectors"(出版社Pouwels P. H. 等、Elsevier, Amsterdam-New York-Oxford, 1985)に記載されている。
本発明の有利なベクターは、自律的又は自己複製プラスミドであり、より有利には、例えば大腸菌に特異的であるベクターのような特異的宿主範囲を有するベクターである。最も有利なものは、pGEX-2T又はpET14bのようなpETベクター、又はその誘導体、特に有利なものは、pGEX-2T又はその誘導体である。特に有利なものは、pGEX2T-TSHR-ED、pGEX2T-TSHR-210及びpGEX2T-TSHR-310である。
本発明の単離かつ精製した組換えポリペプチド及TSHレセプターの部分配列は、原核宿主細胞の細胞質内でジスルフィド結合の形成を可能にする突然変異を有さず、かつ、各々の核酸配列で形質転換できる様々な原核宿主細胞内で産生できる。従って、本発明の更なる対象は、本発明の核酸配列及び/又はベクターで形質転換したその細胞質内にジスルフィド結合の形成を可能にする突然変異を有さない原核宿主細胞である。本発明の原核宿主細胞は、通常はその細胞質内でジスルフィド結合を形成できない。本発明による核酸配列を有するベクターでの適切な宿主細胞の形質転換は、一般に使用されるベクターの種類に応じて周知の方法により達成される。これらの方法に関して、例えばManiatis等、1982, Molecular Cloning, A laboratory Manual, Cold Spring Harbor Laboratory及び市販の方法を参照されたい。
それらの細胞質内にジスルフィド結合の形成を可能にする突然変異を有さない幅広い様々な原核宿主細胞は、本発明の核酸配列の発現において有用である。これらの宿主には、例えば、大腸菌及びシュードモナス属のようなグラム陰性細胞、又はバチルス属及びスプレプトマイセス属のようなグラム陽性細胞の株を含めてもよい。
有利には、宿主細胞は、グラム陰性細胞であり、より有利には大腸菌である。使用できる大腸菌は、例えば、BL21、TG1、W3110、DH1、XL1-Blue及びOrigami株、又はこれらの誘導体であり、これらは市販されているか、又はDSMZ(ドイツ微生物寄託当局、ブラウンシュバイク、ドイツ)から入手可能である。BL21(Novagen社)又はその誘導体を使用するのが最も有利である。
他の態様では、本発明は、被験者の生体液中で、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を検出及び/又は定量化する方法を目的とし、該方法は、
a)前記の生体液を、本発明の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列の1つ以上のエピトープと接触させ、かつ
b)前記グリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は前記グリコシド化されていないTSHレセプターの部分配列及び/又は前記エピトープに結合した自己抗体を検出及び/又は定量化する
ことから成る。
a)前記の生体液を、本発明の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列の1つ以上のエピトープと接触させ、かつ
b)前記グリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は前記グリコシド化されていないTSHレセプターの部分配列及び/又は前記エピトープに結合した自己抗体を検出及び/又は定量化する
ことから成る。
本発明の有利な方法は、
a)前記の生体液を、本発明の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープと接触させ、かつ
b)前記グリコシド化されていない単離かつ精製した組換えポリペプチド及び前記エピトープに結合した自己抗体を検出及び/又は定量化する
ことから成る。
a)前記の生体液を、本発明の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープと接触させ、かつ
b)前記グリコシド化されていない単離かつ精製した組換えポリペプチド及び前記エピトープに結合した自己抗体を検出及び/又は定量化する
ことから成る。
本発明による方法は、アッセイとして行うことができる。アッセイで、本発明のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープを用いる、本発明の方法によって、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を検出及び/又は定量化するための方法と試薬は、通常のものであってよく、かつ本発明の開示を理解する当業者により、よく容認されている診断上かつ免疫診断的方法論の原則に留意しながら設計かつ選択が認められる。このような原則は、例えば、Harlow, E., and Lane, D. "Antibodies: A Laboratory Manual" Cold Spring Harbor Laboratory, Cold Spring Harbor, NY, 349(1988), 著者Rose, Noel R等、Manual of Clinical Laboratory Immunology, 第5版、ASM Press, Washington D. C.(1997), 及び先行版;著者Rich, R.等、Clinical Immunology, 出版社Mosby, St. Louis(1995)に記載されている。
本発明の方法の実施により使用でき、かつキットの形で組み込むことができるアッセイのタイプは多く、例えば、間接アッセイ又は直接アッセイを含む。現在有利に行われている間接アッセイは、競合アッセイと非競合アッセイであり、現在は非競合アッセイが好ましい。本発明のグリコシド化されていない単離かつ精製した組換えポリペプチド、グリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープを利用できる一般的なアッセイの例は、免疫検定法(EIA)とも称される酵素結合免疫吸着検定法(ELISA)、蛍光免疫吸着検定法(LISA)、放射線免疫検定法(RIA)、ウェスタンブロットアッセイ、免疫沈降検定法ならびにフローサイトメトリーアッセイである。これらの種類のアッセイには、免疫測定アッセイ又はサンドイッチ免疫検定法も含まれる。"免疫測定アッセイ"又は"サンドイッチ免疫検定法"という用語は、同時サンドイッチ、順方向サンドイッチ及び逆方向サンドイッチ免疫検定法を含めて意味する。これらの用語は、当業者によく理解されている。なお当業者は、本発明の単離かつ精製した組換えポリペプチド、TSHレセプターの部分配列及びグリコシド化されていないTSHレセプターの部分配列のエピトープが、現在公知の又は将来発開発されると思われる他の変法やアッセイの形でも有用であることも分かるであろう。これらも本発明の範囲内に含めることにする。通常、本発明のアッセイは、ELISA、LISA、RIA、ウェスタンブロット、免疫沈降又はフローサイトメトリーから選択される。有利には、ELISA、より有利には非競合ELISA、最も有利には間接的非競合ELISAが使用される。
本発明による有利な間接的アッセイの限定されない例は、例えば、例8に記載されていて、これは本発明のグリコシド化されていない単離かつ精製した組換えポリペプチドを用いて、患者及び国際基準物からのヒト血清サンプルを、ヒトTSHRに対する自己抗体にどのように間接的にアッセイするのか、次に、どのように標識抗体を検出するかが記載されている。
通常、TSHRに対する自己抗体を検出及び/又は定量化するために標識が使用される。しかし、この分野で公知の多くの様々な標識と標識法があり、これらを本発明で使用できる。標識の一般的なタイプの例には、酵素、放射性同位体、蛍光化合物、化学発光化合物及び生物発光化合物が含まれるが、これらに限定されることはない。通常の当業者は、他の適切な標識も知るようになるか、又はこれを日常的な実験の使用により把握するであろう。さらに、抗原及び抗体複合物へのこれらの標識の結合は、通常の当業者に一般に公知の通常の技法を用いて達成できる。
TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体は、TSHセプターの部分配列及び/又は単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープ及び/又はこれらの自己抗体に結合する二次抗体に結合する、本発明のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHセプターの部分配列及び/又は自己抗体のような抗体を標識することにより、本発明による方法によって検出及び/又は定量化される。
有利には、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合する二次抗体が標識される。これは、通常標識すべき化合物を酵素に結合して行われる。次に、この酵素は後でその基質に暴露される場合に、例えば、塩化物定量法、分光測定法又は蛍光法により検出できる化学部分を産生するように基質と反応する。検出可能なように標識する抗体に使用できる酵素の例には、リンゴ酸デヒドロゲナーゼ、ブドウ球菌ヌクレアーゼ、Δ−V−ステロイドイソメラーゼ、酵母アルコールデヒドロゲナーゼ、α−グリセロホスフェートデヒドロゲナーゼ、トリオースホスフェートイソメラーゼ、ビオチン−アビジンペルオキシダーゼ、西洋ワサビペルオキシダーゼ、アルカリホスファターゼ、アスパラギナーゼ、グルコースオキシダーゼ、βガラクトシダーゼ、リボヌクレアーゼ、ウレアーゼ、カタラーゼ、グルコース−VI−ホスフェートデヒドロゲナーゼ、グルコアミラーゼ及びアセチルコリンエステラーゼが含まれる。
同じく、γカウンター又はシンチレーション・カウンターを用いるような手段により決定できる放射性同位体は、標識として使用できる。特に本発明の目的に有用である同位体は、125I、3H、32P、35P、35S、14C、51Cr、36Cl、57Co、58Co、59Fe、75Seである。インビボ、インビトロ又はin situでの診断では、放射性標識のような標識を直接に使用するか、又は中間官能基を用いることにより使用してもよい。抗体に対する金属カチオンとして存在する放射性同位体を結合するために頻繁に使用される中間基は、ジエチレントリアミンペンタ酢酸(DTPA)である。このように結合される金属カチオンの一般的な例は次のものである:99mTc、123I、111IN、131I、97Ru、67Cu、67Ga及び68Ga。診断の目的で標識するために、非放射性同位体を使用できる。この様式に特に有用な元素は、157Gd、55Mn、162Dy、53Cr及び56Feである。蛍光化合物を標識として使用することもできる。従って、蛍光により標識した抗体を適切な波長の光に当てた場合に、染料の蛍光によりその存在を検出できる。中でも最も一般的に使用される蛍光標識化合物は、フルオロセイン、イソチオシアネート、ローダミン、フィコエリトリン、フィコシアニン、アロフィコシアニン、o−フタルデヒド及びフルオレスカミンである。同じく、152Euのような蛍光発光金属、又は他のランタニド系のものを標識に使用できる。これらの金属は、例えば、ジエチレントリアミンペンタ酢酸(DTPA)又はエチレンジアミン四酢酸(EDTA)のような金属キレート基を用いて抗体分子に結合できる。他の有用な標識は、化学発光化合物である。次に、化学発光−タグ抗原又は抗体の存在は、化学反応の経過の際に生じる発光の存在を検出することにより決定される。
特に有用な化学発光標識化合物の例は、ルミナール、イソルミノール、芳香族アクリジニウムエステル、イミダゾール、アクリジニウム塩、オキサレートエステル及びジオキセタンである。同様に、生物発光化合物を標識に使用してもよい。生物発光は、接触タンパク質が化学発光反応の効率を上げる生物系で見られる化学発光の1つのタイプである。生物発光抗原又は抗体の存在は、発光の存在を検出することにより決定される。標識を目的とする重要な生物発光化合物には、ルシフェラーゼとイクオリンが含まれる。
TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体は、インビボ 、in situ又はインビトロで、血清、プラズマ、リンパ、尿及び唾液のような被験者の生体液中で検出/定量化できる。血清を使用するのが有利である。有利には、これはインビトロで検出/定量化され、その際、生体液は被験者からサンプルとして得られる。被験者からのサンプルの入手に関しては、当業者に公知の通常の方法が使用できる。有利には、生体液サンプルを、固体担体上に固定した1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチドと、及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列と、及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープと接触させる。使用できる適切な固体担体と固定法は、以下に記載されている。単離かつ精製した組換えポリペプチド及び/又はTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープが固体担体上に固定された場合に、前記固体担体に結合した自己抗体が検出及び/又は定量化される。
従って、本発明の有利な方法は、被験者の生体液(その際、生体液は、前記被験者からサンプルとして得られる)中で、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を検出及び/又は定量化する方法であり、該方法は
a)前記サンプルを、固体担体上に固定した本発明の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープと接触させ、かつ
b)前記固体担体に結合させた前記自己抗体を検出及び/又は定量化する
ことから成る。
a)前記サンプルを、固体担体上に固定した本発明の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープと接触させ、かつ
b)前記固体担体に結合させた前記自己抗体を検出及び/又は定量化する
ことから成る。
本発明の自己抗体を検出及び/又は定量化する方法は、更にチログロブリン(TG)及び/又はチロペルオキシダーゼ(TPO)に対する自己抗体を検出及び/又は定量化する方法から成っていてもよい。これは、本発明のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列及び/又はエピトープと固体担体上に固定できる、市販のTG及び/又はTPOのエピトープを使用して達成できる。
本発明は有利には更に
c)検出及び/又は定量化した、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を単離する
ことから成る。アッセイで検出した自己抗体の単離法は当業者に公知であり、例えば、Warren K. G.と Catz IによりJ Neurol Sci. 1991; 103(1): 90-96に記載されている。
c)検出及び/又は定量化した、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を単離する
ことから成る。アッセイで検出した自己抗体の単離法は当業者に公知であり、例えば、Warren K. G.と Catz IによりJ Neurol Sci. 1991; 103(1): 90-96に記載されている。
本発明の方法により検出及び/又は定量化されたTSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体は、アイソタイプIgD、IgE、IgG、IgM及び/又はIgAである。有利には、これらはアイソタイプIgG、IgM及び/又はIgAである。本発明は、IgMタイプの抗−TSHR抗体の検出を初めて記載したものである。
従って、本発明のもう1つの対象は、上記の方法により入手可能な又は得られたアイソタイプIgD、IgE、IgG、IgM及び/又はIgAのTSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体である。アイソタイプIgG、IgM及び/又はIgA のTSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体が有利であり、中でもIgMが最も有利である。
本発明のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープは、キットの製造に理想的である。従って、本発明の他の対象は、場合により試薬及び/又は取扱説明書の付いた、本発明の少なくとも1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は少なくとも1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は少なくとも1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープを有する、被験者の生体液中でTSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して製造された自己抗体を検出及び/又は定量化するためのキットを提供することである。このようなキットは、本発明の方法に関して先に記載したように、更に標識及び標識した化合物を有する。その上、このようなキットは、1つ以上のコンテナー、例えばプレート、バイアル、チューブ及びそのようなものと共に、閉じたコンファインメント中に収容するために仕切られているキャリヤー手段を有していてもよい。前記コンテナーはそれぞれ、使用すべきアッセイの別々の部材から成っている。
キットは、インビボ、in situ又はインビトロで、血清、プラズマ、リンパ、尿及び唾液のような被験者の生体液に利用できる。有利には血清が使用される。有利には、これはインビトロで利用され、その際、生体液は被験者からサンプルとして得られる。
本発明の方法の実施により使用でき、かつキットの形で組み込むことができるアッセイのタイプは多い。本発明のグリコシド化されていない単離かつ精製した組換えポリペプチド及びグリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープを利用できるアッセイの一般的な例は先に記載してある。
このように、本発明のキットは有利には更に間接アッセイ又は直接アッセイのようなアッセイ、有利には間接アッセイ、ならびに競合アッセイ及び非競合アッセイ、有利には非競合アッセイを実施するための試薬を有する。アッセイは、通常はELISA、LISA、RIA、ウェスタンブロット、免疫沈降ならびにフローサイトメトリーから選択されるアッセイを実施する試薬を有する。有利には、キットは、ELISAを実施するための試薬、より有利には非競合ELISA、最も有利には間接的非競合ELISAを実施するための試薬を含む。このような試薬は、当業者に周知であり、かつ例えば、固定化緩衝液、ブロッキング緩衝液、インキュベーション緩衝液、洗浄緩衝液、基質緩衝液及び/又は二次抗体コンジュゲートを有する。
本発明の方法及びキット用の免疫吸着剤として使用できる多くの固体担体がある。利用してもよい周知の材料には、ガラス、ポリスチレン、ポリプロピレンデキストラン、ナイロン、アガロース、デキストラン、アクリルアミド、ニトロセルロース、PVDF及び他の材料が含まれ、これらは、このような材料から形成された又は該材料でコートされたチューブ、ビーズ、膜及びマイクロタイタープレートの形である。本発明の単離かつ精製した組換えポリペプチド及び/又はTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープは、アミド、エステル又はジスルフィド結合による共有結合のような技法により、又は吸着により、電子対を共有して又は物理的に固体担体に結合できる。当業者は、その他の多くの適切な固体担体免疫吸着剤及び前記担体上に抗体を吸着する方法を知るであろう。この結合は、固体担体と本発明の単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープとの間で、例えば、アミド、エステル又はジスルフィド結合による共有結合を使用することにより達成できる。融合させるべきポリペプチドがGSTである場合には、単離かつ精製した組換えポリペプチドは、その表面上にグルタチオンを提供する固体担体とポリペプチドのGST部分の間で、ジスルフィド結合により固体担体上に並ぶように有利に固定される。
現在のところ固体担体として使用するのが有利なものは、ポリスチレン製のマイクロタイタープレートであり、これはNUNC、Costar、Greiner、Falcon又はCoring Incのような市場の様々な供給業者から入手できる。
TSHRに対する自己抗体を検出及び/又は定量化する方法を、固体担体上で行う場合には、通常固体担体はPBS緩衝液又はカーボネート緩衝液のような当業者に公知のコーティング緩衝液を用いることにより、本発明のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープで、及び/又はグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープに結合する自己抗体のような抗体でコートされる。このようなコーティング緩衝液ならびに既にコートされた固体担体も、本発明のキット用の試薬として含まれる。
本発明の上記の方法を実施する有利な様式では、同様に本発明のキット中の試薬として含まれる一定の"ブロッカー"を使用することが重要である。"ブロッカー"は、非特異的タンパク質、プロテアーゼ、又は実験サンプル中に存在するTSHレセプターに応答して産生される自己抗体以外のヒト抗体が、固体担体上の抗原又は抗体を架橋または破壊しないようにするために、又は放射線標識したインディケーターである抗原又は抗体が偽陽性又は偽陰性という結果を生じないようにするために添加される。使用できる通常のブロッカーは、ウシ血清アルブミン(BSA)であり、これが好ましい。ブロッカーはPBS緩衝液のような緩衝溶液に添加できる。固体担体が使用される場合には、ブロッカーは通常固体担体をコートした後に添加される。
生体液を、グリコシド化されていない単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープと接触させる前に、生体液及び/又はグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープを、TSHレセプターの部分配列に融合したポリペプチドで前処理して偽陽性又は偽陰性という結果を回避できる。
本発明のキットは、更にポイント・オブ・ケアテスト(point of care test)を実施するための試薬を有してもよい。含まれるポイント・オブ・ケアテストは、当業者に公知であり、かつ例えばテストストライプ、テストスティック又はbio-CDsである。
本発明のキットは、更にTG及びTPOを検出及び/又は定量化するための試薬を有してもよい。TG及びTPOを検出及び/又は定量化するための通常の試薬は、TG及び/又はTPOの市販のエピトープであり、これを例えば本発明の単離かつ精製した組換えポリペプチド及び/又はTSHレセプターの部分配列及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープと、固体担体上で固定することができる。
固−液相アッセイ形式の他に、同様に液−液相アッセイ形式を本発明の方法とキットに用いてもよい。液−液相アッセイ形式は、固−液相アッセイ形式と比べて反応速度を改善した。特殊な実施態様では、サンプルを操作するのに適切なマイクロシステムプラットフォームのような自動診断システムを用いて、本発明のTSHレセプターの部分配列及び/又は単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列のエピトープを使用して、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を検出してもよい。
本発明のキットは、有利にはTSHレセプターに対する免疫反応と関連する自己免疫疾患の診断に使用される。TSHレセプターに対する免疫反応と関連する自己免疫疾患とは、各々の被験者がTSHレセプターに対する抗体を増す疾患を意味する。一般的に、TSHレセプターに対する免疫反応と関連する自己免疫疾患は、グレーヴス病である。
また本発明は、活性物質として、1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープの製剤学的有効量を、場合により製剤学的に認容性のキャリヤー、希釈剤又は補助剤と組合わせて有する医薬組成物にも関する。
"製剤学的有効量"とは、ヒト又は動物の生体に投与した際に、検出可能な薬理学的及び/又は生理学的作用を誘発する化学材料又は化合物を意味する。各々の製剤学的有効量は、治療すべき特定の患者、治療すべき疾患及び投与方法による。更に、製剤学的有効量は使用される特定の化合物にもよる。
本明細書で記載したような1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープの他に、医薬組成物は1つ以上の製剤学的に認容性のキャリヤー、希釈剤又は補助剤を含有していてもよい。
活性化合物を製剤学的に使用できる調製物にする加工を容易にする認容性のキャリヤー、希釈剤又は補助剤は、使用される用量と濃度では宿主に対して非毒性であり、かつリン酸塩、クエン酸塩及び他の有機酸のような緩衝液が含まれる:アスコルビン酸及びメチオニンを含む抗酸化剤;保存剤(例えば、オクタデシルジメチルベンジル塩化アンモニウム;塩化ヘキサメトニウム;塩化ベンザルコニウム;塩化ベンゼトニウム;フェノール;ブチルアルコール又はベンジルアルコール;メチルパラベン又はプロピルパラベンのようなアルキルパラベン;カテコール;レソルシノール;シクロヘキサノール;3−ペンタノール;及びm−クレゾール);低分子量(約10残基未満)ポリペプチド;血清アルブミンのようなタンパク質;ゼラチン、又は免疫グロブリン;ポリビニルピロリドンのような親水性ポリマー;グリシン、グルタミン、アスパラギン酸、ヒスチジン、アルギニン又はリジンのようなアミノ酸;単糖類、二糖類、及びグルコー、マンノース又はデキストリンを含む他の炭水化物;EDTAのようなキレート剤;スクロース、マンニトール、トレハロース又はソルビトールのような糖;ナトリウムのような塩形成対イオン;金属錯体(例えば、Zn−タンパク質錯体);及び/又はTWEEN(R)、PLURONICS(R)又はポリエチレングリコール(PEG)のような非イオン性界面活性剤。
医薬組成物の投与形は、全身又は局所的であってよい。例えば、このような組成物の投与は、様々な非経口的経路、例えば、皮下、静脈内、皮内、筋肉内、腹腔内、鼻腔内、経皮、頬側経路又は、移植装置を介して、かつ蠕動運動の手段により輸送してもよい。医薬組成物は、適切などの形であってもよい。例えば、溶液、懸濁液、粉末、凍結乾燥物、軟膏又はチンキ剤であってよい。必要であれば、保存薬、安定剤、緩衝液、抗酸化剤及び/又は他の添加剤を含有していてもよい。
同様に、本発明に含まれるものは、TSHレセプターに対する免疫反応と関連する自己免疫疾患の治療又は予防で使用するための、及び/又は診断で使用するための、本発明の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープ及び/又は本発明の医薬組成物である。
更に、TSHレセプターに対する免疫反応と関連する自己免疫疾患を治療又は予防するための医薬品を製造するための、本発明の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープ及び/又は本発明の医薬組成物の使用も本発明に包含される。
TSHレセプターに対する免疫反応と関連する自己免疫疾患の治療は、通常は被験者に治療有効量の本発明の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は本発明の医薬組成物を投与することにより行われる。
本発明の更なる対象は、被験者においてTSHレセプターに対する免疫反応と関連する自己免疫疾患を治療する方法であり、該方法は、本発明の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープ及び/又は医薬組成物と結合する事により、治療有効性が提供することが証明される治療有効量の治療剤を被験者に投与することから成る。
"治療有効量"とは、症状を改善又は予防する、又は治療されている被験者の生存を伸ばすのに有効な量である。治療有効量の決定は、当業者の技量の範囲内である。全身治療に関しては、治療有効量又は用量をインビトロアッセイから初めに推定できる。例えば、用量は細胞培養で決定されるようなIC50を含む循環血漿濃度範囲が達成されるように、動物モデルで調製できる。このような情報を使用して、ヒトでの有用な用量をより正確に得ることができる。初期用量は、当業者に周知の技法を使用して、インビボのデータから、例えば、動物モデルで達成できる。通常の当業者は、動物のデータに基づいてヒトへの投与を容易に最適化でき、かつ当然ながら治療すべき被験者、被験者の重さ、疾患の重度、投与方法及び処方する医師の判断による。
本発明の他の対象は、TSHレセプターの結合相手を同定する方法であり、前記方法は、次の
a)前記結合相手を、1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープと接触させ、かつ
b)前記グリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は前記グリコシド化されていないTSHレセプターの部分配列及び/又は前記グリコシド化されていないTSHレセプターの部分配列のエピトープに結合した結合相手を検出及び/又は定量化し、
c)場合により検出及び/又は定量化した、前記グリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は前記グリコシド化されていないTSHレセプターの部分配列及び/又は前記グリコシド化されていないTSHレセプターの部分配列のエピトープに結合した結合相手を単離する
工程から成る。
a)前記結合相手を、1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は1つ以上のグリコシド化されていないTSHレセプターの部分配列のエピトープと接触させ、かつ
b)前記グリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は前記グリコシド化されていないTSHレセプターの部分配列及び/又は前記グリコシド化されていないTSHレセプターの部分配列のエピトープに結合した結合相手を検出及び/又は定量化し、
c)場合により検出及び/又は定量化した、前記グリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は前記グリコシド化されていないTSHレセプターの部分配列及び/又は前記グリコシド化されていないTSHレセプターの部分配列のエピトープに結合した結合相手を単離する
工程から成る。
この方法の手法と試薬は通常のものであってよく、かつ本発明の開示を理解する当業者により、よく容認されている分析上かつ免疫診断的方法論の原則に留意しながら設計かつ選択されるであろう。このような原則は、例えば、Harlow, E., and Lane, D. "Antibodies: A Laboratory Manual" Cold Spring Harbor Laboratory, Cold Spring Harbor, NY, 349(1988)に記載されている。同定すべき結合相手は、TSHレセプターに対する抗体のような抗体、抗体(Fab)、F(ab)2の抗原結合ドメイン、一本鎖抗体ならびに組換え抗体であってよい。通常、これはTSHレセプターに対する抗体である。単離した抗体は、ELISA、ウェスタンブロット、フローサイトメトリーによるその抗原TSHRへの結合のような通常の方法により、又はそのCDR領域のシーケンシングにより特徴付けることができる。
従って本発明のもう1つの対象は、この方法により得られるTSHレセプターの結合相手であり、該結合相手はTSHを有さない。有利には、結合相手はTSHレセプターとモノクロナール抗−TSHR抗体2C11との結合定数(Kd)よりも高い結合定数を有するTSHレセプターに、及び/又はモノクロナール抗−TSHR抗体4C1に結合する。結合定数(Kd)は、例えば、非線形回帰及びバイアコア(Biacore)分析によって、遊離リガンド濃度により特異的結合を調節することにより決定できる。分析は、市販のデータソフトウェアにより行うことができる。有利には、この方法により得られる結合相手は、IgD、IgE、IgG、IgM又はIgAアイソタイプの抗体であり、より有利にはIgG、IgM又はIgAアイソタイプの抗体である。
実施例
例1 TSHR−ED、TSHR−210、TSHR−310を産生するために使用したヒトTSHレセプターのDNAとペプチド配列
配列TSHR−ED、TSHR−210、TSHR−310は、遺伝子バンク寄託番号M73747(Gl:903759)で入手可能であるようなヒトTSH−レセプターを意味する。ヒトチロトロピンレセプターのアミノ酸配列は、以下の通りである:
例1 TSHR−ED、TSHR−210、TSHR−310を産生するために使用したヒトTSHレセプターのDNAとペプチド配列
配列TSHR−ED、TSHR−210、TSHR−310は、遺伝子バンク寄託番号M73747(Gl:903759)で入手可能であるようなヒトTSH−レセプターを意味する。ヒトチロトロピンレセプターのアミノ酸配列は、以下の通りである:
ヒトTSHレセプターの有利な細胞外部分は、Ntd.134-1315; Aa 22-415からの領域を有する。シグナルペプチドの配列は含まれていない。ここで示す実験に使用されたTSHR配列は、寄託番号M73747(Gl:903759)と称する。
例2 構築物及びクローニング法
提供されたTSHR−変異体(TSHR−ED、TSHR−210、TSHR−310)の配列を、Amersham Biosciences社から市販されているベクターpGEX-2Tを用いて、Schistosoma Japonicum社製のグルタチオンS−トランスフェラーゼ(GST)のC−末端に直接に融合させた。GST配列は、遺伝子バンク寄託番号U13850を意味する。クローニング法では、PCRプライマーにおける制限部位に従って、TSHR変異体をそれらの5’部位と一緒に、pGEX-2Tマルチクローニング部位のBamHI部位に、かつそれらの3’部位と一緒に、このベクターのEcoRI部位にクローニングした。このクローニング法によって、6個の付加的なアミノ酸(グルタミン酸(E)及びフェニルアラニン(F)、イソロイシン(I)、バリン(V)、トレオニン(T)及びアスパラギン酸(D)太字、緑)を、TSHRタンパク質の細胞外部分のC末端リシン(K)に融合させた。この付加的なアミノ酸の直後に、ベクターによってコードされたtga ストップコドンにより読取り枠を中断した。
提供されたTSHR−変異体(TSHR−ED、TSHR−210、TSHR−310)の配列を、Amersham Biosciences社から市販されているベクターpGEX-2Tを用いて、Schistosoma Japonicum社製のグルタチオンS−トランスフェラーゼ(GST)のC−末端に直接に融合させた。GST配列は、遺伝子バンク寄託番号U13850を意味する。クローニング法では、PCRプライマーにおける制限部位に従って、TSHR変異体をそれらの5’部位と一緒に、pGEX-2Tマルチクローニング部位のBamHI部位に、かつそれらの3’部位と一緒に、このベクターのEcoRI部位にクローニングした。このクローニング法によって、6個の付加的なアミノ酸(グルタミン酸(E)及びフェニルアラニン(F)、イソロイシン(I)、バリン(V)、トレオニン(T)及びアスパラギン酸(D)太字、緑)を、TSHRタンパク質の細胞外部分のC末端リシン(K)に融合させた。この付加的なアミノ酸の直後に、ベクターによってコードされたtga ストップコドンにより読取り枠を中断した。
TSHR融合タンパク質1:GST−TSHR−ED(ベクター:pGEX2T-TSHR-ED)
ヒト甲状腺cDNAプール(Invitrogen社)からのプライマーMM38(5’BamHI:TCTCGGATCCATGGGGTGTTCGTCTCCA)と、MM39(3’-EcoRI:ATATGAATTCCTTGTAGCCCATTATGTCTTCAG)を用いて、ヒトTSHレセプターの細胞外ドメインを増幅させ、かつBamHI/EcoRI制限にて、同じ酵素で制限し、制限したベクターpGEX-2T(GE Healthcare, Amersham Biosciences社)の枠内でクローン化した。その結果、配列番号4(Aa)と配列番号7(Ntd.)に相応するGST−TSHR−ED融合構造物(GST=グルタチオン−S−トランスフェラーゼ)が得られた。クローンしたTSHR配列は、Ntd.134-1315(配列番号1に相応するAa 22-415)の領域をつなげた。
ヒト甲状腺cDNAプール(Invitrogen社)からのプライマーMM38(5’BamHI:TCTCGGATCCATGGGGTGTTCGTCTCCA)と、MM39(3’-EcoRI:ATATGAATTCCTTGTAGCCCATTATGTCTTCAG)を用いて、ヒトTSHレセプターの細胞外ドメインを増幅させ、かつBamHI/EcoRI制限にて、同じ酵素で制限し、制限したベクターpGEX-2T(GE Healthcare, Amersham Biosciences社)の枠内でクローン化した。その結果、配列番号4(Aa)と配列番号7(Ntd.)に相応するGST−TSHR−ED融合構造物(GST=グルタチオン−S−トランスフェラーゼ)が得られた。クローンしたTSHR配列は、Ntd.134-1315(配列番号1に相応するAa 22-415)の領域をつなげた。
TSHR−融合タンパク質2:GST-TSHR-210(ベクター:pGEX2T-TSHR-210)
テンプレートとしてpGEX-2T -TSHR-EDを使用し、ヒトTSHレセプターの変異体をプライマーMM126(5’BamHI:CGCGGATCCAATAAATACCTGACAGTTATTGCAAAA)と、MM39(3’-EcoRI:ATATGAATTCCTTGTAGCCCATTATGTCTTCAG)を用いて増幅させた。増幅生成物は、BamHI/EcoRI制限にて、同じ酵素を用いて制限したベクターpGEX-2T(GE Healthcare, Amersham Biosciences社)の枠内でクローン化した。その結果、配列番号5(Aa)と配列番号8(Ntd.)に相応するGST−TSHR−ED融合構造物(GST=グルタチオン−S−トランスフェラーゼ)が得られた。クローンしたTSHR配列は、Ntd.698-1315(配列番号2に相応するAa 210-415)の領域をつなげた。
テンプレートとしてpGEX-2T -TSHR-EDを使用し、ヒトTSHレセプターの変異体をプライマーMM126(5’BamHI:CGCGGATCCAATAAATACCTGACAGTTATTGCAAAA)と、MM39(3’-EcoRI:ATATGAATTCCTTGTAGCCCATTATGTCTTCAG)を用いて増幅させた。増幅生成物は、BamHI/EcoRI制限にて、同じ酵素を用いて制限したベクターpGEX-2T(GE Healthcare, Amersham Biosciences社)の枠内でクローン化した。その結果、配列番号5(Aa)と配列番号8(Ntd.)に相応するGST−TSHR−ED融合構造物(GST=グルタチオン−S−トランスフェラーゼ)が得られた。クローンしたTSHR配列は、Ntd.698-1315(配列番号2に相応するAa 210-415)の領域をつなげた。
TSHR−融合タンパク質3:GST-TSHR-310(ベクター:pGEX2T-TSHR-310)
ヒトTSHレセプターの変異体をプライマーMM127(5’BamHI:CGCGGATCCCGCCAGAGAAAATCTGTAA)と、MM39(3’-EcoRI)を用いて増幅させ、かつBamHI/EcoRI制限にて、同じ酵素を用いて制限したベクターpGEX-2T(GE Healthcare, Amersham Biosciences社)の枠内でクローン化した。その結果、配列番号6(Aa)と配列番号9(Ntd.)に相応するGST−TSHR−ED融合構造物(GST=グルタチオン−S−トランスフェラーゼ)が得られた。クローンしたTSHR配列は、Ntd.998-1315(配列番号3に相応するAa 210-415)の領域をつなげた。
ヒトTSHレセプターの変異体をプライマーMM127(5’BamHI:CGCGGATCCCGCCAGAGAAAATCTGTAA)と、MM39(3’-EcoRI)を用いて増幅させ、かつBamHI/EcoRI制限にて、同じ酵素を用いて制限したベクターpGEX-2T(GE Healthcare, Amersham Biosciences社)の枠内でクローン化した。その結果、配列番号6(Aa)と配列番号9(Ntd.)に相応するGST−TSHR−ED融合構造物(GST=グルタチオン−S−トランスフェラーゼ)が得られた。クローンしたTSHR配列は、Ntd.998-1315(配列番号3に相応するAa 210-415)の領域をつなげた。
例3 組換えGST−TSHR−融合タンパク質の精製
様々なTSHR−変異体の発現と精製は、以下の実験方法に従って行った。
a.細菌株BL21(一般に10ngプラスミドDNA/200μlコンピテント細菌)中でのpGEX2T−TSHRベクター(ED, 210, 310)を新たに形質転換させる
b.選択圧の下で、o/n培養する(アンピシリン100μg/ml最終濃度)
c.o/n培養を希釈(1/20)かつ、対数成長するまで培養株を培養する
d.IPTG(最終濃度:1mM)の添加によりターゲット遺伝子を誘発する
e.更に4時間誘発する
f.遠心分離により細菌を単離する
g.細菌をトリス緩衝生理食塩水(TBS:50mM Tris pH 8.0, 150 mM NaCl)中で再懸濁させ、かつ洗浄する
h.溶菌/可溶化緩衝液(TBS, 1% Triton×100, 1mM DTT, 1mM EDTA)中で細菌を再懸濁させる
i.超音波処理により細菌を崩壊させる(溶解産物調製物)
j.細菌の溶解産物のインキュベーション/撹拌により融合タンパク質を可溶化する(30分/4℃)
k.高速遠心分離により、細菌の溶解産物の不溶性成分を分離する
l.グルタチオン−セファロース(GE Healthcare, 以前のAmersham Pharmacia Biotech社)をアフィニティーマトリックスとして用いて、アフィニティー・クロマトグラフィーにより、GST-TSHR融合タンパク質を細菌の溶解産物(工程kからの上澄液)から精製する
m.TBS中の20mM還元グルタチオンを用いてGST-TSHR融合タンパク質を溶出する
n.溶出液を透析する(TBSに対して)
o.SDS−PAGE/クーマシー菌株により、精製した融合タンパク質の大きさと純度を測定する
p.ポリクロナール抗−GST抗血清とモノクロナール抗−TSHR抗体2C11又は4C1(Serotec社)を用いてウェスタンブロット分析により品質コントロールする
q.タンパク質濃度を光度測定する(OD 280)。
様々なTSHR−変異体の発現と精製は、以下の実験方法に従って行った。
a.細菌株BL21(一般に10ngプラスミドDNA/200μlコンピテント細菌)中でのpGEX2T−TSHRベクター(ED, 210, 310)を新たに形質転換させる
b.選択圧の下で、o/n培養する(アンピシリン100μg/ml最終濃度)
c.o/n培養を希釈(1/20)かつ、対数成長するまで培養株を培養する
d.IPTG(最終濃度:1mM)の添加によりターゲット遺伝子を誘発する
e.更に4時間誘発する
f.遠心分離により細菌を単離する
g.細菌をトリス緩衝生理食塩水(TBS:50mM Tris pH 8.0, 150 mM NaCl)中で再懸濁させ、かつ洗浄する
h.溶菌/可溶化緩衝液(TBS, 1% Triton×100, 1mM DTT, 1mM EDTA)中で細菌を再懸濁させる
i.超音波処理により細菌を崩壊させる(溶解産物調製物)
j.細菌の溶解産物のインキュベーション/撹拌により融合タンパク質を可溶化する(30分/4℃)
k.高速遠心分離により、細菌の溶解産物の不溶性成分を分離する
l.グルタチオン−セファロース(GE Healthcare, 以前のAmersham Pharmacia Biotech社)をアフィニティーマトリックスとして用いて、アフィニティー・クロマトグラフィーにより、GST-TSHR融合タンパク質を細菌の溶解産物(工程kからの上澄液)から精製する
m.TBS中の20mM還元グルタチオンを用いてGST-TSHR融合タンパク質を溶出する
n.溶出液を透析する(TBSに対して)
o.SDS−PAGE/クーマシー菌株により、精製した融合タンパク質の大きさと純度を測定する
p.ポリクロナール抗−GST抗血清とモノクロナール抗−TSHR抗体2C11又は4C1(Serotec社)を用いてウェスタンブロット分析により品質コントロールする
q.タンパク質濃度を光度測定する(OD 280)。
TBS中の単離かつ精製TSHR−変異体は、更なる実験法用の(適切な希釈をして)"すぐに使用できるサンプル"である。
SDS−PAGEとクーマシー菌株によるGST−TSHR−変異体の分析
クロマトグラフィーによる精製と透析の際に、タンパク質をタンパク質サンプル緩衝液中で沸騰/還元させ、かつ引き続きSDS−PAGE(10%SDS−PAG)に課した。図1に示されているような標準的なプロトコールに従って、クーマシー・ブリリアントブルーを用いて染色した。左から右に向かって:TSHR−ED、TSHR−210、TSHR−310、空、タンパク質標準物。
クロマトグラフィーによる精製と透析の際に、タンパク質をタンパク質サンプル緩衝液中で沸騰/還元させ、かつ引き続きSDS−PAGE(10%SDS−PAG)に課した。図1に示されているような標準的なプロトコールに従って、クーマシー・ブリリアントブルーを用いて染色した。左から右に向かって:TSHR−ED、TSHR−210、TSHR−310、空、タンパク質標準物。
ウェスタンブロッティングによるGST−TSHR−変異体の分析
SDS−PAGEの後、タンパク質をゲルからニトロセルロース膜へ移した。図2に示されているように、特異的タンパク質をTSHRに特異的なモノクロナール抗体2C11と適切な二次抗体/基質系(ウサギ抗マウス−HRP、DINOVA及びMetal enhanced DAB, PIERCE)を用いて検出した(左から右に向かって:TSHR−ED、TSHR−210、TSHR−310)。
SDS−PAGEの後、タンパク質をゲルからニトロセルロース膜へ移した。図2に示されているように、特異的タンパク質をTSHRに特異的なモノクロナール抗体2C11と適切な二次抗体/基質系(ウサギ抗マウス−HRP、DINOVA及びMetal enhanced DAB, PIERCE)を用いて検出した(左から右に向かって:TSHR−ED、TSHR−210、TSHR−310)。
例4 マイクロウェルプレート上でのTSHレセプター変異体のコーティング
アフィニティー精製したTSHレセプターの変異体を、適切な濃度のPBS緩衝液で希釈した。次に、PBSコーティング緩衝液中の希釈TSHレセプター120μlを、マイクロタイタープレートのプラスチックウェルに加え、かつ室温で少なくとも6時間又は一晩インキュベートした。コーティング緩衝液から出した後に、ブロッキング緩衝液150μg(PBS緩衝液中1% BSA)を各マイクロウェルに加え、室温で更に30分インキュベートし、非特異的な結合反応を克服した。次に、ブロッキング緩衝液を取り出し、かつELISAにすぐに使用する場合にはマイクロタイタープレートを37℃で2時間乾燥させ、4℃で貯蔵する場合には、ドライパッドを用いてアルミホイルバッグ中に密封した。
アフィニティー精製したTSHレセプターの変異体を、適切な濃度のPBS緩衝液で希釈した。次に、PBSコーティング緩衝液中の希釈TSHレセプター120μlを、マイクロタイタープレートのプラスチックウェルに加え、かつ室温で少なくとも6時間又は一晩インキュベートした。コーティング緩衝液から出した後に、ブロッキング緩衝液150μg(PBS緩衝液中1% BSA)を各マイクロウェルに加え、室温で更に30分インキュベートし、非特異的な結合反応を克服した。次に、ブロッキング緩衝液を取り出し、かつELISAにすぐに使用する場合にはマイクロタイタープレートを37℃で2時間乾燥させ、4℃で貯蔵する場合には、ドライパッドを用いてアルミホイルバッグ中に密封した。
例5 大腸菌発現TSHレセプターの変異体の分析と活性
a. TSHに対する結合活性
精製したGST−TSHRタンパク質の生理学的活性を測定するために、これらが生理学的リガンドであるTSHに結合できるかどうかを調べた。ウシ甲状腺(Sigma, St. Louis)からのTSHをELISAプレート(NUNC, Wiesbaden)上に固定した。空いている結合部位を、ウシ血清アルブミンの3%溶液とのインキュベーションによりブロックした。引き続き、示されたGST−TSHR−変異体と適切なコントロール(GSTタンパク質だけ)をプレート上でインキュベートし、かつウサギ抗−GST(Sigma, St. Louis)をペルオキシダーゼ基質としてのヤギ抗−ウサギ−ペルオキシダーゼ(DIANOVA)及びTMBと組み合わせて用いて、結合を視覚化した。結果は図4に示されている。
b. TSHレセプター抗体産生マウスに対する結合活性
製造指示に従い、細胞外ドメインに結合させることにより、ヒト甲状腺刺激ホルモン(TST)レセプターを認識するTSHレセプター抗体4C1産生マウスを使用した。マイクロタイタープレート(例4から)のプラスチックウェル中に固定させたTSHR−変異体(例3から)の親和性を使用して、マウス抗−TSHR抗体に対する結合活性を試験した。
a. TSHに対する結合活性
精製したGST−TSHRタンパク質の生理学的活性を測定するために、これらが生理学的リガンドであるTSHに結合できるかどうかを調べた。ウシ甲状腺(Sigma, St. Louis)からのTSHをELISAプレート(NUNC, Wiesbaden)上に固定した。空いている結合部位を、ウシ血清アルブミンの3%溶液とのインキュベーションによりブロックした。引き続き、示されたGST−TSHR−変異体と適切なコントロール(GSTタンパク質だけ)をプレート上でインキュベートし、かつウサギ抗−GST(Sigma, St. Louis)をペルオキシダーゼ基質としてのヤギ抗−ウサギ−ペルオキシダーゼ(DIANOVA)及びTMBと組み合わせて用いて、結合を視覚化した。結果は図4に示されている。
b. TSHレセプター抗体産生マウスに対する結合活性
製造指示に従い、細胞外ドメインに結合させることにより、ヒト甲状腺刺激ホルモン(TST)レセプターを認識するTSHレセプター抗体4C1産生マウスを使用した。マイクロタイタープレート(例4から)のプラスチックウェル中に固定させたTSHR−変異体(例3から)の親和性を使用して、マウス抗−TSHR抗体に対する結合活性を試験した。
製造指示に従って、PBS緩衝液中でマウス抗−TSHR抗体を適切な濃度に希釈した。抗体混合物100μlをプラスチックウェル中に加え、かつ室温で30分間インキュベートした。抗体混合物を廃棄した後に、ウェルを適量のPBS緩衝液で3回洗浄した。マウス抗−TSHR抗体に対するアフィニティー精製したTSHR融合タンパク質の結合活性は、西洋ワサビペルオキシダーゼ結合ウサギ抗−マウスIgGにより検出した(図5)。偽陽性を回避するために、TSHR変異体と同じ濃度のGSTをプラスチックウェルに固定し、負のコントロールとして使用した。
例6 陽性TSHR血清中のTRAbs(TSHレセプター自己抗体)の検出
市販のTSHR陽性血清L1とL2(Invent Diagnostic GmbH社)をPBS緩衝液中で希釈した。L1とL2は、種々の患者からプールされ、かつ製造業者によって高活性と低活性を有する陽性抗−TSHR血清である。TSHR変異体、TSHR-ED、TSHR-210及びTSHR-310を例4に倣ってマイクロタイタープレートのプラスチックウェル中に固定した。サンプルをGSTで、又はアフィニティー精製したTSHR融合タンパク質で30分間前処理し、次に、室温で30分間インキュベーションするために、希釈サンプル100μlをウェルに添加した。TSHR変異体に結合した自己抗体のアフィニティーは、基準としての620nmに対して450nmで測定した、基質(TBM,テトラメチルメンジジン)を酸化する西洋ワサビペルオキシダーゼに結合したウサギ抗ヒト免疫グロブリンからのシグナルを計測することにより二次的に検出した(図6)。この結合活性の特異性は、シグナルの損失を引き起こすTSHR変異体でヒト血清を前処理することにより証明できる。
市販のTSHR陽性血清L1とL2(Invent Diagnostic GmbH社)をPBS緩衝液中で希釈した。L1とL2は、種々の患者からプールされ、かつ製造業者によって高活性と低活性を有する陽性抗−TSHR血清である。TSHR変異体、TSHR-ED、TSHR-210及びTSHR-310を例4に倣ってマイクロタイタープレートのプラスチックウェル中に固定した。サンプルをGSTで、又はアフィニティー精製したTSHR融合タンパク質で30分間前処理し、次に、室温で30分間インキュベーションするために、希釈サンプル100μlをウェルに添加した。TSHR変異体に結合した自己抗体のアフィニティーは、基準としての620nmに対して450nmで測定した、基質(TBM,テトラメチルメンジジン)を酸化する西洋ワサビペルオキシダーゼに結合したウサギ抗ヒト免疫グロブリンからのシグナルを計測することにより二次的に検出した(図6)。この結合活性の特異性は、シグナルの損失を引き起こすTSHR変異体でヒト血清を前処理することにより証明できる。
例7 TSHR変異体を固定したマイクロタイタープレートの使用によるヒト血清中でのTRAbs(TSHレセプター自己抗体)の検出
患者血清からのTRAbs及びプールした市販の血清(L2, Invent Diagnostic GmbH社)を、適切なコーティング濃度のマイクロタイタープレート上に固定したTSHR変異体(例4)を用いて検出した。患者血清ならびに市販の血清L2をPBS緩衝液とサンプル100μlで希釈し、次にマイクロタイタープレート上に固定したTSHR変異体とインキュベートした。患者血清中での抗−TSHR自己抗体の検出は、例6で処理したような特異的シグナル応答により実証した。結果は図7に示されている。白棒は精製GSTタンパク質で処理した血清を示し、かつ黒棒は、精製TSHR変異体で処理した血清を示す。
患者血清からのTRAbs及びプールした市販の血清(L2, Invent Diagnostic GmbH社)を、適切なコーティング濃度のマイクロタイタープレート上に固定したTSHR変異体(例4)を用いて検出した。患者血清ならびに市販の血清L2をPBS緩衝液とサンプル100μlで希釈し、次にマイクロタイタープレート上に固定したTSHR変異体とインキュベートした。患者血清中での抗−TSHR自己抗体の検出は、例6で処理したような特異的シグナル応答により実証した。結果は図7に示されている。白棒は精製GSTタンパク質で処理した血清を示し、かつ黒棒は、精製TSHR変異体で処理した血清を示す。
例8 国際基準物90/672のシグナルと比較したヒト血清中のTRAbsの検出
90/672は、アンプル1本当たりのTSH刺激抗体の100ミリ国際単位として定義されている国際基準である。標準物ならびに市販の血清L1及びH07(患者血清)を例6のように処理したが、前処理はせずに、図8に示されているようにそれらのシグナル応答を比較した。GSTとTSHR−EDをコートしたマイクロタイターウェルは、これらの3つの全ての血清のうちで最小のシグナルを示したが、しかしTSHR−310をコートしたマイクロタイターウェルでは強いシグナルが得られた。
90/672は、アンプル1本当たりのTSH刺激抗体の100ミリ国際単位として定義されている国際基準である。標準物ならびに市販の血清L1及びH07(患者血清)を例6のように処理したが、前処理はせずに、図8に示されているようにそれらのシグナル応答を比較した。GSTとTSHR−EDをコートしたマイクロタイターウェルは、これらの3つの全ての血清のうちで最小のシグナルを示したが、しかしTSHR−310をコートしたマイクロタイターウェルでは強いシグナルが得られた。
例9 ヒト血清中での種々のアイソフォームTRAbsの検出
ヒト血清中でのTRAbsのアイソフォームは、例7に記載したような方法で検出した。IgG、IgM及びIgAの特異的応答は、西洋ワサビペルオキシダーゼと結合したIgG、IgM又はIgAに対する免疫グロブリンの特異的ウサギ抗ヒトアイソフォームを用いて定義付けた(図9)。
ヒト血清中でのTRAbsのアイソフォームは、例7に記載したような方法で検出した。IgG、IgM及びIgAの特異的応答は、西洋ワサビペルオキシダーゼと結合したIgG、IgM又はIgAに対する免疫グロブリンの特異的ウサギ抗ヒトアイソフォームを用いて定義付けた(図9)。
例10 抗−TSHR自己抗体に対するTSHR−変異体の用量依存性反応
市販の血清(L2、Invent Diagnostic GmbH社)を希釈し、かつTSHR−EDとTSHR−310の混合物(約50:50)をコートしたマイクロタイタープレートに対するシグナル応答を例6に記載されているようにELISAにより測定した。種々の希釈の結果は図10に示されている。
市販の血清(L2、Invent Diagnostic GmbH社)を希釈し、かつTSHR−EDとTSHR−310の混合物(約50:50)をコートしたマイクロタイタープレートに対するシグナル応答を例6に記載されているようにELISAにより測定した。種々の希釈の結果は図10に示されている。
例11 トロンビンによるGST−TSHR−融合タンパク質TSHR−EDの切断
精製したGST−TSHR−EDを種々の量のトロンビンとインキュベートした(1時間、37℃)。引き続き、SDS−サンプル緩衝液中で沸騰させ、かつSDS−PAGE/ウェスタンブロッティングを行った。TSHR−EDとその断片を抗−TSHRmAb 2C11と適切な二次的試薬を用いて視覚化した。
精製したGST−TSHR−EDを種々の量のトロンビンとインキュベートした(1時間、37℃)。引き続き、SDS−サンプル緩衝液中で沸騰させ、かつSDS−PAGE/ウェスタンブロッティングを行った。TSHR−EDとその断片を抗−TSHRmAb 2C11と適切な二次的試薬を用いて視覚化した。
レーン:
1. 予備染色したマーカー:200,119,66,43,20,14.3 kD
2. GST−TSHR−ED、トロンビン無し
3. GST−TSHR−ED、0.1Uトロンビン
4. GST−TSHR−ED、0.5Uトロンビン
5. GST−TSHR−ED、1Uトロンビン
6. GST−TSHR−ED、2Uトロンビン
例12 グルタチオン固定マイクロウェルによるGST−タグTSHR組換えタンパク質のコーティング
アフィニティー精製したGST−TSHR−EDタンパク質をPBS緩衝液で希釈して適切な濃度にし、かつ先に記載したようにマイクロタイタープレート(Corning社)上に直接コーティングするか、又は製造指示に従ってグルタチオン固定マイクロタイタープレート(NUNC社)上にコートした。抗−TSHR自己抗体IgG又はIgMの、GST−TSHR−EDに対する結合は、例6に記載されているように検出した。図12に示されているように、IgGとIgMの両方に対するGST−TSHR−EDの結合活性は、GST−TSHR−EDを直接にコートしたプレートよりも、グルタチオン固定プレートを介してコートしたGST−TSHR−EDでは高かった。この実験は、同じコーティング濃度では、試験した4つの患者血清(L2、L1、M4及びM21)中、自己抗体IgG(A)とIgM(B)に対するGST−TSHR−EDタンパク質の結合活性はGST−TSHR−EDを直接にコートしたプレートよりも、グルタチオン固定マイクロタイタープレートを介してコートしたGST−TSHR−EDにおいて著しく高いことを示している。
1. 予備染色したマーカー:200,119,66,43,20,14.3 kD
2. GST−TSHR−ED、トロンビン無し
3. GST−TSHR−ED、0.1Uトロンビン
4. GST−TSHR−ED、0.5Uトロンビン
5. GST−TSHR−ED、1Uトロンビン
6. GST−TSHR−ED、2Uトロンビン
例12 グルタチオン固定マイクロウェルによるGST−タグTSHR組換えタンパク質のコーティング
アフィニティー精製したGST−TSHR−EDタンパク質をPBS緩衝液で希釈して適切な濃度にし、かつ先に記載したようにマイクロタイタープレート(Corning社)上に直接コーティングするか、又は製造指示に従ってグルタチオン固定マイクロタイタープレート(NUNC社)上にコートした。抗−TSHR自己抗体IgG又はIgMの、GST−TSHR−EDに対する結合は、例6に記載されているように検出した。図12に示されているように、IgGとIgMの両方に対するGST−TSHR−EDの結合活性は、GST−TSHR−EDを直接にコートしたプレートよりも、グルタチオン固定プレートを介してコートしたGST−TSHR−EDでは高かった。この実験は、同じコーティング濃度では、試験した4つの患者血清(L2、L1、M4及びM21)中、自己抗体IgG(A)とIgM(B)に対するGST−TSHR−EDタンパク質の結合活性はGST−TSHR−EDを直接にコートしたプレートよりも、グルタチオン固定マイクロタイタープレートを介してコートしたGST−TSHR−EDにおいて著しく高いことを示している。
例13 変性したGST−TSHR−ED組換えタンパク質をコートしたマイクロタイタープレートで減少した抗−TSHR自己抗体に対するGST−TSHR−EDの結合活性
アフィニティー精製したGST−TSHR−EDを同じ濃度で、タンパク質を変性せずにマイクロタイタープレートにコーティングし、かつ水浴中で5分間処置し、GST−TSHR−EDタンパク質を変性した。4つの患者血清中の抗−YSHR自己抗体IgGとIgMをコートした上記プレート中で試験した。自己抗体IgG(A)とIgM(B)に対するGST−TSHR−EDの減少した結合活性は、コーティング前に5分間水浴中で処置してGST−TSHR−EDを変性した後に観察された(図13)。
アフィニティー精製したGST−TSHR−EDを同じ濃度で、タンパク質を変性せずにマイクロタイタープレートにコーティングし、かつ水浴中で5分間処置し、GST−TSHR−EDタンパク質を変性した。4つの患者血清中の抗−YSHR自己抗体IgGとIgMをコートした上記プレート中で試験した。自己抗体IgG(A)とIgM(B)に対するGST−TSHR−EDの減少した結合活性は、コーティング前に5分間水浴中で処置してGST−TSHR−EDを変性した後に観察された(図13)。
例14 TSHR−特異的ペプチドスキャンニングによるTSHR−特異的自己抗体エピトープの同定
TSHR特異的自己抗体と反応するエピトープを同定するために、TSHR−特異的ペプチドスキャンニング法を利用した。aa22〜aa415までのヒトTSHRの細胞外ドメインの全体をカバーする7つのアミノ酸(aa)を重複させて短いペプチド(5520-mer)を合成した。ペプチドをELISAプレート上に固定し、かつ各々のヒト血清サンプルを用いてELISAアッセイを行った。この方法により、ヒトTSHRの自己免疫原性線状エピトープの系列(n=8)を同定できた(図15、16及び17)。図14には、ペプチドと反応した個々の血清(血清M23)の反応性が示されている。従って、TSHRのエピトープと反応する患者血清からのTSHRに特異的な自己抗体があることが予想できる。しかし、細菌内で産生された組換えGST−TSHR−EDと強く反応するが、個々のペプチドとは反応しない血清の系列があることも見出された(例:血清460、図18/19)。血清460は、血清M23に匹敵するように組換えGST−TSHR−EDと反応するにもかかわらず、TSHR特異的ペプチドには結合しない(図18/19)。従って、本発明の細菌系で発現したGST−TSHR−EDは、TSHR特異構造的エピトープを示し、かつ各々の患者サンプルがヒトTSHRの線状ならびに構造的エピトープを認識する自己抗体を含有することが予測できる。これらの自己抗体の割合ならびに全体量は、血清サンプルが、TSHR特異的ペプチドセットにより示されるエピトープ及び細菌により発現したGST−TSHR−EDと反応するのか、又は組換えGST−TSHR−EDのみと反応するのかを決定する。
TSHR特異的自己抗体と反応するエピトープを同定するために、TSHR−特異的ペプチドスキャンニング法を利用した。aa22〜aa415までのヒトTSHRの細胞外ドメインの全体をカバーする7つのアミノ酸(aa)を重複させて短いペプチド(5520-mer)を合成した。ペプチドをELISAプレート上に固定し、かつ各々のヒト血清サンプルを用いてELISAアッセイを行った。この方法により、ヒトTSHRの自己免疫原性線状エピトープの系列(n=8)を同定できた(図15、16及び17)。図14には、ペプチドと反応した個々の血清(血清M23)の反応性が示されている。従って、TSHRのエピトープと反応する患者血清からのTSHRに特異的な自己抗体があることが予想できる。しかし、細菌内で産生された組換えGST−TSHR−EDと強く反応するが、個々のペプチドとは反応しない血清の系列があることも見出された(例:血清460、図18/19)。血清460は、血清M23に匹敵するように組換えGST−TSHR−EDと反応するにもかかわらず、TSHR特異的ペプチドには結合しない(図18/19)。従って、本発明の細菌系で発現したGST−TSHR−EDは、TSHR特異構造的エピトープを示し、かつ各々の患者サンプルがヒトTSHRの線状ならびに構造的エピトープを認識する自己抗体を含有することが予測できる。これらの自己抗体の割合ならびに全体量は、血清サンプルが、TSHR特異的ペプチドセットにより示されるエピトープ及び細菌により発現したGST−TSHR−EDと反応するのか、又は組換えGST−TSHR−EDのみと反応するのかを決定する。
例16 エピトープを認識する個々の血清サンプルのペップスキャン(Pepscan)(血清M23)
TSHR−ペプチドをNUNC Maxisorb ELISAプレート(5μg/ml, o/n)上に固定し、かつ非特異的結合部位を飽和した(3% BSA)。血清サンプルをTBS/1%BSA中で1/100希釈し、引き続き全てのウェル中にピペッティングした。図14に示されているように、適切な基質(POD-Blue, Roche)において1:50000希釈で、ペプチドと反応した自己抗体をHRP結合ウサギ抗マウス−Ig(DIANOVA社, Hamburg)で視覚化した。図15に示されているような38個の患者血清の分析ならびに図18に示されているような血清M460の反応性の決定をそれに応じて行った。
TSHR−ペプチドをNUNC Maxisorb ELISAプレート(5μg/ml, o/n)上に固定し、かつ非特異的結合部位を飽和した(3% BSA)。血清サンプルをTBS/1%BSA中で1/100希釈し、引き続き全てのウェル中にピペッティングした。図14に示されているように、適切な基質(POD-Blue, Roche)において1:50000希釈で、ペプチドと反応した自己抗体をHRP結合ウサギ抗マウス−Ig(DIANOVA社, Hamburg)で視覚化した。図15に示されているような38個の患者血清の分析ならびに図18に示されているような血清M460の反応性の決定をそれに応じて行った。
例17 血清23と血清460の比較
組換えタンパク質(GST-TSHR-DEならびに負のコントロールGST)をNUNC Maxisorb ELISAプレート(5μg/ml, o/n)上に固定し、かつ非特異的結合部位を飽和した(3% BSA)。血清サンプルをTBS/1%BSA中で1/100希釈し、引き続きコートしたウェルにピペッティングした。図19に示されているように、適切な基質(POD-Blue, Roche)において1:50000希釈で、組換えタンパク質と反応した自己抗体をHRP結合ウサギ抗マウス−Ig(DIANOVA社, Hamburg)で視覚化した。
組換えタンパク質(GST-TSHR-DEならびに負のコントロールGST)をNUNC Maxisorb ELISAプレート(5μg/ml, o/n)上に固定し、かつ非特異的結合部位を飽和した(3% BSA)。血清サンプルをTBS/1%BSA中で1/100希釈し、引き続きコートしたウェルにピペッティングした。図19に示されているように、適切な基質(POD-Blue, Roche)において1:50000希釈で、組換えタンパク質と反応した自己抗体をHRP結合ウサギ抗マウス−Ig(DIANOVA社, Hamburg)で視覚化した。
例18 同定したホットスポットのコアエピトープ
図17に示されているような自己反応性ホットスポットのコアエピトープは、TSHR特異的エピトープスキャン法により狭められている(図20)。角カッコ内の配列は、有利な最小エピトープ配列を表している。角カッコ内の配列の周囲のアミノ酸は、おそらくTSHR特異的自己抗体の最適な結合に重要である。ホットスポット5/6に関しては、2つのペプチドが関連しているようである。
図17に示されているような自己反応性ホットスポットのコアエピトープは、TSHR特異的エピトープスキャン法により狭められている(図20)。角カッコ内の配列は、有利な最小エピトープ配列を表している。角カッコ内の配列の周囲のアミノ酸は、おそらくTSHR特異的自己抗体の最適な結合に重要である。ホットスポット5/6に関しては、2つのペプチドが関連しているようである。
Claims (44)
- TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質を有する、グリコシド化されていない単離かつ精製した組換えポリペプチドにおいて、次の
a)原核宿主細胞の細胞質内でジスルフィド結合の形成を可能にする突然変異を有さない原核宿主を、前記融合タンパク質をコードする単離かつ精製した核酸配列を有するベクターで形質転換させ、
その際、1つ以上のTSHレセプターの部分配列はポリペプチドに融合し、かつ前記TSHレセプターの部分配列は、主にTSHレセプターの細胞外ドメイン、その断片又はその変異体から成っている;
b)前記原核宿主細胞を培養し、それにより前記融合タンパク質を発現させ、前記原核宿主細胞内に蓄積させ;
c)前記原核宿主細胞を単離し;
d)界面活性剤の存在で前記原核宿主細胞を溶解し;
e)溶解産物の可溶性成分を不溶性成分から分離し;そして
f)前記溶解産物の可溶性成分から融合タンパク質を精製する
ことを含む方法より得られる、グリコシド化されていない単離かつ精製した組換えポリペプチド。 - 融合すべきポリペプチドは、主にグルタチオンSトランスフェラーゼ(GST)、β−グルクロニダーゼ(GUS)、緑色蛍光タンパク質(GFP)又はマルトース結合タンパク質(MBP)もしくはセルロース結合ドメイン(CBD)のような原核結合タンパク質、これらの断片又はこれらの変異体から成る、請求項1に記載のグリコシド化されていない単離かつ精製した組換えポリペプチド。
- 界面活性剤は非イオン性界面活性剤である、請求項1又は2に記載のグリコシド化されていない単離かつ精製した組換えポリペプチド。
- アフィニティー・クロマトグラフィーにより融合タンパク質を溶解産物の可溶性成分から精製する、請求項1から3までのいずれか1項に記載のグリコシド化されていない単離かつ精製した組換えポリペプチド。
- 原核宿主細胞の細胞質内でジスルフィド結合の形成を可能にする突然変異を有さない原核宿主内で発現されるグリコシド化されていない単離かつ精製した組換えポリペプチドであって、前記グリコシド化されていない単離かつ精製した組換えポリペプチドは、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質を有し、その際、1つ以上のTSHレセプターの部分配列は、主にグルタチオンSトランスフェラーゼ(GST)から成るポリペプチド、その断片又はその変異体に融合し、かつ前記TSHレセプターの部分配列は、主にTSHレセプターの細胞外ドメイン、その断片又はその変異体から成っている、グリコシド化されていない単離かつ精製した組換えポリペプチド。
- TSHレセプターの部分配列は、ポリペプチドのC末端に融合する、請求項1から5までのいずれか1項に記載のグリコシド化されていない単離かつ精製した組換えポリペプチド。
- TSHレセプターの部分配列は、TSHレセプターの部分配列内で少なくとも1つのトロンビン切断部位を示す見かけ分子量約45kDaと約35kDaの2つの断片にトロンビンにより切断される、請求項1から6までのいずれか1項に記載のグリコシド化されていない単離かつ精製した組換えポリペプチド。
- TSHレセプターの部分配列は、主に次の1つ以上のアミノ酸配列:
TSHレセプターのN−末端から22〜415番目のアミノ酸配列;
TSHレセプターのN−末端から210〜415番目のアミノ酸配列;
TSHレセプターのN−末端から310〜415番目のアミノ酸配列;
、その断片又はその変異体から成る、請求項1から6までのいずれか1項に記載のグリコシド化されていない単離かつ精製した組換えポリペプチド。 - TSHレセプターの部分配列は、
a)配列番号1に示したTSHレセプターのN末端から22〜415番目のアミノ酸配列を有するアミノ酸配列;
b)a)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
c)配列番号2に示したTSHレセプターのN末端から210〜415番目のアミノ酸配列を有するアミノ酸配列;
d)c)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
e)配列番号3に示したTSHレセプターのN末端から310〜415番目のアミノ酸配列を有するアミノ酸配列;
f)e)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
から成るグループから選択される、請求項1から6までのいずれか1項に記載のグリコシド化されていない単離かつ精製した組換えポリペプチド。 - a)配列番号4に示したアミノ酸配列を有するアミノ酸配列;
b)a)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
c)配列番号5に示したアミノ酸配列を有するアミノ酸配列;
d)c)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
e)配列番号6に示したアミノ酸配列を有するアミノ酸配列;
f)e)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
から成るグループから選択される、請求項1から6までのいずれか1項に記載のグリコシド化されていない単離かつ精製した組換えポリペプチド。 - 請求項10に記載のa)とb)のグリコシド化されていない単離かつ精製した組換えポリペプチドであって、TSHレセプターの部分配列は、トロンビンによってTSHレセプターの部分配列内で少なくとも1つのトロンビン切断部位を示す見かけ分子量約45kDaと約35kDaの2つの断片に切断される、請求項10に記載のa)とb)のグリコシド化されていない単離かつ精製した組換えポリペプチド。
- 国際基準90/672に含まれているTSH、モノクロナール抗−TSHR抗体2C11、モノクロナール抗TSHR抗体4C1及びTSHR自己抗体に結合できる、請求項1から11までのいずれか1項に記載のグリコシド化されていない単離かつ精製した組換えポリペプチド。
- TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できるグリコシド化されていないTSHレセプターの部分配列であって、前記グリコシド化されていないTSHレセプターの部分配列は主にTSHレセプターの細胞外ドメイン、その断片又はその変異体から成っていて、次の
a)原核宿主細胞の細胞質内でジスルフィド結合の形成を可能にする突然変異を有さない原核宿主を、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できる融合タンパク質をコードする単離かつ精製した核酸配列を有するベクターで形質転換し、
その際、1つ以上のTSHレセプターの部分配列は、ポリペプチドに融合し、かつ前記TSHレセプターの部分配列は、主にTSHレセプターの細胞外ドメイン、その断片及びその変異体から成っている;
b)原核宿主細胞を培養し、それにより前記融合タンパク質を発現させ、前記原核宿主細胞内に蓄積させ;
c)前記原核宿主細胞を単離し;
d)界面活性剤の存在で前記原核宿主細胞を溶解し;
e)溶解産物の可溶性成分を不溶性成分から分離し;かつ
f)前記溶解産物の可溶性成分からの融合タンパク質を精製し;
g)前記TSHレセプターの部分配列に融合した前記ポリペプチドを消化又は切断し;かつ
h)前記TSHレセプターの部分配列、その断片又はその変異体を回収する
ことを含む方法により得られる、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体に結合できるグリコシド化されていないTSHレセプターの部分配列。 - ポリペプチドに融合したTSHレセプターの部分配列は、主に次のアミノ酸配列:
TSHレセプターのN末端から22〜415番目のアミノ酸配列;
TSHレセプターのN末端から210〜415番目のアミノ酸配列;及び
TSHレセプターのN末端から310〜415番目のアミノ酸配列
のいずれか1つ、その断片又はその変異体から成る、請求項13に記載のグリコシド化されていないTSHレセプターの部分配列。 - a)配列番号1に示したTSHレセプターのN末端から22〜415番目のアミノ酸配列を有するアミノ酸配列;
b)a)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
c)配列番号2に示したTSHレセプターのN末端から210〜415番目のアミノ酸配列を有するアミノ酸配列;
d)c)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
e)配列番号3に示したTSHレセプターのN末端からの310〜415番目のアミノ酸配列を有するアミノ酸配列;
f)e)で定義したアミノ酸配列に少なくとも80%相同であるアミノ酸配列;
から成るグループから選択される、請求項13に記載のグリコシド化されていないTSHレセプターの部分配列。 - 界面活性剤は、非イオン性界面活性剤である、請求項13から15までのいずれか1項に記載のグリコシド化されていないTSHレセプターの部分配列。
- アフィニティー・クロマトグラフィーにより融合タンパク質を溶解産物の可溶性成分から精製する、請求項13から16までのいずれか1項に記載のグリコシド化されていないTSHレセプターの部分配列。
- a)配列番号10〜27から選択されるアミノ酸配列の少なくとも5個の連続したアミノ酸を有するエピトープ;
b)配列番号10〜27から選択されるアミノ酸配列を有するエピトープ:
c)a)又はb)で定義したアミノ酸配列に少なくとも60%相同であるエピトープ;
から成るグループから選択されるグリコシド化されていないTSHレセプターの部分配列のエピトープ。 - 請求項1から12までのいずれか1項に記載のグリコシド化されていない単離かつ精製した組換えポリペプチドにより構成される融合タンパク質をコードする単離かつ精製した核酸配列。
- 請求項19に記載の核酸配列の少なくとも1つのコピーを有するベクター。
- 請求項19の核酸配列及び/又は請求項20のベクターで形質転換した、その細胞質内でジスルフィド結合の形成を可能にする突然変異を有さない原核宿主細胞。
- 被験者の生体液中で、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を検出及び/又は定量化する方法であって、該方法は
a)生体液を、請求項1から12までのいずれか1項に記載の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は請求項13から17までのいずれか1項に記載の1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は請求項18に記載の1つ以上のエピトープと接触させ、かつ
b)前記グリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は前記グリコシド化されていないTSHレセプターの部分配列及び/又は前記エピトープに結合した自己抗体を検出及び/又は定量化する
ことを含む、被験者の生体液中で、TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を検出及び/又は定量化する方法。 - TSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生される自己抗体を、インビトロで検出及び/又は定量化し、その際、生体液が被験者からのサンプルとして得られる、請求項22に記載の方法。
- 生体液を被験者からサンプルとして得て、かつ前記サンプルを、グリコシド化されていない単離かつ精製した組換えポリペプチド及び/又はグリコシド化されていないTSHレセプターの部分配列及び/又は固体担体上に固定したエピトープと接触させ、かつ前記固体担体に結合した自己抗体を検出及び/又は定量化する、請求項22又は23に記載の方法。
- サンプルをグリコシド化されていない単離かつ精製した組換えポリペプチドと接触させ、1つ以上のTSHレセプターの部分配列を、主にグルタチオンSトランスフェラーゼ(GST)、その断片又はその変異体から成るポリペプチドに融合させ、かつ前記融合タンパク質がその表面上にグルタチオンを提供する固体担体とのジスルフィド結合により固体担体上に並ぶように、前記融合タンパク質を固定する、請求項24に記載の方法。
- 自己抗体は、ELISA、LISA、RIA、ウェスタンブロット、免疫沈降又はフローサイトメトリーから選択されるアッセイにより検出及び/又は定量化される、請求項22から25までのいずれか1項に記載の方法。
- アッセイがELISAである、請求項26に記載の方法。
- 検出及び/又は定量化された自己抗体は、アイソタイプIgG、IgM及び/又はIgAのものである、請求項22から27までのいずれか1項に記載の方法。
- 更に、
c)検出及び/又は定量化した自己抗体を単離する
ことを含む、請求項22から28までのいずれか1項に記載の方法。 - 更に、TG及び/又はTPOに対する自己抗体を検出及び/又は定量化する、請求項22から29までのいずれか1項に記載の方法。
- 請求項22から30までのいずれか1項に記載の方法により得られる又は得られた、アイソタイプIgG、IgM及び/又はIgAのTSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生された自己抗体。
- 場合により試薬及び/又は取扱説明書の付いた、請求項1から12までのいずれか1項に記載の少なくとも1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は請求項13から17までのいずれか1項に記載の少なくとも1つ以上のグリコシド化されていないTSHレセプターの部分配列、及び/又は請求項18に記載の1つ以上のエピトープを有する、被験者の生体液中でTSHレセプターに対する免疫反応と関連する自己免疫疾患に応答して産生された自己抗体を検出及び/又は定量化するためのキット。
- ELISA、LISA、RIA、ウェスタンブロット、免疫沈降又はフローサイトメトリーから選択されるアッセイを実施するための試薬を更に有する、請求項32に記載のキット。
- アッセイはELISAである、請求項33に記載のキット。
- ポイント・オブ・ケアテストを実施するための試薬を更に有する、請求項32に記載のキット。
- TG及びTPOを検出及び/又は定量化するための試薬を更に有する、請求項32から35までのいずれか1項に記載のキット。
- TSHレセプターに対する免疫反応と関連する自己免疫疾患を診断するための、請求項32から36までのいずれか1項に記載のキットの使用。
- 活性物質として、請求項1から12までのいずれか1項に記載の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は請求項13から17までのいずれか1項に記載の1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は請求項18に記載の1つ以上のエピトープの製剤学的有効量を、場合により製剤学的に認容性のキャリヤー、希釈剤又は補助剤と一緒に有する、医薬組成物。
- TSHレセプターに対する免疫反応と関連する自己免疫疾患の治療又は予防で使用するための、及び/又は診断で使用するための、請求項1から12までのいずれか1項に記載の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は請求項13から17までのいずれか1項に記載の1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は請求項18に記載の1つ以上のエピトープ及び/又は請求項38の医薬組成物。
- TSHレセプターに対する免疫反応と関連する自己免疫疾患を治療又は予防するための医薬品を製造するための、請求項1から12までのいずれか1項に記載の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は請求項13から17までのいずれか1項に記載の1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は請求項18に記載の1つ以上のエピトープ及び/又は請求項38に記載の医薬組成物の使用。
- 請求項1から12までのいずれか1項に記載の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は請求項13から17までのいずれか1項に記載の1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は請求項18に記載の1つ以上のエピトープ及び/又は請求項38に記載の医薬組成物との結合により、治療効果を提供することが確認されている治療薬の治療有効量を被験者に投与することから成る、被験者でTSHレセプターに対する免疫反応と関連する自己免疫疾患を治療する方法。
- TSHレセプターの結合相手を同定する方法において、
a)前記結合相手を、請求項1から12までのいずれか1項に記載の1つ以上のグリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は請求項13から17までのいずれか1項に記載の1つ以上のグリコシド化されていないTSHレセプターの部分配列及び/又は請求項18の1つ以上のエピトープと接触させる工程、
b)前記グリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は前記グリコシド化されていないTSHレセプターの部分配列及び/又は前記エピトープに結合した結合相手を検出及び/又は定量化する工程、
c)場合により、前記グリコシド化されていない単離かつ精製した組換えポリペプチド及び/又は前記グリコシド化されていないTSHレセプターの部分配列及び/又は前記エピトープに結合した、検出及び/又は定量化した結合相手を単離する工程
を含むことを特徴とする、TSHレセプターの結合相手を同定する方法。 - 結合相手がTSHを有さない、請求項42に記載の方法により得られるTSHレセプターの結合相手。
- 結合相手は、IgG、IgM又はIgAアイソタイプの抗体である、請求項43に記載の結合相手。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US73802105P | 2005-11-21 | 2005-11-21 | |
| PCT/IB2006/003394 WO2007057778A2 (en) | 2005-11-21 | 2006-11-21 | Recombinant polypeptides and methods for detecting and/or quantifying autoantibodies against tsh receptor |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2009517015A true JP2009517015A (ja) | 2009-04-30 |
| JP2009517015A5 JP2009517015A5 (ja) | 2010-01-14 |
Family
ID=37998447
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008541846A Withdrawn JP2009517015A (ja) | 2005-11-21 | 2006-11-21 | 組換えポリペプチドならびにtshレセプターに対する自己抗体を検出及び/又は定量化する方法 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US20080305098A1 (ja) |
| EP (2) | EP2080772A3 (ja) |
| JP (1) | JP2009517015A (ja) |
| WO (1) | WO2007057778A2 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011136911A (ja) * | 2009-12-25 | 2011-07-14 | Tosoh Corp | 甲状腺刺激ホルモンレセプターの安定化方法 |
| JP2016527304A (ja) * | 2013-08-06 | 2016-09-08 | アピトープ インターナショナル エヌブイ | ペプチド |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010075194A1 (en) * | 2008-12-22 | 2010-07-01 | St. Jude Children's Research Hospital | Prokaryotic expression of soluble, active dkk |
| US9073992B2 (en) * | 2008-12-24 | 2015-07-07 | Rsr Ltd. | Human anti TSHR antibodies |
| US20130189707A1 (en) * | 2010-01-26 | 2013-07-25 | Svetlana Alexandrovna Sergeeva | Method of determination of autoantibody level by means of enzyme immunoassay |
| KR101872060B1 (ko) * | 2011-09-09 | 2018-06-27 | 퀴델 코포레이션 | 자가항체를 검출하기 위한 조성물 및 방법 |
| JP6472789B2 (ja) | 2013-05-14 | 2019-02-20 | シーメンス・ヘルスケア・ダイアグノスティックス・インコーポレーテッドSiemens Healthcare Diagnostics Inc. | 受容体含有安定化液剤 |
| CA2971995A1 (en) | 2014-12-24 | 2016-06-30 | Apitope Technology (Bristol) Limited | Thyroid stimulating hormone receptor (tshr) peptides and use thereof |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20030022826A1 (en) * | 1987-09-08 | 2003-01-30 | Duke University | Use of synthetic peptides to induce tolerance to pathogenic T and B cell epitopes of autoantigens or infectious agents |
| JPH0789991A (ja) * | 1993-09-28 | 1995-04-04 | Mitsubishi Chem Corp | 新規なポリペプチドおよびそれを用いるtsh受容体抗体の測定法 |
| EP1078986B1 (en) | 1999-08-24 | 2007-02-28 | Tosoh Corporation | Secretory thyroid stimulating hormone receptor (TSHR), and method for assaying anti-TSHR antibody using the same |
| ES2466377T3 (es) * | 2001-08-23 | 2014-06-10 | Rsr Limited | Regiones epitópicas de un receptor de tirotropina (TSH), usos de las mismas y anticuerpos para las mismas |
| AU2003285540A1 (en) * | 2002-11-29 | 2004-06-23 | Rsr Limited | Antibody for the thyrotropin receptor and uses thereof |
-
2006
- 2006-11-21 US US12/094,533 patent/US20080305098A1/en not_active Abandoned
- 2006-11-21 JP JP2008541846A patent/JP2009517015A/ja not_active Withdrawn
- 2006-11-21 EP EP09005494A patent/EP2080772A3/en not_active Withdrawn
- 2006-11-21 WO PCT/IB2006/003394 patent/WO2007057778A2/en active Application Filing
- 2006-11-21 EP EP06820995A patent/EP1951753A2/en not_active Withdrawn
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011136911A (ja) * | 2009-12-25 | 2011-07-14 | Tosoh Corp | 甲状腺刺激ホルモンレセプターの安定化方法 |
| JP2016527304A (ja) * | 2013-08-06 | 2016-09-08 | アピトープ インターナショナル エヌブイ | ペプチド |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2007057778A2 (en) | 2007-05-24 |
| EP2080772A2 (en) | 2009-07-22 |
| EP1951753A2 (en) | 2008-08-06 |
| WO2007057778A3 (en) | 2007-11-08 |
| US20080305098A1 (en) | 2008-12-11 |
| EP2080772A3 (en) | 2009-10-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102570713B1 (ko) | SARS-CoV-2 감염의 진단을 위한 방법 및 시약 | |
| JP2009517015A (ja) | 組換えポリペプチドならびにtshレセプターに対する自己抗体を検出及び/又は定量化する方法 | |
| US9840551B2 (en) | Blood markers for diagnosing epithelium derived cancers and monoclonal antibodies thereof | |
| EP2853898B1 (en) | Analysis of myostatin in serum | |
| EP3855186A2 (en) | A method for determining the efficacy of a sars-cov-2 vaccine | |
| JP5379698B2 (ja) | アビバクテリウム・パラガリナラム抗体の検出方法およびキット | |
| CN110684740A (zh) | 一种抗人泛素羧基末端水解酶-1(uch-l1)的单克隆抗体及其应用 | |
| WO2009086398A2 (en) | Anti-t. cruzi antibodies and methods of use | |
| Nagaoka et al. | Antibodies against a short region of PfRipr inhibit Plasmodium falciparum merozoite invasion and PfRipr interaction with Rh5 and SEMA7A | |
| WO2010079739A1 (ja) | 全インフルエンザ菌の測定方法 | |
| EP2461829B1 (en) | Novel proteins | |
| WO2021237534A1 (zh) | 抗新型冠状病毒的抗体、抗体组合、制备方法、包含其的检测试剂盒 | |
| JP2001507447A (ja) | H. pylori診断薬 | |
| CA2785678A1 (en) | Human insulin assay and assay reagent | |
| EP3011008B1 (en) | Method of detecting the presence or absence of autoantibodies | |
| WO2006073133A1 (ja) | 新規タンナーゼ遺伝子およびそのタンパク質 | |
| WO2008068906A1 (ja) | 中皮腫診断剤、中皮腫診断キットおよび中皮腫診断方法 | |
| WO2013071127A1 (en) | Monoclonal antibodies against serotransferrin antigens, and uses therefor | |
| CA2571673A1 (en) | Novel methods of diagnosis of treatment of p. aeruginosa infection and reagents therefor | |
| KR20230054460A (ko) | Hcv 재조합 항원 및 그의 돌연변이체 | |
| JP2007071849A (ja) | 中皮腫診断剤および中皮腫診断キット | |
| JP6407990B2 (ja) | アウグリン免疫学的検定 | |
| EP3761029B1 (en) | A novel assay for the diagnosis of nematode infections | |
| EP4148429A2 (en) | Method and kit for the detection of bovine herpes virus type 1 (bohv-1) antibodies | |
| KR102244121B1 (ko) | 브루셀라균의 omp28에 특이적으로 결합하는 단일클론항체, 상기 항체를 생산하는 하이브리도마 세포주 및 이의 용도 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091119 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20091119 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20101221 |