JP2008534965A - 集積化インピーダンス電極を備えるマルチウェルサンプルプレート及び接続方法 - Google Patents
集積化インピーダンス電極を備えるマルチウェルサンプルプレート及び接続方法 Download PDFInfo
- Publication number
- JP2008534965A JP2008534965A JP2008504172A JP2008504172A JP2008534965A JP 2008534965 A JP2008534965 A JP 2008534965A JP 2008504172 A JP2008504172 A JP 2008504172A JP 2008504172 A JP2008504172 A JP 2008504172A JP 2008534965 A JP2008534965 A JP 2008534965A
- Authority
- JP
- Japan
- Prior art keywords
- impedance measuring
- well
- plate
- electrodes
- measuring device
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/508—Containers for the purpose of retaining a material to be analysed, e.g. test tubes rigid containers not provided for above
- B01L3/5085—Containers for the purpose of retaining a material to be analysed, e.g. test tubes rigid containers not provided for above for multiple samples, e.g. microtitration plates
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/02—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/02—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance
- G01N27/04—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance by investigating resistance
- G01N27/06—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance by investigating resistance of a liquid
- G01N27/07—Construction of measuring vessels; Electrodes therefor
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
- G01N33/48707—Physical analysis of biological material of liquid biological material by electrical means
- G01N33/48728—Investigating individual cells, e.g. by patch clamp, voltage clamp
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0647—Handling flowable solids, e.g. microscopic beads, cells, particles
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/02—Identification, exchange or storage of information
- B01L2300/021—Identification, e.g. bar codes
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/06—Auxiliary integrated devices, integrated components
- B01L2300/0627—Sensor or part of a sensor is integrated
- B01L2300/0645—Electrodes
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/18—Means for temperature control
- B01L2300/1805—Conductive heating, heat from thermostatted solids is conducted to receptacles, e.g. heating plates, blocks
- B01L2300/1827—Conductive heating, heat from thermostatted solids is conducted to receptacles, e.g. heating plates, blocks using resistive heater
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Analytical Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Pathology (AREA)
- Biochemistry (AREA)
- General Physics & Mathematics (AREA)
- Clinical Laboratory Science (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Electrochemistry (AREA)
- Biophysics (AREA)
- Medicinal Chemistry (AREA)
- Food Science & Technology (AREA)
- Urology & Nephrology (AREA)
- Molecular Biology (AREA)
- Investigating Or Analyzing Materials By The Use Of Electric Means (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Abstract
Description
最も広く使用されるスクリーニング方法は、標識化作動薬を利用する抗体や受容体のような選択ターゲットタンパク質に対するライブラリ化合物の競合結合または非競合結合である。この方法は多くの場合、ハイスループットスクリーニング装置で行なわれ、当該スクリーニング装置は、複数の分離マイクロウェルを基板表面に画定し、かつ各ウェル内の構造を測定するマルチウェル装置から成る。分析をハイスループット化するために種々の技術が開発されている。マルチウェル分析プレートを使用することにより並列処理が可能になり、一つのプレートの複数のウェルに分散する複数のサンプルの分析が可能になる。通常、サンプル及び試薬は、マルチウェル分析プレート(マイクロプレートまたはマイクロタイター(microtiter)プレートとしても知られる)に保存され、当該プレートで処理され、および/または分析される。分析では通常、各ウェルのサンプルの光学測定または放射能測定を行なう。マイクロタイタープレートは通常、分析内容を収容する容器として機能する。多くの場合、プレートの表面は、当該表面が複数の分析成分のうちの一つ以上の成分との結合の影響を多かれ少なかれ受け易くなるように処理される。別の構成として(非常に稀であるが)、マイクロタイタープレートは、異なる測定の実施を可能にする各ウェルの電極群のような構造と組み合わせることができる。
複数の電極構造がマイクロウェルプレートに使用されている。米国特許出願公開第2002/0025575号明細書は、ウェルへの挿入に適合させた一対の電極と、低電圧のAC信号を複数の電極に印加する回路とを開示している。この回路は、当該複数の電極をテストサンプルに沈めたときに、それら複数の電極に低電圧のAC信号を印加する。これらの電極に流れる電流を同時測定することにより、テスト化合物における成長または代謝活性のレベルをモニタリングすることができる。電極構造を各プレートウェルに挿入することにより、ハイスループットプロセスが煩雑になり、スループット(処理速度)が下がるので、電極を集積化することが必要であった。基板は複数の分離マイクロウェルを画定し、この場合、マルチ電極カバープレートに取り付けられる電極ピンは、カバーが基板を覆うように載置されると液体に浸漬される。
電気的試験をマルチウェルプレートで行なうことによる利点が得られる一方で、ウェル数の増加に伴ない、多くの電気コンタクトが必要になるということが課題の一つとして挙げられる。ウェル当り2つの電気コンタクトが必要になる場合、96個のウェルプレートを設けると192個の電気コンタクトが必要になり、384個のウェルプレートを設けると768個の電気コンタクトが必要になり、1536個のウェルプレートを設けると3072個の電気コンタクトが必要になる。幾つかの適用例では、必要な電気コンタクトの数は、一つ以上の導体を互いに接続することにより減らすことができるが(例えば、電極群が一つの共通接地線を共有する)、この構成は、接続導体を共有するウェル群の間で干渉が発生する可能性があり、かつ複数のウェルを同時に測定する機能が低下することにより望ましくない場合がある。必要な電気接続の数が少ない場合、ウェル群の電極群は、エッジタイプコネクタを用いることができるマイクロタイタープレートのエッジに達する電気接続線に接続することができる。必要な電気接続の数が多くなる場合、エッジ接続は不便になる。この場合、マイクロタイタープレートの下部の全表面積を使用することが望ましい。
インピーダンス計測
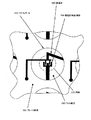
以下の実施例において説明される装置は専用インピーダンス測定システムとのインターフェース接続を3つの方法により行なう。1)組立装置の底部に設けられる電気接触パッドは計測器の電気接触ピンと接触する。各ウェルの電気接続線をインピーダンス測定電子機器にまで配線する。2)装置の下面は熱制御表面に支えられて、装置のウェルの内容物の温度制御を可能にする。3)上部プレートのウェルを計測器の自動ピペット装置に位置合わせして、異なる化合物をウェルの各々に、インピーダンス測定の間に添加することができるようにする。
下部プレートは、1mmの厚さで、122mm×79mmの寸法のBorofloat(商標)ガラス基板により作製した。孔をガラス(0.030インチ厚)に超音波プロセスを使用してドリル開口した。1.6ミクロンの厚さの金をガラスの上面及び下面の両方にスパッタリングにより堆積させた。同時に、スパッタ成膜された金で、ドリル開口孔の内側表面を被覆して、ガラスの上面と下面との間に電気ビアを形成した。次に、フォトリソグラフィ露光及び化学エッチング法を使用して下部プレートの上面に設けられるインピーダンス測定電極をパターニングし、電気接触パッドを下部プレートの下面に形成した。電極は、相互に噛み合う櫛歯状フィンガペア(pair of interdigitated finger combs)であり、幅30ミクロン及び長さ2.5mmのフィンガサイズを有する。対向する櫛歯状フィンガの間のギャップは30ミクロンであった。
下部プレートは、1mmの厚さで、122mm×79mmの寸法のポリスチレンシート基板により作製した。孔をポリスチレン(0.030インチ厚)にドリル開口した。0.5ミクロンの厚さの金をポリスチレンの上面に、金属薄膜マスクまたはステンシルを通してスパッタリングにより堆積させて電極パターンを形成した。電極は、相互に噛み合う櫛歯状フィンガペアであり、幅200ミクロン、及び長さ1.5mmのフィンガサイズを有する。対向する櫛歯状フィンガの間のギャップは200ミクロンであった。電極を形成すると同時に、スパッタ成膜された金で、ドリル開口孔の内側表面を被覆した。次に、0.5ミクロンの厚さの金をポリスチレンの上面に、金属薄膜マスクまたはステンシルを通してスパッタリングにより堆積させて電気接触パッドパターンを形成した。同時に、スパッタ成膜された金で、この場合も同じように、ドリル開口孔の内側表面を被覆して、電気ビアをポリスチレンの上面と下面との間に形成した。金パターンをポリスチレンの上に形成した後、下部プレートをプラズマエッチングして表面への細胞の接着性を高めた。
[実施例3]
下部プレートは、0.005インチの厚さのポリエステルシート基板により作製した。孔をポリスチレン(0.15mm厚)にレーザドリルにより開口して、後の工程で下部プレートに形成されることになる電気ビアと一致するパターンに形成した。導電性銀インクをスクリーン印刷プロセスに使用して、電気接触パッドを下部プレート材料の下面に形成し、当該インクをドリル開口ビアホールに充填した。次に、第2印刷パスを銀インクを用いて行なってパターンを下部プレートの上面に印刷して、パターンがドリル開口ビアから、マイクロプレートウェルの中心部が下部プレート及び上部プレートを接着させるときに形成される場所の近くの位置に向かって延びるようにする。次に、金インクから成るフィンガを印刷により形成して、相互に噛み合う櫛歯状フィンガパターンを2つの銀リードの間に形成した。各金フィンガはこれらの銀リードのうちの一方と一端で重なった。最後の印刷工程では、誘電体インクを印刷して、金フィンガの長さ部分を露出したままにする矩形を除く下部プレートの上面全体を被覆した。金フィンガの先端を絶縁誘電体で被覆することにより、露出金フィンガの合計長が誘電体窓の寸法及びフィンガ幅で決まるようにした。印刷が施された下部プレート材料を酸素雰囲気中で4分間に渡ってプラズマエッチングして細胞接着性を向上させた。エッチングの後、個々の下部プレートをシートから切り出した。
以上、装置の利用可能な実施形態について説明してきたが、種々の代替物、変形物及び等価物を使用することができる。例えば、この技術分野の当業者であれば、インピーダンス測定電極構造は相互に噛み合う櫛歯状フィンガ構造に制限されないことを理解し得る。他の導体構造を別の構成として使用することができる。更に、本出願において列挙した全ての刊行物及び特許文献は本明細書において参照することにより、個々の刊行物及び特許文献が個々に提示された状況と同じ程度に、刊行物及び特許文献の内容の全てが本明細書に、あらゆる目的のために組み込まれる。上記説明は装置の例示としての実施形態としてのみ捉えられるべきであり、これらの実施形態の違いは添付の請求項の差異及び範囲によって適切に規定される。
Claims (104)
- マルチウェルインピーダンス測定装置であって、
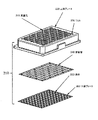
A.分離された複数のサンプルを平板型アレイ構造にて収容する複数のチャンバであって、前記複数のチャンバは下面を有し、かつ該複数のチャンバは複数の貫通孔を含む上部プレートと下部プレートとから形成されており、前記下部プレートは上面及び下面を有し、前記上部プレートは上面及び下面を有し、前記下部プレートの上面は前記上部プレートの下面に密閉固着されている、複数のチャンバと、
B.前記複数のチャンバの下面及び前記下部プレートの上面に平坦に設けられる複数の機能的等価インピーダンス測定電極であって、該複数の電極は前記複数のサンプルに対して露出されており、かつ前記複数の電極の各々は該マルチウェルインピーダンス測定装置内の複数の他の電極の各々から電気的に絶縁されており、かつ前記複数の電極は上面及び下面を有している、複数の機能的等価インピーダンス測定電極と、
C.前記下部プレートの下面から前記複数の電極の各々と電気コンタクトを取るための接続手段と、
を備える、マルチウェルインピーダンス測定装置。 - 前記サンプルは液体である、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記サンプルは固体である、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記サンプルは生物学的化合物である、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記サンプルは分子である、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記貫通孔は円筒形である、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記貫通孔は方形である、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記貫通孔は円錐形である、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記上部及び下部プレートは、プラスチック、エラストマー、セラミックス、複合材料、ガラス、カーボン材料、またはこれらの材料の組み合わせのいずれかにより作製されている、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記プラスチックは、ポリスチレン、ポリカーボネート、ポリアミド、ポリイミド、ポリエチレン、ポリプロピレン、ポリエチレンテレフタレート、シクロオレフィンポリマー、またはポリエステルである、請求項9記載のマルチウェルインピーダンス測定装置。
- 前記プラスチックは射出成形可能なプラスチックである、請求項9記載のマルチウェルインピーダンス測定装置。
- 前記下部プレートは透明である、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは24個のウェルから成る、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは96個のウェルから成る、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは384個のウェルから成る、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは864個のウェルから成る、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは1536個のウェルから成る、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記複数の機能的等価インピーダンス測定電極は2つの同一電極から成る、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記複数の機能的等価インピーダンス測定電極は、電気メッキ、スパッタリング、蒸着、スクリーン印刷、またはパッド印刷によって前記下部プレートの表面に堆積された導電材料により形成されている、請求項1記載の機能的等価電極。
- 前記導電材料は、金、銀、インジウム錫酸化物、銅、または炭素繊維である、請求項1記載の機能的等価電極。
- 前記複数の機能的等価インピーダンス測定電極は、単一層の導電材料により形成されている、請求項1記載の機能的等価電極。
- 前記複数の機能的等価インピーダンス測定電極は、複数層の導電材料により形成されている、請求項1記載の機能的等価電極。
- 前記上部プレートは、接着層、熱ボンディング、または超音波ボンディングを使用して前記下部プレートに密閉固着されている、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記下部プレートの下面から前記複数の電極の各々と電気コンタクトを取るための接続手段は、前記下部プレートの下面に形成された複数の電気接触パッドと、前記下部プレートの上面に設けられた前記複数の電極に前記複数の電気接触パッドを接続する複数の導電ビアとを含む、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記複数の電気接触パッドは、電気メッキ、スパッタリング、蒸着、スクリーン印刷、またはパッド印刷によって前記下部プレートの下面に堆積された導電材料により形成されている、請求項24記載の電気接触パッド。
- 前記導電材料は、金、銀、インジウム錫酸化物、銅、または炭素繊維である、請求項25記載の電気接触パッド。
- 前記複数の電気接触パッドは、導電性インクとして塗布された導電粒子により形成されている、請求項24記載の電気接触パッド。
- 前記導電粒子は、金、銀、白金、または炭素により作製されている、請求項27記載の電気接触パッド。
- 前記複数の機能的等価インピーダンス測定電極は、導電性インクとして塗布された導電粒子により形成されている、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記導電粒子は、金、銀、白金、または炭素により作製されている、請求項29記載のマルチウェルインピーダンス測定装置。
- 前記複数の機能的等価インピーダンス測定電極は、金属層及び導電性インクにより形成されている、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記複数の導電ビアは、金属層及び導電性インクにより形成されている、請求項24記載のマルチウェルインピーダンス測定装置。
- 前記複数の電気接触パッドは、金属層及び導電性インクにより形成されている、請求項24記載のマルチウェルインピーダンス測定装置。
- 計測器によりプレート識別情報を読み取り可能な手段をさらに備える、請求項1記載のマルチウェルインピーダンス測定装置。
- 前記計測器によりプレート識別情報を読み取り可能な手段は、光学的に読み取り可能なパターン、電気的に読み取り可能なパターン、機械的パターン、RFIDタグ、またはメモリチップを含む、請求項34記載のマルチウェルインピーダンス測定装置。
- マルチウェルインピーダンス測定装置であって、
A.分離された複数のサンプルを平板型アレイ構造にて収容する複数のチャンバであって、前記複数のチャンバは下面を有し、かつ該複数のチャンバは複数の孔を含むプレートから形成されており、前記複数の孔は前記プレートの一部分を貫通して延びている、複数のチャンバと、
B.前記複数のチャンバの下面に平坦に設けられる複数の機能的等価インピーダンス測定電極であって、該複数の電極は前記複数のサンプルに対して露出されており、かつ前記複数の電極の各々は該マルチウェルインピーダンス測定装置内の複数の他の電極の各々から電気的に絶縁されており、かつ前記複数の電極は上面及び下面を有し、前記プレートは前記複数の電極の周りに形成されている、複数の機能的等価インピーダンス測定電極と、
C.前記プレートの下面から前記複数の電極と電気コンタクトを取るための接続手段と、
を備える、マルチウェルインピーダンス測定装置。 - 前記サンプルは液体である、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記サンプルは固体である、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記サンプルは生物学的化合物である、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記サンプルは分子である、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記孔は円筒形である、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記孔は方形である、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記孔は円錐形である、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記プレートは、プラスチック、エラストマー、セラミックス、複合材料、ガラス、カーボン材料、またはこれらの材料の組み合わせのいずれかにより作製されている、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記プラスチックは、ポリスチレン、ポリカーボネート、ポリアミド、ポリイミド、ポリエチレン、ポリプロピレン、ポリエチレンテレフタレート、シクロオレフィンポリマー、またはポリエステルである、請求項44記載のマルチウェルインピーダンス測定装置。
- 前記プラスチックは射出成形可能なプラスチックである、請求項44記載のマルチウェルインピーダンス測定装置。
- 前記プレートは透明である、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは24個のウェルから成る、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは96個のウェルから成る、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは384個のウェルから成る、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは864個のウェルから成る、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは1536個のウェルから成る、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記複数の機能的等価インピーダンス測定電極は2つの同一電極から成る、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記複数の機能的等価インピーダンス測定電極は、スパッタリング、蒸着、スクリーン印刷、またはパッド印刷によって前記フレームに堆積された導電材料により形成されている、請求項36記載の機能的等価電極。
- 前記プレートは前記フレーム上に成形されている、請求項54記載の機能的等価電極。
- 前記導電材料は、金、銀、インジウム錫酸化物、または炭素繊維を含む、請求項36記載の機能的に等価な電極。
- 前記複数の機能的等価インピーダンス測定電極は、単一層の導電材料により形成されている、請求項36記載の機能的等価電極。
- 前記複数の機能的等価インピーダンス測定電極は、複数層の導電材料により形成されている、請求項36記載の機能的等価電極。
- 前記プレートの下面から前記複数の電極の各々と電気コンタクトを取るための接続手段は、前記プレートの下面に位置する複数の電気接触パッドと、前記プレートの上面に設けられた前記複数の電極に前記複数の電気接触パッドを接続する複数の導電ビアとを含む、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記複数の電気接触パッドは、電気メッキ、スパッタリング、蒸着、スクリーン印刷、またはパッド印刷によって前記プレートの下面に堆積された導電材料により形成されている、請求項59記載の電気接触パッド。
- 前記導電材料は、金、銀、インジウム錫酸化物、銅、または炭素繊維である、請求項60記載の電気接触パッド。
- 前記複数の電気接触パッドは、導電性インクとして塗布された導電粒子により形成されている、請求項59記載の電気接触パッド。
- 前記導電粒子は、金、銀、白金、または炭素により作製されている、請求項62記載の電気接触パッド。
- 前記複数の機能的等価インピーダンス測定電極は、導電性インクとして塗布された導電粒子により形成されている、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記導電性インクは、金、銀、白金、インジウム錫酸化物、ポリマー、または炭素により作製されている、請求項64記載のマルチウェルインピーダンス測定装置。
- 前記複数の機能的等価インピーダンス測定電極は、金属層及び導電性インクにより形成されている、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記複数の導電ビアは、金属層及び導電性インクにより形成されている、請求項59記載のマルチウェルインピーダンス測定装置。
- 前記複数の電気接触パッドは、金属層及び導電性インクにより形成されている、請求項59記載のマルチウェルインピーダンス測定装置。
- 計測器によりプレート識別情報を読み取り可能な手段をさらに備える、請求項36記載のマルチウェルインピーダンス測定装置。
- 前記計測器によりプレート識別情報を読み取り可能な手段は、光学的に読み取り可能なパターン、電気的に読み取り可能なパターン、機械的パターン、RFIDタグ、またはメモリチップを含む、請求項69記載のマルチウェルインピーダンス測定装置。
- マルチウェルインピーダンス測定装置であって、
A.分離された複数のサンプルを平板型アレイ構造にて収容する複数のチャンバであって、前記複数のチャンバは下面を有し、かつ該複数のチャンバは複数の貫通孔を含む上部プレートと下部プレートとから形成されており、前記下部プレートは上面及び下面を有し、前記上部プレートは上面及び下面を有し、前記下部プレートの上面は前記上部プレートの下面に密閉固着されている、複数のチャンバと、
B.前記複数のチャンバの下面及び前記下部プレートの上面に平坦に設けられる複数の機能的等価インピーダンス測定電極であって、該複数の電極は前記複数のサンプルに対して露出されており、かつ前記複数の電極の各々は該マルチウェルインピーダンス測定装置内の複数の他の電極の各々から電気的に絶縁されており、かつ前記複数の電極は上面及び下面を有している、複数の機能的等価インピーダンス測定電極と、
C.前記下部プレートの下面から前記複数の電極の各々と電気コンタクトを取るための接続手段と、
D.計測器によりプレート識別情報を読み取り可能な手段と、
を備える、マルチウェルインピーダンス測定装置。 - 前記サンプルは液体である、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記サンプルは固体である、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記サンプルは生物学的化合物である、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記サンプルは分子である、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記貫通孔は円筒形である、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記貫通孔は方形である、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記貫通孔は円錐形である、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記上部及び下部プレートは、プラスチック、エラストマー、セラミックス、複合材料、ガラス、カーボン材料、またはこれらの材料の組み合わせのいずれかにより作製されている、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記プラスチックは、ポリスチレン、ポリカーボネート、ポリアミド、ポリイミド、ポリエチレン、ポリプロピレン、ポリエチレンテレフタレート、シクロオレフィンポリマー、またはポリエステルである、請求項79記載のマルチウェルインピーダンス測定装置。
- 前記プラスチックは射出成形可能なプラスチックである、請求項79記載のマルチウェルインピーダンス測定装置。
- 前記下部プレートは透明である、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは24個のウェルから成る、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは96個のウェルから成る、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは384個のウェルから成る、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは864個のウェルから成る、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記平板型アレイは1536個のウェルから成る、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記複数の機能的等価インピーダンス測定電極は、2つの同一電極から成る、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記複数の機能的等価インピーダンス測定電極は、スパッタリング、蒸着、スクリーン印刷、またはパッド印刷によって前記下部プレートの表面に堆積された導電材料により形成されている、請求項71記載の機能的等価電極。
- 前記導電材料は、金、銀、インジウム錫酸化物、または炭素繊維である、請求項71記載の機能的等価電極。
- 前記複数の機能的等価インピーダンス測定電極は、単一層の導電材料により形成されている、請求項71記載の機能的等価電極。
- 前記複数の機能的等価インピーダンス測定電極は、複数層の導電材料により形成されている、請求項71記載の機能的等価電極。
- 前記上部プレートは、接着層、熱ボンディング、または超音波ボンディングを使用して前記下部プレートに密閉固着されている、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記下部プレートの下面から前記複数の電極の各々と電気コンタクトを取るための接続手段は、前記下部プレートの下面に位置する複数の電気接触パッドと、前記下部プレートの上面に設けられた前記複数の電極に前記複数の電気接触パッドを接続する複数の導電ビアとを含む、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記複数の電気接触パッドは、電気メッキ、スパッタリング、スクリーン印刷、またはパッド印刷によって前記下部プレートの下面に堆積された導電材料により形成されている、請求項94記載の電気接触パッド。
- 前記導電材料は、金、銀、インジウム錫酸化物、銅、または炭素繊維である、請求項95記載の電気接触パッド。
- 前記複数の電気接触パッドは、導電性インクとして塗布された導電粒子により形成されている、請求項94記載の電気接触パッド。
- 前記導電粒子は、金、銀、白金、または炭素により作製されている、請求項97記載の電気接触パッド。
- 前記複数の機能的等価インピーダンス測定電極は、導電性インクとして塗布された導電粒子により形成されている、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記導電性インクは、金、銀、白金、インジウム錫酸化物、ポリマー、または炭素により作製されている、請求項99記載のマルチウェルインピーダンス測定装置。
- 前記複数の機能的等価インピーダンス測定電極は、金属層及び導電性インクにより形成されている、請求項71記載のマルチウェルインピーダンス測定装置。
- 前記複数の導電ビアは、金属層及び導電性インクにより形成されている、請求項94記載のマルチウェルインピーダンス測定装置。
- 前記複数の電気接触パッドは、金属層及び導電性インクにより形成されている、請求項94記載のマルチウェルインピーダンス測定装置。
- 前記プレート識別情報を読み取り可能な手段は、光学的に読み取り可能なパターン、電気的に読み取り可能なパターン、機械的パターン、RFIDタグ、またはメモリチップを含む、請求項71記載のマルチウェルインピーダンス測定装置。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11/091,065 US20060216203A1 (en) | 2005-03-28 | 2005-03-28 | Multiwell sample plate with integrated impedance electrodes and connection scheme |
| PCT/US2006/010574 WO2006104839A2 (en) | 2005-03-28 | 2006-03-24 | Multiwell sample plate with integrated impedance electrodes and connection scheme |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008534965A true JP2008534965A (ja) | 2008-08-28 |
| JP2008534965A5 JP2008534965A5 (ja) | 2009-05-14 |
Family
ID=37035384
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008504172A Pending JP2008534965A (ja) | 2005-03-28 | 2006-03-24 | 集積化インピーダンス電極を備えるマルチウェルサンプルプレート及び接続方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20060216203A1 (ja) |
| JP (1) | JP2008534965A (ja) |
| AU (1) | AU2006229917A1 (ja) |
| CA (1) | CA2588447A1 (ja) |
| DE (1) | DE112006000743T5 (ja) |
| GB (1) | GB2435769B (ja) |
| WO (1) | WO2006104839A2 (ja) |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008275456A (ja) * | 2007-04-27 | 2008-11-13 | Atago:Kk | 濃度測定装置 |
| JP2012063287A (ja) * | 2010-09-17 | 2012-03-29 | Hokuto Denko Kk | ウェルユニット及び電気化学的分析方法 |
| JP2016529889A (ja) * | 2013-07-26 | 2016-09-29 | アクシオン バイオシステムズ, インコーポレイテッド | ハイスループット電気生理機能のためのデバイス、システム、及び方法 |
| WO2017154801A1 (ja) * | 2016-03-11 | 2017-09-14 | パナソニックIpマネジメント株式会社 | 電気化学測定システム、電気化学測定装置および電気化学測定方法 |
| JP2018004561A (ja) * | 2016-07-07 | 2018-01-11 | シャープ株式会社 | 被検査体濃度測定方法およびセンサ装置 |
| JP2018059929A (ja) * | 2016-09-30 | 2018-04-12 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | マイクロ流体プレート内部の流体の状態を検出するセンサ、流体を含む試料の調製を制御するシステム、およびマイクロ流体プレート内部の流体の状態を検出する方法 |
| US10067117B2 (en) | 2014-08-12 | 2018-09-04 | Axion Biosystems, Inc. | Cell-based biosensor array and associated methods for manufacturing the same |
| JP2019505180A (ja) * | 2015-12-17 | 2019-02-28 | フリーイェ・ユニヴェルシテイト・ブリュッセルVrije Universieit Brussel | 電気化学インピーダンス分光法を実施するためのシステム及び方法 |
| US10241077B2 (en) | 2015-01-30 | 2019-03-26 | Panasonic Intellectual Property Management Co., Ltd. | Electrochemical measurement device |
| JP7448202B2 (ja) | 2020-06-03 | 2024-03-12 | 国立研究開発法人物質・材料研究機構 | プローブ分子探索装置、及び、プローブ分子の探索方法 |
Families Citing this family (43)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8263375B2 (en) | 2002-12-20 | 2012-09-11 | Acea Biosciences | Dynamic monitoring of activation of G-protein coupled receptor (GPCR) and receptor tyrosine kinase (RTK) in living cells using real-time microelectronic cell sensing technology |
| WO2005047482A2 (en) | 2003-11-12 | 2005-05-26 | Xiao Xu | Real time electronic cell sensing systems and applications for cell-based assays |
| US7560269B2 (en) | 2002-12-20 | 2009-07-14 | Acea Biosciences, Inc. | Real time electronic cell sensing system and applications for cytotoxicity profiling and compound assays |
| US7470533B2 (en) * | 2002-12-20 | 2008-12-30 | Acea Biosciences | Impedance based devices and methods for use in assays |
| US10539523B2 (en) | 2002-12-20 | 2020-01-21 | Acea Biosciences, Inc. | System and method for monitoring cardiomyocyte beating, viability, morphology, and electrophysiological properties |
| US10215748B2 (en) | 2002-12-20 | 2019-02-26 | Acea Biosciences, Inc. | Using impedance-based cell response profiling to identify putative inhibitors for oncogene addicted targets or pathways |
| US10551371B2 (en) | 2003-11-10 | 2020-02-04 | Acea Biosciences, Inc. | System and method for monitoring cardiomyocyte beating, viability and morphology and for screening for pharmacological agents which may induce cardiotoxicity or modulate cardiomyocyte function |
| US11346797B2 (en) | 2002-12-20 | 2022-05-31 | Agilent Technologies, Inc. | System and method for monitoring cardiomyocyte beating, viability, morphology and electrophysiological properties |
| DE102004042729B4 (de) * | 2004-09-03 | 2018-02-01 | Robert Bosch Gmbh | Bio-Chip mit einem Elektrodenarray auf einem Substrat |
| US7411182B2 (en) * | 2006-01-19 | 2008-08-12 | Georgia Tech Research Corp | Reverse-taylor cone ionization systems and methods of use thereof |
| US20070172395A1 (en) * | 2006-01-20 | 2007-07-26 | Applera Corporation | Thermally Conductive Microplate |
| WO2008127429A2 (en) * | 2006-11-21 | 2008-10-23 | Ge Healthcare Bio-Sciences Corp. | Assembling and utilizing rfid sensors in containers |
| US20110220517A1 (en) * | 2008-01-09 | 2011-09-15 | Toto Ltd. | Method for specifically detecting test substance using photocurrent, sensor unit used therefor, and measuring device |
| EP2103933B1 (en) | 2008-02-25 | 2011-07-27 | Universität Leipzig | Device and method for measuring impedance in organotypic tissues |
| EP2291645B1 (en) | 2008-05-05 | 2015-09-09 | Acea Biosciences, Inc. | Label-free monitoring of excitation-contraction coupling and excitable cells using impedance based systems with millisecond time resolution |
| US20110022331A1 (en) * | 2009-07-27 | 2011-01-27 | Meso Scale Technologies, Llc | Assay Information Management Methods and Devices |
| WO2011146531A1 (en) | 2010-05-18 | 2011-11-24 | Acea Biosciences, Inc | Data analysis of impedance-based cardiomyocyte-beating signals as detected on real-time cell analysis (rtca) cardio instruments |
| US20130091890A1 (en) * | 2010-06-28 | 2013-04-18 | Biocision, Llc | Specimen freezing rate regulator device |
| CN108491681A (zh) | 2010-07-27 | 2018-09-04 | 梅索磅秤技术有限公司 | 消耗品数据管理 |
| US10247656B2 (en) * | 2010-09-09 | 2019-04-02 | Children's Hospital & Research Center At Oakland | Single-cell microchamber array |
| WO2012059701A2 (fr) * | 2010-11-05 | 2012-05-10 | Cybio France Sarl | Dispositif et procede de gestion de microplaques dans un systeme de traitement automatise, et procede de traitement de ces microplaques. |
| JP5723197B2 (ja) * | 2011-04-04 | 2015-05-27 | 株式会社エンプラス | 流体取扱装置及び流体取扱システム |
| JP5797926B2 (ja) * | 2011-04-21 | 2015-10-21 | 株式会社エンプラス | 流体取扱装置およびその製造方法ならびに流体取扱システム |
| EP2581742A1 (en) | 2011-10-14 | 2013-04-17 | Universität Leipzig | Device and method for parallel recording of impedance spectra and field potential |
| GB2500658A (en) * | 2012-03-28 | 2013-10-02 | Dna Electronics Ltd | Biosensor device and system |
| AU2014203992B2 (en) * | 2013-01-04 | 2018-03-22 | Meso Scale Technologies, Llc. | Assay apparatuses, methods and reagents |
| GB2531924B (en) * | 2013-03-28 | 2020-04-29 | Indian Council Of Agricultural Res | A device for detection and analysis of mycotoxins |
| US20140368443A1 (en) * | 2013-06-14 | 2014-12-18 | Agilent Technologies, Inc. | System for Automating Laboratory Experiments |
| WO2015078884A1 (en) * | 2013-11-26 | 2015-06-04 | Alleati Ag | Method and microfluidic assembly for antibiotic susceptibility testing |
| EP3234982B1 (en) * | 2014-12-19 | 2019-03-06 | Siemens Healthcare Diagnostics Inc. | Sensor array with anti-diffusion region(s) to extend shelf life |
| EP3351932B1 (en) * | 2015-09-18 | 2020-09-30 | Panasonic Intellectual Property Management Co., Ltd. | Electrochemical measurement device and electrochemical measurement system |
| CN110582569B (zh) | 2017-03-03 | 2024-04-02 | 安捷伦科技有限公司 | 用于iPSC和ESC衍生的心肌细胞的功能成熟的方法和系统 |
| CA3070474A1 (en) * | 2017-08-16 | 2019-02-21 | Amgen Inc. | Adaptive electrode arrangement for implementation in a cell incubator system and applications thereof |
| CN108918635B (zh) * | 2018-05-07 | 2020-06-02 | 清华大学深圳研究生院 | 一种集成生物传感器芯片 |
| EE05830B1 (et) * | 2019-02-08 | 2020-12-15 | Tallinna Tehnikaülikool | Mikrovooluti meetod ja seade |
| DE102019118529A1 (de) * | 2019-07-09 | 2021-01-14 | Hamilton Bonaduz Ag | Impedanzspektroskopie-Sensor mit dichtender Glasur-Deckschicht |
| GB201915480D0 (en) * | 2019-10-25 | 2019-12-11 | Oxford Nanopore Tech Ltd | Improved nanopore sensing device, components and method of manufacture |
| CN110850083B (zh) * | 2019-10-31 | 2023-06-02 | 浙江卫未生物医药科技有限公司 | 一种批量外泌体浓度检测试剂盒及操作方法 |
| CN115151346A (zh) * | 2020-01-24 | 2022-10-04 | 科锐丽亚生物系统公司 | 自动分析物测定系统及与其一起使用的试剂盒 |
| USD941488S1 (en) | 2020-02-07 | 2022-01-18 | Agilent Technologies, Inc. | Instrument for analyzing biological cells |
| DE102020002390A1 (de) * | 2020-04-21 | 2021-10-21 | Innome Gmbh | Anordnung aus Probengefäß und Messelektronikeinheit |
| CA3228270A1 (en) * | 2021-08-13 | 2023-02-16 | Meso Scale Technologies, Llc. | Electrochemical cell devices and methods of manufacturing |
| EP4296351A1 (en) | 2022-06-20 | 2023-12-27 | Dansk Fundamental Metrologi A/S | Non-contact impedance analyzer for real-time detection of microbial growth |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH03122554A (ja) * | 1989-10-06 | 1991-05-24 | Tdk Corp | 電気化学発光検出用容器 |
| JPH04500124A (ja) * | 1988-08-18 | 1992-01-09 | オーストラリアン メンブレイン アンド バイオテクノロジィ リサーチ インスティチュート リミテッド | イオンチャンネル膜バイオセンサーの感受性およびイオン選択性の改善 |
| JPH05322817A (ja) * | 1991-11-19 | 1993-12-07 | Houston Advanced Res Center | 分子を検出する方法および装置 |
| JPH10267887A (ja) * | 1997-01-23 | 1998-10-09 | Daikin Ind Ltd | センサ装置 |
| JP2001133436A (ja) * | 1999-11-01 | 2001-05-18 | Microtec Nition:Kk | マトリックス型電気化学発光用基板 |
| JP2001507805A (ja) * | 1997-10-07 | 2001-06-12 | モトローラ・インコーポレイテッド | 分子受容体の結合現象を電気的に検知するセンサ |
| JP2002202278A (ja) * | 2000-12-28 | 2002-07-19 | Starlite Co Ltd | 試験用装置 |
| JP2003511668A (ja) * | 1999-10-01 | 2003-03-25 | ソフィオン・バイオサイエンス・アクティーゼルスカブ | イオンチャネルの電気生理的性質を測定及び/または監視するための基体及び方法 |
| JP2003529772A (ja) * | 2000-03-30 | 2003-10-07 | インフィネオン テクノロジーズ アクチエンゲゼルシャフト | バイオセンサー、バイオセンサーアレイ、バイオセンサーの電極の製造方法、バイオセンサーの製造方法 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3890201A (en) * | 1974-09-26 | 1975-06-17 | Bactomatic Inc | Multi-chamber impedance measuring module-cap combination |
| US5187096A (en) * | 1991-08-08 | 1993-02-16 | Rensselaer Polytechnic Institute | Cell substrate electrical impedance sensor with multiple electrode array |
| US5708247A (en) * | 1996-02-14 | 1998-01-13 | Selfcare, Inc. | Disposable glucose test strips, and methods and compositions for making same |
| US6599408B1 (en) * | 1998-09-17 | 2003-07-29 | E. I. Du Pont De Nemours And Company | Thick film conductor composition for use in biosensors |
| US20050058990A1 (en) * | 2001-03-24 | 2005-03-17 | Antonio Guia | Biochip devices for ion transport measurement, methods of manufacture, and methods of use |
| EP2420824B1 (en) * | 2001-06-29 | 2018-11-28 | Meso Scale Technologies LLC | Multi-well plate having an array of wells and kit for use in the conduct of an ECL assay |
| GB2386949A (en) * | 2002-03-26 | 2003-10-01 | Sensor Tech Ltd | A multiwell plate for electrochemical detection |
| CN100487133C (zh) * | 2002-07-20 | 2009-05-13 | 艾森生物(杭州)有限公司 | 基于阻抗的检测装置和方法 |
| US7341834B2 (en) * | 2003-12-15 | 2008-03-11 | Geneohn Sciences, Inc. | Multiplexed electrochemical detection system and method |
| WO2005105292A1 (en) * | 2004-04-30 | 2005-11-10 | Gatlik Gmbh | High throughput storage-retrieval and screening platform for research applications based on electro or acoustic sensors |
-
2005
- 2005-03-28 US US11/091,065 patent/US20060216203A1/en not_active Abandoned
-
2006
- 2006-03-24 WO PCT/US2006/010574 patent/WO2006104839A2/en active Application Filing
- 2006-03-24 GB GB0710084A patent/GB2435769B/en not_active Expired - Fee Related
- 2006-03-24 AU AU2006229917A patent/AU2006229917A1/en not_active Abandoned
- 2006-03-24 CA CA002588447A patent/CA2588447A1/en not_active Abandoned
- 2006-03-24 JP JP2008504172A patent/JP2008534965A/ja active Pending
- 2006-03-24 DE DE112006000743T patent/DE112006000743T5/de not_active Withdrawn
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH04500124A (ja) * | 1988-08-18 | 1992-01-09 | オーストラリアン メンブレイン アンド バイオテクノロジィ リサーチ インスティチュート リミテッド | イオンチャンネル膜バイオセンサーの感受性およびイオン選択性の改善 |
| JPH03122554A (ja) * | 1989-10-06 | 1991-05-24 | Tdk Corp | 電気化学発光検出用容器 |
| JPH05322817A (ja) * | 1991-11-19 | 1993-12-07 | Houston Advanced Res Center | 分子を検出する方法および装置 |
| JPH10267887A (ja) * | 1997-01-23 | 1998-10-09 | Daikin Ind Ltd | センサ装置 |
| JP2001507805A (ja) * | 1997-10-07 | 2001-06-12 | モトローラ・インコーポレイテッド | 分子受容体の結合現象を電気的に検知するセンサ |
| JP2003511668A (ja) * | 1999-10-01 | 2003-03-25 | ソフィオン・バイオサイエンス・アクティーゼルスカブ | イオンチャネルの電気生理的性質を測定及び/または監視するための基体及び方法 |
| JP2001133436A (ja) * | 1999-11-01 | 2001-05-18 | Microtec Nition:Kk | マトリックス型電気化学発光用基板 |
| JP2003529772A (ja) * | 2000-03-30 | 2003-10-07 | インフィネオン テクノロジーズ アクチエンゲゼルシャフト | バイオセンサー、バイオセンサーアレイ、バイオセンサーの電極の製造方法、バイオセンサーの製造方法 |
| JP2002202278A (ja) * | 2000-12-28 | 2002-07-19 | Starlite Co Ltd | 試験用装置 |
Cited By (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008275456A (ja) * | 2007-04-27 | 2008-11-13 | Atago:Kk | 濃度測定装置 |
| JP2012063287A (ja) * | 2010-09-17 | 2012-03-29 | Hokuto Denko Kk | ウェルユニット及び電気化学的分析方法 |
| JP2016529889A (ja) * | 2013-07-26 | 2016-09-29 | アクシオン バイオシステムズ, インコーポレイテッド | ハイスループット電気生理機能のためのデバイス、システム、及び方法 |
| US10067117B2 (en) | 2014-08-12 | 2018-09-04 | Axion Biosystems, Inc. | Cell-based biosensor array and associated methods for manufacturing the same |
| US10241077B2 (en) | 2015-01-30 | 2019-03-26 | Panasonic Intellectual Property Management Co., Ltd. | Electrochemical measurement device |
| JP2019505180A (ja) * | 2015-12-17 | 2019-02-28 | フリーイェ・ユニヴェルシテイト・ブリュッセルVrije Universieit Brussel | 電気化学インピーダンス分光法を実施するためのシステム及び方法 |
| US11513089B2 (en) | 2015-12-17 | 2022-11-29 | Vrije Universiteit Brussel | Systems and methods for conducting electrochemical impedance spectroscopy |
| WO2017154801A1 (ja) * | 2016-03-11 | 2017-09-14 | パナソニックIpマネジメント株式会社 | 電気化学測定システム、電気化学測定装置および電気化学測定方法 |
| JPWO2017154801A1 (ja) * | 2016-03-11 | 2019-01-10 | パナソニックIpマネジメント株式会社 | 電気化学測定システム、電気化学測定装置および電気化学測定方法 |
| JP2018004561A (ja) * | 2016-07-07 | 2018-01-11 | シャープ株式会社 | 被検査体濃度測定方法およびセンサ装置 |
| JP2018059929A (ja) * | 2016-09-30 | 2018-04-12 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | マイクロ流体プレート内部の流体の状態を検出するセンサ、流体を含む試料の調製を制御するシステム、およびマイクロ流体プレート内部の流体の状態を検出する方法 |
| JP7448202B2 (ja) | 2020-06-03 | 2024-03-12 | 国立研究開発法人物質・材料研究機構 | プローブ分子探索装置、及び、プローブ分子の探索方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| DE112006000743T5 (de) | 2008-06-05 |
| GB2435769B (en) | 2010-12-01 |
| WO2006104839A2 (en) | 2006-10-05 |
| GB2435769A (en) | 2007-09-05 |
| US20060216203A1 (en) | 2006-09-28 |
| WO2006104839A3 (en) | 2007-10-11 |
| AU2006229917A1 (en) | 2006-10-05 |
| CA2588447A1 (en) | 2006-10-05 |
| GB0710084D0 (en) | 2007-07-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2008534965A (ja) | 集積化インピーダンス電極を備えるマルチウェルサンプルプレート及び接続方法 | |
| US8420313B2 (en) | Multiplexed electrochemical detection system and method | |
| EP2872892B1 (en) | Flexible dna sensor carrier and method | |
| US8562806B2 (en) | Electrochemical biosensor arrays and instruments and methods of making and using same | |
| US7556724B2 (en) | Electrochemical sensor strip and manufacturing method thereof | |
| WO2004001404A1 (en) | Microfabricated sensor arrays | |
| KR20100117173A (ko) | 전기화학적 바이오센서용 전극 스트립 및 그 제조방법 | |
| US11408882B2 (en) | Sensor array | |
| US6126800A (en) | Micro-system with an integrated cuvette for the analysis of liquids | |
| JP2002522749A (ja) | 化学的または生物学的分析マルチポイントマイクロシステム | |
| EP3169992B1 (en) | Sensor array | |
| US6835293B2 (en) | Analysis system | |
| JP5385225B2 (ja) | 生体物質測定装置およびその製造方法 | |
| US20100019782A1 (en) | Cellular potential measurement container | |
| JP2006275724A (ja) | Icタグ搭載型バイオセンサーおよびその包装体 | |
| US20200278313A1 (en) | Sensor assembly and method of using same | |
| Shen et al. | Aqueous and nonaqueous electrochemical sensing on whole-teflon chip | |
| KR100805913B1 (ko) | 일회용 전기 화학 센서 스트립의 구조 및 그 제조 방법 | |
| WO2003027656A2 (en) | Electrochemical control of the redox environment for the analysis of a sample | |
| KR100833389B1 (ko) | 바이오 물질을 검출하는 센서 및 그의 제조 방법 | |
| WO2021094071A1 (en) | An ewod device with sensing apparatus | |
| JP2007232628A (ja) | バイオセンサー |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090324 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090324 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110809 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20111101 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20111109 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120209 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120731 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120921 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120928 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130402 |