JP2007504816A - 細胞、胚または、卵母細胞を取り扱う装置と方法 - Google Patents
細胞、胚または、卵母細胞を取り扱う装置と方法 Download PDFInfo
- Publication number
- JP2007504816A JP2007504816A JP2006525896A JP2006525896A JP2007504816A JP 2007504816 A JP2007504816 A JP 2007504816A JP 2006525896 A JP2006525896 A JP 2006525896A JP 2006525896 A JP2006525896 A JP 2006525896A JP 2007504816 A JP2007504816 A JP 2007504816A
- Authority
- JP
- Japan
- Prior art keywords
- recess
- substrate
- flow
- lid
- fluid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B17/00—Surgical instruments, devices or methods, e.g. tourniquets
- A61B17/42—Gynaecological or obstetrical instruments or methods
- A61B17/425—Gynaecological or obstetrical instruments or methods for reproduction or fertilisation
- A61B17/43—Gynaecological or obstetrical instruments or methods for reproduction or fertilisation for artificial insemination
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B17/00—Surgical instruments, devices or methods, e.g. tourniquets
- A61B17/42—Gynaecological or obstetrical instruments or methods
- A61B17/425—Gynaecological or obstetrical instruments or methods for reproduction or fertilisation
- A61B17/435—Gynaecological or obstetrical instruments or methods for reproduction or fertilisation for embryo or ova transplantation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B17/00—Surgical instruments, devices or methods, e.g. tourniquets
- A61B17/42—Gynaecological or obstetrical instruments or methods
- A61B17/425—Gynaecological or obstetrical instruments or methods for reproduction or fertilisation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61D—VETERINARY INSTRUMENTS, IMPLEMENTS, TOOLS, OR METHODS
- A61D19/00—Instruments or methods for reproduction or fertilisation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61D—VETERINARY INSTRUMENTS, IMPLEMENTS, TOOLS, OR METHODS
- A61D19/00—Instruments or methods for reproduction or fertilisation
- A61D19/02—Instruments or methods for reproduction or fertilisation for artificial insemination
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61D—VETERINARY INSTRUMENTS, IMPLEMENTS, TOOLS, OR METHODS
- A61D19/00—Instruments or methods for reproduction or fertilisation
- A61D19/04—Instruments or methods for reproduction or fertilisation for embryo transplantation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502761—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip specially adapted for handling suspended solids or molecules independently from the bulk fluid flow, e.g. for trapping or sorting beads, for physically stretching molecules
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M21/00—Bioreactors or fermenters specially adapted for specific uses
- C12M21/06—Bioreactors or fermenters specially adapted for specific uses for in vitro fertilization
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M23/00—Constructional details, e.g. recesses, hinges
- C12M23/02—Form or structure of the vessel
- C12M23/12—Well or multiwell plates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M23/00—Constructional details, e.g. recesses, hinges
- C12M23/02—Form or structure of the vessel
- C12M23/16—Microfluidic devices; Capillary tubes
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0647—Handling flowable solids, e.g. microscopic beads, cells, particles
- B01L2200/0668—Trapping microscopic beads
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0684—Venting, avoiding backpressure, avoid gas bubbles
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0809—Geometry, shape and general structure rectangular shaped
- B01L2300/0816—Cards, e.g. flat sample carriers usually with flow in two horizontal directions
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0861—Configuration of multiple channels and/or chambers in a single devices
- B01L2300/0864—Configuration of multiple channels and/or chambers in a single devices comprising only one inlet and multiple receiving wells, e.g. for separation, splitting
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0887—Laminated structure
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5025—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures for parallel transport of multiple samples
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Reproductive Health (AREA)
- Animal Behavior & Ethology (AREA)
- Surgery (AREA)
- Public Health (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Clinical Laboratory Science (AREA)
- Pregnancy & Childbirth (AREA)
- Heart & Thoracic Surgery (AREA)
- Medical Informatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Gynecology & Obstetrics (AREA)
- Transplantation (AREA)
- Genetics & Genomics (AREA)
- Dispersion Chemistry (AREA)
- General Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Sustainable Development (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Fluid Mechanics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Hematology (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Physical Or Chemical Processes And Apparatus (AREA)
Abstract
Description
装置は、多数の胚を、共通な流体状態にさらさせることが可能であると同時に、他の胚への最小限の障害で、個々の胚を選択して取り扱うことができ、
個々のまたは胚のグループを覆う、媒体の素早い交換を可能にすることができ、
ある実施形態では、その場での視覚的評価と選択を可能にするように、卵母細胞の良好な視認性を達成することができ、
胚の環境の制御された状態を維持しながら、搬送または貯蔵のための装置から、所定の閉じ込め構成部材を隔離することができ、
装置の使い捨て部品が、大量に安く作られることを可能にすることができる。
図4aから4hは、図1a〜図1cに従った、基板の一部に形成された凹部構造の部分的な図を示す。図4aの実施形態は、細胞構成要素を受承するようにされた、各々が第二凹部を有する流路52を介して連通する一以上の第一凹部を有する、基板10を有する、流路は、細胞構成要素が、中を通り抜けることができない第一凹部の中に閉じ込められることを目的とするような寸法に作られている。ふた60は、シール面62で基板を閉じて、第一凹部と第二凹部を連通する一以上の流れ流路(64,66)を有している。凹部中の流れのパターンが、ふたの流路の配置によって、決定されるのが、本発明の特徴である。図4aは、紙面の平面に垂直に走っていて、一以上の第一凹部と第二凹部とを連通してもよい、ふた流路の配置を示す。この配置は、図4bの平面図で示されていて、複数の第一凹部50と第二凹部54が、インレット流路64とアウトレット流路66にそれぞれ、平行に接続されている。本実施形態の基板10は、図4cで、ふたは、図4dで示されている。
図4iは、細胞構成要素の保持位置が従来の実施形態よりも、より近接してパックされることができる実施形態を示す。このことは、下位の液体の量全体に、保持位置を取り囲むことを可能にする。ここで、卵母細胞は、基板150中のマイクロ凹部152に保持されて、マイクロ凹部は、前側の流れ流路154と後ろ側の流れ流路156に連通している。前側の流れ流路は、基板150と取り外し可能なふた158との間に形成されていて、取り外されたときに、ピペットによって、卵母細胞を加える、または取り除くために、接近することを可能にする。基板に対して閉じられた位置のときは、図1aの実施形態のように、インレットから、流路154を通ってアウトレットへの流体密封経路を形成する。後ろ側の流路156は、基板と取り外し可能な後ろ側構成要素160との間に、同様に形成されてもよく、あるいは、後ろの構成要素160は、基板に永久に固着されてもよく、または、流路156は、基板自体の中に形成されてもよい。後ろ側の流路は、示されたように、インレットとアウトレットとの間に流れてもよく、また、液体が、どちらの方向にも流れることができる、単一の接続を単に導いてもよい。
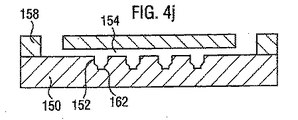
図4j、4kおよび4lは、ここで、凹部のベースから横方向に通じる流路162は、下からの卵母細胞の視認性を、よりよくすることを可能にすることを除いて、図4iの特長に類似した特長を有する更なる実施形態である。図4kは、図4iで番号付けられた部分の平面図を示す。図4jは、卵母細胞凹部を通る図4kのAAでの断面図を示し、図4lは、BBでの断面図を示し、どのように流路162が後ろ側の流れ流路156を妨害するかを示している。
図4mは、卵母細胞を保持するように作用する、その中にくびれを有する基板150に形成された、卵母細胞凹部152の更なる実施形態を示す。凹部は、貯蔵毛管のように作用し、溶媒を満たされたときに、表面張力手段により、溶媒を保持する。基板150は、親水性材料(例えばアクリル)から形成されることができ、凹部の一般的な直径は、1mmよりも小さく、そのため、毛管の保持力は、有効である。卵母細胞は、単に、基板の上面と下面をカバー166と168で覆うことによって、それらの凹部の中に、保持される。これは、卵母細胞を運搬する、非常に簡単で、取り扱うことが簡単な手段を形成する。卵母細胞が、溶媒中で還流された場合には、その後、カバーは、図4nで示されるような流れふた158、160に置き換えられる。インレット流路158を通って、流された液体は、その後、凹部のメニスカスに接触して、溶媒を、凹部を通って流すことを可能にする。メニスカスへの接触と、インレット流路158からの空気の排除は、メニスカスが下側から凹部152の上部に動くように、加えられる圧力によって助けられる。
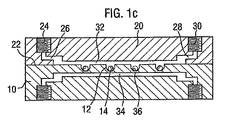
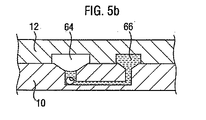
図5a〜5bは、本発明の他の実施形態を示す。図5aでは、第一凹部50は、細胞構成要素を収容するように選択された、直径のベース部分90と、凹部中の液体のピペット操作に適合するように作用するより大きな口部分92を有している。流路52は、第二凹部54に連通し、さらに、ベース部分94と口部分96に連通している。図5bでは、第一および第二流路64と66を有するふた12が取り付けられた、基板が示されている。これらの流路は、図1aの方法で、インレット凹部からアウトレット凹部に流れる。各々の凹部には、より広い口部分とより狭いベース部分の間の接合部分に、毛管ストップがある。基板の材料は、親水材料で用意されていて、そのため、より大きな流路のメニスカスよりも、小さな流路のメニスカスにより大きな圧力が横切る。それゆえ、低圧力でより大きな部分中のメニスカスを動かすのに十分であるが、より小さな部分中のメニスカスを動かすのには、十分ではない。
前の実施形態では、装置は、基板の凹部への流路を備えるためにふたを有している。図6aと図6bは、前の実施形態のように流路手段によって、達成される凹部を通る液体の流れと共に、連続するピペット操作によって、液体を凹部に供給する実施形態を示す。これらの実施形態では、取り外し可能なふたはもはや必要でなく、第一凹部は、開けられたままにでき、処置のすべての段階で、ピペット操作のために、接近可能である。基板10は、凹部流路52に連通する1以上のアウトレット流路66を有する。わずかな負圧が、流路66の液体に加えられ、この圧力は、液体が、インレット凹部の毛管ストップを過ぎるのを強制するのに必要とされる圧力よりも少ない。ピペットが操作され、凹部中に入れられる、各々の一定量のために、溶液は、第一凹部から、流路66に、メニスカスが毛管ストップに到達し、すぐに流れが止まるまで、流れる。凹部を通る流れは、ピペット操作の動作によって制御される。この様に、ピペット操作された体積がベース部分90の体積よりも大きいと、卵母細胞は、最後にピペット操作されたいかなる溶液にも浸される。ピペット操作された体積が、より少ない場合には、ベース部分に混合された溶液が共存し、拡散によって、ゆっくりと混合する。このシステムの時間による、混合の変化を達成するために、凹部中での拡散混合への信頼性が必要である。(卵母細胞を、上部から下部への濃度の変化にさらし、そのため、望ましくないかも知れない)または、一連の一定分量の徐々に変化する濃度に間接的に混合することと、それらを連続的に凹部にピペット操作により入れることが必要である。図6aと6bの実施形態では、卵母細胞は、凹部のベースの位置で保持される。同じ原理が、図6cの実施形態に適用されて、卵母細胞は、凹部のベース部分のくびれ106で保持される。
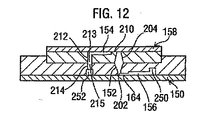
図8と9は、図4oで示されたタイプの更なる実施形態を示し、流れ流路ふたが配置されたときに、卵母細胞、胚、または他の細胞のような1以上の細胞構成要素が、基板上の個々の位置に、確実に保持される。簡単のために、図8の装置は、単一の保持位置を示すが、本発明は、複数のそのような保持位置を有する装置を包含することが理解される。基板(ベース構成要素としてこの例では説明される)150とふた構成要素158は、各々流れシステムを有し、卵母細胞位置を通る流路を完成するように、互いがフィットするように配置され、装置に卵母細胞を乗せる、または、卵母細胞を装置から取り除くために、分離可能なように配置されている。ベース構成要素は、ベースシーリング表面153を有し、ふたは、ふたシーリング表面159を有していて、近接させられるときに、ベースとふたとの間に1以上の液体の経路を完成するように作用する。図8は、ベース上に組立てられたふたを示す。図9は、装置が分解されたときに、2つの構成要素の外観を示すように、ベースから上方に動かされたふたを示す。共通の番号は、図4oと図8と9の共通部分を示す。
Claims (12)
- 第一基板の第一の大きな表面に開口する第一凹部の配列を有する、前記第一基板を有する装置であって、
前記第一凹部は、細胞構成要素を保持するようにされ、
各々の前記凹部に、開口する1以上の流体流路を更に有する、装置。 - 前記凹部は、各々の凹部の所定の位置で、前記細胞構成要素を位置付けるように、先細りされている、請求項1に記載の装置。
- 少なくとも一つの前記一以上の流体流路が、更なる基板の大きな表面と、前記第一基板の大きな表面と、の間に形成されて、前記更なる基板は、前記第一基板に取り外し可能に固定される、請求項1または2に記載の装置。
- 少なくとも一つの前記一以上の流体流路が前記更なる基板の大きな表面と、前記第一基板の大きな表面に形成されていて、前記更なる基板は、前記第一基板に取り外し可能に固定される請求項1または2に記載の装置。
- 少なくとも一つの前記一以上の流体流路は、前記第一基板または更なる基板の本体に形成されていて、前記流路は、他の基板のポートまたは凹部と一直線になる開口部を有していて、前記基板は、前記開口部の周りにシールを提供するようにされた、シーリング面が設けられた、請求項1〜4のいずれか一項に記載の装置。
- 前記一以上の流体流路は、また、前記第一基板の前記第一の大きな表面の一以上の第二の凹部に開口する、請求項1〜5のいずれか一項に記載の装置。
- 前記凹部は、前記基板を通って、基板の更なる大きな面に延びており、前記一以上の流体流路は、前記第一基板の更なる大きな表面に、面するようにされて配置された、更なる基板の大きな表面に形成され、前記更なる基板は、前記第一基板に取り外し可能に固定される、請求項1または2に記載の装置。
- 前記流体流路は、前記第一凹部から横に、配置されていて、前記細胞構成要素は、前記流体流路を観察することなしに、大きな表面に略垂直な、前記第一基板または更なる基板を通して、観察されることができる、請求項1〜7のいずれか一項に記載の装置。
- 一つの基板の前記開口部と、他の基板のポートまたは凹部は、流体流路を満たしたときに、流体の溶媒に、気泡が閉じ込められることを避けるために、大きな表面から距離とともに小さくなるように、先細りにされている、請求項1〜8のいずれか一項に記載の装置。
- 一以上の流体流路は、流体で満たされたときに、前記流体流路からガスポケット(gas pockets)または気泡を取り除くことを可能にする、ガス浸透可能領域が設けられた、請求項1〜9のいずれか一項に記載の装置。
- 前記第一基板と更なる基板を一直線に保持し、それらを互いに係合させる、クランプ手段を含む、請求項1〜10のいずれか一項に記載の装置。
- 請求項1〜11のいずれか一項に記載の装置と、他の細胞構成要素取り扱い手段を含む、細胞構成要素取り扱いシステム。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0321158.8A GB0321158D0 (en) | 2003-09-10 | 2003-09-10 | Apparatus and method for handling cells,embryos or oocytes |
| PCT/GB2004/003886 WO2005023124A2 (en) | 2003-09-10 | 2004-09-10 | Apparatus for handling cells, embryos or oocytes |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2007504816A true JP2007504816A (ja) | 2007-03-08 |
Family
ID=29226804
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006525896A Ceased JP2007504816A (ja) | 2003-09-10 | 2004-09-10 | 細胞、胚または、卵母細胞を取り扱う装置と方法 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US20070264705A1 (ja) |
| EP (1) | EP1667589B8 (ja) |
| JP (1) | JP2007504816A (ja) |
| KR (1) | KR20070033946A (ja) |
| CN (1) | CN1909847A (ja) |
| AT (1) | ATE449572T1 (ja) |
| AU (1) | AU2004269976B2 (ja) |
| BR (1) | BRPI0413949A (ja) |
| CA (1) | CA2538379C (ja) |
| DE (1) | DE602004024319D1 (ja) |
| GB (1) | GB0321158D0 (ja) |
| IL (1) | IL174233A0 (ja) |
| NZ (1) | NZ546464A (ja) |
| WO (1) | WO2005023124A2 (ja) |
Cited By (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009511083A (ja) * | 2005-10-18 | 2009-03-19 | ザ リージェンツ オブ ザ ユニバーシティ オブ ミシガン | マイクロ流体細胞培養デバイスおよびその使用方法 |
| WO2009069819A1 (en) | 2007-11-30 | 2009-06-04 | Canon Kabushiki Kaisha | Living body holding method, living body test method, living body growing method, living body holding sheet, and living body processing device |
| JP2010536348A (ja) * | 2007-08-24 | 2010-12-02 | スマート・バイオシステムズ・エーピーエス | 灌流のための中規模バイオリアクタープラットフォーム |
| JP2010273654A (ja) * | 2009-05-29 | 2010-12-09 | Canon Inc | 物体保持用シート、試験方法及び物体処理装置 |
| US20100323439A1 (en) * | 2005-10-18 | 2010-12-23 | The Regents Of The University Of Michigan | Microfluidic cell culture device |
| JP2012185008A (ja) * | 2011-03-04 | 2012-09-27 | Research Institute Of Biomolecule Metrology Co Ltd | 細胞アッセイ用流路チップ及び検査装置 |
| JP2012529896A (ja) * | 2009-06-16 | 2012-11-29 | ユニバーシテイト レイデン | 生物学的マイクロ流体工学チップおよび関連する方法 |
| JP2013074822A (ja) * | 2011-09-30 | 2013-04-25 | Teruo Fujii | 生物学的対象物の分化制御方法及びその装置 |
| WO2013093961A1 (ja) * | 2011-12-20 | 2013-06-27 | ヤマハ発動機株式会社 | 対象物選別装置および対象物選別方法 |
| JP2014090703A (ja) * | 2012-11-06 | 2014-05-19 | Nissha Printing Co Ltd | 細胞培養担体とその製造方法 |
| JP2014155471A (ja) * | 2013-02-18 | 2014-08-28 | Univ Of Tokyo | 血小板産生流路装置及び血小板産生方法 |
| JP2015528574A (ja) * | 2011-09-14 | 2015-09-28 | ザ ユニバーシティ オブ クィーンズランド | 物質曝露装置 |
| JP2015186474A (ja) * | 2014-03-13 | 2015-10-29 | アークレイ株式会社 | 細胞培養方法、細胞培養部材、及び細胞培養装置 |
| WO2016047751A1 (ja) * | 2014-09-25 | 2016-03-31 | 住友ベークライト株式会社 | 培養容器 |
| JPWO2014007190A1 (ja) * | 2012-07-03 | 2016-06-02 | コニカミノルタ株式会社 | 細胞展開用デバイスおよび希少細胞の検出方法 |
| JP2016163549A (ja) * | 2015-03-06 | 2016-09-08 | 学校法人 中央大学 | マイクロウェルプレート、マイクロウェル装置、細胞解析方法及びマイクロウェルプレートの製造方法 |
| JP2016163591A (ja) * | 2016-06-14 | 2016-09-08 | ヤマハ発動機株式会社 | プレート |
| US10138452B2 (en) | 2014-08-05 | 2018-11-27 | Yamaha Hatsudoki Kabushiki Kaisha | Object-holding device |
| JP2019505761A (ja) * | 2015-12-01 | 2019-02-28 | イラミーナ インコーポレーテッド | 単一細胞の単離および分析物の特徴付けのためのデジタルマイクロ流体システム |
| JPWO2018163687A1 (ja) * | 2017-03-10 | 2019-03-14 | 日本精工株式会社 | マニピュレーションシステム |
Families Citing this family (65)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0120645D0 (en) | 2001-08-24 | 2001-10-17 | Smiths Group Plc | Medico-surgical devices |
| AT500427B1 (de) * | 2002-05-29 | 2009-02-15 | Anagnostics Bioanalysis Gmbh | Vorrichtung zur analyse von bestandteilen einer probe |
| GB0307350D0 (en) | 2003-03-29 | 2003-05-07 | Smiths Group Plc | Catheters |
| US9637715B2 (en) | 2005-07-07 | 2017-05-02 | Emd Millipore Corporation | Cell culture and invasion assay method and system |
| US8257964B2 (en) | 2006-01-04 | 2012-09-04 | Cell ASIC | Microwell cell-culture device and fabrication method |
| US9354156B2 (en) | 2007-02-08 | 2016-05-31 | Emd Millipore Corporation | Microfluidic particle analysis method, device and system |
| EP1904619A4 (en) * | 2005-07-07 | 2012-05-02 | Univ California | METHOD AND DEVICE FOR CELL CULTURE ARRAY |
| US9388374B2 (en) | 2005-07-07 | 2016-07-12 | Emd Millipore Corporation | Microfluidic cell culture systems |
| EP1772722A1 (de) * | 2005-10-07 | 2007-04-11 | Micronas Holding GmbH | Reaktionskammer |
| AT502549B1 (de) * | 2005-10-07 | 2007-06-15 | Anagnostics Bioanalysis Gmbh | Vorrichtung zur analyse von flüssigen proben |
| WO2008106771A1 (en) * | 2007-03-02 | 2008-09-12 | Mark Ungrin | Devices and methods for production of cell aggregates |
| TW200920841A (en) * | 2007-09-25 | 2009-05-16 | Cytyc Corp | Microfluidic apparatus for manipulating imaging and analyzing cells of a cytological specimen |
| WO2009075016A1 (ja) * | 2007-12-10 | 2009-06-18 | Shimadzu Corporation | 微小液滴操作デバイス及びそれを用いた反応処理方法 |
| EP2245453B1 (en) | 2008-01-03 | 2016-10-05 | EMD Millipore Corporation | Microfluidic cell culture array system for automated assays and methods of operation |
| AU2009271203A1 (en) * | 2008-07-16 | 2010-01-21 | Vance Products Incorporated, D/B/A Cook Urological Incorporated | Micro-fluidic cell manipulation and holding device |
| CN102112593A (zh) * | 2008-08-01 | 2011-06-29 | 智能生物系统公司 | 生物反应器平台的腔室 |
| CN101827931A (zh) * | 2008-08-29 | 2010-09-08 | 北京大学 | 用于可准确控制的细胞培养的微流体芯片 |
| US20100075411A1 (en) * | 2008-09-22 | 2010-03-25 | Cecchi Michael D | Specimen manipulation device for micro manipulation and biopsy in assisted reproduction and in vitro fertilization |
| IT1391619B1 (it) * | 2008-11-04 | 2012-01-11 | Silicon Biosystems Spa | Metodo per l'individuazione, selezione e analisi di cellule tumorali |
| US20110229961A1 (en) * | 2008-11-05 | 2011-09-22 | Nanopoint, Inc. | Active microfluidic system for in vitro culture |
| GB0821636D0 (en) * | 2008-11-26 | 2008-12-31 | Ucl Business Plc | Device |
| IT1392842B1 (it) | 2008-12-29 | 2012-03-23 | St Microelectronics Rousset | Microreattore con canali di sfiato per rimuovere aria da una camera di reazione |
| EP2408900B1 (en) * | 2009-03-20 | 2018-01-10 | International Business Machines Corporation | Microorganism culture device and method of operation thereof |
| GB0909923D0 (en) * | 2009-06-09 | 2009-07-22 | Oxford Gene Tech Ip Ltd | Picowell capture devices for analysing single cells or other particles |
| US9353342B2 (en) | 2010-01-21 | 2016-05-31 | Emd Millipore Corporation | Cell culture and gradient migration assay methods and devices |
| US20110312739A1 (en) * | 2010-06-17 | 2011-12-22 | Geneasys Pty Ltd | Single-use test module for pcr amplification of targets and electrochemiluminescent detection of targets |
| CN101947124B (zh) * | 2010-06-25 | 2012-07-04 | 博奥生物有限公司 | 一种集成式微流控芯片装置及其使用方法 |
| CN102580794B (zh) | 2011-01-13 | 2014-03-19 | 博奥生物有限公司 | 可定位细胞及生物体的微流控芯片及其应用 |
| US10526572B2 (en) | 2011-04-01 | 2020-01-07 | EMD Millipore Corporaticn | Cell culture and invasion assay method and system |
| CN102242055B (zh) | 2011-06-03 | 2013-08-14 | 博奥生物有限公司 | 一种精子活力评价及筛选的方法及其专用微流控芯片装置 |
| US10466160B2 (en) | 2011-08-01 | 2019-11-05 | Celsee Diagnostics, Inc. | System and method for retrieving and analyzing particles |
| US9404864B2 (en) | 2013-03-13 | 2016-08-02 | Denovo Sciences, Inc. | System for imaging captured cells |
| CA2842359A1 (en) | 2011-08-01 | 2013-02-07 | Denovo Sciences | Cell capture system and method of use |
| WO2013030155A1 (en) * | 2011-08-26 | 2013-03-07 | Imec | A micro-fluidic device for sorting particles, and methods for sorting particles |
| CN104245917B (zh) | 2011-12-03 | 2017-07-21 | Emd密理博公司 | 用于微流体细胞培养的微型培育系统和方法 |
| WO2013126556A1 (en) * | 2012-02-21 | 2013-08-29 | Indiana University Research And Technology Corporation | Ultrahigh throughput microinjection device |
| ES2725825T3 (es) | 2012-04-16 | 2019-09-27 | Univ Cornell | Sistema de fertilización asistida por inyección de esperma intracitoplasmática automatizada |
| US9914968B2 (en) | 2012-09-26 | 2018-03-13 | Cepheid | Honeycomb tube |
| US9752181B2 (en) | 2013-01-26 | 2017-09-05 | Denovo Sciences, Inc. | System and method for capturing and analyzing cells |
| CN105283248B (zh) * | 2013-05-07 | 2018-02-06 | 基因细胞生物系统有限公司 | 稳固特征件 |
| US9856535B2 (en) | 2013-05-31 | 2018-01-02 | Denovo Sciences, Inc. | System for isolating cells |
| US10391490B2 (en) | 2013-05-31 | 2019-08-27 | Celsee Diagnostics, Inc. | System and method for isolating and analyzing cells |
| CA3004596C (en) * | 2014-11-11 | 2021-07-27 | Aim Biotech Pte. Ltd. | Microfluidic platform for investigating cell-based interactions |
| GB201506445D0 (en) * | 2015-04-16 | 2015-06-03 | Insphero Ag | System for propagating cells |
| EP3377224A1 (en) | 2015-11-20 | 2018-09-26 | Koninklijke Philips N.V. | Microfluidic device possessing structures enabling differential analysis of a single cell's constituents |
| US20170191912A1 (en) | 2016-01-06 | 2017-07-06 | International Business Machines Corporation | Semiconductor manufactured nano-structures for microbe or virus trapping or destruction |
| US20170333901A1 (en) * | 2016-05-17 | 2017-11-23 | City University Of Hong Kong | Cell-trapping device, apparatus comprising it and their use for microinjection into cells |
| EP3472301B1 (en) * | 2016-06-15 | 2023-08-02 | Mimetas B.V. | Cell culture device and methods |
| PT3321681T (pt) | 2016-11-09 | 2021-12-02 | Univ Macau | Sistema de triagem microfluídica e método de utilização |
| CN113916850A (zh) | 2016-11-17 | 2022-01-11 | 伯乐实验室有限公司 | 用于回收和分析粒子的系统和方法 |
| WO2018132610A1 (en) * | 2017-01-13 | 2018-07-19 | Cellular Research, Inc. | Hydrophilic coating of fluidic channels |
| CN106885807B (zh) * | 2017-02-21 | 2020-04-24 | 澳门大学 | 基于微流控技术的大规模活生物体筛选系统 |
| AU2018323449B2 (en) | 2017-08-29 | 2020-09-03 | Bio-Rad Laboratories, Inc. | System and method for isolating and analyzing cells |
| EP3693453B1 (en) * | 2017-10-03 | 2024-03-13 | Nok Corporation | Cell capturing device |
| CN107926766B (zh) * | 2017-10-17 | 2023-07-14 | 杭州晶雁电子科技有限公司 | 一种自动移动的方法 |
| US20190376013A1 (en) * | 2018-06-11 | 2019-12-12 | The University Of Chicago | Microfluidic devices, systems, and methods for investigating three-dimensional cellular structures |
| WO2020069290A1 (en) | 2018-09-28 | 2020-04-02 | Overture Life, Inc. | In vitro fertilization system and components associated therewith |
| US10633693B1 (en) | 2019-04-16 | 2020-04-28 | Celsee Diagnostics, Inc. | System and method for leakage control in a particle capture system |
| CA3138881A1 (en) | 2019-05-07 | 2020-11-12 | Bio-Rad Laboratories, Inc. | System and method for automated single cell processing |
| US11273439B2 (en) | 2019-05-07 | 2022-03-15 | Bio-Rad Laboratories, Inc. | System and method for target material retrieval from microwells |
| TR201909710A2 (tr) * | 2019-06-28 | 2021-01-21 | Koc Ueniversitesi | Üç boyutlu bi̇r mi̇kroçevrede hücreleri̇n kültüre edi̇lmeleri̇ni̇ sağlamak i̇çi̇n bi̇r mi̇kroakişkan platform |
| CN110591915A (zh) * | 2019-09-30 | 2019-12-20 | 北京工业大学 | 一种基于微流控的卵细胞培养装置 |
| US11856947B2 (en) | 2020-02-17 | 2024-01-02 | Cook Medical Technologies Llc | System for automated permeation of a biological material and method of using same |
| WO2022032094A1 (en) | 2020-08-07 | 2022-02-10 | Overture Life, Inc. | Microfluidic devices and methods for delivering solutions to biological material |
| EP4227398A1 (en) * | 2020-10-06 | 2023-08-16 | Riken | Method for detecting target substance, fluid device, and kit |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5931685A (ja) * | 1982-05-10 | 1984-02-20 | バル−イラン・ユニバシテイ− | 細胞を選別するための装置および方法 |
| WO2001048474A1 (en) * | 1999-12-24 | 2001-07-05 | Astrazeneca Ab | Apparatus for and method of making electrical measurements on objects |
| WO2001088087A2 (en) * | 2000-05-12 | 2001-11-22 | The Board Of Trustees Of The University Of Illinois | Microfluidic channel embryo and/or oocyte handling, analysis and biological evaluation |
| JP2003520574A (ja) * | 1999-07-21 | 2003-07-08 | ザ・レジェンツ・オブ・ザ・ユニバーシティー・オブ・カリフォルニア | エレクトロポレーションを制御するための電気インピーダンストモグラフィ |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5726026A (en) | 1992-05-01 | 1998-03-10 | Trustees Of The University Of Pennsylvania | Mesoscale sample preparation device and systems for determination and processing of analytes |
| US6168948B1 (en) * | 1995-06-29 | 2001-01-02 | Affymetrix, Inc. | Miniaturized genetic analysis systems and methods |
| US6132685A (en) * | 1998-08-10 | 2000-10-17 | Caliper Technologies Corporation | High throughput microfluidic systems and methods |
| US6193647B1 (en) * | 1999-04-08 | 2001-02-27 | The Board Of Trustees Of The University Of Illinois | Microfluidic embryo and/or oocyte handling device and method |
| US6281029B1 (en) * | 1999-09-30 | 2001-08-28 | Advanced Micro Devices, Inc. | Probe points for heat dissipation during testing of flip chip IC |
| JP3738899B2 (ja) * | 2000-12-07 | 2006-01-25 | 株式会社 エフェクター細胞研究所 | 微量試料処理装置 |
| US6729352B2 (en) * | 2001-06-07 | 2004-05-04 | Nanostream, Inc. | Microfluidic synthesis devices and methods |
-
2003
- 2003-09-10 GB GBGB0321158.8A patent/GB0321158D0/en not_active Ceased
-
2004
- 2004-09-10 EP EP04768433A patent/EP1667589B8/en not_active Not-in-force
- 2004-09-10 WO PCT/GB2004/003886 patent/WO2005023124A2/en active Application Filing
- 2004-09-10 JP JP2006525896A patent/JP2007504816A/ja not_active Ceased
- 2004-09-10 CN CNA2004800330491A patent/CN1909847A/zh active Pending
- 2004-09-10 AU AU2004269976A patent/AU2004269976B2/en not_active Ceased
- 2004-09-10 US US10/571,575 patent/US20070264705A1/en not_active Abandoned
- 2004-09-10 CA CA2538379A patent/CA2538379C/en not_active Expired - Fee Related
- 2004-09-10 KR KR1020067006679A patent/KR20070033946A/ko active IP Right Grant
- 2004-09-10 AT AT04768433T patent/ATE449572T1/de not_active IP Right Cessation
- 2004-09-10 BR BRPI0413949-6A patent/BRPI0413949A/pt not_active IP Right Cessation
- 2004-09-10 DE DE602004024319T patent/DE602004024319D1/de active Active
- 2004-09-10 NZ NZ546464A patent/NZ546464A/en unknown
-
2006
- 2006-03-09 IL IL174233A patent/IL174233A0/en unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5931685A (ja) * | 1982-05-10 | 1984-02-20 | バル−イラン・ユニバシテイ− | 細胞を選別するための装置および方法 |
| JP2003520574A (ja) * | 1999-07-21 | 2003-07-08 | ザ・レジェンツ・オブ・ザ・ユニバーシティー・オブ・カリフォルニア | エレクトロポレーションを制御するための電気インピーダンストモグラフィ |
| WO2001048474A1 (en) * | 1999-12-24 | 2001-07-05 | Astrazeneca Ab | Apparatus for and method of making electrical measurements on objects |
| WO2001088087A2 (en) * | 2000-05-12 | 2001-11-22 | The Board Of Trustees Of The University Of Illinois | Microfluidic channel embryo and/or oocyte handling, analysis and biological evaluation |
Cited By (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009511083A (ja) * | 2005-10-18 | 2009-03-19 | ザ リージェンツ オブ ザ ユニバーシティ オブ ミシガン | マイクロ流体細胞培養デバイスおよびその使用方法 |
| US20100323439A1 (en) * | 2005-10-18 | 2010-12-23 | The Regents Of The University Of Michigan | Microfluidic cell culture device |
| US8865464B2 (en) | 2005-10-18 | 2014-10-21 | The Regents Of The University Of Michigan | Microfluidic cell culture device |
| JP2010536348A (ja) * | 2007-08-24 | 2010-12-02 | スマート・バイオシステムズ・エーピーエス | 灌流のための中規模バイオリアクタープラットフォーム |
| WO2009069819A1 (en) | 2007-11-30 | 2009-06-04 | Canon Kabushiki Kaisha | Living body holding method, living body test method, living body growing method, living body holding sheet, and living body processing device |
| US9127245B2 (en) | 2007-11-30 | 2015-09-08 | Canon Kabushiki Kaisha | Living body holding method, living body test method, living body growing method, living body holding sheet, and living body processing device |
| JP2010273654A (ja) * | 2009-05-29 | 2010-12-09 | Canon Inc | 物体保持用シート、試験方法及び物体処理装置 |
| JP2012529896A (ja) * | 2009-06-16 | 2012-11-29 | ユニバーシテイト レイデン | 生物学的マイクロ流体工学チップおよび関連する方法 |
| JP2012185008A (ja) * | 2011-03-04 | 2012-09-27 | Research Institute Of Biomolecule Metrology Co Ltd | 細胞アッセイ用流路チップ及び検査装置 |
| US9931629B2 (en) | 2011-09-14 | 2018-04-03 | The University Of Queensland | Substance exposure apparatus |
| JP2015528574A (ja) * | 2011-09-14 | 2015-09-28 | ザ ユニバーシティ オブ クィーンズランド | 物質曝露装置 |
| JP2013074822A (ja) * | 2011-09-30 | 2013-04-25 | Teruo Fujii | 生物学的対象物の分化制御方法及びその装置 |
| JPWO2013093961A1 (ja) * | 2011-12-20 | 2015-04-27 | ヤマハ発動機株式会社 | 対象物選別装置および対象物選別方法 |
| WO2013093961A1 (ja) * | 2011-12-20 | 2013-06-27 | ヤマハ発動機株式会社 | 対象物選別装置および対象物選別方法 |
| JPWO2014007190A1 (ja) * | 2012-07-03 | 2016-06-02 | コニカミノルタ株式会社 | 細胞展開用デバイスおよび希少細胞の検出方法 |
| US10584367B2 (en) | 2012-07-03 | 2020-03-10 | Konica Minolta, Inc. | Cell-spreading device and method for detecting rare cell |
| JP2014090703A (ja) * | 2012-11-06 | 2014-05-19 | Nissha Printing Co Ltd | 細胞培養担体とその製造方法 |
| JP2014155471A (ja) * | 2013-02-18 | 2014-08-28 | Univ Of Tokyo | 血小板産生流路装置及び血小板産生方法 |
| JP2015186474A (ja) * | 2014-03-13 | 2015-10-29 | アークレイ株式会社 | 細胞培養方法、細胞培養部材、及び細胞培養装置 |
| US10138452B2 (en) | 2014-08-05 | 2018-11-27 | Yamaha Hatsudoki Kabushiki Kaisha | Object-holding device |
| WO2016047751A1 (ja) * | 2014-09-25 | 2016-03-31 | 住友ベークライト株式会社 | 培養容器 |
| JP2016163549A (ja) * | 2015-03-06 | 2016-09-08 | 学校法人 中央大学 | マイクロウェルプレート、マイクロウェル装置、細胞解析方法及びマイクロウェルプレートの製造方法 |
| JP2019505761A (ja) * | 2015-12-01 | 2019-02-28 | イラミーナ インコーポレーテッド | 単一細胞の単離および分析物の特徴付けのためのデジタルマイクロ流体システム |
| JP2016163591A (ja) * | 2016-06-14 | 2016-09-08 | ヤマハ発動機株式会社 | プレート |
| JPWO2018163687A1 (ja) * | 2017-03-10 | 2019-03-14 | 日本精工株式会社 | マニピュレーションシステム |
| US11235317B2 (en) | 2017-03-10 | 2022-02-01 | Nsk Ltd. | Tubular instrument and manipulation system |
Also Published As
| Publication number | Publication date |
|---|---|
| DE602004024319D1 (de) | 2010-01-07 |
| AU2004269976B2 (en) | 2010-08-05 |
| US20070264705A1 (en) | 2007-11-15 |
| EP1667589B1 (en) | 2009-11-25 |
| NZ546464A (en) | 2009-10-30 |
| WO2005023124A2 (en) | 2005-03-17 |
| BRPI0413949A (pt) | 2006-10-24 |
| GB0321158D0 (en) | 2003-10-08 |
| EP1667589B8 (en) | 2010-05-26 |
| ATE449572T1 (de) | 2009-12-15 |
| CA2538379A1 (en) | 2005-03-17 |
| AU2004269976A1 (en) | 2005-03-17 |
| KR20070033946A (ko) | 2007-03-27 |
| CN1909847A (zh) | 2007-02-07 |
| IL174233A0 (en) | 2006-08-01 |
| CA2538379C (en) | 2011-01-04 |
| EP1667589A2 (en) | 2006-06-14 |
| WO2005023124A3 (en) | 2005-04-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2007504816A (ja) | 細胞、胚または、卵母細胞を取り扱う装置と方法 | |
| US20110236970A1 (en) | Chamber of a bioreactor platform | |
| US9739699B2 (en) | Device for the study of living cells | |
| US8709790B2 (en) | Valved, microwell cell-culture device and method | |
| JP5028091B2 (ja) | 結晶形成デバイスならびに結晶形成デバイスを作製および使用するためのシステムおよび方法 | |
| US20110104730A1 (en) | Mesoscale bioreactor platform for perfusion | |
| US20100159590A1 (en) | Systems and methods for active microfluidic cell handling | |
| US20110229927A1 (en) | Sample port of a cell culture system | |
| WO2010053951A1 (en) | Active microfluidic system for in vitro culture | |
| JP2007529015A5 (ja) | ||
| CN1980742A (zh) | 对微阵列和其他微型装置进行高浓度点沉积的点样装置及方法 | |
| WO2006097749A1 (en) | Fluidic devices for cell and embryo culture | |
| US9975118B2 (en) | Device for the study of living cells | |
| US7278210B2 (en) | Method for producing a 3-D microscope flow-through cell | |
| JP5892589B2 (ja) | マイクロデバイス及びバイオアッセイシステム | |
| US20210340478A1 (en) | Cell culture chip and making the same | |
| MXPA06002797A (en) | Apparatus for handling cells, embryos or oocytes | |
| JP2020115781A (ja) | 細胞培養チップ | |
| Pearce et al. | Open environment micro device for integration of patch clamp instrumentation with targeted microfluidic chemical delivery | |
| JP2015027266A (ja) | マイクロデバイス及びバイオアッセイシステム |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070910 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20100624 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100727 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20101026 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20101102 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110127 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20111011 |
|
| A045 | Written measure of dismissal of application [lapsed due to lack of payment] |
Free format text: JAPANESE INTERMEDIATE CODE: A045 Effective date: 20120228 |