JP2007167828A - 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム - Google Patents
一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム Download PDFInfo
- Publication number
- JP2007167828A JP2007167828A JP2005373085A JP2005373085A JP2007167828A JP 2007167828 A JP2007167828 A JP 2007167828A JP 2005373085 A JP2005373085 A JP 2005373085A JP 2005373085 A JP2005373085 A JP 2005373085A JP 2007167828 A JP2007167828 A JP 2007167828A
- Authority
- JP
- Japan
- Prior art keywords
- carbon monoxide
- gas
- catalyst
- raw material
- concentration
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/50—Fuel cells
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/52—Improvements relating to the production of bulk chemicals using catalysts, e.g. selective catalysts
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P70/00—Climate change mitigation technologies in the production process for final industrial or consumer products
- Y02P70/50—Manufacturing or production processes characterised by the final manufactured product
Landscapes
- Hydrogen, Water And Hydrids (AREA)
- Catalysts (AREA)
- Fuel Cell (AREA)
Abstract
【課題】一酸化炭素および水素を含有する原料ガス中の一酸化炭素を選択的に酸化して一酸化炭素濃度を低減するための触媒を提供する。
【解決手段】アルミナ担体に少なくともルテニウム酸カリウムを含有する溶液を接触させることにより得られる、アルミナ担体にルテニウムとルテニウム以外の少なくとも1種の白金族元素を担持して成り、かつカリウム含有量が1000質量ppm以下であることを特徴とする水素および一酸化炭素を含有する原料ガス中の一酸化炭素を選択的に酸化するための触媒。
【選択図】図1
【解決手段】アルミナ担体に少なくともルテニウム酸カリウムを含有する溶液を接触させることにより得られる、アルミナ担体にルテニウムとルテニウム以外の少なくとも1種の白金族元素を担持して成り、かつカリウム含有量が1000質量ppm以下であることを特徴とする水素および一酸化炭素を含有する原料ガス中の一酸化炭素を選択的に酸化するための触媒。
【選択図】図1
Description
本発明は一酸化炭素および水素を含有する原料ガス中の一酸化炭素を選択的に酸化して、一酸化炭素濃度を低減するための触媒、該触媒を用いて一酸化炭素濃度を低減する方法および高濃度水素含有ガスを製造する装置並びに該装置を用いた燃料電池システムに関する。
燃料電池は燃料の燃焼反応による自由エネルギー変化を直接電気エネルギーとして取り出せるため、高い効率が得られるという特徴がある。さらに有害物質を排出しないことも相俟って、様々な用途への展開が図られている。特に固体高分子形燃料電池は、出力密度が高く、コンパクトで、しかも低温で作動するのが特徴である。
一般的に燃料電池用の燃料ガスとしては水素を主成分とするガスが用いられるが、その原料には天然ガス、LPG、ナフサ、灯油等の炭化水素、メタノール、エタノール等のアルコール、およびジメチルエーテル等のエーテル等が用いられる。
しかし、これらの原料中には水素以外の元素も存在するため、燃料電池への燃料ガス中に炭素由来の不純物が混入することは避けられない。中でも一酸化炭素は燃料電池の電極触媒として使われている白金系貴金属を被毒するため、燃料ガス中に一酸化炭素が存在すると充分な発電特性が得られなくなる。特に低温作動させる燃料電池ほど一酸化炭素吸着は強く、被毒を受けやすい。このため固体高分子型燃料電池を用いたシステムでは燃料ガス中の一酸化炭素の濃度が低減されていることが必要不可欠である。
しかし、これらの原料中には水素以外の元素も存在するため、燃料電池への燃料ガス中に炭素由来の不純物が混入することは避けられない。中でも一酸化炭素は燃料電池の電極触媒として使われている白金系貴金属を被毒するため、燃料ガス中に一酸化炭素が存在すると充分な発電特性が得られなくなる。特に低温作動させる燃料電池ほど一酸化炭素吸着は強く、被毒を受けやすい。このため固体高分子型燃料電池を用いたシステムでは燃料ガス中の一酸化炭素の濃度が低減されていることが必要不可欠である。
一酸化炭素濃度を低減させる方法としては、原料を改質して得られた改質ガス中の一酸化炭素を水蒸気と反応させ、水素と二酸化炭素に転化する方法、いわゆる水性ガスシフト反応を用いることが考えられるが、通常、この方法では0.5〜1vol%程度までしか一酸化炭素濃度を低減することができない。しかし、燃料電池電極に用いられる触媒の一酸化炭素耐性は用いられる金属種にも依るが、燃料電池が効率よく作動するためには燃料ガス中の一酸化炭素濃度は100volppm以下であることが望ましく、水性ガスシフト反応のみでは不充分である。
そこで、水性ガスシフト反応により0.5〜1vol%程度にまで下げた一酸化炭素濃度をさらに低減することが求められる。
そこで、水性ガスシフト反応により0.5〜1vol%程度にまで下げた一酸化炭素濃度をさらに低減することが求められる。
一酸化炭素濃度をさらに低減する方法としては、一酸化炭素を吸着分離する方法や膜分離する方法が考えられる。しかし、これらの方法では得られる水素純度は高いものの、装置コストが高く、装置サイズも大きくなるという問題があり、現実的でない。
これに対し化学的な方法はより現実的な方法である。化学的方法としては、一酸化炭素をメタン化する方法、酸化して二酸化炭素に転化する方法などが考えられる。また、前段でメタン化し、後段で酸化する二段階処理方法も提案されている(特許文献1参照)。
特開平11−86892号公報
これに対し化学的な方法はより現実的な方法である。化学的方法としては、一酸化炭素をメタン化する方法、酸化して二酸化炭素に転化する方法などが考えられる。また、前段でメタン化し、後段で酸化する二段階処理方法も提案されている(特許文献1参照)。
しかし、一酸化炭素をメタン化する方法では燃料電池の燃料となる水素をロスすることから、効率的には適当ではない。前記二段階処理方法においても、前段での水素のロスは避けられない。従って、一酸化炭素を酸化して二酸化炭素とする方法を採用するのが適当である。この方法においてポイントとなるのは、大過剰に存在する水素中に微量ないし少量混在する一酸化炭素を如何にして選択的に酸化処理できるかである。
本発明者らはかかる課題について鋭意研究した結果、本発明を完成したものである
本発明者らはかかる課題について鋭意研究した結果、本発明を完成したものである
すなわち、本発明の第1は、アルミナ担体に少なくともルテニウム酸カリウムを含有する溶液を接触させることにより得られる、アルミナ担体にルテニウムとルテニウム以外の少なくとも1種の白金族元素を担持して成り、かつカリウム含有量が1000質量ppm以下であることを特徴とする水素および一酸化炭素を含有する原料ガス中の一酸化炭素を選択的に酸化するための触媒に関する。
本発明の第1においては、触媒全量基準で、ルテニウムを0.05〜2質量%および白金を0.0002〜0.5質量%含むことが好ましい。
また本発明の第1においては、ルテニウム酸カリウムと塩化白金酸を含む水溶液を用いることが好ましい。
また本発明の第1においては、塩素の含有量が200質量ppm以下であることが好ましい。
本発明の第1においては、触媒全量基準で、ルテニウムを0.05〜2質量%および白金を0.0002〜0.5質量%含むことが好ましい。
また本発明の第1においては、ルテニウム酸カリウムと塩化白金酸を含む水溶液を用いることが好ましい。
また本発明の第1においては、塩素の含有量が200質量ppm以下であることが好ましい。
本発明の第2は、一酸化炭素および水素を含有する原料ガスと酸素含有ガスとを本発明の第1に記載の触媒の存在下に接触させることにより一酸化炭素を選択的に酸化して原料ガス中の一酸化炭素濃度を低減する方法に関する。
本発明の第2においては、酸素と原料ガス中の一酸化炭素の比がモル比で0.5〜3であることが好ましい。
また本発明の第2においては、原料ガスが、炭化水素、アルコールまたはエーテルを脱硫反応、改質反応および水性ガスシフト反応を行って得られたものであることが好ましい。
また本発明の第2においては、原料ガス中の一酸化炭素濃度が0.1〜2vol%であることが好ましい。
また本発明の第2においては、酸化反応後の生成ガス中の一酸化炭素濃度が100volppm以下であることが好ましい。
本発明の第2においては、酸素と原料ガス中の一酸化炭素の比がモル比で0.5〜3であることが好ましい。
また本発明の第2においては、原料ガスが、炭化水素、アルコールまたはエーテルを脱硫反応、改質反応および水性ガスシフト反応を行って得られたものであることが好ましい。
また本発明の第2においては、原料ガス中の一酸化炭素濃度が0.1〜2vol%であることが好ましい。
また本発明の第2においては、酸化反応後の生成ガス中の一酸化炭素濃度が100volppm以下であることが好ましい。
本発明の第3は、炭化水素、アルコールおよびエーテルから選ばれる燃料を脱硫反応、改質反応および水性ガスシフト反応を行って得られる一酸化炭素および水素を含有する原料ガスと酸素含有ガスとを本発明の第1に記載の触媒の存在下に接触させることにより一酸化炭素を選択的に酸化させて原料ガス中の一酸化炭素濃度を低減し、高濃度水素含有ガスを製造する装置に関する。
本発明の第4は、前記装置から得られた高濃度水素含有ガスを陰極側燃料として供給することを特徴とする燃料電池システムに関する。
本発明の触媒は、一酸化炭素および水素を含有する原料ガスにおいて、一酸化炭素を選択的に酸化するため、生成ガス中の一酸化炭素濃度を100volppm以下、好ましくは50volppm以下、特に好ましくは10volppm以下にまで低減することができ、得られる燃料ガスは特に固体高分子形燃料電池を用いた燃料電池システムに好適に採用できる。
以下、本発明について詳細に説明する。
本発明の触媒は、水素および一酸化炭素を含有する原料ガス中の一酸化炭素を選択的に酸化するための触媒であって、アルミナ担体に少なくともルテニウム酸カリウムを含有する溶液を接触させることにより得られ、アルミナ担体にルテニウムとルテニウム以外の少なくても1種の白金族元素を担持して成り、かつカリウム含有量が1000質量ppm以下であることを特徴とするものである。
本発明の触媒は、水素および一酸化炭素を含有する原料ガス中の一酸化炭素を選択的に酸化するための触媒であって、アルミナ担体に少なくともルテニウム酸カリウムを含有する溶液を接触させることにより得られ、アルミナ担体にルテニウムとルテニウム以外の少なくても1種の白金族元素を担持して成り、かつカリウム含有量が1000質量ppm以下であることを特徴とするものである。
本発明の触媒において、担体としてはアルミナが用いられる。アルミナとしてはBET表面積が120m2/g以上のものが好ましい。BET表面積が120m2/g未満だと金属の分散度が低くなるため好ましくない。
アルミナ担体の形状、大きさ、成型方法は特に限定されるものではなく、また成型時には適度なバインダーを添加して成形性を高めたものであってもよい。
アルミナ担体の形状、大きさ、成型方法は特に限定されるものではなく、また成型時には適度なバインダーを添加して成形性を高めたものであってもよい。
本発明においては、アルミナ担体と、少なくともルテニウム酸カリウムを含有する溶液とを接触させることにより、該アルミナ担体にルテニウムを担持させる。
担持するルテニウムの出発原料としては、ルテニウム酸カリウムの溶液を用いることが必要である。このとき用いる溶媒はルテニウム酸カリウムを溶解できるものであれば特に限定されないが、水またはエタノールが好ましく、特に水が好ましい。
接触方法は特に限定されるものではなく、好ましくはルテニウム酸カリウムの溶液中にアルミナ担体を浸漬させる方法を挙げることができる。
担持するルテニウムの出発原料としては、ルテニウム酸カリウムの溶液を用いることが必要である。このとき用いる溶媒はルテニウム酸カリウムを溶解できるものであれば特に限定されないが、水またはエタノールが好ましく、特に水が好ましい。
接触方法は特に限定されるものではなく、好ましくはルテニウム酸カリウムの溶液中にアルミナ担体を浸漬させる方法を挙げることができる。
また担体には、ルテニウムの他に、ルテニウム以外の少なくとも1種の白金族元素が担持される。ルテニウム以外の白金族元素としては、白金またはパラジウムが好ましく、特に白金が好ましい。
担体にルテニウム以外の白金族元素を担持する方法については特に制限はなく、例えば、含浸法、平衡吸着法およびスプレー法などを用いることができる。
ルテニウム以外の白金族元素として例えば白金を用いる場合は、塩化白金酸を用いることが特に好ましく、担持方法としては、アルミナ担体と塩化白金酸を含有する溶液とを接触させることにより、アルミナ担体に白金を担持させることができる。このとき用いる溶媒は塩化白金酸を溶解できるものであれば特に限定されないが、水または有機酸水溶液が好ましく、特に水が好ましい。
なお、ルテニウムと白金を担持する順序は特に問わず、別々に担持しても同時に担持してもよい。
担体にルテニウム以外の白金族元素を担持する方法については特に制限はなく、例えば、含浸法、平衡吸着法およびスプレー法などを用いることができる。
ルテニウム以外の白金族元素として例えば白金を用いる場合は、塩化白金酸を用いることが特に好ましく、担持方法としては、アルミナ担体と塩化白金酸を含有する溶液とを接触させることにより、アルミナ担体に白金を担持させることができる。このとき用いる溶媒は塩化白金酸を溶解できるものであれば特に限定されないが、水または有機酸水溶液が好ましく、特に水が好ましい。
なお、ルテニウムと白金を担持する順序は特に問わず、別々に担持しても同時に担持してもよい。
ルテニウム金属の担持量については特に限定はないが、触媒全量基準で0.05〜2質量%であることが好ましく、0.1〜1質量%がより好ましい。ルテニウム金属の担持量が0.05質量%より少ないと触媒活性が十分に発揮されず、2質量%より多いと金属の凝集等が起こりやすく,またメタン化反応等の副反応が生じるため好ましくない。
また、ルテニウム以外の白金族元素の担持量についても特に限定はないが、触媒全量基準で0.0002〜0.5質量%であることが好ましく、0.001〜0.1質量%がより好ましい。担持量が0.0002質量%より少ないとルテニウムと相互作用を起こすには量が不十分であるため相乗効果が十分に発揮されず、0.5質量%より多いと金属の凝集等が起こりやすくなるため担持量を増やしても活性の向上が見られないため不経済である。
また、ルテニウム以外の白金族元素の担持量についても特に限定はないが、触媒全量基準で0.0002〜0.5質量%であることが好ましく、0.001〜0.1質量%がより好ましい。担持量が0.0002質量%より少ないとルテニウムと相互作用を起こすには量が不十分であるため相乗効果が十分に発揮されず、0.5質量%より多いと金属の凝集等が起こりやすくなるため担持量を増やしても活性の向上が見られないため不経済である。
以上のようにして、ルテニウムおよびルテニウム以外の白金族元素をアルミナ担体に担持した後、通常、溶媒を除去し、乾燥を行うが、空気中での自然乾燥、加熱乾燥、減圧下での脱気乾燥または加熱気流中での乾燥のいずれの方法を採用することができる。また溶媒をろ別した後、水などで洗浄し、次いで乾燥しても良い。乾燥後、金属を還元することも好ましく行われるが、この場合、水素含有ガス雰囲気での気相還元、ヒドラジンまたは水素化硼素ナトリウムなどを用いる液相還元が好ましい。例えば、水素含有ガス雰囲気で300〜800℃の温度で1〜5時間実施する、またはヒドラジンまたは水素化硼素ナトリウムなどの水溶液に0.5〜5時間攪拌、加熱浸漬する方法などが好ましい。
本発明においては、触媒中に含まれるカリウム量が1000質量ppm以下であることが必要である。1000質量ppmより多いと、十分な反応活性が得られない。
また、触媒中に含まれる塩素量は200質量ppm以下であることが好ましい。200質量ppmより多いと、十分な反応活性が得られない。
また、触媒中に含まれる塩素量は200質量ppm以下であることが好ましい。200質量ppmより多いと、十分な反応活性が得られない。
本発明においては、前記した触媒の存在下に、一酸化炭素および水素を含有する原料ガスと酸素含有ガスとを接触させることにより、一酸化炭素が選択的に酸化されるため原料ガス中の一酸化炭素濃度を低減することができる。
一酸化炭素および水素を含有する原料ガスとしては、通常、燃料電池用の燃料ガスの出発原料(原燃料)として用いられる炭化水素、あるいはアルコールやエーテル等の含酸素炭化水素等を各種方法により改質反応を行って得られる水素を主成分とするガスが用いられる。
原燃料としては、天然ガス、LPG、ナフサ、灯油、ガソリンまたはこれらに相当する各種溜分や、メタン、エタン、プロパン、ブタン等の炭化水素、メタノール、エタノール等の各種アルコール、およびジメチルエーテル等のエーテル等が用いられる。
原燃料としては、天然ガス、LPG、ナフサ、灯油、ガソリンまたはこれらに相当する各種溜分や、メタン、エタン、プロパン、ブタン等の炭化水素、メタノール、エタノール等の各種アルコール、およびジメチルエーテル等のエーテル等が用いられる。
前記原燃料を改質する方法としては、特に限定されるものではなく、水蒸気改質方法、部分酸化改質方法、オートサーマルリフォーミング等の各種方法が挙げられる。本発明においてはこれらのいずれの方法も採用することができる。
なお、硫黄を含んでいる原燃料をそのまま改質工程に供給してしまうと、改質触媒が被毒を受け、改質触媒の活性が発現せず、また寿命も短くなるため、改質反応に先立って、原燃料を脱硫処理しておくことが好ましい。
脱硫反応の条件は、原燃料の状態および硫黄含有量によって異なるため一概には言えないが、通常、反応温度は常温〜450℃が好ましく、特に常温〜300℃が好ましい。反応圧力は常圧〜1MPaが好ましく、常圧〜0.2MPaがさらに好ましい。SVは原料が液体の場合で0.01〜15h−1が好ましく、0.05〜5h−1がさらに好ましく、0.1〜3h−1が特に好ましい。また気体原料の場合では、100〜10000h−1が好ましく、200〜5000h−1がさらに好ましく、300〜2000h−1が特に好ましい。
脱硫反応の条件は、原燃料の状態および硫黄含有量によって異なるため一概には言えないが、通常、反応温度は常温〜450℃が好ましく、特に常温〜300℃が好ましい。反応圧力は常圧〜1MPaが好ましく、常圧〜0.2MPaがさらに好ましい。SVは原料が液体の場合で0.01〜15h−1が好ましく、0.05〜5h−1がさらに好ましく、0.1〜3h−1が特に好ましい。また気体原料の場合では、100〜10000h−1が好ましく、200〜5000h−1がさらに好ましく、300〜2000h−1が特に好ましい。
また改質反応条件も必ずしも限定されるものではないが、通常、反応温度は200〜1,000℃が好ましく、500〜850℃がより好ましい。反応圧力は常圧〜1MPaが好ましく、常圧〜0.2MPaがより好ましい。GHSVは、100〜100,000h−1が好ましく、300〜50,000h−1がより好ましく、500〜30,000h−1が特に好ましい。
改質反応により得られるガス(改質ガス)は、主成分として水素を含むものの、他の成分としては、一酸化炭素、二酸化炭素、水蒸気等が含有される。
改質反応により得られるガス(改質ガス)は、主成分として水素を含むものの、他の成分としては、一酸化炭素、二酸化炭素、水蒸気等が含有される。
本発明においては、原料ガスとして前記改質ガスを直接用いることも可能であるが、かかる改質ガスを予め前処理して一酸化炭素濃度をある程度低減させたものを用いてもよい。
かかる前処理としては、改質ガス中の一酸化炭素濃度を低減させるため、改質ガス中の一酸化炭素を水蒸気と反応させ、水素と二酸化炭素に転化する方法、いわゆる水性ガスシフト反応が挙げられる。水性ガスシフト反応以外の前処理としては、一酸化炭素を吸着分離する方法、あるいは膜分離する方法等が挙げられる。
かかる前処理としては、改質ガス中の一酸化炭素濃度を低減させるため、改質ガス中の一酸化炭素を水蒸気と反応させ、水素と二酸化炭素に転化する方法、いわゆる水性ガスシフト反応が挙げられる。水性ガスシフト反応以外の前処理としては、一酸化炭素を吸着分離する方法、あるいは膜分離する方法等が挙げられる。
本発明においては、改質ガス中の一酸化炭素を低減し、かつ水素を増やすためにも、改質ガスをさらに水性ガスシフト反応したものを原料ガスとするのが好ましく、これにより一酸化炭素濃度の低減をより効果的にすることができる。
水性ガスシフト反応は改質ガスの組成等によって、必ずしも反応条件は限定されるものではないが、通常、反応温度は120〜500℃が好ましく、特に150〜450℃が好ましい。反応圧力は常圧〜1MPaが好ましく、特に常圧〜0.2MPaが好ましい。SVは100〜50,000h−1が好ましく、特に300〜10,000h−1が好ましい。
水性ガスシフト反応は改質ガスの組成等によって、必ずしも反応条件は限定されるものではないが、通常、反応温度は120〜500℃が好ましく、特に150〜450℃が好ましい。反応圧力は常圧〜1MPaが好ましく、特に常圧〜0.2MPaが好ましい。SVは100〜50,000h−1が好ましく、特に300〜10,000h−1が好ましい。
本発明において用いる原料ガスは、一酸化炭素および水素を含有するものであるが、一酸化炭素濃度は、通常0.1〜2vol%、好ましくは0.5〜1vol%である。一方、水素濃度は通常30〜70vol%、好ましくは50〜70vol%である。また、一酸化炭素および水素以外の成分として、例えば窒素、二酸化炭素等が含まれていても良い。
その後、一酸化炭素および水素を含有する原料ガスに酸素含有ガスを加え、本発明の触媒の存在下に選択的酸化反応を行わせ、一酸化炭素を二酸化炭素に転換させることにより原料ガス中の一酸化炭素濃度を低減する。原料ガスに加える酸素含有ガスとしては、特に限定されないが、空気や酸素が挙げられる。
導入する酸素含有ガスの量は、全酸素量と原料ガス中の一酸化炭素の濃度比(モル比)が0.5〜5.0の範囲とすることが好ましく、特に0.5〜3.0が好ましい。前記濃度比が0.5より小さい場合は、化学量論的に酸素が足りないため一酸化炭素との酸化反応が十分に進行しない。また、前記濃度比が5.0より大きい場合は、水素の酸化により、水素濃度の低下、水素の酸化熱により反応温度の上昇、メタンの生成などの副反応が起こりやすくなるため好ましくない。
導入する酸素含有ガスの量は、全酸素量と原料ガス中の一酸化炭素の濃度比(モル比)が0.5〜5.0の範囲とすることが好ましく、特に0.5〜3.0が好ましい。前記濃度比が0.5より小さい場合は、化学量論的に酸素が足りないため一酸化炭素との酸化反応が十分に進行しない。また、前記濃度比が5.0より大きい場合は、水素の酸化により、水素濃度の低下、水素の酸化熱により反応温度の上昇、メタンの生成などの副反応が起こりやすくなるため好ましくない。
一酸化炭素の酸化反応の際の反応圧力は、燃料電池システムの経済性、安全性等も考慮し、常圧〜1MPaの範囲が好ましく、特に常圧〜0.2MPaが好ましい。反応温度としては、一酸化炭素濃度を低下させる温度であれば、特に限定はないが、低温では反応速度が遅くなり、高温では選択性が低下するため、通常は80〜350℃が好ましく、特に100〜300℃が好ましい。GHSVは過剰に高すぎると一酸化炭素の酸化反応が進行しにくくなり、一方低すぎると装置が大きくなりすぎるため、1,000〜50,000h−1の範囲が好ましく、特に3,000〜30,000h−1の範囲が好ましい。
本発明の方法により、原料ガス中の一酸化炭素濃度を100volppm以下、好ましくは50volppm以下、最も好ましくは10volppm以下にまで低減することができる。そのため、本発明の方法により得られる一酸化炭素濃度が低減された燃料ガスは、燃料電池の電極に用いられている貴金属系触媒の被毒、劣化が抑制され、発電効率を高く保ちながら、長寿命を維持することが可能となる。
また本発明は高濃度水素含有ガスを製造するための装置を提供する。本発明の装置は、炭化水素、アルコールおよびエーテルから選ばれる燃料を脱硫反応、改質反応および水性ガスシフト反応を行って得られる一酸化炭素および水素を含有する原料ガスと酸素含有ガスとを前記した本発明の触媒の存在下に接触させることにより一酸化炭素を選択的に酸化して原料ガス中の一酸化炭素濃度を低減し、高濃度水素含有ガスを製造する装置である。
さらに本発明は燃料電池システムを提供する。本発明の燃料電池システムは、前記装置から得られた高濃度水素含有ガスを陰極側燃料として供給することを特徴とする。
本発明の燃料電池システムを以下に説明する。
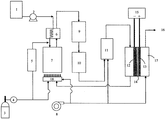
図1は、本発明の燃料電池システムの一例を示す概略図である。
燃料タンク3内の原燃料は燃料ポンプ4を経て脱硫器5に流入する。この時、必要であれば選択酸化反応器11からの水素含有ガスを添加できる。脱硫器5内には例えば銅−亜鉛系あるいはニッケル−亜鉛系の収着剤などを充填することができる。脱硫器5で脱硫された原燃料は水タンク1から水ポンプ2を経た水と混合した後、気化器6に導入され、改質器7に送り込まれる。
本発明の燃料電池システムを以下に説明する。
図1は、本発明の燃料電池システムの一例を示す概略図である。
燃料タンク3内の原燃料は燃料ポンプ4を経て脱硫器5に流入する。この時、必要であれば選択酸化反応器11からの水素含有ガスを添加できる。脱硫器5内には例えば銅−亜鉛系あるいはニッケル−亜鉛系の収着剤などを充填することができる。脱硫器5で脱硫された原燃料は水タンク1から水ポンプ2を経た水と混合した後、気化器6に導入され、改質器7に送り込まれる。
改質器7は加温用バーナー18で加温される。加温用バーナー18の燃料には主に固体高分子型燃料電池17のアノードオフガスを用いるが必要に応じて燃料ポンプ4から吐出される燃料を補充することもできる。改質器7に充填する触媒としてはニッケル系、ルテニウム系、ロジウム系などの触媒を用いることができる。
この様にして製造された水素と一酸化炭素を含有する原料ガスは高温シフト反応器9および低温シフト反応器10により改質反応が行われる。高温シフト反応器9には鉄−クロム系触媒、低温シフト反応器10には銅−亜鉛系触媒等の触媒が充填されている。
この様にして製造された水素と一酸化炭素を含有する原料ガスは高温シフト反応器9および低温シフト反応器10により改質反応が行われる。高温シフト反応器9には鉄−クロム系触媒、低温シフト反応器10には銅−亜鉛系触媒等の触媒が充填されている。
高温シフト反応器9および低温シフト反応器10により改質されたガスは、次に選択酸化反応器11に導かれる。選択酸化反応器11には本発明の触媒が充填されている。改質ガスは空気ブロアー8から供給される空気と混合され、前記触媒の存在下に一酸化炭素の選択酸化が行われ、一酸化炭素濃度は燃料電池の特性に影響を及ぼさない程度まで低減される。
固体高分子形燃料電池17はアノード12、カソード13、固体高分子電解質14からなり、アノード側には上記の方法で得られた一酸化炭素濃度が低減された高純度の水素を含有する燃料ガスが、カソード側には空気ブロアー8から送られる空気が、それぞれ必要であれば適当な加湿処理を行なったあと(加湿装置は図示していない)導入される。
この時、アノードでは水素ガスがプロトンとなり電子を放出する反応が進行し、カソードでは酸素ガスが電子とプロトンを得て水となる反応が進行する。これらの反応を促進するため、それぞれ、アノードには白金黒、活性炭担持のPt触媒あるいはPt−Ru合金触媒などが、カソードには白金黒、活性炭担持のPt触媒などが用いられる。通常アノード、カソードの両触媒とも、必要に応じてポリテトラフルオロエチレン、低分子の高分子電解質膜素材、活性炭などと共に多孔質触媒層に成形される。
この時、アノードでは水素ガスがプロトンとなり電子を放出する反応が進行し、カソードでは酸素ガスが電子とプロトンを得て水となる反応が進行する。これらの反応を促進するため、それぞれ、アノードには白金黒、活性炭担持のPt触媒あるいはPt−Ru合金触媒などが、カソードには白金黒、活性炭担持のPt触媒などが用いられる。通常アノード、カソードの両触媒とも、必要に応じてポリテトラフルオロエチレン、低分子の高分子電解質膜素材、活性炭などと共に多孔質触媒層に成形される。
次いでNafion(デュポン社製)、Gore(ゴア社製)、Flemion(旭硝子社製)、Aciplex(旭化成社製)等の商品名で知られる高分子電解質膜の両側に前述の多孔質触媒層を積層しMEA(Membrane Electrode Assembly)が形成される。さらにMEAを金属材料、グラファイト、カーボンコンポジットなどからなるガス供給機能、集電機能、特にカソードにおいては重要な排水機能等を持つセパレータで挟み込むことで燃料電池が組み立てられる。電気負荷15はアノード、カソードと電気的に連結される。
アノードオフガスは加温用バーナー18において消費される。カソードオフガスは排気口16から排出される。
アノードオフガスは加温用バーナー18において消費される。カソードオフガスは排気口16から排出される。
以下に実施例により本発明を具体的に説明するが、本発明はこれらに限定されるものではない。
(実施例1)
ルテニウム酸カリウム(三津和化学社製)0.194g、塩化白金酸(小島化学薬品製)0.194gを100mlの水に溶解させた水溶液を調製し、この液にアルミナ担体(住友化学社製 KHD−24 BET表面積320m2/g)25.0gを投入し、3時間攪拌しながら含浸し、ろ別した後、空気雰囲気下、120℃で15時間、次いで500℃で3時間水素処理して触媒(1)を得た。担持されたルテニウム量は0.3質量%、白金量は0.03質量%であった。このときのカリウム量は90質量ppm、塩素量は75質量ppmであった。
ルテニウム酸カリウム(三津和化学社製)0.194g、塩化白金酸(小島化学薬品製)0.194gを100mlの水に溶解させた水溶液を調製し、この液にアルミナ担体(住友化学社製 KHD−24 BET表面積320m2/g)25.0gを投入し、3時間攪拌しながら含浸し、ろ別した後、空気雰囲気下、120℃で15時間、次いで500℃で3時間水素処理して触媒(1)を得た。担持されたルテニウム量は0.3質量%、白金量は0.03質量%であった。このときのカリウム量は90質量ppm、塩素量は75質量ppmであった。
(比較例1)
100mlの水にルテニウム酸ナトリウム0.142gを溶解した後、塩化白金酸(小島化学社製)0.194gを溶解し担持液とした。この担持液にアルミナ担体(住友化学社製 KHD−24 BET表面積320m2/g)25.0gを投入し、3時間攪拌しながら含浸し、ろ別した後、空気雰囲気下、120℃で15時間乾燥して触媒(2)を得た。担持されたルテニウム量は0.3質量%、白金量は0.03質量%であった。このときのカリウム量は1600質量ppm、塩素量は75質量ppmであった。
100mlの水にルテニウム酸ナトリウム0.142gを溶解した後、塩化白金酸(小島化学社製)0.194gを溶解し担持液とした。この担持液にアルミナ担体(住友化学社製 KHD−24 BET表面積320m2/g)25.0gを投入し、3時間攪拌しながら含浸し、ろ別した後、空気雰囲気下、120℃で15時間乾燥して触媒(2)を得た。担持されたルテニウム量は0.3質量%、白金量は0.03質量%であった。このときのカリウム量は1600質量ppm、塩素量は75質量ppmであった。
(比較例2)
ルテニウム酸カリウム(三津和化学社製)0.194gを100mlの水に溶解させた水溶液を調製し、この液にアルミナ担体(住友化学社製 KHD−24 BET表面積320m2/g)25.0gを投入し、3時間攪拌しながら含浸し、ろ別した後、空気雰囲気下、120℃で15時間、次いで700℃で3時間水素処理して触媒(3)を得た。担持されたルテニウム量は0.08質量%であった。
ルテニウム酸カリウム(三津和化学社製)0.194gを100mlの水に溶解させた水溶液を調製し、この液にアルミナ担体(住友化学社製 KHD−24 BET表面積320m2/g)25.0gを投入し、3時間攪拌しながら含浸し、ろ別した後、空気雰囲気下、120℃で15時間、次いで700℃で3時間水素処理して触媒(3)を得た。担持されたルテニウム量は0.08質量%であった。
(比較例3)
塩化ルテニウム(和光純薬社製)0.154g、塩化白金酸(小島化学社製)0.194gを100mlの水に溶解させた水溶液を調製し、この液にアルミナ担体(住友化学社製 KHD−24 BET表面積320m2/g)25.0gを投入し、3時間攪拌しながら含浸し、ろ別した後、空気雰囲気下、120℃で15時間乾燥した。この乾燥触媒を100mlの1質量%のヒドラジン(和光純薬社製)水溶液を用いて還元した後、120℃で15時間乾燥して触媒(4)を得た。担持されたルテニウム量は0.3質量%、白金量は0.03質量%であった。このときのカリウム量は検出限界(50質量ppb)以下、塩素量は350質量ppmであった。
塩化ルテニウム(和光純薬社製)0.154g、塩化白金酸(小島化学社製)0.194gを100mlの水に溶解させた水溶液を調製し、この液にアルミナ担体(住友化学社製 KHD−24 BET表面積320m2/g)25.0gを投入し、3時間攪拌しながら含浸し、ろ別した後、空気雰囲気下、120℃で15時間乾燥した。この乾燥触媒を100mlの1質量%のヒドラジン(和光純薬社製)水溶液を用いて還元した後、120℃で15時間乾燥して触媒(4)を得た。担持されたルテニウム量は0.3質量%、白金量は0.03質量%であった。このときのカリウム量は検出限界(50質量ppb)以下、塩素量は350質量ppmであった。
これらの触媒(1)〜(4)をそれぞれ3.0cm3の反応管に充填し、一酸化炭素除去反応評価を行った。
試験ガスとしては、灯油を水蒸気改質し、水性ガスシフト反応して得られた原料ガスに酸素を加えたものを用いた。試験ガス中には、水素58vol%、一酸化炭素0.5vol%、二酸化炭素18vol%、酸素0.5vol%、水21vol%が含まれていた。
反応評価条件は常圧、GHSV=10,000h−1、試験ガス中の一酸化炭素濃度6000volppmの条件で、20時間後の生成ガス中の一酸化炭素濃度の極小値およびその時の反応温度を表1に示した。
試験ガスとしては、灯油を水蒸気改質し、水性ガスシフト反応して得られた原料ガスに酸素を加えたものを用いた。試験ガス中には、水素58vol%、一酸化炭素0.5vol%、二酸化炭素18vol%、酸素0.5vol%、水21vol%が含まれていた。
反応評価条件は常圧、GHSV=10,000h−1、試験ガス中の一酸化炭素濃度6000volppmの条件で、20時間後の生成ガス中の一酸化炭素濃度の極小値およびその時の反応温度を表1に示した。
(実施例2)
触媒(1)を用いて得られた生成ガスを図1の固体高分子形燃料電池アノード極に導入して発電を行ったところ正常に作動した。
触媒(1)を用いて得られた生成ガスを図1の固体高分子形燃料電池アノード極に導入して発電を行ったところ正常に作動した。
1 水タンク
2 水ポンプ
3 燃料タンク
4 燃料ポンプ
5 脱硫器
6 気化器
7 改質器
8 空気ブロアー
9 高温シフト反応器
10 低温シフト反応器
11 選択酸化反応器
12 アノード
13 カソード
14 固体高分子電解質
15 電気負荷
16 排気口
17 固体高分子型燃料電池
18 加温用バーナー
2 水ポンプ
3 燃料タンク
4 燃料ポンプ
5 脱硫器
6 気化器
7 改質器
8 空気ブロアー
9 高温シフト反応器
10 低温シフト反応器
11 選択酸化反応器
12 アノード
13 カソード
14 固体高分子電解質
15 電気負荷
16 排気口
17 固体高分子型燃料電池
18 加温用バーナー
Claims (11)
- アルミナ担体に少なくともルテニウム酸カリウムを含有する溶液を接触させることにより得られる、アルミナ担体にルテニウムとルテニウム以外の少なくとも1種の白金族元素を担持して成り、かつカリウム含有量が1000質量ppm以下であることを特徴とする水素および一酸化炭素を含有する原料ガス中の一酸化炭素を選択的に酸化するための触媒。
- 触媒全量基準で、ルテニウムを0.05〜2質量%および白金を0.0002〜0.5質量%含むことを特徴とする請求項1に記載の触媒。
- ルテニウム酸カリウムと塩化白金酸を含む水溶液を用いることを特徴とする請求項1または2に記載の触媒。
- 塩素の含有量が200質量ppm以下であることを特徴とする請求項1〜3のいずれかの項に記載の触媒。
- 一酸化炭素および水素を含有する原料ガスと酸素含有ガスとを請求項1〜4のいずれかの項に記載の触媒の存在下に接触させることにより一酸化炭素を選択的に酸化して原料ガス中の一酸化炭素濃度を低減する方法。
- 酸素と原料ガス中の一酸化炭素の比がモル比で0.5〜3であることを特徴とする請求項5に記載の方法。
- 原料ガスが、炭化水素、アルコールまたはエーテルを脱硫反応、改質反応および水性ガスシフト反応を行って得られたものであることを特徴とする請求項5または6に記載の方法。
- 原料ガス中の一酸化炭素濃度が0.1〜2vol%であることを特徴とする請求項5〜7のいずれかの項に記載の方法。
- 酸化反応後の生成ガス中の一酸化炭素濃度が100volppm以下であることを特徴とする請求項5〜8のいずれかの項に記載の方法。
- 炭化水素、アルコールおよびエーテルから選ばれる燃料を脱硫反応、改質反応および水性ガスシフト反応を行って得られる一酸化炭素および水素を含有する原料ガスと酸素含有ガスとを請求項1〜4のいずれかの項に記載の触媒の存在下に接触させることにより一酸化炭素を選択的に酸化させて原料ガス中の一酸化炭素濃度を低減し、高濃度水素含有ガスを製造する装置。
- 請求項10に記載の装置から得られた高濃度水素含有ガスを陰極側燃料として供給することを特徴とする燃料電池システム。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005373085A JP2007167828A (ja) | 2005-12-26 | 2005-12-26 | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005373085A JP2007167828A (ja) | 2005-12-26 | 2005-12-26 | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2007167828A true JP2007167828A (ja) | 2007-07-05 |
Family
ID=38295086
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005373085A Pending JP2007167828A (ja) | 2005-12-26 | 2005-12-26 | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2007167828A (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009023869A (ja) * | 2007-07-19 | 2009-02-05 | Aisin Seiki Co Ltd | 脱硫器および改質原料供給システム |
| WO2010113381A1 (ja) * | 2009-03-31 | 2010-10-07 | 新日本石油株式会社 | 一酸化炭素の選択的酸化反応用触媒の製造方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH1029803A (ja) * | 1996-07-15 | 1998-02-03 | Asahi Chem Ind Co Ltd | 燃料電池用水素の精製法 |
| JP2000169107A (ja) * | 1998-12-03 | 2000-06-20 | Idemitsu Kosan Co Ltd | 一酸化炭素の低減された水素含有ガスの製造方法 |
| JP2002113368A (ja) * | 2000-10-11 | 2002-04-16 | Mitsubishi Heavy Ind Ltd | Co選択酸化触媒の製造方法 |
| JP2003265956A (ja) * | 2002-03-14 | 2003-09-24 | Nippon Oil Corp | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム |
| JP2004223415A (ja) * | 2003-01-23 | 2004-08-12 | Nippon Oil Corp | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム |
-
2005
- 2005-12-26 JP JP2005373085A patent/JP2007167828A/ja active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH1029803A (ja) * | 1996-07-15 | 1998-02-03 | Asahi Chem Ind Co Ltd | 燃料電池用水素の精製法 |
| JP2000169107A (ja) * | 1998-12-03 | 2000-06-20 | Idemitsu Kosan Co Ltd | 一酸化炭素の低減された水素含有ガスの製造方法 |
| JP2002113368A (ja) * | 2000-10-11 | 2002-04-16 | Mitsubishi Heavy Ind Ltd | Co選択酸化触媒の製造方法 |
| JP2003265956A (ja) * | 2002-03-14 | 2003-09-24 | Nippon Oil Corp | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム |
| JP2004223415A (ja) * | 2003-01-23 | 2004-08-12 | Nippon Oil Corp | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009023869A (ja) * | 2007-07-19 | 2009-02-05 | Aisin Seiki Co Ltd | 脱硫器および改質原料供給システム |
| WO2010113381A1 (ja) * | 2009-03-31 | 2010-10-07 | 新日本石油株式会社 | 一酸化炭素の選択的酸化反応用触媒の製造方法 |
| JP2010234257A (ja) * | 2009-03-31 | 2010-10-21 | Jx Nippon Oil & Energy Corp | 一酸化炭素の選択的酸化反応用触媒の製造方法 |
| US8349762B2 (en) | 2009-03-31 | 2013-01-08 | Jx Nippon Oil & Energy Corporation | Method for producing catalyst for use in preferential oxidation reaction of carbon monoxide |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101426110B1 (ko) | 등유용 탈황제, 탈황법 및 등유용 탈황제를 이용한 연료 전지 시스템 | |
| JP5105937B2 (ja) | 一酸化炭素濃度を低減する方法 | |
| US8093178B2 (en) | Catalyst for reducing carbon monoxide concentration | |
| JP5204633B2 (ja) | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム | |
| JP3943902B2 (ja) | 炭化水素用脱硫触媒、脱硫方法および燃料電池システム | |
| JP4210130B2 (ja) | 炭化水素の脱硫触媒、脱硫方法及び燃料電池システム | |
| JP4582976B2 (ja) | 一酸化炭素濃度を低減する方法および燃料電池システム | |
| JP2003265956A (ja) | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム | |
| JP4037122B2 (ja) | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム | |
| JP4567930B2 (ja) | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム | |
| JP2007167828A (ja) | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム | |
| JP4011886B2 (ja) | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム | |
| JP4881078B2 (ja) | 一酸化炭素濃度を低減する方法および燃料電池システム | |
| JP5537232B2 (ja) | 一酸化炭素濃度の低減方法、水素製造装置および燃料電池システム | |
| JP2004223415A (ja) | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム | |
| JP5041781B2 (ja) | 一酸化炭素濃度を低減する方法および燃料電池システム | |
| JP2003284950A (ja) | 一酸化炭素を選択的に酸化する触媒、一酸化炭素濃度を低減する方法および燃料電池システム | |
| JP4559676B2 (ja) | 炭化水素用脱硫触媒、脱硫方法および燃料電池システム | |
| JP4125924B2 (ja) | 炭化水素の脱硫方法および燃料電池システム | |
| JP4057314B2 (ja) | 炭化水素の脱硫方法および燃料電池システム | |
| JP4820711B2 (ja) | 触媒の選択酸化能の評価方法および高濃度水素含有ガスの製造方法 | |
| JP2004066035A (ja) | 炭化水素の脱硫方法および燃料電池システム | |
| JP5117014B2 (ja) | 灯油用脱硫剤、脱硫方法およびそれを用いた燃料電池システム | |
| Arpornwichanop et al. | Recent Trends in the Development of Proton Exchange Membrane Fuel Cell Systems | |
| JP2003147372A (ja) | 炭化水素の脱硫方法および燃料電池システム |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20081219 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20101129 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20101207 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20110405 |